Изобретение относится к электрохимическому способу получения порошков гексаборидов металлов лантаноидной группы, которые, благодаря особым физическим и химическим свойствам нашли широкое применение в катодах-компенсаторах стационарных плазменных двигателей космических аппаратов.
В обзорной статье K.Uchida указаны ранние работы по электросинтезу гексаборидов лантаноидов, в которых в качестве электролитов-растворителей используются хорошо растворимые в воде хлоридные расплавы KCl-LiCl и KCl-NaCl [1]. В расплавах такого состава добавки оксидов бора и лантаноидов растворяются в количествах, совершенно недостаточных для электрохимического синтеза гексаборидов. Поэтому в качестве исходного сырья приходится использовать намного более дорогие соли бора и лантаноидов, в частности фторид KBF4 и LnCl3, реже LnF3.
В качестве альтернативы предыдущим исследованиям известно использование в качестве солевого расплава – электролита состава (мас.%): 71,7 Li3AlCl6 + 28,1 Li2B4O7 + 7,1 La2O3, в котором электролизом при 850оС и катодной плотности тока 0,0025 А/см2 получают осадок крупнокристаллического гексаборида лантана LaB6 с размером зерна 1±0,2 мм [2]. К недостаткам этого способа относится плохая растворимость электролита в воде, даже кипящей, что приводит к необходимости растворять соль в разбавленной соляной кислоте, и усложняет технологию отмывки порошка. Определяющая скорость электрохимического синтеза плотность тока 0,0025 А/см2 в этом способе недопустимо мала даже для лабораторного варианта процесса, не говоря уже о промышленном. Размер получаемого порошка гексаборида слишком крупный, что исключает возможность изготовления из него керамических изделий методом «прессование – спекание».
Наиболее близким к заявляемому способу является способ [3]. Здесь описан электролитический способ получения ультрадисперсного порошка гексаборида лантана (LaB6), в котором используют расплавленный электролит - растворитель, основным компонентом которого является эквимольная смесь хлоридов натрия и калия (0,5NaCl-0,5KCl) с добавками безводного хлорида лантана (LaCl3) и тетрафторбората калия (KBF4) в количествах 2,5÷5,0 и 8,0÷11,0% соответственно. Атмосфера над расплавленным электролитом состоит из осушенного и очищенного аргона. Рабочая температура процесса составляет 700±10°С, а указанный интервал плотностей тока на вольфрамовом катоде 0,1÷1,0 А/см2, причем последняя величина плотности тока не подтверждена примерами и явно избыточна. Преимуществом данного способа получения гексаборида является относительно низкая рабочая температура электросинтеза 700°С, хорошая растворимость электролита в воде, что облегчает очистку от него целевого продукта и удовлетворительная чистота продукта. К недостаткам способа можно отнести следующее.
Использование в качестве источника ионов лантана его безводного хлорида LaCl3, приводит к её гидролизу с образованием оксихлоридов LnOCl, поскольку эта соль очень гигроскопична и поглощает влагу из воздуха. Поэтому все препаративные операции (осушка, взвешивание, дробление, загрузка в тигель - электролизёр и т.п.), приходится вести в герметичном перчаточном боксе с атмосферой очищенного аргона. Использование в качестве защитной атмосферы очищенного и осушенного аргона в герметичном электролизёре из жаростойкой стали абсолютно необходимо для защиты графитового или стеклоуглеродного тигля – электролизёра от окисления, а также для предотвращения взаимодействия хлорида LaCl3 с влагой и кислородом воздуха, результатом которого является образование в электролите нерастворимого осадка оксихлорида LnOCl, который не участвует далее в процессе формирования на катоде целевого продукта – гексаборида LnB6. Использование в качестве источника ионов бора его тетрафторбората (KBF4) типично для электролитических способов получения любых боридов, так как это единственная малогигроскопичная бескислородная соль бора, устойчивая к термическому разложению при плавлении, но это и самое дорогое из товарных соединений бора.
Задачей настоящего изобретения является получение порошков гексаборидов лантаноидов электрохимическим способом без использования инертной атмосферы очищенного аргона и дорогостоящих компонентов.
Для этого предложен электрохимический способ получения микродисперсных порошков гексаборидов металлов лантаноидной группы, который, как и прототип, включает синтез в газовой атмосфере гексаборидов лантаноидов из хлоридсодержащего расплава, содержащего ионы бора и ионы лантаноида. Новый способ отличается тем, что в качестве хлоридсодержащего расплава используют расплав состава (CaCl2 – CaO) с добавками оксида бора B2O3 и оксида получаемого лантаноида Ln2O3, причем в процессе электролиза концентрации B2O3 и Ln2O3 поддерживают постоянными в количествах, обеспечивающих атомное соотношение бора к лантаноиду B/Ln = 6 при их суммарной концентрации в расплаве 5-10 мас.% от массы электролита, при этом синтез гексаборидов лантаноидов из хлоридсодержащего расплава осуществляют в атмосфере воздуха в интервале температур 800÷850С0, при катодной плотности тока 0,3-0,5 А/см2.
Растворимость указанных оксидов в расплаве CaCl2 – CaO достигает 5-6% в зависимости от температуры, что вполне достаточно для электросинтеза, и эта растворимость обусловлена образованием диссоциированных соединений [Ca2++(Ln2O4)2-] и [Ca2++(B2O4)2-]. Первым на катоде осаждается бор, далее на нём осаждается лантаноид с деполяризацией за счёт образованием борида, далее идёт совместное соосаждение бора и лантаноида (в кинетическом режиме). Нижний предел температуры электросинтеза (800°С) обусловлен следующими факторами: а) - перегрев электролита над температурой его плавления (772°С) должен быть не менее 25 – 30° для успешного ведения электролиза; б) – при температуре ниже 800°C скорость растворения оксидов бора и лантана недостаточна для ведения интенсивного электролиза. Верхний предел температуры (850°С) обусловлен тем, что при более высокой температуре быстро возрастает летучесть расплава с потерей СаСl2 в виде паров и окисление графитового анода. Электролиз проводится при плотности тока 0,3 - 0,5 А/см2 в течение 2 ÷ 5 часов.
Достигнутый технический результат состоит в том, что методом электросинтеза получены порошки гексаборидов лантаноидов LaB6, SmB6, GdB6 с выходом по затраченному току электролиза (КПД) до 82% при упрощении и удешевлении технологии получения и стоимости целевого продукта.
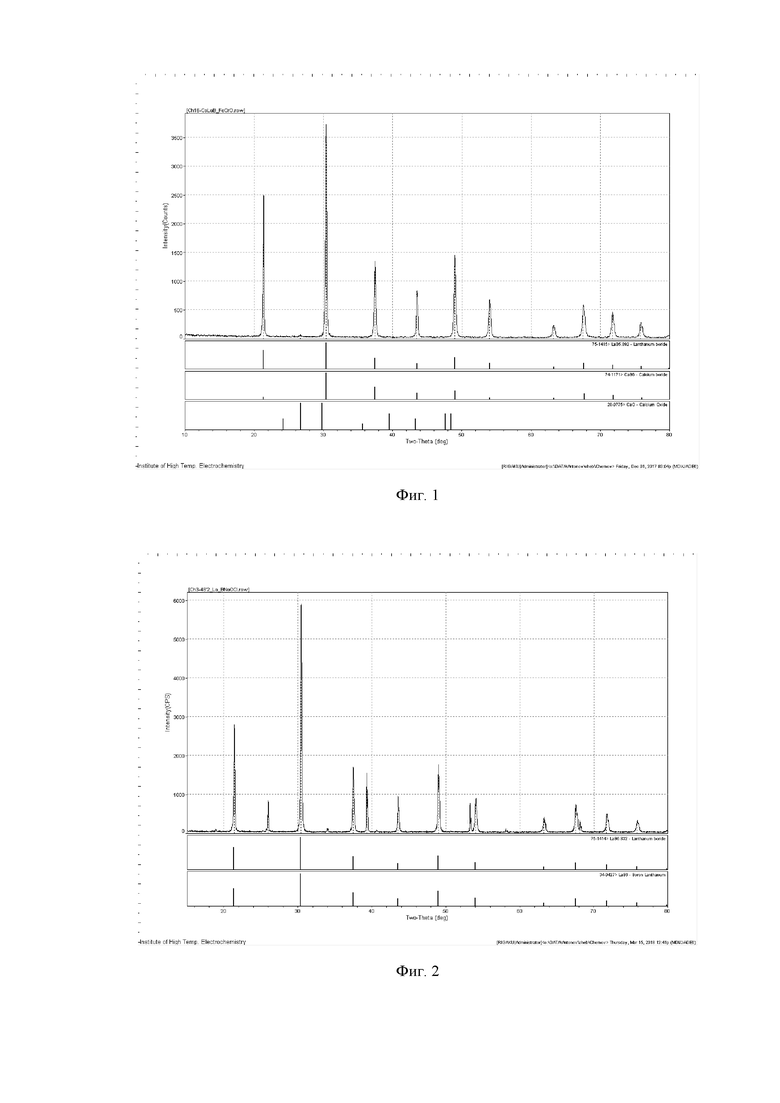
Изобретение иллюстрируется рисунками, где на фиг.1-5 - приведены рентгеновские дифрактограммы катодного осадка полученного гексаборида лантана; на фиг.6 - рентгеновская дифрактограмма катодного осадка полученного гексаборида самария; на фиг.7 - рентгеновская дифрактограмма катодного осадка полученного гексаборида гадолиния.
Способ осуществляли следующим образом. В качестве компонентов электролита использовали:
- Хлорид кальция (CaCl2) технический, кальцинированный, гранулированный, ГОСТ 450 – 77 с изм. 1-3;
- Оксид кальция (CaO) – марки «чда»
- Оксид лантана ТУ 48-4-523-89
- Оксид гадолиния ТУ 48-4-523-89
- Оксид самария ТУ 48-4-523-89
- Борный ангидрид (B2O3) – плавленый, марки «ч», ТУ 6-09-17-249-88.
Наплавление ванны осуществляли следующим образом. Соль CaCl2 наплавляли в тигле при 850°С, сверху на расплав насыпали малыми порциями оксид металла лантаноидной группы и гранулы B2O3, которые по мере нагревания растворялись в расплаве CaCl2. Критерием окончания полного растворения этих добавок является прозрачность солевого расплава. После этого в электролит помещали спиральный молибденовый катод и графитовый анод и включали ток электролиза. В процессе наплавления электролита и в процессе электролиза поддерживали суммарную концентрацию оксидов B2O3+Ln2O3=10% в соотношении, обеспечивающем атомное отношение B/Ln = 6, как это необходимо для формирования осадка LaB6. Конкретные примеры соотношений показаны в примерах при синтезе соответствующих гексаборидов.
Фазовый состав порошков гексаборидов лантаноидной группы определяли с помощью рентгеновского дифрактометра Rigaku D/ Max – 2000, гранулометрический состав исследовали на лазерном дифракционном анализаторе Malvern Mastersizer 2000.
Получение гексаборида лантана
Пример 1. В корундовом тигле при температуре 850°C наплавляли 400 г. хлорида кальция с добавкой 5% оксида кальция, на который сверху малыми порциями (по мере растворения) добавляли оксиды бора и лантана из расчёта их суммарной концентрации 10%, при соотношении 56% B2O3 и 44% La2O3. После полного растворения оксидов температуру снижали до 800°С, в расплав опускали графитовый анод и молибденовый катод. Вначале проводили очистной электролиз расплава плотностью тока 0,3 А/см2 в течение 30 мин для удаления остаточной примеси воды. Далее электролиз по получению LaB6 вели при той же плотности тока в течение 2 часов. После окончания электролиза катод с осадком вынимали из расплава и после остывания до комнатной температуры помещали в стакан с кипящей дистиллированной водой, в котором катодный осадок отмывали от остатков соли. Далее осадок смывали в воронку на бумажный фильтр и дополнительно промывали разбавленной соляной кислотой (10%), затем дистиллированной водой. После этого промытый осадок вместе с фильтром сушили в сушильном шкафу при температуре 80°C. После снятия с фильтра получали мелкодисперсный порошок малинового цвета массой 5 г. Рентгенофазовый анализ показал (фиг.1), что порошок представляет собой гексаборид LaВ6 . Элементный химический анализ показал наличие примесей алюминия, меди и железа, суммарное содержание которых составляет 0,9%. Теоретическая масса LaB6, вычисленная по закону Фарадея, должна быть 5,79 г, а в действительности получено 5 г. Таким образом, выход продукта по затраченному количеству электричества равен 80,3%. Производительность процесса 2,5 г/час.
Пример 2. В корундовом тигле при температуре 850°C наплавили 400 г хлорида кальция, на который сверху засыпали оксид лантана и оксид бора из расчёта их суммарной концентрации 5 мас.% в соотношении 56% B2O3 и 44% La2O3. После 10 мин выдержки в расплав были опущены графитовый анод и молибденовый катод. Вначале проводили очистной электролиз расплава в течение 60 мин для удаления растворённой воды. Далее электролиз по получению LaB6 вели при температуре 850°С при плотности тока ik =0,40 А/см2 в течение 3 часов.
После окончания электролиза катод с осадком вынимали из расплава и после остывания до комнатной температуры помещали в стеклянный стакан с кипящей дистиллированной водой, в котором осадок отмывали от остатков соли методом декантации. Далее осадок смывали в воронку на бумажный фильтр и дополнительно промывали разбавленной соляной кислотой (10%), затем дистиллированной водой. После этого промытый осадок вместе с фильтром сушили в сушильном шкафу при температуре 80°С. После снятия с фильтра получали мелкодисперсный порошок малинового цвета массой 7 г. осадка. Рентгенофазовый анализ (фиг.2) показал, что порошок представляет собой гексаборид LaВ6. Элементный химический анализ показал наличие примесей алюминия, железа, суммарное содержание которых составляет 0,25 мас.%. Выход продукта по затраченному количеству электричества равен 80%. Производительность процесса 2,3 г/час.
Пример 3. В корундовом тигле при температуре 850°С наплавили 400 г хлорида кальция с добавкой 5% оксида кальция, на который сверху засыпали оксид лантана и оксид бора из расчёта их суммарной концентрации 7 мас.% в соотношении 56% B2O3 и 44% La2O3. После 10 мин выдержки в расплав были опущены графитовый анод и молибденовый катод. Вначале проводили очистной электролиз расплава в течение 60 мин для удаления растворённой воды. Далее электролиз по получению LaB6 вели при температуре 850°С, а затем при постоянной величине тока 6 А и плотности тока ik =0,30 А/см2 в течение 3 часов.
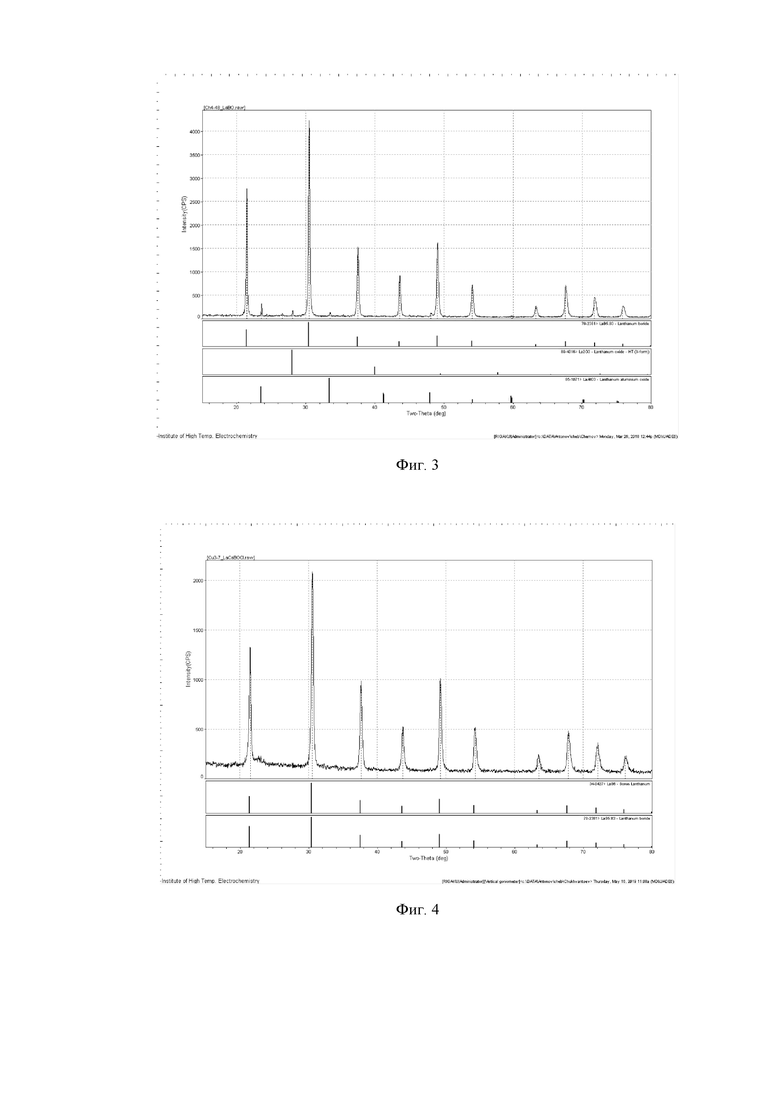
После окончания электролиза катод с осадком вынимали из расплава и после остывания до комнатной температуры помещали в стеклянный стакан с кипящей дистиллированной водой, в котором осадок отмывали от остатков соли методом декантации. Далее осадок смывали в воронку на бумажный фильтр и дополнительно промывали разбавленной соляной кислотой (10%), затем дистиллированной водой. После этого промытый осадок вместе с фильтром сушили в сушильном шкафу при температуре 80°С. После снятия с фильтра получали мелкодисперсный порошок малинового цвета массой 4,5 г. Рентгенофазовый анализ (фиг.3) показал, что порошок представляет собой гексаборид LaВ6. Элементный химический анализ показал наличие примесей алюминия, железа, суммарное содержание которых составляет 0,7 мас.%. Выход продукта по затраченному количеству электричества равен 69%. Производительность процесса 1,5 г/час.
Пример 4. В корундовом тигле при температуре 850°С наплавили 400 г хлорида кальция с добавкой 5% оксида кальция, на который сверху засыпали оксид лантана и оксид бора из расчёта их суммарной концентрации 10 мас.% в соотношении 56% B2O3 и 44% La2O3. После 10 мин выдержки в расплав были опущены графитовый анод и молибденовый катод. Вначале проводили очистной электролиз расплава в течение 60 мин для удаления растворённой воды. Далее электролиз по получению LaB6 вели при температуре 850°С, а затем при постоянной величине тока 10 А и плотности тока ik =0,50 А/см2 в течение 3 часов.
После окончания электролиза катод с осадком вынимали из расплава и после остывания до комнатной температуры помещали в стеклянный стакан с кипящей дистиллированной водой, в котором осадок отмывали от остатков соли методом декантации. Далее осадок смывали в воронку на бумажный фильтр и дополнительно промывали разбавленной соляной кислотой (10%), затем дистиллированной водой. После этого промытый осадок вместе с фильтром сушили в сушильном шкафу при температуре 80°С. После снятия с фильтра получали мелкодисперсный порошок малинового цвета массой 9 г. Рентгенофазовый анализ (фиг.4) показал, что порошок представляет собой гексаборид LaВ6 . Элементный химический анализ показал наличие примесей алюминия, железа, суммарное содержание которых составляет 0,1 мас.%. Выход продукта по затраченному количеству электричества равен 82%. Производительность процесса 3 г/час.
Пример 5. В корундовом тигле при температуре 800°С наплавили 400 г хлорида кальция с добавкой 5% оксида кальция, на который сверху засыпали оксид лантана и оксид бора из расчёта их суммарной концентрации 10 мас.% в соотношении 56% B2O3 и 44% La2O3. После 10 мин выдержки в расплав были опущены графитовый анод и молибденовый катод. Вначале проводили очистной электролиз расплава в течение 60 мин для удаления растворённой воды. Далее электролиз по получению LaB6 вели при температуре 800°С, а затем при постоянной величине тока 10 А и плотности тока ik =0,50 А/см2 в течение 3 часов.
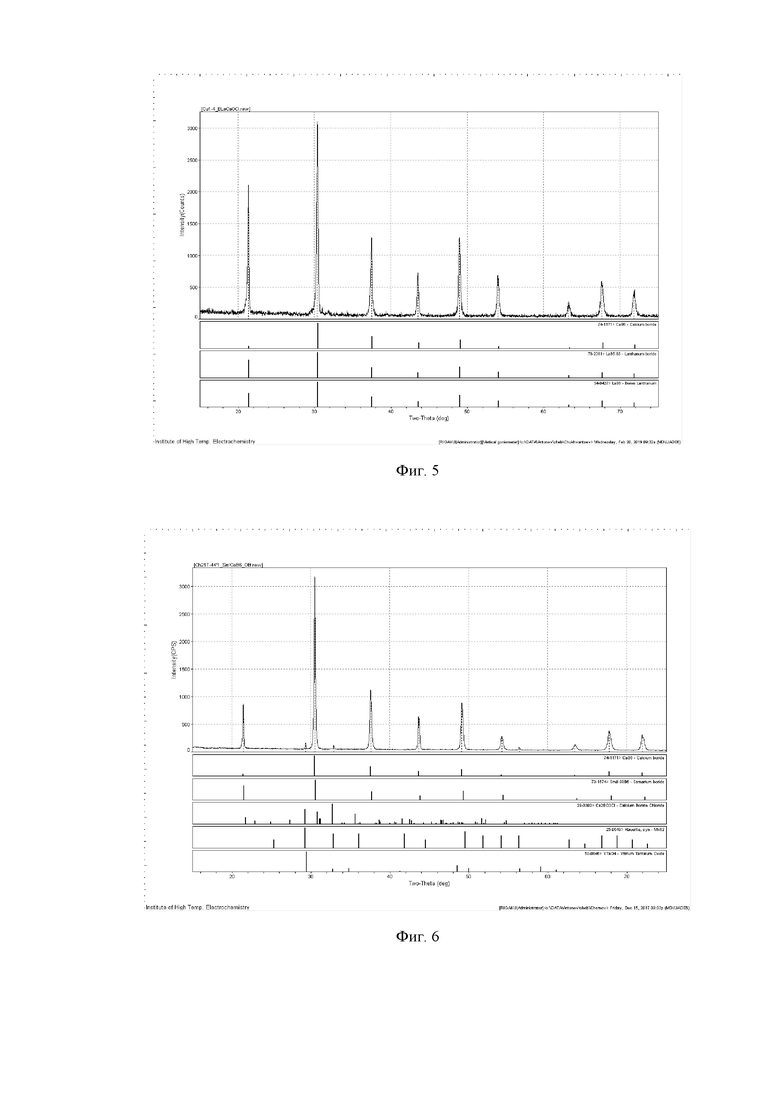
После окончания электролиза катод с осадком вынимали из расплава и после остывания до комнатной температуры помещали в стеклянный стакан с кипящей дистиллированной водой, в котором осадок отмывали от остатков соли методом декантации. Далее осадок смывали в воронку на бумажный фильтр и дополнительно промывали разбавленной соляной кислотой (10%), затем дистиллированной водой. После этого промытый осадок вместе с фильтром сушили в сушильном шкафу при температуре 80°С. После снятия с фильтра получали мелкодисперсный порошок малинового цвета массой 8,5 г. Рентгенофазовый анализ (фиг.5) показал, что порошок представляет собой гексаборид LaВ6. Элементный химический анализ показал наличие примесей алюминия, железа, суммарное содержание которых составляет 0,15 мас.%. Выход продукта по затраченному количеству электричества равен 78%. Производительность процесса 2,83 г/час.
Получение гексаборида самария
В корундовом тигле при температуре 850°С было наплавлено 400 г расплава хлорида кальция с добавкой 5% оксида кальция, на который сверху были засыпали оксиды самария и бора при их суммарной концентрации 7,5% в соотношении 54,5% B2O3 и 45,5% Sm2O3. После 10 минутной выдержки в расплав были опущены графитовый анод и молибденовый катод. Вначале проводили очистной электролиз расплава в течение 30 мин для удаления остаточной примеси воды. Далее электролиз по получению SmB6 вели при той же температуре 850°С, при постоянной плотности тока ik =0,40 А/см2 в течение 2 часов.
После окончания электролиза катод с осадком вынимали из расплава и после остывания до комнатной температуры помещали в стеклянный стакан с кипящей дистиллированной водой, в котором осадок отмывали от остатков соли методом декантации. Далее осадок смывали в воронку на бумажный фильтр и дополнительно промывали разбавленной соляной кислотой (10%), затем дистиллированной водой. После этого промытый осадок вместе с фильтром сушили в сушильном шкафу при температуре 80°С. После снятия с фильтра получали мелкодисперсный порошок черного цвета массой 5 г. Рентгенофазовый анализ (фиг.6) показал, что порошок представляет собой гексаборид SmВ6. Элементный химический анализ показал наличие примесей алюминия, меди и железа, суммарное содержание которых составляет 0,79 мас.%. Теоретическая масса SmB6, вычисленная по закону Фарадея, должна быть 6,1 г, а в действительности получено 5 г. Таким образом, выход продукта по затраченному количеству электричества равен 81%. Производительность процесса 2,5 г/час.
Получение гексаборида гадолиния
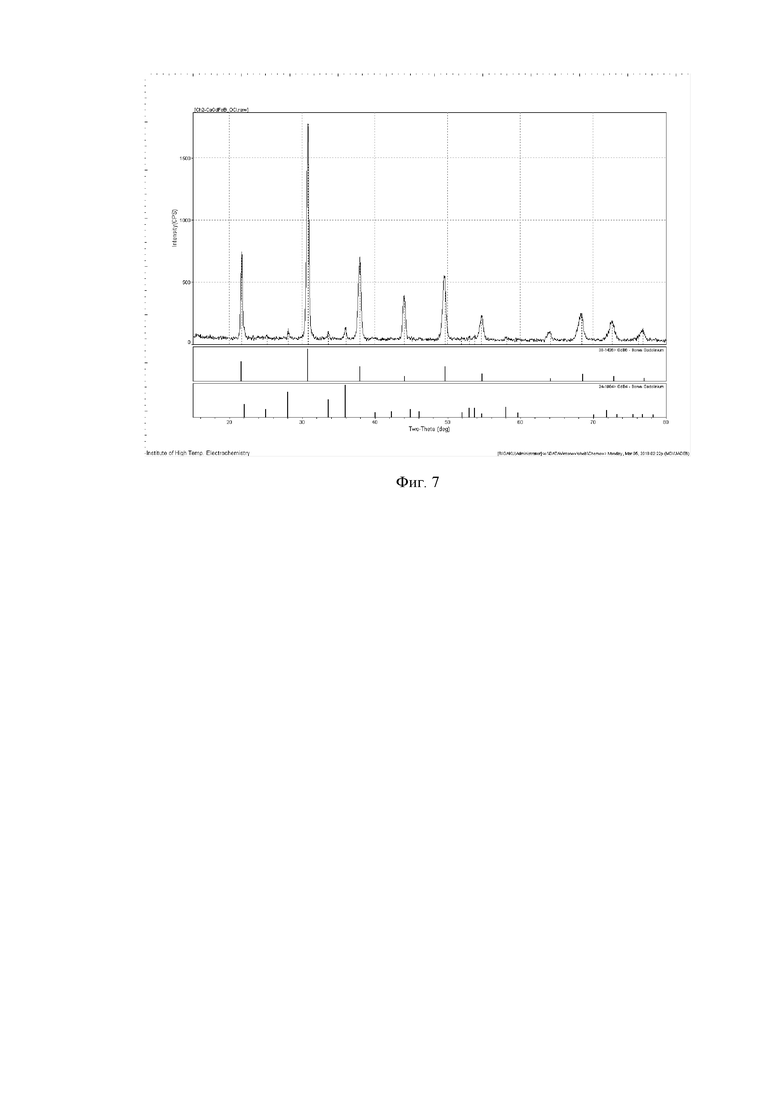
В корундовом тигле при температуре 850°С наплавили 400 г хлорида кальция с добавкой 5% оксида кальция, на который сверху засыпали оксид гадолиния и оксид бора из расчёта их суммарной концентрации 5 мас.% в соотношении 53,5% B2O3 и 46,5% Gd2O3. После 10 мин выдержки в расплав были опущены графитовый анод и молибденовый катод. Вначале проводили очистной электролиз расплава в течение 30 мин для удаления растворённой воды. Далее электролиз по получению GdB6 вели при температуре 850°С при плотности тока ik =0,40 А/см2 в течение 3 часов.
После окончания электролиза катод с осадком вынимали из расплава и после остывания до комнатной температуры помещали в стеклянный стакан с кипящей дистиллированной водой, в котором осадок отмывали от остатков соли методом декантации. Далее осадок смывали в воронку на бумажный фильтр и дополнительно промывали разбавленной соляной кислотой (10%), затем дистиллированной водой. После этого промытый осадок вместе с фильтром сушили в сушильном шкафу при температуре 80°С. После снятия с фильтра получали мелкодисперсный порошок синего цвета массой 7 г. Рентгенофазовый анализ (фиг.7) показал, что порошок представляет собой гексаборид GdВ6. Элементный химический анализ показал наличие примесей алюминия, магния и железа, суммарное содержание которых составляет 0,45 мас.%. Теоретическая масса GdB6, вычисленная по закону Фарадея, должна быть 9,4 г, а в действительности получено 7 г. Таким образом, выход продукта по затраченному количеству электричества равен 74%. Производительность процесса 3,13 г/час.
Таким образом, методом электросинтеза получены порошки гексаборидов лантаноидов LaB6, SmB6, GdB6 с выходом по затраченному току электролиза (КПД) до 82% при упрощении и удешевлении технологии получения и стоимости целевого продукта.
Источники информации
1. Г.В.Самсонов. Тугоплавкие соединения редкоземельных металлов с неметаллами. М.: Металлургия. 1964. - 244 с.
2. K.Uchida. // Surface Technology. 1978. V.7, iss.2. P.137-143.
3. RU 2477340 опубл. 10.03.2013 г.
| название | год | авторы | номер документа |
|---|---|---|---|
| Электрохимический способ получения микродисперсных порошков гексаборидов металлов лантаноидной группы, допированных кальцием | 2021 |
|
RU2781278C1 |
| ЭЛЕКТРОХИМИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ ПОРОШКА ГЕКСАБОРИДА КАЛЬЦИЯ | 2013 |
|
RU2539593C1 |
| Электрохимический способ получения порошков гексаборидов стронция и бария | 2017 |
|
RU2658835C1 |
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ УЛЬТРАДИСПЕРСНОГО ПОРОШКА ГЕКСАБОРИДА ЛАНТАНА | 2011 |
|
RU2477340C2 |
| СПОСОБ ЭЛЕКТРОЛИЗНОГО БОРИРОВАНИЯ СТАЛЬНЫХ ИЗДЕЛИЙ В РАСПЛАВЕ, СОДЕРЖАЩЕМ ОКСИД БОРА | 2011 |
|
RU2478737C1 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОДИСПЕРСНОГО ПОРОШКА ГЕКСАБОРИДА ИТТРИЯ | 2009 |
|
RU2448044C2 |
| Электрохимический способ получения борида молибдена | 2015 |
|
RU2629188C2 |
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ НАНОРАЗМЕРНОГО ПОРОШКА ГЕКСАБОРИДА ЦЕРИЯ | 2013 |
|
RU2540277C1 |
| СОСТАВ РАСПЛАВА ДЛЯ БОРИРОВАНИЯ | 2001 |
|
RU2215060C2 |
| Электрохимический способ получения порошка силицида вольфрама | 2015 |
|
RU2629190C2 |
Изобретение относится к электрохимическому способу получения микродисперсных порошков гексаборидов металлов лантаноидной группы. Способ включает синтез гексаборидов лантаноидов из хлоридсодержащего расплава, содержащего ионы бора и ионы лантаноида. В качестве хлоридсодержащего расплава используют расплав состава (CaCl2 – CaO) с добавками оксида бора B2O3 и оксида получаемого лантаноида Ln2O3. В процессе электролиза концентрации B2O3 и Ln2O3 поддерживают постоянными в количествах, обеспечивающих атомное соотношение бора к лантаноиду B/Ln = 6 при их суммарной концентрации в расплаве 5-10 мас.% от массы электролита. Синтез осуществляют в атмосфере воздуха в интервале температур 800-850°С, при катодной плотности тока 0,3-0,5 А/см2. Предложенный способ позволяет получить порошки гексаборидов лантаноидов с выходом по затраченному току электролиза (КПД) до 82% при упрощении и удешевлении технологии получения и стоимости целевого продукта. 7 ил., 7 пр.
Электрохимический способ получения микродисперсных порошков гексаборидов металлов лантаноидной группы, включающий синтез гексаборидов лантаноидов из хлоридсодержащего расплава, содержащего ионы бора и ионы лантаноида, при этом синтез ведут в газовой атмосфере, отличающийся тем, что в качестве хлоридсодержащего расплава используют расплав состава (CaCl2 – CaO) с добавками оксида бора B2O3 и оксида получаемого лантаноида Ln2O3, причем в процессе электролиза концентрации B2O3 и Ln2O3 поддерживают постоянными в количествах, обеспечивающих атомное соотношение бора к лантаноиду B/Ln = 6 при их суммарной концентрации в расплаве 5-10 мас.% от массы электролита, при этом синтез гексаборидов лантаноидов из хлоридсодержащего расплава осуществляют в атмосфере воздуха в интервале температур 800-850°С, при катодной плотности тока 0,3-0,5 А/см2.
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ УЛЬТРАДИСПЕРСНОГО ПОРОШКА ГЕКСАБОРИДА ЛАНТАНА | 2011 |
|
RU2477340C2 |
| UCHIDA K., Cathodic behavior in the electrodeposition of LaB6, Surface Technology, 1978, v | |||
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Способ приготовления строительного изолирующего материала | 1923 |
|
SU137A1 |
| ЭЛЕКТРОХИМИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ ПОРОШКА ГЕКСАБОРИДА КАЛЬЦИЯ | 2013 |
|
RU2539593C1 |
| ЭЛЕКТРОЛИТИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ НАНОРАЗМЕРНЫХ ПОРОШКОВ ГЕКСАБОРИДА НЕОДИМА | 2008 |
|
RU2389684C2 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОДИСПЕРСНОГО ПОРОШКА ГЕКСАБОРИДА ИТТРИЯ | 2009 |
|
RU2448044C2 |
| US 3902973 A1, 02.09.1975. | |||
Авторы
Даты
2020-06-03—Публикация
2019-12-25—Подача