Изобретение относится к медицине, а именно, к офтальмологии, и может быть использовано в лечении заболеваний органов зрения, в частности, ожогов глаз и катаракты.
Ожоговая травма органов зрения является одной из особо сложных клинических и социальных проблем и по тяжести занимает второе место после проникающих ранений в структуре повреждения органа зрения и регистрируется в 20-42,2% случаев. Основной составляющей взрослого населения с данной патологией (до 70%) являются лица трудоспособного возраста, в возрасте 19-45 лет (63%), преимущественно мужского пола (78%).
Химические ожоги глаз относятся к одному из самых тяжелых видов повреждений органа зрения как по характеру изменения в тканях, так и по исходу. Патологический механизм ожоговой болезни и ее последствий является многофакторным. Согласно литературным данным, при химическом ожоге происходит разрушение мембран эпителия роговицы, нарушается ее архитектоника, химизм, все виды метаболизма, происходят системные изменения в организме (нарушение функций почек, печени, поджелудочной железы). Кроме того, ожоговая травма создает благоприятные условия для развития вторичной инфекции, которая усиливает интоксикацию и отягощает течение ожога. Установлено, что растворы щелочей, взаимодействуя с фосфолипидами плазматических мембран, активируют процессы перекисного окисления липидов, изменяют функциональные и структурные параметры клеточных мембран, что приводит к гибели клетки и проникновению токсических веществ глубоко в ткани. В связи с особенностями кровотока области лимба, в зоне ожога быстро накапливаются токсические продукты, еще более усугубляя патологический процесс. В патогенезе ожоговой травмы лежат фибриноидный синдром, синдром no-reflow, оксидативный стресс, ишемическая нейродеструкция. В течение многих лет ведутся исследования в отношении консервативного лечения ожоговой травмы, ведется поиск наиболее эффективных и безопасных препаратов, изучаются способы и дозы их применения, совершенствуются схемы специфической терапии. В комплексную терапию ожоговой травмы включатся препараты, коррегирующие асептическое воспаление, ускоряющие восстановление поверхности глаза, профилактирующие вторичную инфекцию, купирующие болевой синдром и снижающими внутриглазное давление. Основное направление нейропротекции при ожоговой травме глаза - снижение эксайтотоксичности (ионы магния), энергодефицит (соли янтарной кислоты, тиотриазолин), АФК-зависимые механизмы нейродеструкции (мексидол, эрготеин).
Известен способ лечения ожогов глаз с использованием тиотриазолина. Способ консервативного лечения ожогов глаз заключается в том, что используют 1% раствор тиотриазолина, закапывая его в конъюнктивальную полость глаза четыре раза в день по 2-4 капли и вводят парабульбарно один раз в день 0,5 мл (Патент Украины №21731, МПК (2006) A61F 9/00. Способ консервативного лечения ожогов глаз. - Опубл. 30.04.1998, бюл. №2).
Что же касается катаракты, то возрастная катаракта на сегодняшний день является ведущей причиной излечимой слепоты в мире и наиболее распространенным заболеванием глаз у лиц старше 60 лет. Среди всех офтальмологических заболеваний катаракта составляет около 65%. На 2017 г. более 20 млн. человек во всем мире страдают билатеральной слепотой. Среди всех причин слепоты катаракта занимает около 20%. Растет количество больных катарактой не только среди населения пенсионного возраста, но среди трудоспособного населения, что является не только медицинской, но и социальной проблемой. Наиболее распространено хирургическое лечение катаракты. Однако, на повестку дня ставится вопрос о необходимости разработки эффективных медикаментозных методов профилактики и лечения, основанных на результатах углубленного изучения этиологии и патогенеза помутнений хрусталика.
Имеются многочисленные исследования о роли нарушений белкового обмена, перекисного окисления липидов, энергетического дефицита, а также нарушении кальциевого гомеостаза в патогенезе катаракты. Получены убедительные данные, что дефицит эндогенных антиоксидантов - а-токоферола, глутатиона, карнозина и депривация Se-глутатионпероксидазы приводит к неконтролируемому росту активных форм кислорода (АФК) и окислительной модификации белка. Именно окислительная модификация молекул белка хрусталика, появление в их структуре карбонильных групп приводит к его помутнению. Данные исследования послужили обоснованием для применения антиоксидантов в профилактике и лечении катаракты. Имеются убедительные данные о клинической эффективности селеназы, эмоксипина, в-каротинов, ионола при лечении катаракты.
Известно использование антиоксиданта Тиотриазолина в лечении катаракты в виде 1% глазных капель (https://www.ama.dp.ua/data/doctors/standarts/14/).
Способ лечения ожогов глаз и катаракты при помощи тиотриазолина считаем прототипом.
Однако следует отметить, что в отличие от средства, использованного в предлагаемом способе, в структуре молекулы тиотриазолина не содержится фрагмент аминокислоты L-лизина, который обеспечивает повышение синтеза коллагена, снижение экспрессии провоспалительных цитокинов и усиление реакции иммунного ответа (Вологжанин Д.А., Калинина Н.М., Сосюкин А.Е. и др. Метаболические основы формирования иммунной недостаточности при травматической болезни [Электронный ресурс] // Рос. биомед. журн. Medline. - 2005. - Т. 168, №6. - С. 597-625. http://www.medline.ru).
Кроме того, тиотриазолин не оказывает значимого эффекта при химическом ожоге средней степени тяжести, его эффект был зарегистрирован только при легкой степени ожога роговицы.
Что же касается катаракты, то тиотриазолин оказывает менее выраженное антиоксидантное действие, в частности, он уступает известным средствам по влиянию на тиол-дисульфидную систему хрусталика глаза, менее полноценно нормализуя баланс между ее восстановленными и окисленными интермедиатами. А именно нарушение тиол-дисульфидного равновесия и образование окисленных тиолов приводит к помутнению хрусталика глаза при катаракте.
Общим существенным признаком способа, который заявляется, и прототипа, является следующий:
назначение глазных капель, которые содержат как активное вещество производное 1,2,4-триазола, обладающее антиоксидантным, репаративным, ранозаживляющим и противовоспалительным действием.
В основу изобретения поставлена задача усовершенствования способа лечения ожогов глаз и катаракты путем использования глазных капель, обладающих более сильным терапевтическим эффектом по сравнению с известным, что обеспечит повышение эффективности лечения при практической безвредности вводимого средства.
Поставленная задача решается тем, что в способе лечения ожогов глаз и катаракты путем назначения глазных капель, которые содержат как активное вещество производное 1,2,4-триазола, обладающее антиоксидантным, репаративным, ранозаживляющем и противовоспалительным действием, новым является то, что назначают 1%-2,5% раствор (S)-2,6-диаминогексановой кислоты 3-метил-1,2,4-триазолил-5-тиоацетата (Ангиолин) 3 раза в сутки, при ожогах - в течение 14 суток, а при катаракте - в течение 28 суток.
Причинно-следственная связь между заявляемой совокупностью признаков и достигаемым техническим результатом заключается в следующем.
(S)-2,6-диаминогексановой кислоты 3-метил-1,2,4-триазолил-5-тиоацетат (Ангиолин) проявляет более высокую активность по сравнению с тиотриазолином, так как в структуру его молекулы кроме 3-метил-1,2,4-триазолил-5-тиоацета входит остаток аминокислоты лизина, которая обладает самостоятельным противовоспалительным, иммуномодулирующим и репаративным действием. Кроме того, введение в структуру молекулы (S)-2,6-диаминогексановой кислоты 3-метил-1,2,4-триазолил-5-тиоацетата остатка лизина приводит, по сравнению с тиотриазолином, к значительному снижению токсичности.
Наличие в Ангиолине фрагмента аминокислоты L-лизина обеспечивает ранозаживляющее и противовоспалительное действие за счет повышения синтеза коллагена, снижения экспрессии провоспалительных цитокинов и усиления реакции иммунного ответа. Кроме того, введение L-лизина в структуру молекулы 3-метил-1,2,4-триазолил-5-тиоацетата придает препарату более сильные метаболитотропные, энерготропные и репаративные эффекты и позволяет ликвидировать дефект роговицы при химическом ожоге средней степени тяжести.
Изучалась терапевтическая эффективность 0,5%, 1%, 1,5%, 2% и 2,5% глазных капель. Наиболее эффективными оказались 1% глазные капли, при этом эффективность сохранялась до 2,5% концентрации средства.
Пример 1.
Приводим пример терапевтической эффективности 1% глазных капель на модели экспериментального химического ожога глаз средней степени тяжести у кролей.
Экспериментальные исследования выполнены на 40 глазах 20 кроликов породы Шиншилла обоего пола массой 2,1-3,5 кг. Модель химического ожога воспроизведена по методу Обенбергера (Obenberger, J. Paper strips and rings as simple tools for standardization of experimental eye injuries / J. Obenberger // Ophthalmol. Res. - 1975. - Vol. 7. - P. 363-366) при помощи 10% раствора едкого натра (аппликацией 8 мм круга фильтровальной бумаги), время экспозиции 20 секунд, после предварительной инсталляционной анестезии 0,5%-ным раствором Алкаина. Кроликам с первых суток в конъюнктиву глаза вносили по 0,1 мл глазных капель (Ангиолин) 3 раза в сутки в течение 14 суток. В работе использовали 0,5%; 1,0%; 1,5%; 2,0% и 2,5% капли Ангиолина.
Кроликам контрольной группы вносили тем же объемом физиологический раствор. В каждой группе было по 5 кролей. С первых суток эксперимента проводили офтальмоскопическское обследование животных. Определяли признаки роговичного синдрома - (слезотечение, светобоязнь, режущие боли при раздражении ворсиной, блефароспазм), а также явления хемоза, участки ишемии и поверхностного некроза конъюнктивы, дилятацию сосудов и отек лимба в баллах, которые присваивают в зависимости от выраженности признаков отека, гиперемии, эрозии: 0 баллов - признак отсутствует, 1-балл - признак выражен незначительно, 2-балла - признак выражен умеренно, 3-балла - признак выражен сильно. Дефект роговицы измеряли количественно (диаметр с помощью штангенциркуля).
На 1-е сутки во всех группах животных роговица была недоступна осмотру. С 2-х суток отмечено усиление отека. Только на 3-4-е сутки в контрольной группе роговица была доступна осмотру. У животных был диагностирован ожог средней степени тяжести, т.к к 14 суткам у них определялись: роговичный синдром, явления хемоза, участки ишемии и поверхностного некроза конъюнктивы, дилятация сосудов и отек лимба, роговица напоминала неинтенсивное матовое стекло, серозный иридоциклит с сужением зрачка. Дефект роговицы достигал 6,7 мм (табл. 1). Эпителизация в контрольной группе была завершена полностью у 3 из 5 животных на 14-е сутки, а у 2 животных к этому сроку наблюдения эпителизация не была завершена.
В группах животных, получавших Ангиолин, уже на 2-е сутки лечения роговица была доступна осмотру. Определяли уменьшение дефекта эпителия в виде круга до 3,35 и 2,11 мм к концу 14-х суток. Стоит отметить, что в группах животных, получавших 1%, 1,5%, 2% и 2,5% глазные капли Ангиолина на 14-е сутки отмечалось закрытие дефекта у 2 животных. В группах, получавших Ангиолин, эпителизация протекала быстрее, с ее полным завершением на 8-11 сутки.
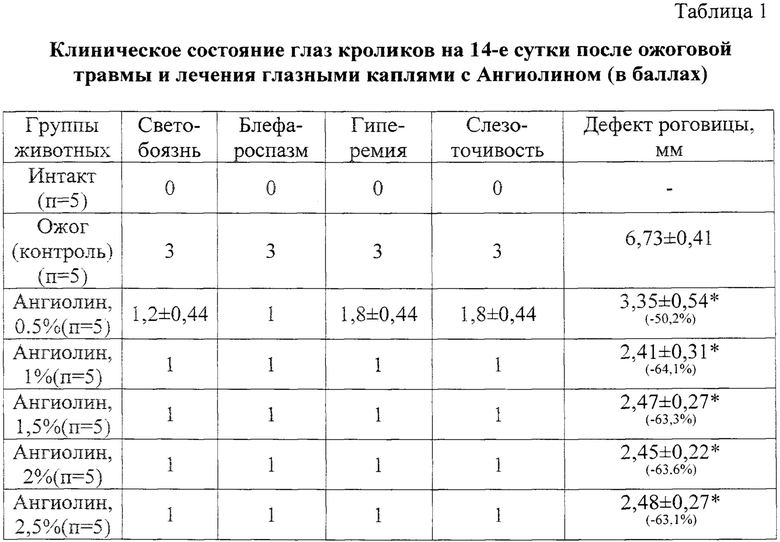
Примечание: 0 баллов - признак отсутствует, 1-балл - признак выражен незначительно, 2-балла - признак выражен умеренно, 3-балла - признак выражен сильно.
* - р<0,05 по отношению к контролю
Таким образом, глазные капли, содержащие Ангиолин в качестве активного ингредиента, проявляют высокую противовоспалительную, ранозаживляющую, репаративную активность при лечении химических ожогов глаз средней степени тяжести.
Пример 2.
Пример эффективности 1% глазных капель Ангиолина в условиях моделирования катаракты.
Исследование проведено на 15 кроликах-самцах (30 глаз) породы Шиншилла средним весом 2-3 кг и возрастом 8-10 месяцев. Исследования выполнены на достаточном количестве экспериментальных животных. Все манипуляции были проведены согласно положению об использовании животных в биомедицинских опытах (Страсбург, 1986 г., с изменениями, внесенными в 1998 г.) и «Загальних етичних принципiв експериментiв на тваринах» ( , 2001), которые согласованы с положениями «Европейской конвенции по защите позвоночных животных, которых используют для экспериментальных и научных целей».
, 2001), которые согласованы с положениями «Европейской конвенции по защите позвоночных животных, которых используют для экспериментальных и научных целей».
На 5 интактных животных (10 глаз) были определены нормальные значения исследуемых показателей. Экспериментальная катаракта воспроизводилась на обоих глазах 10 животных (20 глаз) химической индукцией свободнорадикального окисления биополимеров тканей глаза по методу D.K. Buyan, для чего в стекловидное тело вводили однократно 30 мкл стерильного раствора диквата дибромида в дозе 600 нмоль. Лечение начинали с 7 суток, когда формировались начальные помутнения хрусталиков, и проводили путем инстилляций препаратов в конъюнктивальную полость глаз 3 раза в день. Животные были разделены на три группы.
Первую серию составили интактные животные - 5 животных (10 глаз); вторую группу контрольные животные - с катарактой и без лечения - 5 животных (10 глаз), третью группу - животные с катарактой, получавшие курсом 1% капли «Ангиолин» - 5 животных (10 глаз). Курс лечения составлял 28 суток после 7 суток введения диквата дибромида. По окончании курса лечения (35 сутки эксперимента) животных наркотизировали тиопенталом натрия (40 мг/кг) и энуклеировали глаза и на холоде выделяли хрусталик.
Хрусталик гомогенизировали в гомогенизаторе Поттера в 10-кратном объеме среды при (2°С), содержащей (в ммолях): сахарозы - 250, трис-HCl-буфера - 20, ЭДТА -1 (рН 7,4). При температуре (+4°С) методом дифференциального центрифугирования на рефрижераторной центрифуге Sigma 3-30k (Германия) выделяли цитозольную фракцию. В цитозоле хрусталика определяли интермедиаты тиол-дисульфидной системы, поддерживающей оксидантно/антиоксидантный гомеостаз хрусталика - активность глутатионпероксидазы (ГПР) и глутатионредуктазы (ГР), суммарные SH-группы. Также определяли маркеры окислительной модификации белка - альдегидфенилгидразоны (АФГ) и карбоксифенил гидразоны (КФГ), а также нитротирозин. Активность ГР определяли по спектрофотометрически методике в тесте с окисленным глутатионом и НАДФН. Активность ГПР определяли спектрофотометрически в тесте с гидроперекисью трет-бутила. Содержание восстановленного глутатиона определяли флюорометрически по реакции с о-фталевым ангидридом. Показатели окислительной модификации белка (ОМБ) определяли спектрофотометрически по методу В. Halliwell по взаимодействию окисленных аминокислотных остатков с 2,4-динитрофенил гидразином (2,4-ДНФГ) и образованием альдегидфенилгидразонов (АФГ) и карбоксилфенилгидразона (КФГ), имеющих спектр поглощения при 274 нм 363 нм соответственно. Содержание суммарных SH-групп определяли спектрофотометрически по реакции с 5,5-дитио-бис-7-нитробензойной кислотой. Нитротирозин определяли в цитозольной фракции гомогената твердофазным иммуносорбентным сэндвидж - методом ELISA, ELISA Kit (Cat. № HK 501-02) фирмы Hycult Biotech и выражали в нм/г ткани. Также определяли показатель оптической плотности цитозольной фракции хрусталика, который характеризовал степень помутнения. Этот показатель определяли спектрофотометрически при 440 нм. Результаты исследования рассчитывали с применением стандартного статистического пакета лицензионной программы «STATISTICA® for Windows 6.0» (StatSofflnc, № AXXR712D833214FAN5), a также «SPSS 16.0», «Microsoft Office Excell 2003». Нормальность распределения оценивали по критерию Shapiro-Wilk. Данные представлены в виде среднего значения. Достоверность различий между средними значениями определяли по критерию Стьюдента при нормальном распределении. В случае распределения, отличного от нормального, или анализа порядковых переменных использовали критерий U Mann-Whitney. Для сравнения независимых переменных в более чем двух выборках применяли дисперсионный анализ (ANOVA) при нормальном распределении или критерий Kruskal-Wallis для распределения, отличного от нормального. Для всех видов анализа статистически значимыми считали различия р<0,05 (95%).
Как видно из данных, представленных в таблицах 2 и 3, однократное введение диквата дибромида в стекловидное тело глаза кролика приводит через 7 суток к формированию катаракты. Так, на эти сроки эксперимента у животных контрольной группы наблюдали помутнение хрусталика, о чем свидетельствовало увеличение оптической плотности цитозольной фракции хрусталика на 142%. Помутнения хрусталика происходили на фоне активации оксидативного стресса и угнетения антиоксидатной системы хрусталика (табл. 2 и 3).
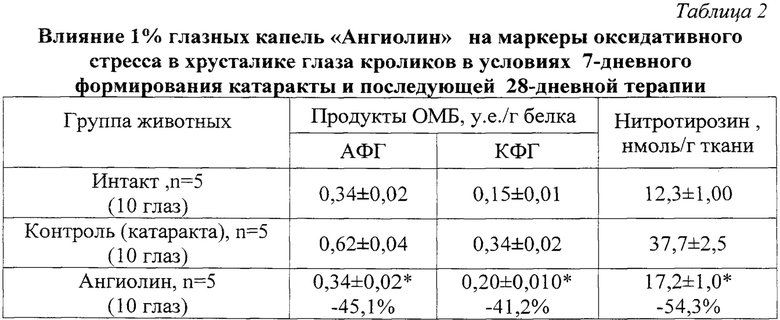
Примечание: *- р<0,05 относительно контроля
В основе помутнения хрусталика лежит окислительная модификация белков, появление в его структуре карбонильных групп. Кроме этого, к помутнению приводит и N-; S-; О-нитрозилирование структурных фрагментов белков хрусталика под действием высокореактивных дериватов NO -пероксинитритом, ионом нитрозония. Так, в цитозольной фракции хрусталика животных контрольной группы наблюдали повышения маркеров окислительной модификации белка - АФГ на 82,3% и КФГ на 133,4%, а также увеличение концентрации нитротирозина на 206,5%. Подобная активация реакций оксидативного стресса происходила на фоне значительного угнетения антиоксидантной функции тиол-дисульфидной системы хрусталика. В цитозоле хрусталика животных контрольной группы регистрировали снижение уровня восстановленного глутатиона на 44,3% и содержания суммарных восстановленных тиольных групп на 73,1%.
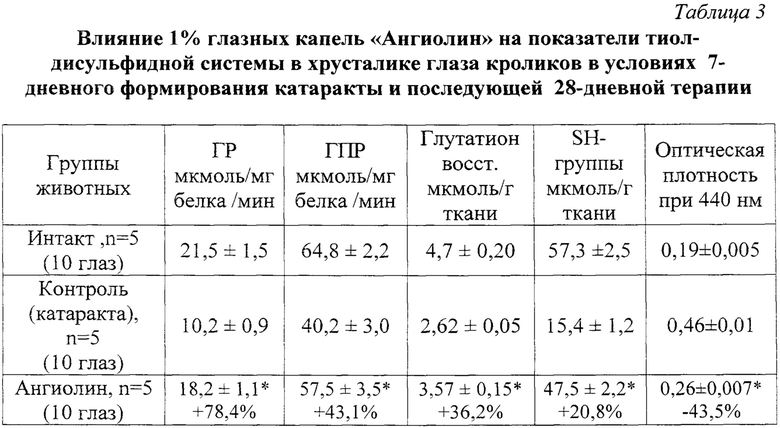
Примечание: * - р<0,05 по отношению к контрольной группе
Курсовое применение 1% глазных капель «Ангиолин» оказывало значительное терапевтическое действие в условиях химической катаракты. Так, применение капель Ангиолина снижало помутнение хрусталика глаза экспериментальных животных на 43,5%» Применение капель Ангиолин приводило и к торможению окислительной модификации - снижению АФГ на 45,1% и КФГ на 41,2%, а также снижению реакций нитрозирующего стресса -уменьшению нитротирозина на 54,3%. Ангиолин оказывал и нормализующее действие на основные показатели тиол-дисульфидной системы хрусталика при моделировании катаракты. Так, в хрусталике глаза экспериментальных животных, получавших курсом капли Ангиолин, регистрировали повышение активности ГПР на 43,1% и ГР на 78,4%. Ангиолин повышал уровень восстановленного глутатиона на 36,2% и содержание суммарных восстановленных тиолов на 20,8% в цитозоле хрусталика экспериментальных животных. В основе механизма антикатарактного действия 1% глазных капель «Ангиолин» лежат его антиоксидантные свойства. Ангиолин является скаведжером активных форм кислорода и NO. Также Ангиолин позитивно влияет на глутатионовое звено тиол-дисульфидной системы, повышая уровень его восстановленных эквивалентов и повышая активность GSH-ферментов. Защитное действие Ангиолина при катаракте реализовывается и за счет повышения экспрессии белка теплового шока - HSP70, который, являясь шапероном, участвует в стабилизации промежуточных конформаций в процессе созревания белков в условиях быстрой адаптации клетки, в ассистировании сборки олигомерных комплексов, а также предотвращении летальной неспецифической ассоциации белков во время оксидативного стресса. HSP70, помимо непосредственной защиты клеточных белков от денатурации и окисления, также с помощью различных механизмов блокирует пути активации апоптоза и стабилизирует клеточные структуры.
Таким образом, можно сделать вывод, что глазные капли, содержащие Ангиолин в качестве активного ингредиента, проявляют значительные противовоспалительные, ранозаживляющие, противоожоговые, репаративные свойства, а также имеют высокий терапевтический эффект при лечении катаракты.
Таким образом, можно сделать вывод, что способ лечения химических ожогов глаз и катаракты с помощью глазных капель, содержащих Ангиолин качестве активного ингредиента, обеспечивает значительный противовоспалительный, ранозаживляющий, противоожоговый, репаративный эффект, а также демонстрирует высокий терапевтический эффект при лечении катаракты.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ раннего консервативного лечения ожогов роговицы легкой и средней степени | 2023 |
|
RU2811887C1 |
| Применение (S)-2,6-диаминогексановой кислоты 3-метил-1,2,4-триазолил-5-тиоацетата как активной основы лекарственных средств для профилактики и лечения нарушений жизнеобеспечивающих функций ЦНС при тяжелых формах острого отравления этанолом | 2016 |
|
RU2613875C1 |
| Способ лечения алкогольной кардиомиопатии | 2017 |
|
RU2642298C1 |
| СПОСОБ КОРРЕКЦИИ НЕВРОЛОГИЧЕСКИХ НАРУШЕНИЙ ПРИ ХРОНИЧЕСКОЙ АЛКОГОЛЬНОЙ ИНТОКСИКАЦИИ | 2014 |
|
RU2561063C1 |
| Глазная мазь на основе 6-метил-3-(тиетан-3-ил)урацила с ранозаживляющим эффектом | 2019 |
|
RU2705392C1 |
| Применение L-лизина тиазотата как активной основы лекарственных средств гепатопротекторного и детоксикационного действия | 2018 |
|
RU2679447C1 |
| ГЛАЗНЫЕ КАПЛИ | 1999 |
|
RU2163123C2 |
| ГЛАЗНЫЕ КАПЛИ | 2002 |
|
RU2216331C1 |
| СПОСОБ ЛЕЧЕНИЯ ОЖОГОВ ГЛАЗА | 2012 |
|
RU2495651C1 |
| Способ лечения катаракты и глазные капли для его осуществления | 2016 |
|
RU2662364C2 |
Изобретение относится к медицине, а именно к экспериментальной медицине и офтальмологии, и может быть использовано для лечения экспериментальных химических ожогов и катаракты, смоделированных на кроликах породы Шиншилла. Для этого в глаза при ожогах закапывают 1%-2,5% раствором (S)-2,6-диаминогексановой кислоты 3-метил-1,2,4-триазолил-5-тиоацетата 3 раза в сутки в течение 14 суток. При катаракте в глаза закапывают 1% раствором (S)-2,6-диаминогексановой кислоты 3-метил-1,2,4-триазолил-5-тиоацетата 3 раза в сутки в течение 28 суток. Способ обеспечивает высокий терапевтический эффект за счёт значительного противовоспалительного, ранозаживляющего, противоожогового, репаративного эффектов вводимого препарата. 3 табл., 2 пр.
Способ лечения экспериментальных химических ожогов и катаракты, смоделированных на кроликах породы Шиншилла, путем введения глазных капель, которые содержат активное вещество производное 1,2,4-триазола, обладающее антиоксидантным, репаративным, ранозаживляющим и противовоспалительным действием, отличающийся тем, что глаза при ожогах закапывают 1%-2,5% раствором (S)-2,6-диаминогексановой кислоты 3-метил-1,2,4-триазолил-5-тиоацетата 3 раза в сутки в течение 14 суток, а при катаракте глаза закапывают 1% раствором (S)-2,6-диаминогексановой кислоты 3-метил-1,2,4-триазолил-5-тиоацетата 3 раза в сутки в течение 28 суток.
| СПОСОБ КОНСЕРВАТИВНОГО ЛЕЧЕНИЯ ОЖОГОВ ГЛАЗ | 1995 |
|
RU2120263C1 |
| ЛИЗИНИЙ 3-МЕТИЛ-1,2,4-ТРИАЗОЛИЛ-5-ТИОАЦЕТАТ, ПРОЯВЛЯЮЩИЙ НЕЙРОПРОТЕКТИВНОЕ, НООТРОПНОЕ, КАРДИОПРОТЕКТИВНОЕ, ЭНДОТЕЛИОТРОПНОЕ, ПРОТИВОИШЕМИЧЕСКОЕ, АНТИОКСИДАНТНОЕ, ПРОТИВОВОСПАЛИТЕЛЬНОЕ И ПРОТИВОГИПОКСИЧЕСКОЕ ДЕЙСТВИЕ, ОБЛАДАЮЩИЙ НИЗКОЙ ТОКСИЧНОСТЬЮ | 2007 |
|
RU2370492C2 |
| СПОСОБ ЛЕЧЕНИЯ ТРАНССУДАТИВНЫХ ФОРМ ЦЕНТРАЛЬНЫХ ХОРИОРЕТИНАЛЬНЫХ ДИСТРОФИЙ | 1996 |
|
RU2120264C1 |
| Средство для лечения заболеваний кожи и слизистых оболочек, для местного применения, обладающее противовоспалительным, антибактериальным, противовирусным, ранозаживляющим, противогрибковым действием | 2016 |
|
RU2626673C1 |
| WO 2013053856 A1, 18.04.2013 | |||
| EA 200801430 A1, 30.12.2008 | |||
| Переносный прибор для проверки действия путевых индукторов точечного индуктивно-резонансного автостопа | 1947 |
|
SU86668A1 |
| Способ ударно-вращательного бурения | 1938 |
|
SU62406A1 |
| Электроизоляционный клеящий материал | 1953 |
|
SU99584A1 |
| ОЧИРОВА Е.К | |||
| и др | |||
| "Медикаментозное лечение ожогов глаз (обзор литературы)" // "Бюллетень ВСНЦ СО РАМН, | |||
Авторы
Даты
2020-01-17—Публикация
2019-02-20—Подача