ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] По заявке испрашивается приоритет предварительной заявки США № 61/279528, поданной 22 октября 2010 года, описание которой, таким образом, в полном объеме включено в настоящий документ посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
[0002] Описание в основном относится к областям геномной инженерии и экспрессии белков в растениях. В частности, настоящее изобретение относится к конструированию ДНК-связывающих доменов, например, белков с цинковыми пальцами, направленных на гены, вовлеченные в синтез жирных кислот, и к способам использования таких белков с цинковыми пальцами для модуляции экспрессии генов, инактивации генов и направленной модификации генов для получения растений с измененными профилями жирных кислот.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
[0003] Диеты с высоким содержанием насыщенных жиров увеличивают содержание липопротеинов низкой плотности (LDL), что, в свою очередь, вызывает отложение холестерина на кровеносных сосудах, предварительное условие тесно, коррелирующее с атеросклерозом и ишемической болезнью сердца (Conner et al., Coronary Heart Disease: Prevention, Complications, and Treatment, J.B. Lippincott, Philadelphia, 1984 pp. 43-64). В отличие от этого показано, что диеты с высоким содержанием мононенасыщенных жиров ослабляют заболевание сердца. Олеиновая кислота, единственная мононенасыщенная жирная кислота в большинстве пищевых растительных масел, снижает LDL также эффективно, как и линолевая кислота, но не влияет на уровни липопротеинов высокой плотности (HDL) (Mensink et al. (1989) New England J. Med., 321:436-441). Кроме того, диеты с высоким содержанием мононенасыщенных жирных кислот также коррелируют со сниженным систолическим артериальным давлением (Williams et al. (1987) J. Am. Med. Assoc., 257:3251-3256, 1987).
[0004] В свете влияния жирных кислот на диету и здоровье проводились попытки изменить профиль жирных кислот растений, используемых в пищевых и промышленных целях. Однако общепринятые способы изменения растений для улучшения профиля жирных кислот основаны на мутагенезе (например, химический, радиационный и т.д.) и/или селекции и требуют времени, трудоемки и не направлены специфически на выбранные гены. См., например, патент США № 5861187.
[0005] Недавно, конструируемые ДНК-связывающие домены, такие как ДНК-связывающие домены мегануклеаз и белки с цинковыми пальцами (ZFP), эффективно использовали для селективной модуляции экспрессии генов и для направленного изменения последовательностей генов у растений (см., например, патенты США №№ 7262054, 7235354, 7220719, 7001768 и 6534261; патентные публикации США №№ 2008/0182332 и с серийным номером США № 12/284888). Белки с цинковыми пальцами (ZFP) представляют собой белки, которые связываются с ДНК, РНК и/или белком специфичным для последовательности образом посредством стабилизированного металлом домена, известного как цинковый палец. См., например, Miller et al. (1985) EMBO J. 4:1609-1614; Rhodes et al. (1993) Sci. Amer. 268(2):56-65; и Klug (1999) J. Mol. Biol. 293:215-218. ZFP, как правило, находятся в факторах транскрипции, и до настоящего времени в нескольких тысячах известных или предполагаемых факторах транскрипции идентифицировано более 10000 последовательностей цинковых пальцев.
[0006] ДНК-связывающие домены также можно использовать с нуклеазными доменами с получением сконструированных нуклеаз. Например, можно изменять ДНК-связывающий домен хоминг-эндонуклеазы с получением новой хоминг-эндонуклеазы. Подобным образом, домены цинковых пальцев также комбинировали с нуклеазными расщепляющими доменами с получением нуклеаз с цинковыми пальцами (ZFN) для специфичного задания двухцепочечного разрыва в области генома, где желательна модификация (например, делеция, мутация, гомологичная рекомбинация или вставка экзогенной последовательности) (см., например, публикации патентных заявок США №№ 2007/0134796; 2005/0064474; 2008/0182332). Конструируемые ZFP значительно облегчают вставку экзогенной последовательности или модификацию эндогенной последовательности в конкретных участках-мишенях у растений и обеспечивают направленное изменение геномов растений с большей эффективностью, чем общепринятые способы (см., например, патенты США №№ 7262054, 7235354, 7220719, 7001768 и 6534261).
[0007] Тем не менее, сохраняется необходимость в композициях и способах для направленного изменения генов, вовлеченных в синтез жирных кислот, для получения растений и растительных продуктов (например, растительных масел), содержащих выбранные жирные кислоты. Посредством продуцирования видов растений со сниженными уровнями конкретных и всех насыщенных жирных кислот в масле семян можно получать масляные пищевые продукты, содержащие меньше насыщенных жирных кислот. Такие продукты приносят пользу для здравоохранения, снижая заболеваемость атеросклерозом и ишемической болезнью сердца.
СУЩНОСТЬ
[0008] Настоящее описание относится к композициям и способам для модуляции экспрессии и направленного изменения в целых растениях или в растительных клетках одного или нескольких генов растений, вовлеченных в биосинтез жирных кислот, таким образом, изменяя состав жирных кислот в целом растении или в растительных клетках. Целые растения или растительные клетки могут принадлежать к односемядольным (однодольным) или двусемянодольным (двудольным) видам растений, включая в некоторых конкретных вариантах осуществления маслопродуцирующие растения, а также включая культивируемые клетки, клетки в растении на любой стадии развития и растительные клетки, выделенные из целого растения, и которые (или их потомство) регенерируют в растения. Растительные клетки могут содержать одну или несколько гомеологичных или паралогичных последовательностей генов, любое количество которых или все из них могут являться мишенью для модификации способами, описываемыми в настоящем документе.
[0009] В одном из аспектов в настоящем документе описан ДНК-связывающий домен (например, белок с цинковыми пальцами (ZFP)), который специфически связывается с геном, вовлеченным в путь биосинтеза жирных кислот у растений. В некоторых вариантах осуществления ген представляет собой ген Brassica napus. В некоторых конкретных вариантах осуществления, ген Brassica napus может кодировать ацетил-КоА-карбоксилазу (ACCазу), β-кетоацил-ACP-синтетазы (KAS, например, KAS I-KAS IV), тиоэстеразу жирных кислот B (FATB, например, FATB1-FATB5, или другие тиоэстеразы пластид), синтазу жирных кислот (FAS), элонгазу жирных кислот (FAE, например, FAE1), тиоэстеразу жирных кислот A (FatA), десатуразу жирных кислот (Fad2, Fad3), G-3-P-дегидрогеназу пластид (GPDH), глицерокиназу (GK), десатуразу белка-носителя стеароилацила (S-ACP-DES) и олеоил-ACP-гидролазу. В некоторых конкретных вариантах осуществления ген может представлять собой ортолог или гомолог этих генов у других видов маслопродуцирующих растений.
[0010] В еще одном дополнительном аспекте также предоставлены слитые белки, содержащие любой из ДНК-связывающих доменов (например, ZFP), описываемых в настоящем документе. В определенных вариантах осуществления слитый белок содержит белок с цинковыми пальцами и домен регуляции транскрипции (например, домен активации или репрессии), также известный как ZFP TF. В других вариантах осуществления слитый белок содержит ZFP и нуклеазный домен с образованием нуклеазы с цинковыми пальцами (ZFN), расщепляющей ген-мишень в представляющей интерес области генома. В определенных вариантах осуществления ZFN включает слитый полипептид, содержащий конструируемый связывающий домен цинковых пальцев со специфичностью к гену, вовлеченному в путь биосинтеза жирных кислот у растений (например, ген, кодирующий ACCазу, KAS I, KAS II, KAS III, KAS IV, FATB1, FATB2, FATB3, FATB4, FATB5, FAS, FAE1, FatA, Fad2, Fad3, GPDH, GK или S-ACP-DES), и домен расщепления, и/или один или несколько слитых полипептидов, содержащих конструируемый связывающий домен цинковых пальцев и полудомен расщепления. В определенных вариантах осуществления связывающие домены цинковых пальцев связываются с участком-мишенью, как показано в таблице 2 или таблице 10A. В определенных вариантах осуществления связывающие домены цинковых пальцев содержат последовательность, выбранную из группы, состоящей из белков с цинковыми пальцами, содержащих домены распознавания (например, единичной цепи), представленные в таблице 1 или таблице 10B. Домены расщепления и полудомены расщепления можно получать, например, из различных рестрикционных эндонуклеаз и/или хоминг-эндонуклеаз. В одном из вариантов осуществления полудомены расщепления получают из рестрикционной эндонуклеазы типа IIS (например, FokI).
[0011] В других аспектах в настоящем документе предоставлены полинуклеотиды, кодирующие любой из ДНК-связывающих доменов (например, белки с цинковыми пальцами) и/или слитые белки, описываемые в настоящем документе. Определенные варианты осуществления, описываемые в настоящем документе, представляет собой экспрессирующий ZFP вектор, содержащий полинуклеотид, кодирующий один или несколько ZFP, описываемых в настоящем документе, функционально связанный с промотором. В одном из вариантов осуществления один или несколько из ZFP представляют собой ZFN.
[0012] ZFP и слитые белки, содержащие эти ZFP, могут связываться с геном, вовлеченным в синтез жирных кислот, и/или расщеплять его в кодирующей области гена или в некодирующей последовательности в гене или рядом с ним, такой как, например, лидерная последовательность, трейлерная последовательность или интрон, или в нетранскрибируемой области, выше или ниже кодирующей области. В определенных вариантах осуществления ZFP или ZFN связываются с кодирующей последовательностью или регуляторной последовательностью гена, вовлеченного в биосинтез жирных кислот, и/или расщепляют их.
[0013] В другом аспекте в настоящем документе описаны композиции, содержащие один или несколько белков, слитых белков или полинуклеотидов, как описано в настоящем документе. Растительные клетки могут содержать один уникальный ген-мишень или несколько паралогичных копий одного и того же гена. Таким образом, композиции могут содержать один или несколько содержащих ZFP белков (и полинуклеотидов, кодирующих их), направленных на один или несколько генов, вовлеченных в синтез жирных кислот в растительной клетке. ZFP могут являться направленными ко всем паралогичным или гомеологичным генам и конкретным выбранным паралогичным или гомеологичным генам в растительной клетке или их сочетанию.
[0014] В другом аспекте в настоящем документе предоставлена растительная клетка-хозяин, содержащая один или несколько белков или полинуклеотидов (например, экспрессирующие ZFP векторы), как описано в настоящем документе. Для полинуклеотидов, растительная клетка-хозяин может являться стабильно трансформированной или транзиторно трансфицированной или являться подвергнутой их сочетанию одним или несколькими экспрессирующими ZFP векторами. В одном из вариантов осуществления один или несколько экспрессирующих ZFP векторов экспрессируют в растительной клетке-хозяине одну или несколько ZFN. В другом варианте осуществления один или несколько экспрессирующих ZFP векторов экспрессируют в растительной клетке-хозяине один или несколько ZFP TF.
[0015] В другом аспекте в настоящем документе описан способ модуляции экспрессии одного или нескольких генов, вовлеченных в биосинтез жирных кислот в растительной клетке, где способ включает: (a) введение в растительную клетку одного или нескольких экспрессирующих векторов, кодирующих один или несколько ZFP TF, которые связываются с участком-мишенью в одном или нескольких генах, вовлеченных в биосинтез жирных кислот, в таких условиях, что происходит экспрессия ZFP TF и модуляция одного или нескольких генов. Модуляция может представлять собой активацию или репрессию. В определенных вариантах осуществления по меньшей мере один участок-мишень находится в гене(ах) ACCазы, KAS I, KAS II, KAS III, KAS IV, FATB1, FATB2, FATB3, FATB4, FATB5, FAS, FAE1, FatA, Fad2, Fad3, GPDH, GK и/или S-ACP-DES. В других вариантах осуществления происходит модуляция более одного гена, вовлеченного в биосинтез жирных кислот. В любом из способов модуляции экспрессии генов, вовлеченных в биосинтез жирных кислот, как описано в настоящем документе, этими способами получают растительные клетки с модифицированным содержанием жирных кислот, например, со снижением количества насыщенных жирных кислот в растительных клетках. В некоторых вариантах осуществления модифицированное содержание жирных кислот в растительных клетках приводит к модифицированному содержанию жирных кислот в семенах растения, например, к снижению количества насыщенных жирных кислот в семенах растения. В некоторых вариантах осуществления растение представляет собой маслопродуцирующее растение с модифицированным содержанием жирных кислот в семенах маслопродуцирующего растения (например, со сниженным содержанием насыщенных жирных кислот). В определенном конкретном варианте осуществления растение представляет собой растение Brassica napus с модифицированным содержанием жирных кислот в семенах растения Brassica napus (например, со сниженным содержанием насыщенных жирных кислот).
[0016] В другом аспекте в настоящем документе описан способ расщепления одного или нескольких генов, вовлеченных в биосинтез жирных кислот в растительной клетке, где способ включает: (a) введение в растительную клетку одного или нескольких экспрессирующих векторов, кодирующих одну или несколько нуклеаз (например, ZFN), которые связываются с участком-мишенью в одном или нескольких генах, вовлеченных в биосинтез жирных кислот, в таких условиях, что происходит экспрессия нуклеаз(ы) (например, ZFN) и расщепление одного или нескольких генов. В определенных вариантах осуществления по меньшей мере один участок-мишень находится в гене, кодирующем ACCазу, KAS I, KAS II, KAS III, KAS IV, FATB1, FATB2, FATB3, FATB4, FATB5, FAS, FAE1, FatA, Fad2, Fad3, GPDH, GK и/или S-ACP-DES. В других вариантах осуществления расщепляется более одного гена, вовлеченного в биосинтез жирных кислот. Кроме того, в любом из способов, описываемых в настоящем документе, расщепление одного или нескольких генов должно приводить к делеции, добавлению и/или замене нуклеотидов в расщепляемой области.
[0017] В еще одном аспекте в настоящем документе описан способ введения в геном растительной клетки экзогенной последовательности, где способ включает стадии: (a) приведения клетки в контакт с экзогенной последовательностью (донорный вектор) и (b) экспрессию в клетке одной или нескольких нуклеаз (например, нуклеаз с цинковыми пальцами), как описано в настоящем документе, где одна или несколько нуклеаз расщепляют хромосомную ДНК так, что расщепление хромосомной ДНК на этапе (b) стимулирует встраивание донорного вектора в геном посредством гомологичной рекомбинации. В определенных вариантах осуществления одна или несколько нуклеаз представляют собой слияния домена расщепления рестрикционной эндонуклеазы типа IIs и сконструированного связывающего домена цинковых пальцев. В других вариантах осуществления нуклеаза содержит хоминг-эндонуклеазу, например, хоминг-эндонуклеазу с модифицированным ДНК-связывающим доменом. В любом из способов, описываемых в настоящем документе, экзогенная последовательность может кодировать белковый продукт.
[0018] В еще одном дополнительном аспекте также предоставлена трансгенная или нетрансгенная растительная клетка, получаемая любым из способов, описанных в настоящем документе.
[0019] В другом аспекте в настоящем документе предоставлено растение, содержащее трансгенную или нетрансгенную растительную клетку, полученную, как описано в настоящем документе.
[0020] В другом аспекте в настоящем документе предоставлено семя растения, содержащее трансгенную или нетрансгенную растительную клетку, полученную, как описано в настоящем документе.
[0021] В другом аспекте в настоящем документе предоставлено масло из семян, получаемое из растения, содержащего трансгенную или нетрансгенную растительную клетку, полученную, как описано в настоящем документе.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0022] Фигура 1 представляет собой схематическое изображение путей биосинтеза жирных кислот в каноле (B. napus). Оно адаптировано по John Shanklin, Brookhaven National Laboratory, Upton, NY (Thelen and Ohlrogge, 2002, Metabolic engineering 4:12-21).
[0023] Фигура 2 представляет собой схематическое изображение положений участков-мишеней в гене KASII для различных иллюстративных направленных на KASII ZFP TF. Числа обозначают участки-мишени ZFP, содержащиеся в конструкциях, приведенных в таблице III. Составы ZFP приведены в таблицах I и II.
[0024] Фигура 3 представляет собой изображение экспрессии мРНК KASII в листьях растений T0, трансформированных активирующей KASII конструкцией ZFP TF 4695, как определено посредством кПЦР-РВ, в виде диаграммы. Для расчета кратности возрастания экспрессии, представленной на диаграмме, применяли среднее по 27 контрольным растениям. В определенных случаях наблюдали более чем 3-кратное возрастание экспрессии мРНК KASII.
[0025] Фигура 4 представляет собой изображение отношений экспрессии KASII-ZFP TF/тубулина в листьях растений T1, детектируемой кПЦР-РВ, в виде диаграммы. Сравнивали три случая вместе с соответствующими нулевыми значениями.
[0026] Фигура 5 представляет собой изображение в виде диаграммы средних отношений экспрессии мРНК KASII/тубулина в содержащих ZFP TF и сегрегирующих ноль-растений T1, каждого из трех событий, как определено посредством кПЦР-РВ. В листья этих растений T1 наблюдали 2-3-кратное повышение экспрессии мРНК KASII.
[0027] Фигуры 6A и 6B представляют собой диаграммы, полученные с применением статистического программного обеспечения JMP для однофакторного анализа жирных кислот(ы)-мишеней, демонстрирующие согласованное и значимое (p = <0,001) снижение всех C16 (6A) и снижение отношений всех C16/всех C18 (6B) в положительных по ZFP TF растений и сестринских ноль-растений в каждом случае. Все C16 включали содержание C16:0 и C16:1, а все C18 включали содержание C18:0, 18:1, 18:2 и 18:3.
[0028] На фигуре 7 приведено выравнивание последовательностей AF318307 и AF244520. Затенение означает области точной гомологии.
[0029] На фигуре 8 приведено выравнивание последовательностей SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:46, SEQ ID NO:30, AC189461 и BH723504. пунктирными линиями над соответствующей последовательностью выделены последовательности прямого и обратного праймеров (SEQ ID NO:28 и 29) для амплификации кДНК β-кетоацил-ACP-синтетазы II. Затенение означает области точной гомологии.
[0030] На фигуре 9 изображена экспрессия генов FatB4 и FatB5 в трансгенных линиях каллюсов B. napus для различных составов ZFP TF, присутствующих в конструкциях pDAB4690-pDAB4692. Анализировали 17 линий для контроля и 25 линий для каждой из конструкций ZFP. Черные столбцы = экспрессия мРНК FatB4; серые столбцы = экспрессия мРНК FatB5.
[0031] На фигуре 10 представлены экспрессии FatB4 и FatB5 в листьях трансгенных растений T0 B. napus, анализируемых с использованием кПЦР-РВ. В трансгенных растениях тестировали три конструкции, содержащие ZFP TF, pDAB4689-pDAB4691. Общее количество независимых трансгенных растений T0, анализируемых в этом эксперименте, составляло 40, 62, 41 и 22 для pDAB4689-pDAB4691 и pDAB8210. соответственно. Контроль Nex710 состоял из 10 растений. Положительными по экспрессии ZFP TF являлись девяносто семь процентов случаев переноса трансгена для 3 конструкций ZFP TF, как определено посредством анализа экспрессии ZFP TF (пример 8.3). Подобные результаты получали, когда посредством эталона для нормализации экспрессии генов FatB использовали экспрессию мРНК природного тубулина. Черный столбец = экспрессия FatB4; серый столбец = экспрессия FatB5.
[0032] Фигура 11 представляет собой диаграмму, демонстрирующую линейную зависимость между экспрессией генов FatB и тубулина при анализе растений T1. Черные квадраты = экспрессия FatB4; серые ромбы = экспрессия FatB5.
[0033] На фигуре 12 представлена кПЦР-РВ для экспрессии FatB4 и FatB5 в листьях растений T1, трансгенных по конструкции ZFP TF pDAB4691. Черные квадраты = экспрессия FatB4; серые ромбы = экспрессия FatB5.
[0034] Фигура 13 представляет собой однофакторный анализ содержания C18:0 на образец с использованием статистического программного обеспечения JMP.
[0035] На фигуре 14 представлен однофакторный анализ общего содержания C16/C18 на образец с использованием программного обеспечения для статистического анализа JMP.
[0036] На фигуре 15 представлен анализ профилей FA T1 зрелых семян, содержащих 4 случая с конструкциями ZFP TF, продемонстрированный с использованием статистического программного обеспечения JMP. На панелях A и B представлен однофакторный анализ содержания C18:0 и содержания C16:0/C18:0 на образец (конструкцию), соответственно.
[0037] На фигуре 16 представлен анализ профилей FA T1 зрелых семян, содержащих 4 случая с конструкциями ZFP TF, продемонстрированный с использованием статистического программного обеспечения JMP. На панелях A и B представлен однофакторный анализ содержания C14:0 и содержания C16:1 на образец (конструкцию), соответственно, подчеркивающий дифференцирующее свойство конструкции pDAS5227. Анализ профилей FA T1 зрелых семян, содержащих 4 случая с конструкциями ZFP TF, продемонстрирован с использованием статистического программного обеспечения JMP. На панелях A и B представлен однофакторный анализ содержания C14:0 и C16:1 на образец (конструкцию), соответственно, подчеркивающий дифференцирующее свойство конструкции pDAS5227.
[0038] На фигуре 17 продемонстрировано снижение экспрессии мРНК FatB5 (черные столбцы) в незрелых семенах T2, трансформированных конструкцией с ZFP TF pDAS5227. Экспрессия ZFP TF представлена экспрессией ERF3 (серые столбцы). Анализировали незрелые семена на 25 DAF из четырех ноль-растений, трех гетерозиготных (5227_12ZF-1) и четырех гомозиготных (5227_12ZF-2) растений T1 в случае 5227-12.
[0039] На фигуре 18 представлено снижение экспрессии мРНК FatB5 (черные столбцы) в незрелых семенах T2, трансформированных конструкцией с ZFP TF pDAS5212. Экспрессия мРНК ZFP TF представлена экспрессией KRAB1 (серые столбцы). Анализировали незрелые семена на 25 DAF из пяти ноль-растений, трех гетерозиготных и четырех гомозиготных растений в случае 5212-4.
[0040] На фигуре 19 представлен однофакторный анализ всех насыщенных жирных кислот (насыщ.) в соответствии с зиготностью семян T2 в случае 5227-12 с ZFP TF. Семена T2, полученные из ноль-растений, гетерозиготных и гомозиготных исходных растений T1, помечали как 5227-12ZF ноль, 5227-12ZF(1) и 5227-12ZF(2), соответственно.
[0041] На фигуре 20 представлен однофакторный анализ всех насыщенных жирных кислот (насыщ.) в соответствии с зиготностью семян T2 в случае 5227-4 с ZFP TF. Семена T2, полученные из растений отрицательного контроля, гетерозиготных и гомозиготных исходных растений T1, помечали как 5227-4ZF ноль, 5227-4ZF(1) и 5227-4ZF(2), соответственно.
ПОДРОБНОЕ ОПИСАНИЕ
[0042] В настоящем документе описаны композиции и способы, пригодные для модуляции экспрессии и направленного расщепления и изменения одного или нескольких генов, вовлеченных в синтез жирных кислот у растений. Регуляцию таких генов можно модулировать, например, используя конструируемые факторы транскрипции с ZFP или модифицируя регуляторные области гена. Гены можно изменять, например, посредством направленного расщепления с последующей внутрихромосомной гомологичной рекомбинацией или посредством направленного расщепления с последующей гомологичной рекомбинацией между экзогенным полинуклеотидом (содержащим одну или несколько областей гомологии с нуклеотидной последовательностью гена) и геномной последовательностью.
[0043] Геномные последовательности включают последовательности, присутствующие в хромосомах, эписомах, геномах органелл (например, митохондрий, пластид), искусственных хромосомах и нуклеиновой кислоте любого другого типа, присутствующие в клетке, например, такие как амплифицированные последовательности, двойные микрохромосомы и геномы эндогенных или инфицирующих бактерий и вирусов. Геномные последовательности могут являться нормальными (т.е., дикого типа) или мутантными; мутантные последовательности могут содержать, например, вставки, делеции, транслокации, перестановки и/или точечные мутации. Геномная последовательность также может содержать один из ряда различных аллелей.
[0044] Композиции, описываемые в настоящем документе, содержат один или несколько ZFP, содержащих конструируемые связывающие домены цинковых пальцев, полинуклеотиды, кодирующие эти полипептиды и комбинации ZFP и кодирующих ZFP полинуклеотидов. Связывающий домен цинковых пальцев может содержать один или несколько цинковых пальцев (например, 2, 3, 4, 5, 6, 7, 8, 9 или более цинковых пальцев), и его можно конструировать для связывания с любой геномной последовательностью гена, включая регуляторные последовательности, функционально связанные с геном, вовлеченным в биосинтез жирных кислот.
[0045] Как описано в настоящем документе, ZFP можно использовать для регуляции экспрессии гена посредством активации или репрессии транскрипции гена. Можно конструировать ZFP, содержащие слияния доменов цинковых пальцев, связанных с регуляторными доменами, с получением химерных факторов транскрипции, активирующих или репрессирующих транскрипцию. ZFP также можно использовать для направленного расщепления представляющей интерес области генома, посредством связывания доменов цинковых пальцев с доменами расщепления нуклеаз (или полудоменами расщепления) с получением нуклеаз с цинковыми пальцами. Таким образом, при идентификации представляющей интерес области-мишени генома, для которой желательны регуляция, расщепление или рекомбинация гена, способами, описываемыми в настоящем документе, можно конструировать белок с цинковыми пальцами, содержащий один или несколько слитых белков, содержащих один или несколько регуляторных доменов и/или доменов расщепления (или полудоменов расщепления), связанных с доменом цинковых пальцев, сконструированным для распознавания генной последовательности в этой геномной области. Присутствие такого содержащего ZFP слитого белка (или белков) в клетке приводит к связыванию слитого белка(ов) с его (их) участком(ами) связывания и изменяет регуляцию или расщепление геномной области или области рядом с ней. Кроме того, если расщепляют геномную область и в клетке также присутствует экзогенный полинуклеотид, гомологичный этой геномной области, между геномной областью и экзогенным полинуклеотидом с высокой вероятностью происходит гомологичная рекомбинация.
[0046] Как показано на фигуре 1, существует несколько генов, вовлеченных в биосинтез жирных кислот. Таким образом, композиции, описываемые в настоящем документе, могут являться направленными на один или несколько из этих генов в растительной клетке, включая в качестве неограничивающих примеров ген(ы) ACCазы, KAS I, KAS II, KAS III, KAS IV, FATB1, FATB2, FATB3, FATB4, FATB5, FAS, FAE1, FatA, Fad2, Fad3, GPDH, GK или S-ACP-DES и ортологи, паралоги и гомеологи этих генов. Например, белки (например, ZFP), описываемые в настоящем документе, могут являться направленными на 1, 2, 3, 4, 5 или более генов, вовлеченных в биосинтез жирных кислот. Таким образом, для направления на представляющие интерес желаемые гены в растении можно комбинировать один или несколько ZFP или экспрессирующих векторов, кодирующих ZFP, различной специфичности.
Общая часть
[0047] Если не указано иначе, при практическом применении способов, а также при получении и применении композиций, описываемых в настоящем документе, используют общепринятые способы в областях молекулярной биологии, биохимии, структуры и анализа хроматина, вычислительной химии, культивирования клеток, рекомбинантных ДНК и связанных областях, как известно специалистам в данной области. Эти способы полностью описаны в литературе. См., например, Sambrook et al. MOLECULAR CLONING: A LABORATORY MANUAL, Second edition, Cold Spring Harbor Laboratory Press, 1989 and Third edition, 2001; Ausubel et al., CURRENT PROTOCOLS IN MOLECULAR BIOLOGY, John Wiley & Sons, New York, 1987 and periodic updates; the series METHODS IN ENZYMOLOGY, Academic Press, San Diego; Wolffe, CHROMATIN STRUCTURE AND FUNCTION, Third edition, Academic Press, San Diego, 1998; METHODS IN ENZYMOLOGY, Vol. 304, "Chromatin" (P.M. Wassarman and A. P. Wolffe, eds.), Academic Press, San Diego, 1999; и METHODS IN MOLECULAR BIOLOGY, Vol. 119, "Chromatin Protocols" (P.B. Becker, ed.) Humana Press, Totowa, 1999.
Определения
[0048] Термины "нуклеиновая кислота", "полинуклеотид" и "олигонуклеотид" используют взаимозаменяемо, и они относятся к дезоксирибонуклеотидному или рибонуклеотидному полимеру, в линейной или кольцевой конформация, и в одно- или двухцепочечной форме. Для целей настоящего описания эти термины не следует рассматривать как ограничивающие в отношении длины полимера. Термины могут включать известные аналоги природных нуклеотидов, а также нуклеотиды, которые модифицированы по группам основания, сахара и/или фосфата (например, тиофосфатные каркасы). Как правило, аналог конкретного нуклеотида обладает той же специфичностью спаривания оснований; например, аналог A образует пару оснований с T.
[0049] Термины "полипептид", "пептид" и "белок" используют взаимозаменяемо для обозначения полимера из аминокислотных остатков. Термин также используют для полимеров из аминокислот, в которых одна или несколько аминокислот представляют собой химические аналоги или модифицированные производные соответствующих природных аминокислот.
[0050] "Связывание" относится к специфичному для последовательности нековалентному взаимодействию между макромолекулами (например, между белком и нуклеиновой кислотой). Не все компоненты связывающего взаимодействия должны являться специфичными для последовательности (например, контакты с фосфатными остатками в каркасе ДНК), при условии, что в целом взаимодействие является специфичным для последовательности. Такие взаимодействия, как правило, характеризуются константой диссоциации (Kd) 10-6 M-1 или ниже. "Аффинность" относится к силе связывания: более высокая аффинность связывания коррелирует с меньшей Kd.
[0051] "Связывающий белок" представляет собой белок, способный нековалентно связываться с другой молекулой. Связывающий белок может связываться, например, с молекулой ДНК (ДНК-связывающий белок), молекулой РНК (РНК-связывающий белок) и/или молекулой белка (белок-связывающий белок). В случае белок-связывающего белка, он может связываться сам с собой (с формированием гомодимеров, гомотримеров и т.д.), и/или он может связываться с одной или несколькими молекулами другого белка или белков. Связывающий белок может обладать более чем одним типом связывающей активности. Например, белки с цинковыми пальцами обладают ДНК-связывающей, РНК-связывающей и белок-связывающей активностью.
[0052] "ДНК-связывающий белок с цинковыми пальцами" (или связывающий домен) представляет собой белок или домен в более крупном белке, который связывает ДНК специфичным для последовательности образом посредством одного или нескольких цинковых пальцев, которые представляют собой области аминокислотной последовательности в связывающем домене, структура которых стабилизирована посредством координационного взаимодействия с ионом цинка. Термин ДНК-связывающий белок с цинковыми пальцами часто сокращают как белок с цинковыми пальцами или ZFP.
[0053] Связывающие домены цинковых пальцев могут являться "конструируемыми" для связывания с предопределенной нуклеотидной последовательностью (например, последовательностью-мишенью в любом гене, вовлеченном в биосинтез жирных кислот). Неограничивающие примеры способов конструирования белков с цинковыми пальцами представляют собой составление и отбор. Составленный белок с цинковыми пальцами представляет собой белок, не встречающийся в природе, состав/композиция которого в основном являются результатом рациональных критериев. Рациональные критерии составления включают применение правил замен и компьютеризированных алгоритмов для обработки информации в базе данных, хранящей информацию о существующих конструкциях ZFP и данных связывания. См., например, патенты США 6140081; 6453242; 6534261 и 6785613; также см. WO 98/53058; WO 98/53059; WO 98/53060; WO 02/016536 и WO 03/016496 и патенты США 6746838; 6866997 и 7030215. Таким образом, "конструируемый" белок с цинковыми пальцами или "неприродный" белок с цинковыми пальцами представляет собой белок, в котором один или несколько компонентов ДНК-связывающих доменов цинковых пальцев (распознающих спиралей) являются неприродными и сконструированы для связывания с предварительно выбранным участком-мишенью.
[0054] "Отобранный" белок с цинковыми пальцами представляет собой белок, не встречающийся в природе, получение которого преимущественно является результатом эмпирического способа, такого как фаговый дисплей, улавливание взаимодействий или отбор гибридов. См. например, US 5789538; US 5925523; US 6007988; US 6013453; US 6200759; US 6733970; US RE39229 и WO 95/19431; WO 96/06166; WO 98/53057; WO 98/54311; WO 00/27878; WO 01/60970 WO 01/88197 и WO 02/099084.
[0055] Термин "последовательность" относится к нуклеотидной последовательности любой длины, которая может представлять собой ДНК или РНК; может являться линейной, кольцевой или разветвленной и может являться одноцепочечной или двухцепочечной. Термин "донорная последовательность" относится к нуклеотидной последовательности, которая вставлена в геном. Донорная последовательность может обладать любой длиной, например, длиной от 2 до 25000 нуклеотидов (или любым целочисленным значением между ними или большим), предпочтительно - длиной приблизительно от 100 до 5000 нуклеотидов (или любым целочисленным значением между ними), более предпочтительно - длиной приблизительно от 200 до 2500 нуклеотидов.
[0056] "Гомологичная последовательность" относится к первой последовательности, обладающей определенной степенью идентичности последовательностей со второй последовательностью, и последовательность которой может быть идентична последовательности второй последовательности. "Гомологичная неидентичная последовательность" относится к первой последовательности, обладающей определенной степенью идентичности последовательностей со второй последовательностью, но последовательность которой не является идентичной последовательности второй последовательности. Например, полинуклеотид, содержащий последовательность дикого типа мутантного гена, гомологичен и неидентичен последовательности мутантного гена. В определенных вариантах осуществления степень гомологии между двумя последовательностями является достаточной для обеспечения гомологичной рекомбинации между ними с использованием нормальных клеточных механизмов. Длина двух гомологичных неидентичных последовательностей может являться любой, а их степень негомологичности может быть настолько малой, как единичный нуклеотид (например, для коррекции точечной геномной мутации посредством гомологичной рекомбинации) или настолько большой, как 10 или более тысяч пар оснований (например, для вставки гена в предопределенный участок хромосомы). Длина двух полинуклеотидов, содержащих гомологичные неидентичные последовательности, не должна являться одинаковой. Например, можно использовать экзогенный полинуклеотид (т.е., донорный полинуклеотид) длиной от 20 до 10000 нуклеотидов или пар нуклеотидов.
[0057] Способы определения идентичности нуклеиновых кислот и аминокислотных последовательностей известны в данной области. Как правило, такие способы включают определение нуклеотидной последовательности мРНК гена и/или определение аминокислотной последовательности, кодируемой ей, и сравнение этих последовательностей со второй нуклеотидной или аминокислотной последовательностью. Геномные последовательности также можно определять и сравнивать таким способом. В основном, идентичность относится к точному соответствию нуклеотид-к-нуклеотиду или аминокислота-к-аминокислоте двух полинуклеотидных или полипептидных последовательностей, соответственно. Две или более последовательностей (полинуклеотидных или аминокислотных) можно сравнивать, определяя процент их идентичности. Процент идентичности двух последовательностей, последовательностей нуклеиновой кислоты или аминокислотных последовательностей, представляет собой число точных соответствий между двумя выровненными последовательностями, разделенное на длину более коротких последовательностей и умноженное на 100. Приблизительное выравнивание последовательностей нуклеиновой кислоты обеспечивает алгоритм локальной гомологии Smith and Waterman, Advances in Applied Mathematics 2:482-489 (1981). Этот алгоритм можно применять для аминокислотных последовательностей, используя оценочную матрицу, разработанную Dayhoff, Atlas of Protein Sequences and Structure, M.O. Dayhoff ed., 5 suppl. 3:353-358, National Biomedical Research Foundation, Washington, D.C., USA, и нормализованную Gribskov, Nucl. Acids Res. 14(6):6745-6763 (1986). Иллюстративная реализация этого алгоритма с определением процента идентичности последовательностей предоставлена Genetics Computer Group (Madison, WI) в практическом приложении "BestFit". Параметры по умолчанию для этого способа описаны в руководстве Wisconsin Sequence Analysis Package Program Manual, Version 8 (1995) (доступной в Genetics Computer Group, Madison, WI). Предпочтительным способом определения процента идентичности в контексте настоящего описания является использование пакета программ MPSRCH, принадлежащего University of Edinburgh, разработанного John F. Collins и Shane S. Sturrok и распространяемого IntelliGenetics, Inc. (Mountain View, CA). Из этого семейства пакетов можно использовать алгоритм Смита-Уотермана, где для оценочной таблицы используют параметры по умолчанию (например, штраф за создание пропуска 12, штраф за продление пропуска единица, и пропуск - шесть). В получаемых данных значение "совпадает" означает идентичность последовательностей. В данной области известны другие подходящие программы для расчета процента идентичности или сходства между последовательностями, например, другой программой выравнивания является BLAST, используемый с параметрами по умолчанию. Например, можно использовать BLASTN и BLASTP с использованием следующих параметров по умолчанию: генетический код=стандартный; фильтр=отсутствует; цепь=обе; порог=60; ожидание=10; матрица=BLOSUM62; описания=50 последовательностей; сортировка=по наибольшему показателю; базы данных=невырожденная, GenBank+EMBL+DDBJ+PDB+трансляции GenBank в CDS+Swiss protein+Spupdate+PIR. Подробности об этих программах можно найти в Интернете. В отношении последовательностей, описываемых в настоящем документе, диапазон желаемых степеней идентичности последовательностей составляет приблизительно от 35% до 100% и любое целочисленное значение между ними. Как правило, процент идентичности последовательностей составляет по меньшей мере 35%-40%; 40%-45%; 45%-50%; 50%-60%; 60%-70%; 70-75%, предпочтительно 80-82%, более предпочтительно 85-90%, даже более предпочтительно 92%, еще более предпочтительно 95%, а наиболее предпочтительно 98%.
[0058] Альтернативно, степень сходства последовательностей полинуклеотидов можно определять посредством гибридизации полинуклеотидов в условиях, допускающих формирование стабильных дуплексов между гомологичными областями, с последующим расщеплением специфичной к одиночной цепи нуклеазой(ами) и определением размеров расщепленных фрагментов. Две последовательности нуклеиновых кислот или две полипептидных последовательности являются в значительной степени гомологичными друг другу, когда идентичность последовательностей составляет по меньшей мере приблизительно 70%-75%, предпочтительно 80%-82%, более предпочтительно 85%-90%, даже более предпочтительно 92%, еще более предпочтительно 95%, а наиболее предпочтительно 98% по сравнению с определенной длиной молекулы, как определяют описанными выше способами. Как применяют в настоящем документе, в значительной степени гомологичные также относится к последовательностям, демонстрирующим полную идентичность с конкретной последовательностью ДНК или полипептидной последовательностью. Последовательности ДНК, гомологичные в значительной степени, можно идентифицировать в эксперименте гибридизации по Саузерну, например, в жестких условиях, как определено для конкретной системы. Определение подходящих условий гибридизации известно специалистам в данной области. См., например, Sambrook et al., выше; Nucleic Acid Hybridization: A Practical Approach, editors B.D. Hames and S.J. Higgins, (1985) Oxford; Washington, DC; IRL Press.
[0059] Селективную гибридизацию двух фрагментов нуклеиновой кислоты можно определять, как указано ниже. Степень идентичности последовательностей двух молекул нуклеиновой кислоты влияет на эффективность и силу событий гибридизации между такими молекулами. Частично идентичная последовательность нуклеиновой кислоты по меньшей мере частично ингибирует гибридизацию полностью идентичной последовательности с молекулой-мишенью. Ингибирование гибридизации полностью идентичной последовательности можно оценивать с использованием анализов гибридизации, которые хорошо известны в данной области (например, саузерн-блот (ДНК), нозерн-блот (РНК), гибридизация в растворе или т.п., см. Sambrook, et al., Molecular Cloning: A Laboratory Manual, Second Edition, (1989) Cold Spring Harbor, N.Y.). Такие анализы можно проводить с использованием варьирующих степеней селективности, например, с использованием условий, варьирующих от низкой до высокой жесткости. Если используют условия низкой жесткости, отсутствие неспецифического связывания можно оценивать с использованием вторичного зонда с отсутствием даже частичной степени идентичности последовательностей (например, зонд менее чем приблизительно с 30% идентичности последовательности с молекулой-мишенью) так, что в отсутствие событий неспецифического связывания вторичный зонд не гибридизируется с мишенью.
[0060] При использовании системы детекции на основе гибридизации выбирают зонд нуклеиновой кислоты, комплементарный эталонной последовательности нуклеиновой кислоты, а затем посредством подбора подходящих условий зонд и эталонную последовательность селективно гибридизируют или связывают друг с другом с формированием дуплексной молекулы. Молекула нуклеиновой кислоты, способная к селективной гибридизации с эталонной последовательностью в умеренно жестких условиях гибридизации, как правило, гибридизируется в условиях, позволяющих детекцию последовательности-мишени нуклеиновой кислоты длиной по меньшей мере приблизительно 10-14 нуклеотидов по меньшей мере приблизительно с 70% идентичностью последовательности с последовательностью выбранного зонда нуклеиновой кислоты. Жесткие условия гибридизации, как правило, позволяют детекцию последовательностей-мишеней нуклеиновой кислоты длиной по меньшей мере приблизительно 10-14 нуклеотидов с идентичностью последовательности, большей чем приблизительно 90-95%, с последовательностью выбранного зонда нуклеиновой кислоты. Условия гибридизации, пригодные для гибридизации зонда/эталонной последовательности, где зонд и эталонная последовательность обладают определенной степенью идентичности последовательностей, можно определять, как известно в данной области (см., например, Nucleic Acid Hybridization: A Practical Approach, editors B.D. Hames and S.J. Higgins, (1985) Oxford; Washington, DC; IRL Press).
[0061] Условия гибридизации хорошо известны специалистам в данной области. Жесткость гибридизации относится к степени, с которой условия гибридизации неблагоприятны для формирования гибридов, содержащих несовпадающие нуклеотиды, с более высокой жесткостью, коррелирующей с меньшей допустимостью для несовпадающих гибридов. Факторы, влияющие на жесткость гибридизации, хорошо известны специалистам в данной области и в качестве неограничивающих примеров включают температуру, pH, ионную силу и концентрацию органических растворителей, например, таких как формамид и диметилсульфоксид. Как известно специалистам в данной области, жесткость гибридизации возрастает при повышении температуры, снижении ионной силы и снижении концентрации растворителей.
[0062] В отношении жесткости условий гибридизации в данной области хорошо известно, что для установления конкретной жесткости можно использовать множество эквивалентных условий, например, варьируя следующие факторы: длину и характер последовательностей, состав оснований различных последовательностей, концентрации солей и других компонентов раствора для гибридизации, присутствие или отсутствие в растворах для гибридизации блокирующих средств (например, декстрансульфата и полиэтиленгликоля), температуру реакции гибридизации и временные параметры, а также варьирование условий отмывки. Выбор конкретного набора условий гибридизации проводят в соответствии со стандартными способами в данной области (см., например, Sambrook, et al., Molecular Cloning: A Laboratory Manual, Second Edition, (1989) Cold Spring Harbor, N.Y.).
[0063] "Рекомбинация" относится к процессу обмена генетической информацией между двумя полинуклеотидами. Для целей настоящего описания "гомологичная рекомбинация (HR)" относится к специализированной форме такого обмена, которая происходит, например, при восстановлении двойных разрывов цепи в клетках. Этот процесс требует гомологии нуклеотидных последовательностей, использует "донорную" молекулу для восстановления матрицы молекулы-"мишени" (т.е., молекулы, где произошел двойной разрыв цепи) и под различными названиями известен как "некроссоверная генная конверсия" или "генная конверсия на коротких участках", так как он приводит к переносу генетической информации от донора к мишени. Без желания быть связанным какой-либо конкретной теорией, такой перенос может вовлекать коррекцию несоответствий гетеродуплекса ДНК, формирующегося между разорванной мишенью и донором, и/или "зависимый от синтеза отжиг цепей", в котором донор применяют для воссоздания генетической информации, которая становится частью мишени и/или связанные процессы. Такая специализированная HR часто приводит к изменению последовательности молекулы-мишени так, что в полинуклеотид-мишень встраивается часть или вся последовательность донорного полинуклеотида.
[0064] "Расщепление" относится к разрыву ковалентного каркаса молекулы ДНК. Расщепление можно инициировать множеством способов, включая в качестве неограничивающих примеров ферментативный или химический гидролиз фосфодиэфирной связи. Возможно одноцепочечное расщепление и двухцепочечное расщепление, и двухцепочечное расщепление может происходить как результат двух отдельных событий одноцепочечного расщепления. Расщепление ДНК может приводить к образованию тупых концов или липких концов. В определенных вариантах осуществления для направленного двухцепочечного расщепления ДНК используют слитые полипептиды.
[0065] "Домен расщепления" содержит одну или несколько полипептидных последовательностей, обладающих каталитической активностью в отношении расщепления ДНК. Домен расщепления может содержаться в одной полипептидной цепи, или расщепляющая активность может являться результатом ассоциации двух (или более) полипептидов.
[0066] "Полудомен расщепления" представляет собой полипептидную последовательность, которая в сочетании со вторым полипептидом (идентичным или отличным) формирует комплекс с расщепляющей активностью (предпочтительно активность расщепления двойной цепи).
[0067] "Хроматин" представляет собой нуклеопротеиновую структуру, содержащую клеточный геном. Клеточный хроматин содержит нуклеиновую кислоту, преимущественно ДНК, и белки, включая гистоны и негистоновые хромосомные белки. Большинство хроматина эукариотических клеток присутствует в форме нуклеосом, где ядро нуклеосомы содержит приблизительно 150 пар оснований ДНК, ассоциированных с октамером, содержащим по два каждого из гистонов H2A, H2B, H3 и H4; и линкерную ДНК (переменной длины в зависимости от организма), расположенную между ядрами нуклеосом. Молекула гистона H, как правило, ассоциирована c линкерной ДНК. Для целей настоящего описания термин "хроматин" предназначен для включения всех типов клеточных нуклеопротеинов, прокариотических и эукариотических. Клеточный хроматин включает хромосомный и эписомный хроматин.
[0068] "Хромосома" представляет собой хроматиновый комплекс, содержащий весь геном клетки или его часть. Геном клетки часто характеризуют посредством его кариотипа, представляющего собой набор всех хромосом, содержащих геном клетки. Геном клетки может содержать одну или несколько хромосом.
[0069] "эписома" представляет собой реплицирующуюся нуклеиновую кислоту, нуклеопротеиновый комплекс или другую структуру, содержащую нуклеиновую кислоту, не являющуюся частью хромосомного кариотипа клетки. Примеры эписом включают плазмиды и определенные вирусные геномы.
[0070] "Достижимая область" представляет собой участок в клеточном хроматине, в котором участок-мишень, присутствующий в нуклеиновой кислоте, может быть связан экзогенной молекулой, распознающей участок-мишень. Без желания быть связанным какой-либо конкретной теорией, полагают, что достижимая область представляет собой область, не упакованную в нуклеосомную структуру. Определенную структуру достижимой области часто можно детектировать по ее чувствительности к химическим и ферментативным зондам, например, нуклеазам.
[0071] "Участок-мишень" или "последовательность-мишень" представляет собой последовательность нуклеиновой кислоты, определяющую часть нуклеиновой кислоты, с которой связывается связывающая молекула при условии наличия условий, достаточных для связывания. Например, последовательность 5'-GAATTC-3' представляет собой участок-мишень для рестрикционной эндонуклеазы EcoRI.
[0072] "Экзогенная" молекула представляет собой молекулу, которая в норме не присутствует в клетке, но которую можно вводить в клетку одним или несколькими генетическими, биохимическими или другими способами. "Присутствие в клетке в норме" определяют в отношении конкретной стадии развития клетки и условий окружающей ее среды. Таким образом, например, молекула, которая присутствует только при эмбриологическом развитии мышцы, представляет собой экзогенную молекулу по отношению к взрослой мышечной клетке. Подобным образом, молекула, индуцируемая тепловым шоком, представляет собой экзогенную молекулу по отношению клетке вне теплового шока. Экзогенная молекула может содержать, например, функционирующую версию неправильно функционирующей эндогенной молекулы или неправильно функционирующую версию нормально функционирующей эндогенной молекулы.
[0073] В частности, экзогенная молекула может представлять собой низкомолекулярное соединение, такое как получают способом комбинаторной химии, или макромолекулу, такую как белок, нуклеиновая кислота, углевод, липид, гликопротеин, липопротеин, полисахарид и любое модифицированное производное указанных выше молекул, или любой комплекс, содержащий одну или несколько из указанных выше молекул. Нуклеиновые кислоты включают ДНК и РНК, могут являться одно- или двухцепочечными; могут являться линейными, разветвленными или кольцевыми; и могут обладать любой длиной. Нуклеиновые кислоты включают нуклеиновые кислоты, способные к формированию дуплексов, а также формирующие триплексы нуклеиновые кислоты. См., например, патенты США №№ 5176996 и 5422251. Белки в качестве неограничивающих примеров включают ДНК-связывающие белки, факторы транскрипции, факторы перестройки хроматина, белки, связывающие метилированную ДНК, полимеразы, метилазы, деметилазы, ацетилазы, деацетилазы, киназы, фосфатазы, интегразы, рекомбиназы, лигазы, топоизомеразы, гиразы и геликазы.
[0074] Экзогенная молекула может являться молекулой того же типа, что и эндогенная молекула, например, экзогенный белок или нуклеиновая кислота. Например, экзогенная нуклеиновая кислота может включать инфицирующий вирусный геном, T-цепь Agrobacterium tumefaciens, плазмиду или эписому, вводимую в клетку, или хромосому, которая в норме не присутствует в клетке. Способы введения экзогенных молекул в клетки известны специалистам в данной области и в качестве неограничивающих примеров включают опосредуемый липидами перенос (т.е., липосомы, содержащие нейтральные и катионные липиды), электропорацию, прямую инъекцию, слияние клеток, бомбардировку частицами, соосаждение с фосфатом кальция, опосредуемый DEAE-декстраном перенос и опосредуемые вирусным вектором перенос. Экзогенная молекула, не являющаяся молекулой растения, может представлять собой, например, антитело млекопитающего (например, человека или гуманизированное).
[0075] В отличие от этого, "эндогенная" молекула представляет собой молекулу, которая в норме присутствует в конкретной клетке в конкретной стадии развития в конкретных условиях окружающей среды. Например, эндогенная нуклеиновая кислота может включать хромосомы, геном митохондрии, хлоропласта или другой органеллы или природную эписомную нуклеиновую кислоту. Дополнительные эндогенные молекулы могут включать белки, например, факторы транскрипции и ферменты.
[0076] "Слитая" молекула представляет собой молекулу, в которой связаны две или более молекулярные субъединицы, предпочтительно ковалентно. Молекулярные субъединицы могут являться молекулами одинакового химического типа или могут являться молекулами различных химических типов. Примеры слитой молекулы первого типа в качестве неограничивающих примеров включают слитые белки (например, содержащее ZFN слияние между ДНК-связывающим доменом ZFP и доменом расщепления) и слитые нуклеиновые кислоты (например, нуклеиновая кислота, кодирующая слитый белок, описанный выше). Примеры слитой молекулы второго типа в качестве неограничивающих примеров включают слияние между формирующей триплекс нуклеиновой кислотой и полипептидом и слияние между связывающим малую бороздку средством и нуклеиновой кислотой.
[0077] Экспрессия слитого белка в клетке может являться результатом доставки слитого белка в клетку или доставки в клетку полинуклеотида, кодирующего слитый белок, где полинуклеотид транскрибируется и транскрипт транслируется с получением слитого белка. Также в экспрессию белка в клетке могут быть вовлечены транссплайсинг, расщепление полипептидов и лигирование полипептидов. Способы доставки полинуклеотидов и полипептидов в клетки предоставлены в другой части этого описания.
[0078] "Ген" для целей настоящего описания включает область ДНК, кодирующую продукт гена (см. ниже), а также все области ДНК, регулирующие получение продукта гена, являются ли такие регуляторные последовательности прилежащими к кодирующим и/или транскрибируемым последовательностям или нет. Таким образом, ген включает, но не обязательно ограничен ими, промоторные последовательности, терминаторы, последовательности регуляции трансляции, такие как участки связывания рибосом и внутренние участки связывания рибосом, энхансеры, сайленсеры, инсуляторы, граничные элементы, участки начала репликации, участки прикрепления к матриксу и области контроля локусов.
[0079] "Экспрессия гена" относится к преобразованию информации, содержащейся в гене, в продукт гена. Продукт гена может представлять собой непосредственный продукт транскрипции гена (например, мРНК, тРНК, рРНК, антисмысловая РНК, рибозим, кшРНК, микро РНК, структурная РНК или РНК любого другого типа) или белок, продуцируемый посредством трансляции мРНК. Продукты генов также включают РНК, модифицируемую такими процессами, как кэпирование, полиаденилирование, метилирование и редактирование, и белки, модифицируемые, например, метилированием, ацетилированием, фосфорилированием, убиквитинилированием, АДФ-рибозилилированием, миристилированием и гликозилированием.
[0080] "Модуляция" экспрессии гена относится к изменению активности гена. Модуляция экспрессии в качестве неограничивающих примеров может включать активацию генов и репрессию генов.
[0081] "Растительные" клетки в качестве неограничивающих примеров включают клетки односемядольных (однодольных) или двусемянодольных (двудольных) растений. Неограничивающие примеры однодольных растений включают злаковые растения, такие как кукуруза, рис, ячмень, овес, пшеница, сорго, рожь, сахарный тростник, ананас, лук, банан и кокос. Неограничивающие примеры двудольных растений включают табак, помидор, подсолнечник, хлопок, сахарную свеклу, картофель, салат-латук, дыню, сою, канолу (рапс) и люцерну. Растительные клетки могут быть из любой части растения и/или с любой стадии развития растения. Таким образом, растительные клетки могут представлять собой клетки из семян растений. В некоторых вариантах осуществления растение или растительная клетка представляют собой растение или происходят из растения, вовлеченного в получение растительных масел для пищевых и/или промышленных видов применения (т.е., "маслопродуцирующее растение"). Иллюстративные маслопродуцирующие растения в качестве неограничивающих примеров включают виды Brassica (например, Brassica napus, включающую сорта канолы), кукурузу, сою, катран, горчицу, касторовый боб, арахис, кунжут, хлопок, семя льна, сафлор, масличную пальму, лен, подсолнечник и кокос.
[0082] "Представляющей интерес областью" является любая область клеточного хроматина, например, такая как ген или некодирующая последовательность в гене или примыкающая к нему, с которой желательно связывать экзогенную молекулу. Связывание можно проводить с целью направленного расщепления ДНК и/или направленной рекомбинации. Представляющая интерес область может находиться, например, в хромосоме, эписоме, геноме органеллы (например, митохондрии, хлоропласта) или в инфицирующем вирусном геноме. Представляющая интерес область может находиться в кодирующей области гена, в транскрибируемых некодирующих областях, например, таких как лидерные последовательности, трейлерные последовательности или интроны, или в нетранскрибируемых областях, выше или ниже кодирующей области. Длина представляющей интерес области может являться насколько малой как одна нуклеотидная пара или может составлять до 25000 пар нуклеотидов, или любое целочисленное количество пар нуклеотидов.
[0083] Термины "функциональная связь" и "функционально связанный" используют взаимозаменяемо в отношении смежного положения двух или более компонентов (таких как элементы последовательности), в которых компоненты расположены так, что оба компонента нормально функционируют и допускают возможность того, что по меньшей мере один из компонентов может опосредовать функцию, выполняемую по меньшей мере одним из других компонентов. В качестве иллюстрации, последовательность регулятора транскрипции, такая как промотор, функционально связана с кодирующей последовательностью, если последовательность регулятора транскрипции контролирует уровень транскрипции кодирующей последовательности в ответ на присутствие или отсутствие одного или нескольких факторов регуляции транскрипции. Последовательность регулятора транскрипции, как правило, функционально связана с кодирующей последовательностью в цис-положении, но не обязательно непосредственно граничит с ней. Например, энхансер представляет собой последовательность регулятора транскрипции, который функционально связан с кодирующей последовательностью, даже если они не являются смежными.
[0084] В отношении слитых полипептидов термин "функционально связанный" может относиться к тому факту, что каждый из компонентов выполняет в связи с другим компонентом ту же функцию, какую он бы выполнял, если бы они не были связаны. Например, в отношении слитого полипептида, в котором ДНК-связывающий домен ZFP слит с регуляторным доменом, ДНК-связывающий домен ZFP и регуляторный домен находятся в функциональной связи, если в слитом полипептиде часть ДНК-связывающего домена ZFP способна связываться со своим участком-мишенью и/или своим участком связывания, тогда как регуляторный домен способен регулировать экспрессию ДНК, находясь вблизи участка-мишени.
[0085] "Функциональный фрагмент" белка, полипептида или нуклеиновой кислоты представляет собой белок, полипептид или нуклеиновую кислоту, последовательность которых не идентична полноразмерному белку, полипептиду или нуклеиновой кислоте, но при этом сохраняет ту же функцию, что и полноразмерный белок, полипептид или нуклеиновая кислота. Функциональный фрагмент может содержать больше, меньше или то же количество остатков, что и соответствующая природная молекула, и/или может содержать одну или несколько замен аминокислот или нуклеотидов. Способы определения функции нуклеиновых кислот (например, кодирующей функции, способности к гибридизации с другой нуклеиновой кислотой) хорошо известны в данной области. Подобным образом, хорошо известны способы определения функции белков. Например, ДНК-связывающую функцию полипептида можно определять, например, посредством связывания на фильтре, сдвига электрофоретической подвижности или анализами иммунопреципитации. Расщепление ДНК можно анализировать электрофорезом в геле. См. Ausubel et al., выше. Способность белка взаимодействовать с другим белком можно определять, например, посредством коиммунопреципитации, двухгибридных анализов или комплементацией, генетической и биохимической. См., например, Fields et al. (1989) Nature 340:245-246; патент США № 5585245 и PCT WO 98/44350.
[0086] Как применяют в настоящем документе, "насыщенные жирные кислоты" в качестве неограничивающих примеров включают лауриновую (C12:0), миристиновую (C14:0), пальмитиновую (C16:0) и стеариновую (C18:0) кислоты. Подобным образом, "мононенасыщенные жирные кислоты" и "полиненасыщенные жирные кислоты" в качестве неограничивающих примеров включают жирные кислоты C18, такие как олеиновая кислота (C18:1), восстановленная линолевая кислота (C18:2) и восстановленная линоленовая кислота (C18:3).
Участки-мишени
[0087] Описываемые способы и композиции включают слитые белки, содержащие ДНК-связывающий домен (например, ZFP) и регуляторный домен или домен расщепления (нуклеазный) (или полудомен расщепления), в которых ДНК-связывающий домен (например, домен цинковых пальцев), связываясь с последовательностью в клеточном хроматине в гене, вовлеченном в синтез жирных кислот, направляет активность домена регуляции транскрипции или домена расщепления (или полудомена расщепления) вблизи с последовательностью и, таким образом, модулирует транскрипцию или индуцирует расщепление вблизи с последовательностью-мишенью.
[0088] Как указано в другой части этого описания, домен цинковых пальцев можно конструировать для связывания практически с любой желаемой последовательностью. Таким образом, после идентификации представляющей интерес области, содержащей последовательность, в которой желательна регуляция, расщепление или рекомбинация, можно конструировать один или несколько связывающих доменов цинковых пальцев со связыванием одной или нескольких последовательностей в представляющей интерес области.
[0089] Выбор участка-мишени в представляющей интерес области генома в клеточном хроматине любого гена, вовлеченного в биосинтез жирных кислот (например, см. фигуру 1), для связывания доменом цинковых пальцев (например, участка-мишени), можно проводить, например, способами, описанными в принадлежащем тем же заявителям патенте США № 6453242 (17 сентября 2002), в котором также описаны способы составления ZFP для связывания с выбранной последовательностью. Специалистам в данной области должно быть понятным, что для выбора участка-мишени также можно использовать простой визуальный осмотр нуклеотидной последовательности. Таким образом, в заявляемых способах можно использовать любые средства выбора участка-мишени.
[0090] В определенных вариантах осуществления ZFP, как описано в настоящем документе, связываются с участком-мишенью в гене, кодирующем ACCазу, KAS I, KAS II, KAS III, KAS IV, FATB1, FATB2, FATB3, FATB4, FATB5, FAS, FAE1, FatA, Fad2, Fad3, GPDH, GK и/или S-ACP-DES.
[0091] Участки-мишени, как правило, состоят из множества смежных подучастков-мишеней. Подучасток-мишень относится к последовательности (как правило, триплету нуклеотидов или квадруплету нуклеотидов, который может перекрываться по одному нуклеотиду со смежным квадруплетом), связываемой отдельным цинковым пальцем. См., например, WO 02/077227. Если цепь, с которой белок с цинковыми пальцами образует большинство контактов, обозначить как цепь-мишень, "цепь первичного распознавания" или "цепь первичного контакта", некоторые белки с цинковыми пальцами связываются с триплетом из трех оснований в цепи-мишени и с четвертым основанием не на цепи-мишени. Как правило, длина участка-мишени составляет по меньшей мере 9 нуклеотидов, и, таким образом, она связана связывающим доменом цинковых пальцев, содержащим по меньшей мере три цинковых пальца. Однако также возможно связывание, например, связывающего домена с 4 пальцами с участком-мишенью из 12 нуклеотидов, связывающего домена с 5 пальцами с участком-мишенью из 15 нуклеотидов или связывающего домена с 6 пальцами с участком-мишенью из 18 нуклеотидов. Очевидно, что также возможно связывание более крупных связывающих доменов (например, с 7, 8, 9 и более пальцами) с более протяженными участками-мишенями.
[0092] Для участка-мишени необязательно являться кратным трем нуклеотидам. Например, в случаях, в которых происходит взаимодействие с перекрещиванием цепей (см., например, патент США 6453242 и WO 02/077227), один или несколько отдельных цинковых пальцев связывающего домена с несколькими пальцами может связываться с перекрывающимися квадруплетными подучастками. Как результат, белок с тремя пальцами может связывать последовательность из 10 нуклеотидов, где десятый нуклеотид является частью квадруплета, связанного с концевым пальцем, белок с четырьмя пальцами может связывать последовательность из 13 нуклеотидов, где тринадцатый нуклеотид является частью квадруплета, связанного с концевым пальцем, и т.д.
[0093] Также на связывание с последовательностью-мишенью влияет длина и характер аминокислотных линкерных последовательностей между отдельными цинковыми пальцами в связывающем домене с несколькими пальцами. Например, присутствие так называемого "неканонического линкера", "длинного линкера" или "структурированного линкера" между соседними цинковыми пальцами в связывающем домене с несколькими пальцами может обеспечивать связь этих пальцев с подучастками, которые не примыкают друг к другу непосредственно. Неограничивающие примеры таких линкеров описаны, например, в патенте США № 6479626 и WO 01/53480. Таким образом, один или несколько подучастков, в участке-мишени для связывающего домена цинковых пальцев, могут быть отделены друг от друга 1, 2, 3, 4, 5 или более нуклеотидами. Предоставляя всего один пример, связывающий домен с четырьмя пальцами может связывать участок-мишень из 13 нуклеотидов, содержащих, последовательно, два смежных подучастка из 3 нуклеотидов, промежуточный нуклеотид и два смежных триплетных подучастка. Также см. заявку США № 61/130099 для композиций и способов для связывания искусственных нуклеаз для связывания с участками-мишенями, разделенными различным количеством нуклеотидов. Расстояние между последовательностями (например, участками-мишенями) относится к количеству нуклеотидов или пар нуклеотидов, находящихся между двумя последовательностями, как измеряют от концов последовательностей, ближайших друг к другу.
[0094] В определенных вариантах осуществления составляют ZFP с функцией фактора транскрипции. Для функции в качестве фактора транскрипции все, что в основном нужно, это простое связывание и достаточная близость к промотору. Точное позиционирование относительно промотора, ориентация и, в определенных пределах, дистанция не очень важны. Это свойство обеспечивает существенную гибкость в выборе участков-мишеней для конструирования искусственных факторов транскрипции. Таким образом, участок-мишень, распознаваемый ZFP, может представлять собой любой подходящий участок в гене-мишени, который обеспечивает активацию или репрессию экспрессии гена ZFP, необязательно связанного с регуляторным доменом. Предпочтительные участки-мишени включают области рядом, ниже или выше участка старта транскрипции. Кроме того, участки-мишени могут представлять собой участки, расположенные в энхансерных областях, репрессорных участках, участках остановки РНК-полимеразы и в особых регуляторных участках (например, участки SP-1, элементы ответа на гипоксию, элементы распознавания ядерного рецептора, участки связывания p53), участках в кодирующей области кДНК или в кодирующей области маркерной экспрессируемой последовательности (EST).
[0095] В других вариантах осуществления составляют ZFP с нуклеазной активностью. Экспрессия содержащего ZFN слитого белка, содержащего связывающий домен цинковых пальцев и домен расщепления (или два слитых белка, где каждый содержит связывающий домен цинковых пальцев и полудомен расщепления), в клетке приводит к расщеплению вблизи последовательности-мишени. В определенных вариантах осуществления расщепление зависит от связывания двух слитых молекул с доменами цинковых пальцев/полудоменами расщепления с разделением участков-мишеней. Два участка-мишени могут находиться на противоположных цепях ДНК, или, альтернативно, оба участка-мишени могут находиться на одной цепи ДНК.
ДНК-связывающие домены
[0096] В практическом осуществлении настоящего изобретения можно использовать любой ДНК-связывающий домен. В определенных вариантах осуществления ДНК-связывающий домен содержит связывающий домен цинковых пальцев с одним или несколькими цинковыми пальцами (Miller et al. (1985) EMBO J. 4:1609-1614; Rhodes (1993) Scientific American Feb.:56-65; патент США № 6453242). Как правило, длина одного домена цинковых пальцев составляет приблизительно 30 аминокислот. Структурные исследования продемонстрировали, что каждый домен цинковых пальцев (мотив) содержит два бета-слоя (удерживаемых в положении бета-изгиба, содержащем два инвариантных остатка цистеина) и альфа-спираль (содержащую два инвариантных остатка гистидина), которые удерживаются в конкретной конформации посредством координационных взаимодействий двух цистеинов и двух гистидинов с атомом цинка.
[0097] Цинковые пальцы включают канонические цинковые пальцы C2H2 (т.е., цинковые пальцы, в которых ион цинка координирован двумя остатками цистеина и двумя остатками гистидина) и неканонические цинковые пальцы, например, такие как цинковые пальцы C3H и C2HC (цинковые пальцы, в которых ион цинка координирован тремя остатками цистеина и одним остатком гистидина, см., например, патентную публикацию США № 2008/0182332) и цинковые пальцы C4 (цинковые пальцы, в которых ион цинка координирован четырьмя остатками цистеина). Также см. WO 02/057293.
[0098] Связывающие домены цинковых пальцев можно конструировать для связывания выбранной последовательности. См., например, Beerli et al. (2002) Nature Biotechnol. 20:135-141; Pabo et al. (2001) Ann. Rev. Biochem. 70:313-340; Isalan et al. (2001) Nature Biotechnol. 19:656-660; Segal et al. (2001) Curr. Opin. Biotechnol. 12:632-637; Choo et al. (2000) Curr. Opin. Struct. Biol. 10:411-416. Конструируемый (или неприродный) связывающий домен цинковых пальцев по сравнению с природным белком с цинковыми пальцами может обладать новой специфичностью связывания. Способы конструирования в качестве неограничивающих примеров включают, рациональное составление и различные типы отбора. Рациональное составление включает, например, использование баз данных, содержащих триплетные (или квадруплетные) нуклеотидные последовательности и конкретные аминокислотные последовательности цинковых пальцев, в которых каждая триплетная или квадруплетная нуклеотидная последовательность ассоциирована с одной или несколькими аминокислотными последовательностями цинковых пальцев, которые связываются с конкретной триплетной или квадруплетной последовательностью. См., например, принадлежащие тем же заявителям патенты США 6453242 и 6534261. Дополнительные способы составления описаны, например, в патентах США 6746838; 6785613; 6866997 и 7030215.
[0099] Иллюстративные способы отбора, включая фаговый дисплей и двухгибридные системы, описаны в патентах США 5789538; 5925523; 6007988; 6013453; 6410248; 6140466; 6200759 и 6242568; а также WO 98/37186; WO 98/53057; WO 00/27878; WO 01/88197 и GB 2338237.
[0100] Увеличение специфичности связывания связывающих доменов цинковых пальцев описано, например, в принадлежащем тем же заявителям патенте США № 6794136.
[0101] Так как отдельный цинковый палец связывается с последовательностью из трех нуклеотидов (т.е., триплетом) (или последовательностью из четырех нуклеотидов, которая может перекрываться по одному нуклеотиду с участком связывания из четырех нуклеотидов соседнего цинкового пальца), длина последовательности, с которой должен связываться конструируемый связывающий домен цинковых пальцев (например, последовательности-мишени), определяется количеством цинковых пальцев в конструируемом связывающем домене цинковых пальцев. Например, для ZFP, в которых мотивы с пальцами не связываются с перекрывающимися подучастками, последовательность-мишень из шести нуклеотидов связана связывающим доменом с двумя пальцами; последовательность-мишень из девяти нуклеотидов связана связывающим доменом с тремя пальцами и т.д. Как указано в настоящем документе, участки связывания для отдельных цинковых пальцев (т.е., подучастки) в участке-мишени не обязательно должны быть смежными, но в зависимости от длины и характера аминокислотных последовательностей между цинковыми пальцами (т.е., линкеров между пальцами) в связывающем домене с несколькими пальцами могут быть разделены одним или несколькими нуклеотидами.
[0102] В связывающем домене цинковых пальцев с несколькими пальцами соседние цинковые пальцы могут быть разделены аминокислотными линкерными последовательностями приблизительно из 5 аминокислот (так называемые "канонические" линкеры между пальцами) или, альтернативно, одним или несколькими неканоническими линкерами. См., например, принадлежащие тем же заявителям патенты США №№ 6453242 и 6534261. Для конструируемых связывающих доменов цинковых пальцев, содержащих более трех пальцев, предпочтительной может являться вставка между определенными цинковыми пальцами более длинных ("неканонических") линкеров между пальцами, так как она может увеличить аффинность и/или специфичность связывания связывающим доменом. См., например, патент США № 6479626 и WO 01/53480. Таким образом, связывающие домены цинковых пальцев с несколькими пальцами также можно характеризовать в отношении присутствия и положения неканонических линкеров между пальцами. Например, связывающий домен цинковых пальцев с шестью пальцами, содержащий три пальца (соединенных двумя каноническими линкерами между пальцами), длинный линкер и три дополнительных пальца (соединенных двумя каноническими линкерами между пальцами) обозначают как конфигурацию 2×3. Подобным образом, связывающий домен, содержащий два пальца (с каноническим линкером между ними), длинный линкер и два дополнительных пальца (соединенных каноническим линкером), обозначают как белок 2×2. Белок, содержащий три единицы с двумя пальцами (в каждой из которых два пальца соединены каноническим линкером) и в котором каждая единица с двумя пальцами соединена с соседними единицами с двумя пальцами длинным линкером, обозначают как белок 3×2.
[0103] Присутствие в связывающем домене с несколькими пальцами между двумя соседними цинковыми пальцами длинного или неканонического линкера между пальцами часто позволяет двум пальцам связываться с подучастками, которые в последовательности-мишени не являются непосредственно смежными. Таким образом, между подучастками в участке-мишени могут существовать пропуски в один или несколько нуклеотидов; например, участок-мишень может содержать один или несколько нуклеотидов, которые не контактируют с цинковым пальцем. Например, связывающий домен цинковых пальцев 2×2 может связываться с двумя последовательностями из шести нуклеотидов, разделенных одним нуклеотидом, например, он связывается с участком-мишенью из 13 нуклеотидов. Также см. Moore et al. (2001a) Proc. Natl. Acad. Sci. USA 98:1432-1436; Moore et al. (2001b) Proc. Natl. Acad. Sci. USA 98:1437-1441 и WO 01/53480.
[0104] Как указано ранее, подучасток-мишень представляет собой последовательность из трех или четырех нуклеотидов, которые связывает один цинковый палец. Для определенных целей единицу с двумя пальцами обозначают как связывающий модуль. Связывающий модуль можно получать, например, выбирая два соседних пальца в белке с несколькими пальцами (как правило, три пальца), который связывает конкретную последовательность-мишень из шести нуклеотидов. Альтернативно, модули можно конструировать посредством сборки отдельных цинковых пальцев. Также см. WO 98/53057 и WO 01/53480.
[0105] В одном из вариантов осуществления в настоящем документе описан связывающий домен цинковых пальцев, содержащий аминокислотную последовательность, как представлено в таблице 1. В другом варианте осуществления описание относится к полинуклеотиду, кодирующему связывающий домен цинковых пальцев, где связывающий домен цинковых пальцев содержит аминокислотную последовательность, как представлено в таблице 1.
[0106] Альтернативно, ДНК-связывающий домен можно получить из нуклеазы. Например, известны распознающие последовательности хоминг-эндонуклеаз и мегануклеаз, таких как I-SceI, I-CeuI, PI-PspI, PI-Sce, I-SceIV, I-CsmI, I-PanI, I-SceII, I-PpoI, I-SceIII, I-CreI, I-TevI, I-TevII и I-TevIII. Также см. патент США № 5420032; патент США № 6833252; Belfort et al. (1997) Nucleic Acids Res. 25:3379-3388; Dujon et al. (1989) Gene 82:115-118; Perler et al. (1994) Nucleic Acids Res. 22, 1125-1127; Jasin (1996) Trends Genet. 12:224-228; Gimble et al. (1996) J. Mol. Biol. 263:163-180; Argast et al. (1998) J. Mol. Biol. 280:345-353 и каталог New England Biolabs. Кроме того, ДНК-связывающую специфичность хоминг-эндонуклеаз и мегануклеаз можно применять в конструировании для связывания неприродных участков-мишеней. См., например, Chevalier et al. (2002) Molec. Cell 10:895-905; Epinat et al. (2003) Nucleic Acids Res. 31:2952-2962; Ashworth et al. (2006) Nature 441:656-659; Paques et al. (2007) Current Gene Therapy 7:49-66; патентную публикацию США № 20070117128.
[0107] В других вариантах осуществления ДНК-связывающий домен содержит природный или конструируемый (неприродный) ДНК-связывающий домен с TAL-эффектором. Известно, что патогенные бактерии растений рода Xanthomonas вызывают множество заболеваний у важных сельскохозяйственных культур. Патогенность Xanthomonas зависит от консервативной системы секреции III типа (T3S), вводящей в растительную клетку более 25 различных эффекторных белков. Среди этих инъецируемых белков находятся подобные активаторам транскрипции (TAL) эффекторы, мимикрирующие активаторы транскрипции растений и манипулирующие транскриптомом растений (см. Kay et al. (2007) Science 318:648-651). Эти белки содержит ДНК-связывающий домен и домен активации транскрипции. Одним из наиболее хорошо охарактеризованных TAL-эффекторов является AvrBs3 из Xanthomonas campestgris пв. Vesicatoria (см. Bonas et al. (1989) Mol Gen Genet 218:127-136 и WO2010079430). TAL-эффекторы содержат централизованный домен из тандемных повторов, где каждый повтор содержит приблизительно 34 аминокислоты, которые являются ключевыми для специфичности связывания ДНК этими белками. Кроме того, они содержат последовательность ядерной локализации и кислый домен активации транскрипции (для обзора см. Schornack S, et al. (2006) J. Plant Physiol. 163(3):256-272). Кроме того, в фитопатогенных бактериях Ralstonia solanacearum в биоваре 1 штамма GMI1000 и в биоваре 4 штамма RS1000 R. solanacearum найдены два гена, обозначенных brg11 и hpx17, гомологичные семейству AvrBs3 Xanthomonas (См. Heuer et al. (2007) Appl. and Envir. Micro 73(13):4379-4384). Эти гены на 98,9% идентичны по нуклеотидной последовательности друг другу, но отличаются делецией 1575 п.н. в домене hpx17 с повторами. Однако оба продукта генов обладают менее чем 40% идентичностью последовательности с семейством белков AvrBs3 Xanthomonas.
[0108] Специфичность этих TAL-эффекторов зависит от последовательностей, находящихся в тандемных повторах. Повторяющаяся последовательность содержит приблизительно 102 п.н. и повторы, как правило, на 91-100% гомологичны друг другу (Bonas et al., там же). Полиморфизм повторов, как правило, расположен в положениях 12 и 13, и полагают, что существует соответствие один-в-один между составом гипервариабельных двойных остатков в положениях 12 и 13 с составом смежных нуклеотидов в последовательности-мишени TAL-эффектора (см. Moscou and Bogdanove, (2009) Science 326:1501 и Boch et al. (2009) Science 326:1509-1512). Экспериментально, природный код для распознавания ДНК этими TAL-эффекторами определен так, что последовательность HD в положениях 12 и 13 приводит к связыванию с цитозином (C), NG связываются с T, NI с A, C, G или T, NN связывается с A или G, а ING связываются T. Эти ДНК-связывающие повторы собирают в белки с новыми комбинациями и количеством повторов с получением искусственных факторов транскрипции, которые способны взаимодействовать с новыми последовательностями и активировать экспрессию неэндогенного репортерного гена в растительных клетках (Boch et al., там же). Конструируемые TAL-белки связывали с полудоменом расщепления FokI с получением слитой нуклеазы с TAL-эффекторным доменом (TALEN), демонстрирующей активность в анализе с репортером в дрожжах (мишень на основе плазмиды). Christian et al. ((2010) Genetics epub 10.1534/genetics.110.120717).
Регуляторные домены
[0109] С регуляторными доменами для модуляции экспрессии гена необязательно можно ассоциировать ДНК-связывающие домены (например, ZFP), описываемые в настоящем документе. ZFP можно ковалентно или нековалентно связывать с одним или несколькими регуляторными доменами, альтернативно двумя или более регуляторными доменами, с двумя или более доменами, являющимися копиями одного домена, или с двумя различными доменами. Регуляторные домены можно ковалентно связывать с ZFP, например, посредством аминокислотного линкера, как часть слитого белка. ZFP также можно связывать с регуляторным доменом посредством нековалентного домена димеризации, например, лейциновой застежки, N-концевого домена белка STAT или связывающего белка FK506 (см., например, O'Shea, Science 254:539 (1991), Barahmand-Pour et al., Curr. Top. Microbiol. Immunol. 211:121-128 (1996); Klemm et al., Annu. Rev. Immunol. 16:569-592 (1998); Klemm et al., Annu. Rev. Immunol. 16:569-592 (1998); Ho et al., Nature 382:822-826 (1996); и Pomeranz et al., Biochem. 37:965 (1998)). Регуляторный домен можно связывать с ZFP в любом подходящем положении, включая C- или N-конец ZFP.
[0110] Общие регуляторные домены для добавления к ZFP включают, например, эффекторные домены из факторов транскрипции (активаторы, репрессоры, коактиваторы, корепрессоры), сайленсеры, рецепторы ядерных гормонов, онкогенные факторы транскрипции (например, представители семейств myc, jun, fos, myb, max, mad, rel, ets, bcl, myb, mos и т.д.); ферменты репарации ДНК и ассоциированные с ними факторы и модификаторы; ферменты перестановок в ДНК и ассоциированные с ними факторы и модификаторы; ассоциированные с хроматином белки и их модификаторы (например, киназы, ацетилазы и деацетилазы) и ферменты модификации ДНК (например, метилтрансферазы, топоизомеразы, геликазы, лигазы, киназы, фосфатазы, полимеразы, эндонуклеазы) и ассоциированные с ними факторы и модификаторы.
[0111] Полипептиды факторов транскрипции, из которых можно получать регуляторный домен, включают полипептиды, вовлеченные в регулируемую и базальную транскрипцию. Такие полипептиды включают факторы транскрипции, их эффекторные домены, коактиваторы, сайленсеры, рецепторы ядерных гормонов (для обзора белков и элементов нуклеиновых кислот, вовлеченных в транскрипцию см., например, Goodrich et al., Cell 84:825-30 (1996); факторы транскрипции в основном рассмотрены в Barnes and Adcock, Clin. Exp. Allergy 25 Suppl. 2:46-9 (1995) и Roeder, Methods Enzymol. 273:165-71(1996)). Факторы транскрипции рецепторов ядерных гормонов описаны, например, в Rosen et al., J. Med. Chem. 38:4855-74 (1995). Семейство факторов транскрипции C/EBP рассмотрено в Wedel et al., Immunobiology 193:171-85 (1995). Коактиваторы и корепрессоры, опосредующие регуляцию транскрипции посредством рецепторов ядерных гормонов рассмотрены, например, в Meier, Eur. J. Endocrinol. 134(2):158-9 (1996); Kaiser et al., Trends Biochem. Sci. 21:342-5 (1996); и Utley et al., Nature 394:498-502 (1998)). Факторы транскрипции GATA, вовлеченные в регуляцию гемопоэза, описаны, например, в Simon, Nat. Genet. 11:9-11 (1995); Weiss et al., Exp. Hematol. 23:99-107. Связывающий TATA-бокс белок (TBP) и ассоциированные с ним TAP-полипептиды (включающие TAF30, TAF55, TAF80, TAF 10, TAFI 50 и TAF250) описаны в Goodrich and Tjian, Curr. Opin. Cell Biol. 6:403-9 (1994) и Hurley, Curr. Opin. Struct. Biol. 6:69-75 (1996). Семейство факторов транскрипции STAT рассмотрено, например, в Barahmand-Pour et al., Curr. Top. Microbiol. Immunol. 211:121-8 (1996). Факторы транскрипции, вовлеченные в заболевания, рассмотрены в Aso et al., J. Clin. Invest. 97:1561-9 (1996).
[0112] В одном из вариантов осуществления в качестве репрессора транскрипции применяют репрессирующий домен KRAB из белка человека KOX-1 (Thiesen et al., New Biologist 2:363-374 (1990); Margolin et al., Proc. Natl. Acad. Sci USA 91:4509-4513 (1994); Pengue et al., Nucl. Acids Res. 22:2908-2914 (1994); Witzgall et al., Proc. Natl. Acad. Sci. USA 91:4514-4518 (1994)). В другом варианте осуществления совместно с KRAB применяют KAP-1, корепрессор KRAB (Friedman et al., Gens Dev. 10:2067-2078 (1996)). Альтернативно, KAP-1 можно использовать с ZFP отдельно. Другие предпочтительные факторы транскрипции и домены факторов транскрипции, которые действуют в качестве репрессоров транскрипции, включают MAD (см., например, Sommer et al., J. Biol. Chem. 273:6632-6642 (1998); Gupta et al., Oncogene 16:1149-1159 (1998); Queva et al., Oncogene 16:967-977 (1998); Larsson et al., Oncogene 15:737-748 (1997); Laherty et al., Cell 89:349-356 (1997); и Cultraro et al., Mol. Cell Biol. 17:2353-2359 (19977)); FKHR (головка в гене рабдосаркомы; Ginsberg et al., Cancer Res. 15:3542-3546 (1998); Epstein et al., Mol. Cell Biol. 18:4118-4130 (1998)); EGR-1 (продукт гена раннего фактора роста 1; Yan et al., Proc. Natl. Acad. Sci USA 95:8298-8303 (1998); и Liu et al., Cancer Gene Ther. 5:3-28 (1998)); репрессорный домен фактора репрессии ets2 (ERD; Sgouras et al., EMBO J. 14:4781-4793 ((19095)); домен взаимодействия smSIN3 MAD (SID; Ayer et al., Mol. Cell Biol. 16:5772-5781 (1996)); и амфифильный репрессирующий домен ERF3 (фактор ответа на этилен 3), EAR (Ohta, M., et al. (2001), Plant Cell 13:1959-1968).
[0113] В одном из вариантов осуществления в качестве активатора транскрипции применяют активирующий домен VP16 HSV (см., например, Hagmann et al., J. Virol. 71:5952-5962 (1997)). Другие предпочтительные факторы транскрипции, которые могут обеспечивать активирующие домены, включают активирующий домен VP64 (Seipel et al., EMBO J. 11:4961-4968 (1996)); рецепторы ядерных гормонов (см., например, Torchia et al., Curr. Opin. Cell Biol. 10:373-383 (1998)); субъединицу p65 ядерного фактора каппа B (Bitko and Barik, J. Virol. 72:5610-5618 (1998) и Doyle and Hunt, Neuroreport 8:2937-2942 (1997)); EGR-1 (продукт гена раннего фактора роста 1; Yan et al., Proc. Natl. Acad. Sci USA 95:8298-8303 (1998); и Liu et al., Cancer Gene Ther. 5:3-28 (1998)); и регуляторный белок пути биосинтеза антоцианина кукурузы, C1 (S.A. Goff, et al., (1991), Genetics and Development 5:298-309).
[0114] Также в качестве регуляторных доменов для ZFP пригодны киназы, фосфатазы и другие модифицирующие полипептиды белки, вовлеченные в регуляцию генов. Такие модификаторы часто вовлечены в запуск или останову транскрипции, опосредованные, например, гормонами. Киназы, вовлеченные в регуляцию транскрипции, рассмотрены в Davis, Mol. Reprod. Dev. 42:459-67 (1995), Jackson et al., Adv. Second Messenger Phosphoprotein Res. 28:279-86 (1993), и Boulikas, Crit. Rev. Eukaryot. Gene Expr. 5:1-77 (1995), тогда как фосфатазы рассмотрены, например, в Schonthal and Semin, Cancer Biol. 6:239-48 (1995). Ядерные тирозинкиназы описаны в Wang, Trends Biochem. Sci. 19:373-6 (1994).
[0115] Как описано, пригодные домены также можно получать из продуктов генов онкогенов (например, представителей семейств myc, jun, fos, myb, max, mad, rel, ets, bcl, myb, mos) и ассоциированных с ними факторов и модификаторов. Онкогены описаны, например, в Cooper, Oncogenes, 2nd ed., The Jones and Bartlett Series in Biology, Boston, Mass., Jones and Bartlett Publishers, 1995. Факторы транскрипции ets рассмотрены в Waslylk et al., Eur. J. Biochem. 211:7-18 (1993) и Crepieux et al., Crit. Rev. Oncog. 5:615-38 (1994). Онкогены myc рассмотрены, например, в Ryan et al., Biochem. J. 314:713-21 (1996). Факторы транскрипции jun и fos описаны, например, в The Fos and Jun Families of Transcription Factors, Angel and Herrlich, eds. (1994). Онкоген max рассмотрен в Hurlin et al., Cold Spring Harb. Symp. Quant. Biol. 59:109-16. Семейство генов myb рассмотрено в Kanei-Ishii et al., Curr. Top. Microbiol. Immunol. 211:89-98 (1996). Семейство mos рассмотрено в Yew et al., Curr. Opin. Genet. Dev. 3:19-25 (1993).
[0116] ZFP могут содержать регуляторные домены, получаемые из ферментов репарации ДНК и ассоциированных с ними факторов и модификаторов. Системы репарации ДНК рассмотрены, например, в Vos, Curr. Opin. Cell Biol. 4:385-95 (1992); Sancar, Ann. Rev. Genet. 29:69-105 (1995); Lehmann, Genet. Eng. 17:1-19 (1995); и Wood, Ann. Rev. Biochem. 65:135-67 (1996). Также в качестве регуляторных доменов можно использовать ферменты перестановок в ДНК и ассоциированные с ними факторы и модификаторы (см., например, Gangloff et al., Experientia 50:261-9 (1994); Sadowski, FASEB J. 7:760-7 (1993)).
[0117] Подобным образом, регуляторные домены можно получать из ферментов модификации ДНК (например, ДНК-метилтрансфераз, -топоизомераз, -геликаз, -лигаз, -киназ, -фосфатаз, -полимераз) и ассоциированных с ними факторов и модификаторов. Геликазы рассмотрены в Matson et al., Bioessays, 16:13-22 (1994), а метилтрансферазы описаны в Cheng, Curr. Opin. Struct. Biol. 5:4-10 (1995). Также пригодными доменами выбора для добавления в ZFP являются ассоциированные с хроматином белки и их модификаторы (например, киназы, ацетилазы и деацетилазы), такие как деацетилаза гистонов (Wolffe, Science 272:371-2 (1996)). В одном из предпочтительных вариантов осуществления регуляторный домен представляет собой ДНК-метилтрансферазу, которая действует в качестве репрессора транскрипции (см., например, Van den Wyngaert et al., FEBS Lett. 426:283-289 (1998); Flynn et al., J. Mol. Biol. 279:101-116 (1998); Okano et al., Nucleic Acids Res. 26:2536-2540 (1998); и Zardo and Caiafa, J. Biol. Chem. 273:16517-16520 (1998)). В другом предпочтительном варианте осуществления в качестве репрессоров транскрипции, которые действуют посредством расщепления генов, используют эндонуклеазы, такие как FokI (см., например, WO95/09233 и PCT/US94/01201).
[0118] Также для получения химерных белков можно использовать факторы, контролирующие структуру, перемещение и локализацию хроматина и ДНК и ассоциированные с ними факторы и модификаторы; факторы, получаемые из микроорганизмов (например, прокариот, эукариот и вирусов), и факторы, ассоциированные с ними или модифицирующие их. В одном из вариантов осуществления в качестве регуляторных доменов используют рекомбиназы и интегразы. В одном из вариантов осуществления в качестве активатора транскрипции применяют гистонацетилтрансферазу (см., например, Jin and Scotto, Mol. Cell Biol. 18:4377-4384 (1998); Wolffe, Science 272:371-372 (1996); Taunton et al., Science 272:408-411 (1996); и Hassig et al., Proc. Natl. Acad. Sci USA 95:3519-3524 (1998)). В другом варианте осуществления в качестве репрессора транскрипции применяют гистондеацетилазу (см., например, Jin and Scotto, Mol. Cell Biol. 18:4377-4384 (1998); Syntichaki and Thireos, J. Biol. Chem. 273: 24414-24419 (1998); Sakaguchi et al., Genes Dev. 12:2831-2841 (1998); и Martinez et al, J. Biol. Chem. 273:23781-23785 (1998)).
[0119] Можно включать линкерные домены между полипептидными доменами, например, между двумя ZFP или между ZFP и регуляторным доменом. Такие линкеры, как правило, представляют собой полипептидные последовательности, такие как последовательности поли-gly длиной приблизительно от 5 до 200 аминокислот. Линкеры могут представлять собой гибкие или жесткие подпоследовательности аминокислот, синтезируемые как часть слитого рекомбинантного белка. См., например, патент США № 6534261; Liu et al., Proc. Nat. Acad. Sci. USA, 95:5525-5530 (1997); Pomerantz et al., Proc. Nat. Acad. Sci. USA 92:9752-9756 (1995); Kim et al., Proc. Nat. Acad. Sci. USA 93:1156-1160 (1996); полностью включенные в настоящий документ посредством ссылки. Альтернативно, гибкие линкеры можно рационально составлять с использованием компьютерной программы, способной к моделированию участков связывания ДНК и самих пептидов (Desjarlais and Berg, Proc. Nat. Acad. Sci. USA 90:2256-2260 (1993), Desjarlais and Berg, Proc. Nat. Acad. Sci. USA 91:11099-11103 (1994), или способами фагового дисплея.
[0120] В других вариантах осуществления для связывания синтетически или рекомбинантно получаемых последовательностей доменов используют химический линкер. Такие гибкие линкеры известны специалистам в данной области. Например, в Shearwater Polymers, Inc. Huntsville, Ala доступны поли(этиленгликолевые) линкеры. Эти линкеры необязательно содержат амидные связи, сульфгидрильные связи или гетерофункциональные связи. Кроме ковалентной связи ZFP с регуляторными доменами, для получения молекул с ZFP, связанными с регуляторными доменами, можно использовать нековалентные способы.
Домены расщепления
[0121] Как указано выше, ДНК-связывающий домен также можно связывать с доменом расщепления (нуклеазой). Например, можно модифицировать специфичность связывания ДНК хоминг-эндонуклеаз, сохраняя нуклеазную функцию. Кроме того, белки с цинковыми пальцами также можно сливать с доменом расщепления с формированием нуклеаз с цинковыми пальцами (ZFN). Часть домена расщепления слитых белков, описываемых в настоящем документе, можно получать из любой эндонуклеазы или экзонуклеазы. Иллюстративные эндонуклеазы, из которых можно получать домен расщепления, в качестве неограничивающих примеров включают рестрикционные эндонуклеазы и хоминг-эндонуклеазы. См., например, Каталог 2002-2003, New England Biolabs, Beverly, MA; и Belfort et al. (1997) Nucleic Acids Res. 25:3379-3388. Известны дополнительные ферменты, расщепляющие ДНК (например, нуклеаза S1; нуклеаза бобов мунг; панкреатическая ДНКаза I; микрококковая нуклеаза; эндонуклеаза дрожжей HO; также см. Linn et al. (eds.) Nucleases, Cold Spring Harbor Laboratory Press, 1993). Один или несколько из этих ферментов (или их функциональные фрагменты) можно использовать в качестве источников доменов расщепления и полудоменов расщепления.
[0122] Подобным образом, из любой нуклеазы или ее части, как указано выше, можно получать полудомен расщепления, которому для проявления расщепляющей активности необходима димеризация. Как правило, если слитые белки содержат полудомены расщепления, для расщепления необходимы два слитых белка. Альтернативно, можно использовать один белок, содержащий два полудомена расщепления. Два полудомена расщепления можно получать из одной и той же эндонуклеазы (или ее функциональных фрагментов), или каждый полудомен расщепления можно получать из различных эндонуклеаз (или их функциональных фрагментов). Кроме того, участки-мишени для двух слитых белков предпочтительно расположены друг относительно друга так, чтобы связывание двух слитых белков с их соответствующими участками-мишенями помещало полудомены расщепления в пространственной ориентации друг относительно друга так, чтобы обеспечивать формирование полудоменами расщепления функционального домена расщепления, например, посредством димеризации. Таким образом, в определенных вариантах осуществления ближайшие границы участков-мишеней разделены 5-8 нуклеотидами или 15-18 нуклеотидами. Однако между двумя участками-мишенями может находиться любое целочисленное количество нуклеотидов или пар нуклеотидов (например, от 2 до 50 пар нуклеотидов или более). Как правило, участок расщепления расположен между участками-мишенями.
[0123] Рестрикционные эндонуклеазы (рестрикционные ферменты) существуют у многих видов и способны к специфичному для последовательности связыванию с ДНК (в участке распознавания) и расщеплению ДНК в участке связывания или рядом с ним. Определенные рестрикционные ферменты (например, типа IIS) расщепляют ДНК в участках вне участка распознавания и содержат раздельные домены связывания и расщепления. Например, фермент типа IIS FokI катализирует двухцепочечное расщепление ДНК, в 9 нуклеотидах от его участка распознавания на одной цепи и в 13 нуклеотидах от его участка распознавания на другой. См., например, патенты США 5356802; 5436150 и 5487994; а также Li et al. (1992) Proc. Natl. Acad. Sci. USA 89:4275-4279; Li et al. (1993) Proc. Natl. Acad. Sci. USA 90:2764-2768; Kim et al. (1994a) Proc. Natl. Acad. Sci. USA 91:883-887; Kim et al. (1994b) J. Biol. Chem. 269:31978-31982. Таким образом, в одном из вариантов осуществления слитые белки содержат домен расщепления (или полудомен расщепления) по меньшей мере из одного рестрикционного фермента типа IIS и один или несколько связывающих доменов цинковых пальцев, которые могут являться конструируемыми или нет.
[0124] Иллюстративным рестрикционным ферментом типа IIS, домен расщепления которого находится отдельно от связывающего домена, является FokI. Этот конкретный фермент активен в качестве димера. Bitinaite et al. (1998) Proc. Natl. Acad. Sci. USA 95:10570-10575. Таким образом, для целей настоящего описания, часть фермента FokI, используемую в описываемых слитых белках, рассматривают как полудомен расщепления. Таким образом, для направленного двухцепочечного расщепления и/или направленного замещения клеточных последовательностей с использованием слияний цинковый палец-FokI, для восстановления каталитически активного домена расщепления можно использовать два слитых белка, где каждый содержит полудомен расщепления FokI. Альтернативно, также можно использовать одну полипептидную молекулу, содержащую связывающий домен цинковых пальцев и два полудомена расщепления FokI. Параметры для направленного расщепления и направленного изменения последовательности с использованием слияний цинковый палец-FokI предоставлены в другой части данного описания.
[0125] Домен расщепления или полудомен расщепления может представлять собой любую часть белка, сохраняющую расщепляющую активность или сохраняющую способность к мультимеризации (например, димеризации) с формированием функционального домена расщепления.
[0126] Иллюстративные рестрикционные ферменты типа IIS описаны в международной публикации WO 07/014275, полностью включенной в настоящий документ. Также отдельные домены связывания и расщепления содержат дополнительные рестрикционные ферменты, и они предусмотрены в настоящем описании. См., например, Roberts et al. (2003) Nucleic Acids Res. 31:418-420.
[0127] В определенных вариантах осуществления домен расщепления содержит один или несколько конструируемых полудоменов расщепления (также обозначаемых как мутантные димеризующиеся домены), минимизирующих или предотвращающих гомодимеризацию, как описано, например, в патентных публикациях США №№ 20050064474; 20060188987; 20080131962, все описания которых полностью включены в настоящий документ посредством ссылки. Мишенями для воздействия на димеризацию полудоменов расщепления FokI являются аминокислотные остатки в положениях 446, 447, 479, 483, 484, 486, 487, 490, 491, 496, 498, 499, 500, 531, 534, 537 и 538 FokI.
[0128] Иллюстративные конструируемые полудомены расщепления FokI, формирующие облигатные гетеродимеры, включают пару, в которой первый полудомен расщепления содержит мутации по аминокислотным остаткам в положениях 490 и 538 FokI, а второй полудомен расщепления содержит мутации по аминокислотным остаткам 486 и 499.
[0129] Таким образом, в определенных вариантах осуществления мутация в 490 замещает Glu (E) на Lys (K); мутация в 538 замещает Iso (I) на Lys (K); мутация в 486 замещает Gln (Q) на Glu (E); а мутация в положении 499 замещает Iso (I) на Lys (K). В частности, конструируемые полудомены расщепления, описываемые в настоящем документе, получали посредством внесения мутаций в положения 490 (E→K) и 538 (I→K) в одном из полудоменов расщепления с получением конструируемого полудомена расщепления, обозначаемого "E490K:I538K", и посредством внесения мутаций в положения 486 (Q→E) и 499 (I→L) в другом полудомене расщепления с получением сконструированного полудомена расщепления, обозначаемого "Q486E:I499K". Конструируемые полудомены расщепления, описываемые в настоящем документе, являются облигатными мутантными гетеродимерами, в которых минимизировано или устранено нарушенное расщепление. См., например, пример 1 патентной публикации США № 2008/0131962, описание которой полностью включено посредством ссылки для всех целей. Также см. Szczepek et al. (2007) Nat Biotechnol 25:786-793. В определенных вариантах осуществления конструируемый полудомен расщепления содержит мутации в положениях 486, 499 и 496 (нумеруемых относительно FokI дикого типа), например, мутации, замещающие остаток дикого типа Gln (Q) в положении 486 на остаток Glu (E), остаток дикого типа Iso (I) в положении 499 на остаток Leu (L) и остаток дикого типа Asn (N) в положении 496 на Asp (D) или остаток Glu (E) (также обозначаемый как домены "ELD" и "ELE", соответственно). В других вариантах осуществления конструируемый полудомен расщепления содержит мутации в положениях 490, 538 и 537 (нумеруемых относительно FokI дикого типа), например, мутации, замещающие остаток дикого типа Glu (E) в положении 490 на остаток Lys (K), остаток дикого типа Iso (I) в положении 538 на остаток Lys (K) и остаток дикого типа His (H) в положении 537 на остаток Lys (K) или остаток Arg (R) (также обозначаемый как домены "KKK" и "KKR", соответственно). В других вариантах осуществления конструируемый полудомен расщепления содержит мутации в положениях 490 и 537 (нумеруемых относительно FokI дикого типа), например, мутации, замещающие остаток дикого типа Glu (E) в положении 490 на остаток Lys (K) и остаток дикого типа His (H) в положении 537 на остаток Lys (K) или остаток Arg (R) (также обозначаемый как домены "KIK" и "KIR", соответственно). (См. предварительную заявку США 61/337769, поданную 8 февраля 2010 года). В других вариантах осуществления конструируемый полудомен расщепления содержит мутации "Sharkey" и/или "Sharkey'" (см. Guo et al., (2010) J. Mol. Biol. doi:10,1016/j.jmb.2010,04,060).
[0130] Конструируемые полудомены расщепления, описываемые в настоящем документе можно получать любым подходящим способом, например, посредством сайт-специфического мутагенеза полудоменов расщепления дикого типа (FokI), как описано в патентных публикациях США №№ 20050064474 и 20080131962.
[0131] Другим предпочтительным рестрикционным ферментом типа IIS является BfiI (см. Zaremba et al., (2004) J. Mol Biol. 336(1):81-92). Домен расщепления этого фермента можно отделять от его ДНК-связывающего домена и функционально связывать с ДНК-связывающим доменом цинковых пальцев с получением ZFN.
Слитые белки
[0132] Способы составления и конструирования слитых белков (и полинуклеотиды, кодирующих их) известны специалистам в данной области. Например, способы составления и конструирования слитых белков, содержащих ДНК-связывающие домены (например, домены цинковых пальцев) и регуляторные домены или домены расщепления (или полудомены расщепления), и полинуклеотидов, кодирующих такие слитые белки, описаны в принадлежащих тем же заявителям патентах США 6453242 и 6534261 и публикациях патентных заявок США 2007/0134796 и 2005/0064474; полностью включенных в настоящий документ посредством ссылки.
[0133] В определенных вариантах осуществления конструируют полинуклеотиды, кодирующие слитые белки. Эти полинуклеотиды можно вставлять в вектор, а вектор вводить в клетку (см. ниже для дополнительного описания векторов и способов введения полинуклеотидов в клетки).
[0134] Как указано выше, в определенных вариантах осуществления слитый белок содержит белок с цинковыми пальцами, связывающийся с участком-мишенью в гене, вовлеченном в биосинтез жирных кислот, и по меньшей мере один домен регуляции транскрипции, например, активирующий или репрессирующий домен.
[0135] В других вариантах осуществления способов, описываемых в настоящем документе, нуклеазы с цинковыми пальцами содержат слитый белок, содержащий связывающий домен цинковых пальцев и полудомен расщепления из рестрикционного фермента FokI, и в клетке экспрессируются два таких белка. Экспрессия двух слитых белков в клетке может являться результатом доставки в клетку двух белков; доставки в клетку одного белка и одной нуклеиновой кислоты, кодирующей один из белков; доставки в клетку двух нуклеиновых кислот, где каждая кодирует один из белков; или доставки в клетку одной нуклеиновой кислоты, кодирующей оба белка. В дополнительных вариантах осуществления слитый белок содержит одну полипептидную цепь, содержащую два полудомена расщепления и связывающий домен цинковых пальцев. В этом случае в клетке экспрессируется один слитый белок и, не желая быть связанным теорией, полагают, что он расщепляет ДНК в результате формирования внутримолекулярного димера из полудоменов расщепления.
[0136] В определенных вариантах осуществления компоненты нуклеаз с цинковыми пальцами (например, слияний ZFP-FokI) расположены так, что домен цинковых пальцев расположен ближе к N-концу слитого белка, а полудомен расщепления расположен ближе к C-концу. Это является зеркальным отражением относительной ориентации домена расщепления в природных димеризующихся доменах расщепления, таких как домены, происходящие из фермента FokI, в котором ДНК-связывающий домен расположен ближе к N-концу, а полудомен расщепления расположен ближе к C-концу. В этих вариантах осуществления димеризация полудоменов расщепления с формированием функциональной нуклеазы обусловлена связыванием слитых белков с участками на противоположных цепях ДНК, где 5'-концы участков связывания расположены проксимально друг относительно друга.
[0137] В дополнительных вариантах осуществления компоненты слитых белков (например, слияния ZFP-FokI) расположены так, что полудомен расщепления расположен ближе к N-концу слитого белка, а домен цинковых пальцев расположен ближе к C-концу. В этих вариантах осуществления димеризация полудоменов расщепления с формированием функциональной нуклеазы обусловлена связыванием слитых белков с участками на противоположных цепях ДНК, где 3'-концы участков связывания расположены проксимально друг относительно друга.
[0138] В дополнительных вариантах осуществления первый слитый белок содержит полудомен расщепления ближе к N-концу слитого белка, а домен цинковых пальцев ближе к C-концу, а второй слитый белок сконструирован так, что домен цинковых пальцев расположен ближе к N-концу слитого белка, а полудомен расщепления расположен ближе к C-концу. В этих вариантах осуществления оба слитых белка связываются с одной и той же цепью ДНК, где участок связывания первого слитого белка, содержащий домен цинковых пальцев ближе к C-концу, расположен с 5'-конца от участка связывания второго слитого белка, содержащего домен цинковых пальцев ближе к N-концу.
[0139] В определенных вариантах осуществления описанных слитых белков аминокислотная последовательность между доменом цинковых пальцев и доменом расщепления (или полудоменом расщепления) обозначают "ZC-линкер". ZC-линкер следует отличать от линкеров между пальцами, описанных выше. Для подробностей получения ZC-линкеров, оптимизирующих расщепление, см., например, патентные публикации США 20050064474A1 и 20030232410 и международную патентную публикацию WO05/084190.
[0140] В одном из вариантов осуществления описание относится к содержащему ZFN белку с цинковыми пальцами с аминокислотными последовательностями с распознающими спиралями, представленными в таблице 1 или таблице 10. В другом варианте осуществления в настоящем документе предоставлен экспрессирующий ZFN вектор, содержащий нуклеотидную последовательность, кодирующую ZFP с распознающими спиралями, представленными в таблице 1 или таблице 10.
Регуляция экспрессии гена
[0141] Для определения того, модулирует ли ZFP экспрессию генов, можно использовать множество анализов. Активность конкретного ZFP можно оценивать с использованием множества анализов in vitro и in vivo, измеряя, например, уровни белка или мРНК, уровни продуктов, активность фермента; активацию или репрессию транскрипции репортерного гена, например, с использованием иммунологических анализов (например, ELISA и иммуногистохимических анализов с антителами), анализов гибридизации (например, защиты от РНКазы, нозерн-блот, гибридизацию in situ, исследования олигонуклеотидных панелей), колориметрических анализов, анализов амплификации, анализов активности ферментов, анализов фенотипа и т.п.
[0142] Как правило, ZFP сначала тестируют на активность in vitro с использованием анализов ELISA, а затем с использованием клеток почки. Часто ZFP сначала тестируют с использованием системы транзиторной экспрессии с репортерным геном, а затем тестируют регуляцию эндогенного гена-мишени в клетках и в целых растениях, in vivo и ex vivo. ZFP можно рекомбинантно экспрессировать в клетке, рекомбинантно экспрессировать в клетках, трансплантированных в растение, или рекомбинантно экспрессировать в трансгенном растении, а также вводить в растение или клетку в виде белка с использованием доставляющих носителей, описанных ниже. Клетки могут быть иммобилизованы, находиться в растворе, их можно инъецировать в растение, или они могут находиться в природе в трансгенном или нетрансгенном растении.
[0143] Модуляцию экспрессии гена тестируют с использованием одного из анализов in vitro или in vivo, описываемых в настоящем документе. Образцы или анализы обрабатывают ZFP и сравнивают с контрольными образцами без тестируемого соединения для исследования степени модуляции. Для регуляции эндогенной экспрессия гена, ZFP, как правило, обладает Kd 200 нМ или менее, более предпочтительно - 100 нМ или менее, более предпочтительно - 50 нМ, наиболее предпочтительно - 25 нМ или менее.
[0144] Эффекты ZFP можно измерять, исследуя любой из параметров, описанный выше. Для оценки влияния ZFP можно использовать любое подходящее изменение экспрессии гена, фенотипическое или физиологическое изменение. Когда функциональные следствия определяют с использованием интактных клеток или растений, также можно измерять ряд таких эффектов, как рост растений, изменения транскрипции известных и неохарактеризованных генетических маркеров (например, исследования нозерн-блоттинга или олигонуклеотидных панелей), изменения клеточного метаболизма, такие как изменения роста клеток или pH, и изменения внутриклеточных вторичных мессенджеров, таких как cGMP.
[0145] Предпочтительные анализы для регуляции ZFP эндогенной экспрессии гена можно проводить in vitro. В одном из предпочтительных форматов анализа in vitro, регуляцию ZFP эндогенной экспрессии гена в культивируемых клетках измеряют, исследуя продукцию белка с использованием анализа ELISA. Тестируемый образец сравнивают с контрольными клетками, обрабатываемыми пустым вектором или посторонним ZFP, который направлен на другой ген.
[0146] В другом варианте осуществления регуляцию ZFP эндогенной экспрессии гена определяют in vitro, измеряя уровень экспрессии мРНК гена-мишени. Уровень экспрессии гена измеряют с использованием амплификации, например, с использованием ПЦР, LCR или анализов гибридизации, например, нозерн-гибридизации, защиты от РНКазы, дот-блоттинга. В одном из вариантов осуществления используют защиту от РНКазы. Уровень белка или мРНК детектируют с использованием непосредственно или опосредованно меченых средств для детекции, например, флуоресцентно или радиоактивно меченых нуклеиновых кислот, радиоактивно или ферментативно меченых антител и т.п., как описано в настоящем документе.
[0147] Альтернативно, можно разрабатывать систему с репортерным геном с использованием промотора гена-мишени, функционально связанного с репортерным геном, таким как люцифераза, зеленый флуоресцентный белок, CAT или β-gal. Как правило, репортерную конструкцию котрансфицируют в культивируемую клетку. После обработки выбранным ZFP количественно измеряют транскрипцию, трансляцию или активность репортерного гена стандартными способами, известными специалистам в данной области.
[0148] Также в качестве предпочтительного варианта изобретения для исследования регуляции эндогенной экспрессии гена in vivo используют трансгенные и нетрансгенные растения. Трансгенные растения могут стабильно экспрессировать выбранный ZFP. Альтернативно, можно использовать растения, транзиторно экспрессирующие выбранный ZFP или в которые вводят ZFP в доставляющем носителе. Регуляцию эндогенной экспрессии гена тестируют с использованием любого из анализов, описываемых в настоящем документе.
Способы направленного расщепления
[0149] Описываемые способы и композиции можно использовать для расщепления ДНК в представляющей интерес области в клеточном хроматине (например, в желаемом или предопределенном участке генома, например, в гене, вовлеченном в биосинтез жирных кислот, или рядом с ним). Для такого направленного расщепления ДНК, связывающий домен цинковых пальцев конструируют для связывания с участком-мишенью в предопределенном участке расщепления или рядом с ним, и слитый белок, содержащий конструируемый связывающий домен цинковых пальцев и домен расщепления, экспрессируют в клетке. После связывания части слитого белка с цинковыми пальцами с участком-мишенью, домен расщепления расщепляет ДНК рядом с участком-мишенью. Точный участок расщепления может зависеть от длины ZC-линкера.
[0150] Альтернативно, в клетке экспрессируют два слитых белка, где каждый содержит связывающий домен цинковых пальцев и полудомен расщепления, и связывают с участками-мишенями, которые расположены рядом таким образом, что восстанавливается функциональный домен расщепления и расщепляет ДНК рядом с участками-мишенями. В одном из вариантов осуществления расщепление происходит между участками-мишенями двух связывающих доменов цинковых пальцев. Один или оба связывающих домена цинковых пальцев могут быть конструируемыми.
[0151] Для направленного расщепления с использованием слитого полипептида из связывающего домена цинковых пальцев-домена расщепления участок связывания может содержать участок расщепления, или ближний конец участка связывания может располагаться на расстоянии 1, 2, 3, 4, 5, 6, 10, 25, 50 или более нуклеотидов (или на любом целочисленном значении от 1 до 50 нуклеотидов) от участка расщепления. Точное положение участка связывания относительно участка расщепления зависит от конкретного домена расщепления и длины ZC-линкера. Для способов, в которых используют два слитых полипептида, где каждый содержит связывающий домен цинковых пальцев и полудомен расщепления, участки связывания, как правило, расположены с двух сторон от участка расщепления. Таким образом, ближний конец первого участка связывания может располагаться на расстоянии 1, 2, 3, 4, 5, 6, 10, 25 или более нуклеотидов (или на любом целочисленном значении от 1 до 50 нуклеотидов) от одной из сторон от участка расщепления, и ближний конец второго участка связывания может располагаться на расстоянии 1, 2, 3, 4, 5, 6, 10, 25 или более нуклеотидов (или на любом целочисленном значении от 1 до 50 нуклеотидов) от другой стороны участка расщепления. Способы картирования участков расщепления in vitro и in vivo известны специалистам в данной области.
[0152] Таким образом, в способах, описываемых в настоящем документе, можно использовать конструируемый связывающий домен цинковых пальцев, слитый с доменом расщепления. В этих случаях связывающий домен конструируют для связывания с последовательностью-мишенью в месте, где желательно расщепление, или рядом с ним. Слитый белок или полинуклеотид, кодирующий его, вводят в растительную клетку. После введения в клетку или экспрессии в ней слитый белок связывается с последовательностью-мишенью и производит расщепление в последовательности-мишени или рядом с ней. Точный участок расщепления зависит от характера домена расщепления и/или присутствия и/или характера линкерных последовательностей между доменами связывания и расщепления. В случаях, когда используют два слитых белка, где каждый содержит полудомен расщепления, расстояние между ближайшими границами участков связывания может составлять 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 25 или более нуклеотидов (или любое целочисленное значение от 1 до 50 нуклеотидов). Оптимальные уровни расщепления также могут зависеть от расстояния между участками связывания двух слитых белков (см., например, Smith et al. (2000) Nucleic Acids Res. 28:3361-3369; Bibikova et al. (2001) Mol. Cell. Biol. 21:289-297) и длины ZC-линкера в каждом слитом белке. Также см. патентную публикацию США 20050064474A1 и международные патентные публикации WO05/084190, WO05/014791 и WO03/080809.
[0153] В определенных вариантах осуществления домен расщепления содержит два полудомена расщепления, которые оба являются частью одного полипептида, содержащего связывающий домен, первый полудомен расщепления и второй полудомен расщепления. Полудомены расщепления могут обладать одинаковой аминокислотной последовательностью или различными аминокислотными последовательностями при условии, что они функционируют с расщеплением ДНК.
[0154] Полудомены расщепления также можно предоставлять в отдельных молекулах. Например, в клетку можно вводить два слитых полипептида, где каждый полипептид содержит связывающий домен и полудомен расщепления. Полудомены расщепления могут обладать одинаковой аминокислотной последовательностью или различными аминокислотными последовательностями при условии, что они функционируют с расщеплением ДНК. Кроме того, связывающие домены связываются с последовательностями-мишенями, которые, как правило, расположены таким образом, что после связывания слитых полипептидов, два полудомена расщепления представляются друг относительно друга в пространственной ориентации, обеспечивающей восстановление домена расщепления (например, посредством димеризации полудоменов), таким образом, располагая полудомены друг относительно друга с формированием функционального домена расщепления, что приводит к расщеплению клеточного хроматина в представляющей интерес области. Как правило, расщепление восстановленным доменом расщепления происходит в участке, расположенном между двух последовательностей-мишеней. Один или оба белка могут быть сконструированы для связывания с их участком-мишенью.
[0155] Два слитых белка могут связываться в представляющей интерес области в одной и той же или противоположной полярности, и их участки связывания (т.е., участки-мишени) могут разделяться любым количеством нуклеотидов, например, от 0 до 200 нуклеотидов или любым целочисленным значением между ними. В определенных вариантах осуществления участки связывания для двух слитых белков, где каждый содержит связывающий домен цинковых пальцев и полудомен расщепления, могут располагаться на расстоянии от 5 до 18 нуклеотидов, например, на расстоянии 5-8 нуклеотидов, или на расстоянии 15-18 нуклеотидов или на расстоянии 6 нуклеотидов или на расстоянии 16 нуклеотидов, как измеряют от конца каждого участка связывания, ближайшего к другому участку связывания, а расщепление происходит между участками связывания.
[0156] Участок, в котором расщепляется ДНК, как правило, расположен между участками связывания для двух слитых белков. Двухцепочечный разрыв ДНК часто является результатом двух одноцепочечных разрывов или "ников" со смещением на 1, 2, 3, 4, 5, 6 или более нуклеотидов (например, расщепление двухцепочечной ДНК природной FokI является результатом одноцепочечных разрывов со смещением на 4 нуклеотида). Таким образом, расщепление не обязательно происходит точно на противоположных сторонах каждой цепи ДНК. Кроме того, структура слитых белков и расстояние между участками-мишенями может влиять на то, произойдет ли расщепление рядом с одной парой нуклеотидов, или расщепление произойдет в различных участках. Однако для большинства применений, включая направленную рекомбинацию и направленный мутагенез (см. ниже), как правило, достаточно расщепления в некотором диапазоне нуклеотидов, и расщепления между конкретными парами оснований не требуется.
[0157] Как указано выше, слитый белок(ки) можно вводить в виде полипептидов и/или в виде полинуклеотидов. Например, в клетку можно вводить два полинуклеотида, где каждый содержит последовательности, кодирующие один из указанных выше полипептидов, и когда полипептиды экспрессируются и каждый связывается с его последовательностью-мишенью, происходит расщепление в последовательности-мишени или рядом с ней. Альтернативно, в клетку вводят один полинуклеотид, содержащий последовательности, кодирующие оба слитых полипептида. Полинуклеотиды могут представлять собой ДНК, РНК или любые модифицированные формы или аналоги ДНК и/или РНК.
[0158] Для увеличения специфичности расщепления в способах, описываемых в настоящем документе, можно использовать дополнительные композиции. Например, одиночные полудомены расщепления могут проявлять ограниченную активность расщепления двух цепей. В способах, где в клетку вводят два слитых белка, где каждый содержит домен цинковых пальцев с тремя пальцами и полудомен расщепления, каждый белок определяет участок-мишень приблизительно из 9 нуклеотидов. Хотя совокупная последовательность-мишень из 18 нуклеотидов, вероятно, является уникальной в геномах млекопитающих и растений, любой данный участок-мишень из 9 нуклеотидов в среднем в геноме человека встречается приблизительно 23000 раз. Таким образом, может происходить неспецифическое расщепление, вследствие специфического связывания одного полудомена с участком. Таким образом, способы, описываемые в настоящем документе, предусматривают использование доминантно-негативного мутанта полудомена расщепления, такого как FokI (или нуклеиновой кислоты, кодирующей его), который экспрессируется в клетке вместе с двумя слитыми белками. Доминантно-негативный мутант способен к димеризации, но не способен к расщеплению, а также блокирует расщепляющую активность полудомена с которым он димеризуется. Обеспечивая молярный избыток доминантно-негативного мутанта по отношению к слитым белкам, только в областях, в которых связаны оба слитых белка, будет содержаться достаточно высокая локальная концентрация функциональных полудоменов расщепления для прохождения димеризации и расщепления. В участках, где связан только один из двух слитых белков, его полудомен расщепления формирует димер с доминантно-негативным мутантным полудоменом, и нежелательного, неспецифического расщепления не происходит.
Экспрессирующие векторы
[0159] Нуклеиновую кислоту, кодирующую один или несколько белков (например, ZFP), как описано в настоящем документе, можно клонировать в вектор для трансформации в прокариотические или эукариотические клетки для репликации и/или экспрессии. Векторы могут представлять собой прокариотические векторы, например, плазмиды или челночные векторы, векторы насекомых, вирусные векторы или эукариотические векторы. Нуклеиновую кислоту, кодирующую ZFP, также можно клонировать в экспрессирующий вектор для введения в растительную клетку.
[0160] Для экспрессии ZFP, последовательности, кодирующие ZFP, как правило, субклонируют в экспрессирующий вектор, содержащий промотор, контролирующий транскрипцию. Подходящие бактериальные и эукариотические промоторы хорошо известны в данной области и описаны, например, в Sambrook et al., Molecular Cloning, A Laboratory Manual (2nd ed. 1989; 3rd ed., 2001); Kriegler, Gene Transfer and Expression: A Laboratory Manual Stockton Press, New York (1990); и Current Protocols in Molecular Biology (Ausubel et al., выше). Бактериальные экспрессирующие системы для экспрессии ZFP доступны, например, для E. coli, видах Bacillus и Salmonella (Palva et al., Gene 22:229-235 (1983)). Наборы для таких экспрессирующих систем являются коммерчески доступными. Эукариотические экспрессирующие системы для клеток млекопитающих, растений, дрожжей и насекомых хорошо известны специалистам в данной области и также являются коммерчески доступными.
[0161] Промотор, используемый для контроля экспрессии кодирующей ZFP нуклеиновой кислоты, зависит от конкретного применения. Например, для экспрессии и очистки ZFP, как правило, используют сильный конститутивный промотор, подходящий для клетки-хозяина.
[0162] В отличие от этого, когда ZFP вводят in vivo для регуляции ген растения (см., раздел "доставка нуклеиновых кислот в растительные клетки", ниже), в зависимости от конкретного применения ZFP используют или конститутивный или индуцибельный промотор. Неограничивающие примеры промоторов растений включают промоторные последовательности, получаемые из убиквитина-3 A. thaliana (ubi-3) (Callis, et al., 1990, J. Biol. Chem. 265-12486-12493); маннопинсинтазы A. tumefaciens (Δmas) (Petolino et al., патент США № 6730824); и/или вирус мозаики жилок маниоки (CsVMV) (Verdaguer et al., (1996), Plant Molecular Biology 31:1129-1139). Также см. раздел примеров.
[0163] Кроме промотора, экспрессирующий вектор, как правило, содержит транскрипционную единицу или экспрессирующую кассету, которая содержит все дополнительные элементы, необходимые для экспрессии нуклеиновой кислоты в клетках-хозяевах, прокариотических или эукариотических. Таким образом, типичная экспрессирующая кассета содержит промотор, функционально связанный, например, с последовательностью нуклеиновой кислоты, кодирующей ZFP, и сигналы, необходимые, например, для эффективного полиаденилирования транскрипта, терминации транскрипции, участков связывания рибосом или терминации трансляции. Дополнительные элементы кассеты могут включать, например, энхансеры, гетерологичные сигналы сплайсинга и/или сигнал ядерной локализации (NLS).
[0164] Конкретный экспрессирующий вектор, используемый для переноса генетической информации в клетку, выбирают, учитывая планируемое применение ZFP, например, экспрессию у растений, животных, бактерий, грибов, простейших и т.д. (см. экспрессирующие векторы, описанные ниже). В данной области известны и подробно описаны стандартные экспрессирующие векторы бактерий и животных, например, в патентной публикации США 20050064474A1 и в международных патентных публикациях WO05/084190, WO05/014791 и WO03/080809.
[0165] Для получения линий клеток бактерий, млекопитающих, растений, дрожжей или насекомых, экспрессирующих большие количества белка, которые затем можно очищать стандартными способами, можно использовать стандартные способы трансфекции (см., например, Colley et al., J. Biol. Chem. 264:17619-17622 (1989); Guide to Protein Purification, in Methods in Enzymology, vol. 182 (Deutscher, ed., 1990)). Трансформацию эукариотических и прокариотических клеток проводят стандартными способами (см., например, Morrison, J. Bact. 132:349-351 (1977); Clark-Curtiss and Curtiss, Methods in Enzymology 101:347-362 (Wu et al., eds., 1983).
[0166] Можно использовать любой из хорошо известных способов введения чужеродных нуклеотидных последовательностей в такие клетки-хозяева. Они включают использование трансфекция с фосфатом кальция, полибрена, слияния протопластов, электропорации, ультразвуковых способов (например, сонопорации), липосом, микроинъекции, "голых" ДНК, плазмидных векторов, вирусных векторов, эписомного и интегративного способа и любого из других хорошо известных способов введения клонированной геномной ДНК, кДНК, синтетической ДНК или другого чужеродного генетического материала в клетку-хозяина (см., например, Sambrook et al., выше). Необходимо только, чтобы конкретным используемым способом генетической инженерии можно было результативно вводить в клетку-хозяина, способную к экспрессии выбранного белка, по меньшей мере один ген.
Доставка нуклеиновых кислот в растительные клетки
[0167] Как указано выше, конструкции ДНК можно вводить в (например, в геном) желаемое растение-хозяина множеством общепринятых способов. Для обзора таких способов см., например, Weissbach and Weissbach Methods for Plant Molecular Biology (1988, Academic Press, N.Y.) Section VIII, pp. 421-463; и Grierson and Corey, Plant Molecular Biology (1988, 2d Ed.), Blackie, London, Ch. 7-9.
[0168] Например, конструкцию ДНК можно вводить непосредственно в геномную ДНК растительной клетки с использованием таких способов, как электропорация и микроинъекция в протопласты растительной клетки, или конструкции ДНК можно вводить непосредственно в ткань растения с использованием биолистических способов, таких как бомбардировка частицами с ДНК (см., например, Klein et al., (1987) Nature 327:70-73). Альтернативно, конструкции ДНК можно комбинировать с подходящими фланкирующими областями Т-ДНК и вводить в общепринятом векторе-хозяине Agrobacterium tumefaciens. Опосредованные Agrobacterium tumefaciens способы трансформации, включая нейтрализацию и использование бинарных векторов, хорошо описаны в научной литературе. См., например, Horsch et al., (1984) Science 233:496-498 и Fraley et al., (1983) Proc. Natl. Acad. Sci. USA 80:4803.
[0169] Кроме того, перенос генов можно осуществлять с применением не являющихся Agrobacterium бактерий или вирусов, таких как виды Rhizobium NGR234, Sinorhizoboium meliloti, Mesorhizobium loti, вирус картофеля X, вирус мозаики цветной капусты и вирус мозаики жилок маниоки и/или вирус табачной мозаики. См., например, Chung et al. (2006) Trends Plant Sci. 11(1):1-4.
[0170] Вирулентное действие хозяина Agrobacterium tumefaciens, когда клетку инфицируют бактериями с использованием бинарного вектора Т-ДНК (Bevan (1984) Nuc. Acid Res. 12:8711-8721) или способов совместного культивирования (Horsch et al. (1985) Science 227:1229-1231), обуславливает вставку конструкции и прилегающего маркера в ДНК растительной клетки. Как правило, систему трансформации с Agrobacterium применяют для конструирования двудольных растений (Bevan et al., (1982) Ann. Rev. Genet 16:357-384; Rogers et al., (1986) Methods Enzymol. 118:627-641). Систему трансформации с Agrobacterium также можно использовать для трансформации, а также переноса ДНК в однодольные растения и растительные клетки. См. патент США № 5591616; Hernalsteen et al., (1984) EMBO J. 3:3039-3041; Hooykass-Van Slogteren et al., (1984) Nature 311:763-764; Grimsley et al. (1987) Nature 325:1677-179; Boulton et al., (1989) Plant Mol. Biol. 12:31-40.; и Gould et al., (1991) Plant Physiol. 95:426-434.
[0171] Альтернативные способы переноса генов и трансформации в качестве неограничивающих примеров включают трансформацию протопластов посредством опосредуемого кальцием, полиэтиленгликолем (PEG) или электропорацией захвата "голой" ДНК (см. Paszkowski et al. (1984) EMBO J. 3:2717-2722, Potrykus et al. (1985) Molec. Gen. Genet. 199:169-177; Fromm et al. (1985) Proc. Nat. Acad. Sci. USA 82:5824-5828; и Shimamoto (1989) Nature 338:274-276) и электропорации тканей растений (D'Halluin et al. (1992) Plant Cell 4:1495-1505). Дополнительные способы трансформации растительных клеток включают микроинъекцию, опосредованный карбидом кремния захват ДНК (Kaeppler et al. (1990) Plant Cell Reporter 9:415-418) и бомбардировку микрочастицами (см. Klein et al. (1988) Proc. Nat. Acad. Sci. USA 85:4305-4309; и Gordon-Kamm et al. (1990) Plant Cell 2:603-618) или наночастицами.
[0172] Описываемые способы и композиции можно использовать для вставки экзогенных последовательностей в предопределенные положения в геноме растительной клетки. Это является полезным, ввиду того, что экспрессия вводимого в геном растения трансгена критически зависит от его участка интеграции. Таким образом, гены, кодирующие, например, питательные вещества, антибиотики или терапевтические молекулы, можно вводить посредством направленной рекомбинации в области геномов растений, подходящие для их экспрессии.
[0173] Трансформированные растительные клетки, получаемые любым из указанных выше способов трансформации, можно культивировать с регенерацией целого растения, обладающего трансформированным генотипом и, таким образом, желаемым фенотипом. Такие способы регенерации основаны на манипуляциях с определенными фитогормонами в среде для выращивания культур тканей, как правило, основываясь на биоцидном и/или гербицидном маркере, вводимом совместно с желаемыми нуклеотидными последовательностями. Регенерация растений из культивируемых протопластов описана в Evans, et al., "Protoplasts Isolation and Culture" in Handbook of Plant Cell Culture, pp. 124-176, Macmillian Publishing Company, New York, 1983; и Binding, Regeneration of Plants, Plant Protoplasts, pp. 21-73, CRC Press, Boca Raton, 1985. Регенерацию также можно осуществлять из каллюса, тканей, органов, пыльцы, эмбрионов растений или их частей. Такие способы регенерации в основном описаны в Klee et al. (1987) Ann. Rev. of Plant Phys. 38:467-486.
[0174] Нуклеиновые кислоты, вводимые в растительную клетку, можно использовать для придания желаемых признаков по существу любому растению. С использованием конструкций нуклеиновых кислот по настоящему описанию и различных способов трансформации, указанных выше, можно сконструировать широкое множество растений и систем растительных клеток с желаемыми физиологическими и агрономическими характеристиками, описываемыми в настоящем документе. В предпочтительных вариантах осуществления растения-мишени и растительные клетки-мишени для конструирования в качестве неограничивающих примеров включают однодольные и двудольные растения, такие как сельскохозяйственные культуры, включая зерновые культуры (например, пшеницу, кукурузу, рис, просо, ячмень), плодовые культуры (например, помидор, яблоко, груша, клубника, апельсин), кормовые культуры (например, люцерна), корнеплоды (например, морковь, картофель, сахарная свекла, батат), листовые овощные культуры (например, салат-латук, шпинат); цветущие растения (например, петуния, роза, хризантема), хвойные и сосновые деревья (например, сосна, пихта, ель); растения, используемые в фитомедицине (например, растения, аккумулирующие тяжелые металлы); масличные культуры (например, подсолнечник, семя рапса, соя), и растения, используемые в экспериментальных целях (например, Arabidopsis). Таким образом, описываемые способы и композиции находят применение для широкого диапазона растений, включая в качестве неограничивающих примеров виды родов Asparagus, Avena, Brassica, Citrus, Citrullus, Capsicum, Cucurbita, Daucus, Erigeron, Glycine, Gossypium, Hordeum, Lactuca, Lolium, Lycopersicon, Malus, Manihot, Nicotiana, Orychophragmus, Oryza, Persea, Phaseolus, Pisum, Pyrus, Prunus, Raphanus, Secale, Solanum, Sorghum, Triticum, Vitis, Vigna и Zea.
[0175] Специалисту в данной области понятно, что после стабильного встраивания экспрессирующей кассеты в трансгенные растения и подтверждения функционирования, ее можно вводить в другие растения посредством полового скрещивания. Можно использовать любой из стандартных способов селекции в зависимости от скрещиваемых видов.
[0176] Трансформированные клетки, каллюс, ткань растения или растение можно идентифицировать и выделять посредством отбора или скрининга конструируемого растительного материала растений на признаки, кодируемые маркерными генами, находящимися в трансформированной ДНК. Например, отбор можно проводить по росту конструируемого растительного материала на средах, содержащих ингибирующее количество антибиотика или гербицида, к которым трансформируемая генная конструкция придает устойчивость. Кроме того, трансформированные растения и растительные клетки также можно идентифицировать посредством скрининга на активность видимых маркерных генов (например, генов β-глюкуронидазы, люциферазы, B или C1), которые могут находиться на рекомбинантных конструкциях нуклеиновых кислот. Такие способы отбора и скрининга хорошо известны специалистам в данной области.
[0177] Также для идентификации трансформантов растений или растительных клеток, содержащих встроенные генные конструкции, можно использовать физические и биохимические способы. Эти способы в качестве неограничивающих примеров включают: 1) Саузерн-анализ или амплификацию ПЦР для детекции и определения структуры вставки рекомбинантной ДНК; 2) Нозерн-блот, защиту от РНКазы S1, достройку праймера или амплификацию ПЦР с обратной транскриптазой для детекции и исследования РНК-транскриптов генных конструкций; 3) ферментативные анализы для детекции ферментативной или рибозимной активности, когда генная конструкция кодирует такие продукты генов; 4) электрофорез белков в геле, способы вестерн-блоттинга, иммунопреципитацию или иммуноферментные анализы, когда продуктами генной конструкции являются белки. Для детекции присутствия или экспрессии рекомбинантной конструкции в конкретных органах и тканях растений также можно использовать дополнительные способы, такие как гибридизация in situ, ферментное окрашивание и иммуноокрашивание. Способы проведения всех этих анализов хорошо известны специалистам в данной области.
[0178] Эффекты манипуляций с генами способами, описываемыми в настоящем документе, можно наблюдать, например, посредством нозерн-блоттинга РНК (например, мРНК), выделенной из представляющих интерес тканей. Как правило, если количество мРНК возрастает, можно полагать, что соответствующий эндогенный ген экспрессируется в большей степени, чем ранее. Можно использовать другие способы измерения активности гена и/или CYP74B. Можно использовать различные типы ферментативных анализов в зависимости от используемого субстрата и способа детекции возрастания или снижения количества продукта реакции или побочного продукта. Кроме того, можно иммунохимически, т.е. посредством ELISA, RIA, EIA и других основанных на антителах анализов, хорошо известных специалистам в данной области, таких как анализ посредством электрофоретического определения (с окрашиванием или с вестерн-блоттингом), измерять уровни экспрессированного белка CYP74B. Трансген можно селективно экспрессировать в определенных тканях или на определенных стадиях развития растений, или трансген можно экспрессировать по существу во всех тканях растений, по существу на всем протяжении жизненного цикла. Однако также применим любой комбинаторный режим экспрессии.
[0179] Настоящее описание также относится к семенам трансгенных растений, описанных выше, где семена содержат трансген или генную конструкцию, и включают семена с желаемыми модифицируемыми профилями масел. Кроме того, настоящее описание относится к потомству, клонам, клеточным линиям или клеткам трансгенных растений, описанных выше, где указанное потомство, клон, клеточная линия или клетка содержат трансген или генную конструкцию.
[0180] Введение эффективных количеств проводят любыми маршрутами, обычно используемыми для приведения ZFP в максимальный контакт с обрабатываемой растительной клеткой. ZFP вводят любым подходящим способом, предпочтительно с приемлемыми носителями. Подходящие способы введения таких модуляторов являются доступными и хорошо известны специалистам в данной области, и, хотя для введения конкретной композиции можно использовать более одного маршрута, конкретный маршрут часто обеспечивает более быструю и более эффективную реакцию, чем другой маршрут.
[0181] Также можно использовать носители и их частично определяет конкретная вводимая композиция, а также конкретный способ, применяемый для введения композиции. Таким образом, существует широкое множество доступных подходящих составов композиций.
Применения
[0182] Как указано выше, направленную модуляцию генов, вовлеченных в синтез жирных кислот, можно использовать для быстрого и эффективного получения растительных масел с желаемым профилем жирных кислот.
[0183] Изменение состава жирных кислот растительных масел маслопродуцирующих растений, например, таких как канола, имеет принципиальное значение для пищевого производства и, таким образом, для здоровой диеты. Например, масличные семена сортов Brassica качества канолы со сниженными уровнями насыщенных жирных кислот в масле семян можно использовать для получения пищевых продуктов, которые способствуют здоровью сердечно-сосудистой системы. Способы и композиции, описываемые в настоящем документе, можно использовать для получения маслопродуцирующих растений с низким содержанием пальмитиновой и/или стеариновой кислот, которое снижает уровни насыщенных жирных кислот в растительном масле. Подобным образом, получение маслопродуцирующих растений с увеличенными уровнями содержания олеиновой кислоты также снижает количество насыщенных жирных кислот в растительном масле.
[0184] Кроме того, способы и композиции, описываемые в настоящем документе, можно использовать для увеличения содержания пальмитиновой кислоты, например, в маслах, получаемых из таких растений. Масла с высоким содержанием пальмитиновой кислоты особенно пригодны в составе маргаринов.
[0185] Кроме того, направленное изменение профилей жирных кислот, как описано в настоящем документе, можно использовать для получения растений (и растительных масел) с низким содержанием линоленовой кислоты. Масла с низким содержанием линоленовой кислоты демонстрируют повышенную стабильность; пищевые продукты, получаемые с использованием этих масел, не портятся в отношении аромата или запаха так быстро, как продукты, получаемые из растительных материалов с высокими концентрациями линоленовой кислоты.
ПРИМЕРЫ
[0186] Ниже предоставлены примеры конкретных вариантов осуществления для осуществления настоящего описания. Примеры предоставлены исключительно с иллюстративными целями и не предназначены для ограничения объема настоящего описания каким бы то ни было образом.
[0187] Предприняты усилия для обеспечения точности в отношении используемых чисел (например, количеств, температур и т.д.), но, разумеется, следует допускать некоторые экспериментальные ошибки и отклонения.
Пример 1: Идентификация последовательностей-мишеней в Brassica napus L
1.1 Идентификация последовательности-мишени
[0188] В этом примере идентифицированы эндогенные последовательности ДНК, кодирующие фермент β-кетоацил-ACP-синтетазу II (KAS II), находящиеся у Brassica napus L (канола) в природе. Эти гены выбирали в качестве иллюстративной мишени для демонстрации регуляции транскрипции посредством конструируемых факторов транскрипции с белками с цинковыми пальцами (ZFP TF), приводящей к желаемой модификации биосинтеза жирных кислот и одновременно измененным профилям в масле семян. Фермент β-кетоацил-ACP-синтетаза II катализирует преобразование 16:0-ACP в 18:0-ACP и последующее образование олеиновой кислоты (Ohlrogge and Browse, 1995, The Plant Cell, 7:957-970). Описанный мутант гена β-кетоацил-ACP-синтетаза II Arabidopsis thaliana fab1 приводил к 65% снижению активности фермента и одновременному увеличению содержания стеариновой кислоты на 7% и 3% в листьях и корнях, соответственно (Wu et al., 1994, Plant Physiology, 106:143-150). Стабильная экспрессия трансформированного трансгена β-кетоацил-ACP-синтетазы II сои в канола снижала содержание пальмитиновой кислоты в семенах на 0,8%, а введение того же гена в табак снижало содержание пальмитиновой кислоты на 2% (патентная публикация Японии № 501446/1995).
[0189] Описаны последовательности кДНК β-кетоацил-ACP-синтетазы II из множества видов растений, включая Arabidopsis thaliana (GenBank: AF318307) и Brassica napus (GenBank: AF244520). Выравнивание последовательностей кДНК A. thaliana и B. napus (GenBank: AF318307 и AF244520, соответственно) продемонстрировало, что последовательность AF244520 являлась неполной (фигура 7). В этой укороченной последовательности ДНК B. napus отсутствовало несколько сотен пар оснований на 5'-конце. Кроме того, так как B. napus представляет собой амфидиплоидный вид, являющийся результатом комбинации наборов хромосом B. rapa (2n=20, AA) и B. oleracea (2n=18, CC) (Morinaga, 1934, Cytologia, 6:62-67; U.N., 1935, Japanese J. Bot., 7:389-452), предсказывают, в этом виде может существовать более одного гена β-кетоацил-ACP-синтетазы II. Идентифицированы и получены дополнительные последовательности 5'-UTR, находящиеся в последовательностях кДНК. Эти 5'-последовательности генов β-кетоацил-ACP-синтетазы II в настоящих примерах служили в качестве мишеней для активации транскрипции посредством ZFP-TF.
1.2 Выделение тотальной РНК
[0190] Тотальную РНК выделяли из незрелых семян Brassica napus (канола) с генотипом Nex710 (Crop Certificate 99-7049208-501) через 15 суток после цветения (DAF) с использованием набора Qiagen's RNEASY® PLANT MINI KIT (Qiagen, Valencia, CA). Тотальную мРНК обрабатывали не содержащей РНКаз ДНКазой в соответствии с рекомендациями производителя для удаления любых контаминирующих ДНК, которые могут амплифицироваться при количественной ПЦР-РВ.
1.3 5' RACE и анализ последовательностей
[0191] Быструю амплификацию концов кДНК (RACE), специфичную для 5'-конца кДНК β-кетоацил-ACP-синтетазы II B. napus (GenBank AF244520), проводили с использованием набора FIRSTCHOICE® RLM-RACE из Ambion (Ambion, Austin, TX) по рекомендациям производителя. Для получения 5'-конца последовательности кДНК, с некэпированной 5'-областью мРНК отжигали синтетический РНК-адаптор. Праймер, поставляемый с набором (5'-CGCGGATCCGAACACTGCGTTTGCTGGCTTTGATGAAA-3') (SEQ ID NO:1), и второй праймер (5'-CTCGAGCTGCTACTGCTAGTTCCGGTGGAGGAGCC-3') (SEQ ID NO:2), которые составлены для связывания внутри частичной последовательности кДНК B. napus (GenBank AF244520), использовали для амплификации фрагмента для определения неизвестной расположенной выше последовательности. Посредством амплификации 5' RACE идентифицировали приблизительно 500 пар оснований новых последовательностей B. napus. При выравнивании амплифицированных последовательностей идентифицированы контиги четырех отчетливо различающихся 5'-последовательностей кДНК генов β-кетоацил-ACP-синтетазы II (SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:46 и SEQ ID NO:30) (фигура 8). Эти 5'-последовательности продемонстрировали высокие уровни гомологии с последовательностями B. rapa (GenBank: AC189461) и B. oleracea (GenBank: BH723504) из той же области.
[0192] В 5'-последовательностях кДНК генов β-кетоацил-ACP-синтетазы II идентифицировали связывание последовательностей ZFP TF. В качестве мишеней для связывания ZFP TF (таблица 1) служили последовательности из расположенной выше генов β-кетоацил-ACP- синтетазы II области (таблица 2). Конструкции плазмид: pDAB4695, pDAB4696, pDAB4697 и pDAB4698, содержащие конструируемые составы ZFP TF, применяли для стабильной трансформации B. napus, как описано в следующих разделах. Предполагали, что конструируемые ZFP TF после экспрессии в растительных клетках будут связываться с эндогенными мишенями β-кетоацил-ACP-синтетазы II, приводя к модифицированной экспрессии мРНК мишени.
Пример 2: Конструирование ДНК-связывающих доменов ZFP, специфичных к гену β-кетоацил-ACP-синтетазы II
[0193] Конструировали белки с цинковыми пальцами к различным участкам-мишеням области промотора и 5'-нетранслируемой и транслируемой области гена β-кетоацил-ACP-синтетазы II B. napus. См., фигуру 2. Распознающие спирали для характерных конструкций ZFP представлены ниже в таблице 1. Участки-мишени для конструкций цинковых пальцев представлены ниже в таблице 2.
Конструкции цинковых пальцев для β-кетоацил-ACP-синтетазы II
Участки-мишени β-кетоацил-ACP-синтетазы II
для цинковых пальцев
NO: 24)
NO: 26)
NO: 27)
[0194] Конструкции из β-кетоацил-ACP-синтетазы II встраивали в экспрессирующие цинковые пальцы векторы, кодирующие белок по меньшей мере с одним пальцем со структурой CCHC. См., патентную публикацию США № 2008/0182332. В частности, последний палец в каждом белке имел структуру (строение) CCHC.
[0195] Затем кодирующие последовательности цинковых пальцев сливали с последовательностями, кодирующими активирующий домен VP16 и сигнал ядерной локализации opaque-2. Экспрессию слитых белков помещали под контроль относительно сильного конститутивного промотора, такого как промотор, происходящий из промотора убиквитина 10 Arabidopsis thaliana (AtUbi10). Иллюстративные векторы приведены в таблице 3 ниже.
Пример 3: Опосредованное ZFP TF повышение экспрессии природного гена(ов) β-кетоацил-ACP-синтетазы II B. napus
[0196] Для оценки функциональности составленных белков с цинковыми пальцами в растительных клетках использовали способы экспрессии таких белков в живых растительных клетках. ДНК, кодирующие белки с цинковыми пальцами, можно доставлять в растительные клетки в условиях, когда ДНК не встроена в геном растительной клетки. Таким образом, молекула ДНК транзиторно присутствует в растительных клетках и действует в качестве матрицы для экспрессии генов. Альтернативно, ДНК, кодирующие белки с цинковыми пальцами, можно доставлять в растительные клетки в условиях, обеспечивающих встраивание ДНК в геном растительной клетки, что приводит к трансгенезу генов, кодирующих белки с цинковыми пальцами так, что молекула ДНК стабильно присутствует в растительных клетках и действует в качестве матрицы для экспрессии генов. Для оценки функциональности белков с цинковыми пальцами в живых растительных клетках специалист в данной области может использовать транзиторную или трансгенную экспрессию ДНК, кодирующих эти белки.
3.1 Составление конструкций
[0197] Бинарные плазмиды, составленные и сконструированные для этого проекта, перечислены в таблице 3.
Описание конструкций для ZFP TF, направленных на
KAS II B. napus
[0198] pDAB4695 представляет собой бинарную плазмиду, содержащую генные экспрессионные кассеты 14025 v3/VP 16 и pat. Эта конструкция содержит следующие генетические элементы: v3 MAR RB7 (область прикрепления к матриксу (Thompson et al., 1997, WO9727207))::v2 промотора AtUbi10 (промотор убиквитина 10 Arabidopsis thaliana (Callis, et al., 1990, J. Biol. Chem. 265- 12486-12493))::слияние v3 цинкового пальца 14025/VP16::v1 3'-UTR ORF23 Atu (3'-нетранслируемая область открытой рамки считывания 23 Agrobacterium tumefaciens (Gelvin et al., 1987, EP222493))::v2 промотора CsVMV (промотор вируса мозаики жилок маниоки (Verdaguer et al., 1996, Plant Molecular Biology 31:1129-1139))::v5 pat (фосфинотрицинацетилтрансфераза (Wohlleben et al., 1988, Gene 70:25-37))::v4 3'-UTR AtuORF1 (3'-нетранслируемая область открытой рамки считывания 1 Agrobacterium tumefaciens (Huang et al., J. Bacteriol. 172:1814-1822)). Бинарную плазмиду конструировали посредством клонирования фрагмента ДНК, содержащего слияние v3 цинкового пальца 14025/VP16, в pDAB3916 по участкам рестрикции NcoI-SacI. Полученная конструкция, которую помечали как pDAB8221, содержала генную экспрессионную кассету v2 промотора AtUbi10::слияние v3 цинкового пальца 14025/VP16::v1 3'-UTR ORF23 Atu. pDAB8221 клонировали в бинарную плазмиду pDAB7309 посредством реакции L-R Gateway® Reaction (Invitrogen, Carlsbad, CA). В данной реакции получали pDAB4695 и подтверждали посредством расщеплений рестрикционными ферментами и реакций секвенирования.
[0199] pDAB4696 представляет собой бинарную плазмиду, содержащую генные экспрессионные кассеты v3 14033/VP 16 и pat. Эта конструкция содержит следующие генетические элементы: v3 MAR RB7::v2 промотора AtUbi10::слияние v3 цинкового пальца 14033/VP16::v1 3'-UTR ORF23 Atu::v2 промотора CsVMV::pat v5::v4 3'-UTR AtuORF1. Бинарную плазмиду конструировали посредством клонирования фрагмента ДНК, содержащего слияние v3 цинкового пальца 14033/VP16, в pDAB3916 по участкам рестрикции NcoI-SacI. Полученная конструкция, которую помечали как pDAB8222, содержала генную экспрессионную кассету v2 промотора AtUbi10::слияние v3 цинкового пальца 14033/VP16::v1 3'-UTR ORF23 Atu. pDAB8222 клонировали в бинарную плазмиду pDAB7309 посредством реакции L-R Gateway® Reaction (Invitrogen, Carlsbad, CA). В данной реакции получали pDAB4696 и подтверждали посредством расщеплений рестрикционными ферментами и реакций секвенирования.
[0200] pDAB4697 представляет собой бинарную плазмиду, содержащую генные экспрессионные кассеты v3 14035/VP 16 и pat. Эта конструкция содержит следующие генетические элементы: v3 MAR RB7::v2 промотора AtUbi10::слияние v3 цинкового пальца 14035/VP16::v1 3'-UTR ORF23 Atu::v2 промотора CsVMV::pat v5::v4 3'-UTR AtuORF1. Бинарную плазмиду конструировали посредством клонирования фрагмента ДНК, содержащего слияние v3 цинкового пальца 14035/VP16, в pDAB3916 по участкам рестрикции NcoI-SacI. Полученная конструкция, которую помечали как pDAB8223, содержала генную экспрессионную кассету v2 промотора AtUbi10::слияние v3 цинкового пальца 14035/VP16::v1 3'-UTR ORF23 Atu. pDAB8223 клонировали в бинарную плазмиду pDAB7309 посредством реакции L-R Gateway® Reaction (Invitrogen, Carlsbad, CA). В данной реакции получали pDAB4697 и подтверждали посредством расщеплений рестрикционными ферментами и реакций секвенирования.
[0201] pDAB4698 представляет собой бинарную плазмиду, содержащую генные экспрессионные кассеты v3 14047/VP 16 и pat. Эта конструкция содержит следующие генетические элементы: v3 MAR RB7::v2 промотора AtUbi10::слияние v3 цинкового пальца 14047/VP16::v1 3'-UTR ORF23 Atu::v2 промотора CsVMV::pat v5::v4 3'-UTR AtuORF1. Бинарную плазмиду конструировали посредством клонирования фрагмента ДНК, содержащего слияние v3 цинкового пальца 14047/VP16, в pDAB3916 по участкам рестрикции NcoI-SacI. Полученная конструкция, которую помечали как pDAB8224, содержала генную экспрессионную кассету v2 промотора AtUbi10::слияние v3 цинкового пальца 14047/VP16::v1 3'-UTR ORF23 Atu. pDAB8224 клонировали в бинарную плазмиду pDAB7309 посредством реакции L-R Gateway® Reaction (Invitrogen, Carlsbad, CA). В данной реакции получали pDAB4698 и подтверждали посредством расщеплений рестрикционными ферментами и реакций секвенирования.
3.2 Трансформация Agrobacterium
[0202] Клетки Agrobacterium получали для электропорации с использованием протокола, описанного в Weigel D., Glazebrook J. Arabidopsis: A Laboratory Manual. Cold Spring Harbor Laboratory Press, 2002: pg123-124. В протоколе проводили незначительные модификации, обеспечивающие оптимальный рост Agrobacterium (т.е. среду YEP заменяли на LB). В 50 мкл клеток Agrobacterium tumefaciens C58::Z707s независимо добавляли 1,5-3 мкг плазмидной ДНК для каждой конструкции и осторожно смешивали. Смесь переносили в холодные 0,2-см кюветы GENE PULSER® (BioRad Hercules, CA) и помещали на лед. Затем кюветы помещали в холодный штатив GENE PULSER® (BioRad, Hercules, CA) и подвергали электропорации при следующих условиях: выходная емкость 25 мкФарад, емкостный компенсатор - 960 мкФ, сопротивление - 200 Ом и напряжение - 2,5 кВ. Сразу после электропорации добавляли 950 мкл среды SOC (Invitrogen, Carlsbad, CA) и смесь переносили в пробирку Falcon 2059 (Becton Dickinson and Co., Franklin Lakes, NJ) или эквивалент. Затем трансформированные клетки инкубировали при 28°C в течение 1 часа. После инкубации 50 мкл, 100 мкл и 200 мкл клеток высевали на отдельные чашки со средой YEP (10 г дрожжевого экстракта, 10 г пептона, 5 г NaCl, 10 г сахарозы и 15 г агара в 1 литре воды), при необходимости содержащей антибиотики. Выращивание проводили в перевернутых чашках при 28°C приблизительно в течение 36-48 часов. Отдельные колонии накалывали и выращивали в 50 мл жидкой YEP (10 г дрожжевого экстракта, 10 г пептона, 5 г NaCl и 10 г сахарозы в 1 литре воды), при необходимости содержащей антибиотики, при 28°C приблизительно в течение 36 часов.
[0203] Штамм Agrobacterium tumefaciens подтверждали кетолактозным тестом. Предположительно трансформированные колонии штрихами наносили на агар с лактозой и инкубировали при 28°C в течение 48 часов. Затем чашки заполняли раствором Бенедикта. Проводили наблюдение за чашками; нанесенные штрихами изоляты, преобразующие раствор Бенедикта из синего в желтый, подтверждали как Agrobacterium (Bouzar, H., Jones, J., Bishop, A. "Simple Cultural Tests for Identification of Agrobacterium Biovars". Methods in Molecular Biology, Volume 44. Humana Press, 1995: 9-13).
[0204] После проведения протокола QIAGEN® low copy mini-prep (Qiagen, Valencia, CA) получали очищенную плазмидную ДНК из бактериальных культур. Целостность ДНК оценивали посредством рестрикционных фрагментов. Идентифицировали клоны с ожидаемым рисунком полос и получали маточные растворы с глицерином, добавляя 500 мкл бактериальной культуры в 500 мкл стерильного глицерина (Sigma Химическ Co., St. Louis, MO) и переворачивая для перемешивания. Маточные растворы с глицерином замораживали на сухом льду и хранили при -80°C.
3.3 Трансформация ZFP TF B. napus
[0205] Получение гипокотильных сегментов: поверхность семян B. napus генотипа Nex 710 стерилизовали 10% коммерческим отбеливателем в течение 10 минут и 3 раза промывали стерильной дистиллированной водой. Семена сушили стерильной бумажной салфеткой, затем помещали в Phyta-tray, содержащий "среду для прорастания", состоящую из минимальной среды MS половинной концентрации (Murashige and Skoog, Physiol Plant 15(3): 473-497, 1962), 20 г/л сахарозы и 8 г/л агара TC (PhytoTechnology Laboratories, Shawnee Mission, KS), и поддерживали в условиях режима выращивания при 23°C и со световым периодом 16 час света/8 час темноты.
[0206] На сутки 5 всходы проверяли на стерильность, Phyta-tray помещали в вытяжной шкаф с ламинарным потоком EDGEGARD® (The Baker Company, Sanford, ME) для поддержания стерильности. Используя стерильный пинцет и анатомические ножницы, растения удаляли из Phyta-tray и надземные области (меристему и семядолю) и корни отделяли и отбрасывали. Гипокотили помещали в чашку Петри 100×25 мм, содержащую стерильную дистиллированную воду, необходимую для предотвращения высушивания. Гипокотили помещали на крышку чашки Петри 100×25 мм и нарезали в поперечном направлении на 3-мм сегменты с использованием скальпеля № 10. Сегменты гипокотилей помещали на "среду для индукции каллюса", состоявшую из среды MS, содержащей 30 г/л сахарозы, 1 мг/л кинетина и 1 мг/л 2,4-D, отвержденной 7 г/л агара TC, содержащую стерильную фильтровальную бумагу. Чашки помещали в чистую ванну STERILITE® и поддерживали при том же режиме выращивания в течение 3 суток, в качестве предварительной обработки.
[0207] Затем на сутки 8 сегменты переносили в стерильные чашки Петри 100×25, содержащие 20 мл "жидкой среды для культивирования", состоящей из минимальной среды Линсмайера и Скуга (1965), содержащей 30 г/л глюкозы, витамины половинной концентрации Gamborg (1968), 215,2 мг/л кинетина и 221,04 мг/л 2,4-D для предварительной обработки в течение 1 часа. "Жидкую среду для культивирования" из гипокотильных сегментов удаляли и 40 мл суспензии Agrobacterium (содержащей pDAB4695, pDAB4696, pDAB4697 или pDAB4698 в Z707s) кратковременно перемешивали на центрифуге "вортекс" 50 Klett и наливали в чашку Петри 100×25 мм, содержащую гипокотильные сегменты для обработки в течение 30 минут. Через 30 минут всю суспензию Agrobacterium удаляли с использованием двойной состыкованной пипетки. Обработанные гипокотили помещали обратно на "среду для индукции каллюса" с фильтровальной бумагой, возвращали в ванну STERILITE®, накрывали темной крышкой и возвращали в помещение для культивирования при том же режиме выращивания, как указано выше, на 3 суток периода совместного культивирования. Через 3 суток гипокотили помещали непосредственно на "среду для индукции каллюса", содержащую 1 мг/л HERBIACE®, помещали обратно в ванну с прозрачной крышкой и возвращали в помещение для культивирования, поддерживая тот же режим выращивания, как указано выше. Через 1 неделю гипокотили переносили непосредственно в "среду для индукции каллюса" с отбором на 3 мг/л HERBIACE® в течение 2 недель для дополнительного развития каллюса и переносили в "среду для индукции каллюса" с отбором на 5 мг/л HERBIACE в течение 2-8 недель для дополнительного развития каллюса. После получения достаточного количества каллюса, его подвергали молекулярному анализу.
[0208] Регенерация растений из выдержанного каллюса канолы: ткань каллюс канолы помещали на "среду для регенерации побегов", состоящую из среды MS, содержащей 30 г/л сахарозы, 3 мг/л бензиламинопурина, 0,5 г/л MES [2-(N-морфолион)этансульфоновой кислоты], 5 мг/л нитрата серебра, 1 мг/л зеатина, 250 мг/л карбенициллина, 300 мг/л тиментина и 7 г/л агара TC с отбором на 5 мг/л HERBIACE®, чашки оборачивали лентой 3M и помещали в условия режима выращивания при 23°C и со световым периодом 16 час света/8 час темноты. Затем ткани помещали в "среду для роста побегов", состоящую из среды MS, содержащей 0,5 г/л MES, 300 мг/л тиментина, 20 г/л сахарозы и 7 г/л агара TC с отбором на 5 мг/л HERBIACE®. Ростки переносили на "среду для укоренения", состоящую из среды MS половинной концентрации, содержащей 10 г/л сахарозы, 0,5 мг/л индолилмасляной кислоты, 300 мг/л тиментина и 8 г/л агара TC с отбором на 5 мг/л HERBIACE®.
[0209] После развития на ростках корней in vitro, их пересаживали в горшки 13,34 см, содержащие смесь Metro Mix 360. Каждое из растений накрывали прозрачным самостоятельным колпаком и помещали в Conviron для акклиматизации. Через 48-72 часов колпаки удаляли для обеспечения циркуляции воздуха. Через семь суток горшки перемещали из Conviron в тепличный лоток для дальнейшего развития. Растения выращивали со световым периодом 16:8 час, с дневной и ночной температурой 22-24°C. После начала удлинения первичного цветкового стебля и формирования цветочных бутонов, все растение закрывали мешком для самоопыления для предотвращения ауткроссинга. Семена, получаемые при самоопылении, собирали приблизительно через четыре месяца после пересаживания.
[0210] Получение Agrobacterium: Agrobacterium из маточного раствора в глицерине за четверо суток перед обработкой штрихами наносили на "полутвердую среду для выращивания бактерий", состоящую из 10 г/л пептона, 10 г/л дрожжевого экстракта, 5 г/л NaCl, 10 г/л сахарозы и 100 мг/л спектиномицина и 250 мг/л стрептомицина и отвержденной 15 г/л агара Bacto, и выращивали в течение двух суток в инкубаторе (Fisher Scientific Isotemp Incubator) при 28°C. Через 2 суток небольшую петлю Agrobacterium помещали в 500 мл стерильную одноразовую колбу с отражателями, содержащую 150 мл "жидкой среды для выращивания бактерий" (такая же, как указано выше, но без отверждающего средства), 250 мг/л стрептомицина и 100 мг/л спектиномицина, выращивали в течение 16 часов в течение ночи при 28°C в темноте на закрытом шейкере (шейкер с охлаждаемым инкубатором New Brunswick Scientific Innova 4330) при 200 об./мин. Через 16 часов культуру Agrobacterium вынимали из шейкера и помещали аликвоты в 50-мл центрифужные пробирки (одну, содержащую 35 мл для получения, и две, содержащие 50 мл, для повторного подтверждения). Центрифужные пробирки помещают в центрифугу (центрифуга Beckman Model J2-21) и центрифугируют при 6000 об./мин в течение 15 минут, а затем ресуспендируют в "жидкой среде для культивирования" до конечной плотности Klett 50 с красным фильтром.
Пример 4: Анализ трансформированных образцов каллюса
[0211] Предположительно трансформированные образцы каллюса B. napus анализировали на изменения экспрессии мРНК эндогенного гена β-кетоацил-ACP-синтетазы II, эндогенного гена тубулина и трансгена ZFP TF. Уровни мРНК тубулина использовали в качестве внутреннего контроля для нормализации экспрессии мРНК ZFP TF и β-кетоацил-ACP-синтетазы II. Данные об экспрессии мРНК ZFP TF использовали для подтверждения присутствия в трансформированных каллюсах по меньшей мере одного функционального трансгена ZFP TF.
4.1 Получение образцов каллюса
[0212] После трансформации ткани гипокотиля Nex710 получали приблизительно 40-50 образцов каллюса B. napus в возрасте восьми недель. Их индивидуально трансформировали конструкциями ZFP TF, pDAB4695, pDAB4696, pDAB4697 и pDAB4698, как описано выше в примере 3.3. Контрольные образцы получали посредством трансформации контрольной бинарной конструкцией, содержащей генную экспрессионную кассету pat (v2 промотора AtUbi10::pat v3::v3 3'-UTR ORF1 Atu). Все образцы до их сбора выращивали в дополненной HERBIACE среде для культивирования клеток.
[0213] Из свежей ткани каллюса получали тотальную РНК с использованием набора QIAGEN RNEASY 96 Kit (Qiagen, Valencia, CA). РНК обрабатывали не содержащей РНКаз ДНКазой по инструкциям к набору для удаления любой контаминирующей геномной ДНК. Синтез первой цепи проводили по инструкциям производителя фермента обратной транскриптазы Superscript® III (Invitrogen, Carlsbad, CA), а в качестве праймеров использовали случайные гексамеры. Синтезированные цепи кДНК разбавляли водой до отношений 1:10 и 1:50 (они обеспечивали достаточное количество матрицы для амплификации нескольких мишеней посредством ПЦР). Каждую аликвоту сохраняли при -20°C на неопределенный срок.
4.2 Анализ экспрессии мРНК β-кетоацил-ACP-синтетазы II
[0214] Реакционные смеси кПЦР-РВ составляли для амплификации кДНК β-кетоацил-ACP-синтетазы II следующим образом: 7,5 мкл 2X основного буфера LC480 Probes Master Buffer (Roche Diagnostic, Indianapolis, IN), 0,3 мкл 10 мкМ маточного раствора геноспецифичного прямого праймера (SEQ ID NO:28: 5'-TTGACTCGAGCTGCTACTGC-3'; положения нуклеотидов 544-563 для SEQ ID NO:3 на выравнивании на фигуре 8), 0,3 мкл 10 мкМ маточного раствора геноспецифичного обратного праймера (SEQ ID NO:29: 5'-TTTCCATATCCATCGCAACA-3'; положения нуклеотидов 588-607 для SEQ ID NO:3 на выравнивании на фигуре 8), 0,15 мкл зонда UPL №25 из LIGHTCYCLER® 480 Probes Master (Roche Diagnostic, Indianapolis, IN), 1,5 мкл 10% (масс./об.) поливинилпирролидона-40 (PVP-40) и 3,9 мкл воды. Зонд UPL (Roche Diagnostics, Indianapolis, USA) представляет собой закрытую нуклеиновую кислоту и, таким образом, имеет более высокую Tm, чем рассчитанная в иных случаях. Перед обработкой стандартов и неизвестных проб все компоненты помещали в морозильник. Размечали и маркировали 384-луночный микропланшет, добавляли 13,5 мкл основной смеси на лунку. К микропланшету несильно прикрепляли герметизирующую фольгу. Планшет центрифугировали в течение 1 минуты при 3000 об./мин в центрифуге для микропланшетов Qiagen. Добавляли 1,5 мкл размороженных разведенных синтезированных цепей кДНК. Кроме того, в отдельные лунки добавляли 1,5 мкл стандартов количества копий, добавляли плазмидную ДНК в ряду разведений от наименьших до наибольших концентраций, эти стандарты сравнивали с кДНК β-кетоацил-ACP-синтетазы II (синтезированной с тотальной мРНК) с количественным подсчетом количества копий. Получали ряд стандартов количества копий ДНК β-кетоацил-ACP-синтетазы II посредством клонирования ампликона-мишени в плазмиде pCR2.1 (Invitrogen, Carlsbad, CA) и получая ряд разведений для количественного определения количества копий. К планшету прочно прикрепляли герметизирующую покрышку с фольгой и центрифугировали, как описано ранее. Программу ПЦР проводили следующим образом: i. активация при 95°C в течение 5 минут; ii. денатурация при 95°C в течение 10 сек @ 4,8°C/сек; iii. отжиг/элонгация при 60°C в течение 25 сек @ 2,5°C/сек; iv. достройка при 72°C в течение 1 сек @ 4,8°C/сек; повторение этапов ii-iv еще 40-50 раз; охлаждение до 38°C в течение 5 сек. ДНК амплифицировали в устройстве для ПЦР с детекцией в реальном времени LC480 (Roche, Indianapolis, IN) или эквивалентном. Размер ампликона составлял 64 пары оснований. Используемые в этом анализе ПЦР последовательности прямого и обратного праймеров точно совпадали с соответствующими последовательностями, находящимися в двух генах-мишенях β-кетоацил-ACP-синтетазы II, SEQ ID NO:3 и 30 (фигура 8). Таким образом, этот анализ представляет собой количественное определение экспрессии двух генов-мишеней β-кетоацил-ACP-синтетазы II.
4.3 Анализ экспрессии мРНК тубулина
[0215] Ген тубулина, природный ген Brassica napus (GenBank: AF258790 и GenBank: DU106489), использовали в качестве эталонного стандарта для точной нормализации сигнала экспрессии мРНК во всех генах в анализах кПЦР-РВ. кДНК, синтезированную для анализа кПЦР-РВ β-кетоацил-ACP-синтетазы II (описанного в примере 4.1), также использовали в анализе кПЦР-РВ тубулина, как описано ниже.
[0216] кПЦР-РВ для детекции и количественного определения ДНК составляли с 0,3 мкл геноспецифического прямого праймера (SEQ ID NO:31: 5'-ACAGCGATTGCCTACAAGG-3') (10 мкМ маточный раствор) и 0,3 мкл геноспецифического обратного праймера (SEQ ID NO:32: 5'-AGATGGTTAAGATCACCAAAGG-3') (10 мкМ маточный раствор), 1,5 мкл 10% (масс./об.) PVP-40, 3,9 мкл воды и 7,5 мкл 2X основной смеси LIGHTCYCLER® 480 SYBR Green I (Roche, Indianapolis, IN). Маркировали и помечали 384-луночный микропланшет, добавляли 13,5 мкл основной смеси на лунку. К микропланшету несильно прикрепляли герметизирующую фольгу. Планшет центрифугировали в течение 1 минуты при 3000 об./мин. в центрифуге для микропланшетов Qiagen. Герметизирующую фольгу удаляли и добавляли 1,5 мкл размороженных разведенных синтезированных цепей кДНК. Кроме того, в отдельные лунки добавляли 1,5 мкл стандартов количества копий, добавляли плазмидной ДНК в ряду разведений от наименьших до наибольших концентраций, эти стандарты сравнивали с кДНК тубулина (синтезированной с тотальной мРНК) с количественным подсчетом количества копий. Получали ряд стандартов количества копий ДНК тубулина посредством клонирования ампликона-мишени в плазмиде pCR2.1 (Invitrogen, Carlsbad, CA) и получая ряд разведений для количественного определения количества копий. К планшету прочно прикрепляли герметизирующую покрышку с фольгой и центрифугировали, как описано ранее. Программу ПЦР проводили следующим образом: i. активация при 95°C в течение 10 минут; ii. денатурация при 95°C в течение 10 сек @ 4,8°C/сек; iii. отжиг/элонгация при 55,5°C в течение 20 сек @ 2,5°C/сек; iv. достройка при 72°C в течение 20 сек @ 4,8°C/сек; повторение этапов ii-iv еще 39 раз; vi. охлаждение до 38°C в течение 5 сек. ДНК амплифицировали в устройстве для ПЦР с детекцией в реальном времени LC480 или эквивалентном. В этой реакции амплифицировали ампликон длиной 307 пар оснований. Обратный праймер для этой реакции перекрывает интрон длиной 78 п.н. на основе последовательности GenBank. Таким образом, ампликоны, амплифицируемые с геномной ДНК, не будут предпочтительными, и контаминанты геномной ДНК будут большей молекулярной массы и их можно легко дифференцировать от ампликонов кДНК, посредством запуска ампликонов на агарозном геле.
4.4 Анализ экспрессии мРНК ZFP TF
[0217] Экспрессию мРНК ZFP TF количественно определяли в образцах кДНК, которые исходно синтезировали для мРНК β-кетоацил-ACP-синтетазы II (описанной в примере 4.1). Анализ ПЦР TaqMan планировали на основе кассеты ZFP с использованием якорных праймеров к последовательности NLS opaque-2 на 5'-конце и последовательности VP16 на 3'-конце. Анализ ПЦР составляли с использованием: 0,5 мкл 10 мкМ маточного раствора прямого праймера "OP2_NLS_F1" (SEQ ID NO:33: 5'-AAGGAAGAGGAAGGAGTCTAACAG-3'), 0,5 мкл 10 мкМ маточного раствора обратного праймера "VP16_R1" (SEQ ID NO:34: 5'-CTTCTGCTCTCCACCGTA-3'), 0,25 мкл 5 мкМ маточного раствора зонда "VP16_MGB_185" (SEQ ID NO:45: 5'-TTGATGGTGAAGATGT-3'), 1,5 мкл 10% (масс./об.) PVP-40, 1,5 мкл 10x буфера для ПЦР с горячим стартом, 1,0 мкл 25 мМ MgCl2, 1,2 мкл dNTP (2,5 мМ каждого), 0,15 мкл полимеразы Hot Start Taq Polymerase (Qiagen, Valencia, CA) и 6,9 мкл воды. Смесь амплифицировали с использованием LIGHTCYCLER® 480 (Roche Diagnostics, USA). Размечали и маркировали 384-луночный микропланшет, добавляли 13,5 мкл основной смеси на лунку. К микропланшету несильно прикрепляли герметизирующую фольгу. Планшет центрифугировали в течение 1 минуты при 3000 об./мин в центрифуге для микропланшетов Qiagen. Герметизирующую фольгу удаляли и добавляли 1,5 мкл размороженных разведенных синтезированных цепей кДНК. К планшету крепко прикрепляли герметизирующую покрышку с фольгой и центрифугировали, как описано ранее. Программу ПЦР проводили следующим образом: i. активация при 95°C в течение 15 минут; ii. денатурация при 95°C в течение 20 сек @ 4,8°C/сек; iii. отжиг/элонгация при 60°C в течение 20 сек @ 2,5°C/сек; iv. достройка при 72°C в течение 55 сек @ 4,8°C/сек; повторение этапов ii-iv еще 44 раза; vi охлаждение до 38°C в течение 5 сек. ДНК амплифицировали в устройстве для ПЦР с детекцией в реальном времени LC480 или эквивалентном. Размер ампликона составлял 775 пар оснований. Количество копий кДНК/мРНК ZFP TF определяли с использованием ряда стандартов, в которых ампликон-мишень клонировали в плазмиду и проводили ряд разведений для анализов ПЦР, как описано для примеров β-кетоацил-ACP-синтетазы II и тубулина, выше.
4.5 Анализ экспрессии образцов каллюса
[0218] Экспрессию мРНК ZFP TF измеряли в образцах трансгенного каллюса в возрасте 8 недель предположительно трансформированных ZFP TF и выращиваемых на селективной среде HERBIACE® (см. пример 3). Присутствие определенного количества экспрессированной мРНК ZFP TF, как измеряли посредством анализа кПЦР-РВ, детектировали в образцах, трансформированных только содержащими ZFP TF конструкциями, но не в образцах, содержащих контрольную конструкцию. Эти данные свидетельствуют, что анализ был специфичен для экспрессии ZFP TF, и что контрольные каллюсы не содержат трансгена ZFP TF.
[0219] Для выявления различий в экспрессии в образцах каллюса на основе результатов кПЦР-РВ рассчитывали отношения экспрессии мРНК β-кетоацил-ACP-синтетазы II и тубулина. Наибольшее повышение экспрессии мРНК β-кетоацил-ACP-синтетазы II наблюдали в образцах каллюса канолы, трансформированных конструкцией pDAB4695 (таблица 4). Это 27% повышение экспрессии являлось статистически значимым (p=0,05) относительно контрольных образцов.
Экспрессия мРНК KASII в образцах каллюса B. napus, трансформированных различными конструкциями ZFP TF
Пример 5: Анализ образцов трансформированных растений T0
5.1 Анализ экспрессии мРНК β-кетоацил-ACP-синтетазы II, тубулина и ZFP TF
[0220] Растения канолы T0, содержащие трансгенную конструкцию pDAB4695, выращивали до растения на стадии 6 листьев и анализировали на экспрессию мРНК эндогенного гена β-кетоацил-ACP-синтетазы II, эндогенного гена тубулина и трансгена ZFP TF. Трансгенные растения сравнивали с контрольными образцами, которые трансформировали бинарной конструкцией, содержащей генную экспрессионную кассету pat (v2 промотора AtUbi10::v3 pat::v3 3'-UTR ORF1 Atu). Из каждого растения дыроколом для бумаги стандартного размера получали образцы шести оттисков листьев на льду и по инструкциям производителя выделяли тотальную мРНК с использованием набора для выделения РНК в 96-луночном формате Qiagen 96-well RNeasy RNA extraction kit (Qiagen, Carlsbad, CA). Анализы экспрессии мРНК β-кетоацил-ACP-синтетазы II, тубулина и ZFP TF проводили с использованием протоколов, описанных выше в примере 4.
[0221] Экспрессия мРНК β-кетоацил-ACP-синтетазы II у независимых трансгенных растений T0 варьировала. В 16 анализируемых случаях наблюдали повышение экспрессии мРНК более чем в 3 раза (фигура 3). Все растения били положительными по экспрессии ZFP TF. Кроме того, для расчета экспрессии мРНК β-кетоацил-ACP-синтетазы II на исходном уровне использовали 27 контрольных растений. Для расчета кратности возрастания экспрессии среднюю экспрессию мРНК β-кетоацил-ACP-синтетазы II на основе контролей на исходном уровне сравнивали с экспрессией мРНК β-кетоацил-ACP-синтетазы II отдельных случаев растений с ZFP TF (фигура 3). Эти растения выращивали до созревания для получения семян T1. Перед цветением все растения индивидуально закрывали мешками для самоопыления для облегчения самоопыления цветов на растении. Семена T1 этих растений собирали приблизительно через 4 месяца после их переноса в теплицу.
[0222] Для дальнейшего исследования выбирали случаи 3, 6 и 12.2 (далее обозначаемый как случай 12), представляющие различные диапазоны экспрессии.
Пример 6: Анализ образцов трансформированных растений T1
6.1 Анализ жирных кислот семян T1
[0223] Для исследования действия ZFP TF на изменение содержания жирных кислот проводили анализ жирных кислот единичных семян в 24 отдельных семенах T1 на случай (таблица 5). Использовали способ анализа метиловых эфиров жирных кислот (FAME) на основе способа AOCS Ce2-66(97), и все значения в таблице 5 приведены как процент от всех жирных кислот, присутствующих в семенах канолы.
Профиль жирных кислот отдельных семян T1,
измеряемый анализом FAME
[0224] Для получения образцов отдельные единичные семена помещали в маркированные кассетные пробирки на 96-луночный планшет для выделения, содержащие один стальной шар диаметром 3,175 мм (Small Parts, Miramar, FL). Пробирки закрывали крышками, и семя подвергали сухому помолу в GenoGrinder (SPEX CertiPrep Group, Metuchen, NJ) в течение 3,0 минут при 1300 ударах/минуту. Крышки удаляли и в каждую лунку добавляли 0,6 мл гептана. Лунки повторно закрывали крышками и помещали обратно в GenoGrinder для дополнительного дробления в течение 2,0 минут при 1200 ударах/мин. Затем образцы вынимали и центрифугировали при 3700 об./мин в течение 10,0 минут при 6°C. Используя роботизированное устройство Beckman Coulter MC Robot, супернатант переносили в 96-луночный планшет со стеклянными вставками (MicroLiter, Suwanee, GA). В образец добавляли 40 мкл 1% метоксида натрия. 30% маточный раствор метоксида натрия разбавляли метанолом (Fluka/Sigma Aldrich, St. Louis, MO). Чашки закрывали покрытой тефлоном панелью и перед анализом GC позволяли инкубироваться при комнатной температуре в течение 4 часов.
[0225] Образцы анализировали на содержание жирных кислот на Agilent 6890 GC-FID (Agilent Technologies, Santa Clara, CA), оборудованном колонкой J&W Scientific DB-23, колонкой 15 метров ×0,25 мм ID и 0,25 мкм толщины пленки, (J&W Scientific, Folsom, CA). Исходная температура термостата составляла 200°C и эту температуру поддерживали в течение запуска. Входной канал устанавливали на коэффициент деления 1:100 и температуру 280°C. В течение первых двух минут скорость изменяемого потока гелия поддерживали на уровне 0,8 мл/мин. Затем поток увеличивали от скорости 1,0 мл/мин до 2,5 мл/мин и удерживали в течение 1,5 минут. Детектор устанавливали на 300°C с постоянной подачей газа-носителя и скоростью в колонке 30 мл/мин, потоком топливного водорода 30 мл/мин и потоком окислителя 400 мл/мин. Используемый для всех образцов объем впрыска составлял 2 мкл.
[0226] Индивидуальные пики метиловых эфиров жирных кислот идентифицировали, проводя сравнения со временем удерживания эталонных стандартов метиловых эфиров (GLC#428, Nu-Chek-Prep, Inc., Elysian, MN) с использованием программного обеспечения Waters Corp. Empower Software. В зависимости от общих интегральных площадей пиков при хроматографии рассчитывали индивидуальные процентные площади для всех анализируемых веществ в эталонном стандарте. Также для идентификации любых загрязнений при GC проводили анализ чистого гептана.
[0227] Сравнение семян T1 с тремя наименьшими уровнями C16:0 (которые с наибольшей вероятностью являлись положительными по ZFP TF растениями) и с тремя наивысшими уровнями C16:0 (которые с наибольшей вероятностью являлись ноль-растениями по ZFP TF) показало, что изменения содержания C16:0 могут происходить в результате сегрегации трансгена ZFP TF (таблица 5). Также во всех случаях наблюдали соответствующее изменение всех C18 (C18:0+C18:1+C18:2+C18:3); семена с низкими уровнями C16:0 содержали увеличенные уровни всех C18 и наоборот. Это происходило, несмотря на вариабельность индивидуального содержания жирных кислот C18:0, C18:1, C18:2 и C18:3 вследствие сегрегации мутантных генов fad2 и fad3 (Hu, X., et al. Theor. Appl. Genet. 2006, 113:497-507) в генотипе Nex710, который подвергали трансформации. Таким образом, предпринимали следующую стадию для идентификации положительных по ZFP TF и сестринских ноль-растений в сегрегирующей популяции T1 в каждом случае для детекции фактического изменения профиля жирных кислот при сходном генетическом фоне.
6.2 Анализ присутствия ZFP TF в растениях T1
[0228] 100-150 всходов T1 всех трех случаев переноса трансгена 3, 6 и 12 подвергали скринингу для идентификации положительных по ZFP TF и сестринских ноль-растений (таблица 6). Растения тестировали на присутствие по меньшей мере одной полноразмерной кассеты трансгена ZFP TF. Из листьев этих растений в соответствии с рекомендациями производителей выделяли тотальную геномную ДНК с использованием набора для выделения QIAGEN PLANT DNEASY extraction kit (Qiagen, Valencia, CA). Протокол модифицировали добавлением к буферу Qiagen AP1 PVP-40 в конечной концентрации 1%. Очищенную гДНК количественно определяли по протоколу количественного определения ДНК PICOGREEN® (Molecular Probes, Inc., Eugene, OR). Образцы ДНК исследовали на присутствие по меньшей мере одной полноразмерной копии трансгена ZFP TF посредством анализа ПЦР, содержащего следующие реагенты: 5 мкл 10X буфера EX Taq (Takara Bio Inc., Otsu, Siga, Japan), 5 мкл 10% поливинилпирролидона-40, 1,0 мкл 10 мкМ маточного раствора прямого праймера ubi10 (SEQ ID NO:35: 5'-GGTCAACGGATCAGGATATTCTTG-3'), 1,0 мкл обратного праймера AtuORF23 (SEQ ID NO:36: 5'-CCATGTTGGCAAAGGCAACC-3'), 10 мкМ маточный раствор, 4 мкл dNTP (2,5 мМ каждого), 0,2 мкл TaKaRa EX Taq™ Hot Start, 31,8 мкл воды и 2 мкл ДНК с концентрацией 10 нг/мкл. Условия проведения циклов ПЦР являлись следующими: 94°C в течение 2 мин, 10 циклов ступенчатой ПЦР с 98°C в течение 10 сек, 65°C в течение 20 сек со снижаемой температурой на 0,5°C в каждом цикле до 60°C с последующими 72°C в течение 3:00 мин. За этим следовало 35 циклов с 98°C в течение 10 сек, 60°C в течение 20 сек и 72°C в течение 3:00 мин и конечной элонгацией при 72°C в течение 10 мин. 5 мкл смеси после каждой реакции запускали на 1% агарозном геле для детекции присутствия полосы ZFP TF ожидаемого размера 2662 п.н.
[0229] Разработан анализ количественной ПЦР с детекцией в реальном времени для гена pat, который молекулярно сцеплен с ZFP TF в конструкции pDAB4695, и его применяли для идентификации положительных по pat и ноль-растений для подтверждения его генетической сегрегации с кассетой ZFP TF, с который он молекулярно сцеплен.
Идентификация положительных по ZFP TF и сестринских ноль-растений в сегрегирующей популяции T1 в трех случаях
ZFP TF/ноль-
растения T1
[0230] Реакционная смесь для анализа ПЦР-РВ TaqMan pat содержала следующее: 3 мкл основной смеси Roche LIGHTCYCLER® Cycler 480 II Probes 2X, 0,6 мкл 10% PVP-40, 0,2 мкл 10 мкМ маточного раствора прямого праймера pat (SEQ ID NO:37: 5'-ACAAGAGTGGATTGATGATCTAGAGAGGT-3'), 0,2 мкл 10 мкМ маточного раствора обратного праймера PAT (SEQ ID NO:38: 5'-CTTTGATGCCTATGTGACACGTAAACAGT-3'), 0,2 мкл 5 мкМ маточного раствора зонда (SEQ ID NO:39: 5'-6FAM-CCAGCGTAAGCAATACCAGCCACAACACC-гаситель-3'), и ее смешивали со следующими реагентами для внутреннего эталонного стандарта HMG (GenBank: AF127919), как указано ниже: 0,2 мкл 10 мкМ маточного раствора прямого праймера HMG (SEQ ID NO:40: 5'-CCTCTCTACCACCGTCTCACATG-3'), 0,2 мкл 10 мкМ маточного раствора обратного праймера HMG (SEQ ID NO:41: 5'-GATCTGGCCGGACTGTTTCA-3'), 0,2 мкл 5 мкМ маточного раствора зонда (SEQ ID NO:42: 5'-6FAM-CGCTCCTCAGCTACCACCTCAACCA-гаситель-3'), 1 мкл ДНК и 0,2 мкл воды. Условия проведения циклов ПЦР представляли собой: 1 цикл с 95°C в течение 5 мин, 40 циклов с 95°C в течение 10 сек, 60°C в течение 40 сек и 72°C в течение 1 сек. Все образцы амплифицировали в трех экземплярах в 384-луночных планшетах вместе с 1-4 копиями стандартов трансгенной геномной ДНК в устройстве для ПЦР Roche LIGHTCYCLER® 480.
[0231] На основании пропорций сегрегации положительных по ZFP TF и ноль-растений в каждом случае, в случаях 3, 6 и 12 происходило приблизительно 2, 1 и 2 вставок трансгена ZFP TF в геноме B. napus, соответственно (таблица 6, колонка 3). Эти данные совпадают с данными по сегрегации гена pat во всех трех случаях.
6.3 Повышение экспрессии мРНК β-кетоацил-ACP-синтетазы II в растениях T1
[0232] Затем все положительные по ZFP TF и сестринские ноль-растения T1, представленные в таблице 6, колонка 3, подвергали анализу экспрессии мРНК гена эндогенной β-кетоацил-ACP-синтетазы II, трансгена ZFP TF и эндогенного гена тубулина. Последний служил в качестве эталонного гена для нормализации экспрессии генов β-кетоацил-ACP-синтетазы II и ZFP TF. Получали образцы шести оттисков листьев из каждого растения на стадии 6 листьев на льду и выделяли тотальную РНК с использованием набора QIAGEN RNAEASY®. Синтез и разведения цепей кДНК проводили, как описано в пример 4.1.
[0233] Для всех трех генов проводили анализ кПЦР-РВ синтезированных кДНК. Анализ экспрессии мРНК β-кетоацил-ACP-синтетазы II и тубулина проводили, как описано в примере 4.2 и примере 4.3, соответственно. Анализ ZFP TF модифицировали. Реакцию ПЦР составляли следующим образом: условия реакции являлись следующими: 7,5 мкл 2X основного буфера LC480 Probes Master Buffer (Roche Diagnostic, Indianapolis, IN), 0,3 мкл геноспецифичного прямого праймера № 1 (SEQ ID NO:43: 5'-TCGATCTTGATATGTTGGGAGA-3') (10 мкМ маточный раствор), 0,3 мкл геноспецифичного обратного праймера № 2 (SEQ ID NO:44: 5'-AGGTGCAGAATCATGTGGTG-3') (10 мкМ маточный раствор), 0,15 мкл зонда UPL № 85, 1,5 мкл 10% (масс./об.) PVP-40 и 3,9 мкл воды. Размечали 384-луночный микропланшет и добавляли 13,5 мкл описанной выше смеси на лунку. К планшету прикрепляли герметизирующую фольгу, и планшет центрифугировали в течение 1 минуты при 3000 об./мин. Пленку удаляли и добавляли 1,5 мкл размороженных разведенных первых цепей на лунку. Кроме того, в отдельные контрольные лунки добавляли стандарты кДНК. Планшет герметизировали герметизирующей покрышкой с фольгой и повторяли этап центрифугирования. Программу ПЦР проводили в следующих условиях: i. Активация при 95°C в течение 5 минут, ii. Денатурация при 95°C в течение 10 сек (@ 4,8°C/сек), iii. Отжиг/элонгация при 60°C в течение 25 сек (@ 2,5°C/сек), iv. Достройка при 72°C в течение 1 сек (@ 4,8°C/сек), v. Повторение этапов ii-iv еще 39-49 раз, vi. Охлаждение до 38°C в течение 5 сек.
[0234] Экспрессия мРНК ZFP TF была наименьшей в случае 6 и наивысшей в случае 3 из положительных по ZFP TF образцов (фигура 4). Ноль-растения не экспрессировали мРНК ZFP TF, что означало, что анализ ZFP TF являлся специфичным для присутствия трансгена ZFP TF. Уровни мРНК гена β-кетоацил-ACP-синтетазы II, мишени для ZFP TF, были повышены в положительных по ZFP TF растениях во всех случаях (фигура 5). При попарном сравнении положительных по ZFP TF и соответствующих сестринских ноль-растений в каждом случае наблюдали до 3-4-кратного возрастания экспрессии мРНК β-кетоацил-ACP-синтетазы II. Уровни повышения экспрессии мРНК β-кетоацил-ACP-синтетазы II являлись связанными с уровнями повышения экспрессии мРНК ZFP TF в каждом случае (фигура 4), например, наименьшими в случае 6 и наибольшими в случае 3.
6.4 Анализ жирных кислот в листьях растений T1
[0235] Совместно со сбором образцов для анализа мРНК, описанного в примере 6.3, проводили сбор второго набора образцов листьев T1 для анализа жирных кислот. Однако на жирные кислоты анализировали только подмножество образцов тех растений, которые выращивали, как показано в таблице 6, колонка 4. Проводили анализ метиловых эфиров жирных кислот (FAME), как указано ниже. Материал листьев массой 10-100 мг собирали на льду, а затем перед реакцией трансметилирования лиофилизировали 0,25M метоксидом натрия в безводном метаноле при 40°C в течение 20 минут. После реакции трансметилирования жирные кислоты три раза экстрагировали раствором гептана, содержащим в качестве суррогатного стандарта гептадеканоин. Выделенные гексановые фракции высушивали и ресуспендировали в известном объеме гептана. Полученные метиловые эфиры жирных кислот (FAME) анализировали посредством GC-FID с использованием капиллярной колонки BPX 70 из SGE (15 м × 0,25 мм × 0,25 мкм). Каждый FAME идентифицировали по его времени удержания и количественно определяли посредством впрыска в качестве калибровочного стандарта эталонной смеси масла семян рапса из Matreya LLC. Завершенность реакции подтверждали, проверяя присутствие эндогенных FAME при четвертой экстракции/получении производных.
[0236] Все три случая при парных сравнениях положительных по ZFP TF и соответствующих сестринских ноль-растений в каждом случае продемонстрировали снижение общего содержания C16:0 и одновременное увеличение содержания всех C18 (таблица 7). Например, положительные по ZFP TF растения в случае 12 по сравнению с их собственными сестринскими ноль-растениями демонстрировали снижение содержания C16:0 на 6,3% и увеличение содержания всех C18 на 1,44%.
Профиль жирных кислот в листьях T1
Пример 7: Анализ трансгенных семян T2 с ZFP TF
[0237] Подмножество положительных по ZFP TF растений, демонстрирующее наивысшую экспрессию мРНК β-кетоацил-ACP- синтетазы II и сестринских ноль-растений в каждом случае, выращивали до созревания с получением семян T2 (таблица 6, колонка 4). Исключением являлся случай 3, где также выращивали небольшое количество положительных по ZFP TF растений с меньшими диапазонами экспрессии. Они могут представлять собой другую сегрегирующую вставку трансгена pDAB4695. Каждое растение T1 закрывали сетчатым мешком для облегчения самоопыления в данном растении. Собирали семена и анализировали уровни жирных кислот.
[0238] Анализ жирных кислот T2 проводили на совокупности из 24 семян на растении, как описано для анализа семян T1 в примере 6.1. Результаты продемонстрировали снижение содержания C16:0 в положительных по ZFP TF растениях во всех трех случаях при попарном сравнении с их соответствующими сестринскими ноль-растениями (таблицы 8A и 8B). Это снижение содержания C16:0 составляло 12,6%, 11,2% и 22,3% для случаев 12, 3 и 6, соответственно. Также наблюдали согласованное снижение содержания C16:1. В соответствии со снижением содержания C16:0 и C16:1 в положительных по ZFP TF растениях при попарном сравнении с соответствующими сестринскими ноль-растениями наблюдали одновременное увеличение содержания всех C18 (C18:0+C18:1+C18:2+C18:3). Все три попарных сравнения положительных по ZFP TF и соответствующих сестринских ноль-растений при анализе с использованием статистического программного обеспечения JMP являлись статистически значимыми (p=<0,001) относительно возрастания содержания всех C16 (C16:0+C16:1) и содержания всех C16/всех C18 (фигура 6, A и B). Хотя на основании наблюдений сестринских ноль-растений эти три случая варьировали по содержанию в них C16:0 (таблицы 8A и 8B), ZFP TF являлся эффективным в снижении содержания C16:0 до приблизительно сходных уровней приблизительно от 2,93 до 3,05. Хотя все положительные по ZFP TF растения в случаях 3 и 12 дают семена (таблицы 8 и 9), из растений в случае 6 семена дает только одно содержащее ZFP TF растение. Это конкретное растение в случае 6 на основе данных о содержании жирных кислот в листьях T1 обладало наибольшим содержанием C16:0. В таблицах 8A и 8B представлено сравнение профилей жирных кислот T2 в трех случаях переноса трансгена B. napus из положительных по ZFP TF pDAB4695 и соответствующих сестринских ноль-растений. Эти данные получали с применением анализа FAME, и они описаны в разделе 6.1. Проводили анализ жирных кислот C12:0-C24:1 и большинство из них представлено в этих таблицах. Все значения представлены в качестве процента от всех жирных кислот, присутствующих в семенах B. napus.
Анализ жирных кислот C16:0, C16:1, C18:0, C:18:1, C:18:2 и C:18:3
Анализ жирных кислот C20:0, C20:1, C20:2, C22:0, C22:1, C24:0 и C24:1
[0239] В таблице 9 представлены общие профили жирных кислот на основе отдельных жирных кислот, представленных в таблицах 8A и 8B.
**Все LC или длинноцепочечные представляют собой сумму следующих цепей атомов углерода: все C18 + все C20 (C20:0+ C20:1+C20:2) + все C22 (C22:0+C22:1) + все C24 (C24:0+C24:1)
***Все насыщ. представляют собой все насыщенные жирные кислоты, представленные в таблицах 8A и 8B.
[0240] Комбинируя все длинноцепочечные жирные кислоты (все C18, все C20, все C22 и все C24), в положительных по ZFP TF растениях в различных случаях по сравнению с сестринскими ноль-растениями наблюдали возрастание от 0,4% до 1,2%. Среди жирных кислот с более длинной цепью заметным являлось увеличение C20:1 на 25% в положительных по ZFP TF растениях в случае 6. Во всех случаях в содержащих ZFP TF растениях также наблюдали снижение содержания всех насыщенных жирных кислот. Оно находилось в диапазоне от 6% снижения в случае 12 до 31% снижения в случае 6.
[0241] Таким образом, проиллюстрирована опосредуемая ZFP TF активация транскрипции гена β-кетоацил-ACP-синтетазы II в растениях T0 и T1 и одновременное снижение содержания всех жирных кислот C16 и увеличение содержания всех жирных кислот C18 в семенах T2. Эти данные демонстрируют успешное применение новых технологий ZFP TF для направления на конкретные гены в пути биосинтеза жирных кислот и их модификации, приводящих к прогнозируемым изменениям профилей масла семян, которые наследуются в поколениях потомства.
Примеры 8-15: Повышение/снижение экспрессии FatB
[0242] Пластиды являются главным участком биосинтеза жирных кислот de novo в высших растениях (Ohlrogge et al., 1979, Proc. Natl. Acad. Sci. USA 76:1194-8; Thelen and Ohlrogge, 2002, Metabolic Engineering 4:12-21). Жирные кислоты, не используемые в плазмидах, экспортируются в цитоплазму посредством специфической активности ацил-ACP-тиоэстераз (FAT) при гидролизе ацил-ацилпереносящих белков (ацил-ACP) с высвобождением свободных жирных кислот. У растений существуют два класса ферментов FAT, FATA и FATB. Для класса FATA in vitro предпочтительны 18:1-ACP, тогда как для класса FATB предпочтительны субстраты насыщенных ацил-ACP, такие как 16:0-ACP и 18:0-ACP, но также он демонстрирует другую гетерогенную субстратную специфичность (Doermann et al., 1995, Arch. Biochem. Biophys. 316:612-618; Voelker et al., 1997, Plant Physiology 114:669-677; Salas and Ohlrogge, 2002, Archives of Biochemistry and Biophysics, 403:25-34). Полагают, что FATB, подобно FATA, также присутствует во всех тканях растения, но преимущественно он экспрессируется в развивающихся семенах (Jha et al., 2006, Plant Physiology and Biochemistry 44:645-655).
[0243] Ядерный геном Arabidopsis кодирует два гена FatA и один ген FatB. Подавление активности FatB может существенно снизить содержание насыщенных жирных кислот в глицеролипидах. Например, в мутанте FatB, полученном посредством вставки Т-ДНК, содержание пальмитата (16:0) и стеарата (18:0) снижалось на 42-56% и 30-50%, соответственно, в зависимости от ткани (Bonaventure et al., The Plant Cell, 2003 15:1020-1033). Скорость роста растений у этого мутанта в значительной степени подавлялась, приводя к 50% снижению сырой массы на 4 неделе по сравнению с диким типом. Это открытие поддерживает точку зрения, что служит FatB в качестве основного фактора, руководящего изменением насыщенных жирных кислот у растений.
[0244] Основная культура масличных семян Brassica napus представляет собой амфидиплоидный вид, близкородственный с модельным видом Arabidopsis, но с размером генома приблизительно в восемь раз большим, чем геном Arabidopsis. В результате у этого вида описано шесть генов FatB (WO 2009/007091) по сравнению с одним у Arabidopsis. Эта сложность затрудняет понимание функции отдельных генов FatB при манипуляциях с ними. И наоборот, присутствие большего количества генов упрощает манипуляции с экспрессией нескольких генов в отношении требуемых показателей желаемых жирных кислот вместо их полного нокаута. Известно, что факторы транскрипции с цинковыми пальцами по существу связываются с любой последовательностью ДНК и модулируют генную функцию генов-мишеней (Van Eenennaam et al., Metab. Eng. 2004 6:101-108; Sanchez et al., 2006, Plant Biotechnology Journal 4:103-114). Как результат, этот инструмент можно применять к генам FatB для понимания их функции в B. napus. Это знание может помочь в манипуляциях с экспрессией от одного до нескольких генов FatB в отношении желаемого "полезного для здоровья" масла семян канолы с меньшим содержанием насыщенных жирных кислот.
[0245] Приведенные ниже примеры 8-15 демонстрируют активацию транскрипции генов FatB у Brassica napus L., приводящую к изменениям профилей жирных кислот в семенах.
Пример 8: Идентификация последовательностей-мишеней для генов FatB у Brassica napus L.
8.1 Идентификация последовательностей-мишеней
[0246] Для поиска и характеристики промоторных последовательностей генов FatB сорта Nex710 Brassica napus использовали модифицированный протокол "прогулки по геному". Эти нуклеотидные последовательности выделяли и идентифицировали для составления и получения ZFP TF, которые можно использовать для модификации экспрессии гена FatB. Конструировали девять библиотек для "прогулки по геному" с использованием набора Clontech Genome Walking Kit (Palo Alto, CA). Эти библиотеки применяли для получения последовательности длиной ≈1 т.п.н. выше участка старта транскрипции генов FatB. На основе последовательностей EST FatB, доступных в общедоступных базах данных, составляли и синтезировали пару прямых вложенных праймеров, специфичных к гену FatB. Пару обратных вложенных праймеров составляли и синтезировали для гибридизации с адаптерными последовательностями. С этих девяти библиотек амплифицировали несколько фрагментов ПЦР. Полученные фрагменты ПЦР клонировали в векторы TOPO (Invitrogen, Carlsbad, CA, USA) и секвенировали для идентификации промоторных последовательностей FatB. На основе этого подхода идентифицировали два гена FatB, FatB4 и FatB5. Выявили, что хотя кодирующие последовательности этих генов FatB являлись высококонсервативными, последовательности в 5'-UTR и промоторных областях различались.
[0247] Экспрессия FatB и количественное определение генов FatB4 и FatB5 посредством анализа количественной ПЦР-РВ в развивающихся семенах B. napus позволяют предположить, что эти гены высокоэкспрессированы в семенах B. napus. Тотальную РНК выделяли, количественно определяли и участки инициации транскрипции картировали, как описано выше в примере 1. Промоторные последовательности этих двух генов использовали для составления ZFP TF для модификации экспрессии на уровне транскрипции.
Пример 9: Конструирование ДНК-связывающих доменов ZFP, специфичных к генам FatB
[0248] Конструировали белки с цинковыми пальцами к различным участкам-мишеням в гене FatB. Ниже в таблицах 10A и 10B представлены участки-мишени и распознающие спирали для характерных составов ZFP.
Участки связывания-мишени FatB для ZFP TF
FatB4 (от 5' к 3')
FatB5 (от 5' к 3')
к FatB
связывания
gcaccgca (SEQ ID NO:48)
FatB5
ccttcatt (SEQ ID NO:52)
FatB5
Области распознающих спиралей ZFP
** Связывающаяся последовательность ZFP для FatB4 и FatB5 является одинаковой, но 3'-фланкирующие последовательности для двух генов различаются.
*** числа представляют цинковый палец (1 представляет палец 1, 2 представляет палец 2 и т.д.)
Пример 10: Опосредованное ZFP TF повышение экспрессии природных генов FatB у B. napus
[0249] Для иллюстрации опосредованного ZFP TF повышения экспрессии FatB в клетках B. napus, получали конструкции, содержащие четыре состава генов ZFP TF (таблицы 10 и 11), эти гены доставляли в клетки B. napus для стабильной экспрессии посредством опосредуемой Agrobacterium трансформации.
10.1 Составление конструкций
[0250] Составленные и сконструированные бинарные плазмиды с ZFP TF перечислены в таблице 11 ниже. Экспрессию генов ZFP TF помещали под контроль относительно сильного конститутивного промотора, такого как промотор, происходящий из промотора вируса мозаики жилок маниоки (CsVMV). Опосредуемую Agrobacterium трансформацию растений проводили, как описано в примере 3.2, со стабильным встраиванием ZFP TF в геном B. napus.
Описание конструкций ZFP TF,
направленных на гены FatB B. napus
[0251] pDAB4689 представляет собой бинарную плазмиду, содержащую генные экспрессионные кассеты последовательности ядерной локализации или NLS opaque-2 (Op-2)/13685/VP 16 и pat. Эта конструкция содержит следующие генетические элементы: v3 MAR RB7 (область прикрепления к матриксу (Thompson et al., 1997, WO9727207))::v2 промотора CsVMV (промотор вируса мозаики жилок маниоки (Verdaguer et al., 1996, Plant Molecular Biology 31:1129-1139))::NLS opaque-2 (Van Eenennaam et al., 2004, Metabolic Engineering 6:101-108; Holmes-Davis et al., 2005, Plant Molecular Biology 57:411-423)/слияние цинкового пальца 13685/VP16 (Jamieson et al., Biochem. Biophy. Res. Commun. 2006, 348:873-879)::v1 3'-UTR AtuORF23 (3'-нетранслируемая область открытой рамки считывания 23 Agrobacterium tumefaciens (Gelvin et al., 1987, EP222493))::v2 промотора AtUbi10 (промотор убиквитина 10 Arabidopsis thaliana (Callis, et al., 1990, J. Biol. Chem. 265-12486-12493))::v5 pat (фосфинотрицинацетилтрансфераза (Wohlleben et al., 1988, Gene 70:25-37))::v4 3'-UTR AtuORF1 (3'-нетранслируемая область открытой рамки считывания 1 Agrobacterium tumefaciens (Huang et al., J. Bacteriol. 172:1814-1822)). Бинарную плазмиду конструировали посредством клонирования фрагмента ДНК, содержащего слияние NLS opaque-2/цинковый палец 13685/VP16, в pDAB3912 по участкам рестрикции NcoI-SacI. Полученная конструкция, которую помечали как pDAB8215, содержала генную экспрессионную кассету v2 промотора CsVMV::слияние NLS opaque-2/цинковый палец 13685/VP16::v1 3'-UTR AtuORF23. pDAB8215 клонировали в бинарную плазмиду pDAB4668 посредством реакции L-R Gateway Reaction (Invitrogen, Carlsbad, CA). В данной реакции получали pDAB4689 и подтверждали посредством расщеплений рестрикционными ферментами и реакций секвенирования.
[0252] pDAB4690 представляет собой бинарную плазмиду, содержащую генные экспрессионные кассеты NLS opaque-2/13714/VP16 и pat. Эта конструкция содержит следующие генетические элементы: v3 MAR RB7::v2 промотора CsVMV::слияние NLS opaque-2/цинковый палец 13714/VP16::v1 3'-UTR AtuORF23::v2 промотора AtUbi10::v5 pat::v4 3'-UTR AtuORF1. Бинарную плазмиду конструировали посредством клонирования фрагмента ДНК, содержащего слияние NLS opaque-2/цинковый палец 13714/VP16, в pDAB3912 по участкам рестрикции NcoI-SacI. Полученная конструкция, которую помечали как pDAB8216, содержала генную экспрессионную кассету v2 промотора CsVMV::слияние NLS opaque-2/цинковый палец 13714/VP16::v1 3'-UTR AtuORF23. pDAB8216 клонировали в бинарную плазмиду pDAB4668 посредством реакции L-R Gateway Reaction (Invitrogen, Carlsbad, CA). В данной реакции получали pDAB4690 и подтверждали посредством расщеплений рестрикционными ферментами и реакций секвенирования.
[0253] pDAB4691 представляет собой бинарную плазмиду, содержащую генные экспрессионные кассеты NLS opaque-2/13722/VP 16 и pat. Эта конструкция содержит следующие генетические элементы: v3 MAR RB7::v2 промотора CsVMV::слияние NLS opaque-2/цинковый палец 13722/VP16::v1 3'-UTR AtuORF23::v2 промотора AtUbi10::v5 pat (фосфинотрицинацетилтрансфераза)::v4 3'-UTR AtuORF1. Бинарную плазмиду конструировали посредством клонирования фрагмента ДНК, содержащего слияние NLS opaque-2/цинковый палец 13722/VP16, в pDAB3912 по участкам рестрикции NcoI-SacI. Полученная конструкция, которую помечали как pDAB8217, содержала генную экспрессионную кассету v2 промотора CsVMV::слияние NLS opaque-2/цинковый палец 13722/VP16::v1 3'-UTR AtuORF23. pDAB8217 клонировали в бинарную плазмиду pDAB4668 посредством реакции L-R Gateway Reaction (Invitrogen, Carlsbad, CA). В данной реакции получали pDAB4691 и подтверждали посредством расщеплений рестрикционными ферментами и реакций секвенирования.
[0254] pDAB4692 представляет собой бинарную плазмиду, содержащую генные экспрессионные кассеты NLS opaque-2/13743/VP 16 и pat. Эта конструкция содержит следующие генетические элементы: v3 MAR RB7 (область прикрепления к матриксу::v2 промотора CsVMV::слияние NLS opaque-2/цинковый палец 13743/VP16::v1 3'-UTR AtuORF23::v2 промотора AtUbi10 (промотор убиквитина 10 Arabidopsis thaliana)::v5 pat::v4 3'-UTR AtuORF1. Бинарную плазмиду конструировали посредством клонирования фрагмента ДНК, содержащего слияние NLS opaque-2/цинковый палец 13743/VP16, в pDAB3912 по участкам рестрикции NcoI-SacI. Полученная конструкция, которую помечали как pDAB8218, содержала генную экспрессионную кассету v2 промотора CsVMV::слияние NLS opaque-2/цинковый палец 13743/VP16::v1 3'-UTR AtuORF23. pDAB8218 клонировали в бинарную плазмиду pDAB4668 посредством реакции L-R Gateway Reaction (Invitrogen, Carlsbad, CA). В данной реакции получали pDAB4692 и подтверждали посредством расщеплений рестрикционными ферментами и реакций секвенирования.
Пример 11: Анализ трансформированных образцов каллюсов
[0255] Линии трансгенных каллюсов B. napus получали посредством трансформации четырех конструкции ZFP TF, pDAB4689-pDAB4692, и контрольной конструкции, pDAB8210, посредством опосредованной Agrobacterium трансформации растений, как описано в примере 3.2. Контрольная конструкция, pDAB8210, содержала генную экспрессионную кассету pat (Промотор AtUbi10/pat/3'-UTR AtuORF1) и кассету ненаправленной ZFN (промотор CsVMV/ZFN/3'-UTR AtuORF23). Из всех линий выделяли тотальную РНК и синтезировали кДНК, как описано в пример 4.1. Единственной модификацией описанного ранее протокола являлось использование в качестве праймеров для реакций получения кДНК праймеров олиго-dT вместо случайных гексамеров и соответствующее изменение реакции кДНК, по инструкциям производителя.
11.1 Анализ экспрессии мРНК FatB4 и FatB5
11.1.1 Анализ FatB4 посредством количественной ПЦР с детекцией в реальном времени (кПЦР-РВ) у B. napus
[0256] Смесь ПЦР для амплификация кДНК FatB4 составляли следующим образом: 1,5 мкл 10X буфера для ПЦР с горячим стартом (Qiagen, Valencia, USA), 1,2 мкл 10 мМ dNTP, 1 мкл 25 мМ MgCl2, 0,15 мкл Qiagen Hot Start Taq (5 Ед/мкл), 0,5 мкл 10 мкМ маточного раствора прямого праймера zz143 (SEQ ID NO:53: CTTTGAACGCTTATCTTCCTC) (10 мкМ маточный раствор), 0,5 мкл 10 мкМ маточного раствора обратного праймера FATB5_R4 (SEQ ID NO:54: TTCCACAACATCTCCCCAAG), 0,25 мкл 5 мкМ маточного раствора зонда TaqMan MGB (Life Technologies, Carlsbad, California) FatB4_MGB_Probe_4 (SEQ ID NO:55: FAM-CTCAGGCTCCACCC), 1,5 мкл 10% (масс./об.) PVP-40 и H2O до 13,5 мкл на одну реакцию. Размечали подходящий квадрант(ы) 384-луночного микропланшета и заполняли в объеме 13,5 мкл основной смеси на лунку. К планшету несильно прикрепляли герметизирующую фольгу. Планшет центрифугировали в течение 1 минуты при 3000 об./мин в центрифуге для микропланшетов Qiagen. Затем в соответствующие лунки добавляли 1,5 мкл размороженных разведенных первых цепей кДНК с последующим добавлением 1,5 мкл стандартов плазмидной кДНК с концентрацией ДНК в контрольных лунках от наименьшей до наибольшей. В завершении герметизирующую фольгу прочно прикрепляли к планшету и центрифугировали. Программу ПЦР проводили в системе для ПЦР с детекцией в реальном времени LIGHTCYCLER® 480 (Roche Diagnostics, Indianapolis, IN, USA) с использованием следующей программы: 1) активация при 95°C в течение 15 минут; 2) денатурация при 95°C в течение 20-30 сек (@ 4,8°C/сек); 3) отжиг при 60°C в течение 20-30 сек (@ 2,5°C/сек); 4) достройка при 72°C в течение 45-60 сек (@ 4,8°C/сек); повторение этапов 2)-4) еще 39-49 раз; 5) охлаждение до 38°C в течение 5 сек для остановки реакции.
[0257] Размер ампликона FatB4 составлял 678 п.н. Эта последовательность перекрывает интрон длиной 79 п.н. на основе геномной последовательности. Кроме того, обратный праймер сконструирован с перекрыванием интрона, таким образом, способствуя специфической амплификации только кДНК FatB4, таким образом, устраняя амплификацию геномной ДНК.
11.1.2 Анализ кПЦР-РВ FatB5 у B. napus
[0258] Смесь ПЦР для амплификации кДНК FatB5 составляли следующим образом: 1,5 мкл 10X буфера для ПЦР с горячим стартом (Qiagen, Valencia, USA), 1,2 мкл 10 мМ dNTP, 1 мкл 25 мМ MgCl2, 0,15 мкл Qiagen Hot Start Taq (5Ед/мкл), 0,5 мкл 10 мкМ маточного раствора прямого праймера zz145 (SEQ ID NO:56: CTTTGAAAGCTCATCTTCCTC), 0,5 мкл 10 мкМ маточного раствора обратного праймера FATB5_R4 (SEQ ID NO:57: TTCCACAACATCTCCCCAAG), 0,25 мкл 5 мкМ маточного раствора зонда TaqMan MGB (Life technologies, Carlsbad, California) FatB5_MGB_Probe_1 (SEQ ID NO:58: FAM-AACCTTCATCCTCCCA), 1,5 мкл 10% (масс./об.) PVP-40 и H2O до 13,5 мкл на одну реакцию. Остальные характеристики анализа и цикла ПЦР являлись такими, как описано для анализа кПЦР-РВ FatB4 в примере 11.1.1.
[0259] Размер получаемого ампликона составлял 678 п.н. Эта последовательность кДНК перекрывает интрон длиной 76 п.н. на основе геномной последовательности. Кроме того, обратный праймер конструировали с перекрыванием интрона, таким образом, способствуя амплификации кДНК FatB5, таким образом, устраняя амплификацию геномной ДНК.
11.2 Анализ экспрессии мРНК тубулина
[0260] Этот анализ проводили, как описано в примере 4.3.
11.3 Анализ экспрессии мРНК ZFP TF
[0261] Анализ мРНК ZFP TF образцов каллюсов T0 проводили в соответствии с примером 4.4. Размер ампликонов в этом анализе составлял менее 1 т.п.н. в зависимости от размера ZFP в каждомй из конструкций. Количественный анализ экспрессии ZFP TF в растениях T0 проводили с использованием анализа на основе активирующего домена VP16, как описано ниже. Смесь для кПЦР-РВ VP16 для амплификация кДНК ZFP TF составляли следующим образом: 7,5 мкл 2X основного буфера LIGHTCYCLER® 480 Probes Master (Roche Diagnostics, Indianapolis, IN, USA), 0,3 мкл 10 мкМ маточного раствора праймера VP16_UPL_F1 (SEQ ID NO:59: TCGATCTTGATATGTTGGGAGA), 0,3 мкл 10 мкМ маточного раствора VP16_UPL_R1 (SEQ ID NO:60: AGGTGCAGAATCATGTGGTG), 0,15 мкл зонда UPL № 85 (Roche Diagnostics, Indianapolis, IN, USA), 1,5 мкл 10% (масс./об.) PVP-40 и H2O до 13,65 мкл. Размечали подходящий квадрант(ы) 384-луночного микропланшета и заполняли в объеме 13,5 мкл основной смеси на лунку. Затем к планшету несильно прикрепляли герметизирующую фольгу. Планшет центрифугировали в течение 1 минуты при 3000 об./мин в центрифуге для микропланшетов Qiagen. Добавляли 1,5 мкл размороженных разведенных первых цепей кДНК с последующим добавлением 1,5 мкл стандартов плазмидной кДНК с концентрацией ДНК в контрольных лунках от наименьшей до наибольшей. Герметизирующую фольгу прочно прикрепляли к планшету и центрифугировали. Программу ПЦР проводили в системе для ПЦР с детекцией в реальном времени LIGHTCYCLER® 480 (Roche Diagnostics, Indianapolis, IN, USA) с использованием следующих условий: 1) активация при 95°C в течение 5 минут; 2) денатурация при 95°C в течение 10 сек (@ 4,8°C/сек); 3) отжиг/элонгация при 60°C в течение 25 сек (@ 2,5°C/сек); 4) достройка при 72°C в течение 1 сек (@ 4,8°C/сек); 5) повторение этапов 2-4 еще 39-49 раз. В заключение реакционную смесь охлаждали до 38°C в течение 5 сек для остановки реакции.
[0262] Размер ампликона VP16 составлял 68 п.н. Этот размер фрагмента соответствует фрагменту VP16, продукции которого ожидали при ПЦР амплификации.
11.4 Анализ экспрессии образцов каллюсов
[0263] Трансгенные линии каллюсов, выращиваемые с отбором на HERBIACE®, посредством кПЦР-РВ анализировали на уровни экспрессии FatB4, FatB5, тубулина и ZFP TF. Ген тубулина служил в качестве эталонного гена для нормализации уровней экспрессии мРНК FatB4, FatB5 и ZFP TF. Для нормализации экспрессии мРНК рассчитывали отношения FatB4/тубулин и FatB5/тубулин. Результаты для составов конструкций pDAB4691 демонстрировали статистически значимое повышение экспрессии мРНК FatB4 и мРНК FatB5 (p=0,005; фиг. 9). Линии каллюсов с pDAB4692 демонстрировали тренд к повышению экспрессии мРНК FatB4 и FatB5, но этот тренд не являлся статистически значимым. В отдельном эксперименте также анализировали линии каллюсов с pDAB4689, продемонстрировавшие тренд к повышению экспрессии, но результаты не являлись статистически значимыми (данные не показаны). В контрольных линиях специфический ампликон ZFP TF не амплифицировался, подтверждая, что анализ ZFP TF был специфичен только для экспрессирующих ZFP TF линий.
Пример 12: Анализ экспрессии образцов трансгенных растений T0
12.1 Анализ актина у B. napus для применения в качестве внутреннего контроля для кПЦР-РВ
[0264] Из всех линий выделяли тотальную РНК и синтезировали кДНК, как описано в примере 11. Смесь ПЦР для амплификации кДНК актина составляли следующим образом (Bo Yang et al., 2007, Plant Science 173:156-171; номер доступа гена актина в GeneBank AF111812): 7,5 мкл 2X основной буфер LIGHTCYCLER® 480 SYBR Green I, 0,3 мкл 10 мкМ маточного раствора праймера BN_Actin_F (SEQ ID NO:61: ACGAGCTACCTGACGGACAAG), 0,3 мкл 10 мкМ маточного раствора BN_Actin_R (SEQ ID NO:62: GAGCGACGGCTGGAAGAGTA), 1,5 мкл 10% (масс./об.) PVP-40 и H2O в достаточном для получения 13,5 мкл объеме. Размечали подходящий квадрант(ы) 384-луночного микропланшета и заполняли в объеме 13,5 мкл основной смеси на лунку. К планшету несильно прикрепляли герметизирующую фольгу. Планшет центрифугировали в течение 1 минуты при 3000 об./мин. в центрифуге для микропланшетов Qiagen. Добавляли 1,5 мкл размороженных разведенных первых цепей кДНК с последующим добавлением 1,5 мкл стандартов плазмидной кДНК с концентрацией ДНК в контрольных лунках от наименьшей до наибольшей. Герметизирующую фольгу прочно прикрепляли к планшету и центрифугировали. Программу ПЦР проводили в системе для ПЦР с детекцией в реальном времени LIGHTCYCLER® 480 (Roche Diagnostics, Indianapolis, IN, USA) с использованием следующих условий: 1) активация при 95°C в течение 10 минут; 2) денатурация при 95°C в течение 10 сек (@ 4,8°C/сек); 3) отжиг/элонгация при 60°C в течение 20 сек (@ 2,5°C/сек); 4) достройка при 72°C в течение 20 сек (@ 4,8°C/сек); 5) повторение этапов 2-4 еще 39-49 раз. В заключение реакционную смесь охлаждали до 38°C в течение 5 сек для остановки реакции. Размер получаемого ампликона составлял 80 п.н.
12.2 Анализ экспрессии мРНК FatB4 и FatB5
[0265] Растения B. napus, трансформированные pDAB4689-pDAB4691, анализировали на повышенную экспрессию мРНК FatB4 и FatB5. Кроме того, применяли два типа контроля. Нетрансгенный контроль состоял из растений Nex710, служивших в качестве отрицательного контроля. Также анализировали второй трансгенный контроль из растений B. napus Nex710, трансформированных pDAB8210. Состав конструкции pDAB8210 содержал две генных экспрессионных кассеты. Генная экспрессионная кассета pat (промотор AtUbi10::ген pat::3'-UTR AtuORF1) и генная экспрессионная кассета ненаправленной нуклеазы с цинковыми пальцами (ZFN) (промотор AtUbi10::ген ZFN::3'-UTR AtuORF23). Полагали, что ZFN, экспрессируемая в pDAB8210, не будет связываться с геномом растений B. napus Nex710 и расщеплять его, и не будет изменять фенотип этих растений.
[0266] Предполагаемые трансгенные каллюсы, выращиваемые с отбором на HERBIACE®, восстанавливали в растения (пример 3.3). Для анализа экспрессии мРНК собирали образцы листьев растений B. napus, выращиваемых в теплице, на стадии 6 листов. Получали образцы шести оттисков листьев из каждого растения и перед выделением РНК помещали на лед. Выделяли тотальную РНК с использованием набора QIAGEN RNEASY. Синтез кДНК и последующие разведения проводили, как описано в примере 11. Протокол анализа экспрессии FatB4 и FatB5 посредством кПЦР-РВ описан выше. Совместно с анализом проводили/не проводили анализ экспрессии ZFP TF. Анализ кПЦР-РВ эталонного гена актина описан выше.
[0267] Экспрессия генов FatB4 и FatB5 листьями T0 с различными конструкциями варьировала (фиг. 10). Наибольшее повышение экспрессии мРНК FatB4 и FatB5 наблюдали в случаях трансгенных растений с pDAB4691, что приводило к общему увеличению экспрессии мРНК в 2,0-2,5 раза по сравнению с нетрансгенными Nex710 и трансгенными контролями с pDAB8210. Экспрессия обоих генов по сравнению с контролями являлась статистически значимой (ниже p=0,05). Таким образом, дополнительное определение характеристик конструкций продолжали с pDAB4691.
Пример 13: Анализ трансгенных растений T1
13.1 Анализ жирных кислот семян T1
[0268] В случае pDAB4691-003-049.1 ("случай 49") наблюдали значимое отличие содержания C18:0 в масличных семенах с "низким" и "высоким" содержанием (таблица 12). Содержание C18:0 семян категории с "низким" содержанием являлось сходным с содержанием в линиях Nex710 (нетрансгенный контроль) и pDAB8210 (трансгенный контроль). Содержание C18:0 в семенах с "высоким" содержанием коррелировало с экспрессией ZFP TF, приводящей к повышению экспрессии гена(ов) FatB. Также наблюдали некоторое повышение C20:0, C22:0 и C24:0 на основе перехода C18:0 в более длинноцепочечные жирные кислоты. Содержание C16:0 в отдельных семенах, по-видимому, не изменялось вне зависимости от категорий с "низким" или "высоким" содержанием. Этот результат указывает на тот факт, что ZFP TF pDAB4691 связывает и повышает экспрессию гена(ов) FatB, специфичных для ферментативных реакций преобразования C18:0-ACP в C18:0, а не реакций преобразования C16:0-ACP в C16:0 (см. пример 1, фиг. 1).
Профиль жирных кислот отдельных семян T1, измеряемый посредством анализа FAME
13.2 Анализ присутствия ZFP TF в растениях T1
[0269] В случае 49 сто семян T1 высаживали в теплицу. Девяносто семь растений дали всходы. Количество копий ZFP TF определяли с использованием анализа кПЦР-РВ pat, как описано в примере 6.2 для растительного материала, выделенного на стадии 2-4 листьев. Случай 49 содержал несколько вставок (≈3 вставки), и в популяции T1 сегрегировали 0-7 копий гена pat, и таким образом, ZFP TF. В популяции T1 идентифицировано только одно ноль-растение.
13.3 Повышение экспрессии мРНК FatB4 и FatB5 в растениях T1
[0270] Анализ экспрессии природного гена FatB проводили во всех 97 растениях сегрегирующей популяции T1. В исследование в качестве контроля включали нетрансгенные растения Nex710, сажали в то же самое время. Получали шесть оттисков листьев на каждое растение и до возможности проведения выделения РНК помещали на лед. Выделяли тотальную РНК с использованием набора QIAGEN RNEASY. Синтез кДНК и последующие разведения проводили, как описано в примере 11. Анализ экспрессии FatB4, FatB5, тубулина и VP16 (ZFP TF) проводили, как описано выше.
[0271] Статистический анализ отношений FatB4/FatB5 и тубулина продемонстрировал значительные линейные тренды с экспрессией тубулина (фиг. 11), указывающие на то, что возрастание FatB4/FatB5 не имеет с возрастанием эндогенного контроля, тубулина, зависимости 1:1. Поэтому в этом анализе отношения не использовались, и тубулин в модели экспрессии FatB4/FatB5 включали в качестве дополнительной переменной. Для исключения любой колинеарности между тубулином и VP16 (ZFP TF), ортогонализировали матрицы связностей для модельных уравнений.
[0272] Ко всем наборам данных в настоящем исследовании применяли приведенную ниже модель: где статусi представляет собой статус трансгенности yijk (трансгенное или ноль/контроль);
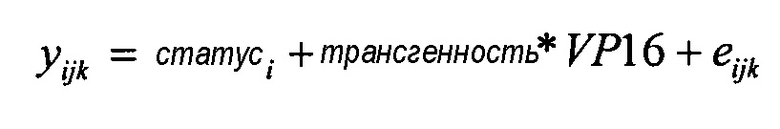
трансгенность*VP16 представляет собой линейную регрессию от VP16, вложенную в трансгенные линии; а eijk представляет собой случайный остаток. При условии, что для каждого образца проводили три повторных измерения, применяли структуру коррелированных остатков:
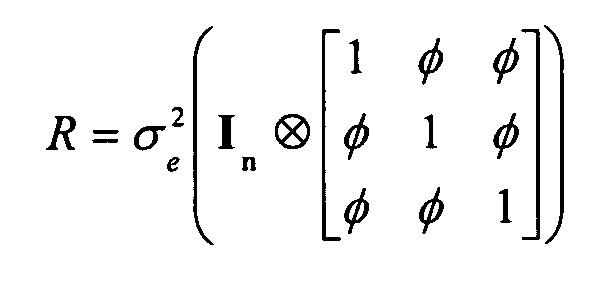 ,
,
где In представляет собой единичную матрицу с рангом, равным количеству образцов, а φ представляет собой корреляцию между остатками повторных измерений.
[0273] Результаты анализа для случая 49 с использованием вложенных моделей регрессии экспрессии FatB4 в зависимости от VP16 выявили значительное повышение экспрессии FatB4, демонстрирующее высокозначимые положительные наклоны (фиг. 12, таблица 13). Для FatB5, модели вложенной регрессии продемонстрировали положительный наклон в отношении повышения экспрессии, и наклон являлся статистически значимым. Для случаев с повышением экспрессии следует отметить, что трансформированные и контрольные растения не формируют одинаковую линию, так что существует некоторое смещение линии и эффектов трансформации.
Результаты для случаев с повышением экспрессии
[0274] Затем растения T1 в случае 49 сортировали на основании отношений экспрессии FatB4/тубулин, а затем FatB5/тубулин для поиска растений с наибольшей экспрессией для получения поколения T2 в теплице. Для выращивания до созревания выбирали восемь растений с наибольшей экспрессией FatB4. Шесть этих растений также обладали наибольшей экспрессией FatB5. Количество копий ZFP TF у этих растений с наибольшей экспрессией варьировало в диапазоне 2-4 копий, тогда как количество копий, сегрегирующее во всем потомстве T1, составляло 0-7 копий. У контрольных растений до состояния созревания для сбора семян T2 также выращивали одно ноль-растение случая 49 и десять контрольных растений Nex710.
13.4 Анализ жирных кислот семян T2
[0275] Анализ жирных кислот (FA) проводили в партии из 24 семян всех растений, как описано в примере 6.1. Профиль FA одного ноль-растения для контроля расчета профилей FA объединяли с десятью контрольными растениями Nex710. В среднем, для случая 49 по сравнению с Nex710 наблюдали 12% увеличение содержания C18:0 (таблицы 14A и 14B). Это увеличение было статистически значимым при p=0,05 (фиг. 13). Также некоторое возрастание продемонстрировали длинноцепочечные FA, такие как C20:0, C22:0 и C24:0, что приводило к возрастанию общего содержания всех насыщенных FA на 5%. Так как фермент FatB катализирует преобразование C18:0-ACP в свободные FA C18:0, в результате активации транскрипции FatB4 и FatB5 накапливается большее количество C18:0 (фиг. 1). pDAB4691 (пример 6, таблицы 1 и 2) специфична к обоим генам FatB4 и FatB5, что приводит к значимым изменениям профиля FA (таблицы 14A и 14B).
Профиль жирных кислот (C16:0, C16:1, C18:0, C18:1, C18:2 и C18:3) трансгенных и контрольных образцов Nex710 в случае 49
Числа в скобках в колонке 2 представляют собой количества анализируемых растений.
Профили жирных кислот (C20:0, C20:1, C20:2, C22:0, C22:1, C24:0, C24:1) трансгенных и контрольных образцов Nex710 в случае 49
Числа в скобках в колонке 2 представляют собой количества анализируемых растений.
[0276] Значимых изменений в общем содержании C16 при повышении экспрессии природных FatB4 и FatB5 не наблюдали. Вероятно, что катализ преобразования C16:0-ACP в C16:0 производится другими генами FatB, а не FatB4 и FatB5, иллюстративными мишенями для повышения экспрессии с использованием конструкции pDAB4691 с ZFP TF (фиг. 1).
[0277] Наблюдали, что в семенах T1 категорий с "низким" и "высоким" содержанием содержание C16:0 отдельных семян не изменяется (таблица 12), что указывает на тот факт, что конструкция pDAB4691 с ZFP TF более специфично связывается геном(ами) FatB, опосредующими ферментативную реакцию преобразования C18:0-ACP в C18:0, а не реакцию преобразования C16:0-ACP в C16:0 (фиг. 1).
[0278] Следует отметить, что повышение экспрессии природных генов β-кетоацил-ACP-синтетазы II (примеры 1-6), индуцируемое ZFP TF, обуславливает различные изменения профилей FA по сравнению с повышением экспрессии генов FatB4 и FatB5. Например, повышение экспрессии гена β-кетоацил-ACP-синтетазы II вызывает статистически значимое снижение содержания C16:0 и C16:1 и одновременное увеличение содержания всех C18 по сравнению с их ноль-сегрегантами (пример 6, фиг. 6, таблицы 5 и 8). В сравнении с этим, опосредуемое ZFP-TF повышение экспрессии гена FatB вызывает статистически значимое увеличение содержания C18:0, но не вызывает видимого изменения содержания C16:0 (фиг. 14). Кроме того, эти изменения профилей FA посредством опосредуемого ZFP TF повышения экспрессии генов β-кетоацил-ACP-синтетаза II и FatB в соответствии с путем биосинтеза FA конкурируют (фиг. 1).
Пример 14: Получение конструкций ZFP TF для трансформации растений
[0279] Получали и конструировали четыре конструкции для подавления транскрипции генов FatB в B. napus L (таблица 15). Для демонстрации снижения экспрессии FatB использовали наилучшие конструкции ZFP для повышения экспрессии FatB, 13722 и 13714 (примеры 9-13). Для конструирования функциональных ZFP TF эти конструкции ZFP сливали с сигналом ядерной локализации opaque-2 и репрессирующим доменом, состоящим из KRAB1 (Hanna-Rose and Hansen, 1996, Trends in Genetics, 12:229-234) или NtERF3 (Ohta et al., The Plant Cell, 2001, 13:1959-1968). Все эти ZFP TF экспрессировали под контролем специфичных для семян промоторов; использовали промотор белка транспорта липидов 2 Arabidopsis thaliana (промотор AtLTP170) (Genbank ID: NC_003076) или промотор Phaseolus vulgaris β-фазеолина (промотор PvPhas) (патент США № 5591605).
Подробная информация о конструкциях ZFP TF для направленного снижения экспрессии генов FatB
[0280] pDAS5203 представляет собой бинарную плазмиду, содержащую генные экспрессионные кассеты NLS opaque-2/13722/KRAB1 и pat. Эта конструкция содержит следующие генетические элементы: Промотор 170 AtLTP::слияние NLS opaque-2/цинковый палец 13722/KRAB1::v1 3'-UTR AtuORF23::v2 промотора AtUbi10::v5 pat::v4 3'-UTR AtuORF1. Бинарную плазмиду конструировали посредством клонирования фрагмента ДНК, содержащего слияние NLS opaque-2/цинковый палец 13722/KRAB1, в донорный вектор Gateway. Полученная конструкция содержала генную экспрессионную кассету промотор 170 AtLTP::слияние NLS opaque-2/цинковый палец 13722/KRAB1::v1 3'-UTR AtuORF23. Эту конструкцию клонировали в бинарную плазмиду посредством реакции L-R Gateway Reaction (Invitrogen, Carlsbad, CA). В этой реакции получали pDAS5203 и подтверждали посредством расщеплений рестрикционными ферментами и реакций секвенирования.
[0281] pDAS5204 представляет собой бинарную плазмиду, содержащую генные экспрессионные кассеты NLS opaque-2/13714/KRAB1 и pat. Эта конструкция содержит следующие генетические элементы: промотор 170 AtLTP::слияние NLS opaque-2/цинковый палец 13714/KRAB1::v1 3'-UTR AtuORF23::v2 промотора AtUbi10::v5 pat::v4 3'-UTR AtuORF1. Бинарную плазмиду конструировали посредством клонирования фрагмента ДНК, содержащего слияние NLS opaque-2/цинковый палец 13714/KRAB1, в донорный вектор Gateway. Полученная конструкция содержала генную экспрессионную кассету промотор 170 AtLTP::слияние NLS opaque-2/цинковый палец 13714/KRAB1::v1 3'-UTR AtuORF23. Эту конструкцию клонировали в бинарную плазмиду посредством реакции L-R Gateway Reaction (Invitrogen, Carlsbad, CA). В этой реакции получали pDAS5204 и подтверждали посредством расщеплений рестрикционными ферментами и реакций секвенирования.
[0282] pDAS5212 представляет собой бинарную плазмиду, содержащую генные экспрессионные кассеты NLS opaque-2/13722/KRAB1 и pat. Эта конструкция содержит следующие генетические элементы: промотор PvPhas::слияние NLS opaque-2/цинковый палец 13722/KRAB1::v1 3'-UTR AtuORF23::v2 промотора AtUbi10::v5 pat::v4 3'-UTR AtuORF1. Бинарную плазмиду конструировали посредством клонирования фрагмента ДНК, содержащего слияние NLS opaque-2/цинковый палец 13722/KRAB1, в донорный вектор Gateway. Полученная конструкция содержала генную экспрессионную кассету промотор PvPhas::слияние NLS opaque-2/цинковый палец 13722/KRAB1::v1 3'-UTR AtuORF23. Эту конструкцию клонировали в бинарную плазмиду посредством реакции L-R Gateway Reaction (Invitrogen, Carlsbad, CA). В этой реакции получали pDAS5212 и подтверждали посредством расщеплений рестрикционными ферментами и реакций секвенирования.
[0283] pDAS5227 представляет собой бинарную плазмиду, содержащую генные экспрессионные кассеты NLS opaque-2/13722/NtERF3 и pat. Эта конструкция содержит следующие генетические элементы: v3 MAR RB7::промотор 170 AtLTP::слияние NLS opaque-2/цинковый палец 13722/NtERF3::v1 3'-UTR AtuORF23::v2 промотора AtUbi10::v5 pat::v4 3'-UTR AtuORF1. Бинарную плазмиду конструировали посредством клонирования фрагмента ДНК, содержащего слияние NLS opaque-2/цинковый палец 13722/NtERF3, в донорный вектор Gateway. Полученная конструкция содержала генную экспрессионную кассету промотор 170 AtLTP::слияние NLS opaque-2/цинковый палец 13722/NtERF3::v1 3'-UTR AtuORF23. Эту конструкцию клонировали в бинарную плазмиду посредством реакции L-R Gateway Reaction (Invitrogen, Carlsbad, CA). В этой реакции получали pDAS5227 и подтверждали посредством расщеплений рестрикционными ферментами и реакций секвенирования.
[0284] Конструкции применяли для стабильной трансформации сорта Nex710 B. napus посредством опосредуемой Agrobacterium трансформации гипокотильных тканей (пример 3.2-3.3). Растения T0, выращиваемые в теплице, подвергали самоопылению и через четыре месяца после высаживания собирали семена T1.
Пример 15: Анализ семян T1 трансгенных по 4 конструкциям ZFP TF
[0285] Семена T1 получали в случаях переноса трансгена (линии) 8, 20, 37 и 15 конструкциями pDAS5203, pDAS5204, pDAS5212 и pDAS5227, соответственно. В качестве контроля использовали семена пяти растений Nex710. Анализ FA проводили на 24 отдельных семенах в каждом случае переноса трансгена из T1, как описано ранее в примере 6.1, с идентификацией сначала конструкции ZFP TF, которая наиболее эффективно изменяет профиль FA.
15.1 Анализ жирных кислот (FA) в семенах T1
[0286] Посредством конструкций pDAS5203, pDAS5212 и pDAS5227 получали случаи переноса трансгена с профилями с наименьшим уровнем всех насыщенных FA по сравнению с контролем Nex710 (таблица 16). Парные различия между каждым из двух случаев конструкций pDAS5203 и pDAS5212 и контролем Nex710 являлись значимыми (p=<0,005). При этом парное различие pDAS5227 продемонстрировало тенденцию к повышению (p=0,06). В одном из случаев применения pDAS5203 выявляли наименьшее содержание всех насыщенных FA 5,3% (не представлено) по сравнению со средними 6,38% в контроле Nex710. Это представляет собой 17% снижение всех насыщенных FA.
Профиль FA в семенах T1 в случаях переноса трансгена несколькими конструкциями
конструк
ции
анализа
насы
щенных
**значение p, равное или меньшее 0,05, считали статистически значимым и рассчитывали с использованием программного обеспечения JMP.
Профиль FA в семенах T1 в случаях переноса трансгена несколькими конструкциями
**значение p, равное или меньшее 0,05, считали статистически значимым и рассчитывали с использованием программного обеспечения JMP.
[0287] Конкретные профили FA в случаях pDAS5203, pDAS5212 и pDAS5227 приводили к 21-25% снижению содержания C18:0 по сравнению с Nex710 (фиг. 15A). Все эти различия являлись статистически значимыми при p=0,001 или менее (таблица 16). Другие длинноцепочечные FA, C20:0, C22:0 и C24:0, также продемонстрировали снижение концентрации. Однако изменений в содержании C16:0 не наблюдали, что в результате приводило к значительному увеличению содержания C16:0/C18:0 во всех случаях переноса трансгена конструкциями (фиг. 165B).
[0288] Профиль FA трансгенных семян при использовании pDAS5227 продемонстрировал явные отличия по сравнению с pDAS5203 и pDAS5212. При использовании pDAS5227 в семенах наблюдали 23% снижение содержания C14:0 (p=0,002) и 19% увеличение содержания C16:1 (p=0,01) по сравнению с Nex710 (фиг. 16A & B, таблица 16). Состав ZFP TF pDAS5227 идентичен составу pDAS5203 и pDAS5212 за исключением присутствия подавляющего транскрипцию домена ERF3, слитого с ZFP вместо домена KRAB1 (таблица 15).
[0289] Другой состав ZFP, 13714, присутствующий в pDAS5204, являлся не таким эффективным в снижении содержания C18:0 по сравнению с составом 13722 (таблица 16). В отличие от состава 13722, связывающегося с обоими генами FatB4 и FatB5, состав 13714 связывается только с геном FatB5 (пример 9, таблица 10B).
15.2 Идентификация растений для анализа мРНК
[0290] Для анализа подавления транскрипции FatB5 выбирали два случая переноса трансгена, 5212[1]-004 и 5227[4]-012, полученные посредством трансформации конструкциями pDAS5212 и pDAS5227, соответственно. В теплице высаживали от пятидесяти до ста семян T1 и выращивали растения. У растений на стадии 2-3 листьев получали четыре оттиска листьев. Этот растительный материал анализировали на количество копий ZFP TF с использованием анализа pat кПЦР-РВ (пример 6.2). Затем для выращивания до созревания для сбора семян T2 случайным образом выбирали ноль-растения по ZFP и положительные по ZFP растения (таблица 17). У этих растений для анализа мРНК FatB через 25 суток после цветения собирали незрелые стручки. Оба случая сегрегировали как при наличии одной копии. Эти случаи обозначали как 5212-4 и 5227-12.
Скрининг случаев переноса трансгена на идентификацию положительных по ZFP и ноль-растений
15.3 Проведение выделения РНК и анализа кПЦР-РВ
[0291] РНК выделяли из незрелых семян Brassica с использованием набора RNAEASY® для растений, полученного из Qiagen (Valencia, CA). Семена помещали в кассетные пробирки, содержащие буфер RLT (Qiagen)/β-меркаптоэтанол (BME) и бусину из нержавеющей стали. Образцы помещали в штатив для кассетных пробирок и гомогенизировали при 500 ударах в минуту в течение 5 минут в бисерной мельнице (Kleco, Visalia, CA). Штатив для пробирок переворачивали на 180 градусов и гомогенизировали дополнительные 5 минут. Затем образцы переносили в 1,5 мл пробирки Eppendorf и центрифугировали в течение 5 минут при 20000×g, и супернатант переносили в чистые пробирки. РНК выделяли, как описано в протоколе производителя (Qiagen; Valencia, CA). РНК элюировали с колонок 50 мкл не содержащей РНКаз воды и в образцах РНК определяли количество с использованием NanoDrop 8000 из Thermo Scientific (Wilmington, DE).
[0292] От десяти до двенадцати микрограмм РНК обрабатывали ДНКазой TURBO DNA-free (каталожный номер AM1907; Applied Biosystems, Foster City, CA) в 1,5-мл пробирках, не содержащих РНКаз/ДНКаз, для удаления геномной ДНК. Для каждого образца РНК получали пятьдесят микролитров реакционной смеси, содержащий РНК, 1X буфер для ДНКазы и 2 Единицы ДНКазы TURBO. Реакционные смеси инкубировали при 37°C в течение 30 минут. В каждую пробирку добавляли пять микролитров (5 мкл) реагента для инактивации ДНКазы и перемешивали. Образцы инкубировали при комнатной температуре в течение трех минут, снова перемешивали и инкубировали при комнатной температуре в течение дополнительных двух минут. Образцы центрифугировали при 20000×g в течение пяти минут. Сорок микролитров (40 мкл) супернатанта удаляли, оставляя ниже взвесь для инактивации ДНКазы. В каждом обработанном ДНКазой образце определяли количество с использованием Nanodrop с тем, чтобы для синтеза ДНК можно было бы использовать эквивалентные количества РНК.
[0293] Для каждого образца РНК получали комплементарную ДНК (кДНК) с использованием набора cDNA High Capacity (Applied Biosystems, Foster City, CA). В кратком изложении, 1,5 мкг РНК использовали в качестве матрицы в пятидесяти микролитрах реакционной смеси, содержащей 1X буфер для обратной транскрипции, 1X dNTP, 1X случайные олигомеры и 125 единиц обратной транскриптазы Multiscribe. Кроме того, для каждого использования 1,5 мкг обработанной ДНКазой РНК получали реакционные смеси без RT в тех же условиях, как указано выше, но без обратной транскриптазы Multiscribe. Все образцы инкубировали при 25°C в течение 10 минут, 37°C в течение 2 часов, 85°C в течение 5 минут и в течение ночи при 4°C.
[0294] Праймеры и зонды для FATB, KASII, ERF3, KRAB1 и тубулина конструировали с использованием программного обеспечения Primer Express 3 из Applied Biosystems (Foster City, CA). Праймеры синтезировали посредством Integrated DNA Technologies (Coralville, IA). Ниже приведены последовательности праймеров:
SEQ ID NO:63: FATB5 fwd - 5'-TCGCTGCCATAACAACCATTT-3';
SEQ ID NO:64: FATB5 rev - 5'-CGCCTGGGTTTCCAGTCA-3';
SEQ ID NO:65: KRAB1 fwd - 5'-AAGGATGTGTTCGTGGATTTCA-3';
SEQ ID NO:66: KRAB1 rev - 5'-CACAATCTGCTGTGCAGTATCAAG-3';
SEQ ID NO:67: ERF3 fwd - 5'-GCGGGCGGGAGTTGTTA-3';
SEQ ID NO:68: ERF3 rev - 5'-CCCCATCGGCGTTACATG-3';
SEQ ID NO:69: ТУБУЛИН fwd - 5'-GAAGCTGAGAACAGCGATTGC-3';
SEQ ID NO:70: ТУБУЛИН rev - 5'-GTTCCTCCTCCCAACGAATG-3'.
Зонды 6FAM/MGB синтезировали в Applied Biosystems (Foster City, CA):
SEQ ID NO:71: зонд 6FAM для FATB5 TTTCTCAGCCGCCA;
SEQ ID NO:72: зонд 6FAM для KRAB1 TAGGGAAGAGTGGAAGCT;
SEQ ID NO:73: зонд 6FAM для ERF3 CAGGCCTCAGCCTT; и
SEQ ID NO:74: зонд 6FAM для тубулина TACAAGGTTTCCAAGTTT.
[0295] Экспрессию генов FatB, ERF3, KRAB1 и тубулина оценивали посредством ПЦР с детекцией в реальном времени с использованием Applied Biosystem 7900HT (Foster City, CA). Для установления динамического равновесия и для эффективности анализа получали стандартную кривую с использованием аликвот нескольких образцов кДНК из различных групп. Затем из исходного разведения делали серийные разведения 1:5 и 1:4. Каждый образец кДНК разбавляли 1:50 10 мМ Tris, pH7,5. Реакционные смеси ПЦР получали в объеме двадцати микролитров, содержащем 1X основную смесь для экспрессии генов (Applied Biosystems; Foster City, CA), 0,8 мкМ прямых и обратных праймеров, 0,2 мкМ геноспецифичного зонда 6FAM/MGB и 4 микролитра разбавленной кДНК. Все реакции проводили в устройстве Applied Biosystem 7900HT с использованием программного обеспечения SDS 2.4 в следующих условиях: Этап 1) 50°C в течение 2 минут; Этап 2) 95°C в течение 10 минут; Этап 3) 95°C в течение 15 секунд; и Этап 4) 60°C в течение 1 минуты. Этап 3 и 4 повторяли 39 дополнительных циклов. Экспрессию гена тубулина оценивали в каждом планшете, тогда как реакции для FatB, ERF3 и KRAB1 проводили раздельно. Все реакции проводили в трех повторениях.
[0296] Стандартные кривые оценивали на регрессию и наклон и по мере необходимости регулировали пороговые значения. Образцы без RT (контроли без обратной транскриптазы, содержащие РНК со всеми компонентами для реакции получения кДНК за исключением обратной транскриптазы) сравнивали с соответствующими образцами с подтверждением наличия различия Ct от 5 до 7. Данные импортировали в Excel для анализа. Средние значения количеств FatB, ERF3 и KRAB1 нормализовали по среднему количеству тубулина и регистрировали как отношения экспрессии FatB и тубулина.
15.4 Анализ снижения экспрессии мРНК специфичного для семян FatB5 в несозревших семенах
[0297] Результаты продемонстрировали, что снижение экспрессии мРНК FatB через 25 суток после цветения (DAF) в несозревших семенах зависело от состояния зиготности растения T1. Например, в незрелых семенах гетерозиготных растений (1 копия) 5227-12 видимого снижения экспрессии мРНК FatB5 не наблюдали (фиг. 17). Однако когда экспрессия ZFP TF в гомозиготных растениях (2 копии) возрастала в 2 раза, наблюдали 21% снижение экспрессии мРНК FatB5 (p=0,025). Подобные результаты получали в другом случае, 5212-4, с другой конструкцией, pDAS5212. В этом случае снова не наблюдали видимого снижения экспрессии FatB5 в гетерозиготных растениях (фиг. 18). Однако в гомозиготных растениях при возрастании экспрессии ZFP TF наблюдали 15% уменьшение количества транскриптов FatB5.
[0298] Ноль-растения, гетерозиготные и гомозиготные растения для двух случаев выращивали до созревания и определяли профили FA в совокупности из 24 семян каждого растения. Этот процесс сегрегации ноль-линий из содержащих ZFP TF линий обеспечивал различия в профилях FA, которые более точно отражали присутствие ZFP TF.
15.4 Анализ профилей FA в созревших семенах T2
[0299] Для случая 5227-12 профили FA в созревших семенах T2 варьировали в зависимости от зиготности ZFP TF родительского растения T1 (таблицы 18A и 18B). Хотя гетерозиготные растения T1 не демонстрировали никакого видимого снижения экспрессии мРНК FatB в незрелых семенах на 25 DAF, профиль FA их семян демонстрировал 8% снижение содержания C18:0. Значимого снижения содержания C16:0 не наблюдали. Кроме того, наблюдали небольшое увеличение C18:1 (олеиновой кислоты) и следующих далее FA, приводящее к общему 5,5% снижению всех насыщенных FA (таблицы 18A и 18B, фиг. 19). Когда растения T1 5227-12 являлись гомозиготными по ZFP TF, выявляли значительное снижение экспрессии мРНК FatB. Профили FA этих семян T2 отличались. Наблюдали 11% увеличение содержания C16:1, приводящее к 2,7% снижению всех насыщенных FA (таблицы 18A и 18B). Однако дополнительного снижения содержания C18:0 по сравнению с гетерозиготными растениями не наблюдали. Эти изменения совпадают с профилем FA созревших семян T1 (пример 15.1).
Измеренный профиль FA зрелых семян T2 в случае 5227-12
растения
насыщенных
(вакце
новая)
C18:1
Профиль FA зрелых семян T2 в случае 5227-12
[0300] Подобные результаты получали для профилей FA созревших семян T2 случая 5212-4. В семенах гетерозиготных растений наблюдали 5,5% снижение содержания C18:0, приводящее к снижению содержания всех FA на 3,2% (таблица 18, фиг. 20). Также наблюдали небольшое возрастание C18:1; другие концентрации оставшихся FA продемонстрировали незначительное снижение. Гомозиготные растения, несмотря на значимое снижение экспрессии мРНК FatB, не продемонстрировали большего снижения содержания C18:0 по сравнению со снижением содержания C18:0 у гетерозиготных растений.
[0301] Таким образом, в этих примерах продемонстрировано подавление транскрипции гена FatB5, специфичной для семян экспрессией ZFP TF. ZFP TF являлись эффективными в осуществлении подавления транскрипции гена-мишени FatB5 у гомозиготных растений T2. Однако снижение содержания C18:0 в гомозиготных семенах T2 было не большим, чем снижение содержания C18:0 в сегрегирующих семенах T2. Эти результаты свидетельствуют, что гомозиготные копии ZFP TF могут запускать механизм обратной связи с регуляцией профилей FA, так как гены FatB являются необходимыми для роста и развития растений (Bonaventure et al., The Plant Cell, 2003 15:1020-1033). Заслуживает внимания, что опосредуемое ZFP TF снижение экспрессии мРНК FatB в незрелых семенах обратно пропорционально повышению экспрессии FatB в отношении изменений содержания C18:0.
[0302] Эти примеры демонстрируют, что направленное на природные гены FatB действие ZFP TF специфически изменяет количество мРНК FatB, таким образом, приводя к специфическим и наследуемым изменениям профилей FA у B. napus.
Профили FA семян T2 случая 5212-4 при различных уровнях зиготности
растения
насыщенных
Профили FA семян T2 случая 5212-4 при различных уровнях зиготности
[0303] Все патенты, патентные заявки и публикации, указанные в настоящем документе, таким образом, полностью включены посредством ссылки для всех целей.
[0304] Хотя в качестве иллюстрации и примера с целью ясности понимания предоставлено подробное описание, специалистам в данной области очевидно, что можно осуществлять различные изменения и модификации без отклонения от сущности или объема описания. Таким образом, указанные выше описания и примеры не следует рассматривать как лимитирующие.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОНСТРУИРУЕМЫЕ БЕЛКИ С ЦИНКОВЫМИ ПАЛЬЦАМИ, НАПРАВЛЕННЫЕ НА ГЕНЫ РАСТЕНИЙ, ВОВЛЕЧЕННЫЕ В БИОСИНТЕЗ ЖИРНЫХ КИСЛОТ | 2010 |
|
RU2568056C2 |
| СПОСОБЫ И СОСТАВЫ ЛЕЧЕНИЯ БОЛЕЗНИ ХАНТИНГТОНА | 2013 |
|
RU2639277C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ ХАНТИНГТОНА | 2015 |
|
RU2691102C2 |
| МОДУЛЯТОРЫ ТАУ И СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ИХ ДОСТАВКИ | 2017 |
|
RU2789459C2 |
| ФУНКЦИОНАЛЬНЫЕ ЛОКУСЫ FAD2 И СООТВЕТСТВУЮЩИЕ СПЕЦИФИЧНЫЕ ДЛЯ САЙТА-МИШЕНИ СВЯЗЫВАЮЩИЕСЯ БЕЛКИ, СПОСОБНЫЕ ИНДУЦИРОВАТЬ НАПРАВЛЕННЫЕ РАЗРЫВЫ | 2013 |
|
RU2656158C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ ХАНТИНГТОНА | 2014 |
|
RU2693891C1 |
| НАПРАВЛЕННАЯ МОДИФИКАЦИЯ МАЛАТДЕГИДРОГЕНАЗЫ | 2013 |
|
RU2658437C2 |
| МОДУЛЯТОРЫ ЭКСПРЕССИИ ГЕНА ОТКРЫТОЙ РАМКИ СЧИТЫВАНИЯ 72 ХРОМОСОМЫ 9 И ИХ ПРИМЕНЕНИЯ | 2020 |
|
RU2828216C2 |
| НАЦЕЛИВАНИЕ НА КЛЕТКИ, ОПОСРЕДУЕМОЕ ХИМЕРНЫМ АНТИГЕННЫМ РЕЦЕПТОРОМ | 2018 |
|
RU2783316C2 |
| БЫСТРЫЙ НАПРАВЛЕННЫЙ АНАЛИЗ СЕЛЬСКОХОЗЯЙСТВЕННЫХ КУЛЬТУР ДЛЯ ОПРЕДЕЛЕНИЯ ДОНОРНОЙ ВСТАВКИ | 2014 |
|
RU2668819C2 |


























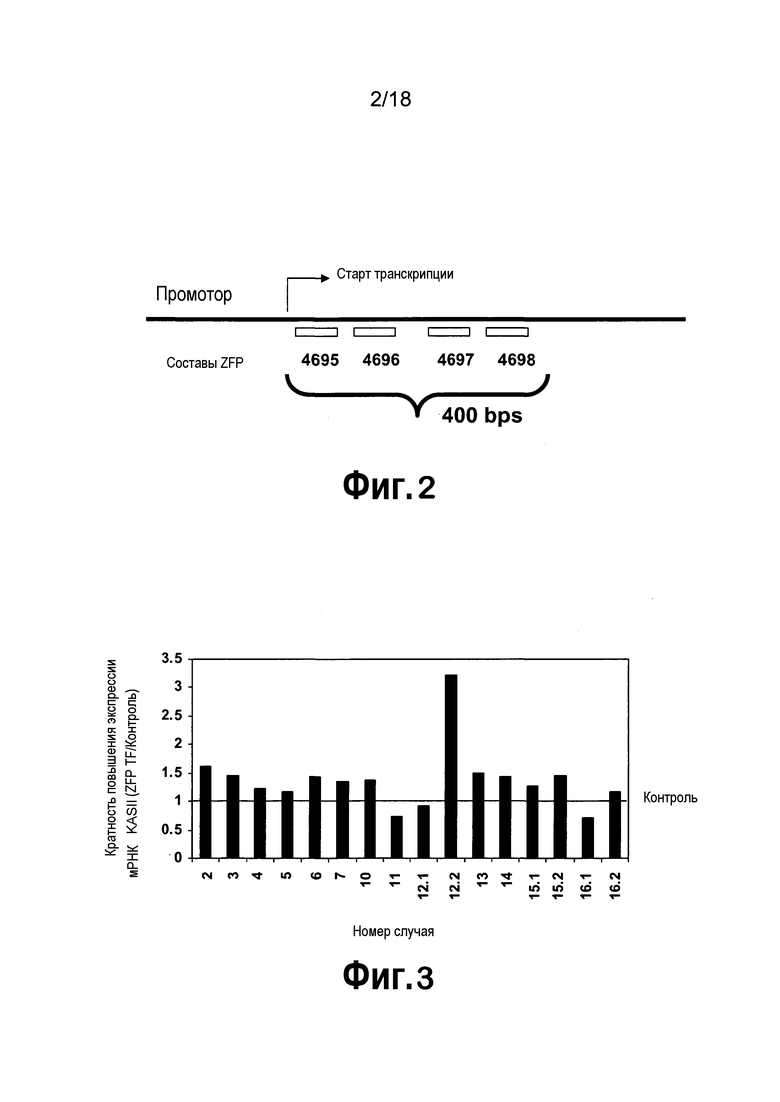

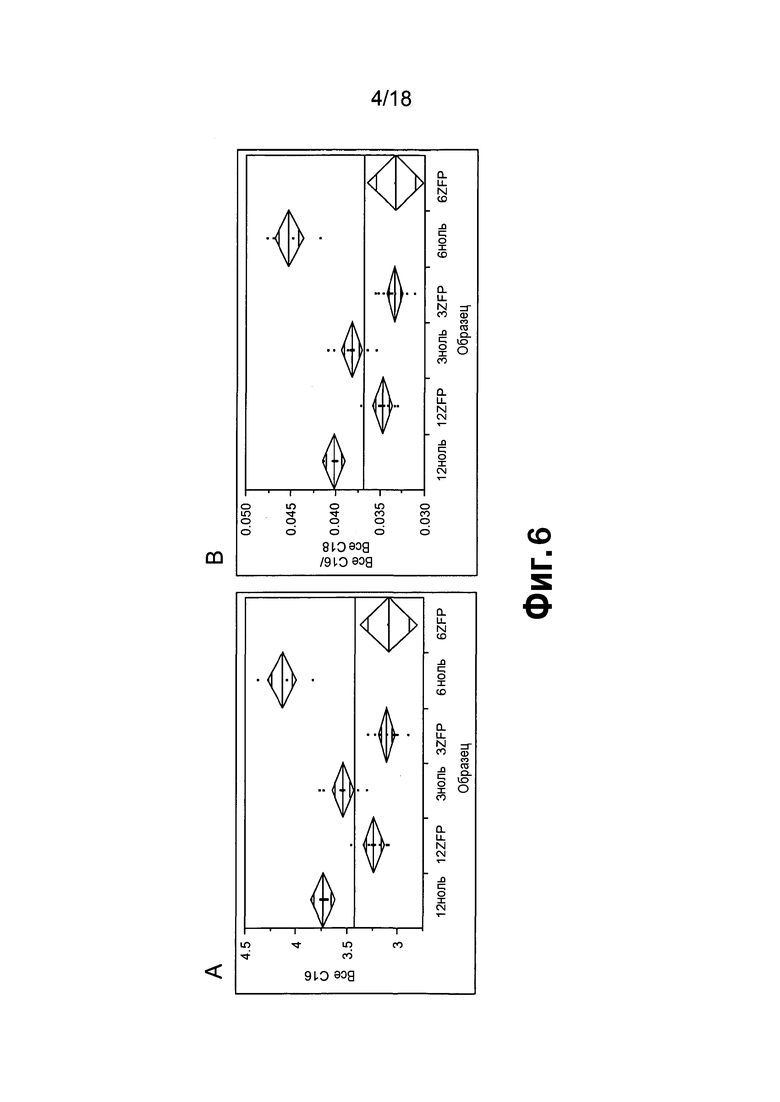



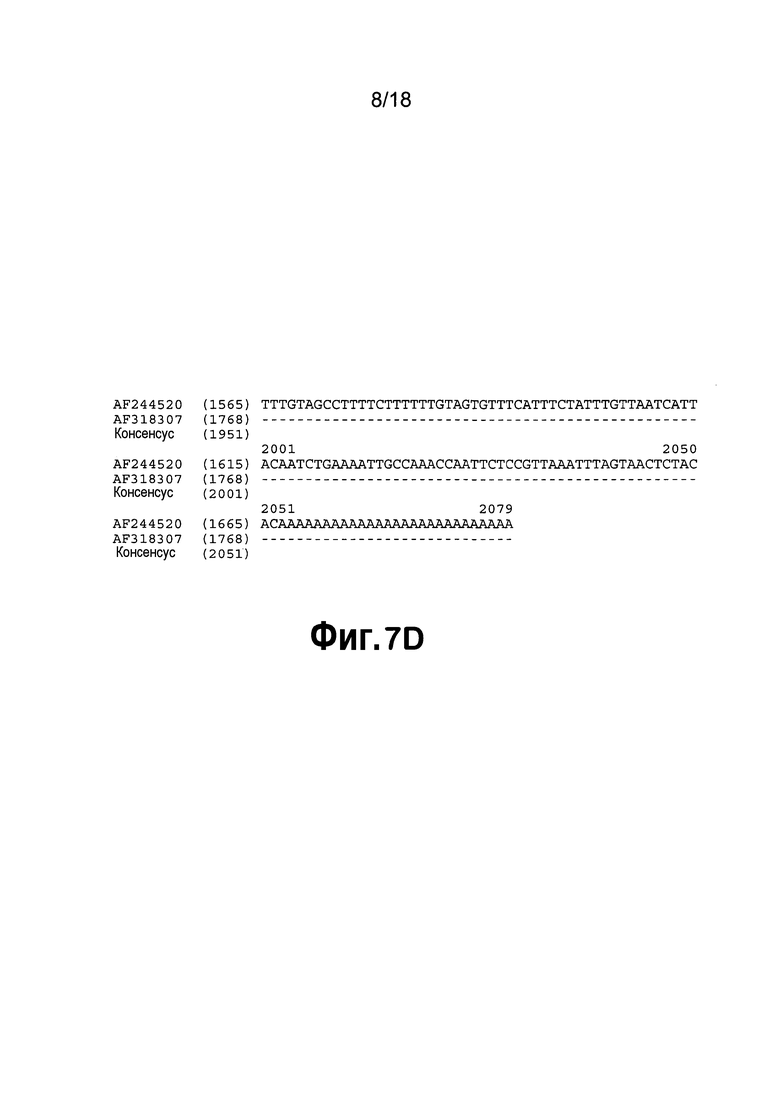

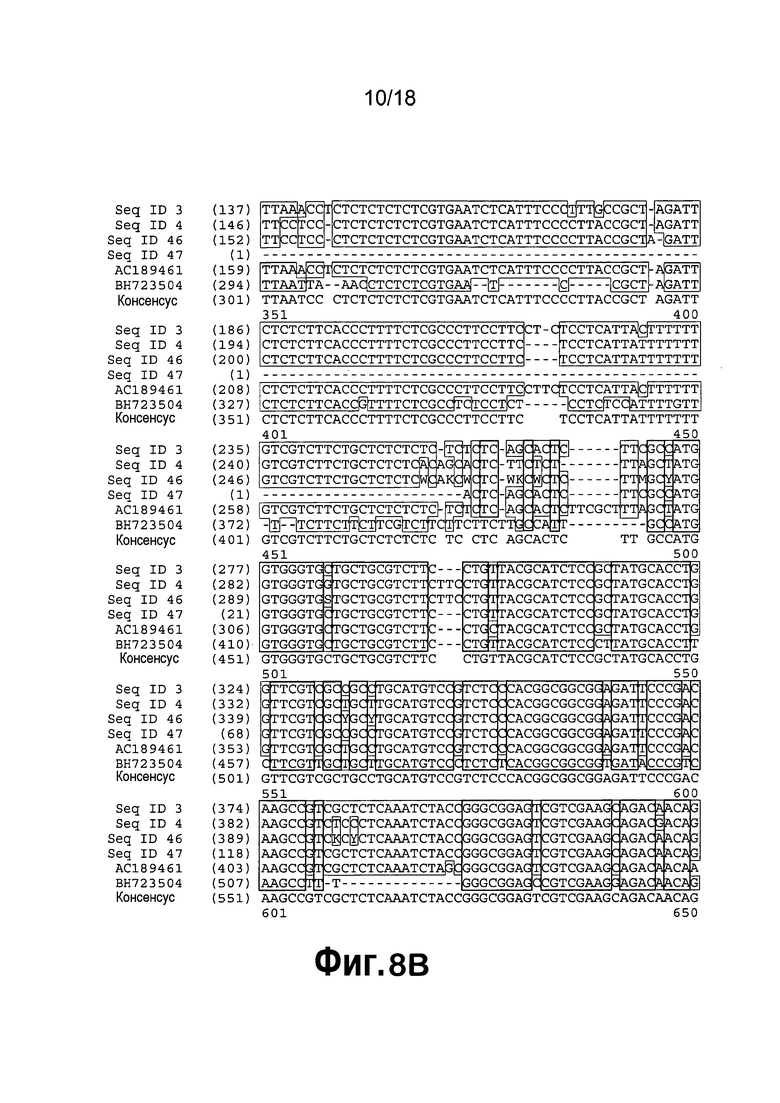
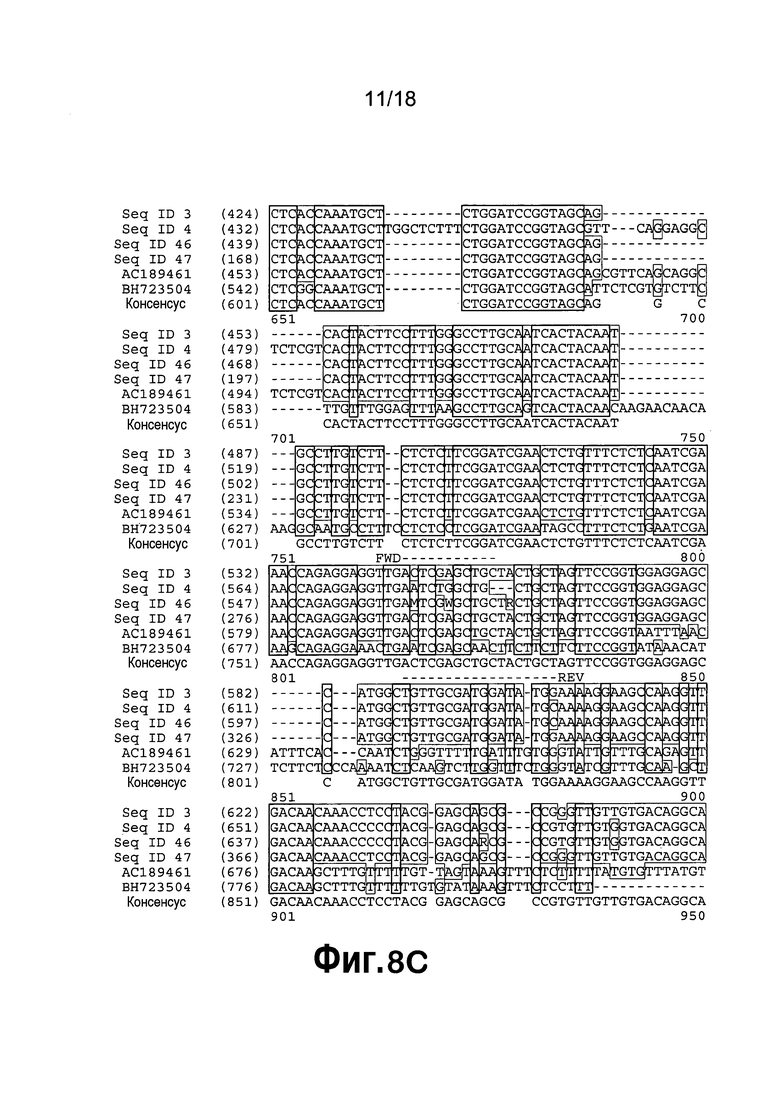

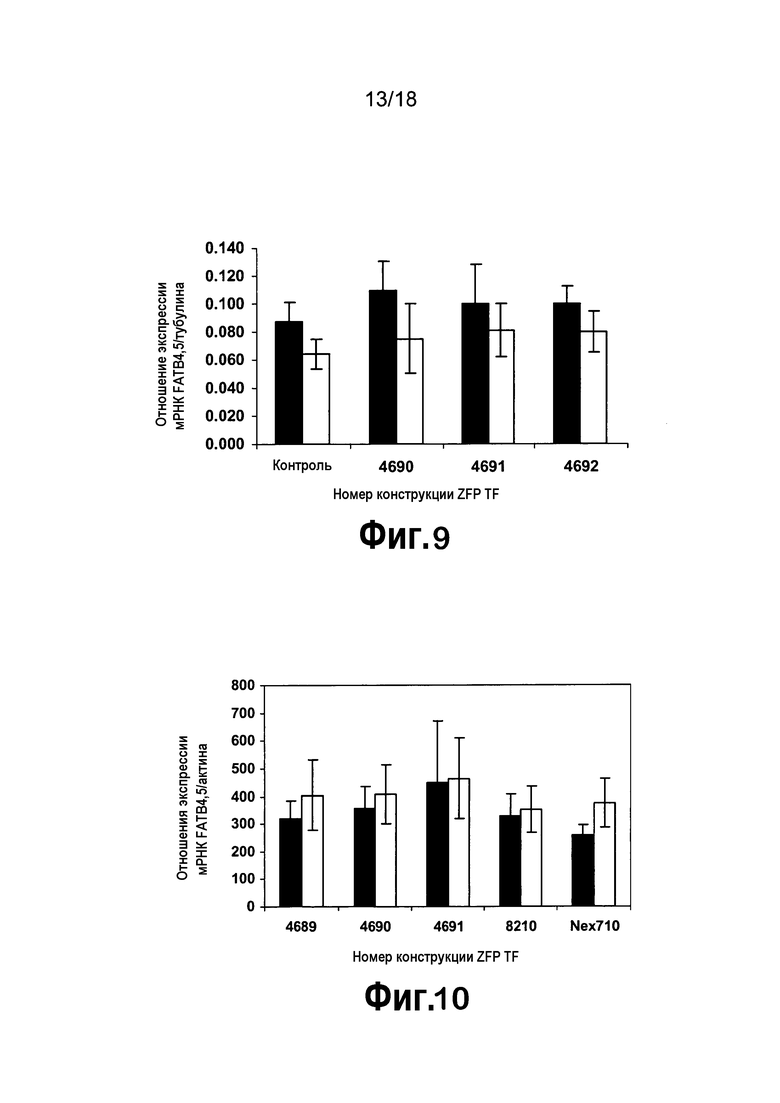
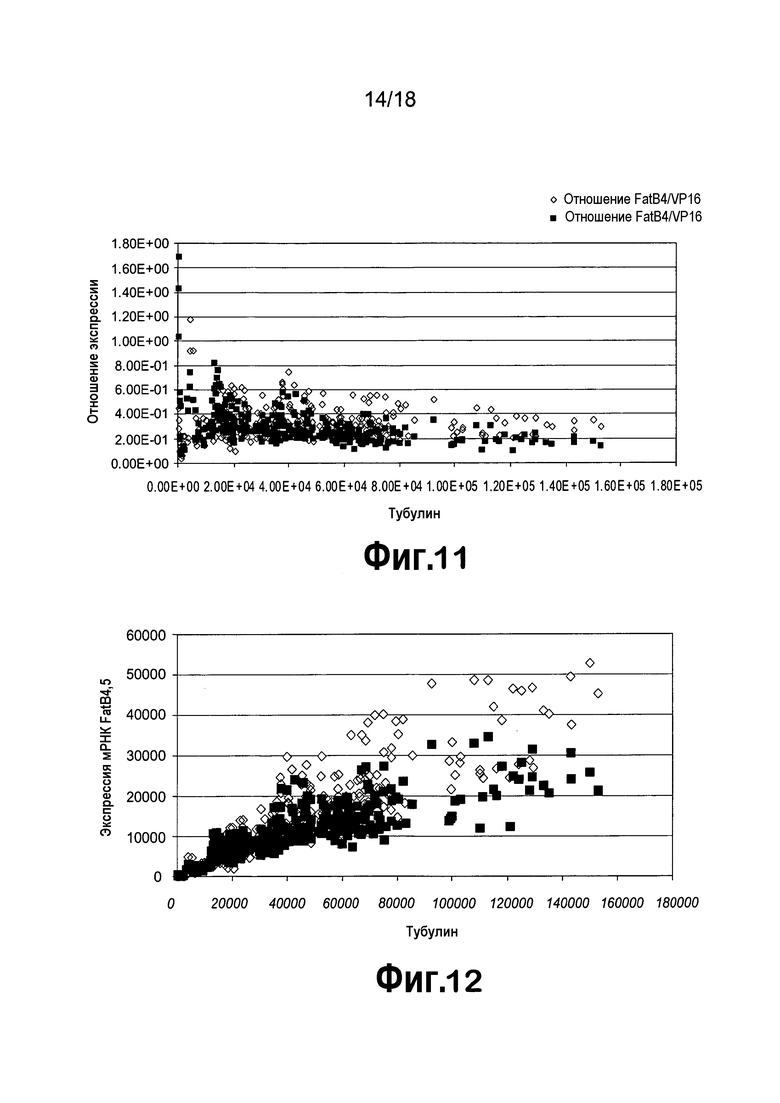
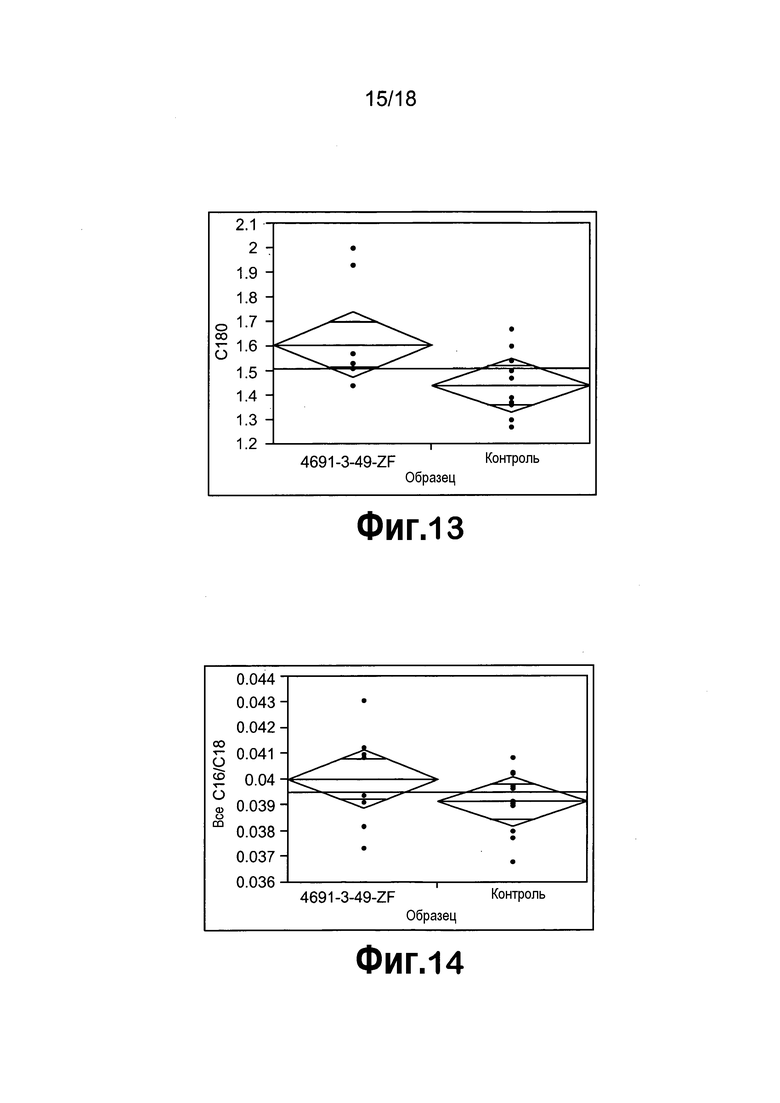
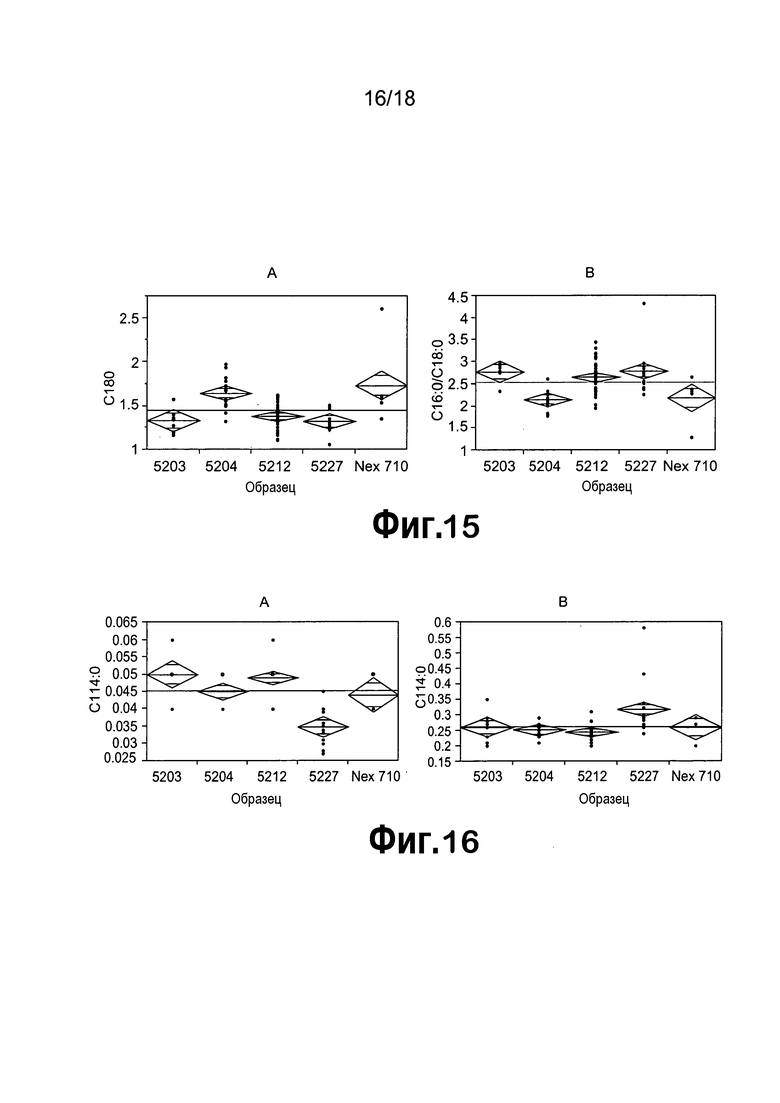
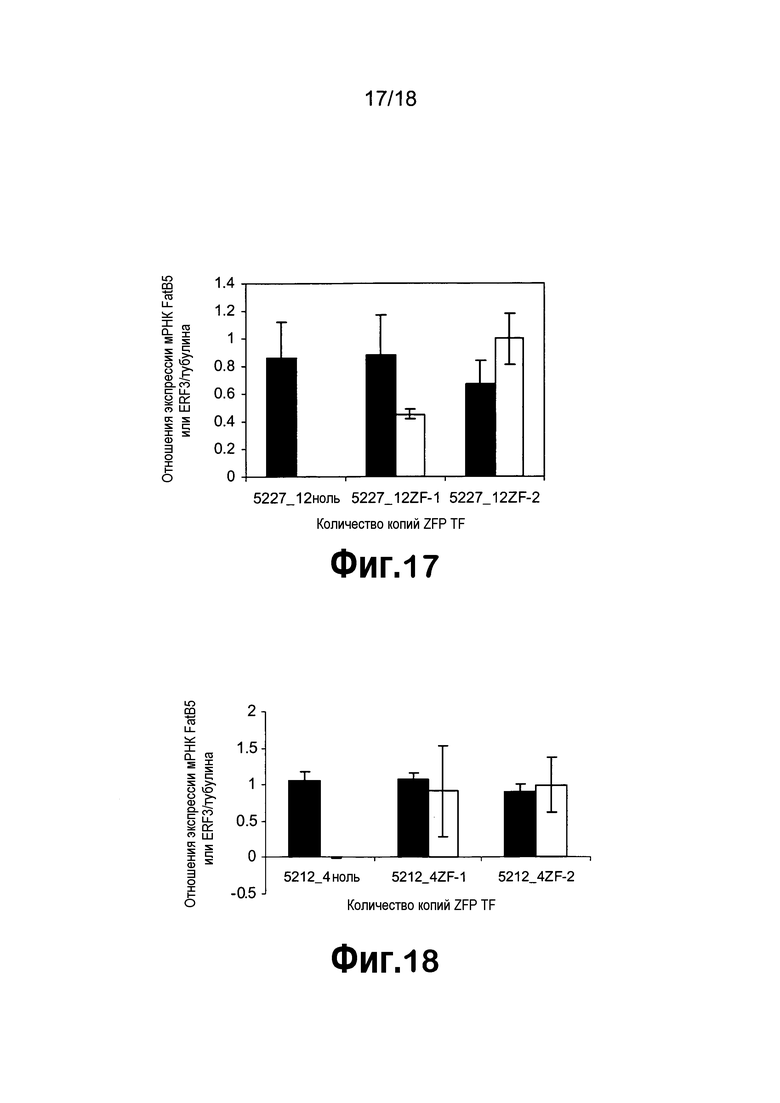
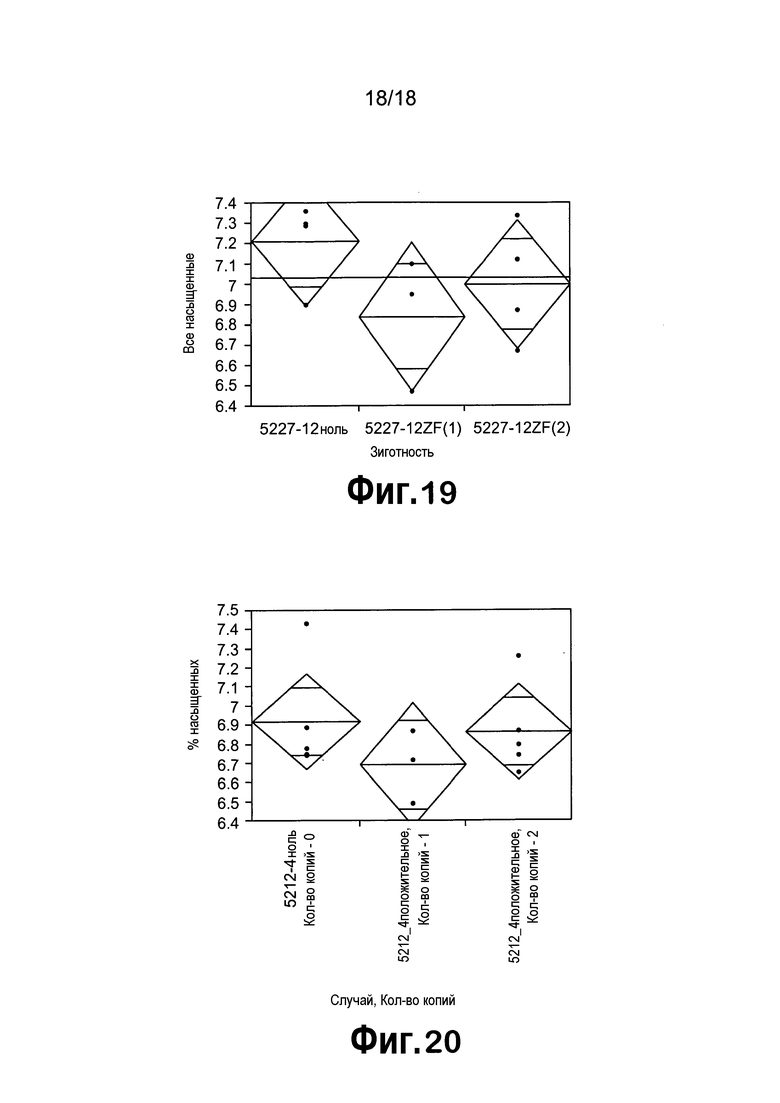
Изобретение относится к неприродному белку с цинковыми пальцами, модулирующему экспрессию гена тиоэстеразы жирных кислот B (FatB), где белок с цинковыми пальцами содержит шесть доменов цинковых пальцев в порядке от F1 до F6, при этом каждый домен цинковых пальцев содержит область распознающей спирали, и где белок с цинковыми пальцами содержит области распознающих спиралей. Изобретение относится также к слитому белку для модулирования экспрессии гена FatB, при этом слитый белок содержит белок с цинковыми пальцами и домен регуляции транскрипции или домен расщепления. Изобретение позволяет получать растения и растительные продукты с уменьшенным содержанием ненасыщенных жирных кислот. 8 н. и 9 з.п. ф-лы, 20 ил., 19 табл., 15 пр.
1. Неприродный белок с цинковыми пальцами, модулирующий экспрессию гена тиоэстеразы жирных кислот B (FatB), где белок с цинковыми пальцами содержит шесть доменов цинковых пальцев в порядке от F1 до F6, при этом каждый домен цинковых пальцев содержит область распознающей спирали, и где белок с цинковыми пальцами содержит области распознающих спиралей, выбранные из группы, состоящей из:
(i) F1: RSDNLSA (SEQ ID NO:75);
F2: QSAHRKT (SEQ ID NO:76);
F3: RSDDLSK (SEQ ID NO:21);
F4: QSSHRKT (SEQ ID NO:77);
F5: RSDHLSV (SEQ ID NO:78); и
F6: QNAHRIE (SEQ ID NO:79);
(ii) F1: RSDNLSA (SEQ ID NO:75);
F2: QSAHRKT (SEQ ID NO:76);
F3: RSDDLSK (SEQ ID NO:21);
F4: QSSHRKT (SEQ ID NO:77);
F5: RSDHLSK (SEQ ID NO:80); и
F6: QNANRIT (SEQ ID NO:81);
(iii) F1: RSDHLST (SEQ ID NO:82);
F2: HSNTRKN (SEQ ID NO:83);
F3: RSDHLSQ (SEQ ID NO:84);
F4: NSASRKN (SEQ ID NO:85);
F5: QSGNLAR (SEQ ID NO:16); и
F6: QSGHLSR (SEQ ID NO:86); или
(iv) F1: NSDSLTE (SEQ ID NO:87);
F2: RRADLSR (SEQ ID NO:88);
F3: RSDSLSA (SEQ ID NO:89);
F4: QNAHRKT (SEQ ID NO:90);
F5: RSDHLSQ (SEQ ID NO:84); и
F6: RNADRIT (SEQ ID NO:91).
2. Слитый белок для модулирования экспрессии гена FatB, при этом слитый белок содержит белок с цинковыми пальцами по п. 1 и домен регуляции транскрипции или домен расщепления.
3. Слитый белок по п. 2, где домен регуляции транскрипции представляет собой домен активации или домен репрессии.
4. Слитый белок по п. 2 или 3, где ген растения содержится в растении Brassica.
5. Слитый белок по п. 4, где белок с цинковыми пальцами связывается с участком-мишенью, как представлено в любой из SEQ ID NO: 47-52.
6. Полинуклеотид, кодирующий белок с цинковыми пальцами по п. 1.
7. Полинуклеотид, кодирующий слитый белок по любому из пп. 2-5.
8. Способ модификации экспрессии гена FatB в растительной клетке, где способ включает
введение в растительную клетку одного или более экспрессирующих векторов, содержащих по меньшей мере один полинуклеотид по п. 7, в таких условиях, что экспрессируются один или более слитых белков и подвергается модификации ген Fat.
9. Способ по п. 8, где модификация включает модуляцию экспрессии по меньшей мере одного гена.
10. Способ по п. 9, где активирована экспрессия по меньшей мере одного гена.
11. Способ по п. 9 или 10, где репрессирована экспрессия по меньшей мере одного гена.
12. Способ по п. 8, где полинуклеотид кодирует нуклеазы с цинковыми пальцами и расщепляется по меньшей мере один ген.
13. Способ по п. 12, дополнительно включающий этап введения донорной нуклеиновой кислоты так, что донорный вектор посредством гомологичной рекомбинации встраивается в участок расщепления.
14. Растительная клетка с модифицированным содержанием жирных кислот, при этом растительная клетка содержит ген FatB, модифицированный любым из способов по любому из пп. 8-13.
15. Растительная клетка по п. 14, где клетка представляет собой клетку семени.
16. Растение с модифицированным содержанием жирных кислот, при этом растение содержит по меньшей мере одну клетку по любому из пп. 14, 15.
17. Семя растения по п. 16, где семя имеет модифицированное содержание жирных кислот и содержит клетку по п. 14.
| US 20040204345, 14.10.2004 | |||
| РЕГУЛИРУЮЩЕЕ ДИФФЕРЕНЦИРОВКУ СРЕДСТВО, СОДЕРЖАЩЕЕ ГЕН, КОТОРЫЙ РЕГУЛИРУЕТ ДИФФЕРЕНЦИРОВКУ ИЗ СТВОЛОВЫХ КЛЕТОК В КЛЕТКИ-ПРИРОДНЫЕ КИЛЛЕРЫ, В КАЧЕСТВЕ ЭФФЕКТИВНОГО ИНГРЕДИЕНТА | 2005 |
|
RU2350649C2 |
| EP 826775, 04.03.1998. | |||
Авторы
Даты
2020-01-31—Публикация
2010-10-22—Подача