ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящей заявке испрашивается приоритет по патентным заявкам США 62/837523, поданной 23 апреля 2019 года, и 62/964844, поданной 23 января 2020 года. Содержание этих приоритетных заявок включено в настоящее описание в качестве ссылки в полном объеме.
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[0002] Настоящая заявка включает список последовательностей, который предоставлен в электронной форме в формате ASCII и включен в настоящее описание в качестве ссылки в полном объеме. Указанная копия ASCII, созданная 21 апреля 2020 года, названа 025297_WO017_SL.txt и имеет размер 19880 байт.
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
[0003] Ген открытой рамки считывания 72 хромосомы 9 (C9orf72) кодирует белок, который широко встречается в нейронах. Полагают, что белок C9orf72 играет важную роль в эндосомальном транспорте. Хотя функция белка C9orf72 не до конца понятна, последние данные указывают на то, что он играет роль в мембранном транспорте в эндолизосомальных путях посредством регуляции функции белков Rab.
[0004] Ген C9orf72 содержит в интроне 1 гексануклеотидный сегмент (G4C2; SEQ ID NO:1). Этот сегмент может повторяться тандемно вплоть до 30 раз без заметного биологического эффекта. Однако повторы более 30 раз - явление, называемое гексануклеотидной экспансией, может приводить к связанным с C9orf72 нарушениям (Renton et al., Neuron (2011) 72:257-68; Douglas, Non-coding RNA Res. (2018) 3:178-87). Эта экспансия обеспечивает аутосомно-доминантный фенотип, и пациенты, как правило, являются гетерозиготными по аллелю с экспансией. Оказалось, что гексануклеотидная экспансия вызывает образование очагов РНК в клетке, что приводит к секвестрации РНК-связывающих белков и нарушению метаболизма РНК. Также оказалось, что при не AUG-зависимой трансляции гексануклеотидная экспансия приводит к продуцированию аномальных белков, содержащих дипептидные повторы (DPR), потенциально с всех шести рамок считывания как в смысловом, так и в антисмысловом направлениях (Freibaum and Taylor, Front Mol Neurosci. (2017) 10:35; Douglas, выше). Эти белки склонны к агрегации (Gendron et al., Acta Neuropathol. (2013) 126:829). DPR были описаны в качестве включений в посмертном материале головного мозга пациентов со связанными с C9orf72 заболеваниями (Riemslagh et al., Acta Neuropathol Commun. (2019) 7:39).
[0005] Связанные с C9orf72 нарушения включают боковой амиотрофический склероз (ALS) и семейную лобно-височную деменцию C9 (C9FTD). ALS характеризуется прогрессирующей мышечной слабостью, уменьшением мышечной массы и постепенным снижением способности передвигаться, говорить, глотать и/или дышать. Ежегодная встречаемость ALS составляет 1-3 случая на 100000 человек, и он является наиболее распространенным нарушением двигательного нейрона с взрослым началом. Это заболевание является смертельным для большинства пациентов в пределах от трех до пяти лет после появления первых симптомов. Мутации в гене C9orf72 ответственны приблизительно за 30-40 процентов семейного ALS в США и Европе, и составляют 5-10% спорадического ALS. У некоторых пациентов со связанным с C9orf72 ALS также развивается состояние, называемое лобно-височной деменцией C9 (FTD) или C9FTD, - нейродегенеративное заболевание, которое влияет на личность, поведение и речь (Benussi et al., Front Aging Neurosci. (2015) 7:171). Индивидуумам, у которых развиваются оба состояния, ставится диагноз ALS-FTD.
[0006] Отсутствует эффективное лечение связанных с C9orf72 нарушений. Таким образом, существует неотложная потребность в эффективных способах терапии этих нарушений.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0007] Настоящее изобретение относится к модуляторам транскрипции C9orf72 человека на основе цинковых пальцев и применению этих модуляторов для лечения связанных с C9orf72 нарушений. В одном аспекте настоящее изобретение относится к слитому белку, содержащему домен белка с цинковыми пальцами (ZFP) и домен репрессора транскрипции, где домен ZFP связывается с областью-мишенью в интронном сегменте (интрон 1a) между экзонами 1a и 1b мутантного аллеля гена C9orf72 человека. Мутантный аллель имеет область экспансии повтора G4C2 (SEQ ID NO:1) в интроне 1a, и слитый белок нацелен на область экспансии повторов. Мутантный аллель может содержат более 30 тандемных повторов G4C2 (например, более 100, 200, 300, 400, 500, 600, 700, 800, 900 или 1000 повторов). Аллель дикого типа может содержать не более 30 таких повторов (например, не более 25, 20, 15, 10 или 5 повторов).
[0008] В некоторых вариантах осуществления слитый белок подавляет транскрипцию содержащих повтор РНК-транскриптов (например, мРНК) с мутантного аллеля и не подавляет транскрипцию транскриптов РНК дикого типа (например, мРНК) с гена.
[0009] В некоторых вариантах осуществления домен ZFP связывается со смысловой последовательностью в области-мишени, где смысловая последовательность содержит один из трех тандемных повторов гексануклеотида GGGGCC (SEQ ID NO:1), GGGCCG (SEQ ID NO:2), GGCCGG (SEQ ID NO:3), GCCGGG (SEQ ID NO:4), CCGGGG (SEQ ID NO:5) или CGGGGC (SEQ ID NO:6). В определенных вариантах осуществления слитый белок подавляет смысловую транскрипцию с мутантного аллеля в клетке человека. В конкретных вариантах осуществления слитый белок подавляет смысловую транскрипцию с промотора 1a C9orf72 и не подавляет смысловую транскрипцию с промотора 1b C9orf72.
[0010] В некоторых вариантах осуществления домен ZFP связывается с антисмысловой последовательностью в области-мишени, где антисмысловая последовательность содержит от одного до трех тандемных повторов гексануклеотида GGCCCC (SEQ ID NO:7), GCCCCG (SEQ ID NO:8), CCCCGG (SEQ ID NO:9), CCCGGC (SEQ ID NO:10), CCGGCC (SEQ ID NO:11) или CGGCCC (SEQ ID NO:12). В определенных вариантах осуществления слитый белок подавляет антисмысловую транскрипцию с мутантного аллеля в клетке человека.
[0011] В некоторых вариантах осуществления слитый белок подавляет как смысловую транскрипцию, так и антисмысловую транскрипцию, с мутантного аллеля C9orf72 в клетке человека. В некоторых вариантах осуществления слитый белок предпочтительно подавляет мутантный аллель C9orf72 по сравнению с аллелем C9orf72 дикого типа.
[0012] В следующих вариантах осуществления слитый белок подавляет смысловую и/или антисмысловую транскрипцию с мутантного аллеля по меньшей мере приблизительно на 30%, 40%, 75%, 90% или 95%.
[0013] В некоторых вариантах осуществления слитый белок имеет один или несколько доменов ZFP, каждый из которых необязательно содержит шесть цинковых пальцев; связывается с последовательностью-мишенью, представленной в таблице 1; и/или содержит шесть цинковых пальцев (в порядке от F1 до F6), причем каждый цинковый палец содержит последовательности ДНК-связывающих (распознающих) спиралей, представленные в одном ряду в таблице 1, и необязательно содержит одну или несколько мутаций остатков вне областей распознающий спирали, как указано в таблице 1. В следующих вариантах осуществления слитый белок связывается с последовательностью-мишенью и содержит цинковые пальцы, соответствующие SBS ID, как показано в таблице 1, причем цинковые пальцы содержат последовательности ДНК-связывающей (распознающей) спирали, представленные в одном ряду таблицы 1 для SBS ID, где SBS ID представляет собой 78021, 75114, 75115, 74969, 79895, 79898, 74986, 79899, 79901, 79902, 79904, 79916, 75027 или 79921.
[0014] В некоторых вариантах осуществления слитый белок имеет один или несколько доменов-репрессоров транскрипции, каждый из которых необязательно содержит аминокислотную последовательность домена KRAB из KOX1 человека, такую как последовательности, дополнительно описанные ниже. В конкретных вариантах осуществления домен ZFP связан с доменом-репрессором транскрипции через пептидный линкер.
[0015] В другом аспекте настоящее изобретение относится к конструкции нуклеиновой кислоты, содержащей кодирующую последовательность для одного или нескольких слитых белков, описанных в настоящем описании, где кодирующая последовательность необязательно функционально связана с элементом регуляции транскрипции. В некоторых вариантах осуществления элемент регуляции транскрипции содержит промотор млекопитающих, который является конститутивно активным или индуцибельным в клетке головного мозга, и где промотор необязательно представляет собой промотор синапсина I человека. В некоторых вариантах осуществления конструкция представляет собой рекомбинантную конструкцию на основе аденоассоциированного вируса ("AAV" или "rAAV"). Также предусматриваются rAAV, содержащие рекомбинантные конструкции AAV и капсиды серотипов 1-10 (например, AAV2, AAV6 или AAV9), или псевдотипов, происходящих из них (например, AAV2/9, AAV2/6 или AAV2/6/9).
[0016] В другом аспекте настоящее изобретение относится к клетке-хозяину, содержащей один или несколько слитых белков и/или одну или несколько конструкций нуклеиновых кислот, как описано в настоящем описании. Клетка-хозяин может представлять собой, например, клетку человека, такую как нейрон или плюрипотентная стволовая клетка (например, эмбриональная стволовая клетка или индуцибельная плюрипотентная стволовая клетка).
[0017] Также предусматриваются фармацевтические композиции, содержащие один или несколько слитых белков, одну или несколько конструкций нуклеиновых кислот (например, конструкций AAV), рекомбинантные вирусы, содержащие конструкции нуклеиновых кислот (например, rAAV), и/или одну или несколько клеток-хозяев, как описано в настоящем описании, как правило, в комбинации с одним или несколькими фармацевтически приемлемыми эксципиентами.
[0018] В другом аспекте настоящее изобретение относится к способу ингибирования транскрипции мутантного аллеля C9orf72 в клетке человека (например, нейрон, глиальная клетка, эпиндемная клетка или нейроэпителиальная клетка), где мутантный аллель содержит область экспансии повтора G4C2 в интроне 1a, причем способ включает введение в клетку одного или нескольких слитых белков, одной или нескольких конструкций нуклеиновой кислоты (например, AAV), одного или нескольких рекомбинантных вирусов, одной или нескольких клеток-хозяев и/или одной или нескольких фармацевтических композиций, как описано в настоящем описании. В некоторых вариантах осуществления клетка находится в головном мозге или спинном мозге пациента, страдающего от связанного с C9orf72 нарушения, такого как ALS или C9FTD.
[0019] В родственном аспекте настоящее изобретение относится к способу лечения пациента, страдающего от связанного с C9orf72 нарушения, необязательно выбранного из бокового амиотрофического склероза (ALS) и семейной лобно-височной деменции C9 (C9FTD), причем способ включает введение пациенту одного или нескольких слитых белков, одной или нескольких конструкций нуклеиновой кислоты (например, AAV), одной или нескольких клеток-хозяев и/или одной или нескольких фармацевтических композиций, как описано в настоящем описании.
[0020] В способах лечения по настоящему изобретению слитый белок может быть введен с использованием рекомбинантного вируса, который экспрессирует слитый белок (например, векторы AAV). В некоторых вариантах осуществления рекомбинантный вирус вводят пациенту интрацеребровентрикулярным, интратекальным, ретроорбитальным (RO), внутривенным, интраназальным и/или интрацистернальным путем. В некоторых вариантах осуществления вводят два или более различных слитых белков по настоящему изобретению, где кодирующие последовательности двух или более слитых белков могут находиться на одном и том же или различных рекомбинантных вирусных векторах.
[0021] Также в рамках настоящего изобретения предусматриваются один или несколько слитых белков, и/или одна или несколько конструкций нуклеиновых кислот, один или несколько рекомбинантных вирусов и одна или несколько фармацевтических композиций для применения в способах лечения, описанных в настоящем описании, и применение слитых белков, конструкций нуклеиновой кислоты и рекомбинантных вирусов для производства лекарственного средства для применения в способах лечения, описанных в настоящем описании.
[0022] Другие признаки, задачи и преимущества изобретения понятны из подробного описания, которое приведено ниже. Однако следует понимать, что подробное описание, хотя и указывает на варианты осуществления и аспекты изобретения, приведено только в качестве иллюстрации, а не ограничения. Различные изменения и модификации в пределах объема изобретения станут понятными специалистам в данной области из подробного описания.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0023] На фиг.1A-C представлена схема гена C9orf72 и транскриптов, которые с них продуцируются.
[0024] На фиг.1A представлена структура как аллеля C9orf72 дикого типа, так и мутантного аллеля C9orf72 с экспансией. Положение экспансии G4C2 на мутантном аллеле с экспансией указано (в геномной области между экзонами 1a и 1b, т.е. в интроне 1a). Экзоны показаны рамками. По материалам Douglas, выше; также см. Rizzu et al. (2016) Acta Neuropathologica Communications 4:37.
[0025] На фиг.1B представлено увеличенное изображение области на мутантном аллеле C9orf72 с экспансией вблизи экспансии G4C2 и представлены промоторы и транскрипты, ассоциированные с аллелем с экспансией. Представлены промоторы, вовлеченные в транскрипцию смысловой цепи (сплошные стрелки) и приблизительное положение промоторов, вовлеченных в антисмысловую транскрипцию (незакрашенные стрелки). Также представлены 5 различных смысловых транскриптов, которые описаны ранее, и приблизительное положение и транскрипты, которые находятся в антисмысловом направлении. Там же.
[0026] На фиг.1C представлена модель подавления промотора 1a и антисмыслового промотора посредством нацеливания ZFP-TF на область с экспансией, где ZFP-TF связывается в положении ниже обоих промоторов и оптимальном для регуляции промотора. Промотор 1b в этой модели не подавляется, поскольку связывание ZFP-TF происходит выше промотора 1b.
[0027] На фиг.2A-D представлено подавление экспрессии C9orf72 ("тотальный C9") в указанных типах клеток с использованием указанных ZFP-TF. Кроме того, на фигуре представлено подавление экспрессии более длинной изоформы мРНК (подвергнутой экспансии), содержащей интрон 1a, которая в основном продуцируется мутантным аллелем с экспансией ("специфическое в отношении содержащей повтор изоформы"). Изоформа с экспансией в основном экспрессируется в линиях пациентов с C9.
[0028] На фиг.2A проиллюстрирован анализ с использованием ПЦР, используемый для анализа тотального C9, и анализа, специфического для антисмысловой содержащей повторы изоформы. На верхней части фигуры представлена геномная структура аллеля дикого типа и аллеля с экспансии, в то время как на нижней части фигуры представлены мРНК-продукты каждого из аллелей. Наборы стрелок на чертежах мРНК указывают на мишени для ПЦР, использованные для анализа тотального C9.
[0029] На фиг.2B-D представлены графики, на которых показаны результаты анализов экспрессии C9orf72 для различных иллюстративных ZFP-TF в клеточной линии дикого типа, происходящей из здорового индивидуума, и фибробластной клеточной линии "C9", происходящей из пациента с ALS. Клеточная линия C9 характеризуется как "5/850", которые относятся к количеству повторов G4C2 на аллель дикого типа (5) и аллель с экспансией (850). Самые левые графики: экспрессия тотального C9orf72 ("тотальный C9") в клетках дикого типа в 3-м раунде скрининга ("раунд 3"). Вторые слева графики: тотальный C9 в клетках C9 в раунде 3. Вторые справа графики: тотальный C9 в клетках C9 во 2-м раунде скрининга ("раунд 2"). Самые правые графики: экспрессия с подвергнутого экспансии аллеля C9orf72 при определении посредством специфического для изоформы анализа C9orf72. Скрининг раунда 2 проводили в клетках C9 для оценки уровней специфических для изоформы (или заболевания) транскриптов C9orf72 против уровней тотальных транскриптов C9 после обработки ZFP-TF. В раунде 3 тотальный C9 определяли в клетках C9 и клетках дикого типа для оценки эффектов ZFP-TF на аллель дикого типа (WT) клеток C9. Для каждой ZFP-TF представлены концентрации 1, 3, 10, 30, 100 и 300 нг мРНК слева направо. На фиг.2B представлены результаты для ZFP-TF 74949, 74951, 74954, 74955 и 74964 на верхних графиках и для 74969, 74971, 74973, 74978 и 74979 на нижних графиках. На фиг.2B представлены SEQ ID NO: 1, 1 и 3, соответственно, в порядке встречаемости. На фиг.2C представлены результаты для ZFP-TF 74983, 74984, 74986, 74987 и 74988 на верхних графиках и 74997, 74998, 75001 и 75003 на нижних графиках. На фиг.2C представлены SEQ ID NO: 4 и 5, соответственно, в порядке встречаемости. На фиг.2D представлены результаты для ZFP-TF 75023, 75027, 75031, 75032, 75055 и 75078 на верхних графиках и 75090, 75105, 75109, 75114 и 75115 на нижних графиках. На фиг.2D представлены SEQ ID NO: 8-11, соответственно, в порядке встречаемости. Последовательность на нижнем из графиков соответствует ДНК-связывающему мотиву для этой ZFP-TF. Каждая ZFP-TF связывается с тремя гексануклеотидными повторами, содержащими этот мотив. Уровни транскрипта нормализовывали к уровням транскрипта зеленого флуоресцентного белка (GFP), экспрессируемого с мРНК GFP трансфицированной с мРНК ZFP-TF. Горизонтальной точечной линией на графиках представлено подавление 50% или 70%, как указано. Например, в случае ZFP-TF 75115 происходило подавление приблизительно 50% тотальных транскриптов изоформы и подавление приблизительно 70% специфичных к содержащей повторы изоформе транскриптов в линии C9, в то время как в линии WT происходило минимальное подавление тотальной изоформы. На графике указано, что остается 30% транскрипта, что указывает на то, что 70% подавлялись.
[0030] На фиг.3 представлена диаграмма промоторных областей для смысловых и антисмысловых транскриптов в аллеле C9orf72 с экспансией. Указаны пары праймеров для специфической детекции смысловых, тотальных и антисмысловых транскриптов. AS: антисмысловой. ddPCR: цифровая капельная ПЦР. На фиг. представлены SEQ ID NO: 1, 1 и 7, соответственно, в порядке встречаемости.
[0031] На фиг.4A и 4B показано, что праймеры, нацеленные на интрон 1b, специфически выявляют антисмысловую пре-мРНК. Цепь-специфическую ПЦР использовали для получения смысловой (S) или антисмысловой (AS) кДНК-матриц из клеток здорового контроля (Con) или клеток C9 (C9). Например, C9-AS указывает на результаты ddPCR, полученные с использованием антисмысловых кДНК-матриц, продуцированных с РНК, выделенной из клеток C9. На фиг.4A показано, что только кДНК-матрица C9-AS продуцирует продукт ПЦР, что указывает на специфичность праймеров для детекции антисмысловой пре-мРНК. На фиг.4B представлено продолжение эксперимента, представленного на фиг.4A, для 7 различных происходящих из пациентов с C9orf72 клеточных линий с различными длинами повторов G4C2 и для 6 различных линий здоровых контролей.
[0032] На фиг.5A-C представлены графики, демонстрирующие подавление транскриптов в клетках C9 при использовании анализов, специфичных к содержащей повторы изоформе. На фиг.5A показано три эксперимента, где ZFP-TF 74949, 74978, 75003, 75027, 75109, 75114, 75115, 74960 и 74967 вводили в трех различных дозах (30, 100 или 300 нг), а затем измеряли количество смыслового транскрипта при заболевании. На фиг.5B представлены три эксперимента, в которых проводилось измерение антисмыслового транскрипта при заболевании. На фиг.5C представлено три прогона, измеряющих тотальный транскрипт C9orf72.
[0033] На фиг.6 представлена репрессия тотального транскрипта C9 совместно с подвергнутыми экспрессии смысловыми и антисмысловыми транскриптами (обуславливающая заболевание изоформа) в трех различных линиях фибробластов, полученных от трех различных пациентов с ALS, каждая из которых содержала различные количества повторов G4C2 (приблизительно 600, 800 и 850 повторов, соответственно) в их подвергнутом экспансии аллеле. После воздействия на клетки 100 нг ZFP-TF 75109, 75114 и 75115 использовали селективный анализ изоформ для оценки уровней экспрессии. Все три ZFP-TF поддерживали селективное подавление во всех трех клеточных линиях.
[0034] На фиг.7 представлено подавление тотального транскрипта C9 в двух клеточных линиях от здоровых индивидуумов с более чем типичным количеством повторов G4C2 в их аллелях. Здоровые индивидуумы, как правило, имеют 2-5 повторов G4C2 в каждом из их аллелей C9orf72. Однако некоторые здоровые индивидуумы имеют больше повторов. Чтобы убедиться, что предоставляется достаточно участков связывания для ZFP-TF, использовали клеточные линии, содержавшие более чем типичное количество повторов (5/8 и 5/20 повторов). Тотальные транскрипты C9 минимально изменены в этих клеточных линиях.
[0035] На фиг.8A-8C представлены результаты анализа на микрочипах, проведенных для первичных фибробластных клеток пациентов с ALS (C921, также называемые C9021), для первичных нейронов мыши и для первичных нейронов человека, демонстрирующие специфичность указанных репрессоров (75027, 75109, 75114 и 75115). ZFP-TF 75027 нацелена на повторяющийся мотив GCCCCG (SEQ ID NO:8), в то время как ZFP-TF 75109, 75114 и 75115 нацелены на мотив CCGGCC (SEQ ID NO:11) в антисмысловой цепи гена C9orf72.
[0036] На фиг.8A представлены результаты анализа на микрочипах для происходящих из пациента первичных фибробластов (C9021) с использованием анализа Thermo Fisher Clariom™ S, который включает 21000 хорошо аннотированных генов в своей базе данных. Анализ проводили через 24 часа после введения в клетки C9021 репрессоров в форме мРНК в количестве 300 нг. На графиках проиллюстрированы гены, которые активировались или подавлялись в ответ на указанные ZFP-TF.
[0037] На фиг.8B представлены результаты анализа на микрочипах для первичных нейронов мыши с использованием анализа Thermo Fisher Clariom™ D, который включает 140000 аннотированных и неаннотированных кодирующих и некодирующих транскриптов в своей базе данных. Анализ проводили через 7 суток после трансдукции AAV. Все клетки трансдуцировали с MOI 3000. На графиках проиллюстрированы гены, которые активировались или подавлялись в ответ на указанные ZFP-TF.
[0038] На фиг.8C представлены результаты анализа на микрочипах для первичных нейронов человека с использованием анализа Thermo Fisher Clariom™ D. Анализ проводили через 19 суток после трансдукции посредством AAV клеток с MOI 3000. На графиках проиллюстрированы гены, которые активировались или подавлялись в ответ на указанные ZFP-TF.
[0039] На фиг.9 представлено связывание мишени ZFP in vivo у трансгенных мышей C9orf72 BAC. На панели A представлена конструкция AAV, использованная для инъекций. Конструкция содержит промотор синапсина, кодирующую последовательность ZFP-KRAB и метку Venus. На панелях B и C представлена схема исследования, согласно которой новорожденным проводили интрацеребровентрикулярную инъекцию (ICV) AAV, содержавшего экспрессирующую конструкцию ZFP-KRAB, и через один месяц их использовали для последующего анализа. На панели D представлены уровни смысловой, антисысловой и тотальной РНК C9 у животных, которым инъецировали ZFP-KRAB (75027) в гиппокамп и кору. На панели E представлены репрезентативные изображения очагов смысловой и антисмысловой РНК и количественное определение в областях аммонова рога (CA) и зубчатой извилины (DG) гиппокампа у животных, которым инъецировали ZFP-KRAB (75027).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0040] Настоящее изобретение относится к факторам транскрипции на основе белков с цинковыми пальцами (ZFP-TF), которые предпочтительно нацелены на аллели гена C9orf72 человека, имеющие область экспансии повторов G4C2, и подавляют транскрипцию этих мутантных аллелей в РНК. Такая область экспансии может иметь более 30 повторов G4C2. ZFP-TF по настоящему изобретению представляют собой слитые белки, содержащие (i) по меньшей мере один домен белка с цинковыми пальцами (ZFP), который специфически связывается с мотивами ДНК в повторах либо на смысловой, либо на антисмысловой цепи мутантного аллеля, и (ii) по меньшей мере один домен репрессора транскрипции, который снижает транскрипцию аллеля в любом или обоих из смыслового и антисмыслового направлений. Ожидается, что снижение уровня транскриптов мутантного C9orf72 в нейронах путем введения ZFP-TF в нервную систему (например, головной и спинной мозг) пациента, будет ингибировать (например, снижать или останавливать) образование вызывающих заболевание цитотоксических материалов в клетках. ZFP-TF по настоящему изобретению могут использоваться для лечения, в том числе предупреждения и облегчения, связанных с C9orf72 нарушений, таких как ALS и C9FTD.
[0041] В настоящем описании описаны способы и композиции для диагностики, предупреждения и/или лечения ALS и FTD. В частности, в рамках настоящего изобретения предусматриваются способы и композиции для модификации (например, модулирования экспрессии) конкретных генов для лечения этих заболеваний, включая применение сконструированных репрессоров факторов транскрипции и нуклеаз. В некоторых вариантах осуществления модулирование экспрессии включает как смысловую, так и/или антисмысловую экспрессию.
[0042] Таким образом, в настоящем описании описаны способы (in vivo, ex vivo и/или in vitro) подавления смысловой и/или антисмысловой транскрипции мутантных аллелей гена C9orf72 с экспансией повторов в клетке (например, нейроне). Способы включают введение в клетки одного или нескольких репрессоров мутантных аллелей гена C9orf72, причем один или несколько репрессоров содержат домен репрессии транскрипции и ДНК-связывающий домен, который связывается с участком-мишенью в мутантных аллелях гена C9orf72. Репрессор(ы) может включать один или несколько факторов транскрипции на основе белков с цинковыми пальцами (ZFP-TF, содержащий ДНК-связывающий домен ZFP), один или несколько факторов транскрипции на основе TAL-эффекторного домена (TALE-TF, содержащий ДНК-связывающий домен - TAL-эффекторный домен) и/или одну или несколько систем факторов транскрипции CRISPR/Cas (содержащая ДНК-связывающий домен единой гидовой РНК). В определенных вариантах осуществления используют два или более различных репрессоров (например, одна или несколько фармацевтических композиций, содержащих два или более различных репрессоров). В определенных вариантах осуществления ген C9orf72 содержит мутантный аллель, содержащий один или несколько повторов (G4C2), необязательно где участок-мишень, связываемый ДНК-связывающим доменом репрессора, находится в одном или нескольких повторах (G4C2). Таким образом, изобретение относится к применению одного или нескольких репрессоров ZFP-TF, TALE-TF или CRISPR/Cas TF (например, составленных в одну или несколько фармацевтических композиций, содержащих один или несколько репрессоров), которые связываются с мутантным подвергнутым экспансии аллелем C9orf72, содержащим один или несколько повторов (G4C2), для подавления смысловой и/или антисмысловой транскрипции (например, на 50%, 70% или более по сравнению с необработанной клеткой/индивидуумом) у индивидуума, нуждающегося в этом (например, индивидуум с ALS и/или FTD, где происходит лечение заболевания и/или смягчение симптомов). В определенных вариантах осуществления смысловая и/или антисмысловая транскрипция не подавляется до более чем 90% от нормальных (контрольных) уровней. В определенных вариантах осуществления как антисмысловая, так и смысловая транскрипция подавляется на одинаковых или различных уровнях (например, антисмысловая и смысловая транскрипция подавляются аналогичным образом); антисмысловая транскрипция подавляется больше, чем смысловая транскрипция, или смысловая транскрипция подавляется больше, чем антисмысловая транскрипция. В определенных вариантах осуществления происходит подавление специфических смысловых транскриптов, в то время как подавление других не происходит. В некоторых вариантах осуществления транскрипция с промотора в сегменте интрона 1b не подавляется, в то время как транскрипция с промотора в интроне 1a и антисмысловых транскриптов подавляется. В определенных вариантах осуществления происходит селективное подавление транскриптов, содержащих экспансию повторов (например, происходит подавление антисмысловой транскрипции, происходит подавление смысловой транскрипции с промотора 1a и/или не происходит подавление смысловой транскрипции с промотора 1b). В определенных вариантах осуществления один или несколько репрессоров ZFP-TF, содержащих области распознающей спирали, как показано в таблице 1, используют в способах и применениях, описанных в настоящем описании, необязательно в комбинации с одним или несколькими различными репрессорами (например, дополнительные различные ZFP-TF, например, одна или несколько дополнительных ZFP-TF, содержащих ZFP, как показано в таблице 1). В определенных вариантах осуществления один или несколько из репрессоров вводят в клетку с использованием одного или нескольких невирусных векторов (например, в качестве мРНК) и/или вирусных векторов (например, AAV, такой как AAV2/9). Множество копий одного или нескольких модуляторов (например, репрессоров) можно вводить с использованием одного и того же или различных способов (например, мРНК и/или AAV). В определенных вариантах осуществления один и тот же или различные способы могут использоваться для доставки одного или нескольких различных модуляторов (например, репрессоров). Способы in vivo и применения у живых индивидуумов (например, людей) могут вовлекать введение (например, одной или нескольких фармацевтических композиций, содержащих репрессоры и/или полинуклеотиды, кодирующие репрессоры) любым подходящим способом, включая, но не ограничиваясь ими, интрацеребровентрикулярный, интратекальный, внутричерепной, ретроорбитальный (RO), внутривенный, интраназальный и/или интрацистернальный. Введение в головной мозг может быть односторонним или двухсторонним (например, гиппокамп). Можно вводить любое количество (дозировку), например, от 1E10 до 1E13 (например, 6E11) вг/полушарие. В любом из способов и применений, описанных в настоящем описании, у индивидуума лечат ALS и/или FTD (и/или лечат один или несколько симптомов этих заболеваний).
[0043] В рамках настоящего изобретения предусматривается генетический модулятор гена C9orf72, причем модулятор содержит ДНК-связывающий домен (например, белок с цинковыми пальцами (ZFP), белок с TAL-эффекторным доменом (TALE) или единая гидовая РНК), который связывается с участком-мишенью в гене C9orf72 по меньшей мере из 12 нуклеотидов; и домен регуляции транскрипции (например, домен репрессии). Также предусматриваются один или несколько полинуклеотидов (например, носитель для вирусной или невирусной доставки генов, например, вектор AAV), кодирующих один или несколько генетических модуляторов, описанных в настоящем описании. В других аспектах в настоящем описании описаны фармацевтические композиции, содержащие один или несколько полинуклеотидов и/или один или несколько носителей для доставки, как описано в настоящем описании. В некоторых вариантах осуществления генетический модулятор включает домен регулятора, генетический модулятор (и фармацевтическая композиция, содержащая один или несколько генетических модуляторов или полинуклеотидов, кодирующих один или несколько генетических модуляторов) модулирует (например, подавляет или активирует) экспрессию гена C9orf72. Могут связываться и/или модулироваться смысловые и/или антисмысловые цепи гена. Также в рамках настоящего изобретения предусматриваются выделенные клетки (в том числе клеточные популяции), содержащие один или несколько генетических модуляторов; один или несколько полинуклеотидов; один или несколько носителей для доставки генов; и/или одну или несколько фармацевтических композиций, как описано в настоящем описании. Также предусматриваются способы и применения для модулирования экспрессии (например, подавления) гена C9orf72 в клетке (in vitro, in vivo или ex vivo), причем способы включают введение (любым способом, включая, но не ограничиваясь ими, интрацеребровентрикулярный, интратекальный, внутричерепной, ретроорбитальный (RO), внутривенный или интрацистернальный) одного или нескольких генетических модуляторов; одного или нескольких полинуклеотидов; одного или нескольких носителей для доставки генов; и/или одной или нескольких фармацевтических композиций, как описано в настоящем описании, в клетки. Способы могут использоваться для лечения и/или предупреждения у индивидуума бокового амиотрофического склероза (ALS) или лобно-височной деменции (FTD). Также предусматривается применение одного или нескольких генетических модуляторов; одного или нескольких полинуклеотидов; одного или нескольких носителей для доставки генов; и/или одной или нескольких фармацевтических композиций для лечения и/или предупреждения ALS или FTD у индивидуума. Также предусматривается набор, содержащий один или несколько генетических модуляторов; один или несколько полинуклеотидов; один или несколько носителей для доставки генов; и/или одну или несколько фармацевтических композиций, как описано в настоящем описании, и необязательно инструкции по применению.
[0044] Таким образом, в одном аспекте предусматриваются сконструированные (не встречающиеся в природе) генетические модуляторы (например, репрессоры) одного или нескольких генов. Эти генетические модуляторы могут включать системы (например, белки с цинковыми пальцами, TAL-эффекторные TALE) белки или CRISPR/dCas-TF), которые модулируют (например, подавляют) экспрессию аллеля. Экспрессия аллелей дикого типа и/или мутантных аллелей может модулироваться вместе или по отдельности. В определенных вариантах осуществления модулирование мутантного аллеля происходит на большем уровне, чем модулирование аллеля дикого типа (например, аллель дикого типа подавляется не более чем на 50% от нормы, однако мутантный аллель подавляется по меньшей мере на 70% по сравнению с контролем без введения). В некоторых вариантах осуществления модулирование экспрессии может включать модулирование как смысловых, так и антисмысловых транскриптов гена C9orf72. В некоторых вариантах осуществления модулирование экспрессии может преимущественно модулировать смысловые транскрипты, в то время как в других вариантах осуществления модулирование экспрессии может преимущественно модулировать антисмысловые транскрипты.
[0045] Мутация с экспансией в аллеле C9orf72 приводит к экспрессии как смыслового, так и антисмыслового продукта РНК, ассоциированного с ALS и FTD, так что в одном варианте осуществления предусматриваются сконструированные факторы транскрипции, предназначенные для подавления экспрессии этих мутантных аллелей C9orf72, для лечения ALS или FTD. Сконструированные белки с цинковыми пальцами или TALE представляют собой не встречающиеся в природе белки с цинковыми пальцами или белки TALE, чьи ДНК-связывающие домены (например, распознающие спирали или RVD) изменены (например, посредством селекции и/или рационального конструирования) для связывания заранее выбранного участка-мишени. Любые из белков цинковых пальцев, описанных в настоящем описании, могут включать 1, 2, 3, 4, 5, 6 или более цинковых пальцев, причем каждый цинковый палец имеет распознающую спираль, которая связывается с субучастком-мишенью с выбранной последовательностью(ями) (например, гене(ах)). В определенных вариантах осуществления ZFP-TF содержат ZFP, имеющий области распознающей спирали, как показано в единичном ряду таблицы 1. Аналогично, любые из белков TALE, описанных в настоящем описании, могут включать любое количество RVD TALE. В некоторых вариантах осуществления по меньшей мере один RVD обладает неспецифическим связыванием ДНК. В некоторых вариантах осуществления по меньшей мере одна распознающая спираль (или RVD) является не встречающейся в природе. В определенных вариантах осуществления TALE-TF содержит TALE, который связывается по меньшей мере с 12 парами оснований участка-мишени, как показано в таблице 1. CRISPR/Cas-TF включает единую гидовую РНК, которая связывается с последовательностью-мишенью. В определенных вариантах осуществления сконструированный фактор транскрипции связывается (например, через ДНК-связывающий домен ZFP, TALE или sg-РНК) с участком-мишенью из по меньшей мере 9-12 пар оснований в ассоциированном с заболеванием гене, например, участке-мишени, содержащем по меньшей мере 9-20 пар оснований (например, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более), включая непрерывные или не являющиеся непрерывными последовательности в этих участках-мишенях (например, участок-мишень, как показано в таблице 1). В определенных вариантах осуществления генетический модулятор включает ДНК-связывающую молекулу (ZFP, TALE, единая гидовая РНК), как описано в настоящем описании, функционально связанную с доменом репрессии транскрипции (с образованием генетического репрессора).
[0046] Таким образом, белки с цинковыми пальцами (ZFP), Cas-белок системы CRISPR/Cas или белки TALE, как описано в настоящем описании, могут находиться в функциональной связи с регуляторным доменом (или функциональным доменом) в качестве части слитой молекулы. Функциональный домен может представлять собой, например, домен активации транскрипции, домен подавления транскрипции и/или нуклеазный (осуществляющий расщепление) домен. Посредством выбора либо домена активации, либо домена подавления, для применения с ДНК-связывающей молекулой, такие молекулы могут использоваться либо для активации, либо для подавления экспрессии генов. В определенных вариантах осуществления функциональный или регуляторный домены могут играть роль в посттрансляционной модификации гистонов. В некоторых случаях домен представляет собой ацетилтрансферазу гистонов (HAT), деацетилазу гистонов (HDAC), метилазу гистонов или фермент, который осуществляет сумоилирование или биотинилирование гистона, или другой домен фермента, который обеспечивает регулируемое подавление генов посредством посттрансляционной модификации гистонов (Kousarides, (2007) Cell 128:693-705). В некоторых вариантах осуществления предусматривается молекула, содержащая ZFP, dCas или TALE, нацеленные на ген (например, C9orf72), как описано в настоящем описании, слитые с доменом репрессии транскрипции, которая может использоваться для подавления экспрессии гена. В некоторых вариантах осуществления способы и композиции по изобретению пригодны для лечения эукариот. В определенных вариантах осуществления активность регуляторного домена регулируется экзогенным низкомолекулярным соединением или лигандом, так что взаимодействие с аппаратом транскрипции клетки не происходит в отсутствии экзогенного лиганда. Такие внешние лиганды контролируют степень взаимодействия ZFP-TF, CRISPR/Cas-TF или TALE-TF с аппаратом транскрипции. Регуляторный домен(ы) может быть функционально связан с любым участком(ами) одного или нескольких ZFP, dCas или TALE, в том числе между одним или несколькими ZFP, dCas или TALE, снаружи от одного или нескольких ZFP, dCas или TALE, и в любой их комбинации. В предпочтительных вариантах осуществления регуляторный домен приводит к подавлению экспрессии гена-мишени (например, C9orf72). Любой из слитых белков, описанных в настоящем описании, может быть составлен в фармацевтическую композицию.
[0047] В некоторых вариантах осуществления искусственный регулятор связывается с промоторной областью выше (например, с 5’-стороны от) участка начала транскрипции (TSS) гена. В некоторых вариантах осуществления искусственный регулятор связывается с областью ниже TSS. В предпочтительных вариантах осуществления искусственный регулятор предпочтительно связывается с областью экспансии повторов в гене C9orf72. В некоторых вариантах осуществления связывание искусственного регулятора с геном C9orf72 подавляет экспрессию промотора в интроне 1a. В некоторых вариантах осуществления связывание искусственного регулятора с геном C9orf72 подавляет экспрессию промотора в интроне 1b. В некоторых вариантах осуществления связывание искусственного регулятора подавляет экспрессию с промотора 1a и антисмыслового промотора, но не подавляет промотор 1b. Также см. фиг.1B и 1C.
[0048] В некоторых вариантах осуществления способы и композиции по изобретению включают применение двух или более слитых молекул, как описано в настоящем описании, например двух или более модуляторов C9orf72 (искусственные факторы транскрипции). Две или более слитых молекулы могут связываться с различными участками-мишенями и содержать одинаковые или различные функциональные домены. Альтернативно две или более слитых молекулы, как описано в настоящем описании, могут связываться с одним и тем же участком-мишенью, но включать различные функциональные домены. В некоторых случаях используют три или более слитых молекул, в других случаях используют четыре или более слитых молекул, в то время как в следующих случаях используют 5 или более слитых молекул. В некоторых вариантах осуществления две или более, три или более, четыре или более, или пять или более слитых молекул (или их компонентов) доставляются в клетку в качестве нуклеиновых кислот. В предпочтительных вариантах осуществления слитые молекулы вызывают репрессию экспрессии гена-мишени. В некоторых вариантах осуществления две слитых молекулы вводят в дозах, где каждая молекула является активной сама по себе, однако в комбинации активность подавления является аддитивной. В некоторых вариантах осуществления две слитых молекулы вводят в дозах, где ни одна из них не является активной сама по себе, однако в комбинации активность подавления является синергичной.
[0049] В другом аспекте предусматривается полинуклеотид, кодирующий любой из ДНК-связывающих доменов, описанных в настоящем описании.
[0050] В некоторых вариантах осуществления полинуклеотид, кодирующий ДНК-связывающий белок, представляет собой мРНК. В некоторых аспектах мРНК может быть химически модифицированной (например, Kormann et al., (2011) Nature Biotechnology 29(2):154-7). В других аспектах мРНК может содержать ARCA-кэп (см. патенты США № 7074596 и 8153773). В следующих вариантах осуществления мРНК может содержать смесь немодифицированных и модифицированных нуклеотидов (см. публикацию патента США № 2012/0195936).
[0051] В другом аспекте предусматривается вектор для доставки генов, содержащий любой из полинуклеотидов (например, репрессоров), как описано в настоящем описании. В определенных вариантах осуществления вектор представляет собой аденовирусный вектор (например, вектор Ad5/F35), лентивирусный вектор (LV), включая компетентные в отношении интеграции или дефектные в отношении интеграции лентивирусные векторы, или вектор на основе аденоассоциированного вируса (AAV). В определенных вариантах осуществления вектор AAV представляет собой вектор AAV2, AAV6, AAV8 или AAV9 или псевдотипированный вектор на основе AAV, такой как AAV2/8, AAV2/5, AAV2/9 и AAV2/6. В некоторых вариантах осуществления вектор на основе AAV представляет собой вектор на основе AAV, способный проходить через гематоэнцефалический барьер (например, публикация патента США № 2015/0079038). В других вариантах осуществления AAV представляет собой молекулу самокомплементарного AAV (sc-AAV) или одноцепочечного (ss-AAV). Также в рамках настоящего изобретения предусматриваются аденовирусные (Ad) векторы, векторы на основе LV или аденоассоциированного вируса (AAV), содержащие последовательность, кодирующую по меньшей мере одну нуклеазу (ZFN или TALEN), и/или донорную последовательность для направленного встраивания в ген-мишень. В определенных вариантах осуществления вектор на основе Ad представляет собой химерный вектор на основе Ad, например вектор Ad5/F35. В определенных вариантах осуществления лентивирусный вектор представляет собой лентивирусный вектор с дефектом интегразы (IDLV) или компетентный в отношении интеграции лентивирусный вектор. В определенных вариантах осуществления вектор является псевдотипированным с оболочкой VSV-G или с другими оболочками.
[0052] Кроме того, также предусматриваются фармацевтические композиции, содержащие нуклеиновые кислоты, и/или слитые конструкции, такие как искусственные факторы транскрипции (например, ZFP, Cas или TALE или слитые молекулы, содержащие ZFP, Cas или TALE). Например, определенные композиции включают нуклеиновую кислоту, содержащую последовательность, которая кодирует одну из ZFP, Cas или TALE, описанных в настоящем описании, функционально связанную с регуляторной последовательностью, в комбинации с фармацевтически приемлемым носителем или разбавителем, где регуляторная последовательность позволяет экспрессию нуклеиновой кислоты в клетке. В определенных вариантах осуществления кодируемый ZFP, Cas, CRISPR/Cas или TALE модулирует аллель дикого типа и/или мутантный аллель. В некоторых вариантах осуществления мутантный аллель предпочтительно модулируется, например, подавляется, в большей степени, чем аллель дикого типа. В некоторых вариантах осуществления фармацевтические композиции содержат ZFP, CRISPR/Cas или TALE, которые предпочтительно модулируют мутантный аллель, и ZFP, CRISPR/Cas или TALE, которые модулируют нейротрофический фактор. Композиции на основе белка включают один или несколько ZFP, CRISPR/Cas или TALE, как описано в настоящем описании, и фармацевтически приемлемый носитель или разбавитель.
[0053] В другом аспекте также предусматривается выделенная клетка, содержащая любой из белков, слитых молекул, полинуклеотидов и/или композиций, как описано в настоящем описании. Выделенная клетка может использоваться в нетерапевтических применениях, таких как предоставление клеточных моделей или моделей на животных для диагностических и/или скрининговых способов, и/или для терапевтических применений, таких как клеточная терапия ex vivo.
[0054] В другом аспекте также предусматриваются фармацевтические композиции, содержащие один или несколько генетических модуляторов, один или несколько полинуклеотидов (например, носителей для доставки генов) и/или одну или несколько (например, популяцию) выделенных клеток, как описано в настоящем описании. В определенных вариантах осуществления фармацевтическая композиция содержит два или более генетических модуляторов. Например, определенные композиции включают нуклеиновую кислоту, содержащую последовательность, которая кодирует один или несколько генетических модуляторов одного из генов, ассоциированных с редким заболеванием (например, C9orf72), как описано в настоящем описании. В определенных вариантах осуществления генетический модулятор(ы) (например, содержащий ZFP, Cas или TALE, описанные в настоящем описании) функционально связан с регуляторной последовательностью, в комбинации с фармацевтически приемлемым носителем или разбавителем, где регуляторная последовательность позволяет экспрессию нуклеиновой кислоты в клетке. В определенных вариантах осуществления кодируемые ZFP, CRISPR/Cas или TALE являются специфичными к мутантному аллелю или аллелю дикого типа (например, C9orf72). В некоторых вариантах осуществления фармацевтические композиции содержат ZFP-TF, CRISPR/Cas-TF или TALE-TF, которые модулируют мутантный аллель и/или аллель дикого типа (например, C9orf72), включая TF, которые предпочтительно модулируют (например, подавляют на большем уровне) мутантный аллель по сравнению с аллелем дикого типа. Композиции на основе белка включают один или несколько генетических модуляторов, как описано в настоящем описании, и фармацевтически приемлемый носитель или разбавитель. В определенных вариантах осуществления используются композиции, содержащие два или более генетических модуляторов (находящихся на одном и том же или различающихся типах векторов, например, на векторах AAV), необязательно где один из генетических модуляторов содержит репрессор ZFP-TF, содержащий ZFP, обозначаемый как 74949, 74978, 75027 или 75109.
[0055] Изобретение также относится к способам и применениям для подавления экспрессии генов у индивидуума, нуждающегося в этом (например, индивидуум с редким заболеванием, как описано в настоящем описании), путем предоставления индивидууму одного или нескольких полинуклеотидов, одного или нескольких носителей для доставки генов и/или фармацевтической композиции, как описано в настоящем описании. В определенных вариантах осуществления композиции, описанные в настоящем описании, используются для подавления экспрессии мутантного C9orf72 у индивидуума, в том числе для лечения и/или предупреждения ALS или FTD. Композиции, описанные в настоящем описании, подавляют экспрессию генов на протяжении длительных периодов времени (4 недели, 3 месяца, от 6 месяцев до года или более) в головном мозге (включая, но не ограничиваясь ими фронтальную долю коры, включая, но не ограничиваясь ими, префронтальную кору, теменную долю коры, затылочную долю коры, височную долю коры, включая, но не ограничиваясь ими, энторинальную кору, гиппокамп, ствол головного мозга, полосатое тело, таламус, средний мозг, мозжечок) и спинной мозг (включая, но не ограничиваясь ими, поясничный, грудной и шейный отделы). Композиции, описанные в настоящем описании, также могут быть предоставлены индивидууму посредством любого пути введения, включая, но не ограничиваясь ими, интрацеребровентрикулярное, интратекальное, внутричерепное, внутривенное, орбитальное (ретроорбитальное (RO)), интраназальное и/или интрацистернальное введение. Также предусматриваются наборы, содержащие одну или несколько композиций (например, генетические модуляторы, полинуклеотиды, фармацевтические композиции и/или клетки), как описано в настоящем описании, а также инструкции по применению этих композиций.
[0056] В другом аспекте в рамках настоящего изобретения предусматриваются способы лечения и/или предупреждения заболеваний ЦНС (например, ALS и/или FTD) с использованием способов и композиций, описанных в настоящем описании. В некоторых вариантах осуществления способы вовлекают композиции, где полинуклеотиды и/или белки могут быть доставлены с использованием вирусного вектора, невирусного вектора (например, плазмида) и/или их комбинаций. В некоторых вариантах осуществления способы вовлекают композиции, содержащие популяции стволовых клеток, содержащих искусственный фактор транскрипции (например, ZFP-TF, TALE-TF или dCas-TF). Введение композиций, как описано в настоящем описании (белки, полинуклеотиды, клетки и/или фармацевтические композиции, содержащие эти белки, полинуклеотиды и/или клетки), приводит к терапевтическому (клиническому) эффекту, включая, но не ограничиваясь ими, смягчение или устранение любого из клинических симптомов, ассоциированных с ALS и/или FTD, а также усиление функции и/или увеличение количества клеток ЦНС (например, нейроны, астроциты, миелин и т.д.). В определенных вариантах осуществления композиции и способы, описанные в настоящем описании, снижают экспрессию смысловых и/или антисмысловых транскриптов гена-мишени (например, C9orf72) по сравнению с контролями без введения искусственных репрессоров, как описано в настоящем описании, по меньшей мере на 30% или 40%, например, по меньшей мере на 50%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90%, по меньшей мере на 95% или более чем на 95%. В некоторых вариантах осуществления достигают снижения по меньшей мере на 50%. В определенных вариантах осуществления искусственный репрессор предпочтительно подавляет мутантный аллель (например, аллель с экспансией) по сравнению с аллелем дикого типа, например, по меньшей мере на 20% (например, подавляет аллель дикого типа не более чем на 50% и мутантный аллель по меньшей мере на 70%). В некоторых вариантах осуществления репрессор предпочтительно подавляет смысловой транскрипт мутантного аллеля, в то время как в других вариантах осуществления репрессор предпочтительно подавляет антисмысловой транскрипт мутантного аллеля. В некоторых вариантах осуществления репрессор подавляет смысловой и антисмысловой транскрипты мутантного аллеля.
[0057] В следующем аспекте в настоящем описании описан способ доставки репрессора гена в головной мозг индивидуума с использованием вирусного или невирусного вектора. В определенных вариантах осуществления вирусный вектор представляет собой вектор на основе AAV9. Доставка может быть осуществлена в любую область головного мозга, например, гиппокамп или энторинальную кору, любым подходящим способом, в том числе с использованием канюли. Любой вектор на основе AAV, который обеспечивает обширную доставку генетического модулятора (например, репрессора) в головной мозг индивидуума, в том числе посредством антероградного и ретроградного аксонального транспорта в области головного мозга, в которые вектор прямо не вводился (например, доставка в скорлупу приводит к доставке в другие структуры, такие как кора, черное вещество, таламус и т.д.). В определенных вариантах осуществления индивидуумом является человек и в других вариантах осуществления индивидуумом является не являющийся человеком примат. Введение может быть осуществлено в однократной дозе или посредством серии доз, вводимых за один раз или посредством многократного введения (с любыми интервалами между введениями).
[0058] Таким образом, в других аспектах в рамках настоящего изобретения описан способ предупреждения и/или лечения заболевания (например, ALS и/или FTD) у индивидуума, причем способ включает введение репрессора гена индивидууму с использованием AAV. В определенных вариантах осуществления репрессор вводят в ЦНС (например, гиппокамп и/или энторинальную кору) или ПНС (например, спинной мозг/спинномозговую жидкость) индивидуума. В других вариантах осуществления репрессор вводят внутривенно. В определенных вариантах осуществления в настоящем описании описан способ предупреждения и/или лечения ALS или FTD у индивидуума, причем способ включает введение репрессора аллеля C9orf72 (дикого типа и/или мутантного) индивидууму с использованием одного или нескольких векторов AAV. В определенных вариантах осуществления AAV, кодирующий генетический модулятор, вводят в ЦНС (головной мозг и/или CSF) посредством любого способа доставки, включая, но не ограничиваясь ими, интрацеребровентрикулярную, интратекальную, внутричерепную, внутривенную, интраназальную, ретроорбитальную или интрацистернальную доставку. В других вариантах осуществления AAV, кодирующий репрессор, вводят непосредственно в паренхиму (например, гиппокамп и/или энторинальную кору) индивидуума. В других вариантах осуществления AAV, кодирующий репрессор, вводят внутривенно (в/в). В любом из способов, описанных в настоящем описании, введение может проводиться один раз (однократное введение) или может проводиться множество раз (с любым периодом времени между введениями) в одинаковых или различных дозах на каждое введение. При введении многократно могут использоваться одинаковые или различные дозировки и/или носители для доставки или пути введения (например, различные векторы AAV, вводимые в/в и/или ICV). Способы включают способы уменьшения снижения мышечной функции, снижения физической координации, скованности мышц, мышечных спазмов, потери речевой функции, затрудненного глотания, когнитивного нарушения, способы уменьшения снижения двигательной функции и/или способы уменьшения снижения одной или нескольких когнитивных функций у индивидуумов с ALS, во всех случаях по сравнению с индивидуумом, у которого способ не проводят, или по сравнению с тем же индивидуумом до проведения способов. Таким образом, способы, описанные в настоящем описании, приводят к снижению биомаркеров и/или симптомов редких заболеваний, таких как ALS или FTD, включая одно или несколько следующих: снижение мышечной функции, ухудшение физической координации, скованность мышц, мышечные спазмы, снижение речевых функций, затрудненность глотания, когнитивное нарушение, изменения химического состава крови и/или цереброспинальной жидкости, ассоциированные с ALS, включая уровни G-CSF, IL-2, IL-15, IL-17, MCP-1, MIP-1α, TNF-α и VEGF (см. Chen et al., Front Immunol. (2018) 9:2122) и/или другие биомаркеры, известные в данной области. В определенных вариантах осуществления способы, кроме того, могут включать введение одного или нескольких генетических репрессоров тау (MAPT), например, у индивидуумов с FTD. См., например, публикацию патента США № 2018/0153921.
[0059] В любом из способов, описанных в настоящем описании, репрессор аллеля-мишени может представлять собой ZFP-TF, например, слитый белок, содержащий ZFP, который специфически связывается с аллелем и доменом репрессии транскрипции (например, KOX, KRAB и т.д.). В других вариантах осуществления репрессор аллеля-мишени может представлять собой TALE-TF, например, слитый белок, содержащий полипептид TALE, который специфически связывается с аллелем гена, и домен подавления транскрипции (например, KOX, KRAB и т.д.). В некоторых вариантах осуществления репрессор аллеля-мишени представляет собой CRISPR/Cas-TF, где нуклеазные домены в белке Cas инактивированы таким образом, чтобы белок более не расщеплял ДНК. Полученный ДНК-связывающий домен РНК-направляемого Cas подвергают слиянию с репрессором транскрипции (например, KOX, KRAB и т.д.) для подавления аллеля-мишени. В некоторых вариантах осуществления сконструированный фактор транскрипции способен подавлять экспрессию мутантного аллеля, но не аллеля дикого типа. В следующих вариантах осуществления ДНК-связывающая молекула предпочтительно распознает экспансию гексамера GGGGCC (SEQ ID NO:1).
[0060] В некоторых вариантах осуществления последовательность, кодирующая генетический репрессор, как описано в настоящем описании (например, ZFP-TF, TALE-TF или CRISPR/Cas-TF) встраивается (интегрируется) в геном, в то время как в других вариантах осуществления последовательность, кодирующая репрессор, поддерживается эписомно. В некоторых случаях нуклеиновая кислота, кодирующая слитую конструкцию TF, встраивается (например, посредством опосредуемой нуклеазой интеграции) в участок "безопасной гавани", содержащий промотор, так что эндогенный промотор запускает экспрессию. В других вариантах осуществления донорная последовательность репрессора (TF) встраивается (посредством опосредуемой нуклеазой интеграции) в участок "безопасной гавани", и донорная последовательность содержит промотор, который запускает экспрессию репрессора. В некоторых вариантах осуществления промоторная последовательность экспрессируется широко, в то время как в других вариантах осуществления промотор является тканеспецифическим или специфическим для типа клеток. В предпочтительных вариантах осуществления промоторная последовательность является специфической для нейрональных клеток. В других вариантах осуществления промоторная последовательность является специфической для мышечных клеток. В некоторых вариантах осуществления выбранный промотор характеризуется тем, что он имеет низкую экспрессию. Неограничивающие примеры пригодных промоторов включают специфические для нейронов промоторы NSE, синапсина, CAMKiia и MECP. Неограничивающие примеры промоторов с повсеместной экспрессией включают CMV, CAG и Ubc. Следующие варианты осуществления включают применение саморегулирующихся промоторов, как описано в публикации патента США № 2015/0267205. Следующие варианты осуществления включают применение саморегулирующихся промоторов, как описано в публикации патента США № 2015/0267205.
[0061] В любом из способов, описанных в настоящем описании, способ может обеспечивать подавление на приблизительно 50% или более, 55% или более, 60% или более, 65% или более, приблизительно 70% или более, приблизительно 75% или более, приблизительно 85% или более, приблизительно 90% или более, приблизительно 92% или более, или приблизительно 95% или, на 98% или более, или 99% или более аллелей-мишеней (например, мутантный C9orf72 или C9orf72 дикого типа) в одном или нескольких нейронах индивидуума (например, индивидуума с ALS). В определенных вариантах осуществления подавление экспрессии аллеля дикого типа у индивидуума происходит не более чем на 50% (по сравнению с индивидуумами без введения) в то время как подавление мутантного аллеля у индивидуума происходит по меньшей мере на 70% (70% или любая более высокая величина) (по сравнению с индивидуумами без введения). В некоторых вариантах осуществления происходит подавление экспрессии антисмыслового промотора по меньшей мере на 70%. В определенных вариантах осуществления экспрессия антисмысловых промоторов, присутствующих в области интрона 1a, 1b и/или 1c C9orf72 подавляется по меньшей мере на 70%, в то время как экспрессия смыслового промотора в области интрона 1b C9orf72 подавляется не более чем на 50%.
[0062] В любом из способов, описанных в настоящем описании, регулятор (например, репрессор или активатор) может быть доставлен индивидууму в качестве белка, полинуклеотида или любой комбинации белка и полинуклеотида. В определенных вариантах осуществления один или несколько репрессоров доставляют с использованием вектора на основе AAV. В других вариантах осуществления по меньшей мере один компонент регулятора (например, sg-РНК системы CRISPR/Cas) доставляют в форме РНК. В других вариантах осуществления регулятор(ы) доставляют с использованием комбинации любых из экспрессирующих конструкций, описанных в настоящем описании, например, одного репрессора (или его части) на одной экспрессирующей конструкции (AAV9) и одного репрессора (или его части) на отдельной экспрессирующей конструкции (AAV или другая вирусная или невирусная конструкция).
[0063] Более того, в любых из способов, описанных в настоящем описании, регулятор (например, репрессор) может быть доставлен в клетку (ex vivo или in vivo) в любой концентрации (дозе), которая обеспечивает желаемый эффект. В некоторых вариантах осуществления регулятор доставляют с использованием вектора на основе аденоассоциированного вируса (AAV) в количестве 10000-500000 векторных геномов/клетка (или любая величина между ними). В определенных вариантах осуществления регулятор доставляют с использованием лентивирусного вектора с MOI от 250 до 1000 (или любая величина между ними). В других вариантах осуществления регулятор доставляют с использованием плазмидного вектора в количестве 0,01-1000 нг/100000 клеток (или любая величина между ними). В других вариантах осуществления репрессор доставляют в качестве мРНК в количестве 150-1500 нг/100000 клеток (или любая величина между ними). Более того, для применений in vivo в любых из способов, описанных в настоящем описании, генетический модулятор(ы) (например, репрессоры) может быть доставлен в любой концентрации (дозе), которая обеспечивает желаемый эффект у индивидуума, нуждающегося в этом. В некоторых вариантах осуществления репрессор доставляют с использованием вектора на основе аденоассоциированного вируса (AAV) в количестве 10000-500000 векторных геномов/клетка (или любая величина между ними). В определенных вариантах осуществления репрессор доставляют с использованием лентивирусного вектора с MOI от 250 до 1000 (или любая величина между ними). В других вариантах осуществления репрессор доставляют с использованием плазмидного вектора в количестве 0,01-1000 нг/100000 клеток (или любая величина между ними). В других вариантах осуществления репрессор доставляют в качестве мРНК в количестве 0,01-3000 нг/количество клеток (например, 50000-200000 (например, 100000) клеток) (или любая величина между ними). В других вариантах осуществления репрессор доставляют с использованием вектора на основе аденоассоциированного вируса (AAV) в фиксированном объеме 1-300 мкл в паренхиму головного мозга в количестве 1E11-1E14 вг/мл. В других вариантах осуществления репрессор доставляют с использованием вектора на основе аденоассоциированного вируса (AAV) в фиксированном объеме 0,5-10 мл в CSF в количестве 1E11-1E14 вг/мл.
[0064] В любом из способов, описанных в настоящем описании, способ может обеспечивать модулирование (например, подавление) приблизительно на 50% или более, 55% или более, 60% или более, 65% или более, приблизительно 70% или более, приблизительно 75% или более, приблизительно 85% или более, приблизительно 90% или более, приблизительно 92% или более, или приблизительно 95% или более аллеля(ей)-мишени в одной или нескольких клетках индивидуума. В некоторых вариантах осуществления аллели дикого типа и мутантные аллели модулируются по-разному, например, мутантный аллель предпочтительно модифицируется по сравнению с аллелем дикого типа (например, мутантный аллель подавляется по меньшей мере на 70% и аллель дикого типа подавляется более чем на 50%).
[0065] В любом из способов, описанных в настоящем описании, способ может обеспечивать модулирование (например, репрессию) на приблизительно 50% или более, 55% или более, 60% или более, 65% или более, приблизительно 70% или более, приблизительно 75% или более, приблизительно 85% или более, приблизительно 90% или более, приблизительно 92% или более, или приблизительно 95% или более антисмысловой экспрессии аллеля(ей)-мишени в одной или нескольких клетках индивидуума. В некоторых вариантах осуществления смысловая экспрессия и антисмысловая экспрессия в мутантных аллелях модулируются по-разному, например, предпочтительно модулируется экспрессия антисмысловых транскриптов по сравнению с экспрессией смысловых транскриптов в мутантном аллеле (например, антисмысловая экспрессия подавляется на по меньшей мере 70% и смысловая экспрессия подавляется не более чем на 50%).
[0066] В следующих аспектах факторы транскрипции, как описано в настоящем описании, такие как факторы транскрипции, содержащие один или несколько белков с цинковыми пальцами (ZFP-TF), TALE (TALE-TF) и CRISPR/Cas-TF, например, ZFP-TF, TALE-TF или CRISPR/Cas-TF, используют для подавления экспрессии мутантного аллеля и/или аллеля дикого типа (например, C9orf72) в головном мозге (например, нейроне) индивидуума. Подавление может составлять приблизительно 50% или более, 55% или более, 60% или более, 65% или более, 70% или более, приблизительно 75% или более, приблизительно 85% или более, приблизительно 90% или более, приблизительно 92% или более, или приблизительно 95% или более в отношении аллелей-мишеней в одной или нескольких клетках индивидуума по сравнению с клетками индивидуума без введения (дикого типа). В определенных вариантах осуществления подавление аллеля дикого типа составляет не более 50% (по сравнению с клетками или индивидуумами без введения) и подавление мутанта (связанный с заболеванием вариант или изоформа) составляет по меньшей мере 70% (по сравнению с клетками или индивидуумами без введения). В определенных вариантах осуществления антисмысловая транскрипция подавляется абсолютно (полностью). В определенных вариантах осуществления подавление смыслового транскрипта составляет не более 50% (по сравнению с клетками или индивидуумами без введения) и подавление антисмыслового транскрипта составляет по меньшей мере 70% (по сравнению с клетками или индивидуумами без введения). В определенных вариантах осуществления для осуществления одного или нескольких способов, описанных в настоящем описании, может использоваться фактор транскрипции с направленным модулированием.
[0067] Таким образом, в настоящем описании описаны способы и композиции для модулирования экспрессии генов, ассоциированных с редкими нарушениями, описанными в настоящем описании, включая подавление с экспрессией экзогенной последовательностью (такой как искусственный TF) или без нее. Композиции и способы могут быть предназначены для применения in vitro (например, для предоставления клеток для исследования гена-мишени посредством его модулирования; для разработки лекарственных средств и/или для получения трансгенных животных или моделей на животных), in vivo или ex vivo, и они включают введение искусственного фактора транскрипции или нуклеазы, которые включают ДНК-связывающую молекулу, направленную на ген, ассоциированный с редким заболеванием, необязательно в случае нуклеазы с донором, который интегрируется в ген после расщепления нуклеазой. В некоторых вариантах осуществления донорный ген (трансген) поддерживается в клетке внехромосомно. В определенных вариантах осуществления клетка находится у пациента с заболеванием. В других вариантах осуществления клетку модифицируют любым из способов, описанных в настоящем описании, и модифицированную клетку вводят индивидууму, нуждающемуся в этом (например, индивидуум с редким заболеванием). Также предусматриваются генно-модифицированные клетки (например, стволовые клетки, клетки-предшественники, T-клетки, мышечные клетки и т.д.), содержащие генно-модифицированный ген (например, экзогенную последовательность), включая клетки, полученные способами, описанными в настоящем описании. Эти клетки могут использоваться для предоставления терапевтического белка(ов) индивидууму с редким заболеванием, например, путем введения клетки(ок) индивидууму, нуждающемуся в этом, или альтернативно путем выделения белка, продуцированного клеткой, и введения белка индивидууму, нуждающемуся в этом (фермент-заместительная терапия).
[0068] Также предусматривается набор, содержащий один или несколько из генетических модуляторов (например, репрессоров) и/или полинуклеотидов, содержащих компоненты модуляторов мишени и/или кодирующих модуляторы мишени (или их компоненты), как описано в настоящем описании. Кроме того, наборы могут содержать клетки (например, нейроны или мышечные клетки), реагенты (например, для детекции и/или количественного определения белка, например, в CSF) и/или инструкции по применения, включая способы, как описано в настоящем описании.
[0069] Способы и композиции по настоящему изобретению дополнительно подробно описаны ниже.
I. Факторы транскрипции на основе белков с цинковыми пальцами
[0070] ZFP-TF по настоящему изобретению представляют собой слитые белки, содержащие ДНК-связывающий домен белка с цинковыми пальцами (ZFP) и домен репрессора транскрипции, где два домена могут быть ассоциированы друг с другом посредством прямой пептидильной связи или пептидного линкера, или посредством димеризации (например, посредством лейциновой молнии, N-концевого домена STAT-белка или связывающего белка FK506). Как используют в рамках изобретения, "слитый белок" относится к полипептиду с ковалентно связанными доменами, а также к комплексу полипептидов, связанных друг с другом посредством нековалентных связей. Домен репрессора транскрипции может быть ассоциирован с доменом ZFP в любом подходящем положении, включая C- или N-конец домена ZFP.
[0071] В некоторых вариантах осуществления ZFP-TF по настоящему изобретению подавляют транскрипцию мутантного гена C9orf72 человека на 45% или более (например, на 50%, 60%, 70%, 80%, 90% или 95% или более). В некоторых вариантах осуществления у пациента одновременно применяют два или более из ZFP-TF по настоящему изобретению, где ZFP-TF связывают различные мотивы ДНК в смысловой и/или антисмысловой цепях области C9orf72 с экспансией, для достижения оптимальной репрессии транскрипции мутанта C9orf72.
A. Мишени доменов ZFP
[0072] Домены ZFP слитых белков по настоящему изобретению предпочтительно связываются с областью экспансии в мутантном аллеле гена C9orf72 человека. Ген C9orf72 человека находится на коротком (p) плече хромосомы 9 в положении 21.2 (9p21.2). Он охватывает пары оснований с 27546546 по 27573866 на хромосоме. Геномная структура C9orf72 человека представлена на фиг.1A. ДНК-связывающий домен ZFP в ZFP-TF направляет слитый белок на область экспансии повторов мутантного гена C9orf72 и доставляет домен репрессора транскрипции слитого белка к области-мишени. Затем домен репрессора подавляет транскрипцию гена C9orf72 посредством РНК-полимеразы.
[0073] В некоторых вариантах осуществления последовательность-мишень в области экспансии имеет длину по меньшей мере 8 п.о. Например, последовательность-мишень может иметь длину от 8 п.о. до 40 п.о., например, длину 12, 15, 16, 17, 18, 19, 20, 21, 24, 27, 30, 33 или 36 п.о. В определенных вариантах осуществления последовательность-мишень ZFP-TF по настоящему изобретению имеет длину 12-20 (например, 12-18, 15-19, 15, 18 или 19) п.о. В некоторых вариантах осуществления последовательность-мишень содержит подпоследовательности, которые не являются соседними.
[0074] Повторы G4C2 дают начало следующим гексануклеотидным мотивам ДНК в смысловой и антисмысловой цепях гена:
Мотивы в смысловой цепи C9orf72:
(i) GGGGCC (SEQ ID NO:1)
(ii) GGGCCG (SEQ ID NO:2)
(iii) GGCCGG (SEQ ID NO:3)
(iv) GCCGGG (SEQ ID NO:4)
(v) CCGGGG (SEQ ID NO:5)
(vi) CGGGGC (SEQ ID NO:6)
Мотивы в антисмысловой цепи C9orf72:
(vii) GGCCCC (SEQ ID NO:7)
(viii) GCCCCG (SEQ ID NO:8)
(ix) CCCCGG (SEQ ID NO:9)
(x) CCCGGC (SEQ ID NO:10)
(xi) CCGGCC (SEQ ID NO:11)
(xii) CGGCCC (SEQ ID NO:12)
В некоторых вариантах осуществления последовательность-мишень ZFP-TF по настоящему изобретению содержит один или несколько (например, 2, 3 или 4) тандемных повторов этих мотивов ДНК. В некоторых вариантах осуществления последовательность-мишень состоит из трех тандемных повторов одного из мотивов. В некоторых вариантах осуществления последовательность-мишень содержит один или несколько (например, 2 или 3) тандемных повторов мотива плюс несколько (например, 1, 2, 3, 4 или 5) нуклеотидов из вышележащей и/или нижележащей соседней последовательности (например, CC(G4C2)2GG) (SEQ ID NO:75).
[0075] Последовательность-мишень может находиться на смысловой цепи гена или антисмысловой цепи гена. В определенных вариантах осуществления ZFP-TF, используемые у пациента, связывают как смысловую, так и антисмысловую цепи мутантного аллеля. Чтобы гарантировать точность нацеливания и снизить неспецифическое связывание ZFP-TF, последовательность выбранной области-мишени C9orf72 предпочтительно обладает гомологией менее 75% (например, менее 70%, менее 65%, менее 60% или менее 50%) с последовательностями других генов в геноме.
[0076] Другие критерии для дальнейшей оценки сегментов мишени включают предшествующую доступность ZFP, связывающихся с такими сегментами или родственными сегментами, простоту конструирования новых ZFP для связывания данного сегмента-мишени, и риск неспецифического связывания.
B. Домены белков с цинковыми пальцами
[0077]"Белок с цинковыми пальцами" или "ZFP" относится к белку, имеющему ДНК-связывающие домены, которые стабилизированы цинком. ZFP связываются с ДНК последовательность-специфическим образом. Индивидуальные ДНК-связывающие домены называют "пальцами". ZFP имеет по меньшей мере один палец, причем каждый палец связывает от двух до четырех пар оснований ДНК, как правило, три или четыре пары оснований ДНК. Каждый цинковый палец, как правило, содержит приблизительно 30 аминокислот и хелатирует цинк. Сконструированная ZFP может иметь новую специфичность связывания по сравнению со встречающимся в природе белком с цинковыми пальцами. Способы конструирования включают, но не ограничиваются ими, рациональное конструирование и различные типы селекции. Рациональное конструирование включает, например, использование баз данных, содержащих триплетные (или квадруплетные) нуклеотидные последовательности и аминокислотные последовательности индивидуальных цинковых пальцев, где каждая триплетная или квадруплетная нуклеотидная последовательность ассоциирована с одной или несколькими аминокислотными последовательностями цинковых пальцев, которые связывают конкретную триплетную или квадруплетную последовательность. См., например, способы конструирования ZFP, подробно описанные в патентах США 5789538; 5925523; 6007988; 6013453; 6140081; 6200759; 6453242; 6534261; 6979539; 8586526; 8841260; 8956828 и 9234016; и международных публикациях патентов WO 95/19431; WO 96/06166; WO 98/53057; WO 98/53058; WO 98/53059; WO 98/53060; WO 98/54311; WO 00/27878; WO 01/60970; WO 01/88197; WO 02/016536; WO 02/099084 и WO 03/016496.
[0078] Домен ZFP в ZFP-TF по настоящему изобретению может включать по меньшей мере три (например, четыре, пять, шесть, семь, восемь, девять, десять, одиннадцать, двенадцать, тринадцать или более) цинковых пальцев. Домен ZFP, имеющий три пальца, как правило, распознает участок-мишень, который включает от 9 до 12 нуклеотидов. Домен ZFP, имеющий четыре пальца, как правило, распознает участок-мишень, который включает от 12 до 15 нуклеотидов. Домен ZFP, имеющий пять пальцев, как правило, распознает участок-мишень, который включает от 15 до 18 нуклеотидов. Домен ZFP, имеющий шесть пальцев, может распознавать участки-мишени, которые включают от 18 до 21 нуклеотида.
[0079] Специфичность домена ZFP к мишени может быть увеличена посредством мутаций остова ZFP, как описано, например, в публикации патента США 2018/0087072. Мутации включают мутации, внесенные в остатки в остове ZFP, которые могут неспецифически взаимодействовать с фосфатами на ДНК-остове, но не вовлечены в специфичность к нуклеотидным мишеням. В некоторых вариантах осуществления эти мутации включают мутацию катионного аминокислотного остатка на нейтральный или анионный аминокислотный остаток. В некоторых вариантах осуществления эти мутации включают мутацию полярного аминокислотного остатка на нейтральный или неполярный аминокислотный остаток. В следующих вариантах осуществления мутации вносят в положениях (-5), (-9) и/или (-14) относительно ДНК-связывающей спирали. В некоторых вариантах осуществления цинковый палец может содержать одну или несколько мутаций в положениях (-5), (-9) и/или (-14). В следующих вариантах осуществления один или несколько цинковых пальцев в домене ZFP с множеством пальцев может содержать мутации в положениях (-5), (-9) и/или (-14). В некоторых вариантах осуществления в аминокислоты в положениях (-5), (-9) и/или (-14) (например, аргинин (R) или лизин (K)) заменяют на аланин (A), лейцин (L), Ser (S), Asp (N), Glu (E), Tyr (Y) и/или глутамин (Q). В некоторых вариантах осуществления остаток R в положении (-5) заменяют на Q.
[0080] Альтернативно ДНК-связывающий домен может происходить из нуклеазы. Например, известны последовательности распознавания для хоминг-эндонуклеаз и мегануклеаз, таких как I-SceI, I-CeuI, PI-PspI, PI-Sce, I-SceIV, I-CsmI, I-PanI, I-SceII, I-PpoI, I-SceIII, I-CreI, I-TevI, I-TevII и I-TevIII. Также см. патенты США 5420032 и 6833252; Belfort et al., Nucleic Acids Res. (1997) 25:3379-88; Dujon et al., Gene (1989) 82:115-8; Perler et al., Nucleic Acids Res. (1994) 22:1125-7; Jasin, Trends Genet. (1996) 12:224-8; Gimble et al., J Mol Biol. (1996) 263:163-80; Argast et al., J Mol Biol. (1998) 280:345-53; и New England Biolabs catalogue.
[0081] В некоторых вариантах осуществления ZFP-TF по настоящему изобретению содержат один или несколько доменов цинковых пальцев. Домены могут быть связаны посредством расширяемого гибкого линкера, так чтобы, например, один домен содержал один или несколько (например, 4, 5 или 6) цинковых пальцев, а другой домен содержал дополнительные один или несколько (например, 4, 5 или 6) цинковых пальцев. В некоторых вариантах осуществления линкер представляет собой стандартный линкер между пальцами, так что набор пальцев содержит один ДНК-связывающий домен, содержащий 8, 9, 10, 11 или 12 или более пальцев. В других вариантах осуществления линкер представляет собой нетипичный линкер, такой как гибкий линкер. Например, два домена ZFP могут быть связаны с репрессором транскрипции TF в конфигурации (от N-конца к C-концу) ZFP-ZFP-TF, TF-ZFP-ZFP, ZFP-TF-ZFP или ZFP-TF-ZFP-TF (два слитых белка ZFP-TF слиты через линкер).
[0082] В некоторых вариантах осуществления ZFP-TF являются "двуручными", т.е. они содержат два кластера цинковых пальцев (два домена ZFP), разделенных промежуточными аминокислотами, так что два домена ZFP связываются с двумя прерывающимися участками-мишенями. Примером связывающего белка с цинковыми пальцами двуручного типа является SIP1, где кластер из четырех цинковых пальцев находится на N-конце белка, и кластер из трех пальцев находится на С-конце (см. Remacle et al., EMBO J. (1999) 18(18):5073-84). Каждый кластер цинковых пальцев в этих белках способен связываться с уникальной последовательность-мишенью, и пространство между двумя последовательностями-мишенями может включать множество нуклеотидов.
[0083] В альтернативных вариантах осуществления вместо ZFP-TF можно использовать белки, которые сходны с ZFP-TF по функции. Например, вместо доменов ZFP слитые белки репрессоров транскрипции могут включать ДНК-связывающий домен, происходящий из ДНК-связывающего домена подобных активаторам транскрипции эффекторов (TALE). См., например, патенты США 8586526 и 9458205; публикации патентов США 2013/0196373 и 2013/0253040; WO 2010/079430; Schornack et al., J Plant Physiol (2006) 163(3):256-72); Kay et al., Science (2007) 318:648-51; Moscou and Bogdanove, Science (2009) 326:1501; и Boch et al., Science (2009) 326:1509-12. В другом примере белки репрессоров транскрипции могут включать ДНК-связывающий домен, который представляет собой единую гидовую РНК системы CRISPR/Cas. См., например, публикацию патента США 2015/0056705; Jinek et al., Science (2012) 337:816; Ramalingam et al., Genome Biol. (2013) 14:107; Hwang et al., (2013) Nature Biotechnology 31(3):227.
C. Домены репрессоров транскрипции
[0084] ZFP-TF по настоящему изобретению содержат один или несколько доменов репрессоров транскрипции, которые снижают активность транскрипции мутантного аллеля C9orf72. Неограничивающие примеры доменов репрессоров транскрипции представляют собой домен KRAB KOX1, KAP-1, MAD, FKHR, EGR-1, ERD, SID, TGF-бета индуцируемого раннего гена (TIEG), v-ERB-A, MBD2, MBD3, представителей семейства DNMT (например, DNMT1, DNMT3A, DNMT3B), Rb и MeCP2. См., например, Bird et al., Cell (1999) 99:451-54; Tyler et al., Cell (1999) 99:443-46; Knoepfler et al., Cell (1999) 99:447-50; и Robertson et al., Nature Genet. (2000) 25:338-42. Дополнительные иллюстративные домены репрессии включают, но не ограничиваются ими, ROM2 и AtHD2A. См., например, Chem et al., Plant Cell (1996) 8:305-21; и Wu et al., Plant J. (2000) 22:19-27.
[0085] В некоторых вариантах осуществления домен репрессора транскрипции включает последовательность из домена Kruppel-ассоциированного бокса (KRAB) белка с цинковыми пальцами человека 10/KOX1 (ZNF10/KOX1) (например, GenBank No. NM_015394.4). Иллюстративная последовательность домена KRAB представляет собой:
DAKSLTAWSR TLVTFKDVFV DFTREEWKLL DTAQQIVYRN VMLENYKNLV SLGYQLTKPD VILRLEKGEE PWLVEREIHQ ETHPDSETAF EIKSSV
(SEQ ID NO:13)
[0086] Также могут использоваться варианты этой последовательности KRAB при условии, что они имеют ту же или сходную функцию репрессора транскрипции.
D. Пептидные линкеры
[0087] Домен ZFP и домен репрессора транскрипции ZFP-TF по настоящему изобретению и/или цинковые пальцы в доменах ZFP могут быть связаны через пептидный линкер, например, не расщепляющийся пептидный линкер приблизительно из 5-200 аминокислот (например, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20 или более аминокислот). Некоторые предпочтительные линкеры представляют собой гибкие аминокислотные последовательности, которые синтезированы в качестве рекомбинантного слитого белка. См., например, описание выше и патенты США 6479626; 6903185; 7153949; 8772453; и 9163245; и WO 2011/139349. Белки, описанные в настоящем описании, могут включать любую комбинацию подходящих линкеров. Неограничивающими примерами линкеров являются DGGGS (SEQ ID NO:14), TGEKP (SEQ ID NO:15), LRQKDGERP (SEQ ID NO:16), GGRR (SEQ ID NO:17), GGRRGGGS (SEQ ID NO:18), LRQRDGERP (SEQ ID NO:19), LRQKDGGGSERP (SEQ ID NO:20), LRQKD(G3S)2ERP (SEQ ID NO:21), TGSQKP (SEQ ID NO:22), LRQKDAARGS (SEQ ID NO:26) и LRQKDAARGSGG (SEQ ID NO:76).
[0088] В некоторых вариантах осуществления пептидный линкер имеет длину от 3 до 20 аминокислотных остатков и богат G и/или S. Неограничивающими примерами таких линкеров являются линкеры G4S-типа ("G4S", описанный как SEQ ID NO: 23), т.е. линкеры, содержащие один или несколько (например, 2, 3 или 4) мотивов GGGGS (SEQ ID NO:23) или их варианты (такие как варианты, которые имеют одну, две или три инсерции, делеции и вставки аминокислот в мотиве).
[0089] В некоторых вариантах осуществления ZFP-TF содержат сигналы ядерной локализации (например, сигналы ядерной локализации из среднего T-антигена SV40) и/или эпитопные метки (например, FLAG и гемагглютинин).
II. Экспрессия ZFP-TF
[0090] ZFP-TF по настоящему изобретению может быть введен пациенту посредством молекулы нуклеиновой кислоты, кодирующей его. Например, молекула нуклеиновой кислоты представляет собой молекулу РНК, и молекулу РНК вводят в головной мозг пациента посредством инъекции композиции, содержащей комплекс липид:нуклеиновая кислота (например, липосома). Альтернативно, ZFP-TF может быть введен пациенту через экспрессирующий нуклеиновую кислоту вектор, содержащий кодирующую последовательность для ZFP-TF. Экспрессирующие векторы могут включать последовательности контроля экспрессии, такие как промоторы, энхансеры, сигнальные последовательности транскрипции и последовательности терминации транскрипции, которые обеспечивают экспрессию кодирующих последовательностей для ZFP-TF в клетках нервной системы (например, центральная нервная система). В некоторых вариантах осуществления экспрессирующий вектор остается присутствующим в клетке в качестве стабильной эписомы. В других вариантах осуществления экспрессирующий вектор интегрируется в геном клетки.
[0091] В некоторых вариантах осуществления промотор на векторе для запуска экспрессии ZFP-TF в головном мозге представляет собой конститутивно активный промотор или индуцибельный промотор. Подходящие промоторы включают, но не ограничиваются ими, промотор длинных концевых повторов (LTR) вируса саркомы Рауса (RSV) (необязательно с энхансером RSV), промотор цитомегаловируса (CMV) (необязательно с энхансером CMV), предранний промотор CMV, промотор вируса 40 обезьян (SV40), промотор дигидрофолатредуктазы (DHFR), промотор β-актина, промотор фосфоглицераткиназы (PGK), промотор EFlα, LTR вируса лейкоза мышей Молони (MoMLV), промотор на основе креатинкиназы (CK6), промотор транстиретина (TTR), промотор тимидинкиназы (TK), отвечающий на тетрациклин промотор (TRE), промотор вируса гепатита B (HBV), промотор α1-антитрипсина человека (hAAT), химерные специфические для печени промоторы (LSP), промотор фактора E2 (E2F), промотор обратной траскриптазы теломеразы человека (hTERT), энхансер CMV/промотор β-актина курицы/β-глобина кролика (промотор CAG; Niwa et al., Gene (1991) 108(2):193-9) и отвечающий на RU-486 промотор. Также можно использовать нейрон-специфические промоторы, такие как промотор синапсина I, промотор кальций/кальмодулин-зависимой протеинкиназы II (CamKII), промотор метил CpG-связывающего белка 2 (MeCP2), промотор холинацетилтрансферазы (ChAT и промотор кальбиндина (Calb). Также можно использовать астроцит-специфические промоторы, такие как промотор глиального фибриллярного кислого белка (GFAP) или промотор представителя L1 семейства 1 альдегиддегидрогеназ (Aldh1L1). Также можно использовать одигодендроцит-специфические промоторы, такие как промотор Olig2. Кроме того, промотор может включать один или несколько саморегулирующихся элементов, где ZFP-TF может связываться с самим собой и подавлять уровень его собственной экспрессии до заданного порогового уровня. См. патент США 9624498.
[0092] Можно использовать любой способ введения последовательности нуклеиновой кислоты в клетку, включая, но не ограничиваясь ими, электропорацию, преципитацию с фосфатом кальция, микроинъекцию, катионные или анионные липосомы, липосомы в комбинации с сигналом ядерной локализации, встречающиеся в природе липосомы (например, экзосомы) или вирусную трансдукцию.
[0093] Для доставки экспрессирующего вектора in vivo можно использовать вирусную трансдукцию. Различные вирусные векторы, известные в данной области, могут быть адаптированы для применения в рамках настоящего изобретения, например, векторы на основе вируса коровьей оспы, аденовирусные векторы, лентивирусные векторы, поксвирусные векторы, векторы на основе вируса герпеса, векторы на основе аденоассоциированного вируса (AAV), ретровирусные векторы и гибридные вирусные векторы. В некоторых вариантах осуществления вирусный вектор, используемый в рамках настоящего изобретения, представляет собой рекомбинантный вектор на основе AAV (rAAV). Векторы на основе AAV особенно пригодны для доставки генов в центральную нервную систему (ЦНС), поскольку AAV инфицируют как делящиеся, так и не делящиеся клетки, и имеют очень низкую иммуногенность, и вирусные геномы существуют в качестве стабильных эписомальных структур для длительной экспрессии (Hadaczek et al., Mol Ther. (2010) 18:1458-61; Zaiss, et al., Gene Ther. (2008) 15:808-16). Можно использовать любой подходящий серотип AAV. Например, AAV может представлять собой AAV1, AAV2, AAV3, AAV3b, AAV4, AAV5, AAV6, AAV7, AAV8, AAV8.2, AAV9 или AAVrh10, или псевдотип (например, AAV2/8, AAV2/5, AAV2/6, AAV2/9 или AAV2/6/9). См., например, патенты США 7198951 и 9585971.
[0094] В некоторых вариантах осуществления экспрессирующий вектор представляет собой вектор на основе AAV, и его вводят в клетку-мишень человека посредством рекомбинантного вириона AAV, геном которого содержит конструкцию, включающую последовательности инвертированных концевых повторов (ITR) AAV на обоих концах для обеспечения продуцирования вириона AAV в системе продуцирования, такой как система продуцирования клетки насекомого/бакуловируса или система продуцирования клеток млекопитающих. AAV можно конструировать так, чтобы его капсидные белки имели сниженную иммуногенность или усиленную способность к трансдукции у человека. В некоторых вариантах осуществления используют AAV9. Вирусные векторы, описанные в настоящем описании, можно получать с использованием способов, известных в данной области. Для получения вирусных частиц можно использовать любой подходящий пермиссивный или упаковывающий тип клеток. Например, в качестве упаковывающей клеточной линии можно использовать клетки млекопитающего (например, 293) или насекомого (например, Sf9).
[0095] Также см. патенты США 6309634; 6453242; 6503717; 6534261; 6599692; 6607882; 6689558; 6824978; 6933113; 6953575; 6979539; 7013219; 7163824; 7182944; 8309355; 8337458; 8586526; 9050299 и 9089667 для способов экспрессии терапевтических белков, включающих ZFP, в нервной системе пациента, нуждающегося в этом.
III. Фармацевтические применения
[0096] ZFP-TF по настоящему изобретению можно использовать для лечения пациентов, нуждающихся в подавлении экспрессии C9orf72, особенно в подавлении экспрессии мутантных аллелей C9orf72. Пациенты страдают от, или имеют риск развития, связанных с C9orf72 нейродегенеративных заболеваний, таких как ALS и C9FTD. Пациенты, имеющие риск, включают пациентов, которые являются генетически предрасположенными, пациентов, которые страдали от неоднократных травм головного мозга, таких как сотрясение, и пациентов, которые подвергались воздействию нейротоксинов внешней среды. Настоящее изобретение относится к способу лечения связанного с C9orf72 неврологического заболевания (например, ALS и C9FTD) у индивидуума, такого как пациент-человек, нуждающийся в этом, включающему введение в нервную систему (например, ЦНС) индивидуума терапевтически эффективного количества (например, количество, которое обеспечивает достаточное подавление экспрессии мутантного аллеля C9orf72) ZFP-TF (например, вектор на основе rAAV, экспрессирующий его). Термин "лечение" охватывает облегчение симптомов, предупреждение возникновения симптомов, замедление прогрессирования заболевания, повышение качества жизни и повышение выживаемости.
[0097] Настоящее изобретение относится к фармацевтической композиции, содержащей вирусный вектор, такой как rAAV, чей рекомбинантный геном содержит экспрессирующую кассету для ZFP-TF. Кроме того, фармацевтическая композиция может содержать фармацевтически приемлемый носитель, такой как вода, солевой раствор (например, фосфатно-солевой буфер), декстроза, глицерин, сахароза, лактоза, желатин, декстран, альбумин или пектин. Кроме того, композиция может содержать вспомогательные вещества, такие как смачивающие вещества или эмульгаторы, pH-буферные средства, стабилизаторы или другие реагенты, которые повышают эффективность фармацевтической композиции. Фармацевтическая композиция может содержать носители для доставки, такие как липосомы, нанокапсулы, микрочастицы, микросферы, липидные частицы и везикулы.
[0098] Клетки, на которые направлены терапевтические средства по настоящему изобретению, представляют собой клетки в головном мозге и/или спинном мозге, включая, но не ограничиваясь ими, нейрональную клетку (например, двигательный нейрон, чувствительный нейрон, дофаминэргический нейрон, холинэргический нейрон, глутаматергический нейрон, GABA-ергический нейрон или серотонинергический нейрон); глиальную клетку (например, олигодендроцит, астроцит, перицит, шванновская клетка или микроглиальная клетка); эпендимальную клетку или нейроэпителиальную клетку. Области головного мозга, на которые осуществляется нацеливание, могут представлять собой области коры, лобно-височные области, энторинальную кору, гиппокамп, мозжечок, мост и продолговатый мозг. Эти области могут быть достигнуты непосредственно путем интрагиппокампальной инъекции, интрацеребральной инъекции, инъекции в большую цистерну (ICM) или более типично посредством интрапаренхиматозной инъекции, интрацеребровентрикулярной (ICV) инъекции, интратекальной инъекции или внутривенной инъекции. Другие пути введения включают, но не ограничиваются ими, интрацеребральное, внутрижелудочковое, интраназальное или внутриглазное введение. В некоторых вариантах осуществления вирусный вектор распространяется через ткань ЦНС после прямого введения в цереброспинальную жидкость (CSF), например, посредством интратекальной и/или интрацеребральной инъекции, или посредством инъекции в большую цистерну или интрацеребровентрикулярной инъекции. В других вариантах осуществления вирусные векторы пересекают гематоэнцефалический барьер и достигают широкого распределения в ткани ЦНС индивидуума после внутривенного введения. В других вариантах осуществления вирусные векторы доставляют непосредственно в области-мишени посредством интрапаренхиматозных инъекций. В некоторых случаях вирусные векторы могут подвергаться ретроградному или антероградному транспорту в другие области головного мозга после интрапаренхиматозной доставки. В некоторых аспектах вирусный вектор имеет выраженные способности к нацеливанию на ткани ЦНС (например, тропизм к тканям ЦНС), которые обеспечивают стабильный и нетоксичный перенос генов с высокой эффективностью.
[0099] В качестве примера, фармацевтическая композиция может быть предоставлена пациенту посредством интравентрикулярного введения, например, в желудочковую область переднего мозга пациента, такую правый латеральный желудочек, левый латеральный желудочек, третий желудочек или четвертый желудочек. Фармацевтическая композиция может быть предоставлена пациенту посредством интрацеребрального введения, например, инъекции композиции в или вблизи головного мозга, продолговатого мозга, моста, мозжечка, внутричерепную полость, менингиальные оболочки, твердую оболочку, паутинную оболочку или мягкую оболочку головного мозга. Интрацеребральное введение в некоторых случаях может включать введение средства в цереброспинальную жидкость (CSF) субарахноидального пространства, окружающего головной мозг.
[00100] В некоторых случаях интрацеребральное введение вовлекает инъекцию с использованием стереотаксических процедур. Стереотаксические процедуры хорошо известны в данной области и, как правило, вовлекают применение компьютера и трехмерного сканирующего устройства, которые используются вместе, для направления инъекции в конкретную область головного мозга, например, область желудочков. Также можно использовать насосы для микроинъекций (например, от World Precision Instruments). В некоторых случаях для доставки композиции, содержащей вирусный вектор, используют насос для микроинъекций. В некоторых случаях скорость инфузии композиции находится в диапазоне от 1 мкл/мин до 100 мкл/мин. Как будет понятно специалисту в данной области скорость инфузии зависит от различных факторов, включая, например, возраст индивидуума, массу тела/размер индивидуума, серотип AAV, требуемую дозировку и внутримозговую область, на которую осуществляют нацеливание. Таким образом, в определенных обстоятельствах другие скорости инфузии могут быть определены специалистом в данной области как подходящие.
[00101] Доставку rAAV индивидууму можно проводить, например, посредством внутривенного введения. В определенных случаях может быть желательной доставка rAAV локально в ткань головного мозга, спинной мозг, цереброспинальную жидкость (CSF), нейрональные клетки, глиальные клетки, менингиальные оболочки, астроциты, олигодендроциты, интерстициальные пространства и т.п. В некоторых случаях рекомбинантные AAV (например, 107-1015 вг/доза) могут быть доставлены непосредственно в ЦНС посредством инъекции в область желудочков и/или в гиппокамп, кору, долю мозжечка или другую область головного мозга. AAV могут быть доставлены с использованием иглы, катетера или сходного устройства, с использованием нейрохирургических способов, известных в данной области, например, посредством стереотактической инъекции. См., например, Stein et al., J Vir. (1999) 73:3424-9; Davidson et al., PNAS. (2000) 97:3428-32; Davidson et al., Nat Genet. (1993) 3:219-223; и Alisky and Davidson, Hum. Gene Ther. (2000) 11:2315-29; патенты США 7837668 и 8092429.
[00102] Если в настоящем описании не определено иначе, научные и технические термины, используемые применительно к настоящему изобретению, имеют значения, которые часто подразумевают специалисты в данной области. Иллюстративные способы и материалы описаны в настоящем описании, хотя для применения на практике или тестирования настоящего изобретения можно использовать способы и материалы, сходные или эквивалентные способам и материалам, описанным в настоящем описании. В случае противоречий настоящее описание, в том числе определения, имеют преимущество. Как правило, номенклатура и способы неврологии, медицины, медицинской и фармацевтической химии и клеточной биологии, описанные в настоящем описании, являются хорошо известными и широко используемыми в данной области. Ферментативные реакции и способы очистки проводят в соответствии с инструкциями производителя, как часто осуществляют в данной области или как описано в настоящем описании. Кроме того, если контекстом не требуется иное, термины в форме единственного числа включают множественное число, и термины в множественном числе включают единственное число. На протяжении настоящего описания и вариантов осуществления слова "иметь" и "содержать", или их варианты, такие как "имеет", "имеющий", "содержит" или "содержащий" подразумевают включение указанного числа или группы чисел, но не исключение любого другого числа или группы чисел. Все публикации и другие ссылки, упоминаемые в настоящем описании, включены в качестве ссылок в полном объеме. Хотя в настоящем описании цитирован ряд документов, это цитирование не подразумевает допущения, что какой-либо из этих документов формирует часть общего знания в данной области. Как используют в рамках изобретения, термин "приблизительно" или "примерно", применяемый к одной или нескольким представляющим интерес величинам, относится к величине, которая является сходной с указанной эталонной величиной. В определенных вариантах осуществления термин относится к диапазону величин, которые входят в пределы 10%, 9%, 8%, 7%, 6%, 5%, 4%, 3%, 2%, 1%, или менее в любом направлении (превышают или являются меньшими) от указанной эталонной величины, если нет иных указаний или иное не очевидно из контекста.
[00103] Чтобы настоящее изобретение стало лучше понятным, приведены следующие варианты осуществления и примеры. Эти варианты осуществления и примеры приводятся только для целей иллюстрации, и их не следует истолковывать как ограничивающие объем изобретения каким-либо образом.
IV. Иллюстративные варианты осуществления
[00104] Неограничивающие иллюстративные варианты осуществления настоящего изобретения описаны ниже.
1. Способ подавления смысловой и/или антисмысловой транскрипции гена C9orf72 в клетке, причем способ включает обработку клетки одним или несколькими репрессорами гена C9orf72, причем один или несколько репрессоров содержат домен репрессии транскрипции и ДНК-связывающий домен, который связывается с участком-мишенью в гене C9orf72, необязательно где один или несколько репрессоров содержат один или несколько факторов транскрипции на основе белков с цинковыми пальцами (ZFP-TF), один или несколько факторов транскрипции на основе TAL-эффекторного домена (TALE-TF), и/или один или несколько факторов транскрипции CRISPR/Cas.
2. Способ по п.1, где C9orf72 содержит мутантный аллель, содержащий один или несколько подвергнутых экспансии (G4C2) повторов, необязательно где участок-мишень находится в одном или нескольких повторах (G4C2).
3. Применение одного или нескольких репрессоров ZFP-TF, TALE-TF и/или CRISPR/Cas TF, которые связываются с мутантным аллелем C9orf72 с экспансией, содержащим один или несколько повторов (G4C2), для подавления смысловой и/или антисмысловой транскрипции у индивидуума, нуждающегося в этом.
4. Способ или применение согласно любому из предшествующих вариантов осуществления, где антисмысловая транскрипция подавляется по меньшей мере на 50% по сравнению с клетками без введения.
5. Способ или применение согласно любому из предшествующих вариантов осуществления, где антисмысловая транскрипция подавляется по меньшей мере на 70% по сравнению с клетками без введения.
6. Способ применения согласно любому из предшествующих вариантов осуществления, где транскрипты, содержащие экспансию повторов, селективно подавляются, необязательно где подавляется антисмысловая транскрипция, подавляется смысловая транскрипция с промотора 1a и/или не подавляется смысловая транскрипция с промотора 1b.
7. Способ или применение согласно любому из предшествующих вариантов осуществления, где один или несколько репрессоров ZFP-TF содержат ZFP, имеющий области распознающей спирали в порядке, представленном в таблице 1.
8. Способ или применение согласно любому из предшествующих вариантов осуществления, где один или несколько репрессоров ZFP-TF вводят в клетку в качестве мРНК или с использованием вирусного вектора.
9. Способ или применение согласно варианту осуществления 8, где вирусный вектор представляет собой вектор на основе Ad или AAV.
10. Способ или применение согласно варианту осуществления 9, где вектор на основе AAV представляет собой вектор на основе AAV2/9.
11. Способ или применение согласно любому из предшествующих вариантов осуществления, где клетка находится в живом индивидууме, и индивидууму вводят один или несколько репрессоров на основе ZFP-TF.
12. Способ или применение согласно варианту осуществления 11, где один или несколько репрессоров на основе ZFP-TF вводят индивидууму интрацеребровентрикулярным, интратекальным, ретроорбитальным (RO), внутривенным, интраназальным и/или интрацистернальным путем.
13. Способ или применение согласно варианту осуществления 12, где репрессор на основе ZFP-TF вводят односторонним или двухсторонним образом в гиппокамп индивидуума, необязательно с использованием вектора на основе AAV в дозе от 1E10 до 1E13 (например, 6E11) вг/полушарие.
14. Способ или применение согласно любому из предшествующих вариантов осуществления, где клетка представляет собой нейрон.
15. Способ или применение согласно любому из предшествующих вариантов осуществления, где вводят два или более репрессоров на основе ZFP-TF.
16. Способ или применение согласно варианту осуществления 15, где два или более репрессоров на основе ZFP-TF находятся на одном и том же или различных невирусных или вирусных векторах.
17. Способ или применение согласно любому из предшествующих вариантов осуществления, где у индивидуума лечат ALS и/или FTD.
18. Способ или применение согласно любому из предшествующих вариантов осуществления, где у индивидуума облегчается один или несколько симптомов ALS и/или FTD.
19. Слитый белок ZFP-TF, который связывается с последовательностью-мишенью и содержит цинковые пальцы, соответствующие SBS ID, как показано в таблице 1, причем цинковые пальцы содержат последовательности ДНК-связывающей (распознающей) спирали, представленные в единичном ряду таблицы 1 для SBS ID, где SBS ID представляет собой 78021.
20. Слитый белок ZFP-TF, который связывается с последовательностью-мишенью и содержит цинковые пальцы, соответствующие SBS ID, как показано в таблице 1, причем цинковые пальцы содержат последовательности ДНК-связывающей (распознающей) спирали, представленные в единичном ряду таблицы 1 для SBS ID, где SBS ID представляет собой 75114.
21. Слитый белок ZFP-TF, который связывается с последовательностью-мишенью и содержит цинковые пальцы, соответствующие SBS ID, как показано в таблице 1, причем цинковые пальцы содержат последовательности ДНК-связывающей (распознающей) спирали, представленные в единичном ряду таблицы 1 для SBS ID, где SBS ID представляет собой 75115.
22. Слитый белок ZFP-TF, который связывается с последовательностью-мишенью и содержит цинковые пальцы, соответствующие SBS ID, как показано в таблице 1, причем цинковые пальцы содержат последовательности ДНК-связывающей (распознающей) спирали, представленные в единичном ряду таблицы 1 для SBS ID, где SBS ID представляет собой 74969.
23. Слитый белок ZFP-TF, который связывается с последовательностью-мишенью и содержит цинковые пальцы, соответствующие SBS ID, как показано в таблице 1, причем цинковые пальцы содержат последовательности ДНК-связывающей (распознающей) спирали, представленные в единичном ряду таблицы 1 для SBS ID, где SBS ID представляет собой 79895.
24. Слитый белок ZFP-TF, который связывается с последовательностью-мишенью и содержит цинковые пальцы, соответствующие SBS ID, как показано в таблице 1, причем цинковые пальцы содержат последовательности ДНК-связывающей (распознающей) спирали, представленные в единичном ряду таблицы 1 для SBS ID, где SBS ID представляет собой 79898.
25. Слитый белок ZFP-TF, который связывается с последовательностью-мишенью и содержит цинковые пальцы, соответствующие SBS ID, как показано в таблице 1, причем цинковые пальцы содержат последовательности ДНК-связывающей (распознающей) спирали, представленные в единичном ряду таблицы 1 для SBS ID, где SBS ID представляет собой 74986.
26. Слитый белок ZFP-TF, который связывается с последовательностью-мишенью и содержит цинковые пальцы, соответствующие SBS ID, как показано в таблице 1, причем цинковые пальцы содержат последовательности ДНК-связывающей (распознающей) спирали, представленные в единичном ряду таблицы 1 для SBS ID, где SBS ID представляет собой 79899.
27. Слитый белок ZFP-TF, который связывается с последовательностью-мишенью и содержит цинковые пальцы, соответствующие SBS ID, как показано в таблице 1, причем цинковые пальцы содержат последовательности ДНК-связывающей (распознающей) спирали, представленные в единичном ряду таблицы 1 для SBS ID, где SBS ID представляет собой 79901.
28. Слитый белок ZFP-TF, который связывается с последовательностью-мишенью и содержит цинковые пальцы, соответствующие SBS ID, как показано в таблице 1, причем цинковые пальцы содержат последовательности ДНК-связывающей (распознающей) спирали, представленные в единичном ряду таблицы 1 для SBS ID, где SBS ID представляет собой 79902.
29. Слитый белок ZFP-TF, который связывается с последовательностью-мишенью и содержит цинковые пальцы, соответствующие SBS ID, как показано в таблице 1, причем цинковые пальцы содержат последовательности ДНК-связывающей (распознающей) спирали, представленные в единичном ряду таблицы 1 для SBS ID, где SBS ID представляет собой 79904.
30. Слитый белок ZFP-TF, который связывается с последовательностью-мишенью и содержит цинковые пальцы, соответствующие SBS ID, как показано в таблице 1, причем цинковые пальцы содержат последовательности ДНК-связывающей (распознающей) спирали, представленные в единичном ряду таблицы 1 для SBS ID, где SBS ID представляет собой 79916.
31. Слитый белок ZFP-TF, который связывается с последовательностью-мишенью и содержит цинковые пальцы, соответствующие SBS ID, как показано в таблице 1, причем цинковые пальцы содержат последовательности ДНК-связывающей (распознающей) спирали, представленные в единичном ряду таблицы 1 для SBS ID, где SBS ID представляет собой 75027.
32. Слитый белок ZFP-TF, который связывается с последовательностью-мишенью и содержит цинковые пальцы, соответствующие SBS ID, как показано в таблице 1, причем цинковые пальцы содержат последовательности ДНК-связывающей (распознающей) спирали, представленные в единичном ряду таблицы 1 для SBS ID, где SBS ID представляет собой 79921.
33. Слитый белок ZFP-TF согласно любому из вариантов осуществления 19-32, где слитый белок ZFP-TF содержит домен репрессора транскрипции, содержащий SEQ ID NO:13.
34. Слитый белок ZFP-TF согласно любому из вариантов осуществления 19-33, где домен цинковых пальцев и домен репрессора транскрипции связаны посредством пептидного линкера, содержащего SEQ ID NO:26.
ПРИМЕРЫ
Пример 1: Искусственные репрессора транскрипции
[00105] Панель ZFP-TF получали для нацеливания на аллели C9orf72 человека с экспансией. Иллюстративные ZFP-TF представлены в таблице 1 ниже. Каждый из этих ZFP-TF содержал домен ZFP, имеющий шесть пальцев, и домен KRAB, как описано выше (SEQ ID NO:13). Пептидный линкер использовали для связывания домена ZFP с доменом KRAB. Линкер имел следующую аминокислотную последовательность: LRQKDAARGS (SEQ ID NO:26).
[00106] В таблице 1 представлена последовательность ДНК участка-мишени и аминокислотная последовательность ДНК-связывающей спирали каждого цинкового пальца (с F1 по F6) в каждом ZFP-TF. SEQ ID NO представлены в скобках. Последовательность-мишень, связываемая доменом ZFP в участке-мишени, представлена прописными буквами, в то время как фланкирующие последовательности представлены строчными буквами. SEQ ID NO:24 представляет собой участок-мишень на смысловой цепи аллеля гена, в то время как SEQ ID NO:25 представляет собой участок-мишень на антисмысловой цепи аллеля гена.
[00107] ДНК-связывающая спираль представляет собой вариабельную часть цинкового пальца и, как правило, содержит шесть или семь аминокислотных остатков. Специфичность ZFP-домена к мишени может быть улучшена посредством мутаций в остове ZFP, как описано, например, в публикации патента США 2018/0087072. Символ "^" в таблице указывает на то, что остаток аргинина (R) в 4-м положении выше 1-й аминокислоты в указанной спирали заменен на глутамин (Q). В каждой последовательности спирали цинкового пальца положения семи ДНК-связывающих аминокислот пронумерованы как -1, +1, +2, +3, +4, +5 и +6. Таким образом, положение для замены R на Q пронумеровано как (-5).
Таблица 1. Иллюстративный ZFP-TF против C9orf72
(SEQ ID NO)
(SEQ ID NO)
CGGGGCCggggcgtg
(24)
(27)
(28)
(27)
(28)
(27)
(28)
CGGGGCCggggcgtg
(24)
(27)
(29)
(27)
(29)
(27)
(29)
CGGGGCCggggcgtg
(24)
(30)
(29)
(30)
(29)
(30)
(29)
CGGGGCCggggcgtg
(24)
(31)
GGGGCCGgggcgtg
(24)
(32)
GGGGCCGGggcgtg
(24)
(33)
GGGGCCGGggcgtg
(24)
(35)
(36)
(35)
(36)
(35)
(36)
GGGGCCGGggcgtg
(24)
(37)
GGGGCCGGggcgtg
(24)
(37)
GGGGCCGGggcgtg
(24)
(38)
GGGGCCGGGgcgtg
(24)
(29)
GGGGCCGGGgcgtg
(24)
(39)
(40)
GGGGCCGGGgcgtg
(24)
(29)
GGGGCCGGGgcgtg
(24)
(29)
GGGGCCGGGgcgtg
(24)
(29)
GGGGCCGGGGcgtg
(24)
(29)
GGGGCCGGGGcgtg
(24)
GGGGCCGGGGcgtg
(24)
GGGGCCGGGGcgtg
(24)
GGCCCCGgccccta
(25)
GGCCCCGgccccta
(25)
(46)
GGCCCCGgccccta
(25)
(41)
GGCCCCGgccccta
(25)
GGCCCCGgccccta
(25)
(45)
GGCCCCGgccccta
(25)
GGCCCCGGccccta
(25)
GGCCCCGGCcccta
(25)
GCCCCGGCCccta
(25)
GCCCCGGCCccta
(25)
GCCCCGGCCccta
(25)
GGGGCCGGggcgtg
(24)
(56)
(33)
(56)
(33)
(56)
GGCCCCGGCcccta
(25)
GCCCCGGCCccta
(25)
GCCCCGGCCccta
(25)
GCCCCGGCCccta
(25)
GGGGCCGGggcgtg
(24)
GGGGCCGGggcgtg
(24)
GGGGCCGGggcgtg
(24)
GGGGCCGGGgcgtg
(24)
GGGGCCGGGgcgtg
(24)
GGGGCCGGGgcgtg
(24)
GGGGCCGGGgcgtg
(24)
GGGGCCGGGgcgtg
(24)
GGCCCCGgccccta
(25)
GGCCCCGgccccta
(25)
GGCCCCGgccccta
(25)
GGCCCCGgccccta
(25)
[00108] ZFP-TF оценивали посредством стандартного анализа SELEX (см., например, Miller et al., Nat Biotech. (2010) doi:10.1038/nbt.1755; Wilen et al., PLoS (2011) 7(4):e1002020). Было показано, что все они связываются с их участками-мишенями.
[00109] В этом исследовании использовали пять типов клеточных линий человека и одну клеточную линию мыши. Клеточная линия фибробластов C9021 была получена от The ALS Institute at Columbia University и происходила от пациента с ALS-FTD. Она содержит 5 повторов G4C2 на ее нормальном аллеле и приблизительно 850 повторов на ее аллеле с экспансией. Клеточные линии фибробластов дикого типа (NDS00035), 353TRAD и 204TDP были получены от National Institute of Neurological Disorders and Stroke. Линия дикого типа содержит два повтора G4C2 на каждом аллеле. Линия 353TRAD содержит 5 повторов на одном аллеле и 8 повторов на другом аллеле. 204TDP имеет 2 повтора на одном аллеле и 20 повторов на другом аллеле. Для всех экспериментов с фибробластами нейроны человека были получены от Cell Dynamics International (iCell GABANeurons Kit, 01434; каталожный номер # R1013; клетки партии # 104901). Нейроны коры мыши были получены от GIBCO (каталожный номер # A15586). В качестве отрицательного контроля использовали ZFP 74960, который связывался с его областью-мишенью, но не имел поддающегося обнаружению эффекта подавления.
[00110] Для всех экспериментов, проводимых на фиробластных клетках, происходящих от пациента, трансфекцию мРНК ZFP-TF в клетки проводили с использованием 96-луночной системы Shuttle Nucleofector от Lonza. Трансфицировали 1, 3, 10, 30, 100 и 300 нг мРНК ZFP-TF на 40000 клеток с использованием набора Amaxa P2 Primary Cells Nucleofector с использованием программы CA-137. После инкубации в течение ночи использовали набор Cells-to-Ct kit (Thermo Fisher Scientific) для получения кДНК из трансфицированных клеток с последующим анализом экспрессии генов с использованием qRT-PCR.
[00111] Для трансдукции нейронов ZFP встраивали в плазмиды AAV6. Нейроны трансдуцировали посредством AAV6-ZFP. Во всех случаях трансдукцию проводили при MOI 3000. Нейроны мыши собирали через 7 суток после трансдукции, в то время как нейроны человека собирали через 19 суток после трансдукции. После сбора клеток их обрабатывали для анализа на микрочипах.
[00112] Скрининговый анализ проводили на протяжении нескольких раундов. В каждом раунде ZFP тестировали при нескольких концентрациях для идентификации ZFP-TF с подходящим паттерном в отношении мишени (селективное подавление). Раунд 2 скрининга проводили в клетках C9 (C9021) для оценки уровней смыслового транскрипта C9orf72 с экспансией (заболевание) против тотальной зрелой мРНК C9orf72 ("тотальный C9") после обработки ZFP-TF. В анализе с использованием RT-PCR использовался набор праймеров/зондов, который нацелен на интронную область 1a.
Смысловой транскрипт C9orf72 с экспансией:
Прямой: 5’ CCCTCTCTCCCCACTACTTG 3’ (SEQ ID NO:61)
Обратный: 5’ CTACAGGCTGCGGTTGTTTCC 3’ (SEQ ID NO:62)
Зонд: 5’ TCTCACAGTACTCGCTGAGGGTGA 3’ (SEQ ID NO:63)
[00113] Экспансия G4C2 приводит к неэффективному сплайсингу и накоплению содержащей экспансию пре-мРНК (фиг.2A). Напротив, пре-мРНК дикого типа (WT), которая эффективно сплайсируется, присутствует на очень низких уровнях. С использованием этого анализа в клетках C9021 авторы изобретения показали, что протестированные ZFP-TF демонстрировали широкий диапазон подавления смыслового транскрипта C9orf72 с экспансией (заболевание). (фиг.2B-D).
[00114] Для оценки подавления тотальной мРНК C9orf72 использовали другой набор праймеров/зондов, означаемый как "Total C9" (фиг.2A):
Тотальная мРНК C9orf72:
Прямой: 5’ CTATGTGTGTGGTGGGATATGG 3’ (SEQ ID NO:58)
Обратный: 5’ CTCCAGGTTATGTGAAGCAGAA 3’ (SEQ ID NO:59)
Зонд: 5’ AGGCCTGCTAAAGGATTCAACTGGAA 3’ (SEQ ID NO:60)
[00115] Этот набор праймеров/зондов может выявлять мРНК, содержащие область, охватывающую экзоны 8 и 9. Эта область присутствует во всех изоформах мРНК C9orf72. Как показано на фиг.2b, многие ZFP-TF продемонстрировали умеренное подавление тотальных транскриптов C9orf72. Например, ZFP-TF 75114 и 75115 подавляли смысловой транскрипт с экспансией (заболевание) более чем на 70%, при сохранении экспрессии тотальной мРНК C9orf72 более чем на 50% (фиг.2D, данные 2 раунда).
[00116] В 3 раунде проводили оценку тотальной мРНК C9orf72 и сравнивали между клетками C9021 и клетками дикого типа (WT) для дальнейшей оценки эффекта протестированных ZFP-TF на уровни тотальной мРНК C9orf72. Эти данные показывают, что уровни тотальной мРНК C9orf72 в мутантных клетках снижались значительно в большей степени, чем в клетках WT (фиг.2B-D) и значительно менее изменялись в клетках дикого типа, обработанных теми же ZFP-TF. В целом, данные иллюстрируют, что для некоторых ZFP, таких как 75109, 75114 и 75115, изоформа с экспансией подавлялась значительно (приблизительно на 70%) при сохранении приблизительно 50% от тотальных транскриптов C9 в линиях фибробластов с пациентами C9.
[00117] Селективное подавление изоформ посредством ZFP-TF 75109, 75114 и 75115 оценивали в трех различных линиях фибробластных клеток, происходящих от пациентов, имевших различную экспансию повторов G4C2 на их аллелях с экспансией (600, 800 и 850) (фиг.6). Все три ZFP демонстрировали сходное поведение, независимо от длины экспансии повтора, иллюстрируя, что селективное подавление посредством ZFP-TF не зависит от длины повторов G4C2.
[00118] Проводили оценку подавления тотального транскрипта C9 в двух клеточных линиях от здоровых индивидуумов с превышающим норму количеством повторов G4C2 в их аллелях (фиг.7). Воздействие на тотальный транскрипт C9 в здоровых клеточных линиях было минимальным. ZFP-опосредуемое подавление тотального транскрипта мРНК C9 в происходящей от пациента клеточной линии (C9021) не является истинным отражением уровней изоформ WT, поскольку анализ ПЦР, использованный для детекции тотального транскрипта мРНК C9, направлен на экзоны 8 и 9, которые присутствуют как в изоформах с экспансией, так и в изоформах без экспансии (WT) (фиг.2A). Подавление тотального транскрипта мРНК C9 в ответ на селективные в отношении изоформ ZFP-TF (75109, 75114 и 75115) оценивали в двух различных линиях от здоровых индивидуумов с различной длиной повторов G4C2 в их аллелях (фиг.7). Клеточная линия 353TREAD имеет 5 повторов на одном аллеле и 8 повторов на другом аллеле, в то время как клеточная линия 204TDP имеет 2 повтора на одном аллеле и 20 повторов на другом аллеле. В то время как в линии C9 C921 происходило подавление тотального транскрипта мРНК C9 зависимым от дозы образом (5 повторов в аллеле без экспансии и 850 повторов в аллеле с экспансией), в двух других клеточных линиях без аллеля с экспансией оно было минимальным, что указывает на то, что подавление тотальной изоформы C9 в линии индивидуума с заболеванием (5/850) является следствием подавления изоформ с экспансией, и экспрессия изоформы без экспансии не изменялось посредством селективных ZFP-TF (фиг.7).
[00119] Без связи с теорией, является возможным, что ZFP-TF по настоящему изобретению способны действовать кооперативно, селективно подавляя аллель с многочисленными повторами. Это может опосредоваться комплексами более высокого порядка, например, посредством привлечения корепрессора KAP1, который ассоциирует со связанными с ZFP доменами KRAB. Согласно этой гипотезе, "каркас" KAP1/KRAB в множестве ZFP-TF повышает стабильность аппарата подавления транскрипции и обеспечивает предпочтительное подавление аллеля C9orf72 с экспансией относительно аллеля дикого типа.
Пример 2: Специфичность подавления C9orf72
[00120] Глобальную специфичность ZFP-TF, представленных в таблице 1, оценивали посредством анализа на микрочипах в 3 клеточных линиях: фибробластные клетки C9021, первичные нейроны коры мыши и нейроны человека. Для клеток C9021, в кратком изложении, 100 нг мРНК, кодирующей ZFP-TF, переносили в 150000 клеток C9021 в четырех экземплярах. Через 24 час тотальную РНК экстрагировали и процессировали в соответствии с протоколом производителя (Affymetrix Genechip MTA1.0). Робастное среднее для множества чипов (RMA) использовали для нормализации исходных сигналов от каждого набора зондов. Анализ проводили с использованием Transcriptome Analysis Console 3.0 (Affymetrix) с опцией "Дифференциальный анализ экспрессии на генном уровне". Трансфицированные посредством ZFP-TF образцы сравнивали с образцами, которые были обработаны посторонним ZFP-TF (который не связывается с участком-мишенью в C9orf72). Сигналы изменения регистрировались для транскриптов (наборов зондов) с >2-кратным отличием среднего сигнала относительно контроля и значением P < 0,05 (односторонний анализ ANOVA, непарный T-критерий для каждого набора зондов). Сходную методику также проводили для нейронов, за исключением того, что их трансдуцировали AAV6 с MOI 3000 и культивировали в течение 7 суток для нейронов мыши и 19 суток для нейронов человека перед сбором.
[00121] Иллюстративные данные представлены на фиг.8A-8C. Данные показывают, что ZFP-TF 75027 демонстрировал несколько неспецифических мишеней в дополнение к C9orf72 (показаны кругами), в то время как ZFP-TF 75109, 75114 и 75115 подавляли только C9orf72 с минимальным неспецифическим действием как в фибробластах, так и в нейронах, как человека, так и мыши. Эти результаты демонстрируют, что репрезентативные ZFP-TF являются в высокой степени специфичными к C9orf72.
Пример 3: Выявление специфического подавление антисмысловых транскриптов
[00122] Поскольку смысловые и антисмысловые транскрипты кодируются перекрывающимися областями ДНК, авторы изобретения разработали стратегию детекции на основе дифференциального процессинга транскриптов. Для смысловой мРНК из аллеля с экспансией интрон, содержащий область экспансии (интрон 1a), подвергается ошибочному сплайсингу и сохраняется, а все другие интроны удаляются, включая интрон 1b. Напротив, область интрона 1b представляет собой спрогнозированный экзон в антисмысловом мРНК-транскрипте и должна быть сохранена. Таким образом, авторы изобретения сконструировали и протестировали праймеры, находящиеся в интроне 1b, и продемонстрировали специфическую детекцию антисмысловых транскриптов, как дополнительно описано ниже.
[00123] Для детекции транскриптов C9orf72 авторы использовали капельную цифровую ПЦР (ddPCR). В кратком изложении, для получения смысловых или антисмысловых кДНК-матриц, РНК очищали из клеток пациентов с C9orf72 и клеток здоровых контролей (линия C9orf72: C9-3, C9-6, C9-7, C9-5, C9-10, C9-11, C9-2, C9-4; контрольные линии: KinALS6, Con3, Kin1ALS17, Con8, Con10, Con1; см. Lagier-Tourenne et al., PNAS (2013) 110(47):E4530-9) и использовали для синтеза кДНК с использованием системы синтеза первой цепи Superscript III (Thermo Fischer Scientific) следующим образом:
1) 0,5 мкг РНК, 0,5 мкл 10 мМ цепь-специфического праймера и смесь dNTP смешивали и доводили до 10 мкл водой. Для получения смысловой матрицы использовали праймер 5’ CTCTAGCGACTGGTGGAATTG 3’ (SEQ ID NO:64). Для получения антисмысловой матрицы использовали праймер 5’ GTGCATGGCAACTGTTTGAATA 3’ (SEQ ID NO:65).
2) Эту реакционную смесь инкубировали при 65°C в течение 5 минут для денатурации и помещали на лед по меньшей мере на 1 минуту.
3) Смесь для синтеза кДНК получали с использованием следующих реагентов: 10x буфер RT (2 мкл); 25 мМ MgCl2 (4 мкл); 0,1 M DTT (2 мкл); РНК-аза OUT (1 мкл); Superscript III (1 мкл).
4) 10 мкл этой реакционной смеси добавляли к смеси РНК и инкубировали при 50°C в течение 50 минут. Затем реакционную смесь инактивировали посредством инкубации в течение 5 минут при 85°C.
[00124] Затем матрицу подвергали ddPCR с использованием меченого зонда в соответствии с протоколами изготовителей. В кратком изложении, реакции ПЦР проводили в 96-луночном планшете для ПЦР ABI с использованием свободной от dUTP смеси ddPCR Supermix for Probes (Bio-Rad). Основную смесь для ПЦР получали в соответствии с инструкциями изготовителя. Ниже представлен набор праймеров-зонда для антисмысловой цепи для области интрона 1b (фиг.3).
Прямой: 5’ CAAAGCCTGGTGGTGTTCAA 3’ (SEQ ID NO:66)
Обратный: 5’ GGACATGACCTGGTTGCTTC 3’ (SEQ ID NO:67)
Зонд: 5’ CGCGGCCAGATAGACCCAATGAGCA 3’(SEQ ID NO:68).
[00125] Реакции проводили следующим образом:
1) Полную основную смесь распределяли равномерно в 8 лунок планшета для ПЦР ABI.
2) В лунки для образца добавляли 10 мкл реакционных смесей для RT, разбавленных в 1:10, или воду.
3) 15 мкл основной смеси переносили в лунки содержавшие RT.
4) Планшет закрывали, встряхивали и кратковременно центрифугировали для осаждения.
Для получения капель использовали кассеты следующим образом:
1) 70 мкл масла для зонда наносили в лунки, обозначенные как "масло" на кассете и в лунки, обозначенные как "образец" наносили 20 мкл реакционных смесей для ddPCR.
2) На кассету помещали резиновое уплотнение.
3) 40 мкл капель переносили в новый 96-луночный планшет Eppendorf. Планшет накрывали алюминиевой фольгой и проводили ПЦР в соответствии с протоколом изготовителя.
[00126] Данные показывают, что в линиях фибробластов C9orf72 эти праймеры амплифицировали экзон в антисмысловой пре-мРНК с экспансией (C9-AS) и что в смысловой области отсутствовала область комплементарности (C9-S) (фиг.4A). Таким образом, праймеры для ddPCR для антисмысловой цепи в данном случае специфически выявляли присутствие антисмысловой пре-мРНК, уровень которой был очевидно повышен в 7 различных происходящих от пациента с C9 линиях фибробластов по сравнению с 6 различными линиями контрольных фибробластов (фиг.4B).
Пример 4: Подавление смысловой и антисмысловой пре-мРНК аллеля с экспансией
[00127] Для тестирования активности репрессоров ZFP-TF в отношении аллеля с экспансией клетки обрабатывали ZFP-TF 74949, 74978, 75003, 75027, 75109, 75114, 75115, 74967 (таблица 1) или 74960 (отрицательный контроль), как описано выше. Два отдельных анализа ПЦР для оценки опосредуемого ZFP-TF подавления использовались исследователями слепым методом в отношении порядка образцов. В каждом анализе использовался отличающийся праймер/зонд (фиг.5A-5C).
[00128] Для прогонов #1 и #2 анализы для количественного определения смысловой цепи с экспансией, антисмысловой цепи с экспансией и тотального C9 проводили, как описано выше, за исключением того, что амплификацию проводили со случайными гексамерами в соответствии со стандартными протоколами в данной области и с праймерами, представленными ниже:
Антисмысловая пре-мРНК C9orf72 с экспансией (фиг.5B): как показано в примере 3 выше.
Смысловая пре-мРНК C9orf72 с экспансией (фиг. 5A): данный набор праймеров/зонда мог выявлять мРНК, содержащие область, охватывающую экзон 1a и интрон 1a.
Прямой: 5’ ACTACTTGCTCTCACAGTACTCG 3’ (SEQ ID NO:69)
Обратный: 5’ TAGCGCGCGACTCCTGAGTTCC 3’ (SEQ ID NO:70)
Зонд: 5’ AGGGAAACAACCGCAGCCTGTAGCAAGCTC 3’ (SEQ ID NO:71).
Тотальная мРНК C9orf72 (фиг.5C): этот набор праймеров/зонда мог выявлять мРНК, содержавшие область в экзоне 2.
Прямой: 5’ TGTGACAGTTGGAATGCAGTGA 3’ (SEQ ID NO:72)
Обратный: 5’ GCCACTTAAAGCAATCTCTGTCTTG 3’ (SEQ ID NO:73)
Зонд: 5’ TCGACTCTTTGCCCACCGCCA 3’ (SEQ ID NO:74).
[00129] Для прогона #3 (фиг. 5A и 5C) использовали праймеры, представленные выше в примере 1 (фиг.2B-2D). Для антисмыслового транскрипта заболевания использовали следующие праймеры/зонд для детекции интронной области 1b (фиг.5B).
Прямой: 5’ CAGCTTCGGTCAGAGAAATGAG 3’ (SEQ ID NO:78)
Обратный: 5’ AAGAGGCGCGGGTAGAA 3’ (SEQ ID NO:79)
Зонд: 5’ CTCTCCTCAGAGCTCGACGCATTT 3’ (SEQ ID NO:80)
[00130] Несмотря на тот факт, что использовали различные наборы праймеров/зонд и использовали различные анализы способом ПЦР (прогон #1 и прогон #2 проводили посредством сходных анализов, но отличных от прогона #3), данные были согласующимися и уровни экспрессии были сравнимыми.
[00131] Взятые вместе, все прогоны неизменно продемонстрировали, что некоторые из ZFP-TF были способными значительно подавлять все транскрипты (смысловые, антисмысловые и тотальные) (например, ZFP-TF 74978, 75003 и 75027), в то время как некоторые ZFP-TF (например, ZFP-TF 75109, 75114 и 75115) селективно подавляли смысловые и антисмысловые транскрипты заболевания, при сохранении тотального транскрипта C9 (селективное подавление).
Пример 5: Модулирование C9orf72 человека в нейронах трансгенных мышей C9orf72 BAC
[00132] Все репрессоры, нацеленные на C9orf72 мышей BAC, клонировали в векторы rAAV6 с использованием промотора CMV для запуска экспрессии. Рекомбинантный AAV продуцируют в клетках HEK293T, очищают с использованием градиента плотности CsCl и титруют посредством qPCR в реальном времени способами, известными в данной области. Очищенный вирус используют для инфицирования культивируемых первичных нейронов коры мыши в количестве 3E5, 1E5, 3E4 и 1E4 вг/клетка. Через 7 суток тотальную РНК экстрагируют и проводят мониторинг экспрессии смысловых и антисмысловых транскриптов C9orf72, а также двух эталонных генов (например Atp5b и Eif4a2) с использованием RT-qPCR.
[00133] Все векторы на основе AAV, кодирующие ZFP-TF, эффективно подавляют их мишени в клетках мышей на протяжении широкого диапазона доз инфицирования, причем некоторые ZFP подавляют мишень более чем на 95% в нескольких дозах. Напротив, не наблюдается подавления генов для вируса CMV-GFP rAAV6, протестированного в эквивалентных дозах, или обработанных имитирующей обработкой нейронов.
Пример 6: Подавление генов in vivo, обеспечиваемое ZFP-TF, доставляемыми посредством AAV
[00134] Трансгенные мыши C9orf72 BAC, использованные для исследований связывания мишени, содержат 98 т.п.н. трансгена человека, содержащего полноразмерный аллель гена C9orf72, имеющий приблизительно 500 повторов G4C2 со значительной фланкирующей последовательностью Liu et al., Neuron (2016) 90(3):521-34). Для этого исследования использовали два ZFP-TF, ZFP-TF 75027 или ZFP-TF 75114, с различной эффективностью (наиболее эффективным является ZFP-TF 75027; фиг. 2D). Экспрессирующие кассеты для двух слитых белков клонировали в вектор rAAV, содержавший промотор синапсина для запуска экспрессии и кодирующую последовательность для саморасщепляющегося пептида (например, пептид 2A, такой как T2A или P2A), за которой следовала Venus-метка для определения биораспределения (фиг.9, панель A). rAAV продуцировали в клетках HEK293T и титровали посредством ddPCR с использованием праймеров на ITR.
[00135] Для оценки эффекта экспрессии ZFP-TF на подавление содержащих экспансию смысловых и антисмысловых транскриптов in vivo, rAAV ZFP-TF доставляли мышам P0 C9-BAC или WT посредством интрацеребровентрикулярных инъекций (ICV). В кратком изложении, носитель (PBS) или ZFP-TF 75027 rAAV или ZFP-TF 75114 rAAV (общая доза 2E10 вг на желудочек) вводили двухсторонним образом (2 мкл на желудочек) новорожденным мышам C9-BAC (подобранным по длине повторов) или мышам WT (фиг.9, панель C). Животных умерщвляли через четыре недели после инъекции и одно полушарие подвергали заливке для анализа очагов РНК, а другое полушарие подвергали микродиссекции на кору, гиппокамп и мозжечок для дальнейшего анализа (фиг.9, панель B). Количественное определение вирусных белков и мРНК и белка Venus продемонстрировало широкое биораспределение с эквивалентной трансдукцией и экспрессией для ZFP-TF 75027 и ZFP-TF 75114.
[00136] Тотальную РНК экстрагировали из тканей коры и гиппокампа и получали кДНК с использованием набора для синтеза кДНК iScript (BioRad). ddPCR проводили для определения экспрессии смыслового и антисмыслового транскриптов с экспансией и тотальных уровней мРНК C9, нормализованных к уровням TBP мыши. Праймеры, используемые для этого анализа, представляли собой:
Тотальная мРНК C9:
Прямой: 5’TGTGACAGTTGGAATGCAGTGA3’ (SEQ ID NO:72)
Обратный: 5’GCCACTTAAAGCAATCTCTGTCTTG3’ (SEQ ID NO:73)
Зонд: 5’TCGACTCTTTGCCCACCGCCA3’ (SEQ ID NO:74)
Смысловая пре-мРНК с экспансией:
Прямой: 5’ ACTACTTGCTCTCACAGTACTCG 3’ (SEQ ID NO:69)
Обратный: 5’ TAGCGCGCGACTCCTGAGTTCC 3’ (SEQ ID NO:70)
Зонд: 5’ AGGGAAACAACCGCAGCCTGTAGCAAGCTC 3’ (SEQ ID NO:71).
Антисмысловая пре-мРНК с экспансией:
Прямой: 5’AGTCGCTAGAGGCGAAAGC3’ (SEQ ID NO:81)
Обратный: 5’CGAGTGGGTGAGTGAGGAG3’ (SEQ ID NO:82)
Зонд: 5’AAGAGGCGCGGGTAGAAGCGGGGGC3’ (SEQ ID NO:83)
[00137] Данные показывают, что ZFP-TF 75027 подавлял уровни тотальной мРНК C9, смысловых и антисмысловых транскриптов с экспансией в гиппокампе и коре животных C9-BAC относительно контролей, которым проводили инъекцию PBS (фиг.9, панель D). (Нельзя было наблюдать селективное подавление с использованием этой модели на животных, поскольку трансгенные мыши не содержат аллель WT C9orf72 человека и ген C9orf72 мыши не содержит повторов G4C2). Не наблюдали подавления посредством ZFP-TF 75114.
[00138] Кроме того, флуоресцентную гибридизацию in situ использовали для измерения уровней агрегатов (очагов) смысловой и антисмысловой РНК, обнаруженных в гиппокампе после инъекций ZFP-TF (фиг.9, панель E). В кратком изложении, 10-мкм срезы подвергали гибридизации с использованием меченных флуорофором зондов: 5’GGCCCCGGCCCCGGCCCC-Cy3 (SEQ ID NO:84) использовали для определения очагов смысловой РНК и 5’GGGGCCGGGGCCGGGGCC-Cy3 (SEQ ID NO:85) использовали для определения очагов антисмысловой РНК. Совмещенные изображения получали на конфокальном микроскопе (LSM880) при увеличении 40x. Количество очагов смысловой и антисмысловой РНК, нормализованное к общему количеству клеток, количественно определяли в области аммонова рога (CA) гиппокампа. Более низкий процент очагов антисмысловой РНК наблюдали у животных, которым инъецировали ZFP-TF 75027.
[00139] Эти результаты показывают, что нацеливание на C9orf72 посредством ZFP-TF может эффективно подавлять экспрессию вызывающего заболевание аллеля C9orf72 in vivo и что можно наблюдать различия в эффективности ZFP-TF.
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> SANGAMO THERAPEUTICS, INC.
<120> МОДУЛЯТОРЫ ЭКСПРЕССИИ ГЕНА ОТКРЫТОЙ РАМКИ СЧИТЫВАНИЯ 72 ХРОМОСОМЫ 9 И
ИХ ПРИМЕНЕНИЯ
<130> 025297.WO017
<140>
<141>
<150> 62/964,844
<151> 2020-01-23
<150> 62/837,523
<151> 2019-04-23
<160> 85
<170> PatentIn version 3.5
<210> 1
<211> 6
<212> ДНК
<213> Homo sapiens
<400> 1
ggggcc 6
<210> 2
<211> 6
<212> ДНК
<213> Homo sapiens
<400> 2
gggccg 6
<210> 3
<211> 6
<212> ДНК
<213> Homo sapiens
<400> 3
ggccgg 6
<210> 4
<211> 6
<212> ДНК
<213> Homo sapiens
<400> 4
gccggg 6
<210> 5
<211> 6
<212> ДНК
<213> Homo sapiens
<400> 5
ccgggg 6
<210> 6
<211> 6
<212> ДНК
<213> Homo sapiens
<400> 6
cggggc 6
<210> 7
<211> 6
<212> ДНК
<213> Homo sapiens
<400> 7
ggcccc 6
<210> 8
<211> 6
<212> ДНК
<213> Homo sapiens
<400> 8
gccccg 6
<210> 9
<211> 6
<212> ДНК
<213> Homo sapiens
<400> 9
ccccgg 6
<210> 10
<211> 6
<212> ДНК
<213> Homo sapiens
<400> 10
cccggc 6
<210> 11
<211> 6
<212> ДНК
<213> Homo sapiens
<400> 11
ccggcc 6
<210> 12
<211> 6
<212> ДНК
<213> Homo sapiens
<400> 12
cggccc 6
<210> 13
<211> 96
<212> БЕЛОК
<213> Homo sapiens
<400> 13
Asp Ala Lys Ser Leu Thr Ala Trp Ser Arg Thr Leu Val Thr Phe Lys
1 5 10 15
Asp Val Phe Val Asp Phe Thr Arg Glu Glu Trp Lys Leu Leu Asp Thr
20 25 30
Ala Gln Gln Ile Val Tyr Arg Asn Val Met Leu Glu Asn Tyr Lys Asn
35 40 45
Leu Val Ser Leu Gly Tyr Gln Leu Thr Lys Pro Asp Val Ile Leu Arg
50 55 60
Leu Glu Lys Gly Glu Glu Pro Trp Leu Val Glu Arg Glu Ile His Gln
65 70 75 80
Glu Thr His Pro Asp Ser Glu Thr Ala Phe Glu Ile Lys Ser Ser Val
85 90 95
<210> 14
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 14
Asp Gly Gly Gly Ser
1 5
<210> 15
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 15
Thr Gly Glu Lys Pro
1 5
<210> 16
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 16
Leu Arg Gln Lys Asp Gly Glu Arg Pro
1 5
<210> 17
<211> 4
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 17
Gly Gly Arg Arg
1
<210> 18
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 18
Gly Gly Arg Arg Gly Gly Gly Ser
1 5
<210> 19
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 19
Leu Arg Gln Arg Asp Gly Glu Arg Pro
1 5
<210> 20
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 20
Leu Arg Gln Lys Asp Gly Gly Gly Ser Glu Arg Pro
1 5 10
<210> 21
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 21
Leu Arg Gln Lys Asp Gly Gly Gly Ser Gly Gly Gly Ser Glu Arg Pro
1 5 10 15
<210> 22
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 22
Thr Gly Ser Gln Lys Pro
1 5
<210> 23
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 23
Gly Gly Gly Gly Ser
1 5
<210> 24
<211> 28
<212> ДНК
<213> Homo sapiens
<400> 24
taggggccgg ggccggggcc ggggcgtg 28
<210> 25
<211> 28
<212> ДНК
<213> Homo sapiens
<400> 25
cacgccccgg ccccggcccc ggccccta 28
<210> 26
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 26
Leu Arg Gln Lys Asp Ala Ala Arg Gly Ser
1 5 10
<210> 27
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 27
Asp Arg Ser Asp Leu Ser Arg
1 5
<210> 28
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 28
Arg Ser Thr His Leu Val Arg
1 5
<210> 29
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 29
Arg Ser Ala His Leu Ser Arg
1 5
<210> 30
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 30
Glu Arg Gly Asp Leu Lys Arg
1 5
<210> 31
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 31
Glu Arg Gly Thr Leu Ala Arg
1 5
<210> 32
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 32
Arg Ser Ala Asp Leu Ser Glu
1 5
<210> 33
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 33
Arg Ser Asp His Leu Ser Glu
1 5
<210> 34
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 34
Asp Arg Ser His Leu Ala Arg
1 5
<210> 35
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 35
Arg Ser Asp His Leu Ser Gln
1 5
<210> 36
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 36
Asp Asn Ser His Arg Thr Arg
1 5
<210> 37
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 37
Arg Asn Gly His Leu Leu Asp
1 5
<210> 38
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 38
Arg Ser Ala His Leu Ser Glu
1 5
<210> 39
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 39
Arg Ser Asp His Leu Ser Arg
1 5
<210> 40
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 40
Asp Trp Thr Thr Arg Arg Arg
1 5
<210> 41
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 41
His Arg Lys Ser Leu Ser Arg
1 5
<210> 42
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 42
Asp Ser Ser Asp Arg Lys Lys
1 5
<210> 43
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 43
Asp Ser Ser Thr Arg Arg Arg
1 5
<210> 44
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 44
Arg Ser Asp Asp Arg Lys Thr
1 5
<210> 45
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 45
Arg Ser Ala Asp Arg Lys Thr
1 5
<210> 46
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 46
Arg Asn Ala Asp Arg Ile Thr
1 5
<210> 47
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 47
Arg Arg Ala Thr Leu Leu Asp
1 5
<210> 48
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 48
Arg Ser Asp Thr Leu Ser Val
1 5
<210> 49
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 49
Asp Thr Ser Thr Arg Thr Lys
1 5
<210> 50
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 50
Arg Ser Ala Thr Leu Ser Glu
1 5
<210> 51
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 51
His His Arg Ser Leu His Arg
1 5
<210> 52
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 52
Thr Ser Ser Asp Arg Thr Lys
1 5
<210> 53
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 53
Asp Arg Ser His Leu Thr Arg
1 5
<210> 54
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 54
Asp Ser Ser Thr Arg Lys Thr
1 5
<210> 55
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 55
Asp Lys Arg Asp Leu Ala Arg
1 5
<210> 56
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 56
Ser Ser Arg Tyr Arg Thr Lys
1 5
<210> 57
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 57
Arg Glu Gln Asp Leu Lys Gln
1 5
<210> 58
<211> 22
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
праймер"
<400> 58
ctatgtgtgt ggtgggatat gg 22
<210> 59
<211> 22
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
праймер"
<400> 59
ctccaggtta tgtgaagcag aa 22
<210> 60
<211> 26
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
зонд"
<400> 60
aggcctgcta aaggattcaa ctggaa 26
<210> 61
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
праймер"
<400> 61
ccctctctcc ccactacttg 20
<210> 62
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
праймер"
<400> 62
ctacaggctg cggttgtttc c 21
<210> 63
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
зонд"
<400> 63
tctcacagta ctcgctgagg gtga 24
<210> 64
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
праймер"
<400> 64
ctctagcgac tggtggaatt g 21
<210> 65
<211> 22
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
праймер"
<400> 65
gtgcatggca actgtttgaa ta 22
<210> 66
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
праймер"
<400> 66
caaagcctgg tggtgttcaa 20
<210> 67
<211> 20
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
праймер"
<400> 67
ggacatgacc tggttgcttc 20
<210> 68
<211> 25
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
зонд"
<400> 68
cgcggccaga tagacccaat gagca 25
<210> 69
<211> 23
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
праймер"
<400> 69
actacttgct ctcacagtac tcg 23
<210> 70
<211> 22
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
праймер"
<400> 70
tagcgcgcga ctcctgagtt cc 22
<210> 71
<211> 30
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
зонд"
<400> 71
agggaaacaa ccgcagcctg tagcaagctc 30
<210> 72
<211> 22
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
праймер"
<400> 72
tgtgacagtt ggaatgcagt ga 22
<210> 73
<211> 25
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
праймер"
<400> 73
gccacttaaa gcaatctctg tcttg 25
<210> 74
<211> 21
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
зонд"
<400> 74
tcgactcttt gcccaccgcc a 21
<210> 75
<211> 16
<212> ДНК
<213> Homo sapiens
<400> 75
ccggggccgg ggccgg 16
<210> 76
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 76
Leu Arg Gln Lys Asp Ala Ala Arg Gly Ser Gly Gly
1 5 10
<210> 77
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
пептид"
<400> 77
Glu Arg Arg Asp Leu Arg Arg
1 5
<210> 78
<211> 22
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
праймер"
<400> 78
cagcttcggt cagagaaatg ag 22
<210> 79
<211> 17
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
праймер"
<400> 79
aagaggcgcg ggtagaa 17
<210> 80
<211> 24
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
зонд"
<400> 80
ctctcctcag agctcgacgc attt 24
<210> 81
<211> 19
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
праймер"
<400> 81
agtcgctaga ggcgaaagc 19
<210> 82
<211> 19
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
праймер"
<400> 82
cgagtgggtg agtgaggag 19
<210> 83
<211> 25
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
зонд"
<400> 83
aagaggcgcg ggtagaagcg ggggc 25
<210> 84
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
зонд"
<400> 84
ggccccggcc ccggcccc 18
<210> 85
<211> 18
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание ="Описание искусственной последовательности: синтетический
зонд"
<400> 85
ggggccgggg ccggggcc 18
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| МОДУЛЯТОРЫ ТАУ И СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ИХ ДОСТАВКИ | 2017 |
|
RU2789459C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ ХАНТИНГТОНА | 2014 |
|
RU2693891C1 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ ХАНТИНГТОНА | 2015 |
|
RU2691102C2 |
| СПОСОБЫ И СОСТАВЫ ЛЕЧЕНИЯ БОЛЕЗНИ ХАНТИНГТОНА | 2013 |
|
RU2639277C2 |
| ЖИВОТНЫЕ, ОТЛИЧНЫЕ ОТ ЧЕЛОВЕКА, ХАРАКТЕРИЗУЮЩИЕСЯ ЭКСПАНСИЕЙ ГЕКСАНУКЛЕОТИДНЫХ ПОВТОРОВ В ЛОКУСЕ C9ORF72 | 2017 |
|
RU2760877C2 |
| КОНСТРУИРУЕМЫЕ БЕЛКИ С ЦИНКОВЫМИ ПАЛЬЦАМИ, НАПРАВЛЕННЫЕ НА ГЕНЫ РАСТЕНИЙ, ВОВЛЕЧЕННЫЕ В БИОСИНТЕЗ ЖИРНЫХ КИСЛОТ | 2010 |
|
RU2712833C2 |
| КОНСТРУИРУЕМЫЕ БЕЛКИ С ЦИНКОВЫМИ ПАЛЬЦАМИ, НАПРАВЛЕННЫЕ НА ГЕНЫ РАСТЕНИЙ, ВОВЛЕЧЕННЫЕ В БИОСИНТЕЗ ЖИРНЫХ КИСЛОТ | 2010 |
|
RU2568056C2 |
| Двухцепочечная РНК, способная снижать экспрессию мутантного аллеля с.607GA гена GNAO1 человека | 2022 |
|
RU2816137C1 |
| ПЕСТИЦИДНЫЕ КОМПОЗИЦИИ И ОТНОСЯЩИЕСЯ К НИМ СПОСОБЫ | 2013 |
|
RU2662672C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ ГЕМОФИЛИИ В | 2011 |
|
RU2608643C2 |
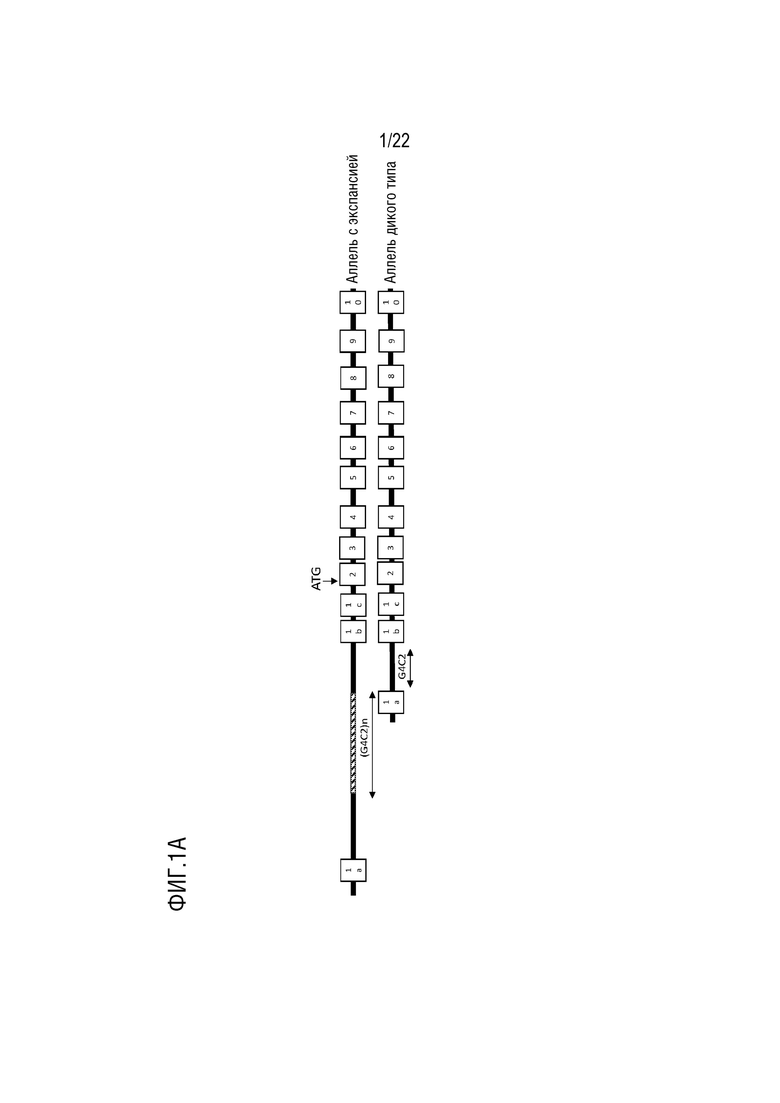
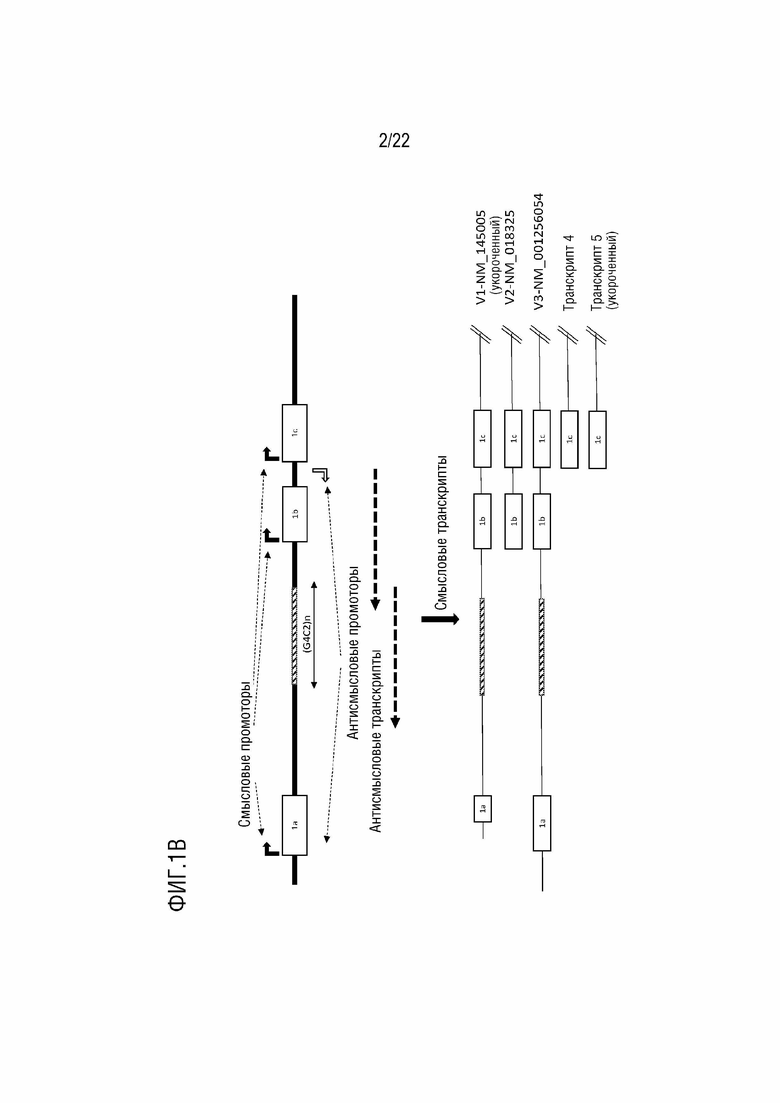
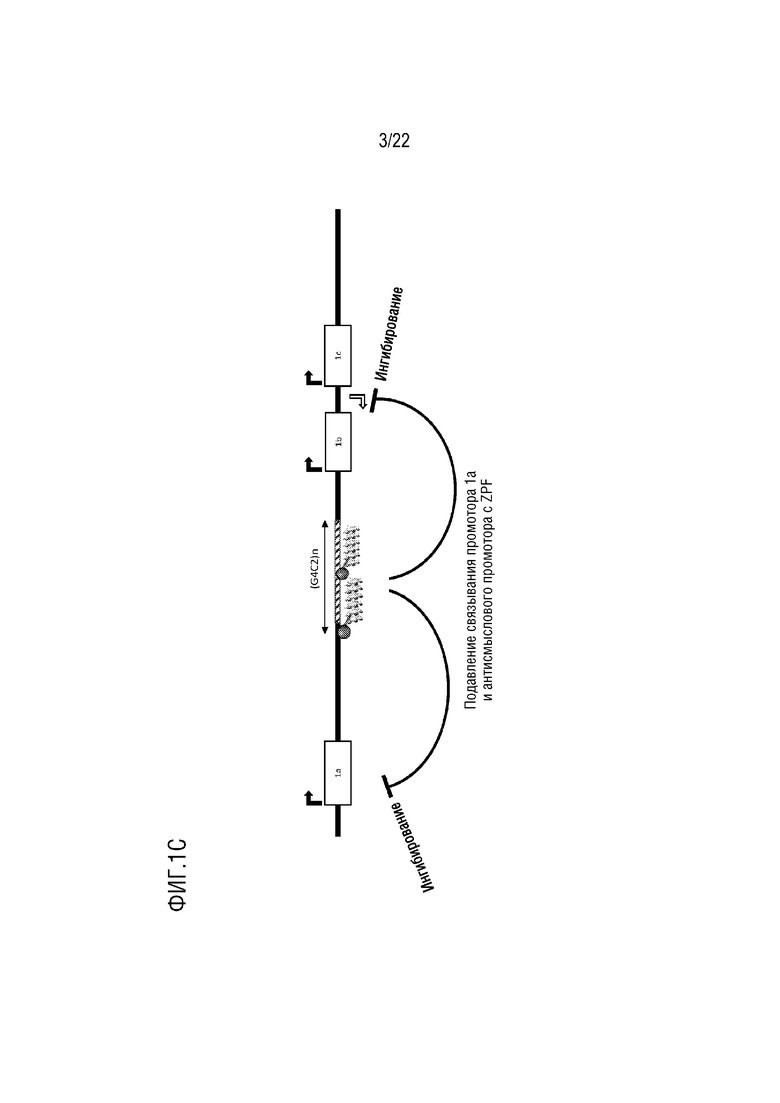
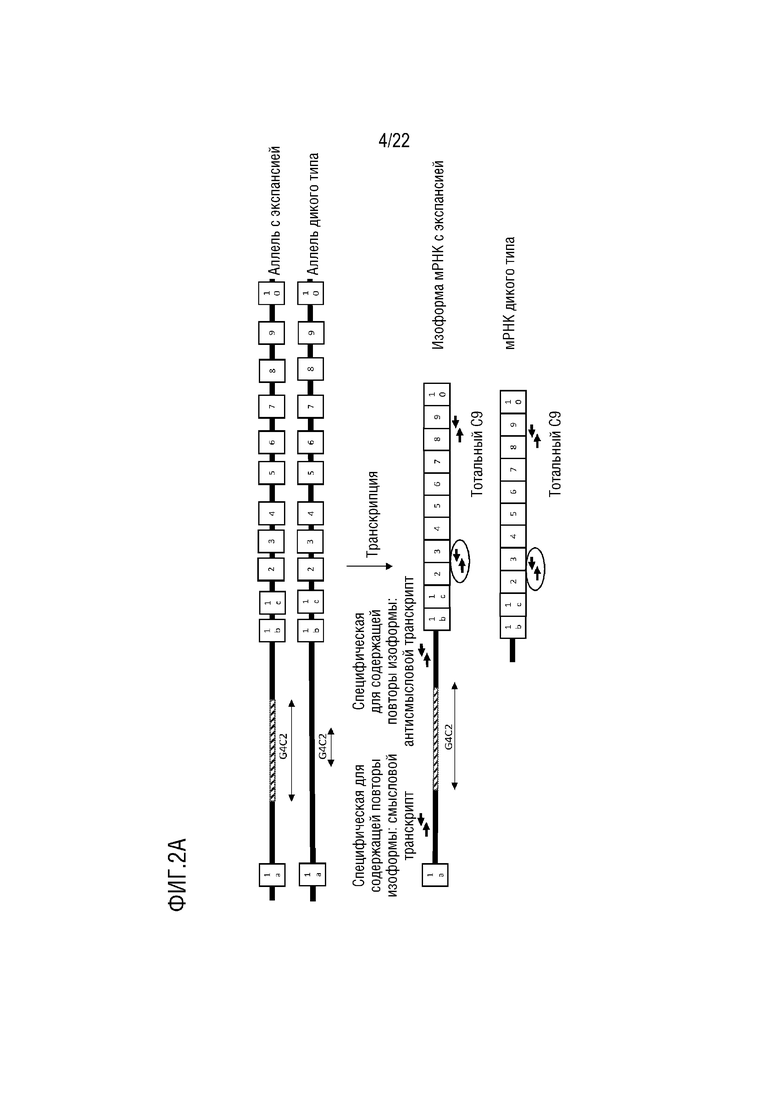
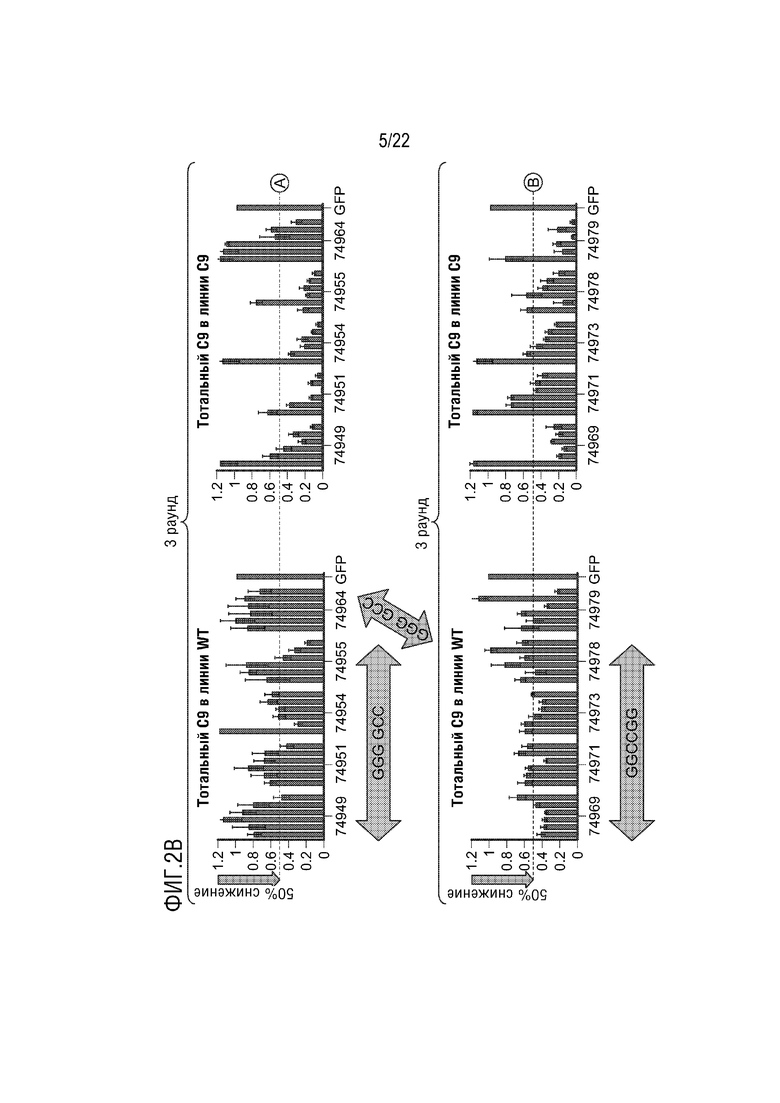
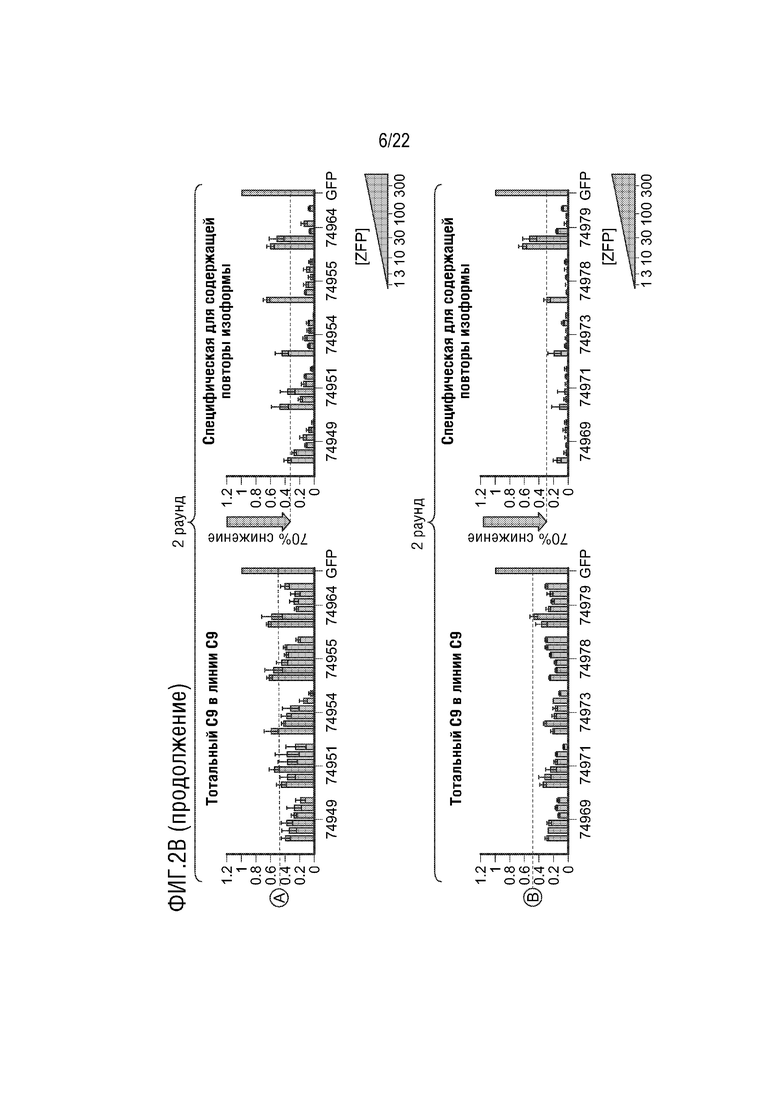
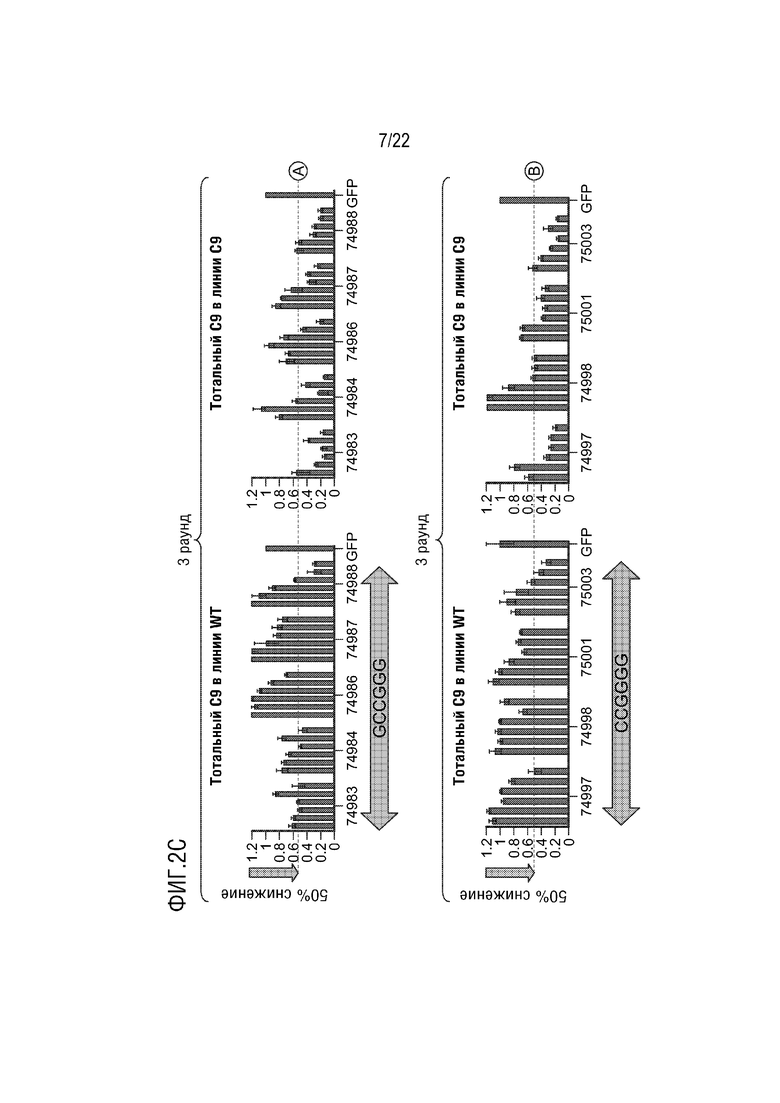
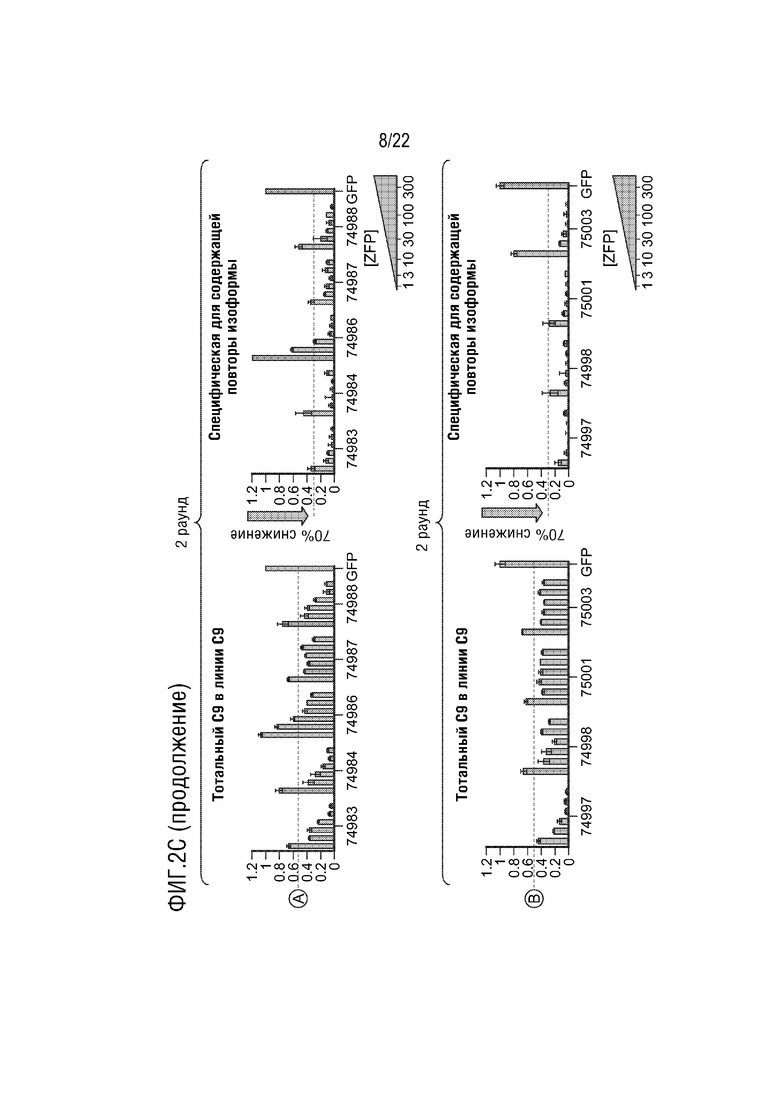
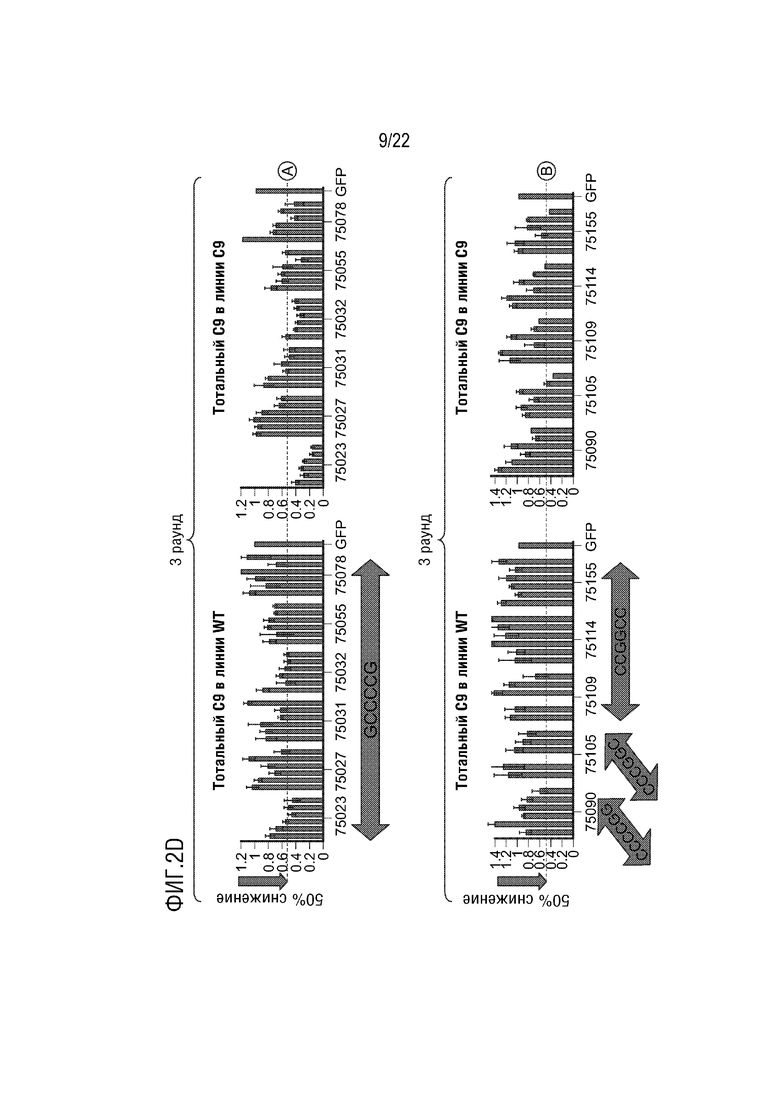
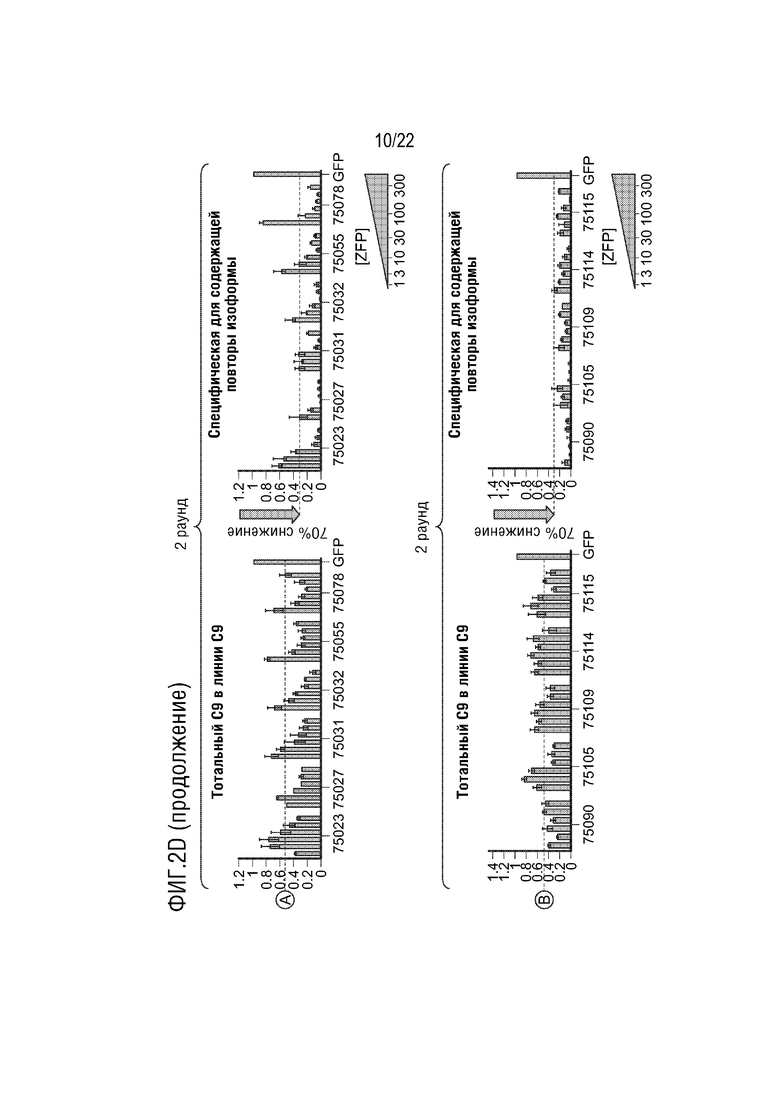
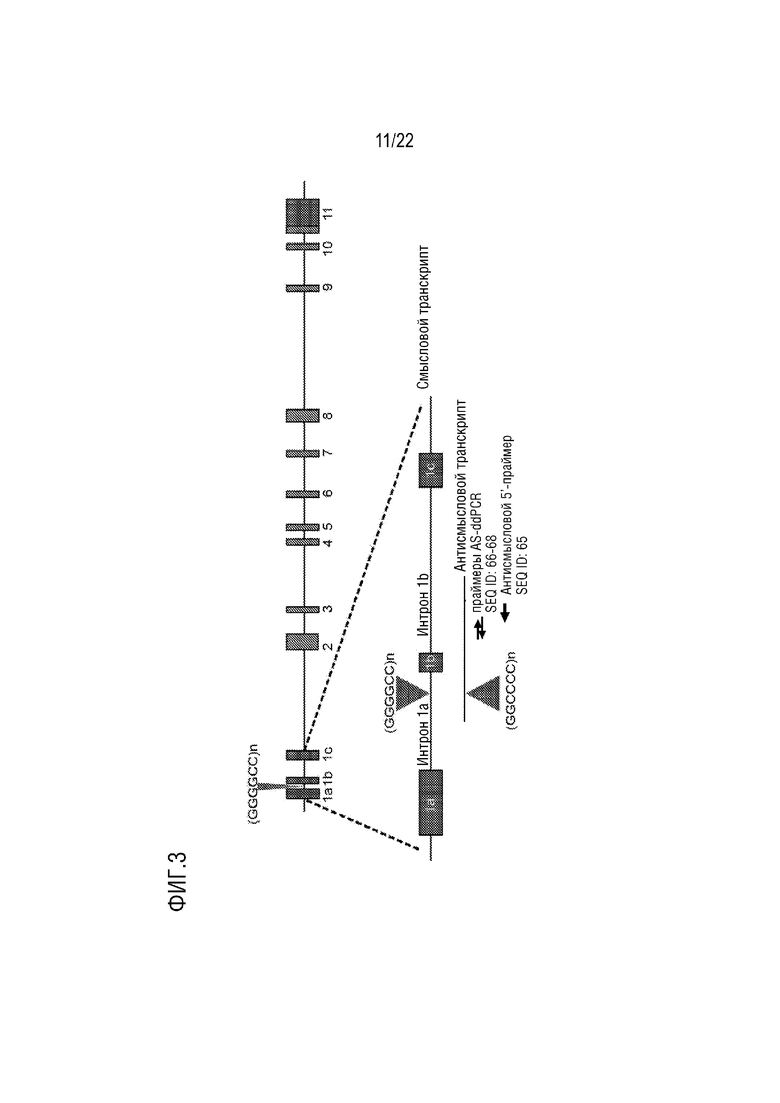
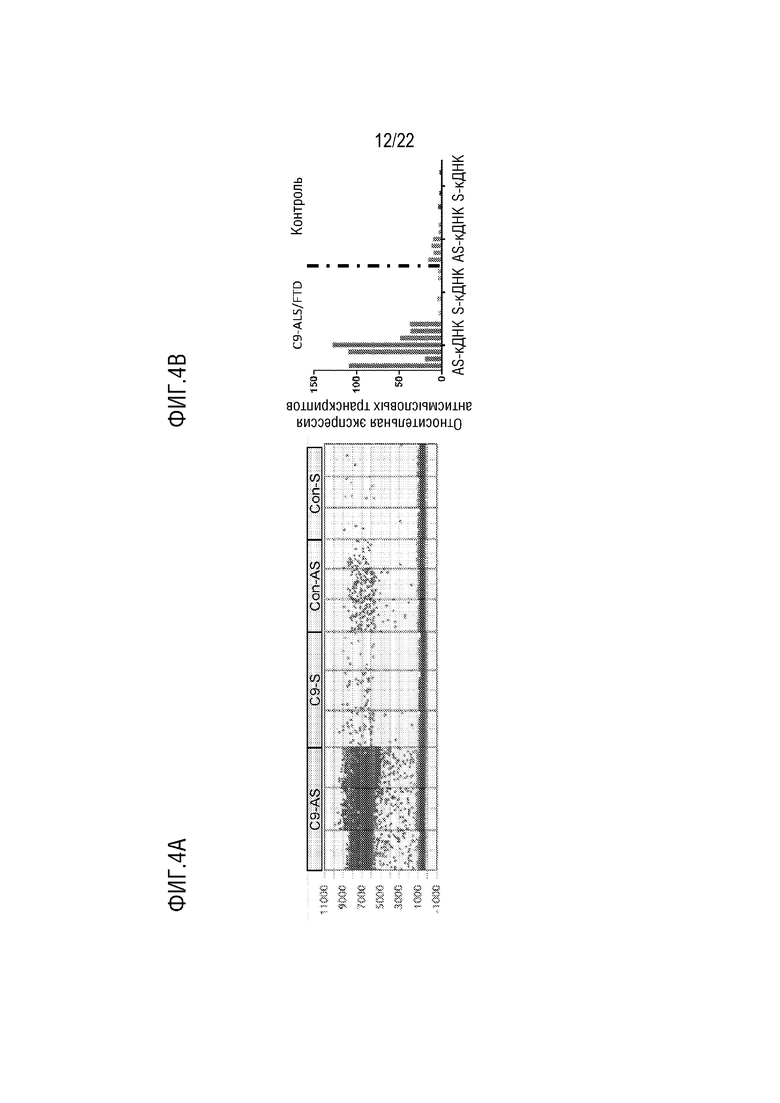



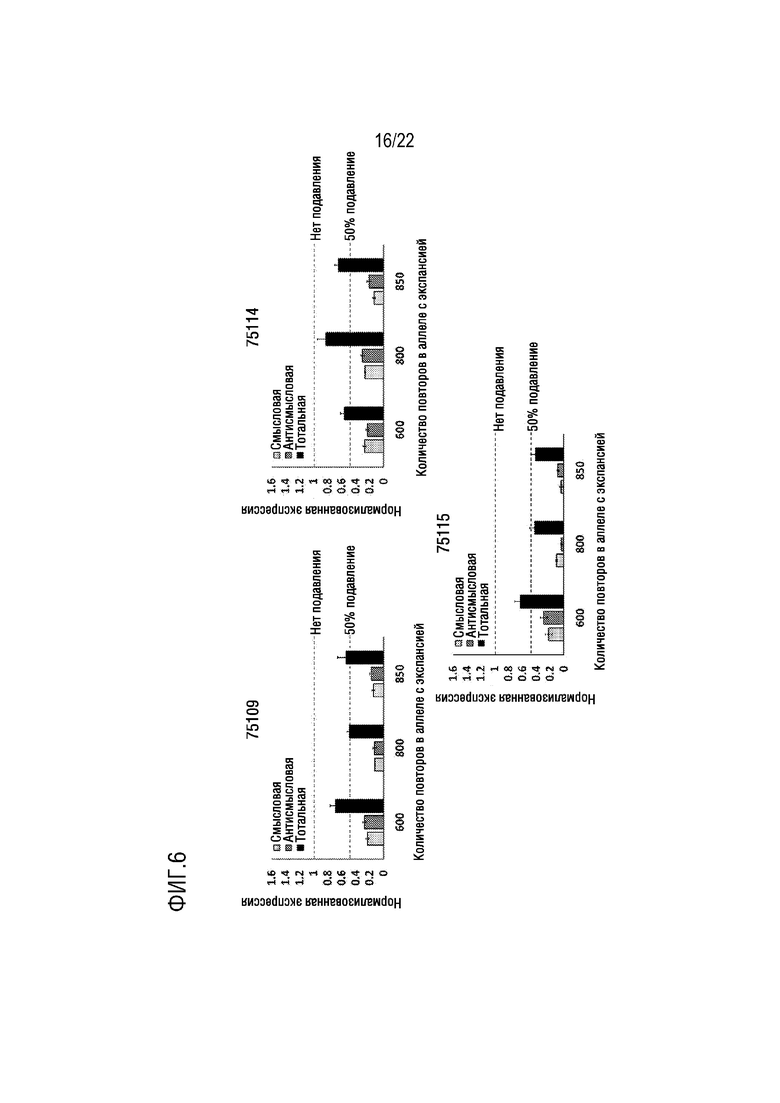
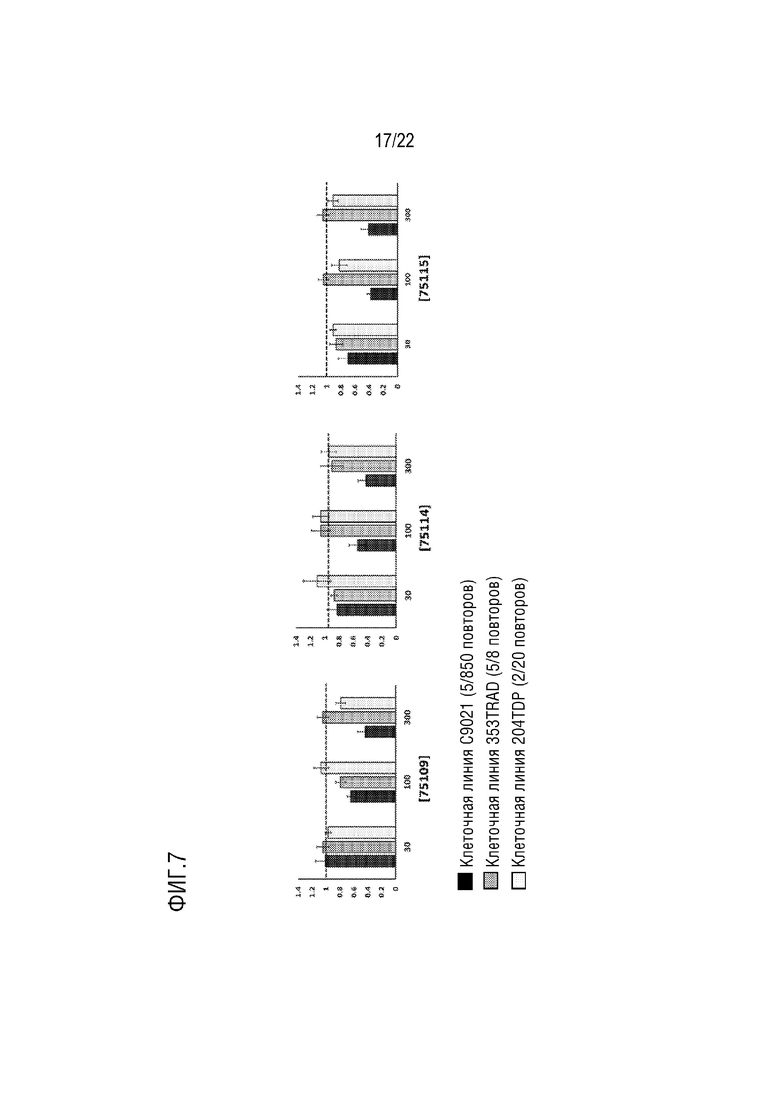

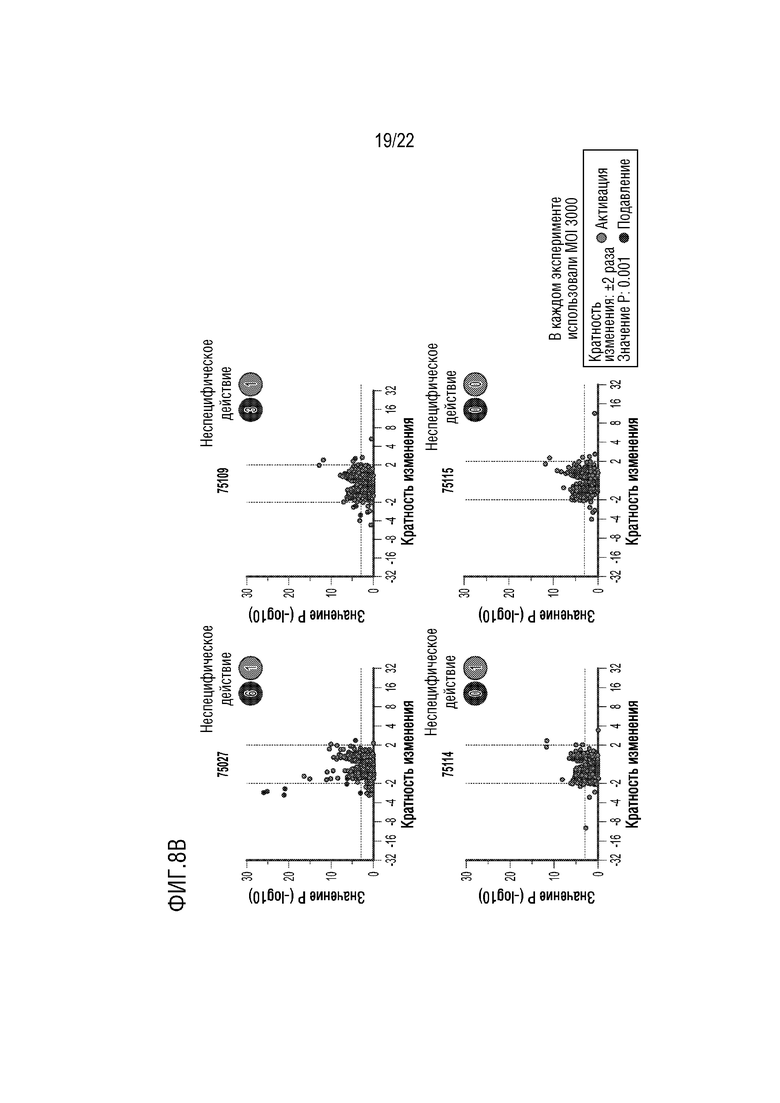
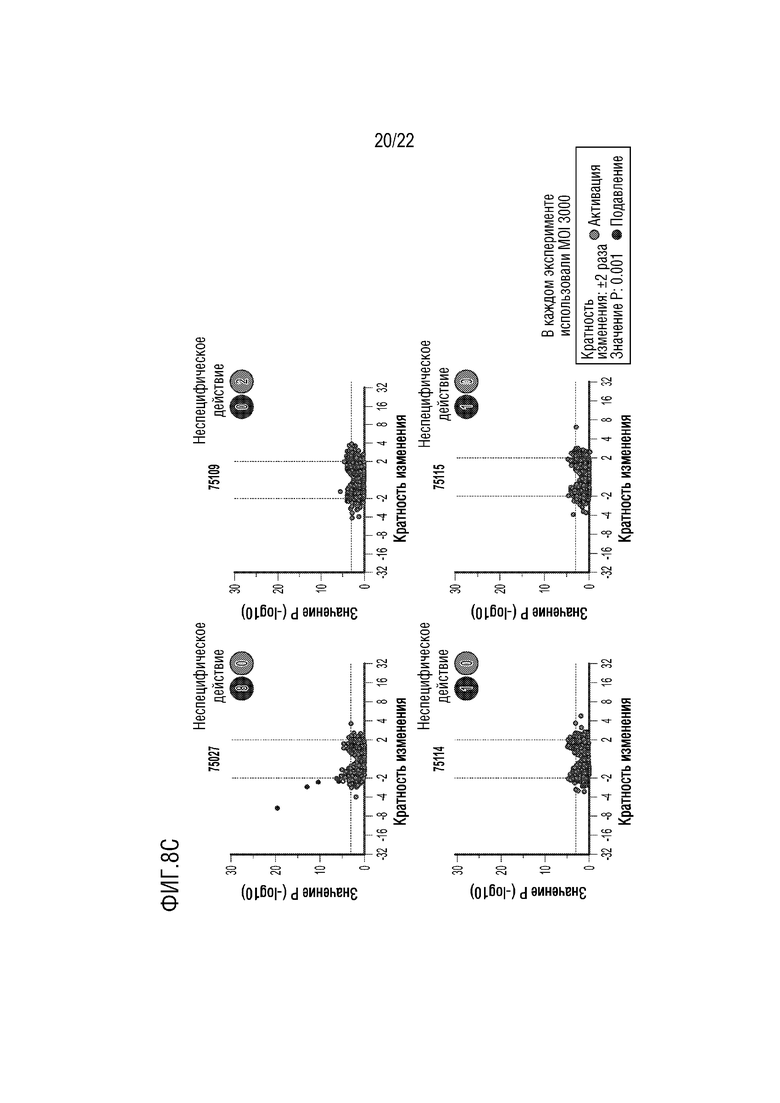
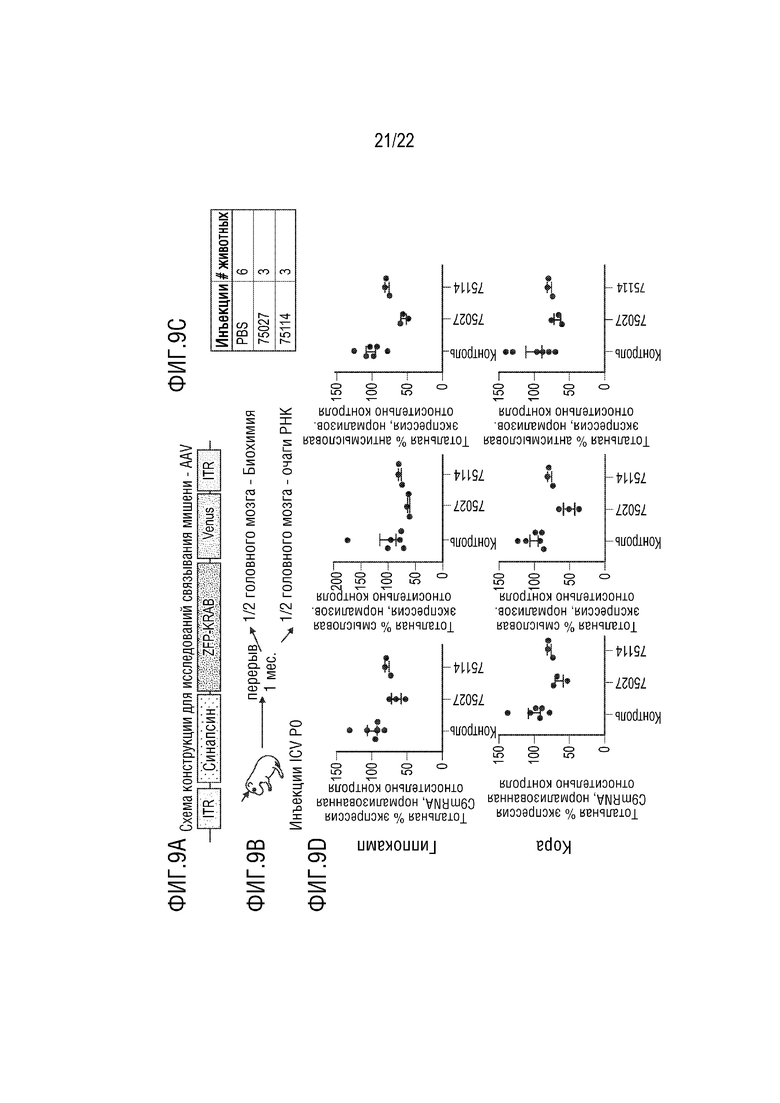
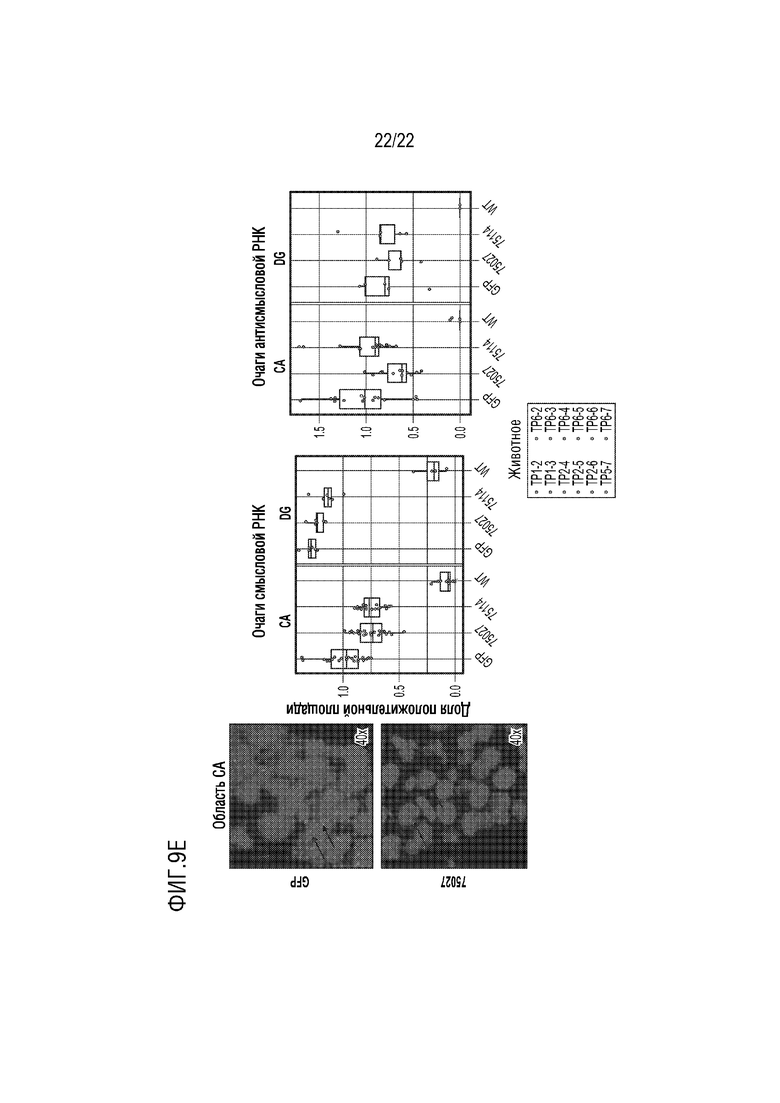
Группа изобретений относится к биотехнологии. Представлены: слитый белок для ингибирования транскрипции мутантного аллеля гена C9orf72 у пациента, нуждающегося в этом, содержащий связывающий ДНК домен белка с цинковыми пальцами (ZFP) и домен репрессора транскрипции, где мутантный аллель C9orf72 содержит более чем 30 тандемных повторов G4C2; конструкция нуклеиновой кислоты для ингибирования транскрипции мутантного аллеля гена C9orf72 у пациента, нуждающегося в этом, содержащая кодирующую последовательность для слитого белка, и её применение для производства лекарственного средства для лечения пациента; клетка-хозяин, содержащая конструкцию нуклеиновой кислоты; рекомбинантный вирус для ингибирования транскрипции мутантного аллеля гена C9orf72 у пациента, нуждающегося в этом, содержащий конструкцию нуклеиновой кислоты. Также раскрыты фармацевтическая композиция для лечения пациента, страдающего от нарушения, выбранного из бокового амиотрофического склероза и семейной лобно-височной деменции, содержащая конструкцию нуклеиновой кислоты; способ ингибирования транскрипции мутантного аллеля гена C9orf72 в клетке человека и способ лечения пациента, страдающего от нарушения, выбранного из бокового амиотрофического склероза и семейной лобно-височной деменции. Изобретение применяется для лечения пациентов, имеющих связанное с C9orf72 заболевание, такое как боковой амиотрофический склероз или лобно-височная деменция. 8 н. и 30 з.п. ф-лы, 22 ил., 1 табл., 4 пр.
1. Слитый белок для ингибирования транскрипции мутантного аллеля гена C9orf72 у пациента, нуждающегося в этом, содержащий связывающий ДНК домен белка с цинковыми пальцами (ZFP) и домен репрессора транскрипции,
где мутантный аллель C9orf72 содержит более чем 30 тандемных повторов G4C2, т.е. SEQ ID NO: 1, и
где связывающий ДНК домен ZFP связывается с сайтом-мишенью в гене C9orf72, где связывающий ДНК домен ZFP содержит шесть пальцев, т.е. F1-F6, соответственно, содержащие области, распознающие спирали, указанные в одном ряду Таблицы, представленной ниже, где домен ZFP содержит одну или несколько мутаций в остатках вне областей, распознающих спирали, и где SEQ ID NO каждой последовательности указан под последовательностью:
27
28
27
28
27
28
27
29
27
29
27
29
30
29
30
29
30
29
31
29
31
29
31
29
32
29
32
29
32
29
33
34
33
34
33
34
35
36
35
36
35
36
37
34
37
34
37
34
37
36
37
36
37
36
38
36
38
36
38
36
29
27
29
27
29
27
39
40
39
40
39
40
29
41
29
41
29
41
29
42
29
42
29
42
29
43
29
43
29
43
29
44
29
44
29
44
29
45
29
45
29
45
29
46
29
46
29
46
29
47
29
47
29
47
48
49
48
49
48
49
46
41
46
41
46
46
45
41
45
41
45
41
50
41
50
41
50
41
45
43
45
43
45
43
32
51
32
51
32
51
33
52
33
52
33
52
53
54
53
54
53
54
55
45
55
45
55
45
31
45
31
45
31
45
77
45
77
45
77
45
33
56
33
56
33
56
57
41
57
41
57
41
46
46
41
46
41
2. Слитый белок по п. 1, где слитый белок подавляет транскрипцию содержащей повторы мРНК с мутантного аллеля и не подавляет транскрипцию с гена мРНК дикого типа.
3. Слитый белок по п. 1 или 2, где домен ZFP связывается со смысловой последовательностью в области-мишени, где смысловая последовательность содержит от одного до трех тандемных повторов гексануклеотида GGGGCC (SEQ ID NO: 1), GGGCCG (SEQ ID NO: 2), GGCCGG (SEQ ID NO: 3), GCCGGG (SEQ ID NO: 4), CCGGGG (SEQ ID NO: 5) или CGGGGC (SEQ ID NO: 6).
4. Слитый белок по любому из пп. 1-3, где слитый белок подавляет смысловую транскрипцию с мутантного аллеля C9orf72 в клетке человека.
5. Слитый белок по п. 4, где слитый белок подавляет смысловую транскрипцию с промотора C9orf72 1a и не подавляет смысловую транскрипцию с промотора C9orf72 1b.
6. Слитый белок по п. 1 или 2, где домен ZFP связывается с антисмысловой последовательностью в области-мишени, где антисмысловая последовательность содержит от одного до трех тандемных повторов гексануклеотидов GGCCCC (SEQ ID NO: 7), GCCCCG (SEQ ID NO: 8), CCCCGG (SEQ ID NO: 9), CCCGGC (SEQ ID NO: 10), CCGGCC (SEQ ID NO: 11) или CGGCCC (SEQ ID NO: 12).
7. Слитый белок по любому из предшествующих пунктов, где слитый белок подавляет антисмысловую транскрипцию с мутантного аллеля C9orf72 в клетке человека.
8. Слитый белок по любому из предшествующих пунктов, где слитый белок подавляет как смысловую транскрипцию, так и антисмысловую транскрипцию с мутантного аллеля C9orf72 в клетке человека.
9. Слитый белок по любому из предшествующих пунктов, где слитый белок подавляет смысловую и/или антисмысловую транскрипцию с мутантного аллеля C9orf72 по меньшей мере приблизительно на 30%, 40%, 75%, 90% или 95%, необязательно где слитый белок не подавляет смысловую транскрипцию с промотора C9orf72 1b.
10. Слитый белок по любому из предшествующих пунктов, где одна или более мутаций представляют собой обусловленные контактом с фосфатами мутации последовательностей ДНК-связывающей распознающей спирали, выбранные из группы, состоящей из:
DRSHLTR (SEQ ID NO: 53), DSSTRKT (SEQ ID NO: 54), DRSHLTR (SEQ ID NO: 53), DSSTRKT (SEQ ID NO: 54), DRSHLTR (SEQ ID NO: 53) и DSSTRKT (SEQ ID NO: 54) для F1-F6 соответственно и замены R- на -Q в положении -5 F1;
DKRDLAR (SEQ ID NO: 55), RSADRKT (SEQ ID NO: 45), DKRDLAR (SEQ ID NO: 55), RSADRKT (SEQ ID NO: 45), DKRDLAR (SEQ ID NO: 55) и RSADRKT (SEQ ID NO: 45) для F1-F6 соответственно и замены R- на -Q в положении -5 F1;
ERRDLRR (SEQ ID NO: 77), RSADRKT (SEQ ID NO: 45), ERRDLRR (SEQ ID NO: 77), RSADRKT (SEQ ID NO: 45), ERRDLRR (SEQ ID NO: 77) и RSADRKT (SEQ ID NO: 45) для F1-F6 соответственно и замены R- на -Q в положении -5 F1;
RSDHLSE (SEQ ID NO: 33), DRSHLAR (SEQ ID NO: 34), RSDHLSE (SEQ ID NO: 33), DRSHLAR (SEQ ID NO: 34), RSDHLSE (SEQ ID NO: 33) и DRSHLAR (SEQ ID NO: 34) для F1-F6 соответственно и замены R- на -Q в положении -5 F2, F3 и F5;
RSDHLSE (SEQ ID NO: 33), DRSHLAR (SEQ ID NO: 34), RSDHLSE (SEQ ID NO: 33), DRSHLAR (SEQ ID NO: 34), RSDHLSE (SEQ ID NO: 33) и DRSHLAR (SEQ ID NO: 34) для F1-F6 соответственно и замены R- на -Q в положении -5 F1, F2, F3 и F5;
RSDHLSE (SEQ ID NO: 33), DRSHLAR (SEQ ID NO: 34), RSDHLSE (SEQ ID NO: 33), DRSHLAR (SEQ ID NO: 34), RSDHLSE (SEQ ID NO: 33) и DRSHLAR (SEQ ID NO: 34) для F1-F6 соответственно и замены R- на -Q в положении -5 F1, F3, F4 и F6;
RSAHLSR (SEQ ID NO: 29), HRKSLSR (SEQ ID NO: 41), RSAHLSR (SEQ ID NO: 29), HRKSLSR (SEQ ID NO: 41), RSAHLSR (SEQ ID NO: 29) и HRKSLSR (SEQ ID NO: 41) для F1-F6 соответственно и замены R- на -Q в положении -5 F1 и F3;
RSAHLSR (SEQ ID NO: 29), HRKSLSR (SEQ ID NO: 41), RSAHLSR (SEQ ID NO: 29), HRKSLSR (SEQ ID NO: 41), RSAHLSR (SEQ ID NO: 29) и HRKSLSR (SEQ ID NO: 41) для F1-F6 соответственно и замены R- на -Q в положении -5 F3 и F5;
RSAHLSR (SEQ ID NO: 29), HRKSLSR (SEQ ID NO: 41), RSAHLSR (SEQ ID NO: 29), HRKSLSR (SEQ ID NO: 41), RSAHLSR (SEQ ID NO: 29) и HRKSLSR (SEQ ID NO: 41) для F1-F6 соответственно и замены R- на -Q в положении -5 F3 и F6;
RSAHLSR (SEQ ID NO: 29), HRKSLSR (SEQ ID NO: 41), RSAHLSR (SEQ ID NO: 29), HRKSLSR (SEQ ID NO: 41), RSAHLSR (SEQ ID NO: 29) и HRKSLSR (SEQ ID NO: 41) для F1-F6 соответственно и замены R- на -Q в положении -5 F2, F3 и F5;
RSAHLSR (SEQ ID NO: 29), HRKSLSR (SEQ ID NO: 41), RSAHLSR (SEQ ID NO: 29), HRKSLSR (SEQ ID NO: 41), RSAHLSR (SEQ ID NO: 29) и HRKSLSR (SEQ ID NO: 41) для F1-F6 соответственно и замены R- на -Q в положении -5 F2, F4 и F6;
REQDLKQ (SEQ ID NO: 57), HRKSLSR (SEQ ID NO: 41), REQDLKQ (SEQ ID NO: 57), HRKSLSR (SEQ ID NO: 41), REQDLKQ (SEQ ID NO: 57) и HRKSLSR (SEQ ID NO: 41) для F1-F6 соответственно и замены R- на -Q в положении -5 F1, F2, F3 и F4;
REQDLKQ (SEQ ID NO: 57), HRKSLSR (SEQ ID NO: 41), REQDLKQ (SEQ ID NO: 57), HRKSLSR (SEQ ID NO: 41), REQDLKQ (SEQ ID NO: 57) и HRKSLSR (SEQ ID NO: 41) для F1-F6 соответственно и замены R- на -Q в положении -5 F2 и F4; и
RNADRIT (SEQ ID NO: 46), HRKSLSR (SEQ ID NO: 41), RNADRIT (SEQ ID NO: 46), HRKSLSR (SEQ ID NO: 41), RNADRIT (SEQ ID NO: 46) и HRKSLSR (SEQ ID NO: 41) для F1-F6 соответственно и замены R- на -Q в положении -5 F1, F2, F3 и F5.
11. Слитый белок по любому из предшествующих пунктов, где домен репрессора транскрипции содержит аминокислотную последовательность домена KRAB из KOX1 человека.
12. Слитый белок по любому из предшествующих пунктов, где домен ZFP связан с доменом репрессора транскрипции через пептидный линкер.
13. Конструкция нуклеиновой кислоты для ингибирования транскрипции мутантного аллеля гена C9orf72 у пациента, нуждающегося в этом, содержащая кодирующую последовательность для слитого белка по любому из пп. 1-12, где кодирующая последовательность функционально связана с элементом регуляции транскрипции и где мутантный аллель C9orf72 содержит более чем 30 тандемных повторов G4C2, т.е. SEQ ID NO: 1.
14. Конструкция нуклеиновой кислоты по п. 13, где элемент регуляции транскрипции представляет собой промотор млекопитающего, который является конститутивно активным или индуцибельным в клетке головного мозга, необязательно где промотор представляет собой промотор синапсина I человека.
15. Конструкция нуклеиновой кислоты по п. 13 или 14, где конструкция представляет собой вирусную конструкцию, необязательно где вирусная конструкция представляет собой рекомбинантную конструкцию аденоассоциированного вируса.
16. Клетка-хозяин для ингибирования транскрипции мутантного аллеля гена C9orf72 у пациента, нуждающегося в этом, содержащая конструкцию нуклеиновой кислоты по любому из пп. 13-15, где мутантный аллель C9orf72 содержит более чем 30 тандемных повторов G4C2, т.е. SEQ ID NO: 1.
17. Клетка-хозяин по п. 16, где клетка-хозяин представляет собой клетку человека.
18. Клетка-хозяин по п. 17, где клетка человека представляет собой нейрон или плюрипотентную стволовую клетку, где стволовая клетка необязательно представляет собой индуцибельную плюрипотентную стволовую клетку (iPSC).
19. Рекомбинантный вирус для ингибирования транскрипции мутантного аллеля гена C9orf72 у пациента, нуждающегося в этом, содержащий конструкцию нуклеиновой кислоты по п. 15, где мутантный аллель C9orf72 содержит более чем 30 тандемных повторов G4C2, т.е. SEQ ID NO: 1, и необязательно где рекомбинантный вирус представляет собой рекомбинантный аденоассоциированный вирус (rAAV).
20. Фармацевтическая композиция для лечения пациента, страдающего от нарушения, выбранного из бокового амиотрофического склероза (ALS) и семейной лобно-височной деменции C9 (C9FTD), содержащая конструкцию нуклеиновой кислоты по любому из пп. 13-15 или рекомбинантный вирус по п. 19 и фармацевтически приемлемый носитель.
21. Способ ингибирования транскрипции мутантного аллеля гена C9orf72 в клетке человека, причем способ включает введение в клетку слитого белка по любому из пп. 1-12, конструкции нуклеиновой кислоты по любому из пп. 13-15, рекомбинантного вируса по п. 19 или фармацевтической композиции по п. 20, где мутантный аллель C9orf72 содержит более чем 30 тандемных повторов G4C2, т.е. SEQ ID NO: 1.
22. Способ по п. 21, где клетка человека представляет собой нейрон, глиальную клетку, эпендимную клетку или нейроэпителиальную клетку.
23. Способ по п. 21 или 22, где клетка находится в головном мозге или спинном мозге пациента, страдающего от связанного с C9orf72 нарушения, выбранного из бокового амиотрофического склероза (ALS) и семейной лобно-височной деменции C9 (C9FTD).
24. Способ лечения пациента, страдающего от нарушения, выбранного из бокового амиотрофического склероза (ALS) и семейной лобно-височной деменции C9 (C9FTD), причем способ включает введение пациенту слитого белка по любому из пп. 1-12, конструкции нуклеиновой кислоты по любому из пп. 13-15, рекомбинантного вируса по п. 19 или фармацевтической композиции по п. 20.
25. Способ по любому из пп. 21-24, где слитый белок вводят посредством рекомбинантного вируса, который экспрессирует слитый белок.
26. Способ по п. 25, где рекомбинантный вирус представляет собой аденоассоциированный вирус (AAV), необязательно серотипа 9 или псевдотипа AAV2/9 или AAV2/6/9.
27. Способ по п. 25 или 26, где рекомбинантный вирус вводят пациенту интрацеребравентрикулярным, интратекальным, внутричерепным, ретроорбитальным (RO), внутривенным, интраназальным и/или интрацистернальным путем.
28. Способ по любому из пп. 21-27, где вводят два или более слитых белка по любому из пп. 1-12, необязательно где кодирующие последовательности для двух или более слитых белков находятся на одном и том же рекомбинантном вирусном векторе.
29. Слитый белок по любому из пп. 1-12, конструкция нуклеиновой кислоты по любому из пп. 13-15, рекомбинантный вирус по п. 19 или фармацевтическая композиция по п. 20 для применения в способе по любому из пп. 21-28.
30. Применение конструкции нуклеиновой кислоты по любому из пп. 13-15 или рекомбинантного вируса по п. 19 для производства лекарственного средства для лечения пациента, нуждающегося в этом, в способе по любому из пп. 24-28.
31. Слитый белок по п. 1, где связывающий ДНК домен ZFP содержит шесть пальцев, соответственно содержащих SEQ ID NO: 33, 34, 33, 34, 33 и 34.
32. Слитый белок по п. 1, где связывающий ДНК домен ZFP содержит шесть пальцев, соответственно содержащих SEQ ID NO: 29, 41, 29, 41, 29 и 41.
33. Слитый белок по п. 1, где связывающий ДНК домен ZFP содержит шесть пальцев, соответственно содержащих SEQ ID NO: 53, 54, 53, 54, 53 и 54.
34. Слитый белок по п. 1, где связывающий ДНК домен ZFP содержит шесть пальцев, соответственно содержащих SEQ ID NO: 55, 45, 55, 45, 55 и 45.
35. Слитый белок по п. 1, где связывающий ДНК домен ZFP содержит шесть пальцев, соответственно содержащих SEQ ID NO: 77, 45, 77, 45, 77 и 45.
36. Слитый белок по п. 1, где связывающий ДНК домен ZFP содержит шесть пальцев, соответственно содержащих SEQ ID NO: 33, 56, 33, 56, 33 и 56.
37. Слитый белок по п. 1, где связывающий ДНК домен ZFP содержит шесть пальцев, соответственно содержащих SEQ ID NO: 57, 41, 57, 41, 57 и 41.
38. Слитый белок по п. 1, где связывающий ДНК домен ZFP содержит шесть пальцев, соответственно содержащих SEQ ID NO: 46, 41, 46, 41, 46 и 41.
| Разборный с внутренней печью кипятильник | 1922 |
|
SU9A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2024-10-08—Публикация
2020-04-23—Подача