Изобретение относится к моноклональным антителам, специфичным к различным штаммам респираторно-синцитиального вируса, в частности, полученным с помощью гибридомы, и могут быть использованы в диагностике, в частности, в диагностических тест-системах.
По оценкам ВОЗ ежегодные эпидемии сезонных заболеваний приводят к 3–5 миллионам случаев тяжёлой болезни и 250 000–500 000 случаев смерти во всём мире. Вирусы, вызывающие простудные заболевания, легко передаются от человека человеку воздушно-капельным путём при выделении инфицированными людьми мельчайших частиц во время кашля или чихания. При этом вирус имеет тенденцию быстро распространяться, вызывая сезонные эпидемии. Большинство инфицированных людей выздоравливает за одну-две недели без какого-либо лечения. Однако для детей, пожилых людей и людей, страдающих серьёзными заболеваниями, такие вирусы представляют опасность — они могут привести к осложнениям основных заболеваний, развитию пневмонии и смерти (WHO, 2017).
Основными причинами ОРВИ у детей и взрослых являются вирусы гриппа (ВГ) типов A, B и C; вирус парагриппа (ВПГ) типов 1, 2 и 3; респираторно-синцитиальный вирус (РСВ); аденовирус (АВ) и риновирус. Все упомянутые вирусы могут вызвать как инфекцию верхних, так и нижних дыхательных путей, кроме того имеют сходные клинические проявления и зачастую не могут быть различены без специальной лабораторной диагностики (Mahony et al., 2011).
Острые респираторные заболевания занимают ведущее место в структуре инфекционных болезней человека и обуславливают 20–50% временных потерь трудоспособности. Экономический ущерб от ОРЗ можно сравнить лишь с затратами на профилактику и лечение длительно текущих сердечно-сосудистых и онкологических заболеваний.
Наиболее важное место в развитии патологии дыхательных путей занимают вирусы гриппа и парагриппа, респираторно-синцитиальный вирус, аденовирусы.
В большинстве случаев заболевания, вызванные этими патогенами, имеют благоприятное течение в виде заболеваний верхних дыхательных путей. Однако у части пациентов, особенно при наличии иммуносупрессии, а также у детей младшего возраста, эти вирусы вызывают осложнённое течение заболевания.
Респираторные вирусы способны выступать в качестве пусковых механизмов возникновения гиперреактивности бронхов, обструкции дыхательных путей и атопий, что способствует формированию хронических обструктивных заболеваний лёгких, включая бронхиальную астму (БА) (Matsumoto & Inoue, 2014). Так, при обострении БА наличие РСВ, ПГ 1 и 3 типов, АВ или вирусов гриппа А или В детектировали в 10–85% случаев у детей и до 44–74% у взрослых (Message et al., 2004; Чучалин и др., 2007; Westerly & Peebles, 2010; Kurai et al., 2013).
Респираторные вирусы являются частой причиной внутрибольничных пневмоний: в 17%, 6% и 4% случаев детектировали РСВ, вирусы парагриппа и гриппа, соответственно (Ning et al., 2017; Walter & Wunderink, 2017).
Дифференциальная диагностика респираторных инфекций необходима для осуществления надзора за заболеваемостью и назначения своевременной терапии, поскольку многие препараты эффективны только на ранних стадиях инфекции. Понимание истинной причины заболевания помогает избежать ненужного использования антибиотиков, которые часто назначают пациентам, инфицированным респираторными вирусами. Быстрое и достоверное обнаружение респираторных патогенов позволяет врачам избежать возникновения внутрибольничных заболеваний, а также прогнозировать возможные осложнения и иммунопатологические явления, которые могут возникнуть при этих инфекциях. Использование точных диагностических тестов даёт возможность клиницистам своевременно поставить диагноз и выявить группы риска. В диагностическом алгоритме должны быть использованы маркеры-индикаторы присоединения бактериальной инфекции. Своевременная дифференциальная диагностика вирусной и бактериальной инфекций особенно актуальна для детей при схожести симптоматики заболеваний, которые могут приводить к неблагоприятному исходу, особенно в группах риска.
Использование при конструировании диагностических тест-систем моноклональных антител (МКА), специфичных к вирусам ОРЗ, обеспечивает высокую чувствительность и специфичность анализа, а также выбор правильной схемы лечения.
Выбор мишеней, к которым должны быть направлены МКА, определяется представительством антигенных детерминант в составе самого вируса и в исследуемых клинических материалах, а также степенью консервативности/вариабельности сайтов-мишеней.
В соответствии с данными литературы о приоритетной роли РСВ в структуре как острых, так и хронических респираторных заболеваний, именно к этому вирусу была получена панель МКА с целью создания диагностической тест-системы на основе ИФА.
Респираторно-синцитиальный вирус (РСВ) и РСВ-инфекция (РСВИ)
РСВИ играет чрезвычайно важную роль в структуре инфекционной патологии дыхательного тракта, особенно у детей первых лет жизни. Заболеваемость РСВИ может превышать таковую, наблюдаемую для гриппа (Lee et al., 2013; Matias et al., 2014). 70% детей переносят РСВИ в возрасте до 1 года, и практически каждый инфицируется в течение первых трёх лет. В развитых индустриальных странах у детей в возрасте до 3 лет, госпитализированных с острыми респираторными заболеваниями с поражением нижних отделов дыхательного тракта, частота диагностирования РСВИ достигает 42–63%. При этом РСВ является причиной 50–90% бронхиолитов, 5–40% пневмоний, 10–30% трахеобронхитов. Согласно метаанализу мировой литературы в развитых странах среди детей, госпитализированных с РСВИ, смертность составляет в среднем 1% (Simoes & Carbonell-Estrany, 2003; Nair et al., 2010; Karron, 2012; Borchers et al., 2013; Bont et al., 2016). Среди госпитализированных пациентов в возрасте до 18 лет с осложнённым анамнезом летальность может достигать 37% (Welliver et al., 2010). Преклонный возраст также является фактором риска тяжёлого течения РСВИ (Lee et al., 2013; Branche & Falsey, 2015).
РСВ является мощным иммуномодулятором и оказывает выраженное иммуносупрессорное действие (Mukherjee et al., 2013; Varga et al., 2013; Gomez et al., 2014). В этой связи индуцируемый им иммунный ответ зачастую оказывает слабое и кратковременное протективное действие, что обуславливает осложнённое течение РСВИ и реинфекции, которые наблюдаются у людей на протяжении всей жизни.
РСВ в значительно большей степени, чем другие часто встречающиеся респираторные вирусы, способствует развитию иммунопатологических проявлений, в том числе обструкции нижних дыхательных путей (Falsey et al., 1995; Byeon et al., 2009), что является специфическим фактором риска, особенно для новорождённых. До 70% детей в возрасте до 1 года, госпитализированных с бронхиолитами, обусловленными РСВ, подвержены рецидивирующим эпизодам бронхообструкции в течение последующих 6–12 лет (Hyvärinen et al., 2007), что связано с риском развития в дальнейшем бронхиальной астмы (Feldman et al., 2015). РСВ у взрослых с неблагоприятным преморбидным фоном способствует развитию хронических лёгочных заболеваний — хронической обструктивной болезни лёгких и бронхиальной астмы (Чучалин и др., 2007). При обследовании пациентов с хронической бронхолёгочной патологией, в частности с бронхиальной астмой, ухудшение общего состояния в 50% случаев вызвано РСВИ (Кривицкая и др., 2015). РСВИ представляет большую опасность для реципиентов костного мозга (Lehners et al., 2016). Частота летальных исходов от РСВИ, регистрируемая среди госпитализированных пациентов в возрасте до 18 лет, составляет около 37% при осложнённом анамнезе (Welliver et al., 2010).
РСВ человека относятся к роду Pneumovirus семейства Paramyxoviridae. Вирионы содержат несегментированную однонитевую антисмысловую минус-РНК. Оболочку вириона составляют 2 основных трансмембранных гликопротеина: белок присоединения G (attachment protein) и белок слияния F (fusion protein), которые являются основными индукторами синтеза РСВ-нейтрализующих антител. РСВ человека существует в виде одного серотипа, но состоит из двух антигенных групп (А и В), что было установлено на основании различий в реагировании МКА (Anderson et al., 1985). Изоляты РСВ из различных групп отличаются генетически. Степень межгрупповых (А/В) отличий в аминокислотных последовательностях (АП) очень сильно варьирует для белков РСВ. Для наиболее консервативных F- и N-белков (внутренний белок, элемент кора вириона) показано до 91% и 96% гомологии АП, соответственно. Наиболее вариабельным из всех является G-белок — только 53–58% гомологии АП между эталонными штаммами РСВ-А и РСВ-В (Collins et al., 2001; Collins & Karron, 2013).
С учётом представленных данных наиболее рациональным для выявления РСВ представляется использование МКА к консервативному F-белку.
Ранее в документе RU 2371726 были описаны антитела к РСВ в составе диагностической тест-системы на основе ИФА для определения уровня антител к вирусным респираторным заболеваниям крупного рогатого скота, однако данные антитела не характеризовались высокой специфичностью именно к РСВ и не были предназначены для диагностики человеческой инфекции.
Таким образом, проблема получения антител, которые бы имели высокую специфичность именно к РСВ, в частности, к группам А и В, и не имели бы специфичности к другим вирусам, является крайне актуальной.
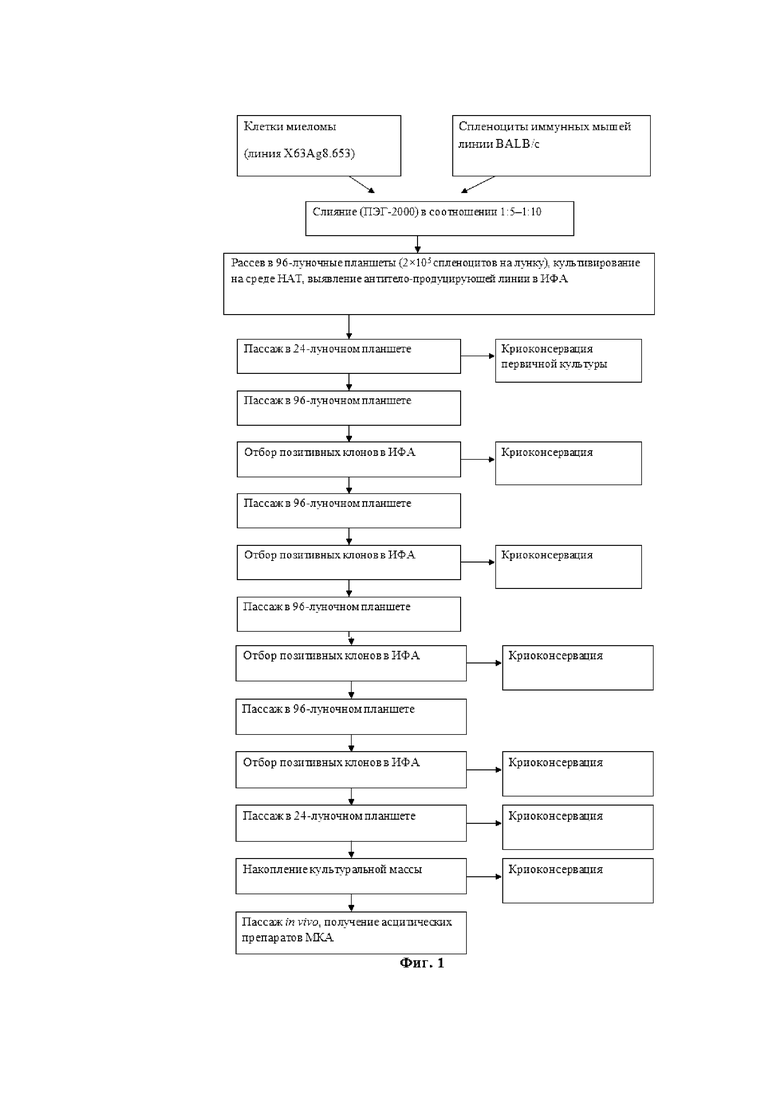
На Фиг. 1 показана схема получения гибридом — продуцентов МКА.
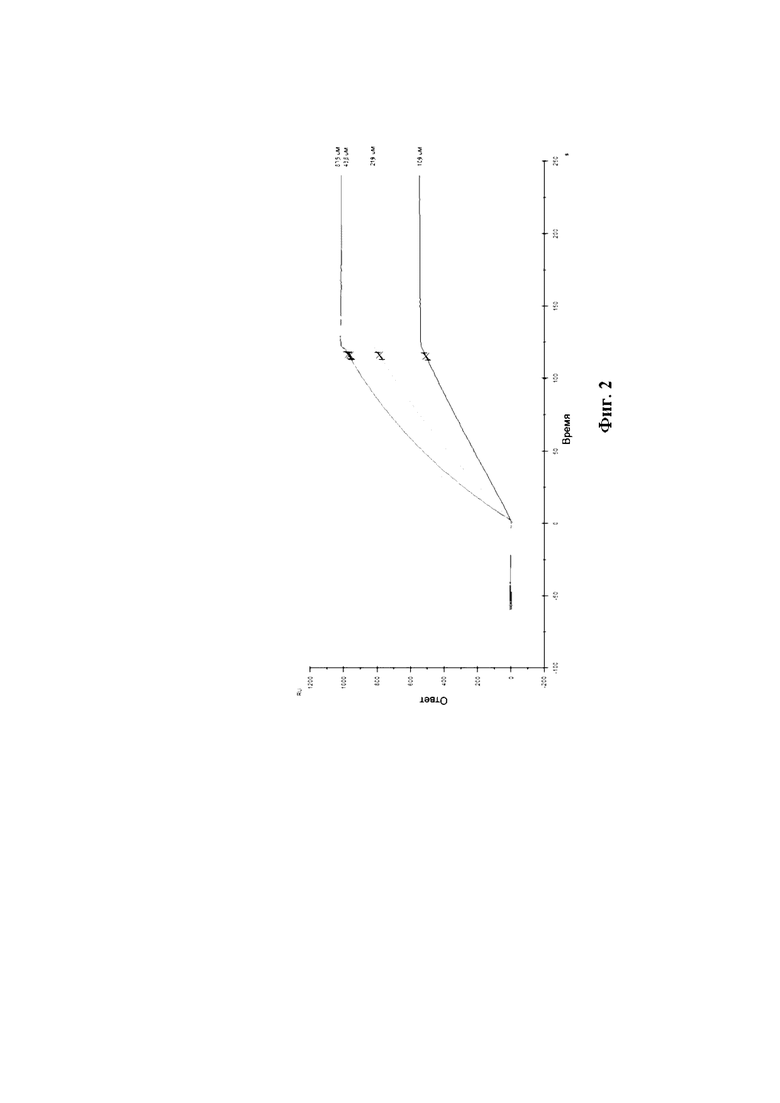
На Фиг. 2 приведена сенсограмма взаимодействия моноклональных антител клона 10G6 с анализируемым штаммом респираторно-синцитиального вируса.
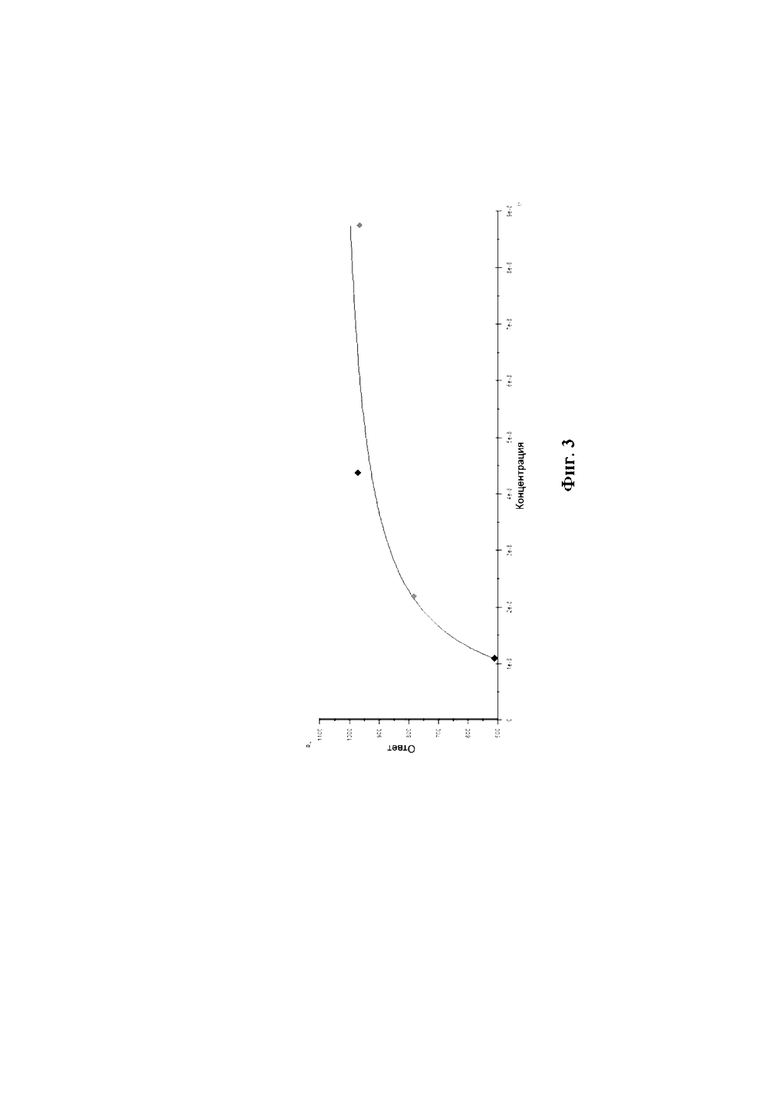
На Фиг. 3 представлена диаграмма аффинности моноклональных антител клона 10G6 к респираторно-синцитиальному вирусу.
Описание изобретения
Данное изобретение описывает моноклональные антитела, специфичные к штаммам респираторно-синцитиального вируса, относящимся к группам А и В, и имеющие высокую специфичность к F-белку. При этом данные антитела представляют собой антитела IgG типа, в частности, мышиные моноклональные антитела.
Описанные антитела могут быть получены способом, включающим:
- получение антитело-продуцирующих спленоцитов;
- накопление клеток мышиной миеломы;
- слияние антитело-продуцирующих спленоцитов с миеломными клетками;
- отбор гибридом;
- введение гибридомы в брюшную полость праймированных пристаном мышей;
- накопление моноклональных антител в асцитах;
- очистка полученных моноклональных антител.
Для получения и накопления антител могут быть использованы специально полученные гибридомы-продуценты моноклональных антител, направленных к F-белку респираторно-синцитиального вируса групп А и В. Такие гибридомы как представители гибридом-продуцентов моноклональных антител, направленных к F-белку респираторно-синцитиального вируса групп А и В, были депонированы как 11G4/RS под номером РККК(П) 786Д, и как 10G6/RS под номером РККК(П) 784Д в Специализированную коллекцию культур клеток ЦКП «Коллекция культур клеток позвоночных» ФГБУН Института цитологии РАН, соответственно.
Моноклональные антитела согласно изобретению могут быть использованы для идентификации респираторно-синцитиального вируса групп А и В, в частности, в диагностических тест-системах.
Более подробно получение и анализ указанных моноклональных антител иллюстрируют примеры, приведённые ниже.
Примеры
Пример 1
Получение МКА к белкам респираторно-синцитиального вируса
Процесс получения гибридом-продуцентов МКА к консервативным эпитопам в составе респираторно-синцитиального вируса состоял из нескольких стадий.
Стадия 1. Очистка вирусов, предназначенных для использования в качестве иммуногена.
Эталонный штамм РСВ, принадлежащий к антигенной группе Long (группа А), полученный из National Institute for Medical Research (Лондон), культивировали в перевиваемой клеточной культуре МА-104 (эпителиальные клетки почки обезьяны) в течение 5–7 суток. В качестве поддерживающей бессывороточной среды использовали среду alpha-МЕМ («Биолот», Россия). Вируссодержащую культуральную жидкость использовали для очистки и концентрации вируса путём ультрацентрифугирования в градиенте плотности сахарозы по методу Orvell (Orvell et al., 1978). Для этого вирусы из культуральной среды осаждали ультрацентрифугированием при 50 000 g в течение 2 ч, суспендировали в малом количестве 10 мМ трис-ЭДТА буфера, рН 7,2 (STE) и производили очистку через градиент 20–60% сахарозы ультрацентрифугированием при 100 000 g в течение 2,5 ч с последующим осаждением вируса из зоны 36–40% сахарозы на дно при 120 000 g в течение 1 ч. Осадок ресуспендировали в STE. Содержание белка в очищенном вирусном материале определяли с использованием набора “Pierce BCA Protein assay kit” (“Thermo Fisher Scientific”, США). Наличие вирусной контаминации и целостность полученных вирионов контролировали с помощью электронной микроскопии. Полученные цельновирионные вирусные суспензии хранили при –80°С.
Стадия 2. Получение антитело-продуцирующих спленоцитов в результате иммунизации мышей соответствующим антигеном под контролем образования специфических сывороточных антител в ИФА.
Мышей линии BALB/c иммунизировали очищенным антигеном, полученным на стадии 1, смешанным с неполным адъювантом Фрейнда путём внутрибрюшинного введения (иммунизации) очищенного ультрацентрифугированием в градиенте плотности сахарозы антигена РСВ в концентрации 50–100 мкг/мл (по 1 мл на мышь). Затем проводили мониторинг иммунизированных животных на образование специфических антител. Животных с достаточно высоким титром антител отбирали в качестве источника антитело-продуцирующих клеток.
Инъекции антигенов проводили двукратно с интервалом в 5 недель. Спустя 7 дней после каждой иммунизации из ретробульбарного синуса мышей брали пробы крови для определения титра сывороточных антител против гомологичного РСВ или рекомбинантного белка в ИФА. Через две недели после последней иммунизации мышей, имевших по данным ИФА антитела в титре 1:10000, бустировали антигеном, полученным на стадии 1, или рекомбинантным белком.
Стадия 3. Определение титра сывороточных антител в ИФА.
Очищенный концентрат РСВ сорбировали на твёрдой поверхности (96-луночный планшет для ИФА) в концентрации 1–5 мкг/мл. После промывания планшета в лунки с сорбированным антигеном вносили серийные двукратные разведения сыворотки от иммунизированной мыши (от 1:10 до 1:20480) и инкубировали в течение часа при температуре 37°C. Для выявления сформированного комплекса антигена с антителом добавляли антитела против IgG мыши, меченные пероксидазой хрена (HRP). После промывания в планшет добавляли субстратную смесь для фермента. В качестве субстрата на стадии детекции использовали раствор ТМБ (3,3’,5,5’-тетраметилбензидин) в концентрации 100 мкг/мл с 0,03% Н2О2. Титр антител оценивали по изменению оптической плотности раствора, регистрируемой спектрофотометрически на фотометре Multiscan FC при длине волны 450 нм.
Стадия 4. Накопление клеток мышиной миеломы.
Через 3 дня после бустер-иммунизации мышь использовали в качестве донора лимфоцитов селезёнки для слияния с клетками мышиной миеломы в целях получения гибридом (Новохатский и др., 1985; Новиков и др., 1988). Для этого проводили гибридизацию спленоцитов иммунизированных мышей с клетками мышиной миеломы в присутствии 50% ПЭГ-2000. В качестве партнёра для слияния при получении гибридом использовали культуру клеток мышиной миеломы линии Х63Аg8.653, адаптированную к росту в среде с добавлением сыворотки крови крупного рогатого скота (КРС), полученную из коллекции ФГБУ «РНЦРХТ». Данный штамм является устойчивым к 8-азагуанину, то есть дефектным по гену гипоксантин-гуанин-фосфорибозил трансферазы.
Выбранную клеточную линию культивировали на среде RPMI-1640 c добавлением глутамина, 2-меркаптоэтанола (МЭ), гентамицина и сыворотки КРС для обеспечения в день слияния со спленоцитами плотности популяции не менее 2×107 клеток/мл. Культивирование миеломы осуществляли в пластиковых культуральных планшетах или во флаконах производства “Sarstedt” или “Nunc” (Германия, США). Клетки размножали при температуре 36–37°С и 100% влажности в атмосфере воздуха с 5–7% СО2. Базовая культуральная среда содержала 90% RPMI-1640 и 10% сыворотки КРС («Биолот», Санкт-Петербург).
Стадия 5. Слияние антитело-продуцирующих спленоцитов с миеломными клетками.
Для получения антитело-продуцирующих клеток у мышей с высокими титрами специфических антител через 3–4 дня после последней бустер-иммунизации удаляли селезёнку и вымывали из неё спленоциты бессывороточной средой (такой как RPMI-1640) или забуференным физиологическим раствором, после чего их смешивали с миеломными клетками в соотношении от 5:1 до 10:1. Затем клетки центрифугировали (10 мин, 1000 об/мин), осадок разрыхляли, после чего, перемешивая, по каплям добавляли 1 мл бессывороточной среды, содержащей 50% (масс/об) ПЭГ (молекулярный вес 1000–4000 Да). Затем медленно добавляли 10 мл бессывороточной среды, после чего смесь центрифугировали.
Осаждённые клетки суспендировали в соответствующем количестве селективной НАТ-среды. Затем клетки переносили в селективную НАТ-среду, приготовленную на основе RPMI-1640 и 20% сыворотки крупного рогатого скота (СКРС) с добавлением гипоксантина (10–4 М), аминоптерина (4×10–7 М) и тимидина (1,6×10–5 М) производства “Sigma-Aldrich” (США), а также 2 мМ глютамина, 1 мМ пирувата натрия (“Sigma-Aldrich”, США), 1 мг/л амфотерицина В и 50 мг/л гентамицина. Суспензию распределяли по ячейкам 96-луночных планшетов для культивирования, содержащих трёхсуточную культуру мышиных макрофагов, и инкубировали в атмосфере 5–7% СО2 при температуре 37°С в течение 3 недель. После 10 суток культивирования НАТ-среду заменяли на более щадящую НТ-среду, а после 20 суток культуры поддерживали на среде RPMI-1640 с СКРС. Для удаления иммуноглобулинов, секретированных неслившимися спленоцитами мышей, культуральную жидкость из ячеек с растущими гибридами отбирали на 5–6, затем 10–12 и на 16–17 дни после слияния.
Стадия 6. Отбор гибридом.
Поскольку используемый штамм миеломы резистентен к 8-азагуанину, он является дефектным по ферменту гипоксантин-гуанин-фосфорибозил трансферазе, и любые не слитые с лимфоцитами миеломные клетки и любые гибриды миелома-миелома не способны выживать в среде НАТ. С другой стороны, гибриды антителообразующих клеток друг с другом, а также гибридомы, образованные антителопродуцирующими и миеломными клетками, могут выживать в этой среде, причём гибриды спленоцитов друг с другом имеют ограниченное время жизни (на протяжении 3–4 пассажей) и отмирают в ходе культивирования, тогда как гибридомы спленоцитов с миеломными клетками (СМ) способны к неограниченному размножению.
Стадия 7. Реклонирование и криоконсервирование гибридом.
Скрининг гибридом проводили методом твердофазного ИФА. Из большого числа активно размножающихся гибридом отбирали гибридомы, активно продуцирующие противовирусные антитела. Для этого в супернатантах гибридом определяли титры специфических антител к вирусу-иммуногену в ИФА. Вирусным материалом (очищенные концентраты), разведённым карбонатно-бикарбонатным буфером (КББ) до концентрации 2–5 мкг/мл, сенсибилизировали планшеты в течение 18 часов при температуре 4°С. После отмывания несвязавшегося антигенного материала 0,01 М фосфатно-солевым буфером (PBS) с добавлением 0,05% Tween 20 (PBS-T), рН 7,2 вносили культуральную жидкость в PBS-T в разведении 1:10 (при тестировании субклонов в 2-х повторах) и инкубировали 1 час при 37°С. Связавшиеся с антигеном антитела детектировали с помощью пероксидазных конъюгатов антител к IgG мыши (“Sigma-Aldrich”, США) в PBS-T в течение 1 часа при температуре 37°С. Пероксидазную реакцию проявляли добавлением субстратной смеси, содержащей 0,1 мг/мл 3,3’,5,5’-тетраметилбензидина (ТМБ) и 0,02% Н2О2 в ацетат-цитратном буфере, рН 5,0. После остановки реакции 2N H2SO4 оптическую плотность измеряли на фотометре Multiscan FC при длине волны 450 нм.
Для последующего клонирования отобранных гибридом СМ использовали метод предельных разведений. Клетки гибридомы разводили из расчёта, чтобы на одну лунку планшета приходилось 1–2 клетки, и затем культивировали их, как выше описано, в ростовой среде в инкубаторе с подачей 5–7% СО2 при температуре 36–37°С. Процедуру клонирования повторяли 3–4 раза для каждого избранного клона, продуцирующего специфические антитела. Клоны — стабильные продуценты антител — отбирали для последующего накопления культивированием в ростовой среде с целью накопления клеток в количестве, достаточном для последующего пассажа на сингенных мышах и криоконсервирования.
Стадия 8. Криоконсервирование гибридом.
Криоконсервированию подвергали культуры гибридомных клеток, находящиеся в логарифмической фазе роста, или клетки, выращенные в перитонеальной полости мышей сингенной линии (при получении асцитных жидкостей). Перед замораживанием клетки подвергали микроскопическому анализу на жизнеспособность и бактериологическому исследованию на отсутствие контаминации микрофлорой. Количество живых клеток оценивали по эксклюзии трипанового синего. После центрифугирования при 1000 об/мин концентрацию клеток доводили до 1–2 млн в мл. Для криоконсервирования клеток использовали среду, состоящую из 90% СКРС и 10% ДМСО (“Sigma-Aldrich”, США). Предварительно охлаждённые до температуры –80°С в парах азота криопробирки с клетками помещали в жидкий азот (для многолетнего хранения при температуре –196°С) и хранили в Криобанке гибридом ФГБУ «НИИ гриппа им. А.А. Смородинцева» Минздрава России.
Полученные гибридомы были депонированы в специализированную коллекцию культур клеток ЦКП «Коллекция культур клеток позвоночных» 08.11.18 под номером РККК(П) 784Д (гибридома 10G6/RS) и 786Д (гибридома 11G4/RS), соответственно.
Стадия 9. Накопление МКА в асцитах.
Асцитные жидкости мышей линии BALB/c, содержащие МКА, секретируемые гибридомой, получали следующим образом. Для этого мышам-реципиентам за 12–14 дней до инокуляции гибридомы вводили внутрибрюшинно 0,5 мл пристана (“Sigma-Aldrich”, США) (Hoogenraad et al., 1983). Восстановленные гибридомы в количестве 5–10 млн инокулировали в брюшную полость праймированных пристаном мышей. Спустя 2–3 недели после образования асцита, контролируемого визуально, делали прокол брюшной стенки и собирали оттекающую жидкость. После центрифугирования асцитов надосадочная жидкость служила источником МКА, а клетки гибридом, прошедшие пассирование на мышах, криоконсервировали. Исследования выполнялись согласно «Правилам проведения работ с использованием экспериментальных животных» (приказ № 266 МЗ РФ от 19.06.2003). Концентрации МКА после очистки составили:
Клон 10G6 — 4,15 мг/мл,
Клон 11G4 — 5,73 мг/мл.
В общем виде схема получения гибридом — продуцентов МКА представлена на Фиг. 1.
Пример 2
Очистка накопленных моноклональных антител к респираторно-синцитиальному вирусу
Препараты мышиных МКА перед очисткой представляли собой асцитные жидкости мышей, содержащие МКА, секретируемые клетками отобранной гибридомы. Очистку фракции МКА проводили методами аффинной хроматографии и гель-фильтрации. Первый этап очистки МКА методом гидрофобной хроматографии предусматривает удаление большей части белковых примесей из исходных препаратов и получение промежуточных препаратов, содержащих как нативную форму IgG, так и продукты их олигомеризации и деградации. Второй этап очистки предусматривает удаление остаточных белковых примесей, а также агрегатов, димеров и фрагментов IgG из промежуточных препаратов методом гель-фильтрации на колонке с сорбентом высокого разрешения.
Концентрацию IgG определяли при помощи спектрофотометра NanoDrop ND-1000 (“Thermo Fisher Scientific”, США) в режиме IgG (коэффициент молярной экстинции E 1% = 13,70). Результат анализа очищенных препаратов МКА подтверждали методом денатурирующего электрофореза в полиакриламидном геле по методу Лэммли. Гель окрашивали коллоидным кумасси и документировали при помощи системы ChemiDoc MP Imaging System (“Bio-Rad”, США) с последующим денситометрическим анализом. При качественной очистке препарат должен представлять собой две мажорных дорожки — тяжёлая цепь антител представлена на уровне ~ 50 кДа, а лёгкая цепь на уровне ~ 25–30 кДа.
Пример 3
Получение МКА к респираторно-синцитиальному вирусу
Было получено 5 МКА к РСВ (клоны 4F2, 5F3, 5H8, 1H3, 5F8) и были проанализированы их аналитические и диагностические характеристики. Все МКА специфически взаимодействовали в непрямом варианте ИФА с очищенным концентратом вируса-иммуногена (РСВ, эталонный штамм Long), сенсибилизированным на твёрдой фазе, при отсутствии перекрёстного реагирования с гетерологичными респираторными вирусами и клеточными антигенами. Свойства МКА были оценены в различных иммунологических реакциях. Для характеристики направленности полученных МКА был проведен вестерн-блоттинг с использованием в качестве антигена очищенного концентрата РСВ, штамм Long. В случае проведения электрофореза (ЭФ) с РСВ, обработанным в условиях мягкого нагревания при нередуцирующих условиях (нагревание при температуре 37°С без β-меркаптоэтанола (МЭ) в течение 1,5 ч), после иммуноблоттинга все МКА взаимодействовали на мембране с тремя белковыми продуктами с молекулярной массой 130, 110 и 70 кДа. Белку с молекулярной массой 70 кДа соответствует мономер поверхностного F-белка РСВ. Согласно данным литературы, две высокомолекулярные полосы представляют собой олигомерные формы F-гликопротеина РСВ — гомодимерную и гомотримерную. По данным других авторов, высокомолекулярные полосы с близкими молекулярными массами на электрофореграмме соответствуют гетероолигомерам двух поверхностных гликопротеинов РСВ: (мономер F-белка 70 кДа + полностью гликозилированная форма G-белка 90 кДа) и (мономер F-белка 70 кДа + форма G-белка с неполным гликозилированием 55 кДа).
После ЭФ вируса, подвергшегося более жёсткой обработке в нередуцирующих условиях (кипячение 2 мин при температуре 100°С без МЭ), все МКА реагировали на мембране после иммуноблоттинга только с мономерной формой F-белка РСВ (70 кДа), что объясняется распадом олигомеров. С РСВ, обработанным в наиболее жёстких редуцирующих условиях при кипячении в течение 2 мин в присутствии МЭ, МКА не взаимодействовали, что свидетельствует о полном разрушении эпитопа-мишени. Таким образом, результаты иммуноблоттинга свидетельствуют о том, что все полученные МКА взаимодействовали с конформационно лабильными эпитопами, присутствующими как в мономерной, так и в олигомерных формах F-белка РСВ.
Все МКА относились к различным изотипам IgG. МКА 5F8 и 5F3 обладали выраженной вируснейтрализующей активностью (до концентрации 9–26 мкг/мл) по отношению к эталонным штаммам РСВ группы А. Для РСВ группы В этот показатель был значительно ниже. Слабая нейтрализующая активность выявлена также для МКА 5Н8. Остальные МКА не оказывали вируснейтрализующего действия (таблица 1).
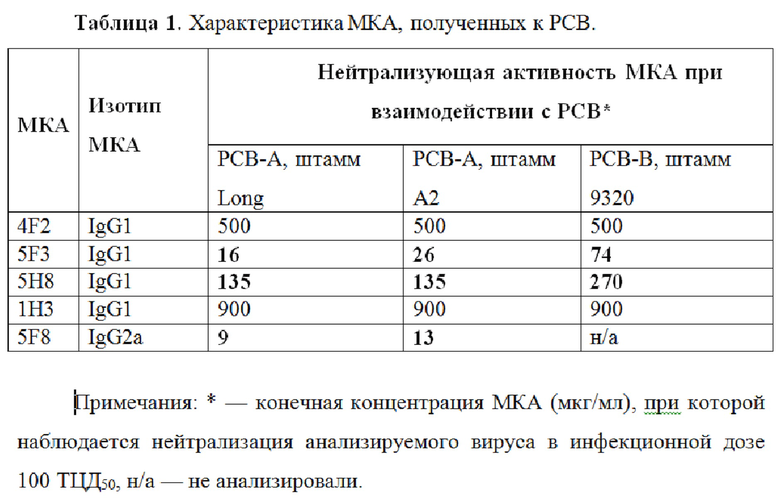
Примечания: * — конечная концентрация МКА (мкг/мл), при которой наблюдается нейтрализация анализируемого вируса в инфекционной дозе 100 ТЦД50, н/а — не анализировали.
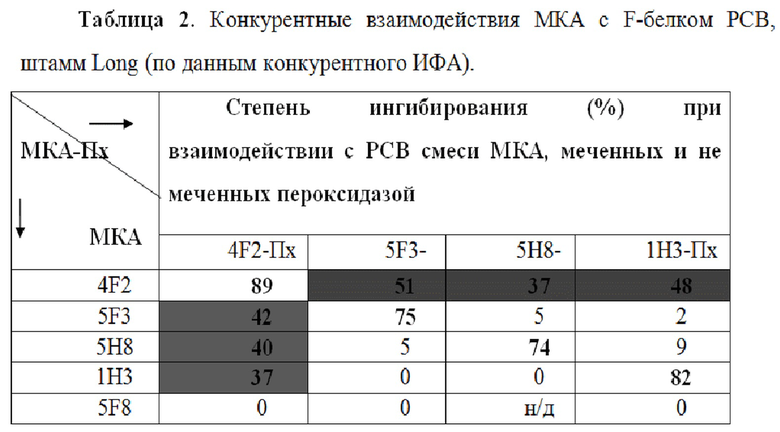
Примечание — степень ингибирования (%):

Для характеристики антигенной направленности МКА был проведён конкурентный ИФА с использованием МКА, меченных и не меченных пероксидазой хрена. Результаты анализа представлены в таблице 2.
Результаты конкурентного ингибирования МКА, меченных и не меченных пероксидазой хрена, показали, что у них наблюдаются следующие особенности взаимодействия с антигеном:
1. МКА 5F3, 5H8 и 1H8 не конкурируют друг с другом за связь с F-белком. Однако эти МКА направлены к детерминантам, частично (на 37−51%) общим с сайтом связывания для МКА 4F2.
2. Сайт взаимодействия МКА 5F8 не имеет общих детерминант с сайтами связывания всех остальных МКА.
Для оценки способности полученных новых МКА взаимодействовать со штаммами РСВ, относящимися к различным антигенным группам, был проведён микрокультуральный ИФА (мк-ИФА, in-cell ELISA) с использованием монослойных культур инфицированных вирусом клеток МА-104. При постановке метода для инфицирования использовали 3 эталонных штамма РСВ: Long и А2 (РСВ-А), а также штамм 9320 (РСВ-В).
Все МКА специфически реагировали в мк-ИФА с инфицированными данными штаммами РСВ клетками МА-104. Фоновые значения OD450 при взаимодействии МКА с монослойными культурами неинфицированных клеток не превышали 0,15. Все полученные МКА практически с одинаковой эффективностью взаимодействовали в мк-ИФА с вирусом-иммуногеном (РСВ, штамм Long). На высокую аффинность МКА при взаимодействии с данным вирусом указывает наличие плато на кривых титрования, наблюдаемое в широком диапазоне концентраций МКА (от 0,5 до 50 мкг/мл). С клетками, инфицированными другим штаммом РСВ-А (А2), все МКА взаимодействовали слабее, чем с РСВ Long. Наименее активными при этом оказались МКА 5H8, 1H3 и 5F8. Эти же 3 МКА значительно слабее, чем другие антитела, реагировали также со штаммом 9320, относящимся к гетерологичной группе В.
Следует отметить, что МКА 5F3 оказались единственными из полученных МКА, которые реагировали с эталонными штаммами группы РСВ-А со значительно большей активностью, чем с РСВ-В. Полученные результаты указывают на то, что МКА 4F2 направлены к консервативным эпитопам F-белка, общим для обеих антигенных групп РСВ. Соответственно, МКА 5H8, 1H3, 5F8 и 5F3 взаимодействуют с более вариабельными эпитопами.
Было показано, что МКА 10G6 и 11G4 специфически взаимодействуют с F-белком РСВ по данным иммуноблоттинга. Спектр взаимодействия данных МКА был проанализирован методом мк-ИФА. Для этого в лунки планшетов с монослойными культурами клеток МА-104 вносили вируссодержащий материал (культуральную среду, содержащую 50–100 ТЦД50 РСВ). После инкубации в СО2-инкубаторе в течение 3–5 суток при 37°С среду удаляли, клетки в лунках фиксировали 80% холодным ацетоном. На фиксированный клеточный монослой наносили по 100 мкл вирусспецифических МКА в рабочем разведении (5–10 мкг/мл) и инкубировали 2 ч при 37°С. На следующем этапе в лунки добавляли по 100 мкл козьих антител против IgG мыши (1/5000), меченных пероксидазой (“Sigma-Aldrich”, США), и инкубировали в течение 1 ч при 37°С. Пероксидазную реакцию проявляли добавлением субстратной смеси, содержащей 0,1 мг/мл 3,3’,5,5’-тетраметилбензидина (ТМБ) и 0,02% Н2О2 в ацетат-цитратном буфере, рН 5,0. После остановки реакции с помощью 2N H2SO4 измеряли оптическую плотность на фотометре при длине волны 450 нм (ОD450).
По результатам мк-ИФА МКА 10G6 и 11G4 показали широкий спектр специфического взаимодействия с референс-штаммами РСВ обеих подгрупп: Long и А2 (РСВ-А), а также со штаммом 9320 (РСВ-В). Помимо этого данные МКА эффективно взаимодействовали со штаммами РСВ, выделенными из клинических образцов (назальных соскобов), полученных от госпитализированных детей Санкт-Петербурга в 2017–2018 гг. При рабочем разведении МКА показатели ОD450 в мк-ИФА превышали для штаммов РСВ 1,0. МКА не показали кросс-реактивности при взаимодействии с клетками, инфицированными гетерологичными вирусами (парагриппом 2 и 3 типа, аденовирусом).
Изоляты РСВ, выделенные в Санкт-Петербурге из клинических материалов в 2018 г. и идентифицированные МКА 10G6 и 11G4 методом мк-ИФА:
RSV/St.Petersburg/457/2018, RSV/St.Petersburg/460/2018, RSV/St.Petersburg/462/2018, RSV/St.Petersburg/466/2018, RSV/St.Petersburg/478/2018, RSV/St.Petersburg/479/2018, RSV/St.Petersburg/494/2018, RSV/St.Petersburg/498/2018, RSV/St.Petersburg/562/2018, RSV/St.Petersburg/570/2018, RSV/St.Petersburg/571/2018, RSV/St.Petersburg/572/2018, RSV/St.Petersburg/654/2018, RSV/St.Petersburg/679/2018, RSV/St.Petersburg/751/2018, RSV/St.Petersburg/949/2018, RSV/St.Petersburg/1335/2018
Идентификация выделенных штаммов РСВ, провёденная с применением МКА методом мк-ИФА, была подтверждена ПЦР.
Описанные МКА могут быть использованы для диагностики, в частности, в диагностических тест-системах, например, в тест-системах по типу «сэндвич»-ИФА.
Пример 4
Активацию сенсорного чипа СМ5 и иммобилизацию на его поверхность антител 10G6 к F-белку РСВ проводили в соответствии с инструкцией производителя (“GE Healthcare”, США). Раствор лиганда (МКА 10G6) готовили в 10 мМ CH3COONa pH 5,0. Поверхность чипа предварительно активировали обработкой 1-этил-3-(3-диметиламинопропил) карбодиимида гидрохлоридом (EDC) и N-гидроксисукцинимидом (NHS) в соотношении 1:1. Далее, в первую ячейку прибора вносили раствор лиганда (50 мкг/мл при скорости потока 10 мкл/мин, время контакта 420 с), иммобилизация которого проходила путём образования ковалентных связей между аминогруппами в полипептидной цепи лиганда и NHS-активированной поверхностью чипа. Затем в первую ячейку вносили 1М раствор этаноламин гидрохлорида-NaOH pH 8,5 для инактивации участков поверхности чипа, не занятых лигандом. Во вторую ячейку прибора вносили только 1М раствор этаноламин гидрохлорида-NaOH pH 8,5 для инактивации поверхности чипа. Таким образом, первая (рабочая) ячейка служила для снятия сигнала взаимодействия лиганд-аналит, вторая (референсная) ячейка служила для снятия фонового сигнала. Увеличение сигнала на 1 RU (Response Unit, единица ответа) соответствовало иммобилизации ≈ 1 пг/мм2 лиганда на поверхность чипа CM5.
Инжектирование аналита (РСВ) проводили в серии двукратных разведений (87,5; 43,8; 21,9; 10,9 нМ). Для регенерации поверхности чипа использовали 10 мМ глицин гидрохлорид pH 2,5.
Связывание антител с аналитом было изучено путём мониторинга изменения значений RU в ходе построения сенсограммы взаимодействия во времени. Полученные кривые взаимодействия были обработаны с использованием программного обеспечения Biacore X100 Evaluation Software (Фиг. 2).
Данное взаимодействие было описано кинетикой Лэнгмюра. Так, рассчитанная по данному приближению (Фиг. 3) равновесная константа диссоциации составила KD = 2,88×10–10 М, что свидетельствует о высокоаффинном взаимодействии МКА 10G6 c РСВ.
Пример 5
Активацию сенсорного чипа СМ5 и иммобилизацию на его поверхность антител 11G4 к F-белку РСВ проводили в соответствии с инструкцией производителя (“GE Healthcare”, США). Раствор лиганда (МКА 11G4) готовили в 10 мМ CH3COONa pH 5,0. Поверхность чипа предварительно активировали обработкой 1-этил-3-(3-диметиламинопропил) карбодиимида гидрохлоридом (EDC) и N-гидроксисукцинимидом (NHS) в соотношении 1:1. Далее, в первую ячейку прибора вносили раствор лиганда (50 мкг/мл при скорости потока 10 мкл/мин, время контакта 420 с), иммобилизация которого проходила путём образования ковалентных связей между аминогруппами в полипептидной цепи лиганда и NHS-активированной поверхностью чипа. Затем в первую ячейку вносили 1М раствор этаноламин гидрохлорида-NaOH pH 8,5 для инактивации участков поверхности чипа, не занятых лигандом. Во вторую ячейку прибора вносили только 1М раствор этаноламин гидрохлорида-NaOH pH 8,5 для инактивации поверхности чипа. Таким образом, первая (рабочая) ячейка служила для снятия сигнала взаимодействия лиганд-аналит, вторая (референсная) ячейка служила для снятия фонового сигнала. Увеличение сигнала на 1 RU соответствовало иммобилизации ≈ 1 пг/мм2 лиганда на поверхность чипа CM5.
Инжектирование аналита (РСВ) проводили в серии двукратных разведений (87,5; 43,8; 21,9; 10,9 нМ). Для регенерации поверхности чипа использовали 10 мМ глицин гидрохлорид pH 2,5.
Связывание антител с аналитом было изучено путём мониторинга изменения значений RU в ходе построения сенсограммы взаимодействия во времени. Полученные кривые взаимодействия были обработаны с использованием программного обеспечения Biacore X100 Evaluation Software. Данное взаимодействие было описано кинетикой Лэнгмюра. Так, рассчитанная по данному приближению равновесная константа диссоциации составила KD = 7,16×10–11 М, что свидетельствует о высокоаффинном взаимодействии МКА 11G4 c РСВ.
Описанные МКА могут быть использованы для диагностики, в частности, в диагностических тест-системах, например, в тест-системах по типу «сэндвич»-ИФА или иных тест-системах.
| название | год | авторы | номер документа |
|---|---|---|---|
| ТЕСТ-СИСТЕМА ДЛЯ ДИАГНОСТИКИ ВОЗБУДИТЕЛЕЙ ОСТРЫХ РЕСПИРАТОРНЫХ ВИРУСНЫХ ИНФЕКЦИЙ | 2019 |
|
RU2733379C1 |
| СПОСОБ ДИАГНОСТИКИ ВОЗБУДИТЕЛЕЙ ОСТРЫХ РЕСПИРАТОРНЫХ ВИРУСНЫХ ИНФЕКЦИЙ | 2019 |
|
RU2726797C1 |
| МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА, СПЕЦИФИЧНЫЕ К РАЗЛИЧНЫМ ШТАММАМ ВИРУСА ГРИППА В | 2018 |
|
RU2714246C1 |
| Штамм гибридных клеток животных Mus musculus 1F1 - продуцент моноклонального антитела к нуклеокапсидному белку N вируса SARS-CoV-2 | 2021 |
|
RU2769817C1 |
| СПОСОБ ПОЛУЧЕНИЯ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ К БЕЛКУ Р30 ВИРУСА АФРИКАНСКОЙ ЧУМЫ СВИНЕЙ С ИСПОЛЬЗОВАНИЕМ РЕКОМБИНАНТНЫХ КОНСТРУКЦИЙ | 2013 |
|
RU2534343C1 |
| ШТАММ ГИБРИДНЫХ КУЛЬТИВИРУЕМЫХ КЛЕТОК ЖИВОТНОГО MUS MUSCULUS L - ПРОДУЦЕНТ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ К А-ДЕТЕРМИНАНТЕ ПОВЕРХНОСТНОГО АНТИГЕНА ВИРУСА ГЕПАТИТА B | 1994 |
|
RU2092553C1 |
| ШТАММ ГИБРИДНЫХ КУЛЬТИВИРУЕМЫХ КЛЕТОК ЖИВОТНОГО MUS MUSCULUS L. - ПРОДУЦЕНТ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ К A-ДЕТЕРМИНАНТЕ ПОВЕРХНОСТНОГО АНТИГЕНА ВИРУСА ГЕПАТИТА B | 1994 |
|
RU2097425C1 |
| ШТАММ ГИБРИДНЫХ КУЛЬТИВИРУЕМЫХ КЛЕТОК ЖИВОТНОГО MUS MUSCULUS L. - ПРОДУЦЕНТ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ К A-ДЕТЕРМИНАНТЕ ПОВЕРХНОСТНОГО АНТИГЕНА ВИРУСА ГЕПАТИТА B | 1994 |
|
RU2097426C1 |
| Штамм гибридных клеток животных Mus musculus 2E1B5 - продуцент моноклонального антитела к рецептор-связывающему домену белка S вируса SARS-CoV-2 | 2021 |
|
RU2771288C1 |
| Моноклональное антитело, специфичное к вирусу Эбола | 2018 |
|
RU2705763C1 |
Изобретение относится к области биотехнологии. Описан способ получения мышиных моноклональных антител, специфичных к F-белку респираторно-синцитиального вируса групп А и В. Способ включает стадии получения антитело-продуцирующих спленоцитов, накопления клеток мышиной миеломы, слияния антитело-продуцирующих спленоцитов с миеломными клетками, отбора гибридом, введения гибридомы в брюшную полость праймированных пристаном мышей, накопления моноклональных антител в асцитах и очистки полученных моноклональных антител. Для получения антител в способе использована гибридома-продуцент моноклональных антител, направленных к F-белку респираторно-синцитиального вируса групп А и В, депонированная как 11G4/RS под номером РККК(П) 786Д, или гибридома-продуцент моноклональных антител, направленных к F-белку респираторно-синцитиального вируса, депонированная как 10G6/RS под номером РККК(П) 784Д в Специализированную коллекцию культур клеток ЦКП «Коллекция культур клеток позвоночных» ФГБУН Института цитологии РАН. Изобретение расширяет способы получения мышиных моноклональных антител, специфичных к F-белку респираторно-синцитиального вируса групп А и В. 3 ил., 2 табл., 5 пр.
Способ получения мышиных моноклональных антител, специфичных к F-белку респираторно-синцитиального вируса групп А и В,
Включающий:
- получение антитело-продуцирующих спленоцитов;
- накопление клеток мышиной миеломы;
- слияние антитело-продуцирующих спленоцитов с миеломными клетками;
- отбор гибридом;
- введение гибридомы в брюшную полость праймированных пристаном мышей;
- накопление моноклональных антител в асцитах;
- очистку полученных моноклональных антител,
причем для получения указанных антител использована гибридома-продуцент моноклональных антител, направленных к F-белку респираторно-синцитиального вируса групп А и В, депонированная как 11G4/RS под номером РККК(П) 786Д, или гибридома-продуцент моноклональных антител, направленных к F-белку респираторно-синцитиального вируса, депонированная как 10G6/RS под номером РККК(П) 784Д в Специализированную коллекцию культур клеток ЦКП «Коллекция культур клеток позвоночных» ФГБУН Института цитологии РАН.
| МОЛЕКУЛА, СПЕЦИФИЧЕСКИ СВЯЗЫВАЮЩАЯСЯ С RSV | 2009 |
|
RU2540020C2 |
| WO 2005079479 A2, 01.09.2005 | |||
| Штамм Paenibacillus polymyxa ВСГУТУ-1 - продуцент экзополисахаридов | 2022 |
|
RU2784088C1 |
Авторы
Даты
2020-02-04—Публикация
2018-12-28—Подача