Изобретение относится к искусственным белкам-иммуногенам, имеющим свойства антигенов вируса Эбола, используемым для создания синтетических полиэпитопных профилактических вакцин против вируса Эбола и может быть использовано в биотехнологии, молекулярной биологии, генетической инженерии и медицине. Существует ряд подходов к созданию вакцин против вируса Эбола, включая ДНК-вакцины, субъединичные вакцины, а также вакцины на основе вирусных векторов [1]. Их защитная эффективность была оценена на моделях нечеловеческих приматов. На сегодняшний день описано несколько препаратов вакцин потенциально перспективных в борьбе с вирусом. Среди них: rVSV-ZEBOV [2], Ad5-ZEBOV [3], GamEvac-Combi [4], и несколько других, находящихся на стадии клинических испытаний.
В основном, разрабатываемые экспериментальные вакцины созданы на основе генетически модифицированных вирусов, кодирующих полноразмерные вирусные антигены, что может явиться причиной нежелательного иммунного ответа на их введение пациенту. Эти вакцины направлены на индукцию как гуморального, так и клеточного иммунного ответов [5]. Следует отметить, что данные о защитной роли нейтрализующих антител против филовирусов, полученные в исследованиях на нечеловеческих приматах (nonhuman primates, NHP), являются противоречивыми. Показано, что некоторые антитела защищают животных от последующего заражения, но не нейтрализуют вирус, тогда как другие нейтрализуют вирус, но не защищают животных [6]. Таким образом, относительная важность нейтрализующих антител по сравнению с теми, которые могут обеспечить защиту через другие механизмы (например, антитело-зависимую клеточную цитотоксичность или Fc-зависимые механизмы) остается неясной. При этом остается открытым вопрос о роли не-нейтрализующих антител (non-neutralizing antibodies) в защите от вируса Эбола, учитывая известный эффект антител зависимого усиления инфекции [7].
Необходимо отметить, что при иммунизации наряду с гуморальным иммунным ответом развивался выраженный клеточный (CD8+ и CD4+) иммунный ответ, что является ключевым моментом для защиты от лихорадки Эбола. Действительно, в различных исследованиях было показано, что ключевую роль в формировании протективного иммунитета к вирусу Эбола играет именно клеточный иммунитет [8, 9].
Чтобы индуцировать оба звена иммунного ответа используют различные системы доставки антигенов Т- и В-лимфоцитам, среди которых ДНК-вакцины имеют ряд преимуществ. Они неинфекционны и легко нарабатываются в больших количествах; их можно использовать многократно, поскольку в отличие от вирусных векторов для ДНК-векторов ранее существовавший иммунитет не имеет значения. Кроме того, ДНК-вакцинация обеспечивает наиболее естественный путь презентации антигенов предшественникам цитотоксических Т-лимфоцитов, а также вызывает индукцию антител. Единственным недостатком ДНК-вакцин является их относительно слабая иммуногенность, в силу чего они требуют многоразового введения для достижения желаемого эффекта [10]. Однако этот недостаток можно преодолеть за счет использования стратегии внутримышечной электропорации, позволяющей значительно повысить эффективность ДНК-вакцинации [11].
Одним из перспективных направлений в разработке противовирусных вакцин является конструирование ДНК-вакцин, кодирующих искусственные полиэпитопные (мозаичные) иммуногены. Такие вакцины представляют собой комбинацию эпитопов, отобранных из разных вирусных белков и объединенных в одной молекуле [12-14]. Прогресс в идентификации T-клеточных эпитопов, а также понимание механизмов процессинга и презентации антигенов по пути МНС I и II классов дает возможность для рационального дизайна искусственных полиэпитопных вакцин, вызывающих ответы цитотоксических (СD8+) и хелперных (CD4+) Т-лимфоцитов [12, 14, 15].
Наиболее близким аналогом (прототипом) является иммунобиологическое средство (вакцина GamEvac-Combi) для индукции специфического иммунитета к вирусу Эбола. В первом варианте прототип включает рекомбинантный аденовирус, содержащий кассету со вставкой модифицированного гена GP вируса Эбола /H.sapiens-wt/SLE/2014/Makona-ЕМ124.1 (GenBank ID KM233045.1) с последовательностью, выбранной из SEQ ID NO 1, SEQ ID NO 2 (патент РФ №2578159, МПК А61К39/12, опубл. 20.03.2016) [23]. Во втором варианте иммунобиологическое средство для индукции специфического иммунитета к вирусу Эбола включает рекомбинантный вирус везикулярного стоматита, содержащий кассету со вставкой модифицированного гена GP вируса Эбола /H.sapiens-wt/SLE/2014/Makona-EM124.1 (GenBank ID KM233045.1) с последовательностью, выбранной из SEQ ID NO 1, SEQ ID NO 2. В третьем варианте иммунобиологическое средство для индукции специфического иммунитета к вирусу Эбола включает рекомбинантный вирус везикулярного стоматита, содержащий кассету со вставкой немодифицированного гена GP вируса Эбола /H.sapiens-wt/1976/Mayinga/Zaire (GenBank ID AF086833.2) с последовательностью SEQ ID NO 3, и рекомбинантный вирус везикулярного стоматита, содержащий кассету со вставкой модифицированного гена GP вируса Эбола /H.sapiens-wt/SLE/2014/Makona-ЕМ124.1 (GenBank ID KM233045.1) с последовательностью, выбранной из SEQ ID NO 1, SEQ ID NO 2, взятые в эффективных соотношениях. Указанное иммунобиологическое средство, изготовленное по 1 или 2 или 3 варианту, вводят в организм млекопитающих в эффективном количестве для индукции специфического иммунитета к вирусу Эбола или при последовательном совместном введении в организм млекопитающих иммунобиологических средств, изготовленных по вариантам 1 и 2 или 1 и 3, с интервалом более чем в 1 неделю в эффективном количестве для индукции специфического иммунитета к вирусу Эбола.
Однако иммунобиологические препараты на основе вирусных векторов неэффективно использовать многократно поскольку ранее приобретенный иммунитет на вектор-носитель отрицательно влияет на иммунный ответ при повторной вакцинации.
Техническим результатом заявляемого изобретения является создание новых искусственных полиэпитопных Т-клеточных иммуногенов, обладающих высокой иммуногенностью (индуцирующих высокий уровень ответа цитотоксических Т-лимфоцитов) для создания профилактической вакцины против вируса Эбола.
Указанный технический результат достигается тем, что создан искусственный ген, кодирующий искусственный Т-клеточный иммуноген EV.CTL, имеющий последовательность SEQ ID NO:3 размером 1881 п.н. и содержащую на 5'-конце последовательность Козак (CCGCCACC) и сайт для эндонуклеазы рестрикции XbaI, а на 3'-конце - три стоп-кодона (TGATGATAG) и сайт для эндонуклеазы рестрикции ApaI.
Указанный технический результат достигается также тем, что создан второй искусственный ген, кодирующий искусственный Т-клеточный иммуноген EV.Th, имеющий последовательность SEQ ID NO: 4 длиной 1146 п.н. и содержащую на 5'-конце последовательность Козак (CCGCCACC) и сайт эндонуклеазы рестрикции EсoRI, а на 3'-конце - три стоп-кодона (TGATGATAG) и сайт эндонуклеазы рестрикции ApaI.
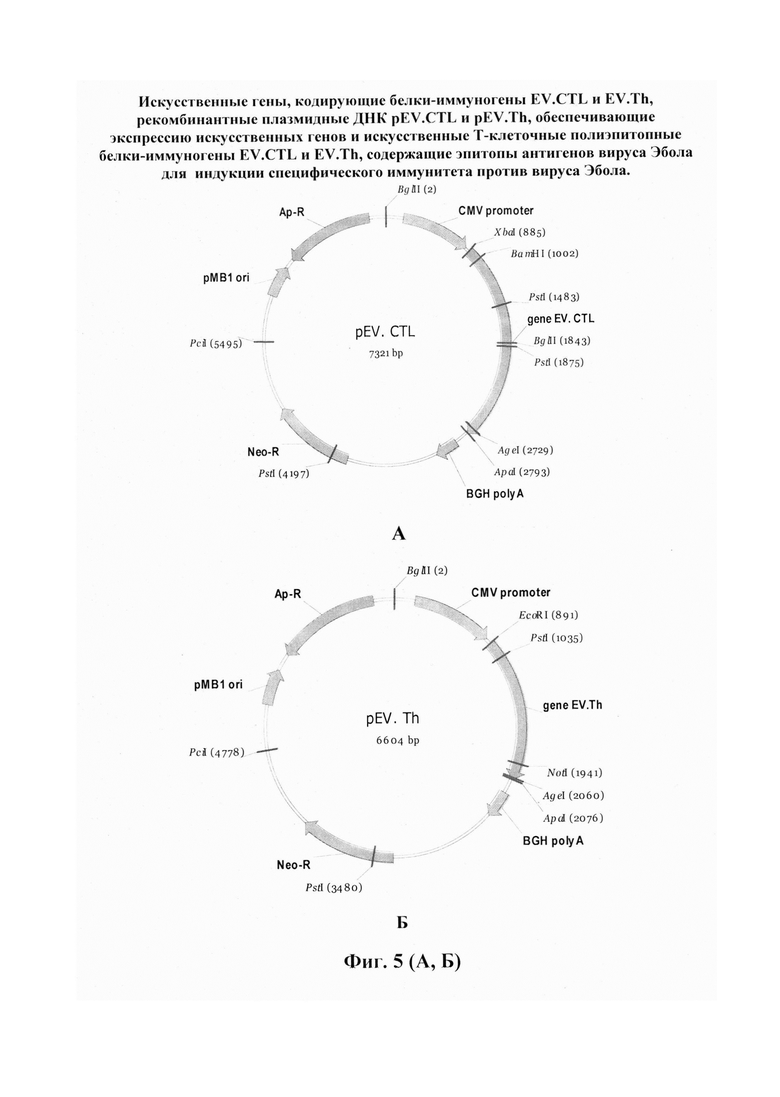
Указанный технический результат достигается тем, что создана рекомбинантная плазмидная ДНК pEV.CTL, имеющая размер 7321 п.н., молекулярную массу 4.8 × 103 кДа, содержащая в соответствии с физической и генетической картой, представленной на Фиг. 5 А целевой ген, кодирующий искусственный Т-клеточный иммуноген EV.CTL, находящийся под контролем промотора CMV, обеспечивающего его экспрессию в клетках млекопитающих и состоящая из следующих фрагментов:
- XbaI-ApaI векторного фрагмента ДНК плазмиды рсDNA3.1-cassette2 размером 5413 п.н., содержащего промотор CMV и последовательность BGH poly A, обеспечивающие экспрессию гена EV.CTL в клетках млекопитающих; ген устойчивости к ампициллину bla (Ap-R)-и pMB1 ori, обеспечивающие селекцию и размножение целевой плазмиды в клетках бактерий Escherichia coli;
- XbaI-ApaI - фрагмента размером 1910 п.н., содержащего ген EV.CTL и последовательность Козак с инициирующим кодоном ATG;
- уникальных сайтов рестрикции: XbaI (885), BamHI(1002), AgeI (2729), ApaI (2793), PciI(5495) и имеющей следующее положение генов:
Указанный технический результат достигается также тем, что создана вторая рекомбинантная плазмидная ДНК pEV.Th, имеющая размер 6604 п.н., молекулярную массу 4.3 × 103 кДа, содержащая в соответствии с физической и генетической картой, представленной на Фиг. 5 Б, целевой ген, кодирующий искусственный Т-клеточный иммуноген EV.Th, находящийся под контролем промотора CMV, обеспечивающего его экспрессию в клетках млекопитающих и состоящая из следующих фрагментов:
- EcoRI- ApaI векторного фрагмента ДНК плазмиды рсDNA3.1-cassette 1 размером 5419 п.н., содержащего промотор CMV и последовательность BGH poly A, обеспечивающие экспрессию гена EV.CTL в клетках млекопитающих; ген устойчивости к ампициллину bla (Ap-R) и pMB1 ori, обеспечивающие селекцию и размножение целевой плазмиды в клетках бактерий Escherichia coli;
- EcoRI- ApaI - фрагмента размером 1187 п.н., содержащего ген EV.Th и последовательность Козак с инициирующим кодоном ATG;
- уникальных сайтов рестрикции: BglII(2), EcoRI(891), NotI(1941), AgeI(2060) ApaI(2076) и имеющей следующее положение генов:
Указанный технический результат достигается тем, что получен поли-CTL-эпитопный белок-иммуноген EV.CTL, имеющий аминокислотную последовательность SEQ ID NO:1 длиной 627 а.к.о. и долей спейсерных последовательностей равной 12.76%, на N-конце которой расположена последовательность убиквитина (MQIFVKTLTGKTITLEVEPSDTIENV KAKIQDKEGIPPDQQRLIFAGKQLEDGRTLSDYNIQKESTLHLVLRLRGV) с 76 а.к.о., а на С-конце - последовательность EPFRDYVDRFYKTLR маркерного эпитопа белка p24 HIV-1, узнаваемого моноклональными антителами 29F2.
Указанный технический результат достигается также тем, что получен второй поли-Th-эпитопный белок-иммуноген EV.Th, имеющий аминокислотную последовательность SEQ ID NO:2 длиной 382 а.к.о., на N-конце которой расположена последоватеьность MGVTGILQLPRDR сигнального пептида, на С-конце - С-концевой фрагмент белка LAMP1 (RKRSHAGYQTI), а на С-конце расположен маркерный эпитоп белка p24 HIV-1, узнаваемый моноклональными антителами 29F2.
На фиг. 1 приведена аминокислотная последовательность полиэпитопного белка иммуногена EV.CTL. На фиг. 2 приведена аминокислотная последовательность полиэпитопного белка иммуногена EV.Th. На фиг. 3 представлена последовательность искусственного гена, кодирующая иммуноген EV.CTL. На фиг. 4 представлена последовательность искусственного гена, кодирующая иммуноген EV.Th. На фиг. 5 А, Б представлены соотвественно физические и генетические карты плазмид pEV.CTL и pEV.Th, кодирующих целевые полиэпитопные иммуногены EV.CTL и EV.Th. На фиг. 6 представлена электрофореграмма в 1 % агарозном геле фрагментов ДНК после гидролиза плазмиды pEV.CTL рестриктазами BglII и DraIII, и плазмиды pEV.Th рестриктазами BglII и PstI. На фиг. 7 изображена электрофореграмма в 1 % агарозном геле продуктов ПЦР, полученных на матрице кДНК, для оценки экспрессии генов EV.CTL и EV.Th в препаратах суммарной РНК, выделенной из клеток 293Т, трансфицированных плазмидами pEV.CTL и pEV.Th. На фиг. 8 приведены данные по экспрессии ДНК-вакцинных конструкций pEV.CTL и pEV.Th в клетках 293T, с помощью иммуногистохимического окрашивания. На фиг. 9 представлены результаты исследования количества IFNγ-продуцирующих Т-клеток в реакции IFNγ-ELISpot у мышей линии BALB/c, иммунизированных ДНК-вакцинными конструкциями, кодирующими целевые иммуногены. На фиг. 10 (А, Б) представлены результаты исследования соотвественно количества IFNγ-продуцирующих CD8+ (А) и CD4+ (Б) Т-клеток, полученные с помощью ICS у мышей линии BALB/c, иммунизированных ДНК-вакцинными конструкциями, кодирующими целевые иммуногены (n = 5).
Пример 1. Дизайн искусственных генов и получение рекомбинантных плазмид - кандидатов ДНК-вакцины против вируса Эбола, кодирующих полиэпитопные иммуногены вируса Эбола
Дизайн искусственных генов, кодирующих EV.CTL и EV.Th иммуногены вируса Эбола, проводился с помощью программы GeneDesigner [16]. Обратная трансляция аминокислотных последовательностей проводилась с учетом частот встречаемости кодонов у человека [17]. Перед инициирующим кодоном ATG размещена последовательность Козак (CCGCCACC). В конце кодирующей последовательности добавлены три стоп-кодона (TAGTGATGA). Спроектированные гены EV.CTL и EV.Th были синтезированы и клонированы в составе векторных плазмид pcDNA3.1-cassette1 и pcDNA3.1-cassette2.
Пример 2. Получение плазмид pEV.CTL и pEV.Th, кодирующих целевые полиэпитопные иммуногены EV.CTL и EV.Th
2.1. Конструирование плазмид pEV.CTL и pEV.Th
Конструирование плазмид проводят с помощью стандартных методов молекулярного клонирования [16]. Гены, кодирующие последовательности искусственных Т-клеточных иммуногенов EV.CTL и EV.Th, были получены химическим синтезом (Евроген, Россия) и клонированы в составе плазмид pcDNA3.1-cassette1 и pcDNA3.1-cassette2 (производных от pcDNA3.1 фирмы Invitrogen, США). Последовательность гена EV.CTL была клонирована в векторной плазмиде pcDNA3.1-cassette2 по сайтам рестрикции XbaI и ApaI (фиг. 5 А), а последовательность гена EV.Th - в векторной плазмиде pcDNA3.1-cassette1 по сайтам рестрикции EcoRI и ApaI (фиг. 5 Б). В результате были сконструированы две рекомбинантные плазмиды: pEV.CTL и pEV.Th - кандидаты ДНК-вакцины против вируса Эбола.
После трансформации клеток E.coli DH5αF' полученные рекомбинантные плазмиды pEV.CTL и pEV.Th, содержащие целевые гены, были отобраны стандартными процедурами скрининга, используя рестрикционный анализ. Последовательности клонированных генов подтверждены секвенированием.
2.2. Подтверждение структуры плазмид рестрикционным анализом
Согласно теоретически рассчитанной нуклеотидной последовательности при гидролизе плазмиды pEV.CTL с помощью эндонуклеаз рестрикции BglII (сайт узнавания A^GATCT) и DraIII (сайт узнавания CACNNN^GTG) должны появиться фрагменты 3913 п.н., 1841 п.н. и 1567 п.н.
Аналогично, при гидролизе плазмиды pEV.Th с помощью эндонуклеаз рестрикции BglII (сайт узнавания A^GATCT) и PstI (сайт узнавания CTGCA^G) должны появиться фрагменты 3126 п.н., 2445 п.н. и 1033 п.н.
На фиг. 6 представлена электрофореграмма в 1 % агарозном геле. Фрагменты ДНК после гидролиза плазмиды pEV.CTL рестриктазами BglII и DraIII, и плазмиды pEV.Th рестриктазами BglII и PstI где:
E-1 - ДНК pE CTL, нативная;
E-1R - ДНК pE CTL, рестириктированная ферментами BglII и DraIII;
E-2 - ДНК pEV.Th, нативная;
E-2R - ДНК pEV.Th, рестириктированная ферментами BglII - PstI;
М - маркеры М12 фирмы СибЭнзим.
Из данных, представленных на фиг. 6 видно, что подвижность фрагментов гидролизата плазмид pEV.CTL и pEV.Th в 1 % агарозном геле относительно маркеров молекулярной массы соответствует подвижности теоретически рассчитанных фрагментов.
2.3. Подтверждение структуры плазмид секвенированием
Нуклеотидные последовательности генов EV.CTL и EV.Th, в составе полученных рекомбинантных плазмид pEV.CTL и pEV.Th, помимо рестрикционного анализа, были также подтверждены секвенированием. Показано, что нуклеотидные последовательности генов в образцах совпадают с теоретически рассчитанными.
2.4. Анализ экспрессии целевых генов
Экспрессию генов в составе плазмид pEV.CTL и pEV.Th оценивали двумя методами: по синтезу специфической мРНК и с помощью иммуноокрашивания трансфицированных клеток. Для оценки синтеза специфических мРНК выделяли суммарную РНК из клеток 293T, трансфицированных плазмидами pEV.CTL и pEV.Th, и получали кДНК в ОТ-ПЦР. Полученную кДНК использовали для проведения ПЦР с использованием пар праймеров (fCTL, rCTL) и (fTh, rTh) к генам EV.CTL и EV.Th, соответственно.
На фиг. 7 представлена электрофореграмма в 1 % агарозном геле продуктов ПЦР, полученных на матрице кДНК, где:
1 - маркер молекулярных весов (М12 “Сибэнзим”);
2 и 3 - продукты ПЦР с праймерами (fCTL, rCTL) и (fTh, rTh), соответственно;
4 и 8 - результаты ПЦР с праймерами (fCTL, rCTL) и (fTh, rTh) и суммарной РНК, выделенной из клеток 293T, трансфицированных плазмидами pEV.CTL и pEV.Th, соответственно (без стадии обратной танскрипции; контроль на отсутствие целевых плазмид в выделенных образцах суммарной РНК);
5 - маркер молекулярных весов (М15 “Сибэнзим”);
6 и 7 - продукты ПЦР 831 и 495 п.о., полученные с использованием в качестве матрицы исходных плазмид pEV.CTL и pEV.Th, соответственно (положительный контроль).
Результаты, представленные на фиг. 7, показывают, что размеры амплифицированных фрагментов соответствуют теоретически рассчитанным размерам продуктов амплификации: 831 п.н. п.о. для гена EV.CTL и 495 п.н. п.о. для гена EV.Th. Аналогичные фрагменты ПЦР были получены при использованием в качестве матрицы исходных целевых плазмид pEV.CTL и pEV.Th (положительный контроль). Полученные данные указывают на наличие специфических мРНК в общей фракции клеточной РНК.
Иммуногистохимическое окрашивание клеток, трансфицированных плазмидами pEV.CTL и pEV.Th оценивали с помощью антител МАТ 29F2/30A6 к маркерному эпитопу EPFRDYVDRFYKTL, входящему в состав всех конструкций. На фиг. 8 приведены данные по регистрации продуктов экспрессии ДНК-вакцинных конструкций pEV.CTL и pEV.Th в клетках 293T, с помощью иммуногистохимического окрашивания: (A) 293T клетки, трансфицированные плазмидой pEV.CTL; (Б) 293T клетки, трансфицированные плазмидой pEV.Th и (B) 293T клетки, трансфицированные векторной плазмидой pcDNA3.1. Результаты, представленные на фиг. 8, свидетельствуют о наличии специфических белков в клетках, трансфицированных целевыми плазмидами. Полученные данные, подтверждают экспрессию целевых генов, как на уровне транскрипции, так и на уровне трансляции.
Пример 3. Исследование иммуногенности ДНК-вакцинных конструкций, кодирующих множественные Т-клеточные эпитопы вируса Эбола
Иммуногенность целевых ДНК-вакцинных конструкций оценивали по их способности индуцировать Т-клеточный ответ у мышей BALB/c через 14 дней после третьей иммунизации. Величину Т-клеточного иммунного ответа определяли с помощью методов IFNγ- ELISpot и ICS.
На фиг. 9 приведены данные исследования количества IFNγ-продуцирующих Т-клеток в реакции IFNγ-ELISpot у мышей линии BALB/c, иммунизированных ДНК-вакцинными конструкциями, кодирующими целевые иммуногены (n = 6 для контрольной группы PBS, n = 10 для остальных групп). На графике представлены количества спотов (количество IFNγ-продуцирующих Т-клеток), полученные для различных экспериментальных и контрольных групп животных. Результаты ELISpot, представленные на фиг. 9, показывают, что индукция специфического ответа наблюдается в обеих экспериментальных группах [pE-CTL+pE-Th] и [pE-CTL], особенно четко, в группе животных, иммунизированных смесью целевых ДНК-вакцинных конструкций [pE-CTL+pE-Th]. Достоверные отличия от обеих отрицательных контрольных групп PBS и pcDNA3.1 были обнаружены только в группе [pE-CTL+pE-Th] (см. табл. 1).
Таблица 1. Результаты статистического анализа данных, полученные в реакции ELISpot
Способность вакцинных конструкций индуцировать ответы IFNγ-продуцирующих CD4+ и CD8+ Т-клеток тестировали с помощью метода ICS после стимуляции специфическими пептидами спленоцитов мышей линии BALB/c, иммунизированных ДНК-вакцинными конструкциями, кодирующими целевые иммуногены. Результаты, представленные на фиг. 10, показывают, что статистически значимые отличия от контроля (группа PBS) (табл. 2) показали ответы IFNγ-продуцирующих CD8+ Т-лимфоцитов (IFNγ+CD8+T-клетки) в группе животных, иммунизированных как ДНК-вакциной pEV.CTL (группа pE-CTL, p = 0.024), так и комбинацией вакцинных конструкций (группа pE-CTL+pE-Th p = 0.024), а также ответы IFNγ-продуцирующих CD4+ Т-хелперов (IFNγ+CD4+T-клетки) в группе животных, иммунизированных комбинацией вакцинных конструкций (pE-CTL+pE-Th¸ p = 0.012). Максимальные ответы IFNγ-продуцирующих CD8+ Т-лимфоцитов и CD4+ T-клеток, были выявлены в группе животных, иммунизированных комбинацией вакцинных конструкций. Возможно данный эффект обусловлен синергетическим действием CD8+ и CD4+ T-лимфоцитов.
Таблица 2. Результаты статистического анализа, полученные с помощью ICS
Для проектирования аминокислотных последовательностей целевых антигенов в работе использовалась программа PolyCTLDesigner, которая была разработана нами ранее для рационального проектирования искусственных полиэпитопных вакцинных конструкций [19]. Программа позволяет рассчитать аминокислотную последовательность полиэпитопного антигена, подбирая оптимальные спейсеры для каждой пары эпитопов и оптимальное взаимное расположение эпитопов в рамках конструкции с учетом современных знаний о специфичности протеасомного процессинга антигенов и о взаимодействии пептидов с TAP. Полученные результаты показали, что спроектированные с помощью программы PolyCTLDesigner искусственные ДНК-вакцинные конструкции, кодирующие CTL и Th-эпитопы антигенов вируса Эбола, обеспечивают экспрессию целевых генов, а также индуцирую вирус-специфические ответы CD4+ и CD8+ Т-лимфоцитов у иммунизированных мышей.
В настоящее время опубликовано несколько работ, содержащих сведения о программном обеспечении, предназначенном для рационального проектирования полиэпитопных Т-клеточных иммуногенов [20-22]. Однако, воспользоваться этими программами не представляется возможным, поскольку они не распространяются по лицензии с открытым исходным кодом.
Таким образом, в данной работе с использованием оригинального программного обеспечения TEpredict/PolyCTLDesigner в составе семи белков вируса Эбола (GP, VP24, VP30, VP35, L, VP40, и NP) предсказаны цитотоксические и Т-хелперные эпитопы, на основе которых проведен дизайн двух полиэпитопных иммуногенов EV.CTL и EV.Th. Получены рекомбинантные плазмиды - кандидаты ДНК-вакцины против вируса Эбола, кодирующие спроектированные антигены. Показано, что сконструированные ДНК-вакцинные конструкции обеспечивают синтез соответствующих мРНК и белков в культуре эукариотических клеток, а также индуцируют у иммунизированных животных статистически значимые ответы как CD4+, так и CD8+ T-лимфоцитов и, следовательно, являются перспективными кандидатами для дальнейших исследований их способности индуцировать цитотоксический и протективный ответы.
Источники патентной и научно-технической информации
1. Marzi A., Feldmann H. Ebola virus vaccines: an overview of current approaches // Expert review of vaccines. 2014, Vol. 13, No. 4, С. 521-531.
2. Henao-Restrepo A.M. et al. Efficacy and effectiveness of an rVSV-vectored vaccine in preventing Ebola virus disease: final results from the Guinea ring vaccination, open-label, cluster-randomised trial (Ebola Ça Suffit!) // Lancet. 2017, Vol. 389, No. 10068, P. 505-518.
3. Wu L. et al. Open-label phase I clinical trial of Ad5-EBOV in Africans in China // Hum Vaccin Immunother. 2017, Vol. 13, No. 9, P. 2078-2085.
4. Dolzhikova I.V. et al. Safety and immunogenicity of GamEvac-Combi, a heterologous VSV- and Ad5-vectored Ebola vaccine: An open phase I/II trial in healthy adults in Russia // Hum Vaccin Immunother. 2017, Vol. 13, No. 3. P. 613-620.
5. Shedlock D.J., Aviles J., Talbott K.T., et al. Induction of broad cytotoxic T cells by protective DNA vaccination against Marburg and Ebola // Mol Ther. 2013; Vol. 21, P. 1432-44.
6. Krause P.R., Bryant P.R., Clark T., Dempsey W., Henchal E., Michael N.L., Regules .JA., Gruber M.F. Immunology of protection from Ebola virus infection // Sci Transl Med. 2015, Vol. 7, No. 286, doi: 10.1126/scitranslmed.aaa8202.
7. Takada A., Ebihara H., Feldmann H. et al. Epitopes required for antibody-dependent enhancement of Ebola virus infection // J. Infec. Dis. 2007. V. 196. P. 347-356.
8. Wilson J.A., Hart M.K. // Protection from Ebola Virus Mediated by Cytotoxic T Lymphocytes Specific for the Viral Nucleoprotein // J. Virol. 2001. V. 75. № 6. P. 2660-2664.
9. Sullivan N.J., Hensley L., Asiedu C., Geisbert T.W., Stanley D., Johnson J., Honko A., Olinger G., Bailey M., Geisbert J.B., Reimann K.A., Bao S., Rao S., Roederer M., Jahrling P.B., Koup R.A., Nabel G.J. CD8+ cellular immunity mediates rAd5 vaccine protection against Ebola virus infection of nonhuman primates // Nat Med. 2011, Vol. 17, No. 9, P.1128-31. doi: 10.1038/nm.2447.
10. Lu S., Wang S., Grimes-Serrano J.M. Current progress of DNA vaccine studies in humans // Expert Rev Vaccines. 2008, Vol. 7, No. 2, P. 175-91.
11. Grant-Klein R.J., Van Deusen N.M., Badger C.V., et al. A multiagent filovirus DNA vaccine delivered by intramuscular electroporation completely protects mice from Ebola and Marburg virus challenge // Hum Vaccin Immunother. 2012, Vol. 8, No. 11, P. 1703-6.
12. Bazhan S.I., Karpenko L.I., Ilyicheva T.N., Belavin P.A., Seregin S.V., Danilyuk N.K., Antonets D.V., Ilyichev A.A. Rational-Design Based Synthetic Polyepitope DNA Vaccine for Eliciting HIV-Specific CD8+ T cell Responses// Mol. Immunol. 2010, Vol.47, No.7-8, P.1507-15.
13. Hanke, T. and A. J. McMichael. Design and construction of an experimental HIV-1 vaccine for a year-2000 clinical trial in Kenya // Nature Medicine 2000, Vol. 6, No. 9, P. 951-955.
14. Karpenko L.I., Bazhan S.I., Antonets D.V., Belaykov I.M. Novel approaches in polyepitope T-cell vaccine development against HIV-1 // Expert Review of Vaccine 2014, Vol.13, No. 1, P.155-73. doi: 10.1586/14760584.2014.861748.
15. Khan M.A., Hossain M.U., Rakib-Uz-Zaman S.M., Morshed M.N. Epitope-based peptide vaccine design and target site depiction against Ebola viruses: an immunoinformatics study // Scand J Immunol. 2015, Vol. 82, N0. 1, P.25-34. doi:10.1111/sji.12302.
16. Villalobos A., Welch M., and Minshull J., In silico design of functional DNA constructs // Methods Mol. Biol. 2012, Vol. 852, P. 197-213.
17. Deml L., Bojak A., Steck S., Graf M., Wild J., Schirmbeck R., Wolf H., and Wagner R., Multiple effects of codon usage optimization on expression and immunogenicity of DNA candidate vaccines encoding the human immunodeficiency virus type 1 Gag protein // J. Virol. 2001, Vol. 75, N. 22, P. 10991-1001.
18. Маниатис Т., Фрич Э., Сэмбрук Дж. Молекулярное клонирование. - М.: Мир. - 1984.
19. Antonets D.V., Bazhan S.I. PolyCTLDesigner: a computational tool for constructing polyepitope T-cell antigens // BMC Res. Notes. 2013, Oct 10;6:407. doi: 10.1186/1756-0500-6-407.
20. Pinchuk, I., B. C. Starcher, B. Livingston, A. Tvninnereim, S. P. Wu, E. Appella, J. Sidney, A. Sette and B. Wizel. A CD8(+) T cell heptaepitope minigene vaccine induces protective immunity against Chlamydia pneumoniae // Journal of Immunology. 2005, Vol. 174, No.9, P. 5729-5739.
21. He Y.Q., R. Rappuol, A.S. De Groot and R.T. Chen. Emerging Vaccine Informatics // Journal of Biomedicine and Biotechnology. Vol. 2010 doi:10.1155/2010/218590.
22. Lee, Y., G. Ferrari and S.C. Lee. Estimating design space available for polyepitopes through consideration of major histocompatibility complex binding motifs // Biomedical Microdevices. 2010, Vol. 12, No.2, P. 207-222.
23. Патент РФ №2578159, МПК А61К39/12, опубл. 20.03.2016 (прототип).
ПРИЛОЖЕНИЕ
--->
Перечень последовательностей
<110> Федеральное бюджетное учреждение науки «Государственный научный центр вирусологии и биотехнологии «Вектор» Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (ФБУН ГНЦ ВБ «Вектор» Роспотребнадзора)
<120> Искусственные гены, кодирующие белки-иммуногены EV.CTL и EV.Th, рекомбинантные плазмидные ДНК pEV.CTL и рEV.Th, обеспечивающие экспрессию искусственных генов и искусственные Т-клеточные полиэпитопные белки-иммуногены EV.CTL и EV.Th, содержащие эпитопы антигенов вируса Эбола для индукции специфического иммунитета против вируса Эбола.
<160> SEQ ID NO 4
<210> SEQ ID NO:1
<211> 627
<212> PRT
<213> Artificial Sequence
<220>
<223> Аминокислотная последовательность искусственного поли-CTL-эпитопного антигена EV.CTL вируса Эбола
<400> 1
Met Gln Ile Phe Val Lys Thr Leu Thr Gly Lys Thr Ile Thr Leu
1 5 10 15
Glu Val Glu Pro Ser Asp Thr Ile Glu Asn Val Lys Ala Lys Ile
20 25 30
Gln Asp Lys Glu Gly Ile Pro Pro Asp Gln Gln Arg Leu Ile Phe
35 40 45
Ala Gly Lys Gln Leu Glu Asp Gly Arg Thr Leu Ser Asp Tyr Asn
50 55 60
Ile Gln Lys Glu Ser Thr Leu His Leu Val Leu Arg Leu Arg Gly
65 70 75
Val Arg Thr Met Met Val Ile Phe Arg Leu Met Arg Ala Asp Leu
80 85 90
Ser Gly His Met Met Val Ile Phe Arg Leu Lys Lys Val Gln Leu
95 100 105
Pro Gln Tyr Phe Thr Phe Ala Asp Leu Ser Lys Gln Ile Pro Ile
110 115 120
Trp Leu Pro Leu Arg Lys Glu Tyr Ala Pro Phe Ala Arg Leu Leu
125 130 135
Arg Val Pro Thr Val Phe His Lys Lys Phe Ile Tyr Phe Gly Lys
140 145 150
Lys Gln Tyr Arg Val Leu Tyr His Arg Tyr Asn Leu Val Ala Asp
155 160 165
Leu Tyr Gln Gly Asp Tyr Lys Leu Phe Leu Ala Phe Pro Arg Cys
170 175 180
Arg Tyr Val His Lys Ala Thr Pro Val Met Ser Arg Phe Ala Ala
185 190 195
Ala Phe Ala Glu Gly Val Val Ala Phe Leu Lys Val Tyr Trp Ala
200 205 210
Gly Ile Glu Phe Arg Thr Val Ala Pro Pro Ala Pro Val Tyr Thr
215 220 225
Leu Ala Ser Ile Gly Thr Ala Phe Arg Thr Thr Ile Gly Glu Trp
230 235 240
Ala Phe Trp Arg Lys Leu Ala Asn Glu Thr Thr Gln Ala Leu Phe
245 250 255
Leu Leu Gln Leu Asn Glu Thr Ile Arg Phe Val His Ser Gly Phe
260 265 270
Ile Tyr Phe Lys Ile Ile Ser Asp Leu Ser Ile Phe Ile Arg Asn
275 280 285
Phe Phe His Ala Ser Leu Ala Tyr Arg Arg Leu Ala Asn Pro Thr
290 295 300
Ala Asp Asp Phe Lys Ile Leu Met Asn Phe His Gln Lys Lys Ala
305 310 315
Asp Leu Ser Phe Thr Pro Gln Phe Leu Leu Gln Leu Tyr Ser Gly
320 325 330
Asn Ile Val His Arg Tyr Ala Asp Leu Ala Arg Thr Ser Phe Phe
335 340 345
Leu Trp Val Ile Arg Thr Phe Ser Ile Leu Asn Arg Lys Arg Lys
350 355 360
Leu Ser Asp Leu Cys Asn Phe Leu Val Ala Asp Leu Val His Met
365 370 375
Met Val Ile Phe Arg Leu Met Ala Asp Leu Lys Ile Met Tyr Asp
380 385 390
His Leu Pro Gly Phe Ala Leu Pro Gln Tyr Phe Thr Phe Asp Leu
395 400 405
Tyr Leu Glu Gly His Gly Phe Arg Phe Arg Phe Leu Ser Phe Ala
410 415 420
Ser Leu Phe Leu Arg Thr Arg Ser Phe Thr Thr His Phe Leu Arg
425 430 435
Leu Met Arg Thr Asn Phe Leu Ile Ala Asp Gly Phe Arg Leu Met
440 445 450
Arg Thr Asn Phe Leu Arg Gly Gln Phe Leu Ser Phe Ala Ser Leu
455 460 465
Arg Ser Phe Ala Ser Leu Phe Leu Pro Lys Arg Leu Ala Ser Thr
470 475 480
Val Ile Tyr Arg Ala Arg Leu Ser Ser Pro Ile Val Leu Ala His
485 490 495
Pro Leu Ala Arg Thr Ala Lys Val Gln Phe Leu Ser Phe Ala Ser
500 505 510
Leu Phe Arg Gly Tyr Leu Glu Gly Thr Arg Thr Leu Arg Phe Arg
515 520 525
Tyr Glu Phe Thr Ala Pro Phe Lys Lys Tyr Phe Thr Phe Asp Leu
530 535 540
Thr Ala Leu Lys Glu Tyr Leu Phe Glu Val Asp Asn Leu Arg Pro
545 550 555
Gly Pro Ala Lys Phe Ser Leu Leu Arg Lys Leu Phe Leu Arg Ala
560 565 570
Thr Thr Glu Leu Arg Lys Asn Tyr Asn Gly Leu Leu Ser Ser Ile
575 580 585
Arg Leu Tyr Asp Arg Leu Ala Ser Thr Val Arg Lys Phe Ile Asn
590 595 600
Lys Leu Asp Ala Leu His Ser Gly Ser Gly Thr Gly Glu Pro Phe
605 610 615
Arg Asp Tyr Val Asp Arg Phe Tyr Lys Thr Leu Arg
620 625
<210> SEQ ID NO:2
<211> 382
<212> PRT
<213> Artificial Sequence
<220>
<223> Аминокислотная последовательность искусственного поли-Th-эпитопного антигена EV.Th вируса Эбола
<400> 1
Met Gly Val Thr Gly Ile Leu Gln Leu Pro Arg Asp Arg Phe Lys
1 5 10 15
Arg Thr Ser Phe Phe Leu Trp Val Ile Ile Leu Phe Gln Arg Thr
20 25 30
Phe Ser Ile Pro Leu Gly Val Ile His Asn Ser Thr Leu Gln Val
35 40 45
Ser Asp Val Asp Lys Leu Arg Arg Thr Asn Thr Asn His Phe Asn
50 55 60
Met Arg Thr Gln Arg Val Lys Glu Gln Leu Ser Leu Lys Met Leu
65 70 75
Ser Leu Ile Arg Ser Asn Ile Leu Lys Phe Ile Asn Lys Leu Asp
80 85 90
Ala Arg Arg Leu Thr Leu Asp Asn Phe Leu Tyr Tyr Leu Thr Thr
95 100 105
Gln Ile His Asn Leu Pro His Arg Ser Leu Arg Ile Leu Lys Pro
110 115 120
Thr Phe Lys His Ala Ser Val Met Ser Arg Leu Arg Arg Thr Gln
125 130 135
Thr Tyr His Phe Ile Arg Thr Ala Lys Gly Arg Ile Thr Lys Leu
140 145 150
Val Asn Asp Tyr Leu Lys Phe Phe Leu Ile Val Gln Ala Leu Lys
155 160 165
His Asn Gly Thr Trp Gln Ala Glu Arg Arg Trp Asp Arg Gln Ser
170 175 180
Leu Ile Met Phe Ile Thr Ala Phe Leu Asn Ile Ala Leu Gln Leu
185 190 195
Pro Cys Glu Ser Ser Ala Val Val Val Ser Gly Leu Arg Thr Leu
200 205 210
Val Pro Gln Ser Asp Arg Arg Ser Ser Ala Phe Ile Leu Glu Ala
215 220 225
Met Val Asn Val Ile Ser Gly Pro Lys Val Leu Met Lys Gln Ile
230 235 240
Pro Ile Trp Leu Pro Leu Gly Val Ala Asp Gln Lys Thr Tyr Ser
245 250 255
Phe Arg Arg Gln Tyr Pro Thr Ala Trp Gln Ser Val Gly His Met
260 265 270
Met Val Ile Phe Arg Leu Met Arg Thr Asn Phe Leu Ile Lys Phe
275 280 285
Leu Leu Ile His Gln Gly Met His Met Val Ala Gly His Arg Arg
290 295 300
Glu Ser Ala Asp Ser Phe Leu Leu Met Leu Cys Leu His His Ala
305 310 315
Tyr Gln Gly Asp Tyr Lys Leu Phe Leu Glu Ser Gly Ala Val Lys
320 325 330
Tyr Leu Glu Arg Arg Ala Lys Phe Val Ala Ala Trp Thr Leu Lys
335 340 345
Ala Ala Ala Ser Gly Ser Gly Glu Pro Phe Arg Asp Tyr Val Asp
350 355 360
Arg Phe Tyr Lys Thr Leu Arg Ser Gly Ser Gly Arg Lys Arg Ser
365 370 375
His Ala Gly Tyr Gln Thr Ile
380
<210> SEQ ID NO:3
<211> 1911
<212> DNA
<213> Artificial Sequence
<220>
<223> Искусственный ген, кодирующий поли-CTL-эпитопный иммуноген вируса Эбола
<400> 2
tc tag acc gcc acc atg caa atc ttt gta aaa acc ctg acc gga 44
Met Gln Ile Phe Val Lys Thr Leu Thr Gly
1 5 10
aag acc atc acc ttg gaa gtg gaa cct agt gac act att gaa aat 89
Lys Thr Ile Thr Leu Glu Val Glu Pro Ser Asp Thr Ile Glu Asn
15 20 25
gtt aag gct aag ata cag gat aaa gag ggg atc cct cct gac cag 134
Val Lys Ala Lys Ile Gln Asp Lys Glu Gly Ile Pro Pro Asp Gln
30 35 40
caa cgg ctc atc ttt gct ggt aaa cag ctc gag gac gga cgg act 179
Gln Arg Leu Ile Phe Ala Gly Lys Gln Leu Glu Asp Gly Arg Thr
45 50 55
ctg tct gat tac aat atc cag aag gaa agc acc cta cac ctg gtt 224
Leu Ser Asp Tyr Asn Ile Gln Lys Glu Ser Thr Leu His Leu Val
60 65 70
cta aga ctg cga ggt gta cgt acg atg atg gta ata ttc cga cta 269
Leu Arg Leu Arg Gly Val Arg Thr Met Met Val Ile Phe Arg Leu
75 80 85
atg agg gcc gat cta tct gga cat atg atg gtt ata ttt cgc ctt 314
Met Arg Ala Asp Leu Ser Gly His Met Met Val Ile Phe Arg Leu
90 95 100
aag aag gtc cag ctg cct cag tat ttt aca ttc gca gac cta agc 359
Lys Lys Val Gln Leu Pro Gln Tyr Phe Thr Phe Ala Asp Leu Ser
105 110 115
aaa cag att ccg atc tgg ttg cca cta cgg aag gag tat gca ccc 404
Lys Gln Ile Pro Ile Trp Leu Pro Leu Arg Lys Glu Tyr Ala Pro
120 125 130
ttt gcc cgg ctg ctg agg gtg ccc acc gta ttt cac aag aag ttc 449
Phe Ala Arg Leu Leu Arg Val Pro Thr Val Phe His Lys Lys Phe
135 140 145
atc tat ttt ggt aaa aag caa tac cga gtc ctg tac cat aga tac 494
Ile Tyr Phe Gly Lys Lys Gln Tyr Arg Val Leu Tyr His Arg Tyr
150 155 160
aac ctg gtc gct gac ctg tac cag ggt gat tac aag ctg ttc ctc 539
Asn Leu Val Ala Asp Leu Tyr Gln Gly Asp Tyr Lys Leu Phe Leu
165 170 175
gcc ttc cca aga tgc agg tat gtt cac aaa gct acc cct gtc atg 584
Ala Phe Pro Arg Cys Arg Tyr Val His Lys Ala Thr Pro Val Met
180 185 190
tcc aga ttc gct gca gcc ttc gca gag ggt gtg gtc gcg ttc ttg 629
Ser Arg Phe Ala Ala Ala Phe Ala Glu Gly Val Val Ala Phe Leu
195 200 205
aag gtc tac tgg gcg gga atc gag ttc cga aca gta gct cct cct 674
Lys Val Tyr Trp Ala Gly Ile Glu Phe Arg Thr Val Ala Pro Pro
210 215 220
gct cct gtt tac acc cta gca agc atc gga acc gcg ttc cgc act 719
Ala Pro Val Tyr Thr Leu Ala Ser Ile Gly Thr Ala Phe Arg Thr
225 230 235
aca att ggg gag tgg gct ttt tgg agg aaa ctc gct aac gag aca 764
Thr Ile Gly Glu Trp Ala Phe Trp Arg Lys Leu Ala Asn Glu Thr
240 245 250
act cag gca ctc ttc ctg cta cag ctg aat gag aca atc agg ttc 809
Thr Gln Ala Leu Phe Leu Leu Gln Leu Asn Glu Thr Ile Arg Phe
255 260 265
gtt cac agt ggg ttc atc tac ttt aaa atc ata agc gac ctt tct 854
Val His Ser Gly Phe Ile Tyr Phe Lys Ile Ile Ser Asp Leu Ser
270 275 280
att ttt ata cgt aat ttt ttc cat gca tct ctc gcc tac agg cgg 899
Ile Phe Ile Arg Asn Phe Phe His Ala Ser Leu Ala Tyr Arg Arg
285 290 295
tta gcg aac cca aca gcc gat gat ttc aag att ttg atg aat ttc 944
Leu Ala Asn Pro Thr Ala Asp Asp Phe Lys Ile Leu Met Asn Phe
300 305 310
cac caa aag aag gca gat ctg agt ttc acc cct cag ttt cta ctg 989
His Gln Lys Lys Ala Asp Leu Ser Phe Thr Pro Gln Phe Leu Leu
315 320 325
cag ctg tac tct ggg aat atc gtg cat agg tac gcc gac ctc gcc 1034
Gln Leu Tyr Ser Gly Asn Ile Val His Arg Tyr Ala Asp Leu Ala
330 335 340
cgc acc tca ttc ttc cta tgg gtc att aga acc ttt agc atc ctt 1079
Arg Thr Ser Phe Phe Leu Trp Val Ile Arg Thr Phe Ser Ile Leu
345 350 355
aat cgc aag cgg aaa ctt agt gac ctt tgt aac ttt ctt gta gcc 1124
Asn Arg Lys Arg Lys Leu Ser Asp Leu Cys Asn Phe Leu Val Ala
360 365 370
gac ctg gtg cac atg atg gtg ata ttt cgc ctg atg gca gac ctc 1169
Asp Leu Val His Met Met Val Ile Phe Arg Leu Met Ala Asp Leu
375 380 385
aag atc atg tat gac cat ctt ccc ggg ttt gcc cta cca cag tat 1214
Lys Ile Met Tyr Asp His Leu Pro Gly Phe Ala Leu Pro Gln Tyr
390 395 400
ttc act ttc gat ctt tac ttg gag gga cac ggg ttt cgc ttt aga 1259
Phe Thr Phe Asp Leu Tyr Leu Glu Gly His Gly Phe Arg Phe Arg
405 410 415
ttt ctg tcg ttt gcc tcc ctt ttt ctg aga acg cgt tcg ttc acc 1304
Phe Leu Ser Phe Ala Ser Leu Phe Leu Arg Thr Arg Ser Phe Thr
420 425 430
acc cac ttt ctg aga ctg atg cgc aca aat ttc ctc atc gcc gac 1349
Thr His Phe Leu Arg Leu Met Arg Thr Asn Phe Leu Ile Ala Asp
435 440 445
ggt ttc cgg ctt atg cgg acc aac ttt ctg cgt ggg caa ttc ctg 1394
Gly Phe Arg Leu Met Arg Thr Asn Phe Leu Arg Gly Gln Phe Leu
450 455 460
agt ttc gcg tct ctg agg agc ttt gca tcc ctg ttc cta ccc aaa 1439
Ser Phe Ala Ser Leu Arg Ser Phe Ala Ser Leu Phe Leu Pro Lys
465 470 475
aga ctg gcc agc aca gtg atc tac cgc gcg aga ctg tcg tcg cct 1484
Arg Leu Ala Ser Thr Val Ile Tyr Arg Ala Arg Leu Ser Ser Pro
480 485 490
att gtt ctg gct cat cca ctg gct cgt act gcc aaa gtt cag ttc 1529
Ile Val Leu Ala His Pro Leu Ala Arg Thr Ala Lys Val Gln Phe
495 500 505
ctt tca ttt gca tca ctg ttc cgt ggg tac ctg gaa ggc acc aga 1574
Leu Ser Phe Ala Ser Leu Phe Arg Gly Tyr Leu Glu Gly Thr Arg
510 515 520
acc ctg aga ttc cgg tac gag ttt acc gct cct ttc aag aaa tac 1619
Thr Leu Arg Phe Arg Tyr Glu Phe Thr Ala Pro Phe Lys Lys Tyr
525 530 535
ttc acc ttt gat ctt acg gcc ctg aag gag tac ttg ttt gag gtg 1664
Phe Thr Phe Asp Leu Thr Ala Leu Lys Glu Tyr Leu Phe Glu Val
540 545 550
gac aac ctg aga ccc ggc cca gcc aaa ttc agc ctc ctg cga aaa 1709
Asp Asn Leu Arg Pro Gly Pro Ala Lys Phe Ser Leu Leu Arg Lys
555 560 565
ttg ttc ttg agg gcc act acc gag ctg cgc aag aat tac aac ggg 1754
Leu Phe Leu Arg Ala Thr Thr Glu Leu Arg Lys Asn Tyr Asn Gly
570 575 580
ctc ctg tca agt atc aga ctt tac gac agg ctg gcc agt acc gta 1799
Leu Leu Ser Ser Ile Arg Leu Tyr Asp Arg Leu Ala Ser Thr Val
585 590 595
agg aag ttc atc aat aag ctc gac gcc ctc cat agc ggg tct ggc 1844
Arg Lys Phe Ile Asn Lys Leu Asp Ala Leu His Ser Gly Ser Gly
600 605 610
acc ggt gag cca ttt aga gat tac gtt gat aga ttc tac aag aca 1889
Thr Gly Glu Pro Phe Arg Asp Tyr Val Asp Arg Phe Tyr Lys Thr
615 620 625
ctg agg tga tga tag ggg ccc 1910
Leu Arg ***
<210> SEQ ID NO:4
<211> 1188
<212> DNA
<213> Artificial Sequence
<220>
<223> Искусственный ген, кодирующий поли-Th-эпитопный иммуноген вируса Эбола
<400> 2
ga att ccc gcc acc atg ggg gtc acc gga ata ctc caa cta ccc 44
Met Gly Val Thr Gly Ile Leu Gln Leu Pro
1 5 10
aga gac cgt ttc aag agg act tca ttc ttt ctt tgg gtg att atc 89
Arg Asp Arg Phe Lys Arg Thr Ser Phe Phe Leu Trp Val Ile Ile
15 20 25
ctc ttt cag agg acc ttt agt att ccc ctc ggt gtt att cac aat 134
Leu Phe Gln Arg Thr Phe Ser Ile Pro Leu Gly Val Ile His Asn
30 35 40
tcg acc ctg cag gtt tcc gac gtt gac aag ctg agg agg acg aac 179
Ser Thr Leu Gln Val Ser Asp Val Asp Lys Leu Arg Arg Thr Asn
45 50 55
acc aac cac ttt aat atg aga acc cag aga gtc aaa gag cag ctg 224
Thr Asn His Phe Asn Met Arg Thr Gln Arg Val Lys Glu Gln Leu
60 65 70
agc tta aaa atg ctg agc ctc att aga agt aat att ctt aag ttt 269
Ser Leu Lys Met Leu Ser Leu Ile Arg Ser Asn Ile Leu Lys Phe
75 80 85
atc aac aaa ctc gat gct agg aga ctc aca ctt gac aat ttc ctg 314
Ile Asn Lys Leu Asp Ala Arg Arg Leu Thr Leu Asp Asn Phe Leu
90 95 100
tat tac ctg acc aca cag ata cat aat ctg ccc cac cgt agt tta 359
Tyr Tyr Leu Thr Thr Gln Ile His Asn Leu Pro His Arg Ser Leu
105 110 115
agg atc tta aaa ccc act ttc aag cat gcg tca gtg atg agc agg 404
Arg Ile Leu Lys Pro Thr Phe Lys His Ala Ser Val Met Ser Arg
120 125 130
ctg cgc cgg aca caa act tac cat ttc ata cga acc gca aag gga 449
Leu Arg Arg Thr Gln Thr Tyr His Phe Ile Arg Thr Ala Lys Gly
135 140 145
cga atc aca aag cta gtg aat gac tac ctg aag ttc ttc ctt atc 494
Arg Ile Thr Lys Leu Val Asn Asp Tyr Leu Lys Phe Phe Leu Ile
150 155 160
gtc caa gca ttg aaa cac aat ggg aca tgg cag gct gaa aga cgc 539
Val Gln Ala Leu Lys His Asn Gly Thr Trp Gln Ala Glu Arg Arg
165 170 175
tgg gat agg cag tcc ctg ata atg ttt atc act gca ttt ctg aac 584
Trp Asp Arg Gln Ser Leu Ile Met Phe Ile Thr Ala Phe Leu Asn
180 185 190
atc gct ctc caa ctt cct tgc gaa tcc tct gct gtg gtg gtc tct 629
Ile Ala Leu Gln Leu Pro Cys Glu Ser Ser Ala Val Val Val Ser
195 200 205
ggg ctg agg act ctc gtc cca caa tcc gac aga cga agc tct gca 674
Gly Leu Arg Thr Leu Val Pro Gln Ser Asp Arg Arg Ser Ser Ala
210 215 220
ttc ata cta gaa gct atg gtt aat gtg atc tcc ggc cct aaa gta 719
Phe Ile Leu Glu Ala Met Val Asn Val Ile Ser Gly Pro Lys Val
225 230 235
ctg atg aaa cag ata cca ata tgg ctt ccc ctg ggc gtg gcc gac 764
Leu Met Lys Gln Ile Pro Ile Trp Leu Pro Leu Gly Val Ala Asp
240 245 250
caa aaa act tat agt ttt cgg aga caa tat cca acc gca tgg cag 809
Gln Lys Thr Tyr Ser Phe Arg Arg Gln Tyr Pro Thr Ala Trp Gln
255 260 265
tcc gta ggt cac atg atg gtc att ttc cgc ctt atg agg aca aac 854
Ser Val Gly His Met Met Val Ile Phe Arg Leu Met Arg Thr Asn
270 275 280
ttc ctg atc aaa ttc ctg ctg att cac cag ggc atg cat atg gtg 899
Phe Leu Ile Lys Phe Leu Leu Ile His Gln Gly Met His Met Val
285 290 295
gct ggt cat agg aga gaa tcg gca gac agt ttt ctg tta atg ctg 944
Ala Gly His Arg Arg Glu Ser Ala Asp Ser Phe Leu Leu Met Leu
300 305 310
tgt tta cac cac gcc tac cag gga gat tat aaa ctg ttc ctt gaa 989
Cys Leu His His Ala Tyr Gln Gly Asp Tyr Lys Leu Phe Leu Glu
315 320 325
agc ggg gct gtg aaa tac ctg gag cgc cgc gcc aaa ttt gtc gcc 1034
Ser Gly Ala Val Lys Tyr Leu Glu Arg Arg Ala Lys Phe Val Ala
330 335 340
gca tgg acc ctg aaa gcg gcc gca tcc ggg tct gga gag ccc ttc 1079
Ala Trp Thr Leu Lys Ala Ala Ala Ser Gly Ser Gly Glu Pro Phe
345 350 355
aga gat tat gtg gac aga ttc tat aag aca ctg aga tca ggg tcg 1124
Arg Asp Tyr Val Asp Arg Phe Tyr Lys Thr Leu Arg Ser Gly Ser
360 365 370
ggt aga aaa aga agc cac gct gga tac cag acc att tga tga tag 1169
Gly Arg Lys Arg Ser His Ala Gly Tyr Gln Thr Ile ***
375 380
acc ggt tcc gga ggg ccc 1187
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ВИРУС ГРИППА, СПОСОБНЫЙ ИНФИЦИРОВАТЬ СОБАЧЬИХ, И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2802222C2 |
| ФРАГМЕНТ ДНК, КОДИРУЮЩИЙ СИНТЕЗ ГЛИКОПРОТЕИНА G ВИРУСА БЕШЕНСТВА, РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК PVG18-1, КОДИРУЮЩАЯ ГЛИКОПРОТЕИН G ВИРУСА БЕШЕНСТВА, ШТАММ БАКТЕРИЙ ESCHERICHIA COLI - ПРОДУЦЕНТ ГЛИКОПРОТЕИНА G ВИРУСА БЕШЕНСТВА | 1991 |
|
RU2008355C1 |
| ИММУНОГЕННЫЕ КОМПОЗИЦИИ ГЛИКОПРОТЕИНА G ВИРУСОВ HENDRA И NIPAH | 2012 |
|
RU2787820C2 |
| Антитела против белка р17 ВИЧ-1 субтипа А | 2019 |
|
RU2727673C1 |
| Вакцина против герпеса | 2019 |
|
RU2731073C1 |
| СПОСОБ УПРАВЛЕНИЯ РИТМОМ СЕРДЦА И СОКРАЩЕНИЕМ ОТДЕЛЬНЫХ КАРДИОМИОЦИТОВ ПРИ ПОМОЩИ ТЕРМОГЕНЕТИКИ | 2022 |
|
RU2802995C1 |
| МАТЕРИАЛЫ И МЕТОДЫ, ИСПОЛЬЗУЕМЫЕ ДЛЯ ЛЕЧЕНИЯ РЕСПИРАТОРНЫХ ЗАБОЛЕВАНИЙ У СОБАК | 2020 |
|
RU2811752C2 |
| КОНСТРУКЦИИ НУКЛЕИНОВОЙ КИСЛОТЫ И ВЕКТОРЫ ДЛЯ ГЕНОТЕРАПИИ ДЛЯ ПРИМЕНЕНИЯ ДЛЯ ЛЕЧЕНИЯ БОЛЕЗНИ ВИЛЬСОНА И ДРУГИХ СОСТОЯНИЙ | 2015 |
|
RU2745567C2 |
| ГЕННАЯ ТЕРАПИЯ ГИПОФОСФАТЕМИЧЕСКИХ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С ФАКТОРОМ РОСТА ФИБРОБЛАСТОВ 23 | 2020 |
|
RU2815545C2 |
| ИММУНОИНДУЦИРУЮЩЕЕ СРЕДСТВО | 2016 |
|
RU2744843C2 |









Изобретение относится к области биотехнологии и молекулярной биологии. Предложены искусственные гены, используемые для создания вакцины против вируса Эбола, кодирующие искусственный Т-клеточный белок-иммуноген EV.CTL и Т-клеточный белок-иммуноген EV.Th соответственно, со свойствами антигенов вируса Эбола, и имеющие последовательность SEQ ID NO: 3 длиной 1881 п.н. и SEQ ID NO: 4 длиной 1146 п.н., соответственно, содержащие на 5'-конце последовательность Козак (CCGCCACC) и сайт эндонуклеазы рестрикции XbaI и EcoRI соответственно, а на 3'-конце - три стоп-кодона (TGATGATAG) и сайт эндонуклеазы рестрикции ApaI, а также соответствующие рекомбинантные плазмиды и полиэпитопные белки-иммуногены. Изобретение может быть использовано в медицине. 6 н.п. ф-лы, 10 ил., 2 табл., 3 пр.
1. Искусственный ген, используемый для создания вакцины против вируса Эбола, кодирующий искусственный Т-клеточный белок-иммуноген EV.CTL со свойствами антигенов вируса Эбола и имеющий последовательность SEQ ID NO: 3 длиной 1881 п.н., содержащую на 5'-конце последовательность Козак (CCGCCACC) и сайт эндонуклеазы рестрикции XbaI, а на 3'-конце - три стоп-кодона (TGATGATAG) и сайт эндонуклеазы рестрикции ApaI.
2. Искусственный ген, используемый для создания вакцины против вируса Эбола, кодирующий искусственный Т-клеточный белок-иммуноген EV.Th со свойствами антигенов вируса Эбола и имеющий последовательность SEQ ID NO: 4 длиной 1146 п.н., содержащую на 5'-конце последовательность Козак (CCGCCACC) и сайт эндонуклеазы рестрикции EcoRI, а на 3'-конце - три стоп-кодона (TGATGATAG) и сайт эндонуклеазы рестрикции ApaI.
3. Рекомбинантная плазмидная ДНК pEV.CTL, используемая для создания вакцины против вируса Эбола, имеющая размер 7321 п.н., молекулярную массу 4.8×103 кДа, содержащая в соответствии с физической и генетической картой, представленной на Фиг. 5 А, целевой ген по п. 1, кодирующий искусственный Т-клеточный белок-иммуноген EV.CTL, находящийся под контролем промотора CMV, обеспечивающего его экспрессию в клетках млекопитающих, и состоящая из следующих фрагментов:
- XbaI-ApaI векторного фрагмента ДНК плазмиды pcDNA3.1-cassette2 размером 5413 п.н., содержащего промотор CMV и последовательность BGH polyA, обеспечивающие экспрессию гена EV.CTL в клетках млекопитающих; ген устойчивости к ампициллину bla (Ap-R) и pMB1 ori, обеспечивающие селекцию и размножение целевой плазмиды в клетках бактерий Escherichia coli;
- XbaI-ApaI - фрагмента размером 1910 п.н., содержащего ген EV.CTL и последовательность Козак с инициирующим кодоном ATG;
- уникальных сайтов рестрикции: XbaI (885), BamHI(1002), AgeI (2729), ApaI (2793), PciI(5495) и имеющей следующее положение генов: эукариотический промотор CMV pr начало (171) - 846).
4. Рекомбинантная плазмидная ДНК pEV.Th, используемая для создания вакцины против вируса Эбола, имеющая размер 6604 п.н., молекулярную массу 4.3×103 кДа, содержащая в соответствии с физической и генетической картой, представленной на Фиг. 5 Б, целевой ген по п. 2, кодирующий искусственный Т-клеточный белок-иммуноген EV.Th, находящийся под контролем промотора CMV, обеспечивающего его экспрессию в клетках млекопитающих и состоящая из следующих фрагментов:
- EcoRI-ApaI векторного фрагмента ДНК плазмиды pcDNA3.1-cassette 1 размером 5419 п.н., содержащего промотор CMV и последовательность BGH poly А, обеспечивающие экспрессию гена EV. CTL в клетках млекопитающих; ген устойчивости к ампициллину bla (Ap-R) и pMB1 ori, обеспечивающие селекцию и размножение целевой плазмиды в клетках бактерий Escherichia coli;
- EcoRI-ApaI - фрагмента размером 1185 п.н., содержащего ген EV.Th и последовательность Козак с инициирующим кодоном ATG;
- уникальных сайтов рестрикции: BglII(2), EcoRI(891), NotI(1941), AgeI(2060) ApaI(2076) и имеющей следующее положение генов:
эукариотический промотор CMV pr начало (171) - конец (846).
5. Поли-CTL-эпитопный белок-иммуноген EV.CTL, имеющий аминокислотную последовательность SEQ ID NO: 1 длиной 627 а.к.о. и долей спейсерных последовательностей равной 12.76%, на N-конце которой расположена последовательность убиквитина (MQIFVKTLTGKTITL EVEPSDTIENVKAKIQDKEGIPPDQQRLIFAGKQLEDGRTLSDYNIQKESTL HLVLRLRGV) с 76 а.к.о., а на С-конце - последовательность EPFRDYVDRFYKTLR маркерного эпитопа белка р24 HIV-1, узнаваемого моноклональными антителами 29F2, и используемый для создания вакцины против вируса Эбола.
6. Поли-Th-эпитопный белок-иммуноген EV.Th, имеющий аминокислотную последовательность SEQ ID NO: 2 длиной 382 а.к.о., на N-конце которой расположена последоватеьность MGVTGILQLPRDR сигнального пептида, на С-конце - С-концевой фрагмент белка LAMP1 (RKRSHAGYQTI), а на С-конце расположен маркерный эпитоп белка р24 HIV-1, узнаваемый моноклональными антителами 29F2 и используемый для создания вакцины против вируса Эбола.
| KULDEEP DHARMA | |||
| Advances in Designing and Developing Vaccines, Drugs, and Therapies to Counter Ebola Virus | |||
| Front | |||
| Immunol., 10.08.2018 | |||
| O | |||
| REYNARD | |||
| Kunjin Virus Replicon-Based Vaccines Expressing Ebola Virus Glycoprotein GP Protect the Guinea Pig Against Lethal Ebola Virus Infection | |||
| J Infect Dis | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| RU | |||
Авторы
Даты
2020-02-06—Публикация
2018-11-15—Подача