Изобретение относится к медицине, а именно к урологии и гематологии, и может быть использовано для прогнозирования развития гнойного пиелонефрита.
Среди всех урологических заболеваний острый пиелонефрит встречается наиболее часто и составляет 14% в структуре болезней почек. Гнойные его формы могут развиваться у 1/3 пациентов. Частота нефрэктомий по поводу гнойного пиелонефрита в отдельных клиниках достигает 40-50%. В настоящее время гнойный пиелонефрит диагностируется клинически, лабораторно, методами функциональной диагностики и рентгенографии.
Диагноз пиелонефрит ставят на основании данных функционального обследования - либо серозная форма, либо уже сформированный гнойный очаг и лабораторного обследования, при котором нет четких значений, указывающих на форму пиелонефрита. Поскольку все современные способы диагностики не способны осуществлять прогнозирование развития гнойного процесса, поиск новых подходов, разработка способов прогнозирования гнойного пиелонефрита на этапе перехода из серозной стадии процесса в гнойную является актуальным.
Известны способы диагностики гнойного пиелонефрита аппаратными методами с помощью ультразвукового исследования (УЗИ), компьюторной томографии (КТ), магнитнорезонансной томографии (МРТ), внутривенной урографии (Н.А. Лопаткин. Урология. Национальное руководство. Москва. 2013 г. 442-444), которые позволяют диагностировать уже развившийся гнойный процесс, но осуществлять прогноз известными способами является невозможным.
Наиболее близким по техническому результату является способ диагностики гнойного пиелонефрита путем лабораторного обследования: общий и биохимический анализ крови, общий анализ мочи, проба Реберга, бактериологический посев мочи с целью выявления возбудителя, его количества и чувствительности к антибактериальным препаратам (Н.А. Лопаткин. Клинические рекомендации. Урология. 2007 г. г Москва. 178-179.).
Однако лабораторные анализы указывают на степень тяжести воспалительного процесса, но не определяют наличие или отсутствие гнойного процесса, тем более не могут спрогнозировать развитие гнойного пиелонефрита.
Авторы предлагают способ прогнозирования развития гнойного пиелонефрита, обладающий высокой информативностью и точностью, что позволяет определить переход серозной стадии пиелонефрита в гнойную путем оценки состояния и изменения со стороны почечных сосудов, а именно повреждение эндотелия сосудов на фоне прогрессирования воспалительного процесса, что невозможно было определить известными способами.
При проведении информационного поиска не было обнаружено способа прогнозирования развития гнойного пиелонефрита.
Техническим результатом заявляемого изобретения является создание способа прогнозирования развития гнойного пиелонефрита, позволяющего выявлять на раннем этапе риск развития гнойного процесса и своевременно скорректировать терапию и, как следствие, более быстрое выздоровление за счет предотвращения развития нагноения воспалительного очага.
Технический результат достигается тем, что забор крови для исследования осуществляют при поступлении пациента в стационар и на 6-7 сутки лечения, свежесобранные образцы крови немедленно помещают на грелку со льдом, центрифугируют в течение дня при 1400g в течение 15 мин, при комнатной температуре, подготавливают последовательные разведения растворенного ET-SROCK в культуральной среде до значения 0,625 фмоль/мл используя как нулевой стандарт и проводят исследование с помощью иммуноферментного набора для количественного определения эндотелина (1-21) человека в сыворотке, плазме, моче, слюне, и супернатантных клеточных культурах, заключающийся во внесении по 50 мкл стандартов (белые крышки), образцов и контролей (желтые крышки) (STD/SAMPLE/CTRL) в соответствующие ячейки в дублях, лунка для бланка остается пустой; добавляют по 200 мкл детектирующих антител (АВ, зеленая крышка флакона) в каждую ячейку, кроме бланка, тщательно перемешивают; накрывают стрипы пленкой и инкубируют в течение ночи 16-24 часа при комнатной температуре 18-26°С; при исследовании удаляют пленку со стрипов, полностью удаляют содержимое ячеек и промывают их, 5 раз 300 мкл, разведенным буфером для промывок (WASHBUF), удаляют остаток жидкости в ячейках после последней промывки переворачиванием стрипов на фильтровальную бумагу; добавляют по 200 мкл ферментного конъюгата (CONJ) во все ячейки, накрывают стрипы пленкой и инкубируйте 1 час при комнатной температуре 18-26°С, удаляют пленку со стрипов. полностью удаляют содержимое ячеек и промывают их, 5 раз по 300 мкл, разведенным буфером для промывок (WASHBUF), удаляют остаток жидкости в ячейках после последней промывки переворачивают стрипы на фильтровальную бумагу; вносят по 200 мкл субстрата (SUB) во все ячейки, инкубируют 30 минут при комнатной температуре 18-26° в темноте; добавляют по 50 мкл стоп-раствора (STOP) во все ячейки, перемешивают содержимое ячеек, немедленно считают оптическую плотность ячеек при 450 нм с длиной волны сравнения 630 нм, вычитают значение оптической плотности (ОП) бланка из значений ОП остальных ячеек, строят калибровочную кривую, оценивают результаты, полученные данным методом с использованием алгоритма 4PL, определяют уровень эндотелина - 1 и при значении 1.20 фмоль/мл и более прогнозируют развитие гнойного пиелонефрита.
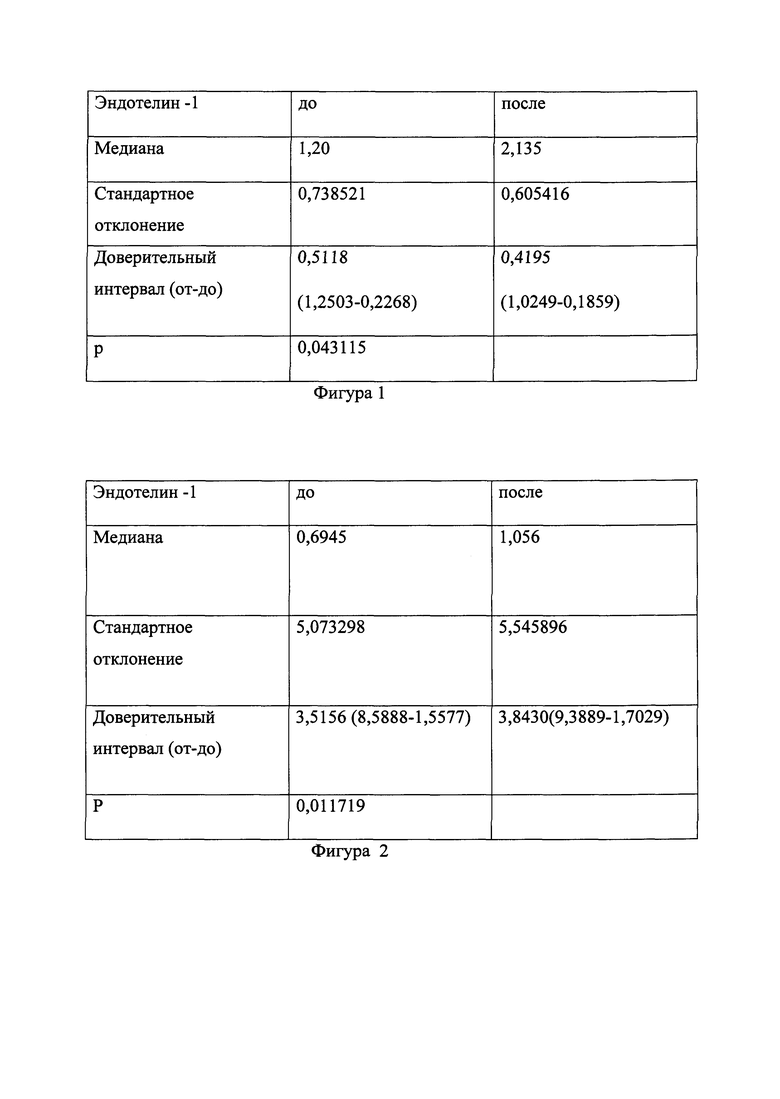
Заявляемый способ проиллюстрирован фигурами 1 и 2 в виде таблиц.
На фигуре 1 приведены данные уровня эдотелин-1у пациентов с пиелонефритом тяжелого течения.
На фигуре 2 приведены данные уровня эдотелин-1у пациентов с пиелонефритом легкого течения.
Статистическую обработку данных расчета достоверности различия показателей до и после лечения проводят с помощью критерия Вилкоксона, сравнение между группами проводится с помощью непараметрического метода U-теста Манна-Уитни. Критический уровень значимости различий (Р), определен как Р<0.05.
Способ осуществляют следующим образом.
Выполнение исследования проводят с помощью иммуноферментного набора (ЗАО «БиоХимМак», Москва), состоящего из реагентов:
PLATE - стрипованый микропланшет с лунками, покрытыми поликлональными антителами к эндотелину в держателе в запечатанном пакете из алюминиевой фольги с осушителем;
WASHBUF - Концентрат буфера для промывок (20-кратный); АВ (зеленая крышка) - Детектирующие антитела, моноклональные мышиные антитела к эндотелину, готовы к испльзованию;
STD (белые крышки) - Стандарты (0-10 фмоль/мл), содержащие синтетический человеческий эндотелии-1 (1-21) в человеческой плазме, лиофилизированные. Флаконы с белыми крышками;
CTRL (желтые крышки) - Контроли, содержащие синтетический человеческий эндотелии-1 (1-21) в человеческой плазме, лиофилизированный. Точные концентрации контролей после разбавления указаны на этикетках флаконов;
CONJ (янтарная крышка) - Ферментный конъюгат, содержащий антимышиные IgG, конъюгированные с пероксидазой хрена, готов к использованию;
SUB (синяя крышка) - Субстрат, содержащий раствор ТМБ, готов к использованию;
STOP (белая крышка) - Стоп-раствор, готов к использованию;
ET-SROCK (красная крышка) - Исходный раствор эндотелина (сток-раствор), содержащий синтетический человеческий эндотелии-1 (1-21), лиофилизированный. Концентрация после разбавления указана на этикетке флакона. Флакон с красной крышкой.
Исследование осуществляют согласно инструкции для иммуноферментного набора для количественного определения эндотелина (1-21) человека в сыворотке, плазме, моче, слюне, и супернатантах клеточных культур.
Проводят сбор образцов: венозную кровь забирают из локтевой вены у пациентов при поступлении и на 6-7 сутки лечения и свежесобранные образцы крови немедленно помещают на грелку со льдом после забора. Исследование, забранного материала, производят в условиях лаборатории, где их центрифугируют в течение дня при 1400g в течение 15 мин, при комнатной температуре (Центрифуга СМ-6М/МТ Elmi, ООО «Детстом-1». г. Москва). Если образцы не планируют анализировать в день взятия, хранят их при температуре -25°С, для длительного хранения при температуре -70°С в низкотемпературном холодильнике MDF-192 Ultralow temperature freezer (фирмы «Sanyo»). Повторные циклы заморозки не допускаются.
Подготавливают последовательные разведения растворенного ET-SROCK (Стокраствора эндотелина-1, флакон с красной крышкой) в культуральной среде до значения 0,625 фмоль/мл. Культуральную среду используют в качестве нулевого стандарта.
Разводят супернатант культуры клеток культуральной средой согласно концентрации 0,625 фмоль/мл.
Протокол анализа:
Перед началом анализа реагенты должны достичь комнатной температуры 18-26°С.
Промаркировывают положения стандартов, бланка, контролей и образцов на схеме анализа, поставляемой с набором.
Извлекают из пакета стрипы микропланшета и пометчают. Неиспользованные стрипы кладут обратно в пакет с осушителем, тщательно закрывают пакет и хранят его при t 2-8°С до истечения срока годности, указанного на этикетке.
Вносят по 50 мкл стандартов (белые крышки), образцов и контролей (желтые крышки) (STD/SAMPLE/CTRL) в соответствующие ячейки в дублях. Лунка для бланка остается пустой.
Добавляют по 200 мкл детектирующих антител (АВ, зеленая крышка флакона) в каждую ячейку, кроме бланка, тщательно перемешивают. Накрывают стрипы пленкой и инкубируют в течение ночи 16-24 часа при комнатной температуре 18-26°С. Убедившись, что ячейки тщательно запечатывают для предотвращения испарения. При исследовании удаляют пленку с стрипов, полностью удаляют содержимое ячеек и промывают их, 5 раз 300 мкл, разведенным буфером для промывок (WASHBUF). Удаляют остаток жидкости в ячейках после последней промывки переворачиванием стрипов на фильтровальную бумагу.
Добавляют по 200 мкл ферментного конъюгата (CONJ) во все ячейки, накрывают стрипы пленкой и инкубируйте 1 час при комнатной температуре 18-26°С. Удаляют пленку с стрипов. Полностью удаляют содержимое ячеек и промойте их, 5 раз по 300 мкл, разведенным буфером для промывок (WASHBUF). Удаляют остаток жидкости в ячейках после последней промывки переворачиванием стрипов на фильтровальную бумагу.
Вносят по 200 мкл субстрата (SUB) во все ячейки. Инкубируют 30 минут при комнатной температуре 18-26°С в темноте. Добавляют по 50 мкл стоп-раствора (STOP) во все ячейки, перемешивают содержимое ячеек. Немедленно считают оптическую плотность ячеек при 450 нм с длиной волны сравнения 630 нм.
Расчет результатов:
Вычитают значение оптической плотности (ОП) бланка из значений ОП остальных ячеек. Строят калибровочную кривую на основе результатов измерения стандартов, используя доступное программное обеспечение или графическую бумагу. Оценивают результаты, полученные данным методом с использованием алгоритма 4PL. При расчете результатов учитывают соответствующий коэффициент разведения.
Характеристика анализа:
Нормальные значения: Для панели образцов, взятых у 15 доноров крови, получили значение медианы 0,34 фмоль/мл. Диапазон стандартов: 0-10 фмоль/мл Объем и тип образца: 50 мкл человеческой сыворотки. Чувствительность (минимально определяемое значение): (0 фмоль/мл + 3 SD): 0,02 фмоль/мл. Время инкубации: В течение ночи / 1 час / 30 минут Перекрестная реактивность: ЕТ 1 (1-21): 100% ЕТ 2 (1-21): 100% ЕТ 3 (1-21):<1%.
Уровень эндотелина-1 в плазме крови человека в норме 0,1-1 фмоль/мл или не выявляется.(1Дремина Н.Н., 1,2Шурыгин М.Г., 1,2Шурыгина И.А. Эндотелины в норме и патологии. INTERNATIONAL JOURNAL OF APPLIED AND FUNDAMENTAL RESEARCH №10, 2016. C. 210-214). При невысоких концентрациях эндотелии аутокринно-паракринным способом действует на эндотелиальные клетки, высвобождая факторы релаксации, а повышение концентрации паракринным способом активирует рецепторы на гладкомышечных клетках и наблюдается сосудистый спазм (Vatter Н. Cerebrovascular characterization of clazosentan, the first nonpeptide endothelin receptor antagonist clinically effective for the treatment of cerebral vasospasm // J. N eurosurg. - 2005. - Vol. 102. - P. 1101-1107.).
При исследовании уровня эндотелина-1 выявлено прогрессивное достоверное его повышение до уровня 1.20 фмоль/мл и более (Фиг. 1), что указывает на развитие гнойного процесса.
Клиническое наблюдение №1. Пациентка В 32 лет госпитализирована в урологическое отделение ГБ 11 г. Барнаула с диагнозом острый пиелонефрит, в экстренном порядке с жалобами на выраженную боль в правом подреберье, повышение температуры тела до 41С, озноб, тошноту, дизурические явления, слабость, недомогание. Больна в течение 3 дней до госпитализации. При осмотре и пальпации выявлена резкая болезненность в правой подреберной области, положительный симптом поколачивания. По данным лабораторного обследования Hb 129 г/л, выраженный лейкоцитоз до 10*109, СОЭ 33 мм/час, уровень лейкоцитов в моче покрывает все поля зрения. По биохимическому анализу крови без отклонений от нормы. По УЗИ доплерографией: без структурных изменений. По данным обзорной и внутривенной рентгенографии замедление выделительной функции почек без признаков обструкции. Дополнительно был проведен иммуноферментный анализ для определения уровня эндотелина-1, при поступлении составлял 1.93 фмоль/мл, что указывает на повреждение эндотелия сосудов в следствие интенсивного воспалительного процесса. Больной сразу было назначено лечение: антибактериальная, противовоспалительная, дезинтоксикационная терапия. На 2 сутки было повторно проведено ультразвуковое исследование с допплерографией и выявлены гипоэхогенные очаги до 12 мм, утолщение коркового слоя до 28 мм с отеком паранефральной клетчатки. В связи с неэффективностью консервативной терапии было проведено оперативное лечение. На 7 сутки был произведен повторный забор крови для определения уровня эндотелина-1, он составил 2.05 фмоль/мл. Такой уровень эндотелина-1 указывает на повреждение эндотелия, но усилившееся в следствие проведенной операции.
Данное клиническое наблюдение показывает, что при поступлении известными методами диагностировать гнойный пиелонефрит не удалось, в то время как уровень эндотелина-1 уже был повышен, что позволило прогнозировать развитие гнойного процесса.
Клиническое наблюдение №2.
Больная А., 23 лет, поступила в урологическое отделение ГБ 11 г. Барнаула в экстренном порядке по направлению терапевта из поликлиники по месту жительства с диагнозом острый пиелонефрит. Пациентка предъявляла жалобы болезненность в правом подреберье, повышение температуры тела до 38.2С, озноб, слабость, недомогание. Больна первые сутки до госпитализации.
При осмотре и пальпации выявлена умеренная болезненность в правой подреберной области, положительный симптом поколачивания справа. По данным лабораторного обследования Hb 132 г/л, L до 10*109, СОЭ 29 мм/час, большое лейкоцитов в моче. По УЗИ доплерографией структурных изменений не выявлено. По данным обзорной и внутривенной рентгенографии без патологии. При лабораторном исследовании с помощью иммуноферментного анализа уровень эндотелина-1 при поступлении 0.62 фмоль/мл (Фиг. 2), что не превышает границы нормы и можно предположить отсутствие воздействия на эндотелий. При заборе крови на 4-е сутки уровень эндотелина-1 понизился до 0.49 фмоль/мл, что говорит о отсутствии риска повреждения сосудов и развития гнойного процесса. Больная была выписана на 10-е сутки с выздоровлением.
Данное клиническое наблюдение показывает, что в данном случае отсутствует риск развития гнойного пиелонефрита.
Заявляемым способом было спрогнозировано развитие гнойного пиелонефрита у 50 пациентов.
Заявляемый способ прогнозирования развития гнойного пиелонефрита позволяет выявить на раннем этапе риск развития гнойного процесса и своевременно предотвратить его развитие путем консервативной терапии; обладает высокой информативностью, высокой точностью за счет начала патогенетического процесса с нарушения кровотока и повреждения эндотелия сосудов. Заявляемый способ является неинвазивным методом, который найдет широкое применение в урологической практике.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ прогнозирования кардиоваскулярных осложнений в течение 12 месяцев после плановой эндоваскулярной реваскуляризации миокарда у больных ишемической болезнью сердца | 2020 |
|
RU2749485C1 |
| СПОСОБ РАННЕЙ ДИАГНОСТИКИ РАЗЛИЧНЫХ ФОРМ ЭССЕНЦИАЛЬНОЙ АРТЕРИАЛЬНОЙ ГИПЕРТЕНЗИИ У ДЕТЕЙ И ПОДРОСТКОВ | 2016 |
|
RU2648453C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭФФЕКТИВНОСТИ ТЕРАПИИ ПРЕЭКЛАМПСИИ | 2011 |
|
RU2475753C1 |
| СПОСОБ РАННЕЙ ДИАГНОСТИКИ ДИАБЕТИЧЕСКОЙ НЕЙРОПАТИИ У ДЕТЕЙ | 2005 |
|
RU2286578C2 |
| СПОСОБ ДИАГНОСТИКИ ГЕСТОЗА ТЯЖЕЛОЙ СТЕПЕНИ | 2011 |
|
RU2476880C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ПАТОЛОГИИ ЦНС У НОВОРОЖДЕННЫХ | 2007 |
|
RU2317014C1 |
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ХРОНИЧЕСКОГО ВИРУСНОГО ГЕПАТИТА И ЦИРРОЗА ПЕЧЕНИ | 2008 |
|
RU2383021C1 |
| СПОСОБ ПРОГНОЗА ИСХОДА СКВОЗНОЙ КЕРАТОПЛАСТИКИ | 2011 |
|
RU2444733C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ИСХОДА ДАКРИОЦИСТОРИНОСТОМИИ | 2006 |
|
RU2310858C1 |
| ПРИМЕНЕНИЕ КОМПЛЕКСА АНТИОКСИДАНТНЫХ ВИТАМИНОВ И АМИНОКИСЛОТ В КАЧЕСТВЕ ДОПОЛНЕНИЯ К СТАНДАРТНЫМ МЕТОДАМ ТЕРАПИИ И СПОСОБ ЛЕЧЕНИЯ ПАПИЛЛОМАВИРУС-АССОЦИИРОВАННЫХ ПРЕДРАКОВЫХ ЗАБОЛЕВАНИЙ ШЕЙКИ МАТКИ И ПРОФИЛАКТИКИ КАНЦЕРОГЕНЕЗА ПРИ ПАПИЛЛОМАВИРУСНОЙ ИНФЕКЦИИ | 2013 |
|
RU2537233C2 |
Изобретение относится к медицине, а именно к урологии и гематологии, и может быть использовано для прогнозирования гнойного пиелонефрита путем исследования венозной крови. Забор крови для исследования осуществляют при поступлении пациента в стационар. Свежесобранные образцы крови немедленно помещают на грелку со льдом, центрифугируют в течение дня при 1400g в течение 15 мин при комнатной температуре, отбирают для исследования супернатант. Подготавливают последовательные разведения растворенного ET-SROCK в культуральной среде до значения 0,625 фмоль/мл, используя как нулевой стандарт. Проводят исследование с помощью иммуноферментного набора для количественного определения эндотелина 1-21 человека в сыворотке, плазме, моче, слюне, и супернатантных клеточных культурах. Вносят по 50 мкл стандартов, образцов и контролей STD/SAMPLE/CTRL в соответствующие ячейки в дублях, лунка для бланка остается пустой. Добавляют по 200 мкл детектирующих антител АВ в каждую ячейку, кроме бланка, перемешивают. Накрывают стрипы пленкой и инкубируют в течение ночи 16-24 часа при комнатной температуре 18-26°С. При исследовании удаляют пленку со стрипов, полностью удаляют содержимое ячеек и промывают их 5 раз по 300 мкл разведенным буфером для промывок WASHBUF. Удаляют остаток жидкости в ячейках после последней промывки переворачиванием стрипов на фильтровальную бумагу. Добавляют по 200 мкл ферментного конъюгата CONJ во все ячейки, накрывают стрипы пленкой и инкубируют 1 час при комнатной температуре 18-26°С. Удаляют пленку со стрипов, полностью удаляют содержимое ячеек и промывают их 5 раз по 300 мкл разведенным буфером для промывок WASHBUF, удаляют остаток жидкости в ячейках после последней промывки, переворачивают стрипы на фильтровальную бумагу. Вносят по 200 мкл субстрата SUB во все ячейки, инкубируют 30 минут при комнатной температуре 18-26°С в темноте. Добавляют по 50 мкл стоп-раствора STOP во все ячейки, перемешивают содержимое ячеек. Немедленно считают оптическую плотность ячеек при 450 нм с длиной волны сравнения 630 нм. Вычитают значение оптической плотности - ОП бланка из значений ОП остальных ячеек, строят калибровочную кривую, оценивают результаты, полученные данным методом с использованием алгоритма 4PL. Определяют уровень эндотелина-1, и при значении 1.20 фмоль/мл и более прогнозируют развитие гнойного пиелонефрита. Способ обеспечивает прогнозирование развития гнойного пиелонефрита, позволяющее определить переход серозной стадии пиелонефрита в гнойную, за счет оценки состояния и изменения со стороны почечных сосудов, а именно повреждение эндотелия сосудов на фоне прогрессирования воспалительного процесса. 2 ил., 2 пр.
Способ прогнозирования гнойного пиелонефрита путем исследования венозной крови, отличающийся тем, что забор крови для исследования осуществляют при поступлении пациента в стационар, свежесобранные образцы крови немедленно помещают на грелку со льдом, центрифугируют в течение дня при 1400g в течение 15 мин при комнатной температуре, отбирают для исследования супернатант, подготавливают последовательные разведения растворенного ET-SROCK в культуральной среде до значения 0,625 фмоль/мл, используя как нулевой стандарт, и проводят исследование с помощью «иммуноферментного набора для количественного определения эндотелина 1-21 человека в сыворотке, плазме, моче, слюне и супернатантных клеточных культурах», заключающееся во внесении по 50 мкл стандартов, образцов и контролей STD/SAMPLE/CTRL в соответствующие ячейки в дублях, лунка для бланка остается пустой; добавляют по 200 мкл детектирующих антител АВ в каждую ячейку, кроме бланка, перемешивают; накрывают стрипы пленкой и инкубируют в течение ночи 16-24 часа при комнатной температуре 18-26°С; при исследовании удаляют пленку со стрипов, полностью удаляют содержимое ячеек и промывают их 5 раз по 300 мкл разведенным буфером для промывок WASHBUF, удаляют остаток жидкости в ячейках после последней промывки переворачиванием стрипов на фильтровальную бумагу; добавляют по 200 мкл ферментного конъюгата CONJ во все ячейки, накрывают стрипы пленкой и инкубируют 1 час при комнатной температуре 18-26°С, удаляют пленку со стрипов, полностью удаляют содержимое ячеек и промывают их 5 раз по 300 мкл разведенным буфером для промывок WASHBUF, удаляют остаток жидкости в ячейках после последней промывки, переворачивают стрипы на фильтровальную бумагу; вносят по 200 мкл субстрата SUB во все ячейки, инкубируют 30 минут при комнатной температуре 18-26°С в темноте; добавляют по 50 мкл стоп-раствора STOP во все ячейки, перемешивают содержимое ячеек, немедленно считают оптическую плотность ячеек при 450 нм с длиной волны сравнения 630 нм, вычитают значение оптической плотности - ОП бланка из значений ОП остальных ячеек, строят калибровочную кривую, оценивают результаты, полученные данным методом с использованием алгоритма 4PL, определяют уровень эндотелина-1 и при значении 1.20 фмоль/мл и более прогнозируют развитие гнойного пиелонефрита.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| R&D Systems Inc | |||
| Способ получения цианистых соединений | 1924 |
|
SU2018A1 |
| СПОСОБ ДИАГНОСТИКИ РАЗЛИЧНЫХ ФОРМ ОСТРОГО ПИЕЛОНЕФРИТА | 2011 |
|
RU2478968C2 |
| СПОСОБ ДИАГНОСТИКИ ОСТРОГО ПИЕЛОНЕФРИТА | 2003 |
|
RU2263918C2 |
| СПОСОБ ДИАГНОСТИКИ СТАДИИ ОСТРОГО ПИЕЛОНЕФРИТА У ДЕТЕЙ | 2003 |
|
RU2236176C1 |
| Гидравлический способ добычи торфа | 1945 |
|
SU68846A1 |
| WO 2011163085 A2, 29.12.2011 | |||
| ДРЕМИНА Н.Н | |||
| и др | |||
| Эндотелины в норме и патологии | |||
| Международный журнал прикладных и фундаментальных исследований | |||
Авторы
Даты
2020-02-25—Публикация
2018-11-27—Подача