Область техники
Изобретение относится к медицине и фармакологии, а именно к биологически-активным веществам пептидной природы, применяемым в качестве средства для лечения депрессии, большого депрессивного расстройства, нейропатической боли, и обладающим нейропротекторной активностью.
Уровень техники
Депрессия является сложным в лечении психическим расстройством: до 30% лиц, страдающий этим расстройством, не удается излечить с помощью известных препаратов.
Для лечения депрессии было разработано множество препаратов: среди них ингибиторы обратного захвата серотонина (сертралин, флуоксетин), ингибиторы обратного захвата норадреналина (ребоксетин), ингибиторы МАО (моклобемид). Следует отметить, что рассмотренные препараты не лишены недостатков: антидепрессантный эффект наступает через продолжительное время, существенная часть пациентов не реагирует на терапию, при приеме ингибиторов МАО необходимо соблюдать специальную диету. Таким образом, существует потребность в альтернативном эффективном и безопасном лечении депрессии.
НМДА-рецептор (N-метил-D-аспартат, НМДА) представляет собой постсинаптический ионотропный рецептор, который активируется за счет действия возбуждающих аминокислот глутамата и глицина, селективно активация происходит от действия синтетического соединения НМДА. НМДА-рецептор локализован постсинаптически и способен пропускать как двухвалентные, так и одновалентные катионы через канал, ассоциированный с рецептором (Foster et al., Nature 1987, 329: 395-396; Mayer et al., Trends in Pharmacol. Sci. 1990 11: 254-260). Считается, что НМДА-рецепторы участвуют в процессах долговременной потенциации и вовлечен в развитие расстройств центральной нервной системы. НМДА-рецептор играет главную роль в синаптической пластичности, которая лежит в основе многих высших когнитивных функций, таких как формирование памяти и обучение, а также в некоторых когнитивных путях и чувствительности к боли (Collingridge et al., The НМДА Receptor, Oxford University Press, 1994). Кроме того, некоторые свойства НМДА-рецепторов позволяют предположить, что они могут участвовать в обработке информации в мозге, которая лежит в основе самосознания. Данный рецептор представляет особый интерес, поскольку, по-видимому, он вовлечен в широкий спектр расстройств ЦНС. Например, во время ишемии головного мозга, вызванной инсультом или травматическим повреждением, чрезмерное количество возбуждающей аминокислоты глутамата высвобождается из поврежденных или лишенных кислорода нейронов. Избыток глутамата связывается с НМДА-рецепторами открывая их ионные каналы; в свою очередь, поток кальция в клетку увеличивает уровень внутриклеточного кальция, который активирует биохимический каскад, приводящий к гибели клеток. Было показано, что активация НМДА-рецептора ответственна за судороги после инсульта, и в некоторых моделях эпилепсии было показано, что активация НМДА-рецептора приводит к судорогам. Факт вовлеченности НМДА-рецептора в развитие нейропсихиатрических нарушений следующим образом: блокирование ионного канала НМДА-рецептора анестетиком фенциклидином вызывает у человека психотическое состояние, сходное с шизофренией (Johnson, K. and Jones, S., 1990). Некоторые блокаторы НМДА-рецептора (кетамин) обладают высоким антидепрессантным эффектом, который характеризуется высокой скоростью наступления клинического эффекта и низкой дозой препарата, необходимой для проявления данного эффекта, но недостаточной для проявления психотомиметических симптомов. Считается, что НМДА-рецептор состоит из четырех белковых цепей, встроенных в постсинаптическую мембрану. Открытие и закрытие канала регулируется связыванием различных лигандов с доменами (аллостерическими сайтами) белка, находящимися на внеклеточной поверхности. Считается, что связывание лигандов влияет на конформационные изменения в общей структуре белка, которые в конечном итоге на характер ионных токов через рецептор. Кинетика ингибирования НМДА-рецептора может быть очень важна для проявления тех или иных физиологических эффектов за счет разного режима работы нейронов. Соединения, которые не снижают ионный ток до нуля за счет связывания в ионной поре (фенциклидин, МК-801), а уменьшают вероятность открытия канала при связывании агонистов имеют хорошие шансы проявлять быстро наступающий антидепрессантный эффект в отсутствии психотомиметических симптомов. Таким образом, соединения, проявляющие антагонистический эффект по отношению к НМДА-рецептору, могут быть применены в клинической практике для терапии таких болезней как большое депрессивное расстройство. Следует отметить, что один из энантиомеров неселективного блокатора НМДА-рецептора кетамина S-кетамин одобрен FDA в 2019 для лечения клинической депрессии в США, а тетрапептид рапастинел, являющийся частичным агонистом НМДА-рецептора, получил отметку прорывного кандидата в лекарства для лечения клинической депрессии в США. Дополнительным плюсом лекарств на основе коротких пептидов является, как правило, хорошая переносимость (Velden WJ, et al., Safety and tolerability of the antimicrobial peptide human lactoferrin 1-11 (hLF1-11), BMC Med. 2009 Sep 8;7:44), высокое проникновение через гематоэнцефалический барьер (проницаемость рапастинела через гематоэнцефалический барьер лучше, чем у героина, по-видимому, за счет активного транспорта (Moskal JR, et al., GLYX-13: a monoclonal antibody-derived peptide that acts as an N-methyl-D-aspartate receptor modulator. Neuropharmacology. 2005 Dec;49(7):1077-87)).
Несмотря на многочисленные исследования в области антагонистов НМДА-рецептора, проблема создания безопасного и эффективного средства для лечения депрессионных расстройств и других заболеваний ЦНС до сих пор является актуальной. Заявляемое изобретение направлено на получение нового биологически активного соединения пептидной природы, подавляющего функциональную активность НМДА-рецептора.
Сущность изобретения
Задачей настоящего изобретения является создание безопасного и эффективного средства для лечения депрессионных расстройств. Для обеспечения безопасного профиля и хорошей проницаемости в ЦНС был проведен поиск соединений, состоящих из коротких пептидов, которые являются структурно схожими с известными химическими ингибиторами НМДА-рецепторов. Указанная задача решается путем создания пептида, состоящего из двух аминокислотных остатков (дипептида), D-Phe-L-Tyr, способного подавлять активность НМДА-рецепторов.
Указанная задача также решается путем создания фармацевтической композиции для лечения или профилактики заболеваний, опосредованных избыточной активностью НМДА-рецепторов, включающей эффективное количество указанного дипептида, а также фармацевтически приемлемый носитель.
Указанная задача также решается путем применения пептида D-Phe-L-Tyr для получения лекарственного средства для лечения или профилактики заболеваний, опосредованных избыточной активностью НМДА-рецепторов.
В некоторых вариантах изобретения заболеваниями, опосредованными избыточной активностью НМДА-рецепторов, являются депрессия, нейропатическая боль, большое депрессивное расстройство, судорожные расстройства, нейродегенеративные заболевания.
Техническим результатом настоящего изобретения является создание нового, физиологически активного дипептида, способного подавлять активность НМДА-рецепторов.
Краткое описание рисунков
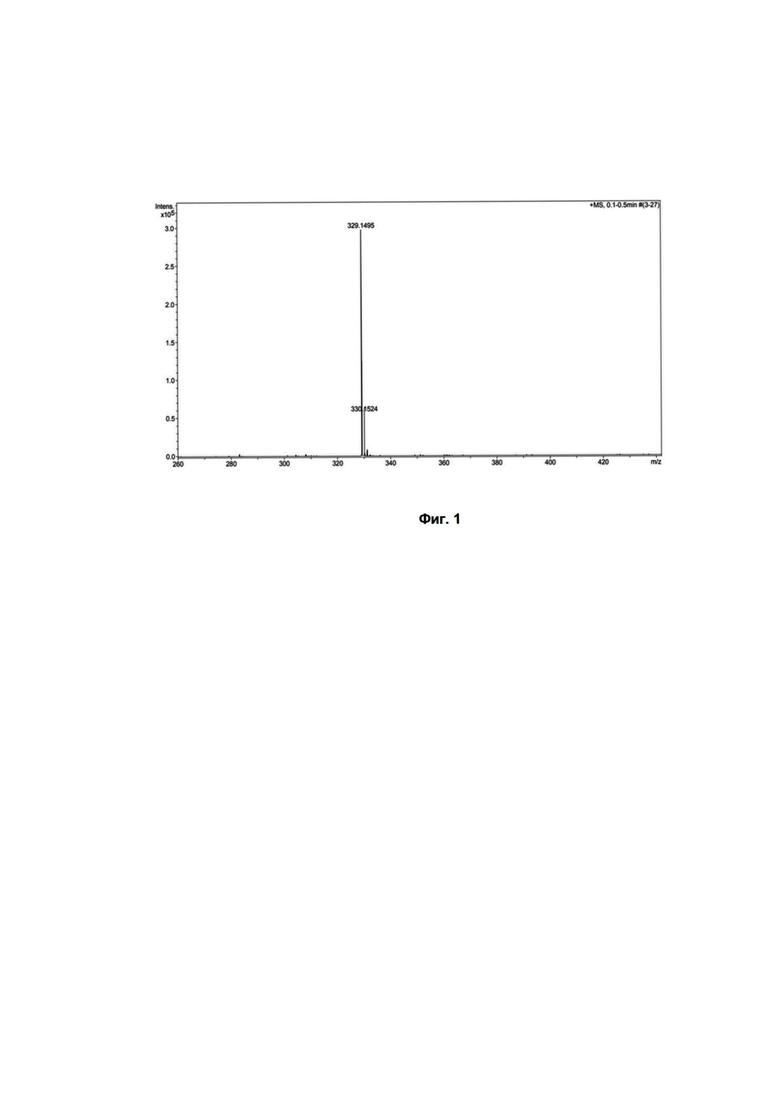
Фиг. 1 - Фиг. 1 Масс-спектр пептида D-Phe-L-Tyr, полученного методом ESI-TOF
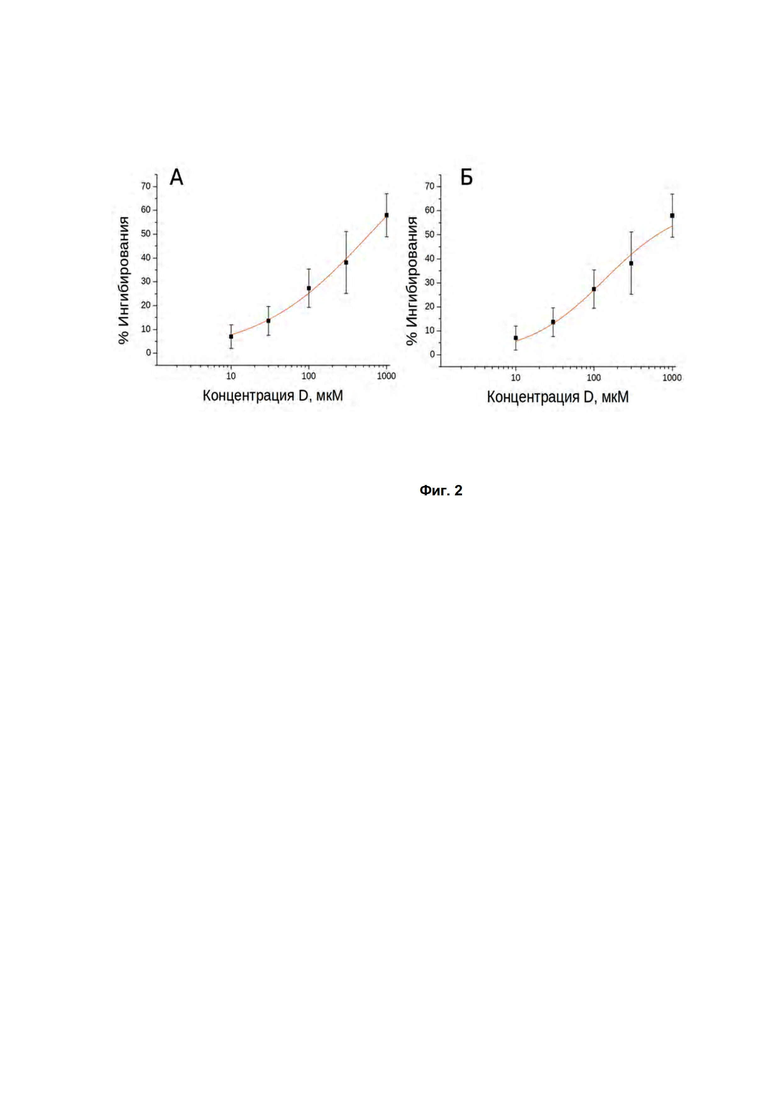
Фиг. 2 - Аппроксимация кривой "доза-эффект" рецепторов в нейронах гиппокампа для дипептида D-Phe-L-Tyr с максимальным эффектом равным 100% (A) или 62% - (Б). D - дипептид D-Phe-L-Tyr.
Подробное раскрытие изобретения
В описании данного изобретения термины «включает» и «включающий» интерпретируются как означающие «включает, помимо всего прочего». Указанные термины не предназначены для того, чтобы их истолковывали как «состоит только из». Если не определено отдельно, технические и научные термины в данной заявке имеют стандартные значения, общепринятые в научной и технической литературе.
Термины «лечение», «терапия» охватывают лечение патологических состояний у млекопитающих, предпочтительно у человека, и включают: а) блокирование (приостановку) течения заболевания, б) облегчение тяжести заболевания, т.е. индукцию регрессии заболевания.
Термин «профилактика», «предотвращение», «превентивная терапия» охватывает устранение факторов риска, а также профилактическое лечение субклинических стадий заболевания у млекопитающих, предпочтительно у человека, направленное на уменьшение вероятности возникновения клинических стадий заболевания. Пациенты для профилактической терапии отбираются на основе факторов, которые, на основании известных данных, влекут увеличение риска возникновения клинических стадий заболевания по сравнению с общим населением. К профилактической терапии относится а) первичная профилактика и б) вторичная профилактика. Первичная профилактика определяется как профилактическое лечение у пациентов, клиническая стадия заболевания у которых еще не наступила. Вторичная профилактика - это предотвращение повторного наступления того же или близкого клинического состояния заболевания.
Под «терапевтически эффективным количеством» подразумевается количество лекарственного препарата (фармацевтической композиции), вводимого или доставляемого пациенту, при котором у пациента с наибольшей вероятностью проявится желаемая реакция на лечение (профилактику). Точное требуемое количество может меняться от субъекта к субъекту в зависимости от возраста, массы тела и общего состояния пациента, тяжести заболевания, методики введения препарата, комбинированного лечения с другими препаратами и т.п. При применении в комбинированной терапии термин «эффективное количество» относится к комбинации количеств активных ингредиентов, прием которых ведет к превентивному или терапевтическому эффекту при последовательном или одновременном приеме.
После смешения пептида по настоящему изобретению с конкретным подходящим фармацевтически допустимым носителем в желаемой дозировке, композиции, составляющие суть изобретения, могут быть введены в организм человека или других животных перорально, интраназально, местно (с помощью кожных пластырей, порошков, мазей или капель), сублингвально, буккально, через слизистые оболочки, в виде спрея для рта или носа и т.п.
Эффективная дозировка соединения, вводимая разово или в виде нескольких отдельных доз, как правило, лежит в диапазоне от 0.5 до 50 мг соединения на кг массы тела пациента. Обычно соединение вводится пациенту, нуждающемуся в таком лечении, в дневной дозировке ориентировочно от 50 до 1000 мг на пациента. Введение может осуществляться как разово, так и несколько раз в день, неделю (или любой другой временной интервал), или время от времени. Например, соединение может быть введено в организм пациента один или несколько раз в день на недельной основе (например, каждый понедельник) в течение неопределенного времени или в течение нескольких недель (например, 4-10 недель).
Кроме того, изобретение предусматривает фармацевтические композиции для предупреждения и/или лечения расстройств, связанных с повышенной активностью НМДА-рецепторов, и характеризующиеся тем, что они содержат терапевтически эффективное количество соединения по изобретению и, по меньшей мере, одно вспомогательное вещество. В некоторых вариантах воплощениях изобретения вспомогательное вещество представляет собой фармацевтически приемлемый носитель и/или эксципиент.
Термин «фармацевтически приемлемый носитель и/или эксципиент» относится к таким носителям и/или эксципиентам, которые, являясь неактивными ингредиентами, в рамках проведенного медицинского заключения, пригодны для использования в контакте с тканями человека и животных без излишней токсичности, раздражения, аллергической реакции и т.д. и отвечают разумному соотношению пользы и риска. «Неактивные ингредиенты» входят в состав лекарственного средства для улучшения его фармакологических характеристик и/или стабильности, для улучшения фармакокинетики и более эффективной доставки к специфическим органам или тканям. Неактивные ингредиенты включают в себя множество веществ, известных специалистам в области фармацевтики, таких как вещества для контроля pH или осмотического давления, антибактериальные агенты, антиоксиданты, поверхностно активные вещества (например, полисорбат 20 или 80), криостабилизаторы, консерванты, растворители, загустители, наполнители, носители (микро- или нано-частицы) и другие вещества.
В различных вариантах изобретения заболеваниями, опосредованными или вызванными избыточной активностью НМДА-рецепторов, являются депрессия, нейропатическая боль, большое депрессивное расстройство, судорожные расстройства, нейродегенеративные заболевания и другие. В различных вариантах данного изобретения лекарственный препарат по изобретению может вводиться пациентам в сочетании с другими препаратами в различных режимах терапии, а также в сочетании с другими приемами терапии.
Структурно НМДА-рецептор представляет собой мультимерный ионотропный глутаматный рецепторы, состоящий из четырех субъединиц (гетеротетрамер двух субъединиц- NR1 и NR2). Самый распространенный у человека НМДА-рецептор состоит из двух субъединиц GluN1 и по одной GluN2A и GluN2B.
Авторами было проведено компьютерное моделирование пептидов небольшого размера, структурно мимикрирующих известные ингибиторы НМДА-рецептора в части связывания с рецептором. Заявляемый дипептид был обнаружен и отобран вследствие его сходства с ифенпродилом и потенциального взаимодействия с сайтом связывания ифенпродила, расположенного на НМДА-рецепторе. Ифенпродил является ингибитором рецептора НМДА, в частности, субъединиц GluN1 (глутамат-связывающего рецептора НМДА 1) и GluN2B (глутамат-связывающей субъединицы рецептора НМДА 2). Для ифенпродила известна активность для всех четырех типов НМДА-рецепторов: для GluN2B IC50 составляет примерно 0.1-0.5 мкМ, на все остальные IC50 около 100 мкМ.
Фармацевтическая композиция согласно изобретению приготавливается с помощью общепринятых в данной области техники приемов и включает фармакологически эффективное количество активного агента, пептида D-Phe-L-Tyr или его фармацевтически приемлемую соль (называемые далее "активное соединение"), составляющее обычно от 0.5 до 10 вес.%, в сочетании с одной или более фармацевтически приемлемыми вспомогательными агентами, такими как носители, разбавители, антиоксиданты, консерванты. Неограниченными примерами фармацевтически приемлемых солей для активного агента согласно изобретению являются хлорид, бромид, тартрат, сукцинат и др.
В соответствии с известными методами фармацевтические композиции могут быть представлены различными жидкими или твердыми формами.
Примеры жидких лекарственных форм для инъекций и парентерального введения включают растворы, эмульсии, суспензии и др.
Композиции, как правило, получают с помощью стандартных процедур, предусматривающих смешение активного соединения с жидким носителем.
Композиции согласно изобретению в форме инъекций или капель в нос содержат от 0.5 до 10% активного соединения и носитель. Инъекционные формы композиции предпочтительно представляют собой изотонические растворы или суспензии. Вышеуказанные формы могут стерилизоваться и содержать добавки, такие как консерванты: натрия метабисульфит, бензойная кислота, натрия бензоат, смесь метилпарабена и пропилпарабена, бензалкония хлорид; стабилизаторы: абрикосовая и аравийская камедь, декстрин, крахмальный клейстер, метилцеллюлоза, твин; соли, регулирующие осмотическое давление (хлорид натрия), или буферы. Кроме того, они могут содержать другие терапевтически полезные вещества.
Для лечения заболеваний, связанных с гиперактивацией НМДА-рецепторов, назначаемая для приема доза активного компонента (пептида D-Phe-L-Tyr) варьирует в зависимости от многих факторов, таких как возраст, пол, вес пациента, симптомы и тяжесть заболевания, конкретно назначаемое соединение, способ приема, форма препарата, в виде которой назначается активное соединение.
Обычно, общая назначаемая доза составляет от 50 до 1000 мг в день. Общая доза может быть разделена на несколько доз, например, для приема от 1 до 4 раз в день. При парентеральном приеме интервал назначаемых доз составляет от 50 до 1000 мг в день, предпочтительно, от 50 до 200 мг; при внутривенных инъекциях - от 50 до 1000 мг в день, предпочтительно, от 50 до 200 мг. Точная доза может быть выбрана лечащим врачом.
Нижеследующие примеры осуществления способа приведены в целях раскрытия характеристик настоящего изобретения и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения.
Пример 1. Синтез дипептида D-Phe-L-Tyr
Синтез дипептида D-Phe-L-Tyr проводили классическим твердофазным методом с использованием Boc/Bzl-методологии и схемы неполного блокирования боковых функций аминокислот. В синтезе применяли сополимер стирола с 1%-дивинилбензола, модифицированный п-метилбензгидриламинной якорной группой (MBHA-resin), к которому первоначально присоединяли производное D-фенилаланина Boc-D-Phe-OH. После завершения синтеза, пептид отделили от полимерной подложки безводным HF с добавкой 10% по объему м-крезола. Пептиды очищали с помощью препаративной ВЭЖХ на колонке Phenomenex Synergy Hydro-RP RP (50 x 250мм). Идентичность полученных препаратов оценивали масс-спектрометрически и методом ЯМР H1. Строение пептида подтверждается масс-спектроскопическим анализом молекулярного пика пептида D-Phe-L-Tyr (Фиг. 1). В результате масс-спектроскопического анализа найдены: исходный пептид - пик 329,1495 Da, соответствующий брутто-формуле C18H21N2O4+. Спектр ЯМР H1: (ДМСО-d6 δ, м.д.): 2.72 м. (2Н); 2.94 м. (2Н); 4.47 с. (1Н); 6.67 м. (2H); 7.02 м. (4Н), 7.27 м. (3Н); 8.06 уш. с. (3Н); 8.84 д. (1Н); 9.49 уш. с. (1Н); 13.0 уш. с. (1H).
Пример 2. Экспериментальное свидетельство ингибирующего эффекта пептида D-Phe-L-Tyr на НМДА/глицин индуцированные токи в нейронах гиппокампа
Эксперименты проводились на нативных рецепторах нейронов, выделенных из переживающих срезов мозга крыс линии Вистар с помощью метода вибродиссоциации (Vorobjev V.S. Neurosci Meth., 1991, 68, 303-307). Исследование действия соединений на НМДА-рецепторы и кальций-непроницаемые АМПА-рецепторы проводилось на пирамидных нейронах гиппокампа, по действию на кальций-проницаемые АМПА рецепторы - на гигантских холинэргических интернейронах стриатума. Активация НМДА рецепторов осуществлялась НМДА (100 мкМ) в присутствии глицина (10 мкМ); активация АМПА рецепторов - каинатом (100 мкМ). Для регистрации токов применялся метод фиксации потенциала в конфигурации «whole cell». Внеклеточный раствор содержал (в мМ): NaCl 143; KCl 5; CaCl2 2.5; D-glucose 10; HEPES 10 (pH доводился до 7.4 при помощи добавления HCl). Пипеточный раствор содержал (в мМ): CsF 100; CsCl 40; NaCl 5; CaCl2 0.5; EGTA 5; HEPES 10 (pH доводился до 7.2 при помощи CsOH). Микропипетки изготавливались из боросиликатного стекла при помощи пуллера P-97 (Sutter Instruments, USA). Исследуемые вещества подавались при помощи перфузирующей системы RSC-200 (BioLogic Science Instruments, France), обеспечивающей смену раствора за не более чем 50 мс. Для записи ответов использовался усилитель EPC 8 (HEKA Elektronik, Germany). Управление экспериментом и запись ответов осуществлялись при помощи персонального компьютера. Исследуемые соединения растворялись в DMSO для приготовления стоковых растворов. Экспериментальные растворы исследуемых веществ приготовлялись путем добавления необходимого количества стокового раствора во внеклеточный раствор, содержащий также агонисты НМДА и глицин. Блокирующее действие исследуемых соединений определялось по их способности ингибировать поддерживающийся при аппликации агониста трансмембранный ток. Действие разных концентраций блокаторов использовалось для построения концентрационных зависимостей и определения величины ИК50 при помощи уравнения Хилла.
Аппроксимация со свободным значением максимального эффекта (Фиг. 2А) дала следующие значения: ИК50 = 600±600 мкМ, коэффициент Хилла = 0.6±0.3, а максимальный эффект - 100±30%. При фиксации максимального эффекта на уровне 62% (Фиг. 2Б), соответствующем уровню полного ингибирования NR2B-содержащих рецепторов ифенпродилом, ИК50 составила 130 ± 30 мкМ, а коэффициент Хилла 0.9 ± 0.2. Следует отметить, что эффективность снижения ионных токов через НМДА рецептор в концентрациях 50 - 100 мкМ для пептида D-Phe-L-Tyr примерно равна 15-20%, что примерно соответствует эффективности снижения ионных токов под действием рапастинела - 12.5 ± 2.4% (100 мкМ рапастинеля, 10 мкМ глицина, 100 мкМ глутамата) (Velden WJ, et al., Safety and tolerability of the antimicrobial peptide human lactoferrin 1-11 (hLF1-11), BMC Med. 2009 Sep 8;7:44).
Пример 3. Сравнение функциональной активности изомеров L-Phe-L-Tyr и D-Phe-L-Tyr
Изомер D-Phe-L-Tyr был выбран на основе компьютерного моделирования и показал свою эффективность при ингибировании НМДА-рецепторов. Дополнительно, авторами было проведено сравнение эффективности ингибирования НМДА-рецепторов для изомеров L-Phe-L-Tyr и D-Phe-L-Tyr. Было показано, что изомер L-Phe-L-Tyr оказался менее эффективен по влиянию на связывание радиоактивно-меченого ифенпродила к НМДА-рецептору. Проведенные радиолигандные исследования по замещению радиоактивно-меченого [3H]-ифенпродила для L-Phe-L-Tyr и D-Phe-L-Tyr продемонстрировали, что в концентрациях 100 мкМ и при насыщающих концентрациях ифенпродила (10 мкМ) L-Phe-L-Tyr не изменяет связывание радиоактивно-меченого ифенпродила (в пределах погрешности +/- 5%), а D-Phe-L-Tyr повышает на 15-20%. Исходя из этих данных, можно предположить отсутствие активности или очень низкую активность для изомера L-Phe-L-Tyr, а также то, что ингибирование НМДА/глицин-индуцированных токов дипептидом D-Phe-L-Tyr обусловлено действием на GluN2A субъединицу, как на наиболее представленный тип НМДА рецептора в ЦНС (GluN1/GluN2A/GluN2B).
При этом ифенпродил связывается, в основном, с GluN2B субъединицей, а GluN2A обладает очень похожим на GluN2B сайтом связывания фенилэтиламинов, но тем не менее с существенно более низким сродством к ифенпродилу. Влияние исследуемых веществ на радиолигандное связывание с НМДА рецепторами изучали с помощью модифицированного метода, описанного в Zhou L.M. et al.,1997). Использовали радиоактивный лиганд [3H]-ифенпродил с удельной активностью 79 Ки/моль, связывающийся с NMDA рецепторами, содержащими NR2B субъединицы. Мембранный препарат для радиолигандного анализа готовили по описанному методу (Novak G., et al., 1993). Ткань гиппокампа измельчали в гомогенизаторе Поттера («тефлон-стекло») в буфере № 1 (5 мМ HEPES/4.5 мМ Трис буфера, рН 7.6), содержащего 0.32 М сахарозы, в соотношении 1 г ткани: 10 мл буфера. Гомогенат разбавляли буфером для исследования № 2 (5 мМ HEPES/4.5 мМ Трис буфера, рН 7.6) в соотношении 1 : 50и центрифугировали 10 мин при 1000g. Затем отбирали супернатант и вновь центрифугировали 20 мин при 25 000g. Осадок гомогенизировали в буфере № 2 в соотношении 1 : 50 и центрифугировали 20 мин при 8000 g. Супернатант и его мягкий, зыбкий надосадочный слой отбирали и центрифугировали 20 мин при 25000g. Полученный осадок суспендировали в буфере № 3 (5 мМ HEPES/4.5 мМ Трис буфера (рН=7.61), 5 мМ Na4EDTA), содержащем, и суспензию вновь центрифугировали. Такая процедура отмывки проводится четыре раза, причем при последней отмывке Na4EDTA исключается из состава. Конечный осадок ресуспендировали в буфере № 2 в соотношении 1:5 и хранили в жидком азоте. Реакционная смесь (конечный объем 0.5 мл) содержит 200 мкл буфера № 2, 50 мкл 50 нМ р-ра меченого лиганда и 250 мкл белковой суспензии. Неспецифическое связывание определяется в присутствии 50 мкл немеченого лиганда. Реакционная смесь инкубируется при комнатной температуре в течение 2 ч. По окончании инкубации пробы фильтруются через стекловолокнистые фильтры GF/B (Whatman), предварительно смоченные в 0.3% полиэтиленамине в течение 2 часов при 4 о С. Каждая пробирка промывается один раз холодным буфером № 2, затем фильтры промываются три раза тем же объемом буфера. Фильтры сушатся на воздухе до полного высыхания и переносятся в сцинтилляционные флаконы, в которые добавляется по 5 мл сцинтилляционной жидкости, содержащей 4 г дифенилоксазола (РРО), 0.2 г дифенилоксазоилбензола (РОРОР) и 1 л толуола. Радиоактивность определяли на сцинтилляционном счетчике TriCarb2800 TR (PerkinElmer, Packard, США) с эффективностью счета около 65%. Исследование влияния изучаемых соединений на связывание [3H]-ифенпродила мембранами гиппокампа крысы проводили при добавлении в инкубационную среду 50 мкл исследуемых соединений в диапазоне концентраций 10-8 - 10-3 М. По результатам ингибирования рассчитывали IC50 для изученных соединений с помощью программы GraphPadPrism_4_Demo.
Пример 4. Раствор для инъекций, содержащий эффективное количество дипептида D-Phe-L-Tyr
Раствор для инъекций (1000 г):
Пептид D-Phe-L-Tyr - 5 г,
Натрия метабисульфит - 1 г,
1 М раствор хлористоводородной кислоты или 1 М раствор натрия гидроксида - до pH 3.5 - 4.0,
вода для инъекций - до 1000 г.
Пример 5. Интраназальная форма фармацевтической композиции, содержащей эффективное количество дипептида D-Phe-L-Tyr
Капли в нос (на 1000 г):
Пептид D-Phe-L-Tyr - 10 г,
метилпарабен - 1 г,
NaCl - 9 г,
Вода дистиллированная - до 1000 г.
Примеры твердых лекарственных форм фармацевтической композиции по настоящему изобретению включают, например, таблетки, пилюли, желатиновые капсулы и др.
Композиции согласно изобретению в форме таблеток содержат от 5 до 30% активного соединения, а также наполнитель(и) или носитель(и). В качестве таковых для таблеток применяются: а) разбавители: свекловичный сахар, лактоза, глюкоза, натрия хлорид, сорбит, маннит, фосфат кальция двузамещенный; б) связующие вещества: магниевый силикат алюминия, крахмальная паста, желатин, трагакант, метилцеллюлоза, карбоксиметилцеллюлоза и поливинилпирролидон; в) разрыхлители: декстроза, агар, альгиновая кислота или ее соли, крахмал.
Пример 6. Таблетированная форма фармацевтической композиции, содержащей эффективное количество дипептида D-Phe-L-Tyr
500 мг таблетки, содержащие по 100 мг пептида D-Phe-L-Tyr
Пептид D-Phe-L-Tyr - 100 мг,
Лактоза - 300 мг,
Альгиновая кислота - 50.0 мг,
Лимонная кислота - 10.0 мг,
Трагакант - 40.0 мг.
Таблетка может быть сформирована посредством прессовки или формовки активного ингредиента с одним или более дополнительными ингредиентами.
Для желатиновых капсул используются дополнительно красители и стабилизаторы. В качестве красителей используются: тартразин, индиго; в качестве стабилизаторов могут быть представлены: натрия метабисульфит, натрия бензоат. Предлагаемые желатиновые капсулы содержат от 1 до 20% активного ингредиента.
Пример 7. Капсульная форма фармацевтической композиции, содержащей эффективное количество дипептида D-Phe-L-Tyr
500 мг капсулы, содержащие по 100 мг пептида D-Phe-L-Tyr.
Пептид D-Phe-L-Tyr - 100 мг,
Глицерин - 100.0 мг,
Сахарный сироп - 250.0 мг,
Мятное масло - 40.0 мг,
Натрия бензоат - 10.0 мг,
Аскорбиновая кислота - 5.0 мг,
Тартразин - 5.0 мг.
Несмотря на то, что изобретение описано со ссылкой на раскрываемые варианты воплощения, для специалистов в данной области должно быть очевидно, что конкретные подробно описанные случаи приведены лишь в целях иллюстрирования настоящего изобретения, и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения. Должно быть, понятно, что возможно осуществление различных модификаций без отступления от сути настоящего изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| АГОНИСТЫ ОКСИТОЦИНОВЫХ РЕЦЕПТОРОВ | 2010 |
|
RU2539692C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2014 |
|
RU2690377C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ ЖЕЛУДОЧНО-КИШЕЧНЫХ РАССТРОЙСТВ | 2004 |
|
RU2353383C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ ЖЕЛУДОЧНО-КИШЕЧНЫХ РАССТРОЙСТВ | 2004 |
|
RU2543350C2 |
| Производные бифенила, обладающие биологической активностью, фармацевтические композиции и способы лечения на основе этих соединений и их применение | 2020 |
|
RU2736511C1 |
| ПЕПТИДНЫЕ КОМПОЗИЦИИ | 2014 |
|
RU2725150C2 |
| ПЕПТИДНЫЕ АНАЛОГИ АЛЬФА-МЕЛАНОЦИТСТИМУЛИРУЮЩЕГО ГОРМОНА | 2009 |
|
RU2496786C2 |
| АНАЛОГИ АЛЬФА- и ГАММА-MSH | 2013 |
|
RU2668791C2 |
| Слитый белок человеческого фактора свертывания IХ (FIX), способ его получения и применения | 2017 |
|
RU2736339C1 |
| КОМПОЗИЦИИ IL-12, НАЦЕЛЕННЫЕ НА EDB | 2019 |
|
RU2758143C1 |
Изобретение относится к биологически-активным веществам пептидной природы, применяемым в качестве средства для лечения депрессии, большого депрессивного расстройства, нейропатической боли и обладающим нейропротекторной активностью. Предложено применение фармацевтической композиции, содержащей D-Phe-L-Tyr, для лечения или профилактики заболеваний, опосредованных избыточной активностью НМДА-рецепторов. Составы фармацевтической композиции могут быть изготовлены в виде раствора для инъекций, а также капель в нос. Предлагаемая фармацевтическая композиция может найти применение в медицине. 2 ил., 7 пр.
Применение фармацевтической композиции, обладающей антагонистической активностью по отношению к НМДА-рецепторам, для лечения или профилактики заболеваний, опосредованных избыточной активностью НМДА-рецепторов, при этом указанная композиция включает эффективное количество дипептида D-Phe-L-Tyr и фармацевтически приемлемый носитель.
| ARIYOSHI, Y | |||
| & TAKEUCHI, H | |||
| "STRUCTURE-ACTIVITY RELATIONSHIPS OF N-β-PHENYLPROPIONYL-l-TYROSINE AND ITS DERIVATIVES ON THE INHIBITION OF AN IDENTIFIABLE GIANT NEURONE OF AN AFRICAN GIANT SNAIL.", British Journal of Pharmacology, 1982, 77(4), 631-639 | |||
| Устройство для записи направления ветра и для отметки затишья | 1929 |
|
SU13644A1 |
| ЗАМЕЩЕННЫЕ ПРОЛИЛТИРОЗИНЫ, ОБЛАДАЮЩИЕ ПСИХОТРОПНОЙ АКТИВНОСТЬЮ | 1995 |
|
RU2091390C1 |
| АНТАГОНИСТЫ РЕЦЕПТОРОВ ЭНДОТЕЛИНА | 1994 |
|
RU2126418C1 |
| СПОСОБ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ РАКОВОГО ЗАБОЛЕВАНИЯ У ЧЕЛОВЕКА, КОТОРОЕ ХАРАКТЕРИЗУЕТСЯ ПОВЫШЕННЫМ УРОВНЕМ ЭКСПРЕССИИ ИЛИ АКТИВНОСТИ Gadd45β ПО СРАВНЕНИЮ С ОБЫЧНЫМИ ЗДОРОВЫМИ КЛЕТКАМИ, В СЛУЧАЕ ЗАВИСИМОСТИ ЖИЗНЕСПОСОБНОСТИ И/ИЛИ РОСТА РАКОВЫХ КЛЕТОК ОТ NF-кВ, И ТРИПЕПТИД. | 2010 |
|
RU2577311C2 |
Авторы
Даты
2020-03-11—Публикация
2019-07-30—Подача