Область техники
В настоящем изобретении предложены соединения, имеющие агонистическую активность в отношении рецептора глюкозозависимого инсулинотропного полипептида (GIP), а также способам их применения в лечении нарушений обмена веществ.
Уровень техники
Диабет и ожирение представляют собой все более распространенные проблемы со здоровьем во всем мире и связаны с различными другими заболеваниями, в частности, с сердечно-сосудистыми заболеваниями (ССЗ), обструктивным апноэ во сне, инсультом, заболеванием периферических артерий, микрососудистыми осложнениями и остеоартритом. Во всем мире диабетом страдают 246 миллионов человек, и согласно оценкам 380 миллионов человек будут страдать диабетом к 2025 году. Многие из них имеют дополнительные факторы риска со стороны сердечно-сосудистой системы, включая высокий/патологический уровень липопротеинов низкой плотности (ЛПНП) и триглицеридов, а также низкий уровень липопротеинов высокой плотности (ЛПВП). Сердечно-сосудистые заболевания являются причиной приблизительно 50% смертей у людей, страдающих диабетом, и показатели заболеваемости и смертности, связанные с ожирением и диабетом, подчеркивают медицинскую потребность в эффективных способах лечения.
Глюкозозависимый инсулинотропный полипептид («GIP», также известный как «желудочный ингибиторный полипептид») представляет собой пептид, состоящий из 42 остатков аминокислот, который секретируется энтероэндокринными K-клетками тонкого кишечника в кровоток в ответ на поступление питательных веществ перорально. GIP ингибирует секрецию желудочной кислоты и, как было показано, является мощным стимулятором секреции инсулина бета-клетками поджелудочной железы после перорального потребления глюкозы («эффект инкретина») (Creutzfeldt, W., et al, 1979, Diabetologia, 16:75-85).
Высвобождение инсулина, вызванное потреблением глюкозы и других питательных веществ, обусловлено гормональными и нервными факторами (Creutzfeldt, W., et al, 1985, Diabetologia, 28: 565-573). Было высказано предположение, что несколько регуляторных пептидов желудочно-кишечного тракта могут играть роль инкретинов, и из указанных кандидатов только GIP и глюкагоноподобный пептид 1 («GLP-1»), как представляется, соответствуют требованиям, которые необходимо учитывать в отношении физиологических стимуляторов постпрандиального высвобождения инсулина (Nauck, et al, 1989, J. Clin. Endocrinol Metab., 69:654-662). Было показано, что комбинированное действие GIP и GLP-1 является достаточным, чтобы объяснить полный эффект инкретина энтероинсулярной оси (Fehmann, Н. С, et al, 1989, FEBS Lett, 252: 109-112).
Специалистам в данной области техники хорошо известны разнообразные и многочисленные общепризнанные и перспективные способы применения GIP. Следовательно, введение соединений согласно настоящему изобретению для индукции агонистического действия может оказывать аналогичный эффект и может иметь аналогичное применение, как и введение GIP. Существующие различные способы применения GIP можно обобщить следующим образом: лечение заболевания, выбранного из группы, состоящей из сахарного диабета 1 типа, сахарного диабета 2 типа (Visboll, Т., 2004, Dan. Med. Bull, 51:364-70), резистентности к инсулину (WO 2005/082928), ожирения (Green В.D., et al, 2004, Current Pharmaceutical Design, 10:3651-3662), нарушения обмена веществ (Gault, V. A., et al, 2003, Biochem. Biophys. Res. Commun., 308:207-213), заболевания центральной нервной системы, нейродегенеративного заболевания, застойной сердечной недостаточности, гипогликемии и расстройств, при которых желательным является снижение потребления пищи и потеря массы тела. В островках поджелудочной железы GIP не только резко усиливает секрецию инсулина, но также стимулирует выработку инсулина путем усиления транскрипции и трансляции проинсулина (Wang, et al, 1996, MoI Cell. Endocrinol, 116:81-87) и усиления размножения и выживания бета-клеток поджелудочной железы (Trumper, et al, 2003, Diabetes, 52:741-750). Помимо влияния на поджелудочную железу для усиления секреции инсулина, GIP также непосредственно влияет на ткани-мишени инсулина, чтобы снизить уровень глюкозы в плазме крови: усиливает поглощение глюкозы в жировой ткани (Eckel, et al, 1979, Diabetes, 28: 1141-1142) и мышечной ткани (O'Harte, et al., 1998, J. Endocrinol, 156: 237-243) и ингибирует выработку глюкозы в печени (Elahi, D., et al., 1986, Can. Physiol. Pharmacol, 65: A18).
Некоторое время назад было установлено, что потеря массы тела, связанная с лечением с использованием агонистов GLP-1, усиливается при совместном введении GLP-1 и GIP (Finan, Sci Transl Med. 2013; 5(209):209ra151. Irwin N et al, 2009, Regul Pept; 153: 70-76. Gault et al, 2011, Clin Sci (Lond); 121:107-117). Например, Finan и коллеги выявили значительное снижение массы тела у мышей с алиментарным ожирением (DIO) после совместного введения в течение периода средней длительности ацилированного агониста GIP и ацилированного агониста GLP-1. Совместное введение вызывало снижение массы тела и жировой массы в большей степени, чем введение указанных агонистов в виде монотерапии. Данные также свидетельствуют о том, что GLP-1 и GIP оказывают аддитивное действие на гликемический контроль (Gault et al, 2011, Clin Sci (Lond); 121:107-117). Результаты исследования, проведенного Gault et al выявили, что совместное введение аналога GLP-1 и ацилированного аналога GIP в течение периода средней длительности приводит к более выраженному снижению уровня глюкозы и инсулинотропному действию при проведении внутрибрюшинного теста на толерантность к глюкозе у мышей ob/ob, чем инъекция агониста GLP-1 или агониста GIP по отдельности. Следовательно, агонисты GIP могут быть особенно эффективными в улучшении гликемического контроля и снижении массы тела при введении в комбинации с агонистом рецептора GLP-1 (в виде компонента одного и того же фармацевтического состава или в виде отдельных составов).
Использование немодифицированного GIP в качестве терапевтического средства, однако, ограничено коротким периодом полувыведения в условиях in vivo, составляющим 2 минуты (Said and Mutt, 1970, Science, 169:1217-1218). В сыворотке крови оба инкретина, GIP и GLP-1, разлагаются под действием дипептидилпептидазы IV ("DPPIV"). Повышение устойчивости GIP к протеолизу не только поддерживает активность GIP в отношении его рецептора, но, что более важно, предотвращает образование фрагментов GIP, некоторые из которых действуют как антагонисты рецепторов GIP (Gault, et al., 2002, J. Endocrinol, 175: 525-533). Описанные модификации включают защиту N-конца GIP от протеолиза DPPIV путем модификации N-концевого остатка тирозина (O'Harte, et al., 2002, Diabetologia, 45: 1281-1291), мутацию аланина в положении 2 (Hinke, et al., 2002, Diabetes, 51: 656-661), мутацию глутаминовой кислоты в положении 3 (Gault, et al., 2003 Biochem Biophys, Res. Commun., 308: 207-213) и мутацию аланина в положении 13 (Gault, et al, 2003, Cell Biol. International, 27: 41-46).
Были поданы следующие заявки на патенты, связанные с действием аналогов GIP на функцию различных органов-мишеней и их потенциальным применением в качестве терапевтических агентов:
в публикации РСТ WO 00/58360 раскрыты пептидные аналоги GIP, которые стимулируют высвобождение инсулина. В частности, в указанной заявке раскрыты специфичные пептидильные аналоги, содержащие по меньшей мере 15 остатков аминокислот с N-конца GIP (1-42).
в публикации РСТ WO 03/082898 раскрыты С-концевые усеченные фрагменты и аналоги GIP, модифицированные на N-конце, а также различные аналоги GIP с восстановленной пептидной связью или изменениями аминокислот, которые расположены возле DPPFV-специфичного сайта расщепления. В указанной заявке дополнительно раскрыты аналоги с различными линкерами между потенциальными сайтами связывания с рецепторами GIP. Предполагается, что соединения согласно указанной заявке пригодны для лечения состояний, опосредованных рецептором GIP, таких как инсулиннезависимый сахарный диабет и ожирение. Также, помимо других терапевтических эффектов соединений согласно настоящему изобретению, описанных в настоящем документе, более тщательный контроль уровня глюкозы в плазме крови может предотвратить долгосрочные осложнения диабета, обеспечивая тем самым улучшенное качество жизни пациентов. В дополнение к улучшению контроля уровня глюкозы в крови GIP также может усилить опосредованную GLP-1 потерю массы тела.
Было показано, что конъюгация аналогов GIP, например, с ПЭГ (полиэтиленгликолем) увеличивает период полувыведения в условиях in vivo, однако были обнаружены потенциальные побочные эффекты пегилированных фармацевтических продуктов, таких как интерферон-бета и рибавирин (J Clin Gastroenterol. 2004 Sep; 38(8):717-22, Gut
2006;55:1350-1359 doi:10.1136/gut.2005.076646).
Следовательно, до сих пор существует потребность в улучшенных и безопасных аналогах GIP, которые стабильны в составах и имеют длительный период полувыведения в условиях in vivo, вследствие снижения чувствительности к протеолизу и снижения клиренса, сохраняя при этом аффинность связывания с рецептором GIP, которая необходима для проявления агонистической активности.
Краткое описание изобретения
В настоящем изобретении предложены аналоги GIP, которые могут обладать измененной активностью GIP, согласно результатам количественного определения эффективности в условиях in vitro, и измененным, предпочтительно увеличенным, терминальным периодом полувыведения (T1/2), согласно результатам определения в исследованиях на мышах в условиях in vivo.
Было обнаружено, что агонисты рецептора GIP согласно настоящему изобретению превосходят существующие аналоги GIP, поскольку указанные агонисты GIP обеспечивают длительный терминальный период полувыведения. Аналоги GIP, следовательно, можно применять в качестве терапевтических средств для лечения нарушений обмена веществ (расстройств метаболизма), включая, но не ограничиваясь ими, сахарный диабет 2 типа, ожирение и связанные расстройства.
Согласно первому аспекту в настоящем изобретении предложен аналог GIP, представленный общей Формулой I:
R1-Tyr-X2-Glu-Gly-Thr-Phe-Ile-Ser-Asp-X10-X11-X12-Glu-Leu-X15-X16-X17-X18-X19-X20-X21-Phe-X23-X24-X25-Leu-X27-X28-X29-Y1-Y2-R2 (I), в которой
R1 представляет собой Н, Ас или пироглутаминовую кислоту (pGlu; (S)-(-)-2-пирролидон-5-карбоновую кислоту), С1-4 алкил, ацетил, формил, бензоил и трифторацетил,
Х2 представляет собой Aib, Ala, D-Ala, Gly, Ser, N-Me-Ser, Ас3с, Ac4c или Ac5c;
X10 представляет собой Tyr, Leu или Ser;
X11 представляет собой Ser или Leu;
X12 представляет собой Lys, Ψ или Ile;
X15 представляет собой Asp или Glu;
X16 представляет собой Ser, Glu, Lys или Ψ;
X17 представляет собой Ilе, Lys, Gln, Arg или Ψ;
X18 представляет собой His, Arg или Ala;
X19 представляет собой Gln, Lys, Ala или Glu;
X20 представляет собой Gln, Lys, Ala, His или Arg;
X21 представляет собой Ala, Leu, Asp или Glu;
X23 представляет собой Val или Ile;
X24 представляет собой Asn или Glu;
X25 представляет собой Tyr или Trp;
Х27 представляет собой Leu, Glu, Ser, Lys или Val;
X28 представляет собой Ala, Ser или Arg;
X29 представляет собой Aib, Gly, Ala, Gln, Thr, Ser или Lys или отсутствует;
Y1 представляет собой Lys-Gly, Gly-Pro-Ser-Ser-Gly-Ala-Pro-Pro-Pro-Ser, Gly-Pro-Ser-Ser-Gly-Ala-Pro-Pro-Ser, Pro-Ser-Ser-Gly-Ala-Pro-Pro-Pro-Ser, Pro-Ser-Ser-Gly-Ala-Pro-Pro-Ser, Gly-Lys-Lys-Asn-Asp-Trp-Lys-His-Asn-Ile-Thr-Gln или отсутствует;
Y2 представляет собой Ψ или отсутствует;
R2 представляет собой -NH2 или -ОН;
причем Ψ представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, и при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем;
при этом указанный аналог GIP содержит один и только один остаток Ψ;
или его фармацевтически приемлемая соль или сольват.
Согласно одному аспекту настоящего изобретения R1 представляет собой Н-, Ас или pGlu.
Комбинации остатков, которые могут присутствовать в некоторых из вариабельных положений формулы I, включают:


Согласно другому аспекту в настоящем изобретении предложен аналог GIP, представленный общей Формулой II:

в которой
R1 представляет собой Н-, Ас или pGlu;
Х2 представляет собой Aib, Ala, D-Ala или Gly;
X12 представляет собой Lys, Ψ или Ilе;
X15 представляет собой Asp или Glu;
X16 представляет собой Ser, Glu, Lys или Ψ;
X17 представляет собой Ilе, Lys, Gln, Arg или Ψ;
X18 представляет собой His, Arg или Ala;
X19 представляет собой Gln или Ala;
Х20 представляет собой Gln, Lys, Ala, His или Arg;
X21 представляет собой Ala, Asp или Glu;
X23 представляет собой Ilе или Val;
Х24 представляет собой Asn или Glu;
Х25 представляет собой Tyr или Trp;
Х27 представляет собой Leu, Glu, Ser, Lys или Val;
X28 представляет собой Ala, Ser или Arg;
X29 представляет собой Aib, Gly, Ala, Gln, Thr, Ser или Lys или отсутствует;
Y1 представляет собой Lys-Gly, Gly-Pro-Ser-Ser-Gly-Ala-Pro-Pro-Pro-, Gly-Pro-Ser-Ser-Gly-Ala-Pro-Pro-Ser, Pro-Ser-Ser-Gly-Ala-Pro-Pro-Pro-Ser, Pro-Ser-Ser-Gly-Ala-Pro-Pro-Ser, Gly-Lys-Lys-Asn-Asp-Trp-Lys-His-Asn-Ile-Thr-Gln или отсутствует;
Y2 представляет собой Ψ или отсутствует;
R2 представляет собой -NH2 или -ОН;
причем Ψ представляет собой остаток Lys, в котором боковая цепь указанного остатка Lys конъюгирована с липофильным заместителем;
при этом указанный аналог GIP содержит один и только один остаток Ψ;
или его фармацевтически приемлемая соль или сольват.
Комбинации остатков, которые могут присутствовать в некоторых из вариабельных положений формулы II, включают:



Согласно другому аспекту в настоящем изобретении предложен аналог GIP, представленный общей Формулой III:
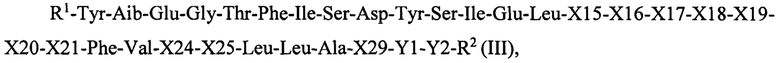
в которой
R1 представляет собой Н-, Ас или pGlu;
X15 представляет собой Asp или Glu;
X16 представляет собой Lys или Ψ;
X17 представляет собой Ilе или Ψ;
X18 представляет собой His или Ala;
Х19 представляет собой Gln или Ala;
Х20 представляет собой Gln, Lys или Arg;
Х21 представляет собой Ala, Asp или Glu;
Х24 представляет собой Asn или Glu;
Х25 представляет собой Tyr или Trp;
Х28 представляет собой Ala, Ser или Arg;
Х29 представляет собой Gln или отсутствует;
Y1 представляет собой Lys-Gly, Gly-Pro-Ser-Ser-Gly-Ala-Pro-Pro-Pro-Ser, Gly-Pro-Ser-Ser-Gly-Ala-Pro-Pro-Ser, Pro-Ser-Ser-Gly-Ala-Pro-Pro-Pro-Ser, Pro-Ser-Ser-Gly-Ala-Pro-Pro-Ser, Gly-Lys-Lys-Asn-Asp-Trp-Lys-His-Asn-Ile-Thr-Gln или отсутствует;
Y2 представляет собой Ψ или отсутствует;
R2 представляет собой -NH2 или -ОН;
причем Ψ представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, и при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем;
при этом указанный аналог GIP содержит один и только один остаток Ψ;
или его фармацевтически приемлемая соль или сольват.
Комбинации остатков, которые могут присутствовать в некоторых из вариабельных положений Формулы III, включают:

Аналог GIP может иметь формулу R1-Z-R2, в которой R1 и R2 соответствуют тем заместителям, которые определены выше, и Z имеет следующую последовательность:
Y-Aib-EGTFISDYSIELDKIHQQDFVNWLLAQKGΨ;
Y-Aib-EGTFISDYSIELDKΨHQQDFVNYLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKΨHQQDFVNWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKΨAAQDFVNWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELEKΨAAKEFVNWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELEKΨAQRAFVEWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELEKIAQRAFVEWLLAQGPSSGAPPPSΨ;
Y-Aib-EGTFISDYSIELEKIAQRAFVEWLLAQΨ;
Y-Aib-EGTFISDYSIELDKΨAAQDFVNWLLAGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKIAAQDFVNWLLAGPSSGAPPPSΨ;
Y-Aib-EGTFISDYSIELDKΨAQRAFVEWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKΨAQRAFIEWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKIAQRAFIEWLLAGPSSGAPPPSKΨ;
Y-Aib-EGTFISDYSIELDKIAQKEFIEWLLAGPSSGAPPPSKΨ;
Y-Aib-EGTFISDYSIELDKIAAQDFIEWLLAGPSSGAPPPSKΨ;
Y-Aib-EGTFISDYSIELDKIAAQDFVEWLLAGPSSGAPPPSKΨ;
Y-Aib-EGTFISDYSIELDKIAQRAFIEWLLAQGPSSGAPPPSKΨ;
Y-Aib-EGTFISDYSIELDKΨAAQAFVNWLLAGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKΨAAQDFVNWLLAAGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKΨAAQDFINWLLAGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKΨAAQDFIEWLLAGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKΨAAQDFIEWLLAGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKΨIAQRAFIEWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSKΨELDKIAQRAFIEWLLAQGPSSGAPPPS;
Y-DAla-EGTFISDYSIELDKKΨAQRAFIEWLLAQGPSSGAPPPS;
Y-DAla-EGTFISDYSIELDKIAAQDFIEWLLAGPSSGAPPPSKΨ;
Y-Aib-EGTFISDYSIELDKΨAAQDFIEWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKΨAAQDFINWLLAQGPSSGAPPPS; или
Y-Aib-EGTFISDYSIELDKΨAAQAFIEWLLAQGPSSGAPPPS.
Аналог GIP может иметь формулу R1-Z-R2, в которой R1 и R2 соответствуют тем заместителям, которые определены выше, и Z имеет последовательность:
Y-Aib-EGTFISDYSIELDK-K(гексадеканоил-изо-Glu)-HQQDFVNWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELD-K(гексадеканоил-изо-Glu)-IHQQDFVNWLLAQGPSSGAPPPS;


Аналог GIP может представлять собой:



Помимо этого, в настоящем изобретении предложена фармацевтическая композиция, содержащая аналог GIP, описанный в настоящем документе, или его фармацевтически приемлемую соль или сольват, в смеси с носителем, предпочтительно с фармацевтически приемлемым носителем. Указанный аналог GIP может представлять собой, например, фармацевтически приемлемую кислотно-аддитивную соль.
Фармацевтическая композиция может быть изготовлена в виде жидкости, пригодной для введения путем инъекции или инфузии. Фармацевтическая композиция может быть изготовлена так, чтобы вызвать контролируемое, например, замедленное высвобождение указанного аналога GIP.
Помимо этого, в настоящем изобретении предложен терапевтический набор, содержащий аналог GIP, описанный в настоящем документе, а также устройство, содержащее аналог GIP, описанный в настоящем документе.
Помимо этого, в настоящем изобретении предложен аналог GIP, описанный в настоящем документе, или его фармацевтически приемлемая соль или сольват, для применения в способе лечения, например, для применения в лечении и/или предотвращении нарушения обмена веществ.
В настоящем изобретении также предложено применение аналога GIP, описанного в настоящем документе, или его фармацевтически приемлемой соли или сольвата, в получении лекарственного средства для лечения и/или предотвращения нарушения обмена веществ.
В настоящем изобретении также предложен способ предотвращения и/или лечения нарушения обмена веществ у субъекта, включающий введение субъекту аналога GIP, описанного в настоящем документе, или его фармацевтически приемлемой соли или сольвата.
Нарушение обмена веществ может включать различные типы диабета или заболевание, связанное диабетом, или ожирение или расстройство, связанное с ожирением. Связь между ожирением и диабетом хорошо известна, поэтому указанные условия могут быть, но не обязательно, отдельными или взаимоисключающими.
Расстройства, связанные с диабетом, включают резистентность к инсулину, непереносимость глюкозы, повышенное содержание глюкозы натощак, преддиабет, сахарный диабет 1 типа, сахарный диабет 2 типа, гестационный диабет, сопровождающийся гипертензией, дислипидемию и их комбинации.
Расстройства, связанные с диабетом, также включают атеросклероз, артериосклероз, ишемическую болезнь сердца, заболевание периферических артерий и инсульт; или состояния, связанные с атерогенной дислипидемией, расстройства, связанные с уровнем липидов в крови, повышенное кровяное давление, гипертензию, протромботическое состояние, провоспалительное состояние и расстройства, связанные с костной тканью, такие как остеопороз.
Расстройство, связанное с уровнем липидов в крови, может быть выбрано из высокого уровня триглицеридов, низкого уровня холестерина-ЛПВП, высокого уровня холестерина-ЛПНП, а также накопления бляшек в стенках артерий, или их комбинации.
Протромботическое состояние может быть выбрано из высокого уровня фибриногена в крови и высокого уровня ингибитора активатора плазминогена 1 в крови.
Провоспалительное состояние может представлять собой повышенный уровень С-реактивного белка в крови.
Расстройства, связанные с ожирением, включают воспаление, связанное с ожирением, заболевание желчного пузыря, связанное с ожирением, и индуцированное ожирением апноэ во сне, или могут быть связаны с состоянием, выбранным из атерогенной дислипидемии, расстройств, связанных с уровнем липидов в крови, повышенного кровяного давления, гипертензии, протромботического состояния и провоспалительного состояния, или их комбинации.
Краткое описание чертежей
Фигура 1: Уровни глюкозы в крови (А-С) и значения площади под кривой зависимости концентрации глюкозы в крови от времени (AUC) (D) в пероральном тесте толерантности к глюкозе (ПТТГ) у мышей после 5-часового голодания. Мышам вводили подкожно носитель, аналог GLP-1, лираглутид (10 нмоль/кг), и агонисты рецептора GIP (соединение 12, 13, 17 и 21 в концентрации 3-300 нмоль/кг) за 4 часа до перорального введения глюкозы через желудочный зонд (t=0). Данные представляют собой средние значения ± SEM; n=6. Статистические различия в сравнении с носителем: *p<0,05, **p<0,01, ***p<0,001.
Фигура 2: Уровни глюкозы в крови (A-D) и значения площади под кривой зависимости концентрации глюкозы в крови от времени (AUC) (Е) в пероральном тесте толерантности к глюкозе (ПТТГ) у мышей после 5-часового голодания. Мышам вводили подкожно носитель и агонисты рецептора GIP (соединения 12, 18, 41, 33 и 35 в концентрации 3-300 нмоль/кг) за 4 часа до перорального введения глюкозы через желудочный зонд (t=0). Данные представляют собой средние значения ± SEM; n=6. Статистические различия в сравнении с носителем: ***p<0,001.
Фигура 3: Относительные изменения массы тела (дельта (Δ) массы тела = масса тела в каждый день исследования - масса тела в день 1) у мышей DIO в течение трех недель лечения. Животным вводили две отдельные инъекции один раз в день подкожно. Первая инъекция содержала носитель 1 или аналог GLP-1, лираглутид (20 нмоль/кг). Вторая инъекция содержала носитель 2 или соединение 12 (3 и 30 нмоль/кг). Агонист GIP вводили только на каждый третий день исследования (начиная с 1-го дня). В другие дни агонист GIP был заменен носителем 2. Данные представляют собой средние значения ± SEM; n=8-9. Статистические различия в сравнении с носителем на 22-й день: ***p<0,001. Статистическое различие (p<0,05) между лираглутидом и лираглутидом, который вводили совместно с агонистом GIP, показано с помощью линии.
Фигура 4: Относительные изменения массы тела (дельта (Δ) массы тела = масса тела в каждый день исследования - масса тела в день 0) у мышей DIO в течение четырех недель лечения с использованием носителя, аналога GLP-1, лираглутида, лираглутида + соединение 10 или 12 (А), лираглутида + соединение 17 (В), лираглутида + соединение 18 (С), лираглутида + соединение 35 (D) или лираглутида + соединение 41 (Е). Животным вводили две отдельные инъекции один раз в день подкожно. Первая инъекция содержала носитель 1 или лираглутид (20 нмоль/кг). Вторая инъекция содержала носитель 2 или агонисты GIP (30 и/или 300 нмоль/кг). Агонисты GIP вводили только на каждый третий день исследования (начиная с 0-го дня). В другие дни агонисты GIP были заменены носителем 2. Данные представляют собой средние значения ± SEM; n=9. Статистические различия в сравнении с носителем на 27-й день: ***p<0,001. Статистические различия (p<0,05) между лираглутидом и лираглутидом, который вводили совместно с агонистом GIP, показаны с помощью линий.
Подробное описание изобретения
Если иное не определено в настоящем документе, научные и технические термины, используемые в данном описании, должны иметь значения, которые обычно понятны специалистам в данной области техники. Как правило, номенклатура и методики, которые относятся к областям химии, молекулярной биологии, клеточной биологии и онкологии, иммунологии, микробиологии, фармакологии и химии белка и нуклеиновых кислот, описанных в настоящем документе, хорошо известны и обычно используются в данной области техники.
Определения
Если не указано иное, следующие определения предназначены для конкретных терминов, используемых в приведенном выше описании.
В данном описании термин «содержат» или варианты, такие как «содержит» или «содержащий» следует понимать как включение указанного целого числа (или компонентов) или группы целых чисел (или компонентов), но не исключение какого-либо другого целого (или компонентов) или группы целых чисел (или компонентов).
Формы единственного числа «а», «an» и «the» включают множественное число, если из контекста явно не следует иное.
Термин «включая» используется для обозначения «включая, но не ограничиваясь ими». Термины «включая» и «включая, но не ограничиваясь ими» используются взаимозаменяемо.
Термины «пациент», «субъект» и «индивидуум» могут быть использованы взаимозаменяемо и относятся к любому человеку или животному, отличному от человека. Указанные термины включают млекопитающих, таких как человек, приматы, сельскохозяйственных животных (например, крупный рогатый скот, свиней), домашних животных (например, собак, кошек) и грызунов (например, мышей и крыс).
Термин «сольват», применительно к настоящему изобретению, относится к комплексу с определенной стехиометрией, образованному растворенным веществом (в данном случае, пептидным конъюгатом или его фармацевтически приемлемой солью в соответствии с настоящим изобретением) и растворителем. В этой связи растворитель может представлять собой, например, воду, этанол или другой фармацевтически приемлемый растворитель, как правило, низкомолекулярные органические соединения, такие как, но не ограничиваясь ими, уксусная кислота или молочная кислота. Если рассматриваемый растворитель представляет собой воду, то такой сольват обычно называют гидратом.
Термин «агонист», применительно к настоящему изобретению, относится к веществу (лиганду), которое активирует передачу сигналов с участием рассматриваемого типа рецепторов. Термин «антагонист», применительно к настоящему изобретению, относится к веществу (лиганду), которое уменьшает передачу сигналов с участием рассматриваемого типа рецепторов.
В тексте настоящего описания и формулы изобретения использованы стандартные однобуквенные и трехбуквенные коды природных (или «протеиногенных») аминокислот, а также общепринятые трехбуквенные коды для других (неприродных или «непротеиногенных») α-аминокислот, таких как Aib (α-аминоизомаслянная кислота), Orn (орнитин) и D-Ala (D-аланин). Все остатки аминокислот в пептидах согласно настоящему изобретению предпочтительно имеют L-конфигурацию, за исключением случаев, когда четко указано иное.
Последовательности, раскрытые в настоящем описании, включают последовательности, содержащие «Н-» фрагмент на амино-конце (N-конце) последовательности, и «-ОН» фрагмент или «-NH2» фрагмент на карбоксильном конце (С-конце) последовательности. В таких случаях, и если не указано иное, фрагмент «Н» на N-конце рассматриваемой последовательности означает атом водорода (т.е. R1=H), что соответствует наличию свободной первичной или вторичной аминогруппы на N-конце, в то время как фрагмент «-ОН» или «-NH2» на С-конце последовательности (т.е. R2=OH или NH2) обозначает карбокси (-СООН) группу или амидо (CONH2) группу на С-конце, соответственно.
Соединения согласно настоящему изобретению обладают биологической активностью GIP, в частности, при лечении нарушений обмена веществ, таких как диабет и ожирение. Активность указанных соединений можно оценить, например, в количественных исследованиях в условиях in vivo, в которых уровень глюкозы в крови или другой вид биологической активности определяют после того как исследуемое животное получило или подверглось воздействию аналога GIP. Соединения согласно настоящему изобретению могут быть особенно эффективными в улучшении гликемического контроля и снижении массы тела при введении совместно с агонистом рецептора GLP-1 пациенту с диабетом и/или избыточной массой тела или субъекту с ожирением. Действие, которое может быть достигнуто при использовании комбинированной терапии, может превосходить то, которое получают при введении агониста рецептора GLP-1 в виде монотерапии у сопоставимых субъектов при введении в соответствии с сопоставимым режимом дозирования. Соединения согласно настоящему изобретению также способны улучшать гликемический контроль и снижать массу тела при введении по отдельности. Группа Y1 и Y2 оказывает стабилизирующее действие на аналоги GIP. Не желая быть связанными соответствием какой-либо теории, авторы настоящего изобретения полагают, что группа, содержащая С-концевую часть эксендина-4 и соединения-агонисты GIP, оказывает влияние на складывание пептида.
При лечении субъекта, страдающего диабетом, или субъекта с избыточной массой тела эффект лечения с использованием аналога GIP согласно настоящему изобретению может быть выше, чем эффект, полученный при использовании эквивалентного количества (по массе или мольному соотношению) GIP человека дикого типа у сопоставимых субъектов, при введении в соответствии с сопоставимым режимом дозирования, по отдельности или в комбинации с другим агентом для лечения диабета или агентом для лечения ожирения.
Активность в количественных исследованиях в условиях in vitro также может быть использована в качестве меры активности соединений. Как правило, соединения обладают активностью (т.е. агонистической активностью) в отношении рецептора GIP (обозначенного GIP-R). Значения ЭК50 можно использовать в качестве численной меры агонистической эффективности в отношении данного рецептора. Значения ЭК50 являются мерой концентрации соединения, необходимой для достижения половины максимальной активности указанного соединения в конкретном количественном исследовании. В любом конкретном количественном исследовании значение ЭК50 соединения в конкретном количественном исследовании может быть оценено по отношению к ЭК50 GIP человека. Следовательно, отношение значения ЭК50 исследуемого соединения к значению ЭК50 GIP человека дикого типа (ЭК50 [исследуемое соединение]/ЭК50 [GIP]) в отношении рецептора GIP человека может быть меньше 10, меньше 5, меньше 1, меньше 0,1, меньше 0,05 или меньше 0,01. Значения ЭК50 могут быть определены с помощью количественного исследования рецептора GIP человека, описанного в приведенных ниже примерах. В указанном количественном исследовании соединения могут иметь, например, значение ЭК50 0,001-0,050 нМ, 0,001-0,030 нМ, 0,001-0,020 нМ или 0,001-0,010 нМ.
Соединения, как правило, обладают минимальной агонистической активностью в отношении рецептора GLP-1 или вообще лишены указанной активности. Например, отношение значения ЭК50 исследуемого соединения к значению ЭК50 агониста GLP-1, эксендина-4 (ЭК50 [исследуемое соединение]/ЭК50 [Ех4]), в отношении рецептора GIP человека может составлять по меньшей мере приблизительно 100, по меньшей мере приблизительно 250, по меньшей мере приблизительно 500, по меньшей мере, приблизительно 750, по меньшей мере приблизительно 1000, по меньшей мере приблизительно 5000 или по меньшей мере приблизительно 10000. (В настоящей заявке термин «приблизительно» используется для обозначения +/-10%.). Значения ЭК50 могут быть определены с помощью количественного анализа с использованием рецептора GLP-1 человека, описанного в приведенных ниже примерах. В указанном количественном исследовании соединение может иметь значение ЭК50, например, по меньшей мере 1 нМ, по меньшей мере 3 нМ, по меньшей мере 5 нМ или по меньшей мере 10 нМ.
Липофильная группа
Соединение согласно настоящему изобретению содержит остаток Ψ, то есть остаток, выбранный из Lys, Arg, Orn и Cys, в котором боковая цепь конъюгирована с липофильным заместителем.
Не желая быть связанными соответствием какой-либо конкретной теории, авторы настоящего изобретения полагают, что заместитель связывается с белками плазмы крови (например, альбумином) в кровотоке, защищая тем самым соединения согласно настоящему изобретению от ферментативного разложения и увеличивая тем самым период полувыведения соединений. Указанный заместитель также может модулировать активность соединения, например, в отношении рецептора GIP.
Заместитель конъюгируют с функциональной группой на дистальном конце боковой цепи, относительно альфа-атома углерода. Нормальная способность боковой цепи Lys, Arg, Orn или Cys участвовать во взаимодействиях, опосредованных указанной функциональной группой (например, внутри- и межмолекулярных взаимодействиях), может быть уменьшена или полностью устранена в присутствии заместителя. Следовательно, общие свойства соединения могут быть относительно нечувствительны к изменениям в фактической аминокислоте, присутствующей в виде остатка Ψ. Следовательно, как полагают, любой из остатков Lys, Arg, Orn и Cys может присутствовать в любом положении, где допускается Ψ. Однако согласно некоторым вариантам реализации настоящего изобретения аминокислотный компонент Ψ предпочтительно представляет собой Lys.
Следовательно, Ψ представляет собой остаток Lys, Arg, Orn или Cys, в котором боковая цепь конъюгирована с заместителем, имеющим формулу -Z1 или -Z2-Z1.
-Z1 представляет собой цепь жирной кислоты, содержащую на конце связь -Х- с Ψ или с Z2;
причем
-Х- представляет собой связь, -СО-, -SO- или -SO2-;
и необязательно Z1 содержит полярную группу на конце цепи, расположенную дистально относительно связи -Х-; причем указанная полярная группа содержит группу карбоновой кислоты или биоизостера карбоновой кислоты, фосфоновой кислоты или сульфоновой кислоты;
и при этом -Z2-, если он присутствует, представляет собой спейсер формулы:
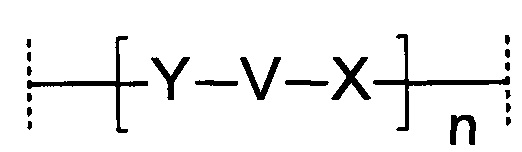
соединяющий Z1 с Ψ;
в котором:
каждый Y независимо представляет собой -NH, -NR, -S или -О, при этом R представляет собой алкил, защитную группу или образует связь с другой частью спейсера Z2;
каждый X независимо представляет собой связь, СО-, SO- или SO2-;
при условии, что в тех случаях, когда Y представляет собой -S, X, с которым он связан, представляет собой связь;
каждый V независимо представляет собой двухвалентный органический фрагмент, связывающий Y и X;
и n 1-10.
Группа Z1
Z1 представляет собой цепь жирной кислоты, содержащую связь с Ψ или Z2, которая упоминается в настоящем документе как -Х-. -Х- может представлять собой, например, связь, ацил (-СО-), сульфинил (-SO-) или сульфонил (-SO2-). Когда Z1 связан непосредственно с Ψ, то есть, когда Z2 не присутствует, -Х- предпочтительно представляет собой ацил (-СО-), сульфинил (-SO-) или сульфонил (-SO2-). Наиболее предпочтительно -Х- представляет собой ацил (-СО-).
Z1 может дополнительно содержать полярную группу, при этом указанная полярная группа может быть расположена на конце цепи, дистально относительно связи -Х-. Другими словами, связь находится в ω-положении по отношению к полярной группе. Полярная группа может быть связана непосредственно с концом цепи жирной кислоты или может быть связана посредством линкера.
Предпочтительно полярная группа представляет собой кислую или слабокислую группу, например, карбоновую кислоту или биоизостер карбоновой кислоты, фосфонат, или сульфонат. Полярная группа может иметь pKa в пределах от -2 до 12 в воде, более предпочтительно от 1 до 7, более предпочтительно от 3 до 6. Некоторые предпочтительные полярные группы имеют pKa от 4 до 5.
Например, но не ограничиваясь ими, полярная группа может включать группу карбоновой кислоты (-СООН) или биоизостера карбоновой кислоты, фосфоновой кислоты (-Р(O)(ОН)2) или сульфоновой кислоты (-SO2OH).
Предпочтительно полярная группа, если она присутствует, включает карбоновую кислоту или биоизостер карбоновой кислоты. Подходящие биоизостеры карбоновых кислот известны в данной области техники. Предпочтительно биоизостер содержит протон, имеющий величину pKa, которая аналогична таковой для соответствующей карбоновой кислоты. Примеры подходящих биоизостеров могут включать, но не ограничиваются ими, тетразол, ацилсульфоамиды, ацилгидроксиламин и производные сквариковой кислоты, как показано ниже (--- указывает точку присоединения):
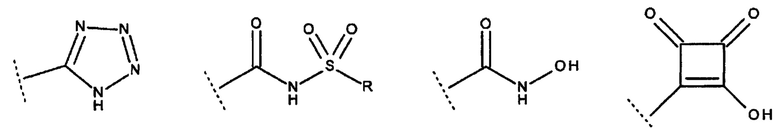
R представляет собой, например, Me, CF3.
В настоящей заявке цепь жирной кислоты относится к фрагменту, содержащему цепь атомов углерода, при этом атомы углерода преимущественно замещены водородом или водородоподобными атомами, например, углеводородной цепью. Указанные цепи жирной кислоты часто называют липофильными, хотя следует понимать, что замещение может изменить липофильные свойства всей молекулы.
Цепь жирной кислоты может быть алифатической. Указанная цепь может быть полностью насыщенной или может содержать одну или более двойных или тройных связей. Каждая двойная связь, если они присутствуют, может находиться в Е- или Z-конфигурации. Цепь жирной кислоты также может содержать один или более фрагментов циклоалкилена или гетероциклоалкилена по всей длине, и дополнительно или в качестве альтернативы может содержать один или более фрагментов арила или гетероарила по всей длине. Например, цепь жирной кислоты может содержать фрагмент фенилена или пиперазинилена по всей длине, как, например, показано ниже (где --- обозначает точки присоединения внутри цепи).
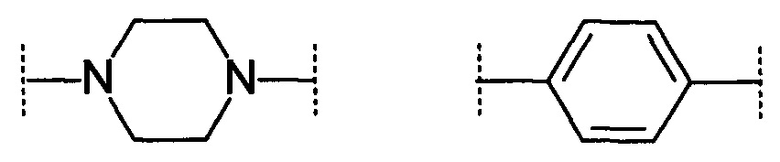
Цепь жирной кислоты может быть получена из жирной кислоты, например, она может быть получена из среднецепочечной жирной кислоты (СЦЖК) с алифатическим хвостом из 6-12 атомов углерода, длинноцепочечной жирной кислоты (ДЦЖК) с алифатическим хвостом из 13-21 атома углерода, или жирной кислоты с очень длинной цепью (ДЦЖК) с алифатическим хвостом из 22 атомов углерода или более. Примеры линейных насыщенных жирных кислот, из которых могут быть получены подходящие цепи жирной кислоты, включают тридециловую (тридекановую) кислоту, миристиновую (тетрадекановую) кислоту, пентадециловую (пентадекановую) кислоту, пальмитиновую (гексадекановую) кислоту и маргариновую (гептадекановую) кислоту. Примеры линейных ненасыщенных жирных кислот, из которых могут быть получены подходящие цепи жирной кислоты, включают миристолеиновую кислоту, пальмитолеиновую кислоту, сапиеновую кислоту и олеиновую кислоту.
Цепь жирной кислоты может быть соединена с Ψ или Z2 с помощью амидной связи, сульфинамидной связи, сульфонамидной связи, или с помощью сложноэфирной связи, или с помощью простой эфирной связи, тиоэфирной или аминной связи. Соответственно, цепь жирной кислоты может содержать связь с Ψ или с Z2 или ацильной (-СО-), сульфинильной (-SO-) или сульфонильной (-SO2-) группой. Предпочтительно цепь жирной кислоты содержит конец, содержащий ацильную (-СО-) группу, и связана с Ψ или Z2 посредством амидной или сложноэфирной связи.
Согласно некоторым вариантам реализации настоящего изобретения Z1 представляет собой группу формулы:
A-B-Alk-X-
в которой
А представляет собой водород или группу карбоновой кислоты, биоизостера карбоновой кислоты, фосфоновой кислоты или сульфоновой кислоты;
В представляет собой связь или линкер;
X представляет собой связь, ацил (-СО-), сульфинил (-SO-) или сульфонил (-SO2-); и
Alk представляет собой цепь жирной кислоты, которая может быть необязательно замещена одним или более заместителями. Цепь жирной кислоты предпочтительно содержит от 6 до 28 атомов углерода в длину (например, С6-28 алкилен), более предпочтительно от 12 до 26 атомов углерода в длину (например, С12-26 алкилен), более предпочтительно от 16 до 22 атомов углерода в длину (например, С16-22 алкилен), и может быть насыщенной или ненасыщенной. Предпочтительно Alk является насыщенным, т.е. предпочтительно Alk представляет собой алкилен.
Необязательные заместители на цепи жирной кислоты могут быть независимо выбраны из фтора, С1-4 алкила, предпочтительно метила; трифторметила, гидроксиметила, амино, гидроксила, С1-4 алкокси, предпочтительно метокси; оксо и карбоксила, и могут быть независимо друг от друга расположены в любой точке вдоль цепи. Согласно некоторым вариантам реализации настоящего изобретения каждый необязательный заместитель выбран из фтора, метила и гидроксила. Если присутствует более одного заместителя, то заместители могут быть одинаковыми или различными. Предпочтительно число заместителей составляет от 0 до 3; более предпочтительно цепь жирной кислоты является незамещенной.
В может представлять собой связь или линкер. В случае если В представляет собой линкер, то он может представлять собой циклоалкилен, гетероциклоалкилен, С6 арил или С5-6 гетероарил, или С6 арилен-О- или С5-6 гетероарилен-O-.
В случае если В представляет собой фенилен, то он может быть выбран, например, из 1,2-фенилена, 1,3-фенилена, 1,4-фенилена, предпочтительно 1,4-фенилена (так что А-В- представляет собой такой заместитель как 4-бензойная кислота или биоизостер 4-бензойной кислоты). В случае если В представляет собой фенилен-О-, он может быть выбран, например, из 1,2-фенилен-О-, 1,3-фенилен-О-, 1,4-фенилен-О-, предпочтительно 1,4-фенилен-О. Каждый фенилен В может быть необязательно замещен одним или более заместителями, выбранными из фтора, метила, трифторметила, амино, гидрокси, С1-4 алкокси, предпочтительно метокси. Следует учитывать, что идентичность и положение заместителей могут быть выбраны так, чтобы незначительно изменить pKa полярной группы. Подходящие индуктивно или мезомерно электроноакцепторные или донорные группы и их позиционные эффекты известны в данной области техники. Согласно некоторым вариантам реализации настоящего изобретения В может представлять собой С5-6 гетероарилен, например, пиридинилен или тиофуранилен, и может быть необязательно замещен, как описано в настоящем документе.
Например, согласно некоторым вариантам реализации настоящего изобретения А-В- может быть выбран из:
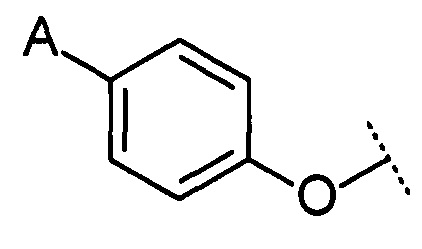 или
или 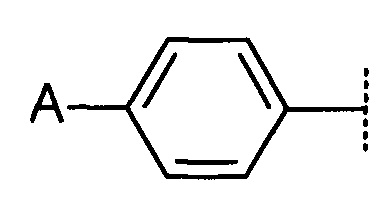 .
.
Предпочтительно А представляет собой Н- или НООС-, и В представляет собой связь.
Следует понимать, что в случае если А представляет собой водород, В представляет собой связь, и Alk обозначает незамещенный алкилен, А-B-Alk- представляет собой алкильную цепь формулы Н3С-(СН2)n-.
Согласно некоторым вариантам реализации настоящего изобретения Z1 представляет собой ацильную группу формулы:
А-В-Alk-(СО)-
или сульфонильную группу формулы:
A-B-Alk-(SO2)-.
Предпочтительно Z1 представляет собой ацильную группу формулы:
А-В-алкилен-(СО)-
в которой А и В соответствуют заместителям, определенным выше.
Согласно некоторым вариантам реализации настоящего изобретения А представляет собой -СООН, и В представляет собой связь. Соответственно, определенные предпочтительные Z1 являются производными длинноцепочечных, насыщенных α,ω-дикарбоновых кислот формулы HOOC-(CH2)12-22-COOH, предпочтительно длинноцепочечных, насыщенных α,ω-дикарбоновых кислот, имеющих четное число атомов углерода в алифатической цепи. Согласно другим вариантам реализации настоящего изобретения А представляет собой Н, и В представляет собой связь. Соответственно, определенные предпочтительные Z1 являются производными длинноцепочечных насыщенных карбоновых кислот формулы НООС-(СН2)12-22-СН3, предпочтительно длинноцепочечных насыщенных карбоновых кислот, содержащих четное число атомов углерода в алифатической цепи.
Например, но не ограничиваясь ими, Z1 может представлять собой:
А-В-С16-20алкилен-(СО)-, в котором А представляет собой Н или -СООН, и В представляет собой связь, например:
17-карбоксигептадеканоил HOOC-(CH2)16-(CO)-;
19-карбоксинонадеканоил HOOC-(CH2)18-(CO)-;
октадеканоил Н3С-(СН2)16-(СО)-;
эйкозаноил Н3С-(СН2)18-(СО)-;
Группа карбоновой кислоты, если она присутствует, может быть заменена биоизостером, как подробно описано в данном документе.
Группа Z2
Z2 представляет собой необязательный спейсер, который соединяет Z1 с боковой цепью аминокислотного компонента Ψ. В наиболее общем случае Z2, если присутствует, представляет собой спейсер, связанный на одном конце с помощью Y, который может представлять собой атом азота, кислорода или серы, и на другом конце с помощью X, который может представлять собой связь или ацил (-СО-), сульфинил (-SO-), сульфонил (-SO2-) или может отсутствовать. Соответственно, Z2, может представлять собой спейсер формулы (--- указывают точки присоединения):
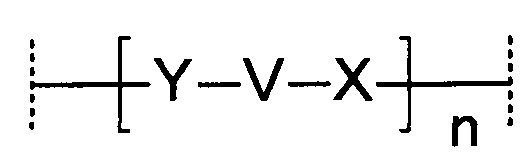
в которой:
Y может представлять собой -NH, -NR, -S или -О, причем R может представлять собой алкил, защитную группу или может образовывать связь с другой частью спейсера, при этом оставшаяся валентность образует связь с Z1;
X может представлять собой связь, СО-, SO- или SO2-, при этом оставшаяся валентность образует связь с боковой цепью аминокислотного компонента Ψ;
V представляет собой двухвалентный органический фрагмент, связывающий Y и X;
и n может быть 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10. Если n равно 2 или более, каждый из Y, V и X не зависит от любого другого Y, V и X.
Соответственно, Z2 может быть связан с каждой стороны с помощью амида, сульфинамида, сульфонамида или сложноэфирных связей, или амино, простой эфирной связи или тиоэфирных связей в зависимости от природы Y и X и соответствующих связывающих групп на Z1 и боковой цепи. Если n равно 2 или более, каждый из V также может быть связан с каждым смежным V с помощью связей, описанных выше. Предпочтительно связи представляют собой амидные связи, сложные эфиры или сульфонамиды, наиболее предпочтительно амиды. Соответственно, согласно некоторым вариантам реализации настоящего изобретения каждый Y представляет собой -NH или -NR, и каждый X представляет собой СО- или SO2-. Наиболее предпочтительно -X- представляет собой ацил (-СО-).
Согласно некоторым вариантам реализации настоящего изобретения Z2 представляет собой спейсер формулы -Sa-, -Sb-, -Sa-Sb- или -Sb-Sa-, причем Sa и Sb соответствуют тем, которые определены ниже.
Согласно некоторым вариантам реализации настоящего изобретения Z2 выбран из -Sa- или -Sb-Sa- то есть, [боковая цепь]-Z2Z1 представляет собой [боковая цепь]-SA-Z1 или [боковая цепь]-SB-SA-Z1.
Группа Sa
Sa может представлять собой один аминокислотный остаток или остаток производного аминокислоты, особенно остаток производного аминокислоты, содержащий сульфинил или сульфонил вместо карбоксильного фрагмента на С-конце. Дополнительно или альтернативно, остаток одной аминокислоты может содержать атом кислорода или серы вместо атома азота на N-конце.
Sa может представлять собой или может содержать азотсодержащий гетероцикл, причем указанный азотсодержащий гетероцикл связан с липофильной группой на одном конце с помощью связи, карбокси, сульфинил или сульфонильной группы, и на другом конце через атом азота кольца. Например, Sa может содержать пиперазиновое кольцо.
Соответственно, Sa представляет собой 5-8-членный гетероцикл, содержащий 1 или 2 атома азота и замещенный группой X, причем X представляет собой связь, СО-, SO- или SO2-, и при этом L, если присутствует, представляет собой С1-4 алкилен (- обозначает точку присоединения в липофильной группе).
Предпочтительно Sa представляет собой 6-членный гетероцикл, содержащий 1 или 2 атома азота, предпочтительно 2, и замещенный группой -СН2СО-, -CH2SO- или -CH2SO2-.
Например, Sa может представлять собой:
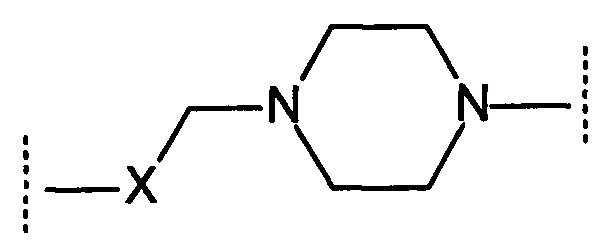 .
.
Например, Sa может представлять собой:
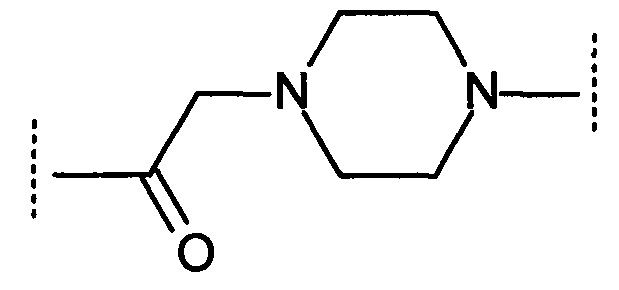
(упоминается в настоящем документе как пиперазин-1-ил-ацетил).
Предпочтительно Sa представляет собой один остаток аминокислоты или пиперазин-1-ил-ацетил. Более предпочтительно Sa представляет собой один остаток аминокислоты.
Согласно некоторым вариантам реализации настоящего изобретения аминокислота может быть выбрана из γ-Glu, α-Glu, α-Asp, β-Asp, Ala, β-Ala (3-аминопропановой кислоты), Dapa (2,3-диаминопропановой кислоты), Dab (2,4-диаминобутановой кислоты), и ГАМК (4-аминобутановой кислоты). Следует понимать, что если присутствует более одного фрагмента карбоновой кислоты или аминогруппы, связь может находиться в любом фрагменте в зависимости от обстоятельств. Любые остатки карбоновой кислоты или аминогруппы, не связанные в пределах остатка, могут быть свободными, т.е. присутствуют в виде свободной карбоновой кислоты или первичного амина, или могут быть дериватизированы. Подходящие способы дериватизации известны в данной области техники. Например, фрагменты карбоновых кислот могут присутствовать в остатках аминокислот Sa в виде сложных эфиров, например, в виде метиловых эфиров. Аминогруппы могут присутствовать в виде алкилированных аминов, например, метилированных аминов, или могут быть защищены в виде амидных или карбаматных фрагментов. Другие подходящие аминокислоты включают β-Ala (3-аминопропановую кислоту) и ГАМК (4-аминобутановую кислоту) и подобные ω-аминокислоты.
Следует понимать, что аминокислоты могут представлять собой D- или L-аминокислоты, или рацемат или смесь энантиомеров. Согласно некоторым вариантам реализации настоящего изобретения аминокислота представляет собой L-аминокислоту. Согласно некоторым вариантам реализации настоящего изобретения аминокислота представляет собой D-аминокислоту.
Согласно некоторым предпочтительным вариантам реализации настоящего изобретения Sa содержит заместитель карбоновой кислоты, такой как γ-Glu, α-Glu, α-Asp, и β-Asp, причем предпочтительными являются их сульфинильные и сульфонильные производные. Соответственно, согласно некоторым вариантам реализации настоящего изобретения остаток аминокислоты представляет собой:
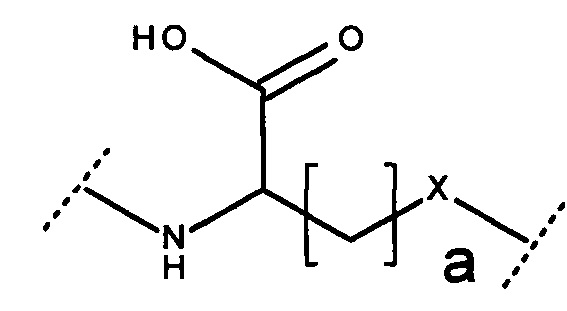 или
или 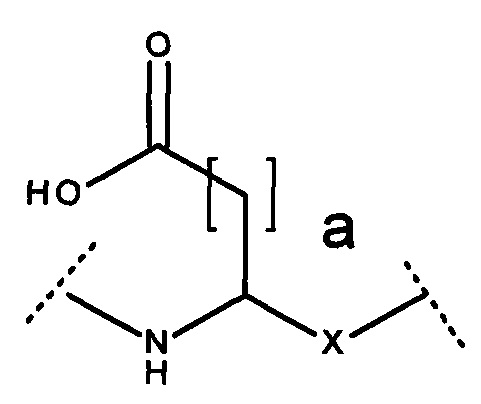
где -Х- представляет собой -СО- -SO-, -SO2-, предпочтительно -СО-, и а равно 1 или 2, предпочтительно 2. Согласно некоторым вариантам реализации настоящего изобретения карбоновая кислота представляет собой сложный эфир, и остаток аминокислоты представляет собой:
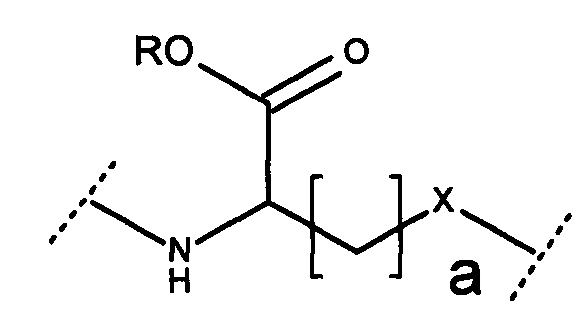 или
или 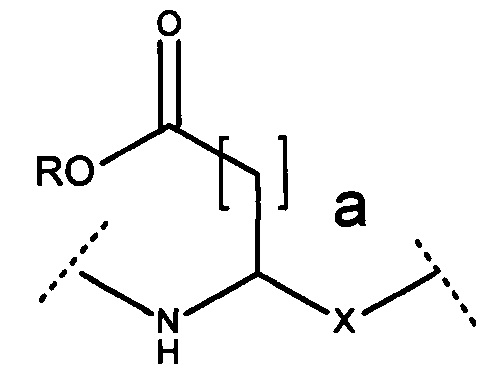
где -Х- представляет собой -СО-, -SO-, -SO2-, предпочтительно -СО-, и а равно 1 или 2, предпочтительно 2, и R представляет собой С1-4 алкил или С6 арил. Предпочтительно R представляет собой С1-4 алкил, предпочтительно метил или этил, более предпочтительно этил.
Предпочтительная группа Sa, содержащая карбоновую кислоту, представляет собой γ-Glu.
Предпочтительно группа Sa выбрана из Dapa или γ-Glu. Наиболее предпочтительно Sa представляет собой γ-Glu.
Группа Sb
Sb может представлять собой линкер общей формулы:
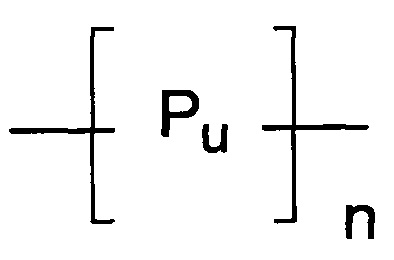
в которой РU представляет собой полимерный блок и n равно 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10. Один конец линкера Sb представляет собой -NH, -NR, -S или -О, при этом R может представлять собой алкил, защитную группу или может образовывать связь с другой частью полимерного блока; в то время как другой конец представляет собой связь или СО-, SO- или SO2-. Соответственно, каждый полимерный блок РU может быть связан с каждой стороны с помощью амидных, сульфинамидных, сульфонамидных или сложноэфирных связей, или с помощью амино, простых эфирных связей или тиоэфирных связей в зависимости от природы Y и X и соответствующих связывающих групп на Z1, SA и Lys.
Согласно некоторым вариантам реализации настоящего изобретения каждый РU может независимо представлять собой блок формулы:
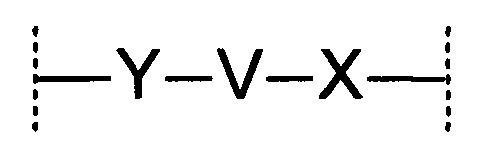
в которой:
Y может представлять собой -NH, -NR, -S или -О, при этом R может представлять собой алкил, защитную группу или может образовывать связь с другой частью линкера, причем оставшаяся валентность образует связь с Z1;
X может представлять собой связь, СО-, SO- или SO2-, причем оставшаяся валентность образует связь с боковой цепью Ψ;
и V представляет собой двухвалентную органическую группу, связывающую Y и X.
Согласно некоторым вариантам реализации настоящего изобретения V представляет собой α-углерод природной или неприродной аминокислоты, то есть V представляет собой CHRAA-, где RAA представляет собой боковую цепь аминокислоты; или V представляет собой необязательно замещенный С1-6 алкилен, или V представляет собой цепь, содержащую один или более последовательных блоков этиленгликоля, также известных как цепь ПЭГ, например, -СН2СН2-(ОСН2СН2)m-O-(СН2)р-, где m равно 0, 1, 2, 3, 4 или 5, и p равно 1, 2, 3, 4 или 5; если X представляет собой СО-, р предпочтительно равно 1, 3, 4 или 5. Необязательные алкиленовые заместители включают фтор, метил, гидрокси, гидроксиметил и амино.
Предпочтительные блоки РU включают:
(i). Одиночные аминокислотные остатки: РUi;
(ii). Дипептидные остатки: РUii; и
(iii). Остатки амино-(ПЭГ)m-карбоновой кислоты: РUiii,
и могут присутствовать в любой комбинации или порядке. Например, SB может содержать один или более любых блоков РUi, РUii и РUiii в любом порядке, или может содержать один или более блоков только РUi, РUii и РUiii, или один или более блоков, выбранных из РUi и РUii, РUi и РUiii, или РUii и РUiii.
(i). Одиночные аминокислотные остатки РUi
Каждый РUi может быть независимо выбран из любого природного или неприродного аминокислотного остатка и, например, может быть выбран из Gly, Pro, Ala, Val, Leu, Ile, Met, Cys, Phe, Tyr, Trp, His, Lys, Arg, Gln, Asn, α-Glu, γ-Glu, Asp, Ser Thr, Dapa, Gaba, Aib, β-Ala, 5-аминопентаноила, 6-аминогексаноила, 7-аминогептаноила, 8-аминооктаноила, 9-аминононаноила и 10-аминодеканоила. Предпочтительно аминокислотные остатки РUi выбраны из Gly, Ser, Ala, Thr и Cys, предпочтительно Gly и Ser.
Согласно некоторым вариантам реализации настоящего изобретения Sb представляет собой -(РUi)n-, где n равно от 1 до 8, более предпочтительно от 5 до 7, наиболее предпочтительно 6. Согласно некоторым предпочтительным вариантам реализации настоящего изобретения Sb представляет собой -(РUi)n-, n равно 6 и каждый из РUi независимо выбран из Gly или Ser, причем предпочтительной последовательностью является -Gly-Ser-Gly-Ser-Gly-Gly-.
(ii). Дипептидные остатки РUii
Каждый блок РUii может быть независимо выбран из любого дипептидного остатка, содержащего два остатка природных или неприродных аминокислот, связанных с помощью амидной связи. Предпочтительные дипептидные остатки РUii включают Gly-Gly, Gly-Ser, Ser-Gly, Gly-Ala, Ala-Gly и Ala-Ala, более предпочтительно Gly-Ser и Gly-Gly.
Согласно некоторым вариантам реализации настоящего изобретения Sb представляет собой -(РUii)n-, где n равно от 2 до 4, более предпочтительно 3, и каждый из РUii независимо выбран из Gly-Ser и Gly-Gly. Согласно некоторым предпочтительным вариантам реализации настоящего изобретения Sb представляет собой -(РUii)n-, n равно 3 и каждый из РUii независимо выбран из Gly-Ser и Gly-Gly, причем предпочтительной последовательностью является -(Gly-Ser)-(Gly-Ser)-(Gly-Gly).
Аминокислоты, имеющие стереогенные центры в пределах РUi и РUii, могут представлять рацемическую смесь, смесь энантиомеров или смесь, содержащую только один тип энантиомеров. Согласно некоторым вариантам реализации настоящего изобретения каждая аминокислота независимо представляет собой L-аминокислоту. Согласно некоторым вариантам реализации настоящего изобретения каждая аминокислота независимо представляет собой D-аминокислоту.
(iii). Остатки РUiii амино-(ПЭГ)m-карбоновой кислоты
Каждый блок РUiii может независимо представлять собой остаток общей формулы:
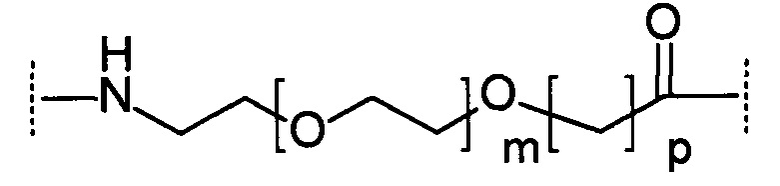
в которой m равно 0, 1, 2, 3, 4 или 5, предпочтительно 1 или 2, и р равно 1, 3, 4 или 5, предпочтительно 1.
Согласно некоторым вариантам реализации настоящего изобретения m равно 1 и р равно 1, то есть РUiii представляет собой остаток 8-амино-3,6-диоксаоктановой кислоты (также известной как {2-[2-аминоэтокси]этокси}уксусная кислота и H2N-PEG3-COOH). Указанный остаток упоминается в настоящем документе как -PEG3-.
Другие более длинные цепи ПЭГ также известны в данной области техники. Например, 11-амино-3,6,9-триоксаундекановая кислота (также известная как H2N-PEG4-COOH или -PEG4-).
Согласно некоторым вариантам реализации настоящего изобретения Sb представляет собой -(РUiii)n-, где n равно от 1 до 3, более предпочтительно 2.
Наиболее предпочтительно Sb представляет собой -PEG3-PEG3-.
Предпочтительные комбинации
Следует понимать, что вышеуказанные предпочтительные варианты можно независимо комбинировать с получением предпочтительных фрагментов -Z1 и -Z2-Z1.
Некоторые предпочтительные фрагменты -Z1 и -Z2-Z1 показаны ниже (в каждом случае - указывает точку присоединения к боковой цепи аминокислотного компонента Ψ):
(i) [17-Карбоксигептадеканоил]-изо-Clu-Peg3-Реg3
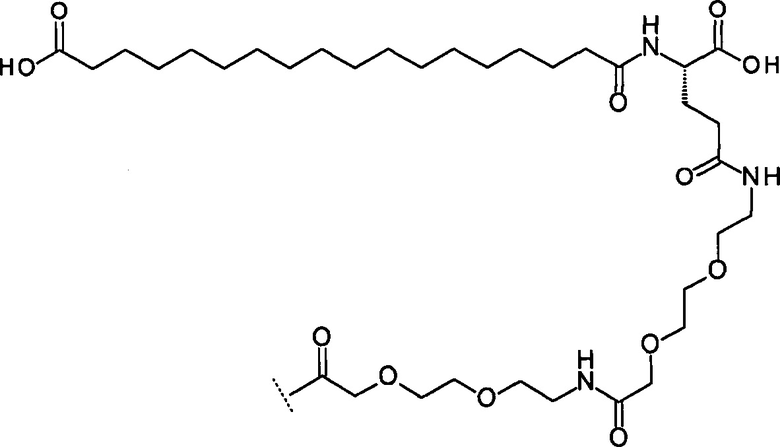
(ii) [17-Карбоксигептадеканоил]-изо-Glu
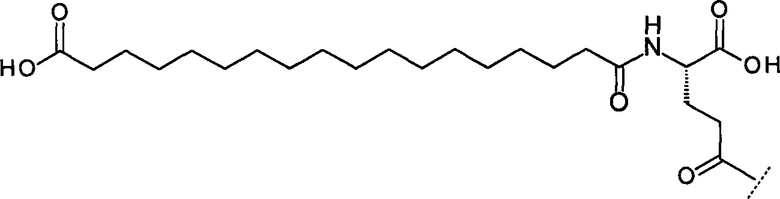
(iii) Октадеканоил-изо-Glu-Peg3-Peg3
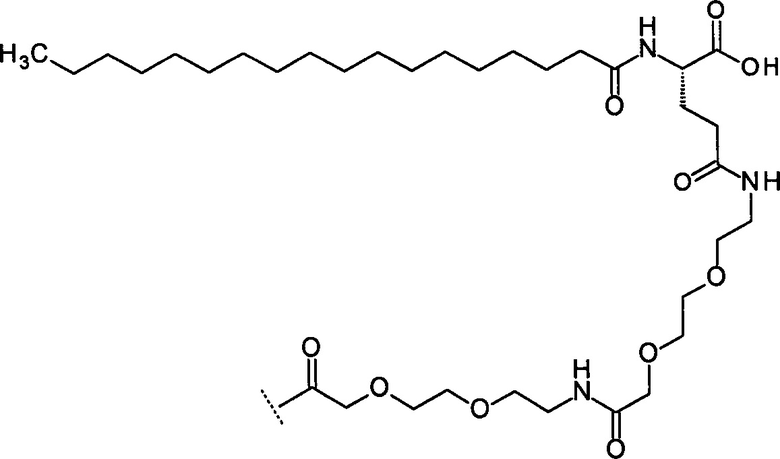
(iv) Эйкозаноил-изо-Glu-Peg3-Peg3
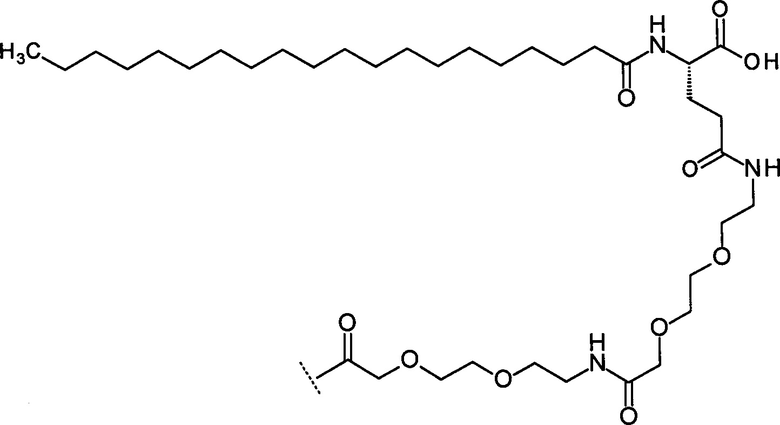
(v) [19-Kapбoкcинoнaдeкaнoил]-изo-Glu-Peg3-Peg3
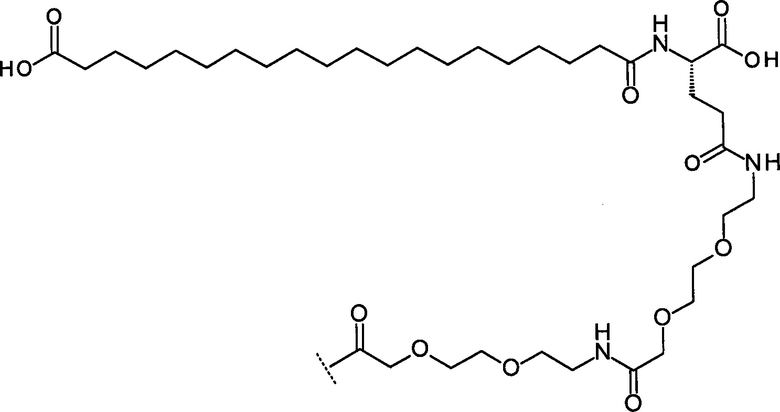
(vi) Октадеканоил-Dapa-Peg3-Peg3
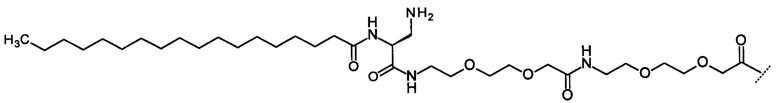
(vii) Гексадеканоил-изо-Glu
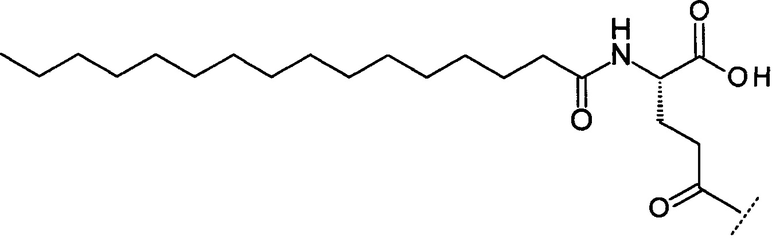
(viii) (19-Карбоксинонадеканоил)-[(пиперазин-1-ил)ацетил]-Peg3-Peg3
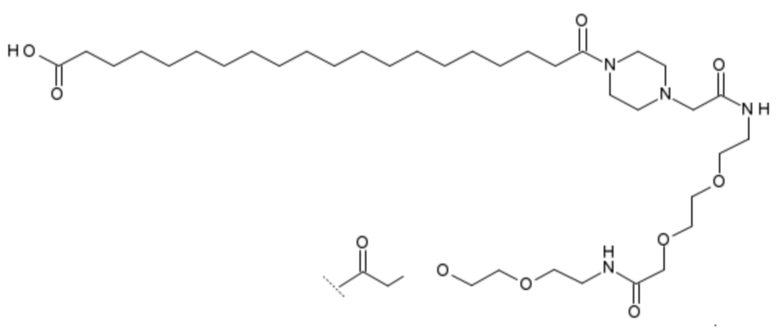
Специалист в данной области техники будет хорошо осведомлено о подходящих способах получения соединений, используемых применительно к настоящему изобретению. Примеры подходящих химических способов описаны, например, в WO 98/08871, WO 00/55184, WO 00/55119, Madsen et al. (J. Med. Chem. 2007, 50, 6126-32) и Knudsen et al. 2000 (J. Med Chem. 43, 1664-1669).
Клиническая применимость
Соединения-аналоги GIP, применительно к настоящему изобретению, могут обеспечить привлекательный способ лечения нарушений обмена веществ (расстройств метаболизма) , включая ожирение, сахарный диабет (различные типы сахарного диабета), расстройств, связанных с ожирением, и расстройств, связанных с диабетом. Соединения- аналоги GIP согласно настоящему изобретению могут быть особенно эффективными в улучшении гликемического контроля и снижении массы тела при введении в комбинации с агонистом рецептора GLP-1 (в виде компонента одного и того же фармацевтического состава или в виде отдельных составов). Агонисты рецептора глюкагоноподобного пептида-1, также известные как агонисты рецептора GLP-1 или миметики инкретинов, являются агонистами рецептора GLP-1. Одним из их преимуществ, по сравнению с более старыми секретагогами инсулина, такими как сульфонилмочевины или меглитиниды, является то, что их применение связано с более низким риском возникновения гипогликемии.
Примеры агонистов GLP-1 включают, но не ограничиваются ими, эксенатид (баета®/бидуреон®), лираглутид (виктоза®), семаглутид, ликсисенатид (ликсумиа®), албиглутид (танзеум®) и таспоглутид.
Диабет включает группу нарушений обмена веществ, характеризующихся гипергликемией, вызванной нарушением секреции инсулина, действия инсулина или обеими причинами. Диабет подразделяется на диабет 1 типа, диабет 2 типа и гестационный диабет на основании патогенных характеристик. Диабет 1 типа составляет 5-10% от всех случаев диабета и вызван аутоиммунным разрушением инсулин-секретирующих панкреатических бета-клеток. Острые симптомы диабета включают чрезмерную выработку мочи и, как следствие, компенсаторную жажду и увеличение потребления жидкости, нечеткость зрения, необъяснимую потерю массы тела, вялость и изменения в энергетическом обмене. Однако симптомы диабета 2 типа часто не тяжелые или могут отсутствовать. Хроническая гипергликемия при диабете связана с длительным повреждением, дисфункцией и недостаточностью различных органов, в частности, глаз, почек, нервов, сердца и кровеносных сосудов.
Сахарный диабет 2 типа составляет 90-95% случаев диабета и развивается в результате сложной комбинации нарушений обмена веществ. Однако симптомы часто не тяжелые или могут отсутствовать. Сахарный диабет 2 типа является следствием сниженной эндогенной выработки инсулина, недостаточной для поддержания уровня глюкозы в плазме крови ниже диагностических порогов.
Гестационный диабет относится к любой степени непереносимости глюкозы, выявленной во время беременности.
Преддиабетические состояния включают нарушенный уровень глюкозы натощак и нарушение толерантности к глюкозе и относятся к тем состояниям, которые возникают, когда уровень глюкозы в крови повышается, но остается ниже уровней, которые установлены для клинического диагноза сахарного диабета.
Большая часть людей с сахарным диабетом 2 типа и преддиабетом подвержены повышенному риску заболеваемости и смертности из-за высокой распространенности дополнительных метаболических факторов риска, включая абдоминальное ожирение (чрезмерное отложение жировой ткани вокруг внутренних органов брюшной полости), атерогенную дислипидемию (расстройства, связанные с уровнями липидов в крови, включая высокий уровень триглицеридов, низкий уровень холестерина-ЛПВП и/или высокий уровень холестерина-ЛПНП, способствующий накоплению бляшек в стенках артерий), повышенное кровяное давление (гипертензию), протромботическое состояние (например, высокий уровень фибриногена или ингибитора активатора плазминогена-1 в крови), и/или провоспалительное состояние (например, повышенный уровень С-реактивного белка в крови).
С другой стороны, ожирение вызывает повышенный риск развития преддиабета, сахарного диабета 2 типа, а также, например, некоторых видов рака, обструктивного апноэ во сне и заболевания желчного пузыря. Дислипидемия связана с повышенным риском развития сердечно-сосудистых заболеваний. Липопротеины (ЛПВП) имеют клиническое значение, поскольку существует обратная корреляция между концентрацией ЛПВП в плазме крови и риском атеросклеротических заболеваний. Большая часть холестерина, депонированного в атеросклеротических бляшках, происходит из ЛПНП и, следовательно, повышение концентрации липопротеинов низкой плотности (ЛПНП) тесно связано с атеросклерозом. Отношение ЛПВП/ЛПНП является клиническим показателем риска развития атеросклероза и, в частности, коронарного атеросклероза.
Аналоги GIP согласно настоящему изобретению могут быть использованы в качестве лекарственных агентов, чтобы предотвратить увеличение массы тела, стимулировать снижение массы тела, уменьшить избыточную массу тела или для лечения ожирения (например, путем контроля аппетита, питания, потребления пищи, потребления калорий и/или расхода энергии и липолиза), включая патологическое ожирение, а также сопутствующие заболевания и патологические состояния, включая, но не ограничиваясь ими, связанное с ожирением воспаление, связанное с ожирением заболевание желчного пузыря и индуцированное ожирением апноэ во сне. Аналоги GIP, применительно к настоящему изобретению, также могут быть использованы для лечения резистентности к инсулину, непереносимости глюкозы, преддиабетических состояний, повышенного уровня глюкозы натощак, сахарного диабета 2 типа, гипертензии, дислипидемии (или комбинации указанных метаболических факторов риска), атеросклероза, артериосклероза, ишемической болезни сердца, заболевания периферических артерий и инсульта. Все из указанных состояний могут быть связаны с ожирением. Однако действие указанных соединений, используемых в соответствии с настоящим изобретением, на указанные состояния может быть опосредовано полностью или частично влиянием на массу тела, или может не зависеть от влияния на массу тела.
Аналоги GIP согласно настоящему изобретению, следовательно, можно применять для лечения и/или предотвращения любых заболеваний, расстройств или состояний, описанных в настоящем документе, включая резистентность к инсулину, непереносимость глюкозы, повышение уровня глюкозы натощак, преддиабет, сахарный диабет 1 типа, сахарный диабет 2 типа, гипертензию при гестационном диабете, дислипидемию или их комбинации. Согласно некоторым вариантам реализации настоящего изобретения расстройства, связанные с диабетом, выбраны из атеросклероза, артериосклероза, ишемической болезни сердца, заболевания периферических артерий и инсульта; или связаны с состоянием, выбранным из атерогенной дислипидемии, расстройств, связанных с уровнем липидов в крови, повышенного кровяного давления, гипертензии, протромботического состояния и провоспалительного состояния или их комбинации. Согласно некоторым вариантам реализации настоящего изобретения расстройство, связанное с уровнем липидов в крови, выбрано из высокого уровня триглицеридов, низкого уровня холестерина-ЛПВП, высокого уровня холестерина-ЛПНП, накопления бляшек в стенках артерий или их комбинации. Согласно некоторым вариантам реализации настоящего изобретения протромботическое состояние выбрано из высоких уровней фибриногена в крови и высокого уровня ингибитора активатора плазминогена-1 в крови. Согласно некоторым вариантам реализации настоящего изобретения провоспалительное состояние представляет собой повышенный уровень С-реактивного белка в крови. Согласно некоторым вариантам реализации настоящего изобретения расстройства, связанные с ожирением, выбраны из воспаления, связанного с ожирением, заболевания желчного пузыря, связанного с ожирением, и индуцированного ожирением апноэ во сне.
Аналоги GIP согласно настоящему изобретению также можно применять для лечения и/или предотвращения любых заболеваний, расстройств или состояний, связанных с остеопорозом, связанным с диабетом, включая повышенный риск переломов костей (Khazai N.B. et al, 2009, Current Opinion in Endocrinology, Diabetes and Obesity, vol. 16, no. 6, 435-445). Увеличение риска переломов, вероятно, связано с нарушением качества костной ткани, а не минеральной плотности костной ткани. Соответствующие механизмы, обусловленные по меньшей мере частично гипергликемией, невропатией, а также более высокой частотой гиповитаминоза D, до сих пор полностью не изучены (Takiishi Т et al, 2010, Endocrinology and Metabolism Clinics of North America, vol. 39, no. 2, 419-446).
Согласно некоторым вариантам реализации в настоящем изобретении предложен терапевтический набор, содержащий аналог GIP (например, соединение-агонист GIP) согласно настоящему изобретению, необязательно в комбинации с фармацевтически приемлемым носителем. Согласно некоторым вариантам реализации в настоящем изобретении предложено устройство, содержащее аналог GIP согласно настоящему изобретению, для доставки аналога GIP субъекту.
Фармацевтические композиции
Аналоги GIP (например, соединения-агонисты GIP) согласно настоящему изобретению, или их соли или сольваты, могут быть изготовлены в виде фармацевтических композиций, приготовленных для хранения или введения, которые, как правило, содержат терапевтически эффективное количество соединения, используемого в соответствии с настоящим изобретением, или его соли или сольвата, в фармацевтически приемлемом носителе. Согласно некоторым вариантам реализации настоящего изобретения фармацевтическая композиция изготовлена в виде жидкости, пригодной для введения путем инъекции или инфузии, или изготовлена так, чтобы вызвать медленное высвобождение аналога GIP.
Терапевтически эффективное количество соединения согласно настоящему изобретению будет зависеть, например, от способа введения, типа млекопитающего, которого лечат, и физических характеристик конкретного исследуемого млекопитающего. Указанные факторы и их взаимосвязь, определяющая указанное количество, хорошо известны квалифицированным специалистам в области медицины. Подходящее количество и способ введения могут быть приспособлены для достижения оптимальной эффективности и могут зависеть от таких факторов, как масса тела, рацион, сопутствующее лекарственное средство, и других факторов, хорошо известных специалистам в области медицины. Дозировки и схема дозирования, наиболее подходящие для использования у человека, могут быть выбраны на основании результатов, полученных с помощью настоящего изобретения, и могут быть подтверждены в правильно спроектированных клинических исследованиях.
Эффективная дозировка и протокол лечения могут быть определены на лабораторных животных с помощью обычных средств, начиная с низкой дозы и постепенно увеличивая дозу, при непрерывном контроле действия, а также путем систематического изменения схемы дозирования. Многочисленные факторы могут быть приняты во внимание клиницистом при определении оптимальной дозы для конкретного субъекта. Соответствующие факторы известны специалистам в данной области техники. Термин «фармацевтически приемлемый носитель» включает любой из стандартных фармацевтических носителей. Фармацевтически приемлемые носители для терапевтического применения хорошо известны в фармацевтической области и описаны, например, в Remington's Pharmaceutical Sciences, Mack Publishing Co. (A.R. Gennaro edit. 1985). Например, может быть использован стерильный физиологический раствор и фосфатно-солевой раствор (ФСБ), имеющий слабокислое или физиологическое значение показателя рН. Подходящие буферные агенты для поддержания рН могут включать, например, фосфат, цитрат, ацетат, лактат, малеат, трис/гидроксиметиламинометан (Tris), N-трис(гидроксиметил)метил-3-аминопропансульфоновую кислоту (TAPS), бикарбонат аммония, диэтаноламин, гистидин, который, согласно некоторым вариантам реализации настоящего изобретения, является предпочтительным буфером, аргинин, лизин или ацетат, или их смеси. Термин также включает любые агенты, перечисленные в фармакопее США для применения у животных, включая применение у человека.
Термин «фармацевтически приемлемая соль» относится к соли соединения. Соли включают фармацевтически приемлемые соли, такие как, например, кислотно-аддитивные соли и основные соли. Примеры кислотно-аддитивных солей включают соли гидрохлорной кислоты, соли лимонной кислоты и соли уксусной кислоты. Примеры основных солей включают соли, в которых катион выбран из щелочных металлов, таких как натрий и калий, щелочноземельных металлов, таких как кальций, и ионов аммония +N(R3)3(R4), где R3 и R4 независимо обозначают необязательно замещенный C1-6 алкил, необязательно замещенный С2-6 алкенил, необязательно замещенный арил или необязательно замещенный гетероарил. Другие примеры фармацевтически приемлемых солей описаны в "Remington's Pharmaceutical Sciences", 17th edition. Ed. Alfonso R. Gennaro (Ed.), Mark Publishing Company, Easton, PA, U.S.A., 1985 и более поздних изданиях, а также в Энциклопедии фармацевтической технологии.
«Лечение» представляет собой подход для получения благоприятных или желаемых клинических результатов. Для целей настоящего изобретения благоприятные или желаемые клинические результаты включают, но не ограничиваются ими, облегчение симптомов, снижение степени тяжести заболевания, стабилизированное (т.е. не ухудшающееся) патологическое состояние, задержку или замедление прогрессирования заболевания, улучшение или временное облегчение патологического состояния и ремиссию (частичную или полную), независимо от того, является она детектируемой или нет. «Лечение» также может означать продление выживаемости по сравнению с ожидаемой выживаемостью, если субъект не получает лечение. «Лечение» представляет собой вмешательство, которое осуществляют для предотвращения развития или изменения патологического течения расстройства. Соответственно, «лечение» относится как к терапевтическому лечению, так и к профилактическим или превентивным мерам согласно некоторым вариантам реализации настоящего изобретения. Субъекты, нуждающиеся в лечении, включают тех, кто уже имеет расстройство, а также тех, у кого нарушение должно быть предотвращено. Лечение подразумевает ингибирование или снижение увеличения патологии или симптомов (например, увеличения массы тела, гипергликемии), по сравнению с отсутствием лечения, и необязательно означает полное устранение соответствующего состояния.
Фармацевтические композиции согласно настоящему изобретению могут быть представлены в виде стандартной лекарственной формы. В указанной форме композиция разделена на единичные дозы, содержащие соответствующие количества активного компонента. Стандартная лекарственная форма может представлять собой упакованный препарат, причем упаковка содержит дискретные количества препаратов, например, упакованные таблетки, капсулы и порошки во флаконах или ампулах. Стандартная лекарственная форма также может представлять собой капсулу, саше или таблетку сама по себе, или может представлять собой соответствующее количество любой из упакованных форм. Композиция может быть обеспечена в виде однократной дозы для инъекции, например, в виде шприца-ручки. Композиции могут быть изготовлены для любого подходящего пути и средства введения. Фармацевтически приемлемые носители или разбавители включают те, которые используют в композициях, подходящих для перорального, ректального, назального или парентерального (включая подкожный, внутримышечный, внутривенный, внутрикожный и чрескожный путь введения) пути введения. Композиции могут быть удобно представлены в стандартной лекарственной форме и могут быть получены любым из способов, хорошо известных в области фармации. Подкожные или трансдермальные способы введения могут быть особенно пригодны для некоторых соединений, описанных в настоящем документе.
Комбинированная терапия
Согласно некоторым вариантам реализации настоящего изобретения аналог GIP, используемый в соответствии с настоящим изобретением, можно вводить как часть комбинированной терапии с по меньшей мере одним другим агентом для лечения диабета, ожирения, дислипидемии или гипертензии.
В таких случаях по меньшей мере два активных агента могут быть введены вместе или по отдельности, и в составе одного и того же фармацевтического состава или в виде отдельных составов. Следовательно, аналог GIP, применяемый в соответствии с настоящим изобретением (или его соль или сольват), может быть использован в комбинации с противодиабетическим агентом, включая, но не ограничиваясь ими, агонист рецептора глюкагоноподобного пептида 1, метформин, сульфонилмочевину, глинид, ингибитор DPP-IV, глитазон или инсулин. Согласно некоторым вариантам реализации настоящего изобретения соединение или его соль или сольват используют в комбинации с инсулином, ингибитором DPP-IV, сульфонилмочевиной или метформином, особенно предпочтительно в комбинации с сульфонилмочевиной или метформином, для достижения надлежащего гликемического контроля. Согласно некоторым предпочтительным вариантам реализации настоящего изобретения соединение или его соль или сольват используют в комбинации с инсулином или аналогом инсулина для достижения надлежащего гликемического контроля. Примеры аналогов инсулина включают, но не ограничиваются ими, лантус® новорапид®, гумалог®, новомикс®, актрафан-НМ®, левемир® и апидра®.
Согласно некоторым вариантам реализации настоящего изобретения аналог GIP или его соль, или сольват могут быть дополнительно использованы в комбинации с одним или более из агентов для лечения ожирения, включая, но не ограничиваясь ими, агонист рецептора глюкагоноподобного пептида 1, пептид YY или его аналог, антагонист рецептора каннабиноидов 1, ингибитор липазы, агонист рецептора меланокортина 4 или антагонист рецептора меланин-концентрирующего гормона 1.
Согласно некоторым вариантам реализации настоящего изобретения аналог GIP или его соль, или сольват могут быть использованы в комбинации с агентом для снижения повышенного кровяного давления, включая, но не ограничиваясь ими, ингибитор ангиотензин-превращающего фермента, блокатор рецепторов ангиотензина II, диуретики, бета-блокаторы или блокатор кальциевых каналов.
Согласно некоторым вариантам реализации настоящего изобретения аналог GIP или его соль могут быть использованы в комбинации с агентом для лечения дислипидемии, включая, но не ограничиваясь ими, статин, фибрат, ниацин и/или ингибитор абсорбции холестерина.
Синтез соединений согласно настоящему изобретению
Молекула нуклеиновой кислоты может кодировать аминокислотную последовательность любого соединения формулы I-III или его предшественника. Кодируемую аминокислотную последовательность можно рассматривать в качестве предшественника соединения согласно настоящему изобретению.
Как правило, в настоящем изобретении указанные последовательности нуклеиновых кислот будут обеспечены в виде конструкций для экспрессии, в которых кодирующая нуклеиновая кислота функционально связана с соответствующими регуляторными последовательностями, чтобы направить экспрессию. Конструкция для экспрессии может быть обеспечена для клетки-хозяина, способной экспрессировать (и, возможно, также секретировать) аминокислотный предшественник, или в виде бесклеточной системы экспрессии.
В настоящем изобретении предложен способ получения аналога GIP согласно настоящему изобретению, причем указанный способ включает экспрессию аминокислотного предшественника аналога GIP и модификацию указанного предшественника так, чтобы обеспечить аналог GIP. Модификация может включать химическую модификацию остатка Lys, Arg или Cys, присутствующего в положении 17, чтобы ввести липофильный фрагмент, модификацию N- или С-конца, и/или модификацию любых других боковых цепей аминокислот в молекуле (например, введение остатка неприродной аминокислоты).
Соединения согласно настоящему изобретению также могут быть изготовлены с помощью стандартных способов синтеза пептидов, например, с помощью стандартных способов твердофазного синтеза или жидкофазного синтеза, путем ступенчатого синтеза или путем сборки фрагментов, и выделения и очистки готового продукта пептидного соединения, или с помощью любых комбинаций рекомбинантных и синтетических способов.
Предпочтительным может быть синтез пептидных соединений согласно настоящему изобретению с помощью твердофазного или жидкофазного синтеза пептидов. Применительно к способам синтеза пептидов см. WO 98/11125, или, среди прочего, Fields, G.B. et al., "Principles and Practice of Solid-Phase Peptide Synthesis"; в: Synthetic Peptides, Gregory A. Grant (ed.), Oxford University Press (2nd edition, 2002), а также примеры синтеза в данном документе.
Примеры
Следующие примеры описывают некоторые варианты реализации настоящего изобретения. Тем не менее, следует понимать, что указанные примеры не являются окончательными в отношении условий и объема настоящего изобретения. Примеры были выполнены с использованием стандартных методик, которые хорошо известны и являются стандартными для специалистов в данной области техники, за исключением иных случаев, подробно описанных в настоящем документе. Следующие примеры представлены исключительно для иллюстративных целей и не должны быть истолкованы никоим образом как ограничивающие объем настоящего изобретения.
В настоящем изобретении раскрыты аналоги GIP, которые проявляют селективность в отношении передачи сигналов, и способы скрининга указанных соединений. Селективность в отношении передачи сигналов может представлять собой, например, предпочтительную активацию пути передачи сигналов или предпочтительное ингибирование пути передачи сигналов, или оба варианта. Аналог, при введении по отдельности или в комбинации с агонистом GLP-1, можно применять для лечения и/или предотвращения заболеваний или состояний, вызванных или характеризующихся избыточной массой тела, включая, но не ограничиваясь ими, ожирение, патологическое ожирение, связанное с ожирением воспаление, связанное с ожирением заболевание желчного пузыря, индуцированное ожирением апноэ во сне, метаболический синдром, преддиабет, резистентность к инсулину, непереносимость глюкозы, сахарный диабет 2 типа, сахарный диабет 1 типа, гипертензию, атерогенную дислипидемию, атеросклероз, артериосклероз, ишемическую болезнь сердца, заболевание периферических артерий и инсульт или микрососудистое заболевание.
В то время как некоторые варианты реализации настоящего изобретения были описаны в качестве иллюстрации, следует понимать, что настоящее изобретение может быть реализовано с использованием множества различных модификаций, изменений и адаптаций, а также с использованием многочисленных эквивалентов или альтернативных решений, которые находятся в пределах квалификации специалистов в данной области техники, не отступая от сущности настоящего изобретения или не выходя за пределы объема формулы изобретения.
Все публикации, патенты и заявки на патенты, упомянутые в настоящем описании, полностью включены в настоящую заявку посредством ссылки в той же степени, как если бы каждая отдельная публикация, патент или заявка на патент были конкретно и индивидуально указаны, как полностью включенные посредством ссылки.
Способы, используемые в настоящем изобретении, описаны ниже, за исключением случаев, когда ясно указано иное.
Пример 1
Общий синтез ацилированных аналогов GIP
Твердофазный пептидный синтез проводили на пептидном синтезаторе СЕМ Liberty Peptide Synthesizer с использованием стандартной Fmoc-реакции. Смолу TentaGel S Ram (1 г; 0,25 ммоль/г) подвергали набуханию в NMP (10 мл) перед использованием и перемещали между трубкой и реакционным сосудом с помощью DCM и NMP.
Связывание
Fmoc-аминокислоту в DMF/DCM (2:1; 0,2 М; 5 мл) добавляли к смоле в микроволновом блоке СЕМ Discover совместно с HATU/DMF или COMU/DMF (0,5 М; 2 мл) и DIPEA-DMF/DCM (2:1) (2,0 М, 1 мл). Смесь для связывания нагревали до 75°С в течение 5 мин, пропуская поток азота через смесь. Затем смолу промывали DMF (4×10 мл).
Снятие защиты
Пиперидин/DMF (20%; 10 мл) добавляли к смоле для первоначального удаления защитной группы, и полученную смесь нагревали с помощью микроволн (30 с; 40°С). Реакционный сосуд осушали, добавляли вторую часть пиперидина/NMP (20% 10 мл) и повторно нагревали (75°С, 3 мин). Затем смолу промывали DMF (6×10 мл).
Ацилирование боковой цепи
Fmoc-Lys(ivDde)-OH или другую аминокислоту с ортогональной защитной группой боковой цепи вводили в положении ацилирования. N-конец пептидного остова затем подвергали Вос-защите с помощью Вос2O или, в другом варианте, с помощью Вос-защищенной аминокислоты на последнем этапе связывания. В то время как пептид оставался связанным со смолой, ортогональную защитную группу боковой цепи селективно отщепляли с помощью свежеприготовленного гидрата гидразина (2-4%) в NMP в течение 2×15 мин. Незащищенную боковую цепь лизина сначала связывали с Fmoc-Glu-OtBu или другой спейсерной аминокислотой, которая была деблокирована с использованием пиперидина и ацилирована липофильным фрагментом с использованием методики связывания пептидов, описанной выше.
Используемые сокращения:
COMU: 1-[(1-(2-цианоэтокси-2-оксоэтилиденаминоокси)диметиламиноморфолинометилен)]метанамин гексафторфосфат
ivDde: 1-(4,4-диметил-2,6-диоксоциклогексилиден)-3-метилбутил
Dde: 1-(4,4-диметил-2,6-диоксоциклогексилиден)этил
DCM: дихлорметан
DMF: N,N-диметилформамид
DIPEA: диизопропилэтиламин
EtOH: этанол
Et2O: диэтиловый эфир
HATU: N-[(диметиламино)-1Н-1,2,3-триазол[4,5-b]пиридин-1-илметилен]-N-метилметанамин гексафторфосфат N-оксид
MeCN: ацетонитрил
NMP: N-метилпирролидон
TFA: трифторуксусная кислота
TIS:триизопропилсилан
Расщепление
Смолу промывали этанолом (3×10 мл) и Et2O (3×10 мл) и высушивали до достижения постоянной массы при комнатной температуре (к.т.). Неочищенный пептид отщепляли от смолы путем обработки TFA/TIS/Н2О (95/2,5/2,5; 40 мл, 2 ч; к.т.). Большую часть TFA удаляли при пониженном давлении, и неочищенный пептид осаждали и промывали три раза диэтиловым эфиром и высушивали до достижения постоянной массы при комнатной температуре.
Очистка неочищенного пептида методом ВЭЖХ
Неочищенный пептид очищали до более чем 90% степени чистоты с помощью препаративной ВЭЖХ с обращенной фазой с использованием PerSeptive Biosystems VISION Workstation, снабженной колонкой С-18 (5 см; 10 мкм) и коллектором фракций, и пептид разделяли на фракции при скорости потока 35 мл/мин с градиентом буфера (0,1% TFA, водн.) и буфера В (0,1% TFA, 90% MeCN, водн.). Фракции исследовали с помощью аналитической ВЭЖХ и МС, и соответствующие фракции объединяли и лиофилизировали. Конечный продукт был охарактеризован с помощью ВЭЖХ и МС. Синтезированные соединения представлены в таблице 1.
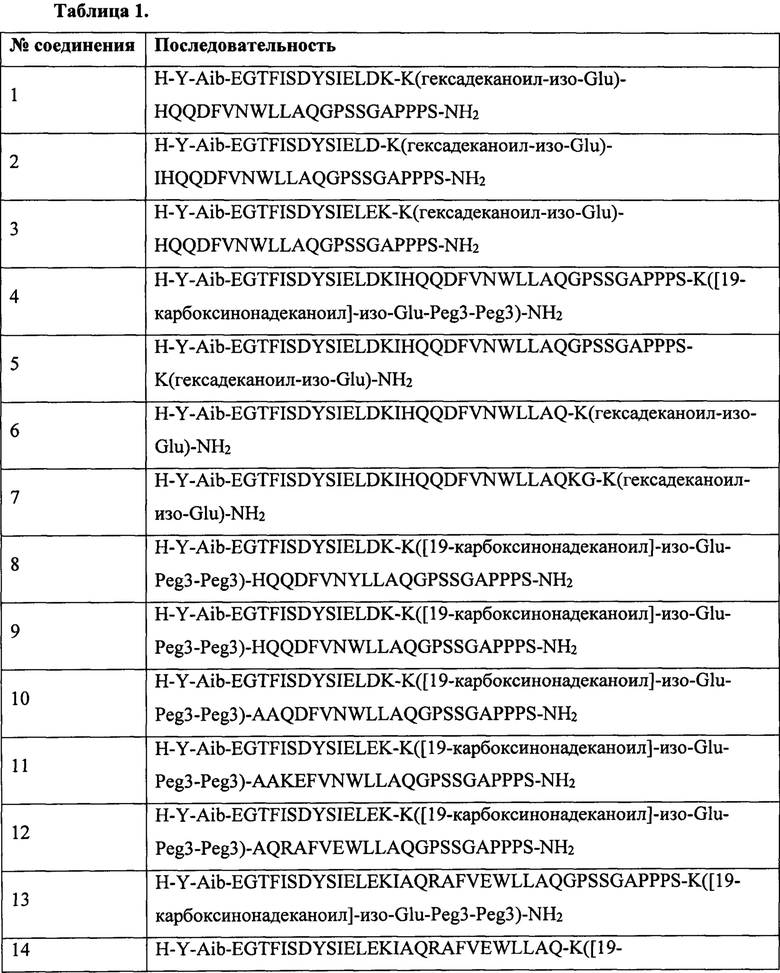
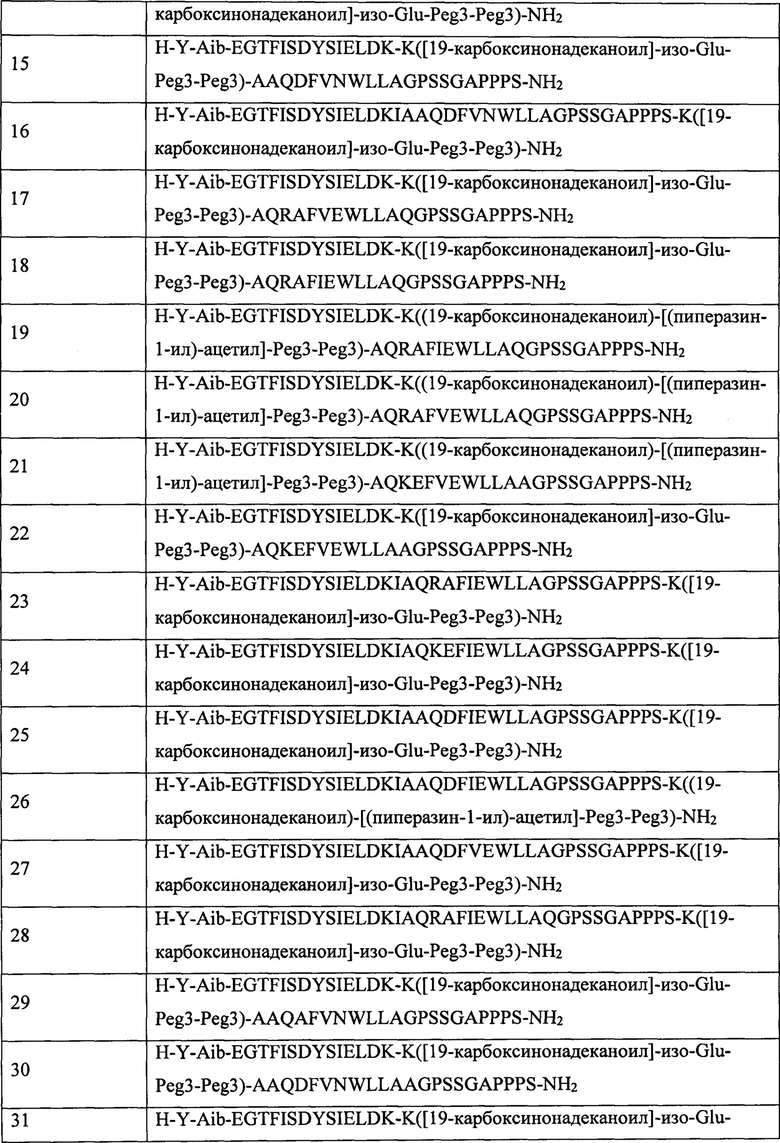

Синтез соединения №9
Твердофазный пептидный синтез проводили на пептидном синтезаторе СЕМ Liberty Peptide Synthesizer с использованием стандартной Fmoc-реакции. Смолу TentaGel S Ram (1,05 г; 0,23 ммоль/г) подвергали набуханию в DMF (10 мл) перед использованием и перемещали между трубкой и реакционным сосудом с помощью DCM и DMF.
Связывание
Fmoc-аминокислоту в DMF/DCM (2:1; 0,2 М; 5 мл) добавляли к смоле в микроволновом блоке СЕМ Discover совместно с COMU/DMF (0,5 М; 2 мл) и DIPEA-DMF/DCM (2:1) (2,0 М, 1 мл). Смесь для связывания нагревали до 75°С в течение 5 мин, пропуская поток азота через смесь. Затем смолу промывали DMF (4×10 мл). Fmoc-Tyr(OtBu)-Ser(Psi Ме,Ме)-ОН псевдопролин использовали для аминокислоты №29 и 30 для связывания с С-конца. Lys 17 встраивали как Fmoc-Lys(Dde)-OH для ортогональной связи. Первые 9 аминокислот и аминокислоту №24 (считая от С-конца) дважды связывали, это означает, что конструируемый блок дважды соединяли перед удалением защитной группы. Boc-Tyr(tBu)-OH встраивали в качестве готового конструируемого блока на N-конце.
Снятие защиты
Пиперидин/DMF (20%; 10 мл) добавляли к смоле для первоначального удаления защитной группы, и полученную смесь нагревали с помощью микроволн (30 с; 40°С). Реакционный сосуд осушали, добавляли вторую часть пиперидина/DMF (20% 10 мл) и повторно нагревали (75°С, 3 мин). Затем смолу промывали DMF (6×10 мл).
Ацилирование боковой цепи
В то время как пептид был связан со смолой, ортогональную защитную группу боковой цепи селективно отщепляли с помощью свежеприготовленного гидрата гидразина (2-4%) в NMP в течение 2×15 мин. Незащищенную боковую цепь лизина сначала связывали с Fmoc-Glu-OtBu и двумя конструируемыми блоками Peg3 с использованием стандартных условий для связывания и снятия защиты, как описано выше. Наконец, липофильный фрагмент встраивали в виде моно-трет-бутилового эфира 19-карбоксинонадекановой кислоты, используя стандартные условия связывания.
Расщепление
Смолу промывали этанолом (3×10 мл) и Et2O (3×10 мл) и высушивали до достижения постоянной массы при комнатной температуре (к.т.). Неочищенный пептид отщепляли от смолы путем обработки TFA/TIS/H2O (95/2,5/2,5; 60 мл, 2 ч; к.т.). Большую часть TFA удаляли при пониженном давлении, и неочищенный пептид осаждали и промывали три раза диэтиловым эфиром и высушивали до достижения постоянной массы при комнатной температуре.
Очистка неочищенного пептида методом ВЭЖХ
Неочищенный пептид сначала очищали до 30% степени чистоты методом препаративной ВЭЖХ с обращенной фазой с использованием насоса Gilson 331 и коллектора фракций Gilson GX281, снабженного колонкой Gemini NX 5 мкм С-18 110А, 10×250 мм, и разделяли на фракции при скорости потока 47 мл/мин с градиентом буфера А (0,1% TFA, водн.) и буфера В (0,1% TFA, 90% MeCN, водн.). Фракции исследовали с помощью аналитической ВЭЖХ и МС, и соответствующие фракции объединяли и лиофилизировали. Вторую очистку проводили с использованием этого же способа, чтобы получить продукт с 96% степенью чистоты (53 мг), согласно результатам определения с помощью ВЭЖХ и МС. Рассчитанная моноизотопная масса 5025,54, установленная масса 5025,72.
Пример 2
Количественное исследование активности рецептора GIP (GIP-R) человека
Действие пептидных конъюгатов согласно настоящему изобретению в условиях in vitro оценивали путем измерения индукции цАМФ после стимуляции соответствующего рецептора GIP или его аналогов, как описано в данном изобретении, с использованием набора AlphaSceen® сАМР от Perkin-Elmer в соответствии с инструкциями. В общих чертах, клетки НЕК293, экспрессирующие GIP-R человека (стабильные клеточные линии, полученные с помощью трансфекции кДНК, кодирующей GIP-R человека, и отбора стабильных клонов) высевали в количестве 30000 клеток/лунку в 96-луночные планшеты для микротитрования, покрытые 0,01% поли-L-лизином, и размножали в течение 1 дня в культуре в 200 мкл среды для размножения (DMEM, 10% ФТС, пенициллин (100 МЕ/мл), стрептомицин (100 мкг/мл)). В день проведения исследования ростовую среду удаляли и клетки промывали один раз с использованием 150 мкл буфера Тирода (соли Тирода (9,6 г/л), 10 мМ HEPES, рН=7,4). Клетки затем инкубировали в 100 мкл буфера для количественного исследования (0,1% масс./об. обработанного щелочью казеина и 100 мкМ IBMX в буфере Тирода), содержащем возрастающие концентрации контрольных и исследуемых соединений в течение 15 мин при 37°С. Буфер для количественного исследования удаляли и клетки лизировали в 80 мкл буфера для лизиса (0,1% масс./об. БСА, 5 мМ HEPES, 0,3% об./об. твин-20) на лунку. Из каждой лунки отбирали по 10 мкл лизированных клеток, переносили в 384-луночный планшет и смешивали с 15 мкл смеси гранул (1 ед./15 мкл анти-цАМФ акцепторных гранул, 1 ед./15 мкл донорных гранул и 1 ед./15 мкл биотинилированного цАМФ в буфере для количественного исследования). Содержимое планшетов перемешивали и инкубировали в темноте в течение часа при комнатной температуре перед измерением с использованием планшет-ридера (Envision™ Perkin-Elmer).
Полученные результаты преобразовывали в концентрации цАМФ с использованием стандартной кривой для цАМФ, полученной в буфере KRBH, содержащем 0,1% (об./об.) ДМСО. Полученные кривые для цАМФ графически представляли в виде зависимости абсолютной концентрации цАМФ (нМ) от логарифма концентрации (концентрации исследуемого соединения) и анализировали с использованием программы для нахождения наилучшей математической модели XLfit.
Параметр, рассчитанный для описания эффективности и агонистической активности каждого исследуемого соединения в отношении рецепторов, представлял собой:
ЭК50, концентрация, которая приводит к полумаксимальному повышению уровней цАМФ, что отражает активность исследуемого соединения. Результаты представлены в таблице 2.
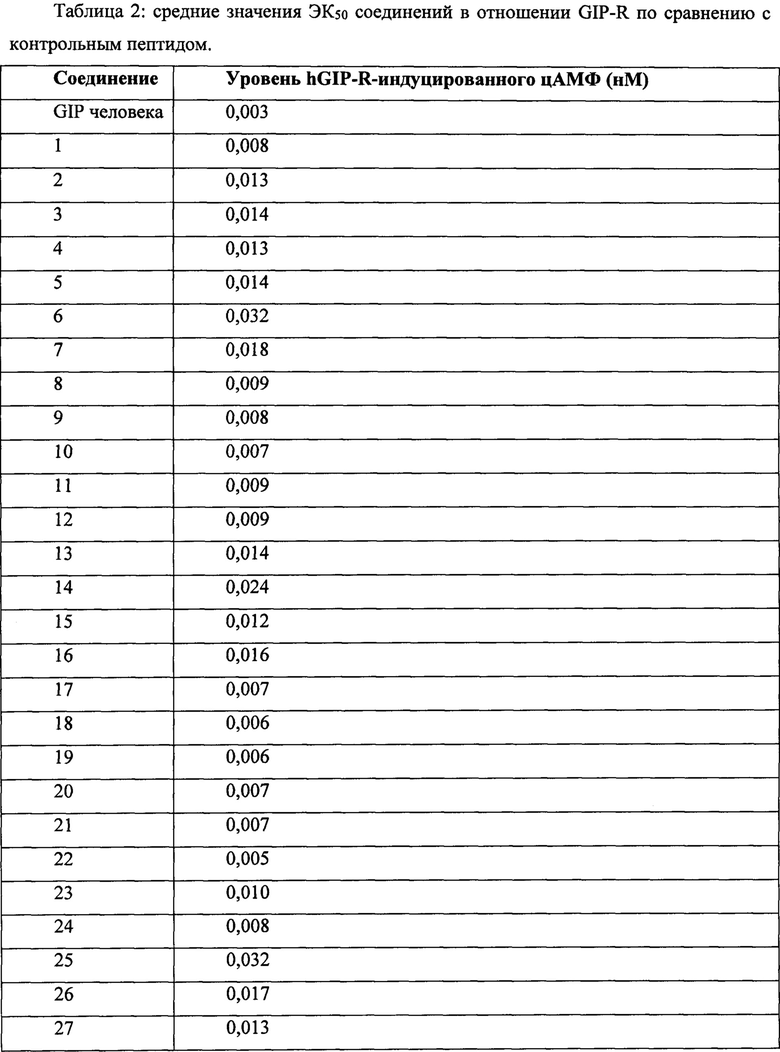
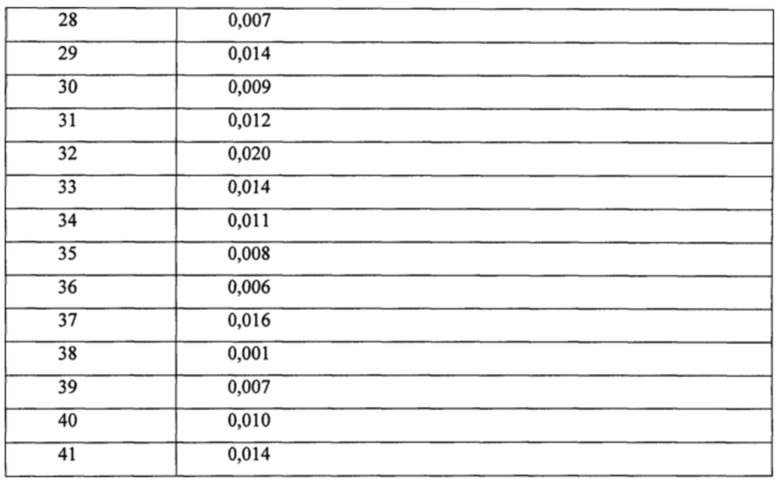
Пример 3
Количественные исследования активности в отношении рецептора GIP (GIP-R) человека и рецептора GLP-1 (GLP-1R) человека
Действие пептидных конъюгатов согласно настоящему изобретению в условиях in vitro оценивали путем измерения индукции цАМФ после стимуляции соответствующего рецептора, используя набор AlphaSceen® сАМР от Perkin-Elmer в соответствии с инструкциями. В общих чертах, клетки НЕК293, экспрессирующие GIP-R человека или GLR-1R (стабильные клеточные линии, полученные с помощью трансфекции вектором экспрессии, содержащим кДНК исследуемого рецептора, и отбора стабильных клонов) высевали в количестве 30000 клеток/лунку в 96-луночные планшеты для микротитрования, покрытые 0,01% поли-L-лизином, и размножали в течение 1 дня в культуре в 200 мкл среды для размножения (DMEM, 10% ФТС, пенициллин (100 МЕ/мл), стрептомицин (100 мкг/мл)). В день проведения количественного исследования ростовую среду удаляли и клетки промывали один раз с использованием 150 мкл буфера Тирода (соли Тирода (9,6 г/л), 10 мМ HEPES, рН=7,4). Клетки затем инкубировали в 100 мкл буфера для количественного исследования (0,05% масс./об. обработанного щелочью казеина и 100 мкМ IBMX в буфере Тирода), содержащем возрастающие концентрации контрольных и исследуемых соединений в течение 15 мин при 37°С. Буфер для количественного исследования удаляли и клетки лизировали в 80 мкл буфера для лизиса (0,1% масс./об. БСА, 5 мМ HEPES, 0,3% об./об. твин-20) на лунку. Из каждой лунки отбирали по 10 мкл лизированных клеток, переносили в 384-луночный планшет и смешивали с 15 мкл смеси гранул (1 ед./15 мкл анти-цАМФ акцепторных гранул, 1 ед./15 мкл донорных гранул и 1 ед./15 мкл биотинилированного цАМФ в буфере для количественного исследования). Содержимое планшетов перемешивали и инкубировали в темноте в течение часа при комнатной температуре перед измерением с использованием планшет-ридера Envision™ (Perkin-Elmer).
Ответ цАМФ нормировали по отношению к положительному и отрицательному контролю (эталонный агонист (0,1 нМ GIP человека или 1 нМ эксендина-4) и буфер для количественного исследования, соответственно), чтобы вычислить ЭК50 и максимальный ответ на основании кривой зависимости ответа от концентрации с использованием 4-параметрической логарифмической (4PL) нелинейной модели регрессии для подбора аппроксимирующей кривой.
Значения ЭК50, концентрации, которая приводит к полумаксимальному повышению уровней цАМФ, что отражает активность исследуемого соединения-агониста, обобщены в таблице 2а.
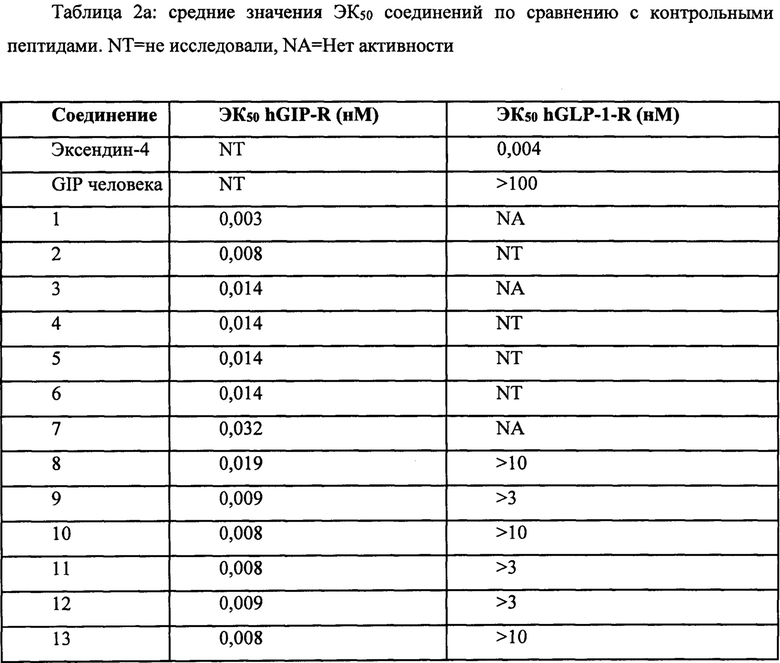
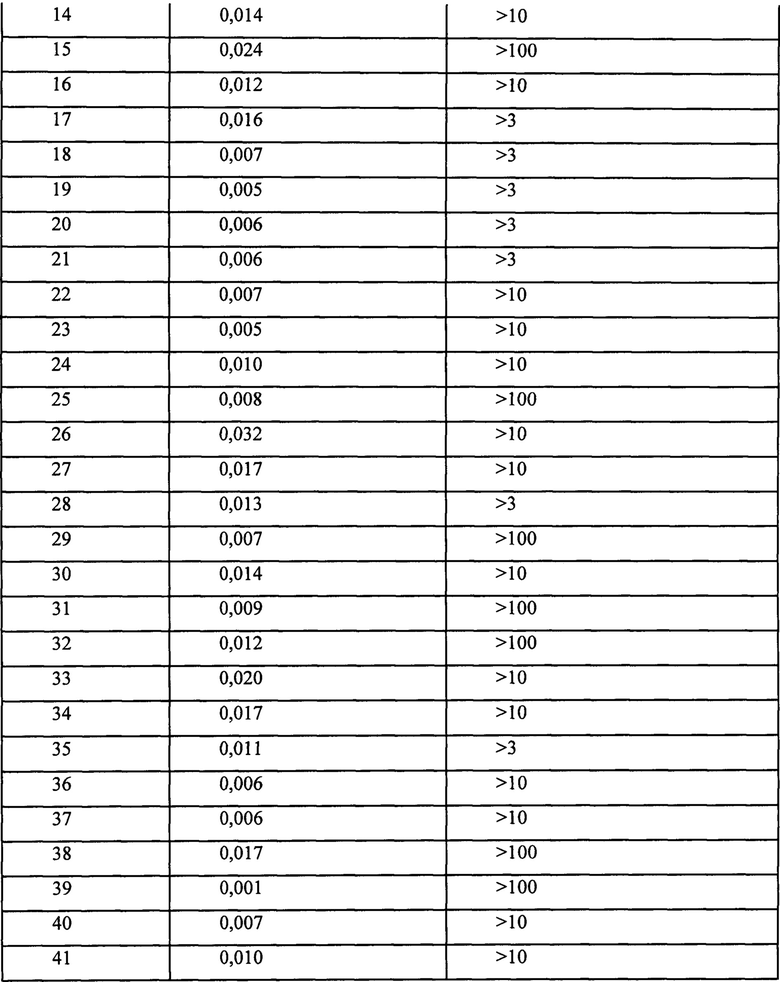
Пример 4
Фармакокинетика выбранных соединений у мышей
Способ
Мышам C57BL/6J (самцы с массой тела приблизительно 25 г) вводили однократно подкожно (п/к) болюсную инъекцию или однократно внутривенно (в/в) болюсную инъекцию каждого исследуемого пептида.
После подкожного введения выбранных соединений (50, 100 или 200 нмоль/кг) отбирали образцы крови в 8 (восьми) временных точках вплоть до 96 часов после введения дозы. После внутривенного введения выбранных соединений (50, 100 или 200 нмоль/кг) отбирали образцы крови в 8 (восьми) временных точках вплоть до 72 часов после введения дозы. Образцы крови отбирали путем сублингвального кровотечения. Носитель представлял собой фосфатный буфер, содержащий маннит (рН=7,5).
В каждой временной точке образцы собирали у двух мышей, т.е. 16 мышей были включены для каждого соединения и каждого пути введения. Мышей умерщвляли с помощью цервикальной дислокации сразу после взятия пробы крови. Образцы плазмы крови исследовали с помощью твердофазной экстракции (SPE) или осаждения белка с последующим исследованием методом жидкостной хроматографии с масс-спектрометрией (ЖХ-МС/МС). Средние концентрации в плазме крови использовали для расчета фармакокинетических параметров с использованием некомпартментного подхода с помощью программного обеспечения Phoenix WinNonlin 6.3. Терминальный период полувыведения из плазмы крови (Т ) определяли как ln(2)/λz, где λz представляет собой величину наклона логарифмической линейной регрессии логарифма концентрации в зависимости от времени в течение терминальной фазы. Биодоступность определяли как AUCinf (s.c.)/AUCinf (i.v.)×100, где AUCinf представляет собой площадь под кривой зависимости концентрации в плазме крови от времени, экстраполированной до бесконечности (AUCinf=AUClast+Clast/λz, где Clast представляет собой последнюю наблюдаемую концентрацию в плазме крови). Тmax представляет собой время после введения дозы, когда наблюдали максимальную концентрацию в плазме крови. Полученные результаты представлены в таблице 3.
) определяли как ln(2)/λz, где λz представляет собой величину наклона логарифмической линейной регрессии логарифма концентрации в зависимости от времени в течение терминальной фазы. Биодоступность определяли как AUCinf (s.c.)/AUCinf (i.v.)×100, где AUCinf представляет собой площадь под кривой зависимости концентрации в плазме крови от времени, экстраполированной до бесконечности (AUCinf=AUClast+Clast/λz, где Clast представляет собой последнюю наблюдаемую концентрацию в плазме крови). Тmax представляет собой время после введения дозы, когда наблюдали максимальную концентрацию в плазме крови. Полученные результаты представлены в таблице 3.
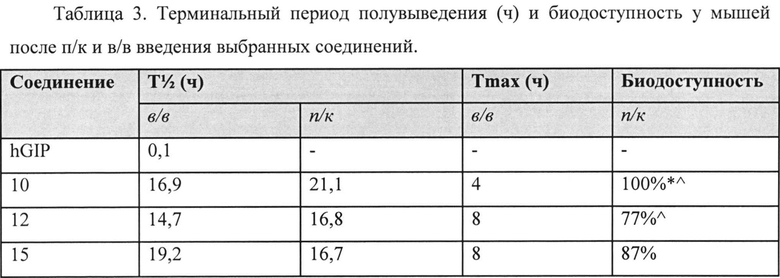
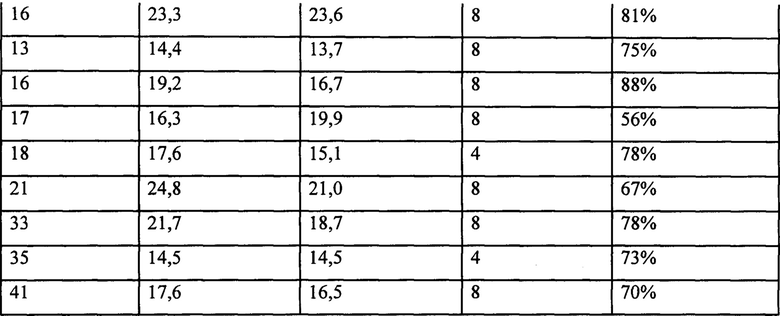
*: Биодоступность была ограничена до 100%.
∧: В повторном исследовании биодоступность соединения 10 составила 77%, а биодоступность соединения 12 составила 98%.
Пример 5
ПТТГ (пероральный тест на толерантность к глюкозе) у нормальных мышей.
Самцы мышей C57BL/6J (Charles River, Германия) получали стандартный корм (Altromin 1324, Brogaarden A/S, Gentofte, Дания) и воду бытового качества с добавлением лимонной кислоты до рН~3,6. Животных содержали в группах по n=3 в комнате с контролируемым световым циклом, температурой и влажностью (12:12 ч цикл свет-темнота, свет включали в 06.00-18.00 ч; 21±1°С; 50-80% относительная влажность). Мышам, в возрасте 10-12 недель, переставали давать корм за 5 часов до ПТТГ. Агонисты рецептора GIP (3-300 нмоль/кг), аналог GLP-1, лираглутид (10 нмоль/кг), и носитель вводили (5 мл/кг) подкожно (п/к) за 4 часа до перорального введения глюкозы через желудочный зонд (t=0 мин; 2 г/кг, 5 мл/кг). Образцы крови собирали из хвостовой вены в момент времени t=0 (перед введением глюкозы), 15, 30, 60 и 120 мин для измерения уровня глюкозы в крови. Результаты (уровень глюкозы в крови и значения площади под кривыми зависимости концентрации глюкозы в крови от времени (AUC). Данные представляют собой средние значения ± SEM, n=6.) 2-х экспериментов представлены на фигуре 1 (А - D) и 2 (А - Е).
Статистический анализ проводили с использованием Graph Pad Prism, версия 5. Значения AUC для концентрации глюкозы в крови сравнивали с использованием однофакторного дисперсионного анализа с последующим применением критерия множественных сравнений Даннетта в сравнении с группой, получавшей носитель. Различия считались статистически значимыми при p<0,05. Статистически значимые различия в сравнении с носителем: *p<0,05, **p<0,01, ***p<0,001.
Пример 6
Действие совместного лечения в течение периода средней длительности с использованием агониста рецептора GIP и агониста рецептора GLP-1 на массу тела у мышей с алиментарным ожирением (DIP) C57BL/6J
В исследовании использовали самцов мышей C57BL/6J (JAX) (Charles River, Великобритания), которые получали корм с высоким содержанием жиров (45% общего объема энергии из жира, D12451 Research Diet Inc.) в течение приблизительно 4 месяцев. Животных содержали в группах по n=3 в комнате с контролируемым световым циклом, температурой и влажностью (12:12 ч цикл свет-темнота, свет включали в 07.00-19.00 ч; 21±2°С; 55±20% относительная влажность). Мышей размещали поодиночке за две недели до начала контрольной фазы. Все мыши получали контрольный носитель (один раз в день подкожно путем инъекции) в течение недели для акклиматизации животных к обработке и инъекциям. Впоследствии, мышей разделяли в соответствии с массой тела в группы лечения (n=8-9). Средняя начальная масса тела составила 39-40 г. Животным затем вводили один раз в день две отдельные подкожные инъекции (каждая инъекция 3 мл/кг) с 1-го по 22-й день. Первая инъекция содержала носитель 1 (буфер на основе 25 мМ фосфата, 125 мМ хлорида натрия, рН=7,4) или аналог GLP-1, лираглутид (20 нмоль/кг). Вторая инъекция содержала носитель 2 (25 мМ фосфата, 205 мМ D-маннита, рН=7,5) или агонист GIP (3 и 30 нмоль/кг). Агонист GIP вводили только каждый третий день исследования (начиная с 1-го дня). В другие дни агонист GIP заменяли носителем 2. Ежедневные инъекции вводили утром (в 9.00-10.00). Массу тела определяли ежедневно на всем протяжении исследования. Изменения массы тела во время исследования представлены на фигуре 3 (дельта Δ = масса тела в каждый день исследования - массу тела в 1-й день. Данные представляют собой средние значения ± SEM).
Статистический анализ проводили с использованием Graph Pad Prism, версия 5. Изменение массы тела мышей, получавших лираглутид, сравнивали с показателями мышей, которым совместно вводили лираглутид и агонист GIP, с использованием двухфакторного дисперсионного анализа с последующим применением теста Бонферрони. Р<0,05 считали статистически значимым. Изменение массы тела у контрольных мышей, получавших носитель, сравнивали с изменениями у мышей, получавших соединение, с использованием двухфакторного дисперсионного анализа с последующим применением теста Бонферрони; ***p<0,001 по сравнению с носителем. Статистические различия в сравнении с носителем на 22-й день представлены на фигуре 3.
Пример 7
Действие совместного лечения в течение периода средней длительности с использованием агонистов рецептора GIP и агониста рецептора GLP-1 на массу тела у мышей с алиментарным ожирением (DIP) C57BL/6J
В исследовании использовали самцов мышей C57BL/6J (JAX) (Charles River, Германия), которые получали корм с высоким содержанием жиров (60% общего объема энергии из жира, DIO Rodent Purified 58Y1 - 58126 от TestDiet) в течение приблизительно 5 месяцев. Животных содержали в группах по n=3 в комнате с контролируемым световым циклом, температурой и влажностью (12:12 ч цикл свет-темнота, свет включали в 06.00-18.00 ч; 21±1°С; 65±15% относительная влажность). Все мыши получали контрольный носитель (один раз в день подкожно путем инъекции) в течение недели для акклиматизации животных к обработке и инъекциям. Впоследствии, мышей разделяли в соответствии с массой тела в группы лечения (n=9). Средняя начальная масса тела составила 40-41 г. Животным затем вводили один раз в день две отдельные подкожные инъекции (каждая инъекция 5 мл/кг) с 0-го по 27-й день. Первая инъекция содержала носитель 1 (буфер на основе 25 мМ фосфата, 125 мМ хлорида натрия, рН=7,4) или аналог GLP-1, лираглутид (20 нмоль/кг). Вторая инъекция содержала носитель 2 (25 мМ фосфата, 205 мМ D-маннита, рН=7,5) или агонист GIP (30 и 300 нмоль/кг). Агонист GIP вводили только каждый третий день исследования (начиная с 0-го дня). В другие дни агонист GIP заменяли носителем 2. Ежедневные инъекции вводили утром (в 9.00-10.00). Массу тела определяли ежедневно на всем протяжении исследования. Изменения массы тела во время исследования (дельта Δ = масса тела в каждый день исследования - массу тела в 0-й день. Данные представляют собой средние значения ± SEM) представлены на фигуре 4А (соединение 10 и 12), В (соединение 17), С (соединение 18), D (соединение 35) и Е (соединение 41).
Статистический анализ проводили с использованием Graph Pad Prism, версия 5. Изменение массы тела мышей, получавших лираглутид, сравнивали с показателями мышей, которым совместно вводили лираглутид и агонист GIP, с использованием двухфакторного дисперсионного анализа с последующим применением теста Бонферрони. Р<0,05 считали статистически значимым (показано с помощью линий ниже кривой изменения массы тела). Изменение массы тела у контрольных мышей, получавших носитель, сравнивали с изменениями у мышей, получавших соединение, с использованием двухфакторного дисперсионного анализа с последующим применением теста Бонферрони; ***p<0,001 по сравнению с носителем. Представлены статистические различия в сравнении с носителем на 27-й день (фигура 4А-Е).
--->
Перечень последовательностей
<110> Zealand Pharma A/S
<120> Соединения-агонисты GIP и способы
<130> GRF/FP7161581
<140> PCT/EP2015/075120
<141> 2015-10-29
<150> DK PA 2014 00629
<151> 2014-10-29
<150> DK PA 2015 00381
<151> 2015-07-04
<160> 89
<170> PatentIn version 3.3
<210> 1
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (17)..(17)
<223> Lys(гексадеканоил-изо-Glu)
<400> 1
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys His Gln Gln Asp Phe Val Asn Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 2
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (16)..(16)
<223> Lys(гексадеканоил-изо-Glu)
<400> 2
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile His Gln Gln Asp Phe Val Asn Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 3
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (17)..(17)
<223> Lys(гексадеканоил-изо-Glu)
<400> 3
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Glu Lys
1 5 10 15
Lys His Gln Gln Asp Phe Val Asn Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 4
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (40)..(40)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 4
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile His Gln Gln Asp Phe Val Asn Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser Lys
35 40
<210> 5
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (40)..(40)
<223> Lys(гексадеканоил-изо-Glu)
<400> 5
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile His Gln Gln Asp Phe Val Asn Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser Lys
35 40
<210> 6
<211> 30
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (30)..(30)
<223> Lys(гексадеканоил-изо-Glu)
<400> 6
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile His Gln Gln Asp Phe Val Asn Trp Leu Leu Ala Gln Lys
20 25 30
<210> 7
<211> 32
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (32)..(32)
<223> Lys(гексадеканоил-изо-Glu)
<400> 7
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile His Gln Gln Asp Phe Val Asn Trp Leu Leu Ala Gln Lys Gly Lys
20 25 30
<210> 8
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (17)..(17)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 8
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys His Gln Gln Asp Phe Val Asn Tyr Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 9
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (17)..(17)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 9
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys His Gln Gln Asp Phe Val Asn Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 10
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (17)..(17)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 10
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Ala Ala Gln Asp Phe Val Asn Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 11
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (17)..(17)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 11
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Glu Lys
1 5 10 15
Lys Ala Ala Lys Glu Phe Val Asn Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 12
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (17)..(17)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 12
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Glu Lys
1 5 10 15
Lys Ala Gln Arg Ala Phe Val Glu Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 13
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (40)..(40)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 13
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Glu Lys
1 5 10 15
Ile Ala Gln Arg Ala Phe Val Glu Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser Lys
35 40
<210> 14
<211> 30
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (30)..(30)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 14
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Glu Lys
1 5 10 15
Ile Ala Gln Arg Ala Phe Val Glu Trp Leu Leu Ala Gln Lys
20 25 30
<210> 15
<211> 38
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (17)..(17)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 15
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Ala Ala Gln Asp Phe Val Asn Trp Leu Leu Ala Gly Pro Ser Ser
20 25 30
Gly Ala Pro Pro Pro Ser
35
<210> 16
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (39)..(39)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 16
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile Ala Ala Gln Asp Phe Val Asn Trp Leu Leu Ala Gly Pro Ser Ser
20 25 30
Gly Ala Pro Pro Pro Ser Lys
35
<210> 17
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (17)..(17)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 17
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Ala Gln Arg Ala Phe Val Glu Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 18
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (17)..(17)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 18
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Ala Gln Arg Ala Phe Ile Glu Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 19
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (17)..(17)
<223> Lys((19-карбоксинонадеканоил)-((пиперазин-1-ил)-ацетил)-Peg3-Peg
3)
<400> 19
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Ala Gln Arg Ala Phe Ile Glu Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 20
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (17)..(17)
<223> Lys((19-карбоксинонадеканоил)-((пиперазин-1-ил)-ацетил)-Peg3-Peg
3)
<400> 20
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Ala Gln Arg Ala Phe Val Glu Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 21
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (17)..(17)
<223> Lys((19-карбоксинонадеканоил)-((пиперазин-1-ил)-ацетил)-Peg3-Peg
3)
<400> 21
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Ala Gln Lys Glu Phe Val Glu Trp Leu Leu Ala Ala Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 22
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (17)..(17)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 22
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Ala Gln Lys Glu Phe Val Glu Trp Leu Leu Ala Ala Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 23
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (39)..(39)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 23
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile Ala Gln Arg Ala Phe Ile Glu Trp Leu Leu Ala Gly Pro Ser Ser
20 25 30
Gly Ala Pro Pro Pro Ser Lys
35
<210> 24
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (39)..(39)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 24
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile Ala Gln Lys Glu Phe Ile Glu Trp Leu Leu Ala Gly Pro Ser Ser
20 25 30
Gly Ala Pro Pro Pro Ser Lys
35
<210> 25
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (39)..(39)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 25
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile Ala Ala Gln Asp Phe Ile Glu Trp Leu Leu Ala Gly Pro Ser Ser
20 25 30
Gly Ala Pro Pro Pro Ser Lys
35
<210> 26
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (39)..(39)
<223> Lys((19-карбоксинонадеканоил)-((пиперазин-1-ил)-ацетил)-Peg3-Peg
3)
<400> 26
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile Ala Ala Gln Asp Phe Ile Glu Trp Leu Leu Ala Gly Pro Ser Ser
20 25 30
Gly Ala Pro Pro Pro Ser Lys
35
<210> 27
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (39)..(39)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 27
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile Ala Ala Gln Asp Phe Val Glu Trp Leu Leu Ala Gly Pro Ser Ser
20 25 30
Gly Ala Pro Pro Pro Ser Lys
35
<210> 28
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (40)..(40)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 28
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile Ala Gln Arg Ala Phe Ile Glu Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser Lys
35 40
<210> 29
<211> 38
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (17)..(17)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 29
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Ala Ala Gln Ala Phe Val Asn Trp Leu Leu Ala Gly Pro Ser Ser
20 25 30
Gly Ala Pro Pro Pro Ser
35
<210> 30
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (17)..(17)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 30
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Ala Ala Gln Asp Phe Val Asn Trp Leu Leu Ala Ala Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 31
<211> 38
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (17)..(17)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 31
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Ala Ala Gln Asp Phe Ile Asn Trp Leu Leu Ala Gly Pro Ser Ser
20 25 30
Gly Ala Pro Pro Pro Ser
35
<210> 32
<211> 38
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (17)..(17)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 32
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Ala Ala Gln Asp Phe Ile Glu Trp Leu Leu Ala Gly Pro Ser Ser
20 25 30
Gly Ala Pro Pro Pro Ser
35
<210> 33
<211> 38
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (17)..(17)
<223> Lys((19-карбоксинонадеканоил)-((пиперазин-1-ил)-ацетил)-Peg3-Peg
3)
<400> 33
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Ala Ala Gln Asp Phe Ile Glu Trp Leu Leu Ala Gly Pro Ser Ser
20 25 30
Gly Ala Pro Pro Pro Ser
35
<210> 34
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (16)..(16)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 34
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile Ala Gln Arg Ala Phe Ile Glu Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 35
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (12)..(12)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 35
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Lys Glu Leu Asp Lys
1 5 10 15
Ile Ala Gln Arg Ala Phe Ile Glu Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 36
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> SITE
<222> (2)..(2)
<223> Xaa представляет собой DAla
<220>
<221> SITE
<222> (17)..(17)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 36
Tyr Xaa Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Ala Gln Arg Ala Phe Ile Glu Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 37
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> SITE
<222> (2)..(2)
<223> Xaa представляет собой DAla
<220>
<221> SITE
<222> (39)..(39)
<223> Lys((19-карбоксинонадеканоил)-((пиперазин-1-ил)-ацетил)-Peg3-Peg
3)
<400> 37
Tyr Xaa Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile Ala Ala Gln Asp Phe Ile Glu Trp Leu Leu Ala Gly Pro Ser Ser
20 25 30
Gly Ala Pro Pro Pro Ser Lys
35
<210> 38
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (17)..(17)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 38
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Ala Ala Gln Asp Phe Ile Glu Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 39
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (17)..(17)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 39
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Ala Ala Gln Asp Phe Ile Asn Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 40
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (17)..(17)
<223> Lys((19-карбоксинонадеканоил)-изо-Glu-Peg3-Peg3)
<400> 40
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Ala Ala Gln Ala Phe Ile Glu Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 41
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> SITE
<222> (17)..(17)
<223> Lys((19-карбоксинонадеканоил)-((пиперазин-1-ил)-ацетил)-Peg3-Peg
3)
<400> 41
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Ala Ala Gln Ala Phe Ile Glu Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 42
<211> 42
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP общей формулы I
<220>
<221> SITE
<222> (1)..(1)
<223> Связанный с R1, причем R1 представляет собой H-, Ac или pGlu
<220>
<221> Вариант
<222> (1)..(42)
<223> Аналог GIP содержит один или только один остаток ?; причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<220>
<221> Вариант
<222> (2)..(2)
<223> Xaa представляет собой Aib, Ala, D-Ala, Gly, Ser, N-Me-Ser, Ac3c, Ac4c или Ac5c
<220>
<221> Вариант
<222> (10)..(10)
<223> Xaa представляет собой Tyr, Leu или Ser
<220>
<221> Вариант
<222> (11)..(11)
<223> Xaa представляет собой Ser или Leu
<220>
<221> Вариант
<222> (12)..(12)
<223> Xaa представляет собой Lys, ? или Ile; причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<220>
<221> Вариант
<222> (15)..(15)
<223> Xaa представляет собой Asp или Glu
<220>
<221> Вариант
<222> (16)..(16)
<223> Xaa представляет собой Ser, Glu, Lys или ?; причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<220>
<221> Вариант
<222> (17)..(17)
<223> Xaa представляет собой Ile, Lys, Gln, Arg или ?; причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<220>
<221> Вариант
<222> (18)..(18)
<223> Xaa представляет собой His, Arg или Ala
<220>
<221> Вариант
<222> (19)..(19)
<223> Xaa представляет собой Gln, Lys, Ala или Glu
<220>
<221> Вариант
<222> (20)..(20)
<223> Xaa представляет собой Gln, Lys, Ala, His или Arg
<220>
<221> Вариант
<222> (21)..(21)
<223> Xaa представляет собой Ala, Leu, Asp или Glu
<220>
<221> Вариант
<222> (23)..(23)
<223> Xaa представляет собой Val или Ile
<220>
<221> Вариант
<222> (24)..(24)
<223> Xaa представляет собой Asn или Glu
<220>
<221> Вариант
<222> (25)..(25)
<223> Xaa представляет собой Tyr или Trp
<220>
<221> Вариант
<222> (27)..(27)
<223> Xaa представляет собой Leu, Glu, Ser, Lys или Val
<220>
<221> Вариант
<222> (28)..(28)
<223> Xaa представляет собой Ala, Ser или Arg
<220>
<221> Вариант
<222> (29)..(29)
<223> Xaa представляет собой Aib, Gly, Ala, Gln, Thr, Ser или Lys, или отсутствует
<220>
<221> Вариант
<222> (30)..(41)
<223> Y1, который может отсутствовать. Если он присутствует, то вплоть до 10 остатков Xaa могут присутствовать или отсутствовать, и Y1 представляет собой Lys-Gly, SEQ ID NO: 43, SEQ ID NO: 44, SEQ ID NO: 45, SEQ ID NO: 46 или SEQ ID NO: 47
<220>
<221> Вариант
<222> (42)..(42)
<223> Xaa представляет собой ? или отсутствует; причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 42
Tyr Xaa Glu Gly Thr Phe Ile Ser Asp Xaa Xaa Xaa Glu Leu Xaa Xaa
1 5 10 15
Xaa Xaa Xaa Xaa Xaa Phe Xaa Xaa Xaa Leu Xaa Xaa Xaa Xaa Xaa Xaa
20 25 30
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
35 40
<210> 43
<211> 10
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность Y1 в SEQ ID NOs: 42, 50, 87 и 89
<400> 43
Gly Pro Ser Ser Gly Ala Pro Pro Pro Ser
1 5 10
<210> 44
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность Y1 в SEQ ID NOs: 42, 48, 50 и 87 - 89
<400> 44
Gly Pro Ser Ser Gly Ala Pro Pro Ser
1 5
<210> 45
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность Y1 в SEQ ID NOs: 42, 48, 50 и 87 - 89
<400> 45
Pro Ser Ser Gly Ala Pro Pro Pro Ser
1 5
<210> 46
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность Y1 в SEQ ID NOs: 42, 48, 50 и 87 - 89
<400> 46
Pro Ser Ser Gly Ala Pro Pro Ser
1 5
<210> 47
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность Y1 в SEQ ID NOs: 42, 48, 50 и 87 - 89
<400> 47
Gly Lys Lys Asn Asp Trp Lys His Asn Ile Thr Gln
1 5 10
<210> 48
<211> 42
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP общей формулы II
<220>
<221> SITE
<222> (1)..(1)
<223> Связанный с R1, причем R1 представляет собой H-, Ac или pGlu
<220>
<221> Вариант
<222> (1)..(42)
<223> Аналог GIP содержит один или только один остаток ?; причем ? представляет собой остаток Lys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<220>
<221> Вариант
<222> (2)..(2)
<223> Xaa представляет собой Aib, Ala, D-Ala, Gly
<220>
<221> Вариант
<222> (12)..(12)
<223> Xaa представляет собой Lys, ? или Ile; причем ? представляет собой остаток Lys, при этом боковая цепь указанного остатка Lys конъюгирована с липофильным заместителем
<220>
<221> Вариант
<222> (15)..(15)
<223> Xaa представляет собой Asp или Glu
<220>
<221> Вариант
<222> (16)..(16)
<223> Xaa представляет собой Ser, Glu, Lys или ?; причем ? представляет собой остаток Lys, при этом боковая цепь указанного остатка Lys конъюгирована с липофильным заместителем
<220>
<221> Вариант
<222> (17)..(17)
<223> Xaa представляет собой Ile, Lys, Gln, Arg или ?; причем ? представляет собой остаток Lys, при этом боковая цепь указанного остатка Lys конъюгирована с липофильным заместителем
<220>
<221> Вариант
<222> (18)..(18)
<223> Xaa представляет собой His, Arg или Ala
<220>
<221> Вариант
<222> (19)..(19)
<223> Xaa представляет собой Gln или Ala
<220>
<221> Вариант
<222> (20)..(20)
<223> Xaa представляет собой Gln, Lys, Ala, His или Arg
<220>
<221> Вариант
<222> (21)..(21)
<223> Xaa представляет собой Ala, Asp или Glu
<220>
<221> Вариант
<222> (23)..(23)
<223> Xaa представляет собой Ile или Val
<220>
<221> Вариант
<222> (24)..(24)
<223> Xaa представляет собой Asn или Glu
<220>
<221> Вариант
<222> (25)..(25)
<223> Xaa представляет собой Tyr или Trp
<220>
<221> Вариант
<222> (27)..(27)
<223> Xaa представляет собой Leu, Glu, Ser, Lys или Val
<220>
<221> Вариант
<222> (28)..(28)
<223> Xaa представляет собой Ala, Ser или Arg
<220>
<221> Вариант
<222> (29)..(29)
<223> Xaa представляет собой Aib, Gly, Ala, Gln, Thr, Ser или Lys, или отсутствует
<220>
<221> Вариант
<222> (30)..(41)
<223> Y1, который может присутствовать. Если Y1 присутсвует, то вплоть до 10 остатков Xaa могут присутствовать или отсутствовать, и Y1 представляет собой Lys-Gly, SEQ ID NO: 44, SEQ ID NO: 45, SEQ ID NO: 46, SEQ ID NO: 47 или SEQ ID NO: 49
<220>
<221> Вариант
<222> (42)..(42)
<223> Xaa представляет собой ? или отсутствует; причем ? представляет собой остаток Lys, при этом боковая цепь указанного остатка Lys конъюгирована с липофильным заместителем
<400> 48
Tyr Xaa Glu Gly Thr Phe Ile Ser Asp Tyr Ser Xaa Glu Leu Xaa Xaa
1 5 10 15
Xaa Xaa Xaa Xaa Xaa Phe Xaa Xaa Xaa Leu Xaa Xaa Xaa Xaa Xaa Xaa
20 25 30
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
35 40
<210> 49
<211> 9
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетическая последовательность Y1 в SEQ ID NOs: 48 и 88
<400> 49
Gly Pro Ser Ser Gly Ala Pro Pro Pro
1 5
<210> 50
<211> 42
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP общей формулы III
<220>
<221> Вариант
<222> (1)..(42)
<223> Аналог GIP содержит один или только один остаток ?; причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<220>
<221> SITE
<222> (1)..(1)
<223> Связанный с R1, причем R1 представляет собой H-, Ac или pGlu
<220>
<221> Вариант
<222> (15)..(15)
<223> Xaa представляет собой Asp или Glu
<220>
<221> Вариант
<222> (16)..(16)
<223> Xaa представляет собой Lys или ?; причем ? представляет собой остаток, который независимо выбран из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<220>
<221> Вариант
<222> (17)..(17)
<223> Xaa представляет собой Ile или ?; причем ? представляет собой остаток, который независимо выбран из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<220>
<221> Вариант
<222> (18)..(18)
<223> Xaa представляет собой His или Ala
<220>
<221> Вариант
<222> (19)..(19)
<223> Xaa представляет собой Gln или Ala
<220>
<221> Вариант
<222> (20)..(20)
<223> Xaa представляет собой Gln, Lys или Arg
<220>
<221> Вариант
<222> (21)..(21)
<223> Xaa представляет собой Ala, Asp или Glu
<220>
<221> Вариант
<222> (24)..(24)
<223> Xaa представляет собой Asn или Glu
<220>
<221> Вариант
<222> (25)..(25)
<223> Xaa представляет собой Tyr или Trp
<220>
<221> Вариант
<222> (29)..(29)
<223> Xaa представляет собой Gln или отсутствует
<220>
<221> Вариант
<222> (30)..(41)
<223> Y1, который может отсутствовать. Если он присутствует, то вплоть до 10 остатков Xaa могут присутствовать или отсутствовать, и Y1 представляет собой Lys-Gly, SEQ ID NO: 43, SEQ ID NO: 44, SEQ ID NO: 45, SEQ ID NO: 46 или SEQ ID NO: 47
<220>
<221> Вариант
<222> (42)..(42)
<223> Xaa представляет собой ? или отсутствует; ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 50
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Xaa Xaa
1 5 10 15
Xaa Xaa Xaa Xaa Xaa Phe Val Xaa Xaa Leu Leu Ala Xaa Xaa Xaa Xaa
20 25 30
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
35 40
<210> 51
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (17)..(17)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 51
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Xaa His Gln Gln Asp Phe Val Asn Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 52
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (16)..(16)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 52
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Xaa
1 5 10 15
Ile His Gln Gln Asp Phe Val Asn Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 53
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (17)..(17)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 53
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Glu Lys
1 5 10 15
Xaa His Gln Gln Asp Phe Val Asn Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 54
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (40)..(40)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 54
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile His Gln Gln Asp Phe Val Asn Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser Xaa
35 40
<210> 55
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (40)..(40)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 55
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile His Gln Gln Asp Phe Val Asn Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser Xaa
35 40
<210> 56
<211> 30
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (30)..(30)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 56
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile His Gln Gln Asp Phe Val Asn Trp Leu Leu Ala Gln Xaa
20 25 30
<210> 57
<211> 32
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (32)..(32)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 57
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile His Gln Gln Asp Phe Val Asn Trp Leu Leu Ala Gln Lys Gly Xaa
20 25 30
<210> 58
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (17)..(17)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 58
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Xaa His Gln Gln Asp Phe Val Asn Tyr Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 59
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (17)..(17)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 59
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Xaa His Gln Gln Asp Phe Val Asn Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 60
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (17)..(17)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 60
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Xaa Ala Ala Gln Asp Phe Val Asn Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 61
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (17)..(17)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 61
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Glu Lys
1 5 10 15
Xaa Ala Ala Lys Glu Phe Val Asn Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 62
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (17)..(17)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 62
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Glu Lys
1 5 10 15
Xaa Ala Gln Arg Ala Phe Val Glu Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 63
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (40)..(40)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 63
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Glu Lys
1 5 10 15
Ile Ala Gln Arg Ala Phe Val Glu Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser Xaa
35 40
<210> 64
<211> 30
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (30)..(30)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 64
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Glu Lys
1 5 10 15
Ile Ala Gln Arg Ala Phe Val Glu Trp Leu Leu Ala Gln Xaa
20 25 30
<210> 65
<211> 38
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (17)..(17)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 65
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Xaa Ala Ala Gln Asp Phe Val Asn Trp Leu Leu Ala Gly Pro Ser Ser
20 25 30
Gly Ala Pro Pro Pro Ser
35
<210> 66
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (39)..(39)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 66
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile Ala Ala Gln Asp Phe Val Asn Trp Leu Leu Ala Gly Pro Ser Ser
20 25 30
Gly Ala Pro Pro Pro Ser Xaa
35
<210> 67
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (18)..(18)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 67
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Xaa Ala Gln Arg Ala Phe Val Glu Trp Leu Leu Ala Gln Gly Pro
20 25 30
Ser Ser Gly Ala Pro Pro Pro Ser
35 40
<210> 68
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (18)..(18)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 68
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Xaa Ala Gln Arg Ala Phe Ile Glu Trp Leu Leu Ala Gln Gly Pro
20 25 30
Ser Ser Gly Ala Pro Pro Pro Ser
35 40
<210> 69
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (40)..(40)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 69
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile Ala Gln Arg Ala Phe Ile Glu Trp Leu Leu Ala Gly Pro Ser Ser
20 25 30
Gly Ala Pro Pro Pro Ser Lys Xaa
35 40
<210> 70
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (40)..(40)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 70
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile Ala Gln Lys Glu Phe Ile Glu Trp Leu Leu Ala Gly Pro Ser Ser
20 25 30
Gly Ala Pro Pro Pro Ser Lys Xaa
35 40
<210> 71
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (40)..(40)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 71
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile Ala Ala Gln Asp Phe Ile Glu Trp Leu Leu Ala Gly Pro Ser Ser
20 25 30
Gly Ala Pro Pro Pro Ser Lys Xaa
35 40
<210> 72
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (40)..(40)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 72
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile Ala Ala Gln Asp Phe Val Glu Trp Leu Leu Ala Gly Pro Ser Ser
20 25 30
Gly Ala Pro Pro Pro Ser Lys Xaa
35 40
<210> 73
<211> 41
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (41)..(41)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 73
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile Ala Gln Arg Ala Phe Ile Glu Trp Leu Leu Ala Gln Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser Lys Xaa
35 40
<210> 74
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (18)..(18)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 74
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Xaa Ala Ala Gln Ala Phe Val Asn Trp Leu Leu Ala Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 75
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (18)..(18)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 75
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Xaa Ala Ala Gln Asp Phe Val Asn Trp Leu Leu Ala Ala Gly Pro
20 25 30
Ser Ser Gly Ala Pro Pro Pro Ser
35 40
<210> 76
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (18)..(18)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 76
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Xaa Ala Ala Gln Asp Phe Ile Asn Trp Leu Leu Ala Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 77
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (18)..(18)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 77
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Xaa Ala Ala Gln Asp Phe Ile Glu Trp Leu Leu Ala Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 78
<211> 39
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (18)..(18)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 78
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Xaa Ala Ala Gln Asp Phe Ile Glu Trp Leu Leu Ala Gly Pro Ser
20 25 30
Ser Gly Ala Pro Pro Pro Ser
35
<210> 79
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (17)..(17)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 79
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Xaa Ile Ala Gln Arg Ala Phe Ile Glu Trp Leu Leu Ala Gln Gly Pro
20 25 30
Ser Ser Gly Ala Pro Pro Pro Ser
35 40
<210> 80
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (13)..(13)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 80
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Lys Xaa Glu Leu Asp
1 5 10 15
Lys Ile Ala Gln Arg Ala Phe Ile Glu Trp Leu Leu Ala Gln Gly Pro
20 25 30
Ser Ser Gly Ala Pro Pro Pro Ser
35 40
<210> 81
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> SITE
<222> (2)..(2)
<223> Xaa представляет собой DAla
<220>
<221> Вариант
<222> (18)..(18)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 81
Tyr Xaa Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Xaa Ala Gln Arg Ala Phe Ile Glu Trp Leu Leu Ala Gln Gly Pro
20 25 30
Ser Ser Gly Ala Pro Pro Pro Ser
35 40
<210> 82
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> SITE
<222> (2)..(2)
<223> Xaa представляет собой DAla
<220>
<221> SITE
<222> (40)..(40)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 82
Tyr Xaa Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Ile Ala Ala Gln Asp Phe Ile Glu Trp Leu Leu Ala Gly Pro Ser Ser
20 25 30
Gly Ala Pro Pro Pro Ser Lys Xaa
35 40
<210> 83
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (18)..(18)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 83
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Xaa Ala Ala Gln Asp Phe Ile Glu Trp Leu Leu Ala Gln Gly Pro
20 25 30
Ser Ser Gly Ala Pro Pro Pro Ser
35 40
<210> 84
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (18)..(18)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 84
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Xaa Ala Ala Gln Asp Phe Ile Asn Trp Leu Leu Ala Gln Gly Pro
20 25 30
Ser Ser Gly Ala Pro Pro Pro Ser
35 40
<210> 85
<211> 40
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP
<220>
<221> MOD_RES
<222> (2)..(2)
<223> Aib
<220>
<221> Вариант
<222> (18)..(18)
<223> Xaa представляет собой ?, причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 85
Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Asp Lys
1 5 10 15
Lys Xaa Ala Ala Gln Ala Phe Ile Glu Trp Leu Leu Ala Gln Gly Pro
20 25 30
Ser Ser Gly Ala Pro Pro Pro Ser
35 40
<210> 86
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический линкер
<400> 86
Gly Ser Gly Ser Gly Gly
1 5
<210> 87
<211> 43
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP общей формулы I
<220>
<221> Вариант
<222> (1)..(1)
<223> Xaa представляет собой H-, Ac или pGlu
<220>
<221> Вариант
<222> (1)..(43)
<223> Аналог GIP содержит один или только один остаток ?; причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<220>
<221> Вариант
<222> (3)..(3)
<223> Xaa представляет собой Aib, Ala, D-Ala, Gly, Ser, N-Me-Ser, Ac3c, Ac4c или Ac5c
<220>
<221> Вариант
<222> (11)..(11)
<223> Xaa представляет собой Tyr, Leu или Ser
<220>
<221> Вариант
<222> (12)..(12)
<223> Xaa представляет собой Ser или Leu
<220>
<221> Вариант
<222> (13)..(13)
<223> Xaa представляет собой Lys, ? или Ile; причем ? представляет собой остаток, который независимо выбран из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<220>
<221> Вариант
<222> (16)..(16)
<223> Xaa представляет собой Asp или Glu
<220>
<221> Вариант
<222> (17)..(17)
<223> Xaa представляет собой Ser, Glu, Lys или ?; причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<220>
<221> Вариант
<222> (18)..(18)
<223> Xaa представляет собой Ile, Lys, Gln, Arg или ?; причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<220>
<221> Вариант
<222> (19)..(19)
<223> Xaa представляет собой His, Arg или Ala
<220>
<221> Вариант
<222> (20)..(20)
<223> Xaa представляет собой Gln, Lys, Ala или Glu
<220>
<221> Вариант
<222> (21)..(21)
<223> Xaa представляет собой Gln, Lys, Ala, His или Arg
<220>
<221> Вариант
<222> (22)..(22)
<223> Xaa представляет собой Ala, Leu, Asp или Glu
<220>
<221> Вариант
<222> (24)..(24)
<223> Xaa представляет собой Val или Ile
<220>
<221> Вариант
<222> (25)..(25)
<223> Xaa представляет собой Asn или Glu
<220>
<221> Вариант
<222> (26)..(26)
<223> Xaa представляет собой Tyr или Trp
<220>
<221> Вариант
<222> (28)..(28)
<223> Xaa представляет собой Leu, Glu, Ser, Lys или Val
<220>
<221> Вариант
<222> (29)..(29)
<223> Xaa представляет собой Ala, Ser или Arg
<220>
<221> Вариант
<222> (30)..(30)
<223> Xaa представляет собой Aib, Gly, Ala, Gln, Thr, Ser или Lys или отсутствует
<220>
<221> Вариант
<222> (31)..(42)
<223> Y1, который может отсутствовать. Если он присутствует, то вплоть до 10 остатков Xaa могут присутствовать или отсутствовать, и Y1 представляет собой Lys-Gly, SEQ ID NO: 43, SEQ ID NO: 44, SEQ ID NO: 45, SEQ ID NO: 46 или SEQ ID NO: 47
<220>
<221> Вариант
<222> (43)..(43)
<223> Xaa представляет собой ? или отсутствует; причем ? представляет собой остаток, который независимо выбран из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 87
Xaa Tyr Xaa Glu Gly Thr Phe Ile Ser Asp Xaa Xaa Xaa Glu Leu Xaa
1 5 10 15
Xaa Xaa Xaa Xaa Xaa Xaa Phe Xaa Xaa Xaa Leu Xaa Xaa Xaa Xaa Xaa
20 25 30
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
35 40
<210> 88
<211> 43
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP общей формулы II
<220>
<221> Вариант
<222> (1)..(1)
<223> Xaa представляет собой H-, Ac или pGlu
<220>
<221> Вариант
<222> (1)..(43)
<223> Аналог GIP содержит один или только один остаток ?; причем ? представляет собой остаток Lys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<220>
<221> Вариант
<222> (3)..(3)
<223> Xaa представляет собой Aib, Ala, D-Ala, Gly
<220>
<221> Вариант
<222> (13)..(13)
<223> Xaa представляет собой Lys, ? или Ile; причем ? представляет собой остаток Lys, при этом боковая цепь указанного остатка Lys конъюгирована с липофильным заместителем
<220>
<221> Вариант
<222> (16)..(16)
<223> Xaa представляет собой Asp или Glu
<220>
<221> Вариант
<222> (17)..(17)
<223> Xaa представляет собой Ser, Glu, Lys или ?; причем ? представляет собой остаток Lys, при этом боковая цепь указанного остатка Lys конъюгирована с липофильным заместителем
<220>
<221> Вариант
<222> (18)..(18)
<223> Xaa представляет собой Ile, Lys, Gln, Arg или ?; причем ? представляет собой остаток Lys, при этом боковая цепь указанного остатка Lys конъюгирована с липофильным заместителем
<220>
<221> Вариант
<222> (19)..(19)
<223> Xaa представляет собой His, Arg или Ala
<220>
<221> Вариант
<222> (20)..(20)
<223> Xaa представляет собой Gln или Ala
<220>
<221> Вариант
<222> (21)..(21)
<223> Xaa представляет собой Gln, Lys, Ala, His или Arg
<220>
<221> Вариант
<222> (22)..(22)
<223> Xaa представляет собой Ala, Asp или Glu
<220>
<221> Вариант
<222> (24)..(24)
<223> Xaa представляет собой Ile или Val
<220>
<221> Вариант
<222> (25)..(25)
<223> Xaa представляет собой Asn или Glu
<220>
<221> Вариант
<222> (26)..(26)
<223> Xaa представляет собой Tyr или Trp
<220>
<221> Вариант
<222> (28)..(28)
<223> Xaa представляет собой Leu, Glu, Ser, Lys или Val
<220>
<221> Вариант
<222> (29)..(29)
<223> Xaa представляет собой Ala, Ser или Arg
<220>
<221> Вариант
<222> (30)..(30)
<223> Xaa представляет собой Aib, Gly, Ala, Gln, Thr, Ser или Lys, или отсутствует
<220>
<221> Вариант
<222> (31)..(42)
<223> Y1, который может отсутствовать. Если он присутствует, то вплоть до 10 остатков Xaa могут присутствовать или отсутствовать, и Y1 представляет собой Lys-Gly, SEQ ID NO: 44, SEQ ID NO: 45, SEQ ID NO: 46, SEQ ID NO: 47 или SEQ ID NO: 49
<220>
<221> Вариант
<222> (43)..(43)
<223> Xaa представляет собой ? или отсутствует; причем ? представляет собой остаток Lys, при этом боковая цепь указанного остатка Lys конъюгирована с липофильным заместителем
<400> 88
Xaa Tyr Xaa Glu Gly Thr Phe Ile Ser Asp Tyr Ser Xaa Glu Leu Xaa
1 5 10 15
Xaa Xaa Xaa Xaa Xaa Xaa Phe Xaa Xaa Xaa Leu Xaa Xaa Xaa Xaa Xaa
20 25 30
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
35 40
<210> 89
<211> 43
<212> Белок
<213> Искусственная последовательность
<220>
<223> Синтетический аналог GIP общей формулы III
<220>
<221> Вариант
<222> (1)..(1)
<223> Xaa представляет собой H-, Ac или pGlu
<220>
<221> Вариант
<222> (1)..(43)
<223> Аналог GIP содержит один или только один остаток ?; причем ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<220>
<221> Вариант
<222> (16)..(16)
<223> Xaa представляет собой Asp или Glu
<220>
<221> Вариант
<222> (17)..(17)
<223> Xaa представляет собой Lys или ?; причем ? представляет собой остаток, который независимо выбран из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<220>
<221> Вариант
<222> (18)..(18)
<223> Xaa представляет собой Ile или ?; причем ? представляет собой остаток, который независимо выбран из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<220>
<221> Вариант
<222> (19)..(19)
<223> Xaa представляет собой His или Ala
<220>
<221> Вариант
<222> (20)..(20)
<223> Xaa представляет собой Gln или Ala
<220>
<221> Вариант
<222> (21)..(21)
<223> Xaa представляет собой Gln, Lys или Arg
<220>
<221> Вариант
<222> (22)..(22)
<223> Xaa представляет собой Ala, Asp или Glu
<220>
<221> Вариант
<222> (25)..(25)
<223> Xaa представляет собой Asn или Glu
<220>
<221> Вариант
<222> (26)..(26)
<223> Xaa представляет собой Tyr или Trp
<220>
<221> Вариант
<222> (30)..(30)
<223> Xaa представляет собой Gln или отсутствует
<220>
<221> Вариант
<222> (31)..(42)
<223> Y1, который может отсутствовать. Если он присутствует, то вплоть до 10 остатков Xaa могут присутствовать или отсутствовать, и Y1 представляет собой Lys-Gly, SEQ ID NO: 43, SEQ ID NO: 44, SEQ ID NO: 45, SEQ ID NO: 46 или SEQ ID NO: 47
<220>
<221> Вариант
<222> (43)..(43)
<223> Xaa представляет собой ? или отсутствует; ? представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем
<400> 89
Xaa Tyr Ala Glu Gly Thr Phe Ile Ser Asp Tyr Ser Ile Glu Leu Xaa
1 5 10 15
Xaa Xaa Xaa Xaa Xaa Xaa Phe Val Xaa Xaa Leu Leu Ala Xaa Xaa Xaa
20 25 30
Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa Xaa
35 40
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| МУЛЬТИАГОНИСТЫ И ИХ ПРИМЕНЕНИЕ | 2022 |
|
RU2833609C2 |
| УЛУЧШЕННЫЕ ПЕПТИДНЫЕ ЛЕКАРСТВЕННЫЕ СРЕДСТВА ДЛЯ ЛЕЧЕНИЯ NASH И ДРУГИХ РАССТРОЙСТВ | 2019 |
|
RU2790209C2 |
| АЦИЛИРОВАННЫЕ ДВОЙНЫЕ АГОНИСТЫ GLP-1/GLP-2 | 2017 |
|
RU2753193C2 |
| ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ КОНЪЮГАТА ТРОЙНОГО АГОНИСТА ДЛИТЕЛЬНОГО ДЕЙСТВИЯ, ОБЛАДАЮЩЕГО АКТИВНОСТЯМИ В ОТНОШЕНИИ ВСЕХ ИЗ РЕЦЕПТОРОВ ГЛЮКАГОНА /GLP-1/GIP, ДЛЯ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЯ ЛЕГКОГО | 2020 |
|
RU2829342C1 |
| Модифицированные аналоги GIP пептида | 2019 |
|
RU2817673C2 |
| ПОЛИПЕПТИДЫ АНАЛОГА АМИЛИНА ЧЕЛОВЕКА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2839688C2 |
| МУЛЬТИРЕЦЕПТОРНЫЙ АГОНИСТ И ЕГО МЕДИЦИНСКОЕ ПРИМЕНЕНИЕ | 2020 |
|
RU2816492C2 |
| КОНСТРУКЦИИ, ИМЕЮЩИЕ SIRP-АЛЬФА ДОМЕН ИЛИ ЕГО ВАРИАНТ | 2016 |
|
RU2740672C2 |
| АНТИТЕЛО, СПЕЦИФИЧНО СВЯЗЫВАЮЩЕЕСЯ С ICAM-1, И ЕГО ПРИМЕНЕНИЕ | 2019 |
|
RU2789757C2 |
| ПЕПТИДНЫЙ АНАЛОГ АЦИЛИРОВАННОГО ОКСИНТОМОДУЛИНА | 2018 |
|
RU2752787C1 |
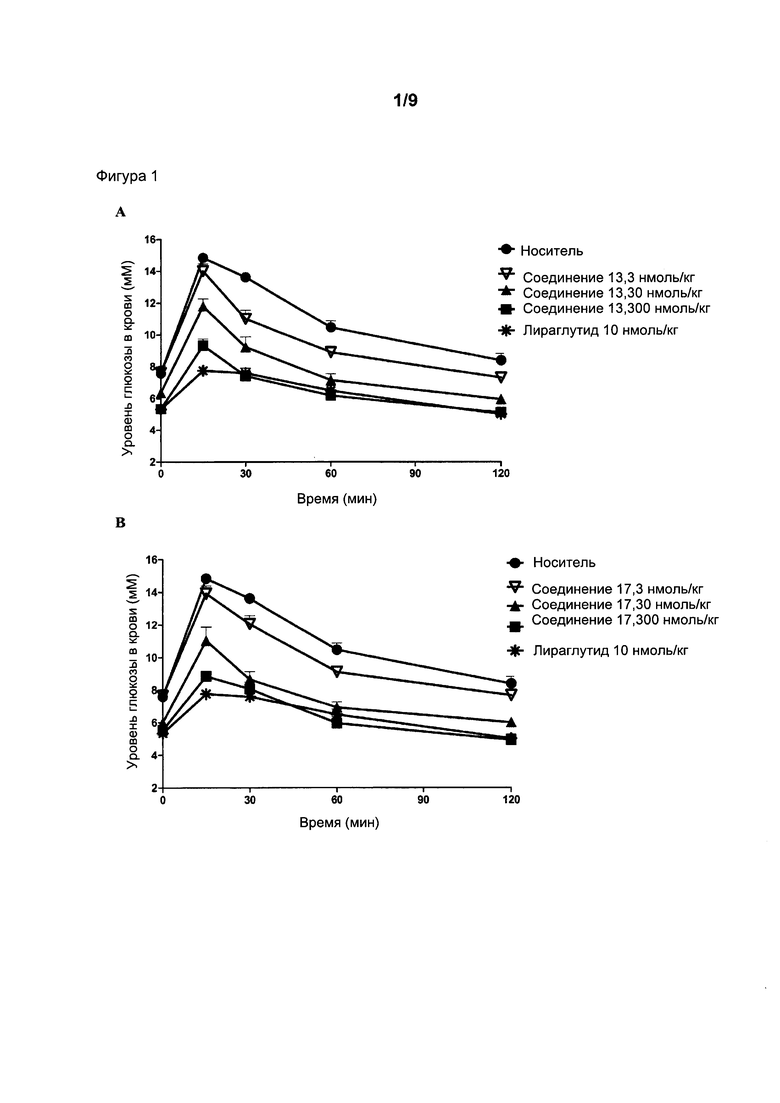
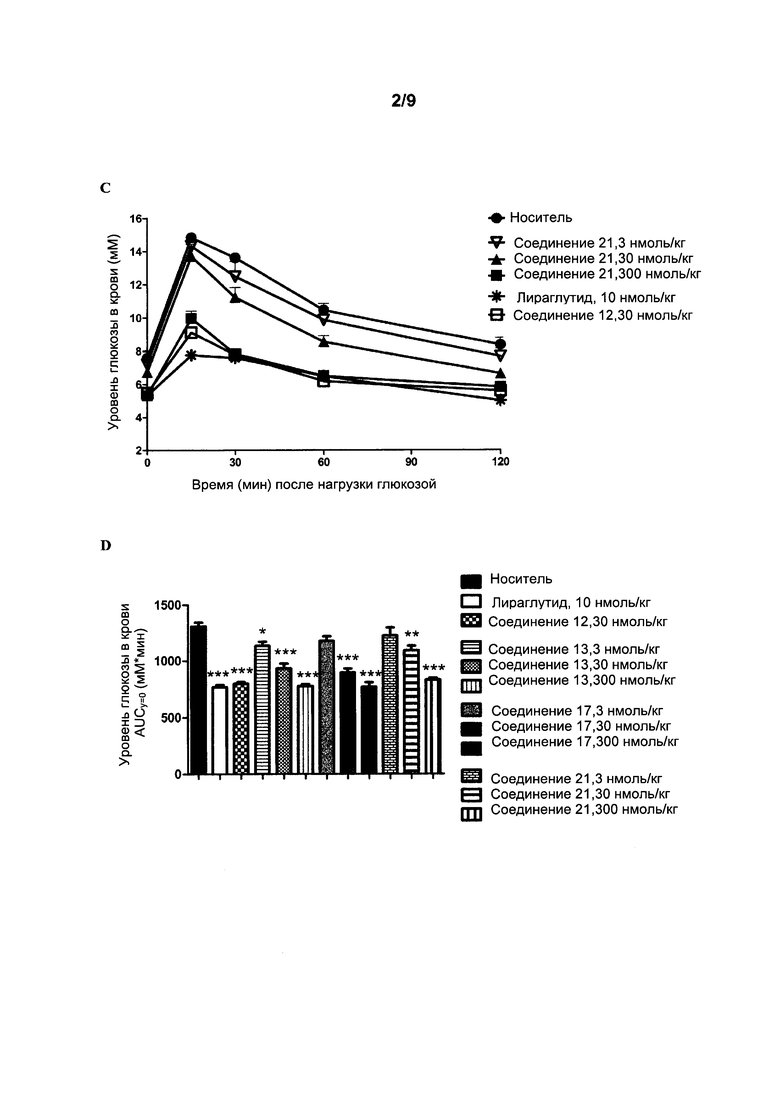
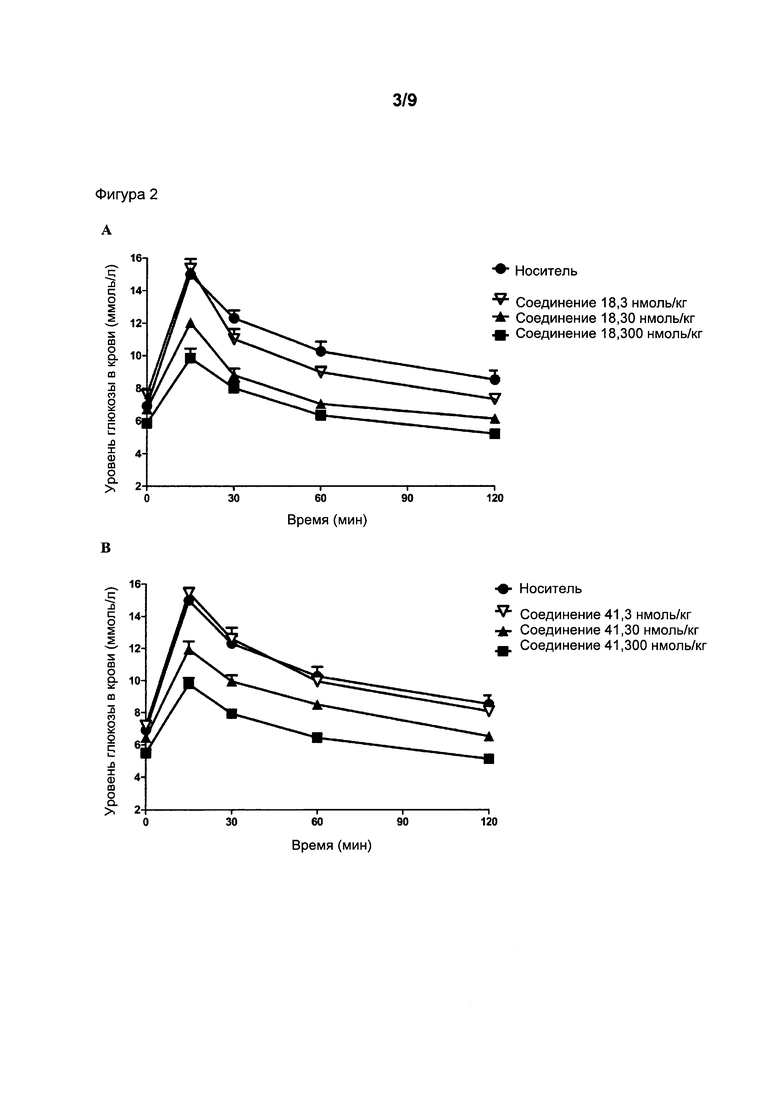
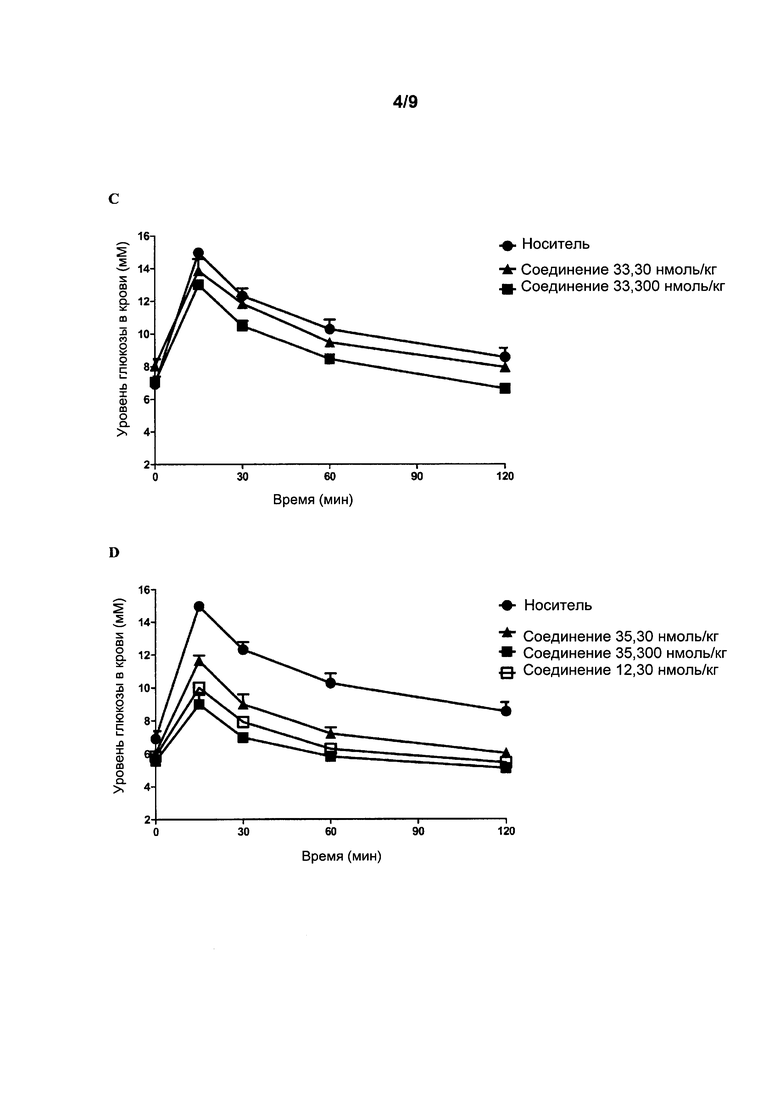
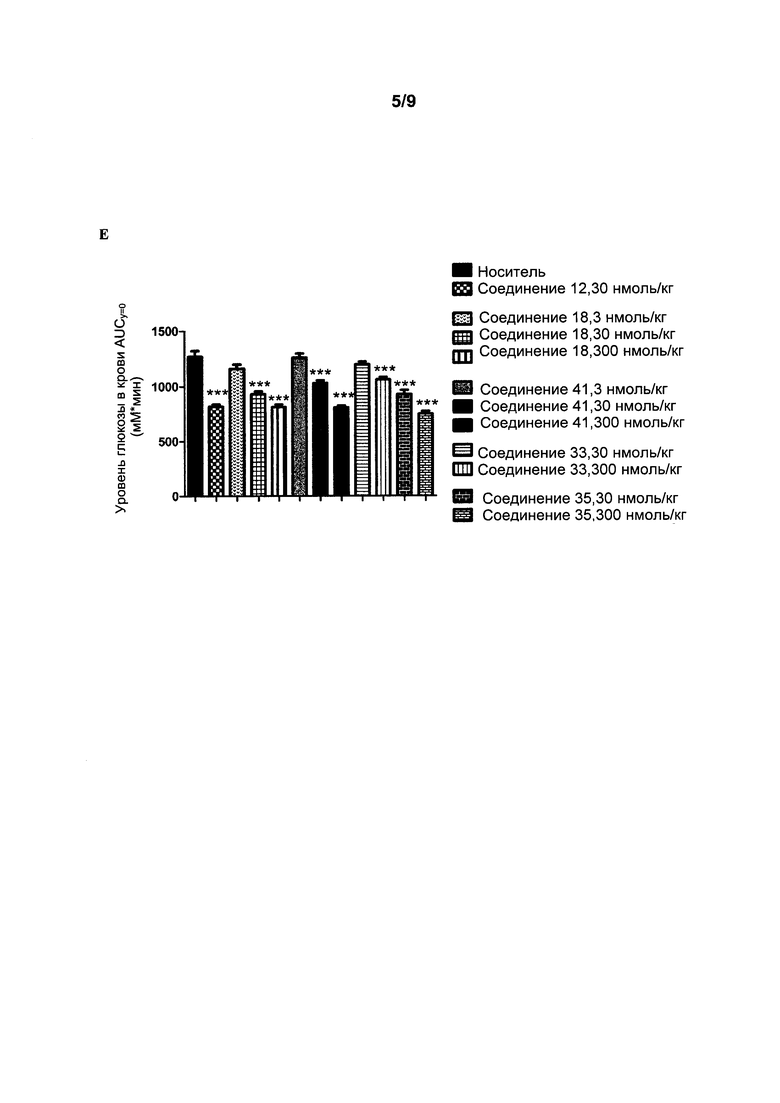
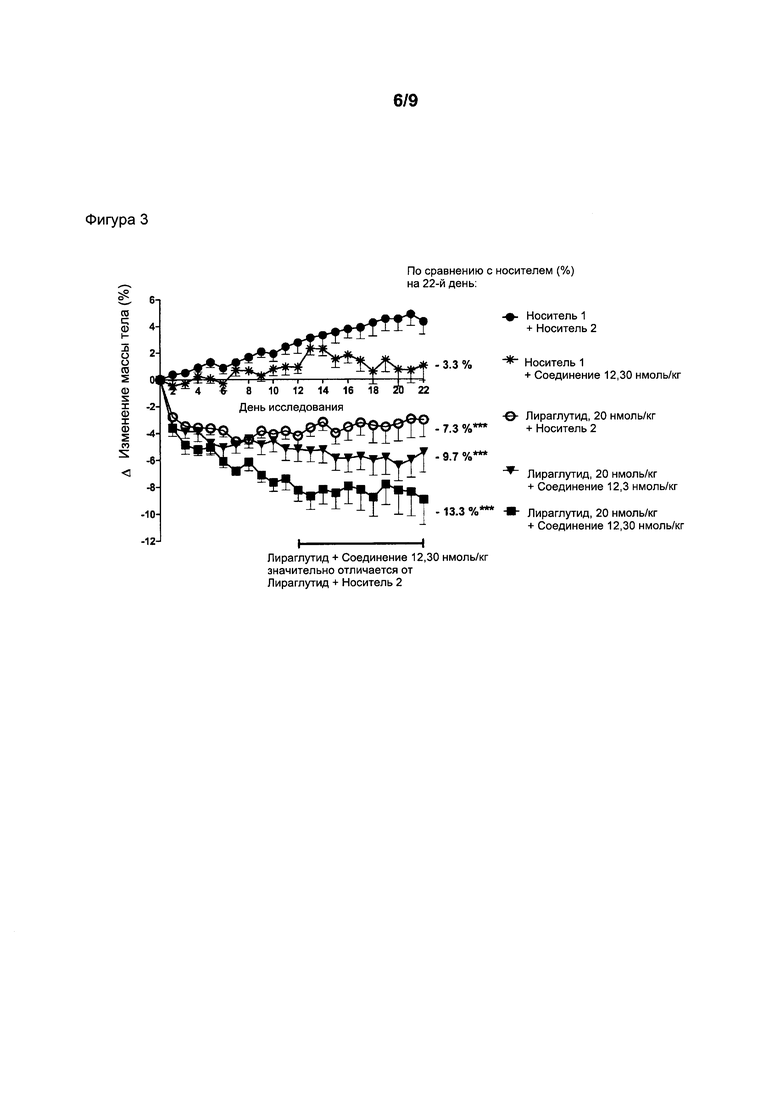
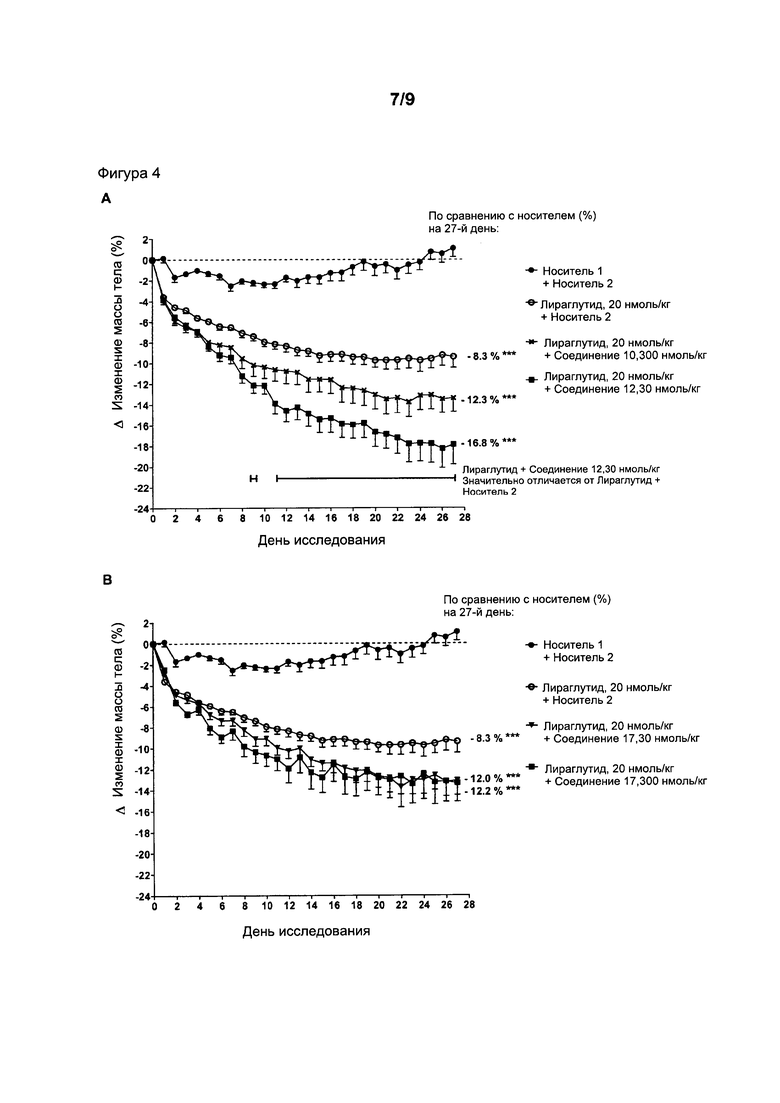
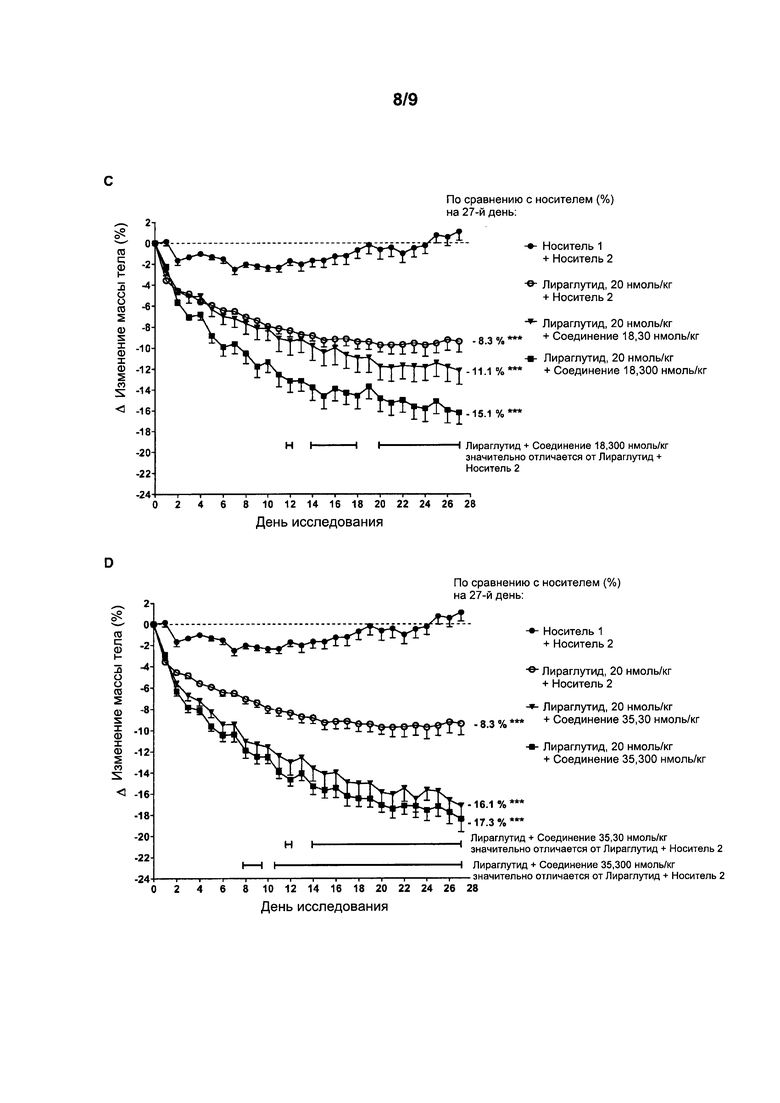
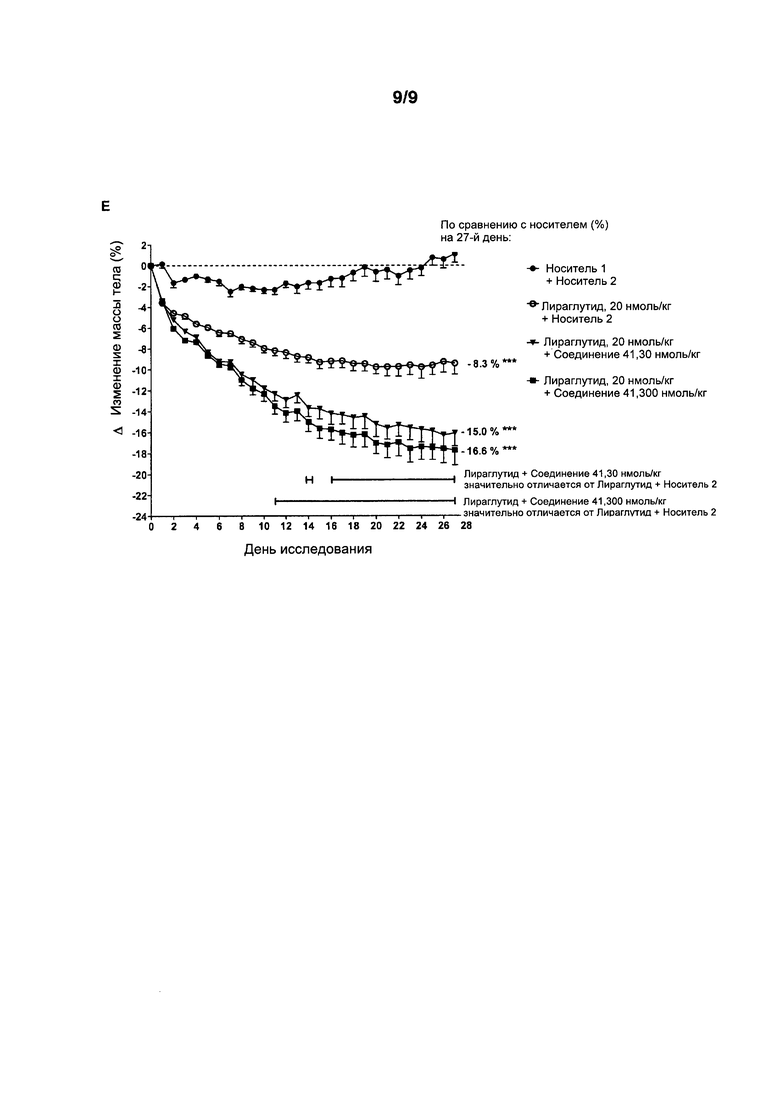
Изобретение относится к области биотехнологии, конкретно к агонисту глюкозозависимого инсулинотропного полипептида (GIP), и может быть применимо в медицине. Агонист GIP в соответствии с настоящим изобретением может быть ацилирован путем его конъюгации с липофильным заместителем, что позволяет увеличить период его полувыведения in vivo вследствие снижения чувствительности к протеолизу и снижения клиренса, сохраняя при этом аффинность связывания с рецептором GIP на достаточном для проявления терапевтического эффекта уровне. Модифицированный агонист GIP по настоящему изобретению может применяться в лечении заболеваний, ассоциированных с нарушениями обмена веществ. 3 н. и 26 з.п. ф-лы, 4 ил., 3 табл., 7 пр.
1. Агонист рецептора глюкозозависимого инсулинотропного полипептида (GIP), представленный общей Формулой I
R1-Tyr-X2-Glu-Gly-Thr-Phe-Ile-Ser-Asp-X10-Х11-X12-Glu-Leu-X15-Х16-Х17-X18-X19-X20-X21-Phe-X23-X24-X25-Leu-X27-X28-X29-Y1-Y2-R2 (I),
в которой
R1 представляет собой H-, Ac или pGlu;
X2 представляет собой Aib, Ala, D-Ala, Gly, Ser, N-Me-Ser, Ас3с, Ac4c или Ac5c;
X10 представляет собой Туr, Leu или Ser;
X11 представляет собой Ser или Leu;
X12 представляет собой Lys, Ψ или Ile;
X15 представляет собой Asp или Glu;
X16 представляет собой Ser, Glu, Lys или Ψ;
X17 представляет собой Ile, Lys, Gln, Arg или Ψ;
X18 представляет собой His, Arg или Ala;
X19 представляет собой Gln, Lys, Ala или Glu;
X20 представляет собой Gln, Lys, Ala, His или Arg;
X21 представляет собой Ala, Leu, Asp или Glu;
X23 представляет собой Val или Ile;
X24 представляет собой Asn или Glu;
X25 представляет собой Туr или Trp;
Х27 представляет собой Leu, Glu, Ser, Lys или Val;
X28 представляет собой Ala, Ser или Arg;
X29 представляет собой Aib, Gly, Ala, Gln, Thr, Ser или Lys или отсутствует;
Y1 представляет собой Lys-Gly, Gly-Pro-Ser-Ser-Gly-Ala-Pro-Pro-Pro-Ser, Gly-Pro-Ser-Ser-Gly-Ala-Pro-Pro-Ser, Pro-Ser-Ser-Gly-Ala-Pro-Pro-Pro-Ser, Pro-Ser-Ser-Gly-Ala-Pro-Pro-Ser, Gly-Lys-Lys-Asn-Asp-Trp-Lys-His-Asn-Ile-Thr-Gln или отсутствует;
Y2 представляет собой Ψ или отсутствует;
R2 представляет собой –NH2 или –ОН;
причем Ψ представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, и при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем;
и при этом указанный агонист содержит один и только один остаток Ψ;
или его фармацевтически приемлемая соль или сольват.
2. Агонист рецептора GIP по п. 1, содержащий один из следующих остатков или одну из следующих комбинаций остатков:
Aib2, Asp15, Lys20;
Aib2, Asp15, Arg20;
Aib2, Asp15, Arg20, Ile23;
Aib2, Ile12, Asp15, Arg20, Ile23, Glu24;
Ile12, Asp15, Ile23;
Ile12, Asp15, Ile23, Glu24;
Ile12, Asp15, Ala21, Ile23;
Aib2, Ala21, Ile23, Glu24;
Aib2, Asp15, Ile23;
Aib2, Asp15, Arg20, Ile23, Gln29;
Aib2, Asp15, Arg20, Gly29;
Aib2, Asp15, Ile17, Arg20, Gly29;
Aib2, Asp15, Ile17, Lys20, Gly29;
DAla2, Asp15, Ile23;
DAla2, Asp15, Ile23, Ala28;
Aib2, Asp15, Ile17, Lys20, Ala28;
Asp15, Ile23, Glu24;
N-Me-Ser2, Asp15, Lys20;
N-Me-Ser2, Asp15, Arg20;
N-Me-Ser2, Asp15, Arg20, Ile23;
N-Me-Ser2, Ile12, Asp15, Arg20, Ile23, Glu24;
N-Me-Ser2, Ala21, Ile23, Glu24;
N-Me-Ser2, Asp15, Ile23;
N-Me-Ser2, Asp15, Arg20, Ile23, Gln29;
N-Me-Ser2, Asp15, Arg20, Gly29;
N-Me-Ser2, Asp15, Ile17, Arg20, Gly29;
N-Me-Ser2, Asp15, Ile17, Lys20, Gly29;
N-Me-Ser2, Asp15, Ile23;
N-Me-Ser2, Asp15, Ile23, Ala28;
Ac3c2, Asp15, Lys20;
Ac3c2, Asp15, Arg20;
Ac3c2, Asp15, Arg20, Ile23;
Ac3c2, Ile12, Asp15, Arg20, Ile23, Glu24;
Ac3c2, Ala21, Ile23, Glu24;
Ac3c2, Asp15, Ile23;
Ac3c2, Asp15, Arg20, Ile23, Gln29;
Ac3c2, Asp15, Arg20, Gly29;
Ac3c2, Asp15, Ile17, Arg20, Gly29;
Ac3c2, Asp15, Ile17, Lys20, Gly29;
Ac3c2, Asp15, Ile23;
Ac3c2, Asp15, Ile23, Ala28
Ac4c2, Asp15, Lys20;
Ac4c2, Asp15, Arg20;
Ac4c2, Asp15, Arg20, Ile23;
Ac4c2, Ile12, Asp15, Arg20, Ile23, Glu24;
Ac4c2, Ala21, Ile23, Glu24;
Ac4c2, Asp15, Ile23;
Ac4c2, Asp15, Arg20, Ile23, Gln29;
Ac4c2, Asp15, Arg20, Gly29;
Ac4c2, Asp15, Ile17, Arg20, Gly29;
Ac4c2, Asp15, Ile17, Lys20, Gly29;
Ac4c2, Asp15, Ile23;
Ac4c2, Asp15, Ile23, Ala28
Ac5c2, Asp15, Lys20;
Ac5c2, Asp15, Arg20;
Ac5c2, Asp15, Arg20, Ile23;
Ac5c2, Ile12, Asp15, Arg20, Ile23, Glu24;
Ac5c2, Ala21, Ile23, Glu24;
Ac5c2, Asp15, Ile23;
Ac5c2, Asp15, Arg20, Ile23, Gln29;
Ac5c2, Asp15, Arg20, Gly29;
Ac5c2, Asp15, Ile17, Arg20, Gly29;
Ac5c2, Asp15, Ile17, Lys20, Gly29;
Ac5c2, Asp15, Ile23;
Ac5c2, Asp15, Ile23, Ala28.
3. Агонист рецептора GIP по п. 1, представленный общей формулой II
R1-Tyr-X2-Glu-Gly-Thr-Phe-Ile-Ser-Asp-Tyr-Ser-X12-Glu-Leu-X15-X16-X17-X18-X19-X20-X21-Phe-X23-X24-X25-Leu-X27-X28-X29-Yl-Y2-R2 (II),
в которой
R1 представляет собой Н-, Ас или pGlu;
Х2 представляет собой Aib, Ala, D-Ala, Gly;
X12 представляет собой Lys, Ψ или Ile;
X15 представляет собой Asp или Glu;
X16 представляет собой Ser, Glu, Lys или Ψ;
X17 представляет собой Ile, Lys, Gln, Arg или Ψ;
X18 представляет собой His, Arg или Ala;
X19 представляет собой Gln или Ala;
Х20 представляет собой Gln, Lys, Ala, His или Arg;
X21 представляет собой Ala, Asp или Glu;
X23 представляет собой Ile или Val;
X24 представляет собой Asn или Glu;
Х25 представляет собой Туr или Trp;
Х27 представляет собой Leu, Glu, Ser, Lys или Val;
X28 представляет собой Ala, Ser или Arg;
X29 представляет собой Aib, Gly, Ala, Gln, Thr, Ser или Lys или отсутствует;
Y1 представляет собой Lys-Gly, Gly-Pro-Ser-Ser-Gly-Ala-Pro-Pro-Pro-, Gly-Pro-Ser-Ser-Gly-Ala-Pro-Pro-Ser, Pro-Ser-Ser-Gly-Ala-Pro-Pro-Pro-Ser, Pro-Ser-Ser-Gly-Ala-Pro-Pro-Ser, Gly-Lys-Lys-Asn-Asp-Trp-Lys-His-Asn-Ile-Thr-Gln или отсутствует;
Y2 представляет собой Ψ или отсутствует;
R2 представляет собой -NH2 или -ОН;
причем Ψ представляет собой остаток Lys, при этом боковая цепь указанного остатка Lys конъюгирована с липофильным заместителем;
и при этом указанный агонист содержит один и только один остаток Ψ;
или его фармацевтически приемлемая соль или сольват.
4. Агонист рецептора GIP по п. 3, содержащий один из следующих остатков или комбинаций остатков:
Aib2, Lys12, Asp15, Lys20;
Aib2, Lys12, Asp15, Arg20;
Aib2, Asp15, Arg20;
Aib2, Ile12, Asp15, Arg20, Glu24;
Ile12, Asp15, Ile23;
Ile12, Asp15, Glu24;
Ile12, Asp15, Ala21;
Aib2, Lys12, Ala21, Glu24;
Aib2, Lys12, Asp15;
Aib2, Lys12, Asp15, Arg20, Gln29;
Aib2, Lys12, Asp15, Arg20, Gly29;
Aib2, Lys12, Asp15, Ile17, Arg20, Gly29;
Aib2, Asp15, Ile17, Lys20, Gly29;
DAla2, Asp15;
DAla2, Asp15, Ala28;
Aib2, Asp15, Ile17, Lys20, Ala28;
Asp15, Glu24;
Ala2, Lys12, Asp15, Lys20;
Ala2, Lys12, Asp15, Arg20;
Ala2, Asp15, Arg20;
Ala2, Ile12, Asp15, Arg20, Glu24;
Ala2, Ile12, Asp15, Ile23;
Ala2, Ile12, Asp15, Glu24;
Ala2, Ile12, Asp15, Ala21;
Ala2, Lys12, Ala21, Glu24;
Ala2, Lys12, Asp15;
Ala2, Lys12, Asp15, Arg20, Gln29;
Ala2, Lys12, Asp15, Arg20, Gly29;
Ala2, Lys12, Asp15, Ile17, Arg20, Gly29;
Ala2, Asp15, Ile17, Lys20, Gly29;
Ala2, Asp15;
Ala2, Asp15, Ala28;
Ala2, Asp15, Ile17, Lys20, Ala28;
Gly2, Lys12, Asp15, Lys20;
Gly2, Lys12, Asp15, Arg20;
Gly2, Asp15, Arg20;
Gly2, Ile12, Asp15, Arg20, Glu24;
Gly2, Ile12, Asp15, Ile23;
Gly2, Ile12, Asp15, Glu24;
Gly2, Ile12, Asp15, Ala21;
Gly2, Lys12, Ala21, Glu24;
Gly2, Lys12, Asp15;
Gly2, Lys12, Asp15, Arg20, Gln29;
Gly2, Lys12, Asp15, Arg20, Gly29;
Gly2, Lys12, Asp15, Ile17, Arg20, Gly29;
Gly2, Asp15, Ile17, Lys20, Gly29;
Gly2, Asp15;
Gly2, Asp15, Ala28;
Gly2, Asp15, Ile17, Lys20, Ala28;
Gly2, Asp15, Glu24.
5. Агонист рецептора GIP по п. 1, представленный общей формулой III
R1-Tyr-Aib-Glu-Gly-Thr-Phe-Ile-Ser-Asp-Tyr-Ser-Ile-Glu-Leu-X15-X16-X17-X18-X19-X20-Х21-Phe-Val-X24-X25-Leu-Leu-Ala-X29-Y1-Y2-R2 (III),
в которой
R1 представляет собой Н-, Ас или pGlu;
X15 представляет собой Asp или Glu;
X16 представляет собой Lys или Ψ;
X17 представляет собой Ile или Ψ;
X18 представляет собой His или Ala;
X19 представляет собой Gln или Ala;
Х20 представляет собой Gln, Lys или Arg;
Х21 представляет собой Ala, Asp или Glu;
Х24 представляет собой Asn или Glu;
Х25 представляет собой Туr или Trp;
Х29 представляет собой Gln или отсутствует;
Y1 представляет собой Lys-Gly, Gly-Pro-Ser-Ser-Gly-Ala-Pro-Pro-Pro-Ser, Gly-Pro-Ser-Ser-Gly-Ala-Pro-Pro-Ser, Pro-Ser-Ser-Gly-Ala-Pro-Pro-Pro-Ser, Pro-Ser-Ser-Gly-Ala-Pro-Pro-Ser, Gly-Lys-Lys-Asn-Asp-Trp-Lys-His-Asn-Ile-Thr-Gln или отсутствует;
Y2 представляет собой Ψ или отсутствует;
R2 представляет собой -NH2 или -ОН;
причем Ψ представляет собой остаток, независимо выбранный из Lys, Arg, Orn и Cys, и при этом боковая цепь указанного остатка конъюгирована с липофильным заместителем;
и при этом указанный агонист содержит один и только один остаток Ψ;
или его фармацевтически приемлемая соль или сольват.
6. Агонист рецептора GIP по п. 5, содержащий один из следующих остатков или комбинаций остатков:
Asp15, Lys20;
Asp15, Arg20;
Asp15, Arg20, Glu24;
Asp15, Lys16;
Asp15, Lys16, Glu24;
Asp15, Ψ16, Ala21;
Ala21, Glu24;
Asp15, Arg20, Gln29;
Asp15, Arg20, Gly29;
Asp15, Ile17, Arg20, Gly29;
Asp15, Ile17, Lys20, Gly29;
Asp15, Ala28;
Asp15, Ile17, Lys20, Ala28;
Asp15, Ile23, Glu24;
Asp15, Ψ17, Lys20;
Asp15, Ψ17, Arg20;
Asp15, Ψ17, Arg20;
Asp15, Ψ17, Arg20, Glu24;
Asp15, Lys16, Ψ17;
Asp15, Lys16, Ψ17, Glu24;
Asp15, Ψ17, Ala21;
Ala21, Ψ17, Glu24;
Asp15, Asp15, Ψ17, Arg20, Gln29;
Asp15, Ψ17, Arg20, Gly29;
Asp15, Ile17, Arg20, Gly29;
Asp15, Ile17, Lys20, Gly29;
Asp15; Ψ17;
Asp15, Ψ17, Ala28;
Asp15, Ile17, Lys20, Ala28;
Asp15, Ψ17, Ile23, Glu24.
7. Агонист рецептора GIP по п. 1, отличающийся тем, что указанный Ψ представляет собой остаток Lys, Arg, Orn или Cys, в котором боковая цепь конъюгирована с заместителем, имеющим формулу -Z1 или -Z2-Z1.
8. Агонист рецептора GIP по п. 7, отличающийся тем, что указанный -Z1 представляет собой цепь жирной кислоты, имеющую на конце связь -Х- с Ψ или с Z2;
причем -Х- представляет собой связь, -СО-, -SO- или -SO2-;
и необязательно Z1 содержит полярную группу в конце цепи, который является дистальным относительно связи -Х-; причем указанная полярная группа содержит группу карбоновой кислоты или биоизостера карбоновой кислоты, фосфоновой кислоты или сульфоновой кислоты.
9. Агонист рецептора GIP по п. 8, отличающийся тем, что указанный Z1 представляет собой группу формулы
A-B-Alk-X-,
в которой
А представляет собой водород или группу карбоновой кислоты, биоизостера карбоновой кислоты, фосфоновой кислоты или сульфоновой кислоты;
В представляет собой связь или линкер;
X представляет собой связь, ацил (-СО-), сульфинил (-SO-) или сульфонил (-SO2-); и
Alk представляет собой цепь жирной кислоты, которая может быть необязательно замещена одним или более заместителями.
10. Агонист рецептора GIP по п. 9, отличающийся тем, что указанный Z1 представляет собой
А-В-С16-20 алкилен-(СО)-,
в котором А представляет собой Н или -СООН и В представляет собой связь, например:
17-карбоксигептадеканоил HOOC-(CH2)16-(CO)-;
19-карбоксинонадеканоил HOOC-(CH2)18-(CO)-;
октадеканоил Н3С-(СН2)16-(СО)-; или
эйкозаноил Н3С-(СН2)18-(СО)-.
11. Агонист рецептора GIP по п. 10, отличающийся тем, что указанный Z2 представляет собой спейсер, связанный на одном конце с Y, который представляет собой атом азота, кислорода или атом серы, и на другом конце с X, который представляет собой связь или ацил (-СО-), сульфинил (-SO-), сульфонил (-SO2-) или отсутствует.
12. Агонист рецептора GIP по п. 11, отличающийся тем, что указанный -Z1-Z2 представляет собой:
(i) [17-Карбоксигептадеканоил]-изо-Glu-Peg3-Peg3
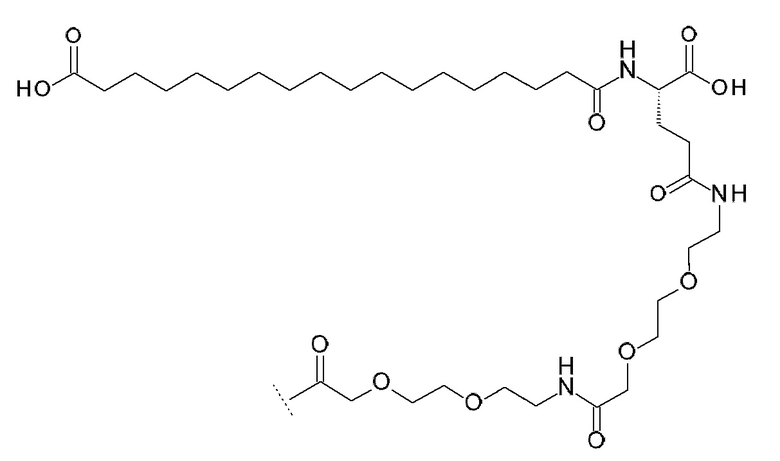
(ii) [17-Карбоксигептадеканоил]-изо-Glu

(iii) Октадеканоил-изо-Glu-Peg3-Peg3
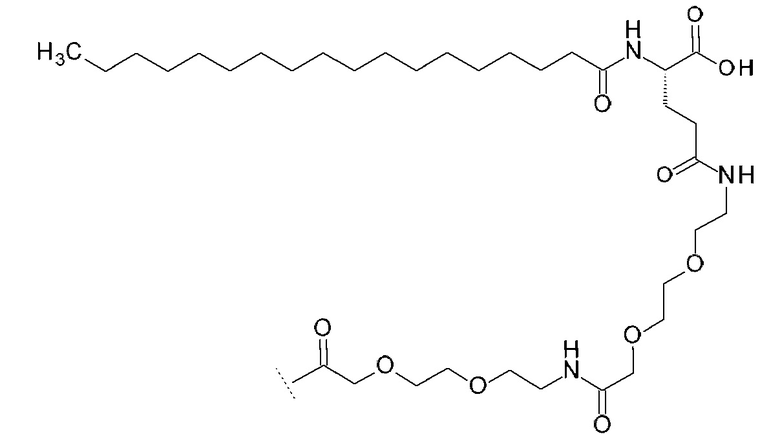
(iv) Эйкозаноил-изо-Glu-Peg3-Peg3
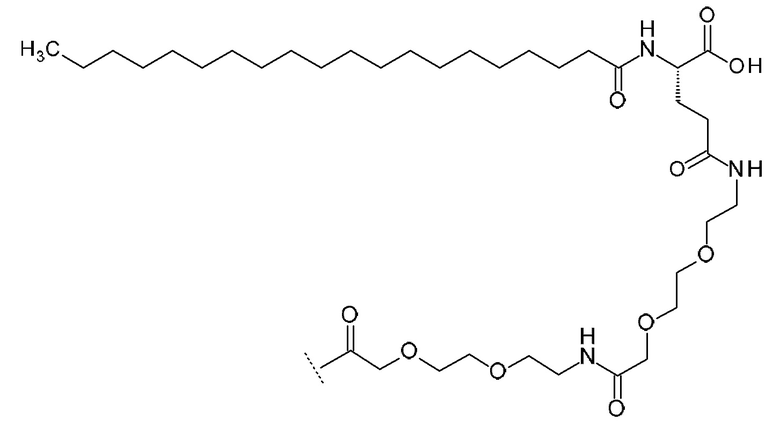
(v) [19-Карбоксинонадеканоил]-изо-Glu-Peg3-Peg3
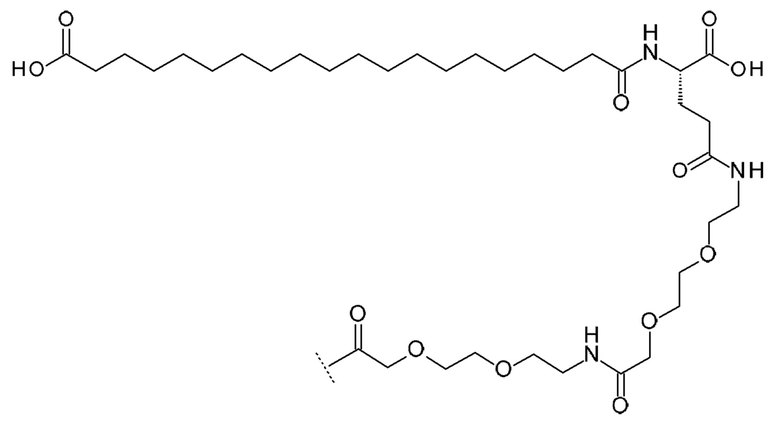
(vi) Октадеканоил-Dapa-Peg3-Peg3
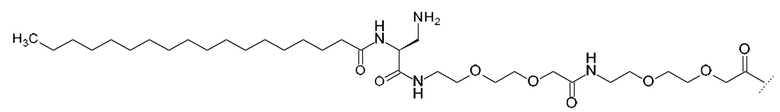
(vii) Гексадеканоил-изо-Glu
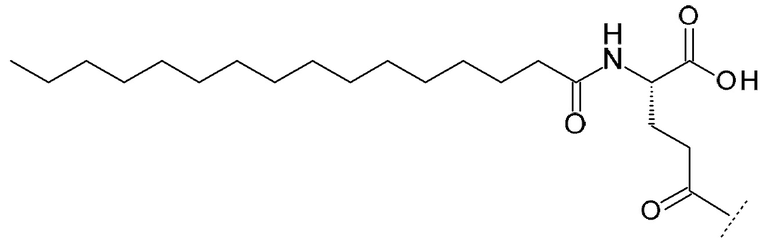
(viii) (19-Карбоксинонадеканоил)-[(пиперазин-1-ил)ацетил]-Peg3-Peg3
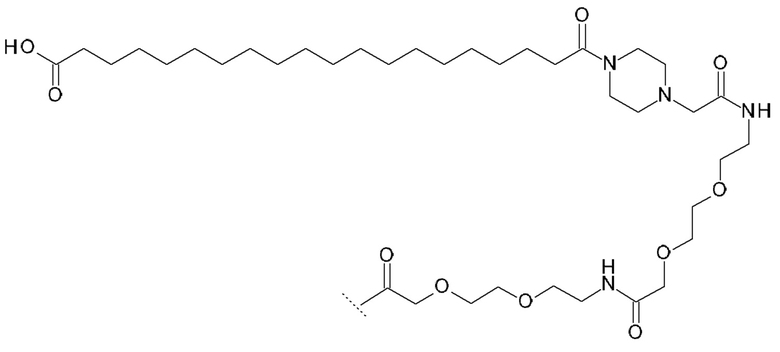
13. Агонист рецептора GIP по п. 1, имеющий последовательность
Y-Aib-EGTFISDYSIELDKΨHQQDFVNWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDΨIHQQDFVNWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELEKΨHQQDFVNWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKIHQQDFVNWLLAQGPSSGAPPPSΨ;
Y-Aib-EGTFISDYSIELDKIHQQDFVNWLLAQGPSSGAPPPSΨ;
Y-Aib-EGTFISDYSIELDKIHQQDFVNWLLAQΨ;
Y-Aib-EGTFISDYSIELDKIHQQDFVNWLLAQKGΨ;
Y-Aib-EGTFISDYSIELDKΨHQQDFVNYLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKΨHQQDFVNWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKΨAAQDFVNWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELEKΨAAKEFVNWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELEKΨAQRAFVEWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELEKIAQRAFVEWLLAQGPSSGAPPPSΨ;
Y-Aib-EGTFISDYSIELEKIAQRAFVEWLLAQΨ;
Y-Aib-EGTFISDYSIELDKΨAAQDFVNWLLAGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKIAAQDFVNWLLAGPSSGAPPPSΨ;
Y-Aib-EGTFISDYSIELDKΨAQRAFVEWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKΨAQRAFIEWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKIAQRAFIEWLLAGPSSGAPPPSKΨ;
Y-Aib-EGTFISDYSIELDKIAQKEFIEWLLAGPSSGAPPPSKΨ;
Y-Aib-EGTFISDYSIELDKIAAQDFIEWLLAGPSSGAPPPSKΨ;
Y-Aib-EGTFISDYSIELDKIAAQDFVEWLLAGPSSGAPPPSKΨ;
Y-Aib-EGTFISDYSIELDKIAQRAFIEWLLAQGPSSGAPPPSKΨ;
Y-Aib-EGTFISDYSIELDKΨAAQAFVNWLLAGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKΨAAQDFVNWLLAAGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKΨAAQDFINWLLAGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKΨAAQDFIEWLLAGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKΨAAQDFIEWLLAGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKΨIAQRAFIEWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSKΨELDKIAQRAFIEWLLAQGPSSGAPPPS;
Y-DAla-EGTFISDYSIELDKΨAQRAFIEWLLAQGPSSGAPPPS;
Y-DAla-EGTFISDYSIELDKIAAQDFIEWLLAGPSSGAPPPSKΨ;
Y-Aib-EGTFISDYSIELDKΨAAQDFIEWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKΨAAQDFINWLLAQGPSSGAPPPS; или
Y-Aib-EGTFISDYSIELDKΨAAQAFIEWLLAQGPSSGAPPPS.
14. Агонист рецептора GIP по п. 1, имеющий последовательность
Y-Aib-EGTFISDYSIELDK-K(гексадеканоил-изо-Glu)-HQQDFVNWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELD-K(гексадеканоил-изо-Glu)-IHQQDFVNWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELEK-K(гексадеканоил-изо-Glu)-HQQDFVNWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKIHQQDFVNWLLAQGPSSGAPPPS-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3);
Y-Aib-EGTFISDYSIELDKIHQQDFVNWLLAQGPSSGAPPPS-K(гексадеканоил-изо-Glu);
Y-Aib-EGTFISDYSIELDKIHQQDFVNWLLAQ-K(гексадеканоил-изо-Glu);
Y-Aib-EGTFISDYSIELDKIHQQDFVNWLLAQKG-K(гексадеканоил-изо-Glu);
Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-HQQDFVNYLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-HQQDFVNWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AAQDFVNWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELEK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AAKEFVNWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELEK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AQRAFVEWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELEKIAQRAFVEWLLAQGPSSGAPPPS-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3);
H-Y-Aib-EGTFISDYSIELEKIAQRAFVEWLLAQ-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3);
H-Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AAQDFVNWLLAGPSSGAPPPS;
H-Y-Aib-EGTFISDYSIELDKIAAQDFVNWLLAGPSSGAPPPS-K([19-карбоксинонадеканоил] -изо-Glu-Peg3-Peg3);
Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AQRAFVEWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AQRAFIEWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDK-K((19-карбоксинонадеканоил)-[(пиперазин-1-ил)-ацетил]-Peg3-Peg3)-AQRAFIEWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDK-K((19-карбоксинонадеканоил)-[(пиперазин-1-ил)-ацетил]-Peg3-Peg3)-AQRAFVEWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDK-K((19-карбоксинонадеканоил)-[(пиперазин-1-ил)-ацетил]-Peg3-Peg3)-AQKEFVEWLLAAGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AQKEFVEWLLAAGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDKIAQRAFIEWLLAGPSSGAPPPS-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3);
Y-Aib-EGTFISDYSIELDKIAQKEFIEWLLAGPSSGAPPPS-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3);
Y-Aib-EGTFISDYSIELDKIAAQDFIEWLLAGPSSGAPPPS-K([19-карбоксинонадеканоил] -изо-Glu-Peg3 -Peg3);
Y-Aib-EGTFISDYSIELDKIAAQDFIEWLLAGPSSGAPPPS-K((19-карбоксинонадеканоил)-[(пиперазин-1-ил)-ацетил]-Peg3-Peg3);
Y-Aib-EGTFISDYSIELDKIAAQDFVEWLLAGPSSGAPPPS-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3);
Y-Aib-EGTFISDYSIELDKIAQRAFIEWLLAQGPSSGAPPPS-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3);
Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AAQAFVNWLLAGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AAQDFVNWLLAAGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AAQDFINWLLAGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AAQDFIEWLLAGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDK-K((19-карбоксинонадеканоил)-[(пиперазин-1-ил)-ацетил]-Peg3-Peg3)-AAQDFIEWLLAGPSSGAPPPS;
Y-Aib-EGTFISDYSIELD-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-IAQRAFIEWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYS-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-ELDKIAQRAFIEWLLAQGPSSGAPPPS;
Y-DAla-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AQRAFIEWLLAQGPSSGAPPPS;
Y-DAla-EGTFISDYSIELDKIAAQDFIEWLLAGPSSGAPPPS-K((19-карбоксинонадеканоил)-[(пиперазин-1-ил)-ацетил]-Peg3-Peg3);
Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AAQDFIEWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AAQDFINWLLAQGPSSGAPPPS;
Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AAQAFIEWLLAQGPSSGAPPPS; или
Y-Aib-EGTFISDYSIELDK-K((19-карбоксинонадеканоил)-[(пиперазин-l-ил)-ацетил]-Peg3-Peg3)-AAQAFIEWLLAQGPSSGAPPPS.
15. Агонист рецептора GIP по п. 1, представляющий собой
H-Y-Aib-EGTFISDYSIELDK-K(гексадеканоил-изо-Glu)-HQQDFVNWLLAQGPSSGAPPPS-NH2;
H-Y-Aib-EGTFISDYSIELD-К(гексадеканоил-изо-Glu)-IHQQDFVNWLLAQGPSSGAPPPS-NH2;
H-Y-Aib-EGTFISDYSIELEK-K(гексадеканоил-изо-Glu)-HQQDFVNWLLAQGPSSGAPPPS-NH2;
H-Y-Aib-EGTFISDYSIELDKIHQQDFVNWLLAQGPSSGAPPPS-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-NH2;
H-Y-Aib-EGTFISDYSIELDKIHQQDFVNWLLAQGPSSGAPPPS-K(гексадеканоил-изо-Glu)-NH2;
H-Y-Aib-EGTFISDYSIELDKIHQQDFVNWLLAQ-K(гексадеканоил-изо-Glu)-NH2;
H-Y-Aib-EGTFISDYSIELDKIHQQDFVNWLLAQKG-K(гексадеканоил-изо-Glu)-NH2;
H-Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-HQQDFVNYLLAQGPSSGAPPPS-NH2;
H-Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-HQQDFVNWLLAQGPSSGAPPPS-NH2
H-Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AAQDFVNWLLAQGPSSGAPPPS-NH2;
H-Y-Aib-EGTFISDYSIELEK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AAKEFVNWLLAQGPSSGAPPPS-NH2;
H-Y-Aib-EGTFISDYSIELEK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AQRAFVEWLLAQGPSSGAPPPS-NH2;
H-Y-Aib-EGTFISDYSIELEKIAQRAFVEWLLAQGPSSGAPPPS-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-NH2;
H-Y- Aib-EGTFISDYSIELEKIAQRAFVEWLLAQ-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-NH2;
H-Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AAQDFVNWLLAGPSSGAPPPS-NH2;
H-Y-Aib-EGTFISDYSIELDKIAAQDFVNWLLAGPSSGAPPPS-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-NH2;
H-Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AQRAFVEWLLAQGPSSGAPPPS-NH2;
H-Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AQRAFIEWLLAQGPSSGAPPPS-NH2;
H-Y-Aib-EGTFISDYSIELDK-K((19-карбоксинонадеканоил)-[(пиперазин-1-ил)-ацетил]-Peg3-Peg3)-AQRAFIEWLLAQGPSSGAPPPS-NH2;
H-Y-Aib-EGTFISDYSIELDK-K((19-карбоксинонадеканоил)-[(пиперазин-1-ил)-ацетил]-Peg3-Peg3)-AQRAFVEWLLAQGPSSGAPPPS-NH2;
H-Y-Aib-EGTFISDYSIELDK-K((19-карбоксинонадеканоил)-[(пиперазин-1-ил)-ацетил]-Peg3-Peg3)-AQKEFVEWLLAAGPSSGAPPPS-NH2;
H-Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AQKEFVEWLLAAGPSSGAPPPS-NH2;
H-Y-Aib-EGTFISDYSIELDKIAQRAFIEWLLAGPSSGAPPPS-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-NH2;
H-Y-Aib-EGTFISDYSIELDKIAQKEFIEWLLAGPSSGAPPPS-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-NH2;
H-Y-Aib-EGTFISDYSIELDKIAAQDFIEWLLAGPSSGAPPPS-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-NH2;
H-Y-Aib-EGTFISDYSIELDKIAAQDFIEWLLAGPSSGAPPPS-K((19-карбоксинонадеканоил)-[(пиперазин-l-ил)-ацетил]-Peg3-Peg3)-NH2;
H-Y-Aib-EGTFISDYSIELDKIAAQDFVEWLLAGPSSGAPPPS-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-NH2;
H-Y-Aib-EGTFISDYSIELDKIAQRAFIEWLLAQGPSSGAPPPS-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-NH2;
H-Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AAQAFVNWLLAGPSSGAPPPS-NH2;
H-Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AAQDFVNWLLAAGPSSGAPPPS-NH2;
H-Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AAQDFINWLLAGPSSGAPPPS-NH2;
H-Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AAQDFIEWLLAGPSSGAPPPS-NH2;
H-Y-Aib-EGTFISDYSIELDK-K((19-карбоксинонадеканоил)-[(пиперазин-1-ил)-ацетил]-Peg3-Peg3)-AAQDFIEWLLAGPSSGAPPPS-NH2;
H-Y-Aib-EGTFISDYSIELD-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-IAQRAFIEWLLAQGPSSGAPPPS-NH2;
H-Y-Aib-EGTFISDYS-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-ELDKIAQRAFIEWLLAQGPSSGAPPPS-NH2;
H-Y-DAla-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AQRAFIEWLLAQGPSSGAPPPS-NH2;
H-Y-DAla-EGTFISDYSIELDKIAAQDFIEWLLAGPSSGAPPPS-K((19- карбоксинонадеканоил)-[(пиперазин-1-ил)-ацетил]-Peg3-Peg3)-NH2;
H-Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AAQDFIEWLLAQGPSSGAPPPS-NH2;
H-Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AAQDFINWLLAQGPSSGAPPPS-NH2;
H-Y-Aib-EGTFISDYSIELDK-K([19-карбоксинонадеканоил]-изо-Glu-Peg3-Peg3)-AAQAFIEWLLAQGPSSGAPPPS-NH2; или
H-Y-Aib-EGTFISDYSIELDK-K((19-карбоксинонадеканоил)-[(пиперазин-1-ил)-ацетил]-Peg3-Peg3)-AAQAFIEWLLAQGPSSGAPPPS-NH2.
16. Фармацевтическая композиция для лечения или предотвращения нарушения обмена веществ, содержащая в эффективном количестве агонист рецептора GIP по любому из пп. 1-15 в смеси с носителем.
17. Фармацевтическая композиция по п. 16, приготовленная в виде жидкости, пригодной для введения путем инъекции или инфузии.
18. Фармацевтическая композиция по п. 16, приготовленная для того, чтобы вызывать контролируемое, например замедленное, высвобождение указанного агониста рецептора GIP.
19. Применение агониста рецептора GIP по любому из пп. 1-15 для лечения или предотвращения нарушения обмена веществ у нуждающегося в этом индивидуума.
20. Применение по п. 19, отличающееся тем, что указанный агонист рецептора GIP вводят как часть комбинированной терапии с противодиабетическим агентом.
21. Применение по п. 19, отличающееся тем, что указанный агонист рецептора GIP вводят как часть комбинированной терапии с агонистом GLP-1.
22. Применение по п. 19, отличающееся тем, что указанное нарушение обмена веществ представляет собой диабет или расстройство, связанное с диабетом, или ожирение или расстройство, связанное с ожирением.
23. Применение по п. 22, отличающееся тем, что указанное расстройство, связанное с диабетом, выбрано из резистентности к инсулину, непереносимости глюкозы, повышения уровня глюкозы натощак, гипогликемии (например, индуцированной введением инсулина), преддиабета, сахарного диабета 1 типа, сахарного диабета 2 типа, гестационного диабета, сопровождающегося гипертензией, дислипидемии или их комбинации.
24. Применение по п. 22, отличающееся тем, что указанное расстройство, связанное с диабетом, выбрано из атеросклероза, артериосклероза, ишемической болезни сердца, заболевания периферических артерий, инсульта или представляет собой состояние, связанное с атерогенной дислипидемией, расстройство, связанное с уровнем липидов в крови, повышенное кровяное давление, гипертензию, протромботическое состояние или провоспалительное состояние.
25. Применение по п. 22, отличающееся тем, что указанное расстройство, связанное с диабетом, представляет собой остеопороз, включающий повышенный риск переломов костей.
26. Применение по п. 24, отличающееся тем, что указанное расстройство, связанное с уровнем липидов в крови, представляет собой высокий уровень триглицеридов, низкий уровень холестерина-ЛПВП, высокий уровень холестерина-ЛПНП, накопление бляшек на стенках артерий или их комбинацию.
27. Применение по п. 24, отличающееся тем, что указанное протромботическое состояние включает высокие уровни фибриногена в крови или высокие уровни ингибитора активатора плазминогена-1 в крови.
28. Применение по п. 24, отличающееся тем, что указанное провоспалительное состояние включает повышенный уровень С-реактивного белка в крови.
29. Применение по п. 22, отличающееся тем, что указанное расстройство, связанное с ожирением, представляет собой связанное с ожирением воспаление, связанное с ожирением заболевание желчного пузыря или индуцированное ожирением апноэ во сне или указанное расстройство может быть связано с состоянием, выбранным из атерогенной дислипидемии, расстройств, связанных с уровнем липидов в крови, повышенного кровяного давления, гипертензии, протромботического состояния и провоспалительного состояния или их комбинации.
| WO 2012167744 A1, 13.12.2012 | |||
| WO 2013164483 A1, 07.11.2013 | |||
| WO 2011094337 A1, 04.08.2011 | |||
| WO 03082898 A2, 09.10.2003 | |||
| Устройство, сигнализирующее о присутствии в шахтах взрывчатой смеси | 1928 |
|
SU11653A1 |
| RU 2012136450 A2, 10.03.2014. | |||
Авторы
Даты
2020-03-17—Публикация
2015-10-29—Подача