[0001] Настоящая патентная заявка заявляет приоритет по международной заявке №PCT/CN2014/083715, поданной 5 августа 2014, которая включена в настоящий документ посредством ссылки в полном объеме для всех целей.
ОБЛАСТЬ ТЕХНИКИ
[0002] Настоящее изобретение относится к антителам и их антигенсвязывающим фрагментам, которые связываются с PD-L1, и к способам применения таких антител и антигенсвязывающих фрагментов.
ОПИСАНИЕ ТЕКСТОВОГО ФАЙЛА, ПРЕДСТАВЛЕННОГО В ЭЛЕКТРОННОМ ВИДЕ
[0003] Содержание текстового файла, представленного в электронном виде вместе с данной заявкой, в полном объеме включено в настоящий документ посредством ссылки: копия перечня последовательностей в машиночитаемом формате (название файла: CRBI_007_01WO_SeqList_ST25.txt); дата записи: 4 августа 2015; размер файла 153 Кб).
УРОВЕНЬ ТЕХНИКИ
[0004] Лиганд 1 рецептора программируемой клеточной смерти (PD-L1) представляет собой лиганд рецептора программируемой клеточной смерти 1 (PD-1). PD-1 экспрессируется в основном на лимфоцитах и имеет два лиганда: PD-L1 и PD-L2. PD-L2 не так распространен, как PD-L1. PD-L1, также известный как кластер дифференцировки 274 (CD274) или гомолог 1 В7 (B7-H1) и представляет собой трансмембранный белок массой 40 кДа типа 1, который кодируется геном CD274. Как PD-L1, так и PD-1 принадлежат надсемейству иммуноглобулинов и состоят из двух внеклеточных доменов Ig, N-концевого вариабельного домена и С-концевого константного домена. Поверхность связывания PD-L1 с белком программируемой клеточной смерти-1 (PD-1) и В7-1 (CD80) находится на IgV-подобном домене (Lin et al. (2008) PNAS 105: 3011-3016). В то время как PD-L1 содержит консервативный короткий внутриклеточный хвост (около 30 аминокислот), PD-1 содержит два цитоплазматических тирозиновых сигнальных мотива, иммунорецепторный тирозиновый ингибирующий мотив (ITIM) и иммунорецепторный тирозиновый переключающий мотив (ITSM). После стимуляции Т-клеток, PD-1 рекрутирует тирозинфосфатазу SHP-2 к мотиву ITSM в цитоплазматическом хвосте, что приводит к дефосфорилированию эффекторных молекул, таких как CD3-дзета, PKC-тета (протеинкиназа-тета) и Zap70, которые участвуют в сигнальном каскаде Т-клеточного CD3 (Freeman et al.(2000) J Exp Med 192: 1027-34; Latchman, et. al.(2001) Nat Immunol 2: 261-8; Carter et al.(2002) Eur J Immunol 32: 634-43).
[0005] PD-L1 широко распространен не только на лейкоцитах и негемопоэтических клетках в лимфоидных и нелимфоидных тканях, но и в различных раковых клетках. Клинические данные свидетельствуют о том, что высокий уровень экспрессии PD-L1 в опухоли связан с повышенной агрессивностью опухоли и неблагоприятным прогнозом. Образование комплекса PD-1/PD-L1 передает ингибирующий сигнал и негативно регулирует иммунные ответы Т-клеток; это ингибирует TКР-опосредованную (Т-клеточный рецептор) клеточную активацию, продукцию цитокинов и пролиферацию Т-клеток (Fife et al.(2011) Nature Immunology 10: 1185-1193); индуцирует истощение или анергию среди родственных антигенспецифических Т-клеток (Hofmeyer et al.(2011) Journal of Biomedicine and Biotechnology 2011: 1-9); способствует дифференциации Т-хелперов в Foxp3+регуляторных Т-клетках (Armanath et al.(2011) Science TransMed 3: 1-13; Francisco et al.(2009) J.Exp.Med.206: 3015-3029); и индуцирует апоптоз эффекторных Т-клеток. Разрушение гена PD-L1 приводит к повышению Т-клеточных ответов и образованию самореактивных Т-клеток (Latchman et al.(2004) PNAS 101: 10691-10696). Блокирование антителом или PD-1 или PD-L1 приводит к усилению противоопухолевого иммунитета (Iwai et al.(2002) PNAS 99: 12293-12297).
[0006] Таким образом, существует важная роль для сигнального пути PD-1/PD-L1 в контроле иммунного ответа. Дисфункция сигналинга PD-1/PD-L1, как представляется, коррелирует с инициацией и развитием таких заболеваний, как рак и вирусные инфекции. Анализ нокаутированных животных привел к пониманию того, что функции PD-1/PD-L1, в основном, заключаются в индуцировании и регуляции периферической толерантности. Таким образом, терапевтическое блокирование сигнального пути PD-1/PD-L1 может быть полезно в преодолении иммунологической толерантности и в лечении рака или инфекции, а также в повышении иммунитета при вакцинации (или с профилактической или с лечебной целью). В данной области техники существует потребность в совершенствовании способов блокирования сигнального пути PD-1/PD-L1.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0007] В одном аспекте настоящее изобретение обеспечивает антитела и их антигенсвязывающие фрагменты, которые связываются с лигандом 1 белка программируемой клеточной смерти-1 (PD-L1). В некоторых вариантах реализации изобретения антитела и их антигенсвязывающие фрагменты связываются с человеческим PD-L1. В некоторых вариантах реализации изобретения антитела и их антигенсвязывающие фрагменты связываются с PD-L1 и блокируют связывание PD-1 и/или СD80 с PD-L1. В дополнительных вариантах реализации изобретения анти-PD-L1 антитела и их фрагменты связываются с PD-L1 и нарушают сигнальный путь PD-L1/PD-1 или PD-L1/CD80. В одном варианте реализации изобретения антитело или его фрагмент представляет собой мышиное антитело, химерное антитело, человеческое антитело или гуманизированное антитело. В одном варианте реализации изобретения анти-PD-L1 антитело или его фрагмент представляет собой моноклональное антитело, scFv, Fab-фрагмент, Fab'-фрагмент, F(ab)'-фрагмент, биспецифическое антитело, иммуноконъюгат или их комбинацию.
[0008] В одном варианте реализации настоящее изобретение обеспечивает выделенное антитело или его фрагмент, содержащий одну или более CDR (область, определяющая комплементарность), выбранную из группы, состоящей из SEQ ID NO: 81-140.
[0009] В одном варианте реализации изобретения антитело или его фрагмент содержит последовательность CDR1 тяжелой цепи, имеющую по меньшей мере 80% гомологии, по меньшей мере 81% гомологии, по меньшей мере 82% гомологии, по меньшей мере 83% гомологии, по меньшей мере 84% гомологии, по меньшей мере 85% гомологии, по меньшей мере 86% гомологии, по меньшей мере 87% гомологии, по меньшей мере 88% гомологии, по меньшей мере 89% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 81, 87, 93, 99, 105, 111, 117, 123, 129 и 135.
[0010] В одном варианте реализации изобретения антитело или его фрагмент содержит последовательность CDR2 тяжелой цепи, имеющую по меньшей мере 80% гомологии, по меньшей мере 81% гомологии, по меньшей мере 82% гомологии, по меньшей мере 83% гомологии, по меньшей мере 84% гомологии, по меньшей мере 85% гомологии, по меньшей мере 86% гомологии, по меньшей мере 87% гомологии, по меньшей мере 88% гомологии, по меньшей мере 89% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 82, 88, 94, 100, 106, 112, 118, 124, 130 и 136.
[0011] В одном варианте реализации изобретения антитело или его фрагмент содержит последовательность CDR3 тяжелой цепи, имеющую по меньшей мере 80% гомологии, по меньшей мере 81% гомологии, по меньшей мере 82% гомологии, по меньшей мере 83% гомологии, по меньшей мере 84% гомологии, по меньшей мере 85% гомологии, по меньшей мере 86% гомологии, по меньшей мере 87% гомологии, по меньшей мере 88% гомологии, по меньшей мере 89% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 83, 89, 95, 101, 107, 113, 119, 125, 131 и 137.
[0012] В одном варианте реализации изобретения антитело или его фрагмент содержит последовательность CDR1 легкой цепи, имеющую по меньшей мере 80% гомологии, по меньшей мере 81% гомологии, по меньшей мере 82% гомологии, по меньшей мере 83% гомологии, по меньшей мере 84% гомологии, по меньшей мере 85% гомологии, по меньшей мере 86% гомологии, по меньшей мере 87% гомологии, по меньшей мере 88% гомологии, по меньшей мере 89% гомологию, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере, 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 84, 90, 96, 102, 108, 114, 120, 126, 132 и 138.
[0013] В одном варианте реализации изобретения антитело или его фрагмент содержит последовательность CDR2 легкой цепи, имеющую по меньшей мере 80% гомологии, по меньшей мере 81% гомологии, по меньшей мере 82% гомологии, по меньшей мере 83% гомологии, по меньшей мере 84% гомологии, по меньшей мере 85% гомологии, по меньшей мере 86% гомологии, по меньшей мере 87% гомологии, по меньшей мере 88% гомологии, по меньшей мере 89% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 85, 91, 97, 103, 109, 115, 121, 127, 133 и 139.
[0014] В одном варианте реализации изобретения антитело или его фрагмент содержит последовательность CDR3 легкой цепи, имеющую по меньшей мере 80% гомологии, по меньшей мере 81% гомологии, по меньшей мере 82% гомологии, по меньшей мере 83% гомологии, по меньшей мере 84% гомологии, по меньшей мере 85% гомологии, по меньшей мере 86% гомологии, по меньшей мере 87% гомологии, по меньшей мере 88% гомологии, по меньшей мере 89% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 86, 92, 98, 104, 110, 116, 122, 128, 134 и 140.
[0015] В одном варианте реализации изобретения антитело или его фрагмент содержит CDR1 тяжелой цепи, состоящую из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 81, 87, 93, 99, 105, 111, 117, 123, 129 и 135; CDR2 тяжелой цепи, состоящую из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 82, 88, 94, 100, 106, 112, 118, 124, 130 и 136; CDR3 тяжелой цепи, состоящую из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 83, 89, 95, 101, 107, 113, 119, 125, 131 и 137; CDR1 легкой цепи, состоящую из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 84, 90, 96, 102, 108, 114, 120, 126, 132 и 138; CDR2 легкой цепи, состоящую из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 85, 91, 97, 103, 109, 115, 121, 127, 133 и 139 и CDR3 легкой цепи, состоящую из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 86, 92, 98, 104, 110, 116, 122, 128, 134 и 140.
[0016] В одном варианте реализации изобретения антитело или его фрагмент связывает PD-L1 и содержит CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью в соответствии с SEQ ID NO: 81, 82, и 83, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью в соответствии с SEQ ID NO: 84, 85 и 86, соответственно. В дополнительном варианте реализации изобретения антитело или фрагмент такого антитела содержит CDR1, CDR2 и CDR3 тяжелой цепи в соответствии с SEQ ID NO: 81, 82, и 83, соответственно, и CDR1, CDR2 и CDR3 легкой цепи в соответствии с SEQ ID NO: 84, 85 и 86, соответственно.
[0017] В одном варианте реализации изобретения антитело или его фрагмент связывает PD-L1 и содержит CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью в соответствии с SEQ ID NO: 87, 88, и 89, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью в соответствии с SEQ ID NO: 90, 91 и 92, соответственно. В дополнительном варианте реализации изобретения антитело или фрагмент такого антитела содержит CDR1, CDR2 и CDR3 тяжелой цепи в соответствии с SEQ ID NO: 87, 88, и 89, соответственно, и CDR1, CDR2 и CDR3 легкой цепи в соответствии с SEQ ID NO: 90, 91 и 92, соответственно.
[0018] В одном варианте реализации изобретения антитело или его фрагмент связывает PD-L1 и содержит CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью в соответствии с SEQ ID NO: 93, 94, и 95, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью в соответствии с SEQ ID NO: 96, 97 и 98, соответственно. В дополнительном варианте реализации изобретения антитело или фрагмент такого антитела содержит CDR1, CDR2 и CDR3 тяжелой цепи в соответствии с SEQ ID NO: 93, 94, и 95, соответственно, и CDR1, CDR2 и CDR3 легкой цепи в соответствии с SEQ ID NO: 96, 97 и 98, соответственно.
[0019] В одном варианте реализации изобретения антитело или его фрагмент связывает PD-L1 и содержит CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью в соответствии с SEQ ID NO: 99, 100 и 101, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью в соответствии с SEQ ID NO: 102, 103 и 104, соответственно. В дополнительном варианте реализации изобретения антитело или фрагмент такого антитела содержит CDR1, CDR2 и CDR3 тяжелой цепи в соответствии с SEQ ID NO: 99, 100, и 101, соответственно, и CDR1, CDR2 и CDR3 легкой цепи в соответствии с SEQ ID NO: 102, 103 и 104, соответственно.
[0020] В одном варианте реализации изобретения антитело или его фрагмент связывает PD-L1 и содержит CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью в соответствии с SEQ ID NO: 105, 106 и 107, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью в соответствии с SEQ ID NO: 108, 109 и 110, соответственно. В дополнительном варианте реализации изобретения антитело или фрагмент такого антитела содержит CDR1, CDR2 и CDR3 тяжелой цепи в соответствии с SEQ ID NO: 105, 106 и 107, соответственно, и CDR1, CDR2 и CDR3 легкой цепи в соответствии с SEQ ID NO: 108, 109 и 110, соответственно.
[0021] В одном варианте реализации изобретения антитело или его фрагмент связывает PD-L1 и содержит CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью в соответствии с SEQ ID NO: 111, 112 и 113, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью в соответствии с SEQ ID NO: 114, 115 и 116, соответственно. В дополнительном варианте реализации изобретения антитело или фрагмент такого антитела содержит CDR1, CDR2 и CDR3 тяжелой цепи в соответствии с SEQ ID NO: 111, 112 и 113 соответственно, и CDR1, CDR2 и CDR3 легкой цепи в соответствии с SEQ ID NO: 114, 115 и 116, соответственно.
[0022] В одном варианте реализации изобретения антитело или его фрагмент связывает PD-L1 и содержит CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью в соответствии с SEQ ID NO: 117, 118 и 119, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью в соответствии с SEQ ID NO: 120, 121 и 122, соответственно. В дополнительном варианте реализации изобретения антитело или фрагмент такого антитела содержит CDR1, CDR2 и CDR3 тяжелой цепи в соответствии с SEQ ID NO: 117, 118 и 119, соответственно, и CDR1, CDR2 и CDR3 легкой цепи в соответствии с SEQ ID NO: 120, 121 и 122, соответственно.
[0023] В одном варианте реализации изобретения антитело или его фрагмент связывает PD-L1 и содержит CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью в соответствии с SEQ ID NO: 123, 124 и 125, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью в соответствии с SEQ ID NO: 126, 127 и 128, соответственно. В дополнительном варианте реализации изобретения антитело или фрагмент такого антитела содержит CDR1, CDR2 и CDR3 тяжелой цепи в соответствии с SEQ ID NO: 123, 124 и 125, соответственно, и CDR1, CDR2 и CDR3 легкой цепи в соответствии с SEQ ID NO: 126, 127 и 128, соответственно.
[0024] В одном варианте реализации изобретения антитело или его фрагмент связывает PD-L1 и содержит CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью в соответствии с SEQ ID NO: 129, 130 и 131, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью в соответствии с SEQ ID NO: 132, 133 и 134, соответственно. В дополнительном варианте реализации изобретения антитело или фрагмент такого антитела содержит CDR1, CDR2 и CDR3 тяжелой цепи в соответствии с SEQ ID NO: 129, 130 и 131, соответственно, и CDR1, CDR2 и CDR3 легкой цепи в соответствии с SEQ ID NO: 132, 133 и 134, соответственно.
[0025] В одном варианте реализации изобретения антитело или его фрагмент связывает PD-L1 и содержит CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью в соответствии с SEQ ID NO: 135, 136 и 137, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью в соответствии с SEQ ID NO: 138, 139 и 140, соответственно. В дополнительном варианте реализации изобретения антитело или фрагмент такого антитела содержит CDR1, CDR2 и CDR3 тяжелой цепи в соответствии с SEQ ID NO: 135, 136 и 137, соответственно, и CDR1, CDR2 и CDR3 легкой цепи в соответствии с SEQ ID NO: 138, 139 и 140, соответственно.
[0026] В одном варианте реализации изобретения антитело или его фрагмент связывает PD-L1 и содержит вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 2, 6, 10, 14, 18, 22, 26, 30, 34, 38, 42, и 46, и вариабельной области легкой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 4, 8, 12, 16, 20, 24, 28, 32, 36, 40, 44 и 48. В дополнительном варианте реализации изобретения выделенное антитело или его фрагмент связывает PD-L1 и содержит вариабельную область тяжелой цепи, состоящую по существу из или состоящую из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 2, 6, 10, 14, 18, 22, 26, 30, 34, 38, 42 и 46; и вариабельной области легкой цепи, содержащей, состоящей по существу из, или состоящей из аминокислотной последовательности, выбранной из группы, состоящей из SEQ ID NO: 4, 8, 12, 16, 20, 24, 28, 32, 36, 40, 44 и 48.
[0027] В одном варианте реализации настоящее изобретение обеспечивает анти-PD-L1 антитела, которые содержат вариабельную область тяжелой цепи антитела, выбранного из группы, состоящей из 13C5, 5G9, 5G11, 8C6, 7B4, 4D1, 4A8, 8H4, 8H3, и 15F1 и вариабельной области легкой цепи антитела, выбранного из группы, состоящей из 13C5, 5G9, 5G11, 8C6, 7B4, 4D1, 4A8, 8H4, 8H3, и 15F1. Таким образом, в одном варианте реализации настоящее изобретение обеспечивает антитело или его фрагмент, содержащий вариабельную область тяжелой цепи, содержащий SEQ ID NO: 2 и вариабельную область легкой цепи, содержащую SEQ ID NO: 4; вариабельную область тяжелой цепи, содержащую SEQ ID NO: 6 и вариабельную область легкой цепи, содержащую SEQ ID NO: 8; вариабельную область тяжелой цепи, содержащую SEQ ID NO: 10 и вариабельную область легкой цепи, содержащую SEQ ID NO: 12; вариабельную область тяжелой цепи, содержащую SEQ ID NO: 14 и вариабельную область легкой цепи, содержащую SEQ ID NO: 16; вариабельную область тяжелой цепи, содержащую SEQ ID NO: 18 и вариабельную область легкой цепи, содержащую SEQ ID NO: 20; вариабельную область тяжелой цепи, содержащую SEQ ID NO: 22 и вариабельную область легкой цепи, содержащую SEQ ID NO: 24; вариабельную область тяжелой цепи, содержащую SEQ ID NO: 26 и вариабельную область легкой цепи, содержащую SEQ ID NO: 28; вариабельную область тяжелой цепи, содержащую SEQ ID NO: 30 и вариабельную область легкой цепи, содержащую SEQ ID NO: 32; вариабельную область тяжелой цепи, содержащую SEQ ID NO: 34 и вариабельную область легкой цепи, содержащую SEQ ID NO: 36; или вариабельную область тяжелой цепи, содержащую SEQ ID NO: 38 и вариабельную область легкой цепи, содержащую SEQ ID NO: 40.
[0028] В одном варианте реализации настоящее изобретение обеспечивает химерное анти-PD-L1 антитело, причем антитело содержит тяжелую цепь, имеющую аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 50, 54, 58, 60, 64, и 66, и легкой цепи, имеющей аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 52, 56, 62 и 68.
[0029] В одном варианте реализации настоящее изобретение обеспечивает гуманизированное анти-PD-L1 антитело, причем антитело содержит вариабельную область тяжелой цепи, имеющую аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 42 и 46. В другом варианте реализации настоящее изобретение обеспечивает гуманизированное анти-PD-L1 антитело, причем антитело содержит вариабельную область легкой цепи, имеющую аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 44 и 48.
[0030] В другом варианте реализации настоящее изобретение обеспечивает гуманизированное анти-PD-L1 антитело, причем антитело содержит вариабельную область тяжелой цепи, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с SEQ ID NO: 42 и вариабельной области легкой цепи, имеющей по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с SEQ ID NO: 44. В другом варианте реализации настоящее изобретение обеспечивает гуманизированное анти-PD-L1 антитело, причем антитело содержит вариабельную область тяжелой цепи, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с SEQ ID NO: 46 и вариабельной области легкой цепи, имеющей по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с SEQ ID NO: 48.
[0031] В одном варианте реализации настоящее изобретение обеспечивает гуманизированное анти-PD-L1 антитело, причем антитело содержит полную тяжелую цепь, имеющую аминокислотную последовательность, имеющую по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 70, 72, 76 и 78. В другом варианте реализации настоящее изобретение обеспечивает гуманизированное анти-PD-L1 антитело, причем антитело содержит полную легкую цепь, имеющую аминокислотные последовательности, имеющие по меньшей мере 80% гомологии, по меньшей мере 85% гомологии, по меньшей мере 90% гомологии, по меньшей мере 91% гомологии, по меньшей мере 92% гомологии, по меньшей мере 93% гомологии, по меньшей мере 94% гомологии, по меньшей мере 95% гомологии, по меньшей мере 96% гомологии, по меньшей мере 97% гомологии, по меньшей мере 98% гомологии, или по меньшей мере 99% гомологии с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 74 и 80.
[0032] В одном варианте реализации настоящее изобретение обеспечивает гуманизированное анти-PD-L1 антитело, причем антитело содержит тяжелую цепь в соответствии с SEQ ID NO: 70 и легкую цепь в соответствии с SEQ ID NO: 74. В другом варианте реализации настоящее изобретение обеспечивает гуманизированное анти-PD-L1 антитело, причем антитело содержит тяжелую цепь в соответствии с SEQ ID NO: 72 и легкую цепь в соответствии с SEQ ID NO: 74. В другом варианте реализации настоящее изобретение обеспечивает гуманизированное анти-PD-L1 антитело, причем антитело содержит тяжелую цепь в соответствии с SEQ ID NO: 76 и легкую цепь в соответствии с SEQ ID NO: 80. В другом варианте реализации настоящее изобретение обеспечивает гуманизированное анти-PD-L1 антитело, причем антитело содержит тяжелую цепь в соответствии с SEQ ID NO: 78 и легкую цепь в соответствии с SEQ ID NO: 80.
[0033] В одном варианте реализации настоящее изобретение обеспечивает анти-PD-L1 антитело или его фрагменты, которые связываются с тем же эпитопом на PD-L1, как и любое из иллюстративных антител, предложенное в данном документе. В одном варианте реализации изобретения антитела или их фрагменты конкурируют с любым из иллюстративных антител, предложенных в данном документе для связывания с PD-L1. Связывание с PD-L1 может быть измерено ИФА (иммуноферментным анализом), проточной цитометрией, поверхностным плазмонным резонансом (ППР), или любым другим способом, известным в данной области техники.
[0034] В одном варианте реализации настоящее изобретение обеспечивает анти-PD-L1 антитела и их фрагменты, которые связываются с PD-L1 с аффинностью связывания kD от около 10 нмоль/л до около 0,01 нмоль/л. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, связываются с PD-L1 с аффинностью связывания kD от около 10 нмоль/л до около 0,05 нмоль/л. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, связываются с PD-L1 с аффинностью связывания kD от около 8 нмоль/л до около 0,1 нмоль/л. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, связываются с PD-L1 с аффинностью связывания kD от около 5 нмоль/л до около 0,2 нмоль/л. В другом варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, связываются с PD-L1 с аффинностью связывания kD около 10 нмоль/л или менее. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, связываются с PD-L1 с аффинностью связывания kD около 6 нмоль/л или менее. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, связываются с PD-L1 с аффинностью связывания kD около 4 нмоль/л или менее. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, связываются с PD-L1 с аффинностью связывания kD около 2 нмоль/л или менее. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, связываются с PD-L1 с аффинностью связывания kD около 1 нмоль/л или менее. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, связываются с PD-L1 с аффинностью связывания kD около 0,75 нмоль/л или менее. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, связываются с PD-L1 с аффинностью связывания kD около 0,5 нмоль/л или менее. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, связываются с PD-L1 с аффинностью связывания kD около 0,25 нмоль/л или менее. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, связываются с PD-L1 с аффинностью связывания kD около 0,2 нмоль/л или менее. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, связываются с PD-L1 с аффинностью связывания kD около 0,15 нмоль/л или менее. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, связываются с PD-L1 с аффинностью связывания kD около 0,1 нмоль/л или менее. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, связываются с PD-L1 с аффинностью связывания kD около 0,075 нмоль/л или менее. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, связываются с PD-L1 с аффинностью связывания kD около 0,05 нмоль/л или менее. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, связываются с PD-L1 с аффинностью связывания kD около 0,025 нмоль/л или менее. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, связываются с PD-L1 с аффинностью связывания kD около 0,02 нмоль/л или менее. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, связываются с PD-L1 с аффинностью связывания kD около 0,015 нмоль/л или менее. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, связываются с PD-L1 с аффинностью связывания kD около 0,01 нмоль/л или менее. В одном варианте реализации изобретения аффинность связывания kD анти-PD-L1 антител и фрагментов, предложенных в данном документе, измеряют с использованием анализа Biacore.
[0035] В одном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, имеют ЭК50 (полумаксимальная эффективная концентрация) связывания для PD-L1 от около от 1 нг/мл до около 2000 нг/мл. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, имеют ЭК50 связывания для PD-L1 от около от 1 нг/мл до около 1500 нг/мл. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, имеют ЭК50 связывания для PD-L1 от около 1 нг/мл до около 1000 нг/мл. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, имеют ЭК50 связывания для PD-L1 от около 2 нг/мл до около 500 нг/мл. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, имеют ЭК50 связывания для PD-L1 от около 2 нг/мл до около 250 нг/мл. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, имеют ЭК50 связывания для PD-L1 от около 5 нг/мл до около 200 нг/мл. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, имеют ЭК50 связывания для PD-L1 от около 5 нг/мл до около 50 нг/мл. В одном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, имеют ЭК50 связывания для PD-L1 около 500 нг/мл или менее, около 400 нг/мл или менее, около 300 нг/мл или менее, около 250 нг/мл или менее, около 200 нг/мл или меньше, около 150 нг/мл или менее, около 100 нг/мл или менее, около 75 нг/мл или менее, около 60 нг/мл или менее, около 50 нг/мл или менее, около 40 нг/мл или менее, или около 30 нг/мл или менее. В одном варианте реализации изобретения ЭК50 анти-PD-L1 антител и их фрагментов, предложенных в данном документе, измеряли с использованием ИФА или проточной цитометрией.
[0036] В одном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, ингибируют связывание PDL1/PD-1 с ИК50 (концентрация полумаксимального ингибирования) от около 1 нг/мл до около 1500 нг/мл. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, ингибируют связывание PDL1/PD-1 с ИК50 от около 2 нг/мл до около 1200 нг/мл. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, ингибируют связывание PD-L1/PD-1 с ИК50 от около 5 нг/мл до около 500 нг/мл. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, ингибируют связывание PDL1/PD-1 с ИК50 от около 5 нг/мл до около 100 нг/мл. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, ингибируют связывание PD-L1/PD-1 с ИК50 от около 10 нг/мл до около 50 нг/мл. В одном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, ингибируют связывание PDL1/PD-1 с ИК50 около 1200 нг/мл или менее, около 1000 нг/мл или менее, около 800 нг/мл или менее, около 400 нг/мл или менее, около 300 нг/мл или менее, около 250 нг/мл или менее, около 200 нг/мл или меньше, около 150 нг/мл или менее, около 100 нг/мл или менее, около 75 нг/мл или менее, около 60 нг/мл или менее, около 50 нг/мл или менее, около 40 нг/мл или менее, около 30 нг/мл или менее, около 20 нг/мл или менее, или около 10 нг/мл или менее. В одном варианте реализации изобретения ИК50 анти-PD-L1 антител и их фрагментов, предложенных в данном документе, измеряли с использованием ИФА или проточной цитометрией.
[0037] В одном варианте реализации изобретения анти-PD-L1 антитело, предложенное в данном документе, представляет собой гуманизированное антитело, имеющее аминокислотную последовательность вариабельной области тяжелой цепи в соответствии с SEQ ID NO: 42 и аминокислотную последовательность вариабельной области легкой цепи в соответствии с SEQ ID NO: 44; или имеющее аминокислотную последовательность вариабельной области тяжелой цепи в соответствии с SEQ ID NO: 46 и аминокислотную последовательность вариабельной области легкой цепи в соответствии с SEQ ID NO: 48; причем анти-PD-L1 антитело имеет ЭК50 связывания PD-L1 около 200 нг/мл или менее, или около 150 нг/мл или менее, или около 100 нг/мл или менее, или около 80 нг/мл или менее, или около 60 нг/мл или менее, или около 50 нг/мл или менее, как измерено с помощью ИФА или проточной цитометрией. В другом варианте реализации изобретения анти-PD-L1 антитело, предложенное в данном документе, представляет собой гуманизированное антитела, имеющее аминокислотную последовательность вариабельной области тяжелой цепи в соответствии с SEQ ID NO: 42 и аминокислотную последовательность вариабельной области легкой цепи в соответствии с SEQ ID NO: 44; или имеющее аминокислотную последовательность вариабельной области тяжелой цепи в соответствии с SEQ ID NO: 46 и аминокислотную последовательность вариабельной области легкой цепи в соответствии с SEQ ID NO: 48; причем анти-PD-L1 антитело имеет ИК50 блокирования PDL1/PD-1 около 1200 нг/мл или менее, или около 1000 нг/мл или менее, или около 800 нг/мл или менее, или около 600 нг/мл или менее, или около 500 нг/мл или менее, или около 400 нг/мл или менее, или около 300 нг/мл или менее, или около 200 нг/мл или менее, или около 100 нг/мл или менее, или около 60 нг/мл или менее, или около 30 нг/мл или менее, или около 25 нг/мл или менее, или около 20 нг/мл или менее, или около 10 нг/мл или менее, как измерено с помощью ИФА или проточной цитометрией. В другом варианте реализации изобретения анти-PD-L1 антитело, предложенное в данном документе, представляет собой гуманизированное антитела, имеющее аминокислотную последовательность вариабельной области тяжелой цепи в соответствии с SEQ ID NO: 42 и аминокислотную последовательность вариабельной области легкой цепи в соответствии с SEQ ID NO: 44; или имеющее аминокислотную последовательность вариабельной области тяжелой цепи в соответствии с SEQ ID NO: 46 и аминокислотную последовательность вариабельной области легкой цепи в соответствии с SEQ ID NO: 48; причем анти-PD-L1 антитело имеет аффинность связывания kD для PD-L1 около 10 нмоль/л или менее, или около 5 нмоль/л или менее, или около 2 нмоль/л или менее, или около 1 нмоль/л или менее, или около 0,5 нмоль/л или менее, или около 0,1 нмоль/л или менее, или около 0,05 нмоль/л или менее, как измерено с помощью анализа Biacore. В одном варианте реализации изобретения гуманизированное анти-PD-L1 антитело имеет аффинность связывания kD для PD-L1 около 2 нмоль/л. В другом варианте реализации изобретения гуманизированное анти-PD-L1 антитело имеет аффинность связывания kD для PD-L1 около 1 нмоль/л. В другом варианте реализации изобретения гуманизированное анти-PD-L1 антитело имеет аффинность связывания kD для PD-L1 около 0,5 нмоль/л. В другом варианте реализации изобретения гуманизированное анти-PD-L1 антитело имеет аффинность связывания kD для PD-L1 около 0,1 нмоль/л.
[0038] В другом варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, связываются с PD-L1, нарушая взаимодействие PD-1/PD-L1 и приводя к повышению Т-клеточной активации. В дополнительном варианте реализации изобретения антитела и их фрагменты связывают PD-L1 и приводят к увеличению Т-клеточной пролиферации и/или продукции цитокинов. Еще в дополнительном варианте реализации изобретения антитела и их фрагменты связывают PD-L1 и приводят к повышению одного или более цитокинов, выбранных из группы, состоящей из ИЛ-2, ИФН-γ, ФНО, ИЛ-1, ИЛ-4, ИЛ-5, ИЛ-6, ИЛ-12, ИЛ-13, ИЛ-17, и ГМ-КСФ (гранулоцитарно-моноцитарный колониестимулирующий фактор). Таким образом, в одном аспекте настоящее изобретение относится к способам модуляции иммунного ответа, включающие контактирование Т-клеток и антигенпрезентирующих клеток с анти-PD-L1 антителом или его фрагментом. В одном варианте реализации изобретения модуляция иммунного ответа с помощью анти-PD-L1 антител и фрагментов, предложенных в данном документе, может быть измерена в реакции смешанной культуры лимфоцитов (СКЛ-реакция). В одном варианте реализации изобретения анти-PD-L1 антитела, предложенные в данном документе, повышают уровень продукции цитокинов из лимфоцитов в СКЛ-реакции. В дополнительном варианте реализации изобретения анти-PD-L1 антитела повышают уровень продукции ИЛ-2 и/или продукции ИФН-(в СКЛ-реакции. Еще в дополнительном варианте реализации изобретения анти-PD-L1 антитела повышают уровень продукции ИЛ-2 и продукции ИФН-(в СКЛ-реакции. В одном варианте реализации изобретения анти-PD-L1 антитела усиливают ответы Т-клеток памяти. В дополнительном варианте реализации изобретения анти-PD-L1 антитела усиливают ответы Т-клеток памяти, как измерено повышением продукции ИФН-(из Т-клеток памяти.
[0039] В одном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, ингибируют функцию регуляторных Т-клеток. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты подавляют супрессию эффекторных Т-клеток посредством регуляторных T-клеток. В другом варианте реализации изобретения анти-PD-L1 антитела и их фрагменты восстанавливают функции эффекторных Т-клеток в присутствии регуляторных T-клеток. В дополнительном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты восстанавливают способность эффекторных Т-клеток пролиферировать и вырабатывать цитокины в присутствии регуляторных T-клеток. Таким образом, в одном варианте реализации настоящее изобретение обеспечивает способ ингибирования супрессорного действия регуляторных Т-клеток в условиях in vitro или у субъекта, который нуждается в этом.
[0040] В одном аспекте предложено выделенное антитело или его фрагмент, который связывается с PD-L1, причем антитело продуцируется гибридомой, выбранной из группы, состоящей из гибридом, называемых в данном документе 13C5, 5G9, 5G11, 8C6, 7B4, 4D1, 4A8, 8H4, 8H3, и 15F1. Таким образом, настоящее изобретение также охватывает гибридомы: 13C5, 5G9, 5G11, 8C6, 7B4, 4D1, 4A8, 8H4, 8H3, и 15F1, а также любые гибридомы, продуцирующие антитела, раскрытые в данном документе. Настоящее изобретение также обеспечивает выделенные полинуклеотиды, кодирующие антитела и их фрагменты, предложенные в данном документе. Векторы экспрессии, содержащие выделенные полинуклеотиды, и клетки-хозяина, содержащие такие векторы экспрессии, также охватываются настоящим изобретением.
[0041] В одном варианте реализации настоящее изобретение обеспечивает иммуноконъюгаты анти-PD-L1 антитела. Таким образом, настоящее изобретение обеспечивает антитело или его фрагмент, который связывается с PD-L1 и который связан или конъюгирован с терапевтическим агентом. Терапевтические агенты, которые могут быть связаны или конъюгированы с анти-PD-L1 антителом могут включать, но не ограничиваясь ими, цитостатики, радиоактивные изотопы, иммуномодуляторы или антитела.
[0042] В одном аспекте настоящее изобретение обеспечивает композиции, содержащие одно или более анти-PD-L1 антитело или его фрагмент, предложенный в данном документе, и фармацевтически приемлемый носитель.
[0043] В одном аспекте настоящее изобретение обеспечивает способы модуляции иммунного ответа у субъекта, причем способ, включающий введение субъекту терапевтически эффективного количества анти-PD-L1 антитела или его фрагмента, предложенного в данном документе. В одном варианте реализации настоящее изобретение обеспечивает способы лечения или профилактики заболевания или расстройства у субъекта, который нуждается в этом, включающие введение субъекту терапевтически эффективного количества анти-PD-L1 антитела или его фрагмента, предложенного в данном документе.
[0044] В одном варианте реализации настоящее изобретение обеспечивает способ усиления противоопухолевых ответов у субъекта, который нуждается в этом, включающий введение субъекту терапевтически эффективного количества анти-PD-L1 антитела или фрагмента согласно настоящему изобретению. В другом варианте реализации настоящее изобретение обеспечивает способ уменьшения опухолей или ингибирования роста опухолевых клеток у субъекта, который нуждается в этом, включающий введение субъекту терапевтически эффективного количества анти-PD-L1 антитела или фрагмента согласно настоящему изобретению. В другом варианте реализации настоящее изобретение обеспечивает способ лечения рака у субъекта, который нуждается в этом, включающий введение субъекту терапевтически эффективного количества анти-PD-L1 антитела или фрагмента согласно настоящему изобретению. В дополнительном варианте реализации изобретения рак выбран из группы, состоящей из лимфомы, лейкемии, меланомы, глиомы, рака молочной железы, рака легкого, рака толстой кишки, рака кости, рака яичника, рака мочевого пузыря, рака почки, рака печени, рака желудка, рака прямой кишки, рака яичек, рака слюнной железы, рака щитовидной железы, рака тимуса, эпителиального рака, рака головы или шеи, рака желудочно-кишечного тракта, рака поджелудочной железы, или их комбинации.
[0045] В другом варианте реализации настоящее изобретение обеспечивает способ лечения инфекционного заболевания у субъекта, который нуждается в этом, включающий введение субъекту терапевтически эффективного количества анти-PD-L1 антитела или фрагмента согласно настоящему изобретению. В дополнительном варианте реализации изобретения инфекционное заболевание выбрано из группы, состоящей из кандидоза, кандидемии, аспергиллеза, стрептококковой пневмонии, стрептококковых кожных и орофарингеальных заболеваний, грамотрицательного сепсиса, туберкулеза, мононуклеоза, гриппа, респираторного заболевания, вызванного респираторно-синцитиальным вирусом, малярии, шистосомоза и трипаносомиаза.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[0046] На Фиг. 1a-г проиллюстрирован набор графиков, отражающих связывание мышиных анти-PD-L1 гибридомных антител с PD-L1 в диапазоне концентраций антител, как измерено посредством с помощью ИФА. Связывание гибридомных антител 8H3-mIgG (m8H3), 15F1-mIgG (m15F1), 5G9-mIgG (m5G9) и 4A8-mIgG (m4A8) проиллюстрировано на Фиг. 1а. Связывание гибридомных антител 5G11-mIgG (m5G11), 7B4-mIgG (m7B4), 4D1-mIgG (m4D1) и 8H4-mIgG (m8H4) проиллюстрировано на Фиг. 1б. Связывание гибридомного антитела 8C6-mIgG (m8C6) проиллюстрировано на Фиг. 1в. Связывание гибридомного антитела 13C5-mIgG (m13C5) проиллюстрировано на Фиг. 1 г. На каждой из Фиг. 1а-1 г, связывание mIgG1 проиллюстрировано как отрицательный контроль.
[0047] На Фиг. 2a-в проиллюстрирован набор графиков, отражающих связывание химерных анти-PD-L1 антител с PD-L1 в диапазоне концентраций, как измерено посредством с помощью ИФА. Связывание химерных антител ch5G11-hIgG4 и ch5G11-hIgG1 проиллюстрировано на Фиг. 2a. Связывание химерных антител ch13C5-hIgG4, ch13C5-hIgG1 и ch8H4-hIgG4 проиллюстрировано на Фиг. 2б. Связывание химерного антитела ch8C6-hIgG4 проиллюстрировано на Фиг. 2в. На каждой из Фиг. 2a-2в, связывание hIgG4 проиллюстрировано как отрицательный контроль.
[0048] На Фиг. 3a-б проиллюстрирован набор графиков, отражающих связывание гуманизированных анти-PD-L1 антител с PD-L1 в диапазоне концентраций антител, как измерено с помощью ИФА. Связывание контрольного hIgG4 и гуманизированных антител hu5G11-hIgG1 и hu5G11-hIgG4 проиллюстрировано на Фиг. 3a. Связывание контрольного hIgG4 и гуманизированных антител hu13C5-hIgG1 и hu13C5-hIgG4 проиллюстрировано на Фиг. 3б.
[0049] На Фиг. 4a-в проиллюстрирован набор графиков, отражающих блокирование взаимодействия PD-1/PD-L1 с помощью гибридомных анти-PD-L1 антител в диапазоне концентраций антител, как измерено с помощью ИФА. Блокирование связывания PD-1/PD-L1 с помощью гибридомных антител 13C5-mIgG (m13C5), 8C6-mIgG (m8C6), 5G9-mIgG (m5G9) и 4A8-mIgG (m4A8) по сравнению с контрольным mIgG1 проиллюстрировано на Фиг. 4a. Блокирование связывания PD-1/PD-L1 с помощью гибридомных антител 5G11-mIgG (m5G11), 7B4-mIgG (m7B4), 4D1-mIgG (m4D1) и 8H4-mIgG (m8H4) по сравнению с контрольным mIgG1 проиллюстрировано на Фиг. 4б. Блокирование связывания PD-1/PD-L1 с помощью гибридомных антител 8H3-mIgG (m8H3) и 15F1-mIgG (m15F1) по сравнению с контрольным mIgG1 проиллюстрировано на Фиг. 4в.
[0050] На Фиг. 5a-в проиллюстрирован набор графиков, отражающих блокирование взаимодействия PD-1/PD-L1 с помощью химерных анти-PD-L1 антител в диапазоне концентраций антител, как измерено с помощью ИФА. Блокирование связывания PD-1/PD-L1 с помощью химерных антител ch5G11 hIgG4 и ch5G11 hIgG1 по сравнению с контрольным hIgG4 проиллюстрировано на Фиг. 5a. Блокирование связывания PD-1/PD-L1 с помощью химерных антител ch8C6-hIgG4 по сравнению с контрольным hIgG4 проиллюстрировано на Фиг. 5б. Блокирование связывания PD-1/PD-L1 с помощью химерных антител ch8H4-hIgG4, ch13C5-hIgG1 и ch13C5-hIgG4 по сравнению с контрольным hIgG4 проиллюстрировано на Фиг. 5в.
[0051] На Фиг. 6a-б проиллюстрирован набор графиков, отражающих блокирование взаимодействия PD-1/PD-L1 гуманизированными анти-PD-L1 антителами в диапазоне концентраций антител, как измерено с помощью ИФА. Блокирование связывания PD-1/PD-L1 с помощью контрольного hIgG4 и гуманизированных антител 5G11-hIgG1 и 5G11-hIgG4 проиллюстрировано на Фиг. 6a. Блокирование связывания PD-1/PD-L1 с помощью контрольного hIgG4 и гуманизированных антител 13C5-hIgG1 и 13C5-hIgG4 проиллюстрировано на Фиг. 6б.
[0052] На Фиг. 7a и 7б проиллюстрировано связывание гибридомных анти-PD-L1 антител с PD-L1 в диапазоне концентраций антител, как измерено с помощью проточной цитометрии. Связывание (как измерено при помощи анализа средней интенсивности флуоресценции) гибридомных антител 4A8, 15F1, 4D1, 13C5, 8H4 и 8H3 по сравнению с контрольным антителом mIgG1 проиллюстрировано на Фиг. 7a. Связывание (как измерено при помощи анализа средней интенсивности флуоресценции) гибридомных антител 5G11, 8C6, 5G9 или 7B4 по сравнению с контрольным антителом mIgG1 проиллюстрировано на Фиг. 7б.
[0053] На Фиг. 8 показано связывание химерных анти-PD-L1 антител с PD-L1 в диапазоне концентраций антител, как измерено с помощью проточной цитометрии. Проиллюстрировано связывание контрольного антитела hIgG4 и химерных антител ch13C5-hIgG1, ch5G11-hIgG1 и ch5G11-hIgG4.
[0054] На Фиг. 9 проиллюстрировано связывание гуманизированных анти-PD-L1 антител с PD-L1 в диапазоне концентраций антител, как измерено с помощью проточной цитометрии. Проиллюстрировано связывание контрольного антитела hIgG4 и гуманизированных антител hu13C5-hIgG1, hu13C5-hIgG4, hu5G11-hIgG1 и hu5G11-hIgG4.
[0055] На Фиг. 10a и 10б проиллюстрировано блокирование взаимодействия PD-1/PD-L1 с помощью гибридомных анти-PD-L1 антител в диапазоне концентраций антител, как измерено с помощью проточной цитометрии. Блокирование связывания PD-1/PD-L1 с помощью контрольного антитела mIgG1 и гибридомных антител m4D1, m5G11, m13C5, m7B4 и m8H4 проиллюстрировано на Фиг. 10a. Блокирование связывания PD-1/PD-L1 с помощью контрольного антитела mIgG1 и гибридомных антител m4A8, m5G9, m8C6, m8H3 и m15F1 проиллюстрировано на Фиг. 10б.
[0056] На Фиг. 11 проиллюстрировано блокирование взаимодействия PD-1/PD-L1 в диапазоне концентраций контрольного антитела hIgG4 или химерных анти-PD-L1 антител ch8C6-hIgG4, ch5G11-hIgG1, ch5G11-hIgG4, ch13C5-hIgG1, ch13C5-hIgG4 или ch8H4-hIgG4, как измерено с помощью проточной цитометрии.
[0057] На Фиг. 12 проиллюстрировано блокирование взаимодействия PD-1/PD-L1 в диапазоне концентраций контрольного антитела hIgG4 или гуманизированных антител hu13C5-hIgG1, hu13C5-hIgG4, hu5G11-hIgG1 или hu5G11-hIgG4, как измерено с помощью проточной цитометрии.
[0058] На Фиг. 13a проиллюстрирован график, демонстрирующий выработку ИЛ-2 (пг/мл) в СКЛ-реакции в ответ на различные концентрации гибридомных анти-PD-L1 антител. На Фиг. 13б проиллюстрирован график, демонстрирующий выработку ИФН-((пг/мл) в СКЛ-реакции в ответ на различные концентрации гибридомных анти-PD-L1 антител. Как на Фиг. 13a, так и на 13б, проиллюстрированы протестированные антитела (слева направо): контрольное mIgG1, m8C6, m4D1, m5G11, m7B4, m8H4, m5G9, m13C5, m8H3 и m15F1. В качестве отрицательных контролей также были включены клеточные стенки только T-клетки и/или только ДК (дендритная клетка). Как проиллюстрировано на оси х на Фиг. 13а и 13б каждое антитело было протестировано при 20 мкг/мл, 2 мкг/мл, 0,2 мкг/мл, 0,02 мкг/мл и 0,002 мкг/мл.
[0059] На Фиг. 14a проиллюстрирован график, демонстрирующий выработку ИЛ-2 (пг/мл) в СКЛ-реакции в ответ на различные концентрации химерных анти-PD-L1 антител. На Фиг. 14б проиллюстрирован график, демонстрирующий выработку ИФН-((пг/мл) в СКЛ-реакции в ответ на различные концентрации химерных анти-PD-L1 антител. Как на Фиг. 14a, так и на 14б, проиллюстрированы протестированные антитела (слева направо): контрольное hIgG4, химерное 8C6-hIgG4, химерное 8H4-hIgG4, химерное 5G11-hIgG4, и химерное 13C5-hIgG1. Как проиллюстрировано на оси х на Фиг. 14а и 14б, каждое антитело было протестировано при 20 мкг/мл, 2 мкг/мл, 0,2 мкг/мл, 0,02 мкг/мл и 0,002 мкг/мл.
[0060] На Фиг. 15a проиллюстрирован график, демонстрирующий выработку ИЛ-2 (пг/мл) в СКЛ-реакции в ответ на различные концентрации гуманизированных анти-PD-L1 антител. На Фиг. 15б проиллюстрирован график, демонстрирующий выработку ИФН-((пг/мл) в СКЛ-реакции в ответ на различные концентрации гуманизированных анти-PD-L1 антител. Как на Фиг. 15a, так и на 15б, проиллюстрированы протестированные антитела (слева направо): контрольное hIgG4, hu13C5-hIgG1, hu13C5-hIgG4, hu5G11-hIgG1 и hu5G11-hIgG4. Как проиллюстрировано на оси х на Фиг. 15а и 15б, каждое антитело было протестировано при 20 мкг/мл, 2 мкг/мл, 0,2 мкг/мл, 0,02 мкг/мл и 0,002 мкг/мл.
[0061] На Фиг. 16 проиллюстрировано влияние химерных (ch) или гуманизированных (hu) анти-PD-L1 антител на Tрег-опосредованное (регуляторными Т-клетками) ингибирование продуцирования ИФН-((пг/мл) в аллогенной СКЛ-реакции с CD4+CD25+регуляторными T-клетками, CD4+CD25- Т-клетками, и дендритными клетками. Протестированные антитела представлены (слева направо): контрольное hIgG4, ch13C5-hIgG1, ch13C5-hIgG4, hu13C5-hIgG1, hu13C5-hIgG4, ch5G11-hIgG1, ch5G11-hIgG4, hu5G11-hIgG1 и hu5G11-hIgG4.
[0062] На Фиг. 17 проиллюстрировано продуцирование ИФН-((пг/мл) из Т-клеток в ответ на костимуляцию аутологичными ДК и анти-СD3 антителом, в присутствии гуманизированного анти-PD-L1 антитела (hu13C5-hIgG1, hu13C5-hIgG4, hu5G11-hIgG1 или hu5G11-hIgG4), изотип контрольного антитела (hIgG4) или в отсутствии антитела.
[0063] На Фиг. 18a и 18б проиллюстрировано влияние гуманизированных анти-PD-L1 антител на имунный ответ Т-клеток, повторно вызванный тетанотоксином, как измерено с помощью анализа выработки ИФН-((пг/мл). Отрицательный контроль hIgG4 или гуманизированное антитело hu13C5-hIgG1, hu13C5-hIgG4, hu5G11-hIgG1 или hu5G11-hIgG4 были протестированы при следующих концентрациях: 20 мкг/мл, 2 мкг/мл, 0,2 мкг/мл, 0,02 мкг/мл и 0,002 мкг/мл.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0064] Взаимодействия PD1/PDL1 ингибируют сигналинг Т-клеточного рецептора путем рекрутинга фосфатаз SHP1 и SHP2, которые препятствуют сигналингу ТКР (Chemnitz et al.(2004) J.Immunol.17: 945-954). PD-L1 может не только способствовать прогрессированию опухоли путем ингибирования PD1-экспрессирующих иммунных эффекторов, но также модулировать клеточный иммунитет при некоторых инфекционных заболеваниях (Mueller et al.(2010) J.Clin.Invest.120: 2508-2515). Кроме того, аллогенные эффекторные Т-клеточные иммунные реакции восприимчивы к модуляции сигнального пути PD-1 в отторжении трансплантата (Lee et al.(2003) J.Immunol.171: 6929-6935). Таким образом, взаимодействие PD-1 с PD-L1 оказывает жизненно важный и широкий спектр иммунорегуляторных функций в активации Т-клеток, толерантности и иммуноопосредованном повреждении тканей. Тем не менее, взаимодействие может быть изменено путем блокирования локального связывания PD-1 с PD-L1 (Iwai et al.(2002) Proc.Nat'l.Acad Sci.USA 99: 12293-7; Brown et al.(2003) J.Immunol.170: 1257-66).
[0065] Было установлено, что PD-1 коррелирует с ростом и развитием рака из-за его роли в защите опухолевых клеток от эффективного иммунного лизиса. Было выявлено, что его лиганд, PD-L1, имеет сильную экспрессию в ряде мышиных и человеческих опухолей, и как предполагается опосредует ускользание от иммунного надзора (Iwai, Y. et al.,Proc.Natl.Acad.Sci.USA.99: 12293-12297 (2002); Strome S.E. et al., Cancer Res.,63: 6501-6505 (2003); Dong et al.(2002) Nat.Med.8: 787-9). В организме человека экспрессия PD-1 (на проникающих в опухоль лимфоцитах) и/или PD-L1 (на опухолевых клетках) была обнаружено в ряде биопсий первичных опухолей, как было оценено с помощью иммуногистохимии. Такие ткани включают рак легкого, печени, яичника, шейки матки, кожи, толстой кишки, глиомы, мочевого пузыря, молочной железы, почки, пищевода, желудка, сквамозные клетки ротовой полости, уротелиальные клетки и рак поджелудочной железы, а также опухоли головы и шеи (Brown J.A.et al.,J.Immunol.170: 1257-1266 (2003); Dong H. et al.,Nat.Med.8: 793-800 (2002); Wintterle et al.,Cancer Res.63: 7462-7467 (2003); Strome S.E. et al.,Cancer Res.,63: 6501-6505 (2003); Thompson R.H. et al., Cancer Res.66: 3381-5(2006); Thompson et al.,Clin.Cancer Res.13: 1757-61(2007); Nomi T. et al., Clin.Cancer Res.13: 2151-7.(2007)). Более поразительно то, что экспрессия лиганда PD-1 на опухолевых клетках коррелирует с плохим прогнозом у больных раком при различных видах опухолей (обзор OkaZaki and Honjo, Int.Immunol.19: 813-824 (2007)).
[0066] Несмотря на то, что взаимодействие между PD-1 и PD-L1 приводит к снижению уровня лимфоцитов, проникающих в опухолевые ткани, снижению пролиферации, опосредованной Т-клеточным рецептором, и ускользанию от иммунного надзора раковых клеток (Dong et al.(2003) J.Mol.Med.81: 281-7; Blank et al.(2005) Cancer Immunol. Immunother.54: 3 07-3 14; Konishi et al.(2004) Clin.Cancer Res.10: 5094-100), было соответствующим образом показано, что блокирование взаимодействия PD-1/PD-L1 повышает опухолеспецифический Т-клеточный иммунитет и является полезным в клиренсе опухолевых клеток с помощью иммунной системы. В мышиной модели агрессивного рака поджелудочной железы, например, Nomi T., et al.(Clin.Cancer Res.13: 2151-2157, 2007) продемонстрирована терапевтическая эффективность блокирования PD-1/PD-L1. Введение или PD-1-, или PD-L1-направленного антитела значительно ингибирует рост опухоли. Блокирование антителом эффективно способствовало опухолереактивной CD8+Т-клеточной инфильтрации в опухоль, приводя к повышению противоопухолевых эффекторов, включая ИФН-γ, гранзим B и перфорин. Кроме того, авторы показали, что блокирование PDL1/PD-1 может быть эффективно в комбинации с химиотерапией для достижения синергетического эффекта. В другом исследовании с использованием модели плоскоклеточной карциномы у мышей, блокирование антителами PD-1 или PD-L1 существенно ингибировало рост опухоли (Tsushima F. et al., Oral Oncol.42: 268-274 (2006)).
[0067] Кроме того, трансфекция линии мышиной мастоцитомы при использовании PD-L1 приводила к снижению лизиса опухолевых клеток при совместном культивировании с опухолеспецифическим клоном CTL (цитотоксический Т-лимфоцит). Лизис был восстановлен после добавления анти-PD-L1 мкАТ (моноклональных антител) (Iwai Y. et al.,Proc.Natl.Acad.Sci.USA.99: 12293-12297 (2002)). Было показано, что в условиях in vivo блокирование взаимодействия PD1/PD-L1 повышает эффективность терапии с применением адоптивного переноса T-клеток в мышиной модели опухоли (Strome S.E. et al., Cancer Res.63: 6501-6505 (2003)). Еще одно подтверждение роли PD-1 в лечении рака происходит из экспериментов, выполненных с PD-1-нокаутированными мышами. PD-L1-экспрессирующие миеломные клетки росли только у животных дикого типа (приводя к росту опухоли и связанного с ним гибели животных), но не у PD-1-дефицитных мышей (Iwai Y., et al.,Proc.Natl.Acad.Sci.USA.99: 12293-12297(2002)). В клинических исследованиях, R.M. Wong et al.(Int.Immunol.19: 1223-1234 (2007)) показано, что блокирование PD-1 с применением полностью человеческого анти-PD-1 антитела, дополненного неименованным числом опухолеспецифических CD8+Т-клеток (CTL) в анализах по стимуляции в условиях ex vivo с помощью вакцинных антигенов и клеток от вакцинированных индивидуумов. В аналогичном исследовании, блокирование антителом PD-L1 привело к повышению цитолитической активности, ассоциированных с опухолью антигенспецифичных цитотоксических Т-клеток, и повышению выработки цитокинов опухолеспецифическими T-хелперами (Blank C. et al., Int. J.Cancer 119: 317-327 (2006)). Те же авторы показали, что блокирование PD-L1 усиливает опухолеспецифические Т-клеточные ответы in vitro при использовании в комбинации с блокированием анти-CTLA-4 (анти-антиген 4 цитотоксических Т-лимфоцитов). В целом, сигнальный путь PD-1/PD-L1 является мишенью для разработки терапевтических антител для лечения рака. Анти-PD-L1 антитела также может быть полезна при хронической вирусной инфекции.CD8+T-клетки памяти, созданные после острой вирусной инфекции, являются высоко функциональными и представляют собой важный компонент защитного иммунитета. Напротив, хронические инфекции часто характеризуются разными степенями функционального нарушения (истощения) вирусоспецифических Т-клеточных ответов, и этот дефект является главной причиной неспособности хозяина устранить устойчивого возбудителя. Хотя функциональные эффекторные Т-клетки первоначально создаются на ранних стадиях инфекции, они постепенно теряют функции в течение хронической инфекции. Barber et al.(Barber et al.,Nature 439: 682-687 (2006)) показали, что у мышей, зараженных лабораторным штаммом ВЛХМ (вирус лимфоцитарного хориоменингита), развилась хроническая инфекция, что привело к высоким уровням вируса в крови и других тканях. У этих мышей первоначально развился эффективный Т-клеточный ответ, но в итоге они поддались инфекции при Т-клеточном истощении. Авторы обнаружили, что снижение числа и функции эффекторных Т-клеток у хронически инфицированных мышей может быть отменено путем введения антител, которые блокируют взаимодействие между PD-1 и PD-L1.
[0068] В одном аспекте настоящее изобретение обеспечивает антитела или их антигенсвязывающие фрагменты, которые связываются с лигандом 1 белка программируемой смерти 1 (PD-L1). В одном варианте реализации изобретения антитела или их фрагменты связываются с человеческим PD-L1. В другом варианте реализации изобретения антитела или их фрагменты связываются с PD-L1 человека и яванского макака. В другом варианте реализации изобретения антитела или их фрагменты блокируют взаимодействие PD-L1 с его рецептором PD-1 на Т-клетках. В одном аспекте настоящее изобретение обеспечивает способы приготовления и применения анти-PD-L1 антител или их фрагментов, а также композиции, содержащие анти-PD-L1 антитела или их фрагменты, в том числе фармацевтические композиции.
[0069] Как используется в данном документе, термин «антитело» относится к связывающему белку, имеющему по меньшей мере один антигенсвязывающий домен. Антитела и их фрагменты согласно настоящему изобретению могут представлять собой полные антитела или их фрагменты. Таким образом, антитела и фрагменты согласно изобретению включают моноклональные антитела или их фрагменты и варианты антител или их фрагментов, а также иммуноконъюгаты. Примеры фрагментов антитела включают Fab-фрагменты, Fab' -фрагменты, F(ab)'-фрагменты, Fv-фрагменты, выделенные CDR- области, одноцепочечных молекул Fv (scFv), и другие фрагменты антител известны в данной области техники. Антитела и их фрагменты могут также включать рекомбинантные полипептиды, слитые белки, и биспецифические антитела. Анти-PD-L1 антитела и их фрагменты, раскрытые в данном документе, могут представлять собой изотип: IgG1, IgG2, IgG3 или IgG4. Термин «изотип» относится к классу антител, кодируемых генами константной области тяжелой цепи. В одном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты, раскрытые в данном документе, имеют изотип IgG1 или IgG4. Антитела и фрагменты к PD-L1 согласно настоящему изобретению могут быть получены из любого вида, включая, но не ограничиваясь ими, мышь, крысу, кролика, примата, ламу и человека. Антитела к PD-L1 и их фрагменты могут быть химерными, гуманизированными или полностью человеческими антителами. В одном варианте реализации изобретения анти-PD-L1 антитела представляют собой антитела, продуцируемые линией гибридомных клеток, полученных с помощью мыши. Таким образом, в одном варианте реализации изобретения анти-PD-L1 антитела представляют собой мышиные антитела. В другом варианте реализации изобретения анти-PD-L1 антитела представляют собой химерные антитела. В дополнительном варианте реализации изобретения химерные антитела представляют собой химерные антитела мыши-человека. В другом варианте реализации изобретения антитела представляют собой гуманизированные антитела. В дополнительном варианте реализации изобретения антитела получены из мышиных антител и являются гуманизированными.
[0070] «Химерное антитело» представляет собой антитело, имеющее по меньшей мере часть вариабельной области тяжелой цепи и по меньшей мере вариабельной области легкой цепи, полученные от одного вида; и по меньшей мере часть константной области, полученной от другого вида. Например, в одном варианте реализации изобретения химерное антитело может включать мышиные вариабельные области и человеческие константные области.
[0071] «Гуманизированное антитело» представляет собой антитело, содержащее области, определяющие комплементарность (CDR), которые являются производными от нечеловеческого антитела; и каркасные области, а также и константные области, которые получены из человеческого антитела. Например, анти-PD-L1 антитела, предложенные в данном документе, могут включать CDR, полученные из одного или более мышиных антител и человеческих каркасных и константных областей. Таким образом, в одном варианте реализации изобретения гуманизированное антитело, предложенное в данном документе, связывается с тем же эпитопом на PD-L1, что и мышиное антитело, из которого получены CDR антитела. Иллюстративные гуманизированные антитела предложены в данном документе. Дополнительные анти-PD-L1 антитела, содержащие CDR тяжелой и легкой цепей, предложенных в данном документе, или их варианты, могут быть созданы с применением любой каркасной последовательности человека, и также охватывается настоящим изобретением. В одном варианте реализации изобретения каркасные последовательности, подходящие для применения в настоящем изобретении, включают те каркасные последовательности, которые являются сходными по структуре с каркасной последовательностью, предложенной в данном документе. Дополнительные модификации в каркасных областях могут быть сделаны для улучшения свойств антител, предложенных в данном документе. Такие дополнительные изменения каркаса могут включать химические модификации; точечные мутации для снижения иммуногенности или удаления Т-клеточных эпитопов; или обратная мутация остатка в исходной последовательности зародышевой линии. В некоторых вариантах реализации изобретения такие модификации включают те, которые связаны с мутациями, иллюстрируемые в данном документе, включая обратную мутацию к последовательности зародышевой линии. Например, в одном варианте реализации изобретения одна или более аминокислот в человеческих каркасных областях VH и/или VL гуманизированных антител, предложенных в данном документе, являются обратно мутировавшими в соответствующие аминокислоты в родительском мышином антителе. В качестве примера, как для VH и VL гуманизированного 5G11 и гуманизированного 13C5, несколько сайтов каркасной аминокислоты вышеупомянутого исходного человеческого антитела являются обратно мутировавшими на соответствующие аминокислотные последовательности в мышиных антителах 5G11 и 13C5. В одном варианте реализации изобретения аминокислота в позиции 53 и/или 60 и/или 67 вариабельной области легкой области являются обратно мутировавшей в соответствующую аминокислоту, обнаруженную в данной позиции вариабельной области легкой цепи мышиного 5G11 или 13C5. В другом варианте реализации изобретения аминокислота в позиции 24 и/или 28 и/или 30 и/или 49 и/или 73 и/или 83 и/или 94 вариабельной области тяжелой цепи являются обратно мутировавшей в соответствующую аминокислоту, обнаруженную в данной позиции вариабельной области тяжелой цепи мышиного 5G11 или 13C5. В одном варианте реализации изобретения гуманизированное антитело 5G11 содержит вариабельную область легкой цепи, причем аминокислота в позиции 60 является мутировавшей из серина (S) в аспарагиновую кислоту (D) и аминокислота в позиции 67 является мутировавшей из серина (S) в тирозин (Y); и вариабельную область тяжелой цепи, причем аминокислота в позиции 24 является мутировавшей из фенилаланина (F) в валин (V), аминокислота в позиции 49 является мутировавшей из аланина (А) в глицин (G), аминокислота в позиции 73 является мутировавшей из треонина (T) в аспарагин (N), и аминокислота в позиции 83 является мутировавшей из треонина (T) в аспарагин (N). В одном варианте реализации изобретения гуманизированное антитело 13C5 содержит вариабельную область легкой цепи, причем аминокислота в позиции 53 является мутировавшей из тирозина (Y) в лизин (L); и вариабельную область тяжелой цепи, причем аминокислота в позиции 28 является мутировавшей из треонина (T) в изолейцин (I), аминокислота в позиции 30 является мутировавшей из серина (S) в аргинин (R), аминокислота в позиции 49 является мутировавшей из серина (S) в аланин (A), и аминокислота в позиции 94 является мутировавшей из тирозина (Y) в аспарагиновую кислоту (D). Дополнительные или альтернативные обратные мутации могут быть сделаны в каркасных областях гуманизированных антител, предложенных в данном документе, в целях улучшения свойств антител. Настоящее изобретение также включает гуманизированные антитела, которые связываются с PD-L1 и содержат каркасные модификации, соответствующие примерам модификаций, описанных в данном документе, в отношении любой подходящей каркасной последовательности, а также других каркасных модификаций, которые иначе улучшают свойства антител.
[0072] Как используется в данном документе, термин «производное», когда используется для обозначения молекулы или полипептида по отношению к эталонному антителу или другому связывающему белку, означает молекулу или полипептид, который способен связывать со специфичностью тот же эпитоп, также как эталонное антитело или другой связывающий белок.
[0073] Антитела и антигенсвязывающие фрагменты, раскрытые в данном документе, являются конкретными для PD-L1. В одном варианте реализации изобретения антитела и их фрагменты являются специфическими для человеческой PD-L1. В одном варианте реализации изобретения антитела и фрагменты, предложенные в данном документе, связываются с PD-L1 человека и примата, но не с PD-L1 любого другого млекопитающего. В дополнительном варианте реализации изобретения антитела и их фрагменты не связываются с мышиным PD-L1. Термины «человеческий PD-L1», «hPD-L1» и «huPD-L1» и тому подобное используются взаимозаменяемо в данном документе и относятся к человеческому PD-L1 и вариантам или изоформам человеческого PD-L1. Под «специфический для» подразумевается, что антитела и их фрагменты связывают PD-L1 с большой аффинностью, чем любую другую цель. Как используется в данном документе, термин «ЭК50» относится к эффективной концентрации, 50% от максимального ответа антитела. Как используется в данном документе, термин «ИК50» относится к ингибирующей концентрации, 50% от максимального ответа антитела. Как ЭК50, так и ИК50 может быть измерена с помощью ИФА или проточной цитометрии, или любым другим способом известным в данной области техники.
[0074] В одном варианте реализации изобретения анти-PD1 антитела и фрагменты или их варианты имеют аффинность связывания (KD) для PD-L1 в диапазоне от около 0,001 нмоль/л до около 100 нмоль/л, от около 0,002 нмоль/л до около 50 нмоль/л, от около 0,005 нмоль/л до около 5 нмоль/л, от около 0,01 нмоль/л до около 1 нмоль/л, или от около 0,05 нмоль/л до около 0,1 нмоль/л. В одном варианте реализации изобретения антитела и их фрагменты имеют аффинность связывания (KD) для PD-L1 около 50 нмоль/л или менее, около 25 нмоль/л или менее, около 20 нмоль/л или менее, около 15 нмоль/л или менее, около 10 нмоль/л или менее, около 8 нмоль/л или менее, около 6 нмоль/л или менее, около 5 нм или менее, около 4 нмоль/л или менее, около 3 нмоль/л или менее, около 2 нмоль/л или менее, около 1 нмоль/л или менее, около 0,9 нмоль/л или менее, около 0,8 нмоль/л или менее, около 0,7 нмоль/л или менее, около 0,6 нмоль/л или менее, около 0,5 нмоль/л или менее, около 0,4 нмоль/л или менее, около 0,3 нмоль/л или менее, около 0,2 нмоль/л или менее, около 0,1 нмоль/л или менее, около 0,09 нмоль/л или менее, около 0,08 нмоль/л или менее, около 0,07 нмоль/л или менее, около 0,06 нмоль/л или менее, около 0,05 нмоль/л или менее, около 0,04 нмоль/л или менее, около 0,03 нмоль/л или менее, около 0,02 нмоль/л или менее, около 0,01 нмоль/л или менее, около 0,009 нмоль/л или менее, около 0,008 нмоль/л или менее, около 0,007 нмоль/л или менее, около 0,006 нмоль/л или менее, около 0,005 нмоль/л или менее, около 0,004 нмоль/л или менее, около 0,003 нмоль/л или менее, около 0,002 нмоль/л или менее, или около 0,001 нмоль/л или менее. В одном варианте реализации изобретения антитела и их фрагменты имеют аффинность связывания (KD) для PD-L1 около 10 нмоль/л, около 9 нмоль/л, около 8 нмоль/л, около 7 нмоль/л, около 6 нмоль/л, около 5 нмоль/л, около 4 нмоль/л, около 3 нмоль/л, около 2 нмоль/л, около 1 нмоль/л, около 0,9 нмоль/л, около 0,8 нмоль/л, около 0,7 нмоль/л, около 0,6 нмоль/л, около 0,5 нмоль/л, около 0,4 нмоль/л, около 0,3 нмоль/л, около 0,2 нмоль/л, около 0,1 нмоль/л, около 0,09 нмоль/л, около 0,08 нмоль/л, около 0,07 нмоль/л, около 0,06 нмоль/л, около 0,05 нмоль/л, около 0,04 нмоль/л, около 0,03 нмоль/л, около 0,02 нмоль/л, около 0,01 нмоль/л, около 0,009 нмоль/л, около 0,008 нмоль/л, около 0,007 нмоль/л, около 0,006 нмоль/л, около 0,005 нмоль/л, около 0,004 нмоль/л, около 0,003 нмоль/л, около 0,002 нмоль/л, или около 0,001 нмоль/л.
[0075] В одном варианте реализации изобретения антитела и фрагменты, предложенные в данном документе, включает легкую цепь и тяжелую цепь, каждая из которых содержит три CDR-области. Иллюстративные последовательности CDR тяжелой цепи (HCDR1, HCDR2 и HCDR3) для антител к PD-L1 согласно настоящему изобретению приводятся ниже в Таблице 1. Иллюстративные последовательности CDR легкой цепи (LCDR1, LCDR2 и LCDR3) для антител к PD-L1 согласно настоящему изобретению приводятся ниже в Таблице 2. Иллюстративные последовательности вариабельных областей и полноразмерных тяжелой и легкой цепей для антител к PD-L1 изобретения приводятся ниже в Таблице 3.
Таблица 1. Последовательности CDR тяжелой цепи
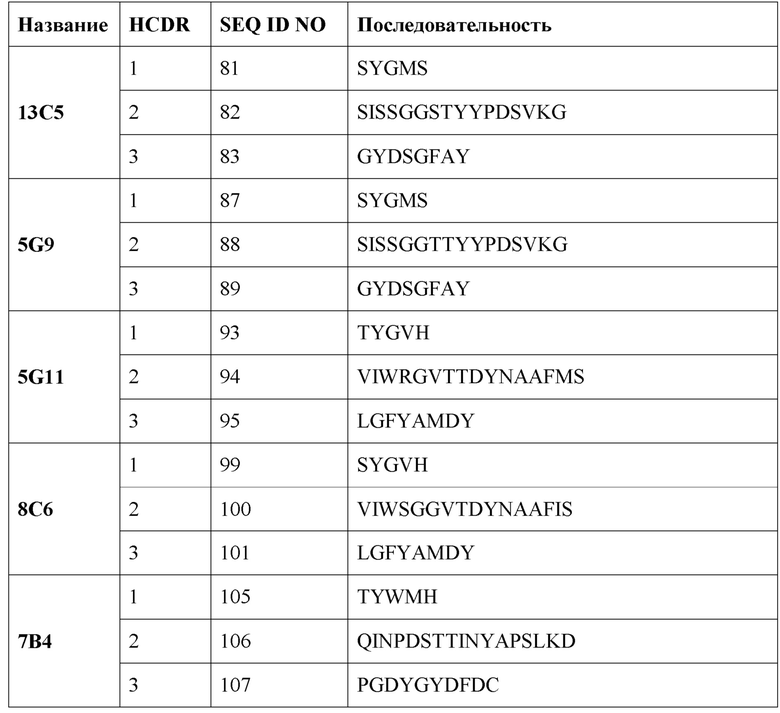
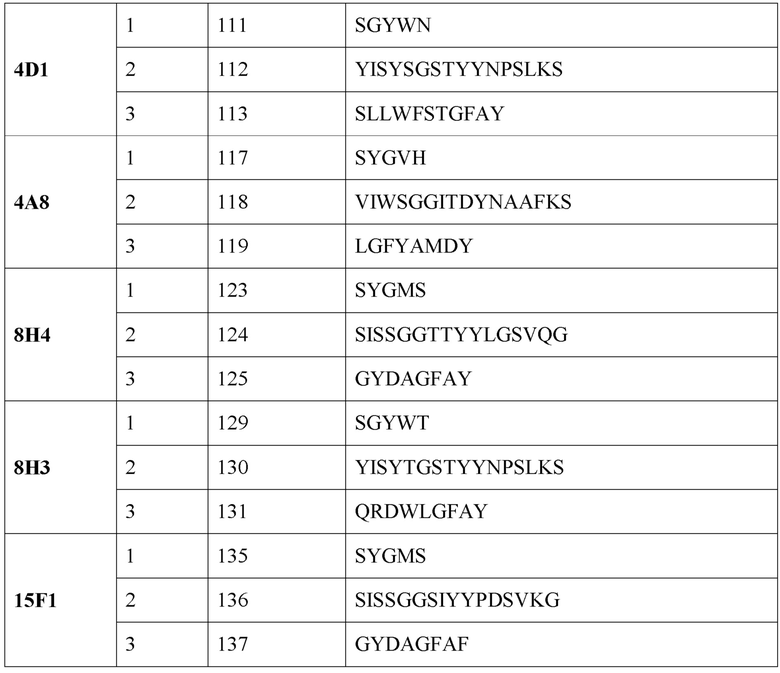
Таблица 2. Последовательности CDR легкой цепи
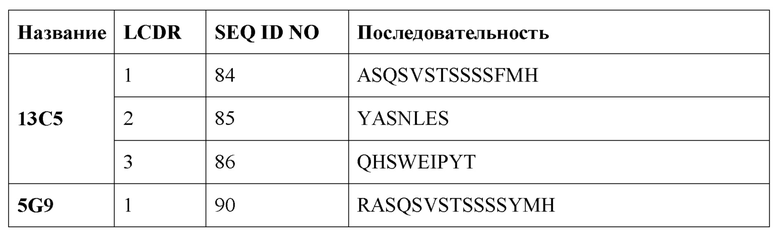
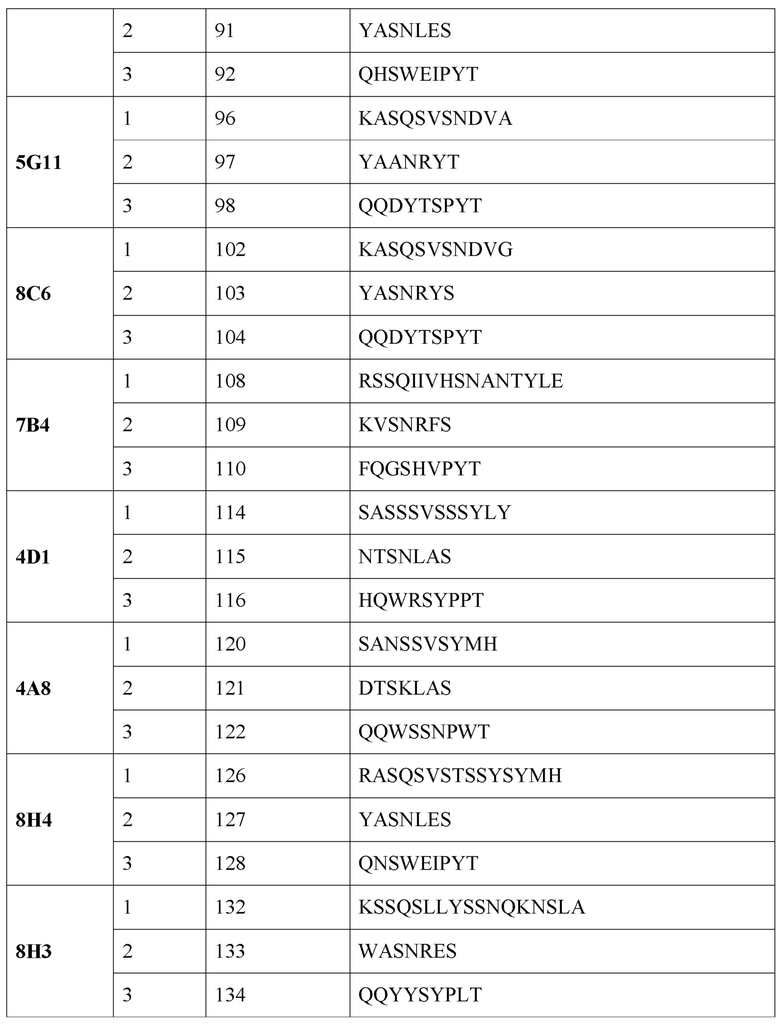

Таблица 3. Аминокислотные последовательности вариабельной области тяжелой цепи и легкой цепи и полноразмерных тяжелой и легкой цепи
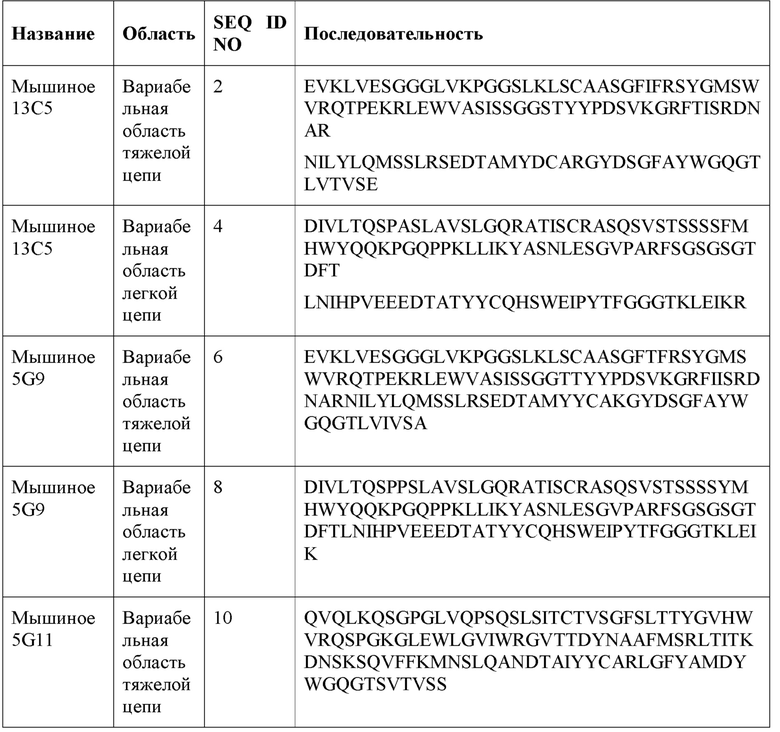

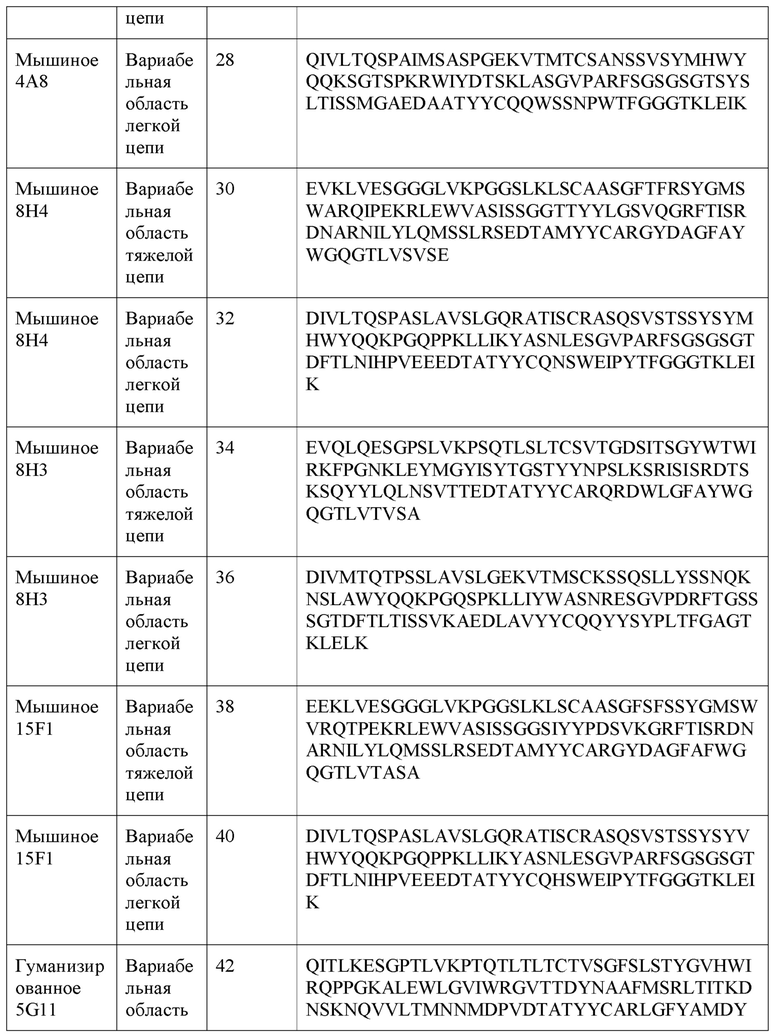
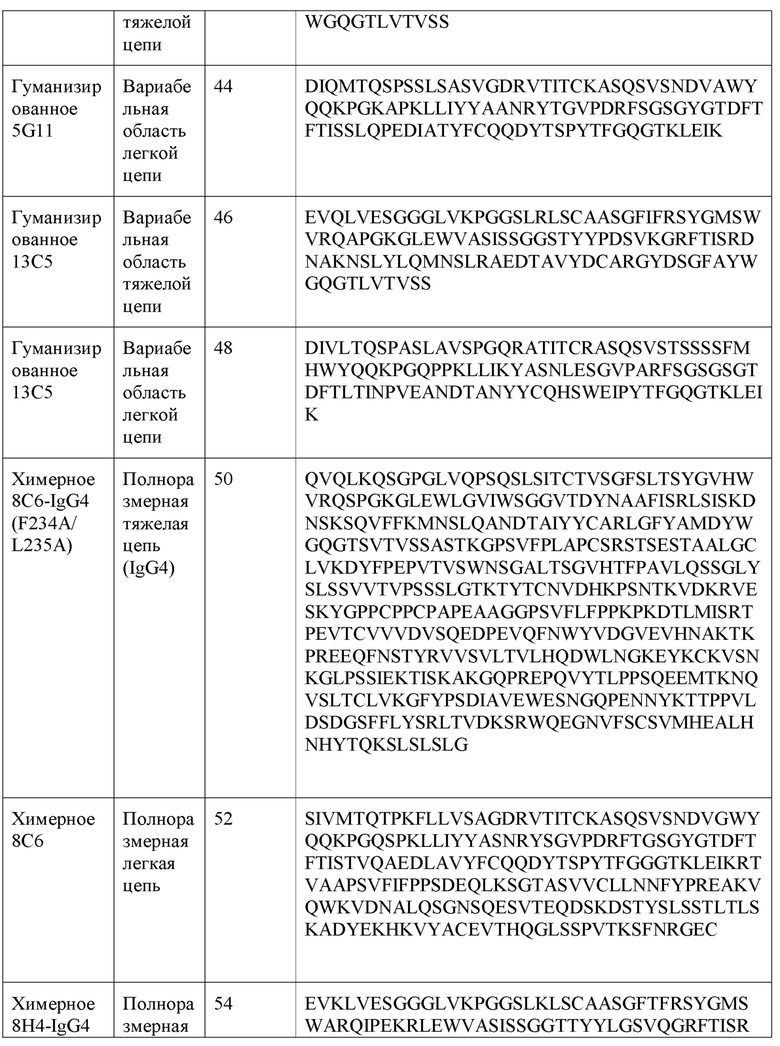
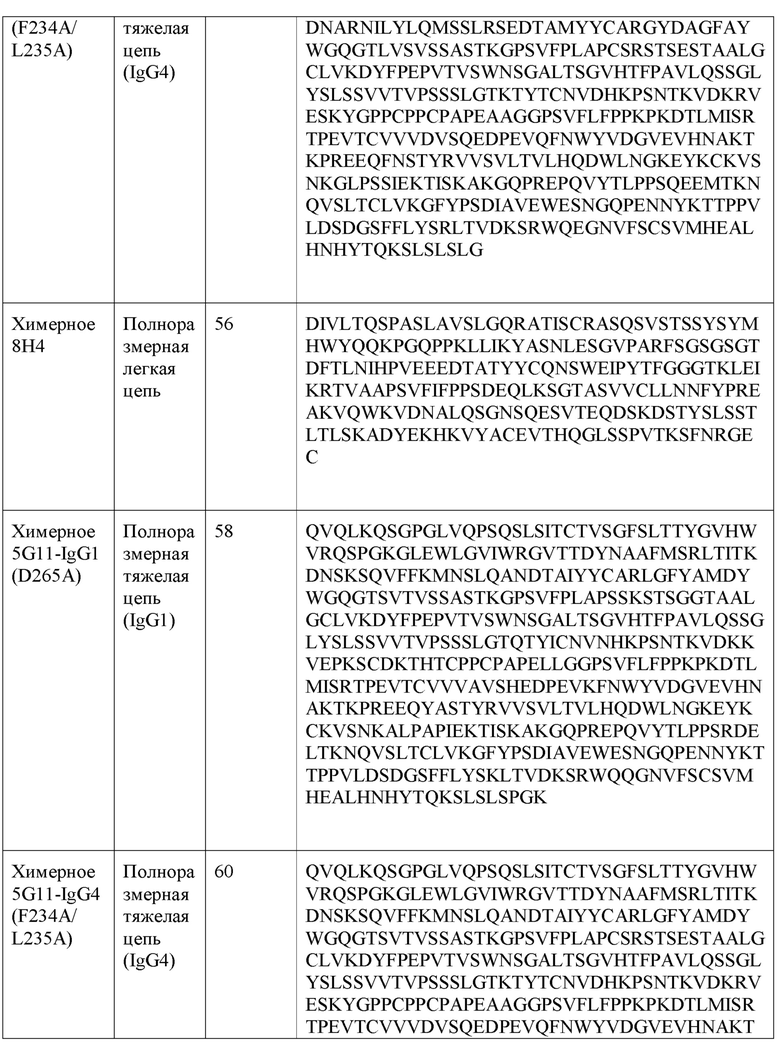
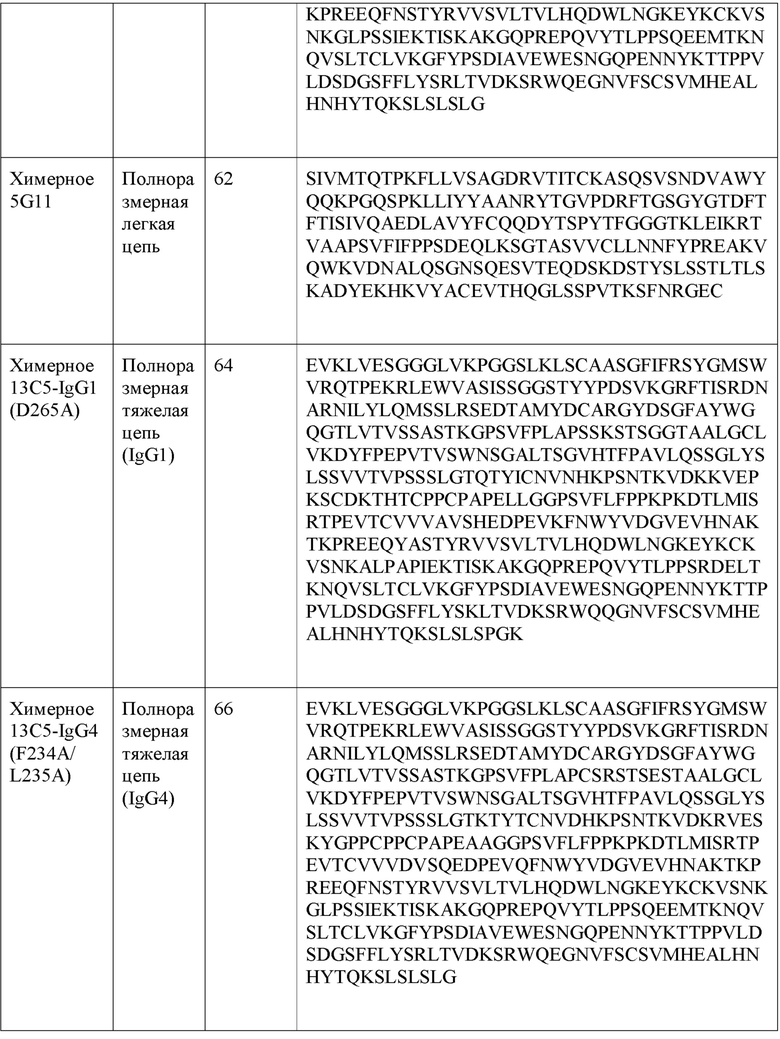
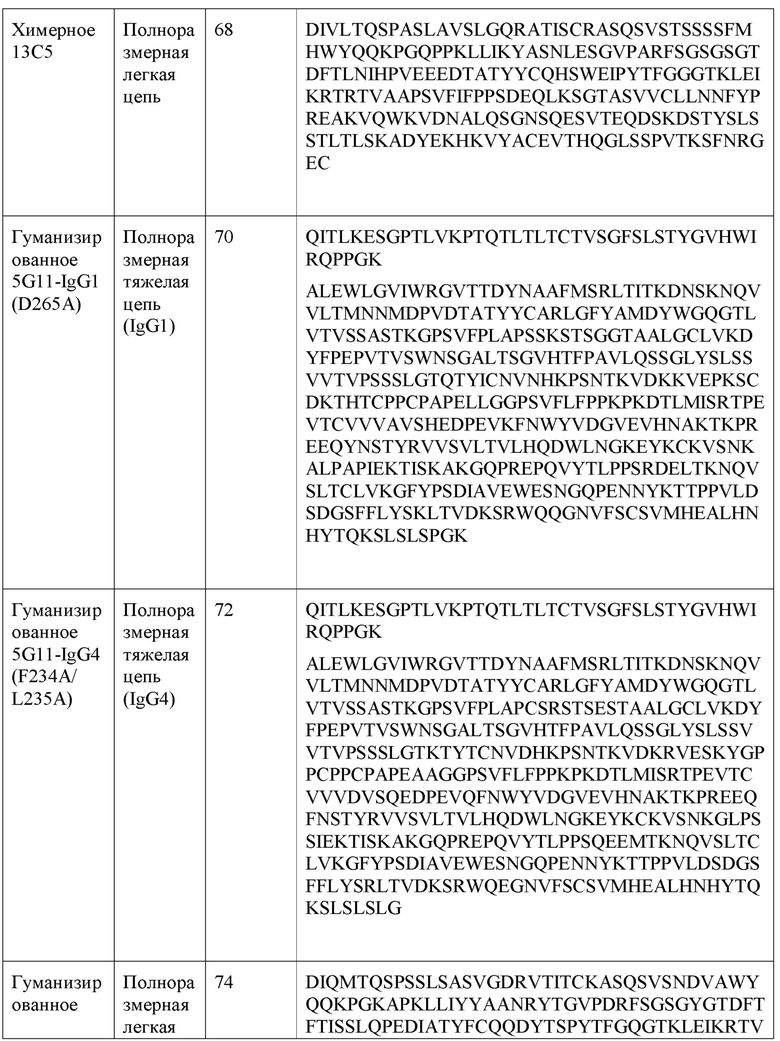
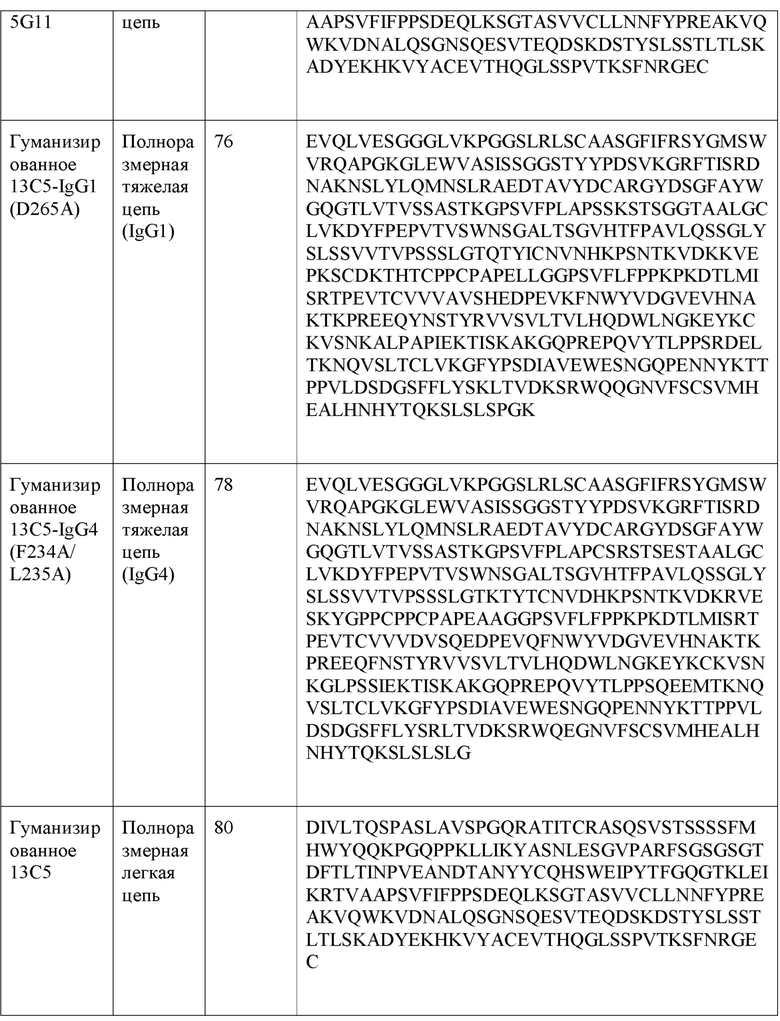
[0076] В одном варианте реализации настоящее изобретение обеспечивает анти-PD-L1 антитела, которые содержат CDR легкой цепи и CDR тяжелой цепи антител 13C5, 5G9, 5G11, 8C6, 7B4, 4D1, 4A8, 8H4, 8H3, и/или 15F1. Cпециалисту в данной области техники должно быть понятно, что CDR тяжелой и легкой цепи антител, предложенных в данном документе, могут быть независимо друг от друга выбраны или скомбинированы с образованием антитела или его связывающего фрагмента, содержащего любую CDR1, CDR2 и CDR3 тяжелой цепи; и любую CDR1, CDR2 и CDR3 легкой цепи из антител, предложенных в данном документе. Таким образом, настоящее изобретение обеспечивает анти-PD-L1 антитела, которые содержат CDR1 тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 81, 87, 93, 99, 105, 111, 117, 123, 129 и 135; CDR2 тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 82, 88, 94, 100, 106, 112, 118, 124, 130 и 136; CDR3 тяжелой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 83, 89, 95, 101, 107, 113, 119, 125, 131 и 137; CDR1 легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 84, 90, 96, 102, 108, 114, 120, 126, 132 и 138; CDR2 легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 85, 91, 97, 103, 109, 115, 121, 127, 133 и 139; и CDR3 легкой цепи, содержащую аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 86, 92, 98, 104, 110, 116, 122, 128, 134 и 140. В одном варианте реализации настоящее изобретение обеспечивает анти-PD-L1 антитела, содержащие CDR-областей тяжелой и легкой цепи, содержащие аминокислотные последовательности, имеющие по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 81%, по меньшей мере 82%, по меньшей мере 83%, по меньшей мере 84%, по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере, 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере, 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, или по меньшей мере 99% гомологии с соответствующими CDR1, CDR2 или CDR3 легкой или тяжелой цепи, предложенные в данном документе. В одном варианте реализации настоящее изобретение обеспечивает анти-PD-L1 антитела, содержащие CDR-области тяжелой и легкой цепи, содержащие аминокислотные последовательности, имеющие 1, 2, 3, 4, 5, или 6 аминокислотных замен, делеций или инсерций по отношению к соответствующим CDR1, CDR2 или CDR3 легкой или тяжелой цепи, предложенные в данном документе.
[0077] В одном варианте реализации настоящее изобретение обеспечивает анти-PD-L1 антитела, которые содержат вариабельную область тяжелой цепи антитела, выбранного из группы, состоящей из 13C5, 5G9, 5G11, 8C6, 7B4, 4D1, 4A8, 8H4, 8H3, и/или 15F1 и вариабельную область легкой цепи антитела, выбранного из группы, состоящей из 13C5, 5G9, 5G11, 8C6, 7B4, 4D1, 4A8, 8H4, 8H3, и/или 15F1. В одном варианте реализации изобретения антитела и фрагменты, предложенные в данном документе, содержат вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, которая имеет по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 81%, по меньшей мере 82%, по меньшей мере 83%, по меньшей мере 84%, по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, или по меньшей мере 99% гомологии с вариабельной областью тяжелой цепи, выбранной из группы, состоящей из SEQ ID NO: 2, 6, 10, 14, 18, 22, 26, 30, 34, 38, 42 и 46. В одном варианте реализации изобретения антитела и фрагменты, предложенные в данном документе, содержат вариабельную область тяжелой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 2, 6, 10, 14, 18, 22, 26, 30, 34, 38, 42, 46, или его вариант, причем вариант содержит 1, 2, 3, 4, 5, 6, 7, 8, 9, или 10 аминокислотных замен или делеций, или их комбинации. В дополнительном варианте реализации изобретения аминокислотные замены представляют собой консервативные замены.
[0078] В одном варианте реализации изобретения антитела и фрагменты, предложенные в данном документе, содержат вариабельную область легкой цепи, содержащую аминокислотную последовательность, которая имеет по меньшей мере 75%, по меньшей мере 80%, по меньшей мере 81%, по меньшей мере 82%, по меньшей мере 83%, по меньшей мере 84%, по меньшей мере 85%, по меньшей мере 86%, по меньшей мере 87%, по меньшей мере 88%, по меньшей мере 89%, по меньшей мере 90%, по меньшей мере 91%, по меньшей мере 92%, по меньшей мере 93%, по меньшей мере 94%, по меньшей мере 95%, по меньшей мере 96%, по меньшей мере 97%, по меньшей мере 98%, или по меньшей мере 99% гомологии с вариабельной областью легкой цепи, выбранной из группы, состоящей из с SEQ ID NO: 4, 8, 12, 16, 20, 24, 28, 32, 36, 40, 44 или 48. В одном варианте реализации изобретения антитела и фрагменты, предложенные в данном документе, содержат вариабельную область легкой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 4, 8, 12, 16, 20, 24, 28, 32, 36, 40, 44, 48, или его вариант, причем вариант содержит 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 или более аминокислотных замен, инсерций или делеций или их комбинации. В дополнительном варианте реализации изобретения аминокислотные замены представляют собой консервативные замены.
[0079] Анти-PD-L1 антитела, раскрытые в данном документе, имеющие одну или более аминокислотную замену, инсерцию, делецию или их комбинации в CDR или вариабельной области легкой или тяжелой цепи, сохраняют биологическую активность соответствующего анти-PD-L1 антитела, которое не имеет аминокислотной замены, вставки или делеции. Таким образом, варианты анти-PD-L1 антител, предложенные в данном документе, сохраняют связывание с PD-L1. Процент гомологии, как используется в данном документе, относится к числу идентичных аминокислотных последовательностей, общих для двух эталонных последовательностей, деленное на общее число аминокислотных позиций, умноженное на 100.
[0080] В некоторых вариантах реализации изобретения анти-PD-L1 антитела, предложенные в данном документе, содержит консервативные аминокислотные замены. Специалисту в данной области техники будет понятно, что консервативная аминокислотная замена представляет собой замену одной аминокислоты другой аминокислотой, которая имеет аналогичные структурные или химические свойства, такие как, например, аналогичную боковую цепь. Иллюстративные консервативные замены описаны в данной области техники, например, в Watson et al. Molecular Biology of the Gene, The Bengamin/Cummings Publication Company, 4th Ed.(1987).
[0081] Специалисту будет понятно, что вариабельные области легкой и тяжелой цепей могут быть независимо выбраны, или смешаны и подобраны из антител, предложенных в данном документе. Таким образом, настоящее изобретение обеспечивает анти-PD-L1 антитела, содержащие вариабельную область тяжелой цепи, имеющую по меньшей мере 80% гомологии с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 2, 6, 10, 14, 18, 22, 26, 30, 34, 38, 42, и 46, и вариабельную область легкой цепи, имеющую по меньшей мере 80% гомологии с аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 4, 8, 12, 16, 20, 24, 28, 32, 36, 40, 44 и 48.
[0082] В одном варианте реализации настоящее изобретение обеспечивает антитела, которые связываются с тем же эпитопом, как любое из иллюстративных антител, описанных в данном документе. Таким образом, в одном варианте реализации настоящее изобретение обеспечивает антитела, которые конкурируют за связывание с PD-L1 с иллюстративными антителами, предложенными в данном документе.
[0083] Анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, могут дополнительно содержать модификации Fc-области для изменения эффекторных функций. Модификации Fc могут быть аминокислотными инсерциями, делециями или заменами, или могут быть химическими модификациями. Например, модификации Fc-области могут быть сделаны для повышения или снижения связывания комплемента, для повышения или снижения антителозависимой клеточноопосредованной цитотоксичности, или для увеличения или уменьшения времени полужизни антитела. Некоторые модификации Fc повышают или снижают аффинность антитела к Fcγ-рецептору, такому как FcγRI, FcγRII, FcγRIII, или FcRn. Различные модификации Fc были описаны в данной области техники, например, в Shields et al., J Biol. Chem 276; 6591 (2001); Tai et al. Blood 119; 2074 (2012); Spiekermann et al.J Exp.Med 196; 303 (2002); Moore et al. mAbs 2: 2; 181 (2010); Medzihradsky Methods in Molecular Biology 446; 293 (2008); Mannan et al. Drug Metabolism and Disposition 35; 86 (2007); и Idusogie et al. J Immunol 164; 4178 (2000). В некоторых вариантах реализации изобретения профиль гликозилирования Fc-области изменяется. В других вариантах реализации изобретения Fc-область модифицирована с помощью пегилирования (например, при взаимодействии антитела или его фрагмента с полиэтиленгликолем (ПЭГ)).
[0084] В одном варианте реализации изобретения антитела или их фрагменты, предложенные в данном документе, представляют собой иммуноконъюгаты, содержащие анти-PD-L1 антитело или его фрагмент и дополнительно содержащие агент, выбранный из группы, включающей дополнительный терапевтический агент, цитотоксический агент, молекулу иммуноадгезии, и визуализирующий агент.В некоторых вариантах реализации изобретения визуализирующий агент выбран из группы, состоящей из радиоактивной метки, фермента, флуоресцентной метки, люминесцентной метки, биолюминесцентной метки, магнитной метки и биотина. В некоторых вариантах реализации визуализирующий агент представляет собой радиоактивную метку, выбранную из группы, состоящей из: 3H, 14C, 35S, 62Cu, 64Cu, 89Zr, 90Y, 99Tc, 111In, 125I, 131I, 177Lu, 166Ho, и 153Sm. В некоторых вариантах реализации изобретения терапевтический агент или цитотоксический агент выбран из группы, включающей химиотерапевтический агент, иммунодепрессант, иммуностимулирующий агент, антиметаболит, алкилирующий агент, антибиотик, ростовой фактор, цитокин, антиангиогенный агент, антимитотический агент, антрациклин, токсин, и апоптотический агент. В некоторых вариантах реализации изобретения связывающий белок конъюгирован непосредственно с агентом. В других вариантах реализации изобретения связывающий белок конъюгирован с агентом через линкер. Подходящие линкеры включают, но не ограничиваясь ими, аминокислотные и полипептидные линкеры, раскрытые в данном документе. Линкеры могут быть расщепляемыми или нерасщепляемыми.
[0085] В одном варианте реализации настоящее изобретение обеспечивает биспецифические или мультиспецифические антитела специфичные к PD-L1 и по меньшей мере один другой антиген или эпитоп.Анти-PD-L1 антитела и их фрагменты, предложенные в данном документе, могут быть протестированы на связывание с PD-L1 с применением анализа связывания, предложенным в данном документе, или любым другим анализом связывания известным специалисту в данной области техники.
[0086] Если не указано иное, то для осуществления настоящего изобретения используются общепринятые методики молекулярной биологии, клеточной биологии, биохимии и иммунологии, которые хорошо известны в данной области техники и описаны, например, в Methods in Molecular Biology, Humana Press; Molecular Cloning: A Laboratory Manual, second edition (Sambrook et al., 1989), Current Protocols in Immunology (J.E.Coliganet al., eds.,1991); Immunobiology (C.A.Janeway and P.Travers, 1997); Antibodies (P.Finch, 1997); Antibodies: a practical approach (D.Catty., ed., IRL Press, 1988-1989); Monoclonal antibodies: a practical approach (P.Shepherd and C.Dean, eds.,Oxford University Press, 2000); Phage display: a laboratory manual (C.Barbas III et al, Cold Spring Harbor Laboratory Press, 2001); и Using antibodies: a laboratory manual (E.Harlow and D.Lane (Cold Spring Harbor Laboratory Press, 1999).
[0087] В одном аспекте настоящее изобретение обеспечивает способы лечения субъекта от заболевания или состояния, отвечающего на повышение, стимуляцию или индукцию иммунного ответа. Как используется в данном документе, термины «лечение» или «лечить» относятся как к терапевтическому лечению, так и к профилактическим или превентивным мерам. Субъекты, нуждающиеся в лечении, включают те субъекты, у которых уже есть заболевание или состояние, а также те, у которых может развиться заболевание или состояние, и у которых объект должен предотвратить, замедлить или ослабить заболевание или состояние. Как используется в данном документе, термин «субъект» обозначает млекопитающее, такое как грызун, животное из семейства кошачьих, псовых, и примат.Предпочтительно, субъект согласно настоящему изобретению представляет собой человека.
[0088] Термин «терапевтически эффективное количество», как используется в данном документе, относится к количеству соединения или композиции, которое является необходимым для обеспечения терапевтической и/или профилактической пользы для испытуемых.
[0089] В одном аспекте антитела и их антигенсвязывающие фрагменты являются полезными в лечении солидных или несолидных опухолей. Таким образом, в одном аспекте настоящее изобретение обеспечивает способы лечения онкологического заболевания. «Рак», как используется в данном документе, относится к физиологическому состоянию у млекопитающих, которое обычно характеризуется нерегулируемым клеточным ростом. Примеры рака включают, но не ограничиваясь ими, карциному, лимфому, бластому, саркому (включая липосаркому, остеогенную саркому ангиосаркому, эндотелиосаркому, лейомиосаркому, хордому, лимфангиосаркому, лимфангиоэндотелиосаркому, рабдомиосаркому, фибросаркому, миксосаркому, хондросаркому), нейроэндокринные опухоли, мезотелиому, синовиому, невриному, менингиому, аденокарциному, меланому и лейкоз или лимфолейкозы. Более конкретные примеры таких видов рака включают плоскоклеточный рак (например, эпителиальный плоскоклеточный рак), лимфому Ходжкина; неходжкинскую лимфому (лимфому Беркитта, мелкоклеточную лимфоцитарную лимфому/хронический лимфолейкоз, фунгоидную гранулему, мантийноклеточую лимфому, фолликулярную лимфому, диффузную крупноклеточную В-клеточную лимфому, лимфому из клеток маргинальной зоны, волосатоклеточный лейкоз и лимфоплазмоцитарный лейкоз), опухоли клеток-предшественников лимфоцитов, включая B-клеточный острый лимфобластный лейкоз/лимфому и Т-клеточный острый лимфобластный лейкоз/лимфому, тимому, опухоли зрелых Т и NK-клеток, включая лейкозы периферических Т-клеток, Т-клеточный лейкоз/Т-клеточные лимфомы взрослых и лейкоз из больших зернистых лимфоцитов, лангергансоклеточный гистиоцитоз, миелоидные неоплазии, такие как острые миелобластные лейкозы, включая ОМЛ с созреванием, ОМЛ без дифференциации, острый промиелоцитарный лейкоз, острый миеломоноцитарный лейкоз и острые моноцитарные лейкозы, миелодиспластические синдромы и хронические миелопролиферативные заболевания, включая хронический миелобластный лейкоз, В-клеточный острый лимфобластный лейкоз/лимфому, Т-клеточный острый лимфобластный лейкоз/лимфому, рак легких, включая мелкоклеточный рак легкого, немелкоклеточный рак легкого, аденокарциному легкого и плоскоклеточный рак легкого, мелкоклеточную карциному легкого, рак брюшной полости, гепатоцеллюлярный рак, рак желудочно-кишечного тракта и желудка, включая опухоль желудочно-кишечного тракта, рак поджелудочной железы, глиобластому, рак шейки матки, рак яичника, рак печени, рак мочевого пузыря, гепатому, рак молочной железы, рак толстой кишки, рак прямой кишки, колоректальный рак, рак эндометрия или тела матки, карциному слюнных желез, рак почек или ренальный рак, рак предстательной железы, рак вульвы, рак щитовидной железы, карциному печени, рак анального канала, пениальный рак, рак яичка, рак пищевода, опухоли желчных путей, опухоли, базально-клеточный рак Юинга, аденокарциномы, рак потовых желез, рак сальных желез, папиллярный рак, папиллярную аденокарциному, цистаденокарциному, медуллярный рак, бронхогенный рак, почечно-клеточный рак, гепатому, карциному желчных протоков, хориокарциному, семиному, эмбриональный рак, опухоль Вильмса, опухоль яичек, рак легкого, рак мочевого пузыря, эпителиальную карциному, глиому, астроцитому, медуллобластому, краниофарингиому, эпендимому, пинеалому, гемангиобластому, невриному слухового нерва, олигодендроглиому, менингиому, меланому, нейробластому, ретинобластому, лейкоз, лимфому, множественную миелому, макроглобулинемию Вальденстрема, миелодиспластическую болезнь, болезни тяжелых цепей, нейроэндокринные опухоли, невриному и другие карциномы, а также рак головы и шеи.
[0090] В одном варианте реализации изобретения антитела и их фрагменты, предложенные в данном документе, являются полезными при лечении заболеваний, вызванных инфекционными агентами. Инфекционные агенты включают, но не ограничиваясь, бактериальные, микологические, паразитарные и вирусные агенты. Примеры таких инфекционных агентов включают следующие: стафилококки, метициллинрезистентный золотистый стафилококк, Escherichia coli, семейство Streptococcaceae, семейство Neisseriaaceae, кокки, семейство Enterobacteriaceae, энтерококки, ванкомицинрезистентный энтерококк, криптококки, гистоплазмы, аспергиллы, семейство Pseudomonadaceae, семейство Vibrionaceae, кампилобактер, семейство Pasteurellaceae, бордетеллы, франциселлы, бруцеллы, легионеллы, семейство Bacteroidaceae, грамотрицательные бациллы, клостридии, коринебактерии, пропионибактерии, грамположительные бациллы, Bacillus anthracis, актиномицеты, нокаожии, микобактерии, трепонемы, боррелии, лептоспиры, микоплазму, уреаплазму, риккетсии, хламидии, кандиды, грибы, вызывающие системные микозы, оппортунистические микозы, простейшие, нематоды, трематоды, цестоды, аденовирусы, вирусы герпеса (в том числе, например, вирус простого герпеса и вирус Эпштейна-Барра и вирус опоясывающего герпеса), поксвирусы, паповавирусы, вирусы гепатита, (в том числе, например, вирус гепатита В и вирус гепатита С), папилломавирусы, ортомиксовирусы (включая, например, грипп A, грипп В, гриппа в и гриппа C), парамиксовирусы, коронавирусы, пикорнавирусы, реовирусы, тогавирусы, флавивирусы, буньявирусы, рабдовирусы, ротавирусы, респираторносинцитиальный вирус, вирус иммунодефицита человека и ретровирусы. Иллюстративные инфекционные заболевания включают, но не ограничиваясь ими, кандидоз, кандидемию, аспергиллез, стрептококковую пневмонию, стрептококковые кожные и орофарингеальные заболеваний, грамотрицательный сепсис, туберкулез, мононуклеоз, грипп, респираторное заболевание, вызванное респираторно-синцитиальным вирусом, малярию, шистосомоз и трипаносомиаз.
[0091] В одном варианте реализации изобретения антитела и их фрагменты, предложенные в данном документе, являются полезными при лечении заболеваний, опосредованных Т-хелперами 2 типа (Th2), таких как, например, астма, аллергия, или болезнь «трансплантат против хозяина».
[0092] В одном варианте реализации изобретения антитела и их фрагменты, предложенные в данном документе, являются полезными для стимуляции иммунного ответа у субъекта, нуждающегося в ней. Например, в одном варианте реализации изобретения анти-PD-L1 антитела и их фрагменты могут быть введены в сочетании с необходимым антигеном с целью индукции иммунного ответа к указанному антигену. Необходимый антиген может быть антигеном, связанным с патогеном, таким как вирус или бактерия. Таким образом, в одном варианте реализации настоящее изобретение обеспечивает вакцину, содержащую анти-PD-L1 антитело и антиген, причем вакцина вызывает антигенспецифический иммунный ответ.
[0093] В одном варианте реализации изобретения анти-PD-L1 антитела, предложенные в данном документе, модулируют функцию регуляторных Т-клеток. СD4+CD25+регуляторные T-клетки представляют собой лимфоциты, которые подавляют или снижают воздействие эффекторных Т-клеточных функций. Термины «регуляторная Т-клетка» и «Tрег» используются взаимозаменяемо в данном документе. В одном варианте реализации изобретения анти-PD-L1 антитела, предложенные в данном документе, предотвращают или восстанавливают ингибирующие эффекты регуляторных Т-клеток на продукцию цитокинов эффекторными Т-клетками. Например, в одном варианте реализации изобретения анти-PD-L1 антитела, предложенные в данном документе, восстанавливают способность к продукции ИФН-(в эффекторных Т-клетках, контактирующих с регуляторными T-клетками.
[0094] В одном варианте реализации изобретения антитела и их фрагменты, раскрытые в данном документе, могут быть введены субъекту по меньшей мере одним способом введения, выбранным из парентерального, подкожного, внутримышечного, внутривенного, внутрисуставного, внутрибронхиального, внутрибрюшного, внутрикапсульного, внутрихрящевого, внутриполостного, внутрижелудочкового, внутримозжечкового, интрацеребровентрикулярного, внутритолстокишечного, интрацервикального, внутрижелудочного, внутрипеченочного, интрамиокардиального, внутрикостного, внутритазового, интраперикардиального, внутрибрюшинного, внутриплеврального, интрапростатического, внутрилегочного, ректального, интраренального, интраретинального, интраспинального, внутрисуставного, интраторакального, интратимпанального, внутриматочного, внутрипузырного, интравитреального, струйного, субконъюнктивального, вагинального, ректального, буккального, сублингвального, интраназального, внутриопухолевого и трансдермального.
[0095] В одном варианте реализации изобретения антитела и их фрагменты, раскрытые в данном документе, могут вводиться субъекту, нуждающемуся в этом, в комбинации с одним или более дополнительным терапевтическим агентом. В одном варианте реализации антитела и их фрагменты могут быть введены субъекту до, во время и/или после введения субъекту дополнительного терапевтического агента. В одном варианте реализации изобретения дополнительный терапевтический агент представляет собой химиотерапевтический агент, радиотерапевтический агент, цитокин, антитело или его фрагмент, или любой другой дополнительный терапевтический агент, который назначается при заболевании, которое подлежит лечению. В одном варианте реализации изобретения анти-PD-L1 антитело и дополнительный терапевтический агент проявляют терапевтический синергизм при совместном назначении, одновременно или последовательно. В одном варианте реализации изобретения анти-PD-L1 антитело и дополнительный терапевтический агент вводят в виде отдельных препаратов. В другом варианте реализации изобретения анти-PD-L1 антитело и дополнительный терапевтический агент вводят в том же препарате. В одном варианте реализации изобретения анти-PD-L1 антитела и фрагменты, предложенные в данном документе, усиливают иммуномодулирующие действие одного или более дополнительных терапевтических агентов. В другом варианте реализации изобретения один или более дополнительный терапевтический агент усиливает действие анти-PD-L1 антитела или его фрагмента.
[0096] Настоящее изобретение обеспечивает выделенные антитела и антигенсвязывающие фрагменты, и нуклеиновые кислоты, кодирующие такие антитела и их фрагменты, а также композиции, содержащие такие выделенные антитела, фрагменты и нуклеиновые кислоты. Термин «выделенное» относится к необходимому соединению (например, антителу или нуклеиновой кислоте), которое было выделено из его окружающей среды. Настоящее изобретение дополнительно обеспечивает фармацевтические композиции, содержащие выделенные антитела или их фрагменты, или нуклеиновые кислоты, кодирующие антитела или их фрагменты, и дополнительно содержащие один или более фармацевтически приемлемый носитель. Фармацевтически приемлемые носители включают в себя, например, вспомогательные вещества, разбавители, инкапсулирующие материалы, наполнители, буферы или другие агенты.
[0097] Использование единственного числа включает множественное число, если специально не указано иное. Слова в единственном числе означают «по меньшей мере один», если специально не указано иное. Использование «или» означает «и/или», если не указано иное. Смысл выражения «по меньшей мере один» эквивалентно смыслу выражения «один или более». Кроме того, использование термина «включая», а также других форм, таких как «включает» и «включенный» не является ограничивающим. Кроме того, такие термины, как «элемент» или «компонент» охватывают как элементы или компоненты, содержащие одну единицу, так и элементы или компоненты, содержащие более одной единицы, если специально не указано иное.
[0098] Хотя вышеприведенное изобретение было описано довольно подробно посредством иллюстраций и примеров с целью ясности понимания, специалистам в данной области техники должно быть очевидно, что в рамках идей настоящего изобретения могут быть осуществлены определенные изменения и модификации без отклонения от сущности и объема прилагаемой формулы изобретения. Следующие ниже примеры приведены только с целью иллюстрации и не предназначены для ограничения объема настоящего изобретения. Специалисты в данной области техники легко найдут множество некритичных параметров, которые можно изменить или модифицировать, чтобы получить аналогичный результат.
ПРИМЕРЫ
Пример 1: Получение моноклонального антитела к hPD-L1
Иммунизация мышей с применением hPD-L1-HisTag и hPD-L1-mFc
[0099] Для получения антител против человеческого PD-L1, кДНК, кодирующие открытую рамку считывания внеклеточного домена hPD-L1, объединенные с гистидиновой меткой (hPD-L1-HisTag, SEQ ID NO: 143 и 144), мышиной Fc (hPD-L1-mFc, SEQ ID Ns: 145 и 146), и человеческой Fc меткой (hPD-L1-hFc, SEQ ID NO: 147 и 148), получали с помощью ПЦР и субклонировали в экспрессирующий вектор pcDNA3.1 (Invitrogen CAT#: V-790), соответственно. После транзиентной экспрессии в клетках FreeStyle 293, hPD-L1-HisTag очищали с помощью колонки, содержащей нитрилотриуксусную кислоту (GE Healthcare), hPD-L1-mFc и hPD-L1-hFc очищали с помощью колонки, содержащей G-белок (GE Healthcare).
[00100] Мышей BALB/cJ иммунизировали каждые 2 недели в течение 6 недель подкожным введением рекомбинантного белка hPD-L1-HisTag (100 мг/мышь) или PD-L1-mFc, эмульгированного равным объемом полного/неполного адъюванта Фрейнда. За три дня до слияния, мышей повторно иммунизировали путем внутривенной инъекции антигеном без адъюванта. Клетки селезенки (1×108) от иммунизированной мыши были слиты с SP2/0 миеломными клетками (1.5×107) с применением ПЭГ Hybri-Max (Sigma Inc.,CAT#: 7181). После слияния клетки распределяли в 96-луночные планшеты по 0,1 мл на лунку и инкубировали в термостате при температуре 37°C, 5% в CO2. На 1-е сутки, клетки подпитывали путем добавления дополнительной 0,1 мл питательной среды, содержащей сыворотку и ГАТ (гипоксантин, аминоптерин и тимидин) плюс 2×метотрексат, на лунку. На 3-и сутки и 7-е сутки 0,1 мл питательной среды из каждой лунки заменяли 0,1 мл свежей гипоксантин-тимидиновой питательной среды. Скрининг, как правило, осуществляли между 9-14 сутками и супернатант культуры испытывали на наличие антител в реакции с hPD-L1-hFc при помощью ИФА.
[00101] Для клонирования выбранной клетки гибридомы, предельное разведение выполняли четыре раза. Клетки гибридомы культивировали на среде Игла, модифицированной по способу Дульбекко (GIBCO, Invitrogen Corporation, Карлсбад, Калифорния), содержащей 10% фетальной сыворотки теленка, 1% пенициллина/стрептомицина, 2% L-глутамина, и корректируемой 1% раствором NaHC03. Затем выбранные клетки гибридомы адаптировали к бессывороточный культуральной среде и антитело очищали из супернатанта с помощью колонки с G-белком (GE healthcare). После промывки с применением PBS, связанные антитела элюируют с помощью 0,1 м глицина при pH 3,0 с последующей нейтрализацией pH, используя 2,0 M трис (трис(гидроксиметил)аминометан). Центрифужный концентратор Ultra-15 (Amicon) использовали для замены буфера и концентрирования антител.
Пример 2: Клонирование и гуманизация последовательностей кДНК анти-PD-L1 антител
Клонирование кДНК иммуноглобулина
[00102] Общую РНК, выделенную из линии гибридомных клеток, продуцирующих антитела к hPD-L1, с помощью мини-набора RNeasy (Qiagen, CAT#: 74104), использовали в качестве матрицы для синтеза первой нити кДНК с помощью обратной транскриптазы SuperScript(II (Life Technology, CAT#: 18064-14) в соответствии с инструкцией производителя. Затем продукт кДНК подвергали ПЦР в 50 мкл объеме реакционной смеси с использованием праймеров вырожденных мышиных IgG (Kettleborough CA, et al, European Journal of Immunology 23: 206-211 (1993), Strebe N, et al, Antibody Engineering 1: 3-14 (2010)). Реакцию проводили в термоциклере S1000((Bio-Rad, Cat #: 184-2000) с 30 циклами: 94°С, 1,5 минуты для денатурации; 50°С, 1 минута для отжига; и 72°С, 1 минута для синтеза. В конце 30-го цикла, реакционную смесь инкубировали еще 7 минут при 72°С для удлинения.
[00103] Смесь ПЦР подвергали электрофорезу в 1% агарозе/трис-боратном геле, содержащем 0,5 мкг/мл бромистого этидия. Фрагменты ДНК, имеющие прогнозируемый размер (около 450 по (пар оснований) для тяжелой цепи и легкой цепи), были выделены из геля и очищены. 3 мкл очищенного продукта ПЦР клонировали в вектор pMD-18T (Takara, CAT#: D101A) и трансформировали в One Shot(TOP10 химически компетентные клетки E.coli (Invitrogen, CAT#: C4040-03). Клоны подвергали скринингу с помощью ПЦР для отбора колоний с использованием универсальных M13 прямых и обратных праймеров, и 10 позитивных клонов из каждой реакции были выбраны для определения последовательности ДНК в обоих направлениях с использованием M13 прямых и M13 обратных праймеров.
[00104] Последовательности вариабельной области тяжелой и легкой цепей антител m4A8 (SEQ ID NO: 25-28), m4D1 (SEQ ID NO: 21-24), m5G9 (SEQ ID NO: 5-8), m5G11 (SEQ ID NO: 9-12), m8C6 (SEQ ID NO: 13-16), m8H3 (SEQ ID NO: 33-36), m8H4 (SEQ ID NO: 29-32), m7B4 (SEQ ID NO: 17-20), m13C5 (SEQ ID NO: 1-4) и m15F1 (SEQ ID NO: 37-40) были амплифицированы из соответствующих гибридомных клонов. Данные антитела демонстрируют необходимые функции, такие как блокирование связывания PD-L1 с PD-1, и усиление активации Т-клеток и высвобождение цитокинов.
Конструирование и экспрессия химерных антител 5G11 и 13C5.
[00105] Химерные легкие цепи 8C6, 8H4, 5G11 и 13C5 (SEQ ID NO: 52, 56, 62 и 68, соответственно) были сконструированы путем связывания ПЦР-клонированных кДНК VL-областей мыши с константной областью каппа-цепи человека, соответственно. Химерные тяжелые цепи 8C6, 8H4, 5G11 и 13C5 (SEQ ID NO: 50 (8C6-IgG4), 54 (8H4-IgG4), 58 (5G11-IgG1), 60 (5G11-IgG4), 64 (13C5-IgG1) и 66 (13C5-IgG4)) были сконструированы путем связывания ПЦР-клонированных кДНК VH-областей мыши с константными областями IgG1 и IgG4. 5'-концы последовательностей кДНК мыши были модифицированы с использованием ПЦР-праймеров, предназначенных для добавления лидерной последовательности как к легкой цепи, так и к тяжелой цепи.
[00106] Клетки Freestyle 293 (200 мл при 106/мл) трансфецировали 100 мкг плазмид, экспрессирующих каждую химерную легкую и тяжелую цепи, и культивировали в течение 6 суток. Затем химерное антитело в супернатанте очищали с помощью колонки, содержащей G-белок (GE healthcare). Связывание химерного антитела с PD-L1 измеряли при помощи ИФА и анализа Biacore, и показали, что оно связывается с PD-L1 с аффинностью сопоставимой с аффинностью мышиного исходного антитела.
Конструирование гуманизированных антител
[00107] Антитела 5G11 и 13C5 гуманизировали с применением подхода трансплантации CDR (см., например, патент США №5225539). Последовательности вариабельной области легкой цепи и тяжелой цепи мышиного антитела 5G11 и 13C5 сравнивали с доступными в банке данных 3D структур белков и нуклеиновых кислот Research Collaboratory for Structural Bioinformatics (RCSB) (http://www.ncbi.nlm.nih.gov/igblast/igblast.cgi). Модели 5G11 и 13C5 были созданы соответственно на основании структуры VH и VL с высокой гомологией последовательностей.
[00108] Матрица человеческих антител должна быть трансплантирована с областями, определяющими комплементарность, (CDR) в VH и VL мышиных антител 5G11 и 13C5, которые были выбраны из зародышевых линий человеческих антител, обладающих высокой степенью гомологии последовательностей с мышиными антителами 5G11 и 13C5, с помощью поиска на веб-сайте международного иммуногенетического информационного сервиса (http://www.imgt.org/3Dstructure-DB/cgi/DomainGapAlign.cgi). Для 5G11 выбранной матричной человеческой VH являлась комбинация IGHV2-5*10 и IGHJ4*01, и выбранной матричной человеческой VL являлась комбинация IGKV1-33*01 и IGKJ2*01. Для 13C5 выбранной матричной человеческой VH являлась комбинация IGHV3-21*04 и IGHJ4*01, и выбранной матричной человеческой VL являлась комбинация IGKV7-3*01 и IGKJ2*01.
[00109] Аминокислотные последовательности CDR вышеупомянутых матричных антител человека были заменены CDR гибридомных антител (мышь) 5G11 (SEQ ID NO 93-98) и 13C5 (SEQ ID NO: 81-86). Каркасные участки указанных выше VH и VL матричного человеческого антитела были трансплантированы с необходимыми аминокислотными последовательностями из VH и VL мышиных антител 5G11 и 13C5 с получением функционального гуманизированного антитела. Что касается VH и VL из 5G11 и 13C5, несколько сайтов каркасного участка аминокислотной последовательности вышеупомянутого матричного человеческого антитела обратно мутировали в соответствующие аминокислотные последовательности в мышиных антителах 5G11 и 13C5. Для вариабельной области легкой цепи гуманизированного антитела 5G11, аминокислота в позиции 60 является мутировавшей из серина (S) в аспарагиновую кислоту (D), и аминокислота в позиции 67 является мутировавшей из серина (S) в тирозин (Y); и для вариабельной области тяжелой цепи гуманизированного антитела 5G11, аминокислота в позиции 24 является мутировавшей из фенилаланина (F) в валин (V), аминокислота в позиции 49 является мутировавшей из аланина (A) в глицин (G), аминокислота в позиции 73 является мутировавшей из треонина (T) в аспарагин (N), и аминокислота в позиции 83 является мутировавшей из треонина (T) в аспарагин (N). Для вариабельной области легкой цепи гуманизированного 13C5, аминокислота в позиции 53 является мутировавшей из тирозина (Y) в лизин (K); и для вариабельной области тяжелой цепи гуманизированного 13C5, аминокислота в позиции 28 является мутировавшей треонина (T) в изолейцин (I), аминокислота в позиции 30 является мутировавшей из серина (S) в аргинин (R), аминокислота в позиции 49 является мутировавшей из серина (S) в аланин (A), и аминокислота в позиции 94 является мутировавшей тирозина (Y) в аспарагиновую кислоту (D). Аминокислотные последовательности VH и VL гуманизированного 5G11 представлены в виде SEQ ID NO: 42 и 44, соответственно; последовательности ДНК, кодирующие VH и VL гуманизированного 5G11, представлены в виде SEQ ID NO: 41 и 43, соответственно. Аминокислотные последовательности VH и VL гуманизированного 13C5 представлены в виде SEQ ID NO: 46 и 48, соответственно); последовательности ДНК, кодирующие VH и VL гуманизированного 13C5, представлены в виде SEQ ID NO: 45 и 47, соответственно.
[00110] Аминокислотные последовательностей полной легкой цепи для гуманизированных антител 5G11 и 13C5 представлены в виде SEQ ID NO: 74 и 80, соответственно. Последовательности ДНК, кодирующие полноразмерное гуманизированное 5G11 и 13C5, представлены в виде SEQ ID NO: 73 и 79, соответственно. Варианты IgG1 и IgG4 гуманизированных антител 5G11 и 13C5. Константная область IgG1 несет мутацию D265A (Clynes R, et al, Nature Medicine 6: 443-446 (2000)), в то время как константная область IgG4 имеет двойную мутацию: F234A и L235A (Xu D, et al, Cellular Immunology 200: 16-26 (2000)). ДНК и аминокислотные последовательности для тяжелой цепи полноразмерного IgG1 гуманизированного антитела 5G11-hIgG1 представлены в виде SEQ ID NO: 69 и 70, соответственно. ДНК и аминокислотные последовательности для тяжелой цепи полноразмерного IgG4 гуманизированного антитела 5G11-hIgG4 представлены в виде SEQ ID NO: 71 и 72, соответственно. ДНК и аминокислотные последовательности для тяжелой цепи полноразмерного IgG1 гуманизированного антитела 13C5-hIgG1 представлены в виде SEQ ID NO: 75 и 76, соответственно. ДНК и аминокислотные последовательности для тяжелой цепи полноразмерного IgG4 гуманизированного антитела 13C5-hIgG4 представлены в виде SEQ ID NO: 77 и 78, соответственно.
Конструирование и экспрессия гуманизированных антител 5G11 и 13C5.
[00111] ДНК, кодирующую легкую и тяжелую цепь гуманизированных антител 13C5 и 5G11, синтезировали и клонировали в экспрессирующий вектор pcDNA3.1 (Invitrogen, CAT: #V-790). Клетки Freestyle 293 (200 мл при 106/мл) трансфецировали 100 мкг плазмид, экспрессирующих каждую гуманизированную легкую и тяжелую цепи, и культивировали в течение 6 суток. Затем гуманизированное антитело в супернатанте очищали с помощью колонки, содержащей G-белок (GE healthcare).
[00112] Кинетику связывания между антителами PD-L1 и PD-L1 измеряли с помощью анализа Biacore, который проводили при 25°С на приборе Biacore3000 и записывали с частотой сбора данных в 1 Гц. Поликлональные кроличьи антимышиные IgG (GE, BR-1008-38) разбавляли 10 мМ ацетата натрия при рН 5.0 и иммобилизовали путем пропускания по опытным и контрольным каналами биосенсора CM5 с около 15000RU с помощью комплекта связывания аминов (GE, BR10050). В начале каждого цикла разведенные тестируемые антитела (1,5 мкг/мл) вводили через опытный канал в течение 1 минуты для захвата. Серии аналитических образцов PD-L1 были приготовлены путем разбавления исходного материала с помощью подвижного буфера до 100 нМ с последующим последовательным разбавлением в 2 раза одним и тем же буфером до 0,78 нМ. Аналитические образцы вводили последовательно по контрольным и опытным каналам в течение 3 минут при скорости потока 30 мкл/мин. Подвижный буфер (PBS с 0,05% Р20) пропускали в течение 10 минут при скорости потока 30 мкл/мин. В конце каждого цикла поверхность биосенсора регенерировали 3-минутной инжекцией 10 мМ глицин-HCl буфера (pH 1,7) при скорости потока 10 мкл/мин. Для каждой инъекции аналитического образца (т.е. каждого цикла), связанные ответы, полученные от поверхности экспериментального сенсора были дважды прокалиброваны вычитанием одновременно записанных ответов от контрольной поверхности с последующим вычитанием ответов от единого образца эталонного подвижного буфера. Константу скорости ассоциации и диссоциации (ka и kd) определяли одновременно дважды прокалиброванными сенсограммами полной серии титрования в модели Ленгмюра (1:1) с использованием программного обеспечения Biaevaluation 4.0. Константу диссоциации, KD, рассчитывали с детерминированной константой скорости, определяемой соотношением KD=kd/ka. Аффинность связывания анти-PD-L1 антител с PD-L1 человека и PD-L1 яванских макак (cyno-PD-L1) приведены в Таблице 4.
Таблица 4. Аффинность связывания PD-L1 анти-PD-L1 антител
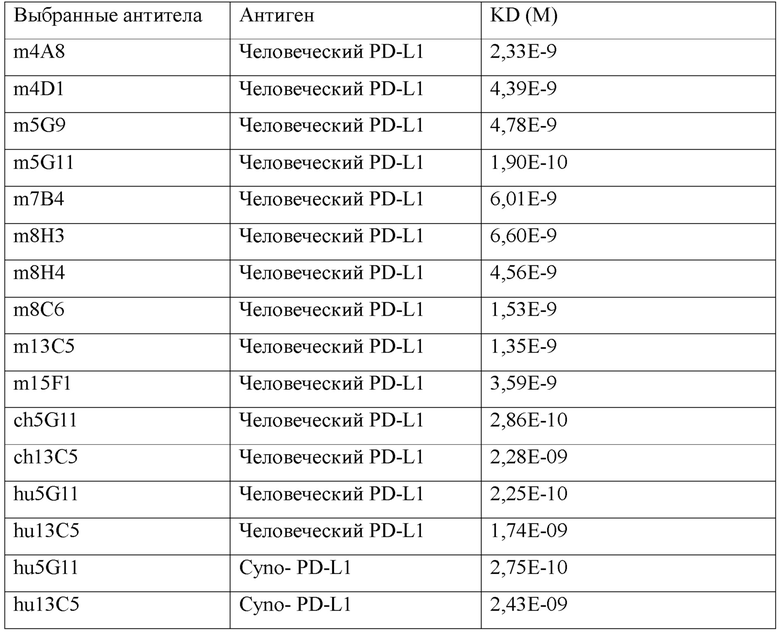
Пример 3: Анализ связывания анти-PD-L1 антител, основанный на ИФА
[00113] Анализ связывания, основанный на ИФА, проводили на основе человеческого PD-L1-mFC (для обнаружения химерного и гуманизированного антитела) и белка PD-L1-hFC (для обнаружения гибридомного антитела). 96-луночные планшеты (Costar, №по каталогу: 9018) покрывали 100 мкл 2 мкг/мл PD-L1-mFc (Crownbio) в покрывающем буфере PBS (Hyclone, №по каталогу: SH30256.01B) в течение ночи при 4°С.Содержимое лунок удаляли аспирацией и неспецифические сайты связывания блокировали путем добавления 200 мкл блокирующего буфера (PBS с 1% (масса/объем) бычьего сывороточного альбумина (BSA, Roche, №по каталогу: 738328)) и инкубировали в течение 1 часа при 37°C. После того, как планшеты три раза промывали буфером для промывки (PBS с 0,05% (объем/объем) Tween 20 (Sigma, №по каталогу: P1379)), 100 мкл на лунку 1:10 серийных разведений гибридомных (Фиг. 1), химерных (Фиг. 2), или гуманизированных (Фиг. 3) анти-PD-L1 антител было добавлено в блокирующий буфер (начиная с 20 мкг/мл) и инкубировали при комнатной температуре в течение 1 часа. Планшеты промывали и инкубировали с 100 мкл на лунку козьего антимышиного IgG (Н+L) (Thermo, №по каталогу: 31432) в блокирующем буфере в течение 60 мин. После того, как планшеты были промыты, 100 мкл на лунку субстратного раствора ТМБ (тетраметил бензидин) (eBioscience, №по каталогу: 00-4201-56) добавляли и планшеты инкубировали в течение 2 минут при комнатной температуре. Затем добавляли 100 мкл на лунку останавливающего раствора (2N H2SO4) для остановки реакции. Колориметрические сигналы получали и считывали при 450 нм с использованием Auto Plate SpectraMax Plus (Supplier: Moleculer Devices; Model: MNR0643; программное обеспечение: SoftMax Pro v5.4). Данные анализировали с помощью программы GraphPad Prism 5 и рассчитывали ЭК50 (Фиг. 1-3; Таблицы 5-7). Эти данные продемонстрировали, что анти-PD-L1 антитела (гибридомные, химерные и гуманизированные) связывают PD-L1, как измерено с помощью ИФА.
Таблица 5. ЭК50 связывания, основанная на ИФА, анти-PD-L1 гибридомного моноклонального антитела с PD-L1
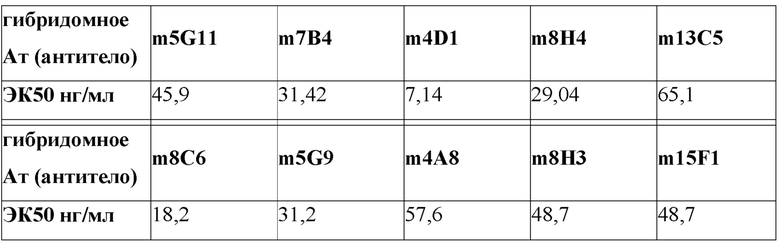
Таблица 6. ЭК50 связывания, основанная на ИФА, анти-PD-L1 химерного антитела с PD-L1
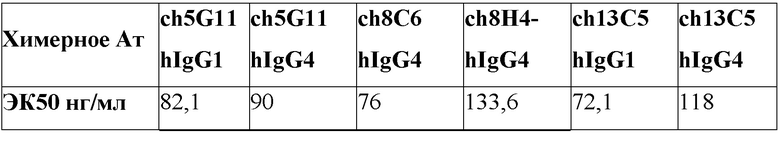
Таблица 7. ЭК50 связывания, основанная на ИФА, анти-PD-L1 антитела с PD-L1
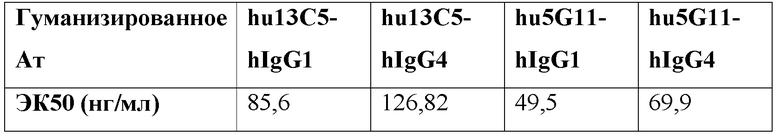
[00114] Анализ блокирования лиганда, основанный на ИФА, проводили с помощью блокирования биотинилированного человеческого PD-L1-mFc, связывающегося с человеческим PD-1-hFC. Антиген PD-1-hFC (Crownbio) суспендировали в буфере PBS (2 мкг/мл, 100 мкл на лунку) и покрывали 96-луночные планшеты (Costar, №по каталогу: 9018), оставляли на ночь при 4°C. Содержимое лунок удаляли аспирацией и неспецифические сайты связывания блокировали путем добавления 200 мкл блокирующего буфера (PBS с 1% (масса/объем) бычьего сывороточного альбумина (BSA, Roche, №по каталогу: 738328)) и инкубировали в течение 1 часа при 37°C. После того, как планшет три раза промывали промывочным буфером (PBS с 0,05% (объем/объем) Tween20 (Sigma, №по каталогу: P1379)), 100 мкл на лунку 1:3 серийных разведений гибридомных (Фиг. 4), химерных (Фиг. 5) или гуманизированных (Фиг. 6) анти-PD-L1 антител было добавлено в блокирующий буфер (начиная с 20 мкг/мл) и инкубировали при 37°C течение 1 часа. Затем 100 мкл PDL-1-mFc-биотина (0,1 мкг/мл) добавляли в каждую лунку и инкубировали при 37°C в течение 2 часов. После того как планшет промыли 3 раза, добавляли вторичное антитело (авидин с пероксидазой хрена, eBioscience, №по каталогу: E07418-1632, 1: 500, 100 мкл на лунку) и инкубировали при 37°C в течение 0,5 часа. После того как планшет промыли, 100 мкл на лунку субстратного раствора ТМБ (eBioscience, №по каталогу: 00-4201-56) добавляли и планшет инкубировали в течение 3 минут при комнатной температуре. Затем добавляли 100 мкл на лунку останавливающего раствора (2N H2SO4) для остановки реакции. Колориметрические сигналы получали и считывали при 450 нм с использованием Auto Plate SpectraMax Plus (Supplier: Moleculer Devices; Model: MNR0643; программное обеспечение: SoftMax Pro v5.4). Данные анализировали с помощью программы GraphPad Prism 5 и рассчитывали ИК50 (Фиг. 4-6; Таблицы 8-10). Эти данные продемонстрировали, что анти-PD-L1 антитела (гибридомные, химерные и гуманизированные) могут блокировать связывание PD-1 с PD-L1 на клеточной поверхности, как измерено с помощью ИФА.
Таблица 8. ИК50 анти-PD-L1 гибридомного моноклонального антитела, ингибирующего связывание PD-1 с PD-L1 на поверхности твердого тела.
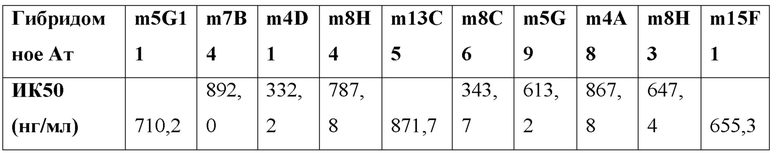
Таблица 9. ИК50 анти-PD-L1 химерного антитела, ингибирующего связывание PD-1 с PD-L1 на поверхности твердого тела
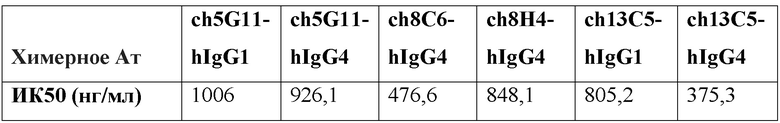
Таблица 10. ИК50 анти-PD-L1 гуманизированного антитела, ингибирующего связывание PD-1 с PD-L1 на поверхности твердого тела
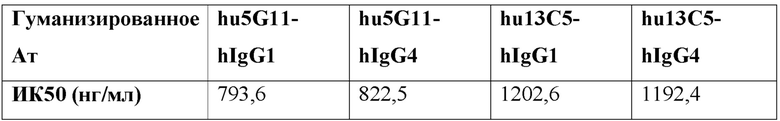
Пример 4: Клеточный анализ связывания анти-PD-L1 антител
[00115] Клеточный анализ связывания анти-PD-L1 антител выполняли на основе связывания с клеточной линией 293T, стабильно экспрессирующей PD-L1 (PD-L1-293T). 2х105 293T-PD-L1 клетки добавляли в каждую лунку 96-луночных культуральных планшетов и инкубировали с указанным антителом (20 мкл/мл в разведении 1: 5) при 4°C в течение 1 ч. После этого клетки промывали три раза буфером для проточной цитометрии, вторичное антитело (ФЭ (фикоэритрин)-козье антимышиное: 1:200; ФЭ- мышиное античеловеческое: 1:10) добавляли к клеткам в количестве 100 мкл/лунку, и инкубировали при температуре 4°C в течение 40 минут.Клетки промывали три раза буфером для проточной цитометрии и анализировали с помощью биоанализатора FACS Array. Связывание гибридомных антител показано на Фиг. 7a и 7б. Связывание химерных антител показано на Фиг. 8. Связывание гуманизированных антител показано на Фиг. 9. Рассчитанные ЭК50 для гибридомных, химерных и гуманизированных антител представлены ниже в Таблицах 11, 12, и 13, соответственно. Эти данные продемонстрировали, что анти-PD-L1 антитела (гибридомные, химерные и гуманизированные) связывают PD-L1, как измерено с помощью проточной цитометрии.
Таблица 11. ЭК50 анти-PD-L1 гибридомного моноклонального антитела с PD-L1 на клеточной поверхности

Таблица 12. ЭК50 анти-PD-L1 химерного антитела с PD-L1 на клеточной поверхности
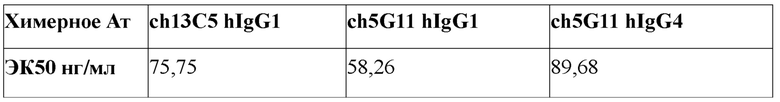
Таблица 13. ЭК50 анти-PD-L1 гуманизированного антитела с PD-L1 на клеточной поверхности

[00116] Влияние анти-PD-L1 антитела на связывание PD-1 с PD-L1 на клеточной поверхности также была исследовано. Кратко, клетки PD-L1-293T суспендировали в буфере для проточной цитометрии (PBS с 3% фетальной телячьей сывороткой). Различные концентрации гибридомных (Фиг. 10), химерных (Фиг. 11), или гуманизированных (Фиг. 12) анти-PD-L1 антител добавляли к клеточной суспензии и инкубировали при температуре 4°C в течение 60 минут в 96-луночных планшетах. Затем белок PD-L1, меченный биотином, добавляли в лунки и инкубировали при температуре 4°C в течение 60 минут.Клетки отмывали 3 раза с использованием PBS и инкубировали с мышиным антибиотин-ФЭ (Biolegend, №по каталогу 409004). Флуоресценцию клеток затем детектировали с помощью анализа проточной цитометрии с использованием биоанализатора FACS Array. Влияние анти-PD-L1 антител на связывание PD-1 с PD-L1-293T измеряли средней интенсивностью флуоресценции (СИФ) окрашивания. Ингибирование связывания PD-1 с помощью анти-PD-L1 гибридомных антител показано на Фиг. 10а и 10б. Ингибирование связывания PD-1 с помощью анти-PD-L1 химерных антител показано на Фиг. 11. Ингибирование связывания PD-1 с помощью анти-PD-L1 гуманизированных антител показано на Фиг. 12. Рассчитанные ЭК50 для гибридомных (Таблица 14), химерных (Таблица 15) и гуманизированных (Таблица 16) антител представлены в таблицах ниже. Эти данные продемонстрировали, что анти-PD-L1 антитела (гибридомные, химерные и гуманизированные) могут блокировать связывание PD-1 с PD-L1 на клеточной поверхности, как измерено с помощью проточной цитометрии.
Таблица 14. ИК50 анти-PD-L1 гибридомного моноклонального антитела, ингибирующего связывание PD-1 с PD-L1 на клеточной поверхности.
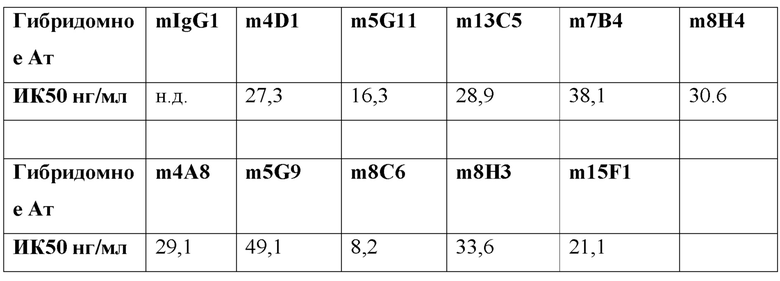
Таблица 15. ИК50 анти-PD-L1 химерного антитела, ингибирующего связывание PD-1 с PD-L1 на клеточной поверхности

Таблица 16. ИК50 анти-PD-L1 гуманизированного антитела, ингибирующего связывание PD-1 с PD-L1 на клеточной поверхности
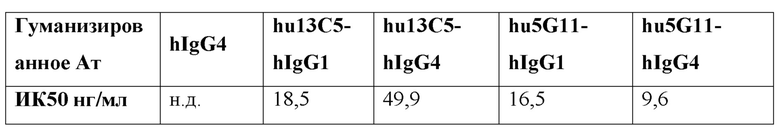
Пример 5: Влияние анти-PD-L1 антител на активацию Т-клеток в реакции смешанной культуры лимфоцитов
[00117] Реакцию смешанной культуры лимфоцитов использовали для демонстрации влияния мышиных (Фиг. 13а, 13б), химерных (Фиг. 14а, 14б), или гуманизированных (Фиг. 15а, 15б) анти-PD-L1 антител в блокировании сигнального пути PD-L1/PD-1 в клетках эффекторных Т-лимфоцитов. Т-клетки в анализе были протестированы на секрецию ИФН-(и ИЛ-2 в присутствии или отсутствии гуманизированных анти-PD-L1 антител.
[00118] Человеческие CD4+ T-клетки были очищены из человеческих МКПК (мононуклеарные клетки периферической крови) с применением набора для выделения с помощью CD4+ негативной селекции (Mitenyi Biotech, №по каталогу 130-091-155). Незрелые дендритные клетки (ДК) были получены из моноцитов, выделенных из человеческих МКПК с применением набора инструментов для получения ДК-МО (дендритные клетки моноцитарного происхождения) (Miltenyi, №по каталогу 130-093-568). Клетки культивировали на питательной среде для дифференцировки ДК-МО в течение 7 суток, а затем индуцировали созревание ДК с использованием питательной среды для созревания ДК-МО в течение 2 суток. Для установления СКЛ-реакции для каждой реакции в общий объем в 200 мкл добавляли 105 очищенных T-клеток и 104 аллогенных зрелых ДК. Тестирование антител проводили при различных концентрациях, как показано на Фиг. 13А, 13б, 14а, 14б, 15а, и 15б (т.е. 20 мкг/мл, 2 мкг/мл, 0,2 мкг/мл 0,02 мкг/мл, 0,002 мкг/мл). В качестве отрицательного контроля использовали или изотип контрольного антитела или отсутствие антитела. Клетки культивировали в течение 5 суток при температуре 37°C. На 6-е сутки уровни ИФН-(и ИЛ-2 в культуральной среде измеряли с помощью набора реагентов для иммуноферментного определения концентрации ИЛ-2 (eBioscience) и набора реагентов для иммуноферментного определения концентрации человеческого ИФН-((R&D, №по каталогу DY285). Результаты продемонстрированы на Фиг. 13а, 14а и 15а для секреции ИЛ-2, и на Фиг. 13б, 14б, и 15б для секреции ИФН-γ. Результаты исследования показали, что гибридомные, химерные и гуманизированные анти-PD-L1 антитела способствуют секреции ИФН-(и ИЛ-2 Т-клетками, демонстрируя зависимость от концентрации. В противоположность этому, культуры, содержащие изотип контрольного антитела, не показали повышение секреции ИФН-(ИЛ-2.
Пример 6: Влияние анти-PD-L1 антител на функции Т-регуляторных клеток
[00119] Т-регуляторные клетки (CD4+, CD25+) представляют собой лимфоциты, которые подавляют иммунный ответ.Влияние регуляторных Т-клеток на секрецию цитокинов эффекторными Т-клетками в СКЛ-реакции тестировали в присутствии или отсутствии химерных или гуманизированных анти-PD-L1 антител. Регуляторные Т-клетки (CD4+CD25+) очищали из МКПК с применением набора для выделения с помощью регуляторных Т-клеток (Miltenyi Biotec, №по каталогу 130-091-301). Незрелые дендритные клетки (ДК) были получены из моноцитов, выделенных из человеческих МКПК с применением набора инструментов для получения ДК-МО (Miltenyi, №по каталогу 130-093-568). Клетки культивировали на питательной среде для дифференцировки ДК-МО в течение 7 суток, а затем индуцировали созревание ДК с использованием питательной среды для созревания ДК-МО в течение 2 суток. Регуляторные Т-клетки добавляли в реакцию смешанной культуры лимфоцитов, содержащую очищенные СD4+ CD25− Т-клетки и аллогенные дендритные клетки в соотношении 4:1 CD4+ CD25− к регуляторным Т-клеткам. Например, в реакцию добавляли 1х10^5 клеток на лунку CD4+CD25- клеток, 1х10^4 клеток на лунку зрелых ДК, и 0.25x10^5 клеток на лунку CD4+CD25+ клеток. Антитела добавляли к каждой реакции в концентрации 10 мкг/мл. В качестве отрицательного контроля использовали или изотип контрольного антитела или отсутствие антитела. Клетки культивировали в течение 5 суток при температуре 37°С.На 5-е сутки, 50 мкл питательной среды отбирали для определения концентрации ИЛ-2 и ИФН-γ. После того, как дополняли каждую лунку 50 мкл культуральной среды, клетки культивировали в течение еще 2-х суток до того, как проводили анализ пролиферации клеток с помощью CTG (анализ жизнеспособности клеток CellTiter-Glo) (Promega, G7573). Уровни ИФН-(и ИЛ-2 в культуральной среде измеряли с помощью набора реагентов для иммуноферментного определения концентрации человеческого ИФН-((R&D, №по каталогу DY285) и набора реагентов для иммуноферментного определения концентрации ИЛ-2 (eBioscience). Как показано на Фиг. 16 химерные и гуманизированные анти-PD-L1 антитела, ch-13C5-hIgG1, ch-13C5-hIgG4, hu-13C5-IgG1, hu-13C5-IgG4, ch-5G11-IgG1, ch-5G11-IgG4, hu-5G11-IgG1, и hu-5G11-IgG4, могут снизить ингибирующий эффект Tрег-клеток на секрецию ИФН-(эффекторными CD4+CD25- Т-клетками, предполагая, что анти-PD-L1 антитела могут модулировать иммунное подавление функции регуляторных Т- клеток.
Пример 7: Влияние гуманизированного анти-PD-L1 антитела на активацию аутологичных Т-клеток
[00120] В данном примере эффект блокирования сигнального пути PD-1/PD-L1 с помощью анти-PD-L1 антитела на активацию Т-клеток был исследован. Очищенные человеческие CD4+Т-клетки (Mitenyi Biotech, №по каталогу 130-091-155) были активированы с использованием 1 мкг/мл растворенного анти-CD3 антитела (R&D, №по каталогу MAB100) в присутствии аутологичных моноцитарных дендритных клеток (ДК). После трех суток активации в присутствии или отсутствии титрованного анти-PD-L1 антитела, культуральную среду отбирали и измеряли концентрацию ИФН-(с помощью иммуноферментного анализа. Результаты, которые представлены на Фиг. 17, также свидетельствуют о том, что блокирование PD-L1 с помощью гуманизированных анти-PD-L1 антител повышают секрецию ИФН-(Т-клетками.
Пример 8: Вторичный иммунный Т-клеточный ответ у человека, вызванный введением столбнячного анатоксина, усилен с помощью гуманизированного анти-PD-L1 антитела
[00121] Для исследования каким образом триггеринг антигенспецифического Т-клеточного рецептора модулируется путем блокирования сигнального пути PD-1/PD-L1 с анти-PD-L1 антителами, анализ вторичного иммунного Т-клеточного ответа применяли с использованием столбнячного анатоксина (ТТ) (антиген) для стимуляции памяти предшественников Т-клеток в крови здоровых доноров, иммунизированных ТТ. С этой целью свежие МКПК из доноров, иммунизированных ТТ недавно [<1 года], высевали в 96-луночные круглодонные планшеты (Costar, №по каталогу 3799) по 4х10^5 клеток на лунку, используя среду RPMI1640 (Invitrogen, №по каталогу A10491-01) с добавлением 80 ед/мл пенициллина, 80 г/мл стрептомицина и 30% аутологичной сыворотки, добавляли гуманизированные 5G11 или 13C5 в различных концентрациях, и стимулировали с помощью 0,1 мкг/мл SEB (стафилококковый энтеротоксин) и 1 мкг/мл ТТ (Astarte Biologies). После совместного культивировании в течение 7 суток при температуре 37°С, 5% CO2, супернатант собирали и измеряли концентрацию ИФН-γ. На Фиг. 18а и 18б представлены результаты анализа с использованием МКПК от двух разных доноров. Результаты исследования демонстрируют, что по сравнению с одним антигеном ТТ, блокирование PD-L1 с применением анти-PD-L1 антитела приводило к повышению секреции ИФН-(Т-клетками памяти.
[00122] В целом, гуманизированные антитела 13C5 и 5G11 сохраняют функциональную активность их исходных антител в процессе очеловечивания.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Crown Bioscience, Inc.
Zha, Jiping
Sun, Ziyong
Qiu, Junzhuan
<120> АНТИ PD-L1 АНТИТЕЛА
<130> CRBI-007/01WO
<150> PCT/CN2014/083715
<151> 2014-08-05
<160> 156
<170> PatentIn версии 3.5
<210> 1
<211> 348
<212> ДНК
<213> Mus sp.
<400> 1
gaggtgaagc tggtggagtc tgggggaggc ttagtgaagc ctggagggtc cctgaaactc 60
tcctgtgcag cctctggatt cattttcaga agctatggca tgtcttgggt tcgccagact 120
ccagagaaga ggctggagtg ggtcgcatcc attagtagtg gtggtagcac ctactatcca 180
gacagtgtga agggccgatt caccatctcc agagataatg ccaggaacat cttgtacctg 240
caaatgagca gtctgaggtc tgaggacacg gccatgtatg actgtgcaag aggctatgat 300
tcggggtttg cttattgggg ccaagggact ctggtcactg tctctgaa 348
<210> 2
<211> 116
<212> ПРТ
<213> Mus sp.
<400> 2
Glu Val Lys Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Ile Phe Arg Ser Tyr
20 25 30
Gly Met Ser Trp Val Arg Gln Thr Pro Glu Lys Arg Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Ser Gly Gly Ser Thr Tyr Tyr Pro Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Arg Asn Ile Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Asp Cys Ala
85 90 95
Arg Gly Tyr Asp Ser Gly Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Glu
115
<210> 3
<211> 336
<212> ДНК
<213> Mus sp.
<400> 3
gacattgtgc tgacacagtc tcctgcttcc ttagctgttt ctctggggca gagggccacc 60
atctcatgca gggccagcca aagtgtcagt acttctagct ctagttttat gcactggtac 120
caacagaaac caggacagcc acccaaactc ctcatcaagt atgcatccaa cctagaatct 180
ggggtccctg ccaggttcag tggcagtggg tctgggacag acttcaccct caacatccat 240
cctgtggagg aggaggatac tgcaacatat tactgtcagc acagttggga gattccgtac 300
acgttcggag gggggaccaa gctggaaata aaacgg 336
<210> 4
<211> 112
<212> ПРТ
<213> Mus sp.
<400> 4
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Arg Ala Ser Gln Ser Val Ser Thr Ser
20 25 30
Ser Ser Ser Phe Met His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Lys Tyr Ala Ser Asn Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Asn Ile His
65 70 75 80
Pro Val Glu Glu Glu Asp Thr Ala Thr Tyr Tyr Cys Gln His Ser Trp
85 90 95
Glu Ile Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
<210> 5
<211> 348
<212> ДНК
<213> Mus sp.
<400> 5
gaagtaaagt tggtggagtc tgggggaggc ttagtgaagc ctggagggtc cctgaaactc 60
tcctgtgcag cctctggatt cactttcaga agctatggca tgtcttgggt tcgccagact 120
ccagagaaga ggctggagtg ggtcgcatcc attagtagtg gtggtaccac ctactatcca 180
gacagtgtga agggccgatt catcatctcc agagataatg ccaggaacat cctgtacctg 240
caaatgagca gtctgaggtc tgaggacacg gccatgtatt attgtgcaaa aggctatgat 300
tcggggtttg cttactgggg ccaagggact ctggtcattg tctctgca 348
<210> 6
<211> 116
<212> ПРТ
<213> Mus sp.
<400> 6
Glu Val Lys Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Ser Tyr
20 25 30
Gly Met Ser Trp Val Arg Gln Thr Pro Glu Lys Arg Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Ser Gly Gly Thr Thr Tyr Tyr Pro Asp Ser Val Lys
50 55 60
Gly Arg Phe Ile Ile Ser Arg Asp Asn Ala Arg Asn Ile Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Lys Gly Tyr Asp Ser Gly Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Ile Val Ser Ala
115
<210> 7
<211> 333
<212> ДНК
<213> Mus sp.
<400> 7
gacattgtgc tgacacagtc tcctccttcc ttagctgtat ctctggggca gagggccacc 60
atctcatgca gggccagcca aagtgtcagt acatctagtt ctagttatat gcactggtac 120
caacagaaac caggacagcc tcccaaactc ctcatcaagt atgcatccaa cctagaatct 180
ggggtccctg ccaggttcag tggcagtggg tctgggacag acttcaccct caacatccat 240
cctgtggagg aggaggatac tgcaacatat tactgtcagc acagttggga gattccgtac 300
acgttcggag gggggaccaa gctggaaata aaa 333
<210> 8
<211> 111
<212> ПРТ
<213> Mus sp.
<400> 8
Asp Ile Val Leu Thr Gln Ser Pro Pro Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Arg Ala Ser Gln Ser Val Ser Thr Ser
20 25 30
Ser Ser Ser Tyr Met His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Lys Tyr Ala Ser Asn Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Asn Ile His
65 70 75 80
Pro Val Glu Glu Glu Asp Thr Ala Thr Tyr Tyr Cys Gln His Ser Trp
85 90 95
Glu Ile Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 9
<211> 348
<212> ДНК
<213> Mus sp.
<400> 9
caggtgcagc tgaagcagtc aggacctggc ctagtgcagc cctcacagag cctgtccatc 60
acctgcacag tctctggttt ctcattaact acctatggtg tacactgggt tcgccagtct 120
ccaggaaagg gtctggaatg gctgggagtg atatggcgtg gtgtaaccac agactataat 180
gcagctttca tgtccagact gaccatcacc aaggacaatt ccaagagcca agttttcttt 240
aaaatgaaca gtctgcaagc taatgacaca gccatatatt actgtgccag actgggtttc 300
tatgctatgg actactgggg tcaaggaacc tcagtcaccg tctcctca 348
<210> 10
<211> 116
<212> ПРТ
<213> Mus sp.
<400> 10
Gln Val Gln Leu Lys Gln Ser Gly Pro Gly Leu Val Gln Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Thr Tyr
20 25 30
Gly Val His Trp Val Arg Gln Ser Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Arg Gly Val Thr Thr Asp Tyr Asn Ala Ala Phe Met
50 55 60
Ser Arg Leu Thr Ile Thr Lys Asp Asn Ser Lys Ser Gln Val Phe Phe
65 70 75 80
Lys Met Asn Ser Leu Gln Ala Asn Asp Thr Ala Ile Tyr Tyr Cys Ala
85 90 95
Arg Leu Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser Val
100 105 110
Thr Val Ser Ser
115
<210> 11
<211> 324
<212> ДНК
<213> Mus sp.
<400> 11
agtattgtga tgacccagac tcccaaattc ctgcttgtat cagcaggaga cagggttacc 60
ataacctgca aggccagtca gagtgtgagt aatgatgtag cttggtacca gcagaagcca 120
gggcagtctc ctaaactgct gatatattat gcagccaatc gctacactgg agtccctgat 180
cgcttcactg gcagtggata tgggacggat ttcactttca ccatcagcat tgtgcaggct 240
gaagacctgg cagtttattt ctgtcagcag gattatacct ctccgtacac gttcggaggg 300
gggaccaagc tggaaataaa acgg 324
<210> 12
<211> 107
<212> ПРТ
<213> Mus sp.
<400> 12
Ser Ile Val Met Thr Gln Thr Pro Lys Phe Leu Leu Val Ser Ala Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Val Ser Asn Asp
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Ala Asn Arg Tyr Thr Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Phe Thr Ile Ser Ile Val Gln Ala
65 70 75 80
Glu Asp Leu Ala Val Tyr Phe Cys Gln Gln Asp Tyr Thr Ser Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 13
<211> 348
<212> ДНК
<213> Mus sp.
<400> 13
caggtgcagc tgaagcagtc aggacctggc ctagtgcagc cctcacagag cctgtccatc 60
acctgcacag tctctggttt ctcattaact agctatggtg tacactgggt tcgccagtct 120
ccaggaaagg gtctggagtg gctgggagtg atatggagtg gtggagtcac agactataat 180
gcagctttca tatccagact gagcatcagc aaggacaatt ccaagagcca agttttcttt 240
aaaatgaaca gtctgcaagc taatgacaca gccatatatt actgtgccag actcggtttc 300
tatgctatgg actactgggg tcaaggaacc tcagtcaccg tctcctca 348
<210> 14
<211> 116
<212> ПРТ
<213> Mus sp.
<400> 14
Gln Val Gln Leu Lys Gln Ser Gly Pro Gly Leu Val Gln Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val His Trp Val Arg Gln Ser Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Ser Gly Gly Val Thr Asp Tyr Asn Ala Ala Phe Ile
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Phe
65 70 75 80
Lys Met Asn Ser Leu Gln Ala Asn Asp Thr Ala Ile Tyr Tyr Cys Ala
85 90 95
Arg Leu Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser Val
100 105 110
Thr Val Ser Ser
115
<210> 15
<211> 321
<212> ДНК
<213> Mus sp.
<400> 15
agtattgtga tgacccagac tcccaaattc ctacttgtat cagcaggaga cagggttacc 60
ataacctgca aggccagtca gagtgtgagt aatgatgtag gttggtacca acagaagcca 120
gggcagtctc ctaaactact gatatactat gcatccaatc gctactctgg agtccctgat 180
cgcttcactg gcagtggata tgggacggat ttcactttca ccatcagcac tgtgcaggct 240
gaagacctgg cagtttattt ctgtcaacaa gattatacct ctccgtacac gttcggaggg 300
gggaccaagc tggaaataaa a 321
<210> 16
<211> 107
<212> ПРТ
<213> Mus sp.
<400> 16
Ser Ile Val Met Thr Gln Thr Pro Lys Phe Leu Leu Val Ser Ala Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Val Ser Asn Asp
20 25 30
Val Gly Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Ser Asn Arg Tyr Ser Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Phe Thr Ile Ser Thr Val Gln Ala
65 70 75 80
Glu Asp Leu Ala Val Tyr Phe Cys Gln Gln Asp Tyr Thr Ser Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 17
<211> 357
<212> ДНК
<213> Mus sp.
<400> 17
gaggtgaagc tgttcgagtc tggaggtggc ctggtgcagc ctggaggatc cctgaaactc 60
tcctgtgtag cctcaggatt cgattttagt acatactgga tgcattgggt ccggcaggct 120
ccagggcaag ggctagaatg gattggacaa attaatccag atagcactac gataaactat 180
gcgccatctc taaaggatag attcatcatc tccagagaca acgccaaaaa tacgctgttc 240
ctgcaaatga gcaaagtgag atctgaggac actgcccttt attactgtgc aaaacccggg 300
gactatggtt acgactttga ctgctggggc caaggcacca ctctcacagt ctcctca 357
<210> 18
<211> 119
<212> ПРТ
<213> Mus sp.
<400> 18
Glu Val Lys Leu Phe Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Val Ala Ser Gly Phe Asp Phe Ser Thr Tyr
20 25 30
Trp Met His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gln Ile Asn Pro Asp Ser Thr Thr Ile Asn Tyr Ala Pro Ser Leu
50 55 60
Lys Asp Arg Phe Ile Ile Ser Arg Asp Asn Ala Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Ser Lys Val Arg Ser Glu Asp Thr Ala Leu Tyr Tyr Cys
85 90 95
Ala Lys Pro Gly Asp Tyr Gly Tyr Asp Phe Asp Cys Trp Gly Gln Gly
100 105 110
Thr Thr Leu Thr Val Ser Ser
115
<210> 19
<211> 339
<212> ДНК
<213> Mus sp.
<400> 19
gatgttttga tgacccaaac tccactctac ctgcctgtca gtcttggaga tcaggcctcc 60
atctcttgca gatctagtca gatcattgta catagtaatg caaacaccta tttagaatgg 120
ttcctgcaga aaccaggcca gtctccaaag ctcctgatct acaaagtttc caaccgattt 180
tctggggtcc cagacaggtt cagtggcagt ggatcaggga cagatttcac actcaagatc 240
agcagagtgg aggctgagga tctgggagtt tattactgct ttcaaggttc acatgttccg 300
tacacgttcg gaggggggac caagctggaa ataaaacgg 339
<210> 20
<211> 112
<212> ПРТ
<213> Mus sp.
<400> 20
Asp Val Leu Met Thr Gln Thr Pro Leu Tyr Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Ile Ile Val His Ser
20 25 30
Asn Ala Asn Thr Tyr Leu Glu Trp Phe Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Tyr Cys Phe Gln Gly
85 90 95
Ser His Val Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 21
<211> 357
<212> ДНК
<213> Mus sp.
<400> 21
gaggtgcagc ttcaggagtc aggacctagc ctcgtgaaac cttctcagac tctgtccctc 60
acctgttctg tcactggcga ctccatcacc agtggttact ggaactggat ccggaaattc 120
ccagggaata aacttgagta catggggtac ataagctaca gtggtagcac ttactacaat 180
ccatctctca aaagtcgaat ctccatcact cgagacacat ccaagaacca gtactacctg 240
cagttgaatt ctgtgactac tgaggacaca gccacatatt actgtgcaag aagtctacta 300
tggttctcta cggggtttgc ttactggggc caagggactc tggtcactgt ctctgca 357
<210> 22
<211> 119
<212> ПРТ
<213> Mus sp.
<400> 22
Glu Val Gln Leu Gln Glu Ser Gly Pro Ser Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ser Val Thr Gly Asp Ser Ile Thr Ser Gly
20 25 30
Tyr Trp Asn Trp Ile Arg Lys Phe Pro Gly Asn Lys Leu Glu Tyr Met
35 40 45
Gly Tyr Ile Ser Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Ile Ser Ile Thr Arg Asp Thr Ser Lys Asn Gln Tyr Tyr Leu
65 70 75 80
Gln Leu Asn Ser Val Thr Thr Glu Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Ser Leu Leu Trp Phe Ser Thr Gly Phe Ala Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ala
115
<210> 23
<211> 324
<212> ДНК
<213> Mus sp.
<400> 23
caaattgttc tcacccagtc tccagcaatc atgtctgcat ctcctgggga gaaggtcacc 60
ttgacctgca gtgccagctc aagtgtaagt tccagctact tgtactggaa ccagcagaag 120
ccaggatcct cccccaaagt ctggatttat aacacatcca acctggcttc tggagtccct 180
gctcgcttca gtggcagtgg gtctgggacc tcttactctc tcacaatcag cagcatggag 240
gctgaagatg ctgcctctta tttctgccat cagtggagaa gttacccacc cacgctcggt 300
gctgggacca agctggagct gaaa 324
<210> 24
<211> 108
<212> ПРТ
<213> Mus sp.
<400> 24
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Leu Thr Cys Ser Ala Ser Ser Ser Val Ser Ser Ser
20 25 30
Tyr Leu Tyr Trp Asn Gln Gln Lys Pro Gly Ser Ser Pro Lys Val Trp
35 40 45
Ile Tyr Asn Thr Ser Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Glu
65 70 75 80
Ala Glu Asp Ala Ala Ser Tyr Phe Cys His Gln Trp Arg Ser Tyr Pro
85 90 95
Pro Thr Leu Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 25
<211> 348
<212> ДНК
<213> Mus sp.
<400> 25
caggtgcagc tgaagcagtc aggacctggc ctagtgcagc cctcacagag cctgtccatc 60
acctgcacag tctctggttt ctcattaact agctatggtg tacactgggt tcgccagtct 120
ccaggaaagg gtctggagtg gctgggagtg atatggagtg gtggaatcac agactataat 180
gcagctttca aatccagact gagcatcagc aaggacaatt ccaagagcca agttttcttt 240
aagatgaaca gtctgcaagc taatgacaca gccatatatt tctgtgccag actgggtttt 300
tatgctatgg actactgggg tcaaggaacc tcagtcaccg tctcctca 348
<210> 26
<211> 116
<212> ПРТ
<213> Mus sp.
<400> 26
Gln Val Gln Leu Lys Gln Ser Gly Pro Gly Leu Val Gln Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val His Trp Val Arg Gln Ser Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Ser Gly Gly Ile Thr Asp Tyr Asn Ala Ala Phe Lys
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Phe
65 70 75 80
Lys Met Asn Ser Leu Gln Ala Asn Asp Thr Ala Ile Tyr Phe Cys Ala
85 90 95
Arg Leu Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser Val
100 105 110
Thr Val Ser Ser
115
<210> 27
<211> 318
<212> ДНК
<213> Mus sp.
<400> 27
caaattgttc tcacccagtc tccagcaatc atgtctgcat ctccagggga gaaggtcacc 60
atgacctgca gtgccaactc aagtgtaagt tacatgcact ggtaccagca gaagtcaggc 120
acttccccca aaagatggat ttatgacaca tccaaactgg cttctggagt ccctgctcgc 180
ttcagtggca gtgggtctgg gacctcttac tctctcacaa tcagcagcat gggggctgaa 240
gatgctgcca cttattactg ccagcagtgg agtagtaacc catggacgtt cggtggaggc 300
accaagctgg aaatcaaa 318
<210> 28
<211> 106
<212> ПРТ
<213> Mus sp.
<400> 28
Gln Ile Val Leu Thr Gln Ser Pro Ala Ile Met Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Ser Ala Asn Ser Ser Val Ser Tyr Met
20 25 30
His Trp Tyr Gln Gln Lys Ser Gly Thr Ser Pro Lys Arg Trp Ile Tyr
35 40 45
Asp Thr Ser Lys Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Ser Ser Met Gly Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Ser Asn Pro Trp Thr
85 90 95
Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 29
<211> 348
<212> ДНК
<213> Mus sp.
<400> 29
gaagtgaaac tggtggagtc tgggggaggc ttagtgaagc ctggagggtc cctgaaactc 60
tcctgtgcag cctctggatt cactttcagg agctatggca tgtcttgggc tcgccagatt 120
ccagagaaga ggctggagtg ggtcgcatcc attagtagtg gtggaaccac ctactatcta 180
gggagtgtgc agggccgatt cacaatctcc agagataatg ccaggaacat cctgtacctg 240
caaatgagca gtctgaggtc tgaggacacg gccatgtatt attgtgcaag aggctatgat 300
gcgggatttg cttactgggg ccaagggact ctggtcagtg tctctgaa 348
<210> 30
<211> 116
<212> ПРТ
<213> Mus sp.
<400> 30
Glu Val Lys Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Ser Tyr
20 25 30
Gly Met Ser Trp Ala Arg Gln Ile Pro Glu Lys Arg Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Ser Gly Gly Thr Thr Tyr Tyr Leu Gly Ser Val Gln
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Arg Asn Ile Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg Gly Tyr Asp Ala Gly Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Ser Val Ser Glu
115
<210> 31
<211> 333
<212> ДНК
<213> Mus sp.
<400> 31
gacattgtgc tgacacagtc tcctgcttcc ttagctgtat ctctggggca gagggccacc 60
atctcatgca gggccagcca aagtgtcagt acatctagct atagttatat gcactggtac 120
caacagaaac caggacagcc tcccaaactc ctcatcaagt atgcatccaa cctagaatct 180
ggggtccctg ccaggttcag tggcagtggg tctgggacag acttcaccct caacatccat 240
cctgtggagg aggaggatac tgcaacatat tactgtcaga acagttggga gattccgtac 300
acgttcggag gggggaccaa gctggaaata aaa 333
<210> 32
<211> 111
<212> ПРТ
<213> Mus sp.
<400> 32
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Arg Ala Ser Gln Ser Val Ser Thr Ser
20 25 30
Ser Tyr Ser Tyr Met His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Lys Tyr Ala Ser Asn Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Asn Ile His
65 70 75 80
Pro Val Glu Glu Glu Asp Thr Ala Thr Tyr Tyr Cys Gln Asn Ser Trp
85 90 95
Glu Ile Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 33
<211> 351
<212> ДНК
<213> Mus sp.
<400> 33
gaggtgcagc ttcaggagtc aggacctagc ctcgtcaaac cttctcagac tctgtccctc 60
acctgttctg tcactggcga ctccatcacc agtggttact ggacctggat ccggaaattc 120
ccagggaata aacttgaata catgggatac ataagctaca ctggtagcac ttactacaat 180
ccatctctca aaagtcgaat ctccatctct cgagacacat ccaagagcca gtactacctg 240
cagttgaatt ctgtgactac tgaggacaca gccacatatt actgtgcaag acagagggat 300
tggttagggt ttgcttactg gggccaaggg actctggtca ctgtctctgc a 351
<210> 34
<211> 117
<212> ПРТ
<213> Mus sp.
<400> 34
Glu Val Gln Leu Gln Glu Ser Gly Pro Ser Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Ser Val Thr Gly Asp Ser Ile Thr Ser Gly
20 25 30
Tyr Trp Thr Trp Ile Arg Lys Phe Pro Gly Asn Lys Leu Glu Tyr Met
35 40 45
Gly Tyr Ile Ser Tyr Thr Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Ile Ser Ile Ser Arg Asp Thr Ser Lys Ser Gln Tyr Tyr Leu
65 70 75 80
Gln Leu Asn Ser Val Thr Thr Glu Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Gln Arg Asp Trp Leu Gly Phe Ala Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ala
115
<210> 35
<211> 339
<212> ДНК
<213> Mus sp.
<400> 35
gatattgtga tgacacagac tccatcctcc ctagctgtgt cacttggaga gaaggttact 60
atgagctgca agtccagtca gagcctttta tatagtagca atcaaaagaa ctccttggcc 120
tggtaccagc agaaaccagg acagtctcct aaactgctga tttactgggc atccaatagg 180
gaatctgggg tccctgatcg cttcacaggc agtagctctg ggacagattt cactctcacc 240
atcagcagtg tgaaggctga agacctggca gtttattact gtcagcaata ttatagctat 300
ccgctcacgt tcggtgctgg gaccaagctg gagctgaaa 339
<210> 36
<211> 113
<212> ПРТ
<213> Mus sp.
<400> 36
Asp Ile Val Met Thr Gln Thr Pro Ser Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Lys Val Thr Met Ser Cys Lys Ser Ser Gln Ser Leu Leu Tyr Ser
20 25 30
Ser Asn Gln Lys Asn Ser Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Ser Pro Lys Leu Leu Ile Tyr Trp Ala Ser Asn Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Ser Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Lys Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Ser Tyr Pro Leu Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu
100 105 110
Lys
<210> 37
<211> 348
<212> ДНК
<213> Mus sp.
<400> 37
gaagagaagc tggtggagtc tgggggaggc ttagtgaagc ctggagggtc cctgaaactc 60
tcctgtgcag cctctggatt cagtttcagt agttatggca tgtcttgggt tcgtcagact 120
ccagagaaga ggctggagtg ggtcgcatcc atcagtagtg gtggtagtat ctactatcca 180
gacagtgtga agggccgatt caccatctcc agagataatg ccaggaacat cctgtacctg 240
caaatgagca gtctgaggtc tgaggacacg gccatgtatt attgtgcaag aggctatgat 300
gcggggtttg ctttctgggg ccaagggaca ctggtcactg cctctgca 348
<210> 38
<211> 116
<212> ПРТ
<213> Mus sp.
<400> 38
Glu Glu Lys Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Ser Phe Ser Ser Tyr
20 25 30
Gly Met Ser Trp Val Arg Gln Thr Pro Glu Lys Arg Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Ser Gly Gly Ser Ile Tyr Tyr Pro Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Arg Asn Ile Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg Gly Tyr Asp Ala Gly Phe Ala Phe Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Ala Ser Ala
115
<210> 39
<211> 333
<212> ДНК
<213> Mus sp.
<400> 39
gacattgtgc tgacacagtc tcctgcttcc ttagctgtat ctctggggca gagggccacc 60
atctcatgca gggccagcca aagtgtcagt acatctagtt atagttatgt gcactggtac 120
caacagaaac caggacagcc acccaaactc ctcatcaagt atgcatccaa cctagaatct 180
ggggtccctg ccaggttcag tggcagtggg tctgggacag acttcaccct caacatccat 240
cctgtggagg aggaggatac tgcaacatat tactgtcagc acagttggga gattccgtac 300
acgttcggag gggggaccaa gctggaaata aaa 333
<210> 40
<211> 111
<212> ПРТ
<213> Mus sp.
<400> 40
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Arg Ala Ser Gln Ser Val Ser Thr Ser
20 25 30
Ser Tyr Ser Tyr Val His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Lys Tyr Ala Ser Asn Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Asn Ile His
65 70 75 80
Pro Val Glu Glu Glu Asp Thr Ala Thr Tyr Tyr Cys Gln His Ser Trp
85 90 95
Glu Ile Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 41
<211> 348
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность вариабельной области тяжелой цепи гуманизированного антитела 5G11
<400> 41
cagatcacac tgaaagaaag cggccctacc ctggtcaagc caactcagac cctgacactg 60
acttgcaccg tgtctgggtt ctctctgagt acatacggag tccactggat caggcagccc 120
cctggcaaag ctctggagtg gctgggagtg atttggcggg gcgtcaccac agactataac 180
gccgctttta tgtcaagact gacaatcact aaggataaca gcaaaaatca ggtggtcctg 240
accatgaaca atatggaccc cgtggatacc gcaacatact attgtgcccg gctggggttc 300
tacgccatgg actattgggg ccaggggact ctggtgaccg tctcgagc 348
<210> 42
<211> 116
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Последовательность вариабельной области тяжелой цепи гуманизированного антитела 5G11
<400> 42
Gln Ile Thr Leu Lys Glu Ser Gly Pro Thr Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Thr Tyr
20 25 30
Gly Val His Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Arg Gly Val Thr Thr Asp Tyr Asn Ala Ala Phe Met
50 55 60
Ser Arg Leu Thr Ile Thr Lys Asp Asn Ser Lys Asn Gln Val Val Leu
65 70 75 80
Thr Met Asn Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Leu Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 43
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность вариабельной области легкой цепи гуманизированного антитела 5G11
<400> 43
gatatccaga tgactcagtc tccaagcagc ctgtctgcat ctgtggggga cagggtcacc 60
atcacatgca aagcatctca gagtgtgtca aacgatgtcg cctggtacca gcagaagccc 120
ggaaaagctc ctaagctgct gatttactat gccgctaatc ggtacactgg cgtgccagac 180
agattcagcg gatccggata tggaaccgat ttcactttta ccatcagctc cctgcagcca 240
gaggacattg ccacatattt ctgtcagcag gattacacaa gcccctatac ttttggccag 300
gggaccaaac tggaaatcaa g 321
<210> 44
<211> 107
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Последовательность вариабельной области легкой цепи гуманизированного антитела 5G11
<400> 44
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Val Ser Asn Asp
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Ala Asn Arg Tyr Thr Gly Val Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Asp Tyr Thr Ser Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 45
<211> 348
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность вариабельной области тяжелой цепи гуманизированного антитела 13C5
<400> 45
gaggtgcagc tggtcgagtc aggagggggg ctggtcaagc caggagggtc actgcgactg 60
agctgcgcag cttccgggtt catctttagg tcttatggca tgagttgggt gcgccaggca 120
ccagggaaag gactggagtg ggtcgcttca atcagctccg gaggcagcac ttactatcct 180
gactccgtga agggccggtt caccatttct agagataacg ccaaaaatag tctgtacctg 240
cagatgaact ctctgcgagc agaagacaca gccgtctacg attgtgctag aggatatgac 300
agcggctttg catactgggg ccaggggacc ctggtgacag tctcgagc 348
<210> 46
<211> 116
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Последовательность вариабельной области тяжелой цепи гуманизированного антитела 13C5
<400> 46
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ile Phe Arg Ser Tyr
20 25 30
Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Ser Gly Gly Ser Thr Tyr Tyr Pro Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Asp Cys Ala
85 90 95
Arg Gly Tyr Asp Ser Gly Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 47
<211> 333
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность вариабельной области легкой цепи гуманизироавнного антитела 13C5
<400> 47
gacattgtgc tgactcagag ccccgcttca ctggcagtgt ctccagggca gcgggcaacc 60
atcacatgca gagcctcaca gagcgtctcc accagctcct ctagtttcat gcactggtac 120
cagcagaagc ccggacagcc ccctaagctg ctgatcaaat atgctagcaa cctggagtcc 180
ggcgtgccag ccaggttctc tggcagtggg tcaggaaccg actttactct gaccattaat 240
cccgtcgaag ccaacgatac agctaattac tattgtcagc attcctggga gatcccttac 300
acatttggcc aggggactaa gctggagatc aag 333
<210> 48
<211> 111
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Последовательность вариабельной области легкой цепи гуманизированного антитела 13C5
<400> 48
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Pro Gly
1 5 10 15
Gln Arg Ala Thr Ile Thr Cys Arg Ala Ser Gln Ser Val Ser Thr Ser
20 25 30
Ser Ser Ser Phe Met His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Lys Tyr Ala Ser Asn Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn
65 70 75 80
Pro Val Glu Ala Asn Asp Thr Ala Asn Tyr Tyr Cys Gln His Ser Trp
85 90 95
Glu Ile Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 49
<211> 1329
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность тяжелой цепи химерного антитела 8C6-IgG4 (F234A/L235A)
<400> 49
caggtgcagc tgaagcagtc aggacctggc ctagtgcagc cctcacagag cctgtccatc 60
acctgcacag tctctggttt ctcattaact agctatggtg tacactgggt tcgccagtct 120
ccaggaaagg gtctggagtg gctgggagtg atatggagtg gtggagtcac agactataat 180
gcagctttca tatccagact gagcatcagc aaggacaatt ccaagagcca agttttcttt 240
aaaatgaaca gtctgcaagc taatgacaca gccatatatt actgtgccag actcggtttc 300
tatgctatgg actactgggg tcaaggaacc tcagtcaccg tctcgagcgc ctccaccaag 360
ggacccagcg tgtttcccct ggccccctgt tccagatcca cctccgaaag cacagccgct 420
ctcggctgcc tggtcaagga ttacttccct gagcccgtga cagtctcctg gaatagcggc 480
gctctgacct ccggcgtgca taccttccct gctgtgctgc aatcctccgg actgtacagc 540
ctgagcagcg tggtcaccgt gccttcctcc agcctgggaa ccaaaaccta cacatgcaac 600
gtggaccaca agcccagcaa caccaaagtg gacaagaggg tggagtccaa gtacggaccc 660
ccttgtcctc cctgccctgc tcctgaagcc gctggaggac ctagcgtgtt cctgtttccc 720
cccaagccca aggacaccct catgatctcc aggacccccg aggtgacctg tgtcgtggtg 780
gacgtgagcc aagaggaccc cgaggtgcag ttcaactggt acgtggatgg cgtcgaggtc 840
cataacgcca agaccaagcc tagggaggag cagttcaaca gcacctacag agtggtgagc 900
gtcctgaccg tgctccacca agactggctg aacggcaagg aatacaagtg caaggtctcc 960
aacaagggac tcccttcctc catcgagaag accatcagca aggccaaggg ccagcccaga 1020
gaaccccaag tctacacact gccccccagc caagaggaaa tgaccaagaa ccaggtgagc 1080
ctgacctgcc tggtgaaagg cttctacccc agcgacattg ctgtcgaatg ggagagcaac 1140
ggccaacccg agaacaacta caagaccacc ccccctgtgc tcgacagcga cggctccttc 1200
ttcctctaca gcaggctgac agtggacaag tccaggtggc aagagggcaa tgtcttcagc 1260
tgtagcgtca tgcacgaggc cctccacaac cactacaccc agaagagcct gtccctctcc 1320
ctgggctga 1329
<210> 50
<211> 442
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательсноть тяжелой цепи химерного антитела 8C6-IgG4 (F234A/L235A)
<400> 50
Gln Val Gln Leu Lys Gln Ser Gly Pro Gly Leu Val Gln Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Ser Tyr
20 25 30
Gly Val His Trp Val Arg Gln Ser Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Ser Gly Gly Val Thr Asp Tyr Asn Ala Ala Phe Ile
50 55 60
Ser Arg Leu Ser Ile Ser Lys Asp Asn Ser Lys Ser Gln Val Phe Phe
65 70 75 80
Lys Met Asn Ser Leu Gln Ala Asn Asp Thr Ala Ile Tyr Tyr Cys Ala
85 90 95
Arg Leu Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro
210 215 220
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
225 230 235 240
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
245 250 255
Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn
260 265 270
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
275 280 285
Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
290 295 300
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
305 310 315 320
Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys
325 330 335
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu
340 345 350
Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
355 360 365
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
370 375 380
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
385 390 395 400
Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly
405 410 415
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
420 425 430
Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440
<210> 51
<211> 645
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность легкой цепи химерного антитела 8C6
<400> 51
agtattgtga tgacccagac tcccaaattc ctacttgtat cagcaggaga cagggttacc 60
ataacctgca aggccagtca gagtgtgagt aatgatgtag gttggtacca acagaagcca 120
gggcagtctc ctaaactact gatatactat gcatccaatc gctactctgg agtccctgat 180
cgcttcactg gcagtggata tgggacggat ttcactttca ccatcagcac tgtgcaggct 240
gaagacctgg cagtttattt ctgtcaacaa gattatacct ctccgtacac gttcggaggg 300
gggaccaagc tggaaataaa acgtacggtg gccgcaccaa gcgtcttcat cttcccgcca 360
tctgatgagc agttgaaatc tggaactgcc tctgttgtgt gcctgctgaa taacttctat 420
cccagagagg ccaaagtaca gtggaaggtg gataacgccc tccaatcggg taactcccag 480
gagagtgtca cagagcagga cagcaaggac agcacctaca gcctcagcag caccctgacg 540
ctgagcaaag cagactacga gaaacacaaa gtctacgcct gcgaagtcac ccatcagggc 600
ctgagctcgc ccgtcacaaa gagctttaac agaggcgagt gctga 645
<210> 52
<211> 214
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность легкой цепи химерного антитела 8C6
<400> 52
Ser Ile Val Met Thr Gln Thr Pro Lys Phe Leu Leu Val Ser Ala Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Val Ser Asn Asp
20 25 30
Val Gly Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Ser Asn Arg Tyr Ser Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Phe Thr Ile Ser Thr Val Gln Ala
65 70 75 80
Glu Asp Leu Ala Val Tyr Phe Cys Gln Gln Asp Tyr Thr Ser Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 53
<211> 1329
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность тяжелой цепи химерного антитела 8H4-IgG4 (F234A/L235A)
<400> 53
gaagtgaaac tggtggagtc tgggggaggc ttagtgaagc ctggagggtc cctgaaactc 60
tcctgtgcag cctctggatt cactttcagg agctatggca tgtcttgggc tcgccagatt 120
ccagagaaga ggctggagtg ggtcgcatcc attagtagtg gtggaaccac ctactatcta 180
gggagtgtgc agggccgatt cacaatctcc agagataatg ccaggaacat cctgtacctg 240
caaatgagca gtctgaggtc tgaggacacg gccatgtatt attgtgcaag aggctatgat 300
gcgggatttg cttactgggg ccaagggact ctggtcagtg tctcgagcgc ctccaccaag 360
ggacccagcg tgtttcccct ggccccctgt tccagatcca cctccgaaag cacagccgct 420
ctcggctgcc tggtcaagga ttacttccct gagcccgtga cagtctcctg gaatagcggc 480
gctctgacct ccggcgtgca taccttccct gctgtgctgc aatcctccgg actgtacagc 540
ctgagcagcg tggtcaccgt gccttcctcc agcctgggaa ccaaaaccta cacatgcaac 600
gtggaccaca agcccagcaa caccaaagtg gacaagaggg tggagtccaa gtacggaccc 660
ccttgtcctc cctgccctgc tcctgaagcc gctggaggac ctagcgtgtt cctgtttccc 720
cccaagccca aggacaccct catgatctcc aggacccccg aggtgacctg tgtcgtggtg 780
gacgtgagcc aagaggaccc cgaggtgcag ttcaactggt acgtggatgg cgtcgaggtc 840
cataacgcca agaccaagcc tagggaggag cagttcaaca gcacctacag agtggtgagc 900
gtcctgaccg tgctccacca agactggctg aacggcaagg aatacaagtg caaggtctcc 960
aacaagggac tcccttcctc catcgagaag accatcagca aggccaaggg ccagcccaga 1020
gaaccccaag tctacacact gccccccagc caagaggaaa tgaccaagaa ccaggtgagc 1080
ctgacctgcc tggtgaaagg cttctacccc agcgacattg ctgtcgaatg ggagagcaac 1140
ggccaacccg agaacaacta caagaccacc ccccctgtgc tcgacagcga cggctccttc 1200
ttcctctaca gcaggctgac agtggacaag tccaggtggc aagagggcaa tgtcttcagc 1260
tgtagcgtca tgcacgaggc cctccacaac cactacaccc agaagagcct gtccctctcc 1320
ctgggctga 1329
<210> 54
<211> 442
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность тяжелой цепи химерного антитела 8H4-IgG4 (F234A/L235A)
<400> 54
Glu Val Lys Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Arg Ser Tyr
20 25 30
Gly Met Ser Trp Ala Arg Gln Ile Pro Glu Lys Arg Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Ser Gly Gly Thr Thr Tyr Tyr Leu Gly Ser Val Gln
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Arg Asn Ile Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Tyr Cys Ala
85 90 95
Arg Gly Tyr Asp Ala Gly Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Ser Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro
210 215 220
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
225 230 235 240
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
245 250 255
Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn
260 265 270
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
275 280 285
Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
290 295 300
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
305 310 315 320
Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys
325 330 335
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu
340 345 350
Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
355 360 365
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
370 375 380
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
385 390 395 400
Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly
405 410 415
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
420 425 430
Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440
<210> 55
<211> 657
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность легкой цепи химерного антитела 8H4
<400> 55
gacattgtgc tgacacagtc tcctgcttcc ttagctgtat ctctggggca gagggccacc 60
atctcatgca gggccagcca aagtgtcagt acatctagct atagttatat gcactggtac 120
caacagaaac caggacagcc tcccaaactc ctcatcaagt atgcatccaa cctagaatct 180
ggggtccctg ccaggttcag tggcagtggg tctgggacag acttcaccct caacatccat 240
cctgtggagg aggaggatac tgcaacatat tactgtcaga acagttggga gattccgtac 300
acgttcggag gggggaccaa gctggaaata aaacgtacgg tggccgcacc aagcgtcttc 360
atcttcccgc catctgatga gcagttgaaa tctggaactg cctctgttgt gtgcctgctg 420
aataacttct atcccagaga ggccaaagta cagtggaagg tggataacgc cctccaatcg 480
ggtaactccc aggagagtgt cacagagcag gacagcaagg acagcaccta cagcctcagc 540
agcaccctga cgctgagcaa agcagactac gagaaacaca aagtctacgc ctgcgaagtc 600
acccatcagg gcctgagctc gcccgtcaca aagagcttta acagaggcga gtgctga 657
<210> 56
<211> 218
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность легкой цепи химерного антитела 8H4
<400> 56
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Arg Ala Ser Gln Ser Val Ser Thr Ser
20 25 30
Ser Tyr Ser Tyr Met His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Lys Tyr Ala Ser Asn Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Asn Ile His
65 70 75 80
Pro Val Glu Glu Glu Asp Thr Ala Thr Tyr Tyr Cys Gln Asn Ser Trp
85 90 95
Glu Ile Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 57
<211> 1341
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность тяжелой цепи химерного антитела 5G11-IgG1 (D265A)
<400> 57
caggtgcagc tgaagcagtc aggacctggc ctagtgcagc cctcacagag cctgtccatc 60
acctgcacag tctctggttt ctcattaact acctatggtg tacactgggt tcgccagtct 120
ccaggaaagg gtctggaatg gctgggagtg atatggcgtg gtgtaaccac agactataat 180
gcagctttca tgtccagact gaccatcacc aaggacaatt ccaagagcca agttttcttt 240
aaaatgaaca gtctgcaagc taatgacaca gccatatatt actgtgccag actgggtttc 300
tatgctatgg actactgggg tcaaggaacc tcagtcaccg tctcgagcgc ctccactaag 360
ggcccatccg tgttccctct ggcaccctcc agcaagagca caagcggagg caccgccgca 420
ctgggctgcc tcgtgaagga ctacttccca gaacccgtga ccgtcagctg gaatagcggc 480
gctctgacca gcggagtcca cactttcccc gcagtgctgc agtccagcgg cctgtacagc 540
ctgagcagcg tggtcactgt gccaagcagc agcctgggca ctcagaccta catctgcaac 600
gtcaaccaca agcccagcaa cacaaaggtg gacaagaagg tcgagcccaa gtcctgcgat 660
aagacccaca cctgccctcc atgtcccgcc cccgagctgc tgggaggacc cagcgtcttc 720
ctgtttcccc ccaagccaaa ggacaccctg atgatcagca ggacccccga agtgacctgc 780
gtcgtggtgg ccgtgagcca cgaagatccc gaggtgaagt tcaactggta cgtggacggc 840
gtggaagtgc acaacgccaa gacaaaaccc agggaggagc agtatgccag cacctacagg 900
gtcgtgagcg tcctgaccgt gctgcaccaa gactggctga acggcaagga gtataagtgc 960
aaggtgagca acaaggcact gcccgccccc atcgagaaga ccatttccaa ggccaagggg 1020
caacctaggg agccacaggt ctacactctg ccccctagca gggacgagct gaccaagaac 1080
caggtctccc tgacttgcct ggtgaagggg ttttatccca gcgacatcgc cgtcgagtgg 1140
gagagcaatg gccagcccga aaacaactac aagaccacac cccctgtgct ggacagcgac 1200
ggcagcttct ttctgtatag caaactgaca gtggataaga gcagatggca gcagggcaac 1260
gtgttctcct gctccgtgat gcacgaggcc ctgcacaatc actacaccca gaagtccctg 1320
agcctgtccc ccggaaaatg a 1341
<210> 58
<211> 446
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность тяжелой цепи химерного антитела 5G11-IgG1 (D265A)
<400> 58
Gln Val Gln Leu Lys Gln Ser Gly Pro Gly Leu Val Gln Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Thr Tyr
20 25 30
Gly Val His Trp Val Arg Gln Ser Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Arg Gly Val Thr Thr Asp Tyr Asn Ala Ala Phe Met
50 55 60
Ser Arg Leu Thr Ile Thr Lys Asp Asn Ser Lys Ser Gln Val Phe Phe
65 70 75 80
Lys Met Asn Ser Leu Gln Ala Asn Asp Thr Ala Ile Tyr Tyr Cys Ala
85 90 95
Arg Leu Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Ala Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 59
<211> 1329
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность тяжелой цепи химерного антитела 5G11-IgG4 (F234A/L235A)
<400> 59
caggtgcagc tgaagcagtc aggacctggc ctagtgcagc cctcacagag cctgtccatc 60
acctgcacag tctctggttt ctcattaact acctatggtg tacactgggt tcgccagtct 120
ccaggaaagg gtctggaatg gctgggagtg atatggcgtg gtgtaaccac agactataat 180
gcagctttca tgtccagact gaccatcacc aaggacaatt ccaagagcca agttttcttt 240
aaaatgaaca gtctgcaagc taatgacaca gccatatatt actgtgccag actgggtttc 300
tatgctatgg actactgggg tcaaggaacc tcagtcaccg tctcgagcgc ctccaccaag 360
ggacccagcg tgtttcccct ggccccctgt tccagatcca cctccgaaag cacagccgct 420
ctcggctgcc tggtcaagga ttacttccct gagcccgtga cagtctcctg gaatagcggc 480
gctctgacct ccggcgtgca taccttccct gctgtgctgc aatcctccgg actgtacagc 540
ctgagcagcg tggtcaccgt gccttcctcc agcctgggaa ccaaaaccta cacatgcaac 600
gtggaccaca agcccagcaa caccaaagtg gacaagaggg tggagtccaa gtacggaccc 660
ccttgtcctc cctgccctgc tcctgaagcc gctggaggac ctagcgtgtt cctgtttccc 720
cccaagccca aggacaccct catgatctcc aggacccccg aggtgacctg tgtcgtggtg 780
gacgtgagcc aagaggaccc cgaggtgcag ttcaactggt acgtggatgg cgtcgaggtc 840
cataacgcca agaccaagcc tagggaggag cagttcaaca gcacctacag agtggtgagc 900
gtcctgaccg tgctccacca agactggctg aacggcaagg aatacaagtg caaggtctcc 960
aacaagggac tcccttcctc catcgagaag accatcagca aggccaaggg ccagcccaga 1020
gaaccccaag tctacacact gccccccagc caagaggaaa tgaccaagaa ccaggtgagc 1080
ctgacctgcc tggtgaaagg cttctacccc agcgacattg ctgtcgaatg ggagagcaac 1140
ggccaacccg agaacaacta caagaccacc ccccctgtgc tcgacagcga cggctccttc 1200
ttcctctaca gcaggctgac agtggacaag tccaggtggc aagagggcaa tgtcttcagc 1260
tgtagcgtca tgcacgaggc cctccacaac cactacaccc agaagagcct gtccctctcc 1320
ctgggctga 1329
<210> 60
<211> 442
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность тяжелой цепи химерного антитела 5G11-IgG4 (F234A/L235A)
<400> 60
Gln Val Gln Leu Lys Gln Ser Gly Pro Gly Leu Val Gln Pro Ser Gln
1 5 10 15
Ser Leu Ser Ile Thr Cys Thr Val Ser Gly Phe Ser Leu Thr Thr Tyr
20 25 30
Gly Val His Trp Val Arg Gln Ser Pro Gly Lys Gly Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Arg Gly Val Thr Thr Asp Tyr Asn Ala Ala Phe Met
50 55 60
Ser Arg Leu Thr Ile Thr Lys Asp Asn Ser Lys Ser Gln Val Phe Phe
65 70 75 80
Lys Met Asn Ser Leu Gln Ala Asn Asp Thr Ala Ile Tyr Tyr Cys Ala
85 90 95
Arg Leu Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Ser Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro
210 215 220
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
225 230 235 240
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
245 250 255
Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn
260 265 270
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
275 280 285
Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
290 295 300
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
305 310 315 320
Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys
325 330 335
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu
340 345 350
Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
355 360 365
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
370 375 380
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
385 390 395 400
Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly
405 410 415
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
420 425 430
Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440
<210> 61
<211> 645
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность легкой цепи химерного антитела 5G11
<400> 61
agtattgtga tgacccagac tcccaaattc ctgcttgtat cagcaggaga cagggttacc 60
ataacctgca aggccagtca gagtgtgagt aatgatgtag cttggtacca gcagaagcca 120
gggcagtctc ctaaactgct gatatattat gcagccaatc gctacactgg agtccctgat 180
cgcttcactg gcagtggata tgggacggat ttcactttca ccatcagcat tgtgcaggct 240
gaagacctgg cagtttattt ctgtcagcag gattatacct ctccgtacac gttcggaggg 300
gggaccaagc tggaaataaa acgtacggtg gccgcaccaa gcgtcttcat cttcccgcca 360
tctgatgagc agttgaaatc tggaactgcc tctgttgtgt gcctgctgaa taacttctat 420
cccagagagg ccaaagtaca gtggaaggtg gataacgccc tccaatcggg taactcccag 480
gagagtgtca cagagcagga cagcaaggac agcacctaca gcctcagcag caccctgacg 540
ctgagcaaag cagactacga gaaacacaaa gtctacgcct gcgaagtcac ccatcagggc 600
ctgagctcgc ccgtcacaaa gagctttaac agaggcgagt gctga 645
<210> 62
<211> 214
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность легкой цепи химерного антитела 5G11
<400> 62
Ser Ile Val Met Thr Gln Thr Pro Lys Phe Leu Leu Val Ser Ala Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Val Ser Asn Asp
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Ala Asn Arg Tyr Thr Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Phe Thr Ile Ser Ile Val Gln Ala
65 70 75 80
Glu Asp Leu Ala Val Tyr Phe Cys Gln Gln Asp Tyr Thr Ser Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 63
<211> 1341
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность тяжелой цепи химерного антитела 13C5-IgG1 (D265A)
<400> 63
gaagtgaagc tggtggagtc tgggggaggc ttagtgaagc ctggagggtc cctgaaactc 60
tcctgtgcag cctctggatt cattttcaga agctatggca tgtcttgggt tcgccagact 120
ccagagaaga ggctggagtg ggtcgcatcc attagtagtg gtggtagcac ctactatcca 180
gacagtgtga agggccgatt caccatctcc agagataatg ccaggaacat cttgtacctg 240
caaatgagca gtctgaggtc tgaggacacg gccatgtatg actgtgcaag aggctatgat 300
tcggggtttg cttattgggg ccaagggact ctggtcactg tctcgagcgc ctccactaag 360
ggcccatccg tgttccctct ggcaccctcc agcaagagca caagcggagg caccgccgca 420
ctgggctgcc tcgtgaagga ctacttccca gaacccgtga ccgtcagctg gaatagcggc 480
gctctgacca gcggagtcca cactttcccc gcagtgctgc agtccagcgg cctgtacagc 540
ctgagcagcg tggtcactgt gccaagcagc agcctgggca ctcagaccta catctgcaac 600
gtcaaccaca agcccagcaa cacaaaggtg gacaagaagg tcgagcccaa gtcctgcgat 660
aagacccaca cctgccctcc atgtcccgcc cccgagctgc tgggaggacc cagcgtcttc 720
ctgtttcccc ccaagccaaa ggacaccctg atgatcagca ggacccccga agtgacctgc 780
gtcgtggtgg ccgtgagcca cgaagatccc gaggtgaagt tcaactggta cgtggacggc 840
gtggaagtgc acaacgccaa gacaaaaccc agggaggagc agtatgccag cacctacagg 900
gtcgtgagcg tcctgaccgt gctgcaccaa gactggctga acggcaagga gtataagtgc 960
aaggtgagca acaaggcact gcccgccccc atcgagaaga ccatttccaa ggccaagggg 1020
caacctaggg agccacaggt ctacactctg ccccctagca gggacgagct gaccaagaac 1080
caggtctccc tgacttgcct ggtgaagggg ttttatccca gcgacatcgc cgtcgagtgg 1140
gagagcaatg gccagcccga aaacaactac aagaccacac cccctgtgct ggacagcgac 1200
ggcagcttct ttctgtatag caaactgaca gtggataaga gcagatggca gcagggcaac 1260
gtgttctcct gctccgtgat gcacgaggcc ctgcacaatc actacaccca gaagtccctg 1320
agcctgtccc ccggaaaatg a 1341
<210> 64
<211> 446
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность тяжелой цепи химерного антитела 13C5-IgG1 (D265A)
<400> 64
Glu Val Lys Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Ile Phe Arg Ser Tyr
20 25 30
Gly Met Ser Trp Val Arg Gln Thr Pro Glu Lys Arg Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Ser Gly Gly Ser Thr Tyr Tyr Pro Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Arg Asn Ile Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Asp Cys Ala
85 90 95
Arg Gly Tyr Asp Ser Gly Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Ala Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Ala Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 65
<211> 1329
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность тяжелой цепи химерного антитела 13C5-IgG4 (F234A/L235A)
<400> 65
gaagtgaagc tggtggagtc tgggggaggc ttagtgaagc ctggagggtc cctgaaactc 60
tcctgtgcag cctctggatt cattttcaga agctatggca tgtcttgggt tcgccagact 120
ccagagaaga ggctggagtg ggtcgcatcc attagtagtg gtggtagcac ctactatcca 180
gacagtgtga agggccgatt caccatctcc agagataatg ccaggaacat cttgtacctg 240
caaatgagca gtctgaggtc tgaggacacg gccatgtatg actgtgcaag aggctatgat 300
tcggggtttg cttattgggg ccaagggact ctggtcactg tctcgagcgc ctccaccaag 360
ggacccagcg tgtttcccct ggccccctgt tccagatcca cctccgaaag cacagccgct 420
ctcggctgcc tggtcaagga ttacttccct gagcccgtga cagtctcctg gaatagcggc 480
gctctgacct ccggcgtgca taccttccct gctgtgctgc aatcctccgg actgtacagc 540
ctgagcagcg tggtcaccgt gccttcctcc agcctgggaa ccaaaaccta cacatgcaac 600
gtggaccaca agcccagcaa caccaaagtg gacaagaggg tggagtccaa gtacggaccc 660
ccttgtcctc cctgccctgc tcctgaagcc gctggaggac ctagcgtgtt cctgtttccc 720
cccaagccca aggacaccct catgatctcc aggacccccg aggtgacctg tgtcgtggtg 780
gacgtgagcc aagaggaccc cgaggtgcag ttcaactggt acgtggatgg cgtcgaggtc 840
cataacgcca agaccaagcc tagggaggag cagttcaaca gcacctacag agtggtgagc 900
gtcctgaccg tgctccacca agactggctg aacggcaagg aatacaagtg caaggtctcc 960
aacaagggac tcccttcctc catcgagaag accatcagca aggccaaggg ccagcccaga 1020
gaaccccaag tctacacact gccccccagc caagaggaaa tgaccaagaa ccaggtgagc 1080
ctgacctgcc tggtgaaagg cttctacccc agcgacattg ctgtcgaatg ggagagcaac 1140
ggccaacccg agaacaacta caagaccacc ccccctgtgc tcgacagcga cggctccttc 1200
ttcctctaca gcaggctgac agtggacaag tccaggtggc aagagggcaa tgtcttcagc 1260
tgtagcgtca tgcacgaggc cctccacaac cactacaccc agaagagcct gtccctctcc 1320
ctgggctga 1329
<210> 66
<211> 442
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность тяжелой цепи химерного антитела 13C5-IgG4 (F234A/L235A)
<400> 66
Glu Val Lys Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Ile Phe Arg Ser Tyr
20 25 30
Gly Met Ser Trp Val Arg Gln Thr Pro Glu Lys Arg Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Ser Gly Gly Ser Thr Tyr Tyr Pro Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Arg Asn Ile Leu Tyr Leu
65 70 75 80
Gln Met Ser Ser Leu Arg Ser Glu Asp Thr Ala Met Tyr Asp Cys Ala
85 90 95
Arg Gly Tyr Asp Ser Gly Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro
210 215 220
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
225 230 235 240
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
245 250 255
Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn
260 265 270
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
275 280 285
Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
290 295 300
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
305 310 315 320
Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys
325 330 335
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu
340 345 350
Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
355 360 365
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
370 375 380
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
385 390 395 400
Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly
405 410 415
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
420 425 430
Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440
<210> 67
<211> 663
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность легкой цепи химерного антитела 13C5
<400> 67
gacattgtgc tgacacagtc tcctgcttcc ttagctgttt ctctggggca gagggccacc 60
atctcatgca gggccagcca aagtgtcagt acttctagct ctagttttat gcactggtac 120
caacagaaac caggacagcc acccaaactc ctcatcaagt atgcatccaa cctagaatct 180
ggggtccctg ccaggttcag tggcagtggg tctgggacag acttcaccct caacatccat 240
cctgtggagg aggaggatac tgcaacatat tactgtcagc acagttggga gattccgtac 300
acgttcggag gggggaccaa gctggaaata aaacgtacgc gtacggtggc cgcaccaagc 360
gtcttcatct tcccgccatc tgatgagcag ttgaaatctg gaactgcctc tgttgtgtgc 420
ctgctgaata acttctatcc cagagaggcc aaagtacagt ggaaggtgga taacgccctc 480
caatcgggta actcccagga gagtgtcaca gagcaggaca gcaaggacag cacctacagc 540
ctcagcagca ccctgacgct gagcaaagca gactacgaga aacacaaagt ctacgcctgc 600
gaagtcaccc atcagggcct gagctcgccc gtcacaaaga gctttaacag aggcgagtgc 660
tga 663
<210> 68
<211> 220
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность легкой цепи химерного антитела 13C5
<400> 68
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Arg Ala Ser Gln Ser Val Ser Thr Ser
20 25 30
Ser Ser Ser Phe Met His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Lys Tyr Ala Ser Asn Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Asn Ile His
65 70 75 80
Pro Val Glu Glu Glu Asp Thr Ala Thr Tyr Tyr Cys Gln His Ser Trp
85 90 95
Glu Ile Pro Tyr Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp
115 120 125
Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn
130 135 140
Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
145 150 155 160
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp
165 170 175
Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr
180 185 190
Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser
195 200 205
Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215 220
<210> 69
<211> 1341
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность тяжелой цепи гуманизированного антитела 5G11-IgG1 (D265A)
<400> 69
cagatcacac tgaaagaaag cggccctacc ctggtcaagc caactcagac cctgacactg 60
acttgcaccg tgtctgggtt ctctctgagt acatacggag tccactggat caggcagccc 120
cctggcaaag ctctggagtg gctgggagtg atttggcggg gcgtcaccac agactataac 180
gccgctttta tgtcaagact gacaatcact aaggataaca gcaaaaatca ggtggtcctg 240
accatgaaca atatggaccc cgtggatacc gcaacatact attgtgcccg gctggggttc 300
tacgccatgg actattgggg ccaggggact ctggtgaccg tctcgagcgc ctccactaag 360
ggcccatccg tgttccctct ggcaccctcc agcaagagca caagcggagg caccgccgca 420
ctgggctgcc tcgtgaagga ctacttccca gaacccgtga ccgtcagctg gaatagcggc 480
gctctgacca gcggagtcca cactttcccc gcagtgctgc agtccagcgg cctgtacagc 540
ctgagcagcg tggtcactgt gccaagcagc agcctgggca ctcagaccta catctgcaac 600
gtcaaccaca agcccagcaa cacaaaggtg gacaagaagg tcgagcccaa gtcctgcgat 660
aagacccaca cctgccctcc atgtcccgcc cccgagctgc tgggaggacc cagcgtcttc 720
ctgtttcccc ccaagccaaa ggacaccctg atgatcagca ggacccccga agtgacctgc 780
gtcgtggtgg ccgtgagcca cgaagatccc gaggtgaagt tcaactggta cgtggacggc 840
gtggaagtgc acaacgccaa gacaaaaccc agggaggagc agtataacag cacctacagg 900
gtcgtgagcg tcctgaccgt gctgcaccaa gactggctga acggcaagga gtataagtgc 960
aaggtgagca acaaggcact gcccgccccc atcgagaaga ccatttccaa ggccaagggg 1020
caacctaggg agccacaggt ctacactctg ccccctagca gggacgagct gaccaagaac 1080
caggtctccc tgacttgcct ggtgaagggg ttttatccca gcgacatcgc cgtcgagtgg 1140
gagagcaatg gccagcccga aaacaactac aagaccacac cccctgtgct ggacagcgac 1200
ggcagcttct ttctgtatag caaactgaca gtggataaga gcagatggca gcagggcaac 1260
gtgttctcct gctccgtgat gcacgaggcc ctgcacaatc actacaccca gaagtccctg 1320
agcctgtccc ccggaaaatg a 1341
<210> 70
<211> 446
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность тяжелой цепи гуманизированного антитела 5G11-IgG1 (D265A)
<400> 70
Gln Ile Thr Leu Lys Glu Ser Gly Pro Thr Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Thr Tyr
20 25 30
Gly Val His Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Arg Gly Val Thr Thr Asp Tyr Asn Ala Ala Phe Met
50 55 60
Ser Arg Leu Thr Ile Thr Lys Asp Asn Ser Lys Asn Gln Val Val Leu
65 70 75 80
Thr Met Asn Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Leu Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Ala Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 71
<211> 1329
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность тяжелой цепи гуманизированного антитела 5G11-IgG4 (F234A/L235A)
<400> 71
cagatcacac tgaaagaaag cggccctacc ctggtcaagc caactcagac cctgacactg 60
acttgcaccg tgtctgggtt ctctctgagt acatacggag tccactggat caggcagccc 120
cctggcaaag ctctggagtg gctgggagtg atttggcggg gcgtcaccac agactataac 180
gccgctttta tgtcaagact gacaatcact aaggataaca gcaaaaatca ggtggtcctg 240
accatgaaca atatggaccc cgtggatacc gcaacatact attgtgcccg gctggggttc 300
tacgccatgg actattgggg ccaggggact ctggtgaccg tctcgagcgc ctccaccaag 360
ggacccagcg tgtttcccct ggccccctgt tccagatcca cctccgaaag cacagccgct 420
ctcggctgcc tggtcaagga ttacttccct gagcccgtga cagtctcctg gaatagcggc 480
gctctgacct ccggcgtgca taccttccct gctgtgctgc aatcctccgg actgtacagc 540
ctgagcagcg tggtcaccgt gccttcctcc agcctgggaa ccaaaaccta cacatgcaac 600
gtggaccaca agcccagcaa caccaaagtg gacaagaggg tggagtccaa gtacggaccc 660
ccttgtcctc cctgccctgc tcctgaagcc gctggaggac ctagcgtgtt cctgtttccc 720
cccaagccca aggacaccct catgatctcc aggacccccg aggtgacctg tgtcgtggtg 780
gacgtgagcc aagaggaccc cgaggtgcag ttcaactggt acgtggatgg cgtcgaggtc 840
cataacgcca agaccaagcc tagggaggag cagttcaaca gcacctacag agtggtgagc 900
gtcctgaccg tgctccacca agactggctg aacggcaagg aatacaagtg caaggtctcc 960
aacaagggac tcccttcctc catcgagaag accatcagca aggccaaggg ccagcccaga 1020
gaaccccaag tctacacact gccccccagc caagaggaaa tgaccaagaa ccaggtgagc 1080
ctgacctgcc tggtgaaagg cttctacccc agcgacattg ctgtcgaatg ggagagcaac 1140
ggccaacccg agaacaacta caagaccacc ccccctgtgc tcgacagcga cggctccttc 1200
ttcctctaca gcaggctgac agtggacaag tccaggtggc aagagggcaa tgtcttcagc 1260
tgtagcgtca tgcacgaggc cctccacaac cactacaccc agaagagcct gtccctctcc 1320
ctgggctga 1329
<210> 72
<211> 442
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность тяжелой цепи гуманизированного антитела 5G11-IgG4 (F234A/L235A)
<400> 72
Gln Ile Thr Leu Lys Glu Ser Gly Pro Thr Leu Val Lys Pro Thr Gln
1 5 10 15
Thr Leu Thr Leu Thr Cys Thr Val Ser Gly Phe Ser Leu Ser Thr Tyr
20 25 30
Gly Val His Trp Ile Arg Gln Pro Pro Gly Lys Ala Leu Glu Trp Leu
35 40 45
Gly Val Ile Trp Arg Gly Val Thr Thr Asp Tyr Asn Ala Ala Phe Met
50 55 60
Ser Arg Leu Thr Ile Thr Lys Asp Asn Ser Lys Asn Gln Val Val Leu
65 70 75 80
Thr Met Asn Asn Met Asp Pro Val Asp Thr Ala Thr Tyr Tyr Cys Ala
85 90 95
Arg Leu Gly Phe Tyr Ala Met Asp Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro
210 215 220
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
225 230 235 240
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
245 250 255
Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn
260 265 270
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
275 280 285
Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
290 295 300
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
305 310 315 320
Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys
325 330 335
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu
340 345 350
Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
355 360 365
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
370 375 380
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
385 390 395 400
Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly
405 410 415
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
420 425 430
Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440
<210> 73
<211> 645
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность легкой цепи гуманизированного антитела 5G11
<400> 73
gatatccaga tgactcagtc tccaagcagc ctgtctgcat ctgtggggga cagggtcacc 60
atcacatgca aagcatctca gagtgtgtca aacgatgtcg cctggtacca gcagaagccc 120
ggaaaagctc ctaagctgct gatttactat gccgctaatc ggtacactgg cgtgccagac 180
agattcagcg gatccggata tggaaccgat ttcactttta ccatcagctc cctgcagcca 240
gaggacattg ccacatattt ctgtcagcag gattacacaa gcccctatac ttttggccag 300
gggaccaaac tggaaatcaa gcgtacggtg gccgcaccaa gcgtcttcat cttcccgcca 360
tctgatgagc agttgaaatc tggaactgcc tctgttgtgt gcctgctgaa taacttctat 420
cccagagagg ccaaagtaca gtggaaggtg gataacgccc tccaatcggg taactcccag 480
gagagtgtca cagagcagga cagcaaggac agcacctaca gcctcagcag caccctgacg 540
ctgagcaaag cagactacga gaaacacaaa gtctacgcct gcgaagtcac ccatcagggc 600
ctgagctcgc ccgtcacaaa gagctttaac agaggcgagt gctga 645
<210> 74
<211> 214
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность легкой цепи гуманизированного антитела 5G11
<400> 74
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Val Ser Asn Asp
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Ala Ala Asn Arg Tyr Thr Gly Val Pro Asp Arg Phe Ser Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Asp Tyr Thr Ser Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 75
<211> 1341
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность тяжелой цепи гуманизированного антитела 13C5-IgG1 (D265A)
<400> 75
gaggtgcagc tggtcgagtc aggagggggg ctggtcaagc caggagggtc actgcgactg 60
agctgcgcag cttccgggtt catctttagg tcttatggca tgagttgggt gcgccaggca 120
ccagggaaag gactggagtg ggtcgcttca atcagctccg gaggcagcac ttactatcct 180
gactccgtga agggccggtt caccatttct agagataacg ccaaaaatag tctgtacctg 240
cagatgaact ctctgcgagc agaagacaca gccgtctacg attgtgctag aggatatgac 300
agcggctttg catactgggg ccaggggacc ctggtgacag tctcgagcgc ctccactaag 360
ggcccatccg tgttccctct ggcaccctcc agcaagagca caagcggagg caccgccgca 420
ctgggctgcc tcgtgaagga ctacttccca gaacccgtga ccgtcagctg gaatagcggc 480
gctctgacca gcggagtcca cactttcccc gcagtgctgc agtccagcgg cctgtacagc 540
ctgagcagcg tggtcactgt gccaagcagc agcctgggca ctcagaccta catctgcaac 600
gtcaaccaca agcccagcaa cacaaaggtg gacaagaagg tcgagcccaa gtcctgcgat 660
aagacccaca cctgccctcc atgtcccgcc cccgagctgc tgggaggacc cagcgtcttc 720
ctgtttcccc ccaagccaaa ggacaccctg atgatcagca ggacccccga agtgacctgc 780
gtcgtggtgg ccgtgagcca cgaagatccc gaggtgaagt tcaactggta cgtggacggc 840
gtggaagtgc acaacgccaa gacaaaaccc agggaggagc agtataacag cacctacagg 900
gtcgtgagcg tcctgaccgt gctgcaccaa gactggctga acggcaagga gtataagtgc 960
aaggtgagca acaaggcact gcccgccccc atcgagaaga ccatttccaa ggccaagggg 1020
caacctaggg agccacaggt ctacactctg ccccctagca gggacgagct gaccaagaac 1080
caggtctccc tgacttgcct ggtgaagggg ttttatccca gcgacatcgc cgtcgagtgg 1140
gagagcaatg gccagcccga aaacaactac aagaccacac cccctgtgct ggacagcgac 1200
ggcagcttct ttctgtatag caaactgaca gtggataaga gcagatggca gcagggcaac 1260
gtgttctcct gctccgtgat gcacgaggcc ctgcacaatc actacaccca gaagtccctg 1320
agcctgtccc ccggaaaatg a 1341
<210> 76
<211> 446
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность тяжелой цепи гуманизированного антитела 13C5-IgG1 (D265A)
<400> 76
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ile Phe Arg Ser Tyr
20 25 30
Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Ser Gly Gly Ser Thr Tyr Tyr Pro Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Asp Cys Ala
85 90 95
Arg Gly Tyr Asp Ser Gly Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
210 215 220
Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe
225 230 235 240
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
245 250 255
Glu Val Thr Cys Val Val Val Ala Val Ser His Glu Asp Pro Glu Val
260 265 270
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
275 280 285
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
290 295 300
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
305 310 315 320
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
325 330 335
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
340 345 350
Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val
355 360 365
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
370 375 380
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
385 390 395 400
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
405 410 415
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
420 425 430
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
435 440 445
<210> 77
<211> 1329
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность тяжелой цепи гуманизированного антитела 13C5-IgG4 (F234A/L235A)
<400> 77
gaggtgcagc tggtcgagtc aggagggggg ctggtcaagc caggagggtc actgcgactg 60
agctgcgcag cttccgggtt catctttagg tcttatggca tgagttgggt gcgccaggca 120
ccagggaaag gactggagtg ggtcgcttca atcagctccg gaggcagcac ttactatcct 180
gactccgtga agggccggtt caccatttct agagataacg ccaaaaatag tctgtacctg 240
cagatgaact ctctgcgagc agaagacaca gccgtctacg attgtgctag aggatatgac 300
agcggctttg catactgggg ccaggggacc ctggtgacag tctcgagcgc ctccaccaag 360
ggacccagcg tgtttcccct ggccccctgt tccagatcca cctccgaaag cacagccgct 420
ctcggctgcc tggtcaagga ttacttccct gagcccgtga cagtctcctg gaatagcggc 480
gctctgacct ccggcgtgca taccttccct gctgtgctgc aatcctccgg actgtacagc 540
ctgagcagcg tggtcaccgt gccttcctcc agcctgggaa ccaaaaccta cacatgcaac 600
gtggaccaca agcccagcaa caccaaagtg gacaagaggg tggagtccaa gtacggaccc 660
ccttgtcctc cctgccctgc tcctgaagcc gctggaggac ctagcgtgtt cctgtttccc 720
cccaagccca aggacaccct catgatctcc aggacccccg aggtgacctg tgtcgtggtg 780
gacgtgagcc aagaggaccc cgaggtgcag ttcaactggt acgtggatgg cgtcgaggtc 840
cataacgcca agaccaagcc tagggaggag cagttcaaca gcacctacag agtggtgagc 900
gtcctgaccg tgctccacca agactggctg aacggcaagg aatacaagtg caaggtctcc 960
aacaagggac tcccttcctc catcgagaag accatcagca aggccaaggg ccagcccaga 1020
gaaccccaag tctacacact gccccccagc caagaggaaa tgaccaagaa ccaggtgagc 1080
ctgacctgcc tggtgaaagg cttctacccc agcgacattg ctgtcgaatg ggagagcaac 1140
ggccaacccg agaacaacta caagaccacc ccccctgtgc tcgacagcga cggctccttc 1200
ttcctctaca gcaggctgac agtggacaag tccaggtggc aagagggcaa tgtcttcagc 1260
tgtagcgtca tgcacgaggc cctccacaac cactacaccc agaagagcct gtccctctcc 1320
ctgggctga 1329
<210> 78
<211> 442
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность тяжелой цепи гуманизированного антитела 13C5-IgG4 (F234A/L235A)
<400> 78
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Ile Phe Arg Ser Tyr
20 25 30
Gly Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ser Ile Ser Ser Gly Gly Ser Thr Tyr Tyr Pro Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Asp Cys Ala
85 90 95
Arg Gly Tyr Asp Ser Gly Phe Ala Tyr Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
115 120 125
Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu
130 135 140
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
145 150 155 160
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
165 170 175
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
180 185 190
Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr
195 200 205
Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro
210 215 220
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
225 230 235 240
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
245 250 255
Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn
260 265 270
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
275 280 285
Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
290 295 300
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
305 310 315 320
Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys
325 330 335
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu
340 345 350
Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe
355 360 365
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
370 375 380
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
385 390 395 400
Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly
405 410 415
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
420 425 430
Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440
<210> 79
<211> 657
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность легкой цепи гуманизированного антитела 13C5
<400> 79
gacattgtgc tgactcagag ccccgcttca ctggcagtgt ctccagggca gcgggcaacc 60
atcacatgca gagcctcaca gagcgtctcc accagctcct ctagtttcat gcactggtac 120
cagcagaagc ccggacagcc ccctaagctg ctgatcaaat atgctagcaa cctggagtcc 180
ggcgtgccag ccaggttctc tggcagtggg tcaggaaccg actttactct gaccattaat 240
cccgtcgaag ccaacgatac agctaattac tattgtcagc attcctggga gatcccttac 300
acatttggcc aggggactaa gctggagatc aagcgtacgg tggccgcacc aagcgtcttc 360
atcttcccgc catctgatga gcagttgaaa tctggaactg cctctgttgt gtgcctgctg 420
aataacttct atcccagaga ggccaaagta cagtggaagg tggataacgc cctccaatcg 480
ggtaactccc aggagagtgt cacagagcag gacagcaagg acagcaccta cagcctcagc 540
agcaccctga cgctgagcaa agcagactac gagaaacaca aagtctacgc ctgcgaagtc 600
acccatcagg gcctgagctc gcccgtcaca aagagcttta acagaggcga gtgctga 657
<210> 80
<211> 218
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Полноразмерная последовательность легкой цепи гуманизированного антитела 13C5
<400> 80
Asp Ile Val Leu Thr Gln Ser Pro Ala Ser Leu Ala Val Ser Pro Gly
1 5 10 15
Gln Arg Ala Thr Ile Thr Cys Arg Ala Ser Gln Ser Val Ser Thr Ser
20 25 30
Ser Ser Ser Phe Met His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Lys Tyr Ala Ser Asn Leu Glu Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Asn
65 70 75 80
Pro Val Glu Ala Asn Asp Thr Ala Asn Tyr Tyr Cys Gln His Ser Trp
85 90 95
Glu Ile Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 81
<211> 5
<212> ПРТ
<213> Mus sp.
<400> 81
Ser Tyr Gly Met Ser
1 5
<210> 82
<211> 16
<212> ПРТ
<213> Mus sp.
<400> 82
Ser Ile Ser Ser Gly Gly Ser Thr Tyr Tyr Pro Asp Ser Val Lys Gly
1 5 10 15
<210> 83
<211> 8
<212> ПРТ
<213> Mus sp.
<400> 83
Gly Tyr Asp Ser Gly Phe Ala Tyr
1 5
<210> 84
<211> 15
<212> ПРТ
<213> Mus sp.
<400> 84
Arg Ala Ser Gln Ser Val Ser Thr Ser Ser Ser Ser Phe Met His
1 5 10 15
<210> 85
<211> 7
<212> ПРТ
<213> Mus sp.
<400> 85
Tyr Ala Ser Asn Leu Glu Ser
1 5
<210> 86
<211> 9
<212> ПРТ
<213> Mus sp.
<400> 86
Gln His Ser Trp Glu Ile Pro Tyr Thr
1 5
<210> 87
<211> 5
<212> ПРТ
<213> Mus sp.
<400> 87
Ser Tyr Gly Met Ser
1 5
<210> 88
<211> 16
<212> ПРТ
<213> Mus sp.
<400> 88
Ser Ile Ser Ser Gly Gly Thr Thr Tyr Tyr Pro Asp Ser Val Lys Gly
1 5 10 15
<210> 89
<211> 8
<212> ПРТ
<213> Mus sp.
<400> 89
Gly Tyr Asp Ser Gly Phe Ala Tyr
1 5
<210> 90
<211> 15
<212> ПРТ
<213> Mus sp.
<400> 90
Arg Ala Ser Gln Ser Val Ser Thr Ser Ser Ser Ser Tyr Met His
1 5 10 15
<210> 91
<211> 7
<212> ПРТ
<213> Mus sp.
<400> 91
Tyr Ala Ser Asn Leu Glu Ser
1 5
<210> 92
<211> 9
<212> ПРТ
<213> Mus sp.
<400> 92
Gln His Ser Trp Glu Ile Pro Tyr Thr
1 5
<210> 93
<211> 5
<212> ПРТ
<213> Mus sp.
<400> 93
Thr Tyr Gly Val His
1 5
<210> 94
<211> 16
<212> ПРТ
<213> Mus sp.
<400> 94
Val Ile Trp Arg Gly Val Thr Thr Asp Tyr Asn Ala Ala Phe Met Ser
1 5 10 15
<210> 95
<211> 8
<212> ПРТ
<213> Mus sp.
<400> 95
Leu Gly Phe Tyr Ala Met Asp Tyr
1 5
<210> 96
<211> 11
<212> ПРТ
<213> Mus sp.
<400> 96
Lys Ala Ser Gln Ser Val Ser Asn Asp Val Ala
1 5 10
<210> 97
<211> 7
<212> ПРТ
<213> Mus sp.
<400> 97
Tyr Ala Ala Asn Arg Tyr Thr
1 5
<210> 98
<211> 9
<212> ПРТ
<213> Mus sp.
<400> 98
Gln Gln Asp Tyr Thr Ser Pro Tyr Thr
1 5
<210> 99
<211> 5
<212> ПРТ
<213> Mus sp.
<400> 99
Ser Tyr Gly Val His
1 5
<210> 100
<211> 16
<212> ПРТ
<213> Mus sp.
<400> 100
Val Ile Trp Ser Gly Gly Val Thr Asp Tyr Asn Ala Ala Phe Ile Ser
1 5 10 15
<210> 101
<211> 8
<212> ПРТ
<213> Mus sp.
<400> 101
Leu Gly Phe Tyr Ala Met Asp Tyr
1 5
<210> 102
<211> 11
<212> ПРТ
<213> Mus sp.
<400> 102
Lys Ala Ser Gln Ser Val Ser Asn Asp Val Gly
1 5 10
<210> 103
<211> 7
<212> ПРТ
<213> Mus sp.
<400> 103
Tyr Ala Ser Asn Arg Tyr Ser
1 5
<210> 104
<211> 9
<212> ПРТ
<213> Mus sp.
<400> 104
Gln Gln Asp Tyr Thr Ser Pro Tyr Thr
1 5
<210> 105
<211> 5
<212> ПРТ
<213> Mus sp.
<400> 105
Thr Tyr Trp Met His
1 5
<210> 106
<211> 17
<212> ПРТ
<213> Mus sp.
<400> 106
Gln Ile Asn Pro Asp Ser Thr Thr Ile Asn Tyr Ala Pro Ser Leu Lys
1 5 10 15
Asp
<210> 107
<211> 10
<212> ПРТ
<213> Mus sp.
<400> 107
Pro Gly Asp Tyr Gly Tyr Asp Phe Asp Cys
1 5 10
<210> 108
<211> 16
<212> ПРТ
<213> Mus sp.
<400> 108
Arg Ser Ser Gln Ile Ile Val His Ser Asn Ala Asn Thr Tyr Leu Glu
1 5 10 15
<210> 109
<211> 7
<212> ПРТ
<213> Mus sp.
<400> 109
Lys Val Ser Asn Arg Phe Ser
1 5
<210> 110
<211> 9
<212> ПРТ
<213> Mus sp.
<400> 110
Phe Gln Gly Ser His Val Pro Tyr Thr
1 5
<210> 111
<211> 5
<212> ПРТ
<213> Mus sp.
<400> 111
Ser Gly Tyr Trp Asn
1 5
<210> 112
<211> 16
<212> ПРТ
<213> Mus sp.
<400> 112
Tyr Ile Ser Tyr Ser Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 113
<211> 11
<212> ПРТ
<213> Mus sp.
<400> 113
Ser Leu Leu Trp Phe Ser Thr Gly Phe Ala Tyr
1 5 10
<210> 114
<211> 12
<212> ПРТ
<213> Mus sp.
<400> 114
Ser Ala Ser Ser Ser Val Ser Ser Ser Tyr Leu Tyr
1 5 10
<210> 115
<211> 7
<212> ПРТ
<213> Mus sp.
<400> 115
Asn Thr Ser Asn Leu Ala Ser
1 5
<210> 116
<211> 9
<212> ПРТ
<213> Mus sp.
<400> 116
His Gln Trp Arg Ser Tyr Pro Pro Thr
1 5
<210> 117
<211> 5
<212> ПРТ
<213> Mus sp.
<400> 117
Ser Tyr Gly Val His
1 5
<210> 118
<211> 16
<212> ПРТ
<213> Mus sp.
<400> 118
Val Ile Trp Ser Gly Gly Ile Thr Asp Tyr Asn Ala Ala Phe Lys Ser
1 5 10 15
<210> 119
<211> 8
<212> ПРТ
<213> Mus sp.
<400> 119
Leu Gly Phe Tyr Ala Met Asp Tyr
1 5
<210> 120
<211> 10
<212> ПРТ
<213> Mus sp.
<400> 120
Ser Ala Asn Ser Ser Val Ser Tyr Met His
1 5 10
<210> 121
<211> 7
<212> ПРТ
<213> Mus sp.
<400> 121
Asp Thr Ser Lys Leu Ala Ser
1 5
<210> 122
<211> 9
<212> ПРТ
<213> Mus sp.
<400> 122
Gln Gln Trp Ser Ser Asn Pro Trp Thr
1 5
<210> 123
<211> 5
<212> ПРТ
<213> Mus sp.
<400> 123
Ser Tyr Gly Met Ser
1 5
<210> 124
<211> 16
<212> ПРТ
<213> Mus sp.
<400> 124
Ser Ile Ser Ser Gly Gly Thr Thr Tyr Tyr Leu Gly Ser Val Gln Gly
1 5 10 15
<210> 125
<211> 8
<212> ПРТ
<213> Mus sp.
<400> 125
Gly Tyr Asp Ala Gly Phe Ala Tyr
1 5
<210> 126
<211> 15
<212> ПРТ
<213> Mus sp.
<400> 126
Arg Ala Ser Gln Ser Val Ser Thr Ser Ser Tyr Ser Tyr Met His
1 5 10 15
<210> 127
<211> 7
<212> ПРТ
<213> Mus sp.
<400> 127
Tyr Ala Ser Asn Leu Glu Ser
1 5
<210> 128
<211> 9
<212> ПРТ
<213> Mus sp.
<400> 128
Gln Asn Ser Trp Glu Ile Pro Tyr Thr
1 5
<210> 129
<211> 5
<212> ПРТ
<213> Mus sp.
<400> 129
Ser Gly Tyr Trp Thr
1 5
<210> 130
<211> 16
<212> ПРТ
<213> Mus sp.
<400> 130
Tyr Ile Ser Tyr Thr Gly Ser Thr Tyr Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 131
<211> 9
<212> ПРТ
<213> Mus sp.
<400> 131
Gln Arg Asp Trp Leu Gly Phe Ala Tyr
1 5
<210> 132
<211> 17
<212> ПРТ
<213> Mus sp.
<400> 132
Lys Ser Ser Gln Ser Leu Leu Tyr Ser Ser Asn Gln Lys Asn Ser Leu
1 5 10 15
Ala
<210> 133
<211> 7
<212> ПРТ
<213> Mus sp.
<400> 133
Trp Ala Ser Asn Arg Glu Ser
1 5
<210> 134
<211> 9
<212> ПРТ
<213> Mus sp.
<400> 134
Gln Gln Tyr Tyr Ser Tyr Pro Leu Thr
1 5
<210> 135
<211> 5
<212> ПРТ
<213> Mus sp.
<400> 135
Ser Tyr Gly Met Ser
1 5
<210> 136
<211> 16
<212> ПРТ
<213> Mus sp.
<400> 136
Ser Ile Ser Ser Gly Gly Ser Ile Tyr Tyr Pro Asp Ser Val Lys Gly
1 5 10 15
<210> 137
<211> 8
<212> ПРТ
<213> Mus sp.
<400> 137
Gly Tyr Asp Ala Gly Phe Ala Phe
1 5
<210> 138
<211> 15
<212> ПРТ
<213> Mus sp.
<400> 138
Arg Ala Ser Gln Ser Val Ser Thr Ser Ser Tyr Ser Tyr Val His
1 5 10 15
<210> 139
<211> 7
<212> ПРТ
<213> Mus sp.
<400> 139
Tyr Ala Ser Asn Leu Glu Ser
1 5
<210> 140
<211> 9
<212> ПРТ
<213> Mus sp.
<400> 140
Gln His Ser Trp Glu Ile Pro Tyr Thr
1 5
<210> 141
<211> 660
<212> ДНК
<213> Homo sapiens
<400> 141
tttactgtca cggttcccaa ggacctatat gtggtagagt atggtagcaa tatgacaatt 60
gaatgcaaat tcccagtaga aaaacaatta gacctggctg cactaattgt ctattgggaa 120
atggaggata agaacattat tcaatttgtg catggagagg aagacctgaa ggttcagcat 180
agtagctaca gacagagggc ccggctgttg aaggaccagc tctccctggg aaatgctgca 240
cttcagatca cagatgtgaa attgcaggat gcaggggtgt accgctgcat gatcagctat 300
ggtggtgccg actacaagcg aattactgtg aaagtcaatg ccccatacaa caaaatcaac 360
caaagaattt tggttgtgga tccagtcacc tctgaacatg aactgacatg tcaggctgag 420
ggctacccca aggccgaagt catctggaca agcagtgacc atcaagtcct gagtggtaag 480
accaccacca ccaattccaa gagagaggag aagcttttca atgtgaccag cacactgaga 540
atcaacacaa caactaatga gattttctac tgcactttta ggagattaga tcctgaggaa 600
aaccatacag ctgaattggt catcccagaa ctacctctgg cacatcctcc aaatgaaagg 660
<210> 142
<211> 220
<212> ПРТ
<213> Homo sapiens
<400> 142
Phe Thr Val Thr Val Pro Lys Asp Leu Tyr Val Val Glu Tyr Gly Ser
1 5 10 15
Asn Met Thr Ile Glu Cys Lys Phe Pro Val Glu Lys Gln Leu Asp Leu
20 25 30
Ala Ala Leu Ile Val Tyr Trp Glu Met Glu Asp Lys Asn Ile Ile Gln
35 40 45
Phe Val His Gly Glu Glu Asp Leu Lys Val Gln His Ser Ser Tyr Arg
50 55 60
Gln Arg Ala Arg Leu Leu Lys Asp Gln Leu Ser Leu Gly Asn Ala Ala
65 70 75 80
Leu Gln Ile Thr Asp Val Lys Leu Gln Asp Ala Gly Val Tyr Arg Cys
85 90 95
Met Ile Ser Tyr Gly Gly Ala Asp Tyr Lys Arg Ile Thr Val Lys Val
100 105 110
Asn Ala Pro Tyr Asn Lys Ile Asn Gln Arg Ile Leu Val Val Asp Pro
115 120 125
Val Thr Ser Glu His Glu Leu Thr Cys Gln Ala Glu Gly Tyr Pro Lys
130 135 140
Ala Glu Val Ile Trp Thr Ser Ser Asp His Gln Val Leu Ser Gly Lys
145 150 155 160
Thr Thr Thr Thr Asn Ser Lys Arg Glu Glu Lys Leu Phe Asn Val Thr
165 170 175
Ser Thr Leu Arg Ile Asn Thr Thr Thr Asn Glu Ile Phe Tyr Cys Thr
180 185 190
Phe Arg Arg Leu Asp Pro Glu Glu Asn His Thr Ala Glu Leu Val Ile
195 200 205
Pro Glu Leu Pro Leu Ala His Pro Pro Asn Glu Arg
210 215 220
<210> 143
<211> 681
<212> ДНК
<213> Homo sapiens
<400> 143
tttactgtca cggttcccaa ggacctatat gtggtagagt atggtagcaa tatgacaatt 60
gaatgcaaat tcccagtaga aaaacaatta gacctggctg cactaattgt ctattgggaa 120
atggaggata agaacattat tcaatttgtg catggagagg aagacctgaa ggttcagcat 180
agtagctaca gacagagggc ccggctgttg aaggaccagc tctccctggg aaatgctgca 240
cttcagatca cagatgtgaa attgcaggat gcaggggtgt accgctgcat gatcagctat 300
ggtggtgccg actacaagcg aattactgtg aaagtcaatg ccccatacaa caaaatcaac 360
caaagaattt tggttgtgga tccagtcacc tctgaacatg aactgacatg tcaggctgag 420
ggctacccca aggccgaagt catctggaca agcagtgacc atcaagtcct gagtggtaag 480
accaccacca ccaattccaa gagagaggag aagcttttca atgtgaccag cacactgaga 540
atcaacacaa caactaatga gattttctac tgcactttta ggagattaga tcctgaggaa 600
aaccatacag ctgaattggt catcccagaa ctacctctgg cacatcctcc aaatgaaagg 660
catcatcacc accatcacta a 681
<210> 144
<211> 226
<212> ПРТ
<213> Homo sapiens
<400> 144
Phe Thr Val Thr Val Pro Lys Asp Leu Tyr Val Val Glu Tyr Gly Ser
1 5 10 15
Asn Met Thr Ile Glu Cys Lys Phe Pro Val Glu Lys Gln Leu Asp Leu
20 25 30
Ala Ala Leu Ile Val Tyr Trp Glu Met Glu Asp Lys Asn Ile Ile Gln
35 40 45
Phe Val His Gly Glu Glu Asp Leu Lys Val Gln His Ser Ser Tyr Arg
50 55 60
Gln Arg Ala Arg Leu Leu Lys Asp Gln Leu Ser Leu Gly Asn Ala Ala
65 70 75 80
Leu Gln Ile Thr Asp Val Lys Leu Gln Asp Ala Gly Val Tyr Arg Cys
85 90 95
Met Ile Ser Tyr Gly Gly Ala Asp Tyr Lys Arg Ile Thr Val Lys Val
100 105 110
Asn Ala Pro Tyr Asn Lys Ile Asn Gln Arg Ile Leu Val Val Asp Pro
115 120 125
Val Thr Ser Glu His Glu Leu Thr Cys Gln Ala Glu Gly Tyr Pro Lys
130 135 140
Ala Glu Val Ile Trp Thr Ser Ser Asp His Gln Val Leu Ser Gly Lys
145 150 155 160
Thr Thr Thr Thr Asn Ser Lys Arg Glu Glu Lys Leu Phe Asn Val Thr
165 170 175
Ser Thr Leu Arg Ile Asn Thr Thr Thr Asn Glu Ile Phe Tyr Cys Thr
180 185 190
Phe Arg Arg Leu Asp Pro Glu Glu Asn His Thr Ala Glu Leu Val Ile
195 200 205
Pro Glu Leu Pro Leu Ala His Pro Pro Asn Glu Arg His His His His
210 215 220
His His
225
<210> 145
<211> 1344
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность PD-L1-mFc человека
<400> 145
tttactgtca cggttcccaa ggacctatat gtggtagagt atggtagcaa tatgacaatt 60
gaatgcaaat tcccagtaga aaaacaatta gacctggctg cactaattgt ctattgggaa 120
atggaggata agaacattat tcaatttgtg catggagagg aagacctgaa ggttcagcat 180
agtagctaca gacagagggc ccggctgttg aaggaccagc tctccctggg aaatgctgca 240
cttcagatca cagatgtgaa attgcaggat gcaggggtgt accgctgcat gatcagctat 300
ggtggtgccg actacaagcg aattactgtg aaagtcaatg ccccatacaa caaaatcaac 360
caaagaattt tggttgtgga tccagtcacc tctgaacatg aactgacatg tcaggctgag 420
ggctacccca aggccgaagt catctggaca agcagtgacc atcaagtcct gagtggtaag 480
accaccacca ccaattccaa gagagaggag aagcttttca atgtgaccag cacactgaga 540
atcaacacaa caactaatga gattttctac tgcactttta ggagattaga tcctgaggaa 600
aaccatacag ctgaattggt catcccagaa ctacctctgg cacatcctcc aaatgaaagg 660
ggtaccagat ctagaggctg caaaccctgt atctgcacag tgcccgaggt gagctccgtg 720
ttcatctttc cccccaagcc caaggacgtg ctgaccatca cactcacacc caaggtcacc 780
tgcgtggtcg tggacatctc caaggacgac cccgaagtcc agttcagctg gttcgtggac 840
gacgtggagg tgcacaccgc tcagacccaa cccagagagg agcagtttaa ctccaccttc 900
aggtccgtgt ccgagctccc catcatgcac caggactggc tgaatggcaa ggagttcaag 960
tgcagggtga actccgctgc tttccccgcc cccattgaga agaccatctc caagaccaag 1020
ggaaggccca aggcccccca ggtgtacacc attccccctc ccaaggagca gatggccaag 1080
gacaaggtgt ccctgacctg tatgatcacc gacttctttc ccgaggacat caccgtcgaa 1140
tggcagtgga acggccagcc cgccgagaac tataagaaca cccaacccat catggacacc 1200
gacggcagct acttcgtgta tagcaagctc aacgtgcaga agagcaactg ggaagccgga 1260
aataccttca cctgctccgt cctgcacgag ggcctgcaca accaccatac cgaaaagagc 1320
ctgagccaca gccccggaaa gtaa 1344
<210> 146
<211> 447
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Последовательность PD-L1-mFc человека
<400> 146
Phe Thr Val Thr Val Pro Lys Asp Leu Tyr Val Val Glu Tyr Gly Ser
1 5 10 15
Asn Met Thr Ile Glu Cys Lys Phe Pro Val Glu Lys Gln Leu Asp Leu
20 25 30
Ala Ala Leu Ile Val Tyr Trp Glu Met Glu Asp Lys Asn Ile Ile Gln
35 40 45
Phe Val His Gly Glu Glu Asp Leu Lys Val Gln His Ser Ser Tyr Arg
50 55 60
Gln Arg Ala Arg Leu Leu Lys Asp Gln Leu Ser Leu Gly Asn Ala Ala
65 70 75 80
Leu Gln Ile Thr Asp Val Lys Leu Gln Asp Ala Gly Val Tyr Arg Cys
85 90 95
Met Ile Ser Tyr Gly Gly Ala Asp Tyr Lys Arg Ile Thr Val Lys Val
100 105 110
Asn Ala Pro Tyr Asn Lys Ile Asn Gln Arg Ile Leu Val Val Asp Pro
115 120 125
Val Thr Ser Glu His Glu Leu Thr Cys Gln Ala Glu Gly Tyr Pro Lys
130 135 140
Ala Glu Val Ile Trp Thr Ser Ser Asp His Gln Val Leu Ser Gly Lys
145 150 155 160
Thr Thr Thr Thr Asn Ser Lys Arg Glu Glu Lys Leu Phe Asn Val Thr
165 170 175
Ser Thr Leu Arg Ile Asn Thr Thr Thr Asn Glu Ile Phe Tyr Cys Thr
180 185 190
Phe Arg Arg Leu Asp Pro Glu Glu Asn His Thr Ala Glu Leu Val Ile
195 200 205
Pro Glu Leu Pro Leu Ala His Pro Pro Asn Glu Arg Gly Thr Arg Ser
210 215 220
Arg Gly Cys Lys Pro Cys Ile Cys Thr Val Pro Glu Val Ser Ser Val
225 230 235 240
Phe Ile Phe Pro Pro Lys Pro Lys Asp Val Leu Thr Ile Thr Leu Thr
245 250 255
Pro Lys Val Thr Cys Val Val Val Asp Ile Ser Lys Asp Asp Pro Glu
260 265 270
Val Gln Phe Ser Trp Phe Val Asp Asp Val Glu Val His Thr Ala Gln
275 280 285
Thr Gln Pro Arg Glu Glu Gln Phe Asn Ser Thr Phe Arg Ser Val Ser
290 295 300
Glu Leu Pro Ile Met His Gln Asp Trp Leu Asn Gly Lys Glu Phe Lys
305 310 315 320
Cys Arg Val Asn Ser Ala Ala Phe Pro Ala Pro Ile Glu Lys Thr Ile
325 330 335
Ser Lys Thr Lys Gly Arg Pro Lys Ala Pro Gln Val Tyr Thr Ile Pro
340 345 350
Pro Pro Lys Glu Gln Met Ala Lys Asp Lys Val Ser Leu Thr Cys Met
355 360 365
Ile Thr Asp Phe Phe Pro Glu Asp Ile Thr Val Glu Trp Gln Trp Asn
370 375 380
Gly Gln Pro Ala Glu Asn Tyr Lys Asn Thr Gln Pro Ile Met Asp Thr
385 390 395 400
Asp Gly Ser Tyr Phe Val Tyr Ser Lys Leu Asn Val Gln Lys Ser Asn
405 410 415
Trp Glu Ala Gly Asn Thr Phe Thr Cys Ser Val Leu His Glu Gly Leu
420 425 430
His Asn His His Thr Glu Lys Ser Leu Ser His Ser Pro Gly Lys
435 440 445
<210> 147
<211> 1374
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность PD-L1-hFc человека
<400> 147
tttactgtca cggttcccaa ggacctatat gtggtagagt atggtagcaa tatgacaatt 60
gaatgcaaat tcccagtaga aaaacaatta gacctggctg cactaattgt ctattgggaa 120
atggaggata agaacattat tcaatttgtg catggagagg aagacctgaa ggttcagcat 180
agtagctaca gacagagggc ccggctgttg aaggaccagc tctccctggg aaatgctgca 240
cttcagatca cagatgtgaa attgcaggat gcaggggtgt accgctgcat gatcagctat 300
ggtggtgccg actacaagcg aattactgtg aaagtcaatg ccccatacaa caaaatcaac 360
caaagaattt tggttgtgga tccagtcacc tctgaacatg aactgacatg tcaggctgag 420
ggctacccca aggccgaagt catctggaca agcagtgacc atcaagtcct gagtggtaag 480
accaccacca ccaattccaa gagagaggag aagcttttca atgtgaccag cacactgaga 540
atcaacacaa caactaatga gattttctac tgcactttta ggagattaga tcctgaggaa 600
aaccatacag ctgaattggt catcccagaa ctacctctgg cacatcctcc aaatgaaagg 660
ggtaccagat ctagagagcc caaatcttct gacaaaactc acacatgccc accgtgccca 720
gcacctgaat tcgagggtgc accgtcagtc ttcctcttcc ccccaaaacc caaggacacc 780
ctcatgatct cccggactcc tgaggtcaca tgcgtggtgg tggacgtaag ccacgaagac 840
cctgaggtca agttcaactg gtacgtggac ggcgtggagg tgcataatgc caagacaaag 900
ccgcgggagg agcagtacaa cagcacgtac cgtgtggtca gcgtcctcac cgtcctgcac 960
caggactggc tgaatggcaa ggagtacaag tgcaaggtct ccaacaaagc cctcccaacc 1020
cccatcgaga aaaccatctc caaagccaaa gggcagcccc gagaaccaca ggtgtacacc 1080
ctgcccccat cccgggatga gctgaccaag aaccaggtca gcctgacctg cctggtcaaa 1140
ggcttctatc caagcgacat cgccgtggag tgggagagca atgggcagcc ggagaacaac 1200
tacaagacca cgcctcccgt gctggactcc gacggctcct tcttcctcta cagcaagctc 1260
accgtggaca agagcaggtg gcagcagggg aacgtcttct catgctccgt gatgcatgag 1320
gctctgcaca accactacac gcagaagagc ctctccctgt ctccgggtaa atga 1374
<210> 148
<211> 457
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Последовательность PD-L1-hFc человека
<400> 148
Phe Thr Val Thr Val Pro Lys Asp Leu Tyr Val Val Glu Tyr Gly Ser
1 5 10 15
Asn Met Thr Ile Glu Cys Lys Phe Pro Val Glu Lys Gln Leu Asp Leu
20 25 30
Ala Ala Leu Ile Val Tyr Trp Glu Met Glu Asp Lys Asn Ile Ile Gln
35 40 45
Phe Val His Gly Glu Glu Asp Leu Lys Val Gln His Ser Ser Tyr Arg
50 55 60
Gln Arg Ala Arg Leu Leu Lys Asp Gln Leu Ser Leu Gly Asn Ala Ala
65 70 75 80
Leu Gln Ile Thr Asp Val Lys Leu Gln Asp Ala Gly Val Tyr Arg Cys
85 90 95
Met Ile Ser Tyr Gly Gly Ala Asp Tyr Lys Arg Ile Thr Val Lys Val
100 105 110
Asn Ala Pro Tyr Asn Lys Ile Asn Gln Arg Ile Leu Val Val Asp Pro
115 120 125
Val Thr Ser Glu His Glu Leu Thr Cys Gln Ala Glu Gly Tyr Pro Lys
130 135 140
Ala Glu Val Ile Trp Thr Ser Ser Asp His Gln Val Leu Ser Gly Lys
145 150 155 160
Thr Thr Thr Thr Asn Ser Lys Arg Glu Glu Lys Leu Phe Asn Val Thr
165 170 175
Ser Thr Leu Arg Ile Asn Thr Thr Thr Asn Glu Ile Phe Tyr Cys Thr
180 185 190
Phe Arg Arg Leu Asp Pro Glu Glu Asn His Thr Ala Glu Leu Val Ile
195 200 205
Pro Glu Leu Pro Leu Ala His Pro Pro Asn Glu Arg Gly Thr Arg Ser
210 215 220
Arg Glu Pro Lys Ser Ser Asp Lys Thr His Thr Cys Pro Pro Cys Pro
225 230 235 240
Ala Pro Glu Phe Glu Gly Ala Pro Ser Val Phe Leu Phe Pro Pro Lys
245 250 255
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
260 265 270
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
275 280 285
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
290 295 300
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
305 310 315 320
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
325 330 335
Ala Leu Pro Thr Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
340 345 350
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu
355 360 365
Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro
370 375 380
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
385 390 395 400
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
405 410 415
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
420 425 430
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
435 440 445
Lys Ser Leu Ser Leu Ser Pro Gly Lys
450 455
<210> 149
<211> 681
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Cyno-PD-L1-HisTag
<400> 149
tttactgtca cggttcccaa ggacctatat gtggtagagt atggcagcaa tatgacaatt 60
gaatgcaaat tcccagtaga aaaacaatta gacctgactt cactaattgt ctattgggaa 120
atggaggata agaacattat tcaatttgtg catggagagg aagacctgaa ggttcagcat 180
agtaactaca gacagagggc ccagctgttg aaggaccagc tctccctggg aaatgctgca 240
cttcggatca cagatgtgaa attgcaggat gcaggggttt accgctgcat gatcagctat 300
ggtggtgccg actacaagcg gattaccgtg aaagtcaatg ctccatacaa caaaatcaac 360
caaagaattt tggttgtcga tccagtcacc tctgaacatg aactaacatg tcaggctgag 420
ggctacccca aggccgaagt catttggaca agcagtgacc atcaagtcct gagtggtaag 480
accaccacca ccaattccaa gagagaggag aagcttttaa atgtgaccag cacactgaga 540
atcaacacaa cagctaatga gattttctac tgcattttta ggagattaga tcctgaggaa 600
aaccatacag ctgaattggt catcccagaa ctacctctgg cgcttcctcc aaatgaaagg 660
catcatcacc accatcacta a 681
<210> 150
<211> 226
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Cyno-PD-L1-HisTag
<400> 150
Phe Thr Val Thr Val Pro Lys Asp Leu Tyr Val Val Glu Tyr Gly Ser
1 5 10 15
Asn Met Thr Ile Glu Cys Lys Phe Pro Val Glu Lys Gln Leu Asp Leu
20 25 30
Thr Ser Leu Ile Val Tyr Trp Glu Met Glu Asp Lys Asn Ile Ile Gln
35 40 45
Phe Val His Gly Glu Glu Asp Leu Lys Val Gln His Ser Asn Tyr Arg
50 55 60
Gln Arg Ala Gln Leu Leu Lys Asp Gln Leu Ser Leu Gly Asn Ala Ala
65 70 75 80
Leu Arg Ile Thr Asp Val Lys Leu Gln Asp Ala Gly Val Tyr Arg Cys
85 90 95
Met Ile Ser Tyr Gly Gly Ala Asp Tyr Lys Arg Ile Thr Val Lys Val
100 105 110
Asn Ala Pro Tyr Asn Lys Ile Asn Gln Arg Ile Leu Val Val Asp Pro
115 120 125
Val Thr Ser Glu His Glu Leu Thr Cys Gln Ala Glu Gly Tyr Pro Lys
130 135 140
Ala Glu Val Ile Trp Thr Ser Ser Asp His Gln Val Leu Ser Gly Lys
145 150 155 160
Thr Thr Thr Thr Asn Ser Lys Arg Glu Glu Lys Leu Leu Asn Val Thr
165 170 175
Ser Thr Leu Arg Ile Asn Thr Thr Ala Asn Glu Ile Phe Tyr Cys Ile
180 185 190
Phe Arg Arg Leu Asp Pro Glu Glu Asn His Thr Ala Glu Leu Val Ile
195 200 205
Pro Glu Leu Pro Leu Ala Leu Pro Pro Asn Glu Arg His His His His
210 215 220
His His
225
<210> 151
<211> 450
<212> ДНК
<213> Homo sapiens
<400> 151
ccaggatggt tcttagactc cccagacagg ccctggaacc cccccacctt ctccccagcc 60
ctgctcgtgg tgaccgaagg ggacaacgcc accttcacct gcagcttctc caacacatcg 120
gagagcttcg tgctaaactg gtaccgcatg agccccagca accagacgga caagctggcc 180
gccttccccg aggaccgcag ccagcccggc caggactgcc gcttccgtgt cacacaactg 240
cccaacgggc gtgacttcca catgagcgtg gtcagggccc ggcgcaatga cagcggcacc 300
tacctctgtg gggccatctc cctggccccc aaggcgcaga tcaaagagag cctgcgggca 360
gagctcaggg tgacagagag aagggcagaa gtgcccacag cccaccccag cccctcaccc 420
aggccagccg gccagttcca aaccctggtg 450
<210> 152
<211> 150
<212> ПРТ
<213> Homo sapiens
<400> 152
Pro Gly Trp Phe Leu Asp Ser Pro Asp Arg Pro Trp Asn Pro Pro Thr
1 5 10 15
Phe Ser Pro Ala Leu Leu Val Val Thr Glu Gly Asp Asn Ala Thr Phe
20 25 30
Thr Cys Ser Phe Ser Asn Thr Ser Glu Ser Phe Val Leu Asn Trp Tyr
35 40 45
Arg Met Ser Pro Ser Asn Gln Thr Asp Lys Leu Ala Ala Phe Pro Glu
50 55 60
Asp Arg Ser Gln Pro Gly Gln Asp Cys Arg Phe Arg Val Thr Gln Leu
65 70 75 80
Pro Asn Gly Arg Asp Phe His Met Ser Val Val Arg Ala Arg Arg Asn
85 90 95
Asp Ser Gly Thr Tyr Leu Cys Gly Ala Ile Ser Leu Ala Pro Lys Ala
100 105 110
Gln Ile Lys Glu Ser Leu Arg Ala Glu Leu Arg Val Thr Glu Arg Arg
115 120 125
Ala Glu Val Pro Thr Ala His Pro Ser Pro Ser Pro Arg Pro Ala Gly
130 135 140
Gln Phe Gln Thr Leu Val
145 150
<210> 153
<211> 1134
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность PD-1-mFc человека
<400> 153
ccaggatggt tcttagactc cccagacagg ccctggaacc cccccacctt ctccccagcc 60
ctgctcgtgg tgaccgaagg ggacaacgcc accttcacct gcagcttctc caacacatcg 120
gagagcttcg tgctaaactg gtaccgcatg agccccagca accagacgga caagctggcc 180
gccttccccg aggaccgcag ccagcccggc caggactgcc gcttccgtgt cacacaactg 240
cccaacgggc gtgacttcca catgagcgtg gtcagggccc ggcgcaatga cagcggcacc 300
tacctctgtg gggccatctc cctggccccc aaggcgcaga tcaaagagag cctgcgggca 360
gagctcaggg tgacagagag aagggcagaa gtgcccacag cccaccccag cccctcaccc 420
aggccagccg gccagttcca aaccctggtg ggtaccagat ctagaggctg caaaccctgt 480
atctgcacag tgcccgaggt gagctccgtg ttcatctttc cccccaagcc caaggacgtg 540
ctgaccatca cactcacacc caaggtcacc tgcgtggtcg tggacatctc caaggacgac 600
cccgaagtcc agttcagctg gttcgtggac gacgtggagg tgcacaccgc tcagacccaa 660
cccagagagg agcagtttaa ctccaccttc aggtccgtgt ccgagctccc catcatgcac 720
caggactggc tgaatggcaa ggagttcaag tgcagggtga actccgctgc tttccccgcc 780
cccattgaga agaccatctc caagaccaag ggaaggccca aggcccccca ggtgtacacc 840
attccccctc ccaaggagca gatggccaag gacaaggtgt ccctgacctg tatgatcacc 900
gacttctttc ccgaggacat caccgtcgaa tggcagtgga acggccagcc cgccgagaac 960
tataagaaca cccaacccat catggacacc gacggcagct acttcgtgta tagcaagctc 1020
aacgtgcaga agagcaactg ggaagccgga aataccttca cctgctccgt cctgcacgag 1080
ggcctgcaca accaccatac cgaaaagagc ctgagccaca gccccggaaa gtaa 1134
<210> 154
<211> 377
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Последовательность PD-1-mFc человека
<400> 154
Pro Gly Trp Phe Leu Asp Ser Pro Asp Arg Pro Trp Asn Pro Pro Thr
1 5 10 15
Phe Ser Pro Ala Leu Leu Val Val Thr Glu Gly Asp Asn Ala Thr Phe
20 25 30
Thr Cys Ser Phe Ser Asn Thr Ser Glu Ser Phe Val Leu Asn Trp Tyr
35 40 45
Arg Met Ser Pro Ser Asn Gln Thr Asp Lys Leu Ala Ala Phe Pro Glu
50 55 60
Asp Arg Ser Gln Pro Gly Gln Asp Cys Arg Phe Arg Val Thr Gln Leu
65 70 75 80
Pro Asn Gly Arg Asp Phe His Met Ser Val Val Arg Ala Arg Arg Asn
85 90 95
Asp Ser Gly Thr Tyr Leu Cys Gly Ala Ile Ser Leu Ala Pro Lys Ala
100 105 110
Gln Ile Lys Glu Ser Leu Arg Ala Glu Leu Arg Val Thr Glu Arg Arg
115 120 125
Ala Glu Val Pro Thr Ala His Pro Ser Pro Ser Pro Arg Pro Ala Gly
130 135 140
Gln Phe Gln Thr Leu Val Gly Thr Arg Ser Arg Gly Cys Lys Pro Cys
145 150 155 160
Ile Cys Thr Val Pro Glu Val Ser Ser Val Phe Ile Phe Pro Pro Lys
165 170 175
Pro Lys Asp Val Leu Thr Ile Thr Leu Thr Pro Lys Val Thr Cys Val
180 185 190
Val Val Asp Ile Ser Lys Asp Asp Pro Glu Val Gln Phe Ser Trp Phe
195 200 205
Val Asp Asp Val Glu Val His Thr Ala Gln Thr Gln Pro Arg Glu Glu
210 215 220
Gln Phe Asn Ser Thr Phe Arg Ser Val Ser Glu Leu Pro Ile Met His
225 230 235 240
Gln Asp Trp Leu Asn Gly Lys Glu Phe Lys Cys Arg Val Asn Ser Ala
245 250 255
Ala Phe Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Thr Lys Gly Arg
260 265 270
Pro Lys Ala Pro Gln Val Tyr Thr Ile Pro Pro Pro Lys Glu Gln Met
275 280 285
Ala Lys Asp Lys Val Ser Leu Thr Cys Met Ile Thr Asp Phe Phe Pro
290 295 300
Glu Asp Ile Thr Val Glu Trp Gln Trp Asn Gly Gln Pro Ala Glu Asn
305 310 315 320
Tyr Lys Asn Thr Gln Pro Ile Met Asp Thr Asp Gly Ser Tyr Phe Val
325 330 335
Tyr Ser Lys Leu Asn Val Gln Lys Ser Asn Trp Glu Ala Gly Asn Thr
340 345 350
Phe Thr Cys Ser Val Leu His Glu Gly Leu His Asn His His Thr Glu
355 360 365
Lys Ser Leu Ser His Ser Pro Gly Lys
370 375
<210> 155
<211> 1164
<212> ДНК
<213> Искусственная последовательность
<220>
<223> Последовательность PD-1-hFc человека
<400> 155
ccaggatggt tcttagactc cccagacagg ccctggaacc cccccacctt ctccccagcc 60
ctgctcgtgg tgaccgaagg ggacaacgcc accttcacct gcagcttctc caacacatcg 120
gagagcttcg tgctaaactg gtaccgcatg agccccagca accagacgga caagctggcc 180
gccttccccg aggaccgcag ccagcccggc caggactgcc gcttccgtgt cacacaactg 240
cccaacgggc gtgacttcca catgagcgtg gtcagggccc ggcgcaatga cagcggcacc 300
tacctctgtg gggccatctc cctggccccc aaggcgcaga tcaaagagag cctgcgggca 360
gagctcaggg tgacagagag aagggcagaa gtgcccacag cccaccccag cccctcaccc 420
aggccagccg gccagttcca aaccctggtg ggtaccagat ctagagagcc caaatcttct 480
gacaaaactc acacatgccc accgtgccca gcacctgaat tcgagggtgc accgtcagtc 540
ttcctcttcc ccccaaaacc caaggacacc ctcatgatct cccggactcc tgaggtcaca 600
tgcgtggtgg tggacgtaag ccacgaagac cctgaggtca agttcaactg gtacgtggac 660
ggcgtggagg tgcataatgc caagacaaag ccgcgggagg agcagtacaa cagcacgtac 720
cgtgtggtca gcgtcctcac cgtcctgcac caggactggc tgaatggcaa ggagtacaag 780
tgcaaggtct ccaacaaagc cctcccaacc cccatcgaga aaaccatctc caaagccaaa 840
gggcagcccc gagaaccaca ggtgtacacc ctgcccccat cccgggatga gctgaccaag 900
aaccaggtca gcctgacctg cctggtcaaa ggcttctatc caagcgacat cgccgtggag 960
tgggagagca atgggcagcc ggagaacaac tacaagacca cgcctcccgt gctggactcc 1020
gacggctcct tcttcctcta cagcaagctc accgtggaca agagcaggtg gcagcagggg 1080
aacgtcttct catgctccgt gatgcatgag gctctgcaca accactacac gcagaagagc 1140
ctctccctgt ctccgggtaa atga 1164
<210> 156
<211> 222
<212> ПРТ
<213> Искусственная последовательность
<220>
<223> Последовательность PD-1-hFc человека
<400> 156
Pro Gly Trp Phe Leu Asp Ser Pro Asp Arg Pro Trp Asn Pro Pro Thr
1 5 10 15
Phe Ser Pro Ala Leu Leu Val Val Thr Glu Gly Asp Asn Ala Thr Phe
20 25 30
Thr Cys Ser Phe Ser Asn Thr Ser Glu Ser Phe Val Leu Asn Trp Tyr
35 40 45
Arg Met Ser Pro Ser Asn Gln Thr Asp Lys Leu Ala Ala Phe Pro Glu
50 55 60
Asp Arg Ser Gln Pro Gly Gln Asp Cys Arg Phe Arg Val Thr Gln Leu
65 70 75 80
Pro Asn Gly Arg Asp Phe His Met Ser Val Val Arg Ala Arg Arg Asn
85 90 95
Asp Ser Gly Thr Tyr Leu Cys Gly Ala Ile Ser Leu Ala Pro Lys Ala
100 105 110
Gln Ile Lys Glu Ser Leu Arg Ala Glu Leu Arg Val Thr Glu Arg Arg
115 120 125
Ala Glu Val Pro Thr Ala His Pro Ser Pro Ser Pro Arg Pro Ala Gly
130 135 140
Gln Phe Gln Thr Leu Val Gly Thr Arg Ser Arg Glu Pro Lys Ser Ser
145 150 155 160
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Phe Glu Gly
165 170 175
Ala Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
180 185 190
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
195 200 205
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
210 215 220
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| МОНОСПЕЦИФИЧЕСКИЕ И БИСПЕЦИФИЧЕСКИЕ БЕЛКИ С РЕГУЛИРОВАНИЕМ ИММУННОЙ КОНТРОЛЬНОЙ ТОЧКИ ДЛЯ ЛЕЧЕНИЯ РАКА | 2018 |
|
RU2793167C2 |
| НОВЫЙ СЛИТЫЙ БЕЛОК, СПЕЦИФИЧНЫЙ ДЛЯ CD137 И PD-L1 | 2019 |
|
RU2818349C2 |
| СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ, СВЯЗЫВАЮЩИЕ PD-L1 и LAG-3 | 2017 |
|
RU2784388C2 |
| СЛИТЫЙ БЕЛОК И ЕГО ПРИМЕНЕНИЕ | 2020 |
|
RU2811120C2 |
| Иммунотерапия с применением антител, связывающих лиганд 1 белка программируемой смерти клеток (PD-L1) | 2017 |
|
RU2766582C2 |
| АНТИТЕЛА ПРОТИВ ЛИГАНДА 1 ПРОГРАММИРУЕМОЙ ГИБЕЛИ И ИХ ПРИМЕНЕНИЯ | 2020 |
|
RU2786235C1 |
| БЕЛКИ УПРАВЛЕНИЯ, НАВИГАЦИИ И КОНТРОЛЯ И СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2019 |
|
RU2811457C2 |
| МУЛЬТИСПЕЦИФИЧЕСКИЕ АНТИТЕЛА И СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2018 |
|
RU2811477C2 |
| АНТИ-PD-L1 АНТИТЕЛО ДЛЯ ДЕТЕКЦИИ PD-L1 | 2018 |
|
RU2758723C2 |
| БИФУНКЦИОНАЛЬНЫЕ БЕЛКИ, КОМБИНИРУЮЩИЕ БЛОКАДУ КОНТРОЛЬНОЙ ТОЧКИ, ДЛЯ ТАРГЕТНОЙ ТЕРАПИИ | 2019 |
|
RU2756899C1 |

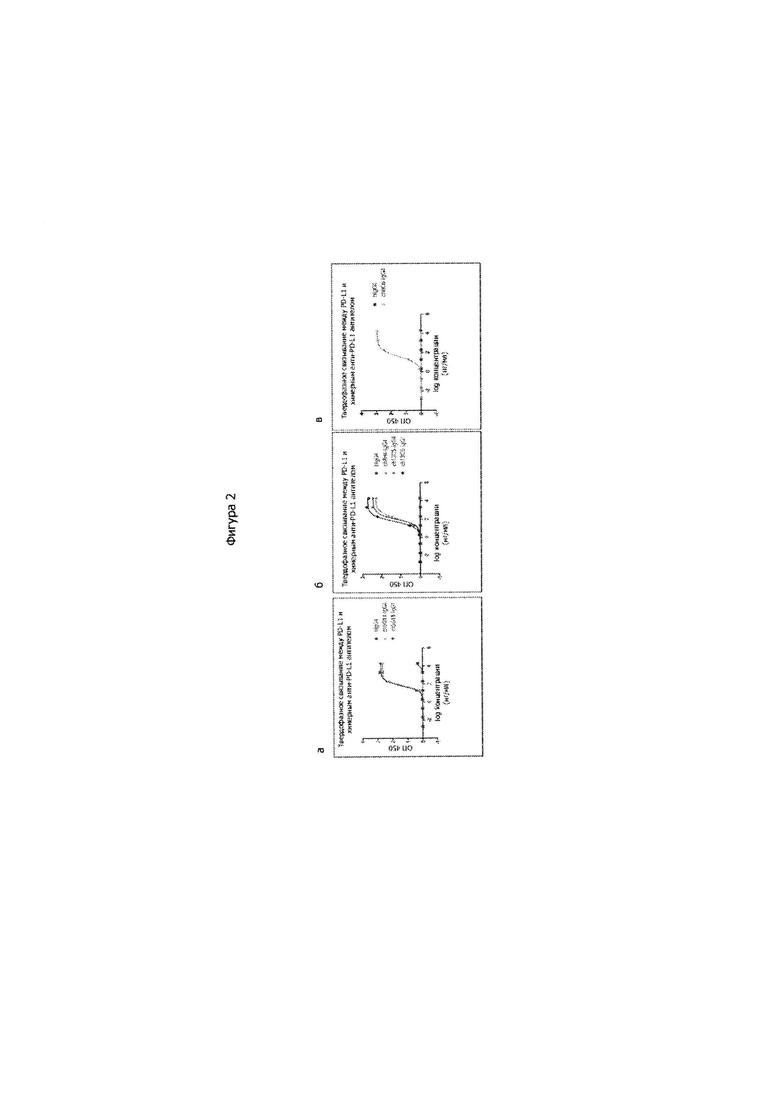


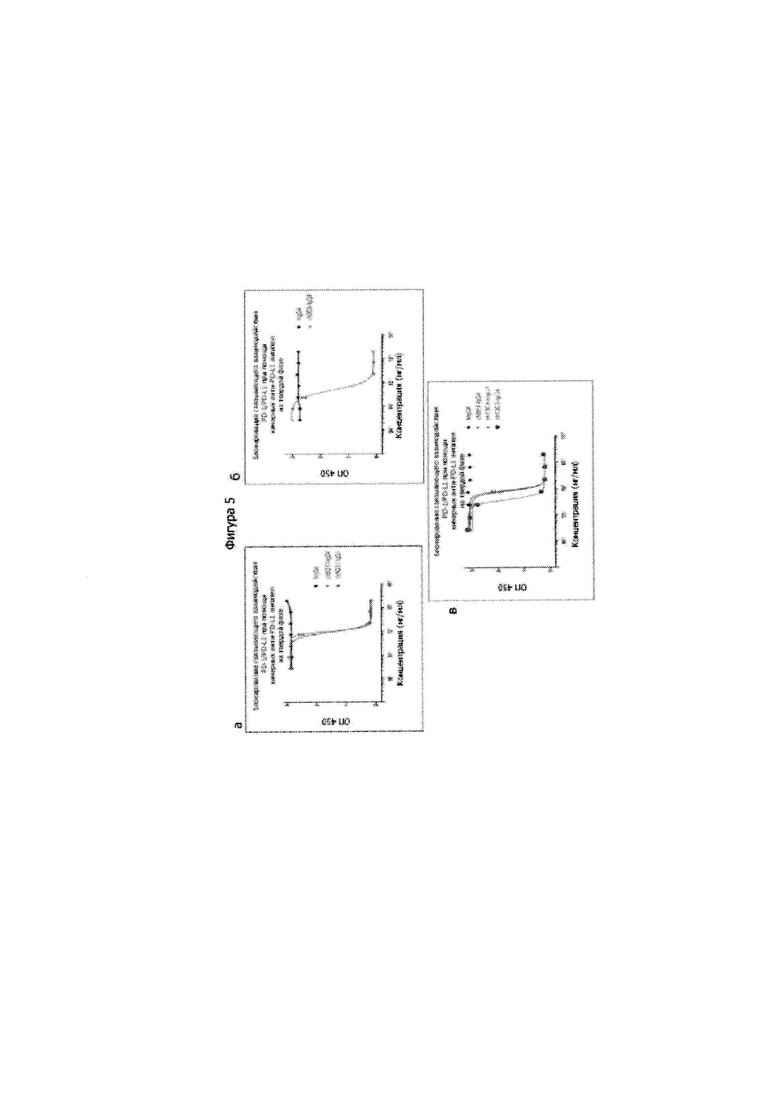







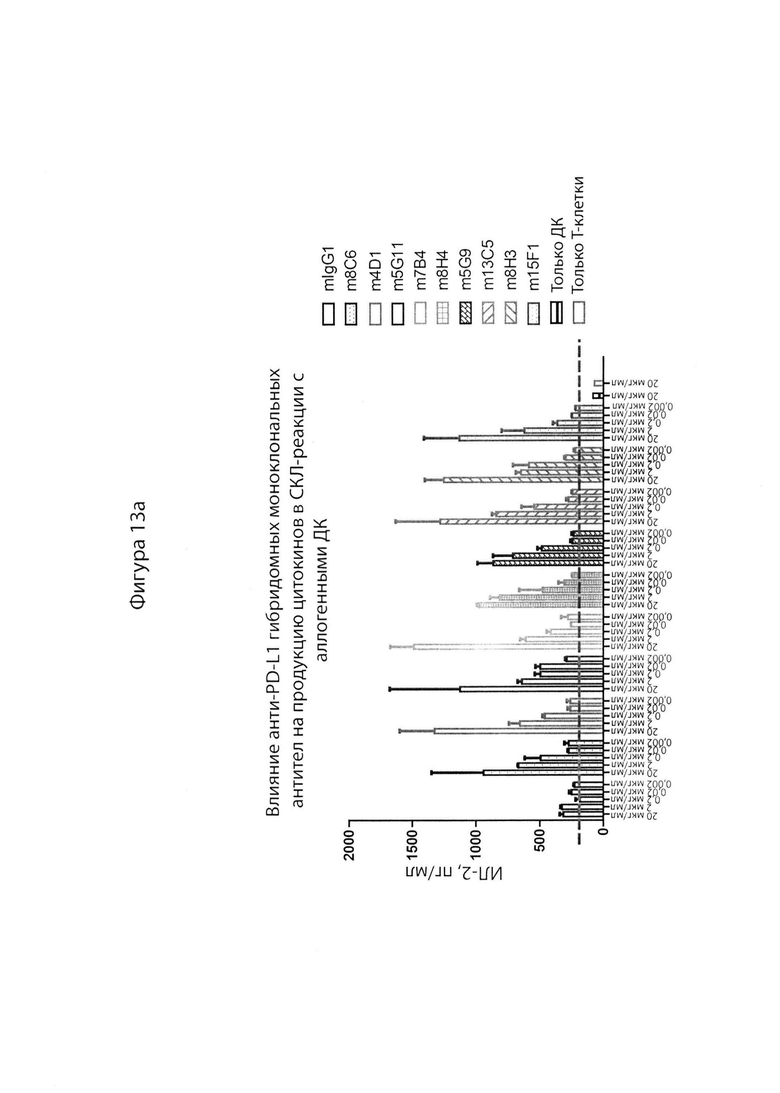


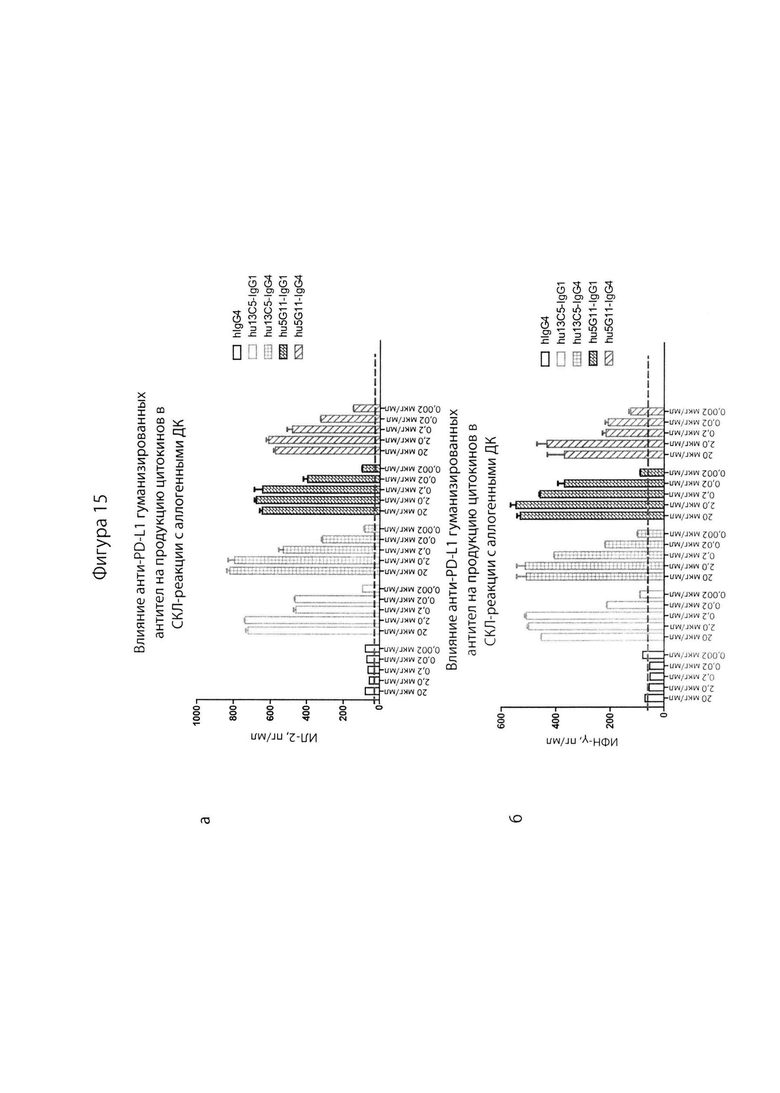



Изобретение относится к области биохимии, в частности к антителу, которое специфично связывается с PD-1. Также раскрыты композиция, содержащая указанное антитело, полинуклеотид, кодирующий указанное антитело, вектор и клетка-хозяин, содержащие указанный полинуклеотид. Раскрыты способы лечения рака и инфекционного заболевания, ассоциированных с PD-1, уменьшения опухоли, ассоциированной с PD-1, способ повышения активации Т-клеток. Изобретение позволяет эффективно лечить заболевания, ассоциированные с PD-1. 9 н. и 33 з.п. ф-лы, 19 ил., 8 пр., 16 табл.
1. Выделенное антитело или его антигенсвязывающий фрагмент, которое связывается с PD-L1, содержащее:
i) CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 93, 94 и 95, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 96, 97 и 98, соответственно;
ii) CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 81, 82 и 83, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 84, 85 и 86, соответственно;
iii) CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 87, 88 и 89, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 90, 91 и 92, соответственно;
iv) CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 99, 100 и 101, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 102, 103 и 104, соответственно;
v) CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 105, 106 и 107, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 108, 109 и 110, соответственно;
vi) CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 111, 112 и 113, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 114, 115 и 116, соответственно;
vii) CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 117, 118 и 119, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 120, 121 и 122, соответственно;
viii) CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 123, 124 и 125, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 126, 127 и 128, соответственно;
ix) CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 129, 130 и 131, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 132, 133 и 134, соответственно; или
x) CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 135, 136 и 137, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 138, 139 и 140, соответственно.
2. Антитело или фрагмент по п. 1, где антитело или его фрагмент содержит CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 81, 82 и 83, соответственно; и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 84, 85 и 86, соответственно.
3. Антитело или фрагмент по п. 1, где антитело или его фрагмент содержит CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 87, 88 и 89, соответственно, и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 90, 91 и 92, соответственно.
4. Антитело или фрагмент по п. 1, где антитело или его фрагмент содержит CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 93, 94 и 95, соответственно, и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 96, 97 и 98, соответственно.
5. Антитело или фрагмент по п. 1, где антитело или его фрагмент содержит CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 99, 100 и 101, соответственно, и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 102, 103 и 104, соответственно.
6. Антитело или фрагмент по п. 1, где антитело или его фрагмент содержит CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 105, 106, и 107, соответственно, и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 108, 109, 110, соответственно.
7. Антитело или фрагмент по п. 1, где антитело или его фрагмент содержит CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 111, 112 и 113, соответственно, и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 114, 115 и 116, соответственно.
8. Антитело или фрагмент по п. 1, где антитело или его фрагмент содержит CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 117, 118 и 119, соответственно, и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 120, 121 и 122, соответственно.
9. Антитело или фрагмент по п. 1, где антитело или его фрагмент содержит CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 123, 124 и 125, соответственно, и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 126, 127 и 128, соответственно.
10. Антитело или фрагмент по п. 1, где антитело или его фрагмент содержит CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 129, 130 и 131, соответственно, и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 132, 133 и 134, соответственно.
11. Антитело или фрагмент по п. 1, где антитело или его фрагмент содержит CDR1, CDR2 и CDR3 тяжелой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 135, 136 и 137, соответственно, и CDR1, CDR2 и CDR3 легкой цепи, содержащие аминокислотную последовательность в соответствии с SEQ ID NO: 138, 139 и 140, соответственно.
12. Выделенное антитело или его фрагмент по любому из пп. 1-11, где антитело или его фрагмент является химерным или гуманизированным.
13. Выделенное антитело или его фрагмент по любому из пп. 1-12, где антитело или фрагмент содержит:
(i) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 2, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 4;
(ii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 6, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 8;
(iii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 10, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 12;
(iv) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 14, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 16;
(v) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 18, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 20;
(vi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 22, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 24;
(vii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 26, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 28;
(viii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 30, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 32;
(ix) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 34, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 36;
(x) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 38, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 40;
(xi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 42, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 44; или
(xii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 46, и вариабельную область легкой цепи, содержащую аминокислотную последовательность, имеющую по меньшей мере 80 % гомологии с SEQ ID NO: 48.
14. Выделенное антитело или его фрагмент по п. 13, где антитело или фрагмент содержит:
(i) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 2, и вариабельную область легкой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 4;
(ii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 6, и вариабельную область легкой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 8;
(iii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 10, и вариабельную область легкой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 12;
(iv) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 14, и вариабельную область легкой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 16;
(v) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 18, и вариабельную область легкой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 20;
(vi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 22, и вариабельную область легкой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 24;
(vii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 26, и вариабельную область легкой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 28;
(viii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 30, и вариабельную область легкой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 32;
(ix) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 34, и вариабельную область легкой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 36;
(x) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 38, и вариабельную область легкой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 40;
(xi) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 42, и вариабельную область легкой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 44; или
(xii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 46, и вариабельную область легкой цепи, содержащую аминокислотную последовательность в соответствии с SEQ ID NO: 48.
15. Выделенное антитело или его фрагмент по п. 1 или 4, где антитело или его фрагмент содержит вариабельную область тяжелой цепи в соответствии с SEQ ID NO: 42 и вариабельную область легкой цепи в соответствии с SEQ ID NO: 44.
16. Выделенное антитело или его фрагмент по п. 1 или 2, где антитело или его фрагмент содержит вариабельную область тяжелой цепи в соответствии с SEQ ID NO: 46 и вариабельную область легкой цепи в соответствии с SEQ ID NO: 48.
17. Выделенное антитело по п. 1 или 4, где антитело содержит тяжелую цепь в соответствии с SEQ ID NO: 70 и легкую цепь в соответствии с SEQ ID NO: 74.
18. Выделенное антитело по п. 1 или 4, где антитело содержит тяжелую цепь в соответствии с SEQ ID NO: 72 и легкую цепь в соответствии с SEQ ID NO: 74.
19. Выделенное антитело по п. 1 или 2, где антитело содержит тяжелую цепь в соответствии с SEQ ID NO: 76 и легкую цепь в соответствии с SEQ ID NO: 80.
20. Выделенное антитело по п. 1 или 2, где антитело содержит тяжелую цепь в соответствии с SEQ ID NO: 78 и легкую цепь в соответствии с SEQ ID NO: 80.
21. Выделенное антитело или его фрагмент по любому из пп. 1-16, отличающееся тем, что указанное антитело является моноклональным антителом, и указанный антигенсвязывающий фрагмент выбирают из группы, состоящей из scFv, Fab-фрагмента, Fab’-фрагмента, и F(ab)’2-фрагмента.
22. Выделенное антитело по любому из пп. 17-20, где указанное антитело является моноклональным антителом.
23. Антитело или его фрагмент по любому из пп. 1-16, или антитело по любому из пп. 17-20, где антитело или его фрагмент связывают или конъюгируют с терапевтическим агентом.
24. Антитело или его фрагмент по п. 23, где терапевтический агент представляет собой цитотоксический препарат, радиоактивный изотоп, иммуномодулятор или антитело.
25. Выделенное антитело или его фрагмент по любому из пп. 1-16, или антитело по любому из пп. 17-20, где антитело или его фрагмент имеет аффинность к PD-L1 от около 10 нмоль/л до около 0,01 нмоль/л.
26. Выделенное антитело или его фрагмент по п. 25, где антитело или его фрагмент имеет аффинность к PD-L1 около 10 нмоль/л или менее.
27. Выделенное антитело или его фрагмент по п. 25, где антитело или его фрагмент имеет аффинность к PD-L1 около 1,0 нмоль/л или менее.
28. Выделенное антитело или его фрагмент по любому из пп. 1-16, или антитело по любому из пп. 17-20, где антитело имеет ЭК50 связывания от около 5 нг/мл до около 1000 нг/мл.
29. Выделенное антитело или его фрагмент по любому из пп. 1-16, или антитело по любому из пп. 17-20, где антитело блокирует связывание PD-L1 с PD-1.
30. Выделенное антитело или его фрагмент по п. 29, где антитело или его фрагмент блокирует связывание PD-L1 с PD-1 при ИК50 от около 5 нг/мл до около 1000 нг/мл.
31. Выделенное антитело или его фрагмент по любому из пп. 1-16, или антитело по любому из пп. 17-20, где антитело или фрагмент повышает активацию T-клеток, на основании измерений выработки воспалительных цитокинов.
32. Выделенное антитело или его фрагмент по п. 31, где антитело или его фрагмент повышает продукцию ИЛ-2 и ИФН-ƨ Т-клетками.
33. Композиция для лечения нарушения, ассоциированного с экспрессией PD-L1, содержащая терапевтически эффективное количество антитела или его антигенсвязывающего фрагмента по любому из пп. 1-32 и фармацевтически приемлемый носитель.
34. Выделенный полинуклеотид, кодирующий антитело или его антигенсвязывающий фрагмент по любому из пп. 1-32.
35. Экспрессирующий вектор, содержащий выделенный полинуклеотид по п. 34.
36. Клетка-хозяин для экспрессии антитела по п. 1, содержащая экспрессирующий вектор по п. 35.
37. Способ повышения активации Т-клеток, включающий стадию, в которой приводят в контакт Т-клетку с антителом или его антигенсвязывающим фрагментом по любому из пп. 1-32.
38. Способ уменьшения опухоли, ассоциированной с экспрессией PD-L1, или ингибирования роста опухолевых клеток, ассоциированных с экспрессией PD-L1, у субъекта, включающий стадию, в которой субъекту вводят терапевтически эффективное количество выделенного антитела или его антигенсвязывающего фрагмента по любому из пп. 1-32.
39. Способ лечения рака, ассоциированного с экспрессией PD-L1, у субъекта, нуждающегося в этом, причем способ включает стадию, в которой субъекту вводят терапевтически эффективное количество выделенного антитела или его антигенсвязывающего фрагмента по любому из пп. 1-32.
40. Способ по п. 39, отличающийся тем, что рак выбирают из группы, состоящей из лимфомы, лейкемии, меланомы, глиомы, рака молочной железы, рака легкого, рака толстой кишки, рака костей, рака яичника, рака мочевого пузыря, рака почки, рака печени, рака желудка, рака прямой кишки, рака яичек, рака слюнной железы, рака щитовидной железы, рака тимуса, эпителиального рака, рака головы или шеи, рак желудочно-кишечного тракта, рака поджелудочной железы, или их комбинации.
41. Способ лечения инфекционного заболевания, ассоциированного с экспрессией PD-L1, у субъекта, нуждающегося в этом, включающий стадию, в которой субъекту вводят терапевтически эффективное количество выделенного антитела или его антигенсвязывающего фрагмента по любому из пп. 1-32.
42. Способ по п. 41, отличающийся тем, что инфекционное заболевание выбирают из группы, состоящей из кандидоза, кандидемии, аспергиллеза, стрептококковой пневмонии, стрептококковых кожных и орофарингеальных заболеваний, грамотрицательного сепсиса, туберкулеза, мононуклеоза, гриппа, респираторного заболевания, вызванного респираторно-синцитиальным вирусом, малярии, шистосомоза и трипаносомиаза.
| МОДИФИЦИРОВАННЫЕ ДЕНДРИТНЫЕ КЛЕТКИ И ИХ ПРИМЕНЕНИЕ В ЛЕЧЕНИИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ | 2008 |
|
RU2484132C2 |
| US 20120328693 A1, 27.12.2012 | |||
| US 20100203056 A1, 12.08.2010 | |||
| AU 2013204861 A1, 09.05.2013. | |||
Авторы
Даты
2020-05-28—Публикация
2015-08-05—Подача