Изобретение относится к моделям в нейробиологии и может быть использовано при физиологических исследованиях формирования ритмической импульсной реакции реверберации и диагностики патологических факторов, влияющих на нейроны.
Реверберация или возвратная повторная ритмическая длительная электрическая активность, характерна для многих структур мозга. Свойствами реверберации могут обладать нервные пути в гиппокампе, неокортексе, миндалина-гиппокамп-кортикальной оси и спинном мозге.
Реверберационная теория была выдвинута известным морфофизиологом Рафаэлем Лоренте-де-Но в начале прошлого века [1]. Она базировалась на существовании в структурах мозга замкнутых нейронных цепей, когда аксоны нервных клеток могут возвращаться обратно к телу клетки. В связи с чем появляется возможность циркуляции нервного импульса по ревербирирующим (постепенно затухающим) кругам возбуждения. Джон Экклс в середине прошлого века создал учение о синаптических "реверберационных кругах возбуждения", о повсеместном наличии "петель обратной связи" [2].
Основную роль в развитии механизма реверберации и в настоящее время отводят химическим синапсам [3]. Синаптическая реверберация рассматривается как вероятный механизм активного поддержания рабочей памяти [4, 5].
Сложность экспериментального доступ к ревербеционным путям мозга затрудняет исследование их электрофизиологических свойств с корреляцией этих свойств с анатомо-морфологическим строением. В связи с этим большинство исследований реверберации основаны на схемах, включающих в основном химические синапсы. Известны математические и созданные на их основе графические [6-11], а так же искусственно созданные биологические модели нервной системы [12], обладающие свойствами реверберации. Эти модели представляют собой нервные клетки, связанные между собой химическими синапсами и описывают предполагаемые (гипотетические) нервные процессы. Однако нет никаких исследований, демонстрирующих, экспериментально или теоретически, участие электрических синапсов в реализации реверберации в мозге.
Наиболее близкой к предлагаемой является модель Лао и Би [12], выполненная на нейронах гиппокампа эмбрионов крыс, представляющая собой систему одиночных нейронов в культуре ткани, предварительно лишенных всех нервных отростков, химических синапсов и мембранных контактов, включая щелевые контакты, то есть электрические синапсы. Исследование Лао и Би построено только на повторно развившихся регенирирующих химических синапсах, связывающих нейроны между собой в рефлекторную дугу. Эта модель используется для доказательства возникновения процесса реверберации с участием только химических синапсов.
Модель выполнена не на естественной нервной структуре, а на специально искусственно созданной культуральной сети из клеток гипокаммпа мозга крысы с редким расположением клеток без предшествующей анатомической специализации, что предполагает невозможность экспериментальной повторной воспроизводимости нервной сети. Исследуемые сети находились в питательной среде с присутствием телячьей сыворотки, состав которой невозможно точно учесть. Для того, чтобы предотвратить разрастание глиальных клеток в создаваемой культуре, авторы добавляли в среду циклоцин-арабинозид. О наличии химических синапсов судили по "шуму" синаптической передачи. В модели культуры клеток регистрировались случайные синхронные полисинаптические спайки. Таким образом, анализировалась реверберационная активность не компактного органа, а случайного набора нескольких неизвестных по функции нейронов, без учета электрических синапсов.
Математические и графические модели реверберации описывают теоретическую возможность возникновения и протекания этого процесса на основе химических или электрических синапсов. Стабильной биологической модели для получения реакции реверберации, в которой нервные клетки контактируют исключительно только через электрические синапсы, нет. Техническая проблема состоит в том, что в эксперименте на культуральной сети из нервных клеток невозможно получить сопоставимые сети, а, следовательно, сопоставимые электрофизиологические результаты по получению реакции реверберации и провести достоверную обработку экспериментальных данных.
Ставится техническая задача разработки биологической модели, представляющей собой нервные клетки и волокна в целостной структуре мозга, связанные электрическими синапсами, на основе которой можно получить реакцию реверберации, и способа ее создания.
Задача решается за счет того, что предлагается нейрофизиологическая модель нервной системы, обладающая свойствами реверберации, представляющая собой ганглии со связанными между собой нервными клетками и нервными волокнами, в которой клетки и волокна соединены между собой посредством щелевых контактов.
Для модели использован ганглий брюшной нервной цепочки медицинской пиявки с находящимися нервными клетками и их отростками, связанными между собой плотными щелевыми контактами, без глиального окружения.
Для создания модели с помощью проназы разрушают соединительнотканные капсулы и глиальные оболочки, денудируя нервные клетки, соединенные между собой отростками, и сохраняя целостность нейрональной сетевой функции нервного ганглия брюшного мозга пиявки, обеспечивая тем самым возникновение щелевых контактов между нервными волокнами и нервными клетками. В общей сложности создается нервный ганглий, обладающий новыми электрофизиологическими функциями.
Действие проназы состоит в том, что, являясь суммой многих протеолитических ферментов широкого круга действия, она в первую очередь действует на глиальные оболочки, окружающие нейроны и его отростки. Удаление глиальных оболочек приводит к сближению нейрональных мембран, их адгезионному взаимодействию, агрегации и образованию щелевых контактов, обладающих свойствами электрических синапсов.
Пиявок наркотизировали в холодной воде, вскрывали с брюшной стороны, извлекали часть брюшной нервной цепочки, состоящую из 7 ганглиев. Второй от головного нервный ганглий с подходящими к нему нервными коннективами помещали в пластиковую камеру и раскалывали на резиновой подложке за окружающие его ткани. Заливали препарат раствором Рингера для пиявки (130 мМ NaCl, 4 мМ KCl, 1.8 мМ CaCl, 48 Мм глюкозы, рН 7.4). На поверхности ганглия были видны два крупных нейрона - клетки Ретциуса. Экстраклеточный отводящий золотой микроэлектрод в стеклянной изоляции подводили к одному из них под контролем микроскопа МБС-10. Остальную часть нервной цепочки через вазелиновый мостик помещали во вторую камеру с биполярными раздражающими электродами. Нервную коннективу между четвертым и пятым ганглиями помещали на электроды и раздражали прямоугольными толчками электрического тока силой в два раза превышающей пороговую, длительностью равной 0.2 мс. Регистрировали спонтанную импульсную активность нейрона Ретциуса. Затем использованный раствор Рингера для пиявки заменяли на раствор Рингера, содержащий проназу в концентрации 0,2-0.4%. В растворе проназы ганглий находился в течение часа. После этого ганглий аккуратно промывали раствором Рингера для пиявки, удаляя проназу и отторгнутые глиальные оболочки. Вновь регистрировали частоту спонтанной импульсной активности и вызванную импульсную активность на одиночный стимул нейрона Ретциуса. Наиболее пригодны для создания моделей взрослые двухгодичные пиявки.
Стимуляцию нервного волокна проводили при помощи электростимулятора ЭСУ-1 (Россия), сигнал регистрировали при помощи усилителя УБП1-02 (Россия). Экспериментальные данные визуально анализировали на осциллографах С1-93 (Россия), цифровом осциллографе GDS-806S (GW Instek, Тайвань), записывали и сохраняли на компьютере.
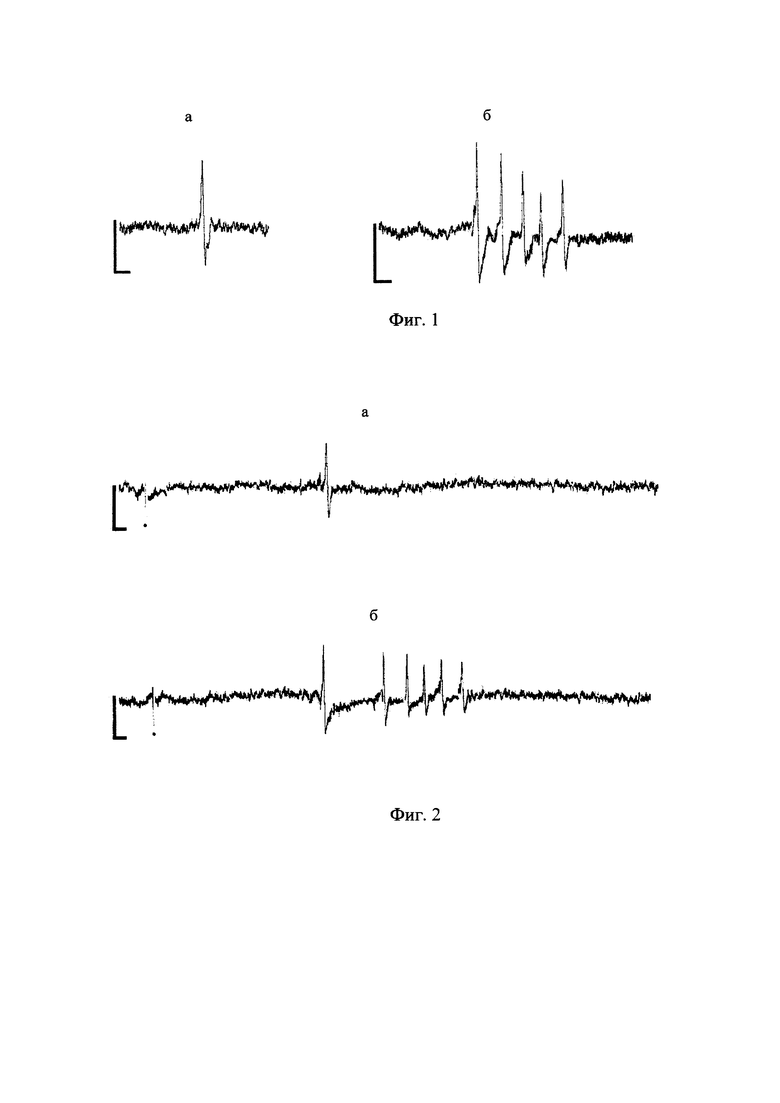
На фиг. 1 представлены осциллограммы спонтанной импульсной активности нейрона Ретциуса: а - в контроле, где нейрон генерирует спонтанные одиночные импульсы, б - после действия проназы, где нейрон генерирует спонтанную пачечную ритмическую импульсную активность - реверберацией. Калибровка: 25 мкВ, 10 мс.
На фиг. 2 представлены осциллограммы вызванной импульсной активность нейрона Ретциуса: а - в контроле, где нейрон отвечает одиночным потенциалом действия на раздражающий стимул, б - после действия проназы, где нейрон отвечает вызванной пачечной ритмической импульсной активностью - реверберационный ответ. Калибровка: 25 мкВ, 10 мс. Точками обозначен артефакт (раздражающий импульс).
Электрофизиологическая регистрация импульсного ответа крупного нейрона (клетки Ретциуса), расположенного на поверхности модели, показывает, что после действия проназы спонтанная импульсная активность нейрона и вызванная импульсная активность нейрона приобретают признаки реверберации.
Технический результат состоит в том, что получена модель, выполненная на естественной нервной структуре - модифицированном нервном брюшном ганглии медицинской пиявки, включающая неповрежденные нервные клетки с отростками и плотными щелевыми контактами (электрическими синапсами), связывающими нейроны между собой в единые сети. Модель находится в растворе Рингера, состав которого соответствует стандартному для пиявки. Модель позволяет получить высокую экспериментальную воспроизводимость электрофизиологических результатов. На модели регистрировалась постоянная спонтанная импульсная активность по реверберационному типу. О наличии электрических синапсов судили по реверберационному импульсному ответу нейрона на раздражающее воздействие. Таким образом, регистрация импульсной активности позволяет анализировать реверберационную реакцию нейрона, находящегося в составе модели нервного ганглия, с преимущественным наличием электрических синапсов.
Список литературы
1.  Vestibulo-ocular reflex arc // Arch. Neurol. Psych. 1933. V. 30. №2. P. 245-291.
Vestibulo-ocular reflex arc // Arch. Neurol. Psych. 1933. V. 30. №2. P. 245-291.
2. Экклс Д. Тормозные пути в центральной нервной системе. М., Наука, 1971. 168 с.
3.  Compte A., Wang X.J. The dynamical stability of reverberatory neural circuits. // Biol Cybern. 2002. V. 87. N. 5-6. P. 471-481.
Compte A., Wang X.J. The dynamical stability of reverberatory neural circuits. // Biol Cybern. 2002. V. 87. N. 5-6. P. 471-481.
4. Ribeiro S., Nicolelis M.A. Reverberation, storage, and postsynaptic propagation of memories during sleep // Learn. Mem. 2004. V. 11. №6. P. 686-696.
5. Wang M., Gamo N.J., Yang Y. et al. Neuronal basis of age - related working memory decline // Nature. 2011. V. 476. №7359. P. 210-213.
6. Constantinidis C., Wang X.J. A neural circuit basis for spatial working memory // Neuroscientist. 2004. V. 10. №6. P. 553-565.
7.  Rosin D P., Worlitzer V.M. et al. Pattern reverberation in networks of excitable systems with connection delays // Chaos. 2017. V. 27. №1: 013114.
Rosin D P., Worlitzer V.M. et al. Pattern reverberation in networks of excitable systems with connection delays // Chaos. 2017. V. 27. №1: 013114.
8. Maciunas K., Snipas M., Paulauskas N. et al. Reverberation of excitation in neuronal networks interconnected through voltage-gated gap junction channels // J. Gen. Physiol. 2016. V. 147. №3. P. 273-288.
9. Sotnikov O.S., Chizhov F.V., Laktionova A.A., Pokrovsky A.N. Syncytial cytoplasmatic communication of neurons and model of electric activity of their population. // Europ. J. Biomed.. Life Sci. 2016. №4. P. 6-11.
10. Volman V., Perc M., Bazhenov M. Gap junctions and epileptic seizures - two sides of the same coin? // PLoS One. 2011. V. 6: e20572.
11. Wang X.J.,  Constantinidis C., Goldman-Rakic P.S. Division of labor among distinct subtypes of inhibitory neurons in a cortical microcircuit of working memory. // Proc Natl. Acad. Sci. USA. 2004. V. 101. №5. P. 1368-1373.
Constantinidis C., Goldman-Rakic P.S. Division of labor among distinct subtypes of inhibitory neurons in a cortical microcircuit of working memory. // Proc Natl. Acad. Sci. USA. 2004. V. 101. №5. P. 1368-1373.
12. Lao P.M., Bi G.Q. Synaptic mechanisms of persistent reverberatory activity in neuronal networks. // Proc. Natl. Acad. Sci. USA. 2005. V. 102. №29. P. 10333-10338.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ МОДЕЛИРОВАНИЯ СИНТИЦИАЛЬНЫХ СВЯЗЕЙ МЕЖДУ КЛЕТКАМИ IN VITRO | 2010 |
|
RU2433484C1 |
| Способ приготовления препарата живого нейрона беспозвоночного животного | 1980 |
|
SU972311A1 |
| ТРОФИЧЕСКИЕ ФАКТОРЫ ДЛЯ РЕГЕНЕРАЦИИ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ | 1995 |
|
RU2157223C2 |
| СПОСОБ ВОССТАНОВЛЕНИЯ ФУНКЦИЙ СПИННОГО МОЗГА ПРИ МОДЕЛИРОВАНИИ ЕГО ПОЛНОГО АНАТОМИЧЕСКОГО ПЕРЕРЫВА В ОСТРОМ ПЕРИОДЕ В ЭКСПЕРИМЕНТЕ | 2007 |
|
RU2341830C1 |
| МАТРИЦА ДЛЯ КЛЕТОЧНОЙ ТРАНСПЛАНТОЛОГИИ | 2011 |
|
RU2521194C2 |
| Способ определения нейротропной активности веществ | 1979 |
|
SU996910A1 |
| ПЕПТИД, СТИМУЛИРУЮЩИЙ РЕГЕНЕРАЦИЮ НЕЙРОНОВ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ И СПОСОБ ЕЕ ПРИМЕНЕНИЯ | 2006 |
|
RU2301678C1 |
| Способ получения глиальных производных индуцированных плюрипотентных стволовых клеток с повышенной экспрессией BDNF для терапии ишемического инсульта | 2023 |
|
RU2829361C1 |
| ГЕНЕТИЧЕСКИЕ НУКЛЕОТИДНЫЕ ПОСЛЕДОВАТЕЛЬНОСТИ ИСКУССТВЕННО МОДИФИЦИРОВАННОГО GDNF С ДЕЛЕТИРОВАННОЙ pro-ОБЛАСТЬЮ, ПРОДУКТ КОТОРЫХ ОБЛАДАЕТ ПОВЫШЕННЫМИ СВОЙСТВАМИ НЕЙРАЛЬНОГО ИНДУКТОРА И СТИМУЛЯТОРА ОБРАЗОВАНИЯ НЕЙРАЛЬНЫХ ОТРОСТКОВ, ПРИГОДНОГО ДЛЯ ТЕРАПИИ НЕЙРАЛЬНЫХ ТРАВМ, ИШЕМИЧЕСКИХ ИНСУЛЬТОВ И НЕЙРОДЕГЕНЕРАТИВНЫХ ЗАБОЛЕВАНИЙ, ВЕКТОР ЭКСПРЕССИИ, МОДИФИЦИРОВАННЫЙ GDNF | 2014 |
|
RU2595377C2 |
| Способ оценки нейротропной и/или нейротоксической активности веществ и их композиций | 2024 |
|
RU2830897C1 |
Изобретение относится к медицине, а именно к экспериментальной нейрофизиологии, и может быть использовано для моделирования нервной системы, обладающей свойствами реверберации, представляющей собой ганглии, и для способа ее создания. Модель создана из брюшного мозга пиявки путем разрушения соединительнотканных капсул и глиальных оболочек при помощи проназы, при этом клетки и волокна в ганглии связаны между собой посредством щелевых контактов. Для создания модели используют брюшной мозг пиявки, при этом с помощью проназы разрушают соединительнотканные капсулы и глиальные оболочки, оставляя интактными нервные клетки, соединенные между собой, и сохраняя целостность нейрональной сетевой функции нервного ганглия пиявки. Способ обеспечивает создание нейрофизиологической модели нервной системы, обладающей свойствами реверберации, за счет создания биологической модели, выполненной на естественной нервной структуре – модифицированном нервном брюшном ганглии медицинской пиявки, включающей неповрежденные нервные клетки с отростками и плотными щелевыми контактами (электрическими синапсами), связывающими нейроны между собой в единые сети. 2 н.п. ф-лы, 2 ил.
1. Нейрофизиологическая модель нервной системы, обладающей свойствами реверберации, представляющая собой ганглии, отличающаяся тем, что она создана из брюшного мозга пиявки путем разрушения соединительнотканных капсул и глиальных оболочек при помощи проназы, при этом клетки и волокна в ганглии связаны между собой посредством щелевых контактов.
2. Способ создания нейрофизиологической модели нервной системы, обладающей свойствами реверберации, отличающийся тем, что для ее создания используют брюшной мозг пиявки, при этом с помощью проназы разрушают соединительнотканные капсулы и глиальные оболочки, оставляя интактными нервные клетки, соединенные между собой, и сохраняя целостность нейрональной сетевой функции нервного ганглия пиявки.
| MACIUNAS K | |||
| et al | |||
| Reverberation of excitation in neuronal networks interconnected through voltage-gated gap junction channels | |||
| J Gen Physiol | |||
| Токарный резец | 1924 |
|
SU2016A1 |
| US 5386497 A1, 31.01.1995 | |||
| JP 2016513526 A, 16.05.2016 | |||
| ЭЗРОХИ В.Л | |||
| и др | |||
| Реверберация возбуждения в переживающих срезах гиппокампальная формация-энторинальная кора крыс | |||
| Оптическая | |||
Авторы
Даты
2020-06-16—Публикация
2019-02-01—Подача