Изобретение относится к области биотехнологии. Может быть использовано для экспрессии опухоль-ассоциированных антигенов с их последующим включением в эндосому через систему комплекса гистосовместимости МНС II.
Ежегодно в мире от злокачественных новообразований умирает около 7 млн. человек. По данным ВОЗ онкологические заболевания по частоте встречаемости стоят на 2 месте, а в некоторых промышленно развитых регионах - на первом месте. Традиционно до недавнего времени основными методами лечения считались: хирургический, цитотоксическая химиотерапия и лучевая терапия.
Достижения иммунологической науки за последние годы привели к созданию принципиально новых подходов и методов терапии онкологических заболеваний.
Так, уже более 40 лет тому назад было показано, что многие опухоли иммуногенны. Однако цитотоксические Т-лимфоциты не активируются при появлении раковых клеток и их специфических антигенов и не способны секретировать цитокины, которые они секретируют при встрече с чужеродными антигенами. Поэтому одна из стратегий борьбы с опухолями заключается в стимулировании иммунной системы к узнаванию опухолевых клеток.
В частности, были предприняты попытки создания индивидуальных противоопухолевых вакцин (А.Ю. Барышников, Принципы и практика вакцинотерапии рака, Бюллетень СО РАМН, №2(112). 2004, стр. 59-63).
В настоящее время значительное внимание уделяется применению дендритных клеток и препаратов (вакцин) на их основе.
Дендритные клетки являются профессиональными антиген-презентирующими клетками (АПК) и играют ключевую роль в формировании первичного иммунного ответа. Важной особенностью дендритных клеток является их способность захватывать из окружающей среды различные антигены при помощи пино- и эндоцитоза. После поглощения антигена дендритные клетки мигрируют в лимфоидные органы, где презентируют антигенные детерминанты в контексте главного комплекса гистосовместимости (МНС) различным популяциям Т-лимфоцитов. Существует два типа рецепторов главного комплекса гистосовместимости. Рецепторы МНС I экспрессируются во всех ядерных клетках организма, осуществляя механизм распознавания «свой-чужой» и презентируют эндогенные антигены, такие как вирусные или раковые антигены. В данном случае связывание рецептора и антигена происходит в эндоплазматическом ретикулуме. Рецепторы МНС II экспрессируются антигенпрезентирующими клетками и другими типами клеток крови, например В-клетками, и презентируют экзогенные антигены, поглощенные в результате эндоцитоза. В отличие от МНС I, связывание МНС II и антигена происходит в области эндосомы. В случае МНС I презентация чужеродного антигена, например, вирусного пептида, вызывает активацию CD8+ цитотоксических Т-лимфоцитов и приводит к немедленному иммунному ответу. В результате происходит уничтожение зараженной клетки. Презентация чужеродного экзогенного пептида молекулами комплекса МНС II вызывает активацию как CD8+ цитотоксических Т-лимфоцитов, так и активацию CD4+ хэлперных Т-лимфоцитов, что приводит к возникновению механизма «иммунной памяти». Такой механизм характеризуется возникновением популяции В-лимфоцитов, продуцирующих специфические антитела и популяции более специфичных цитотоксических Т-лимфоцитов, нацеленных на чужеродный антиген.
Известен способ индукции высокого уровня CD4+ и CD8+ Т-клеточного ответа и специфических типов цитокинов с целью достижения высокого уровня защиты и терапевтической активности за счет иммуногенных HER2-специфичных конструкций полиэпитопа, содержащих CTL и/или эпитопы Th и оптимизированные последовательности спейсера. Конструкции могут использоваться для продуцирования антигенпредставляющих клеток, например, дендритных клеток (DC), для представления желаемых эпитопов лимфоцитам (заявка ЕА 201290813 (А1), опубл. 2013-04-30).
Известен способ экспрессии полиэпитопных опухоль-ассоциированных антигенов в дендритных клетках, способных стимулировать специфические цитотоксические клетки, основанный на использовании рекомбинантной плазмидной ДНК pCI-UB-POLYEPI, которая содержит 11 эпитопов опухоль-ассоциированных антигенов колоректального рака, имеет размер 6355 п.н. (патент РФ 2507265, опубл. 20.02.2014). Данный источник может быть указан в качестве ближайшего аналога-прототипа.
Задачей изобретения является создание системы, способной включать специфические антигенные детерминанты через систему комплекса МНС II, что позволяет значительно расширить возможности применения дендритных клеток пациента, и тем самым увеличить эффективность противораковой терапии.
Задача решается ДНК конструкцией на основе лентивирусого вектора для экспрессии опухоль-ассоциированных антигенов с последующим их транспортом в эндосому через систему комплекса МНС П.
Предлагаемые плазмидные лентивирусные конструкции включают последовательность инвариантного домена CD74/Ii комплекса МНС II, в качестве лидирующей сигнальной области, присоединенной к целевым полипептидам (антигенам). CD74/Ii выступает в роли сигнальной последовательности, направляющей транспортировку комплекса МНС II в эндосомальный компартмент.
Техническим результатом изобретения является создание универсальной лентивирусной системы, позволяющей транспортировать широкий спектр слитых белков-антигенов в эндосому, где они будут расщеплены и презентированы молекулами комплекса МНС II.
В отличие от случая с комплексом МНС I, МНС II препятствует присоединению эндогенных пептидных молекул в области шероховатого ЭПР (эндоплазматического ретикулума). Также CD74/Ii выступает в роли сигнальной последовательности, направляющей транспортировку комплекса МНС II в эндосомальный компартмент. В эндосоме МНС II претерпевает протеолитическое расщепление, в результате которого происходит отщепление Ii домена и присоединение уже протеолизированных экзогенных пептидов (антигенов). Таким образом, использование последовательности CD74/Ii в качестве лидирующей сигнальной области, присоединенной к целевым полипептидам (антигенам), экспрессированным с плазмидных ДНК или из генома дендритной клетки, позволит транспортировать такие слитые белки в эндосому, где они будут расщеплены и презентированы молекулами комплекса МНС II.
Согласно изобретению экспрессии может подлежать широкий спектр опухоль-ассоциированных антигенов, например: СБА, TGF-PRII (колоректальная карцинома), TAG-72 (карцинома простаты), HPV Е6, Е7 (цервикальная карцинома), BING-4, SSX-2, TRP-1/-2 ( меланома), Cyclin-B1, EphA3, Her2/neu (мульти рак), Ер-САМ (рак груди), простато-специфический антиген (рак простаты), BRCA1/2 (карцинома груди и яичников), MUC1 ( дуктальная карцинома), Ig, ТСЯ(лимфома) и т.п.
Для доставки последовательностей антигенов, слитых с сигнальными последовательностями CD74/Ii цепей, в антигенпрезентирующие дендритные клетки использована методика лентивирусного переноса целевых последовательностей.
Использование лентивирусных векторов имеет несколько значительных преимуществ по сравнению с такими подходами, как трансфекционный перенос плазмидных ДНК или электропорирование клеток ДНК конструкциями:
- лентивирусные векторы способны быстро интегрироваться в геном клетки-мишени, обеспечивая стабильную экспрессию трансгена;
- лентивирусные векторы позволяют клонировать достаточно длинные последовательности ДНК до 10 т.п.о, при этом сохраняют высокий уровень упаковки вирусных частиц и свою трансдукционную способность;
- лентивирусные векторы обладают широким тропизмом за счет внедрения типирующих белков в оболочку вирусных частиц. Данное свойство позволяет значительно увеличить трансдукционную способность вируса для определенного типа клеток, что крайне важно в работе с труднотрансфецируемыми первичными культурами клеток крови;
- лентивирусные векторы позволяют доставить ДНК даже в труднотрансфецируемые, неделящиеся клетки, в том числе, первичные дифференцированные клетки, такие как дендритные клетки и лимфоциты.
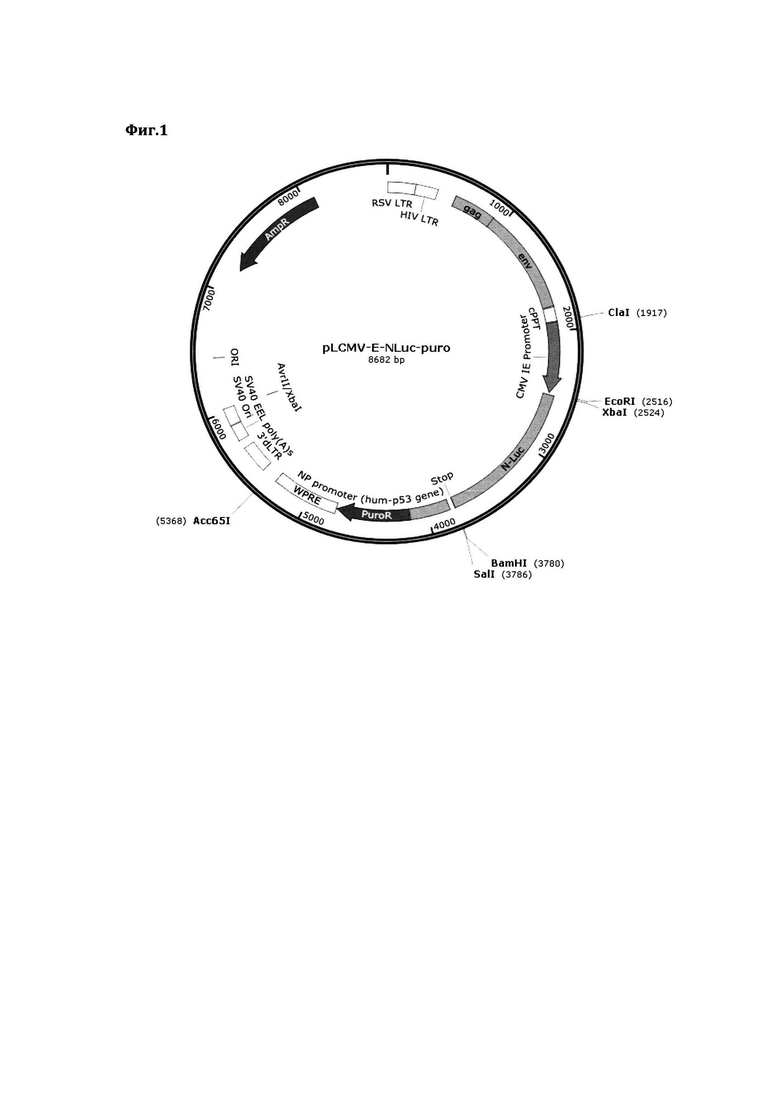
В качестве основного генетического каркаса, формирующего лентивирусную векторную систему использовалась ранее сконструированная нами универсальная плазмидная лентивирусная ДНК конструкция (Фиг. 1). Изображение иллюстрирует схему плазмидной лентивирусной ДНК-конструкции pLA-CMV-ELuc-puro.
В состав данной плазмиды входит ряд ключевых генетических элементов:
- AmpR - последовательность устойчивости к ампициллину, необходимая для амплификации плазмидной ДНК в клетках бактериального штамма E. coli;
- HIV 5' и 3' LTR - длинные концевые повторы ретровирусов (в частности, вируса иммунодефицита человека), обеспечивают встраивание последовательности генома вируса в геном клетки хозяина;
- сРРТ (central polypurine tract) - центральный полипуриновый тракт, способствует встраиванию ДНК вируса в геном митотически неактивных клеток;
- CMV - промотерный регион, обеспечивает стабильный и высокий уровень экспрессии 3' нижележащей последовательности ДНК;
- NLuc - участок N-концевой области люциферазы, на 5' и 3' концах содержит ряд консенсусных участков, распознаваемых ферментами рестрикции-модификации;
- WPRE (Woodchuck hepatitis virus Posttranscriptional Regulatory Element) - энхансерный регион, способствует повышению уровня экспрессии целевых белков.
Презентация опухоль-ассоциированных антигенов, опосредованная молекулами главного комплекса гистосовместимости II, напрямую зависит от эффективного переноса новоэксперссированного антигена в область эндосомального компартмента. В связи с тем, что одним из основных регуляторов транспортировки МНС II в эндосому является белок CD74/Ii, который используют в качестве сигнальной последовательности, направляющей антиген в эндосому. Однако, большая часть последовательности полипептида служит для формирования особой пространственной структуры белка, необходимой для его взаимодействия с молекулой МНС II. За саму транспортировку CD74 отвечает лишь небольшая функциональная область, которая может использоваться отдельно.
Более того, в данный N-концевой домен может входить несколько вариантов еще более коротких последовательностей, отвечающих за перенос CD74/Ii-MHC II. Для определения сигнальной последовательности, приводящей к наилучшей загрузке в МНС II было протестировано несколько вариантов сигнальных пептидов CD74/Ii-рецептора.
Для амплификации была использована серия праймеров (табл). Изображение иллюстрирует последовательности праймеров для амплификации различных сигнальных участков N-концевого домена инвариантной цепи.
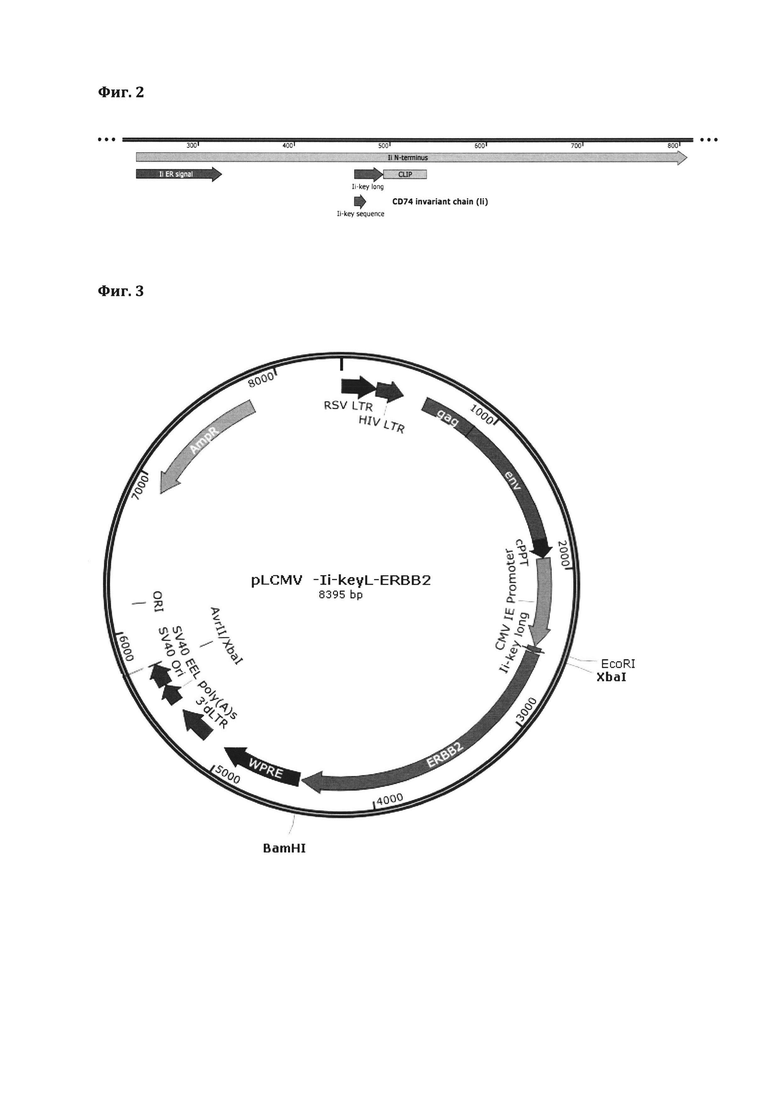
Схема последовательности белка CD74 с отмеченными участками сигнальных пептидов эндосомальной локализации представлена на фиг. 2
В качестве наиболее оптимального варианта отобран удлиненный вариант сигнального участка Ii key (далее в тексте обозначается как "Ii key long"). В качестве опухолевого антигена используют белок ERBB2 (HER2/neu). Рецептор ERBB2 является одним из высокоспецифичных онкологических маркеров, за счет того, что повышенная амплификация и экспрессия данного рецептора характерна для ряда агрессивных типов рака молочной железы и некоторых других видов злокачественных опухолеобразований. Рецептор также ERBB2 является одним из самых больших специфичных опухолевых антигенов, поэтому успешная презентация антигенных детерминант такой молекулы позволит судить об успешности загрузки остальных опухоль-ассоциированных антигенов.
Таким образом, получена лентивирусная ДНК-конструкция, несущая в своем составе последовательность опухоль-ассоциированного антигена ERBB2/HER2 и последовательность сигнального участка гена CD74, обеспечивающего транспорт данного антигена в эндосому (фиг. 3). Изображение иллюстрирует схему лентивирусной плазмидной ДНК конструкции pLA-CMV-Ii-key-long-ERBB2, содержащей последовательность сигнального участка Ii key long. Данная конструкция является одним из предпочтительных, но не ограничивающих изобретение вариантов.
Изобретение иллюстрировано следующим графическим материалом:
Фиг. 1 - Схема плазмидной лентивирусной ДНК-конструкции pLA-CMV-ELuc-puro
Фиг. 2 - Схема последовательности белка CD74 с отмеченными участками сигнальных пептидов эндосомальной локализации
Фиг. 3 - Схема лентивирусной плазмидной ДНК конструкции pLA-CMV-Ii-key-long-ERBB2, содержащей последовательность сигнального участка Ii key long.
Табл. - Последовательности праймеров для амплификации различных сигнальных участков N-концевого домена инвариантной цепи.
SEQ ID№1 CD74 N-концевой участок
Нуклеотидная последовательность
ATGGATGACCAGCGCGACCTTATCTCCAACAATGAGCAACTGCCCATGCTGGGCCGGCGCCCTGGGGCCCCGGAGAGCAAGTGCAGCCGCGGAGCCCTGTACACAGGCTTTTCCATCCTGGTGACTCTGCTCCTCGCTGGCCAGGCCACCACCGCCTACTTCCTGTACCAGCAGCAGGGCCGGCTGGACAAACTGACAGTCACCTCCCAGAACCTGCAGCTGGAGAACCTGCGCATGAAGCTTCCCAAGCCTCCCAAGCCTGTGAGCAAGATGCGCATGGCCACCCCGCTGCTGATGCAGGCGCTGCCCATGGGAGCCCTGCCCCAGGGGCCCATGCAGAATGCCACCAAGTATGGCAACATGACAGAGGACCATGTGATGCACCTGCTCCAGAATGCTGACCCCCTGAAGGTGTACCCGCCACTGAAGGGGAGCTTCCCGGAGAACCTGAGACACCTTAAGAACACCATGGAGACCATAGACTGGAAGGTCTTTGAGAGCTGGATGCACCATTGGCTCCTGTTTGAAATGAGCAGGCACTCCTTGGAGCAAAAGCCCACTGACGCTCCACCG
Аминокислотная последовательность
MDDQRDLISNNEQLPMLGRRPGAPESKCSRGALYTGFSILVTLLLAGQATTAYFLYQQQGRLDKLTVTSQNLQLENLRMKLPKPPKPVSKMRMATPLLMQALPMGALPQGPMQNATKYGNMTEDHVMHLLQNADPLKVYPPLKGSFPENLRHLKNTMETIDWKVFESWMHHWLLFEMSRHSLEQKPTDAPP
SEQ ID №2 Ii-ER сигнальная последовательность
Нуклеотидная последовательность
ATGGATGACCAGCGCGACCTTATCTCCAACAATGAGCAACTGCCCATGCTGGGCCGGCGCCCTGGGGCCCCGGAGAGCAAGTGCAGCCGC
Аминокислотная последовательность
MDDQRDLISNNEQLPMLGRRPGAPESKCSR
SEQ ID №3 Ii key сигнальная последовательность
Нуклеотидная последовательность
CTGCGCATGAAG
Аминокислотная последовательность
LRMK
SEQ ID №4
Ii key long (удлиненная сигнальная последовательность)
Нуклеотидная последовательность
CTGCGCATGAAGCTTCCCAAGCCTCCCAAG
Аминокислотная последовательность
LRMKLPKPPK
SEQ ID №5 CLIP сигнальная последовательность
Нуклеотидная последовательность
CCTGTGAGCAAGATGCGCATGGCCACCCCGCTGCTGATGCAGGCG
Аминокислотная последовательность
PVSKMRMATPLLMQA

| название | год | авторы | номер документа |
|---|---|---|---|
| Полиэпитопная противоопухолевая вакцинная конструкция, содержащая эпитопы опухоль-ассоциированных антигенов, фармацевтическая композиция и ее применение для стимуляции специфического противоопухолевого иммунного ответа | 2016 |
|
RU2684235C2 |
| ПОЛИЭПИТОПНЫЕ ИММУНОГЕННЫЕ ПОЛИПЕПТИДЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2013 |
|
RU2598265C2 |
| Способ получения in vitro популяций активированных антигенспецифических противоопухолевых цитотоксических Т-лимфоцитов, специфичных к эпитопам опухоль-ассоциированного антигена | 2016 |
|
RU2619186C1 |
| ГЕНЕТИЧЕСКАЯ КОНСТРУКЦИЯ ДЛЯ ИНДУКЦИИ ПРОЛИФЕРАЦИИ ПЕРИФЕРИЧЕСКИХ МОНОЦИТОВ IN VITRO | 2017 |
|
RU2697797C2 |
| Биомедицинский клеточный продукт для терапии злокачественных новообразований | 2023 |
|
RU2813531C1 |
| ПРОФИЛАКТИЧЕСКАЯ ПРОТИВОРАКОВАЯ ВАКЦИНА | 2004 |
|
RU2556128C2 |
| Искусственный ген MEL-TCI, кодирующий полиэпитопный белок-иммуноген MEL-TCI, рекомбинантная плазмидная ДНК pMEL-TCI, обеспечивающая экспрессию искусственного гена MEL-TCI и искусственный белок-иммуноген MEL-TCI, содержащий CTL- и Th-эпитопы антигенов меланомы, рестриктированные множественными аллелями HLA I и II класса | 2017 |
|
RU2650872C1 |
| ПРОФИЛАКТИЧЕСКАЯ ПРОТИВОРАКОВАЯ ВАКЦИНА | 2004 |
|
RU2385163C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ПРОТИВООПУХОЛЕВЫМ ЭФФЕКТОМ, И СПОСОБ СНИЖЕНИЯ ИНГИБИРУЮЩЕГО ЭФФЕКТА PD-L1 НА Т-КЛЕТКИ ЧЕЛОВЕКА | 2016 |
|
RU2688692C2 |
| ХИМЕРНЫЕ АНТИГЕННЫЕ РЕЦЕПТОРЫ С МУТИРОВАННЫМИ КОСТИМУЛЯТОРНЫМИ ДОМЕНАМИ CD28 | 2018 |
|
RU2800922C2 |
Настоящее изобретение относится к области иммунологии. Предложена система на основе лентивирусной ДНК-конструкции для стабильной экспрессии опухоль-ассоциированных антигенов с последующим их транспортом в эндосому через систему комплекса MHC II. Данное изобретение может найти дальнейшее применение в стимулировании иммунной системы к узнаванию опухолевых клеток. 2 з.п. ф-лы, 3 ил., 1 табл.
1. Система на основе лентивирусной ДНК-конструкции для стабильной экспрессии опухоль-ассоциированных антигенов с последующим их транспортом в эндосому через систему комплекса МНС II, характеризующаяся тем, что она содержит нуклеотидную последовательность SEQ ID №4, кодирующую инвариантный домен комплекса МНС II CD74/Ii в качестве лидирующей сигнальной области, необходимой для транспорта белка в эндосому, присоединенную к нуклеотидной последовательности, кодирующей целевую полипептидную последовательность опухоль-ассоциированного антигена.
2. Система на основе лентивирусной ДНК-конструкции по п. 1, характеризующаяся тем, что целевой полипептидной последовательностью опухоль-ассоциированного антигена является последовательность опухоль-ассоциированного антигена ERBB2/HER2.
3. Система на основе лентивирусной ДНК-конструкции по п. 1 или 2, характеризующаяся тем, что для амплификации последовательности инвариантного домена комплекса МНС II CD74/Ii используют праймеры, выбранные из:
SEQ ID №6 AGAGAGGAATTCCATGCTGCGCATGAAGC
SEQ ID №7 AGAGAGTCTAGACTTGGGAGGCTTGGGAAGCTTCATG
| ROWE H et al | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Насос | 1917 |
|
SU13A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Приспособление для съемки жилетно-карманным фотографическим аппаратом со штатива | 1921 |
|
SU310A1 |
| RIMAWI M et al | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Приспособление для соединения пучка кисти с трубкою или втулкою, служащей для прикрепления ручки | 1915 |
|
SU66A1 |
| Говорящий кинематограф | 1920 |
|
SU111A1 |
| DATTA MW et | |||
| al | |||
| "Expression of MHC Class | |||
Авторы
Даты
2020-07-02—Публикация
2018-12-28—Подача