Изобретение относится к медицине, а именно к онкологии и эндокринологии.
Выявляемость рака щитовидной железы (РЩЖ) значительно увеличилась за последние три десятилетия. Рост распространенности РЩЖ отмечается во всем мире, во всех возрастных группах, как у мужчин, так и у женщин. Широкое использование ультразвуковых методов диагностики (УЗИ), КТ, МРТ, привело к эпидемии узловой патологии среди населения и, соответственно, к увеличению количества необоснованных оперативных вмешательств. Несмотря на большое количество диагностических методов, используемых в тиреоидологии, ни один из них не может достоверно дифференцировать доброкачественное образование от злокачественного. В настоящее время изучается возможность создания систем стратификации риска, которые наряду с УЗИ могли бы более точно предсказать вероятность онкозаболевания у того или иного пациента и более четко определить показания для инвазивных методов диагностики, что особенно важно для некоторых групп пациентов, таких как беременные женщины, пожилые или ослабленные пациенты. Используемые модели стратификации риска рака щитовидной железы, как правило, основаны исключительно на ультразвуковых характеристиках узловых образований. Основной является система TIRADS и ее модификации: EU-TIRADS (European Thyroid Association Guidelines for Ultrasound Malignancy Risk Stratification of Thyroid Nodules in Adults: The EU-TIRADS. Gilles Russ, Steen J. Bonnema et al. European Thyroid Journal, 6, 5, 2017), ACR-TIRADS (ACR Thyroid Imaging, Reporting and Data System (TI-RADS): White Paper of the ACR TI-RADS Committee, Franklin N. Tessler, William D. iddleton et al. Journal of the American College of Radiology, 14, 5, 5 2017), K-TIRADS (A multicenter prospective validation study for the Korean thyroid imaging reporting and data system in patients with thyroid nodules. Eun Ju Ha, Won Jin Moon et al. Korean Journal of Radiology, 17, 5, 9 2016). Однако к настоящему моменту накоплены данные о других предикторах развития РЩЖ, таких как пол, возраст пациента, уровень ТТГ, семейный анамнез РЩЖ, облучение области голова/шея в анамнезе, наличие инсулинорезистентности (Vigneri R., Malandrino P., Vigneri P. The changing epidemiology of thyroid cancer // Current Opinion in Oncology. 2015. №1 (27). C. 1-7.) На основании этих данных возникла концепция комплексной модели стратификации риска РЩЖ, которая бы включала в себя биохимические, клинические и ультразвуковые предикторы.
Из уровня техники известен способ диагностики опухолей щитовидной железы у больных узловыми образованиями щитовидной железы (патент RU 2407427), согласно которому проводят цитологическое, ультразвуковое и клинико-анамнестическое обследование щитовидной железы и по результатам обследования определяют следующие параметры: ультразвуковые - интранодулярный кровоток в узловом образовании - X1, неровный контур узла - Х2, гипоэхогенность узлового образования - Х3, кальцинаты в узловом образовании - Х4, неоднородность узлового образования - Х5, отсутствие ободка «хало» - Х6, цитологические - папиллярные структуры - Х7, внутриядерные включения - Х8, клинико-анамнестические - быстрый рост узла в щитовидной железе - Х9. При наличии признака ставят значение «1», при его отсутствии - «0». На основании полученных данных рассчитывают значения Y1 и Y2 по заявленным функциям. При этом если значение Y2 больше, чем Y1, устанавливают диагноз опухоли щитовидной железы, если значение Y1 больше Y2 - исключают диагноз опухоли щитовидной железы.
Известен также способ диагностики рака щитовидной железы у больных с дооперационным цитологическим диагнозом «фолликулярная опухоль», представленный в патенте RU 2493770. При этом в качестве диагностических параметров используют следующие: гипоэхогенность узлового образования - X1, неоднородность узлового образования - Х2, отсутствие ободка «хало» - Х3, неровный контур узлового образования - Х4, кальцинаты в узловом образовании - Х5, интранодулярный кровоток в узловом образовании - Х6; определяют клинико-анамнестические параметры: мужской пол - Х7, размер узлового образования больше 2 см - Х8, быстрый рост узла в щитовидной железе ≤1 года - Х9, повышенная плотность узлового образования, определяемая при пальпации, - X10, увеличенные шейные лимфоузлы - X11, тиреотоксикоз - X12, анамнез заболевания ≤1 года - Х13.
Недостатками известных способов являются необходимость проведения инвазивного исследования (ТАБ) для получения цитологических характеристик, отсутствие включения биохимических маркеров, использование субъективных методов диагностики (пальпация), что повышает риск получения ошибочных выводов.
Наиболее близким к предлагаемому решению является способ прогнозирования РЩЖ, основанный на оценке 6 диагностических факторов из числа клинических и лабораторно-инструментальных параметров с применением балльной системы, позволяющей соотнести итоговую сумму баллов с вероятностью наличия РЩЖ (Witczak, J., Taylor, P., Chai, J. et al. Predicting malignancy in thyroid nodules: feasibility of a predictive model integrating clinical, biochemical, and ultrasound characteristics. Thyroid Res 9,4 (2016)). В качестве диагностических факторов используют уровень ТТГ >2,5 мМЕ/л (1 балл), возрастная группа менее 30 лет или более 60 лет (1 балл), наличие микрокальцинатов в узле (2 балла), мужской пол (2 балла), нечеткие контуры узла (2 балла), смешанная эхогенность (1 балл), гипоэхогенность (2 балла). Сумма баллов более 4 высокочувствительна (86,9%), а более 7 высокоспецифична (94,87%) для злокачественных новообразований. В то время как сумма баллов равная или менее 2 свидетельствует о доброкачественности образований.
Данная модель достаточно проста в использовании, не требует введения дополнительных мощностей и расширения лабораторной базы, однако она разработана на популяции в условиях достаточного йодного обеспечения, т.е. не может быть применима у лиц, проживающих в условиях йодного дефицита. Необходимость учитывать обеспечение региона йодом продиктована тем, что отмечается значительная связь между длительным йоддефицитом и фолликулярными, папиллярными и анапластическими гистотипами. Известны многочисленные механизмы, связывающие между собой йодную недостаточность и РЩЖ. Выраженный дефицит йода может вызвать повышение уровня ТТГ, что увеличит пролиферацию тиреоцитов. Также дефицит йода может способствовать ангиогенезу в тканях РЩЖ за счет увеличения экспрессии мРНК VEGF. В опухолевых клетках дефицит йода может также активировать дополнительные сигналы, такие как путь mTOR / p70S6K. Низкий уровень йода может также содействовать развитию РЩЖ, способствуя образованию свободно-радикальных форм кислорода (ROS), опосредованных Н2О2, что может привести к повреждению ДНК и соматическим мутациям.
Технической проблемой, решаемой настоящим изобретением, является создание простого и точного способа определения вероятности наличия РЩЖ у пациентов с узловыми образованиями щитовидной железы с учетом регионов их проживания, характеризующихся степенью йодного обеспечения, т.е. проживающих в условиях, как йодного дефицита, так и в условиях достаточного йодного обеспечения.
Достигаемым техническим результатом является обеспечение возможности получения достоверной и объективной прогнозной оценки наличия РЩЖ (с вероятностью не менее 90%) особенно у пациентов в условиях умеренного йодного дефицита посредством использования комплекса критериев, полученных по итогам лучевых, биохимических и гормональных методов исследования.
Технический результат достигается при реализации способа прогнозирования наличия рака щитовидной железы у пациентов с узловыми образованиями щитовидной железы, включающего проведение исследования узловых образований лучевым методом, биохимическое и гормональное исследование образца сыворотки крови пациента, по результатам исследований оценивают характеристики узловых образований: локализацию, эхогенность, васкуляризацию, наличие микрокальцинатов, уровень ТТГ и триглицеридов, при этом в качестве диагностических признаков используют:
локализацию узлового образования щитовидной железы (А), при этом в случае обнаружении локализации в среднем и нижнем сегментах долей щитовидной железы присваивают 0 баллов, в верхушке доли - 1 балл, в перешейке - 2 балла,
наличие микрокальцинатов (В), при этом при обнаружении микрокальцинатов присваивают 5 баллов, отсутствие микрокальцинтов определяют как 0 баллов,
тип эхогенности узлового образования (С), при этом гиперэхогенному или изоэхогенному узловому образованию присваивают 0 баллов, гипоэхогенному - 2 балла,
тип узлового кровотока (D), при этом периферическому кровотоку присваивают 0 баллов, интранодулярному или смешанному - 2 балла,
уровень тиреотропного гормона ТТГ (Е), при этом при значениях ТТГ меньших 1,17 мМЕ/л, присваивают 0 баллов, при значениях ТТГ больших или равных 1,17 мМЕ/л, присваивают 1 балл,
уровень триглицеридов (F), при этом при значениях триглицеридов меньших 0,94 ммоль/л, присваивают 0 баллов, при значениях триглицеридов больших или равных 0,94 ммоль/л, присваивают 1 балл,
рассчитывают значение R, соответствующее сумме баллов, по формуле: R=A+B+C+D+E+F и в случае рассчитанного значения R<6 делают вывод о низкой вероятности наличия рака щитовидной железы, при R≥6 делают вывод о высокой вероятности наличия рака щитовидной железы.
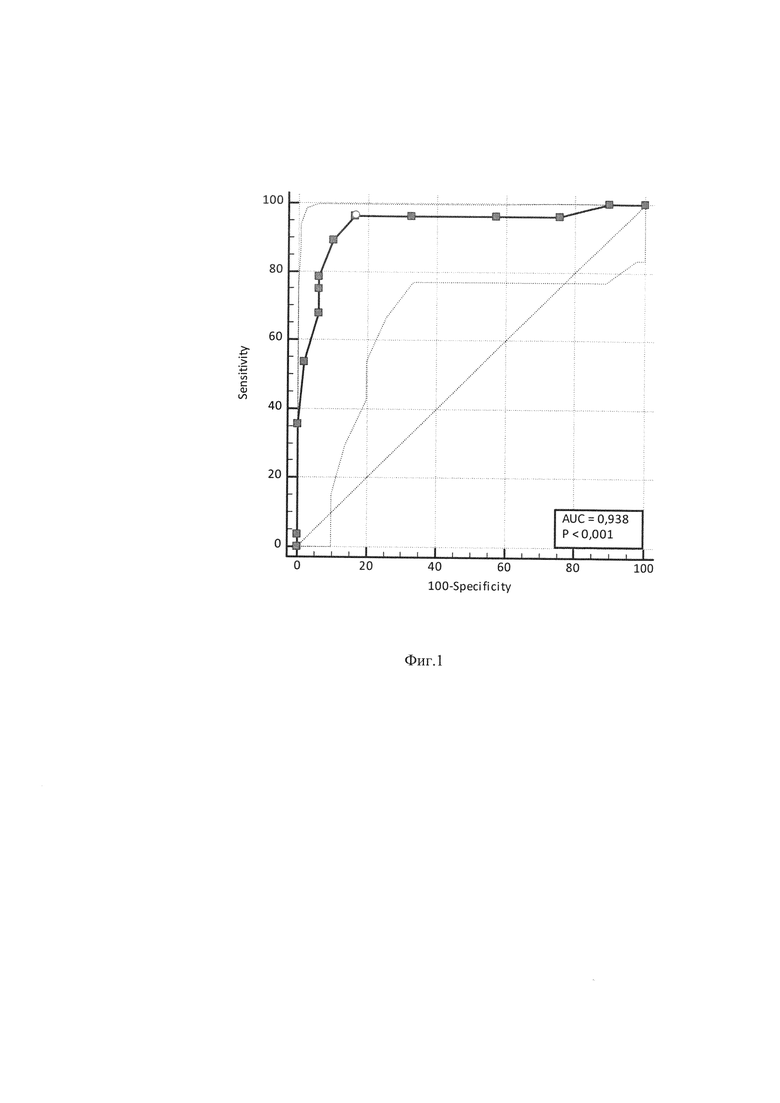
Изобретение поясняется графиками, где на Фиг. 1 представлены ROC-кривые прогнозирования.
При разработке способа прогнозирования на первом этапе было ретроспективно исследовано 89 узловых образований щитовидной железы, проведена оценка результатов клинических, ультразвуковых, лабораторных исследований на основании клинико-морфологического сопоставления (анализ историй болезни и протоколов гистологического исследования послеоперационного материала). На втором этапе с помощью корреляционного анализа выделены наиболее значимые факторы, высоко достоверно ассоциированные с гистологическим типом опухоли, определены вероятные качественные разновидности каждого из этих факторов.
По результатам анализа средний возраст составил 54,52±10,900 лет. По полу пациенты были распределены следующим образом: 66 женщин (74,2%) и 23 мужчины (25,8%). У 2 больных диагностирован (2,2%) фолликулярный рак, у 37 (41,6%) - папиллярный рак, фолликулярная аденома у 16 (18,0%), коллоидный зоб у 34 (38,2%).
Больные, у которых были диагностирован РЩЖ были моложе (50,4±11,789 лет и 57,44±9,270 соответственно, р=0,002), имели более высокий уровень триглицеридов (1,3076±0,68883 ммоль/л и 1,0037±0,52102 ммоль/л, р=0,031), глюкозы (5,5373±0,86527 ммоль/л и 5,4962±0,44485, р=0,003), ЛНП (3,5473±0,88638 и 2,9807±0,99450) и более высокий уровень ТТГ (2,0205±1,04412 и 1,6865±1,19351, р=0,046) по сравнению с больными с доброкачественными образованиями. Среди больных с РЩЖ было больше женщин (40,5% против 14,3% соотв, р=0,008), больных, переносивших облучение (13,5% и 1,9% соотв, р=0,032). По данным УЗИ злокачественные образования чаще локализовались в области верхушки или перешейка щитовидной железы (40,5% против 19,3% соотв, р=0,037), чаще отмечалась гипоэхогенность узла (62,2% против 26,9%, р=0,001), нечеткость контуров узла (25,0% против 6,0%), р=0,012), наличие микрокальцинатов в узле (66,7% против 9,6%, р-0,0001), смешанный узловой кровоток (73,0% и 42,3%, р=0,004).
На последнем этапе работы при помощи метода линейной регрессии построена модель оценки риска наличия рака щитовидной железы у пациентов с узловыми образованиями (Таблица 1). 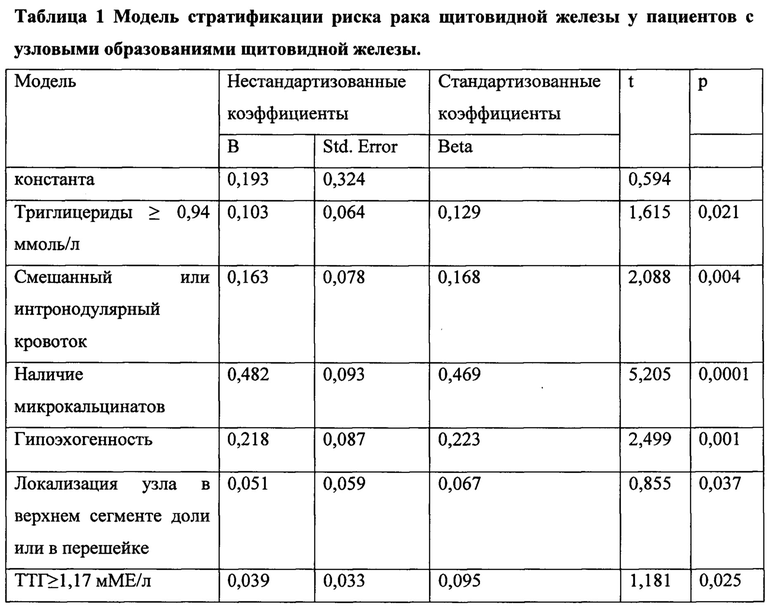
Другие факторы, такие как пол, возраст, ИМТ, нарушение углеводного обмена (сахарный диабет, нарушение толерантности к глюкозе), уровень глюкозы сыворотки крови натощак, уровень общего холестерина, уровень ЛПНП, уровень ЛПВП, размер узлового образования, края и форма узла в регрессионном анализе не показали независимой ассоциации с вероятностью диагностики злокачественного новообразования. На основании проведенных исследований была получена формула для расчета прогноза:
R=A+B+C+D+E+F,
где:
R - риск наличия рака щитовидной железы,
А - локализация узловых образования щитовидной железы (средний и нижний сегменты долей щитовидной железы - 0 баллов, верхушка доли - 1 балл, перешеек -2 балла),
В - наличие микрокальцинатов (есть микрокальцинаты - 5 баллов, нет микрокальцинтов - 0 баллов),
С - эхогенность узла (гиперэхогенный узел - 0 баллов, изоэхогенный узел - 0 баллов, гипоэхогенный узел - 2 балла),
D - узловой кровоток (периферический кровоток - 0 баллов, интронодулярный или смешанный (периферический+интронодулярный) - 2 балла),
Е - уровень тиреотропного гормона (ТТГ) (ТТГ <1,17 мМЕ/л - 0 баллов, ТТГ ≥1,17 мМЕ/л - 1 балл),
F - уровень триглицеридов (триглицериды <0.94 ммоль/л - 0 баллов, триглицериды ≥0.94 ммоль/л -1 балл).
Полученная сумма баллов может быть переведена в вероятность наличия рака щитовидной железы в соответствии со следующей таблицей (Таблица 2).
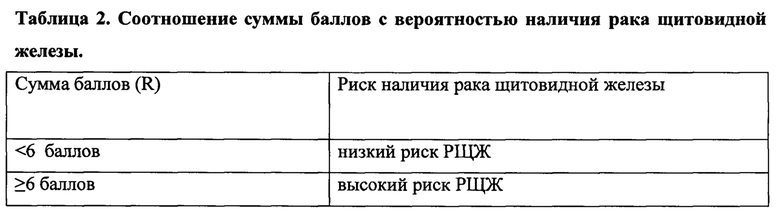
Согласно построенной на основании математической модели ROC-кривой (Фиг. 1), разработанный способ характеризуется хорошей разрешающей способностью (площадь под кривой 0,938): повышение чувствительности (96,43%) сопряжено с сохранением достаточно высокой специфичности (83,67%). Эффективность (однозначность вывода) и надежность (безошибочность вывода) способа также оказались равнозначно высокие - 90% (72 случая из 80).
Практическое применение представленного способа заключается в том, что при обращении к эндокринологу/терапевту проводится обследование больного по представленной ниже схеме; признаки кодируются исходя из их качественных и количественных характеристик по заданному шифру (шифрование выполнено в ходе статистической обработки) (таблица 3). Значимые факторы в кодовом выражении подставляются в разработанную на основании математической модели формулу, по итогам работы с которой получается величина прогноза. 
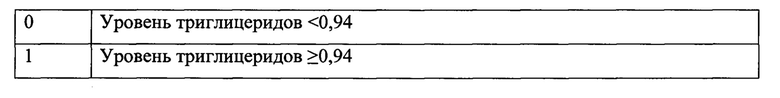
Для удобства каждодневного использования формула для расчета величины прогноза вводится однократно в MicrosoftOfficeExcel. Далее в ячейки вводятся данные. В результате вычисляется значение риска рака щитовидной железы у пациентов с узловыми образованиями щитовидной железы.
Клинический пример №1
Пациентка Т., 58 лет, с многоузловым нетоксическим зобом обратилась к эндокринологу. По результатам обследования выявлено гипоэхогенное образование («2») в области перешейка ЩЖ («2»), с микрокальцинатами («5»), интронодуллярным кровотоком («2»), размерами 14×8×14 мм. При этом уровень ТТГ 2,4 мМЕ/л («1»), триглицериды 1,33 ммоль/л («1»).
Риск наличия рака щитовидной железы для данной пациентки составил: 2+2+5+2+1+1=13.
Вероятность наличия рака щитовидной железы - высокая.
Данный диагноз был подтвержден гистологическими исследованиями тканей щитовидной железы после проведенного хирургического лечения. Полученный результат - гистологически папиллярный рак щитовидной железы с прорастанием капсулы ЩЖ и окружающей подкожно-жировой клетчатки.
Клинический пример №2
Пациент Ш., 38 лет, обратился к эндокринологу. При обследовании впервые выявлено изоэхогенное образование («0») в области перешейка ЩЖ («2»), с внутренним кровотоком («2»), без микрокальцинатов («0»). При этом уровень ТТГ 1,3 мМЕ/л («1»), триглицериды 1,28 ммоль/л («1»).
Риск наличия рака щитовидной железы для данного пациента составил: 0+2+2+0+1+1=6.
Вероятность наличия рака щитовидной железы - высокая.
Данный диагноз был подтвержден гистологическими исследования тканей щитовидной железы после проведенного хирургического лечения. Полученный результат: гистологически папиллярный рак щитовидной железы без капсулы с прорастанием в капсулу щитовидной железы и окружающую подкожно-жировую клетчатку, множественный метастазы в региональные лимфоузлы.
Клинический пример №3
Пациентка Ю., 65 лет, с многоузловым нетоксическим зобом обратилась к эндокринологу по поводу дискомфорта в области шеи. При обследовании выявлено изоэхогенное («0») узловое образование верхнего сегмента («1») левой доли ЩЖ со смешанным кровотоком («2»), без микрокальцинатов («0»), размерами 13×12×11. При этом уровень ТТГ 3,02 мМЕ/л («1»), триглицериды 2,29 ммоль/л («1»).
Риск наличия рака щитовидной железы для данной пациентки составил: 0+1+2+0+1+1=5.
Вероятность наличия рака щитовидной железы - низкая.
Данный диагноз был подтвержден гистологическими исследования тканей щитовидной железы после проведенного хирургического лечения. Полученный результат - фолликулярная аденома.
Таким образом, предлагаемый способ позволяет с вероятностью более 90% сделать безошибочный прогноз (надежность методики) риска наличия рака щитовидной железы у пациента с узловыми образованиями щитовидной железы, тем самым помочь в выборе терапевтической стратегии: наблюдение или оперативное вмешательство. Способ является простым и доступным, так как включает 6 наиболее значимых показателей, и более точным, поскольку разработан при изучении пациентов в условиях умеренного йодного дефицита.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ выбора тактики лечения узловых образований щитовидной железы | 2023 |
|
RU2823767C1 |
| Способ оценки риска наличия рака щитовидной железы у пациентов с синдромом узлового зоба | 2023 |
|
RU2814933C1 |
| Способ определения предрасположенности к развитию рака щитовидной железы | 2023 |
|
RU2812681C1 |
| Способ дифференциальной диагностики новообразований щитовидной железы | 2019 |
|
RU2705110C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ВЕРОЯТНОСТИ ЗЛОКАЧЕСТВЕННОСТИ УЗЛА ЩИТОВИДНОЙ ЖЕЛЕЗЫ | 2018 |
|
RU2706948C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПОКАЗАНИЙ К ИНВАЗИВНЫМ ИССЛЕДОВАНИЯМ ПРИ УЗЛОВЫХ ОБРАЗОВАНИЯХ ЩИТОВИДНОЙ ЖЕЛЕЗЫ | 2010 |
|
RU2432903C1 |
| Способ комплексной дооперационной дифференциальной диагностики доброкачественных и злокачественных узловых образований щитовидной железы | 2022 |
|
RU2805941C1 |
| Способ дооперационной дифференциальной диагностики доброкачественных и злокачественных узловых образований щитовидной железы | 2021 |
|
RU2783304C1 |
| СПОСОБ ИНТРАОПЕРАЦИОННОЙ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ УЗЛОВЫХ ЗАБОЛЕВАНИЙ ЩИТОВИДНОЙ ЖЕЛЕЗЫ | 2005 |
|
RU2299687C1 |
| Способ дооперационного определения объема хирургического лечения высокодифференцированного рака щитовидной железы | 2018 |
|
RU2709140C1 |
Изобретение относится к медицине, а именно к онкологии и эндокринологии и может быть использовано для оценки риска наличия рака щитовидной железы (РЩЖ) у пациентов с узловыми образованиями щитовидной железы. Проводят исследования узловых образований лучевым методом. Биохимическое и гормональное исследование образца сыворотки крови пациента. По результатам исследований определяют диагностические признаки, в качестве которых используют: локализацию узлового образования щитовидной железы, наличие микрокальцинатов, тип эхогенности узлового образования, тип узлового кровотока, уровень тиреотропного гормона, уровень триглицеридов. Риск наличия рака щитовидной железы рассчитывают по оригинальной расчетной формуле. Способ обеспечивает получение достоверной и объективной оценки наличия РЩЖ (с вероятностью не менее 90%) особенно у пациентов в условиях умеренного йодного дефицита. 3 табл., 3 пр., 1 ил.
Способ оценки риска наличия рака щитовидной железы у пациента с узловыми образованиями щитовидной железы, включающий проведение исследования узловых образований лучевым методом, проведение биохимического и гормонального исследования образца сыворотки крови пациента, определение по результатам исследований диагностических признаков, в качестве которых используют:
локализацию узлового образования щитовидной железы (А), при этом в случае обнаружения локализации в среднем и нижнем сегментах долей щитовидной железы присваивают 0 баллов, в верхушке доли - 1 балл, в перешейке - 2 балла,
наличие микрокальцинатов (В), при этом при обнаружении микрокальцинатов присваивают 5 баллов, отсутствие микрокальцинтов определяют как 0 баллов,
тип эхогенности узлового образования (С), при этом гиперэхогенному или изоэхогенному узловому образованию присваивают 0 баллов, гипоэхогенному - 2 балла,
тип узлового кровотока (D), при этом периферическому кровотоку присваивают 0 баллов, интранодулярному или смешанному - 2 балла,
уровень тиреотропного гормона ТТГ (Е), при этом при значениях ТТГ меньших 1,17 мМЕ/л, присваивают 0 баллов, при значениях ТТГ больших или равных 1,17 мМЕ/л, присваивают 1 балл,
уровень триглицеридов (F), при этом при значениях триглицеридов меньших 0,94 ммоль/л, присваивают 0 баллов, при значениях триглицеридов больших или равных 0,94 ммоль/л, присваивают 1 балл,
рассчитывают значение R, соответствующее сумме баллов, по формуле: R=A+B+C+D+E+F и в случае рассчитанного значения R<6 делают вывод о низкой вероятности наличия рака щитовидной железы, при R≥6 делают вывод о высокой вероятности наличия рака щитовидной железы.
| Witczak, J | |||
| et al | |||
| Predicting malignancy in thyroid nodules: feasibility of a predictive model integrating clinical, biochemical, and ultrasound characteristics | |||
| Thyroid Res., 2016, 9, p | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЧИСЛА СЛУЧАЕВ РАКА ЩИТОВИДНОЙ ЖЕЛЕЗЫ | 2003 |
|
RU2264168C2 |
| WO 2010061407 A1 03.06.2010 | |||
| Новосад С | |||
| В | |||
| и др | |||
| Современные прогностические модели стратификации риска рака щитовидной железы, | |||
Авторы
Даты
2020-07-03—Публикация
2019-11-22—Подача