Настоящее изобретение относится к определенным конструкциям полиспецифических антител, фармацевтическим композициям, включающим конструкцию, ДНК, кодирующим конструкции, и векторам, включающим их. Настоящее изобретение также распространяется на способ экспрессии конструкций, например, в клетке-хозяине и способы их приготовления в виде фармацевтической композиции. Настоящее изобретение также относится к применению конструкций полиспецифических антител и композиций в лечении.
Существует ряд подходов для создания биспецифических антител, многие из которых основаны на формате, впервые описанном Morrison et al. (Coloma and Morrison 1997, Nat Biotechnol. 15, 159-163), включающем слияние одноцепочечных вариабельных фрагментов (scFv) с целыми антителами, например, IgG, или с Fab-фрагментами антител, Schoonjans et al., 2000, Journal of Immunology, 165, 7050-7057.
В случае Fab-scFv, VH- и VL-домены scFv, используемые в таких биспецифических и триспецифических молекулах, обычно удерживаются вместе с помощью пептидных линкеров. Однако, в случае некоторых комбинаций VH и VL вариабельных доменов, пептидные линкеры не способны придавать scFv достаточную устойчивость, что приводит к «дыханию» вариабельных доменов и беспорядочному межмолекулярному спариванию с вариабельными доменами и, таким образом, тенденции к образованию мультимеров через их одноцепочечную Fv-часть. Это показано на фиг. 1, в контексте биспецифической молекулы.
Авторы настоящего изобретения реконструировали молекулы полиспецифических антител, будучи заинтересованными обеспечить молекулы антител с эквивалентной функциональностью, при одновременной минимизации мультимеризации на стадии экспрессии и/или после очистки. Это способствует увеличению выхода полученного «мономерного» материала и дает молекулы с подходящей стабильностью для применения в лечении после очистки, концентрирования и приготовления лекарственного средства.
Таким образом, в одном аспекте обеспечивается молекула полиспецифического антитела, включающая:
a) полипептидную(ой) цепь(и) формулы (I): VH-СН1-Х-V1; и
b) полипептидную(ой) цепь(и) формулы (II): VL-CL-Y-V2;
или состоящая из a) и b), где:
VН представляет собой вариабельный домен тяжелой цепи;
CH1 представляет собой домен константной области тяжелой цепи, например, ее домен 1;
Х представляет собой связь или линкер;
Y представляет собой связь или линкер;
V1 представляет собой dsFv, sdAb, scFv или dsscFv;
VL представляет собой вариабельный домен легкой цепи;
CL представляет собой домен из константной области легкой цепи, такой как Cкаппа;
V2 представляет собой dsFv, sdAb, scFv или dsscFv;
причем по крайней мере один из V1 или V2 представляет собой dsFv или dsscFv.
Преимущественно, когда молекулы полиспецифических антител настоящего изобретения сводят к минимуму величину агрегации, наблюдаемой после очистки, и максимизируют количество мономера в препаратах конструкции в фармацевтических концентрациях, в том числе сохраняют высокие уровни мономера в течение длительного времени при хранении, например, мономер может присутствовать в виде 50%, 60%, 70% или 75% или больше, например, 80 или 90% или больше, например, 91, 92, 93, 94, 95, 96, 97, 98 или 99% или больше от общего белка.
Подробное описание изобретения
«Полиспецифическое антитело», как здесь используется, относится к молекуле антитела, описанной здесь, которая имеет два или более связывающих доменов, например, два или три связывающих домена.
В одном варианте осуществления конструкция антитела представляет собой триспецифическое антитело.
«Триспецифическое антитело», как здесь используется, относится к молекуле антитела с тремя антигенсвязывающими сайтами, которые могут независимо связывать одинаковые или различные антигены. В одном примере молекула триспецифичного антитела связывается с двумя различными антигенами, т.е. два связывающих сайта связывают один и тот же антиген, а третий связывающий сайт связывает второй, отличный антиген. Предпочтительно, когда три связывающих сайта молекулы триспецифического антитела настоящего изобретения независимо связывают три различных антигена.
В одном варианте осуществления конструкция представляет собой биспецифическое антитело.
«Биспецифическая молекула», как здесь используется, относится к молекуле с двумя антигенсвязывающими сайтами, которые могут связывать одинаковые или различные антигены.
В одном варианте осуществления все домены связывают один и тот же антиген, включая связывание с одним и тем же эпитопом антигена или связывание различных эпитопов антигена.
В одном варианте осуществления имеется три связывающих домена, и каждый из трех связывающих доменов связывает другой (отличный) антиген.
В одном варианте осуществления имеется три связывающих домена, и два связывающих домена связывают один и тот же антиген, включая связывание с одним и тем же эпитопом или различными эпитопами одного и того же антигена, а третий связывающий домен связывает другой (отличный) антиген.
«Антигенсвязывающий сайт», как здесь используется, относится к части молекулы, которая включает пару вариабельных областей, в частности, родственную пару, которые специфически взаимодействуют с антигеном-мишенью.
Связывающие домены, как здесь используются, включают однодоменное антитело, т.е. вариабельную область и антигенсвязывающие сайты.
«Специфически», как здесь используется, предназначен для ссылки на связывающий сайт или связывающий домен, который распознает только антиген, по отношению к которому он является специфическим, или связывающий сайт или связывающий домен, который обладает значительно более высокой аффинностью к антигену, по отношению к которому он является специфическим, по сравнению с аффинностью к антигенам, по отношению к которым он является неспецифическим, например, в 5, 6, 7, 8, 9, 10 раз более высокой аффинностью.
Аффинность может быть определена с помощью стандартного анализа, например, поверхностного плазмонного резонанса, такого как BIAcore.
В одном из вариантов осуществления молекула полиспецифического антитела в соответствии с настоящим изобретением обеспечивается в виде димера тяжелой и легкой цепи: формулы (I) и (II), соответственно, где VН-СН1-часть вместе с VL-CL-частью образуют функциональный Fab- или Fab'-фрагмент.
VН представляет собой вариабельный домен, например, вариабельный домен тяжелой цепи. В одном варианте осуществления VН представляет собой вариабельный домен тяжелой цепи. В одном варианте осуществления VН представляет собой химерный вариабельный домен, то есть он содержит компоненты, происходящие от по крайней мере двух видов, например, человеческую каркасную область и нечеловеческие CDR. В одном варианте осуществления VН является гуманизированным. В одном варианте осуществления VН является человеческим.
VL представляет собой вариабельный домен, например, вариабельный домен легкой цепи. В одном варианте осуществления VL представляет собой вариабельный домен легкой цепи. В одном варианте осуществления VL представляет собой химерный вариабельный домен, то есть он содержит компоненты, происходящие от по крайней мере двух видов, например, человеческую каркасную область и нечеловеческие CDR. В одном варианте осуществления VL является гуманизированным. В одном варианте осуществления VL является человеческим.
Обычно VH и VL вместе образуют антигенсвязывающий домен. В одном варианте осуществления VH и VL образуют пару когнатного распознавания.
«Пара когнатного распознавания», как здесь используется, относится к паре вариабельных доменов из одного антитела, которое было образовано in vivo, т.е. встречающемуся в природе спариванию вариабельных доменов, выделенных из хозяина. Поэтому парой когнатного распознавания является пара VH и VL. В одном примере пара когнатного распознавания связывает антиген в кооперации.
«Вариабельная область», как здесь используется, относится к области в цепи антитела, включающей CDR и каркасную область, в частности подходящую каркасную область.
Вариабельные области для применения в настоящем изобретении будут, как правило, происходить из антитела, которое может быть создано любым способом, известным в данной области техники.
«Происходящий из (от)», относится к тому, что используемая последовательность или последовательность, очень схожая с используемой последовательностью, была получена из исходного генетического материала, такого как легкая или тяжелая цепь антитела.
Термин «очень схожая», как здесь используется, предназначен для ссылки на аминокислотную последовательность, которая по всей ее длине схожа на 95% или больше, например, схожа на 96, 97, 98 или 99%.
Вариабельные области для применения в настоящем изобретении, как описано выше для VH и VL, могут быть из любого подходящего источника и могут быть, например, полностью человеческими или гуманизированными.
В одном варианте осуществления связывающий домен, образованный VH и VL, являются специфическим в отношении первого антигена.
В одном варианте осуществления связывающий домен, образованный V1, являются специфическим в отношении второго антигена.
В одном варианте осуществления связывающий домен, образованный V2, являются специфическим в отношении второго или третьего антигена.
В одном варианте осуществления CH1-домен является встречающимся в природе доменом 1 из тяжелой цепи антитела или его производным.
В одном варианте осуществления СL-фрагмент, в легкой цепи, представляет собой последовательность константной области каппа или последовательность константной области лямбда или ее производное.
Термин «производное встречающегося в природе домена, как здесь используется, предназначен для ссылки на то, когда один, два, три, четыре или пять аминокислот во встречающейся в природе последовательности были заменены или удалены, например, для оптимизации свойств домена, например, в результате устранения нежелательных свойств, но при этом отличительный признак(и) домена сохраняется.
В одном варианте осуществления одна или более встречающихся в природе или сконструированных межцепочечных (т.е. между легкой и тяжелой цепями) дисульфидных связей присутствуют в функциональном Fab- или Fab'-фрагменте.
В одном варианте осуществления «природная» дисульфидная связь присутствует между CH1 и CL в полипептидных цепях формулы (I) и (II).
Когда CL-домен происходит либо из кappa, либо из лямбда, природным положением для образующего связь цистеина является 214 в cKappa и cLambda человека (Kabat numbering 4th edition 1987).
Точное местоположение образующего дисульфидную связь цистеина в CH1 зависит от конкретного домена, используемого фактически. Так, например, в гамма-1 человека природное положение дисульфидной связи находится в положении 233 (Kabat numbering 4th edition 1987). Положение образующего связь цистеина в случае других человеческих изотипов, таких как гамма 2, 3, 4, IgM и IgD, известно, например, положение 127 для человеческого IgM, IgE, IgG2, IgG3, IgG4 и 128 в тяжелой цепи человеческого IgD и IgA2B.
Необязательно дисульфидная связь может быть между VH и VL полипептидов формулы I и II.
В одном варианте осуществления полиспецифическое антитело в соответствии с настоящим изобретением имеет дисульфидную связь в положении, эквивалентном или соответствующем таковому, встречающемуся в природе между CH1 и CL.
В одном варианте осуществления константная область, включающая CH1, и константная область, такая как CL, имеет дисульфидную связь, которая находится во не встречающемся в природе положении. Она может быть создана в молекуле путем введения цистеина(ов) в аминокислотную цепь в требуемом положении или положениях. Эта неприродная дисульфидная связь присутствует в дополнение к или в качестве альтернативы природной дисульфидной связи, присутствующей между CH1 и CL. Цистеин(ы) в природных положениях может быть заменен аминокислотой, такой как серин, которая неспособна к образованию дисульфидного мостика.
Введение сконструированных цистеинов может быть осуществлено с использованием любого способа, известного в данной области техники. Эти способы включают, но без ограничения, мутагенез с использованием ПЦР с перекрывающимися праймерами, сайт-направленный мутагенез или кассетный мутагенез (смотрите, в общем, Sambrook et al., Molecular Cloning, A Laboratory Manual, Cold Spring Harbour Laboratory Press, Cold Spring Harbour, NY, 1989; Ausbel et al., Current Protocols in Molecular Biology, Greene Publishing & Wiley-Interscience, NY, 1993). Наборы для сайт-направленного мутагенеза коммерчески доступны, например, набор для сайт-направленного мутагенеза QuikChange® (Stratagene, La Jolla, CA). Кассетный мутагенез может быть выполнен на основе Wells et al., 1985, Gene, 34:315-323. В качестве альтернативы, мутанты могут быть получены путем общего генного синтеза посредством отжига, лигирования и ПЦР-амплификации и клонирования перекрывающихся олигонуклеотидов.
В одном варианте осуществления дисульфидная связь между CH1 и CL полностью отсутствует, например, образующие межцепочные связи цистеины могут быть заменены другой аминокислотой, такой как серин. Таким образом, в одном варианте осуществления нет межцепочечных дисульфидных связей в функциональном Fab-фрагменте молекулы. В сообщениях, таких как заявка WO2005/003170, включенная сюда посредством ссылки, описывается, как обеспечить Fab-фрагменты без межцепочечной дисульфидной связи.
V1 представляет собой dsFv, sdAb, scFv или dsscFv, например, dsFv, scFv или dsscFv.
V2 представляет собой dsFv, sdAb, scFv или dsscFv, например dsFv, scFv или dsscFv.
В одном варианте и V1, и V2 представляют собой dsscFv.
В одном варианте и V1, и V2 представляют собой dsFv. Когда и V1, и V2 представляют собой dsFv, или VH, или VL вариабельный домен является одинаковым для V1 и V2. В одном варианте осуществления V1 и V2 имеют один и тот же VH вариабельный домен. В другом варианте осуществления V1 и V2 имеют один и тот же VL вариабельный домен. В одном варианте осуществления VH и VL вариабельные домены являются одинаковыми для V1 и V2. Последнее делает возможным сшивание, которое может быть желательным для некоторых целей.
В одном варианте осуществления V1 представляет собой dsFv, а V2 представляет собой scFv. В одном варианте осуществления V1 представляет собой scFv, а V2 представляет собой dsFv. В одном варианте осуществления V1 представляет собой dsscFv, а V2 представляет собой dsFv. В одном варианте осуществления V1 представляет собой dsFv, а V2 представляет собой dsscFv. В одном варианте осуществления V1 представляет собой dsscFv, а V2 представляет собой scFv. В одном варианте осуществления V1 представляет собой scFv, а V2 представляет собой dsscFv. В одном варианте осуществления V1 не представляет собой scFv. В одном варианте осуществления V2 не представляет собой scFv. В одном варианте осуществления ни V1, ни V2 не представляет собой scFv.
Таким образом, в одном аспекте обеспечивается молекула полиспецифического антитела, включающая:
a) полипептидную(ой) цепь(и) формулы (I): VH-СН1-Х-V1; и
b) полипептидную(ой) цепь(и) формулы (II): VL-CL-Y-V2;
или состоящая из a) и b), где:
VН представляет собой вариабельный домен тяжелой цепи;
CH1 представляет собой домен константной области тяжелой цепи, например, ее домен 1;
Х представляет собой связь или линкер;
Y представляет собой связь или линкер;
V1 представляет собой dsFv или dsscFv;
VL представляет собой вариабельный домен легкой цепи;
CL представляет собой домен из константной области, например, домен из константной области легкой цепи, такой как Cкаппа;
V2 представляет собой dsFv или dsscFv.
«Одноцепочечный вариабельный фрагмент» или «scFv», как здесь используется, относится к одноцепочечному вариабельному фрагменту, состоящему из или включающему вариабельный домен тяжелой цепи (VH) и вариабельный домен легкой цепи (VL), который стабилизирован с помощью пептидного линкера между VH и VL вариабельными доменами. Вариабельные домены VH и VL могут быть в любой подходящей ориентации, например, С-конец VH может быть связан с N-концом VL, или С-конец VL может быть связан с N- концом VH.
«Стабилизированный через дисульфидную связь одноцепочечный вариабельный фрагмент» или «dsscFv», как здесь используется, относится к одноцепочечному вариабельному фрагменту, который стабилизирован с помощью пептидного линкера между VH и VL вариабельными доменами, а также включает междоменную дисульфидную связь между VH и VL.
«Стабилизированный через дисульфидную связь вариабельный фрагмент» или «dsFv», как здесь используется, относится к одноцепочечному вариабельному фрагменту, который не включает пептидный линкер между VH и VL вариабельными доменами, а вместо этого стабилизирован через междоменную дисульфидную связь между VH и VL.
«Однодоменное антитело» или «sdAb», как здесь используется, относится к фрагменту антитела, состоящему из одного мономерного вариабельного домена антитела, такого как VH или VL или VHH.
В одном варианте осуществления, когда V1 и/или V2 представляют собой dsFv или dsscFv, дисульфидная связь между вариабельными доменами VH и VL из V1 и/или V2 находится между двумя из остатков, перечисленных ниже (если в контексте не указано иное, нумерация по Kabat используется в приведенном ниже списке). Везде, где делается ссылка на нумерацию по Kabat, соответствующей ссылкой является Kabat et al., 1987, in Sequences of Proteins of Immunological Interest, US Department of Health and Human Services, NIH, USA.
В одном варианте осуществления дисульфидная связь находится в положении, выбираемом из группы, включающей:
• VH37+VL95C, смотрите, например, Protein Science 6, 781-788 Zhu et al (1997);
VH44+VL100, смотрите, например, Biochemistry 33 5451-5459 Reiter et al (1994); или Journal of Biological Chemistry Vol. 269 No. 28 pp.18327-18331 Reiter et al. (1994); или Protein Engineering, vol.10 no.12 pp.1453-1459 Rajagopal et al (1997);
VH44+VL105, смотрите, например, J Biochem. 118, 825-831 Luo et al. (1995);
VH45+VL87, смотрите, например, Protein Science 6, 781-788 Zhu et al. (1997);
VH55+VL101, смотрите, например, FEBS Letters 377 135-139 Young et al. (1995);
VH100+VL50, смотрите, например, Biochemistry 29 1362-1367 Glockshuber et al. (1990);
VH100b+VL49;
VH98+VL46, смотрите, например, Protein Science 6, 781-788 Zhu et al. (1997);
VH101+VL46;
VH105+VL43, смотрите, например, Proc. Natl. Acad. Sci. USA Vol. 90 pp.7538-7542 Brinkmann et al. (1993); или Proteins 19, 35-47 Jung et al. (1994),
VH106+VL57, смотрите, например, FEBS Letters 377 135-139 Young et al. (1995)
и соответствующем ему положении в паре вариабельных областей, расположенной в молекуле.
В одном варианте осуществления дисульфидная связь образуется между положениями VH44 и VL100.
Пары аминокислот, перечисленные выше, находятся в положениях, способствующих замещению цистеинами, так что дисульфидные связи могут быть образованы. Цистеины могут быть сконструированы в этих желаемых положениях с помощью известных методов. В одном варианте осуществления, следовательно, сконструированный цистеин в соответствии с настоящим изобретением относится к месту, где встречающийся в природе остаток в данном положении аминокислоты заменен на остаток цистеина.
Введение сконструированных цистеинов может быть осуществлено с использованием любого способа, известного в данной области техники. Эти способы включают, но без ограничения, мутагенез с использованием ПЦР с перекрывающимися праймерами, сайт-направленный мутагенез или кассетный мутагенез (смотрите, в общем, Sambrook et al., Molecular Cloning, A Laboratory Manual, Cold Spring Harbour Laboratory Press, Cold Spring Harbour, NY, 1989; Ausbel et al., Current Protocols in Molecular Biology, Greene Publishing & Wiley-Interscience, NY, 1993). Наборы для сайт-направленного мутагенеза коммерчески доступны, например, набор для сайт-направленного мутагенеза QuikChange® (Stratagene, La Jolla, CA). Кассетный мутагенез может быть выполнен на основе Wells et al., 1985, Gene, 34:315-323. В качестве альтернативы, мутанты могут быть получены путем общего генного синтеза посредством отжига, лигирования и ПЦР-амплификации и клонирования перекрывающихся олигонуклеотидов.
Соответственно, в одном варианте осуществления, когда V1 и/или V2 представляют собой dsFv или dsscFv, вариабельные домены VH и VL из V1 и/или вариабельные домены VH и VL из V2 могут быть связаны дисульфидной связью между двумя остатками цистеина, причем положение пары остатков цистеина выбирают из группы, состоящей из: VН37 и VL95, VH44 и VL100, VH44 и VL105, VH45 и VL87, VH100 и VL50, VH100b и VL49, VH98 и VL46, VH101 и VL46, VH105 и VL43 и VH106 и VL57.
В одном варианте осуществления, когда V1 и/или V2 представляют собой dsFv или dsscFv, вариабельные домены VH и VL из V1 и/или вариабельные домены VH и VL из V2 могут быть связаны дисульфидной связью между двумя остатками цистеина, одним в VH и одним в VL, которые находятся вне CDR, причем положение пары остатков цистеина выбирают из группы, состоящей из VH37 и VL95, VH44 и VL100, VH44 и VL105, VH45 и VL87, VH100 и VL50, VH98 и VL46, VH105 и VL43 и VH106 и VL57.
В одном варианте осуществления, когда V1 представляет собой dsFv или dsscFv, вариабельные домены VH и VL из V1 связаны дисульфидной связью между двумя сконструированными остатками цистеина, одним в положении VH44 и другим в VL100.
В одном варианте осуществления, когда V2 представляет собой dsFv или dsscFv, вариабельные домены VH и VL из V2 связаны дисульфидной связью между двумя сконструированными остатками цистеина, одним в положении VH44 и другим в VL100.
В одном варианте осуществления, когда V1 представляет собой dsFv, dsscFv или scFv, VH-домен V1 присоединен к X.
В одном варианте осуществления, когда V1 представляет собой dsFv, dsscFv или scFv, VL -домен V1 присоединен к X.
В одном варианте осуществления, когда V2 представляет собой dsFv, dsscFv или scFv, VH-домен V2 присоединен к Y.
В одном варианте осуществления, когда V2 представляет собой dsFv, dsscFv или scFv, VL-домен V2 присоединен к Y.
Специалисту будет понятно, что, когда V1 и/или V2 представляет собой dsFv, полиспецифическое антитело будет включать третий полипептид, кодирующий соответствующий свободный VH- или VL-домен, который не присоединен к X или Y. Когда и V1, и V2 представляют собой dsFv, то «свободный вариабельный домен» (т.е. домен, связанный с помощью дисульфидной связи с оставшейся частью полипептида) будет общим для обеих цепей. Таким образом, в то время как фактический вариабельный домен, слитый или связанный через X или Y с полипептидом, может быть различным в каждой полипептидной цепи, свободные вариабельные домены в паре с ним будут, как правило, идентичны друг другу.
В одном варианте осуществления Х представляет собой связь.
В одном варианте осуществления Y представляет собой связь.
В одном варианте осуществления и X, и Y представляют собой связи.
В одном варианте осуществления Х представляет собой линкер, предпочтительно пептидный линкер, например, подходящий пептид для соединения частей CH1 и V1.
В одном варианте осуществления Y представляет собой линкер, предпочтительно пептидный линкер, например, подходящий пептид для соединения частей CL и V2.
В одном варианте осуществления как X, так и Y являются линкерами. В одном варианте осуществления Х и Y представляют собой пептидные линкеры.
Используемый здесь термин «пептидный линкер» относится к пептиду, состоящему из аминокислот. Ряд подходящих пептидных линкеров будет известен специалисту в данной области техники.
В одном варианте осуществления длина пептидного линкера составляет 50 аминокислот или меньше, например, 20 аминокислот или меньше, например, приблизительно 15 аминокислот, или меньше, например, 9, 10, 11, 12, 13 или 14 аминокислот.
В одном варианте осуществления линкер выбирают из последовательности, представленной в последовательности 1-67.
В одном варианте осуществления линкер выбирают из последовательности, представленной в SEQ ID NO:1 или SEQ ID NO:2.
В одном варианте осуществления Х имеет последовательность SGGGGTGGGGS (SEQ ID NO:1).
В одном варианте осуществления Y имеет последовательность SGGGGTGGGGS (SEQ ID NO:1).
В одном варианте осуществления Х имеет последовательность SGGGGSGGGGS (SEQ ID NO:2). В одном варианте осуществления Y имеет последовательность SGGGGSGGGGS (SEQ ID NO:2).
В одном варианте осуществления Х имеет последовательность, приведенную в SEQ ID NO:1, а Y имеет последовательности, приведенную в SEQ ID NO:2.
В одном варианте осуществления Х имеет последовательность, приведенную в SEQ ID NO:69 или 70. В одном варианте осуществления Y имеет последовательность, приведенную в SEQ ID NO:69 или 70. В одном варианте осуществления Х имеет последовательность, приведенную в SEQ ID NO:69, а Y имеет последовательность, приведенную в SEQ ID NO:70.
Таблица 1. Последовательности шарнирных линкеров
Таблица 2. Последовательности гибких линкеров
(S) является необязательным в последовательностях 14-18.
Примеры жестких линкеров включают пептидные последовательности GAPAPAAPAPA (SEQ ID NO:52), РРРР (SEQ ID NO:53) и PPP.
В одном варианте осуществления пептидный линкер представляет собой связывающий альбумин пептид.
Примеры связывающих альбумин пептидов представлены в WO2007/106120 и включают:
Таблица 3
Преимущественно, когда использование связывающих альбумин пептидов в качестве линкера может увеличить полупериод существования молекулы полиспецифического антитела.
В одном варианте осуществления, когда V1 представляет собой scFv или dsscFv, есть линкер, например, подходящий пептид для соединения вариабельных доменов VH и VL из V1.
В одном варианте осуществления, когда V2 представляет собой scFv или dsscFv, есть линкер, например, подходящий пептид для соединения вариабельных доменов VH и VL из V2.
В одном варианте осуществления длина пептидного линкера в scFv или dsscFv находится в диапазоне приблизительно от 12 до 25 аминокислот, например от 15 до 20 аминокислот.
В одном варианте осуществления, когда V1 представляет собой scFv или dsscFv, линкер, соединяющий вариабельные домены VH и VL из V1, имеет последовательность GGGGSGGGGSGGGGSGGGGS (SEQ ID NO:68).
В одном варианте осуществления, когда V2 представляет собой scFv или dsscFv, линкер, соединяющий вариабельные домены VH и VL из V2, имеет последовательность GGGGSGGGGSGGGGSGGGGS (SEQ ID NO:68).
В одном варианте осуществления, когда V1 представляет собой scFv или dsscFv, линкер, соединяющий вариабельные домены VH и VL из V1, имеет последовательность SGGGGSGGGGSGGGGS (SEQ ID NO:69).
В одном варианте осуществления, когда V2 представляет собой scFv или dsscFv, линкер, соединяющий вариабельные домены VH и VL из V2, имеет последовательность SGGGGSGGGGSGGGGS (SEQ ID NO:69).
В одном варианте осуществления, когда V1 представляет собой scFv или dsscFv, линкер, соединяющий вариабельные домены VH и VL из V1, имеет последовательность SGGGGSGGGGTGGGGS (SEQ ID NO:70).
В одном варианте осуществления, когда V2 представляет собой scFv или dsscFv, линкер, соединяющий вариабельные домены VH и VL из V2, имеет последовательность SGGGGSGGGGTGGGGS SEQ ID NO:70).
Соответственно, в одном аспекте обеспечивается молекула полиспецифического антитела, включающая:
a) полипептидную(ой) цепь(и) формулы (I): VH-СН1-Х-V1; и
b) полипептидную(ой) цепь(и) формулы (II): VL-CL-Y-V2;
или состоящая из a) и b), где:
VН представляет собой вариабельный домен тяжелой цепи;
CH1 представляет собой домен константной области тяжелой цепи, например, ее домен 1;
Х представляет собой связь или линкер;
Y представляет собой связь или линкер;
V1 представляет собой dsFv, sdAb, scFv или dsscFv;
VL представляет собой вариабельный домен легкой цепи;
CL представляет собой домен из константной области легкой цепи, такой как Cкаппа;
V2 представляет собой dsFv, sdAb, scFv или dsscFv;
причем по крайней мере один из V1 или V2 представляет собой dsFv или dsscFv.
Настоящим изобретением также обеспечиваются последовательности, которые схожи на 80%, 90%, 91%, 92%, 93% 94%, 95% 96%, 97%, 98% или 99% с последовательностью, раскрытой здесь.
Используемый здесь термин «идентичность» указывает на то, что в каком-либо конкретном положении в совмещенных последовательностях аминокислотный остаток идентичен между последовательностями.
Используемый здесь термин «сходство» указывает на то, что в каком-либо конкретном положении в совмещенных последовательностях аминокислотный остаток представляет собой таковой схожего типа между последовательностями. Например, лейцин может быть заменен на изолейцин или валин. Другие аминокислоты, которые часто могут быть заменены друг другом, включают, но без ограничения:
- фенилаланин, тирозин и триптофан (аминокислоты, имеющие ароматические боковые цепи);
- лизин, аргинин и гистидин (аминокислоты, имеющие основные боковые цепи);
- аспартат и глутамат (аминокислоты, имеющие кислотные боковые цепи);
- аспарагин и глутамин (аминокислоты, имеющие боковые цепи с амидной группой); а также
- цистеин и метионин (аминокислоты, имеющие серосодержащие боковые цепи).
Степени идентичности и схожести можно легко вычислить (Computational Molecular Biology, Lesk, A.M., ed., Oxford University Press, New York, 1988; Biocomputing. Informatics and Genome Projects, Smith, D.W., ed., Academic Press, New York, 1993; Computer Analysis of Sequence Data, Part 1, Griffin, A.M., and Griffin, H.G., eds., Humana Press, New Jersey, 1994; Sequence Analysis in Molecular Biology, von Heinje, G., Academic Press, 1987, Sequence Analysis Primer, Gribskov, M. and Devereux, J., eds., M Stockton Press, New York, 1991, программное обеспечение BLAST™, доступное от NCBI (Altschul, S.F. et al., 1990, J. Mol. Biol. 215:403-410; Gish, W. & States, D.J. 1993, Nature Genet. 3:266-272. Madden, T.L. et al., 1996, Meth. Enzymol. 266:131-141; Altschul, S.F. et al., 1997, Nucleic Acids Res. 25:3389-3402; Zhang, J. & Madden, T.L. 1997, Genome Res. 7:649-656).
Антитела для применения в конструкциях полиспецифических антител настоящего изобретения могут быть созданы любым подходящим способом, известным в данной области техники.
Антитела, созданные против полипептида-антигена, могут быть получены, когда иммунизации животного необходима, путем введения полипептидов животному, предпочтительно, не являющемуся человеком животному, используя хорошо известные и общепринятые протоколы, смотрите, например, Handbook of Experimental Immunology, D. M. Weir (ed.), Vol 4, Blackwell Scientific Publishers, Oxford, England, 1986). Многие теплокровные животные, такие как кролики, мыши, крысы, овцы, коровы, верблюды или свиньи, могут быть подвергнуты иммунизации. Однако мыши, кролики, свиньи и крысы являются, как правило, наиболее подходящими.
Моноклональные антитела могут быть получены любым способом, известным в данной области, таким как метод получения гибридом (Kohler & Milstein, 1975, Nature, 256:495-497), метод получения триом, метод получения человеческих В-клеточных гибридом (Kozbor et al. 1983, Immunology Today, 4:72) и метод получения EBV-гибридом (Cole et al., Monoclonal Antibodies and Cancer Therapy, pp77-96, Alan R Liss, Inc., 1985).
Антитела могут быть также получены с использованием методов получения антител с использованием одиночных лимфоцитов путем клонировании и экспрессии кДНК вариабельных областей иммуноглобулинов, созданных исходя из одиночных лимфоцитов, отобранных для получения специфических антител с помощью, например, методов, описанных Babcook, J. et al 1996, Proc. Natl. Acad. Sci. USA 93(15):7843-7848l; WO92/02551; WO2004/051268 и WO2004/106377.
Антитела для применения в настоящем изобретении также могут быть получены с использованием различных способов фагового дисплея, которые известны в данной области техники и включают те, которые раскрыты Brinkman и др. (в J. Immunol. Methods, 1995, 182: 41-50), Ames и др. (J. Immunol. Methods, 1995, 184:177-186), Kettleborough и др. (Eur. J. Immunol. 1994, 24:952-958), Persic и др. (Gene, 1997 187:9-18), Burton и др. (Advances in Immunology, 1994, 57:191-280) и WO90/02809; WO91/10737; WO92/01047; WO92/18619; WO93/11236; WO95/15982; WO95/20401; и в патентах США 5698426; 5223409; 5403484; 5580717; 5427908; 5750753; 5821047; 5571698; 5427908; 5516637; 5780225; 5658727; 5733743; 5969108, и WO20011/30305.
В одном варианте осуществления полиспецифические молекулы в соответствии с настоящим изобретением являются гуманизированными.
Термин «гуманизированные» (которые включают CDR-привитые антитела), как здесь используется, относится к молекулам, имеющим один или более определяющих комплементарность участков (CDR) из не являющегося человеком вида и каркасную область из молекулы иммуноглобулина человека (смотрите, например, патент США №5585089; WO91/09967). Следует принять во внимание, что может быть только необходимо перенести определяющие специфичность остатки CDR, а не весь CDR (смотрите, например, Kashmiri et al., 2005, Methods, 36, 25-34). Гуманизированные антитела могут необязательно включать, кроме того, один или более остатков каркасной области, происходящих из не являющегося человеком вида, от которого происходят CDR.
Используемый здесь термин «молекула гуманизированного антитела» относится к молекуле антитела, в которой тяжелая и/или легкая цепь содержит один или более CDR (в том числе, если желательно, один или более модифицированных CDR) из донорного антитела (например, мышиного моноклонального антитела), привитых в каркасную область вариабельной области тяжелой и/или легкой цепи акцепторного антитела (например, антитела человека). Для обзора смотрите Vaughan et al. Nature Biotechnology, 16, 535-539, 1998. В одном варианте осуществления вместо того, чтобы переносить весь CDR, только один или более из определяющих специфичность остатков из любого из CDR, описанных здесь выше, переносят в каркасную область антитела человека (смотрите, например, Kashmiri et al., 2005, Methods, 36, 25-34). В одном варианте осуществления только определяющие специфичность остатки из одного или более CDR, описанных здесь выше, переносят в каркасную область антитела человека. В другом варианте осуществления только определяющие специфичность остатки из каждого из CDR, описанных здесь выше, переносят в каркасную область антитела человека.
В случае прививки CDR или определяющих специфичность остатков, любая соответствующая акцепторная последовательность каркасной области вариабельной области может использоваться с учетом класса/типа донорного антитела, из которого происходят CDR, в том числе каркасные области мыши, примата и человека. Соответственно, гуманизированное антитело в соответствии с настоящим изобретением имеет вариабельный домен, включающий человеческие акцепторные каркасные области, а также один или более CDR, предусмотренных здесь.
Примерами человеческих каркасных областей, которые могут использоваться в настоящем изобретении, являются KOL, NEWM, REI, EU, TUR, TEI, LAY и POM (Kabat et al. выше). Например, KOL и NEWM могут быть использованы для тяжелой цепи, REI может быть использована для легкой цепи, а EU, LAY и POM могут быть использованы как для тяжелой цепи, так и для легкой цепи. В качестве альтернативы, могут быть использованы последовательности зародышевой линии человека; они доступны по адресу: http://www2.mrc-lmb.cam.ac.uk/vbase/list2.php.
В молекуле гуманизированного антитела настоящего изобретения акцепторные тяжелые и легкие цепи не должны обязательно быть получены из одного и того же антитела, и могут, если желательно, включать составные цепи, имеющие каркасные области, происходящие из разных цепей.
Каркасные области не должны иметь точно такую же последовательность, как у акцепторного антитела. Например, необычные остатки могут быть заменены на более часто встречающиеся остатки для этого класса или типа акцепторной цепи. В качестве альтернативы, отобранные остатки в акцепторных каркасных областях могут быть заменены так, чтобы они соответствовали остатку, обнаруживаемому в том же положении в донорном антителе (смотрите Reichmann et al., 1998, Nature, 332, 323-324). Такие замены должны быть сведены к минимуму, необходимому для восстановления аффинности донорного антитела. Протокол отбора остатков в акцепторных каркасных областях, которые, возможно, должны быть заменены, приводится в WO91/09967.
Производные каркасных областей могут содержать 1, 2, 3 или 4 аминокислоты, замененные на альтернативную аминокислоту, например, донорский серин.
Донорскими остатками являются остатки из донорного антитела, т.е. антитела, из которого были первоначально получены CDR. Донорские остатки могут быть заменены соответствующим остатком, происходящим из человеческой рецепторной каркасной области (акцепторных остатков).
В одном варианте осуществления полиспецифические антитела настоящего изобретения являются полностью человеческими, в частности, один или более из вариабельных доменов являются полностью человеческими.
Полностью человеческими молекулами являются те, в которых все вариабельные области и константные области (если присутствует) как тяжелой, так и легкой цепей имеют человеческое происхождение, или по существу идентичны последовательностям человеческого происхождения, необязательно из одного и того же антитела. Примеры полностью человеческих антител могут включать антитела, продуцированные, например, с помощью способов фагового дисплея, описанных выше, и антитела, продуцируемые мышами, у которых гены вариабельных областей и, необязательно, константных областей иммуноглобулинов мыши были заменены их человеческими аналогами, например, как описано в общих чертах в EP0546073 патенте США №5545806, патенте США №5569825, патенте США №5625126, патенте США №5633425, патенте США №5661016, патенте США №5770429, EP0438474 и EP0463151.
В одном варианте осуществления молекулы полиспецифических антител настоящего изобретения способны селективно связывать два, три или более различных антигенов, представляющих интерес.
В одном варианте осуществления представляющие интерес антигены, связываемые антигенсвязывающим доменом, образованным VH/VL, или V1 или V2, независимо выбирают из клеточно-ассоциированного белка, например, белка клеточной поверхности на таких клетках, как бактериальные клетки, дрожжевые клетки, Т-клетки, В-клетки, эндотелиальные клетки или опухолевые клетки, а также растворимый белок.
Представляющими интерес антигенами также могут быть любые имеющие отношение к медицине белки, такие как те белки, экспрессия который увеличивается во время болезни или инфекции, например, рецепторы и/или их соответствующие лиганды. Конкретные примеры антигенов включают рецепторы клеточной поверхности, такие как Т-клеточные или В-клеточные, передающие сигналы рецепторы, костимулирующие молекулы, ингибиторы контрольной точки клеточного цикла, рецепторы клеток-природных киллеров, рецепторы иммуноглобулинов, рецепторы семейства TNFR, рецепторы семейства B7, адгезивные молекулы, интегрины, рецепторы цитокиов/хемокинов, GPCR, рецепторов факторов роста, рецепторы, киназы, тканеспецифические антигены, раковые антигены, распознающие патогены рецепторы, рецепторы комплемента, рецепторы гормонов или растворимые молекулы, такие как цитокины, хемокины, лейкотриены, факторы роста, гормоны или ферменты или ионные каналы, эпитопы, фрагменты и их посттрансляционно модифицированные формы.
В одном варианте осуществления молекула полиспецифического антитела настоящего изобретения может использоваться для функционального изменения активности антигена(ов), представляющего интерес. Например, слитый с антителом белок может нейтрализовать активность указанного антигена, породить антагонизм или агонизм в ее отношении, прямо или косвенно.
В одном варианте осуществления V1 и V2 являются специфическими в отношении одного и того же антигена, например, связываются с его одним и тем же или отличным эпитопом. В одном варианте осуществления V1 является специфическим в отношении человеческого сывороточного альбумина. В одном варианте осуществления V2 является специфическим в отношении человеческого сывороточного альбумина. В одном варианте осуществления V1 и V2 являются специфическими в отношении двух различных антигенов.
В одном варианте осуществления V1 и V2 являются специфическими в отношении одинаковых антигенов, например, одинаковых или различных эпитопов одного и того же антигена.
В одном варианте осуществления представляющий интерес антиген, связываемый VH/VL, или V1 или V2, обеспечивает возможность мобилизации эффекторных функций, таких как активация пути активации системы комплемента и/или рекрутмент эффекторных клеток.
Мобилизация эффекторной функции может быть прямой в том плане, что эффекторная функция связана с клеткой, несущий молекула рекрута на своей поверхности. Непрямая мобилизация может происходить, когда связывание антигена с антигенсвязывающим доменом (например, V1 или V2) в молекуле в соответствии с настоящим изобретением с рекрутом-полипептидом вызывает высвобождение, например, фактора, который, в свою очередь, может прямо или косвенно мобилизовать эффекторную функцию, или может происходить через активацию сигнального пути. Примеры включают IL2, IL6, IL8, IFNγ, гистамин, C1q, опсонин и другие члены классического и альтернативного каскадов активации комплемента, такие как C2, C4, C3-конвертаза и С5-С9.
Используемый здесь термин «рекрут-полипептид» включает FcγR, такой как FcγRI, FcγRII и FcγRIII, белок пути активации комплемента, такой как, но без ограничения, C1q и C3, белок CD-маркер (маркер кластера дифференцировки) или его фрагмент, который сохраняет способность к мобилизации клеточно-опосредованной эффекторной функции либо непосредственно, либо косвенно. Рекрут-полипептид также включает молекулы иммуноглобулина, такие как IgG1, IgG2, IgG3, IgG4, IgE и IgA, которые обладают эффекторной функцией.
В одном варианте осуществления антигенсвязывающий домен (например, V1 или V2 или VH/VL) в молекуле полиспецифического антитела в соответствии с настоящим изобретением обладает специфичностью в отношении белка пути активации комплемента, при этом C1q является особенно предпочтительным.
Кроме того, молекулы полиспецифических антител настоящего изобретения могут быть использованы для образования хелатных комплексов с радионуклидами благодаря однодоменному антителу, которое связывается с белком хелатором нуклидов. Такие слитые белки используются при визуализации или в подходах к терапии, заключающихся в направленной доставке радионуклидов.
В одном варианте осуществления антигенсвязывающий домен в молекуле в соответствии с настоящим изобретением (например, V1 или V2 или VH/VL) обладает специфичностью в отношении белка-носителя в сыворотке крови, циркулирующей молекулы иммуноглобулина, или CD35/CR1, например, для обеспечения удлиненного полупериода существования фрагменту антитела со специфичность в отношении указанного представляющего интерес антигена путем связывания с указанным белком-носителем в сыворотке крови, циркулирующей молекулой иммуноглобулина или CD35/CR1.
Используемый здесь термин «белки-носители в сыворотке крови» включают тироксин-связывающий белок, транстиретин, α1-кислый гликопротеин, трансферрин, фибриноген и альбумин, или фрагмент любого из них.
Используемый здесь термин «циркулирующая молекула иммуноглобулина» включает IgG1, IgG2, IgG3, IgG4, sIgA, IgM и IgD, или фрагмент любого из этих соединений.
CD35/CR1 представляет собой белок, присутствующих на эритроцитах, который имеет полупериод существования, составляющий 36 дней (нормальный диапазон от 28 до 47 дней; Lanaro et al., 1971, Cancer, 28 (3):658-661).
В одном варианте осуществления представляющий интерес антиген, в отношении которого VH/VL обладает специфичностью, представляет собой белок-носитель в сыворотке крови, такой как носитель в сыворотке человека, такой как сывороточный альбумин человека.
В одном варианте осуществления представляющий интерес антиген, в отношении которого V1 обладает специфичностью, представляет собой белок-носитель в сыворотке крови, такой как носитель в сыворотке человека, такой как сывороточный альбумин человека.
В одном варианте осуществления представляющий интерес антиген, в отношении которого V2 обладает специфичностью, представляет собой белок-носитель в сыворотке крови, такой как носитель в сыворотке человека, такой как сывороточный альбумин человека.
В одном варианте осуществления только один из VH/VL, V1 или V2 обладает специфичностью в отношении белка-носителя в сыворотке крови, такого как носитель в сыворотке человека, такой как сывороточный альбумин человека.
В одном варианте осуществления сайт связывания в конструкции настоящего изобретения включает 6 CDR, например, SEQ ID NO:71 для CDRH1, SEQ ID NO:72 для CDRH2, SEQ ID NO:73 для CDRH3, SEQ ID NO:74 для CDRL1, SEQ ID NO:75 для CDRL2 и SEQ ID NO:76 для CDRL3.
В одном варианте осуществления указанные 6 CDR, SEQ ID NO:71-76, находятся в положении VH/VL в конструкциях настоящего изобретения. В одном варианте осуществления указанные 6 CDR, SEQ ID NO:71-76, находятся в положении V1 в конструкциях настоящего изобретения. В одном варианте осуществления указанные 6 CDR, SEQ ID NO:71-76, находятся в положении в положении V2 в конструкциях настоящего изобретения. В одном варианте осуществления указанные 6 CDR, SEQ ID NO:71-76, находятся в положении V1 и V2 в конструкциях настоящего изобретения. В одном варианте осуществления указанные 6 CDR, SEQ ID NO:71-76, находятся в положении VH/VL и V1 в конструкциях настоящего изобретения. В одном варианте осуществления указанные 6 CDR, SEQ ID NO:71-76, находятся в положении VH/VL и V2 в конструкциях настоящего изобретения.
В одном варианте осуществления альбуминсвязывающий сайт в конструкции настоящего изобретения включает вариабельный домен тяжелой цепи, выбираемый из SEQ ID NO:77 и SEQ ID NO:78, и вариабельный домен легкой цепи, выбираемый из SEQ ID NO:79 и SEQ ID NO:80, в частности SEQ ID NO:77 и 79 или SEQ ID NO:78 и 80 для тяжелой цепи и легкой цепи, соответственно. В одном варианте осуществления эти домены находятся в положении VH/VL в конструкциях настоящего изобретения. В одном варианте осуществления эти вариабельные домены находятся в положении V1. В одном варианте осуществления эти вариабельные домены находятся в положении V2. В одном варианте осуществления эти вариабельные домены находятся в положении V1 и V2. В одном варианте осуществления эти вариабельные домены находятся в положении VH/VL и V1 в конструкциях настоящего изобретения. В одном варианте осуществления эти вариабельные домены находятся в положении VH/VL и V2 в конструкциях настоящего изобретения. Когда вариабельные домены находятся в двух местах в конструкциях настоящего изобретения, одна и та пара вариабельных доменов может быть в каждом месте, или могут быть использованы две различные пары вариабельных доменов.
В одном варианте осуществления молекулы полиспецифических антител настоящего изобретения преобразуют для обеспечения увеличенной аффинности к антигену-мишени или антигенам-мишеням. Такие варианты могут быть получены с помощью ряда протоколов по созреванию аффинности, включая мутирование CDR (Yang et al J. Mol. Biol., 254, 392-403, 1995), перетасовку цепей (Marks et al., Bio/Technology, 10, 779-783, 1992), использование мутаторов штаммов E. coli (Low et al., J. Mol. Biol., 250, 359-368, 1996), перетасовку ДНК (Patten et al., Curr. Opin. Biotechnol., 8, 724-733, 1997), фаговый дисплей (Thompson et al., J. Mol. Biol., 256, 77-88, 1996) и ПЦР с имитацией полового размножения (Crameri et al Nature, 391, 288-291, 1998). Vaughan и др. (выше) обсуждают эти способы созревания аффинности.
Увеличенная аффинность, как здесь используется в этом контексте, относится к увеличению по сравнению с исходной молекулы.
Если желательно, конструкция полиспецифического антитела для применения в настоящем изобретении может быть конъюгирована с одной или более эффекторных молекул. Следует принять во внимание, что эффекторная молекула может включать одну эффекторную молекулу или две или более таких молекул, связанных между собой так, чтобы образовать единый компонент, который может быть присоединен к антителам настоящего изобретения. Если желательно получить фрагмент антитела, связанный с эффекторной молекулой, его можно получить с помощью стандартных химических методик или методов рекомбинантных ДНК, в которых фрагмент антитела связывают либо непосредственно, либо с помощью сшивающего агента с эффекторной молекулой. Методы конъюгации таких эффекторных молекул с антителами хорошо известны в данной области (смотрите Hellstrom et al. Controlled Drug Delivery, 2nd Ed., Robinson et al eds., 1987, pp. 623-53; Thorpe et al 1982, Immunol. Rev., 62:119-58 и Dubowchik et al 1999, Pharmacology and Therapeutics, 83, 67-123). Конкретные химические методики включают, например, те, которые описаны в WO93/06231, W092/22583, WO89/00195, WO89/01476 и WO03031581. В качестве альтернативы, если эффекторной молекулой является белок или полипептид, связь может быть достигнута с использованием методов рекомбинантных ДНК, например, как описано в WO86/01533 и EP0392745.
Используемый здесь термин «эффекторная молекула» включает, например, биологически активные белки, например, ферменты, другие антитела или фрагменты антител, синтетические или встречающиеся в природе полимеры, нуклеиновые кислоты и их фрагменты, например, ДНК, РНК и их фрагменты, радионуклиды, в частности, радиойод, радиоизотопы, хелатные металлы, наночастицы и репортерные группы, такие как флуоресцентные соединения или соединения, которые могут быть детектированы с помощью ЯМР или ESR (ЭПР).
Другие эффекторные молекулы могут включать хелатные радионуклиды, такие как 111In и 90Y, Lu177, Bismuth213, Californium252, Iridiuml92 и Tungstenl88/Rheniuml88; или лекарственные средства, такие как, но без ограничения, алкилфосфохолины, ингибиторы топоизомеразы I, таксоиды и сурамин.
Другие эффекторные молекулы включают белки, пептиды и ферменты. Представляющие интерес ферменты включают, но без ограничения, протеолитические ферменты, гидролазы, лиазы, изомеразы, трансферазы. Представляющие интерес белки, полипептиды и пептиды включают, но без ограничения, иммуноглобулины, токсины, такие как абрин, рицин A, экзотоксин синегнойной палочки или дифтерийный токсин, белок, такой как инсулин, α-интерферон, β-интерферон, фактор роста нервов, тромбоцитарный фактор роста или тканевой активатор плазминогена, тромботический агент или антиангиогенный агент, например, ангиостатин или эндостатин, или модификатор биологических реакций, такой как лимфокин, интерлейкин-1 (IL-1), интерлейкин-2 (IL-2), гранулоцитарномакрофагальный колониестимулирующий фактор (GM-CSF), гранулоцитарный колониестимулирующий фактор (G-CSF), фактор роста нервов (NGF) или другой фактор роста и иммуноглобулины.
Другие эффекторные молекулы могут включать детектируемые вещества, применимые, например, в диагностике. Примеры детектируемых веществ включают различные ферменты, простетические группы, флуоресцентные материалы, люминесцентные материалы, биолюминесцентные материалы, радионуклиды, испускающие позитроны металлы (для применения в позитронно-эмиссионной томографии) и ионы нерадиоактивных парамагнитных металлов. Смотрите в общем патент США №4741900 в отношении ионов металлов, которые могут быть конъюгированы с антителами для применения в качестве диагностических средств. Подходящие ферменты включают пероксидазу хрена, щелочную фосфатазу, бета-галактозидазу или ацетилхолинэстеразу; подходящие простетические группы включают стрептавидин, авидин и биотин; подходящие флуоресцентные материалы включают умбеллиферон, флуоресцеин, изотиоцианат флуоресцеин, родамин, дихлортриазиниламин флуоресцеина, дансилхлорид и фикоэритрин; подходящие люминесцентные материалы включают люминол; подходящие биолюминесцентные материалы включают люциферазу, люциферин и экворин; и подходящие радионуклиды включают 125I, 131I, 111In и 99Tc.
В другом варианте осуществления эффекторная молекула может увеличить полупериод существования антитела in vivo, и/или уменьшить иммуногенность антитела, и/или улучшить доставку антитела через эпителиальный барьер к иммунной системе. Примеры подходящих эффекторных молекул этого типа включают полимеры, альбумин, альбуминсвязывающие белки или альбуминсвязывающие соединения, такие как те, которые описаны в WO05/117984.
Если эффекторная молекула представляет собой полимер, он может, в общем, быть синтетическим или встречающимся в природе полимером, например, необязательно замещенным полиалкиленом, полиалкенилом или полиоксиалкиленом с прямой или разветвленной цепью или разветвленным или неразветвленным полисахаридом, например гомо- или гетерополисахаридом.
Конкретные необязательные заместители, которые могут присутствовать в указанных выше синтетических полимерах, включают одну или более гидроксигрупп, метиловых или метоксигрупп.
Конкретные примеры синтетических полимеров включают необязательно замещенный неразветвленный или разветвленный полиэтиленгликоль, полипропиленгликол, поливиниловый спирт или их производные, особенно необязательно замещенный полиэтиленгликоль, например, метоксиполиэтиленгликоль или его производные.
Конкретные встречающиеся в природе полимеры включают лактозу, амилозу, декстран, гликоген или их производные.
Используемый здесь термин «производные» предназначен для включения реакционно-способных производных, например, тиол-селективных реакционно-способных групп, таких как малеимиды и тому подобное. Реакционно-способная группа может быть связана с полимером непосредственно или через сегмент линкера. Следует принять во внимание, что остаток такой группы будет в некоторых случаях образовывать часть продукта в качестве связывающей группы между фрагментом антитела и полимером.
Размером полимера можно варьировать по желанию, но, как правило, он будет, как правило, находиться в диапазоне средних молекулярных масс от 500 Да до 50000 Да, например от 5000 до 40000 Да, например, от 20000 до 40000 Да. Размер полимера может, в частности, быть выбран на основе предполагаемого применения продукта, например, способности к локализации в определенных тканях, таких как опухоли, или к увеличению полупериода существования в кровотоке (для обзора смотрите Chapman, 2002, Advanced Drug Delivery Reviews, 54, 531-545). Так, например, если продукт предназначен для покидания кровотока и проникновения в ткань, например, для применения в лечении опухоли, может быть предпочтительно использовать полимер с небольшой молекулярной массой, например, с молекулярной массой, составляющей приблизительно 5000 Да. Для применений, когда продукт остается в кровотоке, может быть предпочтительно использовать полимер с более высокой молекулярной массой, например, имеющий молекулярную массу в диапазоне от 20000 Да до 40000 Да.
Подходящие полимеры включают полиалкилен, такой как полиэтиленгликоль или особенно метоксиполиэтиленгликоль или его производное, и особенно с молекулярной массой в диапазоне от приблизительно 15000 Да до приблизительно 40000 Да.
В одном варианте осуществления антитела для применения в настоящем изобретении присоединены к компонентам в виде полиэтиленгликоля (ПЭГ). В одном конкретном примере антитело представляет собой фрагмент антитела, и молекулы ПЭГ могут быть присоединены через любую доступную боковую цепь аминокислоты или концевую функциональную группу аминокислоты, находящуюся во фрагменте антитела, например, любую свободную амино-, иминогруппу, тиольную, гидроксильную или карбоксильную группу. Такие аминокислоты могут встречаться в природе во фрагменте антитела или могут быть сконструированы во фрагменте, используя методы рекомбинантных ДНК (смотрите, например, патент США №5219996; патент США №5667425; W098/25971, WO2008/038024). В одном варианте осуществления молекула антитела настоящего изобретения представляет собой модифицированный Fab-фрагмент, причем модификация представляет собой добавление к С-концу его тяжелой цепи одной или более аминокислот, чтобы позволить присоединение эффекторной молекулы. Соответственно, когда дополнительные аминокислоты образуют модифицированную шарнирную область, содержащую один или более остатков цистеина, к которым может быть присоединена эффекторная молекула. Несколько сайтов могут быть использованы для присоединения двух или более молекул ПЭГ.
Соответственно, когда молекулы ПЭГ ковалентно связаны через тиольную группу по крайней мере одного остатка цистеина, находящегося во фрагменте антитела. Каждая молекула полимера, присоединенная к модифицированному фрагменту антитела, может быть ковалентно связана с атомом серы остатка цистеина, находящегося во фрагменте. Ковалентная связь будет, как правило, дисульфидной связью или, в частности, связью сера-углерод. Если тиольная группа используется в качестве точки присоединения, соответствующим образом активированные эффекторные молекулы, например тиол-селективные производные, такие как малеимиды и производные цистеина, могут использоваться. Активированный полимер может использоваться в качестве исходного материала при получении фрагментов антител, модифицированных с использованием полимера, как описано выше. Активированный полимер может представлять собой любой полимер, содержащий тиольную реакционно-способную группу, например, α-галогенкарбоновую кислоту или сложный эфир, например, иодацетамид, имид, например, малеимид, винилсульфон или дисульфид. Такие исходные материалы могут быть куплены (например, у Nektar, ранее Shearwater Polymers Inc., Huntsville, AL, США) или могут быть получены из коммерчески доступных исходных материалов, используя обычные химические методики. Конкретные молекулы ПЭГ включают 20K метокси-ПЭГ-амин (получаемый от Nektar, ранее Shearwater; Rapp Polymere и SunBio) и М-PEG-SPA (получаемый от Nektar, ранее Shearwater).
В одном варианте осуществления F(аb')2, Fab или Fab' в молекуле является ПЭГилированным, т.е. содержит ПЭГ (полиэтиленгликоль), ковалентно присоединенный к нему, например, в соответствии со способом, описанным в ЕР0948544 или ЕР1090037 [смотри также "Poly(ethyleneglycol) Chemistry, Biotechnical and Biomedical Applications", 1992, J. Milton Harris (ed), Plenum Press, New York, "Poly(ethyleneglycol) Chemistry and Biological Applications", 1997, J. Milton Harris and S. Zalipsky (eds), American Chemical Society, Washington DC and "Bioconjugation Protein Coupling Techniques for the Biomedical Sciences", 1998, M. Aslam and A. Dent, Grove Publishers, New York; Chapman, A. 2002, Advanced Drug Delivery Reviews 2002, 54:531-545]. В одном варианте осуществления ПЭГ присоединен к цистеину в шарнирной области. В одном примере, ПЭГ-модифицированный Fab-фрагмент содержит малеимидную группу, ковалентно связанную с одной тиольной группой в модифицированной шарнирной области. Остаток лизина может быть ковалентно связан с малеимидной группой, и к каждой из аминных групп в остатке лизина может быть присоединен полимер метоксиполиэтиленгликоль, имеющий молекулярную массу, составляющую приблизительно 20000 Да. Таким образом, общая молекулярная масса ПЭГ, присоединенного к Fab-фрагменту, может составлять приблизительно 40000 Да.
Конкретные молекулы ПЭГ включают 2-[3-(N-малеимидо)пропионамидо]этиламид N,N'-бис(метоксиполи(этиленгликоль) М.м. 20000)-модифицированного лизина, также известный как PEG2MAL40K (который можно получить от Nektar, ранее Shearwater).
Альтернативные источники ПЭГ линкеров включают NOF, которые поставляют GL2-400MA2 (где m в приведенной ниже структуре равно 5) и GL2-400MA (где m равно 2), а n составляет приблизительно 450:
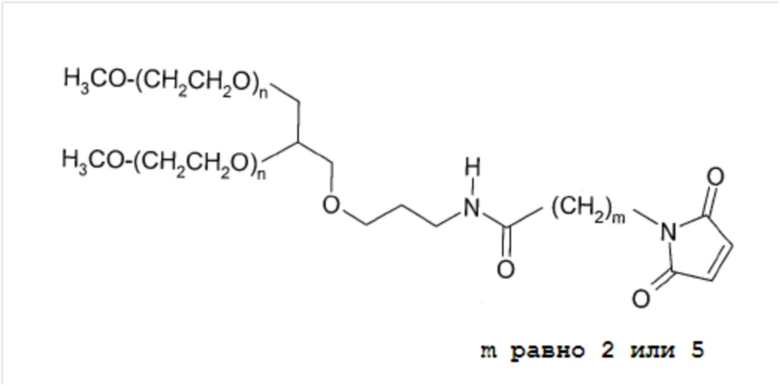
То есть каждый из ПЭГ составляет приблизительно 20000 Да.
Другие альтернативные эффекторные молекулы ПЭГ следующего типа:
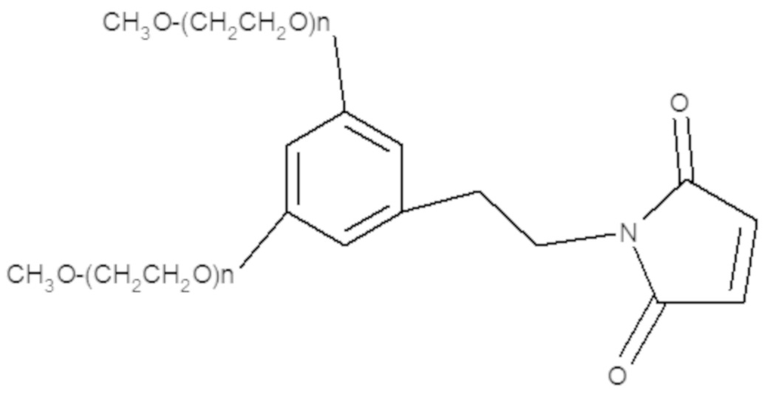
доступны от Dr. Reddy, NOF и Jenkem.
В одном варианте осуществления обеспечивается молекула антитела, которая является ПЭГилированной (например, с использованием описанного здесь ПЭГ) молекулой, присоединенной через остаток аминокислоты цистеина или приблизительно аминокислоты 226 в цепи, например, аминокислоты 226 тяжелой цепи (в соответствии с непрерывной нумерацией).
В одном варианте осуществления обеспечивается полинуклеотидная последовательность, кодирующая молекулу настоящего изобретения, такая как последовательность ДНК.
В одном варианте осуществления обеспечивается полинуклеотидная последовательность, кодирующая один или более, например, два или более, или три или более полипептидных компонентов молекулы настоящего изобретения, например:
a) полипептидную цепь формулы (I): VH-СН1-Х-V1; и
b) полипептидную цепь формулы (II): VL-CL-Y-V2;
где:
VН представляет собой вариабельный домен тяжелой цепи;
CH1 представляет собой домен константной области тяжелой цепи, например, ее домен 1;
Х представляет собой связь или линкер;
Y представляет собой связь или линкер;
V1 представляет собой dsFv, sdAb, scFv или dsscFv;
VL представляет собой вариабельный домен легкой цепи;
CL представляет собой домен из константной области легкой цепи, такой как Cкаппа;
V2 представляет собой dsFv, sdAb, scFv или dsscFv;
причем по крайней мере один из V1 или V2 представляет собой dsFv или dsscFv.
В одном варианте осуществления полинуклеотид, такой как ДНК, включен в вектор.
Специалисту будет понятно, что, когда V1 и/или V2 представляет собой dsFv, полиспецифическое антитело будет включать третий полипептид, кодирующий соответствующий свободный VH- или VL-домен, который не присоединен к X или Y. Соответственно, полиспецифический белок настоящего изобретения может кодироваться одним или более, двумя или более или тремя или более полинуклеотидов, и они могут быть включены в один или более векторов.
Общие методы, с помощью которых могут быть сконструированы векторы, методы трансфекции и способы культивирования хорошо известны специалистам в данной области техники. В связи с этим делается ссылка на ʺCurrent Protocols in Molecular Biologyʺ, 1999, F. M. Ausubel (ed), Wiley Interscience, New York and the Maniatis Manual produced by Cold Spring Harbor Publishing.
Также обеспечивается клетка-хозяин, включающая один или более векторов для клонирования или экспрессионных векторов, включающих одну или более последовательностей ДНК, кодирующих полиспецифической белок настоящего изобретения. Любая подходящая система клетка-хозяин/вектор может быть использована для экспрессии последовательностей ДНК, кодирующих молекулу антитела настоящего изобретения. Бактериальные системы, например E.coli и другие микробные системы, могут использоваться, или экспрессионные системы с использованием эукариотических клеток-хозяев, например клеток млекопитающих, могут быть также использованы. Подходящие клетки млекопитающих-хозяева включают CHO, миеломные клетки, клетки миеломы NSO и клетки SP2, клетки COS или клетки гибридомы.
Настоящим изобретением также обеспечивает способ продукции полиспецифического белка в соответствии с настоящим изобретением, включающий культивирование клетки-хозяина, содержащей вектор настоящего изобретения, в условиях, подходящих для того, чтобы приводить к экспрессии белка с ДНК, кодирующей полиспецифический белок настоящего изобретения, и выделение полиспецифического белка.
Для получения продуктов, включающих как тяжелые, так и легкие цепи, линия клеток может быть трансфецирована двумя векторами, при этом первый вектор кодирует полипептид легкой цепи, а второй вектор кодирует полипептид тяжелой цепи. В качестве альтернативы, один вектор может быть использован, при этом вектор включает последовательности, кодирующие полипептиды легкой цепи и тяжелой цепи. В одном примере линия клеток может быть трансфецирована двумя векторами, каждый из которых кодирует полипептидную цепь молекулы антитела настоящего изобретения. Если V1 и/или V2 представляют собой dsFv, линия клеток может быть трансфецирована тремя векторами, каждый из которых кодирует полипептидную цепь полиспецифического белка настоящего изобретения.
В одном варианте осуществления линию клеток трансфецируют двумя векторами, каждый из которых кодирует отличный полипептид, выбираемый из:
a) полипептидной цепи формулы (I): VH-СН1-Х-V1; и
b) полипептидной цепи формулы (II): VL-CL-Y-V2;
где:
VН представляет собой вариабельный домен тяжелой цепи;
CH1 представляет собой домен константной области тяжелой цепи, например, ее домен 1;
Х представляет собой связь или линкер;
Y представляет собой связь или линкер;
V1 представляет собой dsFv, sdAb, scFv или dsscFv;
VL представляет собой вариабельный домен легкой цепи;
CL представляет собой домен из константной области легкой цепи, такой как Cкаппа;
V2 представляет собой dsFv, sdAb, scFv или dsscFv;
причем по крайней мере один из V1 или V2 представляет собой dsFv или dsscFv.
В одном варианте осуществления, когда V1 представляет собой dsFv, и VH-домен V1 присоединен к X, линия клеток может быть трансфецирована третьим вектором, который кодирует VL-домен V1.
В одном варианте осуществления, когда V1 представляет собой dsFv, и VL-домен V1 присоединен к X, линия клеток может быть трансфецирована третьим вектором, который кодирует VH-домен V1.
В одном варианте осуществления, когда V2 представляет собой dsFv, и VH-домен V2 присоединен к Y, линия клеток может быть трансфецирована третьим вектором, который кодирует VL-домен V2.
В одном варианте осуществления, когда V2 представляет собой dsFv, и VL-домен V2 присоединен к Y, линия клеток может быть трансфецирована третьим вектором, который кодирует VH-домен V2.
В одном варианте осуществления, когда и V1, и V2 представляют собой dsFv, и VL-домен V2 присоединен к Y, и VL-домен V1 присоединен к X, линия клеток может быть трансфецирована третьим вектором, который кодирует общий как для V1, так и для V2 VH-домен.
В одном варианте осуществления, когда и V1, и V2 представляют собой dsFv, и VH-домен V2 присоединен к Y, и VH-домен V1 присоединен к X, линия леток может быть трансфецирована третьим вектором, который кодирует общий как для V1, так и для V2 VH-домен.
Следует иметь в виду, что соотношение каждого вектора, трансфецированного в клетку-хозяина, может быть изменено с целью оптимизации экспрессии продукта в виде полиспецифического антитела. В одном варианте осуществления, когда используются два вектора, соотношение векторов может быть 1:1. В одном варианте осуществления, когда используются три вектора, соотношение векторов может быть 1:1:1. Будет понятно, что специалист может найти оптимальное соотношение путем обычной проверки уровней экспрессии белка после трансфекции. Альтернативно или дополнительно, уровни экспрессии каждой полипептидной цепи полиспецифической конструкции с каждого вектора можно регулировать с помощью одинаковых или отличных промоторов.
Следует иметь в виду, что два или более, или, если присутствуют, три из полипептидных компонентов могут кодироваться полинуклеотидом в одном векторе. Следует также иметь в виду, что, когда два или более, в частности, три или более, из полипептидных компонентов кодируются полинуклеотидом в одном векторе, относительная экспрессия каждого полипептидного компонента может быть изменена путем использования отличных промоторов для каждого полинуклеотида, кодирующего полипептидный компонент настоящего изобретения.
В одном варианте осуществления вектор включает одну полинуклеотидную последовательность, кодирующую два или, если присутствуют, три полипептидных цепи молекулы полиспецифического антитела настоящего изобретения, под контролем одного промотора.
В одном варианте осуществления вектор включает одну полинуклеотидную последовательность, кодирующую два или, если присутствуют, три полипептидных цепи молекулы полиспецифического антитела настоящего изобретения, причем каждая полинуклеотидная последовательность, кодирующая каждую полипептидную цепь, находится под контролем отличного промотора.
Полиспецифические белки в соответствии с настоящим изобретением экспрессируются на хороших уровнях, исходя из клеток-хозяев. Таким образом, свойства антител и/или их фрагментов, по всей видимости, оптимизированы и способствуют коммерческому производству.
Преимущественно, когда молекулы полиспецифических антител настоящего изобретения сводят к минимуму величину агрегации, наблюдаемой после очистки, и максимизируют количество мономера в препаратах конструкции в фармацевтических концентрациях, например, мономер может присутствовать в виде 50%, 60%, 70% или 75% или больше, например, 80 или 90% или больше, например, 91, 92, 93, 94, 95, 96, 97, 98 или 99% или больше от общего белка. В одном примере очищенный образец молекулы полиспецифического антитела настоящего изобретения остается мономерным на более 98% или 99% после 28 дней хранения при 4°С. В одном примере очищенный образец молекулы полиспецифического антитела настоящего изобретения в концентрации 5 мг/мл в фосфатно-солевом буфере (PBS) остается мономерным на более чем 98% после 28 дней хранения при 4°С.
Молекулы антител настоящего изобретения и композиции, включающие их, применимы в лечении, например, в лечении и/или профилактике патологического состояния.
Настоящим изобретением также обеспечивается фармацевтическая или диагностическая композиция, включающая молекулу антитела настоящего изобретения в комбинации с одним или более фармацевтически приемлемых эксципиентов, разбавителей или носителей. Соответственно, предусмотрено применение антитела настоящего изобретения в лечении и для производства лекарственного средства, в частности, по показанию, раскрытому здесь.
Композиция будет обычно поставляться в виде части стерильной фармацевтической композиции, которая будет, как правило, включать фармацевтически приемлемый носитель. Фармацевтическая композиция настоящего изобретения может дополнительно включать фармацевтически приемлемый адъювант.
Настоящим изобретением также обеспечивается способ приготовления фармацевтической или диагностической композиции, включающий добавление и смешивание молекулы антитела настоящего изобретения вместе с одним или более из фармацевтически приемлемого эксципиента, разбавителя или носителя.
Молекула антитела может быть единственным активным ингредиентом в фармацевтической или диагностической композиции или может дополняться другими активными ингредиентами, включая другие являющиеся антителами ингредиенты, например, антитела против IL-1β, Т-клеток, IFNγ или LPS или не являющиеся антителами ингредиенты, такие как ксантины. Другие подходящие активные ингредиенты включают антитела, способные индуцировать толерантность, например, антитела против CD3 или CD4.
В дополнительном варианте осуществления изобретения антитело, фрагмент или композицию в соответствии с настоящим изобретением используют в комбинации с дополнительным фармацевтически активным агентом.
Соответственно, когда фармацевтические композиции содержат терапевтически эффективное количество молекулы антитела настоящего изобретения. Используемый здесь термин «терапевтически эффективное количество» относится к количеству терапевтического средства, необходимому для лечения, ослабления или предотвращения целевого заболевания или состояния, или для достижения детектируемого терапевтического или профилактического эффекта. Для любого антитела, терапевтически эффективное количество может быть оценено первоначально или в анализах на клеточных культурах, или в моделях на животных, как правило, на грызунах, кроликах, собаках, свиньях или приматах. Модель на животном может быть также использована для определения соответствующего диапазона концентраций и пути введения. Такая информация может затем быть использована для определения подходящих доз и путей их введения людям.
Точное терапевтически эффективное количество для являющегося человеком субъекта будет зависеть от тяжести болезненного состояния, общего состояния здоровья субъекта, возраста, веса и пола субъекта, диеты, времени и частоты введения, комбинации(й) лекарственных средств, чувствительности реакции и толерантности/ответа к(на) терапии(ю). Это количество может быть определено с помощью обычного экспериментирования и находится в рамках решения практикующего врача. Как правило, терапевтически эффективное количество будет составлять от 0,01 мг/кг до 50 мг/кг, например, от 0,1 мг/кг до 20 мг/кг. В качестве альтернативы, доза может быть от 1 до 500 мг в день, например, от 10 до 100, 200, 300 или 400 мг в день. Фармацевтические композиции могут быть удобно представлены в виде единичных дозированных форм, содержащих заранее определенное количество активного агента настоящего изобретения.
Композиции могут вводиться пациенту индивидуально или могут вводиться в комбинации (например, одновременно, последовательно или раздельно) с другими агентами, лекарственными средствами или гормонами.
Доза, в которой вводят молекулу антитела настоящего изобретения, зависит от природы состояния, подлежащего лечению, степени присутствующего воспаления и от того, используется ли молекула антитела профилактически или для лечения существующего состояния.
Частота введения дозы будет зависеть от полупериода существования молекулы антитела и продолжительности ее эффекта. Если молекула антитела имеет короткий полупериод существования (например, от 2 до 10 часов), может быть необходимым назначение одной или более доз в день. В качестве альтернативы, если молекула антитела имеет большой полупериод существования (например, от 2 до 15 дней), может быть только необходимым назначение дозы один раз в день, один раз в неделю или даже один раз в 1 или 2 месяца.
Фармацевтически приемлемый носитель не должен сам по себе индуцировать выработку антител, вредных для индивидуума, получающего композицию, и не должен быть токсичным. Подходящими носителями могут быть крупные, медленно метаболизируемые макромолекулы, такие как белки, полипептиды, липосомы, полисахариды, полимолочные кислоты, полигликолевые кислоты, полимерные аминокислоты, сополимеры аминокислот и неактивные вирусные частицы.
Могут использоваться фармацевтически приемлемые соли, например, соли неорганических кислот, такие как гидрохлориды, гидробромиды, фосфаты и сульфаты, или соли органических кислот, такие как ацетаты, пропионаты, малонаты и бензоаты.
Фармацевтически приемлемые носители в терапевтических композициях могут дополнительно содержать жидкости, такие как вода, физиологический раствор, глицерин и этанол. Кроме того, вспомогательные вещества, такие как смачивающие вещества или эмульгаторы или рН-буферные вещества, могут присутствовать в таких композициях. Такие носители позволяют приготовить фармацевтические композиции в виде таблеток, пилюль, драже, капсул, жидкостей, гелей, сиропов, взвесей и суспензий, для приема внутрь пациентом.
Подходящие формы для введения включают формы, подходящие для парентерального введения, например, путем инъекции или инфузии, например, путем болюсной инъекции или непрерывной инфузии. Если продукт предназначен для инъекции или инфузии, он может иметь форму суспензии, раствора или эмульсии в масляном или водном носителе, и он может содержать вспомогательные агенты, такие как суспендирующие агенты, консерванты, стабилизаторы и/или диспергирующие агенты. В качестве альтернативы, молекула антитела может быть в сухой форме, для восстановления перед применением соответствующей стерильной жидкостью.
После приготовления композиции настоящего изобретения можно вводить непосредственно субъекту. Субъектами, подвергаемыми лечению, могут быть животные. Однако в одном или более вариантах осуществления композиции приспособлены для введения являющимся людьми субъектам.
В одном варианте осуществления, в композициях в соответствии с настоящим изобретением, рН конечного препарата не является соответствующим значению изоэлектрической точки антитела или его фрагмента, в результате, если значение рН препарата составляет 7, то pI от 8-9 или выше может быть подходящим. Не желая ограничиваться какой-либо теорией, полагают, что это может, в конечном счете, обеспечить конечный препарат с увеличенной стабильностью, например, антитело или его фрагмент остается в растворе.
Фармацевтические композиции этого изобретения могут быть введены любым рядом путей, включая, но без ограничения, пероральный, внутривенный, внутримышечный, внутриартериальный, интрамедуллярный, интратекальный, внутрижелудочковый, трансдермальный, чрескожный (например, смотрите WO98/20734), подкожный, внутрибрюшинный, интраназальный, энтеральный, местный, сублингвальный, интравагинальный или ректальный пути. Безыгольные шприцы также могут быть использованы для введения фармацевтических композиций настоящего изобретения. Как правило, терапевтические композиции могут быть приготовлены в виде инъецируемых препаратов, в виде или жидких растворов, или суспензий. Твердые формы, подходящие для растворения или суспендирования в жидких носителях перед инъекцией, также могут быть приготовлены. Предпочтительно молекулы антител настоящего изобретения вводят подкожно, путем ингаляции или местно.
Прямая доставка композиций будет обычно выполняться путем инъекции, подкожно, внутрибрюшинно, внутривенно или внутримышечно, или они будут доставлены в интерстициальное пространство ткани. Композиции могут быть также введены в определенную ткань, представляющую интерес. При этом схема лечения может представлять собой схему введения однократной дозы или схему введения многократных доз.
Следует принять во внимание, что активным ингредиентом в композиции будет молекула антитела. Как таковая, она будет подвержена деградации в желудочно-кишечном тракте. Таким образом, если композиция должна вводиться путем с использованием желудочно-кишечного тракта, композиция должна будет содержать агенты, которые защищают антитело от деградации, но которые высвобождают антитело после его всасывания из желудочно-кишечного тракта.
Подробное обсуждение фармацевтически приемлемых носителей доступно в Remington's Pharmaceutical Sciences (Mack Publishing Company, N.J. 1991).
В одном варианте осуществления композиция предоставляется в виде препарата для местного применения, в том числе и ингаляции.
Подходящие ингаляционные препараты включают ингаляционные порошки, дозирующие аэрозоли, содержащие газы-пропелленты, или ингаляционные растворы, не содержащие газы-пропелленты (такие как распыляемые растворы или суспензии). Ингаляционные порошки в соответствии с настоящим изобретением, содержащие активное вещество, могут состоять исключительно из вышеупомянутых активных веществ или смеси вышеупомянутых активных веществ с физиологически приемлемым эксципиентом.
Эти ингаляционные порошки могут включать моносахариды (например, глюкозу или арабинозу), дисахариды (например, лактозу, сахарозу, мальтозу), олиго- и полисахариды (например, декстраны), полиспирты (например, сорбит, маннит, ксилит), соли (например, хлорид натрия, карбонат кальция) или их смеси друг с другом. Соответственно использовать моно- или дисахариды, лактозу или глюкозу, в частности, но не исключительно, в виде их гидратов.
Для частиц для осаждения в легких требуется размер частиц, составляющий менее 10 мкм, например, 1-9 мкм, например от 0,1 до 5 мкм, в частности, от 1 до 5 мкм. Размер частиц активного агента (такого как антитело или фрагмент антитела) имеет первостепенное значение.
Газы-пропелленты, которые могут использоваться для приготовления ингаляционных аэрозолей, известны в данной области техники. Подходящие газы-пропелленты выбирают из числа углеводородов, таких как н-пропан, н-бутан или изобутан, и галогенсодержащих углеводородов, таких как хлорированные и/или фторированные производные метана, этана, пропана, бутана, циклопропана или циклобутана. Вышеупомянутые газы-пропелленты могут использоваться сами по себе или в виде их смесей.
Особенно подходящими газами-пропеллентами являются галогенированные производные алканов, выбираемые из числа TG11, TG12, TG134а и TG227. Из вышеупомянутых галогенированных углеводородов, TG134a (1,1,1,2-тетрафторэтан) и TG227 (1,1,1,2,3,3,3-гептафторпропан) и их смеси являются особенно подходящими.
Содержащие газы-пропелленты ингаляционные аэрозоли могут также содержать другие ингредиенты, такие как сорастворители, стабилизаторы, поверхностно-активные вещества (ПАВ), антиоксиданты, смазочные материалы и средства для доведения рН. Все эти ингредиенты известны в данной области техники.
Содержащие газы-пропелленты ингаляционные аэрозоли в соответствии с настоящим изобретением могут содержать до 5% в весовом отношении активного вещества. Аэрозоли в соответствии с настоящим изобретением содержат, например, от 0,002 до 5% в весовом отношении, от 0,01 до 3% в весовом отношении, от 0,015 до 2% в весовом отношении, от 0,1 до 2% в весовом отношении, от 0,5 до 2% в весовом отношении или от 0,5 до 1% в весовом отношении активного вещества.
В качестве альтернативы местные введения в легкие могут также иметь место при введении жидкого препарата в виде раствора или суспензии, например, используя такое устройство, как небулайзер, например, небулайзер, соединенный с компрессором (например, небулайзер Pari LC-Jet Plus(R), соединенный с компрессором Pari Master(R) производства Pari Respiratory Equipment, Inc., Richmond, Va).
В одном варианте осуществления препарат предоставляется в виде дискретных ампул, содержащих единичную дозу для доставки путем распыления.
В одном варианте осуществления антитело поставляется в лиофилизированной форме, для восстановления, или в качестве альтернативы в виде суспензионной композиции.
Антитело настоящего изобретения может доставляться диспергированным в растворителе, например, в виде раствора или суспензии. Его можно суспендировать в соответствующем физиологическом растворе, например физиологическом солевом растворе, фармакологически приемлемом растворителе или забуференном растворе. Забуференные растворы, известные в данной области техники, могут содержать от 0,05 мг до 0,15 мг динатрия эдетата, от 8,0 мг до 9,0 мг NaCl, от 0,15 мг до 0,25 мг полисорбата, от 0,25 мг до 0,30 мг безводной лимонной кислоты и от 0,45 мг до 0,55 мг цитрата натрия на 1 мл воды с тем, чтобы достичь рН, составляющего приблизительно от 4,0 до 5,0. Как упоминалось выше, суспензию можно приготовить, например, из лиофилизированного антитела.
Терапевтические препараты в виде суспензий или растворов также могут содержать один или более эксципиентов. Эксципиенты хорошо известны в данной области техники и включают буферы (например, цитратный буфер, фосфатный буфер, ацетатный буфер и бикарбонатный буфер), аминокислоты, мочевину, спирты, аскорбиновую кислоту, фосфолипиды, белки (например, сывороточный альбумин), EDTA, хлорид натрия, липосомы, маннит, сорбит и глицерин. Растворы или суспензии могут быть инкапсулированы в липосомы или биоразлагаемые микросферы. Препарат будет, как правило, предоставляться в по существу стерильной форме, используя стерильные процессы производства.
Они могут включать производство и стерилизацию фильтрацией забуференного раствора растворителя, используемого для рецептуры, суспендирование в асептических условиях антитела в стерильном забуференном растворе растворителя и диспергирование препарата в стерильных сосудах способами, хорошо известными специалистам со средним уровнем компетентности в данной области техники.
Распыляемый препарат в соответствии с настоящим изобретением может быть предоставлен, например, в виде упаковок однократной дозы (например, в герметичных пластиковых контейнерах или флаконах), упакованных в конверты из фольги. Каждый флакон содержит стандартную дозу в объеме, например, 2 мл, буферного раствора растворителя.
Антитела настоящего изобретения, как полагают, пригодны для доставки посредством распыления.
Также предполагается, что антитело настоящего изобретения может быть введено с использованием генной терапии. Для достижения этого, последовательности ДНК, кодирующие тяжелую и легкую цепи молекулы антитела, под контролем соответствующих ДНК-компонентов вводят пациенту, так что цепи антитела экспрессируются с ДНК-последовательностей и собираются in situ.
Патологическое состояние или расстройство может, например, быть выбрано из группы, состоящей из инфекций (вирусных, бактериальных, грибковых и паразитарных), эндотоксинового бактериально-токсического шока, связанного с инфекцией, артрита, такого как ревматоидный артрит, астмы, такой как тяжелая астма, хронической обструктивной болезни легких (COPD), воспалительного заболевания органов таза, болезни Альцгеймера, воспалительного заболевания кишечника, болезни Крона, неспецифического язвенного колита, болезни Пейрони, глютеновой болезни, заболевания желчного пузыря, Пилонидальной болезни, перитонита, псориаза, васкулита, хирургических спаек, инсульта, диабета типа I, болезни Лайма, менингоэнцефалита, аутоиммунного увеита, иммунноопосредованных воспалительных заболеваний центральной и периферической нервной системы, таких как рассеянный склероз, волчанка (например, системная красная волчанка) и синдром Гийена-Барра, атопического дерматита, аутоиммунного гепатита, фиброзирующего альвеолита, болезни Грейвса, IgA-нефропатии, идиопатической тромбоцитопенической пурпуры, болезни Меньера, пузырчатки, первичного билиарного цирроза печени, саркоидоза, склеродермии, гранулематоза Вегенера, других аутоиммунных заболеваний, панкреатита, травмы (операции), реакции «трансплантат против хозяина», отторжения трансплантата, заболевания сердца, включая ишемические заболевания, такие как инфаркт миокарда, а также атеросклероза, внутрисосудистого свертывания, резорбции кости, остеопороза, остеоартрита, периодонтита и гипохлогидрии.
Настоящим изобретением также обеспечивается молекула полиспецифического антитела в соответствии с настоящим изобретением для применения в лечении или профилактике боли, особенно боли, связанной с воспалением.
Таким образом, обеспечивается полиспецифическое антитело в соответствии с настоящим изобретением для применения в лечении и способы лечения, используя его.
В одном варианте осуществления обеспечивается способ очистки полиспецифического антитела (в частности, антитела или фрагмента в соответствии с настоящим изобретением).
В одном варианте осуществления обеспечивается способ очистки полиспецифического антитела (в частности, антитела или фрагмента в соответствии с настоящим изобретением), включающий стадии: выполнение анионообменной хроматографии в режиме отсутствия связывания, так что примеси задерживаются на колонке, а антитело сохраняется в несвязанной фракции. Эта стадия может, например, выполняться при рН, составляющем приблизительно 6-8.
Способ может, кроме того, включать начальную стадию захвата, используя катионообменную хроматографию, выполняемую, например, при рН, составляющем приблизительно 4-5.
Способ может, кроме того, включать дополнительную хроматографическую стадию (стадии) для обеспечения продукта, и связанные с эти способом примеси надлежащим образом устраняются из потока продукции.
Способ очистки может также включать одну или более стадий ультрафильтрации, например, стадию концентрирования и диафильтрации.
Используемый выше термин «очищенная форма» предназначен для ссылки на по крайней мере 90% степень чистоты, например, 91, 92, 93, 94, 95, 96, 97, 98, 99% в весовом отношении или более степень чистоты.
Термин «по существу не содержит эндотоксин», как правило, предназначен для ссылки на содержание эндотоксина, составляющее 1 единицу эндотоксина на мг продукта в виде антитела или меньше, например, 0,5 или 0,1 единицы эндотоксина на мг продукта.
Термин «по существу не содержит белок или ДНК клетки-хозяина», как правило, предназначен для ссылки на содержание белка и/или ДНК клетки-хозяина, составляющее 400 мкг на мг продукта в виде антитела или меньше, например 100 мкг на мг или меньше, в частности 20 мкг на мг, в соответствующих случаях.
Молекула антитела настоящего изобретения также может использоваться в диагностике, например в in vivo диагностике и при визуализации болезненных состояний.
В одном варианте осуществления обеспечивается способ отбора конструкции полиспецифического белка в соответствии с настоящим изобретением, включающий:
a) определение выхода мономерного полипецифического белка, когда или V1, или V2 представляет собой dsscFv, для конкретной пары вариабельных областей;
b) определение выхода мономерного полипецифического белка, когда тот из V1 или V2, который был проверен на стадии (а), представляет собой dsFv, для той же самой конкретной пары вариабельных областей; и
c) сравнение выхода мономера, определенного на стадиях (а) и (b), и отбор полиспецифическего белка с наибольшим выхода мономера.
Как правило, «пара вариабельных областей» на стадии (а) и (b) этого способа представляет собой пару VH и VL. Обычно VH и VL вместе образуют антигенсвязывающий домен, V1 или V2. Таким образом, способ позволяет проверить пару VH и VL в виде как dsscFv, так и dsFv в конструкциях настоящего изобретения, и самая мономерная конструкция отбирается на стадии (с).
Как правило, на стадии (а) и (b) этого способа, выход определяется после очистки, например, после аффинной хроматографии. Выход мономера может быть определен, используя любой подходящий способ, такой как гельпроникающая хроматография.
«Включающий (содержащий)» в контексте настоящего описания, как предполагается, означает включающий. Там, где это технически возможно, варианты осуществления настоящего изобретения могут быть объединены. Варианты осуществления описаны здесь как включающие определенные признаки/элементы. Настоящее изобретение также распространяется на отдельные варианты осуществления, состоящие или по существу состоящие из указанных признаков/элементов.
Технические ссылки, такие как патенты и заявки включены, сюда посредством ссылки. Любые варианты осуществления, указанные здесь конкретно и в явной форме, могут стать основой отказа от права, либо отдельно, либо в комбинации с одним или более дополнительными вариантами осуществления.
Настоящее изобретение далее описывается в качестве лишь иллюстрации в следующих примерах, которые отсылают к прилагаемым чертежам, на которых:
Краткое описание чертежей
На фиг. 1 продемонстрированы конструкции Fab-2xdsscFv и Fab-dsscFv-dsFv настоящего изобретения.
На фиг. 2 продемонстрирован анализ с помощью электрофореза в SDS-ПААГ очищенных с использованием белка-G, экспрессированных в HEK293 белков Fab-1xdsscFv, 1xscFv и Fab-2xdsscFv.
На фиг. 3 продемонстрирован анализ с помощью G3000 SE-HPLC очищенных с использованием белка-G, экспрессированных в HEK293 белков Fab-1xdsscFv, 1xscFv и Fab-2xdsscFv.
На фиг. 4 продемонстрирован анализ с помощью электрофореза в SDS-ПААГ очищенных, экспрессированных в HEK293 белков Fab-2xdsscFv#3.
На фиг. 5 продемонстрирован анализ с помощью S200 SE-HPLC очищенных, экспрессированных в HEK293 белков Fab-2xdsscFv#3.
На фиг. 6 продемонстрирован анализ с помощью электрофореза в SDS-ПААГ различных очищенных с использованием белка-G конструкций Fab-dsscFv-dsFv настоящего изобретения. (A) Образцов Fab-dsscFv-dsscFv. (В) Образцов Fab-dsscFv-dsFv.
На фиг. 7 продемонстрирован анализ с помощью G3000 SE-HPLC очищенных с использованием белка-G конструкций Fab-dssFv-dsFv настоящего изобретения.
На фиг. 8 продемонстрирован анализ с помощью электрофореза в SDS-ПААГ различных конструкций в соответствии с настоящим изобретением в восстанавливающих условиях.
На фиг. 9 продемонстрирован анализ с помощью G3000 SE-HPLC зависимости от времени мономерных форматов Fab-1xdsscFv-1xscFv и Fab-2xdsscFv.
На фиг. 10 продемонстрирован анализ с помощью электрофореза в SDS-ПААГ очищенных с использованием белка-G, экспрессированных в EXPiHEK форматов Fab-2xscFv и Fab-2xdsscFv.
ПРИМЕРЫ
Фрагменты антител против антигена 1 обозначены #1.
Фрагменты антител против антигена 2 обозначены #2.
Фрагменты антител против антигена 3 обозначены #3.
Фрагменты антител против антигена 4 обозначены #4.
Пример 1: Fab-2xdsscFv
Конструирование плазмид для экспрессии в клетках млекопитающих
Плазмиды для экспрессии Fab#2-(HC)dsscFv#3,(LC)dsscFv#4 и Fab#2(LC)dsscFv#3,(HC)dsscFv#4 (смотрите фиг. 1) были сконструированы путем слияния scFv#3 и scFv#4 с С-концом константной области каппа человека аллотипа Km3 легкой цепи #2, используя гибкий линкер SGGGGSGGGGS [также упоминаемый здесь как S, 2xG4S] (SEQ ID NO:2), или путем слияния scFv#3 и scFv#4 с С-концом CH1 константной области гамма-1 человека изотипа γ1 тяжелой цепи #2, используя гибкий линкер SGGGGTGGGGS [также упоминаемый здесь как S, G4T, G4S] (SEQ ID NO:1). Кроме того, точечные мутации были введены в ДНК-последовательности в выбранные остатки в каркасной области как VL#3/VL#4, так и VH#3/VH#4. Были введены мутации (в G44C в тяжелой цепи и G10°C легкой цепи) для создания межцепочечной дисульфидной связи между тяжелой и легкой цепями Fv#3. Были введены мутации (в G44C в тяжелой цепи и Q10°C в легкой цепи) для создания межцепочечной дисульфидной связи между тяжелой и легкой цепями Fv#4.
Фрагменты генов, кодирующие scFv#4 и dsscFv#4 (с ориентацией vHvL и vLvH), были получены химически и слиты с Fab#2, как описано выше, для создания:
Плазмиды e1: Light#2-(SGGGGSGGGGS [SEQ ID NO:2])-dsvL#4-(GGGGSGGGGSGGGGSGGGGS [SEQ ID NO:68])-dsvH#4;
Плазмиды e2: Light#2-(SGGGGSGGGGS [SEQ ID NO:2])-vH#4-(GGGGSGGGGSGGGGSGGGGS [SEQ ID NO:68])-vL#4;
Плазмиды f2: Light#2-(SGGGGSGGGGS [SEQ ID NO:2])-dsvH#4-(GGGGSGGGGSGGGGSGGGGS [SEQ ID NO:68])-dsvL#4;
Плазмиды g1: Heavy#2-(SGGGGTGGGGS [SEQ ID NO:1])-vL#4-(GGGGSGGGGSGGGGSGGGGS [SEQ ID NO:68])-vH#4;
Плазмиды h1: Heavy#2-(SGGGGTGGGGS [SEQ ID NO:1])-dsvL#4-(GGGGSGGGGSGGGGSGGGGS [SEQ ID NO:68])-dsvH#4;
Плазмиды g2: Heavy#2-(SGGGGTGGGGS [SEQ ID NO:1])-vH#4-(GGGGSGGGGSGGGGSGGGGS [SEQ ID NO:68])-vL#4; и
Плазмиды h2: Heavy#2-(SGGGGTGGGGS [SEQ ID NO:1])-dsvH#4-(GGGGSGGGGSGGGGSGGGGS [SEQ ID NO: 68])-dsvL#4.
Плазмида pND1 (Fab#2 Heavy-(SGGGGTGGGGS SEQ ID NO:1)-dsvH#3-(GGGGSGGGGSGGGGSGGGGS SEQ ID NO:68)-dsvL#3) [плазмида i] уже имелась в распоряжении. Фрагмент гена, кодирующий dsHLscFv#3, был вырезан из pND1 и слит с легкой цепью #2, как описано выше, для создания: Light#2-(SGGGGSGGGGS SEQ ID NO:2)-dsvH#3-(GGGGSGGGGSGGGGSGGGGS SEQ ID NO:68)-dsvL#3 [плазмиды j].
Все форматы слияния с Fab были клонированы в векторы для экспрессии в клетках млекопитающих под контролем промотора HCMV-MIE и последовательности полиА SV40E.
Экспрессия в HEK293 форматов Fab-1xdsscFv-1xscFv и Fab-2xdsscFv
Клетки НЕК293 трансфецировали соответствующими плазмидами с использованием реагента для трансфекции 293-фектина от Invitrogen в соответствии с инструкциями изготовителя. Плазмиды были смешаны, как показано в таблице 4, для экспрессии различных конструкций:
Таблица 4
2. Плазмида i
2. Плазмида i
2. Плазмида i
2. Плазмида i
2. Плазмида j
2. Плазмида j
2. Плазмида j
2. Плазмида j
Соотношение плазмид, используемых для трансфекций, было 1:1. Всего 50 мкг плазмидной ДНК инкубировали с 125 мкл 293-фектина+4,25 мл среды OptiMEM в течение 20 мин при комнатной температуре. Затем смесь добавляли к 50 мл клеток НЕК293 в виде суспензии с концентрацией 1×106 клеток/мл и инкубировали при встряхивании при 37°С. Супернатанты собирали на 10-й день путем центрифугирования при 1500хg для удаления клеток, и супернатант пропускали через фильтр с размером пор 0,22 мкм. Уровень экспрессии определяли с помощью HPLC с использованием белка-G.
В таблице 5 приведены результаты анализа с помощью HPLC с использованием белка-G. Как можно видеть, уровни экспрессии всех конструкций были сравнимы друг с другом, охватывая диапазон 11-23 мкг/мл. Конструкции, помеченные звездочкой (*), экспрессировали с использованием отдельной трансфекции, поэтому абсолютные уровни экспрессии LC-scFv#3,HC-scFv#4 нельзя сравнивать с НС-scFv#3,LC-scFv#4.
Таблица 5
Очистка с использованием белка-G экспрессированных в HEK293 форматов Fab-1xdsscFv-1xscFv и Fab-2xdsscFv
Приблизительно 50 мл супернатантов клеток HEK293 концентрировали в ~25 раз до ~2 мл, используя центрифужные концентраторы с отсеканием по молекулярной массе=10 кДа. Сконцентрированные супернатанты наносили на 1мл колонку HiTrap Protein-G FF (GE Healthcare), уравновешенную в 20 мМ фосфате, 40 мМ NaCl, рН 7,4. Колонку промывали 20 мМ фосфатом, 40 мМ NaCl, рН 7,4, и связанный материал элюировали с использованием 0,1 М глицина/HCl pH2,7. Пик элюции собирали, и рН доводили до ~рН 7,0 с помощью 2 М Трис/HCl pH 8,5. Элюаты с доведенным рН концентрировали, и буфер заменяли на PBS рН 7,4, используя центрифужные концентраторы с отсеканием по молекулярной массе=10 кДа.
Анализ с помощью электрофореза в SDS-ПААГ очищенных с использованием белка-G, экспрессированных в HEK293 форматов Fab-1xdsscFv-1xscFv и Fab-2xdsscFv
Образцы (2 мкг) были разведены с использованием PBS до объема 9,75 мкл, к которому добавляли 3,75 мкл 4xLDS буфера для образцов и 1,5 мкл 100 мМ N-этилмалеимида (невосстановленные образцы) или 1,5 мкл 10хNuPAGE восстановителя (восстановленные образцы). Образцы встряхивали, инкубировали при 70°С в течение 10 мин, охлаждали и центрифугировали при 12500 оборотах в минуту в течение 30 секунд. Приготовленные образцы наносили на 4-20% акриламидный гель в Трис/глицине с SDS, и электрофорез проводили в течение ~100 минут при 125В, постоянном напряжении. Использовали маркер молекулярной массы SeeBluePlus2 (Life Technologies). Гели окрашивали с использованием красителя для белков Instant Blue (Expedeon) и обесцвечивали дистиллированной водой.
Ожидаемые размеры полос после электрофореза в SDS-ПААГ в восстанавливающих и невосстанавливающих условиях приведены в таблице 6.
Таблица 6:
Для всех белков, невосстанавливающий гель должен был показать полосу, соответствующую М.м. ~100 кДа, в то время как восстанавливающие гели должны были показать дублет, соответствующий М.м. ~50 кДа, с одинаковым окрашиванием в обеих полосах.
Для всех белков Fab-1xdsscFv-1xscFv и Fab-2xdsscFv, гели после электрофореза в SDS-ПААГ в восстанавливающих условиях показали рисунки полос, которые свидетельствовали о правильной экспрессии конструкций по показателю положения миграции и интенсивности окрашивания, с дублетом, соответствующим М.м. ~50 кДа (фиг. 2B, D). Дополнительная самая верхняя незначительная полоса соответствует невосстановленному полноразмерному белку. Как и следовало ожидать, в невосстанавливающем геле наблюдаются связанные дисульфидными связями мультимеры (фиг. 2A, C), которые исчезают в восстанавливающих условиях (фиг. 2B, D). Минорные полосы, соответствующие М.м. ~50 кДа, в невосстанавливающем геле (фиг. 2A, C) могут соответствовать неполному образованию дисульфидной связи между тяжелой и легкой цепями в Fab-фрагменте.
Анализ с помощью G3000 SE-HPLC очищенных с использованием белка-G, экспрессированных в HEK293 форматов Fab-1xdsscFv-1xscFv и Fab-2xdsscFv
10 мкг образцов очищенных белков (100 мкл 0,1 мг/мл маточного раствора, разведенного в PBS) вводили в колонку TSK Gel G3000SWXL, 7,8×300 мм, (Tosoh) через 3 дня после очистки и разделяли с использованием изократического градиента 200 мМ фосфата рН 7,0 со скоростью 1 мл/мин. Обнаружение сигнала осуществляли по поглощению при 280 нм.
Результаты показаны на фиг. 3. Как видно из фиг.3, после очистки с использованием белка-G, форматы Fab-1xdsscFv-1xscFv и Fab-2xdsscFv были на 83-89% мономерами.
Хотя все образцы имеют схожие уровни мономера в исследовании, те образцы, которые содержат scFv без дисульфида Fv, находятся в динамическом равновесии. Это означает, что % мономера, определяемый в исследовании для этих образцов, зависит от концентрации образца, более концентрированные образцы дают более высокий % мономера, а менее концентрированные образцы дают более низкий % мономера. Напротив, образцы, в которых оба scFv содержат дисульфид, являются стабильными и не находятся в динамическом равновесии. Поэтому % мономера, определяемый в исследовании, не изменяется с изменением концентрации образца.
Поскольку мономеры и мультимеры в форматах Fab-2xdsscFv стабильны и не находятся в динамическом равновесии, образцы могут быть легко дополнительно очищены, чтобы увеличить % мономера. Очищенные мономерные образцы также будут оставаться мономерными, даже когда концентрация конструкции в данном препарате увеличивается, тем самым делая конструкции очень подходящими для использования в фармацевтических препаратах. Напротив, Fab-2xscFv может после очистки в виде мономера подвергаться межмолекулярному динамическому обмену доменами между vL и vH scFv-доменов. По этой причине, кроме повышенного риска образования димера, тримера, структур высшего порядка и агрегатов такие молекулы трудно наблюдать, поскольку неагрегированные формы могут разложиться на мономеры после стадий разбавления, которые используются во время аналитических методов. Следовательно, Fab-2xdsscFv вносят дополнительную ясность при анализе фармацевтических композиций.
Экспрессия в CHOS форматов Fab-1xdsscFv-lxscFv и Fab-2xdsscFv
Клетки CHOS трансфецировали соответствующими плазмидами методами электропорации в масштабе 1 л. Плазмиды были смешаны, как показано в таблице 7, для экспрессии белка. Культуры выращивали в среде CD-CHO, дополненной 2 мМ GlutaMAX, и инкубировали при 37°С с 8% CО2 при 140 оборотах в минуту в течение 24 ч, а затем инкубировали еще в течение 13 дней при 32°С. На 4-й день после трансфекции, бутират натрия в конечной концентрации, составляющей 3 мМ, добавляли к культуре. На 14 день после трансфекции супернатанты культур собирали центрифугированием и стерилизовали через фильтр с размером пор 0,22 мкм. Титры экспрессии измеряли с помощью HPLC с использованием белка-G (таблица 8).
Таблица 7:
1. Плазмида j
1. Плазмида j
1. Плазмида j
1. Плазмида j
Таблица 8:
Очистка с использованием белка-G экспрессированных в CHO форматов Fab-1xdsscFv-1xscFv и Fab-2xdsscFv
1 л супернатантов СНО концентрировали в ~25 раз до ~40 мл, используя кювету с перемешиванием Amicon с отсеканием по молекулярной массе=10 кДа. Сконцентрированные супернатанты вносили в систему очистки AKTA Express Purification с колонкой с белком G и PBS в качестве подвижного буфера. Связанный материал элюировали с использованием 0,1 М глицина/HCl pH 2,7, и рН доводили до ~рН 7,0 с помощью 2 М Трис/HCl pH 8,5. Элюированный материал затем концентрировали с использованием концентраторов с отсеканием по молекулярной массе=10 кДа, и полученный концентрат загружали на колонку с Superdex (GE Healthcare) для гель-фильтрации с PBS в качестве подвижного буфера. Индивидуальные пики элюции собирали и анализировали с помощью эксклюзионной HPLC для определения мономерной фракции. Итоговый мономерный белок концентрировали до 5 мг/мл в PBS и хранили при 4°С.
Анализ с помощью электрофореза в SDS-ПААГ очищенных с использованием белка-G, экспрессированной в CHOS мономерной фракции форматов Fab-1xdsscFv-1xscFv и Fab-2xdsscFv
Образцы (2 мкг) были разведены с использованием PBS до объема 9,75 мкл, к которому добавляли 3,75 мкл 4xLDS буфера для образцов и 1,5 мкл 100 мМ N-этилмалеимида (невосстановленные образцы) или 1,5 мкл 10хNuPAGE восстановителя (восстановленные образцы). Образцы встряхивали, инкубировали при 70°С в течение 10 мин, охлаждали и центрифугировали при 12500 оборотах в минуту в течение 30 секунд. Приготовленные образцы наносили на 4-20% акриламидный гель в Трис/глицине с SDS, и электрофорез проводили в течение ~100 минут при 125В, постоянном напряжении. Использовали маркер молекулярной массы Markl2 (Life Technologies). Гели окрашивали с использованием красителя для белков Instant Blue (Expedeon) и обесцвечивали дистиллированной водой.
Ожидаемые размеры полос после электрофореза в SDS-ПААГ в восстанавливающих и невосстанавливающих условиях приведены в таблице 9.
Таблица 9:
Для всех белков, невосстанавливающий гель должен был показать полосу, соответствующую М.м. ~100 кДа, в то время как восстанавливающие гели должны были показать дублет, соответствующий М.м. ~50 кДа, с одинаковым окрашиванием в обеих полосах.
Для всех белков Fab-1xdsscFv-1xscFv и Fab-2xdsscFv, гели после электрофореза в SDS-ПААГ в восстанавливающих условиях показали рисунки полос, которые свидетельствовали о том, что конструкции являются мономерными и правильно экспрессированными, по показателю положения миграции и интенсивности окрашивания, с дублетом, соответствующим М.м. ~50 кДа (фиг. 8B, D). Дополнительная самая верхняя незначительная полоса соответствует невосстановленному полноразмерному белку (фиг. 8B, D). Для всех белков, невосстанавливающий гель показал полосу, соответствующую М.м. ~100 кДа, свидетельствующую о полноразмерном белке (фиг. 8А, а). Незначительные полосы, соответствующие М.м. ~50 кДа, в невосстанавливающем геля (фиг. 8A, b) могут соответствовать неполному образованию дисульфидной связи между тяжелой и легкой цепями в Fab-фрагменте.
Анализ с помощью G3000 SE-HPLC зависимости от времени мономерных форматов Fab-1xdsscFv-lxscFv и Fab-2xdsscFv
5 мг/мл очищенного мономера форматов антител хранили при 4°С в PBS и анализировали на 4-й день, 14-й день и 28-й день после очистки. Образцы разводили в PBS до 10 мкг и вносили в колонку TSK Gel G3000SWXL, 7,8×300 мм, (Tosoh) и разделяли с использованием изократического градиента 200 мМ фосфата рН 7,0 со скоростью 1 мл/мин. Обнаружение сигнала осуществляли по поглощению при 280 нм. Результаты показаны на фиг. 9. На 4-й день после очистки, анализ Fab-2xdsscFv показал, что большая часть белка была мономерной в начале эксперимента (сплошные линии) и оставалась мономерной и стабильной с течением времени, при этом <1% определялось как мультимеры (димеры, тримеры, структуры высшего порядка и крупные агрегаты). С другой стороны, для Fab-1xdsscFv-1xscFv было выявлено большее количество случаев мультимеризации, которое, как наблюдалось, увеличивалось линейно с течением времени (пунктирные линии). Действительно, встречаемость мультимеризации оказалась более выраженной в случае форматов, содержащих не стабилизированные с помощью дисульфидной связи scFv в ориентации VL/VH. Однако, очевидно, что форматы, которые содержат scFv без дисульфида Fv, находятся в динамическом равновесии и более склонны к мультимеризации при хранении, чем scFv которые стабилизированы с помощью дисульфидной связи. В самом деле, форматы, которые содержат scFv, оба из которых являются стабилизированными с помощью дисульфидной связи, как было показано, остаются мономерными даже тогда, когда концентрация белка в данном препарате увеличивается. Это делает конструкции, в которых оба scFv содержат дисульфид Fv, идеально подходящими для применения в фармацевтических препаратах, в случае которых критически важно, чтобы риск образования мультимеров высшего порядка или больших агрегатов в периоды хранения был незначительным.
Пример 2: Fab-2xdsscFv (бивалентный с двумя одинаковыми dsscFv)
Конструирование плазмид для экспрессии в клетках млекопитающих
Плазмиды для экспрессии Fab#2-(НС)dsscFv#3,(LC)dsscFv#3 (смотрите фиг. 4) были сконструированы путем слияния sscFv#3 с С-концом константной области каппа человека аллотипа Km3 легкой цепи #2, используя гибкий линкер SGGGGSGGGGS [также упоминаемый здесь как S, 2xG4S] (SEQ ID NO:2), или путем слияния scFv#3 с С-концом CH1 константной области гамма-1 человека изотипа γ1 тяжелой цепи #2, используя гибкий линкер SGGGGTGGGGS [также упоминаемый здесь как S, G4T, G4S] (SEQ ID NO:1). Точечные мутации были введены в ДНК-последовательности в выбранные остатки в каркасной области как vL#3/vL#1, так и vH#3/vH#1. Были введены мутации (в G44C в тяжелой цепи и G10°C легкой цепи) для создания межцепочечной дисульфидной связи между тяжелой и легкой цепями Fv#3.
Плазмида pND1 (Fab#2 Heavy-(SGGGGTGGGGS [SEQ ID NO:1)-dsvH# 3-(GGGGSGGGGSGGGGSGGGGS [SEQ ID NO:68])-dsvL#3) [плазмида i] уже была в распоряжении. Фрагмент гена, кодирующий dsHLscFv#3, был вырезан из pND1 и слит с легкой цепью #2, как описано выше, для создания: Light#2-(SGGGGSGGGGS [SEQ ID NO:2])-dsvH#3- (GGGGSGGGGSGGGGSGGGGS [SEQ ID NO:68])-dsvL#3 [плазмиды j].
Форматы слияния с Fab были клонированы в векторы для экспрессии в клетках млекопитающих под контролем промотора HCMV-MIE и последовательности полиА SV40E.
Экспрессия в HEK293 Fab-2xdsscFv#3
Клетки НЕК293 трансфецировали соответствующими плазмидами с использованием реагента для трансфекции 293-фектина от Invitrogen в соответствии с инструкциями изготовителя. Плазмиды были смешаны, как показано в таблице 10, для экспрессии белка:
Таблица 10
2. Плазмида i
Соотношение плазмид, используемых для трансфекций, было 1:1. Всего 50 мкг плазмидной ДНК инкубировали с 125 мкл 293-фектина+4,25 мл среды OptiMEM в течение 20 мин при комнатной температуре. Затем смесь добавляли к 50 мл клеток НЕК293 в виде суспензии с концентрацией 1×106 клеток/мл и инкубировали при встряхивании при 37°С. Супернатанты собирали на 10-й день путем центрифугирования при 1500хg для удаления клеток, и супернатант пропускали через фильтр с размером пор 0,22 мкм. Уровень экспрессии определяли с помощью HPLC с использованием белка-G. В таблице 11 приведены результаты анализа с помощью HPLC с использованием белка-G. Уровень экспрессии составлял 2 мкг/мл.
Таблица 11
Очистка экспрессированного в HEK293 Fab-2xdsscFv#3
Приблизительно 50 мл супернатантов клеток HEK293 концентрировали в ~25 раз до ~2 мл, используя центрифужные концентраторы с отсеканием по молекулярной массе=10 кДа. Сконцентрированные супернатанты очищали и в дальнейшем концентрировали, и буфер заменяли на PBS рН 7,4, используя центрифужные концентраторы с отсеканием по молекулярной массе=10 кДа.
Анализ с помощью электрофореза в SDS-ПААГ очищенного с использованием белка-G, экспрессированного в HEK293 Fab-2xdsscFv#3
Образцы (2 мкг) были разведены с использованием PBS до объема 9,75 мкл, к которому добавляли 3,75 мкл 4xLDS буфера для образцов и 1,5 мкл 100 мМ N-этилмалеимида (невосстановленные образцы) или 1,5 мкл 10хNuPAGE восстановителя (восстановленные образцы). Образцы встряхивали, инкубировали при 70°С в течение 10 мин, охлаждали и центрифугировали при 12500 оборотах в минуту в течение 30 секунд. Приготовленные образцы наносили на 4-20% акриламидный гель в Трис/глицине с SDS, и электрофорез проводили в течение ~100 минут при 125В, постоянном напряжении. Использовали маркер молекулярной массы SeeBluePlus2 (Life Technologies). Гели окрашивали с использованием красителя для белков Instant Blue (Expedeon) и обесцвечивали дистиллированной водой. Ожидаемые размеры полос после электрофореза в SDS-ПААГ в восстанавливающих и невосстанавливающих условиях приведены в таблице 12.
Таблица 12:
Невосстанавливающий гель должен был показать полосу, соответствующую М.м. ~100 кДа, в то время как восстанавливающий гель должен был показать дублет, соответствующий М.м. ~50 кДа, с одинаковым окрашиванием в обеих полосах.
Гели после электрофореза в SDS-ПААГ в восстанавливающих условиях показали рисунки полос, которые свидетельствовали о правильной экспрессии конструкций по показателю положения миграции и интенсивности окрашивания, с дублетом, соответствующим М.м. ~50 кДа (фиг. 4B), однако некоторые дополнительные незначительные виды также наблюдались, возможно, вследствие неоптимальной схемы очистки, в отличие от стандартного способа очистки с использованием белка-G, который, как правило, используют для очистки Fab. В невосстанавливающем геле наблюдаются связанные дисульфидными связями мультимеры (фиг. 4A), которые исчезают в восстанавливающих условиях (фиг. 4В).
Анализ с помощью S200 SE-HPLC очищенного, экспрессированного в HEK293 Fab-2xdsscFv#3
10 мкг образцов очищенных белков (100 мкл 0,1 мг/мл маточного раствора, разведенного в PBS) вводили в колонку с Superdex 200 10/300 GL Tricorn (GE Healthcare) через 3 дня после очистки и разделяли с использованием изократического градиента PBS рН 7,4 со скоростью 1 мл/мин, с непрерывной детекцией поглощения при 280 нм. Результаты показаны на фиг. 5. Как видно из фиг. 5, после очистки формат Fab-2xdsscFv#3 был на 81% мономером.
Пример 3: Fab-(HC)dsscFv-(LC)dsFv
Конструирование плазмид Fab#2-(НС)dsscFv#3-(LC)dsscFv#1 и Fab#2(HC)dsscFv#3(LC)dsFv#1 (со связью LC-vL) для экспрессии в клетках млекопитающих
Слитые с Fab#2 белки для экспрессии Fab#2-(HC)dsscFv#3- (LC)dsscFv#1 и Fab#2-(HC)dsscFv#3-(LC)dsFv#1 (со связью LC-vL) (смотрите фиг. 6) были сконструированы путем слияния или dsscFv#1 (dsvH-4xG4S-dsvL) или dsvL#1 с С-концом константной области каппа человека аллотипа Km3 легкой цепи #2, используя гибкий линкер SGGGGSGGGGSGGGGS (SEQ ID NO:69), для создания:
Light#2-(SGGGGSGGGGSGGGGS [SEQ ID NO:69])-dsscFv#1 [плазмиды b] и
Light#2-(SGGGGSGGGGSGGGGS [SEQ ID NO:69])-dsvL#1 [плазмиды с]; и
путем слияния HLdsscFv#3 (dsvH-4xG4S-dsvL) с С-концом CH1 константной области гамма-1 человека изотипа γ1 тяжелой цепи #2, используя гибкий линкер SGGGGSGGGGTGGGGS (SEQ ID NO: 70), для создания:
Heavy#2-(SGGGGSGGGGTGGGGS [SEQ ID NO:70])-dsscFv#3 [плазмиды а].
Точечные мутации (в G44C в тяжелой цепи и G10°C в легкой цепи) были введены в ДНК-последовательности в выбранные остатки в каркасной области vL#3, vH#3, vL#1 и vH#1, чтобы создать межцепочечную дисульфидную связь между тяжелой и легкой цепями Fv#3 и Fv#1. Гены слияний Fab с тяжелой и легкой цепями были клонированы в векторы для экспрессии в клетках млекопитающих под контролем промотора HCMV-MIE и последовательности полиА SV40E. Гены, кодирующие:
Heavy#2-(SGGGGSGGGGTGGGGS [SEQ ID NO:70])-dsscFv#3 [плазмида а] и
свободный домен dsvH#1 [плазмида d]
были получены химически и по отдельности клонировали в векторы для экспрессии в клетках млекопитающих под контролем промотора HCMV-MIE и последовательности полиА SV40E.
Гены, кодирующие dsscFv#1 и dsvL#1, были получены химически и слиты с С-концом легкой цепи # 2, чтобы создать:
Light#2-(SGGGGSGGGGSGGGGS [SEQ ID NO:69])-dsscFv#1 [плазмиду b] и
Light#2- (SGGGGSGGGGSGGGGS [SEQ ID NO:69])-dsvL#1 [плазмиду с]
и полные конструкции были клонированы в вектор для экспрессии в клетках млекопитающих под контролем промотора HCMV-MIE и последовательности полиА SV40E.
Экспрессия в HEK293:
Fab#2-(HC)dsscFv#3-(LC)dsscFv#1 и
Fab#2-(HC)dsscFv#3-(LC)dsFv#1 (со связью LC-vL)
Клетки НЕК293 трансфецировали соответствующими плазмидами с использованием реагента для трансфекции 293-фектина от Invitrogen в соответствии с инструкциями изготовителя. Плазмиды были смешаны, как изложено ниже, для экспрессии различных конструкций, как показано в таблице 13 ниже:
Таблица 13
2. Плазмида b
2. Плазмида c
3. Плазмида d
Для комбинации двух плазмид соотношение плазмид, используемых для трансфекций, было 1:1, тогда как для комбинации 3 плазмид соотношение было 1:1:1. Всего 50 мкг плазмидной ДНК инкубировали с 125 мкл 293-фектина+4,25 мл среды OptiMEM в течение 20 мин при комнатной температуре. Затем смесь добавляли к 50 мл клеток НЕК293 в виде суспензии с концентрацией 1×106 клеток/мл и инкубировали при встряхивании при 37°С. Супернатанты собирали на 10-й день путем центрифугирования при 1500хg для удаления клеток, и супернатант пропускали через фильтр с размером пор 0,22 мкм. Уровень экспрессии определяли с помощью HPLC с использованием белка-G.
Результаты представлены в таблице 14. Как можно видеть, уровни экспрессии обеих конструкций были сравнимы друг с другом (16-18 мкг/мл). В литературе были сообщения, что экспрессия Fv-фрагментов, в которых отсутствует либо линкер между vL и vH, либо мотив димеризации, чтобы сблизить vL и vH, имеют существенно более низкие уровни экспрессии, чем связанные Fv. Неожиданным образом, это не отмечалось в этих данных, в которых не было существенных различий, отмечаемых между уровнем экспрессии каждого типа конструкции.
Таблица 14
Очистка с использованием белка-G экспрессированных в HEK293 Fab#2-(HC)dsscFv#3-(LC)dsscFv#1 и Fab#2-(HC)dsscFv#3-(LC)dsFv#1 (со связью LC-vL)
Приблизительно 50 мл супернатантов клеток HEK293 концентрировали в ~25 раз до ~2 мл, используя центрифужные концентраторы с отсеканием по молекулярной массе=10 кДа. Сконцентрированные супернатанты наносили на 1-мл колонку HiTrap Protein-G FF (GE Healthcare), уравновешенную в 20 мМ фосфате, 40 мМ NaCl, рН 7,4. Колонку промывали 20 мМ фосфатом, 40 мМ NaCl, рН 7,4, и связанный материал элюировали с использованием 0,1 М глицина/HCl pH 2,7. Пик элюции собирали, и рН доводили до ~рН 7,0 с помощью 2 М Трис/HCl pH 8,5. Элюаты с доведенным рН концентрировали, и буфер заменяли на PBS рН 7,4, используя центрифужные концентраторы с отсеканием по молекулярной массе=10 кДа.
Анализ с помощью электрофореза в SDS-ПААГ очищенных с использованием белка-G, экспрессированных в HEK293 Fab#2-(HC)dsscFv#3-(LC)dsscFv#1 и Fab#2-(HC)dsscFv#3-(LC)dsFv#1 (со связью LC-vL)
Образцы (2 мкг) были разведены с использованием PBS до объема 9,75 мкл, к которому добавляли 3,75 мкл 4xLDS буфера для образцов и 1,5 мкл 100 мМ N-этилмалеимида (невосстановленные образцы) или 1,5 мкл 10хNuPAGE восстановителя (восстановленные образцы). Образцы встряхивали, инкубировали при 70°С в течение 10 мин, охлаждали и центрифугировали при 12500 оборотах в минуту в течение 30 секунд. Приготовленные образцы наносили на 4-20% акриламидный гель в Трис/глицине с SDS, и электрофорез проводили в течение ~100 минут при 125В, постоянном напряжении. Использовали маркер молекулярной массы SeeBluePlus2 (Life Technologies). Гели окрашивали с использованием красителя для белков Instant Blue (Expedeon) и обесцвечивали дистиллированной водой.
Результаты показаны на фиг. 6. Для Fab#2-(HC)dsscFv#3-(LC)dsscFv#1, невосстанавливающий гель должен был показать полосу, соответствующую М.м. ~100 кДа, в то время как восстанавливающий гель должен был показать дублет, соответствующий М.м. ~50 кДа, с примерно одинаковым окрашиванием в обеих полосах. Для Fab#2-(HC)dsscFv#3-(LC)dsFv#1 (со связью LC-vL), невосстанавливающий гель должен был показать полосу, соответствующую М.м. ~100 кДа, в то время как восстанавливающий гель должен был показать 3 полосы, соответствующие М.м. ~50, ~36 и ~13 кДа, с окрашиванием примерно в соотношении 3:2:1 от верхней к нижней полосе.
Гели после электрофореза в SDS-ПААГ в восстанавливающих условиях показали рисунки полос, которые свидетельствовали о правильной экспрессии конструкций по показателю как положения миграции, так и интенсивности окрашивания. Гели после электрофореза в SDS-ПААГ в невосстанавливающих условиях показали рисунки значительных полос >200 кДа для Fab-2xdsscFv, которые соответствовали мультимеризации (фиг. 6А, дорожка 2), но меньше высокомолекулярных молекул отмечалось в образце Fab-dsscFv-dsFv (фиг. 6В, дорожка 2).
Анализ с помощью G3000 SE-HPLC очищенных с использованием белка-G, экспрессированных в HEK293 Fab#2-(HC)dsscFv#3-(LC)dsscFv#1 и Fab#2-(HC)dsscFv#3-(LC)dsFv#1 (со связью LC-vL)
10 мкг образцов очищенных белков (100 мкл 0,1 мг/мл маточного раствора, разведенного в PBS) вводили в колонку TSK Gel G3000SWXL, 7,8×300 мм, (Tosoh) через 3 дня после очистки и разделяли с использованием изократического градиента 200 мМ фосфата рН 7,0 со скоростью 1 мл/мин. Обнаружение сигнала осуществляли по поглощению при 280 нм.
Результаты показаны на фиг. 7. После очистки с использованием белка-G Fab#2-(HC)dsscFv#3-(LC)dsFv#1 (со связью LC-vL) был на 91% мономером, тогда как Fab#2-(HC)dsscFv#3-(LC)dsscFv#1 был на 30% мономером.
Известно, что dsscFv#1 особенно склонен к мультимеризации. Учитывая, что мультимеры физически соединены с помощью линкера dsscFv (vL1#1 или vH#1 спарен с vH#1 или vL1#1 из отличной полипептидной цепи), при замене dsscFv#1 на dsFv#1 (который не содержит линкер scFv), наблюдалось значительное увеличение процента полученного мономера.
Таким образом, для специалиста будет очевидно, что, в зависимости от склонности dsscFv к мультимеризации, в некоторых случаях было бы выгодно использовать dsFv вместо dsscFv.
Пример 4. Определенная с помощью Biacore аффинность и демонстрация одновременного связывания антигенов-мишеней
Аффинности и кинетические параметры для взаимодействий Fab#2-(HC)dsHLscFv#3(LC)dsHLscFv#4 определяли с помощью поверхностного плазмонного резонанса (SPR), проводимого на BIAcore Т100 или BIAcore 3000, используя сенсорные чипы CM5 (GE Healthcare Bio-Sciences AB) и подвижный буфер HBS-EP (10 мМ HEPES (рН 7,4), 150 мМ NaCl, 3 мМ EDTA 0,05% в объемном отношении поверхностно-активного вещества Р20). Все эксперименты проводили при 25°С. Образцы антител были захвачены на поверхность сенсорного чипа, используя или специфический в отношении F(аb')2 человека козий Fab (Jackson ImmunoResearch), или моноклональное антитело против CH1 человека собственного производства. Ковалентная иммобилизация захватываемого антитела была достигнута с помощью стандартной химической реакции сочетания с аминами до уровня, составляющего 6000-7000 единиц ответа (RU). Антиген #2, #3 или #4 титровали отдельно над захваченным антителом. Каждый цикл анализа состоял из первого захвата образца антитела, используя 1-мин инъекцию, до фазы ассоциации, состоящей из 3-мин инъекции антигена, после чего диссоциацию наблюдали в течение 10 мин. После каждого цикла поверхность захвата регенерировали с помощью 2×1-мин инъекций 40 мМ HCl с последующей 30-сек инъекцией 5 мМ NaOH. Используемые скорости потока составляли 10 мкл мин-1 для захвата, 30 мкл мин-1 для фаз ассоциации и диссоциации, и 10 мкл мин-1 для регенерации. Кинетические параметры определяли путем одновременной комплексной подгонки полученных сенсограмм к стандартной модели связывания в соотношении 1:1, используя программное обеспечение BIAcore T100 Evaluation v2.0.1 или BIAcore 3000 BIAEvaluation v3.2. Результаты приведены в таблице 15. Антитело показало ожидаемые аффинности в пМ-нМ диапазоне для проверенных антигенов.
Таблица 15:
Способность Fab#2-(HC)dsHLscFv#3(LC)dsHLscFv#4 к одновременному связыванию со всеми 3 антигенами оценивали путем захвата триспецифичного антитела на сенсорный чип с помощью иммобилизованного F(аb')2 против IgG человека. Каждый антиген или смешанный раствор антигена #2, #3 и #4 титровали над захваченным антителом в течение 3-мин инъекций. Ответы в виде связывания, наблюдаемые для независимых инъекций, и объединенные ответы приведены в таблице 16. Ответ в виде связывание для раствора объединенных антигенов #2/#3/#4 был равен сумме ответов на независимые инъекции. Это подтверждает, что Fab#2-(HC)dsHLscFv#3(LC)dsHLscFv#4 способен к одновременному связыванию всех 3-х проверяемых антигенов.
Таблица 16:
Пример 5. Сравнение выхода мономера между форматами Fab-2xscFv и Fab-2xdsscFv
Клетки EXpiHEK были трансфецированы соответствующими плазмидами методами электропорации в 50-мл масштабе. Плазмиды были смешаны, как показано в таблице 17, для экспрессии белка. Культуры выращивали в среде для экспрессии в EXpiHEK и инкубировали при 37°С с 8% СО2 при 120 оборотах в минуту в течение 16-18 ч перед добавлением энхансера 1 и 2. Затем культуры инкубировали в течение еще 4 дней при 37°С. Супернатант культур собирали центрифугированием и стерилизовали пропусканием через фильтр с размером пор 0,22 мкм. Титры экспрессии измеряли с помощью HPLC с использованием белка-G (таблица 18).
Таблица 17:
2. Плазмида l1
2. Плазмида l2
2. Плазмида n1
2. Плазмида n2
2. Плазмида p1
2. Плазмида p2
2. Плазмида r1
2. Плазмида r2
Таблица 18:
Очистка с использованием белка-G экспрессированных в EXPiHEK форматов Fab-2xscFvFv и Fab-2xdsscFv
Супернатанты концентрировали в ~25 раз до ~2 мл, используя центрифужные концентраторы с отсеканием по молекулярной массе=10 кДа. Сконцентрированные супернатанты очищали с помощью HPLC с использованием белка-G, используя фосфатный буфер, рН 7,4. Связанный материал элюировали с использованием 0,1 М глицина/HCl pH 2,7, и рН доводили до ~рН 7,0 с помощью 2 М Трис/HCl pH 8,5. Элюированный материал концентрировали, используя концентраторы с отсеканием по молекулярной массе=10 кДа, и буфер заменяли на PBS. Очищенный белок концентрировали до ~4-5 мг/мл в PBS и хранили при 4°С.
Анализ с помощью электрофореза в SDS-ПААГ очищенных с использованием белка-G, экспрессированных в EXPiHEK форматов Fab-2xscFv и Fab-2xdsscFv
Образцы (2 мкг) были разведены с использованием PBS до объема 9,75 мкл, к которому добавляли 3,75 мкл 4xLDS буфера для образцов и 1,5 мкл 100 мМ N-этилмалеимида (невосстановленные образцы) или 1,5 мкл 10хNuPAGE восстановителя (восстановленные образцы). Образцы встряхивали, инкубировали при 70°С в течение 10 мин, охлаждали и центрифугировали при 12500 оборотах в минуту в течение 30 секунд. Приготовленные образцы наносили на 4-20% акриламидный гель в Трис/глицине с SDS, и электрофорез проводили в течение ~100 минут при 125В, постоянном напряжении. Использовали маркер молекулярной массы Seeblue2 (Life Technologies). Гели окрашивали с использованием красителя для белков Instant Blue (Expedeon) и обесцвечивали дистиллированной водой.
Ожидаемые размеры полос после электрофореза в SDS-ПААГ в восстанавливающих и невосстанавливающих условиях приведены в таблице 19.
Таблица 19:
Для всех белков, невосстанавливающий гель должен был показать полосу, соответствующую М.м. ~100 кДа, в то время как восстанавливающие гели должны были показать дублет, соответствующий М.м. ~50 кДа, с одинаковым окрашиванием в обеих полосах.
Для всех белков Fab-2xscFv и Fab-2xdsscFv, гели после электрофореза в SDS-ПААГ в восстанавливающих условиях показали рисунки полос, которые свидетельствовали о правильной экспрессии конструкций по показателю положения миграции и интенсивности окрашивания, с дублетом, соответствующим М.м. ~50 кДа (фиг. 10B, а). Дополнительная самая верхняя незначительная полоса соответствует невосстановленному полноразмерному белку (фиг. 10B, b). Для всех белков, невосстанавливающий гель показал полосу, соответствующую М.м. ~130 кДа, свидетельствующую о полноразмерном белке (фиг. 10А, а). Полосы, соответствующие М.м. ~50 кДа, в невосстанавливающем геле (фиг. 10A, b) могут соответствовать неполному образованию дисульфидной связи между тяжелой и легкой цепями в Fab-фрагменте.
Анализ с помощью G3000 SE-HPLC форматов Fab-2xscFv и Fab-2xdsscFv
Очищенные белки антител в концентрации ~5 мг/мл хранили при 4°С в PBS в течение 24 часов перед анализом. Образцы, эквивалентные концентрации 25 мкг, вносили в колонку TSK Gel G3000SWXL, 7,8×300 мм, (Tosoh) и разделяли с использованием изократического градиента 200 мМ фосфата рН 7,0 со скоростью 1 мл/мин. Обнаружение сигнала осуществляли по поглощению при 280 нм. Результаты показаны в таблице 20. Анализ показал, что все белки Fab-2xdsscFv были на >90% мономерными. С другой стороны, для всех Fab-2xscFv было обнаружено большее количество случаев мультимеризации. Очевидно, что форматы, которые содержат scFv с дисульфидом Fv, являются более мономерными по сравнению с scFv без дисульфида Fv. Это указывает на преимущество использования форматов с scFv, которые содержат дисульфиды Fv, что касается выбора терапевтических молекул со стабильными свойствами, а также характеристик, которые были бы выгодны в производственном процессе.
Таблица 20:
--->
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> UCB Biopharma SPRL
<120> Конструкции полиспецифических антител
<130> G0228_WO
<160> 80
<170> Патент в версии 3.5
<210> 1
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> Пептидный линкер
<400> 1
Ser Gly Gly Gly Gly Thr Gly Gly Gly Gly Ser
1 5 10
<210> 2
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> Пептидный линкер
<400> 2
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10
<210> 3
<211> 8
<212> Белок
<213> Искусственная последовательность
<220>
<223> Шарнирный линкер
<400> 3
Asp Lys Thr His Thr Cys Ala Ala
1 5
<210> 4
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> Шарнирный линкер
<400> 4
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala
1 5 10
<210> 5
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<223> Шарнирный линкер
<400> 5
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Thr Cys Pro Pro Cys
1 5 10 15
Pro Ala
<210> 6
<211> 25
<212> Белок
<213> Искусственная последовательность
<220>
<223> Шарнирный линкер
<400> 6
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Thr Cys Pro Pro Cys
1 5 10 15
Pro Ala Thr Cys Pro Pro Cys Pro Ala
20 25
<210> 7
<211> 30
<212> Белок
<213> Искусственная последовательность
<220>
<223> Шарнирный линкер
<400> 7
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Gly Lys Pro Thr Leu
1 5 10 15
Tyr Asn Ser Leu Val Met Ser Asp Thr Ala Gly Thr Cys Tyr
20 25 30
<210> 8
<211> 31
<212> Белок
<213> Искусственная последовательность
<220>
<223> Шарнирный линкер
<400> 8
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Gly Lys Pro Thr His
1 5 10 15
Val Asn Val Ser Val Val Met Ala Glu Val Asp Gly Thr Cys Tyr
20 25 30
<210> 9
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<223> Шарнирный линкер
<400> 9
Asp Lys Thr His Thr Cys Cys Val Glu Cys Pro Pro Cys Pro Ala
1 5 10 15
<210> 10
<211> 26
<212> Белок
<213> Искусственная последовательность
<220>
<223> Шарнирный линкер
<400> 10
Asp Lys Thr His Thr Cys Pro Arg Cys Pro Glu Pro Lys Ser Cys Asp
1 5 10 15
Thr Pro Pro Pro Cys Pro Arg Cys Pro Ala
20 25
<210> 11
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> Шарнирный линкер
<400> 11
Asp Lys Thr His Thr Cys Pro Ser Cys Pro Ala
1 5 10
<210> 12
<211> 7
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 12
Ser Gly Gly Gly Gly Ser Glu
1 5
<210> 13
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 13
Asp Lys Thr His Thr Ser
1 5
<210> 14
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 14
Ser Gly Gly Gly Gly Ser
1 5
<210> 15
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 15
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10
<210> 16
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 16
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 17
<211> 21
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 17
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
Gly Gly Gly Gly Ser
20
<210> 18
<211> 26
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 18
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
20 25
<210> 19
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 19
Ala Ala Ala Gly Ser Gly Gly Ala Ser Ala Ser
1 5 10
<210> 20
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<220>
<221> разный признак
<222> (7)..(7)
<223> Xaa может представлять собой встречающуюся в природе аминокислоту.
<400> 20
Ala Ala Ala Gly Ser Gly Xaa Gly Gly Gly Ser Gly Ala Ser Ala Ser
1 5 10 15
<210> 21
<211> 21
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<220>
<221> разный признак
<222> (7)..(7)
<223> Xaa может представлять собой встречающуюся в природе аминокислоту.
<220>
<221> разный признак
<222> (12)..(12)
<223> Xaa может представлять собой встречающуюся в природе аминокислоту.
<400> 21
Ala Ala Ala Gly Ser Gly Xaa Gly Gly Gly Ser Xaa Gly Gly Gly Ser
1 5 10 15
Gly Ala Ser Ala Ser
20
<210> 22
<211> 26
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<220>
<221> разный признак
<222> (7)..(7)
<223> Xaa может представлять собой встречающуюся в природе аминокислоту.
<220>
<221> разный признак
<222> (12)..(12)
<223> Xaa может представлять собой встречающуюся в природе аминокислоту.
<220>
<221> разный признак
<222> (17)..(17)
<223> Xaa может представлять собой встречающуюся в природе аминокислоту.
<400> 22
Ala Ala Ala Gly Ser Gly Xaa Gly Gly Gly Ser Xaa Gly Gly Gly Ser
1 5 10 15
Xaa Gly Gly Gly Ser Gly Ala Ser Ala Ser
20 25
<210> 23
<211> 31
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<220>
<221> разный признак
<222> (7)..(7)
<223> Xaa может представлять собой встречающуюся в природе аминокислоту.
<220>
<221> разный признак
<222> (12)..(12)
<223> Xaa может представлять собой встречающуюся в природе аминокислоту.
<220>
<221> разный признак
<222> (17)..(17)
<223> Xaa может представлять собой встречающуюся в природе аминокислоту.
<220>
<221> разный признак
<222> (22)..(22)
<223> Xaa может представлять собой встречающуюся в природе аминокислоту.
<400> 23
Ala Ala Ala Gly Ser Gly Xaa Gly Gly Gly Ser Xaa Gly Gly Gly Ser
1 5 10 15
Xaa Gly Gly Gly Ser Xaa Gly Gly Gly Ser Gly Ala Ser Ala Ser
20 25 30
<210> 24
<211> 13
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<220>
<221> разный признак
<222> (7)..(7)
<223> Xaa может представлять собой встречающуюся в природе аминокислоту.
<400> 24
Ala Ala Ala Gly Ser Gly Xaa Ser Gly Ala Ser Ala Ser
1 5 10
<210> 25
<211> 28
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 25
Pro Gly Gly Asn Arg Gly Thr Thr Thr Thr Arg Arg Pro Ala Thr Thr
1 5 10 15
Thr Gly Ser Ser Pro Gly Pro Thr Gln Ser His Tyr
20 25
<210> 26
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 26
Ala Thr Thr Thr Gly Ser Ser Pro Gly Pro Thr
1 5 10
<210> 27
<211> 6
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 27
Ala Thr Thr Thr Gly Ser
1 5
<210> 28
<211> 21
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 28
Glu Pro Ser Gly Pro Ile Ser Thr Ile Asn Ser Pro Pro Ser Lys Glu
1 5 10 15
Ser His Lys Ser Pro
20
<210> 29
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 29
Gly Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp
1 5 10 15
<210> 30
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 30
Gly Gly Gly Gly Ile Ala Pro Ser Met Val Gly Gly Gly Gly Ser
1 5 10 15
<210> 31
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 31
Gly Gly Gly Gly Lys Val Glu Gly Ala Gly Gly Gly Gly Gly Ser
1 5 10 15
<210> 32
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 32
Gly Gly Gly Gly Ser Met Lys Ser His Asp Gly Gly Gly Gly Ser
1 5 10 15
<210> 33
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 33
Gly Gly Gly Gly Asn Leu Ile Thr Ile Val Gly Gly Gly Gly Ser
1 5 10 15
<210> 34
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 34
Gly Gly Gly Gly Val Val Pro Ser Leu Pro Gly Gly Gly Gly Ser
1 5 10 15
<210> 35
<211> 12
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 35
Gly Gly Glu Lys Ser Ile Pro Gly Gly Gly Gly Ser
1 5 10
<210> 36
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 36
Arg Pro Leu Ser Tyr Arg Pro Pro Phe Pro Phe Gly Phe Pro Ser Val
1 5 10 15
Arg Pro
<210> 37
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 37
Tyr Pro Arg Ser Ile Tyr Ile Arg Arg Arg His Pro Ser Pro Ser Leu
1 5 10 15
Thr Thr
<210> 38
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 38
Thr Pro Ser His Leu Ser His Ile Leu Pro Ser Phe Gly Leu Pro Thr
1 5 10 15
Phe Asn
<210> 39
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 39
Arg Pro Val Ser Pro Phe Thr Phe Pro Arg Leu Ser Asn Ser Trp Leu
1 5 10 15
Pro Ala
<210> 40
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 40
Ser Pro Ala Ala His Phe Pro Arg Ser Ile Pro Arg Pro Gly Pro Ile
1 5 10 15
Arg Thr
<210> 41
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 41
Ala Pro Gly Pro Ser Ala Pro Ser His Arg Ser Leu Pro Ser Arg Ala
1 5 10 15
Phe Gly
<210> 42
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 42
Pro Arg Asn Ser Ile His Phe Leu His Pro Leu Leu Val Ala Pro Leu
1 5 10 15
Gly Ala
<210> 43
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 43
Met Pro Ser Leu Ser Gly Val Leu Gln Val Arg Tyr Leu Ser Pro Pro
1 5 10 15
Asp Leu
<210> 44
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 44
Ser Pro Gln Tyr Pro Ser Pro Leu Thr Leu Thr Leu Pro Pro His Pro
1 5 10 15
Ser Leu
<210> 45
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 45
Asn Pro Ser Leu Asn Pro Pro Ser Tyr Leu His Arg Ala Pro Ser Arg
1 5 10 15
Ile Ser
<210> 46
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 46
Leu Pro Trp Arg Thr Ser Leu Leu Pro Ser Leu Pro Leu Arg Arg Arg
1 5 10 15
Pro
<210> 47
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 47
Pro Pro Leu Phe Ala Lys Gly Pro Val Gly Leu Leu Ser Arg Ser Phe
1 5 10 15
Pro Pro
<210> 48
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 48
Val Pro Pro Ala Pro Val Val Ser Leu Arg Ser Ala His Ala Arg Pro
1 5 10 15
Pro Tyr
<210> 49
<211> 17
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 49
Leu Arg Pro Thr Pro Pro Arg Val Arg Ser Tyr Thr Cys Cys Pro Thr
1 5 10 15
Pro
<210> 50
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 50
Pro Asn Val Ala His Val Leu Pro Leu Leu Thr Val Pro Trp Asp Asn
1 5 10 15
Leu Arg
<210> 51
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 51
Cys Asn Pro Leu Leu Pro Leu Cys Ala Arg Ser Pro Ala Val Arg Thr
1 5 10 15
Phe Pro
<210> 52
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> Жесткий линкер
<400> 52
Gly Ala Pro Ala Pro Ala Ala Pro Ala Pro Ala
1 5 10
<210> 53
<211> 4
<212> Белок
<213> Искусственная последовательность
<220>
<223> Жесткий линкер
<400> 53
Pro Pro Pro Pro
1
<210> 54
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> Связывающий альбумин пептид
<400> 54
Asp Leu Cys Leu Arg Asp Trp Gly Cys Leu Trp
1 5 10
<210> 55
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> Связывающий альбумин пептид
<400> 55
Asp Ile Cys Leu Pro Arg Trp Gly Cys Leu Trp
1 5 10
<210> 56
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<223> Связывающий альбумин пептид
<400> 56
Met Glu Asp Ile Cys Leu Pro Arg Trp Gly Cys Leu Trp Gly Asp
1 5 10 15
<210> 57
<211> 20
<212> Белок
<213> Искусственная последовательность
<220>
<223> Связывающий альбумин пептид
<400> 57
Gln Arg Leu Met Glu Asp Ile Cys Leu Pro Arg Trp Gly Cys Leu Trp
1 5 10 15
Glu Asp Asp Glu
20
<210> 58
<211> 20
<212> Белок
<213> Искусственная последовательность
<220>
<223> Связывающий альбумин пептид
<400> 58
Gln Gly Leu Ile Gly Asp Ile Cys Leu Pro Arg Trp Gly Cys Leu Trp
1 5 10 15
Gly Arg Ser Val
20
<210> 59
<211> 21
<212> Белок
<213> Искусственная последовательность
<220>
<223> Связывающий альбумин пептид
<400> 59
Gln Gly Leu Ile Gly Asp Ile Cys Leu Pro Arg Trp Gly Cys Leu Trp
1 5 10 15
Gly Arg Ser Val Lys
20
<210> 60
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<223> Связывающий альбумин пептид
<400> 60
Glu Asp Ile Cys Leu Pro Arg Trp Gly Cys Leu Trp Glu Asp Asp
1 5 10 15
<210> 61
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<223> Связывающий альбумин пептид
<400> 61
Arg Leu Met Glu Asp Ile Cys Leu Pro Arg Trp Gly Cys Leu Trp Glu
1 5 10 15
Asp Asp
<210> 62
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> Связывающий альбумин пептид
<400> 62
Met Glu Asp Ile Cys Leu Pro Arg Trp Gly Cys Leu Trp Glu Asp Asp
1 5 10 15
<210> 63
<211> 15
<212> Белок
<213> Искусственная последовательность
<220>
<223> Связывающий альбумин пептид
<400> 63
Met Glu Asp Ile Cys Leu Pro Arg Trp Gly Cys Leu Trp Glu Asp
1 5 10 15
<210> 64
<211> 18
<212> Белок
<213> Искусственная последовательность
<220>
<223> Связывающий альбумин пептид
<400> 64
Arg Leu Met Glu Asp Ile Cys Leu Ala Arg Trp Gly Cys Leu Trp Glu
1 5 10 15
Asp Asp
<210> 65
<211> 20
<212> Белок
<213> Искусственная последовательность
<220>
<223> Связывающий альбумин пептид
<400> 65
Glu Val Arg Ser Phe Cys Thr Arg Trp Pro Ala Glu Lys Ser Cys Lys
1 5 10 15
Pro Leu Arg Gly
20
<210> 66
<211> 20
<212> Белок
<213> Искусственная последовательность
<220>
<223> Связывающий альбумин пептид
<400> 66
Arg Ala Pro Glu Ser Phe Val Cys Tyr Trp Glu Thr Ile Cys Phe Glu
1 5 10 15
Arg Ser Glu Gln
20
<210> 67
<211> 11
<212> Белок
<213> Искусственная последовательность
<220>
<223> Связывающий альбумин пептид
<400> 67
Glu Met Cys Tyr Phe Pro Gly Ile Cys Trp Met
1 5 10
<210> 68
<211> 20
<212> Белок
<213> Искусственная последовательность
<220>
<223> Связывающий альбумин пептид
<400> 68
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser
20
<210> 69
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 69
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
1 5 10 15
<210> 70
<211> 16
<212> Белок
<213> Искусственная последовательность
<220>
<223> Гибкий линкер
<400> 70
Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Thr Gly Gly Gly Gly Ser
1 5 10 15
<210> 71
<211> 10
<212> Белок
<213> Искусственный
<220>
<223> CDRH1 dAbH1
<400> 71
Gly Ile Asp Leu Ser Asn Tyr Ala Ile Asn
1 5 10
<210> 72
<211> 16
<212> Белок
<213> Искусственный
<220>
<223> CDRH2 dAbH1
<400> 72
Ile Ile Trp Ala Ser Gly Thr Thr Phe Tyr Ala Thr Trp Ala Lys Gly
1 5 10 15
<210> 73
<211> 13
<212> Белок
<213> Искусственный
<220>
<223> CDRH3 dAbH1
<400> 73
Thr Val Pro Gly Tyr Ser Thr Ala Pro Tyr Phe Asp Leu
1 5 10
<210> 74
<211> 12
<212> Белок
<213> Искусственный
<220>
<223> CDRL1 dAbL1
<400> 74
Gln Ser Ser Pro Ser Val Trp Ser Asn Phe Leu Ser
1 5 10
<210> 75
<211> 7
<212> Белок
<213> Искусственный
<220>
<223> CDRL2 dAbL1
<400> 75
Glu Ala Ser Lys Leu Thr Ser
1 5
<210> 76
<211> 11
<212> Белок
<213> Искусственный
<220>
<223> CDRL3 dAbL1
<400> 76
Gly Gly Gly Tyr Ser Ser Ile Ser Asp Thr Thr
1 5 10
<210> 77
<211> 121
<212> Белок
<213> Искусственный
<220>
<223> Вариабельный домен тяжелой цепи антитела против альбумина (не дц)
<400> 77
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Ile Asp Leu Ser Asn Tyr
20 25 30
Ala Ile Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly Ile Ile Trp Ala Ser Gly Thr Thr Phe Tyr Ala Thr Trp Ala Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Thr Val Pro Gly Tyr Ser Thr Ala Pro Tyr Phe Asp Leu Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 78
<211> 121
<212> Белок
<213> Искусственный
<220>
<223> Вариабельный домен тяжелой цепи антитела против альбумина (дц)
<400> 78
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Ile Asp Leu Ser Asn Tyr
20 25 30
Ala Ile Asn Trp Val Arg Gln Ala Pro Gly Lys Cys Leu Glu Trp Ile
35 40 45
Gly Ile Ile Trp Ala Ser Gly Thr Thr Phe Tyr Ala Thr Trp Ala Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Thr Val Pro Gly Tyr Ser Thr Ala Pro Tyr Phe Asp Leu Trp Gly
100 105 110
Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 79
<211> 112
<212> Белок
<213> Искусственный
<220>
<223> Вариабельный домен легкой цепи антитела против альбумина (не дц)
<400> 79
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gln Ser Ser Pro Ser Val Trp Ser Asn
20 25 30
Phe Leu Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Glu Ala Ser Lys Leu Thr Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gly Gly Gly Tyr Ser Ser Ile
85 90 95
Ser Asp Thr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr
100 105 110
<210> 80
<211> 112
<212> Белок
<213> Искусственный
<220>
<223> Вариабельный домен легкой цепи антитела против альбумина (дц)
<400> 80
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gln Ser Ser Pro Ser Val Trp Ser Asn
20 25 30
Phe Leu Ser Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu
35 40 45
Ile Tyr Glu Ala Ser Lys Leu Thr Ser Gly Val Pro Ser Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln
65 70 75 80
Pro Glu Asp Phe Ala Thr Tyr Tyr Cys Gly Gly Gly Tyr Ser Ser Ile
85 90 95
Ser Asp Thr Thr Phe Gly Cys Gly Thr Lys Val Glu Ile Lys Arg Thr
100 105 110
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| КОНСТРУКЦИИ ПОЛИСПЕЦИФИЧЕСКИХ АНТИТЕЛ | 2015 |
|
RU2784673C2 |
| МУЛЬТИСПЕЦИФИЧЕСКОЕ АНТИТЕЛО СО СПЕЦИФИЧНОСТЬЮ СВЯЗЫВАНИЯ IL-13 И IL-17 ЧЕЛОВЕКА | 2020 |
|
RU2827946C1 |
| МОЛЕКУЛЫ СО СПЕЦИФИЧНОСТЬЮ К CD45 И CD79 | 2015 |
|
RU2747980C2 |
| МОЛЕКУЛЫ СО СПЕЦИФИЧНОСТЬЮ В ОТНОШЕНИИ CD79 И CD22 | 2015 |
|
RU2743590C2 |
| АНТИТЕЛА, СОДЕРЖАЩИЕ ПОЛИПЕПТИД, ВСТРОЕННЫЙ В УЧАСТОК КАРКАСНОЙ ОБЛАСТИ 3 | 2019 |
|
RU2796254C2 |
| АНТИТЕЛО К SIRPα И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2822496C1 |
| МОДИФИЦИРОВАННЫЕ АНТИТЕЛА IGG, КОТОРЫЕ СВЯЗЫВАЮТСЯ С ТРАНСФОРМИРУЮЩИМ ФАКТОРОМ РОСТА БЕТА-1 С ВЫСОКОЙ АФФИННОСТЬЮ, АВИДНОСТЬЮ И СПЕЦИФИЧНОСТЬЮ | 2016 |
|
RU2728858C2 |
| СВЯЗЫВАЮЩИЕ МОЛЕКУЛЫ, ВЫЗЫВАЮЩИЕ КЛЕТОЧНУЮ АКТИВАЦИЮ | 2019 |
|
RU2770620C1 |
| АНТИТЕЛА ПРОТИВ PD-1 И КОМПОЗИЦИИ | 2016 |
|
RU2750675C1 |
| АНТИТЕЛА ПРОТИВ НtrА1 И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2016 |
|
RU2750285C2 |
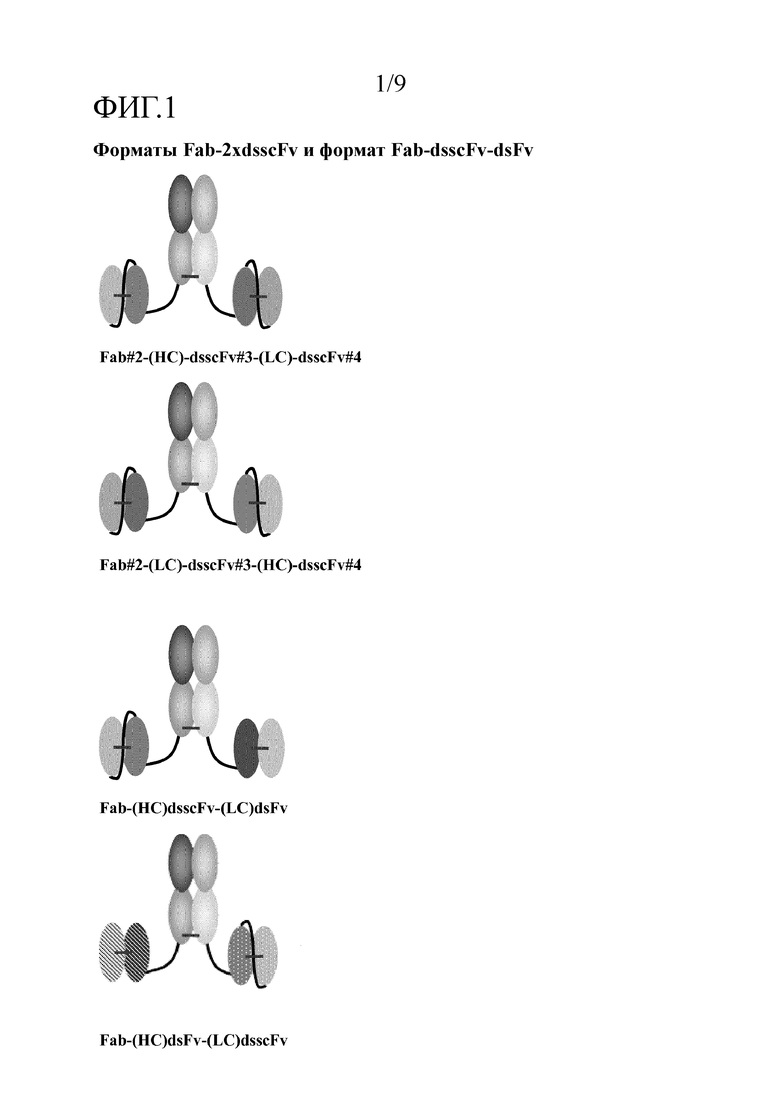
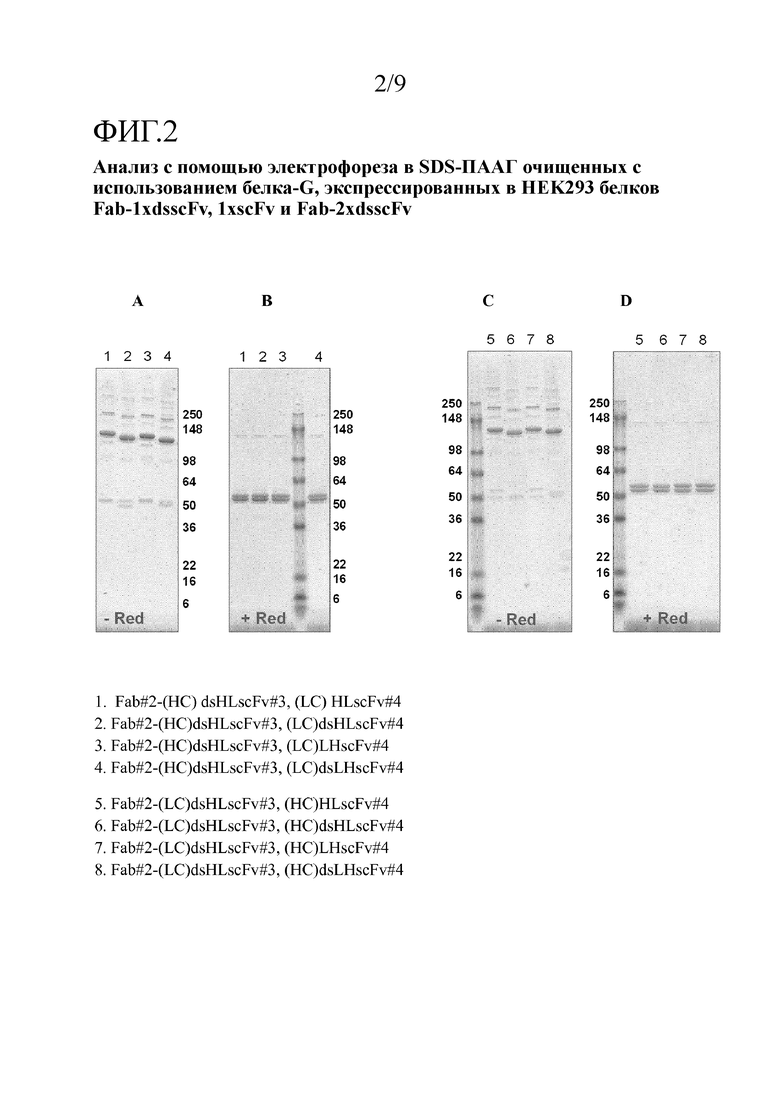
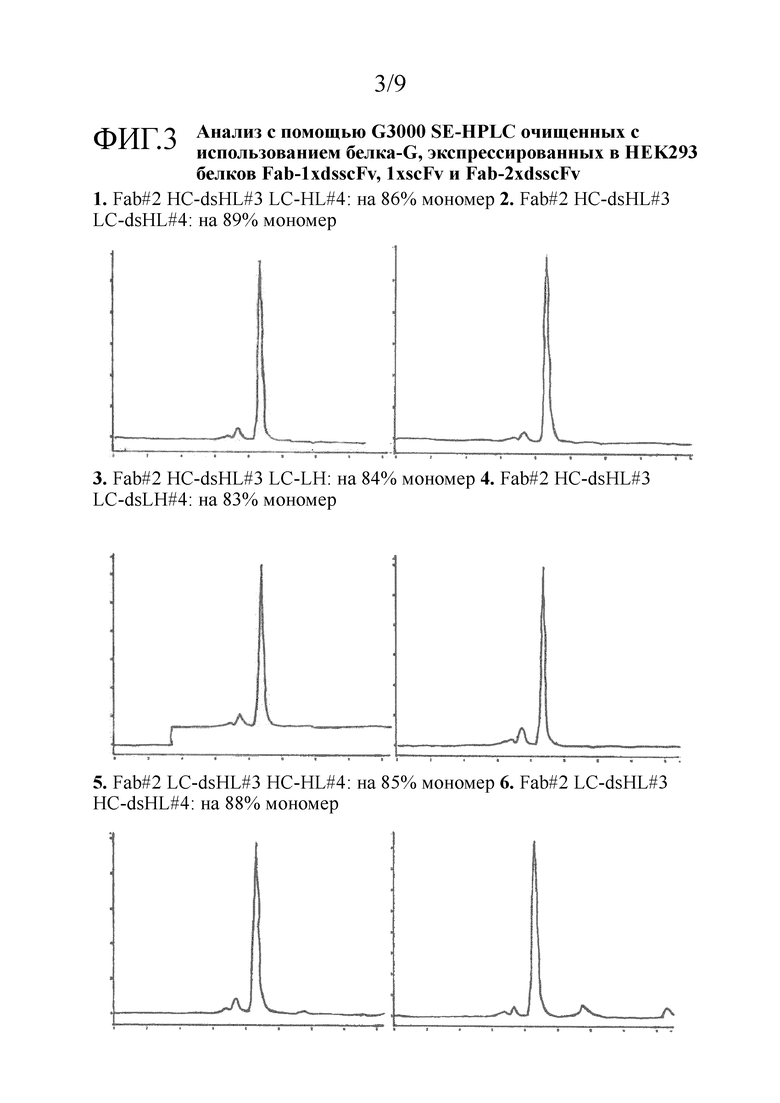

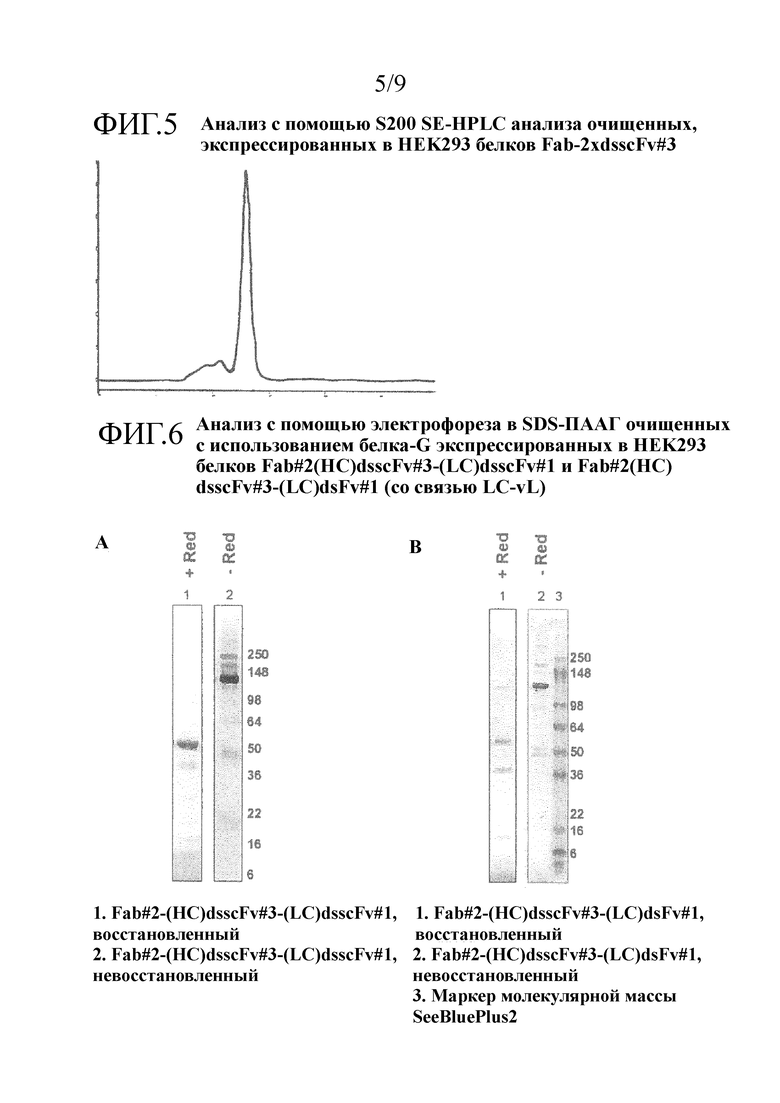
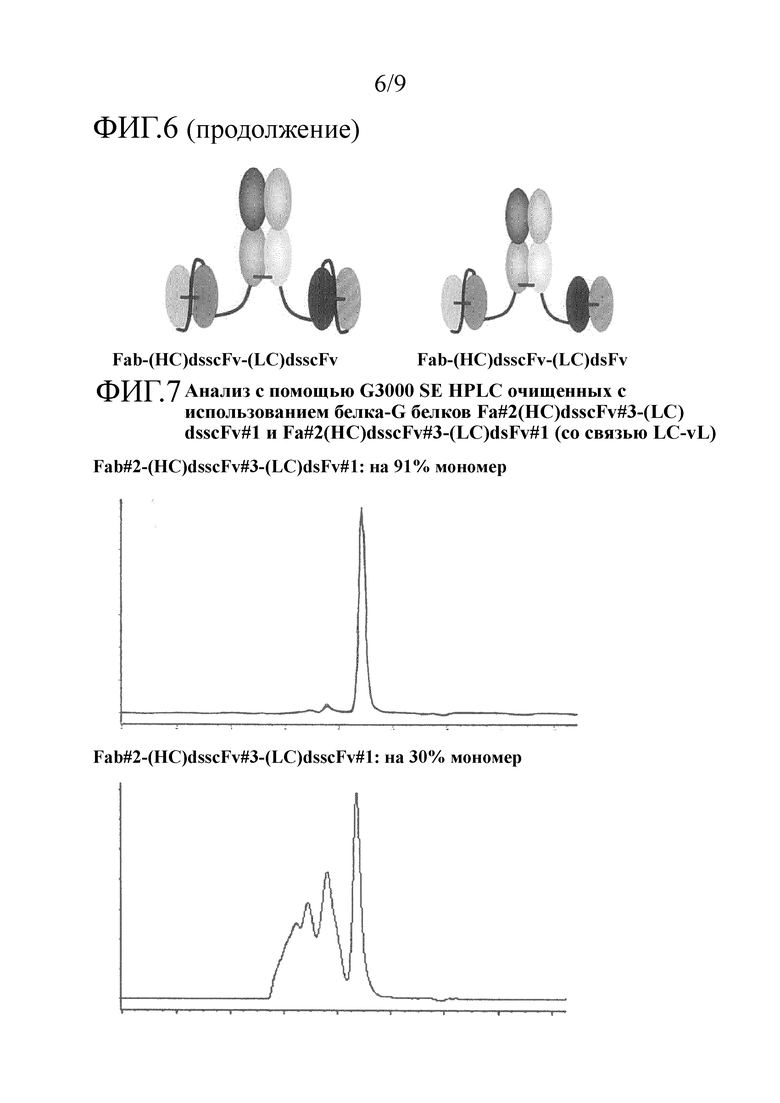
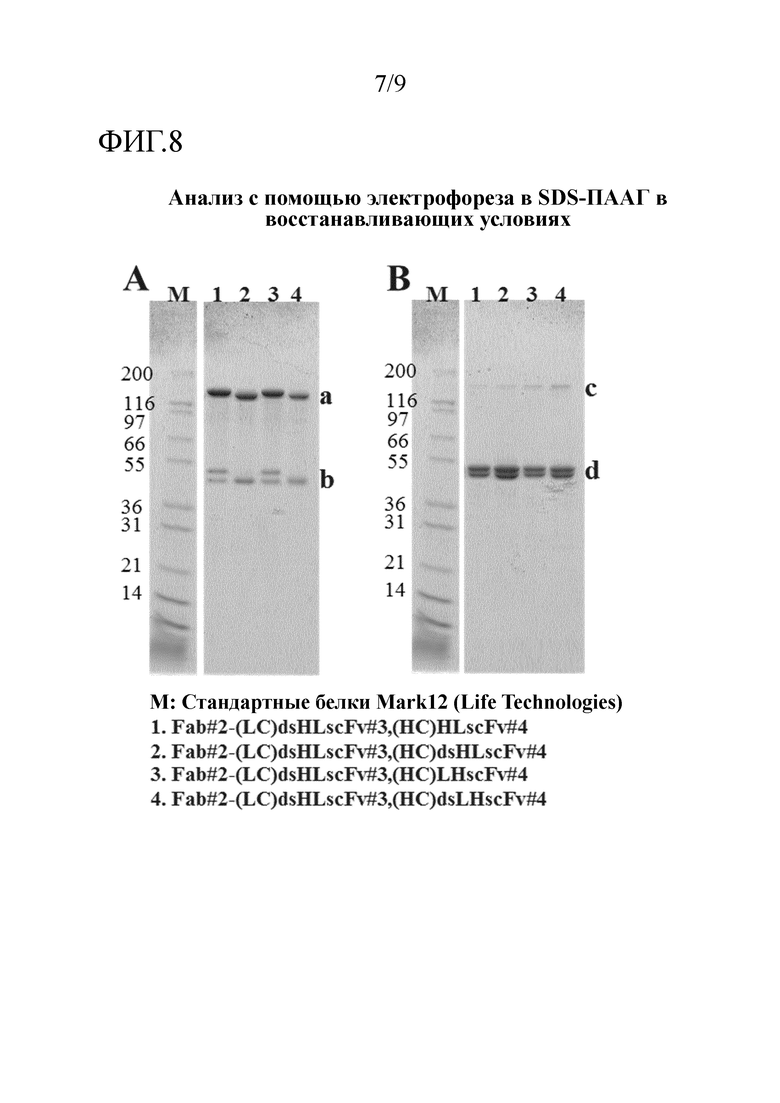
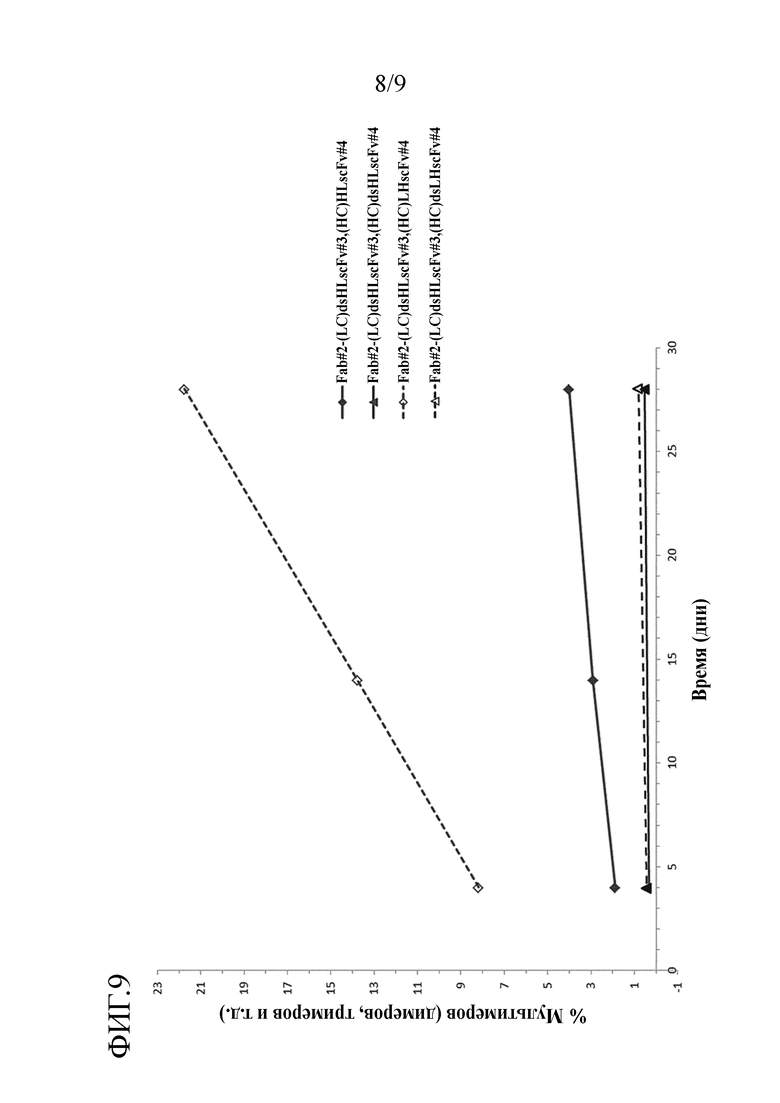
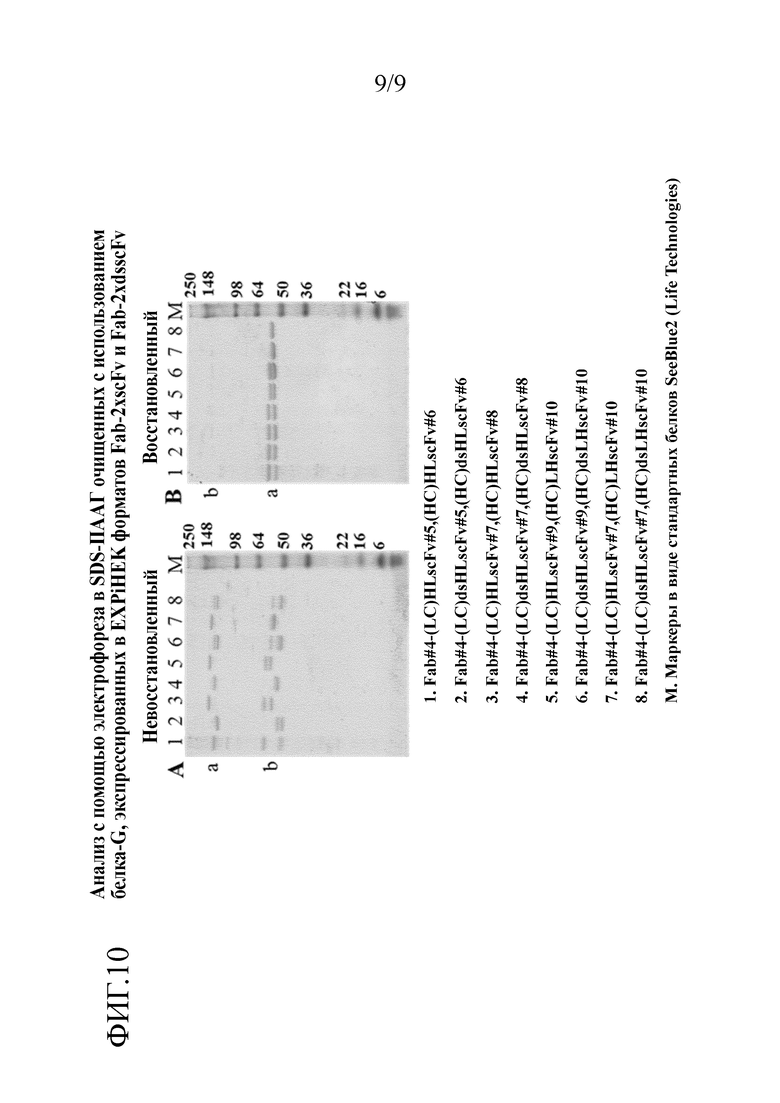
Изобретение относится к области биохимии, в частности к молекуле триспецифического антитела. Также раскрыты полинуклеотид, кодирующий указанное антитело; экспрессионный вектор, клетка-хозяин. Раскрыт способ получения указанного триспецифического антитела. Изобретение обладает способностью эффективно получать триспецифическое антитело. 6 н. и 19 з.п. ф-лы, 10 ил., 20 табл., 5 пр.
1. Молекула триспецифического антитела, включающая:
a) полипептидную цепь формулы (I): VH-СН1-Х-V1; и
b) полипептидную цепь формулы (II): VL-CL-Y-V2;
или состоящую из a) и b), где:
VН представляет собой вариабельный домен тяжелой цепи;
CH1 представляет собой домен константной области тяжелой цепи, например, ее домен 1;
Х представляет собой связь или линкер;
Y представляет собой связь или линкер;
V1 представляет собой dsFv или dsscFv;
VL представляет собой вариабельный домен легкой цепи;
CL представляет собой домен из константной области легкой цепи, такой как Cкаппа;
V2 представляет собой dsFv или dsscFv;
причем по крайней мере один из V1 или V2 представляет собой dsFv или dsscFv, и
где VH и VL вместе образуют связывающий сайт, специфичный в отношении первого антигена, V1 образует связывающий сайт, специфичный в отношении второго антигена, и V2 образует связывающий сайт, специфичный в отношении третьего антигена,
где указанная молекула антитела способна одновременно селективно связывать первый, второй и третий антигены.
2. Молекула триспецифического антитела по п. 1, где Х представляет собой линкер.
3. Молекула триспецифического антитела по п. 1 или 2, где Y представляет собой линкер.
4. Молекула триспецифического антитела по любому из пп. 1-3, где V1 представляет собой dsFv, и V2 представляет собой dsFv.
5. Молекула триспецифического антитела по любому из пп. 1-3, где V1 представляет собой dsscFv, и V2 представляет собой dsscFv.
6. Молекула триспецифического антитела по любому из пп. 1-3, где V1 представляет собой dsscFv, а V2 представляет собой dsFv, или где V1 представляет собой dsFv, а V2 представляет собой dsscFv.
7. Молекула триспецифического антитела по п. 5, где только один из VH/VL, V1 или V2 обладает специфичностью в отношении белка-носителя в сыворотке крови.
8. Молекула триспецифического антитела по п. 7, где белок-носитель в сыворотке крови выбран из группы, состоящей из альбумина, тироксин-связывающего белка, транстиретина, α1-кислого гликопротеина, трансферрина и фибриногена или фрагмента любого из них.
9. Молекула триспецифического антитела по п. 7 или 8, где белок-носитель в сыворотке крови представляет собой человеческий белок-носитель в сыворотке крови, и где указанные VH/VL или V1 или V2, обладающие специфичностью в отношении белка-носителя в сыворотке крови, образуют сайт связывания альбумина.
10. Молекула триспецифического антитела по п. 9, где указанный сайт связывания альбумина включает CDRH1 с последовательностью SEQ ID NO:71, CDRH2 с последовательностью SEQ ID NO:72, CDRH3 с последовательностью SEQ ID NO:73, CDRL1 с последовательностью SEQ ID NO:74, CDRL2 с последовательностью SEQ ID NO:75 и CDRL3 с последовательностью SEQ ID NO:76; или вариабельный домен тяжелой цепи с последовательностью, выбранной из SEQ ID NO:77 и SEQ ID NO:78, и вариабельный домен легкой цепи с последовательностью, выбранной из SEQ ID NO:79 и SEQ ID NO:80.
11. Молекула триспецифического антитела по п. 10, где 6 CDR с SEQ ID NO:71-76 или вариабельные домены с SEQ ID NO:77-80 находятся в положении VH/VL или V1 или V2.
12. Молекула триспецифического антитела по п. 10 или 11, где вариабельный домен тяжелой цепи с последовательностью SEQ ID NO:78 и вариабельный домен легкой цепи с последовательностью ID NO:80 находятся в положении V2, и где вариабельный домен легкой цепи или вариабельный домен тяжелой цепи V2 присоединены к Y, например, через пептидную связь.
13. Молекула триспецифического антитела по любому из пп. 1-12, в которой вариабельный домен легкой цепи или вариабельный домен тяжелой цепи из V1 присоединен к Х, например, с помощью пептидной связи.
14. Молекула триспецифического антитела по любому из пп. 1-13, в которой вариабельный домен легкой цепи или вариабельный домен тяжелой цепи из V2 присоединен к Y, например, с помощью пептидной связи.
15. Молекула триспецифического антитела по любому из пп. 1-14, в которой вариабельные домены легкой цепи и тяжелой цепи из V1 и/или вариабельные домены легкой цепи и тяжелой цепи из V2 связаны дисульфидной связью между двумя сконструированными остатками цистеина.
16. Молекула триспецифического антитела по любому из пп. 1-15, в которой вариабельные домены тяжелой цепи и легкой цепи из V1 и/или V2 связаны дисульфидной связью между двумя остатками цистеина, причем положение пары остатков цистеина выбирают из группы, включающей или состоящей из: VН37 и VL95, VH44 и VL100, VH44 и VL105, VH45 и VL87, VH100 и VL50, VH100b и VL49, VH98 и VL46, VH101 и VL46, VH105 и VL43 и VH106 и VL57, причем значения, относящиеся к VH и VL, выбирают независимо в данном V1 или V2.
17. Молекула триспецифического антитела по п. 16, в которой положением пары сконструированных остатков цистеина является VH44 и VL100.
18. Молекула триспецифического антитела по любому из пп. 1-17, где Х представляет собой пептидный линкер, например, SEQ ID NO:1, 2, 69 и 70.
19. Молекула триспецифического антитела по любому из пп. 1-18, где Y представляет собой пептидный линкер, например, SEQ ID NO:1, 2, 69 и 70.
20. Молекула триспецифического антитела по п. 1, в которой каждый из трех связывающих доменов связывает отличный антиген.
21. Полинуклеотид, кодирующий молекулу триспецифического антитела или его полипептидную цепь по любому из пп. 1-20.
22. Экспрессионный вектор, включающий полинуклеотид или полинуклеотиды, определенные в п. 21.
23. Клетка-хозяин для экспрессирования триспецифического антитела, включающая один или более полинуклеотидов или векторов по п. 21 или 22, соответственно.
24. Клетка-хозяин для экспрессирования триспецифического антитела, включающая два или три вектора, при этом каждый вектор включает полинуклеотид, кодирующий отличную полипептидную цепь молекулы триспецифического антитела по любому из пп. 1-20.
25. Способ получения триспецифического антитела, включающий экспрессию молекулы триспецифического антитела из клетки-хозяина, определенной в п. 23 или 24.
| WO 2013068571, 16.05.2013 | |||
| WO 2013049234 A2, 04.04.2013 | |||
| Снеготаялка | 1929 |
|
SU15992A1 |
| КАТОК МАШИНЫ ДЛЯ УПЛОТНЕНИЯ ГРУНТА | 2012 |
|
RU2578230C1 |
| АНТАГОНИСТЫ АКТИВИНА-ActRIIa-Fc И ИХ ПРИМЕНЕНИЕ ДЛЯ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ | 2008 |
|
RU2473362C2 |
Авторы
Даты
2020-07-06—Публикация
2015-06-25—Подача