Изобретение относится к области технической электрохимии, в частности к нанесению каталитически активных слоев гибридного полимер-оксидного материала (далее гибридного материала) на стальные изделия. Может быть использовано в качестве твердых катализаторов разложения пероксида водорода.
Известны катализаторы разложения пероксида водорода на основе нестехиометрического оксида кобальта на никелевой подложке состава CoxOy(OH)z/Ni, где х=0,65…0,71, y=1,34…1,79, z=1,3…1,52, полученные анодным окислением ионов Со2+ из электролита, содержащего CoSO4 и NH4F, авторов О.А. Стадник, B.C. Воробец, Г.Я. Колбасова [Наноразмерные оксиды титана и кобальта для электродов электрохимических сенсоров кислорода // Химия, физика и технология поверхности. 2007. Вып. 13. С. 173-177]. Их каталитическую активность оценивали в реакции разложения пероксида водорода газометрическим методом по величине константы скорости реакции, определяемой графически. В зависимости от состава электролита значения констант скорости для процесса разложения пероксида водорода в присутствии оксидного соединения кобальта при температуре 30°С составляли (0,109-0,510)⋅10-5моль⋅с-1.
Известен способ получения неорганических/полимерных каталитических гибридных материалов, используемых для иммобилизации комплексных металлических молекулярных катализаторов [Пат. RU №2584988 МПК B01J 31/34, B01J 31/38, опубл. 27.05.2016. Неорганические/полимерные каталитические гибридные материалы с высокой активностью в различных растворителях. 2016. Бюл. №15. Сава Харуо (JP), Барбаро Пьерлуиджи (IT), Бьянкини Клаудио (IT), Лигуори Франческа (IT), Сасика Масатоси (JP)].
Недостатком способа получения данных материалов является многостадийность процесса, заключающегося в приготовлении раствора предшественника путем растворения неорганических оксидов и полимерных добавок с последующей нейтрализацией кислотой в водном растворе, нанесении полученной смеси литьевым способом на пластину, разравнивании раствора ракелем при постоянной скорости до заданной толщины и сушке.
Известен также способ получения электролитических покрытий на основе сплава Ni-Mo и полипиррола, предложенный в работе J. Niedbala, A. Budniok, Е. Lagiewka [Electrolytical Obtaining of Ni-Mo Coating with Polypyrrole // Materials Scienc Forum. 2006. Vols. 514-516. P. 1176-1181].
Процесс осаждения покрытия на поверхности стали проводят из электролита, полученного путем смешения двух растворов в соотношении 1:1. Первый раствор содержит, моль дм-3: Na2MoO4 - 0,035; NiSO4 - 0,75; Na3C6H5O7 - 0,45; рН 6,0-7,0. Второй раствор содержит, моль⋅дм-3: NaClO4 - 0,05; пиррол C4H5N - 0,1. Температура электролиза составляет 25°С.
Недостатками данного способа получения являются трудоемкость процесса, невозможность управления структурой получаемых материалов, невозможность получения гибридных материалов, состоящих из оксидов металлов в полимерном массиве.
Наиболее близким по технической сущности материалом, обладающим каталитической активностью в реакции разложения пероксида водорода газометрическим методом являются каталитически активные оксидные соединения на твердом носителе, полученные авторами Z.I. Bespalova, A.V. Khramenkova [A study of the possibility of obtaining catalytically active oxide compounds on a solid support by transient electrolysis // Russian Journal of Applied Chemistry. 2013. Vol. 86. №4. P. 539-544] методом нестационарного электролиза. Основными фазами данного материала являются оксиды молибдена МоО3, MoO2, Mo18O52, шпинель Fe3O4 и молибдаты кобальта, никеля и железа CoMoO4, NiMoO4, FeMoO4. Каталитическую активность полученных оксидных соединений на твердом носителе исследовали газометрическим методом при температуре 20±2°С в реакции разложения пероксида водорода. Значение константы скорости каталитического разложения пероксида водорода, вычисленное по кинетическому уравнению реакции первого порядка, составило 0,3718⋅10-5 с-1.
Наиболее близким по технической сущности и достигаемому результату предлагаемому способу является способ получения покрытия из оксидов металлов на стали [Пат. RU №2449061 МПК C25D 11/34, C25D 3/56 Способ получения покрытий из оксидов металлов на стали, опубл. 27.04.2012. Ж.И. Беспалова (RU), И.В. Смирницкая (RU), А.В. Храменкова (RU)]. Способ включает оксидирование с использованием переменного тока при температуре 30-40°С в электролите, содержащем лимонную кислоту, соли кобальта, никеля, молибдена, железа, желатин и борную кислоту, а оксидирование осуществляют с использованием переменного асимметричного тока. Недостатком данного способа получения является длительное время формирования оксидной пленки - 60 мин.
Изобретение направлено на повышение каталитической активности гибридных материалов на поверхности стали, снижение энергозатрат и трудоемкости процесса получения гибридных материалов.
Задача в части состава гибридного материала достигается за счет того, что гибридный материал, содержащий оксиды молибдена MoO3, MoO2, Mo18O52, оксид железа (III) Fe2O3, а также молибдаты кобальта, никеля и железа CoMoO4, NiMoO4, FeMoO4, дополнительно содержит поливинилпирролидон, в матрицу которого иммобилизованы MoO3, MoO2, Mo18O52, Fe2O3, CoMoO4, NiMoO4, FeMoO4.
А в части способа достигается в осаждении каталитически активных слоев гибридного материала на стали на основе оксидов молибдена MoO3, MoO2, Mo18O52, оксида железа (III) Fe2O3, а также молибдатов кобальта, никеля и железа CoMoO4, NiMoO4, FeMoO4, иммобилизованных в матрицу поливинилпирролидона, путем их осаждения из водного раствора электролита, содержащего соли молибдена, кобальта, никеля, железа и водорастворимый полимер - поливинилпирролидон при соотношении средних за период катодного и анодного токов 1,3:1, рН 4-5, температуре 60°С, при следующем соотношении компонентов (г⋅л-1):
Введение в состав электролита поливинилпирролидона позволяет получить гибридный материал на основе оксидных соединений переходных металлов и полимера на твердом носителе. Гибридные материалы такого рода позволяют объединить заданные свойства и гибкость органического полимера с высокой термической и механической стабильностью, а также транспортными свойствами неорганических оксидов.
Переменный ток при соответствующей форме дает возможность нанесения гибридного материала на твердый носитель при пониженных температурах; делает процесс более энергетически выгодным ввиду возможности использования низких напряжений; увеличивает скорость электролиза и, соответственно, производительность процесса; позволяет в широком интервале изменять физико-химические свойства гибридных материалов с помощью параметров электролиза (плотности тока, состава и концентрации компонентов электролита) и получать более плотные и высокодисперсные осадки, а также повысить верхний предел рабочей плотности тока и снизить внутреннее напряжение. То есть позволяет регулировать чисто электрическим путем свойства гибридных материалов. Такие материалы, получаемые на токе переменной полярности, отличаются от гибридных материалов, полученных на постоянном токе, более развитой микроструктурой, пористостью и повышенными механическими характеристиками.
Предлагаемый способ получения гибридного материала на стали на основе оксидов переходных металлов (молибдена, железа, кобальта и никеля), иммобилизованных в полимерную матрицу поливинилпирролидона, позволил:
- снизить плотность тока и напряжение при оксидировании;
- снизить время электролиза;
- получить гибридный материал на твердом носителе;
- реализовать процессы комплексообразования в твердой фазе;
- реализовать равномерное распределение оксидных соединений переходных металлов в полимерном массиве;
- увеличить каталитическую активность материалов подобного рода в реакции разложения пероксида водорода.
Формирование гибридных материалов проводили на предварительно подготовленной по стандартной методике поверхности стали марки Ст3 при поляризации переменным асимметричным током промышленной частоты, представляющим собой две полусинусоиды разной амплитуды из электролита, содержащего соли молибдена, никеля, кобальта, железа, лимонную и борную кислоты, поливинилпирролидон. В качестве рабочего электрода использовали макроэлектроды из Ст3 30×20×2 мм (с обеих сторон). Противоэлектродом служил кобальт.
Для экспериментальной проверки предлагаемого способа были сформированы слои гибридного материала на поверхности стали.
Пример. Пластины стали марки Ст3 размером 30×20×2 мм (с обеих сторон), предварительно подготовленные по стандартной методике, погружали в водный раствор электролита следующего состава:
и получали гибридный материал при соотношении средних за период катодного и анодного тока 1,3:1, напряжении 15-20 В, температуре 60°С. Время электролиза составило 40 мин.
Анализ вещества гибридных материалов осуществляли с использованием порошкового рентгеновского дифрактометра ARL X'tra (2007). Съемку проводили на излучении CuKα1 (длина волны 1,5406 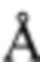 ) со скоростью 5 град⋅мин-1. Ввиду рентгеноаморфности гибридный полимер-оксидный материал перед проведением рентгенофазового анализа термообрабатывали в атмосфере кислорода при температуре 650°С в течение 40 мин. Расшифровку рентгенограмм осуществляли с использованием базы данных PDF - 2. Исследование микроструктуры поверхности образцов гибридного материала проводили с помощью метода электронной микроскопии на двулучевой станции (FIB-SEM) Zeiss Crossbeam 540. Элементный состав определяли с использованием рентгеновского микрофлуоресцентного спектрометра Bruker М4 TORNADO с пространственным разрешением до 25 мкм. Съемку ИК спектров поглощения проводили с помощью инфракрасного Фурье спектрометра Bruker VERTEX 70. ИК - спектры поглощения снимали как для чистого ПВП, так и для гибридного материала.
) со скоростью 5 град⋅мин-1. Ввиду рентгеноаморфности гибридный полимер-оксидный материал перед проведением рентгенофазового анализа термообрабатывали в атмосфере кислорода при температуре 650°С в течение 40 мин. Расшифровку рентгенограмм осуществляли с использованием базы данных PDF - 2. Исследование микроструктуры поверхности образцов гибридного материала проводили с помощью метода электронной микроскопии на двулучевой станции (FIB-SEM) Zeiss Crossbeam 540. Элементный состав определяли с использованием рентгеновского микрофлуоресцентного спектрометра Bruker М4 TORNADO с пространственным разрешением до 25 мкм. Съемку ИК спектров поглощения проводили с помощью инфракрасного Фурье спектрометра Bruker VERTEX 70. ИК - спектры поглощения снимали как для чистого ПВП, так и для гибридного материала.
Морфология поверхности разработанного гибридного материала имеет трещинообразный характер. Его основными компонентами, как показал рентгенофлуоресцентный микроанализ, являются железо, кобальт, никель и молибден.
Основными фазами полученного гибридного материала являются оксиды молибдена MoO3, MoO2, Mo18O52, оксид железа (III) Fe2O3, а также сложные оксиды FeMoO4, NiMoO4, CoMoO4, что согласуется с данными элементного анализа. Из анализа ИК спектров поглощения гибридного материала и чистого поливинилпирролидона видно, что на спектре чистого поливинилпирролидона присутствуют пики, отвечающие валентным колебаниям С=O и C-N при 1665 и 1286 см-1 соответственно, а также деформационным колебаниям СН2 при 1421 см-1. Из сопоставления ИК спектров гибридного материала и чистого поливинилпирролидона видно, что на спектре гибридного полимер-оксидного материала наблюдается синий сдвиг. Он проявляется в смещении характерных полос поглощения в сторону более низких волновых чисел - 1629 см-1 для группы С=O и 1384 см-1 для δ - СН2. Известно, что синий сдвиг колебательной полосы группы С=O может быть отнесен к изменению характера связи р - π, сопряженной с амидной группой поливинилпирролидона. Последнее может быть обусловлено раскрытием полимерных цепей поливинилпирролидона из-за инкорпорирования в их структуру молекул металлов или оксидов металлов. Кроме того, интенсивность и ширина пиков спектра гибридного материала превышают интенсивность и ширину тех же пиков для чистого поливинилпирролидона, что также служит подтверждением внедрения оксидных соединений переходных металлов в полимерную матрицу поливинилпирролидона. Полосы поглощения 1096 и 668 см-1 на спектре гибридного материала могут быть отнесены к связям Со-О и Fe-OH соответственно.
Исследование каталитических свойств гибридных материалов на поверхности стали Ст3 проводили с использованием газометрического метода разложения пероксида водорода. Исследование проводили при комнатной температуре. Концентрацию исходного раствора пероксида водорода определяли по ГОСТ 10929-76. Она составила 11,83%.
Константа скорости процесса каталитического разложения пероксида водорода к газометрическим методом составила 7,58⋅10-5 с-1, что превосходит значение константы скорости каталитического разложения пероксида водорода, вычисленное по кинетическому уравнению реакции первого порядка, равно 0,3718⋅10-5 с-1 для материала, полученного авторами Z.I. Bespalova, A.V. Khramenkova [A study of the possibility of obtaining catalytically active oxide compounds on a solid support by transient electrolysis // Russian Journal of Applied Chemistry. 2013. Vol. 86. №4. P. 539-544].
Концентрация раствора H2O2 после разложения составила 0,12%, что свидетельствует о каталитической активности гибридного материала.
При этом следует отметить, что при использовании в качестве катализатора чистой стали в отсутствии гибридного материала разложение пероксида водорода не наблюдалось.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИОННОГО ЭЛЕКТРОДНОГО МАТЕРИАЛА НА ОСНОВЕ КОБАЛЬТ ВАНАДИЕВОГО ОКСИДА И ОКСИДНЫХ СОЕДИНЕНИЙ МОЛИБДЕНА | 2014 |
|
RU2570070C1 |
| Способ получения гибридного электродного материала на основе углеродной ткани с полимер-оксидным слоем | 2023 |
|
RU2814848C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСИДНОГО ПОКРЫТИЯ НА СТАЛИ | 2010 |
|
RU2449062C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОКРЫТИЯ ИЗ ОКСИДОВ МЕТАЛЛОВ НА СТАЛИ | 2010 |
|
RU2449061C1 |
| ОКСИДНЫЙ КАТАЛИЗАТОР И СПОСОБ ЕГО ПОЛУЧЕНИЯ, А ТАКЖЕ СПОСОБЫ ПОЛУЧЕНИЯ НЕНАСЫЩЕННОГО АЛЬДЕГИДА, ДИОЛЕФИНА И НЕНАСЫЩЕННОГО НИТРИЛА | 2013 |
|
RU2615762C2 |
| СПОСОБ ПОЛУЧЕНИЯ ГИБРИДНОГО МАТЕРИАЛА ДЛЯ ЭЛЕКТРОДОВ ХИМИЧЕСКИХ ИСТОЧНИКОВ ТОКА | 2024 |
|
RU2831230C1 |
| Способ получения гибкого электродного материала | 2023 |
|
RU2807173C1 |
| СПОСОБ ОКИСЛИТЕЛЬНОГО ДЕГИДРИРОВАНИЯ МЕТАНОЛА | 2010 |
|
RU2443464C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИБКОГО АНОДНОГО МАТЕРИАЛА НА ОСНОВЕ МОДИФИЦИРОВАННОЙ УГЛЕРОДНОЙ ТКАНИ | 2024 |
|
RU2826545C1 |
| Способ получения оптически черного гибридного покрытия на стали | 2023 |
|
RU2805024C1 |
Изобретение относится к области технической электрохимии, в частности к нанесению каталитически активных слоев гибридного полимер-оксидного материала на стальные изделия. Описан способ получения каталитически активного гибридного полимер-оксидного материала для разложения пероксида водорода, заключающийся в осаждении каталитически активных слоев гибридного материала на стали, отличающийся тем, что гибридный полимер-оксидный материал на поверхности стали формируют на основе оксидов молибдена MoO3, MoO2, Mo18O52, оксида железа (III) Fe2O3, а также молибдатов кобальта, никеля и железа CoMoO4, NiMoO4, FeMoO4, иммобилизованных в матрицу поливинилпирролидона, путем их осаждения из водного раствора электролита, содержащего соли молибдена, кобальта, никеля, железа и водорастворимый полимер - поливинилпирролидон при соотношении средних за период катодного и анодного токов 1,3:1, рН 4-5, температуре 60°С, при следующем соотношении компонентов (г⋅л-1): гептамолибдат аммония ((NH4)6Mo7O24⋅4H2O) 40,0-50,0, сульфат кобальта (CoSO4⋅7H2O) 80,0-100,0, сульфат железа (II) (FeSO4⋅7H2O) 6,0-12,0, сульфат никеля (NiSO4⋅7H2O) 20,0-30,0, хлорид кобальта (CoCl2⋅6H2O) 10,0-16,0, борная кислота (H3BO3) 20,0-30,0, лимонная кислота (C6H8O7) 3,0-4,0, поливинилпирролидон ((C6H9NO)n) 1,0-6,0. Изобретение направлено на повышение каталитической активности гибридных материалов на поверхности стали, снижение энергозатрат и трудоемкости процесса получения гибридных материалов. 2 н.п. ф-лы, 1 пр.
1. Способ получения каталитически активного гибридного полимер-оксидного материала для разложения пероксида водорода, заключающийся в осаждении каталитически активных слоев гибридного материала на стали, отличающийся тем, что гибридный полимер-оксидный материал на поверхности стали формируют на основе оксидов молибдена MoO3, MoO2, Mo18O52, оксида железа (III) Fe2O3, а также молибдатов кобальта, никеля и железа CoMoO4, NiMoO4, FeMoO4, иммобилизованных в матрицу поливинилпирролидона, путем их осаждения из водного раствора электролита, содержащего соли молибдена, кобальта, никеля, железа и водорастворимый полимер - поливинилпирролидон при соотношении средних за период катодного и анодного токов 1,3:1, рН 4-5, температуре 60°С, при следующем соотношении компонентов (г⋅л-1):
2. Каталитически активный гибридный полимер-оксидный материал для разложения пероксида водорода, полученный способом по п. 1, содержащий оксиды молибдена MoO3, MoO2, Mo18O52, оксид железа (III) Fe2O3, а также молибдаты кобальта, никеля и железа CoMoO4, NiMoO4, FeMoO4, отличающийся тем, что дополнительно содержит поливинилпирролидон, в матрицу которого иммобилизованы MoO3, MoO2, Mo18O52, Fe2O3, CoMoO4, NiMoO4, FeMoO4.
| А.И.Храменкова, Д.Н.Арискина " Исследование топографии поверхности и термических свойств гибридных полимер-оксидных покрытий, полученных методом нестационарного электролиза", 14.01.2019, Южно-Российский государственный политехнический университет имени М.И.Платова | |||
| В.В | |||
| Бочкарев "Оптимизация технологических процессов органического синтеза", 2010 |
Авторы
Даты
2020-09-08—Публикация
2019-08-30—Подача