Изобретение относится к фармакологии и биотехнологии и может быть использовано в медико-биологической промышленности и медицине.
Разработан способ получения фермента метионин - гамма-лиазы (МГЛ) [1] и лекарственное средство в виде готовой лекарственной формы (ГЛФ МГЛ) на основе этого фермента, а также способ применения этого лекарственного средства для торможения роста опухолей: меланомы В 16 - путем комбинированной терапии в сочетании с пиридоксином и немелкоклеточного рака легкого человека - путем комбинированной терапии в сочетании с дексорубицином.
МГЛ (КФ 4.4.1.11) является пиридоксаль-5'-фосфат - зависимым ферментом, катализирующим реакцию γ-расщепления L-метионина с образованием метилмеркаптана, иона аммония и α-кетобутирата:
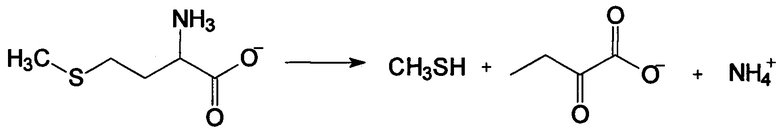
МГЛ также катализирует реакцию β-расщепления L-цистеина и его S-замещенных производных, а также реакции γ- и β-замещения в молекулах L-метионина, L-цистеина и их аналогов [2]. Фермент обнаружен в бактериях Pseudomonas putida, C. freundii, Aeromonas sp., Clostridium sporogenes, Phophyromonas gingivalis, Brevivacterium linens BL2, а также у простейших эукариот Trichomonas vaginalis [3] и Entamoeba histolytica [4]. Однако стационарные кинетические параметры определены лишь для ферментов из P. putida [5, 6], Т. vaginalis [3] и C. freundii [7].
Известны штаммы, которые используют для получения рекомбинантной МГЛ из таких бактерий как P. putida и Т. vaginalis, имеется патент на получение рекомбинантной МГЛ из P. putida [8]. Заявлена возможность улучшения свойств МГЛ при помощи изучения структуры белка и основанной на этом белковой инженерии [9]. Обнаружен ген megL, кодирующий МГЛ в бактериях семейства Enterobacteriaceae [10]. Имеется ряд патентов [11-15], в которых заявлены способы выделения МГЛ, однако отсутствуют стабилизация готовой формы и стадия термообработки в ходе ее выделения и очистки.
Ближайший аналог способа получения фермента метионин-гамма-лиазы изложен в патенте US 5,861,154 [8] заявлена возможность получения рекомбинантной МГЛ с использованием гибридной плазмиды pYH301, в которой ген megL из P. putida расположен под контролем Plac промотора. Способ выделения и очистки фермента не заявлен. Согласно данному патенту инкубация при 37°С в присутствии 1 мМ изопропил-бета-D-1-тиогалактопиранозида (ИПТГ) в течение 17 часов штамма Е. coli JM109, содержащего плазмиду pYH301, приводит к получению биомассы, бесклеточный экстракт которой, обладает целевой активностью 0.82 ед/мг.
Ближайший аналог лекарственного средства - фермент метионин-гамма-лиаза в US 5,861,154[8]. Нет стабилизирующего агента. Противоопухолевая активность показана в публикациях [16-19].
Задачи заявляемой группы изобретений:
- расширить арсенал способов получения фермента МГЛ,
- разработать противоопухолевое лекарственное средство на основе фермента МГЛ.
Задачи решены путем:
- разработки способа получения МГЛ путем культивирования рекомбинантного штамма-продуцента Escherichia coli на богатой питательной среде, содержащей триптон, дрожжевой экстракт, глицерин и глюкозу в фосфатном буфере, а также сульфат аммония и гидроксид натрия, с индукцией биосинтеза лактозой и ИПТГ, и последовательной очистки этого фермента методами хроматографии и ультрафильтрации, включающими стадию термообработки в присутствии этилового спирта,
- разработки противоопухолевого лекарственного средства в виде готовой лекарственной формы ГЛФ МГЛ, включающего фермент МГЛ и трегалозу,
- применения лекарственного средства ГЛФ-МГЛ для торможения роста опухоли - меланома В 16 - путем комбинированной терапии в сочетании с пиридоксином,
- применения лекарственного средства ГЛФ-МГЛ для торможения роста опухоли -немелкоклеточный рак легкого человека - путем комбинированной терапии в сочетании с дексорубицином.
Способ получения фермента МГЛ в общем виде
В качестве штамма - продуцента МГЛ используют клетки штамма Е. coli MDG1216 (ВКПМ В-13174 во Всероссийской коллекции промышленных микроорганизмов), способные синтезировать РНК-полимеразу фага Т7, трансформированные рекомбинантной плазмидой рЕТ 28a::megL_sporogenes, содержащей природную последовательность гена megL под контролем Т7 промотора и терминатора транскрипции. Ген megL, кодирующий МГЛ взят из С. sporogenes [1].
Для биосинтеза используют среду, не содержащую NaCl (Rich medium) [1] с дополнительными добавками в процессе индукции биосинтеза белка, в частности сульфата аммония в количестве 25-350 г/л и, на последней фазе биосинтеза, гидроксида натрия в количестве 0,5-4,0 г/л.
На первом этапе проводят биосинтез МГЛ в биореакторе, что позволяет получить культуру высокой оптической плотности CD600 порядка 50-70 и получить выход целевого продукта порядка 42-55 г мокрой биомассы с литра с содержанием MGL до 45% от общего содержания клеточного белка. Общее время ферментации составляет от 10 до 14 часов.
Полученную в результате биосинтеза биомассу используют для очистки МГЛ. Очистку целевого белка проводят путем дезинтеграции клеток, центрифугированием, прогревом лизатов с этиловым спиртом в концентрации 20 (мас. %) при температуре 50°С, осаждением примесных компонентов с помощью ПЭГ-6000 и последовательной хроматографии на сорбентах Q-Sepharose (Pharmacia & Upjohn), а затем Phenyl-Sepharose FF (Pharmacia & Upjohn) с ультрафильтрацией.
Активность МГЛ определяют с помощью модифицированного метода Ристона [15]. Удельная активность полученной МГЛ в реакции γ-элиминирования L-метионина составляет от 15 до 32 ед./мг с Km 0,7±0,11 mM.
Полученный в результате раствор целевого белка, имеющий чистоту не менее 95% по МГЛ, является фармакологической субстанцией (ФС) и может храниться как минимум 7 дней в темном месте при температуре 4°С.
Для получения заявляемого лекарственного средства ГЛФ МГЛ, к полученной ФС МГЛ добавляют стабилизатор - трегалозу [20] в соотношении 1:1 с последующей лиофилизацией полученного раствора. Полученное лекарственное средство ГЛФ МГЛ представляет собой аморфный порошок, в составе которого присутствуют целевой белок и стабилизатор. ГЛФ может храниться как минимум 2 года в темном месте при температуре 4°С.
Разработано применение заявляемого лекарственного средства ГЛФ МГЛ путем внутрибрюшинного введения в сочетании с пиридоксином или в сочетании с антрациклиновым антибиотиком доксорубицином.
Заявляемая группа изобретений проиллюстрирована следующими фигурами
Фиг. 1. Электрофоретический анализ препарата ГЛФ_МГЛ: 5% - 0,2 мкг; 100% - 4 мкг.
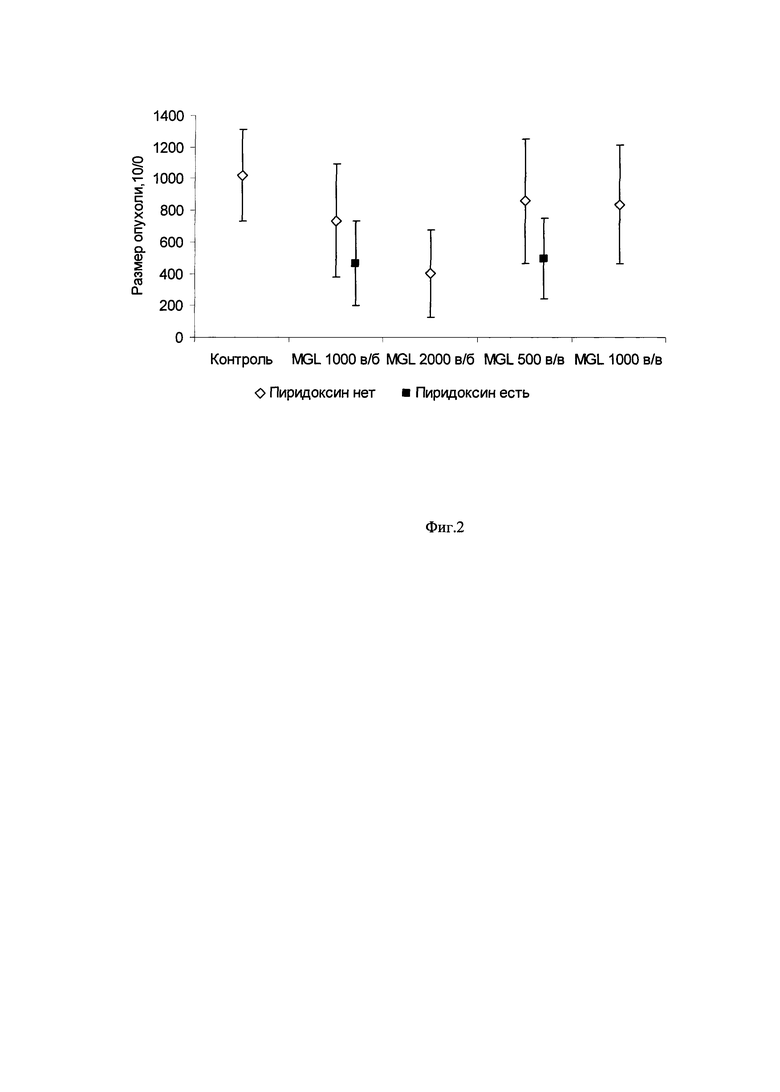
Фиг. 2. Средние размеры опухолей у мышей с меланомой В16, МГЛ или МГЛ + пиридоксин, 10-е сутки, 95% ДИ. MgSO4 *7H2O.
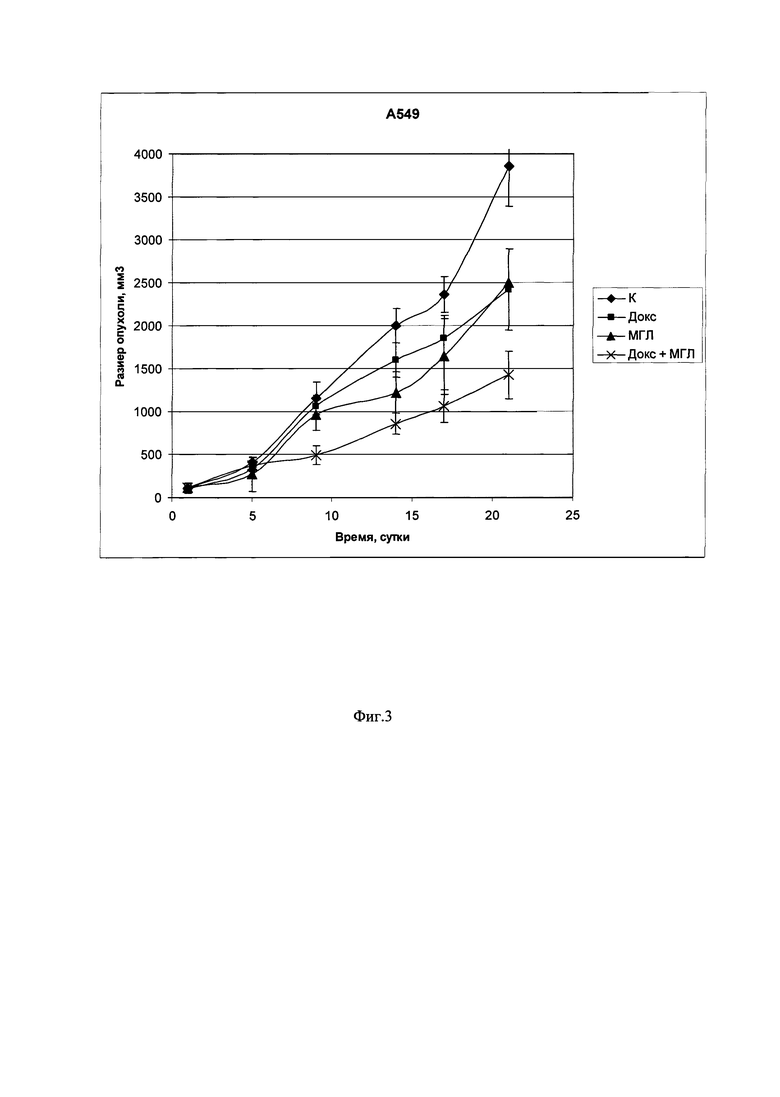
Фиг. 3. Противоопухолевая активность препарата МГЛ на модели ксенографтов опухолей человека у бестимусных мышей (аденокарцинома легкого Льюис А549). Зависимость размера опухоли от времени после трансплантации. K - без терапии, Доке - терапия доксорубицином 2 мг/кг пятикратно, МГЛ - терапия ГЛФ МГЛ 1000 ед/кг десятикратно.
Пример 1. Получение фермента МГЛ
Биосинтез МГЛ осуществляют в биореакторе объемом 15 дм (рабочий объем ~ 10 л) с использованием штамма Е. coli MDG1216, полученного путем трансформации Е. cjli BL21 (DE3), плазмидой pET-28a::megL-Sporogenes [1]. Данный штамм обеспечивает транскрипцию гена megL находящегося под контролем промотора фага Т7 с лактозным оператором.
Стерилизацию среды проводят в ферментере в объеме 6,3 л Среда имеет следующий состав: триптон, дрожжевой экстракт, глицерин (70, 35 и 31 г, соответственно). Соли: KH2PO4, (NH4)2SO4 и Na2HPO4*12H2O (29,7, 61,2 и 161,1 г., соответственно) стерилизуют отдельно от среды в объеме 450 мл и затем добавляются в ферментёр. Добавки готовят отдельно согласно таблице 1.
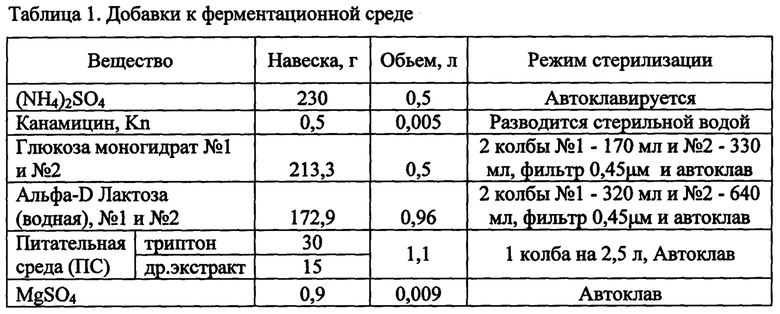
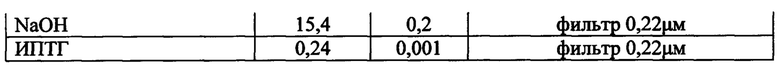
После автоклавирования раствор сульфата аммония и лактозу №2 добавляют к питательной среде (ПС).
Сульфат магния, Kn и глюкозу №1 добавляют в ферментер непосредственно перед засевом. Посевную культуру выращивают в среде триптон, дрожжевой экстракт и глицерин (11,3, 5,6 и 5,3 г/л соответственно) в объеме 300 мл (две колбы по 150 мл) при температуре 37°С, с аэрацией 200 об/мин до оптической плотности (OD=0,5). Ферментацию проводят при 37°С, с аэрацией, обеспечивающей содержание кислорода в среде (DO) кислорода не ниже 20% (после начала индукции DO не должно превышать 60%). Добавление глюкозы №2 начинают при достижении культурой OD=5±l, со скоростью подачи, обеспечивающей содержание глюкозы в среде от 5 до 10 г/л. По окончании добавления глюкозы и достижении культурой OD=25 осуществляют индукцию биосинтеза MGL добавлением в ферментационную среду лактозы №1 и ИПТГ. Через час после начала индукции начинают добавлять ПС с равномерной скоростью 10 мл/мин. Через 3,5 часа после начала индукции начинают добавлять раствор гидроокида натрия с равномерной скоростью 3 мл/мин. Аммиаком и серной кислотой поддерживают рН=6,9±0,1. Пеногаситель добавляют по мере появления пены. Контроль биосинтеза осуществляют по появлению в выхлопе метилмеркаптана и нежно-розовой окраски биомассы. В случае биосинтеза МГЛ из С. sporogenes в клетках Е. coli интенсивность окраски неплохо коррелирует с процентным содержанием МГЛ и удельной активностью на грамм биомассы. Общее время ферментации 12,5 часов.
В результате ферментации получено от 510 г мокрой биомассы с содержанием MGL порядка 44% от общего содержания клеточного белка.
Пример 2. Очистка фермента МГЛ
Полученную в ходе ферментации биомассу используют для выделения целевого белка. Для этого 200 г клеток суспендируют в соотношении 1:5 в 10 мМ калий-фосфатном буфере, рН 7,2, содержащем 0,001 М тетранатриевую соль этилендиаминтетрауксусной кислоты, 0,01% дитиотреитол, 0,01 мМ пиридоксальфосфат (буфер 1). Разрушение клеточной биомассы проводят на дезинтеграторе APV-1000 в присутствии 1 мМ фенилметилсульфонилфторида. Клеточный лизат центрифугируют, супернатант подвергают термообработке (50°С) в присутствии 20 мас. % этилового спирта. Далее проводят осаждение примесных компонентов с помощью раствора ПЭГ 6000 (конечная концентрация 10%).
Полученный супернатант после разведения в 2,5 раза наносят на колонку с сорбентом Q-Sepharose, уравновешенным буфером 1. Основной пик элюируют с колонки 0,3 М KCl в том же буфере. Ультрафильтрацию собранного пика осуществляют на установке «VivaFlow» с использованием мембранного модуля с порогом отсечения 50 кДа. После увеличения содержания KCl в ретентате до 1 М, раствор наносят на колонку с сорбентом Phenyl-Sepharose FF, уравновешенным буфером 1, содержащим 1 М KCl. Целевой фермент в данных условиях не связывается с сорбентом и выходит в проскоке. Концентрирование фракции, содержащей МГЛ, проводят на установке Amicon на мембране UM-50. Содержание KCl в концентрате составляет до 1,5 М; концентрат наносят на колонку с сорбентом Phenyl-Sepharose FF, уравновешенным буфером 1, содержащим 1,5 М KCL. МГЛ элюируют с колонки путем снижения содержания соли в буфере до 0,75 М.
Контроль примесей в препарате целевого белка осуществляют с помощью электрофореза в полиакриламидном геле (SDS-PAAG) в денатурирующих условиях [21] с нанесением на дорожку не менее 4 мкг препарата (Фиг. 1).
В результате получают гомогенный препарат МГЛ (содержание целевого белка не менее 95%), который обладает в реакции γ-элиминирования L-метионина удельной активностью 24 ед/мг с Km 0,7±0,11 mM. Активность МГЛ определяют с помощью модифицированного метода Ристона [22]. Хранение полученного раствора МГЛ при +2-8°С допустимо до 7 дней.
Пример 3. Получение лекарственного средства ГЛФ МГЛ
Обессоливание полученного раствора МГЛ и перевод в 20 мМ натрий-фосфатный буфер, рН 7,2, содержащий 0,15 М натрия хлорид, 0,01 мМ пиридоксальфосфат, проводят с помощью ультрадиафильтрации на установке «VivaFlow» (Sartorius) с использованием мембраны с порогом отсечения 50 кДа. К полученному раствору белка добавляют трегалозу в соотношении ~1:1 (по массе).
Конечный препарат подвергают стерилизующей фильтрации. Стерильный раствор лекарственного средства разливают по флаконам из темного стекла (2000±200 МЕ/флакон) и лиофилизируют (ALPHA 1-4 LD). Хранение при +2-8°С.
Пример 4. Оценка влияния лекарственного средства ГЛФ МГЛ на развитие опухоли меланомы В16
Влияние ГЛФ МГЛ на развитие опухоли на модели перевиваемой опухоли меланомы В16 оценивают при многократном введении в следующих комбинациях:
1) ---Эффект ГЛФ МГЛ при терапии мышей с опухолью в монотерапии.
2) ---Эффект ГЛФ МГЛ при терапии мышей с опухолью в комбинированной терапии в сочетании с пиридоксином при внутривенном и внутрибрюшинном введении препарата.
Клетки меланомы В16 перевивают на самках и самцах мышей линии С57В16 подкожно по 0,5 мл взвеси опухолевой ткани в растворе Хенкса или среде 199 (1:10) через 12-16 дней. Перевиваемость 100%. Средняя продолжительность жизнв (СПЖ)=21-31 день.
Животных содержат в контролируемых условиях окружающей среды (18-22°С, относительная влажность 50-65%). Мониторинг температуры и влажности осуществляют с помощью климатической установки. В комнатах содержания животных поддерживают 12 ч. цикл освещения при 8-10-кратной смене объема воздуха в час.
Животных акклиматизируют в виварии в течение 14 дней до введения в эксперимент. Во время этого периода осуществляют ежедневный осмотр внешнего состояния животных. Животных с обнаруженными в ходе осмотра отклонениями в экспериментальные группы не включают.
В день начала опыта всех мышей взвешивают на электронных весах MW-T series, с ценой деления 0,01 г («CAS», США) для контроля качества здоровья. В экспериментальные группы отбирают животных без признаков отклонений внешнего вида, случайным образом, с индивидуальным отклонением массы от среднего значения в пределах одного пола не более чем на 20%.
Инъекционные растворы препаратов готовят ex tempore с добавлением изотонического раствора натрия хлорида и вводят мышам внутрибрюшинно (в/б), с помощью одноразовых пластиковых шприцов 1,0 мл. Вводимые дозы каждого препарата рассчитаны индивидуально на мышь.
ГЛФ МГЛ вводят внутривенно (в/в) или в/б 20-кратно в дозах 500, 1000 или 2000 Е/кг, интервал между введениями 12 ч. Пиридоксин вводят в дозе 300 мг/кг. Эффективность лечения мышей оценивают по торможению роста опухоли (ТРО), Значимыми считают ТРО >50%. Показатели эффективности определяют в сравнении с контролем (животные без лечения) [23].
Статистический анализ данных проводят в программе IBM SPSS Statistics 21. Сравнения выполняют с помощью одно- и двухфакторного дисперсионного анализа, попарные сравнения групп по критерию Тьюки [1]. Приведены среднее и среднеквадратическое отклонение (M±s). Различия считают значимыми при р≤0,05.
В таблице 2 и на фиг. 2 приведены данные влияния ГЛФ МГЛ в монотерапии и в сочетании с пиридоксином при внутривенном и внутрибрюшинном введении. 
Для модели меланомы В16 показана умеренная чувствительность к терапии ГЛФ МГЛ. Добавление к схеме лечения пиридоксина достоверно повышает противоопухолевую активность фермента. По сравнению с контрольной группой на 10-е сутки после трансплантации наблюдают достоверный значимый противоопухолевый эффект: ТРО 59% в 1-ый день после окончания лечения в группе 2000 Е/кг в/б (р=0,045), 53% в 1-ый день после окончания лечения в группе МГЛ 1000 Е/кг в/б + пиридоксин (р=0,085 различия не достоверны) и 50% в 1-ый день после окончания лечения в группе 500 Е/кг в/в + пиридоксин (р=0,104 различия недостоверны).
Различия между группами МГЛ 1000 Е/кг в/б + пиридоксин и МГЛ 1000 Е/кг в/б достоверно отличаются на 3 сутки после окончания лечения (р=0,034 различия достоверны), что говорит о влиянии пиридоксина на повышение противоопухолевой активности МГЛ при данной схеме лечения. МГЛ 500 Е/кг в/в + пиридоксин и МГЛ 500 Е/кг в/в статистически не достоверны (р>0,05), что говорит о сопоставимой противоопухолевой активности МГЛ и МГЛ в сочетании с пиридоксином.
Пример 5. Оценка влияния лекарственного средства ГЛФ МГЛ на развитие опухоли модель Льюис А549.
Оценку противоопухолевого эффекта ГЛФ МГЛ проводят с использованием модели ксенографтов опухоли человека у бестимусных мышей с аденокарциномой легкого Льюис А549. Проверка влияния ГЛФ МГЛ на развитие опухоли на указанной модели перевиваемой опухоли человека осуществляют в комбинации с доксорубицином при многократном введении:
1) Эффект ГЛФ МГЛ при терапии мышей с опухолью в монотерапии.
2) Эффект комбинированного воздействия МГЛ и доксорубицина на рост опухоли.
Для оценки эффективности комбинированной терапии с доксорубицином используют следующие дозировки:
1) МГЛ вводят в дозе 1000 Е/кг 10-кратно с интервалом 24 ч.
2) Доксорубицин вводят в дозе 2 мг/кг 5-кратно с интервалом 48 ч.
Мышей содержат в стерильных клетках с аэросистемой по 2 особи в каждой в специализированном однокоридорном кондиционируемом отсеке при температуре 26-28°С и нормированной влажности на стерильных экструдированных кормах и стерильной питьевой воде.
Используют адаптированную к росту in vivo у бестимусных мышей опухоль человека -немелкоклеточный рак легкого А549.
Взвесь клеток имплантируют мышам под кожу бока по 3,5-5,0 млн клеток на мышь. Опухоль от доноров извлекают и используют для приготовления прививочного материала. Инокулят для трансплантации мышам готовят из опухолевых узлов (1-3 пассажи). Последние после достижения объема 0,8-1,0 см3 дезинтегрируют механически с помощью медицинских ножниц и затем готовят 10% взвесь ткани опухоли ex tempore в питательной среде 199. Полученную взвесь трансплантируют мышам под кожу бока по 0,4 мл на мышь стерильным пластиковым шприцем 1,0 мл с иглой 18G. Перед каждой инъекцией взвесь 4-5 раз перемешивают с помощью индивидуального шприца. Кожу в месте инъекции предварительно обрабатывают 70% спиртом. Между инъекциями чашка Петри с имплантационной взвесью остается закрытой стерильной крышкой. После инъекции иглу извлекают, плотно захватывая вместе со складкой кожи для предупреждения вытекания взвеси.
Инъекционные растворы препаратов готовят ex tempore с добавлением изотонического раствора натрия хлорида и вводят мышам в/б с помощью одноразовых пластиковых шприцов 1,0 мл. Вводимые дозы каждого препарата рассчитаны индивидуально на мышь. ГЛФ МГЛ вводят в/в или в/б 20-кратно в дозах 500, 1000 или 2000 Е/кг, интервал между введениями 12 ч. Пиридоксин вводят в дозе 300 мг/кг.
Эффективность лечения мышей оценивают по торможению роста опухоли (ТРО), Значимыми считают ТРО >50%. Показатели эффективности определяют в сравнении с контролем [12].
Статистический анализ данных выполняют в среде пакета IBM SPSS Statistics 21. Сравнения выполняют с помощью одно- и двухфакторного дисперсионного анализа, попарные сравнения групп по критерию Тьюки. Приведены среднее и среднеквадратическое отклонение (M±s). Различия считают значимыми при р≤0,05.
На фиг. 3 приведены данные влияния ГЛФ МГЛ в монотерапии и в сочетании с доксорубицином при внутрибрюшинном введении.
Лечение начинают при достижении опухоли средних размеров 100-120 мм3.
Видно, что монотерапия как доксорубицином, так и МГЛ слабо эффективна, на 14-е сутки после начала лечения (5-е сутки после окончания лечения) ТРО в группе доксорубицина составляет 20%, в группе МГЛ - 39%. В группе МГЛ, хотя не были достигнуты значения биологически значимого ТРО >50%, различия с контрольной группой достоверны, из-за небольшого разброса значений размеров опухолей между группами (р=0.008). Максимальный эффект достигнут в группе комбинированной терапии доксорубицином и МГЛ, ТРО=57% (р<0.001). Указанный эффект сохраняется на протяжении 12 суток после окончания терапии (до окончания эксперимента). Переносимость мышей удовлетворительная, гибели животных от токсичности не отмечено.
Таким образом, разработан способ получения фермента МГЛ, который позволяет синтезировать до 45% МГЛ, в расчете на суммарный клеточный белок, с удельной активностью от 15 до 32 ед./мг с Km порядка 0,7±0,11 mM в реакциях γ-элиминирования для природного субстрата L-метионина.
Заявляемое лекарственное средство ГЛФ МГЛ обладает противоопухолевым эффектом (более 50% ТРО), что продемонстрировано при применении его для торможения роста опухоли - меланома В 16 - путем комбинированной терапии в сочетании с пиридоксином, а также для торможения роста опухоли - немелкоклеточный рак легкого человека - путем комбинированной терапии в сочетании с доксорубицином.
Источники информации
1. Anufrieva NV, Morozova ЕА, Kulikova VV, Bazhulina NP, Manukhov IV, Degtev DI, Gnuchikh EY, Rodionov AN, Zavilgelsky GB, Demidkina TV. (2015) Acta Naturae., 7(4): 128-35.
2. Tanaka, H., Esaki, N. & Soda, K. (1985) Enzyme Microb. Technol, 7, 530-537.
3. McKie, A.E., Edlind, Т., Walker, J., Mottram, J.M. & Coombs, G.H. (1998) J. Biol. Chem., 273, 5549-5556.
4. Tokoro, M., Asai, Т., Kobayashi, S., Takeuchi, Т., Nozaki, T. (2003) J. Biol. Chem., 278, 42717-42727
5. Esaki, N., Nakayama, Т., Sawada, S., Tanaka, H., and Soda, K. (1985) Biochemistry, 24, 3857-3862.
6. Inoe, H., Inagaki, K., Adachi, N., Tamura, Т., Esaki, N., Soda, K. & Tanaka, H. (2000). Biosci. Biotechnol. Biochem., 64, 2336-2343.
7. Манухов И.В., Мамаева Д.В., Морозова Е.А., Расторгуев С.М., Фалеев Н.Г., Демидкина Т.В., Завильгельский Г.Б. (2006) Биохимия, 71(4): 842-851.
8. United States Patent 5,861,154. Soda, et al. January 19, 1999. Recombinant L-methionine gamma.-lyase.
9. United States Patent 7,118,903. Inagaki, et al. October 10, 2006. L-methionine gamma-lyase with modified function.
10. Manukhov IV, Mamaeva DV, Rastorguev SM, Faleev NG, Morozova EA, Demidkina TV, Zavilgelsky GB. (2005) J Bacteriol. 187(11): 3889-93.
11. WO/2015/121348 PHARMACEUTICAL COMPOSITION COMPRISING ERYTHROCYTES ENCAPSULATING A PLP-DEPENDENT ENZYME AND ITS COFACTOR 20/08/2015
12. US 6,461,851 High expression modules containing two or more tandem copies of a methioninase encoding sequence 05/01/2000
13. US 5888506 A Methioninase formulations 19.08.1997
14. US 5715835 A Methods for treating and reducing the potential for cardiovascular disease using methioninase compositions 07.01.1995
15. US 5690929 Use of methioninase and chemotherapy agents in chemotherapy
16. Hoffman R.M., 2015, Expert Opin. Biol. Ther. 15(1), 21-31
17. Tan Y., Xu M., Tan X.-Z., Tan X., Wang X., Saikawa Y., Nagahama Т., Sun X., Lenz M., Hoffman R.M. 1997. Protein. Exp. Purif. 9,233-245,
18. Yoshioka Т., Wada Т., Uchida N., Maki H., Yoshida H., Ide N., Kasai H., Hojo K., Shono K., Maekawa R., Yagi S., Hoffman R.M. 1998. Cancer Res. 58, 2583-2587,
19. Tan Y., Xu M., Hoffman R.M. (2010) Anticancer Res., 30, 793-798
20. Патент РФ №2537139.14.01.2009. Порошковые белковые композиции и способы их получения.
21. Laemmli, U.K. (1970). Nature, 227, 680-685.
22. Wriston, J.С. (1970). Asparaginase. Methods in Enzymology, 17A, 732-742
23. Руководство по проведению доклинических исследований лекарственных средств (иммунобиологические лекарственные препараты). Часть вторая / Под ред. А.Н. Миронова. - М.: Гриф и К. 2012; 966
| название | год | авторы | номер документа |
|---|---|---|---|
| Химерный фермент на основе L-метионин-гамма-лиазы, слитой с VHH антителом М456, и фрагмент ДНК, кодирующий указанный фермент | 2022 |
|
RU2813802C1 |
| Химерный фермент МГЛ-S3 - метионин-гамма-лиаза, слитая с S3 доменом белка VGF из Vaccinia virus, способ получения МГЛ-S3 и противоопухолевый препарат на основе этого фермента | 2022 |
|
RU2816486C2 |
| СПЕЦИФИЧЕСКАЯ СОЧЕТАННАЯ ТЕРАПИЯ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ ЦИТОСТАТИКОМ И ЕГО МОДИФИКАТОРОМ | 2015 |
|
RU2571551C1 |
| СРЕДСТВО С ПРОТИВООПУХОЛЕВОЙ И АНТИМЕТАСТАТИЧЕСКОЙ АКТИВНОСТЬЮ, ПРОТИВОВОСПАЛИТЕЛЬНЫМ И ПРОТИВОАЛЛЕРГЕННЫМ ДЕЙСТВИЕМ | 2018 |
|
RU2686672C1 |
| Противоопухолевое средство в виде ультракоротких одноцепочечных полидезоксирибонуклеотидов | 2022 |
|
RU2794757C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЭРИТРОЦИТЫ, В КОТОРЫХ ЗАКЛЮЧЕН ФЕРМЕНТ, ЗАВИСИМЫЙ ОТ ПИРИДОКСАЛЬФОСФАТА, И ЕГО КОФАКТОР | 2015 |
|
RU2697086C2 |
| СПОСОБ ПОТЕНЦИРОВАНИЯ АКТИВНОСТИ ПРОТИВООПУХОЛЕВЫХ ЦИТОСТАТИЧЕСКИХ ПРЕПАРАТОВ | 2017 |
|
RU2714140C2 |
| СРЕДСТВО, УСИЛИВАЮЩЕЕ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ ХИМИОПРЕПАРАТОВ, И СПОСОБ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2002 |
|
RU2250775C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЭРИТРОЦИТЫ, В КОТОРЫХ ЗАКЛЮЧЕН ФЕРМЕНТ, ЗАВИСИМЫЙ ОТ ПИРИДОКСАЛЬФОСФАТА, И ЕГО КОФАКТОР | 2015 |
|
RU2744659C2 |
| СРЕДСТВО И СПОСОБ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2005 |
|
RU2283658C1 |
Изобретение относится к области биотехнологии. Разработан способ получения фермента метионин-гамма-лиазы (МГЛ) и противоопухолевое лекарственное средство ГЛФ МГЛ на основе этого фермента. Способ с использованием штамма Е.coli MDG1216 позволяет синтезировать до 45% МГЛ, в расчете на суммарный клеточный белок, с удельной активностью от 15 до 32 ед./мг с Km порядка 0,7±0,11 mM в реакциях γ-элиминирования для природного субстрата L-метионина. Заявляемое лекарственное средство ГЛФ МГЛ обладает противоопухолевым эффектом (более 50% ТРО), что продемонстрировано при применении его для торможения роста опухоли - меланома В 16 - путем комбинированной терапии в сочетании с пиридоксином, а также для торможения роста опухоли - немелкоклеточный рак легкого человека - путем комбинированной терапии в сочетании с дексорубицином. 2 н.п. ф-лы, 3 ил., 4 пр., 2 табл.
1. Способ получения фермента метионин-гамма-лиазы путем культивирования рекомбинантного штамма-продуцента Esherichia coli на среде, содержашей триптон, дрожжевой экстракт, глицерин и глюкозу в фосфатном буфере, индукции биосинтеза фермента лактозой и изопропил-бета-D-1-тиогалактопиранозидом, очисткой фермента методами хроматографии и ультрафильтрации, отличающийся тем, что в качестве штамма-продуцента используют штамм Esherichia coli ПКПМ В-13174, в среду для культивирования дополнительно добавляют сульфат аммония от 25 до 60 г/л и гидроксид натрия от 0,5 до 4 г/л, а в стадию очистки дополнительно включают термообработку в присутствии этилового спирта при 50°С, причем гидроксид натрия вносят на последней стадии биосинтеза.
2. Применение метионин-гамма-лиазы, полученной способом по п.1, для торможения роста опухоли – немелкоклеточного рака легкого человека – путем комбинированной терапии в сочетании с доксорубицином.
| US 5861154 A, 19.01.1999 | |||
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК pMSIN4, КОДИРУЮЩАЯ ГИБРИДНЫЙ ПОЛИПЕПТИД - ПРЕДШЕСТВЕННИК ИНСУЛИНА ЧЕЛОВЕКА, ШТАММ BL21(DE3)/pMSIN4-ПРОДУЦЕНТ РЕКОМБИНАНТНОГО ИНСУЛИНА ЧЕЛОВЕКА, СПОСОБ ПОЛУЧЕНИЯ РЕКОМБИНАНТНОГО ИНСУЛИНА ЧЕЛОВЕКА | 2011 |
|
RU2447149C1 |
| ШТАММ-ПРОДУЦЕНТ БЕЗМЕТИОНИНОВОГО CRM197 НА ОСНОВЕ КЛЕТОК E. coli BL21 (DE3) | 2015 |
|
RU2575621C1 |
| В.В.СОВА, М.И.КУСАЙКИН | |||
| Выделение и очистка белков | |||
| Методическое пособие по курсу "Химия и биохимия белков и ферментов", Владивосток, 2006 | |||
| Д.Ж.ДАВЫДОВ и др | |||
| ИСПОЛЬЗОВАНИЕ ПИРИДОКСИНА ДЛЯ ПОВЫШЕНИЯ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТИ МЕТИОНИН-ГАММА-ЛИАЗЫ НА МОДЕЛЯХ | |||
Авторы
Даты
2020-10-01—Публикация
2018-06-04—Подача