Изобретение относится к фармакологии и биотехнологии и может быть использовано в медико-биологической промышленности и медицине.
Разработан химерный фермент L-метионин-гамма-лиаза (МГЛ) [1] сшитый с S3 доменом ростового фактора VGF (vaccinia growth factor) [2] вируса оспы. Химерный белок, получивший название МГЛ-S3, проявляет метиониназную активность и способен задерживаться на поверхности опухолевых клеток за счёт взаимодействия с рецептором эпидермального ростового фактора (EGFR). Разработан способ получения (биосинтеза, выделения и очистки) МГЛ-S3 и хранения его в лиофильно высушенном виде. Протестировано воздействие препарата МГЛ-S3 на клетки линий нейробластомы SH-SY5Y и аденокарциномы A549. Для клеток протестированных линий раковых клеток показана цитотоксичность препарата МГЛ-S3. При смене культивационной среды МГЛ-S3 способен задерживаться на клетках и продолжать расщепление метионина, сохраняя тем самым цитотоксическое воздействие.
МГЛ (КФ 4.4.1.11) является пиридоксаль-5'-фосфат - зависимым ферментом, катализирующим реакцию γ-расщепления L-метионина с образованием метилмеркаптана, иона аммония и α-кетобутирата:
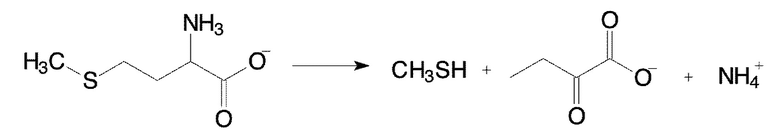
МГЛ также катализирует реакцию β-расщепления L-цистеина и его S-замещенных производных, а также реакции β- и γ-замещения в молекулах L-метионина, L-цистеина и их аналогов [3]. Фермент был обнаружен в бактериях Pseudomonas putida, Citrobacter freundii , Aeromonas sp., Clostridium sporogenes, Phophyromonas gingivalis, Brevivacterium linens BL2, а также у простейших эукариот Trichomonas vaginalis [4] и Entamoeba histolytica [5]. Однако стационарные кинетические параметры определены лишь для ферментов из P. putida [6, 7], Т. vaginalis [4] и C. freundii [8].
Известны штаммы, которые используют для получения рекомбинантной МГЛ из таких бактерий как P. putida и T. vaginalis, имеется патент на получение рекомбинантной МГЛ из P. putida [9]. Заявлена возможность улучшения свойств МГЛ при помощи изучения структуры белка и основанной на этом белковой инженерии [10]. Обнаружен ген megL, кодирующий МГЛ в бактериях семейства Enterobacteriaceae [11]. В патенте US 5,861,154 [9] заявлена возможность получения рекомбинантной МГЛ с использованием гибридной плазмиды pYH301, в которой ген megL из P. putida расположен под контролем Plac промотора. Способ выделения и очистки фермента не заявлен, стабилизирующие агенты не применяются. Согласно данного патента инкубация на 37°С в присутствии изопропил-β-D-1-тиогалактопиранозид (ИПТГ) 1 мМ в течение 17 часов штамма Escherichia coli JM109, содержащего плазмиду pYH301, приводит к получению биомассы, бесклеточный экстракт которой, обладает целевой активностью 0,81 ед/мг.
Противоопухолевая активность МГЛ показана в публикациях [12-17].
В патенте WO2004112717A3 [18] заявлена возможность получения химерно слитых белков МГЛ с коньюгатами, связывающимися с рецепторами ростовых факторов. В качестве лигандов для распознавания гиперэкспрессированных на опухолевых клетках рецепторов были предложены урокиназа, эпидермальный ростовой фактор, трансформирующий ростовой фактор альфа, инсулиноподобный фактор роста, интерлейкин-4, интерлейкин-6, фактор роста тромбоцитов, фактор роста фибробластов, ламинин, фактор роста эндотелий сосудов, аннексин V, различные антитела и фрагменты лигандов. Применение S3 домена ростового фактора вируса оспы в данном документе не описано.
Гиперэкспрессия семейства рецепторов эпидермального фактора роста, в том числе EGFR, - очень распространённый маркер опухолевых клеток [19, 20].
Большинство нативных антагонистов EGFR имеют структуру, состоящую из трех дисульфидный петель [21]. Обычно именно третья дисульфидная цепь ответственна за связывание с рецептором и может использоваться для конструирования таргетных препаратов [22]. Домен S3 (третья дисульфидная петля) белка VGF из вируса оспы применяется для целевого поражения раковых клеток в работах [2], где он используется в составе химерного белка с TNF и GFP. В данных работах необходимо применение ТАТ, HBD или другой системы типа CPP (сell-penetrating peptide) для транспортировки цитотоксического агента в клетку.
Идея применения S3 в составе химерного белка с МГЛ состоит в том, что можно создать безметиониновую зону в организме вокруг раковых клеток в сóлидных (твёрдых) опухолях. В таких условиях отпадает необходимость транспорта МГЛ внутрь раковой клетки.
Ближайший аналог способа получения фермента изложен в патенте РФ № 2733440 [23]. Согласно этому документу для биосинтеза МГЛ (кодируется природным геном без модификаций в гетерологичной системе E. coli) требуется добавление в среду сульфата аммония, очистка включает в себя стадию соосаждения спиртом, а применение в качестве антиракового препарата наиболее успешно в комбинации с доксорубицином. Модификация препарата с целью его таргетирования к раковым клеткам в данном патенте не рассматривается.
Задачи заявляемого изобретения:
- разработать новый химерный белок для использования в качестве препарата в антираковой терапии,
- разработать способ биосинтеза, выделения и очистки фермента МГЛ-S3,
- разработать препарат для терапии рака с возможностью длительного хранения на основе фермента МГЛ-S3.
Задачи решены путем:
- разработки штамма-продуцента, несущего ген, кодирующий химерный фермент - МГЛ слитый с S3 доменом белка VGF из генома вируса оспы;
- разработки способа получения фермента МГЛ-S3 путем культивирования рекомбинантного штамма-продуцента E. coli на богатой питательной среде, содержащей триптон, дрожжевой экстракт, глицерин и глюкозу в фосфатном буфере, с индукцией биосинтеза лактозой и ИПТГ, и последовательной очистки этого фермента методом хроматографии и ультрафильтрации, отличающийся тем, что очистка включает стадию осаждения в 35% сульфате аммония нецелевых белков с последующим осаждением целевого белка в 50% сульфате аммония;
- разработки противоопухолевого препарата с возможностью хранения в течении двух лет в виде лиофилизата, включающего фермент МГЛ-S3, детергент Tween-20, трегалозу или маннозу;
- применения препарата МГЛ-S3 для торможения роста раковых клеток нейробластомы SH-SY5Y и аденокарциномы A549.
Способ получения химерного фермента МГЛ-S3 в общем виде
Ген, кодирующий химерный фермент - МГЛ слитый с S3 доменом белка VGF из генома вируса оспы, получается путём клонирования гена megL (или другого, кодирующего МГЛ), сшитого 3’ концом через последовательность, кодирующую несколько линкерных аминокислот, или без оной с 5’ концом последовательности, кодирующей S3 домен ростового фактора вируса оспы.
Для биосинтеза используют среду, не содержащую NaCl (типа Rich medium) [25] c дополнительными добавками в процессе индукции биосинтеза белка, в частности сульфата аммония до 60 г/л и гидроксид натрия до 4 г/л.
Биосинтез МГЛ-S3 проводят в биореакторе, что позволяет получить культуру высокой оптической плотности OD600 порядка 50-70 и получить выход целевого продукта порядка 42 - 55 г. мокрой биомассы с литра с содержанием МГЛ-S3 от 35 до 45 % от общего содержания клеточного белка. Общее время ферментации составляет от 11 до 14 часов.
Очистка рекомбинантного белка МГЛ-S3 из полученной биомассы проходит в несколько стадий. Клетки биомассы лизируют в присутствии EDTA, PMSF и пиродоксаль-фосфата на поточном дезинтеграторе. Полученный в результате лизиса клеточный дебрис, мембранную фракцию и нерастворимые белки штамма-продуцента отделяют осаждением с помощью центрифугирования. Осветленный лизат подвергают температурной обработке (35°C, 5 минут) в присутствии спирта (20% этанола), образовавшийся осадок отделяют центрифугированием. Надосадочную фракцию наносят на анионо-обменный хроматографический сорбент, например, Q-Sepharose (Cytiva, США) или CПС-Био Q (ООО «Техносорбент», Россия) batch-методом. Перед элюцией целевого белка МГЛ-S3 в градиенте хлористого калия проводят промывку сорбента с нанесенным белком с помощью Triton-X114 с целью очистки целевого белка от липополисахаридов штамма-продуцента. На следующем шаге проводят неизбирательное осаждение сульфатом аммония. Сначала содержание сульфата аммония доводится до 35% с целью высаливания примесных белков, содержащихся в осадке после центрифугирования. Далее во фракции растворимых клеточных белков концентрация сульфата аммония доводится до 50% и МГЛ-S3 теряет растворимость и собирается в осадке после центрифугирования. На данном этапе возможно долговременное хранение МГЛ-S3 в виде сульфатаммонийного осадка при -80°С (до 4 месяцев). После этого осадок растворяют и проводят гель-фильтрацию с целью перевода в буферный раствор соответствующей готовой лекарственной форме, например, на хроматографической колонке Hiprep 26/10 Desalting (Cytiva, США).
Метионазную активность МГЛ-S3 определяют с помощью модифицированного метода Ристона [24], в последовательных ферментативной и колориметрической реакциях на реактив Несслера, дающего возможность определения концентрации аммиака, образующегося после распада метионина. Удельная активность полученной МГЛ в реакции γ-элиминирования L-метионина составляет от 7 до 9 ед./мг.
Полученный в результате раствор целевого белка, имеющий чистоту не менее 90% по МГЛ-S3, является фармакологической субстанцией и может храниться как минимум 7 дней в тёмном месте при температуре 4°С.
Для получения заявляемого препарата МГЛ-S3, к полученной фармакологической субстанции добавляют стабилизатор – трегалозу (или маннозу) в соотношении к белку w/w 28:1 с последующей лиофилизацией полученного раствора. Полученный препарат МГЛ-S3 представляет собой аморфный порошок, в составе которого присутствуют целевой белок, стабилизатор, и компоненты физраствора. Препарат может храниться как минимум 2 года в темноте при температуре 4°С.
Цитотоксическую активность препарата по отношению к раковым клеткам тестируют по торможению роста опухолевых клеток нейробластомы SH-SY5Y и аденокарциномы A549 после добавления в среду МГЛ-S3 из расчёта 0,1-2 ед./мл с помощью окраски пропидий иодидом или стандартного МТТ-теста с последующим подсчётом клеток на проточном цитофлуориметре.
Пример 1. Конструирование гена, кодирующего МГЛ-S3
Синтезируется нуклеотидная последовательность, состоящая из природного гена megL из C. sporogenes, кодирующего МГЛ сшиваемого 3’ концом через линкер, кодирующий 4 Gly с 5’ концом последовательности S3 домена.
Полученный химерный ген megL-4G-S3 клонируется под контроль сильного промотора фага Т7 в составе гибридной плазмиды используя для этого вектор pET-28a. Гибридная плазмида получила название pMGL-S3. Клетки штамма Escherichia coli BL21 (DE3), содержащие в хромосоме ген, кодирующий РНК-полимеразу фага Т7 трансформируются плазмидой pMGL-S3.
Полученный в результате штамм–продуцент, способный синтезировать химерный белок МГЛ-S3, получил название E. coli MBR1701.
Пример 2. Биосинтез целевого белка МГЛ-S3
Биосинтез МГЛ осуществляют в биореакторе объёмом 15 дм3 (рабочий объём ~ 10 л) с использованием штамма E. coli MBR1701. Данный штамм обеспечивает транскрипцию гена megL-4G-S3 находящегося под контролем промотора фага Т7 с лактозным оператором.
Стерилизацию среды проводят в ферментёре в объёме 6,3 л. Среда имеет следующий состав: триптон, дрожжевой экстракт, глицерин (70, 35 и 31 г, соответственно). Соли: KH2PO4, (NH4)2SO4 и Na2HPO4*12H2O (29,7, 61,2 и 161,1 г. соответственно) стерилизуют отдельно от среды в объёме 450 мл и затем добавляются в ферментёр. Добавки готовят отдельно согласно таблице 1.
Таблица 1. Добавки к ферментационной среде
После автоклавирования раствор сульфата аммония и лактозу № 2 добавляют к питательной среде (ПС).
Сульфат магния, канамицин, и глюкозу №1 добавляют в ферментёр непосредственно перед засевом. Посевную культуру выращивают в среде триптон, дрожжевой экстракт и глицерин (11,3, 5,6 и 5,3 г/л соответственно) в объёме 300 мл (две колбы по 150 мл) при температуре 37°С, с аэрацией 200 об/мин до оптической плотности (OD=0,5). Ферментацию проводят при 37°С, с аэрацией, обеспечивающей содержание кислорода в среде (DO) кислорода не ниже 20 % (после начала индукции DO не должно превышать 60%). Добавление глюкозы № 2 начинают при достижении культурой OD = 5±1, со скоростью подачи, обеспечивающей содержание глюкозы в среде от 5 до 10 г/л. По окончании добавления глюкозы и достижении культурой OD = 25 осуществляют индукцию биосинтеза МГЛ-S3 добавлением в ферментационную среду лактозы № 1 и ИПТГ. Через час после начала индукции начинают добавлять ПС с равномерной скоростью 10 мл/мин. Через 3,5 часа после начала индукции начинают добавлять раствор гидрооксида натрия с равномерной скоростью 3 мл/мин. Аммиаком и серной кислотой поддерживают pH=6,9±0,1. Пеногаситель добавляют по мере появления пены. Контроль биосинтеза осуществляют по появлению в выхлопе метилмеркаптана и нежно-розовой окраски биомассы. В случае биосинтеза МГЛ-S3 в клетках E. coli интенсивность окраски неплохо коррелирует с процентным содержанием МГЛ-S3 и удельной метиониназной активностью на грамм биомассы так же как для природного фермента из C. sporogenes. Общее время ферментации 12 часов.
В результате ферментации получают от 440 г мокрой биомассы с содержанием МГЛ-S3 порядка 41 % от общего содержания клеточного белка.
Пример 3. Очистка фермента и получение лиофилизированного фермента МГЛ-S3
Полученную в ходе ферментации биомассу используют для выделения целевого белка. Для этого 200 г клеток суспендируют в соотношении 1:5 в 10 мМ калий-фосфатном буфере, рН 7,2, содержащем 0,001 М тетранатриевую соль этилендиаминтетрауксусной кислоты, 0,01% дитиотреитол, 0,01 мМ пиридоксальфосфат (буфер 1). Разрушение клеточной биомассы проводят на проточном дезинтеграторе M-110P (Microfluidics, США) или APV-1000 (APV Systems, США) в присутствии 1 мМ фенилметилсульфонилфторида. Клеточный лизат центрифугируют при 10000g 40 минут, полученный в супернатанте осветлённый клеточный лизат подвергают термообработке (50оС) в присутствии 20 мас. % этилового спирта и повторно центрифугируют при 10000g 40 минут.
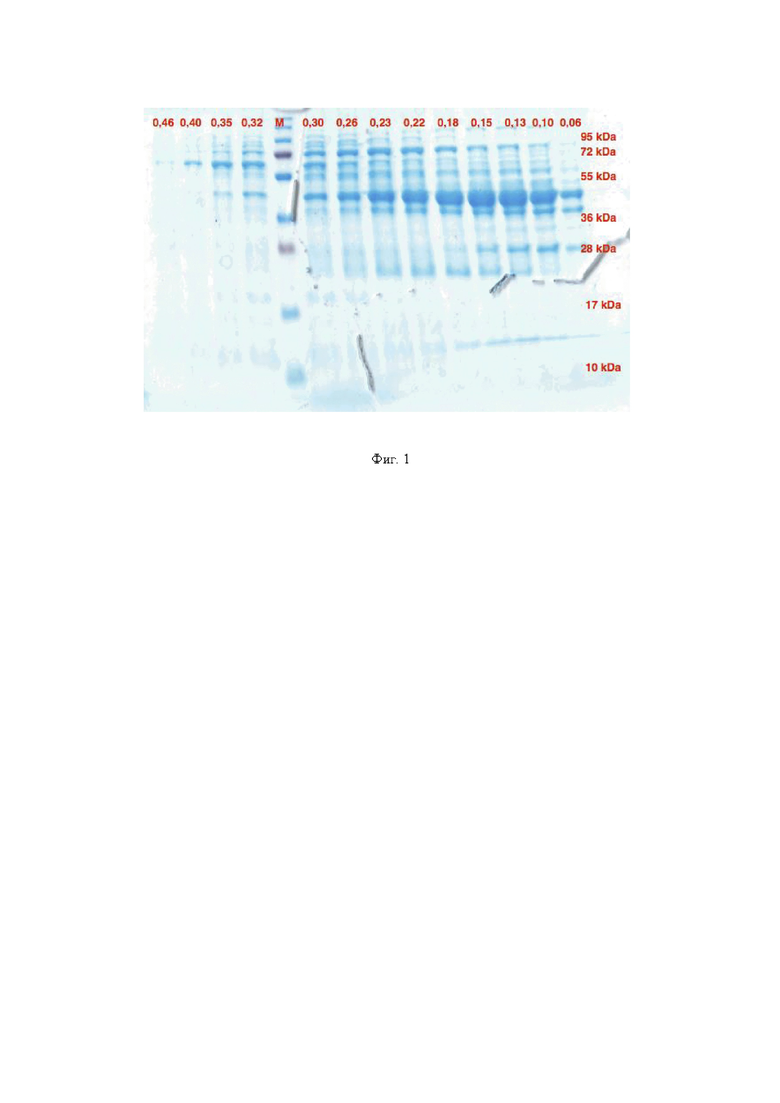
Полученный супернатант после разведения в 2,5 раза наносят на колонку с анионообменным сорбентом, например Q-Sepharose (Cytiva, США) или СПС-био-Q (ООО “Техсорбент”, Россия), уравновешенным буфером 1. Колонку последовательно промывают буфером 1, буфером 1 с добавлением 0,5% (v/v) Triton X-114, буфером 1 с добавлением 5% изопропанола, буфером 1. После промывок сорбента с целью удаления эндотоксинов белок элюируют в градиенте KCl. Целевой белок элюируют в диапазоне концентраций 0,05 M KCl до 0,3 M KCl. Результаты проведения этой стадии очистки проиллюстрированы на фигуре 1. Представлены фракции белка после анионно-обменной хроматографии. Фракции расположены справа налево соответственно росту концентрации KCl от нуля до 1 М. Вверху показана молярность KCl во фракциях. Cправа приведены значения маркера молекулярных масс. Фракции с наибольшим относительным содержанием МГЛ-S3 к примесным белкам расположены в начале грандиента KCl, при концентрациях KCl более 0,2 М начинает элюироваться гораздо больше нецелевых примесных белков штамма-продуцента. Суммарный выход белка после этой стадии составляет приблизительно 50% по отношению к содержавшемуся в биомассе. К собранным фракциям МГЛ-S3 при постоянном перемешивания постепенно добавлять сульфат аммония до содержания 35% (масс.) в буферном растворе. После этого проводят центрифугирование при 10000 g в течении 30 минут. Далее отделяют супернатант декантированием и при постоянном перемешивании доводят степень насыщения сульфатом аммония до 50%. Проводят центрифугирование при 10000 g в течении 30 минут. На фигуре 2 представлена электрофореграмма ПААГ ДСН осадков белка в 35% и 50% сульфате аммония. На дорожки, пронумерованные от 1 до 6, нанесен осадок МГЛ-S3 после 35% сульфата аммония 0,2, 1 и 5 мкг и после 50% сульфата аммония 0,2, 1 и 5 мкг соответственно. Дорожка 7 - маркер молекулярных масс. Как видно из рисунка 2, при высаливании 35% сульфатом аммония удаляется большая часть приместных белков. Cуммарный выход целевого белка на этой стадии – 40% по отношению к содержанию целевого белка в лизируемой биомассе. На фигуре 3 приведена фотография осадка белка в 50% сульфате аммония, характерный оранжевый цвет белка сохраняется и свидетельствует о наличии МГЛ-S3 в осадке.
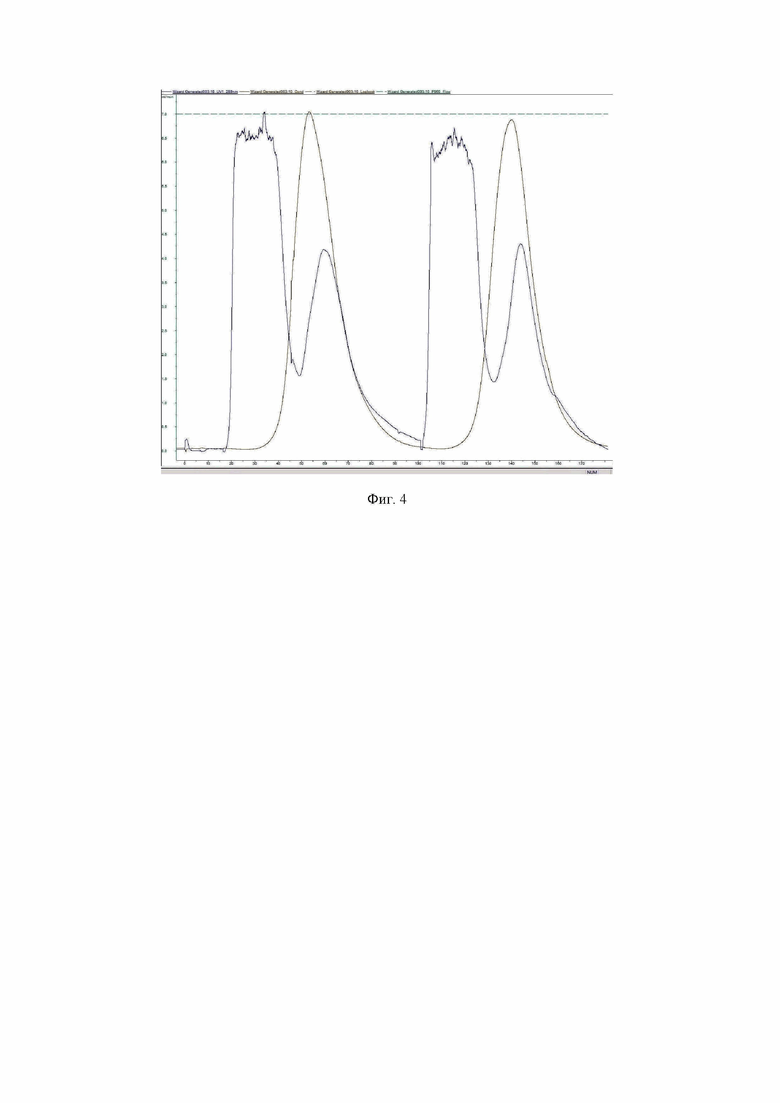
Для отделения от сульфата аммония и полной смены буфера проводится десальтирование с помощью гель-проникающей хроматографии, например на колонке HiPrep 26/10 Desalting (Cytiva, США) или на колонке с аналогичными геометрическими характеристиками заполненной сорбентом СПС-био-ОН (ООО “Техсорбент”, Россия). Осадок растворяют в натрий-фосфатном буфере и наносятся на гель-фильтрационную колонку. На фигуре 4 приведена хроматограмма двух десальтирований с помощью гель фильтрации. Оптическая плотность на 280 нм обозначено синей кривой, проводимость обозначена коричневой кривой. После нанесения образца на колонку целевой белок собирают при начале роста оптической плотности на 280 нм. Cбор образца заканчивают, когда падает оптическая плотность элюата при 280 нм и начинает расти проводимость.
Результатом выделения и очистки белка по описанному методу является раствор белка МГЛ-S3 в фосфатно-солевом буфере с 5-пиридоксаль-фосфатом.
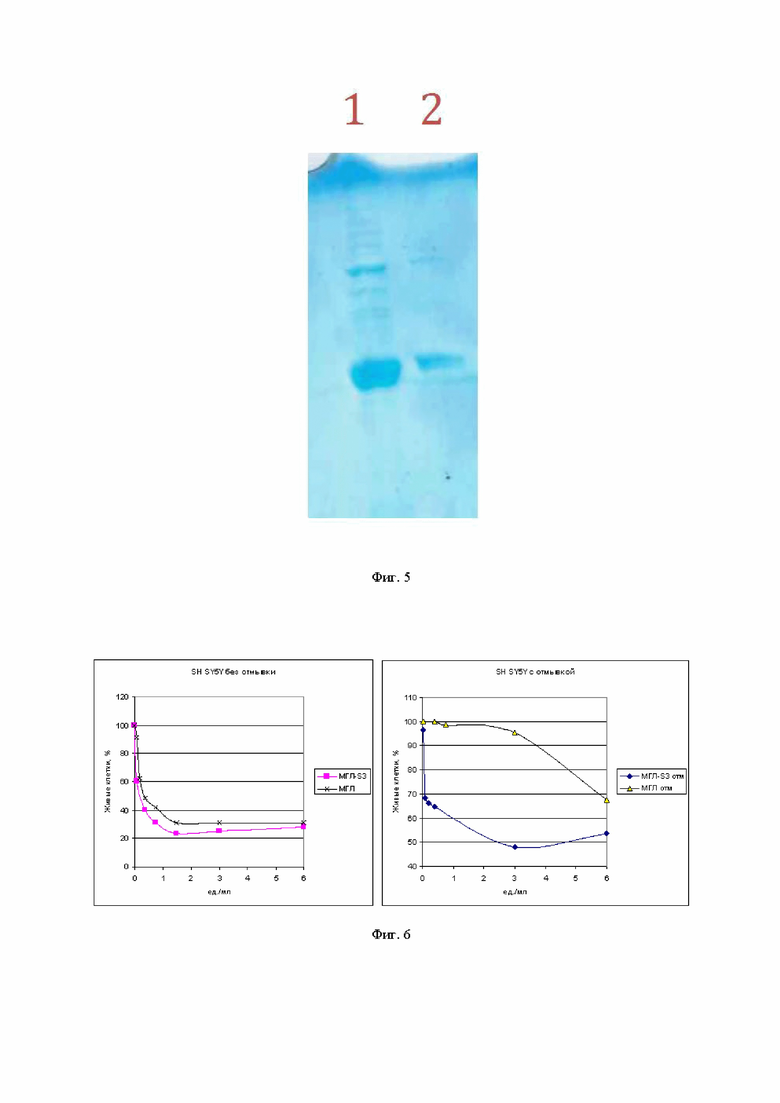
Результаты очистки МГЛ-S3 по описанному методу проиллюстрированы электрофореграммой (ДСН ПААГ) на фигуре 5. На первой дорожке - 2 мкг МГЛ-S3, а на второй - 1 мкг МГЛ-S3. Чистота образца составляет не менее 90%.
Определение активности осуществляется с помощью реактива Несслера, взаимодействующего с аммиаком с образованием продукта оранжевого цвета. Реакционная смесь состояла из 304 мкл рабочего буфера (100 мм калий-фосфатного буфера (рН 8,0), содержащего 0,01 мМ пиридоксальфосфата и 0,01% дитиотреитола) и 76 мкл 100 мм L-метионина. Реакцию инициировали добавлением 20 мкл очищенного фермента (2 мг/мл). Реакционную смесь инкубировали при 37°C в течение 1 мин, затем реакцию останавливали добавлением 100 мкл 1,5 М трихлоруксусной кислоты. Полученную смесь центрифугировали при 10000 g в течение 5 мин на 4°C для удаления осадков. Количество аммиака, выделяющегося в надосадочной жидкости, определяли с помощью колориметрического метода путем добавления 50 мкл реагента Несслера в образец, содержащий 50 мкл надосадочной жидкости и 1150 мкл дистиллированной воды. Содержимое в образце перемешивали и инкубировали при комнатной температуре в течение 12 мин, а OD измеряли при 450 нм. Аммиак, образующийся в результате реакции, определяли на основе стандартной кривой, полученной с сульфатом аммония. Одна единица (Ед) активности L-метиониназы определяется как количество фермента, которое выделяет один мкмоль аммиака в минуту при 37°C. Полученный препарат обладал удельной активностью в районе 8-9 МЕ/мл.
Хранение полученного раствора МГЛ при +2-8оС допустимо до 7 дней.
Для хранения фермента МГЛ-S3 после хроматографической очистки в течении длительного времени его необходимо лиофилизовать. Для этого к раствору МГЛ-S3 добавляют трегалозу или маннозу в соотношении ~28 : 1 (по массе). Полученный препарат подвергают стерилизующей фильтрации. Стерильный раствор фермента разливают по стерильным флаконам темного стекла (2000±200 МЕ/флакон) и лиофилизируют (ЛС -500, «ПроИнТех», РФ). Лиофилизованный продукт хранят при +2-8°С.
Пример 4. Оценка цитотоксического влияния и адгезии фермента МГЛ-S3 на клетках нейробластомы
Влияние МГЛ-S3 на жизнеспособность клеток нейробластомы SH-SY5Y проводилась с помощью окраски пропидий иодидом с последующим подсчётом на проточном цитофлуориметре или стандартного МТТ-теста на 96-луночном планшете.
Клетки выращивались в среде DMEM с добавками в инкубаторе при 37°С и 5% CO2.
При конфлюэнтности 80% клетки в экспоненциальной фазе роста трипсинизировали, суспендировали в свежей среде с добавлением 5×10-5 М PLP и высевали в 96-луночные планшеты в концентрации 4×104 клеток/мл. Клетки обрабатывали 0,4% раствором трипанового синего и подсчитывали с помощью Cell Counter Luna.
Через 24 ч в лунки добавляли различные концентрации испытуемых препаратов, растворенных в фосфатно-солевом буфере. Для исключения неспецифической сорбции препарата после 30 минут инкубации с препаратами часть лунок два раза отмывали средой.
Жизнеспособность клеток оценивали с помощью окраски пропидий иодидом с последующим подсчётом живых клеток и клеток в стадии некроза на проточном цитофлуориметре.
На фигуре 6 показаны результаты подсчёта живых клеток без отмывки (левая картинка) и с отмывкой (правая картинка) для обычного МГЛ и МГЛ-S3 на клеточной линии SH-SY5Y. Как видно из приведённых данных препарат МГЛ-S3 обладает цитотоксическим действием на клетки нейробластомы SH-SY5Y и способен, в отличие от обычной МГЛ, связываться с клетками сохраняя цитотоксическое воздействие после двойной отмывки средой.
Пример 5. Оценка цитотоксического влияния и адгезии фермента МГЛ-S3 на клетки аденокарциномы А549
Клетки немелкоклеточного рака легкого А549 выращивали в среде RPMI 1640 с добавками на матрасах при 37°С и 5% СО2. После конфлюэнтности в 80% клетки в экспоненциальной фазе роста трипсинизировали, суспендировали в свежей среде с добавлением 5×10-5 М PLP и высевали в 96-луночные планшеты в концентрации 4×105 клеток/мл. Клетки обрабатывали 0,4% раствором трипанового синего и подсчитывали с помощью Cell Counter Luna (Logos bio, Корея). Через 24 ч в лунки добавляли различные концентрации испытуемых препаратов, растворенных в фосфатно-солевом буфере. Для исключения неспецифической сорбции препарата после 30 минут инкубации с препаратами часть лунок два раза отмывали средой.
Жизнеспособность клеток оценивали с помощью МТТ-теста. Поглощение кристаллов МТТ-формазона, растворенных в ДМСО, измеряли при 540 нм на планшетном ридере.
На фигуре 7 показаны результаты МТТ-теста без отмывки (левая картинка) и с отмывкой (правая картинка) для обычной МГЛ и МГЛ-S3 на клеточной линии A549. Как видно из приведённых данных препарат МГЛ-S3 обладает цитотоксическим действием на клетки аденокарциномы A549 и способен, в отличие от обычной МГЛ, связываться с клетками сохраняя цитотоксическое воздействие после двойной отмывки средой.
Заключение
Таким образом, разработан способ получения фермента МГЛ-S3, который позволяет синтезировать МГЛ-S3 в количестве до 45%по отношению к суммарному клеточному белку, с удельной активностью порядка 9 ед./мг в реакциях гамма-элиминирования для природного субстрата L-метионина.
Заявленный фермент МГЛ-S3 обладает противоопухолевым эффектом, что продемонстрировано в тестах на клеточную жизнеспособность на клетках нейробластомы SH-SY5Y и аденокарциномы A549, а также способен связываться с ними оставаясь на поверхности клеток при смене культивационной среды.
Использованные источники информации:
1. Anufrieva NV, Morozova EA, Kulikova VV, Bazhulina NP, Manukhov IV, Degtev DI, Gnuchikh EY, Rodionov AN, Zavilgelsky GB, Demidkina TV. Сульфоксиды - аналоги L-метионина и L-цистеина как пролекарства против грамположительных и грамотрицательных бактерий. Acta Naturae. 2015, 7(4):128-35.
2. L.T. Nguyen, X.Z. Yang, X. Du, J.W. Wang, R. Zhang, J. Zhao, F.J. Wang, Y. Dong, P.F. Li, Enhancing tumor-specific intracellular delivering efficiency of cell-penetrating peptide by fusion with a peptide targeting to EGFR, Amino Acids. 2015, 47, 997–1006.
3. Tanaka, H., Esaki, N. & Soda, K. A versatile bacterial enzyme: l-methionine γ-lyase. Enzyme Microb. Technol. 1985, 7, 530-537.
4. McKie, A.E., Edlind, T., Walker, J., Mottram, J.M. & Coombs, G.H. The Primitive protozoon trichomonas vaginalis contains two methionine g-lyase genes that encode members of the g-family of pyridoxal 5’-phosphate-dependent enzymes. J. Biol. Chem. 1998, 273, 5549-5556.
5. Tokoro, M., Asai, T., Kobayashi, S., Takeuchi, T., Nozaki, T. Identification and characterization of two isoenzymes of methionine gamma-lyase from Entamoeba histolytica: a key enzyme of sulfur-amino acid degradation in an anaerobic parasitic protist that lacks forward and reverse trans-sulfuration pathways. J. Biol. Chem. 2003, 278, 42717-42727.
6. Esaki, N., Nakayama, T., Sawada, S., Tanaka, H., and Soda, K. Proton nmr studies of substrate hydrogen exchange reactions catalyzed by L-methionine .gamma.-lyase. Biochemistry. 1985, 24, 3857-3862.
7. Inoe, H., Inagaki, K., Adachi, N., Tamura, T., Esaki, N., Soda, K. & Tanaka, H. Role of tyrosine 114 of L-methionine gamma-lyase from Pseudomonas putida. Biosci. Biotechnol. Biochem. 2000, 64, 2336-2343.
8. Манухов И. В., Мамаева Д. В., Морозова Е. А., Расторгуев С. М., Фалеев Н. Г., Демидкина Т. В., Завильгельский Г. Б. Биохимия (Biochemistry (Mosc)) 2006 апрель; 71(4); 842-851. Манухов И. В., Мамаева Д. В., Морозова Е. А., Расторгуев С. М., Фалеев Н. Г., Демидкина Т. В., Завильгельский Г. Б. L-метионин-гамма-лиаза Citrobacter freundii: клонирование гена и кинетические параметры фермента. Биохимия. 2006, 71(4):842-851.
9. United States Patent 5,861,154. Soda, et al. January 19, 1999. Recombinant L-methionine gamma.-lyase.
10. United States Patent 7,118,903. Inagaki, et al. October 10, 2006. L-methionine gamma-lyase with modified function.
11. Manukhov IV, Mamaeva DV, Rastorguev SM, Faleev NG, Morozova EA, Demidkina TV, Zavilgelsky GB. A gene encoding L-methionine gamma-lyase is present in Enterobacteriaceae family genomes: identification and characterization of Citrobacter freundii L-methionine gamma-lyase. J Bacteriol. 2005, 187(11):3889-93.
12. Hoffman R.M., Development of recombinant methioninase to target the general cancer-specific metabolic defect of methionine dependence: a 40-year odyssey. Expert Opin. Biol. Ther. 2015, 15(1), 21-31.
13. Tan Y., Xu M., Tan X.-Z. , Tan X., Wang X., Saikawa Y., Nagahama T., Sun X., Lenz M., Hoffman R.M. Overexpression and large-scale production of recombinantl-methionine-α-deamino-γ-mercaptomethane-lyase for novel anticancer therapy. 1997. Protein. Exp.Purif. 9, 233-245.
14. Yoshioka T., Wada T., Uchida N., Maki H., Yoshida H., Ide N., Kasai H., Hojo K., Shono K., Maekawa R., Yagi S., Hoffman R.M. Anticancer efficacy in vivo and in vitro, synergy with 5-fluorouracil, and safety of recombinant methioninase. 1998. Cancer Res. 58, 2583-2587.
15. Tan Y., Xu M., Hoffman R.M. Broad selective efficacy of rMETase and PEG-rMETase on cancer cells in vitro. Anticancer Res. 2010, 30, 793-798.
16. Pokrovsky VS, Yu Anisimova N, Zh Davydov D, Bazhenov SV, Bulushova NV, Zavilgelsky GB, Kotova VY, Manukhov IV. Methionine gamma lyase from Clostridium sporogenes increases the anticancer effect of doxorubicin in A549 cells and human cancer xenografts. Invest New Drugs. 2019 Jun 15. doi: 10.1007/s10637-018-0619-4.
17. Pokrovsky V.S., Anisimova N.Yu., Davydov D.Zh., Bazhenov S.V., Bulushova N.V., Zavilgelsky G.B., Kotova V.Y., I.V. Manukhov. Methionine dependence of cancer and aging: methods and protocols. R.M. Hoffman, Editor. Chapter 18. Methionine gamma lyase from Clostridium sporogenes increases the anticancer effect of doxorubicin in A549 cancer cells in vitro and human cancer xenografts. Springer Nature. Springer Science+Business Media, LLC, Humana Press. ISBN 978-1-4939-8795-5. 2019.
18. WO 2004112717 A3 Conjugate for the specific targeting of anticancer agents to cancer cells and production thereof.
19. Yarden, Y., Pines, G. The ERBB network: at last, cancer therapy meets systems biology. Nat Rev Cancer 2012, 12, 553–563. https://doi.org/10.1038/nrc3309
20. Ciardiello F., Tortora G. EGFR antagonists in cancer treatment. New England Journal of Medicine. 2008. 358(11) 1160-1174.
21. Appella E., Weber I. T., Blasi F. Structure and function of epidermal growth factor-like regions in proteins. FEBS letters. 1988. 231(1) 1-4.
22. Y Ding, W Tan, R Hu, W Chen, Y Hou. Construction of a novel fusion protein harboring mouse interferon γ and epidermal growth factor receptor binding domain and enhancement of its antitumor activity. Science in China Series C: Life Sciences. 1997. 40(3) 293-300.
23. Патент РФ № 2733440 от 04.06.2020 (дата приоритета 2018) «Способ получения фермента метионин-гамма-лиазы, противоопухолевое лекарственное средство ГЛФ МГЛ на основе этого фермента и применение этого средства для торможения роста опухоли (варианты)». Авторы: Манухов И.В., Баженов С.В., Гнучих Е.Ю., Покровский В.С., Давыдов Д.Ж., Котова В.Ю., Булушова Н.В., Завильгельский Г.Б.
24. Wriston, J. C. Asparaginase. Methods in Enzymology. 1970, 17A, 732-742.
25. Studier F.W. Protein production by auto-induction in high-density shaking cultures. // Protein Expr. Purif. 2005, 41, 207–234.
| название | год | авторы | номер документа |
|---|---|---|---|
| Химерный фермент на основе L-метионин-гамма-лиазы, слитой с VHH антителом М456, и фрагмент ДНК, кодирующий указанный фермент | 2022 |
|
RU2813802C1 |
| Способ получения фермента метионин-гамма-лиазы, противоопухолевое лекарственное средство ГЛФ МГЛ на основе этого фермента и применение этого средства для торможения роста опухоли (варианты) | 2018 |
|
RU2733440C2 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАЛКИЛ ТИОСУЛЬФИНАТОВ С ПОМОЩЬЮ ДВУХКОМПОНЕНТНОЙ СИСТЕМЫ МЕТИОНИН-γ-ЛИАЗА + СУЛЬФОКСИДЫ S-АЛКИЛ-L-ЦИСТЕИНА | 2021 |
|
RU2814985C2 |
| Способ получения фермента протеин-глутаминазы для пищевой промышленности в Escherichia coli | 2022 |
|
RU2810598C2 |
| ХИМЕРНЫЙ БЕЛОК ДЛЯ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ ЛИМФОМ | 2004 |
|
RU2297241C2 |
| РЕКОМБИНАНТНАЯ ДНК, ОБЕСПЕЧИВАЮЩАЯ В СОСТАВЕ ПЛАЗМИДНОГО ВЕКТОРА СИНТЕЗ В КЛЕТКАХ E.coli ХИМЕРНОГО БЕЛКА АПОЛИПОПРОТЕИНА A-I ЧЕЛОВЕКА | 2014 |
|
RU2573930C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДНАЯ ДНК PTRCTE-OPH И ПРОДУЦЕНТ ФЕРМЕНТА ОРГАНОФОСФАТГИДРОЛАЗЫ | 2002 |
|
RU2232807C1 |
| РЕКОМБИНАНТНЫЙ ХИМЕРНЫЙ БЕЛОК ANTH1, КОДИРУЮЩАЯ ЕГО НУКЛЕИНОВАЯ КИСЛОТА И ИХ ПРИМЕНЕНИЕ | 2003 |
|
RU2322455C2 |
| СПОСОБ ЛЕЧЕНИЯ РАКА У МЛЕКОПИТАЮЩЕГО, ВКЛЮЧАЯ ЧЕЛОВЕКА, С ПРИМЕНЕНИМ ДЕПЛЕЦИИ МЕТИОНИНА И АСПАРАГИНА | 2017 |
|
RU2733389C2 |
| ГИБРИДНЫЙ БЕЛОК НА ОСНОВЕ L-АСПАРАГИНАЗЫ Wolinella succinogenes, ШТАММ Escherichia coli - ПРОДУЦЕНТ ГИБРИДНОГО БЕЛКА (ВАРИАНТЫ) И СПОСОБ ПОЛУЧЕНИЯ ГИБРИДНОГО БЕЛКА, ОБЛАДАЮЩЕГО ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2014 |
|
RU2562166C1 |

Изобретение относится к биотехнологии. Предложен препарат, представляющий из себя белок МГЛ-S3, лиофилизированный совместно с трегалозой при соотношении 1 к 28 по массе, где МГЛ-S3 является химерным ферментом метионин-гамма-лиазой с S3 доменом ростового фактора вируса оспы на C-конце, обладающим метиониназной активностью, способным оказывать цитотоксическое воздействие на опухолевые клетки и способным связываться с опухолевыми клетками, оставаясь на поверхности клеток и продолжая оказывать цитотоксический эффект в МТТ- или PI-тесте при смене культивационной среды. Также предложен способ получения препарата на основе химерного фермента МГЛ-S3. Изобретение может быть эффективно использовано для терапии рака. 2 н.п. ф-лы, 7 ил., 1 табл., 5 пр.
1. Препарат, представляющий из себя белок МГЛ-S3, лиофилизированный совместно с трегалозой при соотношении 1 к 28 по массе, где МГЛ-S3 является химерным ферментом метионин-гамма-лиазой с S3 доменом ростового фактора вируса оспы на C-конце, обладающим метиониназной активностью, способным оказывать цитотоксическое воздействие на опухолевые клетки и способным связываться с опухолевыми клетками, оставаясь на поверхности клеток и продолжая оказывать цитотоксический эффект в МТТ- или PI-тесте при смене культивационной среды.
2. Способ получения препарата на основе химерного фермента МГЛ-S3, состоящий в культивировании рекомбинантного штамма-продуцента Escherichia coli на богатой питательной среде, содержащей триптон, дрожжевой экстракт, глицерин, KH2PO4, (NH4)2SO4, и Na2HPO4, и добавки: глюкоза, добавляемая при старте ферментации и при достижении OD = 5, лактоза и изопропил-β-D-1-тиогалактопиранозид, добавляемые для индукции биосинтеза при OD = 25, очистке этого фермента с помощью лизирования, термоосаждения в присутствии 20 мас. % этилового спирта при 50 °С, анионно-обменной хроматографии c элюированием градиентом KCl и сбором основной фракции белка до 0,2 M KCl, переосаждении в 35% и 50% насыщенном растворе сульфата аммония с последующей гель-фильтрацией и лиофилизации с добавлением трегалозы при соотношении 28 мг трегалозы на 1 мг белка.
| БОНДАРЕВ Н.А | |||
| и др | |||
| Разработка продуцента противоопухолевого препарата на основе фермента L-метионин-у-лиазы | |||
| Способ восстановления спиралей из вольфрамовой проволоки для электрических ламп накаливания, наполненных газом | 1924 |
|
SU2020A1 |
| Второе издание: переработанное и дополненное / Отв.ред | |||
| И.А | |||
| Алешковский, А.В | |||
| Андриянов, Е.А | |||
| Антипов | |||
| [Электронный ресурс] - М.: МАКС Пресс, 2020 | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| опт | |||
Авторы
Даты
2024-04-01—Публикация
2022-05-20—Подача