Изобретение относится к медицине, конкретно к фармакологии, и может быть использовано для коррекции нарушений иммунной системы при патологических состояниях, связанных с недостаточностью Th1-зависимого типа иммунного ответа (хронические, вялотекущие и рецидивирующие инфекционные, а также онкологические заболевания).
Антигенпрезентирующие клетки, прежде всего макрофаги, принадлежат к системе врожденного иммунитета и играют ключевую роль в защите организма от патогенов. Активированные макрофаги имеют два разных фенотипа M1 (классически активированный) и М2 (альтернативно активированный). Поляризация классически активированных провоспалительных макрофагов, обусловленная липополисахаридом (ЛПС), либо его сочетанием с Th-1 цитокинами, такими как интерферон-гамма (ИФН-γ), гранулоцитарно-макрофагальный колониестимулирующий фактор (ГМ-КСФ), характеризуется продукцией провоспалительных цитокинов, интерлейкина-1β (ИЛ-1β), ИЛ-6, ИЛ-12, ИЛ-23 и фактора некроза опухолей альфа (ФНО-α), реактивных форм азота и кислорода, способствует элиминации микроорганизмов и опухолевых клеток. В то время М2, которые являются противовоспалительными и иммунорегуляторными, поляризованы Th2-цитокинами (ИЛ-4 и ИЛ-13) продуцируют противовоспалительные цитокины, такие как ИЛ-10 и транформирующий фактор роста бета (ТФР-β), участвуют в реализации воспаления посредством фагоцитоза апоптотических нейтрофилов, снижают выработку провоспалительных цитокинов и усиливают синтез медиаторов, необходимых для ремоделирования тканей, ангиогенеза и заживления ран. Макрофаги обеспечивают презентацию антигенов клеткам иммунной системы, направляют поляризацию Th и поддерживают протекание Th1/Th2-зависимых реакций. При тяжелых формах воспаления макрофаги сначала проявляют фенотип M1, продуцируя провоспалительные цитокины, но, если фаза M1 затягивается и воспаление может приводить к повреждению ткани М2 начинают секретировать большое количество ИЛ-10 и ТФР-β для подавления воспаления, что способствует восстановлению тканей, ремоделированию, васкулогенезу и сохранению гомеостаза [1, 2]. Таким образом, баланс M1 (ИЛ-12 и ФНО-α) и М2 (ИЛ-10) опосредованных цитокинов является определяющим для направления поляризации иммунного ответа по Th1 или Th2 типу, а секреция антигенпрезентирующими клетками ИЛ-12 и ФНО-α необходимым условием эффективного противомикробного и противоопухолевого иммунитета [3].
Известно, что водорастворимые полисахариды, выделенные из ряда высших цветковых растений, обладают иммуномоделирующими свойствами, могут связываться практически со всеми рецепторами антигенпрезентирующих клеток, через их активацию оказывать влияние на поляризацию лимфоцитов и способствовать развитию как Th1 - так и Th2-зависимого иммунного ответа [4, 5]. Ряска многокорневая (Lemna polyrrhiza L. (синоним Многокоренник обыкновенный Spirodela polyrrhiza (L.) Schleid.)) - многолетнее мелкое водное растение относится к группе растений из семейства рясковых, семейства Ароидные (Araceae), растет в застойных водоемах повсеместно в европейской части России, на Кавказе, в Сибири, на Дальнем Востоке, в Средней Азии, Китае и Японии. В народной медицине, как правило, используют, заготовленное во время цветения растение, в качестве жаропонижающего, потогонного и мочегонного средства. Полезные свойства ряски многокорневой, обусловлены высоким содержанием в листьях солей брома и йода, протеина, однако, в этой траве практически нет аскорбиновой кислоты [6].
Задачей данного изобретения является расширение арсенала эффективных иммуномодулирующих средств растительного происхождения, обладающих способностью к избирательной стимуляции продукции иммунокомпетентными клетками интерлейкина-1 бета, интерлейкина-12, фактора некроза опухоли-альфа и интерферона гамма.
Поставленная задача решается путем применения водорастворимых полисахаридов с молекулярной массой 1053 кДа, 628 кДа и 35 кДа, полученных из травы водного растения ряски многокоренной (Lemna polyrrhiza L.), в качестве стимулятора продукции макрофагами ИЛ-β, ИЛ-12 и ФНО-α и лимфоцитами ИФН-γ, следствием чего является активация Th1-зависимого типа иммунного ответа.
Принципиально новым в предлагаемом изобретении является применение в качестве иммуномодулирующего средства комплекса водорастворимых полисахаридов с молекулярными массами 1053 кДа, 628 кДа и 35 кДа с относительным содержанием 61,24; 5,37; и 33,39%, соответственно, выделенных из травы ряски многокоренной.
Новое свойство водорастворимых полисахаридов с молекулярной массой 1053 кДа, 628 кДа и 35 кДа, полученных из травы ряски многокоренной, было обнаружено в результате экспериментальных исследований и для специалиста явным образом не вытекает из уровня техники и описание этих свойств не обнаружено авторами в патентной и научно-медицинской литературе.
Таким образом, предлагаемое техническое решение соответствует критериям изобретения, а именно - «новизна», «изобретательский уровень» и «промышленная применимость».
Изобретение будет понятно из следующего описания. Водорастворимые полисахариды выделяли из травы ряски многокоренной (LP), которую заготавливали в местах естественного произрастания в середине вегетационного сезона, высушивали до воздушно-сухого состояния (влажность менее 6%). Навеску 20,0 г полученного сырья при нагревании на кипящей водяной бане экстрагировали раствором 400 мл очищенной воды и 2 мл концентрированной HCl (рН=4,0) в соотношении сырье: экстрагент - 1:20 при периодическом перемешивании в течение 3-4 ч. Образовавшийся раствор отделяли фильтрованием через многослойный тканевый фильтр, полученный фильтрат упаривали до 1/5 от исходного объема на роторном испарителе при температуре не более 50°С, добавляли трехкратный объем 96% этанола и отстаивали 24 ч при температуре 2-4°С. Затем жидкую часть отфильтровывали через бумажный фильтр и осадок растворяли в 100 мл очищенной воды при перемешивании на магнитной мешалке в течение 3 ч при комнатной температуре. Для удаления не растворившегося остатка (мельчайшие частицы сырья, денатурированный белок и пр.) раствор центрифугировали (4000 об/мин, в течение 30 мин), центрифугат диализировали через полупроницаемую мембрану с диаметром пор 15 кДа в течение 48 ч в 50-кратном объеме очищенной воды при комнатной температуре и перемешивании на магнитной мешалке, меняя воду через 24 ч. После диализа раствор замораживали и лиофильно высушивали. Выход водорастворимых ПС из травы ряски многокоренной составлял 2,78% от массы воздушно-сухого сырья (табл. 1). Полученный образец полисахаридный комплекс был стандартизован по содержанию углеводов (спектрофотометрический метод [7]), белка (метод Брэдфорда [8]) и нуклеиновых кислот [9]
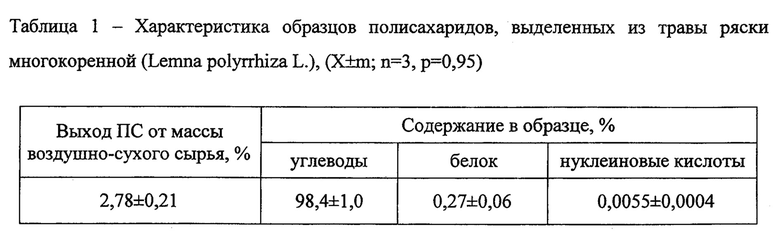
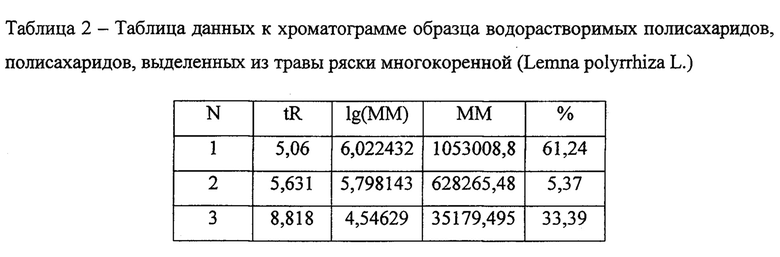
Анализ молекулярно-массового распределения ПС LP, проведенного на жидкостном хроматографе Ultimate 3000 (Германия, «Dionex») в колонке TSK GMPWXL 300×78 mm, 13 μm, подвижная фаза - вода, скорость потока 1 мл/мин, детектирование рефрактометрическое, температура ячейки детектора 40°С (калибровочная прямая по растворам декстранов молекулярной массой 1000, 17000, 40000, 250000, 500000, 1200000 Да при тех же условиях хроматографирования) выявил, что полученное вещество состоит из трех полисахаридов с молекулярными массами 1053 кДа, 628 кДа и 35 кДа с относительным содержанием 61,24; 5,37; и 33,39% (табл. 2).
Хроматограмма силилированного образца гидролизата ПС ряски многокоренной, разделение которого проводили на газовом хроматографе Agilent 7890А (США) в колонке 1 MS 30 м, внутренний диаметр капилляра 0,25 мкм, скорость потока газа-носителя (Не) 1 мл/мин, в градиенте температур: 70 град. - 2 минуты, далее 10 градусов в минуту (до 300 град.), температура инжектора 280 град., затем детектировали на масс-спектрометре Agilent 5975S (США), ионизация электронным ударом, сканирование m/z 33-600, температура ионного источника 120 град, показала, что полученный из травы ряски многокоренной полисахаридный комплекс является глюкоуронаном с небольшим содержанием арабинозы, галактозы и фруктозы. ПС, полученные из травы ряски многокоренной, относятся к кислым полисахаридам (содержание глюкуроновой кислоты около 30,28%), отличительным моносахаридом является арабиноза (табл. 3).

Эксперименты проведены на линейных мышах C57BL/6 в возрасте 8-10 недель, полученных из отдела экспериментальных биологических моделей НИИФиРМ им. Е.Д. Гольдберга Томский НИМЦ.
Для выделения макрофагов (МФ) животных забивали дислокацией шейного отдела позвоночника, брюшную полость промывали ледяным изотоническим раствором хлорида натрия (ФР), клетки осаждали, ресуспендировали в культуральной среде и оценивали их жизнеспособность в тесте с 0,1% трипановым синим, затем помещали в пластиковые чашки Петри (1,5-2,0×106клеток/мл), культивировали 2 ч (при 37°С в атмосфере 5% СО2 и абсолютной влажности) в полной культуральной среде, содержащей 10% ЭТС, после чего собирали прилипшую к пластику фракцию клеток. Спленоциты получали гомогенизацией селезенок в стеклянном гомогенизаторе в стерильных условиях. Полученную суспензию клеток фильтровали через 4-слойный капрон, промывали холодным ФР, ресуспендировали в культуральной среде в экспериментах использовали суспензии, содержащие не менее 95% жизнеспособных клеток. Мононуклеары получали наслаивая цельную кровь здоровых доноров с добавлением гепарина (10 ЕД/мл) на жидкость для сепарации клеток «Histopaque-1077» («Sigma-Aldrich»), центрифугировали 15 минут при 400 g. Клетки, сформировавшие кольцо на градиенте плотности, собирали, отмывали холодным ФР, ресуспендировали в полной культуральной среде, оценивали жизнеспособность. Полученные МФ (3,0×106 клеток/мл), спленоциты (2,5×106 клеток/мл) или мононуклеары (2,5-3,0×106 клеток/мл) помещали в 96-луночные планшеты и культивировали в среде, состоящей из RPMI 1640 («Sigma», США) с добавлением 10% ЭТС («Hyc1one»), 20 мМ HEPES («Sigma»), 0,05 мМ 2-меркаптоэтанола («Sigma»), 50 мкг/мл гентамицина («Sigma»Pyn) и 2 мМ L-глютамина («Sigma») при 37°С в атмосфере с 5% СО2 и абсолютной влажности, в присутствии 20 мкг/мл ПС, выделенных из ряски многокоренной; 4 мкг/мл конканавалина А (Кон А); 5 мкг/мл митогена лаконоса (МЛ); 1 мкг/мл липополисахарида (ЛПС, серотип O111:В4, «Sigma»). Через 24 ч от начала культивирования собирали из лунок надосадок, разливали на аликвоты и хранили при 20°С, твердофазным иммуноферментным методом при помощи тест-систем измеряли в нем концентрацию цитокинов мышей (ИЛ-1β, ИЛ-4, ИЛ-10, ИЛ-12, ФНО-α, ИФН-γ («eBioscience», «InVitroGen»)) или человека (ИЛ-12, ИЛ-10 и ИФН-Y («R@D Systems»), ФНО-α, ИЛ-4 («Вектор-Бэст»)) согласно прилагаемым протоколам на автоматическом анализаторе ChemWell®Combo.
Водорастворимые полисахариды, выделенные из ряски многокоренной, вводили мышам по 7,5 мг/кг массы тела ежедневно внутрибрюшинно в течение 10 дней в 0,1 мл ФР (животным контрольной группы вводили 0,1 мл ФР). Th1-зависимый тип иммунного ответа у животных моделировали иммунизацией эритроцитами барана (1×108 клеток) внутрибрюшинной инъекцией в 0,1 мл ФР через 5 дней от начала введения веществ.
Для оценки действия исследуемого вещества на клеточное звено иммунитета использовали реакцию гиперчувствительности замедленного типа [10]. Для этого на 5-е сутки после иммунизации животным проводили вторую (разрешающую) инъекцию эритроцитов барана в подушечку задней лапы - «опытная лапа» (108 эритроцитов барана в 0,05 мл изотонического раствора хлорида натрия). В «контрольную» контрлатеральную лапу вводили 0,05 мл стерильного ФР. Через 24 часа животных забивали, обе лапы отрезали по выступу кости выше пяточного сустава и ниже сочленения мало- и большеберцовой кости, взвешивали, местную воспалительную реакцию оценивали по разнице массы опытной и контрольной лап.
Для оценки действия исследуемого вещества на гуморальное звено иммунитета использовали реакцию антителообразования по методу Ерне [11]. Для этого на 5-е сутки после иммунизации (на пике IgM-AOK и IgG-AOK), в предварительно нагретых до 49-53°С пробирках смешивали 0,2 мл взвеси спленоцитов, полученных как описано выше, 0,9 мл среды для культивирования (0,7% агар «Difco» в среде 199), 0,2 мл 20%-ой взвеси эритроцитов барана и 0,1 мл комплемента (ФГУП «НПО «Микроген»), полученную смесь помещали во влажную камеру Горяева, инкубировали 2 ч при 37°С, затем подсчитывали зоны гемолиза при помощи светового микроскопа. Уровень гемагглютининов в сыворотке крови определяли по способности антител, содержащихся в сыворотке крови иммунизированных животных, агглютинировать эритроциты барана, используемые в качестве антигена. Для этого к 0,025 мл сыворотки крови мышей, полученной на 5-е сутки после иммунизации, прогретой для инактивации комплемента при 56°С, раститрованной в 96-луночном круглодонном планшете с шагом 1/2, добавляли 0,025 мл 1% суспензии эритроцитов барана, инкубировали при 37°С 2 часа, затем оценивали реакцию. За титр принимали последнее разведение исследуемой сыворотки, при котором наблюдается агглютинация антигена. Титр выражали величиной log2 [10].
Полученные в ходе исследования данные обрабатывали с помощью пакета статистических программ Statistica 8,0. Для каждой выборки вычислялось среднее арифметическое (X), ошибка среднего арифметического (m), среднее арифметическое отклонение (σ). Проверка на нормальность распределения проводилась с помощью критерия Шапиро-Уилка. Сравнение выборочных средних осуществлялось по критерию Даннета для сравнения нескольких экспериментальных выборок с одной контрольной в случае нормального распределения или по критерию Крускалла-Уоллиса для к-несвязанных выборок (к>2) и критерия Данна в случае распределения, отличающегося от нормального.
Пример 1.
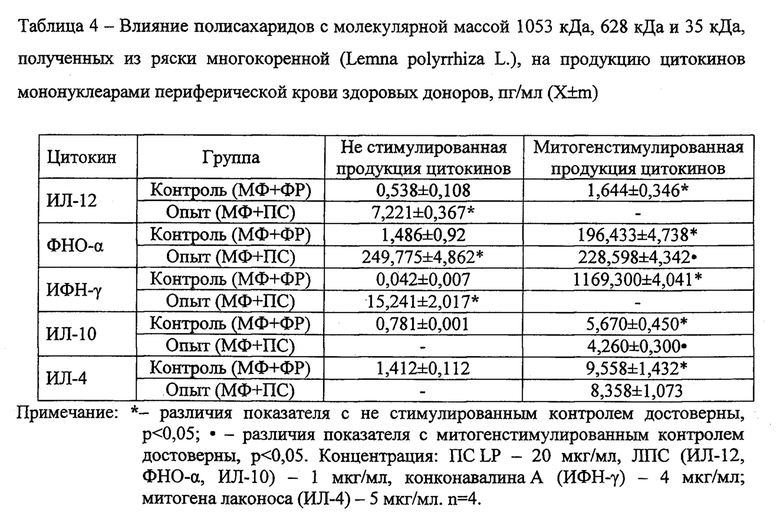
Инкубация мононуклеаров периферической крови здоровых доноров с водорастворимыми полисахаридами с молекулярной массой 1053 кДа, 628 кДа и 35 кДа, полученными из ряски многокоренной, приводила многократному усилению их Th-1 цитокин-секретирующей активности: концентрация ИЛ-12 в супернатанте клеток возрастала относительно интактного контроля в 13,4 раза, ФНО-α и ИФН-γ в 166 и 363 раза, соответственно (табл. 4). Кроме того, было показано, что на фоне ЛПС стимуляции клетки усиливали также продукцию ФНО-α, достоверно превышая в 1,2 раза значения показателя митогенстимулированного контроля. При этом ПС значительно снижали ЛПС-стимулированную продукцию ключевого Th-2 цитокина ИЛ-10 в 1,3 раза и не влияли на активированную митогеном локоноса продукцию ИЛ-4.
На модели клеток мышей показано, что водорастворимые ПС ряски многокоренной также усиливали синтез провоспалительных цитокинов ИЛ-1β, ИЛ-12 и ФНО-α перитонеальными макрофагами и ИФН-γ лимфоцитами селезенки в 11,3, 1,5, 50 и 103,6 раза, соответственно (табл. 5). Митоген-стимулированная продукция ИФН-γ иммунокомпетентными клетками также усиливалась при инкубации с ПС в 6,5 раз. На фоне выявленного повышения концентрации Th-1 цитокинов ПС LP снижали в 2,5 раза секрецию противоспалительного ИЛ-4 на фоне стимуляции митогеном локоноса, митогенстимулированная продукция ИЛ-10 не изменялась.

Пример. 2.
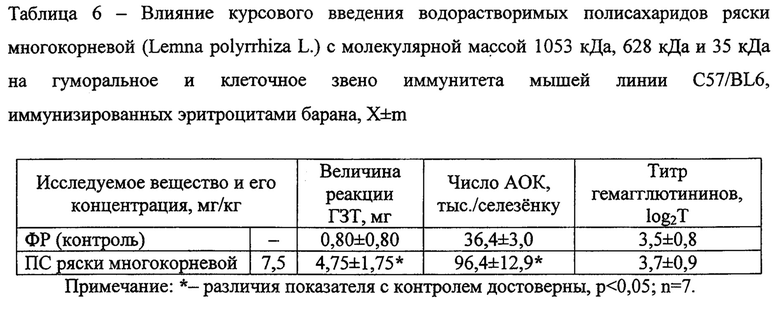
Водорастворимые полисахариды, с молекулярной массой 1053 кДа, 628 кДа и 35 кДа, полученные из травы ряски многокоренной, оказывали значительное влияние на показатели гуморального и клеточного Th1-зависимого иммунного ответа. Курсовое введение ПС ряски многокоренной приводило к значительному в 2,6 раза усилению активности антителообразующих клеток в 2,6 раза с 36,4±3,0 тыс/селезенку в контроле до 96,4±12,9 тыс/селезенку. Титр синтезируемых ими гемагглютининов не изменялся (табл. 6). Также в 5,9 раза усиливало реакцию гиперчувствительности замедленного типа у мышей C57/BL6, с практически нулевых значений до 4,75±1,75 мг.
Таким образом, в ходе исследования установлено, что водорастворимые полисахариды с молекулярной массой 1053, 628 и 35 кДа, выделенные из травы ряски многокоренной (Lemna polyrrhiza L.), обладают способностью активировать показатели Th1 типа иммунного ответа, а именно, на фоне стимуляции выработки антигенпрезентирующими клетками ключевых провоспалительных цитокинов ИЛ-1β, ИЛ-12, ФНО-α и лимфоидными клетками ИФН-γ снижать продукцию противовоспалительных цитокинов ИЛ-4 и ИЛ-10, стимулировать протекание иммунного ответа, вызванного эритроцитами барана.
Выявленные свойства водорастворимых полисахаридов с молекулярной массой 1053, 628 и 35 кДа, выделенных из травы ряски многокоренной (Lemna polyrrhiza L.), можно использовать в качестве средств, способных стимулировать иммунный ответ при инфекционно-воспалительных процессах и онкологических заболеваниях.
Литература
1. Stow, J.L. Cytokine secretion in macrophages and other cells: pathways and mediators / J.L. Stow et al. // Immunobiology. - 2009. - V. 214. - Is. 7. - P. 601-612.
2. Laria, A. The macrophages in rheumatic diseases / A. Laria et al. // J. Inflamm. Res. - 2016. - V. 9. - P. 1-11.
3. Ma, X. TNF-a and IL-12: a balancing act in macrophage functioning / X. Ma. // Microbes and Infection. - 2001. - V. 3. - P. 121-129.
4. Schepetkin, LA. Botanical polysaccharides: macrophage immunomodulation and therapeutic potential /1.A.Schepetkin, M.T. Quinn // Int. Immunopharmacol. - 2006. - V. 6. - Is. 3. - P. 317-733.
5. Данилец, М.Г. Фармакологическая регуляция функционального состояния макрофагов при иммунном ответе: автореф... дисс.докт.биол.наук - 2011. - Томск. - 43 стр.
6. Буданцев, А.Л. Дикорастущие полезные растения России / А.Л. Буданцев, Е.Е. Лесиовская // СПб.: СПХФА. - 2001. - с. 358-361.
7. Dubois, М. Colorimetric method for determination of sugar and related substances / M. Dubois et. al. // Anal.Chem. - 1956. - V. 28. - Is. 3. - P. 350-356.
8. Bradford, M.M., A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding / M.M. Bradford // Analyt. Biochem. - 1976. - V. 72. - P. 248-254.
9. Спирин, A.C. Спектрофотометрическое определение суммарного количества нуклеиновых кислот / А.С.Спирин // Биохимия. - 1958. - Т.23. - Вып.5. - С.656-661.
10. Хаитов, P.M. Экспериментальное изучение иммунотропной активности фармакологических препаратов (методические рекомендации) / P.M. Хаитов и др. // Ведомости Фармакологического Комитета. - 1999. - №1. - С.31-36.
11. Ierne, N.K. Plaque formation in agar by single antibody production cells / N.K. Ierne, A.A. Nordin // Science. - 1963. - V. 140. - Is. 3565. - P. 405-408.
| название | год | авторы | номер документа |
|---|---|---|---|
| Средство, обладающее иммуномодулирующей активностью | 2017 |
|
RU2657819C1 |
| Средство, обладающее иммуномодулирующей активностью | 2018 |
|
RU2697526C1 |
| Средство, гуминовой природы, обладающее иммуномодулирующей активностью | 2019 |
|
RU2716504C1 |
| Средство гуминовой природы, обладающее иммуномодулирующей активностью | 2017 |
|
RU2662094C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ИММУНОМОДУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 2011 |
|
RU2470656C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ИММУНОМОДУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 2010 |
|
RU2421232C1 |
| СРЕДСТВО НА ОСНОВЕ АРАБИНОГАЛАКТОУРОНАНОВ, ОБЛАДАЮЩЕЕ ИММУНОМОДУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 2024 |
|
RU2836422C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ИММУНОМОДУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 2010 |
|
RU2423141C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ИММУНОМОДУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 2007 |
|
RU2329821C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ИММУНОМОДУЛИРУЮЩЕЙ АКТИВНОСТЬЮ | 2007 |
|
RU2337700C1 |
Изобретение относится к фармацевтической промышленности, а именно к применению комплекса водорастворимых полисахаридов в качестве средства, обладающего иммуномодулирующей активностью, для индуцирования продукции провоспалительных цитокинов - интерлейкина-12, фактора некроза опухоли-альфа макрофагами и интерферона-гамма лимфоцитами, ингибирования продукции противовоспалительных цитокинов - интерлейкина-4 и интерлейкина-10 и стимуляции иммунного ответа, вызванного эритроцитами барана. Применение комплекса водорастворимых полисахаридов с молекулярными массами 1053 кДа, 628 кДа и 35 кДа и относительным их содержанием 61,24 мас.%; 5,37 мас.% и 33,39 мас.% соответственно, выделенных из травы ряски многокоренной (Lemna polyrrhyza L.), в качестве средства, обладающего иммуномодулирующей активностью, для индуцирования продукции провоспалительных цитокинов - интерлейкина-12, фактора некроза опухоли-альфа макрофагами и интерферона-гамма лимфоцитами, ингибирования продукции противовоспалительных цитокинов - интерлейкина-4 и интерлейкина-10 и стимуляции иммунного ответа, вызванного эритроцитами барана, при этом указанные полисахариды получены путем экстракции в течение 3-4 ч растительного сырья, высушенного до воздушно-сухого состояния с влажностью менее 6%, на кипящей водяной бане очищенной водой с добавлением HCl рН=4,0 в соотношении сырье:экстрагент - 1:20, фильтрации через многослойный тканевый фильтр, упаривания фильтрата до 1/5 от исходного объема на роторном испарителе при температуре не более 50°С, отстаивания 24 ч при температуре 2-4°С в трехкратном объеме 96% этанола, фильтрации через бумажный фильтр, растворения осадка в очищенной воде на магнитной мешалке в течение 3 ч при комнатной температуре, удаления не растворившегося остатка из мельчайших частиц сырья и денатурированного белка центрифугированием в течение 30 мин при 4000 об/мин, диализа через полупроницаемую мембрану с диаметром пор 15 кДа в течение 48 ч в 50-кратном объеме очищенной воды при комнатной температуре и перемешивании на магнитной мешалке со сменой воды через 24 ч, замораживания диализата и его лиофильной сушки. Вышеописанный комплекс водорастворимых полисахаридов является активатором воспалительных свойств макрофагов и Th1-зависимого типа иммунного ответа, обладает выраженной иммуномодулирующей активностью, для индуцирования продукции провоспалительных цитокинов - интерлейкина-12, фактора некроза опухоли-альфа макрофагами и интерферона-гамма лимфоцитами, ингибирования продукции противовоспалительных цитокинов - интерлейкина-4 и интерлейкина-10 и стимуляции иммунного ответа, вызванного эритроцитами барана. 6 табл., 2 пр.
Применение комплекса водорастворимых полисахаридов с молекулярными массами 1053 кДа, 628 кДа и 35 кДа и относительным их содержанием 61,24 мас.%; 5,37 мас.% и 33,39 мас.% соответственно, выделенных из травы ряски многокоренной (Lemna polyrrhyza L.), в качестве средства, обладающего иммуномодулирующей активностью, для индуцирования продукции провоспалительных цитокинов - интерлейкина-12, фактора некроза опухоли-альфа макрофагами и интерферона-гамма лимфоцитами, ингибирования продукции противовоспалительных цитокинов - интерлейкина-4 и интерлейкина-10 и стимуляции иммунного ответа, вызванного эритроцитами барана, характеризующегося тем, что указанные полисахариды получены путем экстракции в течение 3-4 ч растительного сырья, высушенного до воздушно-сухого состояния с влажностью менее 6%, на кипящей водяной бане очищенной водой с добавлением HCl рН=4,0 в соотношении сырье: экстрагент - 1:20, фильтрации через многослойный тканевый фильтр, упаривания фильтрата до 1/5 от исходного объема на роторном испарителе при температуре не более 50°С, отстаивания 24 ч при температуре 2-4°С в трехкратном объеме 96% этанола, фильтрации через бумажный фильтр, растворения осадка в очищенной воде на магнитной мешалке в течение 3 ч при комнатной температуре, удаления не растворившегося остатка из мельчайших частиц сырья и денатурированного белка центрифугированием в течение 30 мин при 4000 об/мин, диализа через полупроницаемую мембрану с диаметром пор 15 кДа в течение 48 ч в 50-кратном объеме очищенной воды при комнатной температуре и перемешивании на магнитной мешалке со сменой воды через 24 ч, замораживания диализата и его лиофильной сушки.
| Средство, обладающее иммуномодулирующей активностью | 2017 |
|
RU2657819C1 |
| RU 2175843 C1, 20.11.2001 | |||
| СПОСОБ ПОЛУЧЕНИЯ ВЕЩЕСТВА, ОБЛАДАЮЩЕГО ИММУНОСТИМУЛИРУЮЩЕЙ, ПРОТИВОВИРУСНОЙ И АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТЬЮ, ВЕЩЕСТВО, ПОЛУЧЕНОЕ ЭТИМ СПОСОБОМ, И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕГО ОСНОВЕ | 2001 |
|
RU2195308C1 |
Авторы
Даты
2020-10-16—Публикация
2019-06-13—Подача