Изобретение относится к биотехнологии, касается получения стандартных образцов (СО) для контроля специфической активности препаратов иммуноглобулинов человека против клещевого энцефалита (КЭ) и может быть использовано в области производства и контроля иммунобиологических препаратов, диагностических тест-систем.
Основным действующим веществом донорских препаратов иммуноглобулинов против КЭ являются иммуноглобулины G (IgG) плазмы крови, нейтрализующие вирус КЭ. В связи с тем, что терапевтический эффект препарата (при условии соблюдения сроков его введения) коррелирует с количеством антител, методы контроля специфической активности должны гарантировать надежность полученных с их использованием результатов. Специфическую активность препаратов иммуноглобулинов человека против КЭ, выпускаемых только в Российской Федерации, подтверждают в реакции торможения гемагглютинации (РТГА) в соответствии с инструкциями по применению наборов реагентов без использования соответствующего СО, в связи с его отсутствием. Перспективным методом контроля специфической активности иммуноглобулинов человека против КЭ является иммуноферментный анализ (ИФА).
Для повышения достоверности результатов определения основного действующего вещества иммунобиологических препаратов рекомендуется использовать СО, идентичные по свойствам, составу и происхождению исследуемым образцам (принцип «like versus Нке») [1]. Применение этого принципа при разработке способа получения СО обосновано тем, что количественное определения антител к вирусу КЭ проводят методом серийных разведений путем сравнения кривых (результатов) титрования СО и исследуемого препарата. В ИФА аналитический сигнал, полученный для СО, сравнивают с аналитическим сигналом пробы с анализируемым образцом. В связи с этим, очевидно, что получение идентичных по составу и свойствам СО и исследуемого препарата позволяет улучшить аналитические характеристики методик количественного определения антител IgG человека к вирусу КЭ.
Согласно рекомендациям ВОЗ [1] основной задачей получения стандартного образца является обеспечение постоянства содержания основного компонента СО в процессе хранения, транспортирования и использования, так как изменение этого параметра СО может снижать точность количественного определения IgG к вирусу КЭ в препаратах иммуноглобулинов человека.
Ближайшими к способу получения СО являются:
1) способ получения Международного стандарта ВОЗ, сыворотки против клещевого энцефалита (WHO International Standard Anti-tick borne encephalitis serum (Louping III), NIBSC code: TILI), утвержденной Национальным Институтом биологических стандартов и контроля (National Biological Institute for Biological Standards and Control (NIBSC)) в 2008 году. Сыворотку получают путем иммунизации овец тест-штаммом вируса КЭ, относящегося к Шотландскому энцефаломиелиту овец [2].
2) способ получения Международного стандарта ВОЗ, сыворотки против клещевого энцефалита (WHO International Standard Anti-tick borne encephalitis serum (Sophyn & Absettarov), NIBSC code: TISA), утвержденной Национальным Институтом биологических стандартов и контроля (National Biological Institute for Biological Standards and Control (NIBSC)) в 2008 году. Сыворотку получают путем иммунизации овец тест-штаммами вируса КЭ Софьин и Абсеттаров [3].
Стандарты ВОЗ представляют собой иммунную сыворотку крови овец, что ограничивает их применение в ИФА, так как метод выявляет IgG человека к вирусу КЭ. Сыворотку разливают по ампулам, лиофилизируют.Флакон стандарта ВОЗ до использования хранят при температуре минус 20°С, после регидратации содержимого хранение не предусмотрено [2, 3].
Транспортировка такого образца требует специального оборудования для соблюдения температурного режима на всех этапах холодовой цепи.
Также известен способ получения антител для производства диагностических препаратов вируса КЭ (RU 2063245 С1). Антитела получают путем иммунизации крыс линии Wistar 10% мозговой вируссодержащей суспензией крысят-сосунков. Накопление иммунной асцитической жидкости крыс (ИАЖ) индуцируют инокуляцией клеток-опухоли яичника крыс. ИАЖ собирают во флаконы, добавляют хлороформ до конечной концентрации 10%, инкубируют смесь при 37°С, выстаивают в течение 18-20 часов при температуре от 4 до 10°С, после чего центрифугируют в течение 30-40 минут при 5000-6000 об/мин, выделение иммуноглобулина из надосадочной жидкости проводят полиэтиленгликолем.
Недостатки вышеуказанного способа: полученные антитела не являются антителами человеческого происхождения и не могут применяться в методе ИФА для контроля специфической активности препаратов иммуноглобулинов человека против КЭ; производство связано с культивированием вирулентных штаммов вируса КЭ, который относится к патогенным биологическим агентам II группы, что требует обеспечения особых условий безопасности в соответствии с требованиями действующих санитарных правил работы с микроорганизмами I-II группы патогенности (опасности). Кроме того, одним из фракционирующих реагентов при получении антител является хлороформ - органическое химическое соединение, относящееся ко II классу опасности. Его использование требует специального оборудования, а высокая концентрация хлороформа оказывает токсическое действие на персонал.
Полученные таким способом асцитические жидкости, обогащенные антителами к вирусу КЭ, используют в качестве положительного контроля в методе РТГА. Содержание антител в них, как правило, составляет 1:1280, в то время как выпускаемые в нашей стране препараты иммуноглобулина человека против КЭ обычно обладают специфической активностью от 1:80 до 1:320. Содержание антител в положительной контрольной сыворотке -1:1280 - находится вне аналитической области определений специфической активности в препаратах иммуноглобулина человека против КЭ.
Из источников патентной информации известен способ получения лиофилизированных положительных контрольных сывороток, используемых в иммуноферментных тест-системах для определения специфических антител к вирусам и микроорганизмам (RU 2011202 С1). Сыворотку крови человека, содержащую специфические антитела, смешивают с компонентами стабилизатора (ЭДТА, пептидные компоненты или смесь пептидных и углеводных компонентов), разливают по 0,1 мл во флаконы объемом 5-10 мл и подвергают лиофильному высушиванию. Остаточная влажность экспериментальных образцов не превышает 2%. Однако известно, что процесс лиофилизации до остаточной влажности, не превышающей 1%, обеспечивает длительное хранение СО иммунобиологических препаратов [1]. Сыворотка содержит специфические антитела разных классов, в то время как в лечебных иммунобиологических препаратах основным действующим веществом является IgG, поэтому в качестве СО следует использовать белковую фракцию плазмы, обогащенную антителами IgG.
Известно, что для получения препаратов иммуноглобулина человека на стадии выделения IgG из плазмы наиболее часто используется метод спиртового фракционирования, а также ультрафильтрация на полых волокнах (мембранах) с заданным диапазоном пропускания биомолекул. Поэтому является обоснованным включение этих стадий в технологическую схему получения СО, так как это позволит изготовить СО наиболее близкий по свойствам и составу препаратам иммуноглобулина человека против КЭ.
Основными задачами, на решение которых направлен заявляемый способ, являются:
- создание стандартного образца содержания IgG человека к вирусу КЭ, идентичного по происхождению, составу и свойствам анализируемому материалу - препаратам иммуноглобулинов человека против КЭ;
- повышение стабильности свойств и состава СО в процессе хранения, транспортирования и использования.
Решение поставленных задач возможно благодаря тому, что сырьем для получения СО является иммунная плазма, заготовленная методом плазмафереза от доноров, имеющих естественные антитела к вирусу КЭ или направленно иммунизированных вакцинами против КЭ, а также использования технологии производства препаратов иммуноглобулинов человека против КЭ. Кроме того, стабилизация физико-химических и биологических свойств СО достигается добавлением в него стабилизирующих соединений, таких как глицин и L-пролин до конечных концентраций 12,5 г/л, корректировкой рН до значения 5,0±0,5, стерильным розливом и лиофильным высушиванием. Плазма, которая является сырьем для производства СО, должна быть предварительно проверена на отсутствие поверхностного антигена вируса гепатита В (HBsAg), антигена р24 ВИЧ-1, антител к вирусу иммунодефицита человека (ВИЧ-1, ВИЧ-2), вирусу гепатита С.
Способ получения СО включает следующие стадии:
- отбор плазмы человека с специфической активностью 1:10 и выше, проверенной на отсутствие маркеров гемотрансмиссивных инфекций;
- получение концентрата иммуноглобулина G (не менее 95% от общего белка) в соответствии с производственным регламентом изготовления препарата иммуноглобулина человека против КЭ;
- доведение содержания антител к вирусу КЭ от 1:80 до 1:320;
- внесение в концентрат иммуноглобулина G глицина и L-пролина до конечных концентраций 12,5 г/л;
- доведение величины рН до значения 4,5-5,5;
- стерильный розлив в асептических условиях;
- лиофильное высушивание до показателя остаточной влажности не более 1%.
Между совокупностью существенных признаков СО и достигаемым техническим результатом существует комплекс причинно-следственных связей, а именно:
1) способ изготовления СО позволяет обеспечить идентичность свойств и состава стандартного и анализируемых образцов иммуноглобулинов человека против КЭ, за счет чего достигается возможность использования в двух иммунологических реакциях - РТГА и ИФА, а также повышается достоверность определения специфической активности препаратов иммуноглобулинов человека против КЭ;
2) способ получения СО позволяет обеспечить постоянство концентрации IgG к вирусу КЭ в процессе хранения, транспортирования и использования, в том числе при отклонении температурных режимов хранения от регламентированных и многократном использовании регидратированной формы СО: сохранность антител гарантируется в течение 3 лет при режиме хранения (5±3)°С, а также допускается повышение температуры до (25±5)°С в процессе транспортировки. После регидратации (восстановления) СО может быть использован в соответствии с инструкцией по применению в течение 1 месяца, за счет чего достигается упрощение способа транспортирования и более эффективное использование заявляемого СО.
Полученный по заявленному способу стандартный образец полностью отвечает требованиям, предъявляемым к стандартным образцам для контроля иммунобиологических препаратов [1].
Краткое описание чертежей и графических материалов:
Табл. 1 Константы скоростей инактивации при изучении стабильности стандартного образца содержания антител IgG человека к вирусу клещевого энцефалита в методе «ускоренного старения»
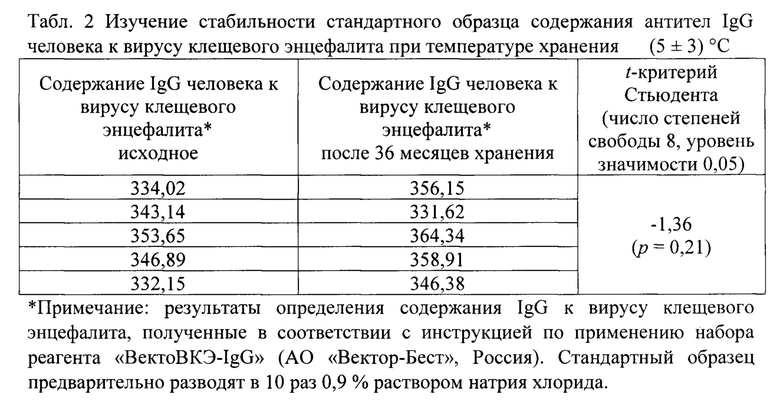
Табл. 2 Изучение стабильности стандартного образца содержания антител IgG человека к вирусу клещевого энцефалита при температуре хранения (5±3)°С
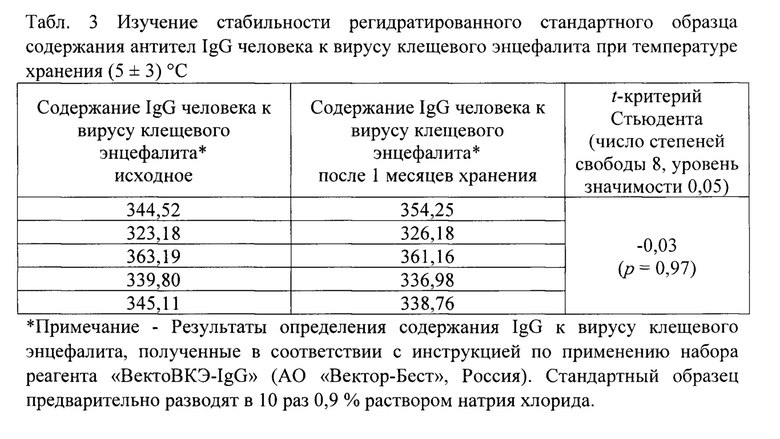
Табл. 3 Изучение стабильности регидратированного стандартного образца содержания антител IgG человека к вирусу клещевого энцефалита при температуре хранения (5±3)°С
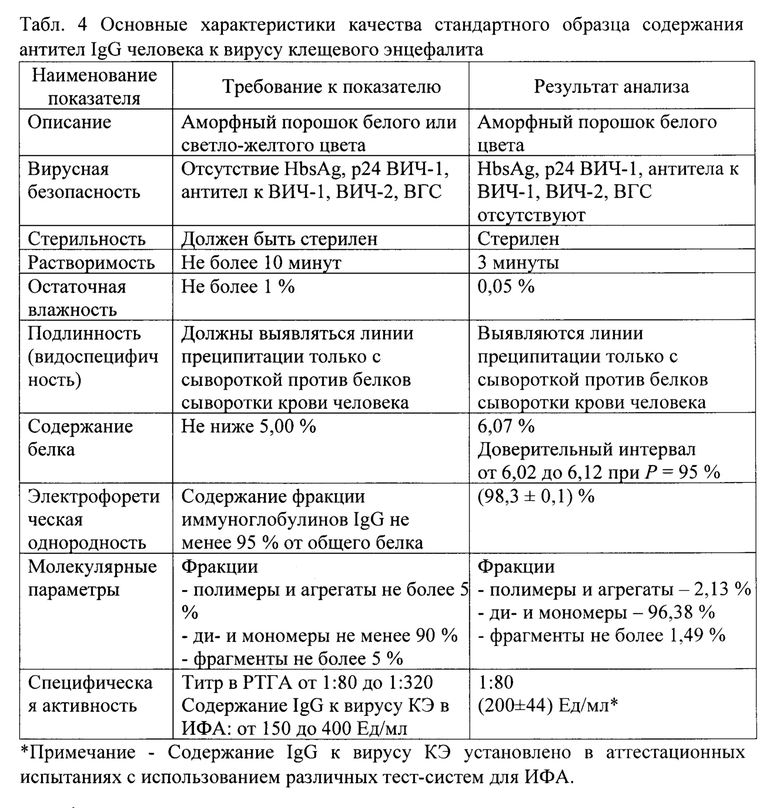
Табл. 4 Основные характеристики качества стандартного образца содержания антител IgG человека к вирусу клещевого энцефалита
Возможность осуществления заявленного изобретения может быть проиллюстрирована следующими примерами.
Пример 1. Сырьем для получения СО является плазма крови иммунизированных доноров или доноров-реконвалесцентов, содержащая специфические антитела IgG.
Отбор доноров для иммунизации и контроль состояния их здоровья в процессе вакцинации осуществляют в соответствии с действующими требованиями. Возможное влияние систематических плазмодач и предыдущих иммунизаций на показатели иммунологической реактивности доноров исключают путем привлечения лиц, первично или эпизодически сдающих плазму, в анамнезе которых отсутствуют какие-либо прививки в течение последних 3-5 лет.Иммунизацию доноров осуществляют вакциной КЭ культуральной очищенной инактивированной сухой концентрированной производства ФГУП ПИПВЭ им. М.П. Чумакова РАМН, Россия или аналогичной. Вакцину вводят подкожно в область плеча по схеме: двукратно по 0,5 мл с интервалом между прививками 5-7 месяцев. Ревакцинацию осуществляют в той же дозе через 1 год после завершения первичного курса, затем с интервалом 3 года. Оценку содержания антител к вирусу КЭ в образцах сыворотки крови иммунизированных доноров проводят через 1 неделю после окончания курса вакцинации.
Заготовку иммунной плазмы осуществляют методом прерывистого плазмафереза в соответствии с действующими инструкциями, используя напольные рефрижераторные центрифуги RotoSilenta 630 RS (Andreas Hettich GmbH & Co.KG, Германия) и методом автоматического плазмафереза с использованием аппарата для донорского плазмафереза PCS 2 (Heamonetics, США). Плазму, заготовленную в первичную упаковочную тару, подвергают быстрому замораживанию в шоковом замораживателе NZKR 48/80 (Frigera, Чехия) или аппарате медицинском для температурной обработки крови MBF 21 (Dometic S.A.R.L., Люксембург) при температуре минус 70°С в течение 1 ч 20 мин. Замороженную плазму перемещают в морозильный ларь D-LT (Derby A/S - Gram A/S, Германия), где выдерживают при температуре не выше минус 35°С до получения результатов тестов на соответствие спецификации и результатов выявления антител к вирусу КЭ. Далее замороженную в первичной упаковке плазму перемещают во вторичную групповую тару - полимерный ящик вместимостью 30 «компопластов», которую немедленно транспортируют в камеру низкотемпературную сборную теплоизоляционную для хранения препаратов крови модели «ISO-160» (Teledor, Германия). Температура хранения плазмы не превышает минус 35°С.Контроль показаний термодатчика осуществляют не реже 2 раз в сутки с обязательной регистрацией в «Журнале учета температуры хранения плазмы». Значительные колебания температуры хранения плазмы не допускаются.
Для загрузки на фракционирование отбирают плазму с титром антител на момент плазмодачи не менее 1:10. По окончании карантинизации плазму размораживают при комнатной температуре в течение 3 суток. Фракционирование проводят в соответствии с Производственным Регламентом получения иммуноглобулина человека против КЭ до получения концентрата иммуноглобулина G.
Специфическую активность раствора иммуноглобулина доводят до значений титра в диапазоне от 1:80 до 1:320, концентрацию вносимых веществ: L-пролина 12,5 г/л, глицина 12,5 г/л. Корректируют величину рН до значения 5,0±0,5. Затем в асептических условиях полученный раствор подвергают стерилизующей фильтрации, розливу в стерильные флаконы из нейтрального стекла.
Флаконы с раствором иммуноглобулина (растворитель вода) замораживают при температуре минус (40±1)°С не менее 24 часов. Высота раствора во флаконе 20 мм.
В контрольные флаконы строго вертикально устанавливают датчики температуры.
Змеевик десублиматора установки для лиофильного высушивания LZ-45 (Frigera, Чехия) охлаждают до температуры минус (55±5)°С, полки стойки - до температуры минус (30±5)°С.Камеру закрывают крышкой и через 30 - 40 мин включают вакуумный насос установки. При достижении ваккуума 0,3...0,15 Торр, температуры материала минус (45±5)°С включают систему нагревания.
Процесс высушивания проводят в течение (28±2) ч до температуры образца (35±3)°С при значении вакуума (0,15±0,05) Торр.
Все флаконы закрывают стерильными резиновыми пробками и завальцовывают алюминиевыми колпачками. Серия СО составляет 500 флаконов.
Пример 2. Важным требованием к СО является стабильность содержания IgG к вирусу КЭ в процессе хранения, которая достигается внесением стабилизирующих добавок, корректировкой значений рН 5,0±0,5 и лиофильным высушиванием до показателя остаточной влажности не более 1%. Оценку стабильности проводят методом ускоренного старения с использованием уравнений кинетики химических реакций. Учитывая, что активность образца при определенной температуре со временем уменьшается по закону мономолекулярной реакции, выражают константу скорости реакции при температуре Т (К) как функцию активности. Поскольку зависимость константы скорости инактивации от температуры подчиняется уравнению Аррениуса и носит линейный характер, зная три константы при трех разных температурах, методом экстраполяции определяют константу при предполагаемой температуре хранения (4°С) и рассчитывают время, в течение которого концентрация активного вещества уменьшается на 1%.
Образцы закладывают на хранение в суховоздушные термостаты при температурах 30, 45 и 56°С, через 24, 38, 52, 74, 130 и 210 суток хранения контролируют содержание антител методом ИФА.
Логарифмы константы дезактивации представлены в Табл. 1. Рассчитанный срок годности составил 4,04 года, что позволило предварительно установить срок хранения стандартного образца - 3 года.
В ходе ускоренных испытаний снижение содержания антител IgG человека к вирусу КЭ наблюдалось не ранее, чем на 52 сутки хранения в режимах 30, 45°С, что позволяет хранить СО в течение недлительного времени при повышенных температурах без изменения концентрации IgG к вирусу КЭ. Благодаря этому упрощаются требования к транспортированию СО.
Пример 3. Результаты ускоренных испытаний подтверждают контролем стабильности при температуре хранения СО от 2 до 8°С. Продолжительность контроля составляет 36 месяцев. С использованием t-критерия Стьюдента подтверждают статистическую эквивалентность результатов определения исходного содержания антител IgG человека к вирусу КЭ и к концу срока хранения - 36 месяцев (Табл. 2).
Таким образом, заявляемый способ получения СО обеспечивает стабильность аттестуемой характеристики в течение 36 месяцев.
Пример 4. С целью изучения срока использования регидратированного СО содержимое флаконов с СО восстанавливают в 1,6 мл воды очищенной. Для моделирования многократного использования флаконы с СО в течение 1 месяца два раза в неделю оставляют при комнатной температуре на 2 часа, каждый раз отбирая автоматическим дозатором по 100 мкл пробы. Затем снова помещают в холодильник и продолжают хранить при температуре от 2 до 8°С. С использованием t-критерия Стьюдента подтверждают статистическую эквивалентность результатов определения исходного содержания антител IgG человека к вирусу КЭ и к концу срока наблюдения (Табл. 3).
Данные, представленные в Табл. 3, подтверждают, что регидратированный СО может применяться в течение месяца без потери специфической активности, что повышает эффективность использования СО содержания антител к вирусу КЭ.
Пример 5. В готовом лиофилизированном стандарте контролируют некоторые физико-химические параметры (время растворения, подлинность, белок, электрофоретическую однородность, молекулярные параметры, остаточную влажность), специфическую активность, вирусную безопасность. Указанные характеристики стандартного образца представлены в Табл.4.
Из данных, представленных в Табл. 4, следует, что СО представляет собой выделенную из плазмы крови доноров иммунологически активную белковую фракцию, основным компонентом которой является IgG человека к вирусу КЭ с специфической активностью 1:80; процесс лиофилизации проведен до остаточной влажности 0,05%, что соответствует заявленному требованию для лиофильных форм СО иммунобиологических препаратов -не более 1%, образец хорошо растворяется в воде, стерилен, не содержит маркеров гемотрансмиссивных инфекций. При этом СО содержания антител IgG человека к вирусу КЭ имеет близость свойств и состава к анализируемым препаратам иммуноглобулина человека против КЭ. За счет чего достигается повышение достоверности результатов определения специфической активности препаратов иммуноглобулинов против КЭ, а также возможность использования СО в иммунологических методах - РТГА и ИФА.
Пример 6. Хранение и транспортирование стандартного образца.
Экземпляры СО хранят при температуре (5±3)°С в защищенном от света месте. Транспортирование осуществляется всеми видами крытого транспорта.
Допускается недлительное (до 30 суток) повышение температуры до (25±5)°С в процессе хранения и транспортировки.
Регидратированный образец хранят при температуре (5±3)°С в течение 1 месяца.
Аналогичным образом, с учетом раскрытия изобретения в описании, специалистом в данной области могут быть получены, выполнены другие варианты изобретения, которые охватываются формулой изобретения, приводимой ниже.
СПИСОК ЛИТЕРАТУРЫ
1. WHO expert committee on biological Standardization. Annex 2 Recommendation for the preparation, characterization, and establishment of international and other biological reference standards // WHO Technical Report Series. 2006. №932. P. 73-131.
2. Лист-вкладыш к Международному стандарту ВОЗ: сыворотка против клещевого энцефалита, NIBSC code: TILI [Электронный ресурс] URL: https://www.nibsc.org/documents/ifu/TILI.pdf (дата обращения 16.12.2019).
3. Лист-вкладыш к Международному стандарту ВОЗ: сыворотка против клещевого энцефалита, NIBSC code: TISA [Электронный ресурс] URL: https://www.nibsc.org/documents/ifu/TISA.pdf (дата обращения 16.12.2019).
Приложение

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ИММУНОГЛОБУЛИНА ЧЕЛОВЕКА ПРОТИВ КЛЕЩЕВОГО ЭНЦЕФАЛИТА ДЛЯ ВНУТРИВЕННОГО ВВЕДЕНИЯ | 1996 |
|
RU2141342C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ПАНЕЛИ СЫВОРОТОК ДЛЯ ОПРЕДЕЛЕНИЯ АНТИТЕЛ К ВИРУСУ ГЕПАТИТА В | 2007 |
|
RU2367960C2 |
| СПОСОБ КОМПЛЕКСНОГО ЛЕЧЕНИЯ БОЛЬНЫХ КЛЕЩЕВЫМ ЭНЦЕФАЛИТОМ | 1998 |
|
RU2158606C2 |
| Композиция для определения содержания иммуноглобулинов IgA в лекарственных препаратах | 2022 |
|
RU2794887C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ РАБОЧЕГО СТАНДАРТА СЫВОРОТОК, СОДЕРЖАЩИХ АНТИТЕЛА К ВИРУСУ ГЕПАТИТА С | 2008 |
|
RU2380711C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЛИОФИЛИЗИРОВАННОГО ПРЕПАРАТА НА ОСНОВЕ РЕКОМБИНАНТНОГО α-2-ИНТЕРФЕРОНА ПРОТИВ ВИРУСНЫХ БОЛЕЗНЕЙ ПЛОТОЯДНЫХ | 1995 |
|
RU2121364C1 |
| Иммунобиологическое средство для профилактики заболеваний, вызванных вирусом клещевого энцефалита на основе рекомбинантного вируса рода Flavivirus | 2022 |
|
RU2795800C1 |
| СПОСОБ ПОЛУЧЕНИЯ И АТТЕСТАЦИИ СТАНДАРТНОГО ОБРАЗЦА АНТИГЕНА ВИРУСА КЛЕЩЕВОГО ЭНЦЕФАЛИТА | 2017 |
|
RU2667957C1 |
| ПРЕПАРАТ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ДИФТЕРИИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1999 |
|
RU2174408C2 |
| ПРОТИВОВИРУСНЫЙ ПРЕПАРАТ И СПОСОБ ПОЛУЧЕНИЯ ИММУНОГЛОБУЛИНА ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ВИРУСНЫХ ЗАБОЛЕВАНИЙ | 1999 |
|
RU2144379C1 |
Изобретение относится к биотехнологии, а именно к получению стандартного образца содержания антител IgG человека к вирусу клещевого энцефалита. Способ включает отбор субстанции плазмы доноров, проверенной на отсутствие поверхностного антигена вируса гепатита В (HBsAg), антигена р24 ВИЧ-1, антител к вирусу иммунодефицита человека (ВИЧ-1, ВИЧ-2), вирусу гепатита С, с активностью 1:10 и выше; выделение специфической иммуноглобулиновой фракции спиртовым методом при низких температурах с последующими стадиями ультрафильтрации и концентрирования до получения раствора иммуноглобулина G (не менее 95% от общей белковой фракции) с содержанием антител человека к вирусу КЭ в титре от 1:80 до 1:320; внесение стабилизаторов до конечных концентраций глицина - 12,5 г/л, L-пролина - 12,5 г/л; корректировку величины рН до значений 5,0±0,5; стерильный розлив; лиофильное высушивание до показателя остаточной влажности не более 1%. Техническим результатом заявляемого изобретения являются идентичность стандартного образца по составу и свойствам анализируемому материалу - препаратам иммуноглобулинов человека против КЭ, и повышение сохранности антител IgG к вирусу КЭ в процессе хранения, транспортирования и использования стандартного образца. 6 пр., 4 табл.
Способ получения стандартного образца содержания антител IgG человека к вирусу клещевого энцефалита для контроля специфической активности препаратов иммуноглобулинов человека против клещевого энцефалита, отличающийся тем, что в качестве сырья используют плазму крови доноров, содержащую антитела к вирусу КЭ, со специфической активностью 1:10 и выше, проверенную на отсутствие поверхностного антигена вируса гепатита В (HBsAg), антигена р24 ВИЧ-1, антител к вирусу иммунодефицита человека (ВИЧ-1, ВИЧ-2), вирусу гепатита С; получают раствор иммуноглобулина с содержанием фракции IgG не менее 95% от общего белка в соответствии с производственным регламентом изготовления препарата иммуноглобулина человека против КЭ, устанавливают содержание антител к вирусу КЭ от 1:80 до 1:320, вносят глицин и L-пролин в концентрациях 12,5 г/л, корректируют величину рН до значения 5,0±0,5, стерильно разливают и лиофильно высушивают до величины остаточной влажности не более 1%.
| Лист-вкладыш к Международному стандарту ВОЗ: сыворотка против клещевого энцефалита, NIBSC code: TILI [Электронный ресурс] URL: https://www.nibsc.org/documents/ifu/TILI.pdf (дата обращения 16.12.2019) | |||
| КОРМЩИКОВА Е.С | |||
| и др | |||
| Выбор композиции стандартного образца антител человека к вирусу клещевого энцефалита, Актуальные вопросы трансфузиологии и |
Авторы
Даты
2020-11-09—Публикация
2020-04-03—Подача