ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Изобретение относится к биотехнологии, в частности, к технологии получения вакцины против герпеса, а именно, вакцины на основе химерного белка или синтетической ДНК, кодирующей указанный химерный белок.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Предполагается, что более 3,7 миллиардов человек младше 50 лет заражены вирусом герпеса (http://meddaily.ru/article/30Oct2015/virgherp; http://vitaportal.ru/dermatologiya/genitalnyj-gerpes-mirovaya-statistika.html). В этой связи создание вакцины против герпеса является весьма актуальной и практически важной задачей.
Одной из проблем, стоящей перед исследователями при создании вакцин в данной области, является существование разных типов вируса герпеса. Herpesviridae (герпесвирусы) - большое семейство оболочечных, двуцепочечных ДНК-содержащих вирусов, являющихся причиной различных инфекции, начиная с пузырьков на губах («простуды») и ветрянки до мононуклеоза и сходных заболеваний у животных, включая человека. Отличительной особенностью заболеваний является нахождение вирусов в организме животного в латентном состоянии. Герпесвирусы человека включают 8 типов вирусов, обозначаемых I-VIII, представителями которых являются вирус простого герпеса первого типа (HSV-1) и HSV-2, вирус ветряной оспы (VZV), вирус Эпштейна-Барра (EBV), цитомегаловирус (HCMV), розеоловирусы и герпесвирусы, ассоциированные с саркомой Капоши (KSHV).
В этой связи современные исследования в области создания препаратов против вирусов герпеса направлены на разработку рекомбинантных вакцин на основе антигенов вирусов герпеса человека типов I-VIII.
Все герпетические вакцины можно подразделить на три основных вида: живые вакцины, инактивированные и рекомбинантные. К живым вакцинам относится, в частности, вирионная герпетическая вакцина против вирусов герпеса 1 и 2 типов, полученная выращиванием на поверхности стационарного микроносителя первичной культуры клеток почек кролика (Андонов П. и соавт. "Вопросы вирусологии", 1979, N 6, стр. 665-671). Данная технология, однако, не позволяет достичь высоких урожаев и концентрации вирусов ввиду использования первично трипсинизированных клеток. Кроме того к недостаткам живой вакцины можно отнести то, что вакцины этого типа нельзя использовать при лечении людей из-за онкогенности некоторых видов герпеса.
Примером инактивированных вакцин является вакцина против вируса простого герпеса (US 4816250), при получении которой инфицированные клетки эмбриона человека MRC 5 после инкубирования обрабатывают поверхностно-активным веществом, а полипептидные цепи цитоплазматической фракции фиксируют. Данный метод довольно сложен и включает использование антител, иммобилизованных на сефарозе. Кроме того использование инактивированных вакцин вызывает достаточно слабый иммунный ответ, что вызывает необходимость применения нескольких разовых доз (бустерных иммунизаций).
В настоящее время считают, что наиболее перспективной антигерпетической вакциной может служить ДНК-вакцина, представляющая собой генно-инженерную конструкцию, обеспечивающую синтез вирусных белков in vivo. Важнейшими преимуществами ДНК-вакцин являются способность активации как клеточного, так и гуморального иммунитета, а также долговременная экспрессия антигенов, что обеспечивает более длительный и стойкий иммунитет. Эти особенности ДНК-вакцины обеспечивают повышенную эффективность для лечения инфекций, вызванных различными типами вирусов герпеса человека, так как показана ведущая роль Т-клеточного иммунитета в борьбе с данными инфекциями.
Из EA 201391109 известен подход, заключающийся в объединении молекул нуклеиновых кислот, кодирующих белки разных герпесвирусов, для создания ДНК-вакцины. В частности, указанные белки могут быть выбраны из белков оболочки вирусов. Раскрыта возможность создания поливалентной вакцины, содержащей кодирующую последовательность двух или более антигенов, кодирующих разные эпитопы герпесвируса, которые могут быть представлены в одном векторе для обеспечения их совместной экспрессии в одной клетке. При этом согласно данному документу, эпитопы, представленные в одном векторе, относятся к одному штамму вируса герпеса, и экспрессируются в виде отдельных белков, каждый из которых несет свой эпитоп.
WO 2013078299 относится к вакцинам и иммуногенным композициям против HSV-2, содержащим носитель, адъювант и нуклеиновую кислоту, кодирующую по меньшей мере один полипептид вируса герпеса HSV-2. Указанная композиция может содержать комбинацию нуклеиновых кислот, кодирующих два или более антигена, выбранных из ICP4, ICP4.9, gL2, gG2 и gD2.
В RU 228386 C2 раскрыты ДНК-вакцины для индуцирования иммунного ответа у животных, в частности, собак, кошек и лошадей, против 1-3 вирусов герпеса, где вакцины содержат несколько плазмид, каждая из которых экспрессирует свой антиген вируса герпеса с последовательностью, оптимизированной путем делеции фрагмента трансмембранного домена.
Авторы настоящего изобретения неожиданно обнаружили, что использование химерного белка, включающего набор эпитопов различных штаммов герпесвирусов человека, а именно штаммов I-VIII, характеризующегося последовательностью SEQ ID NO: 4, или структурно близкими (гомологичными) последовательностями, эффективно обеспечивает индукцию разнонаправленного иммунного ответа против инфекции вируса герпеса. Таким образом, в отличие от предложенных согласно уровню техники вакцин, изобретение предусматривает введение лишь одного терапевтического агента для достижения иммунного ответа против различных штаммов вируса герпеса, что облегчает схему введения, улучшает комлпаентность и также может обеспечивать более эффективную иммунизацию по сравнению с известными вакцинами.
Таким образом, целью настоящего изобретения является получение улучшенных ДНК-вакцин, индуцирующих эффективный защитный и иммунный ответ против разных герпесвирусов человека типов I-VIII посредством химерного гена, кодирующего и экспрессирующего химерный белок, характеризующийся последовательностью SEQ ID NO: 4 или гомологичными последовательностями. Преимуществом настоящего изобретения является кодирование нескольких эпитопов разных типов герпесвирусов в рамках одного химерного гена в одной плазмиде, что облегчает контроль экспрессии указанного гена в клетке-хозяине и индуцирование иммунного ответа, а также позволяет объединить в одной конструкции лекарственный препарат против всех восьми типов вирусов герпеса, вызывающих заболевания у людей.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В одном из воплощений изобретения предложен химерный белок для индуцирования и/или облегчения индукции иммунного ответа в результате инфекции герпесвируса, имеющий последовательность, которая гомологична по меньшей мере на 70% последовательности SEQ ID NO: 4.
В одном из воплощений изобретения предложена синтетическая нуклеиновая кислота, кодирующая указанный химерный белок или последовательность, гомологичную SEQ ID NO: 2 или 4 по меньшей мере на 70%. В одном из предпочтительных воплощений синтетическая нуклеиновая кислота имеет последовательность, которая по меньшей мере на 70% идентична последовательности SEQ ID NO: 3.
В одном из воплощений изобретения предложен вектор для экспрессии синтетической нуклеиновой кислоты, кодирующей химерный белок с последовательностью SEQ ID NO: 4.
В одном из воплощений также предложена клетка-хозяин, содержащая указанный выше вектор и предназначенная для продуцирования химерного белка по изобретению.
Еще в одном воплощении предложен способ получения указанного выше вектора, включающий культивирование клетки-хозяина, как определено выше, и выделение и очистку вектора из биомассы клеток.
Также в изобретении предложены разные воплощения вакцин для индуцирования иммунного ответа против инфекции герпесвируса, содержащие химерный белок либо синтетическую нуклеиновую кислоту, как определено выше, и фармацевтически приемлемое вспомогательное вещество.
ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
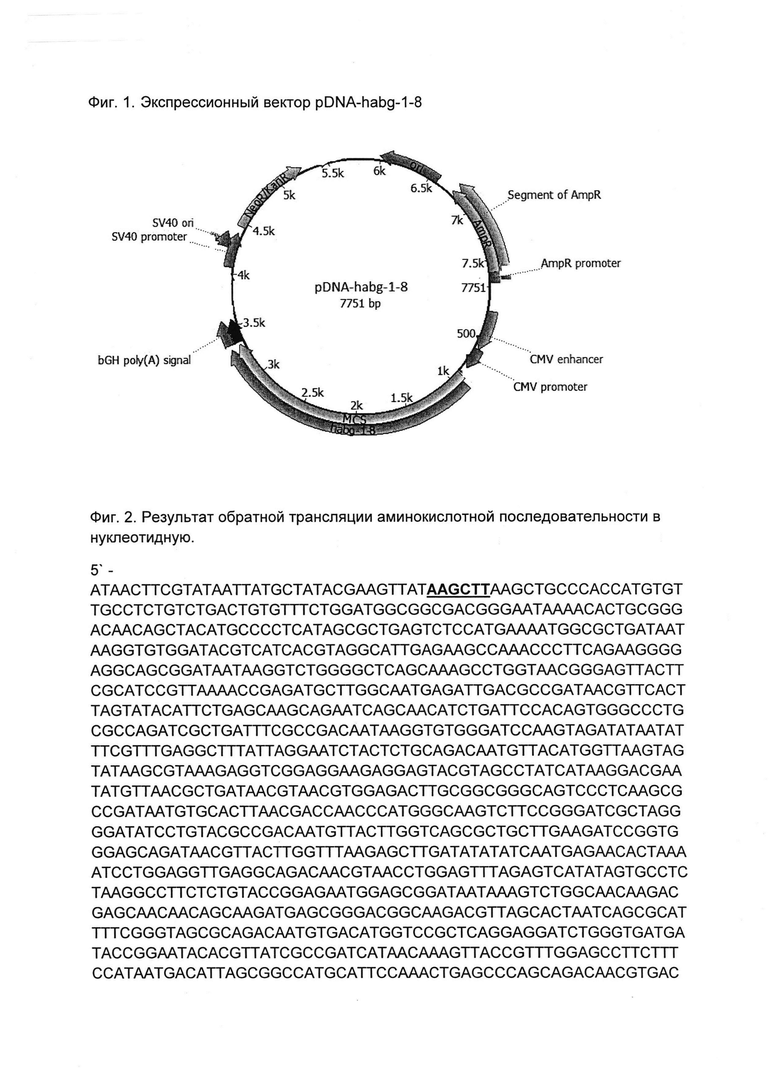
На Фиг. 1 показана карта экспрессионного вектора pDNA-habg-1-8, представляющего собой одно из воплощений вектора по изобретению, где используются следующие обозначения:
CMVenhancer - энхансер предранних генов цитомегаловируса
CMVpromoter - промотор предранних генов цитомегаловируса
AmpR - ген устойчивости к ампициллину
AmpRpromoter - промотор гена устойчивости к ампициллину
bGHpoly(A) signal - сигнал полиаденилирования гена бычьего гормона роста
habg-1-8 - ген, кодирующий химерный белок по изобретению
SV40 promoter - промотор ранних белков вируса SV40
NeoR - ген устойчивости к неомицину
Ori - точка начала репликация
На Фиг. 2 показана нуклеотидная последовательность, полученная путем обратной трансляции аминокислотной последовательности химерного белка по изобретению. Триплеты были оптимизированы для экспрессии в организме человека, были выбраны наиболее часто встречающиеся кодоны. Полужирным шрифтом выделен сайт рестрикции HindIII и курсивом - Xhol.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Определения
Если не определено иное в данной заявке, научные и технические термины, используемые в связи с настоящим изобретением, имеют значения, которые обычно понятны специалистам в данной области. В общем, используемые номенклатура и методы клеточной и тканевой культуры, молекулярной биологии, иммунологии, микробиологии, генетики и химии белков и нуклеиновых кислот, гибридизации, аналитической химии, синтетической органической химии и медицинской и фармацевтической химии, описанные в данной заявке, представляют собой номенклатуру и методы, хорошо известные и обычно использующиеся в данной области.
Способы и методы по настоящему изобретению обычно осуществляют в соответствии с традиционными способами, хорошо известными в данной области, и как описано в различных общих и более конкретных источниках, которые цитируются и обсуждаются в настоящем описании, если не указано иное. См., например, Sambrook J. & Russell D. Molecular Cloning: A Laboratory Manual, 3rd ed., Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y. (2000); Ausubel et al., Short Protocols in Molecular Biology: A Compendium of Methods from Current Protocols in Molecular Biology, Wiley, John & Sons, Inc. (2002); Harlow and Lane Using Antibodies: A Laboratory Manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y. (1998); и Coligan et al., Short Protocols in Protein Science, Wiley, John & Sons, Inc. (2003).
Способы введения мутации в аминокислоты белка хорошо известны специалистам в данной области (см., например, Ausubel (ed.), Current Protocols in Molecular Biology, John Wiley and Sons, Inc. (1994); T. Maniatis, E.F. Fritsch and J. Sambrook, Molecular Cloning: A Laboratory Manual, Cold Spring Harbor laboratory, Cold Spring Harbor, N.Y. (1989)).
Используемая здесь терминология предназначена для целей описания конкретных вариантов воплощения изобретения и не является ограничивающей. При использовании в настоящем описании и формуле изобретения, формы единственного числа включают множественного число, если контекст явным образом не указывает на иное.
Термины "антиген", "иммуноген" и "эпитоп", которые, как подразумевается в данной заявке, используются взаимозаменяемо, относятся к молекуле, способной связываться антителом, В-клеточным рецептором (BCR) или Т-клеточным рецептором (TCR), если он представлен молекулами МНС (главный комплекс гистосовместимости). Использованные в данной заявке термины "антиген" и "иммуноген" также охватывают Т-клеточные эпитопы. Кроме того, антиген может распознаваться иммунной системой и/или способен индуцировать гуморальный иммунный ответ и/или клеточный иммунный ответ, приводящий к активации В- и/или Т-лимфоцитов. Антиген может иметь один или более эпитопов (например, В- и Т-эпитопов). Предполагают, что специфическая реакция, рассмотренная выше, указывает, что антиген будет предпочтительно реагировать, обычно высокоселективным образом, с его соответствующим антителом или TCR, а не с множеством других антител или TCR, которые могут быть индуцированы другими антигенами. Антигены также могут представлять собой смеси нескольких индивидуальных антигенов. Оба термина "антиген" и "иммуноген" охватывают без ограничений полипептиды.
Ссылки на аминокислотные остатки, использованные в настоящей заявке, обозначены однобуквенным или трехбуквенным кодом (см., например, Lehninger, Biochemistry, 2nd edition, Worth Publishers, New York, 1975, p. 72).
Термин "пептид" или "полипептид" относится к полимеру из аминокислот независимо от длины полимера; таким образом, фрагменты белка, олигопептиды и белки включены в определение пептида или полипептида. Этот термин также не определяет или не исключает постэкспрессионные модификации полипептидов, например, полипептидов, которые включают ковалентное присоединение гликозильных групп, ацетильных групп, фосфатных групп, липидных групп и тому подобного, однозначно охвачены термином "полипептид". В данное определение также включены полипептиды, которые содержат один или более аналогов аминокислоты (включая, например, не встречающиеся в природе аминокислоты, аминокислоты, которые встречаются в природе только вне неродственной биологической системы, модифицированные аминокислоты из систем млекопитающих и т.д.), полипептиды с замещенными связями, а также другие модификации, известные в данной области, как природные, так и не природные.
Термины "гомологичная последовательность" и "идентичная последовательность", которые используются здесь взаимозаменяемо, означает, например, что в последовательности, обладающей, например, 80% идентичности какой-либо другой последовательности, 80% идентичных аминокислот или нуклеотидов присутствует в том же положении при выравнивании последовательностей, которое можно осуществить известными в данной области техники способами.
Идентичность аминокислотной или нуклеотидной последовательности может быть определена традиционно с использованием известных компьютерных программ, таких как Bestfit, FASTA или BLAST (см., например, Pearson, Methods Enzymol. 183:63-98 (1990); Pearson, Methods Mol. Biol. 132:185-219 (2000); Altschul et al., J. Mol. Biol. 215:403-410 (1990); Altschul et al., Nucelic Acids Res. 25:3389-3402 (1997)).
Термин "адъювант" относится к любой молекуле, которую добавляют к вакцине по изобретению, для усиления иммуногенности указанной вакцины.
Термин "приблизительно" и аналогичные ему, такие как "около" и "примерно", при использовании здесь вместе с определенным значением, указывают на это значение плюс/минус 10%.
Химерный белок
Одной из задач настоящего изобретения является обеспечение технологии получения методом генной инженерии лекарственного препарата против герпеса для предупреждения и/или лечения заболевания, вызванного инфекцией герпесвируса, на основе химерного белка, имеющего последовательность SEQ ID NO: 4.
Химерный белок по настоящему изобретению обладает иммуногенной активностью, в частности, он обладает способностью индуцировать и/или облегчать индукцию иммунного ответа, в частности, гуморального и/или клеточного иммунного ответа в результате инфекции герпесвируса, выбранного из герпесвирусов типов I-VIII. В одном из воплощений, химерный белок по изобретению обладает иммуногенной активностью в отношении вируса простого герпеса человека.
Химерный белок по изобретению обеспечивает получение единой конструкции, содержащей несколько эпитопов герпесвирусов I-VIII типов, что позволяет облегчить индуцирование иммунного ответа.
Авторы настоящего изобретения неожиданно обнаружили, что при использовании эпитопов, принадлежащих разным типам герпесвирусов (типы I-VIII), возможно получить химерный белок, обладающий иммуногенной активностью.
Для конструирования химерного белка по изобретению использованы эпитопы разных типов герпесвирусов, выбранных из: gD и gB герпесвируса I типа (HV-1); gE HV-II, gp350 и LMP2 (поздний мембранный белок 2) HV-4; гликопротеиновый пентамер gH/gL/UL128/UL130/UL131A и димер gH/gL HV-5; IEP1 (немедленно-ранний белок 1), AVP (антигенный вирусный белок), рр85 (фосфопротеин 85), gH и главный капсидный белок HV-6A и HV-6B; gB и gp65 HV-7; LANA 1 (поздний ядерный антиген), K12, gB и K8.1 HV-8.
Эпитопы герпесвирусов в химерном белке по изобретению соединены посредством ковалентных связей и с помощью линкерных доменов, таких как полипептидные линкеры, или с помощью шарнирной области IgG человека. В частности, указанные линкеры могут быть выбраны из группы, состоящей из ADNKVW, ADNVHL, ADNVTW, RDGKTL, ADHNKVTVW, RDNKTL, RDHVTL, ADNKCL, ADEGNKVW.
В наиболее предпочтительном воплощении часть эпитопов, составляющих химерный белок по изобретению, соединены друг с другом без использования линкера: EVTD и QIADF (gH/gL HV-5); RDNSYMPLIALSLHENG (фосфобелок рр85 HV-6A и HV-6B) и DGGDGNKTL (поздний ядерный антиген (LANA 1) HV-8).
Функциональные элементы химерного белка расположены таким образом, чтобы иммунопротеасома производила правильное расщепление эпитопов и их последующую презентацию.
В одном из воплощений изобретения для активации антиген-презентации иммунопротеасомой в последовательность химерного белка могут быть включены эпитопы вирусов, отличных от вирусов герпеса. В одном из предпочтительных воплощений, на концах последовательности химерного белка по изобретению, имеющего последовательность SEQ ID NO: 4, могут быть включены эпитопы вируса лейкемии мышей Морони, выбранные из CCLCLTVFL и SSWDFITV, образуя, таким образом, последовательность SEQ ID NO: 2 или гомологичную ей по меньшей мере на 70%.
В таблице 1 ниже приведены аминокислотные последовательности функциональных элементов химерного белка по изобретению, имеющего последовательность SEQ ID NO: 4.
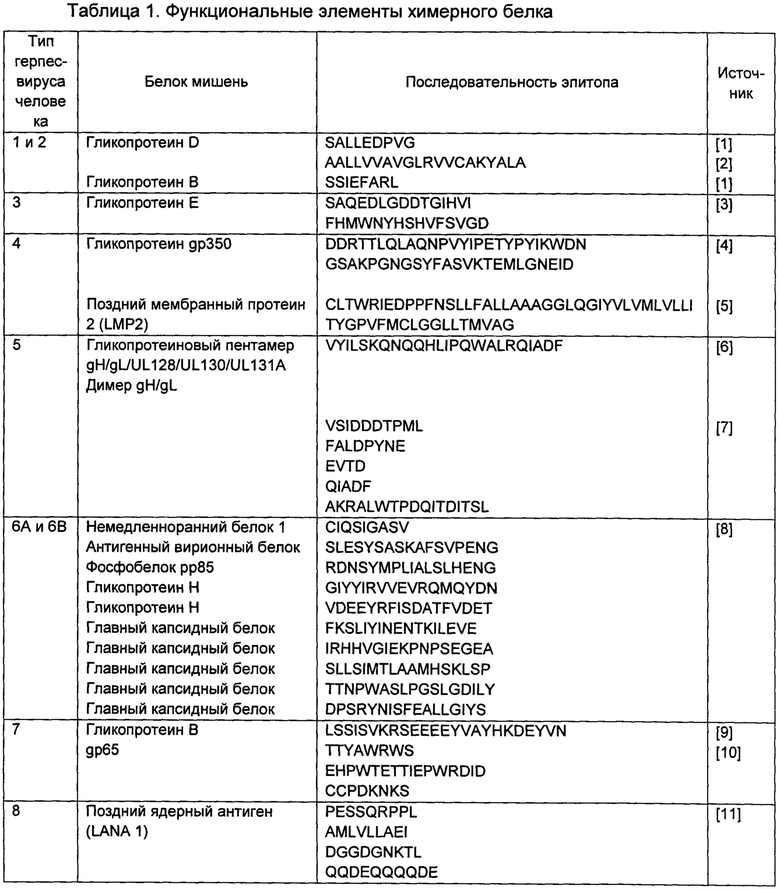

Таким образом, авторами настоящего изобретения была сконструирована последовательность химерного белка по изобретению (жирным шрифтом показаны эпитопы герпесвирусов; подчеркнуты линкеры между эпитопами):

Таким образом, химерный белок по изобретению отличается тем, что содержит эпитопы разных типов герпесвирусов и характеризуется последовательностью SEQ ID NO: 4, либо последовательностью, гомологичной последовательности SEQ ID NO: 4 по меньшей мере на 70%.
Специалисту в данной области понятно, что настоящее изобретение также охватывает аминокислотные последовательности химерного белка, обладающие эквивалентными химическими функциями и свойствами, которые получены любым известным в данной области техники способом, например, путем сайт-направленного мутагенеза или путем химического синтеза. Подобные варианты являются результатом консервативных аминокислотных замен, вставок и/или делеций в последовательности SEQ ID NO: 4.
В соответствии с настоящим изобретением, аминокислотная последовательность химерного белка имеет последовательность, гомологичную (идентичную) последовательности SEQ ID NO: 4 по меньшей мере на 70%, 75%, 80%, 85% или 90%. Более предпочтительно, аминокислотная последовательность химерного белка по изобретению гомологична последовательности SEQ ID NO: 4 по меньшей мере на 95%, 96%, 97%, 98% или 99%. При этом, данный белок сохраняет свою биологическую функцию, то есть, входящие в его состав аминокислотные последовательности обеспечивают генерацию антител, способных распознавать соответствующие эпитопы вирусов герпеса, а в случае, если белок подлежит экспрессии непосредственно в организме пациента, то его последовательность способна обеспечить адекватный посттрансляционный процессинг. Для специалиста в области генетический инженерии, знакомого с концепцией консервативных замен, не составит труда подобрать модификации последовательности SEQ ID NO: 4, удовлетворяющие указанным выше критериям и попадающие в указанный процент гомологии.
Химерный белок по изобретению может быть получен с помощью различных экспрессионных систем. Подходящие системы экспрессии включают без ограничений дрожжи, такие как S. cerevisiae, бактерии, такие как Е. coli и систему на основе бакуловируса (например, в клетках насекомых). В некоторых воплощениях, химерный белок может быть получен в системе клеток животного.
В одном из воплощений изобретения химерный белок может быть конъюгирован с другой молекулой, например, для увеличения его времени полужизни, растворимости, биодоступности или иммуногенности. Молекулы, которые могут быть конъюгированы с химерным белком по изобретению, включают без ограничений, биотин, полиэтиленгликоль, нуклеиновые кислоты, полисахариды и белки других патогенов или вирусов. Конъюгация может быть прямой или опосредованной (например, через линкер).
В некоторых воплощениях химерный белок может быть соединен на его C- или N-конце с меткой, сигналом секреции или другой сигнальной последовательностью. Примеры подобных меток и последовательностей описаны в WO 2013078299.
Нуклеиновая кислота
В изобретении также предложена нуклеотидная последовательность, кодирующая любую аминокислотную последовательность, раскрытую в настоящем описании для индуцирования и/или облегчения индукции иммунного ответа в результате инфекции герпесвируса. Указанная нуклеотидная последовательность позволяет упростить контроль экспрессии эпитопов герпесвирусов в клетке за счет того, что они содержатся в одном химерном белке. Подобные нуклеотидные последовательности представляют собой кодирующие последовательности, соответствующие эквивалентным пептидным последовательностям, и могут быть клонированы в векторе экспрессии вместе со стартовым кодоном, подходящей сигнальной последовательностью и кодоном терминации. Нуклеотидная последовательность может представлять собой ДНК или РНК. Предпочтительно нуклеотидной последовательностью является последовательность ДНК.
В наиболее предпочтительном воплощении нуклеотидная последовательность по изобретению содержит последовательность SEQ ID NO: 3. В одном из воплощений, нуклеотидная последовательность по изобретению состоит из последовательности SEQ ID NO: 3. В одном из воплощений, нуклеотидная последовательность по изобретению является гомологичной последовательности SEQ ID NO: 3 по меньшей мере на 70%. В одном из воплощений, нуклеотидная последовательность по изобретению является гомологичной последовательности SEQ ID NO: 3 по меньшей мере на 75%, предпочтительно 80%, 85%, 90%, 95%, 96%, 97%, 98% или 99%. При этом, данная нуклеотидная последовательность сохраняет свои биологические свойства, то есть, она способна экспрессировать белок, обладающий предусмотренными в данном изобретении свойствами, обеспечивая адекватную транскрипцию и трансляцию. Для специалиста в области генетический инженерии, знакомого с понятиями консервативных замен и вырожденности генетического кода, не составит труда подобрать модификации последовательности SEQ ID NO: 3, удовлетворяющие указанным выше критериям и попадающие в указанный процент гомологии
В одном из воплощений предложена нуклеотидная последовательность, которая гибридизуется в жестких условиях с любой из упомянутых выше последовательностей.
В одном из воплощений предложена нуклеотидная последовательность SEQ ID NO: 1, кодирующая химерный белок по изобретению, на концах которого находятся эпитопы вируса лейкемии мышей Морони, представляющие собой CCLCLTVFL и SSWDFITV. В одном из воплощений предложена нуклеотидная последовательность, которая гомологична последовательности SEQ ID NO: 1 по меньшей мере на 70%, 71%, 72%, 73%, 74%, 75%, 76%, 77%, 78%, 79%, 80%, 81%, 82%, 83%, 84%, 85%, 86%, 87%, 88%, 89%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99%.
Нуклеиновая кислота, кодирующая химерный белок по настоящему изобретению, способна экспрессироваться в клетке-хозяине. Нуклеотидная последовательность, кодирующая химерный белок по изобретению может быть оптимизирована для обеспечения стабильного и высокого уровня экспрессии указанного химерного белка. Клетка-хозяин может быть как прокариотической, так и эукариотической. Эукариотическая клетка-хозяин может быть клеткой млекопитающего, в частности человека.
Химерный ген
Настоящее изобретение также относится к химерному гену, содержащему в функциональном сцеплении друг с другом по меньшей мере один промотор, который является функциональным в организме-хозяине, нуклеиновую кислоту в соответствии с изобретением и терминаторный элемент, который является функциональным в том же организме-хозяине. Различные элементы, которые может содержать химерный ген, представляют собой, во-первых, элементы, регулирующие транскрипцию, трансляцию и созревание белков, такие как промотор, последовательность, кодирующая сигнальный пептид или транзитный пептид, или терминаторный элемент, составляющий сигнал полиаденилирования, и, во-вторых, полинуклеотид, кодирующий белок. Выбор регуляторных элементов зависит от клетки-хозяина, в котором они должны функционировать и специалисты в данной области техники способны без дополнительного экспериментирования выбрать необходимые регуляторные элементы.
Выражение "в функциональном сцеплении друг с другом" означает, что указанные элементы химерного гена сцеплены друг с другом таким образом, что на функцию одного из этих элементов влияет функция другого. Например, промотор функционально сцеплен с кодирующей последовательностью, когда он способен влиять на экспрессию указанной кодирующей последовательности. Конструирование химерного гена в соответствии с изобретением и сборку различных его элементов можно осуществить, используя методики, хорошо известные специалистам в данной области техники, в частности, описанные в Sambrook et al. (1989, Molecular Cloning: A Laboratory Manual, Nolan C. ed., New York: Cold Spring Harbor Laboratory Press). Выбор регуляторных элементов, составляющих химерный ген, существенно зависит от организма-хозяина, в котором они должны функционировать, и специалисты в данной области техники способны выбрать регуляторные элементы, которые являются функциональными в организме-хозяине, представляющего собой объект интереса. Термин "функциональный" указывает на способность функционировать в данном организме-хозяине.
Промоторы, которые могут содержать химерный ген в соответствии с изобретением, являются либо конститутивными, либо индуцибельными. Например, универсально эффективным промотором, используемым для экспрессии в клетках млекопитающих, является pCMV (промотор цитомегаловируса).
В соответствии с изобретением химерный ген может также содержать другие регуляторные последовательности, которые локализованы между промотором и кодирующей последовательностью, такие как транскрипционные активаторы (энхансеры).
Вектор
Настоящее изобретение также относится к экспрессионному вектору, содержащему нуклеиновую кислоту по изобретению. Вектор может быть кольцевым или линейным, одноцепочечным или двуцепочечным.
В одном из воплощений настоящего изобретения предложен вектор для введения и экспрессии химерного гена в клетке-хозяине. Вектор по изобретению способен к экспрессии указанного химерного гена в клетке организма млекопитающего, в частности, в клетке человека, в количестве, которое является эффективным для индуцирования иммунного ответа. В одном из предпочтительных воплощений указанный вектор представляет собой нуклеиново-кислотную структуру, способную к репликации в бактериальной клетке-хозяине.
Подходящие векторы известны специалисту в данной области и включают, например, плазмиды, космиды, искусственные хромосомы (например, бактериальные или дрожжевые), бактериофаги, вирусные векторы (например, ретровирусы, лентивирусы, аденовирусы, адено-ассоциированные вирусы), в частности, бакуловирусные векторы. Предпочтительно, вектор в соответствии с изобретением представляет собой плазмиду. Как правило, основными качествами этого вектора должна быть способность к поддержанию самого себя и самостоятельной репликации в клетках организма-хозяина, в частности, за счет присутствия точки начала репликации, и к экспрессии в них лиганда. В целях стабильной трансформации организма-хозяина вектор может также интегрироваться в геном. Тогда состав вектора может быть ограничен элементами, требующимися для синтеза герпесвирусного эпитопа в хозяевах. Выбор подходящего вектора, а также методики вставки гена в вектор известны специалисту в данной области и описаны, например, в Sambrook et al. (1989, Molecular Cloning: A Laboratory Manual, Nolan C. ed., New York: Cold Spring Harbor Laboratory Press) и Маниатис и др. (1984. Молекулярное клонирование).
В одном из предпочтительных воплощений вектор может быть выбран из pcDNA3 и pcDNA3.1 (Invitrogen), которые содержат цитомегаловирусный промотор и сигнал полиаденилирования гена гормона роста быка. В другом предпочтительном воплощении вектор может быть выбран из pVAX (Invitrogen), pCI, VR1012 DNA (Vical Inc.), pJW4303, pVAC1-mcs, pVAC2-mcs (InvivoGen). В еще одном предпочтительном воплощении вектор может представлять собой вирусный вектор, например, на основе аденовирусов (например, AD5), ортопоксвирусов, альфавирусов или любого другого подходящего для целей изобретения вектора, который коммерчески доступен и известен специалисту в данной области техники.
Регуляторные элементы, необходимые для экспрессии включают промотор, инициирующий кодон, стоп-кодон и сигнал полиаденилирования. Дополнительно, для эффективной экспрессии антигена в состав вектора может быть включен энхансер. Указанные элементы являются функционально-связанными с кодирующей антиген последовательностью и должны быть подходящими для функционирования в клетке-хозяине.
Инициирующий кодон может быть расположен выше кодирующей последовательности антигена. Стоп-кодон может быть расположен ниже кодирующей последовательности антигена. Инициирующий и стоп-кодоны могут располагаться в одной рамке считывания с кодирующей последовательностью антигена.
Примерами сигналов полиаденилирования, пригодных в рамках настоящего изобретения, в частности для получения генетической вакцины для человека, являются без ограничений сигналы полиаденилирования SV40 и LTR (длинные концевые повторы).
Промотор может являться промотором вируса обезьян 40 (SV40), промотором вируса опухоли молочной железы мыши (MMTV), промотором цитомегаловируса (CMV), промотором вируса Эпштейна-Барра (EBV). Промотор также может являться промотором гена человека, например, гена актина человека, гена миозина человека, гена гемоглобина человека. Промотор также может являться тканеспецифичным промотором, например, промотором, специфичным для мышцы и кожи, природным или синтетическим. В частности, для экспрессии в гепатоцитах подходит промотор гена десмина, для экспрессии в кератиноцитах - промотор гена гидроксилазы витамина D3. Примеры таких промоторов описаны в US 20040175727.
Вектор может включать гены для маркеров трансформации, указывающие на трансформацию бактериальной клетки вектором. Маркером трансформации может быть селективный маркерный ген, используемый для отличия и отбора клеток, являющихся эффективно трансформированными, то есть теми, в которых присутствует вектор, от клеток без вектора. Такие маркеры хорошо известны специалистам в данной области техники. Общепринято используемые селективные маркеры включают гены, которые придают устойчивость к специфичным антибиотикам, таким как ампициллин, неомицин и др. Некоторые векторы могут также включать маркерные гены, которые только указывают, какие клетки были трансформированы вектором. Такими генами могут быть гены, кодирующие пигменты или ферменты, регулирующие образование пигментов в трансформированных клетках. Подобные селективные маркерные гены, в частности, описаны в WO 91/02071, WO 95/06128, WO 96/38567 и WO 97/04103. Индикаторный маркерный ген может представлять собой последовательность гена lacZ, кодирующего фермент β-галактозидазу. Другие используемые маркеры трансформации включают, например, гены люциферазы и GFP.
Предпочтительным вектором по изобретению является плазмида. Предпочтительной плазмидой является плазмида, сконструированная для обеспечения экспрессии трансгенных генетических последовательностей. Большое число векторов известно и охарактеризовано (например, база http://genome-www.stanford.edu/vectordb/vector_pages/plasmid_pages/Plasmid.html). Примеры плазмид, которые позволяют относительно легко вводить экспрессионные кассеты, хорошо известны в данной области техники и доступны коммерческим путем (WO 1990002189, US 20140065699, US 2001/0016351).
В одном из воплощений настоящего изобретения вектор может быть пригоден для трансфекции клеток нуклеиновой кислотой, кодирующей химерный белок по изобретению, причем трансформированную клетку-хозяина культивируют и поддерживают в условиях, в которых происходит экспрессия указанного химерного белка. Способы трансформации для введения векторов в различные клетки и организмы хорошо известны. Например, векторную конструкцию можно вводить методом хлорида кальция/теплового шока (методом химически компетентных клеток), электропорации, посредством плазмидной конъюгации, бомбардировки частицами, с использованием генного пистолета, липосомных носителей и т.д.
Вектор трансформируют в организм с целью экспрессии химерного белка по изобретению. В предпочтительном воплощении вектор трансформируют в организм, который представляет собой бактерию. В более предпочтительном варианте воплощения вектор трансформируют в клетку человека.
Способы
В еще одном аспекте изобретение относится к способу получения вакцины против герпесвирусов, который состоит из отбора иммуногенных эпитопов вирусов герпеса человека на основе определения МНС-лигандов, образующихся в результате презентации иммунными клетками вирусного эпитопа, конвертации полученных аминокислотных последовательностей в нуклеотидные последовательности и их последующей кодоновой оптимизации для экспрессии в клетке-хозяине.
В другом аспекте изобретение относится к способу получения вектора, содержащего нуклеиновую кислоту с последовательностью SEQ ID NO: 3, состоящего из этапа культивирования клетки-хозяина, несущей в себе вектор (плазмиду) по изобретению, этапа выделения целевого продукта из биомассы указанных клеток и последующего этапа, состоящего в очистке целевого продукта. В предпочтительном воплощении плазмиду выделяют щелочным методом, и очистку продукта проводят с помощью аффинной хроматографии на полимиксин-Б-сефарозе.
Клетка
В изобретении также предложена клетка, трансформированная указанным вектором для продуцирования химерного белка по изобретению. Может быть использована любая клетка, обычно используемая в комбинации с экспрессирующимися векторами, описанными выше. Клетка для продуцирования химерного белка по изобретению может представлять собой эукариотическую или прокариотическую клетку. Эукариотическая клетка может быть выбрана из клетки животного или растения, например, клетка может представлять собой клетку дрожжей, СНО (клетки яичника китайского хомячка), Vero. Прокариотическая клетка может представлять собой, например, клетку Е. coli и ее штаммы BL21(DE3), BLR(DE3), origami 2(DE3), Bacillus или другие грамположительные бактерии, такие как Lactococcus lactis. Предпочтительные клеточные системы экспрессии включают Е. coli, такие как Е. coli DH10B.
Выражение "трансформированная клетка-хозяин" означает клетку-хозяина, которая дополнительно несет плазмиду, по меньшей мере один химерный ген в соответствии с изобретением, и которая, следовательно, продуцирует химерный белок в культуральной среде. Для получения организмов-хозяев в соответствии с изобретением специалисты в данной области техники могут использовать один из многих известных способов трансформации.
Вакцина
В предпочтительном воплощении предложена вакцина для индукции иммунного ответа против инфекции герпесвируса, содержащая химерный белок с последовательностью SEQ ID NO: 4 или химерный белок, аминокислотная последовательность которого по меньшей мере на 70, 75, 80, 85, 90, 95, 96, 97, 98 или 99% гомологична (идентична) последовательности SEQ ID NO: 4, и фармацевтически приемлемое вспомогательное вещество.
В наиболее предпочтительном воплощении изобретения предложена ДНК-вакцина для индукции иммунного ответа против инфекции герпесвируса, содержащая нуклеиновую кислоту, кодирующую химерный белок по изобретению, где последовательность нуклеиновой кислоты по меньшей мере на 70, предпочтительно на 75, 80, 85, 90, 95, 96, 97, 98 99%, либо наиболее предпочтительно полностью идентична последовательности SEQ ID NO: 3, и фармацевтически приемлемое вспомогательное вещество.
Вакцину по изобретению можно применять для индукции иммунных реакций, включая терапевтические или профилактические иммунные реакции. В одном из воплощений вакцина по изобретению позволяет получать антитела и/или Т-лимфоциты, направленные против по меньшей мере одного антигена герпесвируса. В другом аспекте вакцина также позволяет выделять такие антитела и клетки.
Будучи введенной субъекту, нуждающемуся в этом, вакцина по изобретению может стимулировать врожденный иммунный ответ, антительный ответ или клеточно-опосредованный иммунный ответ, или их комбинацию. В некоторых воплощениях вакцина по изобретению стимулирует инфильтрацию макрофагами, образование нейтрофилами антивирусных соединений, включающих ФНОα, оксид азота, интерфероны и ИЛ-12.
В некоторых воплощениях вакцина по изобретению вызывает клеточно-опосредованный иммунный ответ, который включает образование противовирусных цитокинов, CD4+ Т-клеток и/или CD8+ Т-клеток.
В одном из аспектов изобретения указанная вакцина обеспечивает защитный иммунитет, позволяющий вакцинированному субъекту отложить начало проявления симптомов заболевания или снизить тяжесть симптомов. В некоторых аспектах снижение тяжести симптомов происходит по меньшей мере на 30, 40, 50, 60, 70, 80 или 90%. В некоторых аспектах, применение вакцины позволяет обеспечить полное ингибирование инфекции герпесвирусом или появление симптомов инфекции.
В одном из аспектов изобретения указанную вакцину вводят субъекту, страдающему от инфекции герпесвируса, в количестве, достаточном для лечения этого субъекта. Лечение субъекта, таким образом, относится к исчезновению или снижению тяжести симптомов инфекции герпесвируса. В некоторых аспектах изобретения лечение относится к снижению продолжительности проявления симптомов заболевания.
Вакцина может дополнительно включать фармацевтически приемлемое вспомогательное вещество. Фармацевтически приемлемое вспомогательное вещество может представлять собой функциональную молекулу, например, среду-носитель, адъювант, носитель или разбавитель. Фармацевтически приемлемое вещество может включать поверхностно-активные вещества, например, иммуностимулирующие комплексы, неполный адъювант Фрейнда, ионы кальция, вирусные белки, полианионы, поликатионы, наночастицы или везикулы, например, сквален, гиалуроновую кислоту, липиды или другие известные специалисту в данной области агенты, облегчающие трансфекцию.
В одном из воплощений изобретения вакцина дополнительно содержит фармацевтически вспомогательное вещество, представляющее собой адъювант, который дополнительно усиливает и/или опосредует иммунный ответ, выбранный из врожденного ответа и/или адаптивного иммунного ответа. Адъювант может быть выбран из группы, включающей без ограничений альфа-интерферон, бета-интерферон, гамма-интерферон, липополисахариды, монофософориллипиды, CpG-содержащую ДНК, тромбоцитарный фактор роста, фактор некроза опухоли (ФНО), рецептор ФНО, эпидермальный фактор роста, эпителиальный хемокин, ассоциированный со слизистыми, фактор роста сосудов, фактор роста нервов, фактор роста эндотелия сосудов, интерлейкин-4 (ИЛ-4), ИЛ-7, ИЛ-18. Адъювант может представлять собой цитокин, который может быть выбран из белка или нуклеиновой кислоты, способной экспрессировать белок цитокина. Примеры подходящих адъювантов раскрыты в WO 2013078299.
В одном из воплощений вакцина по изобретению дополнительно содержит фармацевтически приемлемый носитель или разбавитель. Подходящие носители хорошо известны специалистам в данной области техники и включают без ограничений белки, сахара и т.д. Такие носители могут быть водными или неводными растворами, суспензиями и эмульсиями. Примеры неводных носителей включают без ограничений пропиленгликоль, полиэтиленгликоль, растительные масла, такие как оливковое масло, и инъецируемые органические сложные эфиры, такие как этилолеат. Водные носители включают без ограничений воду, водноспиртовые растворы, эмульсии и суспензии, включающие солевой раствор.
Выражение "адаптивный иммунный ответ" относится к иммунному ответу, основанному на активации компонента иммунной системы, придающего специфичность и память в отношении антигена или патогена. Такой ответ может быть высокоспецифичен в отношении антигена или патогена, и более эффективен при втором и последующих контактах с антигеном или патогеном. Такой адаптивный иммунный ответ может быть основан на активации лимфоцитов, таких как Т-клетки или В-клетки.
Выражение "врожденный иммунный ответ" относится к ответу, основанному на неспецифической системе распознавания и не меняется при последующем контакте с антигеном или патогеном. Такая система может быть основана на клетках иммунной системы, таких как, например моноциты, макрофаги или естественные киллеры (NK), или естественные киллеры Т (NKT) клетки.
В одном из воплощений вакцина по изобретению вызывает усиленный иммунный ответ. Под усиленным иммунным ответом подразумевается увеличение интенсивности иммунного ответа, продолжительности иммунного ответа, широты ответа, выраженного, например, в спектре определяемых антител или Т-клеточных ответов, или улучшение на клиническом уровне в контексте заболеваемости, ослабления боли или симптомов.
В одном из воплощений вакцина по изобретению обеспечивает широкий спектр иммунного ответа, направленный против разных штаммов вирусов герпеса человека.
В одном из воплощений настоящее изобретение относится к способам предупреждения и/или лечения инфекции герпесвируса, уничтожения клеток организма-хозяина, инфицированных герпесвирусом, ингибирования вирусной репликации, увеличения секреции противовирусных и/или иммуномодулирующих лимфокинов или усиления продукции антител, специфичных к герпесвирусу. Указанные способы включают введение субъекту, нуждающемуся в этом, химерного белка, нуклеиновой кислоты или вакцинной композиции по изобретению. Введение осуществляют путем инъекции или через слизистую оболочку, или с помощью комбинации этих путей. Путь инъекции может быть, например, интраперитонеальным, внутрикожным, подкожным, внутрисосудистым или внутримышечным путем.
Эффективное количество вакцины, которое необходимо ввести субъекту, для лечения или профилактики инфекции или иного состояния, вызванного герпесвирусом, практикующий врач может определить исходя из степени тяжести заболевания или состояния и желаемого уровня продукции антител. Например, подходящая дозировка может находиться в диапазоне от приблизительно 1 мкг до приблизительно 1 мг для 70 кг пациента.
Могут использовать любой путь введения через слизистую оболочку, например, мочеполовой путь, такой как, например, влагалищный путь, желудочно-кишечный путь, аноректальный путь, респираторный путь, через слизистые оболочки верхних дыхательных путей или с помощью комбинации указанных путей. Вакцину можно вводить перорально, парентерально, сублингвально, трансдермально, внутривенно, внутриартериально, подкожно, внутримышечно или посредством комбинации указанных путей. Вакцину можно вводить с помощью генного пистолета (US 7638332, WO 0233108), электропорацией (US 2004167458, WO 2005025669, US 6697669, US 7328064, Hirao LA et al. Intradermal/subcutaneous immunization by electroporation improves plasmid vaccine delivery and potency in pigs and rhesus macaques. Vaccine. 2008 Jan 17; 26(3):440-8), с помощью микроконтейнеров из полиматериалов или липосомных носителей, с помощью бактериальных носителей и "теней" - неживых клеток грамотрицательных бактерий (Donnelly J.J., Ulmer J.В. DNA vaccines for viral diseases. 1999. Braz. J. Med. Biol. Res. 32, 215-222), и бактериофагов (WO 2006095345, Brown WL et al. RNA bacteriophage capsid-mediated drug delivery and epitope presentation. Intervirology. 2002; 45(4-6):371-80). Таким образом, может быть использован любой путь введения вакцины по изобретению, который обеспечивает желаемый результат.
Список литературы
1. Accardo A. et al. Self-assembled or mixed peptide amphiphile micelles from herpes simplex virus glycoproteins as potential immunomodulatory treatment // Int. J. Nanomedicine. 2014. Vol. 9, №1. P. 2137-2148.
2. Kim M. et al. Immunodominant epitopes in herpes simplex virus type 2 glycoprotein D are recognized by CD4 lymphocytes from both HSV-1 and HSV-2 seropositive subjects. // J. Immunol. 2008. Vol. 181, №9. P. 6604-6615.
3. Liu J. et al. A monoclonal antibody-based VZV glycoprotein E quantitative assay and its application on antigen quantitation in VZV vaccine // Appl. Microbiol. Biotechnol. 2015. Vol. 99, №11. P. 4845-4853.
4. Tanner J.E. et al. Peptides Designed To Spatially Depict the Epstein-Barr Virus Major Virion Glycoprotein gp350 Neutralization Epitope Elicit Antibodies That Block Virus-Neutralizing Antibody 72A1 Interaction with the Native gp350 Molecule // J. Virol. 2015. Vol. 89, №9. P. 4932-4941.
5. Lin X. et al. Chimerically fused antigen rich of overlapped epitopes from latent membrane protein 2 (LMP2) of Epstein-Barr virus as a potential vaccine and diagnostic agent // Cell Mol Immunol. Chinese Society of Immunology and The University of Science and Technology, 2015.
6. Ciferri С. et al. Structural and biochemical studies of HCMV gH/gL/gO and Pentamer reveal mutually exclusive cell entry complexes // Proc. Natl. Acad. Sci. U.S.A. 2015. Vol. 112, №6. P. 1767-1772.
7. Ciferri C. et al. Antigenic Characterization of the HCMV gH/gL/gO and Pentamer Cell Entry Complexes Reveals Binding Sites for Potently Neutralizing Human Antibodies // PLOS Pathog. 2015. Vol. 11, №10. P. e1005230.
8. Becerra A. et al. Immune response to HHV-6 and implications for immunotherapy // Curr. Opin. Virol. Elsevier B.V., 2014. Vol. 9. P. 154-161.
9. Franti M. et al. Immune Reactivity of Human Sera to the Glycoprotein В of Human Herpesvirus 7 // J. Clin. Microbiol. 2002. Vol. 40, №1. P. 44-51.
10. Skrincosky D. et al. Epitope mapping of human herpesvirus-7 gp65 using monoclonal antibodies // Arch. Virol. 2001. Vol. 146. P. 1705-1722.
11. Lepone L. et al. Monofunctional and polyfunctional CD8+ T cell responses to human herpesvirus 8 lytic and latency proteins. // Clin. Vaccine Immunol. 2010. Vol. 17, №10. P. 1507-1516.
12. Kloetzel P.M. Antigen processing by the proteasome. // Nat. Rev. Mol. Cell Biol. 2001. Vol. 2, №3. P. 179-187.
13. Calis J.J. a et al. Role of peptide processing predictions in T cell epitope identification: Contribution of different prediction programs // Immunogenetics. 2015. Vol. 67, №2. P. 85-93.
14. Van Hall T. et al. Differential Influence on Cytotoxic T Lymphocyte Epitope Presentation by Controlled Expression of Either Proteasome Immunosubunits or Pa28 // J. Exp. Med. 2000. Vol. 192, №4. P. 483-494.
ПРИМЕРЫ
Настоящее изобретение проиллюстрировано примерами. Следует понимать, что указанные примеры приведены в качестве в качестве иллюстрации настоящего изобретения и показывают предпочтительные варианты воплощения. На основании вышеприведенного описания и указанных примеров специалист в данной области может сделать различные изменения и модификации изобретения не выходя за его рамки. Подобные изменения и модификации также входят в объем прилагаемой формулы изобретения.
Дополнительной технической задачей при создании настоящего изобретения являлось создание синтетической последовательности ДНК, кодирующей химерный белок с последовательностью SEQ ID NO: 2 а также разработка эффективной технологии ее выделения и очистки, создание эффективного эукариотического экспрессионного вектора на основе pcDNA3.1, а также получение трансфецированных данными векторами клеток штамма Е. coli DH10B.
В данном аспекте указанный технический результат достигается за счет:
- создания синтетической последовательности ДНК, кодирующей химерный белок с последовательностью SEQ ID NO: 2, содержащей ген habg-1-8, с оптимизированным для синтеза в человеческих клетках кодонным составом и имеющей последовательность SEQ ID NO: 1;
- конструирования плазмидного экспрессионного вектора pDNA-habg-1-8, схема которого приведена на рис. 1, содержащего вышеуказанную последовательность ДНК и селективный маркер устойчивости к ампициллину;
- создания штамма клеток E. coli DH10B - продуцента плазмидной ДНК pDNA-habg-1-8;
- создания технологии получения плазмидной ДНК, включающей двустадийный способ очистки ДНК-конструкции из биомассы путем щелочного выделения и аффинной хроматографии для очистки от эндотоксинов клеточной стенки на полимиксин-Б-сефарозе.
Данная последовательность ДНК была синтезирована методом ПЦР с использованием перекрывающихся последовательностей олигонуклеотидов, предварительно синтезированных химическим путем с помощью синтезатора нуклеиновых кислот. Синтетическая ДНК, кодирующая химерный белок по изобретению, имеет последовательность SEQ ID NO: 1 и содержит ген habg-1-8, с оптимизированным для синтеза в человеческих клетках кодонным составом.
С использованием вектора pDNA-habg-1-8 был получен штамм клеток E. coli BL21 DE3 pDNA-habg-1-8 - продуцент плазмидной ДНК pDNA-habg-1-8. Штамм был получен методом трансформации. Идентификация родовой/видовой принадлежности осуществлялась по морфологическим признакам и микроскопией. Соответствие генотипу проверяли по ауксотрофным мутациям - штамм не сбраживает лактозу, арабинозу и галактозу, и не растет на средах, не содержащих лейцин.
Из биомассы штамма была выделена плазмидная ДНК-конструкция pDNA-habg-1-8, кодирующая химерный белок, с последовательностью SEQ ID NO: 1, представляет собой двуцепочечную кольцевую молекулу ДНК длиной 7751 п.н. со следующими физико-химическими свойствами:
- Молекулярный вес - 2396,16 кДа;
- Содержание GC-nap - 50,37%;
- Температура плавления - 85,46°C.
Пример 1. Дизайн нуклеотидной последовательности гена habg-1-8, кодирующего химерный белок по изобретению.
Была смоделирована белковая последовательность SEQ ID NO: 4, которая представляет собой полипептид, собранный из иммуногенных эпитопов разных вирусов герпеса человека специально для эффективной презентации антигенов иммунопротеасомой, на основе базы данных МНС-лигандов SYFPEITHI в программе EpiToolKit 2.0 (P.М. Kloetzel, Antigen Processing by the Proteasome. Nature Reviews. Molecular Cell Biology, 2 (2001), 179-87). Предполагается, что презентированные эпитопы могут распознаваться Т-лимфоцитами, то есть что экспрессирующийся в клетках человека белок с последовательностью SEQ ID NO: 4 вызовет активацию специализированных Т-клеточных клонов, а именно цитотоксических Т-лимфоцитов, в результате чего образуется эффективный иммунный ответ (A. Patronov and I. Doytchinova, 'T-Cell Epitope Vaccine Design by Immunoinformatics.', Open Biology, 3 (2013), 120139).
Затем последовательность аминокислотных остатков данного полипептида была переведена в нуклеотидную последовательность в программе Unipro UGENE с учетом кодоновой оптимизации для экспрессии в клетках человека. Были выбраны наиболее часто встречающиеся кодоны. Данная кодирующая последовательность, представленная в SEQ ID NO: 1, была синтезирована методом ПЦР с использованием перекрывающихся последовательностей олигонуклеотидов, предварительно синтезированных химическим путем с помощью синтезатора нуклеиновых кислот.
Пример 2. Получение плазмидной ДНК, кодирующей химерный белок по изобретению.
Искусственный ген habg-1-8 клонировали в экспрессионный вектор pDNA3.1 для последующей экспрессии в эукариотических клетках. Для этого провели реакцию рестрикции по сайтам XhoI и HindIII с последующим лигированием в вектор при +20°C в течение 2 часов. Применение рестриктаз HindIII и XhoI обусловлено тем, что они имеют по одному сайту рестрикции в плазмиде pcDNA3.1, а также могут работать максимально эффективно в одном буфере NEBuffer 2.1 (50 mM NaCl, 10 mM Tris-HCl, 10 mM MgCl2, 100 μg/ml BSA, pH 7.9, 25°C). Использование двух рестриктаз также гарантирует встройку гена интереса в правильном направлении. В результате был получен эукариотический экспрессионный вектор pDNA-habg-1-8, схема которого приведена на Фиг. 1, содержащий последовательность SEQ ID NO: 1 и селективный маркер устойчивости к ампициллину.
Пример 3. Конструирование прокариотического штамма для амплификации плазмидной ДНК pDNA-habg-1-8.
Данной плазмидной ДНК трансформировали клетки Е. coli штамма DH10B методом электропорации с использованием устройства Bio-Rad Pulser. После трансформации клетки инкубировали в SOC-среде (2% бактотриптон, 0.5% дрожжевой экстракт, 10 мМ NaCl, 2.5 мМ KCl, 10 мМ MgCl2, 10 мМ MgSO4, 20 мМ глюкоза) в течение 40 мин при +37°C.
Бактериальные колонии, содержащие вектор, отбираются по признаку устойчивости к антибиотику ампициллину на селективной питательной среде (LB-агар, 50 мг/мл антибиотика). Выросшие на такой среде колонии проверяли на наличие гена интереса habg-1-8.
Созданный штамм характеризуется следующими свойствами:
Культурально-морфологические особенности штамма ГИММ (генно-инженерно-модифицированного микроорганизма): грамотрицательные прямые палочки, размером 1,1-1,5×2,0-3,0 мкм, одиночные, спор и капсул не образуют; каталазоположительные, оксидазоотрицательные, факультативные анаэробы.
Клетки хорошо растут на простых питательных средах, содержащих и не содержащих ампициллин. На агаризованной среде - колонии гладкие, круглые, слабовыпуклые, с ровным краем. В жидких средах образуют равномерную светорассеивающую суспензию, при хранении без перемешивания оседают на дно. Клетки растут в интервале температур от 8°C до 43°C, интервал для культивирования - 28-38°C, оптимум роста при 37°C, интервал pH 5-7. Катализируют D-глюкозу и некоторые другие углеводы с образованием кислоты и газа, не сбраживают лактозу, арабинозу и галактозу. Реакция Фогес-Проскауэра отрицательная, не образуют H2S, но гидролизуют мочевину.
Продуктивность штамма - не менее 0,5 мг плазмидной ДНК на 1 г биомассы.
В запаянных ампулах, штамм лиофильно высушенный в среде, содержащей на 30 мл воды - 5 г сахарозы, 1,5 г желатина, хранится при комнатной температуре в течение 20 лет.
Культивирование при температуре 28-38°C в термостате или качалке, в агаризованной (2% агара) или жидкой LB-среде, соответственно. Селективные условия - добавление 100 мкг/мл ампициллина.
Ферментацию ведут в жидкой LB-среде с добавлением 100 мкг/мл ампициллина, при перемешивании и аэрировании, автоматическом титровании pH, при температуре 28-38°C.
Пример 4. Получение плазмидной ДНК.
Из выросших клонов выделяли плазмидную ДНК щелочным методом. Данный метод заключается в обработке суспензии бактериальных клеток раствором щелочи с детергентом, таким как додецилсульфат натрия, что приводит к денатурации молекул белков и нуклеиновых кислот. После чего проводят ренатурацию смеси раствором ацетата аммония высокой концентрации, вследствие чего плазмидная ДНК возвращается в нативную конформацию благодаря своим физико-химическим свойствам, тогда как белки и геномная ДНК остаются в виде осадка.
Раствор, содержащий целевую плазмидную ДНК, отделяют от осадка центрифугированием при высоких оборотах, после чего ДНК-конструкцию осаждают из супернатанта добавлением изопропилового спирта. Полученный осадок растворяют в физиологическом растворе и обрабатывают рибонуклеазой А для гидролиза молекул РНК. Целевую ДНК-конструкцию переосаждают из раствора после обработки РНКазой А с помощью смеси 96% этанола и 10М ацетата аммония в соотношении 3:1. Осадок, составляющий pDNA-habg-1-8, перерастворяют в физиологическом растворе.
Полученный таким образом раствор плазмидной ДНК затем очищают с помощью аффинной хроматографии с использованием полимиксин-Б-сефарозы от бактериальных эндотоксинов.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> ООО "РД-БИОТЕХ"
<120> ХИМЕРНЫЙ БЕЛОК, СИНТЕТИЧЕСКАЯ ДНК, КОДИРУЮЩАЯ УКАЗАННЫЙ БЕЛОК,
ЭКСПРЕССИОННЫЙ ВЕКТОР, ШТАММ-ПРОДУЦЕНТ СИНТЕТИЧЕСКОЙ ДНК И
СПОСОБ ПОЛУЧЕНИЯ ПЛАЗМИДНОЙ ДНК
<170> PatentIn версия 3.5
<210> 1
<211> 2379
<212> ДНК
<213> Искусственная последовательность
<221> ДНК
<222> (1)..(2379)
<223> Оптимизированный химерный ген
<400> 1
atgtgttgcc tctgtctgac tgtgtttctg gatggcggcg acgggaataa aacactgcgg 60
gacaacagct acatgcccct catagcgctg agtctccatg aaaatggcgc tgataataag 120
gtgtggatac gtcatcacgt aggcattgag aagccaaacc cttcagaagg ggaggcagcg 180
gataataagg tctggggctc agcaaagcct ggtaacggga gttacttcgc atccgttaaa 240
accgagatgc ttggcaatga gattgacgcc gataacgttc acttagtata cattctgagc 300
aagcagaatc agcaacatct gattccacag tgggccctgc gccagatcgc tgatttcgcc 360
gacaataagg tgtgggatcc aagtagatat aatatttcgt ttgaggcttt attaggaatc 420
tactctgcag acaatgttac atggttaagt agtataagcg taaagaggtc ggaggaagag 480
gagtacgtag cctatcataa ggacgaatat gttaacgctg ataacgtaac gtggagactt 540
gcggcgggca gtccctcaag cgccgataat gtgcacttaa cgaccaaccc atgggcaagt 600
cttccgggat cgctagggga tatcctgtac gccgacaatg ttacttggtc agcgctgctt 660
gaagatccgg tgggagcaga taacgttact tggtttaaga gcttgatata tatcaatgag 720
aacactaaaa tcctggaggt tgaggcagac aacgtaacct ggagtttaga gtcatatagt 780
gcctctaagg ccttctctgt accggagaat ggagcggata ataaagtctg gcaacaagac 840
gagcaacaac agcaagatga gcgggacggc aagacgttag cactaatcag cgcattttcg 900
ggtagcgcag acaatgtgac atggtccgct caggaggatc tgggtgatga taccggaata 960
cacgttatcg ccgatcataa caaagttacc gtttggagcc ttctttccat aatgacatta 1020
gcggccatgc attccaaact gagcccagca gacaacgtga cgtggatgct tatgataatc 1080
atagtaattg ctattgctga caacgtaacc tggtttcata tgtggaacta ccattcgcat 1140
gtcttctccg taggtgatgc ggacaacgtt acttggccgg tggtatcgac ccatgagcaa 1200
attgctgaca atgtcacctg gtttgcatta gatccctata atgaagcaga taacaaggtc 1260
tgggcgaagc gggctttgtg gactcccgat cagataaccg atattacgtc gttgcgtgat 1320
aataaaacat tggtagacga ggagtatcgc ttcataagtg acgcgacgtt tgtcgatgag 1380
acggcggata acaaagtgtg gtcatccatg aaagtaaacg tcaatggagt ggccgacaat 1440
aaggtttggg tttcaattga tgatgatacg ccgatgctaa gagatcatgt cactctagct 1500
gcgctgctcg tggtcgccgt tggactcaga gttgtgtgcg ccaagtatgc actggccgcc 1560
gacaatgtca cgtggacgac gtatgcgtgg cggtggtctg ctgataacaa ggtttgggga 1620
atttactaca tcagagtagt agaggtccgc caaatgcaat atgataacgc cgacaacaaa 1680
tgtctcagtt ctattgagtt tgcgaggcta gcagataatg tccacctagc aatgctagtt 1740
ttgttggcgg aaatagccga cgaaggaaac aaggtttggt gcattcaatc gattggcgcg 1800
tcggtggctg acaataaagt gtgggagcat ccgtggacgg aaaccacgat agaaccctgg 1860
cgtgatatcg acgcagataa taaggtatgg tgttgtcccg ataaaaacaa gtcggccgac 1920
aatgtgcact tatgtctcac atggcgtatt gaagaccctc cgtttaactc gcttctcttc 1980
gcattactag cggcagctgg tggactacaa ggtatttatg tccttgtcat gctggtctta 2040
ttaatagcgg ataatgtcac ctggtggcgg ttgggggcaa ttcctcctct agttgccgac 2100
aataaatgtc tacctgagtc ctctcaacgt cctcccttag ctgataatgt ccacttagag 2160
gtaaccgatc agatagctga tttcgcagat aacaaggtat ggacttatgg cccagttttc 2220
atgtgtttag gaggactcct tacgatggtt gcgggggcgg ataatgttca ccttgatgat 2280
cggacgacct tacagctagc ccagaatccg gtatacattc ccgagaccta cccctatatc 2340
aaatgggaca atagttcatg ggatttcatt accgtctga 2379
<210> 2
<211> 791
<212> Протеин
<213> Искусственная последовательность
<400> 2
Cys Cys Leu Cys Leu Thr Val Phe Leu Asp Gly Gly Asp Gly Asn Lys
1 5 10 15
Thr Leu Arg Asp Asn Ser Tyr Met Pro Leu Ile Ala Leu Ser Leu His
20 25 30
Glu Asn Gly Ala Asp Asn Lys Val Trp Ile Arg His His Val Gly Ile
35 40 45
Glu Lys Pro Asn Pro Ser Glu Gly Glu Ala Ala Asp Asn Lys Val Trp
50 55 60
Gly Ser Ala Lys Pro Gly Asn Gly Ser Tyr Phe Ala Ser Val Lys Thr
65 70 75 80
Glu Met Leu Gly Asn Glu Ile Asp Ala Asp Asn Val His Leu Val Tyr
85 90 95
Ile Leu Ser Lys Gln Asn Gln Gln His Leu Ile Pro Gln Trp Ala Leu
100 105 110
Arg Gln Ile Ala Asp Phe Ala Asp Asn Lys Val Trp Asp Pro Ser Arg
115 120 125
Tyr Asn Ile Ser Phe Glu Ala Leu Leu Gly Ile Tyr Ser Ala Asp Asn
130 135 140
Val Thr Trp Leu Ser Ser Ile Ser Val Lys Arg Ser Glu Glu Glu Glu
145 150 155 160
Tyr Val Ala Tyr His Lys Asp Glu Tyr Val Asn Ala Asp Asn Val Thr
165 170 175
Trp Arg Leu Ala Ala Gly Ser Pro Ser Ser Ala Asp Asn Val His Leu
180 185 190
Thr Thr Asn Pro Trp Ala Ser Leu Pro Gly Ser Leu Gly Asp Ile Leu
195 200 205
Tyr Ala Asp Asn Val Thr Trp Ser Ala Leu Leu Glu Asp Pro Val Gly
210 215 220
Ala Asp Asn Val Thr Trp Phe Lys Ser Leu Ile Tyr Ile Asn Glu Asn
225 230 235 240
Thr Lys Ile Leu Glu Val Glu Ala Asp Asn Val Thr Trp Ser Leu Glu
245 250 255
Ser Tyr Ser Ala Ser Lys Ala Phe Ser Val Pro Glu Asn Gly Ala Asp
260 265 270
Asn Lys Val Trp Gln Gln Asp Glu Gln Gln Gln Gln Asp Glu Arg Asp
275 280 285
Gly Lys Thr Leu Ala Leu Ile Ser Ala Phe Ser Gly Ser Ala Asp Asn
290 295 300
Val Thr Trp Ser Ala Gln Glu Asp Leu Gly Asp Asp Thr Gly Ile His
305 310 315 320
Val Ile Ala Asp His Asn Lys Val Thr Val Trp Ser Leu Leu Ser Ile
325 330 335
Met Thr Leu Ala Ala Met His Ser Lys Leu Ser Pro Ala Asp Asn Val
340 345 350
Thr Trp Met Leu Met Ile Ile Ile Val Ile Ala Ile Ala Asp Asn Val
355 360 365
Thr Trp Phe His Met Trp Asn Tyr His Ser His Val Phe Ser Val Gly
370 375 380
Asp Ala Asp Asn Val Thr Trp Pro Val Val Ser Thr His Glu Gln Ile
385 390 395 400
Ala Asp Asn Val Thr Trp Phe Ala Leu Asp Pro Tyr Asn Glu Ala Asp
405 410 415
Asn Lys Val Trp Ala Lys Arg Ala Leu Trp Thr Pro Asp Gln Ile Thr
420 425 430
Asp Ile Thr Ser Leu Arg Asp Asn Lys Thr Leu Val Asp Glu Glu Tyr
435 440 445
Arg Phe Ile Ser Asp Ala Thr Phe Val Asp Glu Thr Ala Asp Asn Lys
450 455 460
Val Trp Ser Ser Met Lys Val Asn Val Asn Gly Val Ala Asp Asn Lys
465 470 475 480
Val Trp Val Ser Ile Asp Asp Asp Thr Pro Met Leu Arg Asp His Val
485 490 495
Thr Leu Ala Ala Leu Leu Val Val Ala Val Gly Leu Arg Val Val Cys
500 505 510
Ala Lys Tyr Ala Leu Ala Ala Asp Asn Val Thr Trp Thr Thr Tyr Ala
515 520 525
Trp Arg Trp Ser Ala Asp Asn Lys Val Trp Gly Ile Tyr Tyr Ile Arg
530 535 540
Val Val Glu Val Arg Gln Met Gln Tyr Asp Asn Ala Asp Asn Lys Cys
545 550 555 560
Leu Ser Ser Ile Glu Phe Ala Arg Leu Ala Asp Asn Val His Leu Ala
565 570 575
Met Leu Val Leu Leu Ala Glu Ile Ala Asp Glu Gly Asn Lys Val Trp
580 585 590
Cys Ile Gln Ser Ile Gly Ala Ser Val Ala Asp Asn Lys Val Trp Glu
595 600 605
His Pro Trp Thr Glu Thr Thr Ile Glu Pro Trp Arg Asp Ile Asp Ala
610 615 620
Asp Asn Lys Val Trp Cys Cys Pro Asp Lys Asn Lys Ser Ala Asp Asn
625 630 635 640
Val His Leu Cys Leu Thr Trp Arg Ile Glu Asp Pro Pro Phe Asn Ser
645 650 655
Leu Leu Phe Ala Leu Leu Ala Ala Ala Gly Gly Leu Gln Gly Ile Tyr
660 665 670
Val Leu Val Met Leu Val Leu Leu Ile Ala Asp Asn Val Thr Trp Trp
675 680 685
Arg Leu Gly Ala Ile Pro Pro Leu Val Ala Asp Asn Lys Cys Leu Pro
690 695 700
Glu Ser Ser Gln Arg Pro Pro Leu Ala Asp Asn Val His Leu Glu Val
705 710 715 720
Thr Asp Gln Ile Ala Asp Phe Ala Asp Asn Lys Val Trp Thr Tyr Gly
725 730 735
Pro Val Phe Met Cys Leu Gly Gly Leu Leu Thr Met Val Ala Gly Ala
740 745 750
Asp Asn Val His Leu Asp Asp Arg Thr Thr Leu Gln Leu Ala Gln Asn
755 760 765
Pro Val Tyr Ile Pro Glu Thr Tyr Pro Tyr Ile Lys Trp Asp Asn Ser
770 775 780
Ser Trp Asp Phe Ile Thr Val
785 790
<210> 3
<211> 2379
<212> ДНК
<213> Искусственная последовательность
<221> ДНК
<222> (1)..(2323)
<223> Оптимизированный химерный ген
<400> 3
gatggcggcg acgggaataa aacactgcgg gacaacagct acatgcccct catagcgctg 60
agtctccatg aaaatggcgc tgataataag gtgtggatac gtcatcacgt aggcattgag 120
aagccaaacc cttcagaagg ggaggcagcg gataataagg tctggggctc agcaaagcct 180
ggtaacggga gttacttcgc atccgttaaa accgagatgc ttggcaatga gattgacgcc 240
gataacgttc acttagtata cattctgagc aagcagaatc agcaacatct gattccacag 300
tgggccctgc gccagatcgc tgatttcgcc gacaataagg tgtgggatcc aagtagatat 360
aatatttcgt ttgaggcttt attaggaatc tactctgcag acaatgttac atggttaagt 420
agtataagcg taaagaggtc ggaggaagag gagtacgtag cctatcataa ggacgaatat 480
gttaacgctg ataacgtaac gtggagactt gcggcgggca gtccctcaag cgccgataat 540
gtgcacttaa cgaccaaccc atgggcaagt cttccgggat cgctagggga tatcctgtac 600
gccgacaatg ttacttggtc agcgctgctt gaagatccgg tgggagcaga taacgttact 660
tggtttaaga gcttgatata tatcaatgag aacactaaaa tcctggaggt tgaggcagac 720
aacgtaacct ggagtttaga gtcatatagt gcctctaagg ccttctctgt accggagaat 780
ggagcggata ataaagtctg gcaacaagac gagcaacaac agcaagatga gcgggacggc 840
aagacgttag cactaatcag cgcattttcg ggtagcgcag acaatgtgac atggtccgct 900
caggaggatc tgggtgatga taccggaata cacgttatcg ccgatcataa caaagttacc 960
gtttggagcc ttctttccat aatgacatta gcggccatgc attccaaact gagcccagca 1020
gacaacgtga cgtggatgct tatgataatc atagtaattg ctattgctga caacgtaacc 1080
tggtttcata tgtggaacta ccattcgcat gtcttctccg taggtgatgc ggacaacgtt 1140
acttggccgg tggtatcgac ccatgagcaa attgctgaca atgtcacctg gtttgcatta 1200
gatccctata atgaagcaga taacaaggtc tgggcgaagc gggctttgtg gactcccgat 1260
cagataaccg atattacgtc gttgcgtgat aataaaacat tggtagacga ggagtatcgc 1320
ttcataagtg acgcgacgtt tgtcgatgag acggcggata acaaagtgtg gtcatccatg 1380
aaagtaaacg tcaatggagt ggccgacaat aaggtttggg tttcaattga tgatgatacg 1440
ccgatgctaa gagatcatgt cactctagct gcgctgctcg tggtcgccgt tggactcaga 1500
gttgtgtgcg ccaagtatgc actggccgcc gacaatgtca cgtggacgac gtatgcgtgg 1560
cggtggtctg ctgataacaa ggtttgggga atttactaca tcagagtagt agaggtccgc 1620
caaatgcaat atgataacgc cgacaacaaa tgtctcagtt ctattgagtt tgcgaggcta 1680
gcagataatg tccacctagc aatgctagtt ttgttggcgg aaatagccga cgaaggaaac 1740
aaggtttggt gcattcaatc gattggcgcg tcggtggctg acaataaagt gtgggagcat 1800
ccgtggacgg aaaccacgat agaaccctgg cgtgatatcg acgcagataa taaggtatgg 1860
tgttgtcccg ataaaaacaa gtcggccgac aatgtgcact tatgtctcac atggcgtatt 1920
gaagaccctc cgtttaactc gcttctcttc gcattactag cggcagctgg tggactacaa 1980
ggtatttatg tccttgtcat gctggtctta ttaatagcgg ataatgtcac ctggtggcgg 2040
ttgggggcaa ttcctcctct agttgccgac aataaatgtc tacctgagtc ctctcaacgt 2100
cctcccttag ctgataatgt ccacttagag gtaaccgatc agatagctga tttcgcagat 2160
aacaaggtat ggacttatgg cccagttttc atgtgtttag gaggactcct tacgatggtt 2220
gcgggggcgg ataatgttca ccttgatgat cggacgacct tacagctagc ccagaatccg 2280
gtatacattc ccgagaccta cccctatatc aaatgggaca ata 2323
<210> 4
<211> 794
<212> Протеин
<213> Искусственная последовательность
<400> 4
Asp Gly Gly Asp Gly Asn Lys Thr Leu Arg Asp Asn Ser Tyr Met Pro
1 5 10 15
Leu Ile Ala Leu Ser Leu His Glu Asn Gly Ala Asp Asn Lys Val Trp
20 25 30
Ile Arg His His Val Gly Ile Glu Lys Pro Asn Pro Ser Glu Gly Glu
35 40 45
Ala Ala Asp Asn Lys Val Trp Gly Ser Ala Lys Pro Gly Asn Gly Ser
50 55 60
Tyr Phe Ala Ser Val Lys Thr Glu Met Leu Gly Asn Glu Ile Asp Ala
65 70 75 80
Asp Asn Val His Leu Val Tyr Ile Leu Ser Lys Gln Asn Gln Gln His
85 90 95
Leu Ile Pro Gln Trp Ala Leu Arg Gln Ile Ala Asp Phe Ala Asp Asn
100 105 110
Lys Val Trp Asp Pro Ser Arg Tyr Asn Ile Ser Phe Glu Ala Leu Leu
115 120 125
Gly Ile Tyr Ser Ala Asp Asn Val Thr Trp Leu Ser Ser Ile Ser Val
130 135 140
Lys Arg Ser Glu Glu Glu Glu Tyr Val Ala Tyr His Lys Asp Glu Tyr
145 150 155 160
Val Asn Ala Asp Asn Val Thr Trp Arg Leu Ala Ala Gly Ser Pro Ser
165 170 175
Ser Ala Asp Asn Val His Leu Thr Thr Asn Pro Trp Ala Ser Leu Pro
180 185 190
Gly Ser Leu Gly Asp Ile Leu Tyr Ala Asp Asn Val Thr Trp Ser Ala
195 200 205
Leu Leu Glu Asp Pro Val Gly Ala Asp Asn Val Thr Trp Phe Lys Ser
210 215 220
Leu Ile Tyr Ile Asn Glu Asn Thr Lys Ile Leu Glu Val Glu Ala Asp
225 230 235 240
Asn Val Thr Trp Ser Leu Glu Ser Tyr Ser Ala Ser Lys Ala Phe Ser
245 250 255
Val Pro Glu Asn Gly Ala Asp Asn Lys Val Trp Gln Gln Asp Glu Gln
260 265 270
Gln Gln Gln Asp Glu Arg Asp Gly Lys Thr Leu Ala Leu Ile Ser Ala
275 280 285
Phe Ser Gly Ser Ala Asp Asn Val Thr Trp Ser Ala Gln Glu Asp Leu
290 295 300
Gly Asp Asp Thr Gly Ile His Val Ile Ala Asp His Asn Lys Val Thr
305 310 315 320
Val Trp Ser Leu Leu Ser Ile Met Thr Leu Ala Ala Met His Ser Lys
325 330 335
Leu Ser Pro Ala Asp Asn Val Thr Trp Met Leu Met Ile Ile Ile Val
340 345 350
Ile Ala Ile Ala Asp Asn Val Thr Trp Phe His Met Trp Asn Tyr His
355 360 365
Ser His Val Phe Ser Val Gly Asp Ala Asp Asn Val Thr Trp Pro Val
370 375 380
Val Ser Thr His Glu Gln Ile Ala Asp Asn Val Thr Trp Phe Ala Leu
385 390 395 400
Asp Pro Tyr Asn Glu Ala Asp Asn Lys Val Trp Ala Lys Arg Ala Leu
405 410 415
Trp Thr Pro Asp Gln Ile Thr Asp Ile Thr Ser Leu Arg Asp Asn Lys
420 425 430
Thr Leu Val Asp Glu Glu Tyr Arg Phe Ile Ser Asp Ala Thr Phe Val
435 440 445
Asp Glu Thr Ala Asp Asn Lys Val Trp Ser Ser Met Lys Val Asn Val
450 455 460
Asn Gly Val Ala Asp Asn Lys Val Trp Val Ser Ile Asp Asp Asp Thr
465 470 475 480
Pro Met Leu Arg Asp His Val Thr Leu Ala Ala Leu Leu Val Val Ala
485 490 495
Val Gly Leu Arg Val Val Cys Ala Lys Tyr Ala Leu Ala Ala Asp Asn
500 505 510
Val Thr Trp Thr Thr Tyr Ala Trp Arg Trp Ser Ala Asp Asn Lys Val
515 520 525
Trp Gly Ile Tyr Tyr Ile Arg Val Val Glu Val Arg Gln Met Gln Tyr
530 535 540
Asp Asn Ala Asp Asn Lys Cys Leu Ser Ser Ile Glu Phe Ala Arg Leu
545 550 555 560
Ala Asp Asn Val His Leu Ala Met Leu Val Leu Leu Ala Glu Ile Ala
565 570 575
Asp Glu Gly Asn Lys Val Trp Cys Ile Gln Ser Ile Gly Ala Ser Val
580 585 590
Ala Asp Asn Lys Val Trp Glu His Pro Trp Thr Glu Thr Thr Ile Glu
595 600 605
Pro Trp Arg Asp Ile Asp Ala Asp Asn Lys Val Trp Cys Cys Pro Asp
610 615 620
Lys Asn Lys Ser Ala Asp Asn Val His Leu Cys Leu Thr Trp Arg Ile
625 630 635 640
Glu Asp Pro Pro Phe Asn Ser Leu Leu Phe Ala Leu Leu Ala Ala Ala
645 650 655
Gly Gly Leu Gln Gly Ile Tyr Val Leu Val Met Leu Val Leu Leu Ile
660 665 670
Ala Asp Asn Val Thr Trp Trp Arg Leu Gly Ala Ile Pro Pro Leu Val
675 680 685
Ala Asp Asn Lys Cys Leu Pro Glu Ser Ser Gln Arg Pro Pro Leu Ala
690 695 700
Asp Asn Val His Leu Glu Val Thr Asp Gln Ile Ala Asp Phe Ala Asp
705 710 715 720
Asn Lys Val Trp Thr Tyr Gly Pro Val Phe Met Cys Leu Gly Gly Leu
725 730 735
Leu Thr Met Val Ala Gly Ala Asp Asn Val His Leu Asp Asp Arg Thr
740 745 750
Thr Leu Gln Leu Ala Gln Asn Pro Val Tyr Ile Pro Glu Thr Tyr Pro
755 760 765
Tyr Ile Lys Trp Asp Asn
770
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ХИМЕРНЫЙ БЕЛОК L1 ПАПИЛЛОМАВИРУСА | 2020 |
|
RU2808002C2 |
| ХИМЕРНЫЙ БЕЛОК | 2016 |
|
RU2746755C2 |
| БЕЛОК, СВЯЗЫВАЮЩИЙ АНТИГЕН ST2 | 2021 |
|
RU2841164C2 |
| СВЯЗЫВАЮЩИЙ RGMa БЕЛОК И ЕГО ИСПОЛЬЗОВАНИЕ | 2016 |
|
RU2809500C2 |
| ГЕРПЕСВИРУС С ИЗМЕНЕННЫМ СПЕКТРОМ МИШЕНЕЙ, СОДЕРЖАЩИЙ ГИБРИДНЫЙ ГЛИКОПРОТЕИН Н | 2016 |
|
RU2732120C2 |
| СЛИТЫЙ БЕЛОК | 2016 |
|
RU2748643C2 |
| БИСПЕЦИФИЧЕСКИЙ БЕЛОК | 2019 |
|
RU2784486C1 |
| МОДУЛЯЦИЯ АКТИВНОСТИ REP БЕЛКА ПРИ ПОЛУЧЕНИИ ДНК С ЗАМКНУТЫМИ КОНЦАМИ (ЗКДНК) | 2020 |
|
RU2812850C2 |
| СЛИТЫЙ БЕЛОК ИЗ БЕЛКА DCTN1 С БЕЛКОМ RET | 2018 |
|
RU2813996C2 |
| БЕЛОК И ВАКЦИНА ПРОТИВ ИНФЕКЦИИ SARS-CoV-2 | 2020 |
|
RU2815060C1 |

Изобретение относится к области биотехнологии. Описана группа изобретений, включающая химерный белок для индуцирования и/или облегчения индукции иммунного ответа в результате инфекции герпесвируса, синтетическую нуклеиновую кислоту, представляющую собой ДНК, вектор, содержащий вышеуказанную ДНК, клетку-хозяин для продуцирования химерного белка, способ получения вышеуказанного вектора, вакцину для индуцирования иммунного ответа против инфекции герпесвируса, содержащую вышеуказанный химерный белок, и вакцину для индуцирования иммунного ответа против инфекции герпесвируса, содержащую вышеуказанную ДНК. В одном из вариантов реализации химерный белок содержит последовательность, которая гомологична по меньшей мере на 70% последовательности SEQ ID NO: 4. Изобретение расширяет арсенал средств для индуцирования иммунного ответа против инфекции герпесвируса 7 н. и 17 з.п. ф-лы, 2 ил., 1 табл., 4 пр.
1. Химерный белок для индуцирования и/или облегчения индукции иммунного ответа в результате инфекции герпесвируса, имеющий последовательность, которая гомологична по меньшей мере на 70% последовательности SEQ ID NO: 4.
2. Химерный белок по п. 1, имеющий последовательность, которая гомологична последовательности SEQ ID NO: 4 по меньшей мере на предпочтительно 71%, предпочтительно 72%, предпочтительно 73%, предпочтительно 74%, предпочтительно 75%, предпочтительно 76%, предпочтительно 77%, предпочтительно 78%, предпочтительно 79%, предпочтительно 80%, предпочтительно 81%, предпочтительно 82%, предпочтительно 83%, предпочтительно 84%, предпочтительно 85%, предпочтительно 86%, предпочтительно 87%, предпочтительно 88%, предпочтительно 89%, предпочтительно 90%, предпочтительно 91%, предпочтительно 92%, предпочтительно 93%, предпочтительно 94%, предпочтительно 95%, предпочтительно 96%, предпочтительно 97%, предпочтительно 98%, предпочтительно 99%.
3. Химерный белок по п. 1, имеющий последовательность SEQ ID NO: 2 или гомологичную ей по меньшей мере на 70%, предпочтительно 71%, предпочтительно 72%, предпочтительно 73%, предпочтительно 74%, предпочтительно 75%, предпочтительно 76%, предпочтительно 77%, предпочтительно 78%, предпочтительно 79%, предпочтительно 80%, предпочтительно 81%, предпочтительно 82%, предпочтительно 83%, предпочтительно 84%, предпочтительно 85%, предпочтительно 86%, предпочтительно 87%, предпочтительно 88%, предпочтительно 89%, предпочтительно 90%, предпочтительно 91%, предпочтительно 92%, предпочтительно 93%, предпочтительно 94%, предпочтительно 95%, предпочтительно 96%, предпочтительно 97%, предпочтительно 98%, предпочтительно 99%.
4. Синтетическая нуклеиновая кислота, которая представляет собой ДНК, кодирующая химерный белок по любому из пп. 1-3.
5. Нуклеиновая кислота по п. 4, имеющая последовательность, идентичную SEQ ID NO: 3 по меньшей мере на 70%, предпочтительно 71%, предпочтительно 72%, предпочтительно 73%, предпочтительно 74%, предпочтительно 75%, предпочтительно 76%, предпочтительно 77%, предпочтительно 78%, предпочтительно 79%, предпочтительно 80%, предпочтительно 81%, предпочтительно 82%, предпочтительно 83%, предпочтительно 84%, предпочтительно 85%, предпочтительно 86%, предпочтительно 87%, предпочтительно 88%, предпочтительно 89%, предпочтительно 90%, предпочтительно 91%, предпочтительно 92%, предпочтительно 93%, предпочтительно 94%, предпочтительно 95%, предпочтительно 96%, предпочтительно 97%, предпочтительно 98%, предпочтительно 99%.
6. Нуклеиновая кислота по п. 4, имеющая последовательность SEQ ID NO: 1 или гомологичную ей по меньшей мере на 70%, предпочтительно 71%, предпочтительно 72%, предпочтительно 73%, предпочтительно 74%, предпочтительно 75%, предпочтительно 76%, предпочтительно 77%, предпочтительно 78%, предпочтительно 79%, предпочтительно 80%, предпочтительно 81%, предпочтительно 82%, предпочтительно 83%, предпочтительно 84%, предпочтительно 85%, предпочтительно 86%, предпочтительно 87%, предпочтительно 88%, предпочтительно 89%, предпочтительно 90%, предпочтительно 91%, предпочтительно 92%, предпочтительно 93%, предпочтительно 94%, предпочтительно 95%, предпочтительно 96%, предпочтительно 97%, предпочтительно 98%, предпочтительно 99%.
7. Вектор, содержащий ДНК по п. 4 или 5, для экспрессии указанной ДНК в клетке-хозяине.
8. Вектор по п. 7, который представляет собой плазмиду.
9. Вектор по п. 7, который предназначен для экспрессии указанной ДНК в бактериальной клетке-хозяине.
10. Клетка-хозяин, содержащая вектор по п. 7, для продуцировация химерного белка по п. 1.
11. Клетка по п. 10, которая представляет собой эукариотическую или прокариотическую клетку.
12. Клетка по п. 11, где эукариотическая клетка выбрана из клетки дрожжей, растительной клетки или клетки животного.
13. Клетка по п. 10, которая представляет собой бактериальную клетку.
14. Клетка по п. 13, где бактериальная клетка представляет собой Escherichia coli.
15. Клетка по п. 14, где Escherichia coli выбрана из штамма E. coli DH10B.
16. Способ получения вектора по п. 7, включающий культивирование клетки-хозяина по п. 10, выделение целевого продукта, представляющего собой вектор по п. 7, из биомассы указанных клеток и последующую очистку целевого продукта.
17. Способ по п. 16, где целевой продукт выделяют из биомассы штамма клеток E. coli DH10B.
18. Способ по п. 16 или 17, где целевой продукт выделяют щелочным методом.
19. Способ по п. 16, где очистку осуществляют методом аффинной хроматографии.
20. Способ по п. 19, где метод аффинной хроматографии проводят на полимиксин-Б-сефарозе.
21. Вакцина для индуцирования иммунного ответа против инфекции герпесвируса, содержащая эффективное количество ДНК по п. 4 и фармацевтически приемлемое вспомогательное вещество.
22. Вакцина по п. 21, где фармацевтически приемлемое вспомогательное вещество выбрано из группы, состоящей из функциональной молекулы, среды-носителя, адъюванта, переносчика или разбавителя, поверхностно-активных веществ, иммуностимулирующих комплексов, неполного адъюванта Фрейнда, ионов кальция, вирусных белков, полианионов, поликатионов, наночастиц или везикул, сквалена, гиалуроновой кислоты или липидов.
23. Вакцина для индуцирования иммунного ответа против инфекции герпесвируса, содержащая эффективное количество химерного белка по п. 1 и фармацевтически приемлемое вспомогательное вещество.
24. Вакцина по п. 23, где фармацевтически приемлемое вспомогательное вещество выбрано из группы, состоящей из функциональной молекулы, среды-носителя, адъюванта, переносчика или разбавителя, поверхностно-активных веществ, иммуностимулирующих комплексов, неполного адъюванта Фрейнда, ионов кальция, вирусных белков, полианионов, поликатионов, наночастиц или везикул, сквалена, гиалуроновой кислоты или липидов.
| EA 201391109 A1, 31.03.2014 | |||
| RU 2014131474 A1, 20.02.2016 | |||
| US 20150190502 A1, 09.07.2015 | |||
| СПОСОБ ЛЕЧЕНИЯ ИНФЕКЦИЙ, ВЫЗВАННЫХ ВИРУСОМ ПРОСТОГО ГЕРПЕСА ПЕРВОГО И ВТОРОГО ТИПОВ, ЦИТОМЕГАЛОВИРУСОМ, ВИРУСОМ ЭПШТЕЙНА-БАРР | 2008 |
|
RU2391981C2 |
Авторы
Даты
2020-11-17—Публикация
2016-11-18—Подача