ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Данное изобретение относится к кобальтовой смеси, которая является новым источником кобальта для домашних жвачных животных. Используя преимущества смеси солей кобальта, представляющей собой комбинацию быстрого высвобождения кобальта и медленного высвобождения кобальта в рубце жвачных животных, кобальт становиться доступным для усвоения бактериями рубца жвачных животных в течение стабильного периода времени для продуцирования бактериями витамина В12, необходимого для здоровья животных и продуцирования молока в период лактации.
УРОВЕНЬ ТЕХНИКИ
Витамин B12 уникален среди витаминов тем, что содержит не только органическую молекулу, но и незаменимый микроэлемент кобальт. Витамин В12 не вырабатывается ни растениями, ни животными и может синтезироваться только некоторыми видами микроорганизмов. Бактерии в кишечнике человека могут вырабатывать достаточное количество витамина B12 для нормальных суточных потребностей в неорганических солях кобальта в рационе. Витамин В12 также вырабатывается в больших количествах обогащенными популяциями бактерий в рубце жвачных животных и в слепой кишке других травоядных видов.
Витамин В12 участвует во многих биохимических процессах, необходимых для жизни. Он действует как кофермент для некоторых ферментов, которые катализируют перенос атома водорода от одного атома углерода к соседнему атому в обмен на алкильную, карбоксильную, гидроксильную или аминогруппу. Дефицит витамина В12 приводит к развитию тяжелого заболевания пернициозной анемии. Пернициозная анемия, как следует из названия, включает снижение концентрации гемоглобина, возникающее в результате состояние, а последствия также включают серьезные нарушения центральной нервной системы, которые могут привести к аномальным ощущениям, движениям и мышлению у людей.
Известно, что витамин B12 оказывает положительное влияние на молочную продуктивность дойных коров, смотрите, например, Journal of Dairy Science, 2005 February; 88(2): 671-6, Girard et al., показывающий, что в ранний период лактации запас витамина B12, если он недостаточен, ограничивает молочную продуктивность коров. Поскольку кобальт необходим для питания животных в качестве важнейшего компонента для продуцирования витамина B12, таким образом, из этого следует, что жвачным животным требуется достаточный запас кобальта в рационе для эффективного питания животных и эффективной молочной продуктивности. У жвачных животных растворимая часть рубцового материала (твердых веществ и жидкостей) возобновляется быстрее, чем твердые вещества. Это означает, что высокорастворимые источники кобальта будут оставаться в рубце меньше времени, чем нерастворимые формы. Данное изобретение относится к способности бактерий жвачных животных продуцировать витамин B12. О необходимости увеличения продуцирования B12 можно судить по увеличению продуктивности при введении B12, смотрите ранее приведенную статью Journal Dairy Science.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Способ и композиция, которая является уникальным источником кобальта для увеличения продуцирования витамина В12 в рубце. Она обладает преимуществом источника медленного высвобождения кобальта в комбинации с источником быстрого высвобождения кобальта. Источник быстрого высвобождения ионов кобальта, который представляет собой растворимый источник кобальта, быстрее возобновляется в рубце, чем возобновляются твердые источники кобальта. Таким образом, более медленное высвобождение в частности более длинные полимерные цепи лигандов кобальта усваиваются в течение более длительного периода времени, обеспечивая более медленное высвобождение кобальта. При таком подходе часть кобальтовой смеси растворима, а другая часть практически нерастворима; нерастворимая часть останется в рубце дольше. Когда бактерии потребляют, например, полисахарид кобальта, они высвобождают кобальт для продуцирования B12. Альтернативно, неразлагаемые в рубце полимеры, такие как полиакриловая кислота, просто медленно высвобождают кобальт. Неожиданно, что такое регулирование или медленное высвобождение кобальта бактериями рубца в комбинации с более быстрым высвобождением, таким как растворимая соль источника кобальта, например мономерного сахара, как показывают данные, обладает способностью более высокого продуцирования B12, чем полностью растворимый источник кобальта или полностью нерастворимый источник.
КРАТКОЕ ОПИСАНИЕ ФИГУР
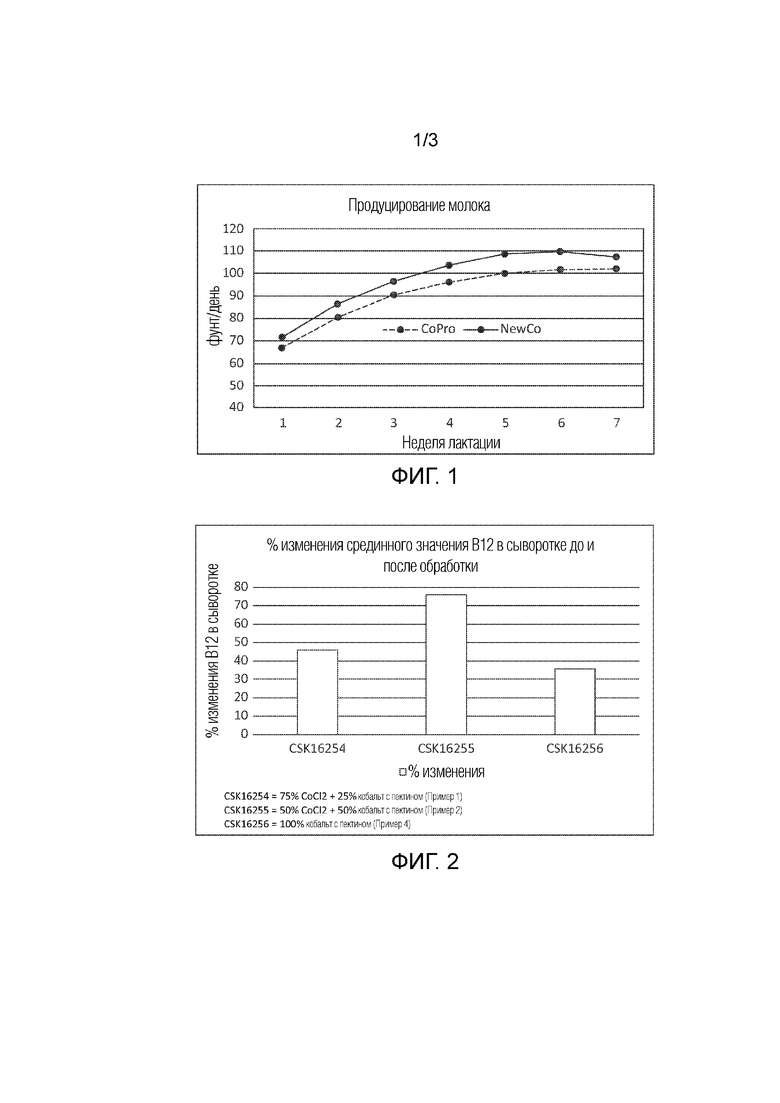
На фиг. 1 представлен график сравнения продуцирования молока, где единственным отличием в корме для животных является источник кобальта.
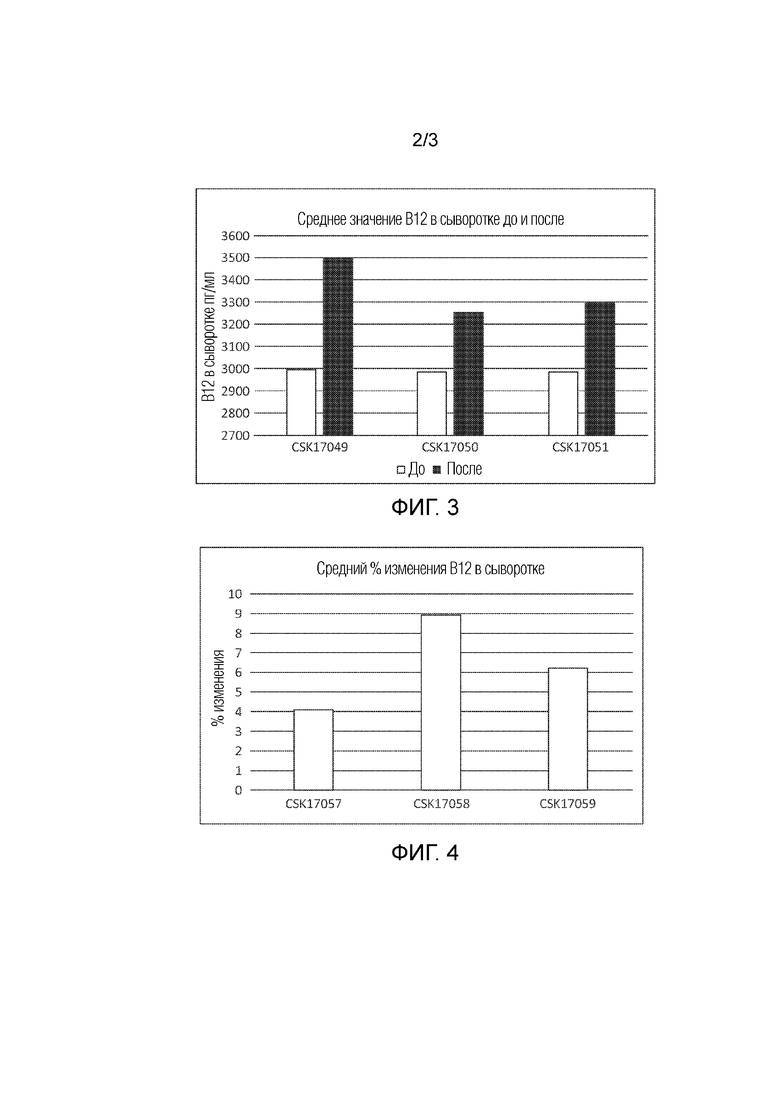
На фиг. 2 представлен анализ статус В12 в сыворотке овец после использования изобретения для препаратов из примеров 1, 2 и 4.
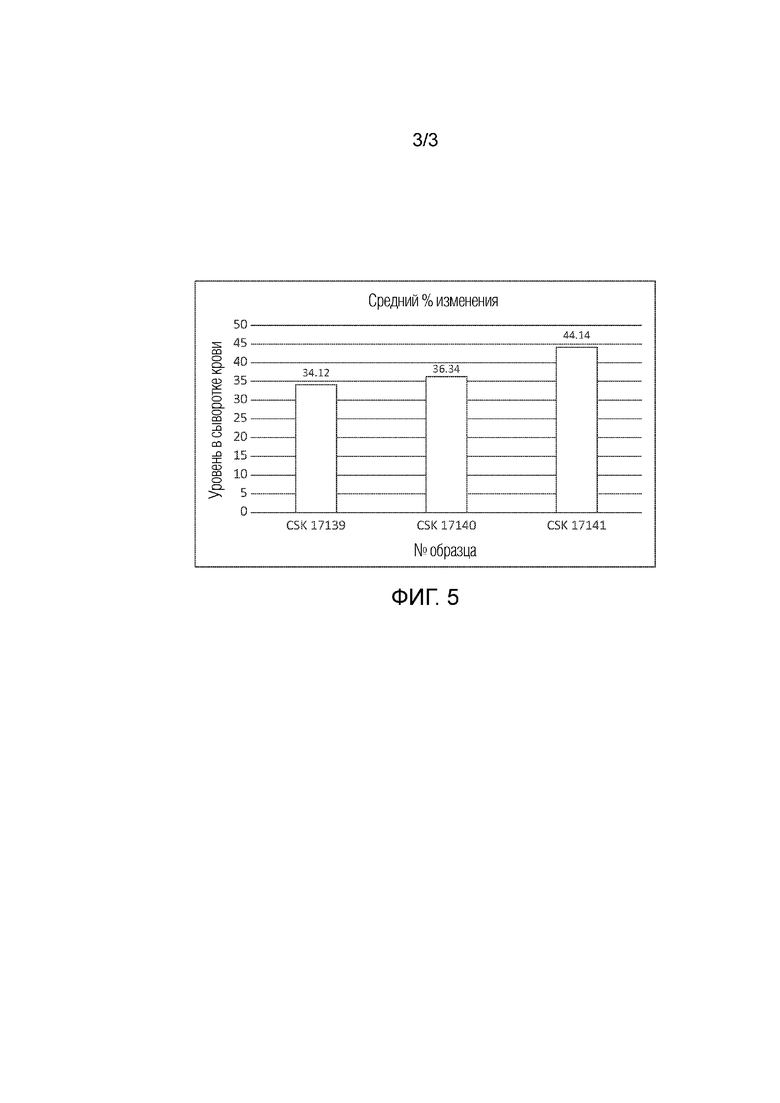
На фиг. 3 показаны уровни B12 в сыворотке до и после обработки для препаратов из примеров 4 и 8.
На фиг. 4 показаны уровни B12 в сыворотке до и после обработки для композиций из примеров 13, 2 и 15.
На фиг. 5 показан B12 в сыворотке крови до и после обработки для композиций из примеров 7, 9 и 10.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение охватывает смесь источника быстрого высвобождения кобальта и источника медленного высвобождения кобальта, которая при скармливании жвачным животным позволяет бактериям рубца сразу использовать некоторое количество ионов кобальта (с быстрым высвобождением) для продуцирования витамина В12 при наличии остатка дополнительных ионов кобальта с медленным высвобождением, поскольку он более медленно метаболизируется микроорганизмами рубца. Исследования неожиданно продемонстрировали, что такая комбинация источников с быстрым и медленным высвобождением кобальта приводит к более рациональному и эффективному продуцированию витамина B12, чем любой из этих источников в отдельности. Не желая быть связанными какой-либо теорией, считается, что это происходит потому, что ионы с быстрым высвобождением проходят через рубец быстрее, чем бактерии могут их метаболизировать для получения витамина В12, поэтому большая часть их «теряется». В противоположность источник медленного высвобождения кобальта осуществляет, по мере того, как микроорганизмы рубца постепенно метаболизируют более крупные молекулы в большей степени нерастворимых полимеров, высвобождение кобальта с получением витамина В12. В случае только медленного высвобождения время «теряется» при ограниченном количестве кобальта, доступного для получения меньшего количества В12.
Источники быстрого высвобождения кобальта включают растворимые неорганические и органические источники кобальта, такие как хлорид кобальта, сульфат кобальта, ацетат кобальта и другие комплексы быстрого высвобождения (растворимого) кобальта с мономерным сахаром, такие как, например, глюкогептонат кобальта или глюконат кобальта, как показано в предыдущем патенте США 4678854 от 7 июля 1987, раскрытие которого включено здесь посредством ссылки.
Источники медленного высвобождения кобальта включают нерастворимые и частично растворимые полимерные лиганды кобальта, такие как лиганды альгиновая кислота, пектин, полиакрил и карбоксиметилцеллюлоза комплексов с кобальтом, а также другие включающие кобальт полимерные комплексы с боковыми группами карбоновой кислоты, причем все они являются в значительной степени нерастворимыми.
Источник быстрого высвобождения кобальта позволяет кобальту сразу стать доступным для бактерий из жидкости в рубце, хотя большая часть его проходит так быстро, что он не может быть использован полностью. Источник медленного высвобождения кобальта остается в рубце и проходит через него, только после того как микроорганизмы метаболизируют полимер, или соль медленно высвобождает кобальт, что приводит к постепенно доступному источнику кобальта для получения витамина В12 или постепенному высвобождению кобальта из нерастворимой формы.
Ключевым моментом является наличие некоторого количества растворимого кобальта, связанного с полимером, и некоторой части его, являющейся нерастворимой. Это создает условия, при которых растворимая фракция может сразу начать использоваться бактериями. По мере того как жидкость возобновляется в рубце, кобальт, доступный бактериям во всех растворимых веществах (неорганических или низкомолекулярных лигандах), будет удаляться из рубца. К этому времени бактерии будут разлагать полимер из связанного с полимером кобальта, высвобождая эту фракцию кобальта в рубцовую жидкость. По существу, эта «нерастворимая» фракция является источником регулируемого высвобождения кобальта. Неожиданно, но лучше всего иметь в наличие оба вида кобальта для оптимизации продуцирования витамина В12. Нерастворимая часть, связанная с полимером, может быть получена из любого кислотосодержащего полимера. Основными примерами являются пектин и альгиновая кислота.
Согласно данному изобретению, предложен способ регулирования высвобождения кобальта в рубце бактериями рубца для превращения в витамин B12, включающий:
скармливание жвачным животным смешанного источника кобальта:
источника быстрого высвобождения кобальта и источника медленного высвобождения кобальта;
в котором источник быстрого высвобождения кобальта выбирают из группы, состоящей из растворимых неорганических или органических источников ионов кобальта и комплексов растворимого кобальта с мономерным сахаром;
в котором источник медленного высвобождения кобальта представляет собой полимерный комплекс с боковыми группами карбоновых кислот, выбранными из альгиновой кислоты, альгината кобальта, пектина, полиакриловой кислоты и карбоксиметилцеллюлозы; и
указанный источник быстрого высвобождения кобальта составляет от около 25 вес.% до около 75 вес.% общего источника кобальта, а остальная часть общего источника кобальта является источником медленного высвобождения кобальта.
В некоторых вариантах изобретения предложен способ, в котором смешанный источник кобальта содержит около 50 вес.% источника быстрого высвобождения кобальта и около 50 вес.% источника медленного высвобождения кобальта. Источником медленного высвобождения кобальта может быть кобальт с пектином. Источник кобальта может быть выбран из кобальта с альгиновой кислотой или альгината кобальта.
В некоторых вариантах изобретения предложена композиция смешанного источника кобальта для скармливания жвачным животным с целью регулирования скорости высвобождения кобальта в рубце для превращения бактериями рубца в витамин B12, содержащая:
источник быстрого высвобождения кобальта и источник медленного высвобождения кобальта;
в котором источник быстрого высвобождения кобальта выбирают из группы, состоящей из растворимых неорганических или органических источников ионов кобальта и комплексов растворимого кобальта с мономерным сахаром;
в котором источник медленного высвобождения кобальта представляет собой полимерный комплекс с боковыми группами карбоновых кислот, выбранными из альгиновой кислоты, альгината кобальта, пектина, полиакриловой кислоты и карбоксиметилцеллюлозы; и
указанный источник быстрого высвобождения кобальта составляет от около 25 вес.% до около 75 вес.% общего источника кобальта, а остальная часть общего источника кобальта является источником медленного высвобождения кобальта. Композиция может содержать смешанный источник кобальта в количестве около 50 вес.% источника быстрого высвобождения кобальта и около 50 вес.% источника медленного высвобождения кобальта. В предложенной композиции источником медленного высвобождения кобальта может являться кобальт с пектином. Источником кобальта может являться кобальт с альгиновой кислотой.
Приведенные ниже примеры предлагаются в качестве иллюстрации вариантов осуществления изобретения с пониманием того, что они не являются ограничивающими, поскольку также могут быть приведены другие примеры. Однако считается, что они представляют изобретение и данные, полученные при использовании изобретения.
ПРИМЕР 1
Кобальт с пектином - 2 экв. кобальта, 10 экв. NaOH, 12 часов при 20°C
В 750 мл деионизированной воды добавляют гидроксид натрия (59,92 г, 1,49 моль). В этот щелочной раствор медленно добавляют пектин (30,01 г, 0,169 моль субъединиц карбоновой кислоты) для тонкого диспергирования на поверхности раствора. Тонкая дисперсия быстро превращается в темно-оранжевую суспензию, которую перемешивают в течение 12 часов при 20°C. Значение рН доводят до 8,8 с использованием кислоты 12 М HCl, на этом этапе в реакцию добавляют одной порцией твердое вещество CoCl2·6H2O (80,42 г, 0,338 моль). Полученную розовую суспензию перемешивают в течение еще 1 часа и затем сушат при 88°C в течение 12 часов. Конечный синий порошок гомогенизируют и анализируют на содержание кобальта.
На фиг. 1 сравнивается продуцирование молока, где единственным отличием в корме для животных является источник кобальта. Источник CoPro представляет собой глюкогептонат кобальта. Это растворимый лиганд мономерный сахар для кобальта. При использовании нами примера нового источника кобальта, представляющего собой 75% хлорида кобальта и 25% кобальта с пектином, было отмечено увеличение продуцирования молока.
Таблица 1.
Это увеличение продуцирования молока было статистически значимым.
ПРИМЕР 2
Кобальт с пектином - 1 экв. кобальта, 10 экв. NaOH, 12 часов при 20°C
В 750 мл деионизированной воды добавляют гидроксид натрия (60,02 г, 1,50 моль). В этот щелочной раствор медленно добавляют пектин (30,05 г, 0,169 моль субъединиц карбоновой кислоты) для тонкого диспергирования на поверхности раствора. Тонкая дисперсия быстро превращается в темно-оранжевую суспензию, которую перемешивают в течение 12 часов при 20°C. Значение рН доводят до 8,8 с использованием кислоты 12 М HCl, на этом этапе в реакцию добавляют одной порцией твердое вещество CoCl2·6H2O (40,44 г, 0,170 моль). Полученную розовую суспензию перемешивают в течение еще 1 часа и затем сушат при 88°C в течение 12 часов. Конечный синий порошок гомогенизируют и анализируют на содержание кобальта.
ПРИМЕР 3
Кобальт с пектином - 0,66 экв. кобальта, 10 экв. NaOH, 12 часов при 20°C
В 750 мл деионизированной воды добавляют гидроксид натрия (60,09 г, 1,50 моль). В этот щелочной раствор медленно добавляют пектин (30,03 г, 0,169 моль субъединиц карбоновой кислоты) для тонкого диспергирования на поверхности раствора. Тонкая дисперсия быстро превращается в темно-оранжевую суспензию, которую перемешивают в течение 12 часов при 20°C. Значение рН доводят до 8,8 с использованием кислоты 12 М HCl, на этом этапе в реакцию добавляют одной порцией твердое вещество CoCl2·6H2O (26,50 г, 0,112 моль). Полученную розовую суспензию перемешивают в течение еще 1 часа и затем сушат при 88°C в течение 12 часов. Конечный синий порошок гомогенизируют и анализируют на содержание кобальта.
ПРИМЕР 4
Кобальт с пектином - 0,5 экв. кобальта, 10 экв. NaOH, 12 часов при 20°C
В 750 мл деионизированной воды добавляют гидроксид натрия (59,96 г, 1,49 моль). В этот щелочной раствор медленно добавляют пектин (29,99 г, 0,169 моль субъединиц карбоновой кислоты) для тонкого диспергирования на поверхности раствора. Тонкая дисперсия быстро превращается в темно-оранжевую суспензию, которую перемешивают в течение 12 часов при 20°C. Значение рН доводят до 8,8 с использованием кислоты 12 М HCl, на этом этапе в реакцию добавляют одной порцией твердое вещество CoCl2·6H2O (20,11 г, 0,085 моль). Полученную розовую суспензию перемешивают в течение еще 1 часа и затем сушат при 88°C в течение 12 часов. Конечный синий порошок гомогенизируют и анализируют на содержание кобальта.
ПРИМЕР 5
Кобальт с альгиновой кислотой - 2 экв. кобальта, 10 экв. NaOH, 12 часов при 20°C
В 750 мл деионизированной воды добавляют гидроксид натрия (60,01 г, 1,50 моль). В этот щелочной раствор медленно добавляют альгиновую кислоту (29,90 г, 0,168 моль субъединиц карбоновой кислоты) для тонкого диспергирования на поверхности раствора. Тонкая дисперсия быстро превращается в темно-желто-коричневую суспензию, которую перемешивают в течение 12 часов при 20°C. Значение рН доводят до 8,8 с использованием кислоты 12 М HCl, на этом этапе в реакцию добавляют одной порцией твердое вещество CoCl2·6H2O (80,41 г, 0,338 моль). Полученную розовую суспензию перемешивают в течение еще 1 часа и затем сушат при 88°C в течение 12 часов. Конечный синий порошок гомогенизируют и анализируют на содержание кобальта.
ПРИМЕР 6
Кобальт с альгиновой кислотой - 1 экв. кобальта, 10 экв. NaOH, 12 часов при 20°C
В 750 мл деионизированной воды добавляют гидроксид натрия (59,95 г, 1,49 моль). В этот щелочной раствор медленно добавляют альгиновую кислоту (30,01 г, 0,169 моль субъединиц карбоновой кислоты) для тонкого диспергирования на поверхности раствора. Тонкая дисперсия быстро превращается в темно-желто-коричневую суспензию, которую перемешивают в течение 12 часов при 20°C. Значение рН доводят до 8,8 с использованием кислоты 12 М HCl, на этом этапе в реакцию добавляют одной порцией твердое вещество CoCl2·6H2O (40,15 г, 0,168 моль). Полученную розовую суспензию перемешивают в течение еще 1 часа и затем сушат при 88°C в течение 12 часов. Конечный синий порошок гомогенизируют и анализируют на содержание кобальта.
ПРИМЕР 7
Кобальт с альгиновой кислотой - 0,66 экв. кобальта, 10 экв. NaOH, 12 часов при 20°C
В 750 мл деионизированной воды добавляют гидроксид натрия (59,99 г, 1,50 моль). В этот щелочной раствор медленно добавляют альгиновую кислоту (29,98 г, 0,169 моль субъединиц карбоновой кислоты) для тонкого диспергирования на поверхности раствора. Тонкая дисперсия быстро превращается в темно-желто-коричневую суспензию, которую перемешивают в течение 12 часов при 20°C. Значение рН доводят до 8,8 с использованием кислоты 12 М HCl, на этом этапе в реакцию добавляют одной порцией твердое вещество CoCl2·6H2O (26,53 г, 0,112 моль). Полученную розовую суспензию перемешивают в течение еще 1 часа и затем сушат при 88°C в течение 12 часов. Конечный синий порошок гомогенизируют и анализируют на содержание кобальта.
ПРИМЕР 8
Кобальт с альгиновой кислотой - 0,5 экв. кобальта, 10 экв. NaOH, 12 часов при 20°C
В 750 мл деионизированной воды добавляют гидроксид натрия (60,02 г, 1,50 моль). В этот щелочной раствор медленно добавляют альгиновую кислоту (30,06 г, 0,169 моль субъединиц карбоновой кислоты) для тонкого диспергирования на поверхности раствора. Тонкая дисперсия быстро превращается в темно-желто-коричневую суспензию, которую перемешивают в течение 12 часов при 20°C. Значение рН доводят до 8,8 с использованием кислоты 12 М HCl, на этом этапе в реакцию добавляют одной порцией твердое вещество CoCl2·6H2O (20,08 г, 0,085 моль). Полученную розовую суспензию перемешивают в течение еще 1 часа и затем сушат при 88°C в течение 12 часов. Конечный синий порошок гомогенизируют и анализируют на содержание кобальта.
ПРИМЕР 9
Кобальт с полиакриловой кислотой - 2 экв. кобальта, 1 экв. NaOH
В 750 мл деионизированной воды добавляют гидроксид натрия (2,04 г, 0,051 моль). В этот щелочной раствор добавляют одной порцией 50% полиакриловую кислоту (7,57 г, 0,051 моль субъединиц карбоновой кислоты). Прозрачный раствор перемешивают в течение 10 минут, после чего добавляют одной порцией CoCl2·6H2O (24,28 г, 0,102 моль). Розовую суспензию перемешивают в течение еще одного часа при комнатной температуре и затем сушат при 88°C в течение 12 часов. Конечный синий порошок гомогенизируют и анализируют на содержание кобальта.
ПРИМЕР 10
Кобальт с полиакриловой кислотой - 1 экв. кобальта, 1 экв. NaOH
В 750 мл деионизированной воды добавляют гидроксид натрия (2,10 г, 0,051 моль). В этот щелочной раствор добавляют одной порцией 50% полиакриловую кислоту (7,54 г, 0,051 моль субъединиц карбоновой кислоты). Прозрачный раствор перемешивают в течение 10 минут, после чего добавляют одной порцией CoCl2·6H2O (12,14 г, 0,051 моль). Розовую суспензию перемешивают в течение еще одного часа при комнатной температуре и затем сушат при 88°C в течение 12 часов. Конечный синий порошок гомогенизируют и анализируют на содержание кобальта.
ПРИМЕР 11
Кобальт с полиакриловой кислотой - 0,66 экв. кобальта, 1 экв. NaOH
В 750 мл деионизированной воды добавляют гидроксид натрия (2,04 г, 0,051 моль). В этот щелочной раствор добавляют одной порцией 50% полиакриловую кислоту (7,60 г, 0,051 моль субъединиц карбоновой кислоты). Прозрачный раствор перемешивают в течение 10 минут, после чего добавляют одной порцией CoCl2·6H2O (8,00 г, 0,034 моль). Розовую суспензию перемешивают в течение еще одного часа при комнатной температуре и затем сушат при 88°C в течение 12 часов. Конечный синий порошок гомогенизируют и анализируют на содержание кобальта.
ПРИМЕР 12
Кобальт с полиакриловой кислотой - 0,5 экв. кобальта, 1 экв. NaOH
В 750 мл деионизированной воды добавляют гидроксид натрия (2,01 г, 0,051 моль). В этот щелочной раствор добавляют одной порцией 50% полиакриловую кислоту (7,57 г, 0,051 моль субъединиц карбоновой кислоты). Прозрачный раствор перемешивают в течение 10 минут, после чего добавляют одной порцией CoCl2·6H2O (6,08 г, 0,102 моль). Розовую суспензию перемешивают в течение еще одного часа при комнатной температуре и затем сушат при 88°C в течение 12 часов. Конечный синий порошок гомогенизируют и анализируют на содержание кобальта.
ПРИМЕР 13
Кобальт с пектином 1 экв. кобальта (50% органического/50% неорганического) - 2,5 часа при 70°C - 1 экв. основания -отсутствие HCl
В 370 мл деионизированной воды добавляют гидроксид натрия (6,74 г, 0,168 моль). В этот щелочной раствор медленно добавляют пектин (30,01 г, 0,169 моль субъединиц карбоновой кислоты) для тонкого диспергирования на поверхности раствора. Тонкая дисперсия быстро превращается в темно-оранжевую суспензию, которую перемешивают в течение 2,5 часов при 70°C. На этом этапе в реакцию добавляют одной порцией твердое вещество CoCl2·6H2O (40,21 г, 0,169 моль), и значение рН 12,31 соответственно снижают до 5,868. Полученную розовую суспензию перемешивают в течение еще 1 часа и затем сушат при 88°C в течение 12 часов. Конечный синий порошок гомогенизируют и анализируют на содержание кобальта и молекулярную массу.
ПРИМЕР 14
Кобальт с пектином - 1 экв. кобальта, 1 экв. NaOH, 2 часа при 70°C, остановка реакции HCl
В 370 мл деионизированной воды добавляют гидроксид натрия (6,79 г, 0,169 моль). В этот щелочной раствор медленно добавляют пектин (40,49 г, 0,169 моль субъединиц карбоновой кислоты) для тонкого диспергирования на поверхности раствора. Тонкая дисперсия быстро превращается в темно-оранжевую суспензию, которую перемешивают в течение 2 часов при 70°C. Значение рН доводят до 8,8 с использованием кислоты 12 М HCl (10,5 мл, 126 ммоль), на этом этапе в реакцию добавляют одной порцией твердое вещество CoCl2·6H2O (40,08 г, 0,170 моль). Полученную розовую суспензию перемешивают в течение еще 1 часа и затем сушат при 88°C в течение 12 часов. Конечный синий порошок гомогенизируют и анализируют на содержание кобальта.
ПРИМЕР 15
Кобальт с пектином - 0,66 экв. кобальта, 1 экв. NaOH, 2 часа при 70°C, без остановки реакции HCl
В 370 мл деионизированной воды добавляют гидроксид натрия (6,70 г, 0,168 моль). В этот щелочной раствор медленно добавляют пектин (40,45 г, 0,169 моль субъединиц карбоновой кислоты) для тонкого диспергирования на поверхности раствора. Тонкая дисперсия быстро превращается в темно-оранжевую суспензию, которую перемешивают в течение 2 часов при 70°C. На этом этапе в реакцию добавляют одной порцией твердое вещество CoCl2·6H2O (26,40 г, 0,112 моль), и значение рН 12,45 соответственно снижают до 5,938. Полученную розовую суспензию перемешивают в течение еще 1 часа и затем сушат при 88°C в течение 12 часов. Конечный синий порошок гомогенизируют и анализируют на содержание кобальта и молекулярную массу.
ПРИМЕР 16
Кобальт с пектином - 0,5 экв. кобальта, 1 экв. NaOH, 2 часа при 70°C, без остановки реакции HCl
В 370 мл деионизированной воды добавляют гидроксид натрия (6,81 г, 0,169 моль). В этот щелочной раствор медленно добавляют пектин (40,53 г, 0,169 моль субъединиц карбоновой кислоты) для тонкого диспергирования на поверхности раствора. Тонкая дисперсия быстро превращается в темно-оранжевую суспензию, которую перемешивают в течение 2 часов при 70°C. На этом этапе в реакцию добавляют одной порцией твердое вещество CoCl2·6H2O (20,07 г, 0,085 моль), и значение рН 12,40 соответственно снижают до 5,871. Полученную розовую суспензию перемешивают в течение еще 1 часа и затем сушат при 88°C в течение 12 часов. Конечный синий порошок гомогенизируют и анализируют на содержание кобальта и молекулярную массу.
ПРИМЕР 17
Кобальт с пектином - 1 экв. кобальта, 2 экв. NaOH, 2 часа при 70°C, остановка реакции HCl
В 370 мл деионизированной воды добавляют гидроксид натрия (13,51 г, 0,338 моль). В этот щелочной раствор медленно добавляют пектин (40,46 г, 0,169 моль субъединиц карбоновой кислоты) для тонкого диспергирования на поверхности раствора. Тонкая дисперсия быстро превращается в темно-оранжевую суспензию, которую перемешивают в течение 2 часов при 70°C. Значение рН доводят до 8,8 с использованием кислоты 12 М HCl (21,5 мл, 258 ммоль), на этом этапе в реакцию добавляют одной порцией твердое вещество CoCl2·6H2O (39,91 г, 0,169 моль). Полученную розовую суспензию перемешивают в течение еще 1 часа и затем сушат при 88°C в течение 12 часов. Конечный синий порошок гомогенизируют и анализируют на содержание кобальта.
ПРИМЕР 18
Кобальт с пектином - 1 экв. кобальта, 4 экв. NaOH, 2 часа при 70°C, остановка реакции HCl
В 370 мл деионизированной воды добавляют гидроксид натрия (27,01 г, 0,68 моль). В этот щелочной раствор медленно добавляют пектин (40,54 г, 0,169 моль субъединиц карбоновой кислоты) для тонкого диспергирования на поверхности раствора. Тонкая дисперсия быстро превращается в темно-оранжевую суспензию, которую перемешивают в течение 2 часов при 70°C. Значение рН доводят до 8,8 с использованием кислоты 12 М HCl (43 мл, 516 ммоль), на этом этапе в реакцию добавляют одной порцией твердое вещество CoCl2·6H2O (39,91 г, 0,169 моль). Полученную розовую суспензию перемешивают в течение еще 1 часа и затем сушат при 88°C в течение 12 часов. Конечный синий порошок гомогенизируют и анализируют на содержание кобальта.
ПРИМЕР 19
Кобальт с пектином - 1,5 экв. кобальта, 1 экв. NaOH, 2 часа при 70°C, остановка реакции HCl
В 370 мл деионизированной воды добавляют гидроксид натрия (6,74 г, 0,168 моль). В этот щелочной раствор медленно добавляют пектин (40,48 г, 0,169 моль субъединиц карбоновой кислоты) для тонкого диспергирования на поверхности раствора. Тонкая дисперсия быстро превращается в темно-оранжевую суспензию, которую перемешивают в течение 2 часов при 70°C. Значение рН доводят до 8,8 с использованием кислоты 12 М HCl (10,8 мл, 130 ммоль), на этом этапе в реакцию добавляют одной порцией твердое вещество CoCl2·6H2O (60,03 г, 0,26 моль). Полученную розовую суспензию перемешивают в течение еще 1 часа и затем сушат при 88°C в течение 12 часов. Конечный синий порошок гомогенизируют и анализируют на содержание кобальта.
ПРИМЕР 20
Кобальт с пектином - 1 экв. кобальта, 1 экв. NaOH, 2 часа при 20°C, остановка реакции HCl
В 370 мл деионизированной воды добавляют гидроксид натрия (6,81 г, 0,169 моль). В этот щелочной раствор медленно добавляют пектин (40,5 г, 0,169 моль субъединиц карбоновой кислоты) для тонкого диспергирования на поверхности раствора. Тонкая дисперсия быстро превращается в темно-оранжевую суспензию, которую перемешивают в течение 2 часов при 20°C. Значение рН доводят до 8,8 с использованием кислоты 12 М HCl (10,5 мл, 126 ммоль), на этом этапе в реакцию добавляют одной порцией твердое вещество CoCl2·6H2O (40,8 г, 0,170 моль). Полученную розовую суспензию перемешивают в течение еще 1 часа и затем сушат при 88°C в течение 12 часов. Конечный синий порошок гомогенизируют и анализируют на содержание кобальта.
ПРИМЕР 21
Данные до и после обработки по результатам приема данного источника кобальта овцами показаны на фиг. 2. Были изучены три источника кобальта, представленные на фиг. 2 CSK16254 представлял собой 75% CoCl2 и 25% кобальта с пектином (пример 1), CSK16255 представлял собой 50% CoCl2 и 50% кобальта с пектином (пример 2), CSK16256 представлял собой 100% кобальта с пектином (пример 4). Это исследование демонстрирует, что наличие комбинации растворимого и мономерного лиганда с источником связанного с полимером кобальта эффективнее по сравнению с только формой связанного с полимером кобальта.
ПРИМЕР 22
Фиг. 3 и приведенные данные отображают изменение уровней B12 у овец. Предварительная обработка проводится дополнительно до обработок кобальтом, а последующая проводится после обработок кобальтом. CSK17049 представляет собой 25% глюкогептоната кобальта и 75% кобальта с пектином из примера 4, CSK17050 представляет собой 25% хлорида кобальта и 75% кобальта с пектином из примера 4, и CSK17051 представляет собой 25% хлорида кобальта и 75% кобальта с альгиновой кислотой из примера 8. Данные демонстрируют, что все эти комбинации дают сильное повышение витамина B12 у овец.
ПРИМЕР 23
Фиг. 4 и приведенные данные отображают среднее изменение уровней B12 у овец до и после обработок кобальтом. Предварительная обработка проводится дополнительно до обработок кобальтом, а последующая проводится после обработок кобальтом. CSK17057 представляет собой 50% хлорида кобальта и 50% кобальта с пектином из примера 13, CSK17058 представляет собой 50% хлорида кобальта и 50% кобальта с пектином из примера 2, и CSK17059 представляет собой 25% хлорида кобальта и 75% кобальта с пектином из примера 15. Данные демонстрируют, что все эти комбинации дают сильное повышение витамина B12 у овец.
ПРИМЕР 24
Фиг. 5 и приведенные данные отображают среднее изменение уровней B12 у овец до и после обработки кобальтом. Предварительная обработка проводится дополнительно до обработок кобальтом, а последующая проводится после обработки. CSK17139 представляет собой 75% хлорида кобальта и 25% кобальта с полиакриловой кислотой из примера 9. CSK17140 представляет собой 50% хлорида кобальта и 50% кобальта с полиакриловой кислотой из примера 10. CSK17141 представляет собой 25% хлорида кобальта и 75% кобальта с альгиновой кислотой из примера 7. Данные демонстрируют, что все эти комбинации дают сильное повышение витамина B12 у овец.
Как поясняется ранее, примеры 1-24 являются только иллюстративными. Они представляются для обеспечения обоснования прилагаемых пунктов формулы изобретения. Заявитель намерен полагаться на доктрину эквивалентов для соответствующего объема. Понятно, что другие источники кобальта, которые обеспечивают быстрое высвобождение и медленное высвобождение в комбинации при скармливании жвачным животным, рассматриваются при условии, что они позволяют использовать изобретение для повышения продуцирования витамина B12 у жвачных, особенно в период лактации.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛЕТУЧИЕ ЖИРНЫЕ КИСЛОТЫ БЕЗ ЗАПАХА ДЛЯ ПРИМЕНЕНИЯ В КАЧЕСТВЕ ИСТОЧНИКА ЭНЕРГИИ ДЛЯ ЖВАЧНЫХ ЖИВОТНЫХ, СВИНЕЙ И ДОМАШНЕЙ ПТИЦЫ | 2016 |
|
RU2678423C1 |
| ПРИМЕНЕНИЕ ПАРА-НИТРОАМИНОПРОИЗВОДНЫХ В КОРМЕ ДЛЯ СНИЖЕНИЯ ВЫДЕЛЕНИЯ МЕТАНА У ЖВАЧНЫХ ЖИВОТНЫХ | 2013 |
|
RU2615390C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНОГО ИНДОЛОПИРРОЛОКАРБАЗОЛА | 2003 |
|
RU2337105C2 |
| НЕТКАНЫЙ МАТЕРИАЛ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ | 1992 |
|
RU2133127C1 |
| ПРОИЗВОДНЫЕ ЦИКЛОПРОПИЛ-β-АМИНОКИСЛОТЫ | 2004 |
|
RU2312853C2 |
| Кормовая добавка для крупного рогатого скота, улучшающая деструкцию структурных углеводов в рубце | 2023 |
|
RU2804123C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА АММОКСИДИРОВАНИЯ И СПОСОБ ПОЛУЧЕНИЯ АКРИЛОНИТРИЛА | 2017 |
|
RU2729070C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЧАСТИЧНО ФТОРИРОВАННЫХ АРОМАТИЧЕСКИХ АМИНОВ | 2009 |
|
RU2400470C1 |
| СПОСОБ ПОЛУЧЕНИЯ 6-УНДЕКАНОНА И ЕГО ПРОИЗВОДНЫХ | 2019 |
|
RU2788086C2 |
| ПРОИЗВОДНЫЕ ФЕНИЛОКСАДИАЗОЛА В КАЧЕСТВЕ ИНГИБИТОРОВ PGDS | 2010 |
|
RU2572608C2 |
Изобретение относится к ветеринарии, в частности к композиции для скармливания жвачным животным и способу регулирования высвобождения кобальта в рубце бактериями рубца для превращения в витамин B12. Способ включает скармливание жвачным животным смешанного источника кобальта, а именно источника быстрого высвобождения кобальта и источника медленного высвобождения кобальта. Источник быстрого высвобождения кобальта выбирают из группы, состоящей из растворимых неорганических или органических источников ионов кобальта и комплексов растворимого кобальта с мономерным сахаром. Источник медленного высвобождения кобальта представляет собой полимерный комплекс с боковыми группами карбоновых кислот, выбранными из альгиновой кислоты, альгината кобальта, пектина, полиакриловой кислоты и карбоксиметилцеллюлозы. Источник быстрого высвобождения кобальта составляет от 25 до 75 вес.% общего источника кобальта, а остальная часть общего источника кобальта является источником медленного высвобождения кобальта. Использование группы изобретений позволит регулировать скорость высвобождения кобальта в рубце для превращения бактериями рубца в витамин B12. 2 н. и 6 з.п. ф-лы, 1 табл., 24 пр., 5 ил.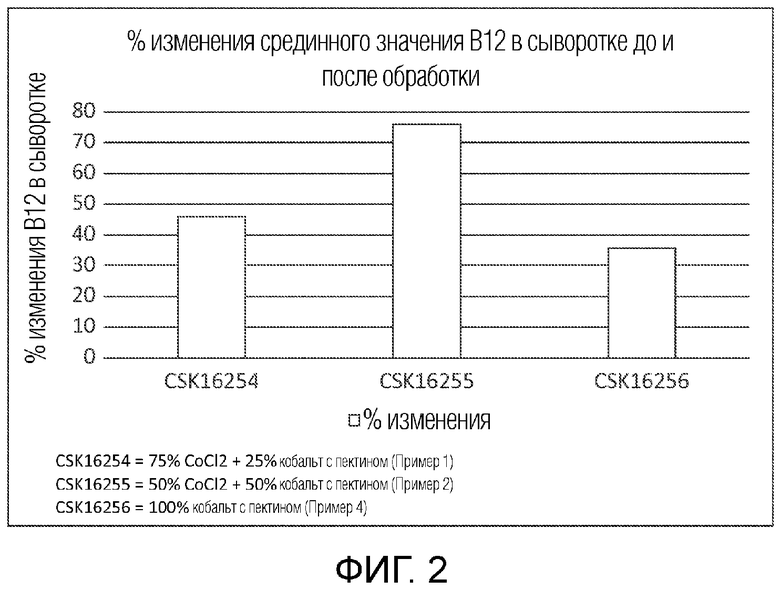
1. Способ регулирования высвобождения кобальта в рубце бактериями рубца для превращения в витамин B12, включающий:
скармливание жвачным животным смешанного источника кобальта:
источника быстрого высвобождения кобальта и источника медленного высвобождения кобальта;
в котором источник быстрого высвобождения кобальта выбирают из группы, состоящей из растворимых неорганических или органических источников ионов кобальта и комплексов растворимого кобальта с мономерным сахаром;
в котором источник медленного высвобождения кобальта представляет собой полимерный комплекс с боковыми группами карбоновых кислот, выбранными из альгиновой кислоты, альгината кобальта, пектина, полиакриловой кислоты и карбоксиметилцеллюлозы; и
указанный источник быстрого высвобождения кобальта составляет от 25 до 75 вес.% общего источника кобальта, а остальная часть общего источника кобальта является источником медленного высвобождения кобальта.
2. Способ по п. 1, в котором смешанный источник кобальта содержит 50 вес.% источника быстрого высвобождения кобальта и 50 вес.% источника медленного высвобождения кобальта.
3. Способ по п. 1, в котором источником медленного высвобождения кобальта является кобальт с пектином.
4. Способ по п. 1, в котором источник кобальта выбирают из кобальта с альгиновой кислотой или альгината кобальта.
5. Композиция смешанного источника кобальта для скармливания жвачным животным с целью регулирования скорости высвобождения кобальта в рубце для превращения бактериями рубца в витамин B12, содержащая:
источник быстрого высвобождения кобальта и источник медленного высвобождения кобальта;
в котором источник быстрого высвобождения кобальта выбирают из группы, состоящей из растворимых неорганических или органических источников ионов кобальта и комплексов растворимого кобальта с мономерным сахаром;
в котором источник медленного высвобождения кобальта представляет собой полимерный комплекс с боковыми группами карбоновых кислот, выбранными из альгиновой кислоты, альгината кобальта, пектина, полиакриловой кислоты и карбоксиметилцеллюлозы; и
указанный источник быстрого высвобождения кобальта составляет от 25 до 75 вес.% общего источника кобальта, а остальная часть общего источника кобальта является источником медленного высвобождения кобальта.
6. Композиция по п. 5, в которой смешанный источник кобальта содержит 50 вес.% источника быстрого высвобождения кобальта и 50 вес.% источника медленного высвобождения кобальта.
7. Композиция по п. 5, в которой источником медленного высвобождения кобальта является кобальт с пектином.
8. Композиция по п. 5, в которой источником кобальта является кобальт с альгиновой кислотой.
| GB 866924 A, 03.05.1961 | |||
| K UCHIDA et al | |||
| "Effect of feeding a combination of zinc, manganese and copper amino acid complexes, and cobalt glucoheptonate on performance of early lactation high producing dairy cows", ANIMAL FEED SCIENCE AND TECHNOLOGY, vol | |||
| Домовый номерной фонарь, служащий одновременно для указания названия улицы и номера дома и для освещения прилежащего участка улицы | 1917 |
|
SU93A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Приспособление для градации давления в воздухопроводе воздушных тормозов | 1921 |
|
SU193A1 |
| D T PAL et al | |||
Авторы
Даты
2020-12-30—Публикация
2018-06-28—Подача