Изобретение относится к фармакологии, а именно к биологически активным веществам, обладающим цитотоксической активностью по отношению к культуре клеток рака легкого А 549, и может быть использовано при производстве противоопухолевых лекарственных средств
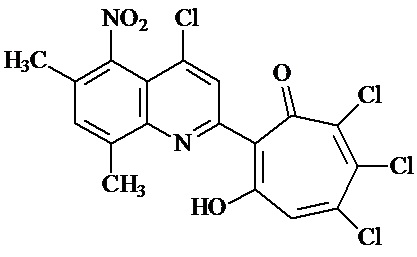 (1)
(1)
обладающих цитотоксической активностью по отношению к культуре клеток рака легкого А 549, и может быть использовано при производстве противоопухолевых лекарственных средств.
В настоящее время в мире онкологические заболевания являются одной из основных причин смертности. По оценкам Международного агентства по исследованию рака, в 2018 году было зарегистрировано 18,1 миллиона новых случаев заболевания и 9,6 миллиона случаев смерти от злокачественных новообразований [1]. По данным Всемирной организации здравоохранения (ВОЗ) от рака умирает каждый шестой человек. В России ежегодно выявляется почти 600 тыс., а умирает около 300 тыс. онкобольных [2]. Рак является одной из самых значимых медицинских и общественных проблем, как в России, так и в большинстве стран мира. Первое место по распространенности среди мужчин и лидирующее место по смертности среди всех онкологических заболеваний занимает рак легкого [3].
Основными подходами к терапии злокачественных новообразований является хирургическое лечение и цитотоксическая химиотерапия, которая включает введение противоопухолевых препаратов по стандартизированной схеме лечения [4]. На сегодняшний день общепринятым стандартом первой линии терапии многих видов рака является применение препаратов на основе платины, обладающих цитотоксическим эффектом широкого спектра действия [5, 6, 7]. К ним относятся цисплатин, карбоплатин и оксалиплатин с различной эффективностью и токсичностью [8]. Их противоопухолевая активность связана со способностью повреждать ДНК, что впоследствии приводит к апоптозу опухолевых клеток [9]. В комбинации с другими противоопухолевыми препаратами (этопозид, паклитаксел, блеомицин, гемцитабин, циклофосфамид) платиновые агенты используются для лечения рака легкого, рака яичников, рака поджелудочной железы, рака молочной железы, меланомы и лимфом [10, 11, 12]. Несмотря на широкое применение, все цитостатики вызывают многочисленные нежелательные токсические эффекты: нейротоксичность, тошнота, рвота, потеря мышечной массы [7, 8]. В связи со значительным ростом онкологических заболеваний актуальным является разработка и внедрение новых противоопухолевых средств, которые обладали бы высокой эффективностью на фоне низкого риска развития нежелательных реакций.
Первым этапом в поиске новых противоопухолевых соединений в экспериментальной клеточной биологии является тест на жизнеспособность, который позволяет проводить начальный отбор перспективных лекарственных средств среди вновь синтезированных соединений [6].
В ряду 2-хинолин-2-ил-производных 1,3-трополона известен 2-(4h-1,3-бензоксазин-4-он-2-ил)-4,5,6-трихлор-1,3-трополон, обладающий антибактериальной активностью против госпитальных штаммов грамотрицательных и грамположительных бактерий [9].
Известны в этом ряду 2-гетарилзамещенные 1,3-трополона, обладающие антимикробным действием [10].
Известен в этом ряду также 2-[7-ацетил-9,11-ди(трет-бутил)-4-метил-5-хлорбензо[b][1,4]оксазепино[7,6,5-de]-хинолин-2-ил]-5,6,7-трихлор-1,3-трополон, проявляющий цитотоксическую активность в отношении опухолевых клеток молочной железы MCF-7 (Human breast carcinoma) в концентрации IC50 12.96 μг/мл, а также опухолевых эпителиальных клеток KB, опухолевых клеток легких Lu и печени Hep-G2 в концентрациях IC50 > 128 μг/мл [11].
Наиболее близким по выполнению является 5,7-ди(трет-бутил)-4-нитро-2-(4,7-дихлор-5-нитро-8-метилхинолин-2-ил)-1,3-трополон, проявляющий цитотоксическую активность на клеточные линии OVCAR-8, OVCAR-3, H441, HCT-116, Panc1, A549 (IC50 мкM =3.89±0.6927) [12].
Технический результат достигается 2-(6,8-диметил-5-нитро-4-хлорхинолин-2-ил)-5,6,7-трихлор-1,3-трополоном формулы 1

Синтез соединения 1 заключается в реакции расширения о-хинонового цикла, протекающей между 5-нитро-2,6,8-триметил-4-хлорхинолином 2 и 3,4,5,6-тетрахлор-1,2-бензохиноном 3 при кипячении в диоксане:
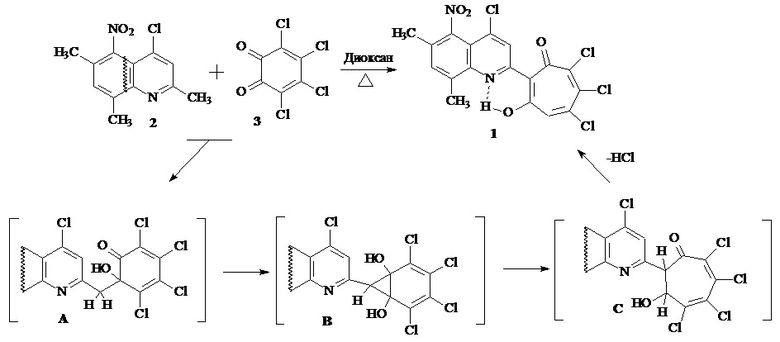 Механизм образования трополоновой системы 1 включает стадию альдольной конденсации с образованием интермедиата А, циклизацию А в норкарадиеновое производное B и перегруппировку B в дигидротрополон С. Окончательное формирование 1,3-трополонового фрагмента сопровождается дегидрохлорированием С, что ведет к основному продукту 1.
Механизм образования трополоновой системы 1 включает стадию альдольной конденсации с образованием интермедиата А, циклизацию А в норкарадиеновое производное B и перегруппировку B в дигидротрополон С. Окончательное формирование 1,3-трополонового фрагмента сопровождается дегидрохлорированием С, что ведет к основному продукту 1.
Строение соединения 1 установлено данными ЯМР 1Н и ИК-спектроскопии, масс-спектрометрии.
Ниже приведен пример синтеза 2-(6,8-диметил-5-нитро-4-хлорхинолин-2-ил)-5,6,7-трихлор-1,3-трополона 1.
Пример. 2-(6,8-диметил-5-нитро-4-хлорхинолин-2-ил)-5,6,7-трихлор-1,3-трополон (1). Раствор 20,6 г (0,083 моль) 3,4,5,6-тетрахлор-1,2-бензохинона (3), 21 г (0,083 моль) 5-нитро-2,6,8-триметил-4-хлорхинолина (2) кипятили в 60 мл диоксана 2 часа. Охлаждали раствор и отфильтровывали выпавший осадок. Получали 17 г соединения (1). Маточный раствор пропускали через хроматографическую колонку с силикагелем (элюент - CH2Cl2). Собирали ярко-желтую фракцию с Rf 0.5. Отгоняли растворитель и получали 2,8 г соединения (1). Выход 19,8 г (52 %), ярко-желтые кристаллы (бензол), т.пл. 205-207°С.
Спектр ЯМР 1Н, (600 МГц), δ, м.д. (CDCl3): 2.44 (3H, с, CH3), 2.74 (3H, c, CH3), 7.16 (1H, s, 4-СHтроп.), 7.57 (1H, с, CHаром.), 8.40 (1H, с, CHаром), 19.00 (1H, с, OH). Спектр ЯМР 13С, (151 МГц), δ, м.д. (CDCl3): 17.66, 18.58, 112.15, 115.85, 123.85, 130.12, 131.39, 132.78, 134.09, 135.00, 136.29, 138.46, 138.55, 141.58, 144.01, 153.73, 173.61, 181.87. ИК-спектр, ν/см-1: 3122, 3051, 1621, 1585, 1538, 1496, 1462, 1434, 1385, 1362, 1320, 1289, 1260, 1199, 1127, 1110, 1069, 1027, 1006, 945, 880, 840, 782, 756, 741, 712, 699. Масс-спектр (ЭУ, 70 эВ), m/z (Iотн (%)): 432 (M+-CO, 85), 395 (16), 386 (37), 365 (17), 350 (18), 337 (16), 314 (13), 286 (25), 250 (25), 214 (31), 188 (23), 166 (30), 147 (62), 139 (50), 119 (58), 99 (37), 84 (87), 77 (57), 62 (100), 50 (57), 38 (77). C18H10Cl4N2O4 (M= 460.10). Вычислено: C 46.99; Н 2.19; N 6.09. Найдено: C 46.90; Н 2.12; N 6.02.
Исследование фармакологической активности
Материалы и методы
Эксперимент проведен на устойчивой клеточной линии немелкоклеточного рака легкого A549.
МТТ-колориметрический тест для оценки жизнеспособности клеток основан на восстановлении при помощи НАДФ-H-зависимых клеточных оксидоредуктазных ферментов тетразолиевого красителя 3-(4,5-диметилтиазол-2-ил)-2,5-дифенил-тетразолиум бромида в нерастворимый в воде, но растроримый в ДМСО формазан, который имеет пурпурно-синее окрашивание. Оценку жизнеспособности проводят по уменьшению оптической плотности опытных проб по сравнению с контрольными [13].
Клетки рассаживали в 96-луночный планшет и культивировали в стандартных стерильных условиях: питательная среда DMEM, 10% ЭТС, 5% CO2, температура плюс 37°C. Вещество добавляли в концентрации от 0,004 до 2,226 мкМ. Клетки далее инкубировали в тех же стандартных стерильных условиях в течение 72 ч, после чего к ним добавляли по 20 мкл рабочего раствора МТТ. Инкубировали еще 2 часа в условиях СО2-инкубатора. Образовавшиеся кристаллы формазана растворяли в ДМСО и измеряли оптическую плотность (длины волн: возбуждение/эмиссия 540 нм / 590 нм).
Статистическая обработка результатов исследования проводилась с использованием теста Вилкоксона, критерия Краскела-Уолиса с постобработкой тестом Данна. Обсчет реализован в программе GraphPad Prism 5.0.
Результаты исследований
Об уровне цитотоксической активности судили по изменению степени флуоресценции в лунках, обработанных веществом по сравнению с контрольными лунками (без воздействия).
Ингибирующая концентрация IC50 2-(6,8-диметил-5-нитро-4-хлорхинолин-2-ил)-5,6,7-трихлор-1,3-трополона в отношении культуры клеток рака легкого А 549 составила 0,21±0,01 мкМ, что значимо меньше ингибирующей концентрации IC50 широко используемого в терапии рака Циспластина, равной 3,84±0,23 [8] (отличия статистически достоверны по отношению к группе контроля, р≤0,05, по критерию Краскела-Уолиса).
Таким образом, 2-(6,8-диметил-5-нитро-4-хлорхинолин-2-ил)-5,6,7-трихлор-1,3-трополон проявляет цитотоксическую активность в отношении клеточной линии рака легкого A549, при этом концентрация IC50 предлагаемого соединения ниже, чем концентрация IC50 наиболее близкого по структуре соединения (IC50 = 3.89±0.6927 мкM; [12]), и ниже, чем концентрация широко используемого в терапии опухолей, в том числе и рака легкого, Циспластина.
Литература
1. Bray F., Ferlay J., Soerjomataram I., Siegel R.L., Torre L.A., Jemal A. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries // CA Cancer J Clin. - 2018. - Vol. 68. - № 6. - P. 394-424. doi: 10.3322/caac.21492.
2. Злокачественные новообразования в России в 2017 году (Заболеваемость и смертность). Под ред. Каприна А.Д., Старинского В.В., Петровой Г.В. - М.: МНИОИ им. П.А. Герцена - филиал ФГБУ «НМИЦ радиологии» Минздрава России, 2018. - 250 с.
3. Noone A.M., Howlader N., Krapcho M., Miller D., Brest A., Yu M. SEER Cancer Statistics Review, 1975-2015. // National Cancer Institute. Bethesda, MD. - 2018. https://seer.cancer.gov/csr/1975_2015/.
4. Holohan C., Van Schaeybroeck S., Longley D.B., Johnston P.G. Cancer drug resistance: an evolving paradigm. //Nat. Rev. Cancer. - 2013. - Vol. 13. - P. 714-726. doi: 10.1038/nrc3599.
5. Румянцев А.А., Покатаев И.А., Тюляндин С.А. Современные аспекты антиангиогенной терапии при раке яичников // Медицинский совет. - 2018. - № 19. - С. 19-21. doi:10.21518/2079-701X-2018-19-17-21.
6. Bai L., Gao Ch., Liu Q., Yu C., Zhang Zh., Cai L., Yang B., Qian Y., Yang J., Liao X. Research progress in modern structure of platinum complexes. // Eur. J. Med. Chem. - 2017. - Vol. 140. - P. 349-382. https://doi.org/10.1016/j.ejmech.2017.09.034.
7. Moreira-Pais A., Ferreira R., R.G. da Costa. Platinum-induced muscle wasting in cancer chemotherapy: Mechanisms and potential targets for therapeutic intervention // Life Sciences. - 2018. - Vol. 208. - P. 1-9. https://doi.org/10.1016/j.lfs.2018.07.010.
8. Cheff D.M., Hall M.D. A drug of such damned nature.1 Challenges and opportunities in translational platinum drug research // J. Med. Chem. - 2017. - Vol. 60. - P. 4517-4532. doi: 10.1021/acs.jmedchem.6b01351.
9. Саяпин Ю.А., Гусаков Е.А., Дороган И.В., Тупаева И.О., Теймуразов М.Г., Фурсова Н.К., Овчинников К.В., Минкин В.И. Новый 2- (4h-1,3-бензоксазин-4-он-2-ил)-1,3-трополон: синтез, структураиантибактериальныесвойства // Биоорганическая химия, 2016, том 42, № 2, с. 247-2522.
10. Патент на изобретение РФ № 2314295, МПК C07D 215/14, 2008 г.
11. Зыонг Нгиа Банг, Саяпин Ю.А., Хоанг Лам, Нгуен Данг Дык, Комиссаров В.Н.. Синтез и цитотоксическая активность производных [бензо[b][1,4]оксазепино[7,6,5-de]хинолин-2-ил]-1,3-трополонов // Химия гетероциклических соединений. - 2015. - 51(3). - С. 291-294.
12. Патент на изобретение РФ № 2702648, МПК C07D 215/18, 2019 г.
13. Berridge M.V., Herst P.M., Tan A.S. Tetrazolium dyes as tool sincell biology: new insights into their cellular reduction // Biotechnology Annual Review. - 2005. - 11. - Р. 127-152.
| название | год | авторы | номер документа |
|---|---|---|---|
| 2-(1,1-Диметил-1H-бензо[e]индолин-2-ил)-5,6,7-трихлор-1,3-трополон, обладающий цитотоксической активностью по отношению к культуре клеток рака кожи А431 и рака легкого Н1299 | 2023 |
|
RU2810581C1 |
| Средство, обладающее цитотоксической активностью в отношении культуры клеток глиомы U87MG | 2024 |
|
RU2839886C1 |
| 5,7-Ди(трет-бутил)-2-(4,7-дихлор-8-метил-5-нитрохинолин-2-ил)-4-нитро-1,3-трополон, обладающий цитотоксической активностью | 2019 |
|
RU2702648C1 |
| Натрий-кобальт-полигалактуронат, обладающий противоопухолевой активностью | 2023 |
|
RU2794885C1 |
| Новые пространственно-затрудненные фенолы, содержащие бензофуроксановые фрагменты, обладающие противоопухолевой активностью | 2022 |
|
RU2796810C1 |
| Противоопухолевые средства на основе макро- и микроэлементсодержащих полигалактуронатов (варианты) | 2022 |
|
RU2792613C1 |
| N-(2-(2-(2-азидоэтокси)этокси)этил)-4,6-ди(азиридин-1-ил)-1,3,5-триазин-2-амин, обладающий цитотоксическим действием | 2023 |
|
RU2825828C1 |
| Бромсодержащие пространственно-затрудненные фенолы, обладающие противоопухолевой активностью | 2023 |
|
RU2822270C1 |
| Средство на основе енаминогидразонотиазольного производного усниновой кислоты, обладающее способностью усиливать цитотоксическое, противоопухолевое и антиметастатическое действие топотекана | 2024 |
|
RU2833910C1 |
| Метил 6-[(4-(азиридин-1-ил)-6-хлоро-1,3,5-триазин-2-ил)амино]гексаноат, обладающий цитотоксическим действием | 2022 |
|
RU2791798C1 |
Настоящее изобретение относится к применению 2-(6,8-диметил-5-нитро-4-хлорхинолин-2-ил)-5,6,7-трихлор-1,3-трополона формулы 1
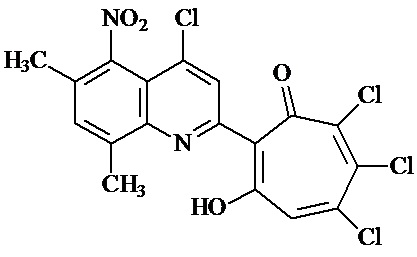
в качестве средства, обладающего цитотоксической активностью в отношении культуры клеток немелкоклеточного рака легких А 549. Технический результат: органическое соединение формулы 1 позволяет ингибировать рост опухолевых клеток легкого в меньшей концентрации по сравнению с концентрациями известных в данном ряду соединений, обладающих цитотоксической активностью. 1 з.п. ф-лы, 1 пр.
1. Применение 2-(6,8-диметил-5-нитро-4-хлорхинолин-2-ил)-5,6,7-трихлор-1,3-трополон формулы 1
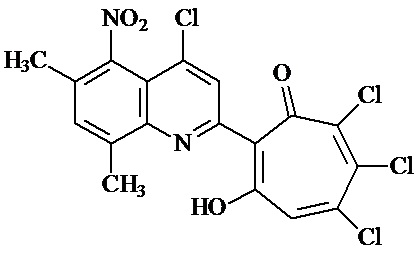
в качестве средства, обладающего цитотоксической активностью в отношении культуры клеток немелкоклеточного рака легких А 549.
2. Применение 2-(6,8-диметил-5-нитро-4-хлорхинолин-2-ил)-5,6,7-трихлор-1,3-трополон по п.1 для изготовления фармацевтической композиции.
| SAYAPIN Y.A | |||
| et al | |||
| Synthesis, structure, and photoisomerization of derivatives of 2-(2-quinolyl)-1,3-tropolones prepared by the condensation of 2-methylquinolines with 3,4,5,6-tetrachloro-1,2-benzoquinone, Tetrahedron, 2010, vol | |||
| Приспособление для соединения пучка кисти с трубкою или втулкою, служащей для прикрепления ручки | 1915 |
|
SU66A1 |
| УСТРОЙСТВО ДЛЯ РЕГУЛИРОВАНИЯ ТЕМПЕРАТУРЫ ПОМЕЩЕНИЙ | 1928 |
|
SU8763A1 |
| 5,7-Ди(трет-бутил)-2-(4,7-дихлор-8-метил-5-нитрохинолин-2-ил)-4-нитро-1,3-трополон, обладающий цитотоксической активностью | 2019 |
|
RU2702648C1 |
| 2-ГЕТАРИЛЗАМЕЩЕННЫЕ 1,3-ТРОПОЛОНА, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ АНТИМИКРОБНОГО ДЕЙСТВИЯ | 2006 |
|
RU2314295C2 |
| ЗЫОНГ Н.Б | |||
| и др | |||
| Синтез и цитотоксическая | |||
Авторы
Даты
2021-01-25—Публикация
2020-07-17—Подача