ОБЛАСТЬ ТЕХНИКИ
[001] Данное изобретение относится к фармацевтически приемлемым лекарственным формам, содержащим оксалатные соли тенелиглиптина и их сольваты, необязательно дополнительно содержащим молекулы класса бигуанидов. В данном документе также предложено применение указанных лекарственных форм и лечение нарушения метаболизма глюкозы у пациентов, нуждающихся в этом.
УРОВЕНЬ ТЕХНИКИ
[002] Ингибиторы дипептидилпептидазы-4 (DPP-IV) представляют собой класс антидиабетических лекарств, действующих посредством ингибирования разложения инкретинов, глюкагоноподобного пептида-1 (GLP-1) и глюкозозависимого инсулинотропаного пептида (GIP). Обобщенно указанные соединения называют «глиптинами».
[003] Ингибиторы DPP-IV широко используют в комбинированной терапии вместе с другими антидиабетическими лекарствами.
[004] В данной области техники существует потребность в обеспечении новых и стабильных лекарственных форм, эффективных по своей сути и демонстрирующих улучшенную стабильность и технологичность.
КРАТКОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
[005] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие оксалатные соли соединения Формулы (I) и их сольваты, и по меньшей мере один или более фармацевтически приемлемых носителей, разбавителей, связующих веществ, смазывающих веществ, разрыхлителей и стабилизирующих агентов. В одном аспекте данного варианта реализации разбавитель выбран из группы, состоящей из маннита, сорбита, ксилита, крахмала, лактозы, целлюлозы, дигидрофосфата кальция и т.п., предпочтительно маннита или лактозы. В другом аспекте связующее вещество выбрано из группы, состоящей из гидроксипропилцеллюлозы, поливинилового спирта, повидона, коповидона, этилцеллюлозы, гипромеллозы и т.п., предпочтительно гипромеллозы или гидроксипропилцеллюлозы. В другом аспекте данного варианта реализации смазывающее вещество представляет собой глицерилдибегенат, стеарилфумарат натрия или кальция, стеарат магния, стеариновую кислоту, глицерилпальмитостеарат и т.п., предпочтительно глицерилдибегенат. В другом аспекте данного варианта реализации разрыхлитель выбран из группы, состоящей из гидроксипропилцеллюлозы с низкой степенью замещения, кросповидона, кроскармеллозы натрия, крахмалгликолята натрия и т.п., предпочтительно гидроксипропилцеллюлозы с низкой степенью замещения. В другом аспекте данного варианта реализации стабилизирующий агент выбран из по меньшей мере одного стабилизатора; по меньшей мере одного комплексообразующего агента; по меньшей мере одного полимера; по меньшей мере одного хелатообразующего агента; и их комбинаций.
[006] В одном аспекте данного варианта реализации в настоящем изобретении предложена фармацевтическая композиция, в которой
(a) оксалатная соль соединения (I) и ее сольват выбран из 2,5 оксалата тенелиглиптина или 3,0 оксалата тенелиглиптина и их сольватов
(b) разбавитель выбран из маннита или лактозы
(c) связующее вещество выбрано из гидроксипропилцеллюлозы или гипромеллозы
(d) смазывающее вещество выбрано из глицерилдибегената или стеарата магния
(e) разрыхлитель выбран из гидроксипропилцеллюлозы с низкой степенью замещения, кросповидона, кроскармеллозы натрия
(f) стабилизирующий агент выбран из щавелевой кислоты, бета-циклодекстрина, гидроксипропилцеллюлозы, ЭДТК и их комбинаций.
[007] В одном или более аспектах данного варианта реализации предложена фармацевтическая композиция, содержащая
(a) оксалатную соль соединения (I) и ее сольват, представляющий собой n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0
(b) разбавитель, представляющий собой маннит
(c) связующее вещество, представляющее собой гипромеллозу
(d) смазывающее вещество, представляющее собой глицерилдибегенат
(e) разрыхлитель, представляющий собой гидроксипропилцеллюлозу с низкой степенью замещения
(f) стабилизирующий агент выбран из щавелевой кислоты, бета-циклодекстрина, гидроксипропилцеллюлозы, ЭДТК и их комбинаций.
[008] В одном или более аспектах данного варианта реализации предложена фармацевтическая композиция, содержащая
(а) оксалатную соль соединения (I) и ее сольват, представляющий собой n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0
(b) разбавитель, представляющий собой лактозу
(c) связующее вещество, представляющее собой гипромеллозу
(d) смазывающее вещество, представляющее собой глицерилдибегенат
(e) разрыхлитель, представляющий собой гидроксипропилцеллюлозу с низкой степенью замещения
(f) стабилизирующий агент выбран из щавелевой кислоты, бета-циклодекстрина, гидроксипропилцеллюлозы, ЭДТК и их комбинаций.
[009] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие от около 0,5% до около 80,0% по массе оксалатной соли соединения (I) и ее сольвата, от около 10% до около 95% по массе разбавителя, от около 0,1% до около 10,0% по массе связующего вещества, от около 0,1% до около 20,0% по массе смазывающего вещества, от около 0,1% до около 30% по массе разрыхлителя и от около 0,05% до около 30% по массе стабилизирующего агента. В одном аспекте оксалатная соль соединения (I) и ее сольват представляет собой 2,5 оксалат тенелиглиптина или 3,0 оксалат тенелиглиптина и их сольват. В другом аспекте данного варианта реализации сольват представляет собой n. гидрат. В другом аспекте данного варианта реализации оксалатная соль соединения (I) и ее сольват представляет собой n. гидрат 2,5 оксалата тенелиглиптина или n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0.
[0010] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие от около 5% до около 40,0% по массе оксалатной соли соединения (I) и ее сольвата, от около 15% до около 95% по массе разбавителя, от около 0,1% до около 10% по массе связующего вещества, от около 0,1% до около 20,0% по массе смазывающего вещества, от около 0,1% до около 30% по массе разрыхлителя и от около 0,1% до около 20% по массе стабилизирующего агента. В одном аспекте оксалатная соль соединения (I) и ее сольват представляет собой 2,5 оксалат тенелиглиптина или 3,0 оксалат тенелиглиптина и их сольват. В другом аспекте данного варианта реализации сольват представляет собой n. гидрат. В другом аспекте данного варианта реализации оксалатная соль соединения (I) и ее сольват представляет собой n. гидрат 2,5 оксалата тенелиглиптина или n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0.
[0011] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие от около 5% до около 40,0% по массе оксалатной соли соединения (I) и ее сольвата, от около 30% до около 80% по массе разбавителя, от около 0,1% до около 10% по массе связующего вещества, от около 0,1% до около 20,0% по массе смазывающего вещества, от около 0,1% до около 30% по массе разрыхлителя и от около 0,1% до около 20% по массе стабилизирующего агента. В одном аспекте оксалатная соль соединения (I) и ее сольват представляет собой 2,5 оксалат тенелиглиптина или 3,0 оксалат тенелиглиптина и их сольват. В другом аспекте данного варианта реализации сольват представляет собой n. гидрат. В другом аспекте данного варианта реализации оксалатная соль соединения (I) и ее сольват представляет собой n. гидрат 2,5 оксалата тенелиглиптина или n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0.
[0012] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие от около 5% до около 15,0% по массе n. гидрата 3,0 оксалата тенелиглиптина, от около 30% до около 80% по массе разбавителя, от около 0,1% до около 10% по массе связующего вещества, от около 1,0% до около 15,0% по массе смазывающего вещества, от около 1,0% до около 20% по массе разрыхлителя и от около 0,5% до около 15% по массе стабилизирующего агента.
[0013] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие от около 0,5% до около 10,0% по массе n. гидрата 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, от около 5% до около 40% по массе разбавителя, от около 0,1% до около 10% по массе связующего вещества, от около 0,5% до около 5,0% по массе смазывающего вещества, от около 0,5% до около 10% по массе разрыхлителя и от около 0,1% до около 10% по массе стабилизирующего агента и один или более антидиабетических агентов.
[0014] В одном аспекте один или более антидиабетических агентов, содержащихся в фармацевтической композиции по данному изобретению, выбраны из группы, состоящей из соединений класса сульфонилмочевины и их солей, соединений класса глитазона и их солей, соединений класса бигуанидина и их солей, соединений класса ингибиторов альфа-глюкозидазы и их солей, соединений класса ингибиторов SGLT2 и их солей, и их комбинаций. В одном аспекте
[0015] В одном варианте реализации данного изобретения фармацевтические композиции содержат стабилизирующий агент, который представляет собой щавелевую кислоту, содержащуюся в количестве от около 0,5% до около 5,0% по массе.
[0016] В одном варианте реализации данного изобретения фармацевтические композиции содержат стабилизирующий агент, который представляет собой бета-циклодекстрин, содержащийся в количестве от около 0,5% до около 5,0% по массе.
[0017] В одном варианте реализации данного изобретения фармацевтические композиции содержат стабилизирующий агент, который представляет собой гидроксипропилцеллюлозу, содержащуюся в количестве от около 0,1% до около 5,0% по массе.
[0018] В одном варианте реализации данного изобретения фармацевтические композиции содержат стабилизирующий агент, который представляет собой ЭДТК, содержащуюся в количестве от около 0,5% до около 5,0% по массе.
[0019] В одном варианте реализации оксалатные соли соединения Формулы (I) в фармацевтической композиции по данному изобретению представляют собой n. гидрат 2,5 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, характеризующийся диаграммой рентгеновской порошковой дифракции, содержащей пики отражения при 5,68°, 6,56°, 16,44°, 17,72°, 18,34°, 21,12°, 21,67°, 23,15°, 23,86°, 24,99°±2Θ.
[0020] В одном варианте реализации оксалатные соли соединения Формулы (I) в фармацевтической композиции по данному изобретению представляют собой n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, характеризующийся диаграммой рентгеновской порошковой дифракции, содержащей пики отражения при 5,69°, 6,57°, 16,43°, 17,71°, 21,66°, 23,15°, 23,86°, 24,99°±2Θ.
[0021] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие оксалатные соли соединения Формулы (I).
[0022] В одном аспекте данного изобретения фармацевтические композиции указанных оксалатных солей соединения Формулы (I) и их сольватов, содержащихся в фармацевтической композиции по данному изобретению, являются по существу чистыми.
[0023] В одном варианте реализации данного изобретения предложена фармацевтическая композиция, содержащая оксалатную соль соединения формулы (I)
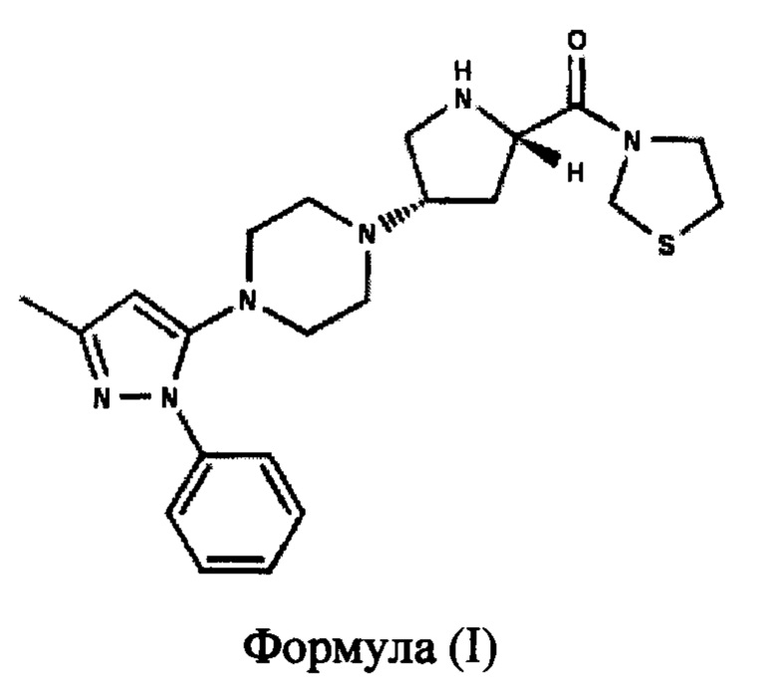
[0024] и ее сольват; и по меньшей мере один или более антидиабетических агентов, выбранных из группы, состоящей из соединений класса сульфонилмочевины и их солей, соединений класса глитазона и их солей, соединений класса бигуанида и их солей, соединений класса ингибиторов альфа-глюкозидазы и их солей, соединений класса ингибиторов SGLT2 и их солей, и их комбинаций. В одном аспекте данного варианта реализации фармацевтические композиции содержат соединения класса сульфонилмочевины, который включает глимепирид, глипирид, толбутамид, толазамид, глибенкламид, гликлазид и т.п. В другом аспекте данного варианта реализации фармацевтические композиции содержат соединения класса глитазона, который включает пиоглитазон, росиглитазон и т.п. В другом аспекте данного варианта реализации фармацевтические композиции содержат соединения класса бигуанида, который включает метформин, буформин, фенформин и т.п. или их фармацевтически приемлемые соли. В другом аспекте данного варианта реализации фармацевтические композиции содержат соединения класса ингибиторов альфа-глюкозидазы, который включает воглибозу, акарбозу, миглитол и т.п. В другом аспекте данного варианта реализации фармацевтические композиции содержат соединения класса ингибиторов SGLT2, который включает ремоглифлозин, дапаглифлозин, канаглифлозин, эмпаглифлозин, лузеоглифлозин и т.п., их соли, сложные эфиры или сольваты.
[0025] В одном варианте реализации данного изобретения предложена фармацевтическая композиция, содержащая птидрат 2,5 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, и метформин с пролонгированным высвобождением, причем мас./мас. отношение n. гидрата 2,5 оксалата тенелиглиптина к метформину находится в диапазоне 1:10-1:50.
[0026] В одном варианте реализации данного изобретения предложена фармацевтическая композиция, содержащая n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, и метформин, причем мас./мас. отношение n. гидрата 3,0 оксалата тенелиглиптина к метформину находится в диапазоне 1:10-1:50.
[0027] В одном варианте реализации данного изобретения предложена фармацевтическая композиция, содержащая смесь n. гидрата 2,5 оксалата тенелиглиптина и n. гидрата 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0; и метформин, причем мас./мас. отношение указанной смеси к метформину находится в диапазоне 1:10-1:50.
[0028] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие оксалатную соль соединения формулы (I) и ее сольват, причем указанная оксалатная соль имеет чистоту по меньшей мере 99%, а содержание соединения формулы (II) составляет менее 1,0%.
[0029] В одном аспекте данного изобретения предложены фармацевтические композиции, содержащие: (i) по меньшей мере одно из (а) оксалатных солей соединения Формулы (I) и их сольватов; (b) n. гидрата 2,5 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0; (с) 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0; (ii) по меньшей мере одно или более антидиабетических агентов, выбранных из группы, состоящей из соединений класса сульфонилмочевины и их солей, соединений класса глитазона и их солей, соединений класса бигуанида и их солей, соединений класса ингибиторов альфа-глюкозидазы и их солей, соединений класса ингибиторов SGLT2 и их солей, и их комбинаций; и (iii) по меньшей мере один или более фармацевтически приемлемых носителей, разбавителей и вспомогательных веществ.
[0030] В другом аспекте данного изобретения предложены фармацевтические композиции, содержащие (i) оксалатные соли соединения Формулы (I) и их сольваты; или (ii) n. гидрат 2,5 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0; или (iii) n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0; или (iv) n. гидрат 2.5 оксалата тенелиглиптина и n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0; или (v) любое из пп. (i)-(iv) и по меньшей мере один или более антидиабетических агентов, выбранных из группы, состоящей из соединений класса сульфонилмочевины и их солей, соединений класса глитазона и их солей, соединений класса бигуанида и их солей, соединений класса ингибиторов альфа-глюкозидазы и их солей, соединений класса ингибиторов SGLT2 и их солей, и их комбинаций, для применения при профилактическом или радикальном лечении нарушения метаболизма глюкозы у пациента.
[0031] В другом аспекте данного изобретения предложен способ профилактического или радикального лечения пациента с нарушением метаболизма глюкозы, включающий введение физиологически релевантного количества фармацевтических композиций, содержащих (i) оксалатные соли соединения Формулы (I) и их сольваты; или (ii) n. гидрат 2,5 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0; или (iii) n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0; или (iv) n. гидрат 2,5 оксалата тенелиглиптина и n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0; или (v) любое из пп. (i)-(iv) и по меньшей мере один или более антидиабетических агентов, выбранных из группы, состоящей из соединений класса сульфонилмочевины и их солей, соединений класса глитазона и их солей, соединений класса бигуанида и их солей, соединений класса ингибиторов альфа-глюкозидазы и их солей, соединений класса ингибиторов SGLT2 и их солей, и их комбинаций.
[0032] Изложенная сущность изобретения не предназначена для определения существенных признаков заявленного объекта изобретения, а также не предназначена для использования при определении или ограничении объема заявленного объекта изобретения.
ЗАДАЧИ ИЗОБРЕТЕНИЯ
[0033] Задача данного изобретения заключается в обеспечении фармацевтически приемлемых лекарственных форм, содержащих оксалатные соли тенелиглиптина и их сольваты, с превосходной технологичностью.
[0034] Задача данного изобретения заключается в обеспечении фармацевтически приемлемых лекарственных форм, содержащих оксалатные соли тенелиглиптина и их сольваты, с превосходной стабильностью.
[0035] Другая задача данного изобретения заключается в обеспечении фармацевтически приемлемых лекарственных форм, содержащих оксалатные соли тенелиглиптина и их сольваты и по меньшей мере один или более антидиабетических агентов, выбранных из группы, состоящей из соединений класса сульфонилмочевины и их солей, соединений класса глитазона и их солей, соединений класса бигуанида и их солей, соединений класса ингибиторов альфа-глюкозидазы и их солей, соединений класса ингибиторов SGLT2 и их солей, и их комбинаций, с превосходными характеристиками, такими как технологичность и стабильность.
[0036] Другая задача данного изобретения заключается в обеспечении фармацевтически приемлемых лекарственных форм, содержащих оксалатные соли тенелиглиптина и их сольваты, необязательно дополнительно содержащих по меньшей мере один или более антидиабетических агентов, выбранных из группы, состоящей из соединений класса сульфонилмочевины и их солей, соединений класса глитазона и их солей, соединений класса бигуанида и их солей, соединений класса ингибиторов альфа-глюкозидазы и их солей, соединений класса ингибиторов SGLT2 и их солей, и их комбинаций, подходящих при лечении или сдерживании развития нарушений метаболизма глюкозы у пациентов.
КРАТКОЕ ОПИСАНИЕ СОПРОВОЖДАЮЩИХ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[0037] Следующие графические материалы образуют часть данного описания и включены для дополнительной иллюстрации аспектов данного изобретения. Изобретение может быть более понятным со ссылкой на указанные графические материалы в сочетании с подробным описанием вариантов реализации, представленным в данном документе.
[0038] На Фиг. 1 изображена диаграмма рентгеновской порошковой дифракции кристаллического n. гидрата 2,5 оксалата тенелиглиптина, в соответствии с одним из вариантов реализации данного изобретения.
[0039] На Фиг. 2 изображена термограмма дифференциальной сканирующей калориметрии кристаллического n. гидрата 2,5 оксалата тенелиглиптина, в соответствии с одним из вариантов реализации данного изобретения.
[0040] На Фиг. 3 изображен ИК-спектр с Фурье-преобразованием кристаллического n. гидрата 2,5 оксалата тенелиглиптина, в соответствии с одним из вариантов реализации данного изобретения.
[0041] На Фиг. 4 изображена диаграмма рентгеновской порошковой дифракции кристаллического n. гидрата 3,0 оксалата тенелиглиптина, в соответствии с одним из вариантов реализации данного изобретения.
[0042] На Фиг. 5А-В изображена термограмма дифференциальной сканирующей калориметрии кристаллического n. гидрата 3,0 оксалата тенелиглиптина, в соответствии с одним из вариантов реализации данного изобретения.
[0043] На Фиг. 6 изображен ИК-спектр с Фурье-преобразованием кристаллического n. гидрата 3,0 оксалата тенелиглиптина, в соответствии с одним из вариантов реализации данного изобретения.
ПОДРОБНОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
[0044] Специалистам в данной области техники понятно, что изобретение, описанное в данном документе, допускает изменения и модификации, отличные от тех, которые конкретно описаны. Следует понимать, что изобретение, описанное в данном документе, включает все такие изменения и модификации. Данное изобретение также включает все стадии, характеристики, композиции и способы, упомянутые или указанные в данном описании, отдельно или в совокупности, и любые и все комбинации любых двух или более из указанных стадий или характеристик.
Определения
[0045] Для удобства, перед дальнейшем описанием данного изобретения, здесь собраны некоторые термины, используемые в описании и примерах. Указанные определения следует читать в свете остальной части описания и понимать так, как это понимают специалисты в данной области техники. Если не указано иное, все технические и научные термины, используемые в данном документе, имеют такое же значение, какое обычно понимается специалистами в данной области техники. Термины, используемые в данном описании, определены следующим образом, при отсутствии иного ограничения в конкретных случаях.
[0046] Ниже представлено определение терминов, использованных в данном документе. Если определение, указанное в данной заявке, и определение, указанное позже в заявлении приоритета обычной заявки на основании данной предварительной заявки, противоречат, то при определении значения терминов следует руководствоваться определением, данным в обычной заявке.
[0047] Термин «сольват» означает агрегат, состоящий из иона или молекулы растворенного вещества и одной или более молекул растворителя. Сольваты могут представлять собой, но не ограничиваются ими, сольват с ацетоном, сольват с этанолом, сольват с метанолом, сольват с бутанолом, сольват с ТВА, сольват с хлороформом и другие органические и неорганические сольваты.
[0048] Термин «гидрат» означает соединение, обычно кристаллическое, в котором одна или более молекул воды химически связаны с другим соединением, или молекулой, или элементом.
[0049] В данном описании и формуле изобретения формы единственного числа включают ссылку на множественное число, если из контекста очевидно не следует иное.
[0050] Данное описание не ограничивается объемом конкретных вариантов реализации, описанных в данном документе, которые предназначены лишь для целей иллюстрации.
[0051] Термин «соль» или «фармацевтически приемлемая соль» в данном контексте означает соли, которые с медицинской точки зрения подходят для применения в контакте с тканями человека и низших животных без чрезмерной токсичности, раздражения и аллергической реакции, соразмерно с разумным соотношением польза/риск, и эффективны для предполагаемого применения.
[0052] Термин «кристаллический» в данном контексте означает имеющий периодически повторяющееся расположение молекул или плоскостей наружных поверхностей.
[0053] Термин «аморфный» в данном контексте означает по существу не имеющий периодически повторяющегося расположения молекул или плоскостей наружных поверхностей.
[0054] Если не указано иное, проценты, указанные в данном описании, представляют собой проценты масса/масса (мас./мас).
[0055] Термин «стабилизирующие агенты» в данном контексте означает фармацевтически приемлемое вспомогательное вещество, которое стабилизирует фармацевтическую композицию и ограничивает или предотвращает химическое разложение активного фармацевтического ингредиента, содержащегося в указанной композиции.
[0056] Термин «терапевтически эффективное количество» означает такое количество оксалатной соли соединения Формулы (I) или ее сольвата, которое вызывает биологический ответ в ткани пациента
[0057] Термин «профилактическое» в контексте лечения означает такое количество оксалатной соли соединения Формулы (I) или ее сольвата, которое предотвращает или снижает вероятность возникновения нарушения метаболизма глюкозы у пациента или появления клинических симптомов нарушения метаболизма глюкозы у пациента.
[0058] Термин «радикальное» в контексте лечения означает такое количество оксалатной соли соединения Формулы (I) или ее сольвата, которое лечит или сдерживает развитие нарушения метаболизма глюкозы у пациента.
[0059] Термин «метформин» в данном контексте, если не указано иное, означает метформин, его фармацевтически приемлемую соль или гидрат.
[0060] Термин «вспомогательные вещества» относится, в целом, к веществам, отличным от фармацевтически активных ингредиентов, которые участвуют в производственном процессе или содержатся в готовой лекарственной форме фармацевтического продукта.
[0061] Термин «носители» относится, в целом, к любому веществу или субстрату, используемому в процессе доставки лекарства, которое служит для улучшения селективности, эффективности и/или безопасности введения лекарства.
[0062] Термин «нарушение метаболизма глюкозы» включает различные метаболические расстройства с участием глюкозы у людей, такие как сахарный диабет, гипергликемия, гипогликемия, гликозурия и т.п. Кроме того, сахарный диабет включает сахарный диабет I типа и II типа.
[0063] Термин «разбавители» относится, в целом, к наполнителям/разбавителям, которые можно использовать для увеличения насыпного объема или улучшения характеристик текучести.
[0064] 3-{(2S,4S)-4-[4-(3-метил-1-фенил-1Н-пиразол-5-ил)пиперазин-1-ил]пирролидин-2-илкарбонил}тиазолидин, также известный как тенелиглиптин, представлен Формулой (I), и взаимозаменяемо упоминается в данном описании как тенелиглиптин или соединение Формулы (I).
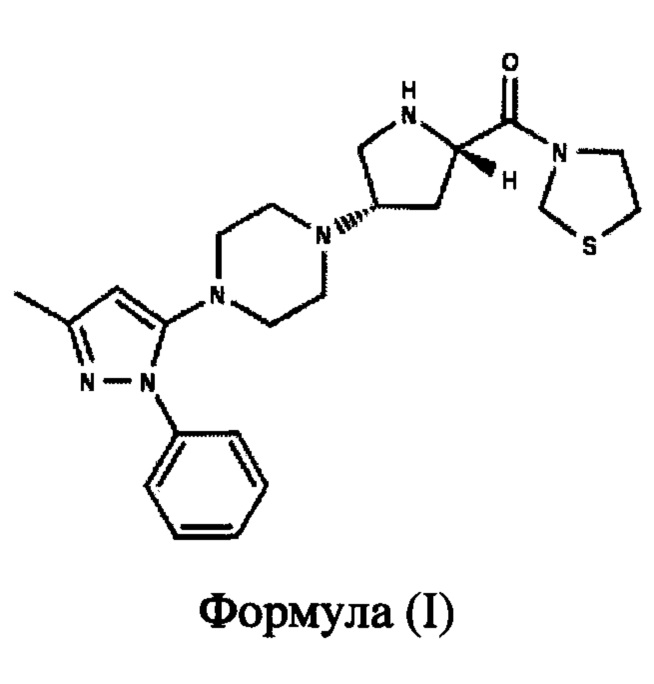
[0065] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие оксалатные соли соединения Формулы (I).
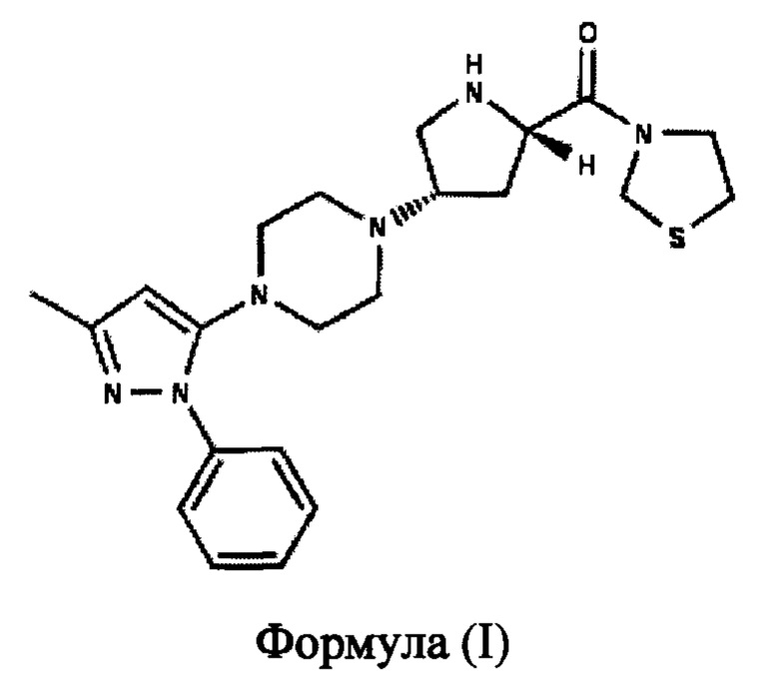
или их сольваты и по меньшей мере один или более фармацевтически приемлемых носителей, разбавителей, связующих веществ, смазывающих веществ, разрыхлителей и стабилизирующих агентов. В одном варианте реализации указанный сольват предпочтительно представляет собой n. гидрат, где n равен от 1,0 до 4,0. В предпочтительном варианте реализации n равен 1,0. В одном аспекте данного варианта реализации разбавитель выбран из группы, состоящей из маннита, сорбита, ксилита, крахмала, лактозы, целлюлозы, дигидрофосфата кальция и т.п., предпочтительно маннита или лактозы.В другом аспекте связующее вещество выбрано из группы, состоящей из гидроксипропилцеллюлозы, поливинилового спирта, повидона, коповидона, этилцеллюлозы, гипромеллозы и т.п., предпочтительно гипромеллозы или гидроксипропилцеллюлозы. В другом аспекте данного варианта реализации смазывающее вещество представляет собой глицерилдибегенат, стеарилфумарат натрия или кальция, стеарат магния, стеариновую кислоту, глицерилпальмитостеарат и т.п., предпочтительно глицерилдибегенат. В другом аспекте данного варианта реализации разрыхлитель выбран из группы, состоящей из гидроксипропилцеллюлозы с низкой степенью замещения, кросповидона, кроскармеллозы натрия, крахмалгликолята натрия и т.п., предпочтительно гидроксипропилцеллюлозы с низкой степенью замещения. В другом аспекте данного варианта реализации стабилизирующий агент выбран из по меньшей мере одного стабилизатора; по меньшей мере одного комплексообразующего агента; по меньшей мере одного полимера; по меньшей мере одного хелатообразующего агента; и их комбинаций.
[0066] В одном варианте реализации фармацевтическая композиция содержит n. гидрат 2,5 оксалата тенелиглиптина, где n равен от 1,0 до 4,0. В предпочтительном варианте реализации фармацевтическая композиция содержит 1,0 гидрат 2,5 оксалата тенелиглиптина.
[0067] В другом варианте реализации фармацевтическая композиция содержит n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0. В предпочтительном варианте реализации фармацевтическая композиция содержит 1,0 гидрат 3,0 оксалата тенелиглиптина.
[0068] В другом варианте реализации фармацевтическая композиция содержит n. гидрат 2,5 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, и n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0. В предпочтительном варианте реализации фармацевтическая композиция моногидрат 2,5 оксалата тенилиглиптина и моногидрат 3,0 оксалата тенилиглиптина.
[0069] В одном варианте реализации сольватированная оксалатная соль тенелиглиптина, содержащаяся в фармацевтической композиции, имеет чистоту 10-100%. В другом варианте реализации степень чистоты составляет 20-100%. В другом варианте реализации чистота составляет 30-100%. В другом варианте реализации чистота составляет 40-100%. В другом варианте реализации чистота составляет 50-100%. В другом варианте реализации чистота составляет 60-100%. В другом варианте реализации чистота составляет 70-100%. В другом варианте реализации чистота составляет 80-100%. В другом варианте реализации чистота составляет 90-100%. В предпочтительном варианте реализации чистота составляет более 99%. В более предпочтительном варианте реализации чистота составляет более 99,5%. В одном варианте реализации сольватированная оксалатная соль тенелиглиптина, содержащаяся в фармацевтической композиции, является по существу чистой.
[0070] В одном варианте реализации n. гидрат 2,5 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, содержащийся в фармацевтической композиции, имеет чистоту 10-100%. В другом варианте реализации степень чистоты составляет 20-100%. В другом варианте реализации чистота составляет 30-100%. В другом варианте реализации чистота составляет 40-100%. В другом варианте реализации чистота составляет 50-100%. В другом варианте реализации чистота составляет 60-100%. В другом варианте реализации чистота составляет 70-100%. В другом варианте реализации чистота составляет 80-100%. В другом варианте реализации чистота составляет 90-100%. В предпочтительном варианте реализации чистота составляет более 99%. В более предпочтительном варианте реализации чистота составляет более 99,5%. В одном варианте реализации n. гидрат 2,5 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, содержащийся в фармацевтической композиции, является по существу чистым.
[0071] В одном варианте реализации n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, содержащийся в фармацевтической композиции, имеет чистоту 10-100%. В другом варианте реализации степень чистоты составляет 20-100%. В другом варианте реализации чистота составляет 30-100%. В другом варианте реализации чистота составляет 40-100%. В другом варианте реализации чистота составляет 50-100%. В другом варианте реализации чистота составляет 60-100%. В другом варианте реализации чистота составляет 70-100%. В другом варианте реализации чистота составляет 80-100%. В другом варианте реализации чистота составляет 90-100%. В предпочтительном варианте реализации чистота составляет более 99%. В более предпочтительном варианте реализации чистота составляет более 99,5%. В одном варианте реализации агидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, содержащийся в фармацевтической композиции, является по существу чистым.
[0072] n. Гидрат 2,5 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, содержащийся в фармацевтических композициях, описанных в данном документе, существует в кристаллической форме.
[0073] n. Гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, содержащийся в фармацевтических композициях, описанных в данном документе, существует в кристаллической форме.
[0074] n. Гидрат 2,5 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, содержащийся в фармацевтических композициях, описанных в данном документе, существует в аморфной форме.
[0075] n. Гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, содержащийся в фармацевтических композициях, описанных в данном документе, существует в аморфной форме.
[0076] В одном варианте реализации данного изобретения предложены фармацевтические композиции, описанные в данном документе, в которых n. гидрат 2,5 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, характеризуется диаграммой рентгеновской порошковой дифракции, содержащей пики отражения при 5,68°, 6,56°, 16,44°, 17,72°, 18,34°, 21,12°, 21,67°, 23,15°, 23,86°, 24,99°±2Θ, и имеет диаграмму рентгеновской порошковой дифракции, представленную на Фиг. 1.
[0077] В одном варианте реализации данного изобретения предложены фармацевтические композиции, описанные в данном документе, в которых n. гидрат 2,5 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, характеризуется термограммой дифференциальной сканирующей калориметрии (ДСК) с эндотермой при 152,76°С и 169,68°С, и представленной кривой ДСК на Фиг. 2.
[0078] В одном варианте реализации данного изобретения предложены фармацевтические композиции, описанные в данном документе, в которых n. гидрат 2,5 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, характеризуется пиками инфракрасного поглощения (ИК) при 3452,22, 3011,77, 2540,88, 1721,37, 1650,04, 1207,43, 922,34, 708,96, 477,35 см-1, и представленными на Фиг. 3.
[0079] В одном варианте реализации данного изобретения предложены фармацевтические композиции, описанные в данном документе, в которых n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, характеризуется диаграммой рентгеновской порошковой дифракции, содержащей пики отражения при 5,69°, 6,57°, 16,43°, 17,71°, 21,66°, 23,15°, 23,86°, 24,99°±2Θ, и имеет диаграмму рентгеновской порошковой дифракции, представленную на Фиг. 4.
[0080] В одном варианте реализации данного изобретения предложены фармацевтические композиции, описанные в данном документе, в которых n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, характеризуется термограммой дифференциальной сканирующей калориметрии (ДСК) с эндотермой при 177,34°С, и представленной кривой ДСК на Фиг. 5А, и при 171,6°С, как показано на Фиг. 5В.
[0081] В одном варианте реализации данного изобретения предложены фармацевтические композиции, описанные в данном документе, в которых n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, характеризуется пиками инфракрасного поглощения (ИК) при 3464,93, 3011,34, 2537,55, 1911,30, 1720,10, 1651,64, 1456,82, 1363,34, 1209,29, 922,88, 709,74, 475,21 см-1, и представленными на Фиг. 6.
[0082] В одном варианте реализации предложены фармацевтические композиции, содержащие n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, и по меньшей мере один или более фармацевтически приемлемых носителей, разбавителей и вспомогательных веществ. В одном предпочтительном варианте реализации n равен 1,0.
[0083] В одном конкретном варианте реализации предложены фармацевтические композиции, содержащие n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, причем указанная соль существует в кристаллической или аморфной форме.
[0084] В одном варианте реализации предложены фармацевтические композиции, содержащие n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, характеризующийся диаграммой рентгеновской порошковой дифракции, содержащей пики отражения при 5,69°, 6,57°, 16,43°, 17,71°, 21,66°, 23,15°, 23,86°, 24,99°±2Θ, и имеющий диаграмму рентгеновской порошковой дифракции, представленную на Фиг. 4.
[0085] В другом варианте реализации предложены фармацевтические композиции, содержащие n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, который является по существу чистым.
[0086] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие n. гидрат 2,5 оксалата тенелиглиптина и n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, и по меньшей мере один или более фармацевтически приемлемых носителей, разбавителей и вспомогательных веществ. В предпочтительном аспекте данного варианта реализации n равен 1,0. В предпочтительном аспекте данного варианта реализации n. гидрат 2,5 оксалата тенелиглиптина и n. гидрат 3,0 оксалата тенелиглиптина являются по существу чистыми.
[0087] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие оксалатные соли соединения Формулы (I), которые содержат
a. по меньшей мере один стабилизатор;
b. по меньшей мере один комплексообразующий агент;
c. по меньшей мере один полимер;
d. по меньшей мере один хелатообразующий агент; и
e. их комбинации.
[0088] В предпочтительном варианте реализации указанные фармацевтические композиции дополнительно содержат по меньшей мере один стабилизатор, который представляет собой фармацевтически приемлемую органическую кислоту, выбранную из группы, состоящей из щавелевой кислоты, лимонной кислоты, винной кислоты. В более предпочтительном варианте реализации стабилизатор представляет собой щавелевую кислоту.
[0089] В предпочтительном варианте реализации указанные фармацевтические композиции дополнительно содержат по меньшей мере один комплексообразующий агент, выбранный из группы, состоящей из альфа-циклодекстрина, бета-циклодекстрина, гамма-циклодекстрина, метил-бета-циклодекстрина, гидроксипропил-бета-циклодекстрина, их производных и их комбинаций.
[0090] В более предпочтительном варианте реализации комплексообразующий агент представляет собой гидроксипропил-бета-циклодекстрин.
[0091] В предпочтительном варианте реализации указанные фармацевтические композиции дополнительно содержат по меньшей мере один полимер, выбранный из группы, состоящей из желатина, поливинилового спирта, коповидона, гидроксипропилцеллюлозы, этилцеллюлозы, поливинилпирролидона, гидроксипропилметилцеллюлозы и их комбинаций. В более предпочтительном варианте реализации указанный полимер представляет собой гидроксипропилцеллюлозу.
[0092] В одном варианте реализации указанные фармацевтические композиции дополнительно содержат по меньшей мере один хелатообразующий агент, выбранный из группы, состоящей из ЭТДК, сульфата цинка, аскорбата железа (II), карбоната кальция, хлорида натрия, хлорида калия и их комбинаций. В более предпочтительном варианте реализации хелатообразующий агент представляет собой ЭДТК.
[0093] В одном варианте реализации указанные фармацевтические композиции дополнительно содержат стабилизатор и по меньшей мере один полимер. Указанный стабилизатор представляет собой щавелевую кислоту. Указанный полимер выбран низ группы, состоящей из желатина, поливинилового спирта, коповидона, гидроксипропилцеллюлозы, этилцеллюлозы, поливинилпирролидона, гидроксипропилметилцеллюлозы и их комбинаций, предпочтительно гидроксипропилцеллюлозы.
[0094] В предпочтительном варианте реализации указанные фармацевтические композиции дополнительно содержат по меньшей мере один стабилизатор, по меньшей мере один полимер и по меньшей мере один комплексообразующий агент. В одном варианте реализации указанный стабилизатор представляет собой щавелевую кислоту. В другом варианте реализации указанный полимер выбран низ группы, состоящей из желатина, поливинилового спирта, коповидона, гидроксипропилцеллюлозы, этилцеллюлозы, поливинилпирролидона, гидроксипропилметилцеллюлозы и их комбинаций, предпочтительно гидроксипропилцеллюлозы. В одном варианте реализации указанный комплексообразующий агент выбран из группы, состоящей из бета-циклодекстрина, гидроксипропил-бета-циклодекстрина и их комбинаций, предпочтительно гидроксипропил-бета-циклодекстрина.
[0095] В предпочтительном варианте реализации фармацевтические композиции по данному изобретению дополнительно содержат по меньшей мере один полимер и по меньшей мере один хелатообразующий агент. В одном варианте реализации указанный полимер выбран низ группы, состоящей из желатина, поливинилового спирта, коповидона, гидроксипропилцеллюлозы, этилцеллюлозы, поливинилпирролидона, гидроксипропилметилцеллюлозы и их комбинаций, предпочтительно гидроксипропилцеллюлозы. В другом варианте реализации указанный хелатообразующий агент выбран из группы, состоящей из ЭТДК, сульфата цинка, аскорбата железа (II), карбоната кальция, хлорида натрия, хлорида калия и их комбинаций, предпочтительно ЭДТК.
[0096] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие
(a) оксалатную соль соединения (I) и ее сольват, выбранный из 2,5 оксалата тенелиглиптина или 3,0 оксалата тенелиглиптина и их сольватов
(b) разбавитель, выбранный из маннита или лактозы
(c) связующее вещество, выбранное из гидроксипропилцеллюлозы или гипромеллозы
(d) смазывающее вещество, выбранное из глицерилдибегената или стеарата магния
(e) разрыхлитель, выбранный из гидроксипропилцеллюлозы с низкой степенью замещения, кросповидона, кроскармеллозы натрия
[0097] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие
(a) оксалатную соль соединения (I) и ее сольват, представляющий собой n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0
(b) разбавитель, представляющий собой маннит
(c) связующее вещество, представляющее собой гипромеллозу
(d) смазывающее вещество, представляющее собой глицерилдибегенат
(e) разрыхлитель, представляющий собой гидроксипропилцеллюлозу с низкой степенью замещения
(f) стабилизирующий агент, выбранный из щавелевой кислоты, бета-циклодекстрина, гидроксипропилцеллюлозы, ЭДТК и их комбинаций.
[0098] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие
(a) оксалатную соль соединения (I) и ее сольват, представляющий собой n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0
(b) разбавитель, представляющий собой лактозу
(c) связующее вещество, представляющее собой гипромеллозу
(d) смазывающее вещество, представляющее собой глицерилдибегенат
(e) разрыхлитель, представляющий собой гидроксипропилцеллюлозу с низкой степенью замещения
(f) стабилизирующий агент, выбранный из щавелевой кислоты, бета-циклодекстрина, гидроксипропилцеллюлозы, ЭДТК и их комбинаций.
[0099] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие от около 0,5% до около 80,0% по массе оксалатной соли соединения (I) и ее сольвата, от около 10% до около 95% по массе разбавителя, от около 0,1% до около 10,0% по массе связующего вещества, от около 0,1% до около 20,0% по массе смазывающего вещества, от около 0,1% до около 30% по массе разрыхлителя и от около 0,05% до около 30% по массе стабилизирующего агента.
[00100] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие от около 5% до около 40,0% по массе оксалатной соли соединения (I) и ее сольвата, от около 15% до около 95% по массе разбавителя, от около 0,1% до около 10% по массе связующего вещества, от около 0,1% до около 20,0% по массе смазывающего вещества, от около 0,1% до около 30% по массе разрыхлителя и от около 0,1% до около 20% по массе стабилизирующего агента.
[00101] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие от около 5% до около 40,0% по массе оксалатной соли соединения (I) и ее сольвата, от около 30% до около 80% по массе разбавителя, от около 0,1% до около 10% по массе связующего вещества, от около 0,1% до около 20,0% по массе смазывающего вещества, от около 0,1% до около 30% по массе разрыхлителя и от около 0,1% до около 20% по массе стабилизирующего агента.
[00102] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие от около 5% до около 15,0% по массе n. гидрата 3,0 оксалата тенелиглиптина, от около 30% до около 80% по массе разбавителя, от около 0,1% до около 10% по массе связующего вещества, от около 1,0% до около 15,0% по массе смазывающего вещества, от около 1,0% до около 20% по массе разрыхлителя и от около 0,5% до около 15% по массе стабилизирующего агента. В одном аспекте данного варианта реализации n. гидрат 3,0 оксалата тенелиглиптина представляет собой кристаллический n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0.
[00103] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие от около 0,5% до около 10,0% по массе n. гидрата 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, от около 5% до около 40% по массе разбавителя, от около 0,1% до около 10% по массе связующего вещества, от около 0,5% до около 5,0% по массе смазывающего вещества, от около 0,5% до около 10% по массе разрыхлителя и от около 0,1% до около 10% по массе стабилизирующего агента и один или более антидиабетических агентов. В одном аспекте данного варианта реализации n. гидрат 3,0 оксалата тенелиглиптина представляет собой кристаллический n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0.
[00104] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие по существу чистую оксалатную соль соединения формулы (I) и ее сольваты.
[00105] В одном варианте реализации данного изобретения предложены фармацевтические композиции, в которых чистота оксалатной соли соединения формулы (I) составляет более 98,0%.
[00106] В другом варианте реализации данного изобретения предложены фармацевтические композиции, в которых чистота оксалатной соли соединения формулы (I) составляет более 99,0%.
[00107] В одном варианте реализации данного изобретения предложены фармацевтические композиции, в которых чистота оксалатной соли соединения формулы (I) составляет более 99,5%.
[00108] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие по существу чистую оксалатную соль соединения формулы (I) и ее сольваты, причем указанная оксалатная соль соединения формулы (I) представляет собой 2,5 оксалат тенелиглиптина или 3,0 оксалат тенелиглиптина и их сольваты.
[00109] В одном варианте реализации данного изобретения также предложены фармацевтические композиции, описанные в данном документе, дополнительно содержащие по меньшей мере один или более антидиабетических агентов, выбранных из группы, состоящей из соединений класса сульфонилмочевины и их солей, соединений класса глитазона и их солей, соединений класса бигуанидина и их солей, соединений класса ингибиторов альфа-глюкозидазы и их солей, соединений класса ингибиторов SGLT2 и их солей, и их комбинаций.
[00110] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие оксалатную соль соединения формулы (I) и ее сольваты и по меньшей мере один или более антидиабетических агентов, выбранных из группы, состоящей из соединений класса сульфонилмочевины и их солей, соединений класса глитазона и их солей, соединений класса бигуанида и их солей, соединений класса ингибиторов альфа-глюкозидазы и их солей, соединений класса ингибиторов SGLT2 и их солей, и их комбинаций.
[00111] В одном варианте реализации указанные соединения класса сульфонилмочевины, используемые в фармацевтических композициях по данному изобретению, включают глимепирид, глипирид, толбутамид, толазамид, глибенкламид, гликлазид и т.п. В предпочтительном варианте реализации сульфонилмочевинное соединение представляет собой глимепирид.
[00112] В одном варианте реализации указанные соединения класса глитазона, используемые в фармацевтических композициях по данному изобретению, включают пиоглитазон, росиглитазон и т.п. В предпочтительном варианте реализации глитазоновое соединение представляет собой пиоглитазон.
[00113] В другом варианте реализации указанные соединения класса ингибиторов альфа-глюкозидазы, используемые в фармацевтических композициях по данному изобретению, включают воглибозу, акарбозу, миглитол и т.п. В предпочтительном варианте реализации ингибитор альфа-глюкозидазы представляет собой воглибозу.
[00114] В одном варианте реализации указанные соединения класса ингибиторов SGLT2 включают ремоглифлозин, дапаглифлозин, канатлифлозин, эмпаглифлозин, лузеоглифлозин и т.п.
[00115] В одном варианте реализации указанные соединения класса бигуанида включают метформин, буформин, фенформин и т.п. В предпочтительном варианте реализации указанный член молекул класса бигуанидов представляет собой метформин или его фармацевтически приемлемую соль. В предпочтительном варианте реализации указанный член класса бигуанида представляет собой гидрохлорид метформина. В другом варианте реализации указанный класс бигуанида представляет собой смесь метформина и гидрохлорида метформина.
[00116] В одном варианте реализации метформиновая часть фармацевтической композиции по данному изобретению представляет собой слой с мгновенным высвобождением или слой с пролонгированным высвобождением. В одном варианте реализации метформиновая часть, содержащаяся в указанных фармацевтических композициях, представляет собой слой с мгновенным высвобождением. В предпочтительном варианте реализации метформиновая часть, содержащаяся в указанных фармацевтических композициях, представляет собой слой с пролонгированным высвобождением. В другом варианте реализации метформин, содержащийся в указанный фармацевтических композициях, представляет собой смесь слоев метформина с мгновенным и пролонгированным высвобождением.
[00117] В одном варианте реализации фармацевтические композиции, описанные в данном документе, дополнительно содержат по меньшей мере один стабилизатор, по меньшей мере один комплексообразующий агент, по меньшей мере один полимер, по меньшей мере один хелатообразующий агент и их комбинации.
[00118] Фармацевтические композиции по данному изобретению, содержащие по меньшей мере один стабилизатор, по меньшей мере один комплексообразующий агент, по меньшей мере один полимер, по меньшей мере один хелатообразующий агент или их комбинации, стабилизируют сольватированные оксалатные соли тенелиглиптина и ингибируют образование соединения Формулы (II) в указанных фармацевтических композициях.
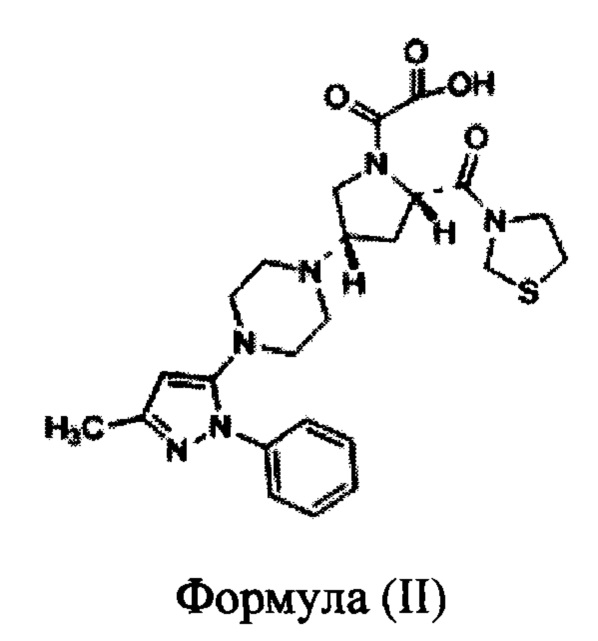
[00119] В одном варианте реализации предложены фармацевтические композиции, содержащие по меньшей мере один стабилизатор, по меньшей мере один комплексообразующий агент, по меньшей мере один полимер, по меньшей мере один хелатообразующий агент и их комбинации, действуют для стабилизации n. гидрата 2,5 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0.
[00120] В одном варианте реализации предложены фармацевтические композиции, содержащие по меньшей мере один стабилизатор, по меньшей мере один комплексообразующий агент, по меньшей мере один полимер, по меньшей мере один хелатообразующий агент и их комбинации, действуют для стабилизации n. гидрата 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0.
[00121] В одном варианте реализации предложены фармацевтические композиции, содержащие по меньшей мере один стабилизатор, по меньшей мере один комплексообразующий агент, по меньшей мере один полимер, по меньшей мере один хелатообразующий агент и их комбинации, действуют для стабилизации смеси n. гидрата 2,5 оксалата тенелиглиптина и n. гидрата 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0.
[00122] В одном варианте реализации предложены фармацевтические композиции, содержащие оксалатную соль соединения формулы (I) и ее сольват, причем указанная оксалатная соль имеет чистоту по меньшей мере 99%, а содержание соединения формулы (II) составляет менее 1,0%.
[00123] В одном варианте реализации предложены фармацевтические композиции, содержащие оксалатную соль соединения формулы (I) и ее сольват, причем указанная оксалатная соль имеет чистоту по меньшей мере 99,5%, а содержание соединения формулы (II) составляет менее 0,5%.
[00124] В одном варианте реализации предложены фармацевтические композиции, содержащие оксалатную соль соединения формулы (I) и ее сольват, причем указанная оксалатная соль имеет чистоту по меньшей мере 99,9%, а содержание соединения формулы (II) составляет менее 0,1%.
[00125] В одном варианте реализации предложены фармацевтические композиции, содержащие 2,5 оксалат тенелиглиптина и его сольват, причем указанная оксалатная соль имеет чистоту по меньшей мере 99%, а содержание соединения формулы (II) составляет менее 1,0%.
[00126] В одном варианте реализации предложены фармацевтические композиции, содержащие 2,5 оксалат тенелиглиптина и его сольват, причем указанная оксалатная соль имеет чистоту по меньшей мере 99,5%, а содержание соединения формулы (II) составляет менее 0,5%. В предпочтительном варианте реализации сольват представляет собой n. гидрат. В другом аспекте данного варианта реализации предложены фармацевтические композиции, содержащие n. гидрат 2,5 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0.
[00127] В одном варианте реализации предложены фармацевтические композиции, содержащие 2,5 оксалат тенелиглиптина и его сольват, причем указанная оксалатная соль имеет чистоту по меньшей мере 99,9%, а содержание примеси В составляет менее 0,1%. В предпочтительном варианте реализации сольват представляет собой n. гидрат. В другом аспекте данного варианта реализации предложены фармацевтические композиции, содержащие n. гидрат 2,5 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0.
[00128] В одном варианте реализации предложены фармацевтические композиции, содержащие 3,0 оксалат тенелиглиптина и его сольват, причем указанная оксалатная соль имеет чистоту по меньшей мере 99%, а содержание соединения формулы (II) составляет менее 1,0%. В предпочтительном варианте реализации сольват представляет собой n. гидрат. В другом аспекте данного варианта реализации предложены фармацевтические композиции, содержащие n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0.
[00129] В одном варианте реализации предложены фармацевтические композиции, содержащие 3,0 оксалат тенелиглиптина и его сольват, причем указанная оксалатная соль имеет чистоту по меньшей мере 99,5%, а содержание примеси В составляет менее 0,5%. В предпочтительном варианте реализации сольват представляет собой n. гидрат. В другом аспекте данного варианта реализации предложены фармацевтические композиции, содержащие n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0.
[00130] В одном варианте реализации предложены фармацевтические композиции, содержащие 3,0 оксалат тенелиглиптина и его сольват, причем указанная оксалатная соль имеет чистоту по меньшей мере 99,9%, а содержание примеси В составляет менее 0,1%. В предпочтительном варианте реализации сольват представляет собой n. гидрат. В другом аспекте данного варианта реализации предложены фармацевтические композиции, содержащие n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0.
[00131] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие n. гидрат 3,0 оксалата тенелиглиптина и его сольват, причем указанная оксалатная соль имеет чистоту по меньшей мере 99%, а содержание соединения формулы (II) составляет менее 1,0%.
[00132] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие n. гидрат 3,0 оксалата тенелиглиптина и его сольват, причем указанная оксалатная соль имеет чистоту по меньшей мере 99,5%, а содержание соединения формулы (II) составляет менее 0,5%.
[00133] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие n. гидрат 3,0 оксалата тенелиглиптина и его сольват, причем указанная оксалатная соль имеет чистоту по меньшей мере 99,9%, а содержание соединения формулы (II) составляет менее 0,1%.
[00134] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие n. гидрат 3,0 оксалата тенелиглиптина, имеющего чистоту по меньшей мере 99,0%, по меньшей мере 99,5%, по меньшей мере 99,9%, в кристаллической форме.
[00135] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, и метформин с пролонгированным высвобождением, в которых мас./мас. отношение тенелиглиптина к метформину находится в диапазоне 1:10-1:50, предпочтительно в диапазоне 1:10-1:40, в частности, около 1:15 или 1:31.
[00136] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие n. гидрат 2,5 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, и метформин с пролонгированным высвобождением, в которых мас/мас. отношение тенелиглиптина к метформину находится в диапазоне 1:10-1:50, предпочтительно в диапазоне 1:10-1:40, в частности, около 1:15 или 1:31.
[00137] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие смесь n. гидрата 2,5 оксалата тенелиглиптина и n. гидрата 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, и метформин с пролонгированным высвобождением, в которых мас/мас. отношение тенелиглиптина к метформину находится в диапазоне около 1:10-1:50, предпочтительно в диапазоне около 1:10-1:40, в частности, около 1:15 или 1:31.
[00138] В конкретном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие n. гидрат 2,5 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, и метформин с пролонгированным высвобождением, и по меньшей мере один или более фармацевтически приемлемых носителей, разбавителей и вспомогательных веществ.
[00139] В конкретном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, и метформин с пролонгированным высвобождением, и по меньшей мере один или более фармацевтически приемлемых носителей, разбавителей и вспомогательных веществ.
[00140] В конкретном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие смесь n. гидрата 2,5 оксалата тенелиглиптина и n. гидрата 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, и метформин с пролонгированным высвобождением, и по меньшей мере один или более фармацевтически приемлемых носителей, разбавителей и вспомогательных веществ.
[00141] В данном изобретении предложены фармацевтические композиции, описанные в данном документе, для применения при профилактическом лечении нарушения метаболизма глюкозы у пациента.
[00142] В данном изобретении предложены фармацевтические композиции, описанные в данном документе, для применения при радикальном лечении нарушения метаболизма глюкозы у пациента.
[00143] В данном изобретении предложен способ профилактического и радикального лечения пациента с нарушением метаболизма глюкозы, включающий введение физиологически релевантного количества фармацевтических композиций, описанных в данном документе.
[00144] В данном изобретении предложен способ радикального лечения пациента с нарушением метаболизма глюкозы, включающий введение физиологически релевантного количества фармацевтических композиций, описанных в данном документе.
[00145] В одном варианте реализации данного изобретения предложены фармацевтические композиции, описанные в данном документе, содержащие гранулы n. гидрата оксалатных солей тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0. В конкретном варианте реализации предложены фармацевтические композиции, описанные в данном документе, содержащие гранулы n. гидрата 2,5 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0. В конкретном варианте реализации предложены фармацевтические композиции, описанные в данном документе, содержащие гранулы n. гидрата 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0.
[00146] В одном варианте реализации данного изобретения предложен способ получения фармацевтической композиции оксалатной соли соединения формулы (I), включающий стадии:
(a) просеивания оксалатной соли соединения формулы (I) с фармацевтически приемлемыми вспомогательными веществами или одним или более антидиабетическими агентами или их смесью;
(b) гранулирования просеянного материала, полученного на стадии (а), с раствором связующего вещества;
(c) сушки и просеивания гранулята, полученного на стадии (b);
(d) смазывания просеянного гранулята, полученного на стадии (с), подходящим смазывающим агентом с получением смеси;
(e) прессования смазанной смеси, полученной на стадии (d), с получением таблетки, или наполнения капсул смесью, полученной на стадии (d);
(f) необязательно прессования смазанной смеси, полученной на стадии (d), со смесью одного или более антидиабетических агентов с получением таблетки, или наполнения капсул указанной смесью.
Стадия (а) описанного выше способа включает просеивание оксалатной соли соединения формулы (I) и ее сольвата с подходящими вспомогательными веществами. В одном варианте реализации оксалатная соль соединения формулы (I) и ее сольват представляет собой 2,5 оксалат тенелиглиптина или 3,0 оксалат тенелиглиптина и их сольват. В одном предпочтительном варианте реализации указанный сольват представляет собой n. гидрат. В одном предпочтительном варианте реализации оксалатная соль соединения формулы (I) и ее сольват представляет собой n. гидрат 2,5 оксалата тенелиглиптина или n. гидрат 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0.
[00147] В одном варианте реализации данного изобретения предложен способ получения фармацевтической композиции, содержащей оксалатную соль соединения формулы (I) и ее сольват, включающий стадии:
(a) просеивания фармацевтически приемлемых вспомогательных веществ;
(b) получения раствора связующего вещества, содержащего оксалатную соль соединения формулы (I) и ее сольват;
(c) гранулирования просеянных фармацевтических приемлемых вспомогательных веществ, полученных на стадии (а), с раствором связующего вещества, полученным на стадии (b);
(d) сушки и просеивания гранулята, полученного на стадии (с);
(e) смазывания просеянного гранулята, полученного на стадии (с), просеянными фармацевтически приемлемыми вспомогательными веществами с получением смеси;
(f) прессования смазанной смеси, полученной на стадии (d), с получением таблетки, или наполнения капсул смесью, полученной на стадии (d);
(g) необязательно прессования смазанной смеси, полученной на стадии (d), со смесью одного или более антидиабетических агентов с получением таблетки, или наполнения капсул указанной смесью.
[00148] В одном варианте реализации данного изобретения предложен способ получения фармацевтической композиции, содержащей оксалатную соль соединения формулы (I) и ее сольват, включающий стадии:
(a) получения раствора оксалатной соли соединения формулы (I) и ее сольвата со стабилизатором или комплексообразующим агентом
(b) распылительной сушки раствора, полученного на стадии (а)
(c) просеивания высушенной распылением смеси, полученной на стадии (b)
(d) смазывания просеянного гранулята, полученного на стадии (с), просеянными фармацевтически приемлемыми вспомогательными веществами;
(e) прессования смазанной смеси, полученной на стадии (d), с получением таблетки, или наполнения капсул смесью, полученной на стадии (d).
[00149] В одном варианте реализации данного изобретения предложен способ получения фармацевтической композиции, содержащей оксалатную соль соединения формулы (I) и ее сольват, включающий стадии:
(a) просеивания n. гидрата 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, с фармацевтически приемлемыми вспомогательными веществами или одним или более антидиабетическими агентами или их смесью;
(b) гранулирования просеянного материала, полученного на стадии (а), с раствором связующего вещества;
(c) сушки и просеивания гранулята, полученного на стадии (b);
(d) смазывания просеянного гранулята, полученного на стадии (с), подходящим смазывающим агентом с получением смеси;
(e) прессования смазанной смеси, полученной на стадии (d), с получением таблетки, или наполнения капсул смесью, полученной на стадии (d);
(f) необязательно прессования смазанной смеси, полученной на стадии (d), со смесью одного или более антидиабетических агентов с получением таблетки, или наполнения капсул указанной смесью.
[00150] В одном варианте реализации данного изобретения предложен способ получения фармацевтической композиции, содержащей n. гидрат 3,0 оксалата тенелиглиптина, включающий стадии:
(a) просеивания фармацевтически приемлемых вспомогательных веществ;
(b) получения раствора связующего вещества, содержащего n. гидрат 3,0 оксалата тенелиглиптина;
(c) гранулирования просеянных фармацевтических приемлемых вспомогательных веществ, полученных на стадии (а), с раствором связующего вещества, полученным на стадии (b);
(d) сушки и просеивания гранулята, полученного на стадии (с);
(e) смазывания просеянного гранулята, полученного на стадии (с), просеянными фармацевтически приемлемыми вспомогательными веществами с получением смеси;
(f) прессования смазанной смеси, полученной на стадии (d), с получением таблетки, или наполнения капсул смесью, полученной на стадии (d); и
(g) необязательно прессования смазанной смеси, полученной на стадии (d), со смесью одного или более антидиабетических агентов с получением таблетки, или наполнения капсул указанной смесью.
[00151] В одном варианте реализации данного изобретения предложен способ получения фармацевтической композиции, содержащей n. гидрат 3,0 оксалата тенелиглиптина, включающий стадии:
(a) получения раствора n. гидрата 3,0 оксалата тенелиглиптина со стабилизатором или комплексообразующим агентом;
(b) распылительной сушки раствора, полученного на стадии (а);
(c) просеивания высушенной распылением смеси, полученной на стадии (b);
(d) смазывания просеянного гранулята, полученного на стадии (с), просеянными фармацевтически приемлемыми вспомогательными веществами; и
(e) прессования смазанной смеси, полученной на стадии (d), с получением таблетки, или наполнения капсул смесью, полученной на стадии (d).
[00152] В одном варианте реализации гранулы оксалатной соли соединения (I) и ее сольвата, предусмотренные данным изобретением, можно получать из оксалатной соли соединения (I) и ее сольвата в сочетании с подходящими разбавителями, смазывающими агентами, связующими агентами, разжижающими агентами, разрыхлителями, солюбилизаторами и т.п.
[00153] В одном варианте реализации гранулы 2,5 оксалата тенелиглиптина и его сольвата, предусмотренные данным изобретением, можно получать из 2,5 оксалата тенелиглиптина и его сольвата в сочетании с подходящими разбавителями, смазывающими агентами, связующими агентами, разжижающими агентами, разрыхлителями, солюбилизаторами и т.п.
[00154] В одном варианте реализации гранулы 3,0 оксалата тенелиглиптина и его сольвата, предусмотренные данным изобретением, можно получать из 3,0 оксалата тенелиглиптина и его сольвата в сочетании с подходящими разбавителями, смазывающими агентами, связующими агентами, разжижающими агентами, разрыхлителями, солюбилизаторами и т.п.
[00155] В одном варианте реализации гранулы n. гидрата 2,5 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, предусмотренные данным изобретением, можно получать из n. гидрата 2,5 оксалата тенелиглиптина в сочетании с подходящими разбавителями, смазывающими агентами, связующими агентами, разжижающими агентами, разрыхлителями, солюбилизаторами и т.п.
[00156] В одном варианте реализации гранулы n. гидрата 3,0 оксалата тенелиглиптина, предусмотренные данным изобретением, можно получать из n. гидрата 3,0 оксалата тенелиглиптина в сочетании с подходящими разбавителями, смазывающими агентами, связующими агентами, разжижающими агентами, разрыхлителями, солюбилизаторами и т.п.
[00157] Подходящее связующее вещество включает, но не ограничивается этим, гидроксипропилцеллюлозу, поливиниловый спирт, повидон, коповидон, этилцеллюлозу, гипромеллозу и т.п.
[00158] Подходящие разбавители включают, но не ограничиваются этим, маннит, сорбит, ксилит, крахмал, лактозу, целлюлозу, дигидрофосфат кальция и т.п.
[00159] Подходящие смазывающие вещества включают, но не ограничиваются ими, глицерилдибегенат, стеарилфумарат натрия или кальция, стеарат магния, стеариновую кислоту, глицерилпальмитостеарат.
[00160] Гранулы оксалатной соли соединения формулы (I) и ее сольвата можно получать смешиванием оксалатной соли соединения формулы (I) и фармацевтически приемлемых вспомогательных веществ; добавлением раствора связующего вещества к смеси соединения формулы (I) и фармацевтически приемлемых вспомогательных веществ и высушиванием влажной смеси оксалатной соли соединения формулы (I) и фармацевтически приемлемых вспомогательных веществ с последующим просеиванием с получением гранул.
[00161] Альтернативно, гранулы оксалатной соли соединения формулы (I) и ее сольвата можно получать после смешивания оксалатной соли соединения формулы (I) и фармацевтически приемлемых вспомогательных веществ, раствор связующего вещества можно распылять на указанную смесь в реакторе с псевдоожиженным слоем, с последующим высушиванием влажных гранул и дальнейшим необязательным просеиванием. В качестве другой альтернативы, чешуйки оксалатной соли соединения формулы (I) можно получать сухим смешиванием оксалатной соли соединения формулы (I) и фармацевтически приемлемых вспомогательных веществ с получением смеси; уплотнением смеси прокаткой один или более раз с получением чешуек, с последующим гранулированием и просеиванием чешуек. Гранулы или чешуйки оксалатной соли соединения формулы (I) можно смазывать любым смазывающим веществом, упомянутым выше. Затем указанную смесь можно подавать в таблеточную машину или ей можно наполнять капсулы с помощью машины для наполнения капсул. Необязательно, на таблетку можно наносить покрытие. Раствор или суспензия покрывающего агента содержит вспомогательные вещества, такие как гипромеллоза, полиэтиленгликоль, окрашивающий агент, такой как красный или желтый оксид железа, диоксид титана и тальк. Альтернативно, указанными таблетками можно наполнять капсулы подходящего размера. Объем капсулы может быть выбран соответствующим образом, в диапазоне от 0,13 до 1,37 мл, для вмещения смазанной смеси или таблеток, содержащих оксалатную соль соединения формулы (I). В одном аспекте данного варианта реализации оксалатная соль соединения формулы (I), используемая для получения гранул, содержащих тенелиглиптин, представляет собой 3,0 оксалат тенелиглиптина или его сольват. В первом аспекте данного варианта реализации 3,0 оксалат тенелиглиптина или его сольват существует в кристаллической форме.
[00162] В альтернативном варианте способ прямого прессования для получения таблеток тенелиглиптина также предусмотрен данным изобретением. Таблетки получают смешиванием тенелиглиптина с одним или более фармацевтически приемлемыми вспомогательными веществами с получением смеси для прямого прессования; прессованием указанной смеси с получением таблетки; необязательно на таблетку можно наносить покрытие, как описано выше.
[00163] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие оксалатную соль соединения формулы (I) и ее сольват и метформин или его фармацевтически приемлемую соль, как описано в данном документе, причем содержание метформина или его фармацевтически приемлемой соли может быть соответствующим образом выбрано так, чтобы обеспечивать доставку дозы метформина в диапазоне 1-2000 мг, предпочтительно 250-1000 мг, более предпочтительно 500-1000 мг, еще более предпочтительно 500 мг или 1000 мг. Такая фармацевтическая композиция содержит тенелиглиптин и метформин в отдельных частях. Например, многослойная композиция, содержащая тенелиглиптин и метформин в отдельных слоях двух- или трехслойной таблетки; композиция, содержащая метформин в ядре и тенелиглиптин в покрытии, и другие подобные варианты.
[00164] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие оксалатные соли тенелиглиптина и их сольваты и по меньшей мере один или более антидиабетических агентов, выбранных из группы, состоящей из соединений класса сульфонилмочевины и их солей, соединений класса глитазона и их солей, соединений класса бигуанида и их солей, соединений класса ингибиторов глюкозидазы и их солей, соединений класса ингибиторов SGLT2 и их солей, и их комбинаций, как описано в данном документе, причем массовая концентрация оксалатных солей тенелиглиптина и их сольватов составляет от 0,5 до 10,0%, предпочтительно от 0,5 до 8,0%. В предпочтительном варианте реализации антидиабетический агент представляет собой метформин и его соли. В более предпочтительном варианте реализации антидиабетический агент представляет собой метформин с пролонгированным высвобождением. В одном варианте реализации размер дозы метформина с пролонгированным высвобождением в указанной фармацевтической композиции составляет 500 мг. В другом варианте реализации размер дозы метформина с пролонгированным высвобождением в указанной фармацевтической композиции составляет 1000 мг.
[00165] В одном варианте реализации данного изобретения предложены фармацевтические композиции, содержащие оксалатные соли тенелиглиптина и их сольват, предпочтительно n. гидрат 3,0 оксалата тенелиглиптина, и метформин или его фармацевтически приемлемую соль, предпочтительно метформин с пролонгированным высвобождением, как описано в данном документе, причем мас./мас. отношение тенелиглиптина к метформину в указанной композиции находится в диапазоне 1:10-1:50. В одном варианте реализации указанное мас./мас. отношение составляет около 1:15. В другом варианте реализации указанное мас./мас. Отношение составляет около 1:31. В одном варианте реализации размер дозы тенелиглиптина находится в диапазоне около 5-50%, предпочтительно 20-40%, более предпочтительно 25-35%.В одном варианте реализации размер дозы метформина находится в диапазоне 100-2000 мг, предпочтительно 500-1000 мг, более предпочтительно 500 мг или 1000 мг.
[00166] В одном варианте реализации данного изобретения предложен способ лечения, предупреждения или замедления прогрессирования метаболического расстройства посредством введения пациенту, нуждающемуся в этом, фармацевтической композиции, содержащей оксалатную соль соединения формулы (I) и по меньшей мере один другой антидиабетический агент, причем указанное метаболическое расстройство выбрано из группы, состоящей из сахарного диабета 1 типа, сахарного диабета 2 типа, нарушения переносимости глюкозы (IGT), нарушения уровня глюкозы в крови натощак (IFG), гипергликемии, постпрандиальной гипергликемии, избыточного веса, ожирения, инсулинорезистентности и метаболического синдрома, у пациента, нуждающегося в этом.
[00167] В одном варианте реализации данного изобретения предложен способ лечения сахарного диабета 2 типа посредством введения пациенту, нуждающемуся в этом, фармацевтической композиции, содержащей оксалатную соль соединения формулы (I) и по меньшей мере одного другого антидиабетического агента или их фармацевтически приемлемые соли.
[00168] В одном варианте реализации данного изобретения предложен способ улучшения гликемического контроля у пациента, проходящего монотерапию антидиабетическим лекарством, посредством введения пациенту, нуждающемуся в этом, фармацевтической композиции, содержащей оксалатную соль соединения формулы (I) и по меньшей мере один другой антидиабетический агент или их фармацевтически приемлемые соли.
[00169] В одном варианте реализации данного изобретения предложен способ улучшения гликемического контроля и/или уменьшения уровня глюкозы в плазме натощак, пострандиальной глюкозы в плазме и/или гликозилированного гемоглобина HbA1c у пациента посредством введения пациенту, нуждающемуся в этом, фармацевтической композиции, содержащей оксалатную соль соединения формулы (I) и по меньшей мере один другой антидиабетический агент или их фармацевтически приемлемые соли.
[00170] В одном варианте реализации данного изобретения предложен способ лечения, предупреждения или замедления прогрессирования патологического состояния или расстройства, выбранного из группы, состоящей из осложнений сахарного диабета, у пациента посредством введения пациенту, нуждающемуся в этом, фармацевтической композиции, содержащей оксалатную соль соединения формулы (I) и по меньшей мере один другой антидиабетический агент или их фармацевтически приемлемые соли. Осложнения сахарного диабета по данному изобретению включают катаракты и микро- или макрососудистые заболевания, такие как нефропатия, ретинопатия, невропатия, нарушение способности к обучению и памяти, нейродегенеративные или когнитивные расстройства, кардио- или церебрососудистые заболевания, ишемия тканей, синдром диабетической стопы или язвы, артериосклероз, гипертензия, эндотелиальная дисфункция, инфаркт миокарда, острый коронарный синдром, нестабильная стенокардия, стабильная стенокардия, инсульт, окклюзионная болезнь периферических артерий, кардиомиопатия, сердечная недостаточность, нарушения сердечного ритма и сосудистый рестеноз, и т.п.
[00171] В одном варианте реализации данного изобретения предложен способ лечения, предупреждения или замедления прогрессирования дегенерации бета-клеток поджелудочной железы и/или снижения функциональности бета-клеток поджелудочной железы; и/или улучшения и/или восстановления функциональности бета-клеток поджелудочной железы и/или восстановления функциональности секреции инсулина поджелудочной железой у пациента посредством введения пациенту, нуждающемуся в этом, фармацевтической композиции, содержащей оксалатную соль соединения формулы (I) и по меньшей мере один другой антидиабетический агент или их фармацевтически приемлемые соли.
ПРИМЕРЫ
[00172] Следующие примеры представлены для обеспечения того, что предположительно является наиболее применимым и понятным описанием способов и концептуальных аспектов данного изобретения. Примеры, приведенные ниже, являются исключительно иллюстрацией данного изобретения, и они не предназначены для его ограничения до описанных вариантов реализации. Варианты и изменения, понятные специалистам в данной области техники, входят в объем и сущность настоящего изобретения.
Пример 1
Фармацевтически композиции, содержащие n. гидрат 3,0 оксалата тенелиглиптина
[00173] В представленных ниже таблицах описаны иллюстративные композиции, содержащие n. гидрат 3,0 оксалата тенелиглиптина, предпочтительно моногидрат.
[00174] В Таблице 1 представлена лекарственная форма, содержащая щавелевую кислоту в качестве стабилизатора для предупреждения деградации n. гидрата 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0.
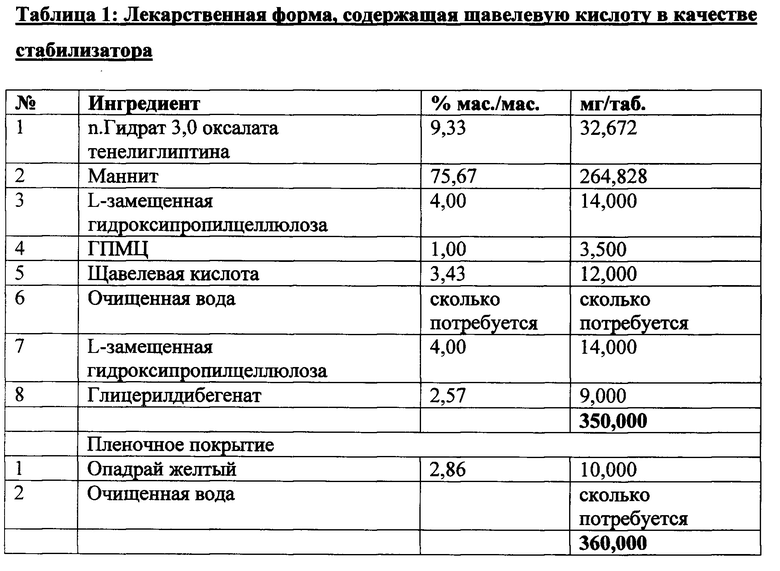
[00175] Производственный процесс:
1. Просеивание: совместно просеивали оксалат тенелиглиптина, L-ГПЦ и маннит через сито №060 меш;
2. Получение связующего вещества: добавляли и растворяли при перемешивании щавелевую кислоту и гидроксипропилцеллюлозу в очищенной воде;
3. Гранулирование: гранулировали материалы, полученные на стадии 1, с раствором связующего вещества, полученным на стадии 2, при подходящих технологических параметрах в реакторе с псевдоожиженным слоем (FBP). После завершения гранулирования высушивали влажную массу до достижения требуемого значения потерь при высушивании (LoD);
4. Просеивали отсортированные гранулы через сито №030 меш. Измельчали остаток с помощью 1,0 мм решета и просеивали через сито №030 меш;
5. Совместно просеивали L-гидроксипропилцеллюлозу и глицерилдибегенат через сито №040 меш;
6. Смазывание: смазывали гранулы, полученные на стадии 4, с просеянными вспомогательными веществами, полученными на стадии 5, в подходящем смесителе;
7. Прессование: прессовали смазанную смесь с применением подходящего оборудования и технологических параметров;
8. Нанесение покрытия: наносили покрытие на прессованные таблетки с применением водной дисперсии опадрай желтого; и
9. упаковывали таблетки с пленочным покрытием в блистерную упаковку.
[00176] В Таблице 2 представлена лекарственная форма, содержащая щавелевую кислоту, полимер и комплексообразующий агент для предупреждения деградации n. гидрата 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0.
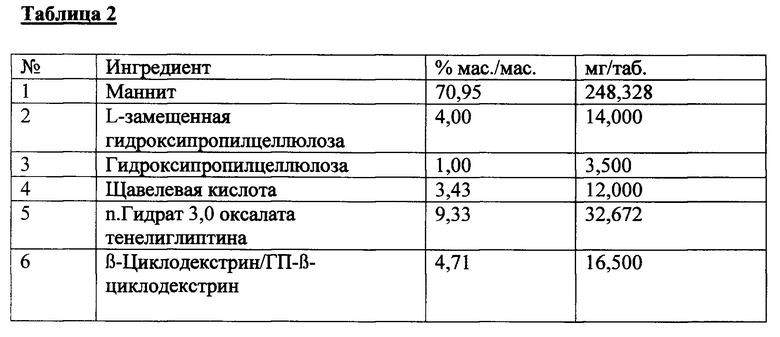

[00177] Производственный процесс:
1. Просеивание: совместно просеивали L-ГПЦ и маннит через сито №060 меш;
2. Получение связующего вещества: добавляли и растворяли при перемешивании щавелевую кислоту, β-циклодекстрин и гидроксипропилцеллюлозу в очищенной воде;
3. Гранулирование: гранулировали материалы, полученные на стадии 1, с раствором связующего вещества, полученным на стадии 2, при подходящих технологических параметрах в реакторе с псевдоожиженным слоем (FBP). После завершения гранулирования высушивали влажную массу до достижения требуемого значения потерь при высушивании (LoD);
4. Просеивали отсортированные гранулы через сито №030 меш. Измельчали остаток с помощью 1,0 мм решета и просеивали через сито №030 меш;
5. Совместно просеивали L-гидроксипропилцеллюлозу и глицерилдибегенат через сито №040 меш;
6. Смазывание: смазывали гранулы, полученные на стадии 4, с просеянными вспомогательными веществами, полученными на стадии 5, в подходящем смесителе;
7. Прессование: прессовали смазанную смесь с применением подходящего оборудования и технологических параметров;
8. Нанесение покрытия: наносили покрытие на прессованные таблетки с применением водной дисперсии опадрай желтого; и
9. упаковывали таблетки с пленочным покрытием в блистерную упаковку.
[00178] В Таблице 3 представлена лекарственная форма, содержащая комплексообразующий агент для предупреждения деградации n. гидрата 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0.
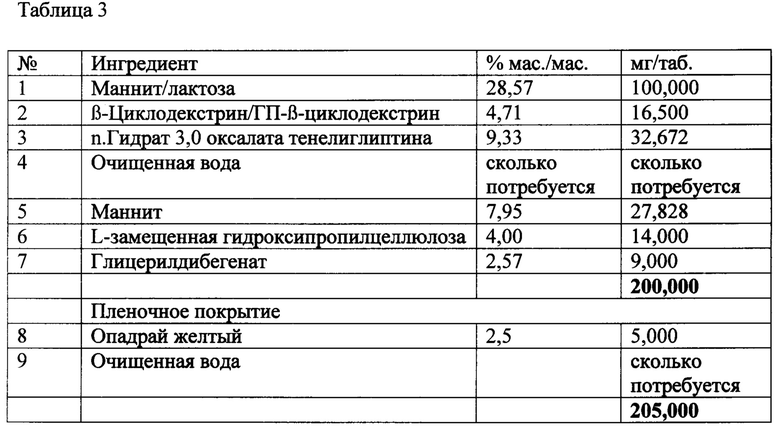
[00179] Производственный процесс:
1. Получение раствора: добавляли и растворяли маннит, В-циклодекстрин и оксалат тенелиглиптина в очищенной воде при перемешивании;
2. Сушили распылением раствор, полученный на стадии 1;
3. Просеивали высушенный распылением материал через сито №030 меш;
4. Совместно просеивали маннит, L-гидроксипропилцеллюлозу и глицерилдибегенат через сито №040 меш;
5. Смазывание: смазывали гранулы, полученные на стадии 3, с просеянными вспомогательными веществами, полученными на стадии 4, в подходящем смесителе;
6. Прессование: прессовали смазанную смесь с применением подходящего оборудования и технологических параметров;
7. Нанесение покрытия: наносили покрытие на прессованные таблетки с применением водной дисперсии опадрай желтого; и
8. упаковывали таблетки с пленочным покрытием в блистерную упаковку.
[00180] В Таблице 4 представлена лекарственная форма, содержащая полимер для предупреждения деградации n. гидрата 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0.

[00181] Производственный процесс:
1. Просеивание: просеивали L-ГПЦ и маннит через сито №060 меш;
2. Получение связующего вещества: добавляли и растворяли при перемешивании гидроксипропилцеллюлозу в очищенной воде;
3. Гранулирование: гранулировали материалы, полученные на стадии 1, с раствором связующего вещества, полученным на стадии 2, при подходящих технологических параметрах в реакторе с псевдоожиженным слоем (FBP). После завершения гранулирования высушивали влажную массу до достижения требуемого значения потерь при высушивании (LoD);
4. Просеивали отсортированные гранулы через сито №030 меш. Измельчали остаток с помощью 1,0 мм решета и просеивали через сито №030 меш;
5. Совместно просеивали маннит, L-гидроксипропилцеллюлозу и глицерилдибегенат через сито №040 меш;
6. Смазывание: смазывали гранулы, полученные на стадии 4, с просеянными вспомогательными веществами, полученными на стадии 5, в подходящем смесителе;
7. Прессование: прессовали смазанную смесь с применением подходящего оборудования и технологических параметров;
8. Нанесение покрытия: наносили покрытие на прессованные таблетки с применением водной дисперсии опадрай желтого; и
9. упаковывали таблетки с пленочным покрытием в блистерную упаковку.
[00182] В Таблице 5 представлена лекарственная форма, содержащая полимер для предупреждения деградации n. гидрата 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0.
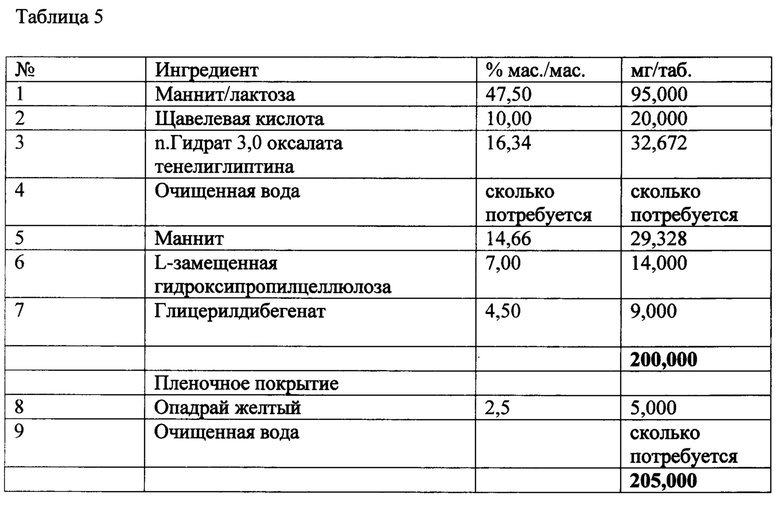
[00183] Производственный процесс:
1. Получение раствора: добавляли и растворяли маннит, щавелевую кислоту и оксалат тенелиглиптина в очищенной воде при перемешивании;
2. Сушили распылением раствор, полученный на стадии 1;
3. Просеивали высушенный распылением материал через сито №030 меш;
4. Совместно просеивали маннит, L-гидроксипропилцеллюлозу и глицерилдибегенат через сито №040 меш;
5. Смазывание: смазывали гранулы, полученные на стадии 3, с просеянными вспомогательными веществами, полученными на стадии 4, в подходящем смесителе;
6. Прессование: прессовали смазанную смесь с применением подходящего оборудования и технологических параметров;
7. Нанесение покрытия: наносили покрытие на прессованные таблетки с применением водной дисперсии опадрай желтого; и
8. упаковывали таблетки с пленочным покрытием в блистерную упаковку.
[00184] В Таблице 6 представлена лекарственная форма, содержащая полимер и хелатообразующий агент для предупреждения деградации n. гидрата 3,0 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0.
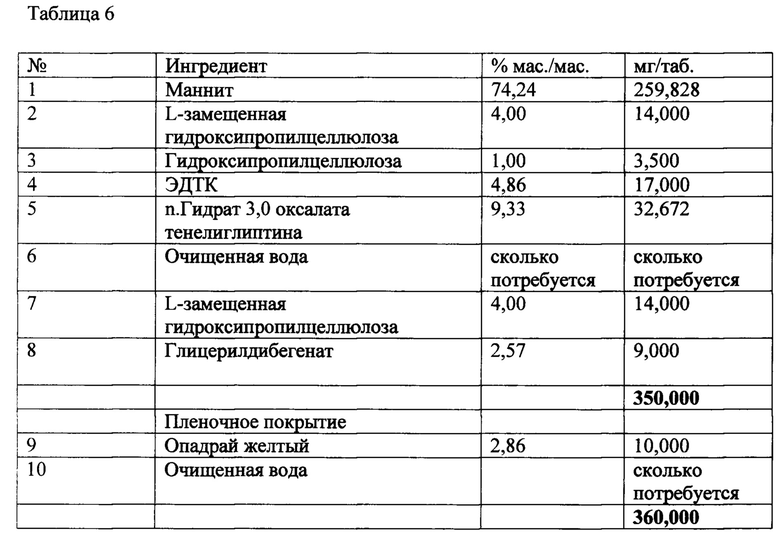
[00185] Производственный процесс:
1. Просеивание: совместно просеивали L-ГПЦ и маннит через сито №060 меш;
2. Получение связующего вещества: добавляли и растворяли при перемешивании щавелевую кислоту, ЭДТК и гидроксипропилцеллюлозу в очищенной воде;
3. Гранулирование: гранулировали материалы, полученные на стадии 1, с раствором связующего вещества, полученным на стадии 2, при подходящих технологических параметрах в реакторе с псевдоожиженным слоем (FBP). После завершения гранулирования высушивали влажную массу до достижения требуемого значения потерь при высушивании (LoD);
4. Просеивали отсортированные гранулы через сито №030 меш. Измельчали остаток с помощью 1,0 мм решета и просеивали через сито №030 меш;
5. Совместно просеивали L-гидроксипропилцеллюлозу и глицерилдибегенат через сито №040 меш;
6. Смазывание: смазывали гранулы, полученные на стадии 4, с просеянными вспомогательными веществами, полученными на стадии 5, в подходящем смесителе;
7. Прессование: прессовали смазанную смесь с применением подходящего оборудования и технологических параметров;
8. Нанесение покрытия: наносили покрытие на прессованные таблетки с применением водной дисперсии опадрай желтого; и
9. упаковывали таблетки с пленочным покрытием в блистерную упаковку.
[00186] Специалистам в данной области техники понятно, что иллюстративные лекарственные формы, описанные в данном документе, могут быть модифицированы специалистами в данной области техники без отступления от предполагаемой сущности данного изобретения. Кроме того, специалистам в соответствующей области техники понятно, что подобные лекарственные формы, содержащие n. гидрат 2,5 оксалата тенелиглиптина, где n равен от 1,0 до 4,0, предпочтительно 1,0, предусмотрены данным описанием и входят в область знаний специалистов в данной области техники, к которой они относятся, включая любые модификации.
Пример 2: Способ комбинирования 3,0 оксалата тенелиглиптина и метформина HCl
[00187] Метформиновая часть (для дозы 500 мг): Гидрохлорид метформина измельчали с помощью универсального измельчителя. Совместно просеивали измельченный гидрохлорид метформина и карбоксиметилцеллюлозу натрия через сито №40 меш из нержавеющей стали. Гуаровую камедь просеивали через сито №100 меш из нержавеющей стали. Просеянный гидрохлорид метформина, карбоксиметилцеллюлозу и гуаровую камедь гранулировали в скоростном смесителе-грануляторе в течение 20 минут. Раствор связующего вещества получали посредством добавления метилпарабена и пропилпарабена в очищенную воду при перемешивании. Гранулированную смесь гидрохлорида метформина, карбоксиметилцеллюлозы и гуаровой камеди гранулировали с раствором связующего вещества в сушилке с псевдоожиженным слоем. Полученную влажную гранулированную массу сушили с получением гранул. Полученные гранулы просеивали через сито №16 на вибрационном просеивателе. Гранулы слишком большого размера собирали и измельчали на универсальном измельчителе. Измельченные гранулы собирали и просеивали через сита №16 на вибрационном просеивателе. Совместно просеивали гидроксипропилметилцеллюлозу, пептизированный крахмал, полиэтиленоксид и гидрированное касторовое масло через сито №40, и просеивали стеарат магния через сито №40 на вибрационном просеивателе. Смазывали полученную предварительную смесь, смешивая мелкие гранулы и совместно просеянную гидроксипропилметилцеллюлозу, пептизированный крахмал, полиэтиленоксид и гидрированное касторовое масло. Измельченные гранулы смазывали смазывающей предварительной смесью в смесителе с получением смеси метформина HCl.
[00188] Метформиновая часть (для дозы 1000 мг): Гидрохлорид метформина измельчали на универсальном измельчителе и просеивали через сито №40 из нержавеющей стали. Просеивали карбоксиметилцеллюлозу натрия через сито №40 меш из нержавеющей стали. Гуаровую камедь просеивали через сито №100 меш из нержавеющей стали. Просеянный гидрохлорид метфтормина и карбоксиметилцеллюлозу гранулировали в скоростном смесителе-грануляторе в течение 20 минут. Раствор связующего вещества получали посредством добавления метилпарабена и пропилпарабена в очищенную воду при перемешивании. Гранулировали смесь гидрохлорида метформина, карбоксиметилцеллюлозы с очищенной водой, используя подходящие технологические параметры. Полученную влажную гранулированную массу частично сушили и просеивали через сито №16. Частично высушенные гранулы сушили в сушилке с псевдоожиженным слоем. Просеивали высушенные гранулы через сито №16 на вибрационном просеивателе. Гранулы слишком большого размера собирали и измельчали на универсальном измельчителе. Измельченные гранулы собирали и просеивали через сита №16 на вибрационном просеивателе. Совместно просеивали гидроксипропилметилцеллюлозу и маисовый крахмал через сито №40 на вибрационном просеивателе, и просеивали стеарат магния через сито №60. Измельченные гранулы смазывали совместно просеянной гидроксипропилметилцеллюлозой и маисовым крахмалом и просеянным стеаратом магния в подходящем смесителе.
Пример 3
Стабильность n. гидрата 3,0 оксалата тенелиглиптина в лекарственных формах
[00189] Ниже в Таблице 7 представлен профиль стабильности лекарственной формы, описанной в Таблице 1, через 1 месяц и 2 месяца.
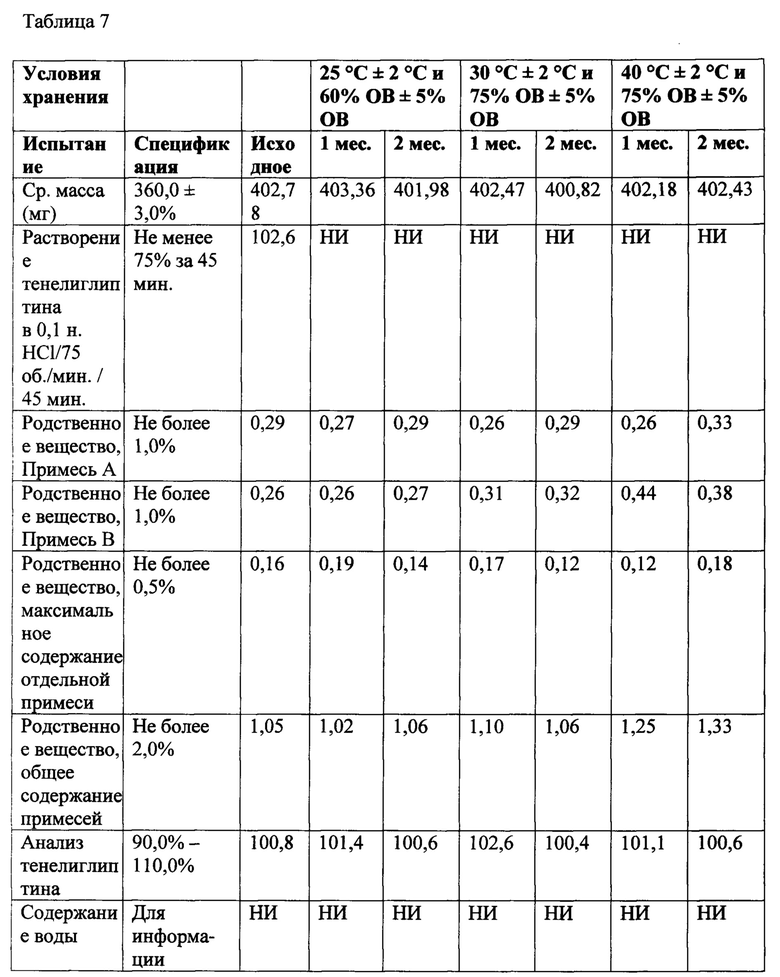
[00190] Как показано выше в Таблице 7, можно сделать вывод, что даже через 2 месяца хранения при 40°С±2°С и 75% OB±5% ОВ, содержание примеси В (нежелательного побочного продукта лекарственной формы, приводящего к потере оксалата) ниже допустимого значения 1% мас./мас.Такие же результаты наблюдали также для лекарственных форм, представленных в Таблицах 2-6. Следует понимать, что улучшенная стабильность каждой из лекарственных форм, представленных в Таблицах 1-6, обусловлена, в частности, присутствием щавелевой кислоты, полимера, комплексообразующего агента, хелатообразующего агента или их комбинаций. Преимущественная и неожиданная стабильность лекарственной формы, полученной с добавлением любого из соединений: щавелевой кислоты, полимера, комплексообразующего агента, хелатообразующего агента, или их комбинаций может быть еще более понятна при рассмотрении лекарственных форм, представленных ниже, которые не содержат щавелевой кислоты, полимера, комплексообразующего агента, хелатообразующего агента или их комбинаций и, следовательно, демонстрируют повышенное содержание примеси В за пределами допустимых значений.
[00191] В Таблице 8 представлена лекарственная форма, демонстрирующая недопустимое содержание примеси В.
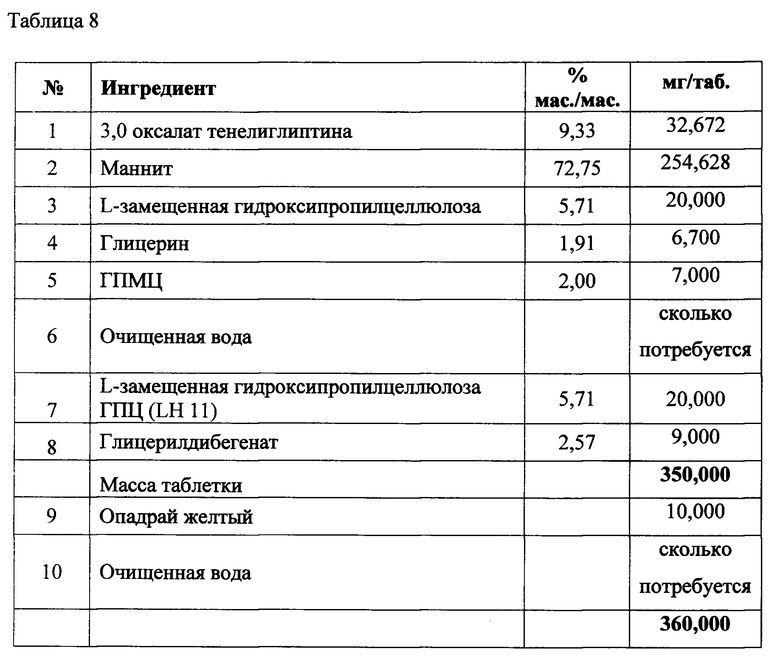
[00192] В Таблице 9 представлен профиль стабильности лекарственной формы, описанной в Таблице 8.
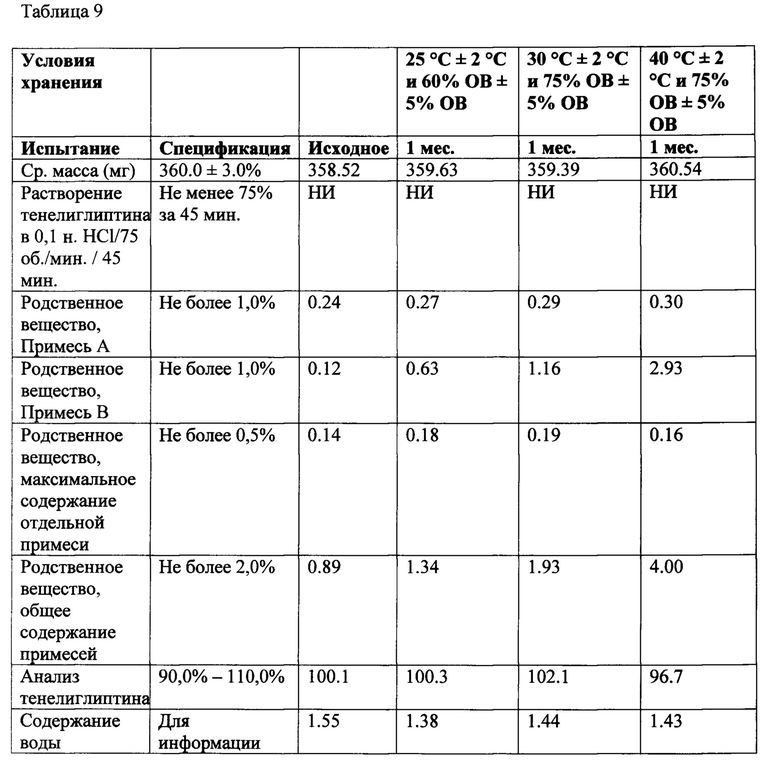
[00193] В Таблице 10 представлена лекарственная форма, демонстрирующая недопустимое содержание примеси В.

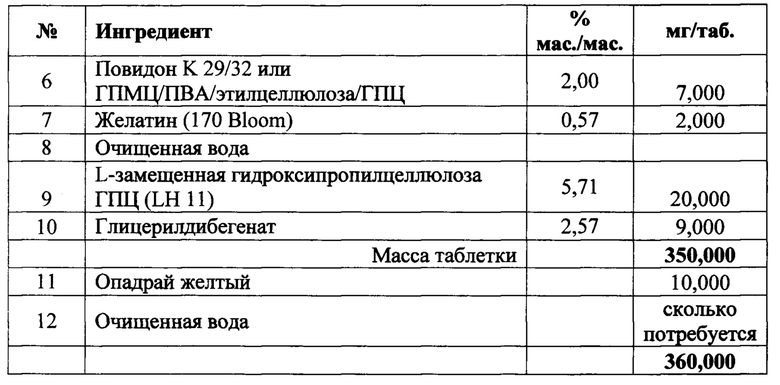
[00194] В Таблице 11 представлен профиль стабильности лекарственной формы, описанной в Таблице 10.


[00195] В Таблице 12 представлена лекарственная форма, демонстрирующая недопустимое содержание примеси В.
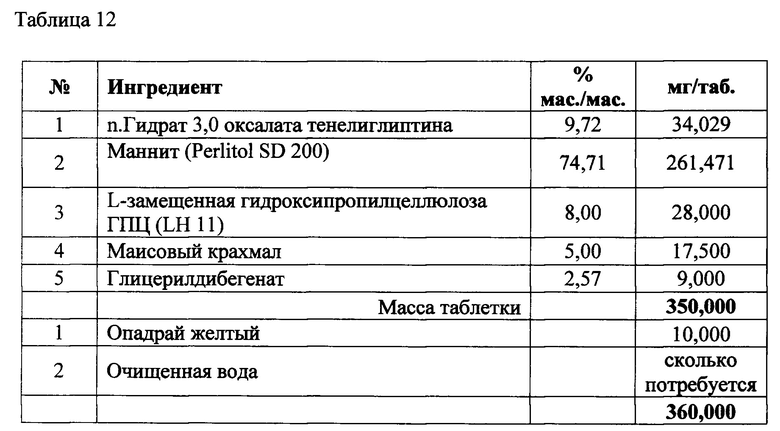
[00196] В Таблице 13а представлен профиль стабильности лекарственной формы, описанной в Таблице 12.
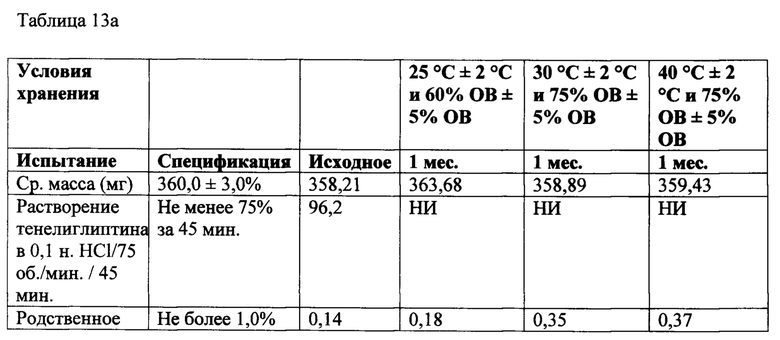
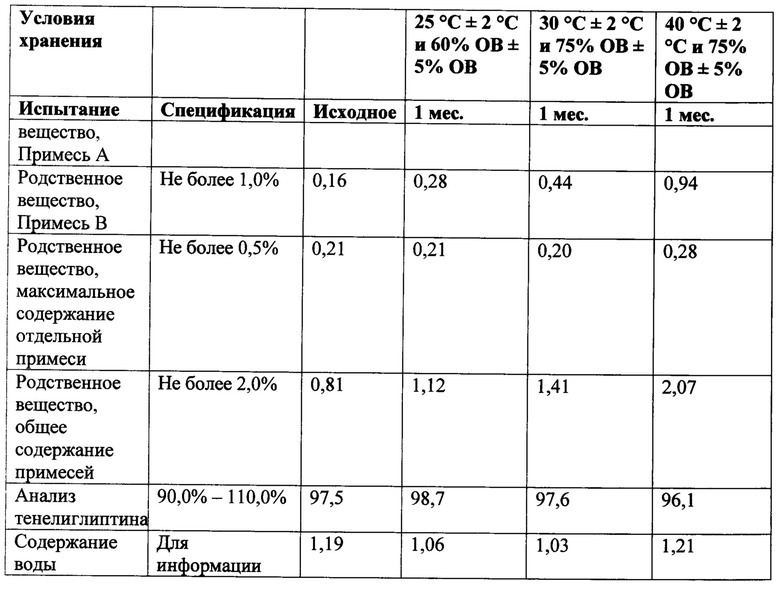
[00197] В Таблице 13b представлен профиль стабильности лекарственной формы, описанной в Таблице 12.
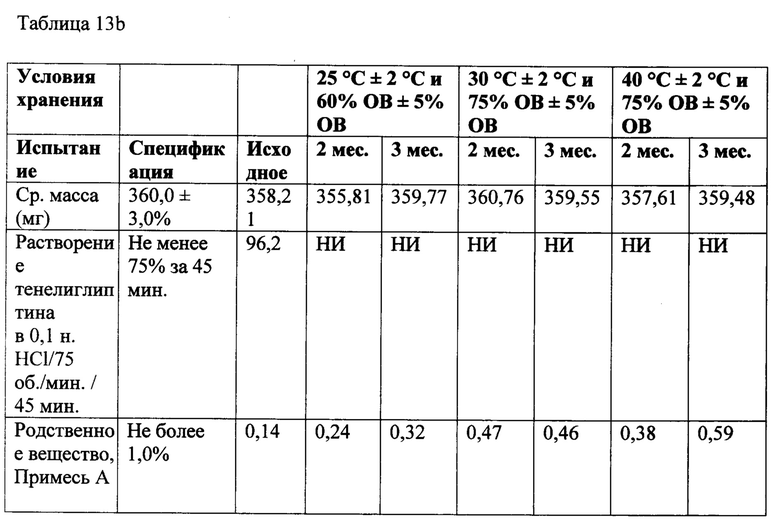
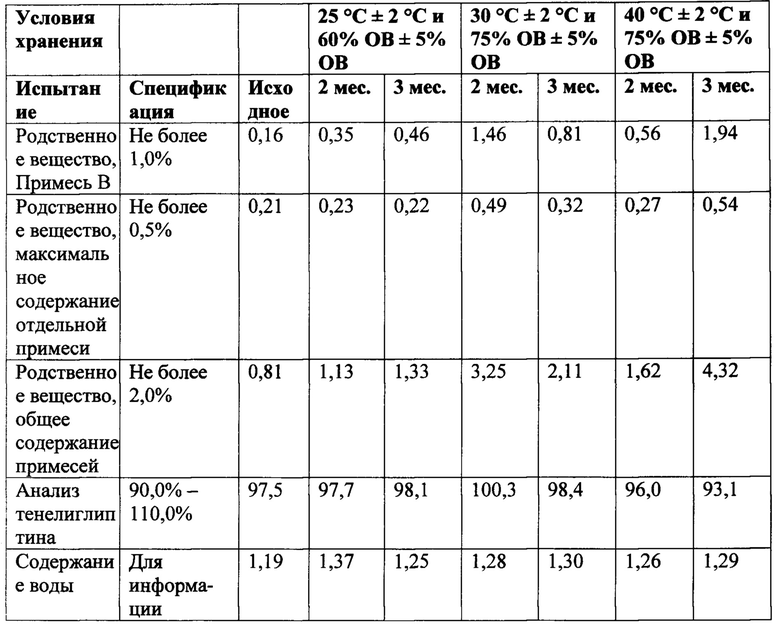
Пример 4
Лекарственные формы, содержащие n. гидрат 3,0 тенелиглиптина и глимепирид
[00198] В Таблице 14а представлена лекарственная форма, содержащая n. гидрат 3,0 оксалата тенелиглиптина и глимепирид.
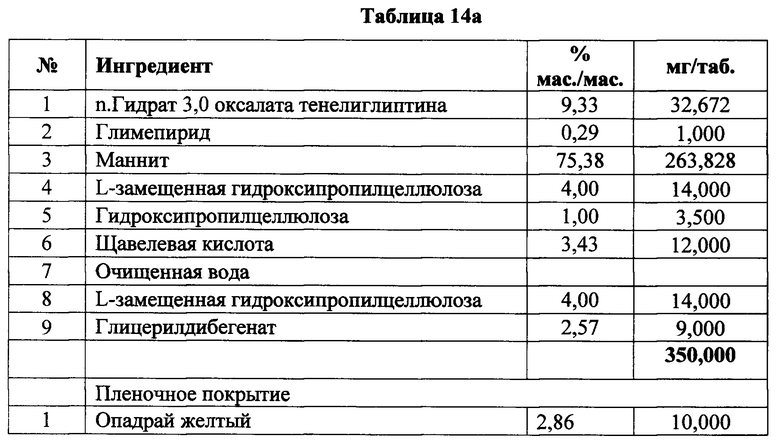
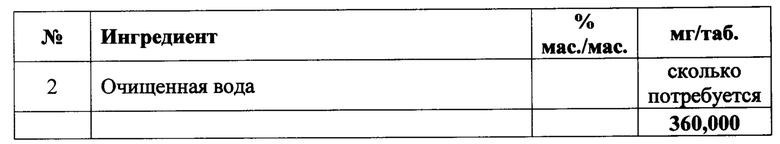
[00199] В Таблице 14b представлена лекарственная форма, содержащая n. гидрат 3,0 оксалата тенелиглиптина и глимепирид (монослойная стратегия 2).

[00200] Краткая стратегия производственного процесса для получения лекарственной формы, описанной в Таблице 14а-b.
1. Просеивание: совместно просеивали оксалат тенелиглиптина, глимепирид, L-ГПЦ и маннит через сито №060 меш;
2. Получение связующего вещества: добавляли и растворяли при перемешивании щавелевую кислоту и гидроксипропилцеллюлозу в очищенной воде;
3. Гранулирование: гранулировали материалы, полученные на стадии 1, с раствором связующего вещества, полученным на стадии 2. После завершения гранулирования сушили влажную массу;
4. Просеивали отсортированные гранулы через сито №030 меш. Измельчали остаток с помощью 1,0 мм решета и просеивали через сито №030 меш;
5. Совместно просеивали L-гидроксипропилцеллюлозу и глицерилдибегенат через сито №040 меш;
6. Смазывание: смазывали гранулы, полученные на стадии 4, с просеянными вспомогательными веществами, полученными на стадии 5, в подходящем смесителе;
7. Прессование: прессовали смазанную смесь с применением подходящего оборудования и технологических параметров;
8. Нанесение покрытия: наносили покрытие на прессованные таблетки с применением водной дисперсии опадрай желтого; и
9. упаковывали таблетки с пленочным покрытием в блистерную упаковку.
[00201] В Таблице 14 с представлена лекарственная форма, содержащая n. гидрат 3,0 оксалата тенелиглиптина и глимепирид.
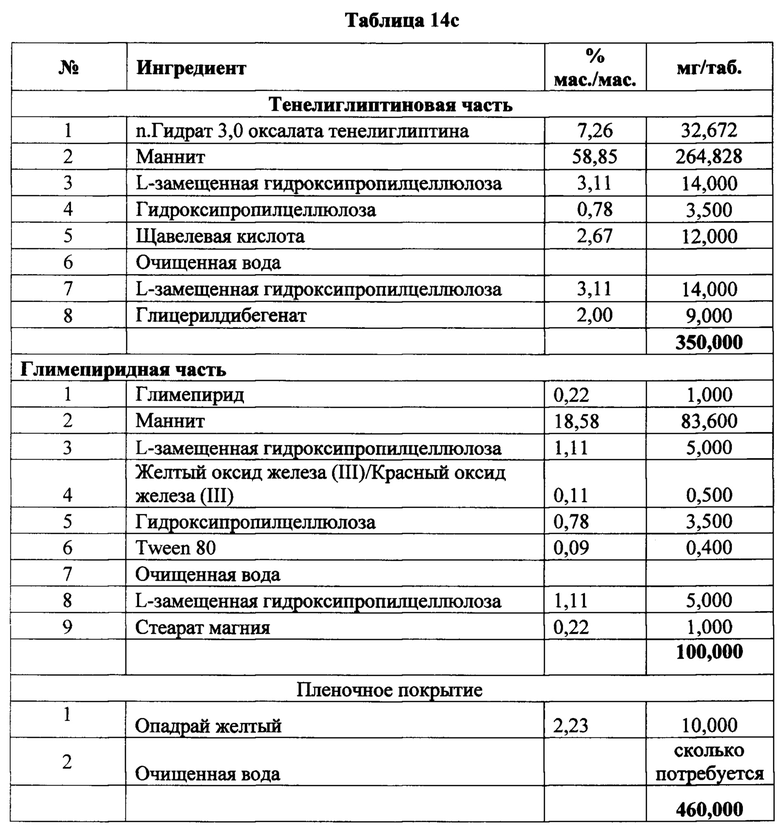
[00202] В Таблице 14d представлена лекарственная форма, содержащая плтщрат 3,0 оксалата тенелиглиптина и глимепирид (двухслойная стратегия 2).

[00203] Краткая стратегия производственного процесса для получения лекарственной формы, описанной в Таблице 14c-d.
Тенелиглиптиновая часть:
1. Просеивание: совместно просеивали оксалат тенелиглиптина, L-ГПЦ и маннит через сито №060 меш;
2. Получение связующего вещества: добавляли и растворяли при перемешивании щавелевую кислоту и гидроксипропилцеллюлозу в очищенной воде;
3. Гранулирование: гранулировали материалы, полученные на стадии 1, с раствором связующего вещества, полученным на стадии 2. После завершения гранулирования сушили влажную массу;
4. Просеивали отсортированные гранулы через сито №030 меш. Измельчали остаток с помощью 1,0 мм решета и просеивали через сито №030 меш;
5. Совместно просеивали L-гидроксипропилцеллюлозу и глицерилдибегенат через сито №040 меш; и
6. Смазывание: смазывали гранулы, полученные на стадии 4, с просеянными вспомогательными веществами, полученными на стадии 5, в подходящем смесителе.
Глимепиридная часть:
1. Просеивание: совместно просеивали глимепирид, L-ГПЦ и маннит через сито №060 меш; Просеивали желтый оксид железа (III) через сито №0100 меш;
2. Получение связующего вещества: добавляли и растворяли при перемешивании Tween 80 и гидроксипропилцеллюлозу в очищенной воде;
3. Гранулирование: гранулировали материалы, полученные на стадии 1, с раствором связующего вещества, полученным на стадии 2. После завершения гранулирования сушили влажную массу;
4. Просеивали отсортированные гранулы через сито №030 меш. Измельчали остаток с помощью 1,0 мм решета и просеивали через сито №030 меш;
5. Совместно просеивали L-гидроксипропилцеллюлозу и стеарат магния через сито №040 меш; и
6. Смазывание: смазывали гранулы, полученные на стадии 4, с просеянными вспомогательными веществами, полученными на стадии 5, в подходящем смесителе.
Прессование, нанесение покрытия, упаковка: Прессовали обе смазанные смеси тенелиглиптиновой части и глимепиридной части с помощью подходящего устройства, используя машину для двухслойного прессования. Наносили покрытие на прессованные таблетки с применением водной дисперсии опадрай желтого. Упаковывали таблетки с пленочным покрытием в блистерную упаковку.
Пример 5
Лекарственные формы, содержащие n. гидрат 3,0 тенелиглиптина и пиоглитазон
[00204] В Таблице 15а представлена лекарственная форма, содержащая n. гидрат 3,0 оксалата тенелиглиптина и пиоглитазон (монослойная стратегия 1).

[00205] В Таблице 15b представлена лекарственная форма, содержащая n. гидрат 3,0 оксалата тенелиглиптина и пиоглитазон.
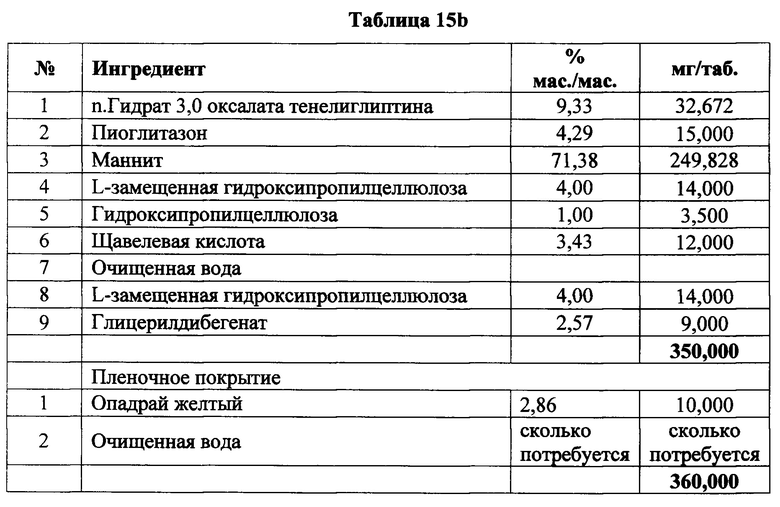
[00206] Краткая стратегия производственного процесса для получения лекарственной формы, описанной в Таблице 15а-b.
1. Просеивание: совместно просеивали оксалат тенелиглиптина, пиоглитазон, L-ГПЦ и маннит через сито №060 меш;
2. Получение связующего вещества: добавляли и растворяли при перемешивании щавелевую кислоту и гидроксипропилцеллюлозу в очищенной воде;
3. Гранулирование: гранулировали материалы, полученные на стадии 1, с раствором связующего вещества, полученным на стадии 2. После завершения гранулирования сушили влажную массу;
4. Просеивали отсортированные гранулы через сито №030 меш. Измельчали остаток с помощью 1,0 мм решета и просеивали через сито №030 меш;
5. Совместно просеивали L-гидроксипропилцеллюлозу и глицерилдибегенат через сито №040 меш;
6. Смазывание: смазывали гранулы, полученные на стадии 4, с просеянными вспомогательными веществами, полученными на стадии 5, в подходящем смесителе;
7. Прессование: прессовали смазанную смесь с применением подходящего оборудования и технологических параметров;
8. Нанесение покрытия: наносили покрытие на прессованные таблетки с применением водной дисперсии опадрай желтого; и
9. Упаковывали таблетки с пленочным покрытием в блистерную упаковку.
[00207] В Таблице 15 с представлена лекарственная форма, содержащая n. гидрат 3,0 оксалата тенелиглиптина и пиоглитазон (двухслойная стратегия 1).
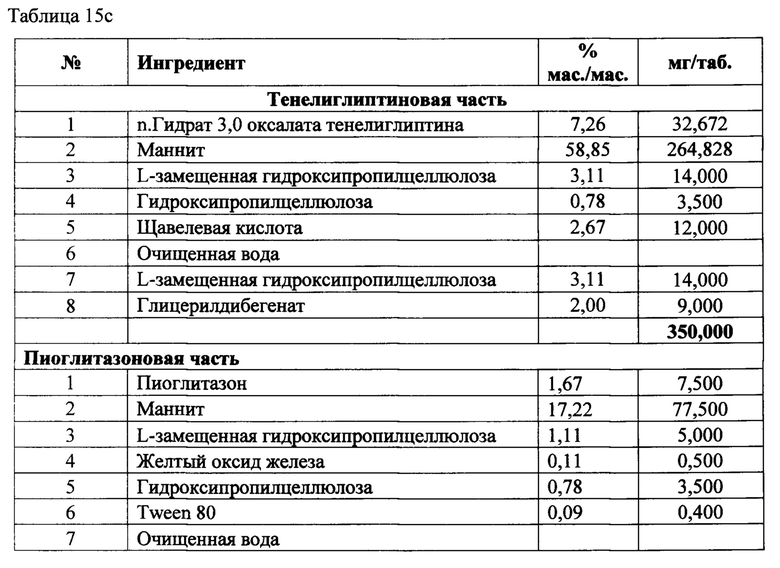

[00208] В Таблице 15d представлена лекарственная форма, содержащая n. гидрат 3,0 оксалата тенелиглиптина и пиоглитазон.
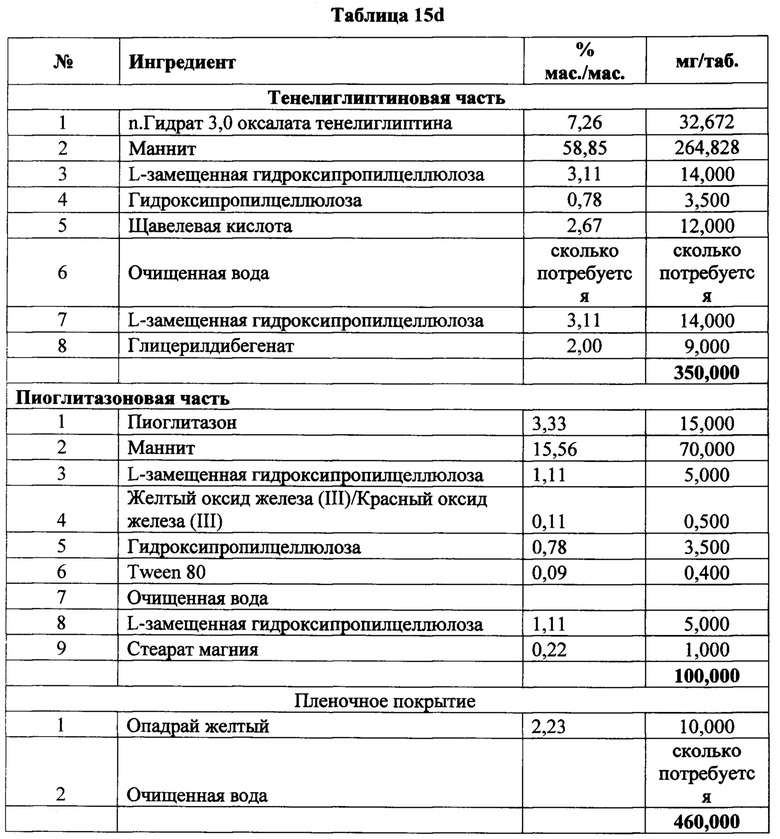
[00209] Краткая стратегия производственного процесса для получения лекарственной формы, описанной в Таблице 15c-d.
Тенелиглиптиновая часть:
1. Просеивание: совместно просеивали оксалат тенелиглиптина, L-ГПЦ и маннит через сито №060 меш;
2. Получение связующего вещества: добавляли и растворяли при перемешивании щавелевую кислоту и гидроксипропилцеллюлозу в очищенной воде;
3. Гранулирование: гранулировали материалы, полученные на стадии 1, с раствором связующего вещества, полученным на стадии 2. После завершения гранулирования сушили влажную массу;
4. Просеивали отсортированные гранулы через сито №030 меш. Измельчали остаток с помощью 1,0 мм решета и просеивали через сито №030 меш;
5. Совместно просеивали L-гидроксипропилцеллюлозу и глицерилдибегенат через сито №040 меш; и
6. Смазывание: смазывали гранулы, полученные на стадии 4, с просеянными вспомогательными веществами, полученными на стадии 5, в подходящем смесителе.
Пиоглитазоновая часть
1. Просеивание: совместно просеивали пиоглитазон, L-ГПЦ и маннит через сито №060 меш; Просеивали желтый оксид железа (III) через сито №0100 меш;
2. Получение связующего вещества: добавляли и растворяли при перемешивании гидроксипропилцеллюлозу в очищенной воде;
3. Гранулирование: гранулировали материалы, полученные на стадии 1, с раствором связующего вещества, полученным на стадии 2. После завершения гранулирования сушили влажную массу;
4. Просеивали отсортированные гранулы через сито №030 меш. Измельчали остаток с помощью 1,0 мм решета и просеивали через сито №030 меш;
5. Совместно просеивали L-гидроксипропилцеллюлозу и стеарат магния через сито №040 меш; и
6. Смазывание: смазывали гранулы, полученные на стадии 4, с просеянными вспомогательными веществами, полученными на стадии 5, в подходящем смесителе.
Прессование, нанесение покрытия, упаковка: Прессовали обе смазанные смеси тенелиглиптиновой части и пиоглитазоновой части с помощью подходящего устройства, используя машину для двухслойного прессования. Наносили покрытие на прессованные таблетки с применением водной дисперсии опадрай желтого.
Пример 6
Лекарственные формы, содержащие n. гидрат 3,0 тенелиглиптина и воглибозу
[00210] В Таблице 16а представлена лекарственная форма, содержащая n. гидрат 3,0 оксалата тенелиглиптина и воглибозу.
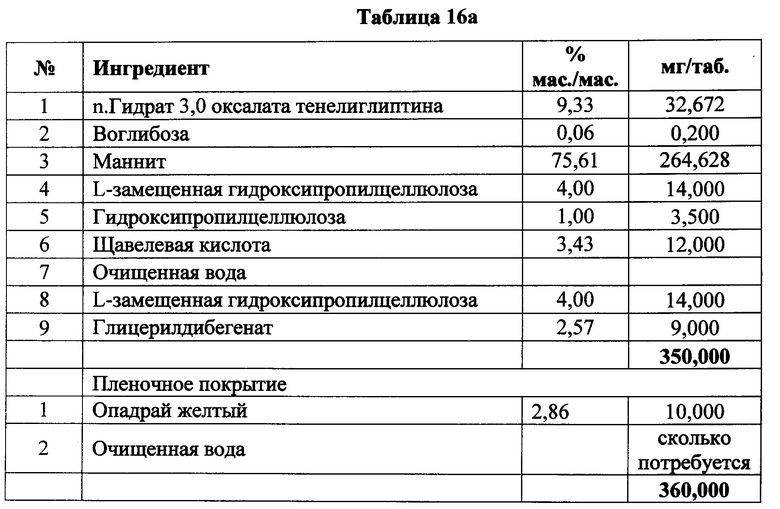
[00211] В Таблице 16b представлена лекарственная форма, содержащая n. гидрат 3,0 оксалата тенелиглиптина и воглибозу.
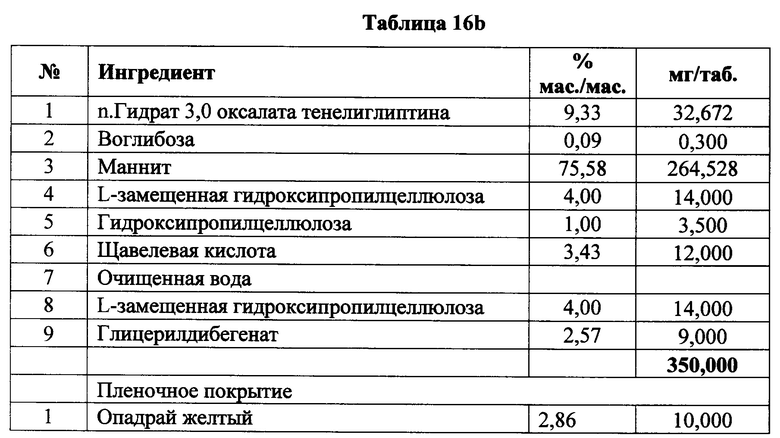
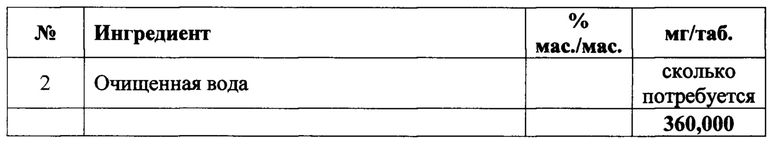
[00212] Краткая стратегия производственного процесса для получения лекарственной формы, описанной в Таблице 16а-b.
1. Просеивание: совместно просеивали оксалат тенелиглиптина, воглибозу, L-ГПЦ и маннит через сито №060 меш;
2. Получение связующего вещества: добавляли и растворяли при перемешивании щавелевую кислоту и гидроксипропилцеллюлозу в очищенной воде;
3. Гранулирование: гранулировали материалы, полученные на стадии 1, с раствором связующего вещества, полученным на стадии 2. После завершения гранулирования сушили влажную массу;
4. Просеивали отсортированные гранулы через сито №030 меш. Измельчали остаток с помощью 1,0 мм решета и просеивали через сито №030 меш;
5. Совместно просеивали L-гидроксипропилцеллюлозу и глицерилдибегенат через сито №040 меш;
6. Смазывание: смазывали гранулы, полученные на стадии 4, с просеянными вспомогательными веществами, полученными на стадии 5, в подходящем смесителе;
7. Прессование: прессовали смазанную смесь с применением подходящего оборудования и технологических параметров;
8. Нанесение покрытия: наносили покрытие на прессованные таблетки с применением водной дисперсии опадрай желтого; и
9. Упаковывали таблетки с пленочным покрытием в блистерную упаковку.
[00213] В Таблице 16 с представлена лекарственная форма, содержащая n. гидрат 3,0 оксалата тенелиглиптина и воглибозу.

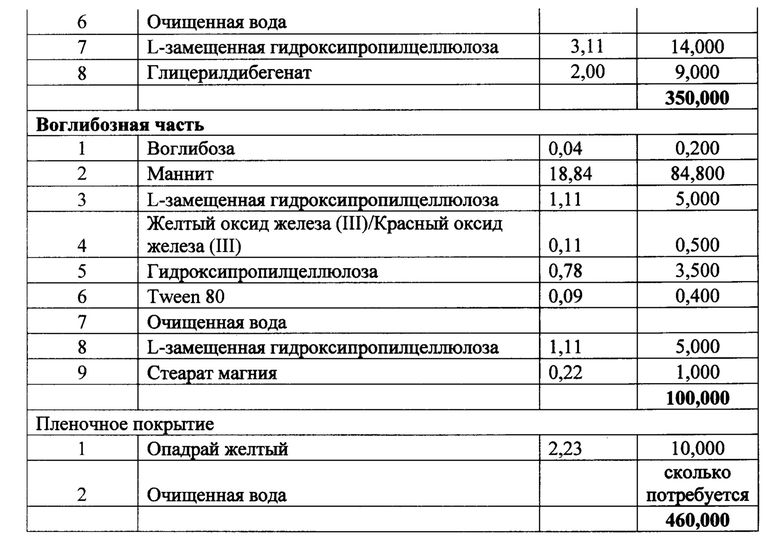
[00214] В Таблице 16d представлена лекарственная форма, содержащая n. гидрат 3,0 оксалата тенелиглиптина и воглибозу.


[00215] Краткая стратегия производственного процесса для получения лекарственной формы, описанной в Таблице 16c-d:
Тенелиглиптиновая часть:
1. Просеивание: совместно просеивали оксалат тенелиглиптина, L-ГПЦ и маннит через сито №060 меш;
2. Получение связующего вещества: добавляли и растворяли при перемешивании щавелевую кислоту и гидроксипропилцеллюлозу в очищенной воде;
3. Гранулирование: гранулировали материалы, полученные на стадии 1, с раствором связующего вещества, полученным на стадии 2. После завершения гранулирования сушили влажную массу;
4. Просеивали отсортированные гранулы через сито №030 меш. Измельчали остаток с помощью 1,0 мм решета и просеивали через сито №030 меш;
5. Совместно просеивали L-гидроксипропилцеллюлозу и глицерилдибегенат через сито №040 меш; и
6. Смазывание: смазывали гранулы, полученные на стадии 4, с просеянными вспомогательными веществами, полученными на стадии 5, в подходящем смесителе.
Воглибозная часть
1. Просеивание: совместно просеивали воглибозу, L-ГПЦ и маннит через сито №060 меш; Просеивали желтый оксид железа (III) через сито №0100 меш;
2. добавляли и растворяли при перемешивании гидроксипропилцеллюлозу в очищенной воде;
3. гранулировали материалы, полученные на стадии 1, с раствором связующего вещества, полученным на стадии 2. После завершения гранулирования сушили влажную массу;
4. Просеивали отсортированные гранулы через сито №030 меш. Измельчали остаток с помощью 1,0 мм решета и просеивали через сито №030 меш;
5. Совместно просеивали L-гидроксипропилцеллюлозу и стеарат магния через сито №040 меш; и
6. Смазывание: смазывали гранулы, полученные на стадии 4, с просеянными вспомогательными веществами, полученными на стадии 5, в подходящем смесителе.
[00216] Несмотря на то, что данное изобретение было описано со ссылкой на конкретные варианты реализации, следует понимать, что эти варианты реализации и примеры лишь иллюстрируют принципы и применение данного изобретения. Поэтому следует понимать, что могут быть сделаны многочисленные модификации иллюстративных вариантов реализации, и что могут быть разработаны другие схемы без отступления от сущности и объема данного изобретения, описанного в данном документе.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭСЦИТАЛОПРАМ И ТВЕРДАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ЕГО СОДЕРЖАЩАЯ | 2007 |
|
RU2463039C2 |
| ФАРМАЦЕВТИЧЕСКОЕ КОМБИНИРОВАННОЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО | 2014 |
|
RU2639818C2 |
| КРИСТАЛЛИЧЕСКИЕ ФОРМЫ ГИДРОХЛОРИДА ФИНГОЛИМОДА | 2009 |
|
RU2549899C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТЕНЕЛИГЛИПТИНА | 2013 |
|
RU2654069C2 |
| Композиции перорально распадающихся таблеток, содержащие кортикостероиды, для лечения эозинофильного эзофагита | 2014 |
|
RU2678695C2 |
| ПЕРОРАЛЬНОЕ ВВЕДЕНИЕ КАЛЬЦИТОНИНА | 2003 |
|
RU2355417C2 |
| Комбинированная композиция, содержащая метформин замедленного высвобождения и ингибитор HMG-CoA-редуктазы немедленного высвобождения | 2014 |
|
RU2651460C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ЛИГАНДЫ СИГМА РЕЦЕПТОРА | 2010 |
|
RU2549882C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ ФАРМАКОЛОГИЧЕСКИ ДЕЙСТВУЮЩИХ ВЕЩЕСТВ | 2001 |
|
RU2287999C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ МЕТФОРМИНА С ДЛИТЕЛЬНЫМ ВЫСВОБОЖДЕНИЕМ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 2006 |
|
RU2433821C2 |
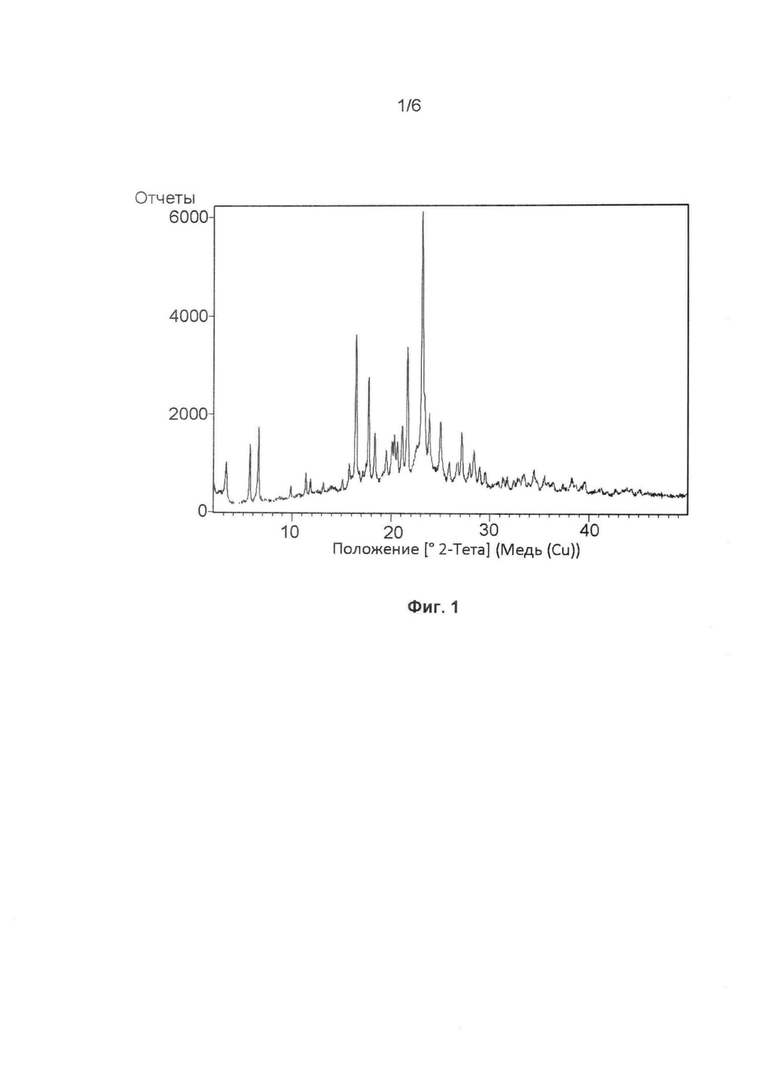
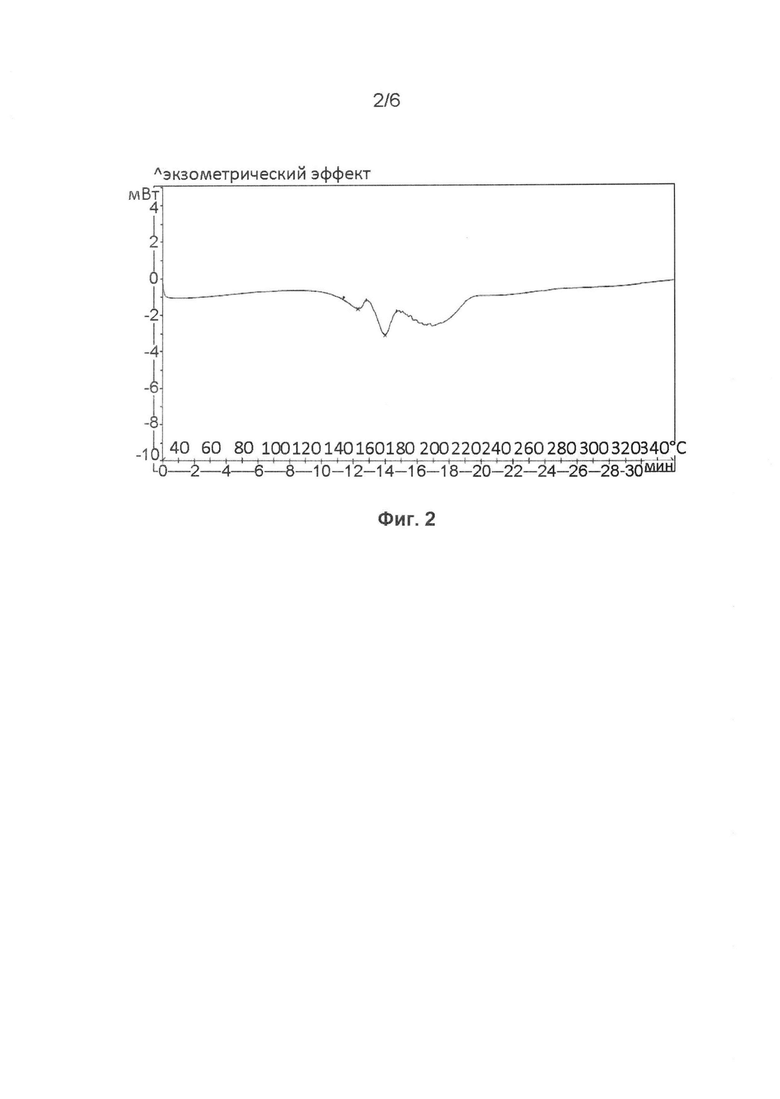
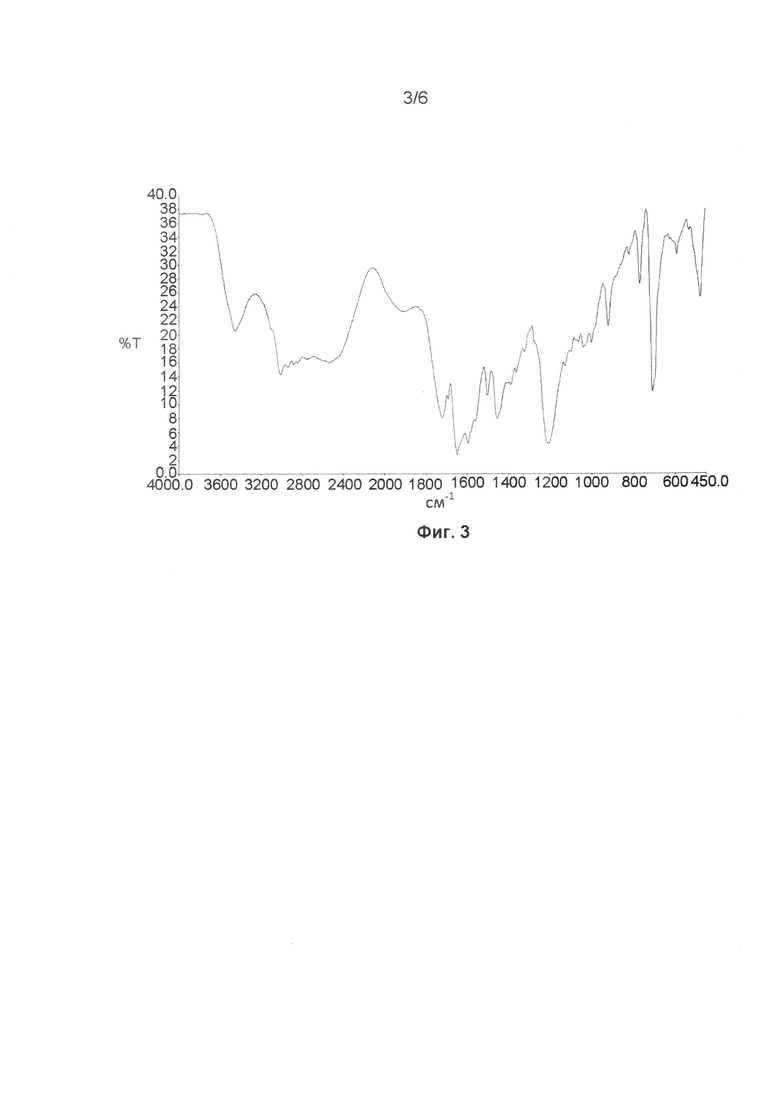

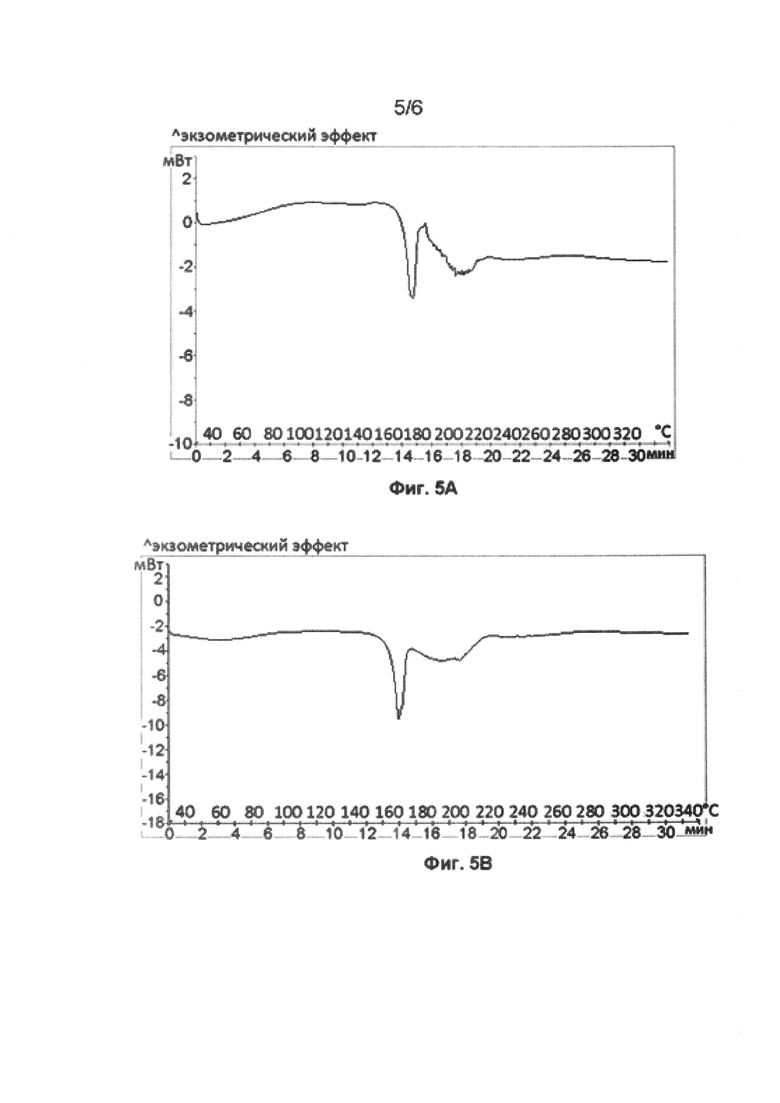
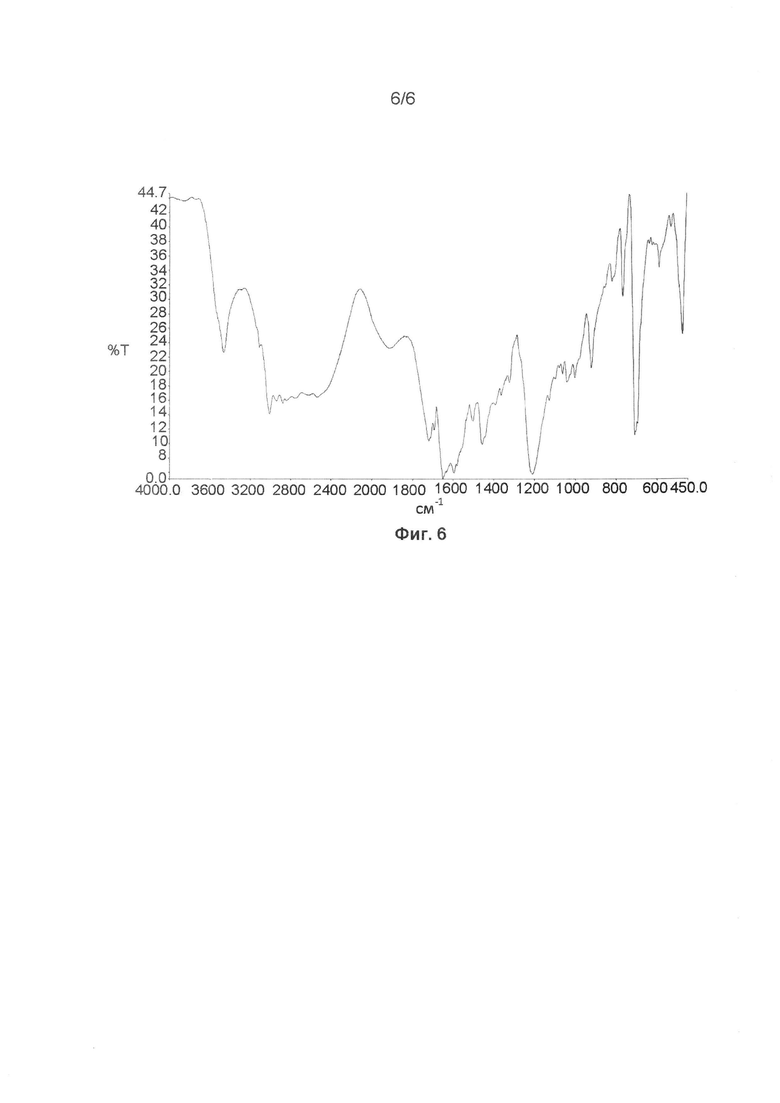
Группа изобретений относится к области фармацевтики, а именно к фармацевтической композиции для профилактического или радикального лечения сахарного диабета, содержащей n.гидрат 2,5 оксалат тенелиглиптина или n.гидрат 3,0 оксалат тенелиглиптина, имеющий концентрацию в диапазоне от 0,5 мас.% до 80 мас.%, от 10 мас.% до 95 мас.% по меньшей мере одного фармацевтически приемлемого разбавителя, от 0,1 мас.% до 10 мас.% связующих веществ, от 0,1 мас.% до 20 мас.% смазывающих веществ, от 0,1 мас.% до 30 мас.% разрыхлителей и необязательно от 0,05 мас.% до 30 мас.% стабилизирующих агентов. Также группа изобретений относится к способу получения указанной фармацевтической композиции включающему стадии просеивания, гранулирования, сушки и просеивания гранулята, смазывания просеянного гранулята и прессования смеси с получением таблетки или наполнения смесью капсул. Группа изобретений обеспечивает стабильные фармацевтические композиции тенелиглиптина. 2 н. и 4 з.п. ф-лы, 7 ил., 26 табл., 6 пр.
1. Фармацевтическая композиция для профилактического или радикального лечения сахарного диабета, содержащая n.гидрат 2,5 оксалат тенелиглиптина или n.гидрат 3,0 оксалат тенелиглиптина, имеющий концентрацию в диапазоне от 0,5 мас.% до 80 мас.%, и по меньшей мере один или более фармацевтически приемлемых разбавителей, имеющих концентрацию в диапазоне от 10 мас.% до 95 мас.% и выбранных из группы, состоящей из маннита, лактозы и крахмала; связующих веществ, имеющих концентрацию в диапазоне от 0,1 мас.% до 10 мас.% и выбранных из группы, состоящей из гидроксипропилцеллюлозы, поливинилового спирта, повидона, этилцеллюлозы и гипромеллозы; смазывающих веществ, имеющих концентрацию в диапазоне от 0,1 мас.% до 20 мас.% и выбранных из группы, состоящей из глицерилдибегената и стеарата магния; разрыхлителей, имеющих концентрацию в диапазоне от 0,1 мас.% до 30 мас.% и выбранных из группы, состоящей из гидроксипропилцеллюлозы с низкой степенью замещения и крахмалгликолята натрия; и необязательно стабилизирующих агентов, имеющих концентрацию в диапазоне от 0,05 мас.% до 30 мас.% и выбранных из группы, состоящей из щавелевой кислоты, бета-циклодекстрина, гидроксипропил-бета-циклодекстрина, желатина, гидроксипропилцеллюлозы, гидроксипропилметилцеллюлозы и ЭДТК.
2. Фармацевтическая композиция по п. 1, отличающаяся тем, что указанный n в гидрате равен от 1,0 до 4,0.
3. Фармацевтическая композиция для профилактического или радикального лечения сахарного диабета, содержащая: от 5 мас.% до 15,0 мас.% n.гидрата 3,0 оксалата тенелиглиптина; от 30 мас.% до 80 мас.% разбавителя, выбранного из маннита и крахмала; от 0,1 мас.% до 10 мас.% связующего, выбранного из гидроксипропилцеллюлозы и гидроксипропилметилцеллюлозы;, от 1,0 мас.% до 15,0 мас.% смазывающего вещества, выбранного из стеарата магния и глицерилдибегената; от 1,0 мас.% до 20 мас.% разрыхлителя, выбранного из гидроксипропилцеллюлозы с низкой степенью замещения и крахмалгликолята натрия; и необязательно от 0,5 мас.% до 15 мас.% щавелевой кислоты.
4. Фармацевтическая композиция по п. 3, отличающаяся тем, что указанный n в гидрате равен от 1,0 до 4,0.
5. Способ получения фармацевтической композиции по пп. 1-3 , включающий стадии:
(a) просеивания n.гидрата 2,5 оксалата тенелиглиптина или n.гидрата 3,0 оксалата тенелиглиптина с фармацевтически приемлемыми вспомогательными веществами;
(b) гранулирования просеянного материала, полученного на стадии (a), с раствором связующего вещества;
(c) сушки и просеивания гранулята, полученного на стадии (b);
(d) смазывания просеянного гранулята, полученного на стадии (c), подходящим смазывающим агентом с получением смеси; и
(e) прессования смазанной смеси, полученной на стадии (d), с получением таблетки или наполнения капсул смесью, полученной на стадии (d).
6. Способ по п. 5, отличающийся тем, что n равен от 1,0 до 4,0.
| WO 2015132679 A1, 11.09.2015 | |||
| WO 2015012365 A1, 29.01.2015 | |||
| WO 2016104643 A1, 30.06.2016 | |||
| US 2013196898 A1, 01.08.2013 | |||
| WO 2016051368 A1, 07.04.2016 | |||
| US 2012276166 A1, 01.11.2012 | |||
| WO 2011074660 A1, 23.06.2011 | |||
| MORISSETTE S.L | |||
| et al | |||
| High-throughput crystallization: polymorphs, salts, co-crystals and solvates of pharmaceutical solids // Advanced |
Авторы
Даты
2021-02-05—Публикация
2018-02-02—Подача