Предлагаемое изобретение относится к области органической химии, конкретно, к 16-азатрицикло[9.4.1.02,10]гексадека-2,12,14-триенам формулы (1), способу их получения и применению.
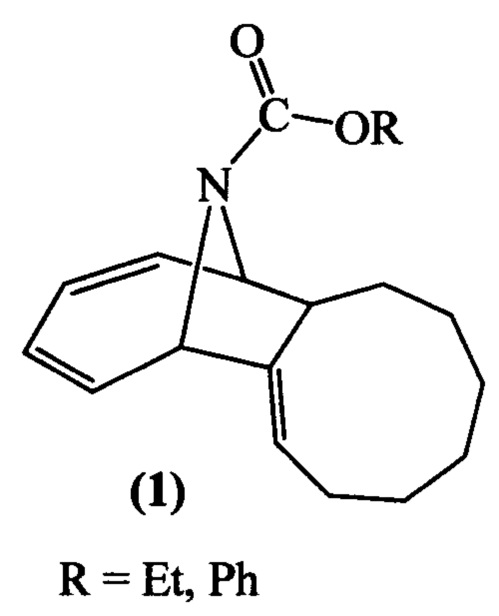
Указанные соединения относятся к классу гетероциклических соединений и могут найти применение в качестве ключевых прекурсоров в синтезе ценных биологически активных соединений и современных лекарственных препаратов, проявляющих противоопухолевую, противовирусную и другие виды активности (Е. Wright, Т. Gallagher, С.G.V. Sharples, S. Wonnacott, Bioorg. Med. Chem. Lett. 1997, 7, 2867-2870; H. Gohlke, D. Gundisch, S. Schwarz, G. Seitz, M. C. Tilotta, T. Wegge, J. Med. Chem. 2002, 45, 1064-1072; H. Gohlke, S. Schwarz, D. Gundisch, M.C. Tilotta, A. Weber, T. Wegge, G. Seitz, J. Med. Chem. 2003, 46, 2031-2048; С.V.G. Sharples, G. Karig, G.L. Simpson, J.A. Spencer, E. Wright, N.S. Millar, S. Wonnacott, T. Gallagher, J. Med. Chem. 2002, 45, 3235-3245).
Известен способ [J.H. Rigby, H.S. Ateeq, N.R. Choler, J.A. Henshilwood, K.M. Short, P.M. Sugathapala, Chromium(0) promoted [6π+2π] cycloaddition reactions // Tetrahedron, 1993, V. 49, P. 5495-5506] получения 9-азабицикло[4.2.1]нона-2,4-диена (2) на основе [6π+2π]-циклоприсоединения N-карбометоксиазепина к этилакрилату в присутствии каталитических количеств (η6-нафталин)трикарбонилхрома(0) (9 мол%) по схеме:
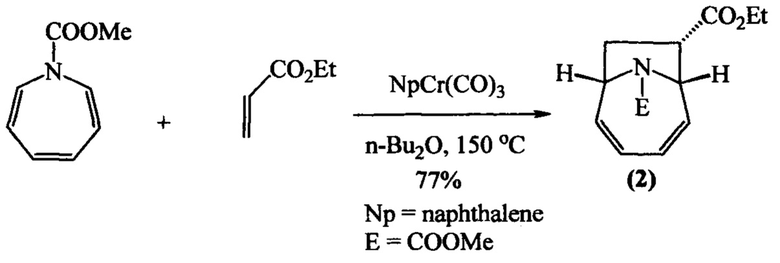
Известным способом не могут быть получены 16-азатрицикло[9.4.1.02,10]гексадека-2,12,14-триены формулы (1).
Известен способ [K. Chaffee, J.В. Sheridan, A. Aistars, Photoinduced [6+2] cycloadditions of alkynes to tricarbonyl(cycloheptatriene)chromium(0) // Organometallics, 1992, V. 11, P. 18-19] получения дизамещенных Cr-содержащих комплексов 9-азабицикло[4.2.1]нона-2,4,7-триенов (3) реакцией фотоиндуцированного [6π+2π]-циклоприсоединения алкинов к трикарбонил(η6-N-карбоэтоксиазепин)хрому(0) по схеме:
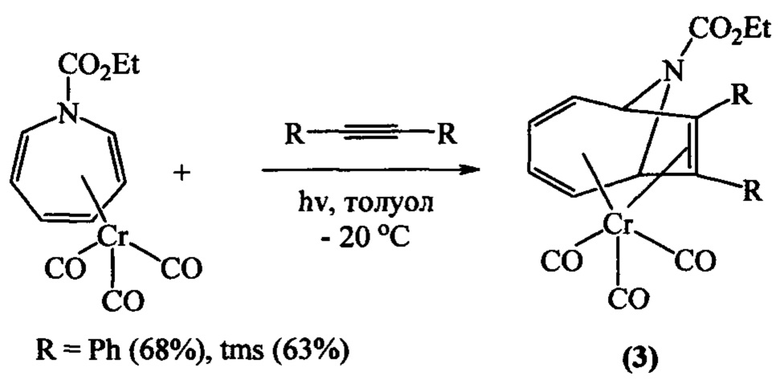
Известным способом не могут быть получены 16-азатрицикло[9.4.1.02,10]гексадека-2,12,14-триены (1).
Таким образом, в литературе отсутствуют сведения по синтезу 16-азатрицикло[9.4.1.02,10]гексадека-2,12,14-триенов формулы (1).
Предлагается новый способ синтеза 16-азатрицикло[9.4.1.02,10]гексадека-2,12,14-триенов формулы (1).
Сущность способа заключается во взаимодействии N-замещенных азепинов общей формулы (4) 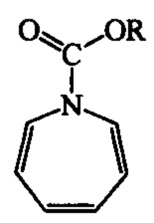 (где R=Et, Ph) с 1,2-циклононадиеном (ЦНД) в присутствии каталитической системы Co(acac)2(dppe)/Zn/ZnI2, при мольном соотношении ЦНД : азепин : Co(acac)2(dppe) : Zn : ZnI2= (1.3-2.0):1:(0.05-0.15):(0.15-0.45):(0.1-0.3), предпочтительно 1.3:1:0.1:0.3:0.2. Реакцию проводят в ампуле при 20-80°С. Время реакции 20-48 ч, выход целевого продукта 38-80%. В качестве растворителя необходимо использовать 1,2-дихлорэтан.
(где R=Et, Ph) с 1,2-циклононадиеном (ЦНД) в присутствии каталитической системы Co(acac)2(dppe)/Zn/ZnI2, при мольном соотношении ЦНД : азепин : Co(acac)2(dppe) : Zn : ZnI2= (1.3-2.0):1:(0.05-0.15):(0.15-0.45):(0.1-0.3), предпочтительно 1.3:1:0.1:0.3:0.2. Реакцию проводят в ампуле при 20-80°С. Время реакции 20-48 ч, выход целевого продукта 38-80%. В качестве растворителя необходимо использовать 1,2-дихлорэтан.
Реакция протекает по схеме:
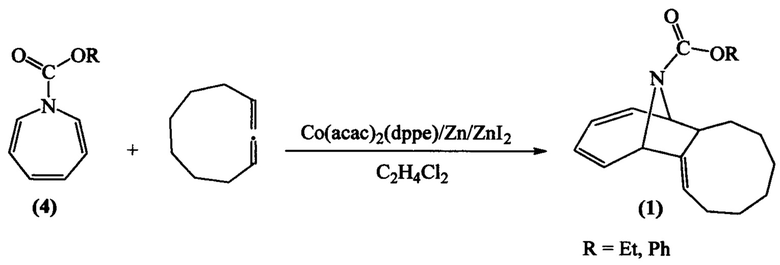
Целевые продукты формулы (1) образуются только лишь с участием 1,2-циклононадиена, N-замещенных азепинов и каталитической системы Co(acac)2(dppe)/Zn/ZnI2. В присутствии других комплексов переходных металлов (например, Cp2ZrCl2, Cp2TiCl2, Zr(acac)4, Pd(acac)2, Ni(acac)2, Fe(асас)3) целевые продукты (1) не образуются.
Проведение реакции в присутствии катализатора Co(acac)2(dppe) больше 0.1 ммоль на 1 ммоль N-замещенного азепина не приводит к существенному увеличению выхода целевого продукта (1). Использование в реакции катализатора Co(acac)2(dppe) менее 0.1 ммоль на 1 ммоль N-замещенного азепина снижает выход аддуктов (1), что связано с уменьшением каталитически активных центров в реакционной массе. Опыты проводили при 20-80°С. При более высокой температуре (например, 100°С) происходит уменьшение выхода содимеров, вероятно, вследствие побочных процессов разложения и полимеризации. При меньшей температуре (например, 20°С) снижается скорость реакции.
Существенные отличия предлагаемого способа:
Предлагаемый способ базируется на использовании в качестве исходных реагентов N-замещенных азепинов и 1,2-циклононадиена в присутствии каталитической системы Co(acac)2(dppe)/Zn/ZnI2. В известных способах:
1. аддукт (2) получен с использованием трикарбонил(η6-N-карбоэтоксиазепин)хрома(0) и дизамещенных алкинов в результате фотоиндуцированной реакции;
2. аддукт (3) получен при использовании в качестве исходных соединений N-карбометоксиазепина и этилакрилата под действием катализатора (η6-нафталин)трикарбонилхрома(0).
Предлагаемый способ обладает следующими преимуществами:
1. Способ позволяет получать с высокими выходами 16-азатрицикло[9.4.1.02,10]гексадека-2,12,14-триены (1), синтез которых в литературе не описан.
Способ поясняется следующими примерами:
ПРИМЕР 1. В стеклянную ампулу в атмосфере сухого аргона загружали 0.066 г (0.1 ммоль) Co(acac)2(dppe), и 0.020 г (0.3 ммоль) цинкового порошка в 1.5 мл 1,2-дихлорэтана. Смесь перемешивали при комнатной температуре 2 минуты. Затем добавляли 0.165 г (1 ммоль) N-карбоэтоксиазепина, 0.159 г (1.3 ммоль) 1,2-циклононадиена, 1.5 мл 1,2-дихлорэтана и 0.064 г (0.2 ммоль) ZnI2. После нагревания при 60°С в течение 20 ч, ампулу вскрывали, содержимое отфильтровывали, легкие растворители удаляли под вакуумом, остаток хроматографировали на колонке SiO2 элюент (петролейный эфир → петролейный эфир / этилацетат 15:1 → 10:1 → 5:1). Получали этил 16-азатрицикло[9.4.1.02,10]гексадека-2,12,14-триен-16-карбоксилат (1) с выходом 78%.
Спектральные характеристики этил 16-азатрицикло[9.4.1.02,10]гексадека-2,12,14-триен-16-карбоксилата (1):
Существует в виде двух N-(CO)OEt ротамеров. 1Н ЯМР (500 МГц, CDCl3, δ, мд): 6.36 (дд, J=9.8 Гц, J=6.5 Гц, 1Н), 6.27 (дд, J=10.4 Гц, J=6.4 Гц, 1Н), 6.04 (ддд, J=21.8 Гц, J=11.4 Гц, J=5.4 Гц, 2Н), 5.63-5.74 (м, 4Н), 5.21-5.30 (м, 2Н), 5.19 (д, J=6.3 Гц, 1Н), 5.11 (д, J=6.3 Гц, 1Н), 4.27 (д, J=5.4 Гц, 1Н), 4.09-4.22 (м, 5Н), 2.98 (д, J=6.2 Гц, 2Н), 2.07-2.28 (м, 4Н), 1.71-1.90 (м, 4Н), 1.30-1.59 (м, 16Н), 1.19-1.30 (м, 6Н). 13С ЯМР (125 МГц, CDCl3, δ, мд): 155.0, 154.9, 150.7, 149.7, 138.9, 138.89, 136.4, 136.2, 123.9, 123.85, 123.7 (3С), 123.5, 66.7, 66.6, 61.0 (2С), 59.3 (2С), 58.3, 57.6, 33.2, 33.15, 29.0 (2С), 28.4, 28.3, 26.9, 26.8, 26.6, 26.59, 22.1, 22.06, 14.7, 14.67.
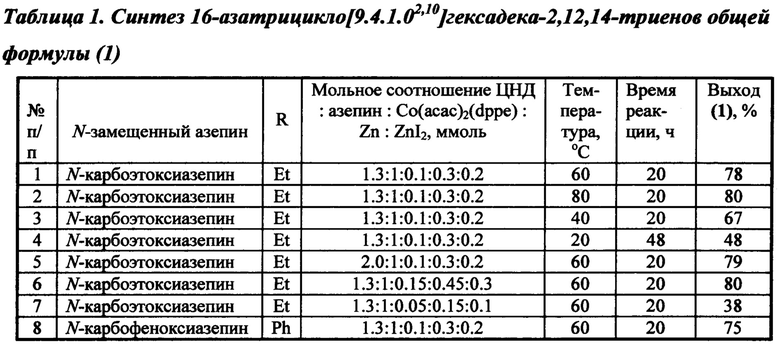
Другие примеры, подтверждающие способ, приведены в таблице 1.
ПРИМЕР 2. Оценка противоопухолевой активности заявленных соединений общей формулы (1) осуществлена методом проточной цитофлуориметрии, по отношению к четырем клеточным линиям: Jurkat, K562, U937 и HL60.
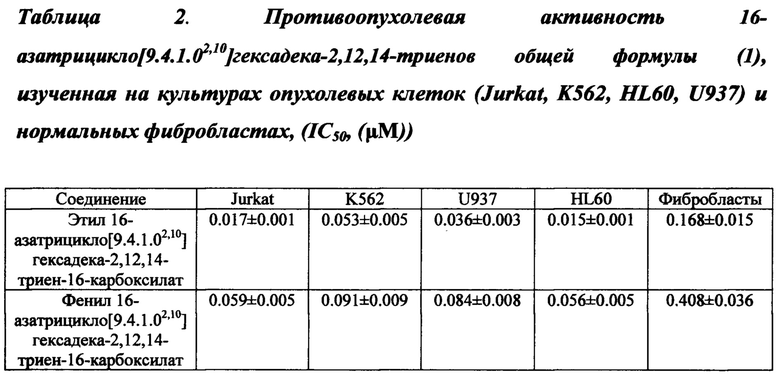
Установлено, что цитотоксическая активность имеет выраженный дозозависимый характер, индивидуально для каждого исследуемого соединения. В целом, значения ингибирующей концентрации IC50, полученные в результате экспозиции исследуемых соединений (1) на упомянутых выше клеточных линиях с последующим окрашиванием клеток красителем 7AAD варьируются в зависимости от клеточной культуры в интервале 0.015±0.001-0.091±0.009 μМ. 16-Азатрицикло[9.4.1.02,10]гексадека-2,12,14-триен, содержащий этоксикарбонильный заместитель показал более высокую цитотоксическую активность (IC50=0.015±0.001-0.053±0.005 μМ), нежели азатрицикл с феноксикарбонильным заместителем (IC50=0.056±0.005-0.091±0.009 μМ).
| название | год | авторы | номер документа |
|---|---|---|---|
| ЗАМЕЩЕННЫЕ 9-АЗАБИЦИКЛО [4.2.1]НОНА-2,4,7-ТРИЕНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ В КАЧЕСТВЕ СРЕДСТВ С ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2020 |
|
RU2751350C1 |
| ЗАМЕЩЕННЫЕ 9-АЗАБИЦИКЛО[4.2.1]НОНА-2,4,7-ТРИЕНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ В КАЧЕСТВЕ СРЕДСТВ С ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2020 |
|
RU2746853C1 |
| ЗАМЕЩЕННЫЕ (Е)-9-АЗАБИЦИКЛО[4.2.1]НОНА-2,4-ДИЕНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ В КАЧЕСТВЕ СРЕДСТВ С ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2020 |
|
RU2751352C1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ 1-ГИДРОКСИМЕТИЛ-ЗАМЕЩЕННЫХ БИЦИКЛО[4.2.1]НОНА-2,4,7-ТРИЕНОВ, ПРОЯВЛЯЮЩИХ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 2019 |
|
RU2735661C1 |
| СПОСОБ СОВМЕСТНОГО ПОЛУЧЕНИЯ 1-МЕТИЛ-ЗАМЕЩЕННЫХ БИЦИКЛО[4.2.1]НОНА-2,4,7-ТРИЕНОВ, ПРОЯВЛЯЮЩИХ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 2019 |
|
RU2735663C1 |
| СПОСОБ ПОЛУЧЕНИЯ (Е)-БИЦИКЛО[4.2.2]ДЕКА-2,4,7-ТРИЕНОВ | 2015 |
|
RU2605428C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИЦИКЛО[4.2.1]НОНА-2,4-ДИЕНОВ | 2013 |
|
RU2551278C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-СОДЕРЖАЩИХ БИЦИКЛО[4.2.1]НОНА-2,4,7-ТРИЕНОВ, ПРОЯВЛЯЮЩИХ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 2019 |
|
RU2735662C1 |
| СПОСОБ ПОЛУЧЕНИЯ Si-СОДЕРЖАЩИХ БИЦИКЛО[4.2.1]НОНА-2,4,7-ТРИЕНОВ, ПРОЯВЛЯЮЩИХ ПРОТИВООПУХОЛЕВУЮ АКТИВНОСТЬ | 2018 |
|
RU2726195C2 |
| СПОСОБ ПОЛУЧЕНИЯ БИС-(ЭНДО-БИЦИКЛО[4.2.1]НОНА-2,4-ДИЕНОВ) | 2013 |
|
RU2556007C2 |
Изобретение относится к области органического синтеза, конкретно, к 16-азатрицикло[9.4.1.02,10]гексадека-2,12,14-триенам формулы (1). Указанные соединения относятся к классу гетероциклических соединений и могут найти применение в качестве ключевых прекурсоров в синтезе ценных биологически активных соединений и современных лекарственных противоопухолевых препаратов. Соединения по изобретению получают путем взаимодействия N-замещенных азепинов формулы (а) (где R=Et, Ph) с 1,2-циклононадиеном (ЦНД) в присутствии катализатора Co(acac)2(dppe)/Zn/ZnI2 при мольном соотношении ЦНД : азепин : Co(acac)2(dppe) : Zn : ZnI2= (1.3-2.0):1:(0.05-0.15):(0.15-0.45):(0.1-0.3), в ампуле при 20-80°С, в 1,2-дихлорэтане в течение 20-48 ч. Технический результат - 16-азатрицикло[9.4.1.02,10]гексадека-2,12,14-триены формулы (1) в качестве средств с противоопухолевой активностью. 3 н.з. ф-лы, 2 табл., 2 пр.
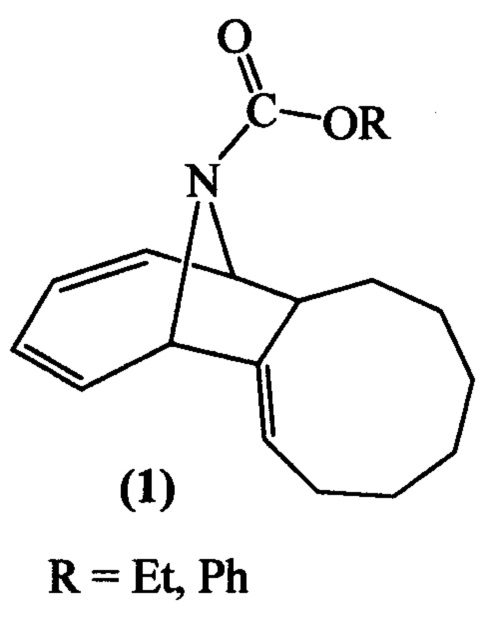 (1),
(1), 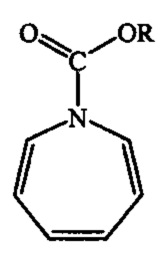 (а)
(а)
1. 16-Азатрицикло[9.4.1.02,10]гексадека-2,12,14-триены общей формулы (1):
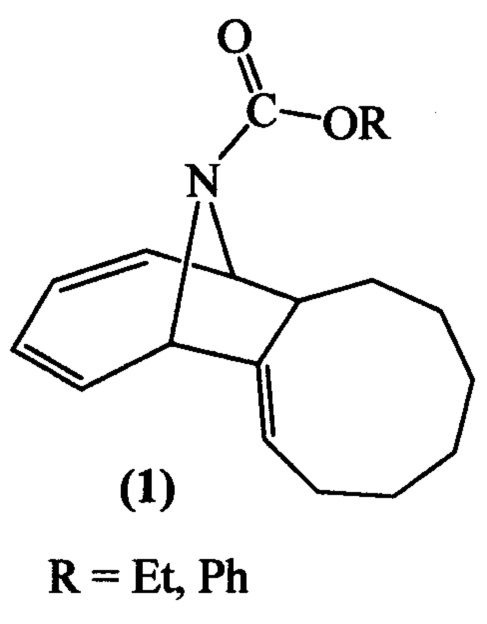
2. Способ каталитического получения 16-азатрицикло[9.4.1.02,10]гексадека-2,12,14-триенов общей формулы (1) по п.1, отличающийся тем, что реакцию проводят взаимодействием N-замещенных азепинов формулы 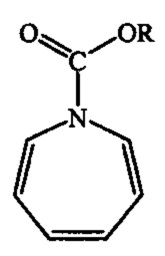 (где R=Et, Ph) с 1,2-циклононадиеном (ЦНД), в присутствии катализатора Co(acac)2(dppe)/Zn/ZnI2, при мольном соотношении ЦНД : азепин : Co(acac)2(dppe) : Zn : ZnI2= (1.3-2.0):1:(0.05-0.15):(0.15-0.45):(0.1-0.3), в ампуле при 20-80°С, в 1,2-дихлорэтане в течение 20-48 ч.
(где R=Et, Ph) с 1,2-циклононадиеном (ЦНД), в присутствии катализатора Co(acac)2(dppe)/Zn/ZnI2, при мольном соотношении ЦНД : азепин : Co(acac)2(dppe) : Zn : ZnI2= (1.3-2.0):1:(0.05-0.15):(0.15-0.45):(0.1-0.3), в ампуле при 20-80°С, в 1,2-дихлорэтане в течение 20-48 ч.
3. Применение 16-азатрицикло[9.4.1.02,10]гексадека-2,12,14-триенов формулы (1) по п.1 в качестве средств с противоопухолевой активностью.
| Howard L.Mansell: "Synthetic approaches to Anatoxin-a", TETRAHEDRON, 1996, vol.52, no.17, pp.6025-60-61 | |||
| Philip J.Parsons et al.: "Synthesis of (±)-Anatoxin-a and Analogues, TETRAHEDRON, 2000, vol.56, pp.309-315 | |||
| Дьяконов В | |||
| А | |||
| и др | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
Авторы
Даты
2021-02-10—Публикация
2020-07-02—Подача