Изобретение относится к способам получения селективных сорбентов для твердофазной экстракции производных пирролидона из биологических жидкостей. Изобретение может быть использовано для подготовки проб биологических жидкостей к идентификации анализируемых веществ хромато-масс-спектрометрическим методом.
Одним из вариантов изолирования определяемых веществ при проведении химико-токсикологического анализа является жидкость-жидкостная экстракция (ЖЖЭ). Данный вариант изолирования способствует увеличению потерь анализируемых веществ в связи с большим количеством различных этапов (фильтрация, очистка, изолирование анализируемых веществ методом ЖЖЭ в несколько стадий, концентрирование), использованием лабораторной посуды, материал которой сорбирует анализируемые вещества. Кроме этого, аналитик сталкивается с проблемами, связанными с недостаточной воспроизводимостью результатов измерения, низкой степенью извлечения и очистки определяемых компонентов.
Альтернативой ЖЖЭ является твердофазная экстракция (ТФЭ). Пробы большого объема могут быть обработаны с использованием сравнительно малых количеств твердой фазы, что в свою очередь требует малого объема растворителей для последующей десорбции сконцентрированных соединений, следовательно, отсутствует необходимость дополнительного концентрирования и существенно уменьшается риск загрязнения образца.
Для ТФЭ характерны более широкие возможности варьирования природы и силы взаимодействий образца с сорбентом и элюентом, чем для ЖЖЭ и, вследствие чего осуществляется более селективное и количественное извлечение анализируемого вещества. За счет специфических взаимодействий можно селективно концентрировать и извлекать каждое из определяемых соединений или отделять их от мешающих компонентов.
Известен способ получения сорбента, представляющего собой полимер, состоящий из некислотного мономера и сшивающего реагента, которые содержат полярные функциональные группы для анализа и выделения нитрозаминов из биологических жидкостей [1]. Способ реализуется при использовании двух моноалкенильных мономеров метакриловой кислоты, который является кислотным, 2-гидроксиэтилметакрилата (ГЭМА), который является нейтральным и двух сшивающих реагентов (ди- или триалкенильные мономеры), а именно, пентаэритриттриакрилат (ПЭТРА), который является гидрофильным, и этиленгликольдиметакрилата (ЭГДМА) который является гидрофобным. Для каждой комбинации, раствор для полимеризации предварительно готовят путем растворения моноалкенильного мономера, сшивающего реагента и радикального инициатора, такого как 2,2'-азобис-(2-метилпропионитрил) (АИБН), в хлороформе или другом апротонном растворителе. Раствор переносят в сосуд для полимеризации и герметизируют. Полимеризацию инициируют при 70°С и эту температуру поддерживают в течение 24 ч. Полученный полимер грубо измельчают, экстрагируют сначала смесью метанол: уксусная кислота 4:1 и затем метанолом для удаления непрореагировавших мономеров и сушат. Недостатком этого полимера является отсутствие диффузии внутрь объема полимера и эффективная работа только поверхности сорбента.
Известен способ получения молекулярно импринтированного полимера для селективного улавливания молекул пахучих веществ [2]. Используется метод радикальной полимеризацией в этаноле. Анализируемое соединение (Na-гексаноилглутамин) добавляют к комбинации мономера и сшивающего агента при концентрации анализируемого соединения 200 мкМ, т.е. 200 нмоль/мл. Смесь оставляют на 12 часов при комнатной температуре (25°С), а затем остаточное количество Na-гексаноилглутамина, не связанное с сорбентом, анализируют с помощью анализа способом жидкостной хроматографии, сопряженной с масс-спектрометрией (ВЭЖХ-МС/МС). Однако основными недостатком получаемого сорбента является относительно низкая емкость сорбента.
Наиболее близким решением является способ получения полимера с молекулярными отпечатками афлатоксина [3]. Способ включает в себя получение полимера методом радикальной полимеризации с применением афлатоксина (1,0 ммоль, темплат), метакриловой кислоты (2,0 ммоль, мономер) и ЭГДМА (5,0 ммоль, сшивающий агент) в смеси ацетонитрила и толуола (1:3 об./об.) при разных молярных отношениях афлатоксина относительно метакриловой кислоты и мономера относительно сшивающего агента. Раствор перемешивали в течении 1 часа при комнатной температуре. Далее добавляли АИБН (0,01 моль, инициатор) медленно нагревали и выдерживали в течение 30 мин при 60-65°С для осаждения микросфер полимера. Основным недостатком предложенного способа получения является низкая селективность полученного сорбента.
Задачей настоящего изобретения является получение селективного сорбента для ТФЭ производных пирролидона из биологических жидкостей.
Эта задача решается тем, что для получения сорбента используют комбинацию функциональных мономеров - метакриловую кислоту 0,25 г и диаллиламин 0,25 г; структурный мономер - акриламид 1,25 г, в качестве сшивающего агента используют N,N'-метилен-бис-акриламид 0,25 г; радикальную полимеризацию проводят в присутствии темплата - производного пирролидона 0,25 г в водной среде с последующим добавлением 0,1 г персульфата аммония, 100 мкл N,N,N',N'-тетраметилэтилендиамина, и дальнейшим охлаждением при +8°С; сорбент измельчают, промывают изопропиловым спиртом и хлороформом для удаления темплата из пор сорбента, сушат при комнатной температуре до постоянной массы и повторно измельчают до размеров частиц 500 мкм.
Преимуществом настоящего предложения является повышенная селективность полученного сорбента в связи с использованием заданных функциональных мономеров, сшивающих агентов, активаторов полимеризации и подобранных условий.
Способ реализуется следующим образом. Для получения сорбента используют комбинацию функциональных мономеров - метакриловую кислоту 0,25 г и диаллиламин 0,25 г; структурный мономер - акриламид 1,25 г, в качестве сшивающего агента используют N,N'-метилен-бис-акриламид 0,25 г; радикальную полимеризацию проводят в присутствии темплата - производного пирролидона 0,25 г в водной среде с последующим добавлением 0,1 г персульфата аммония, 100 мкл N,N,N',N'-тетраметилэтилендиамина, и дальнейшим охлаждением при +8°С; сорбент измельчают, промывают изопропиловым спиртом и хлороформом для удаления темплата из пор сорбента, сушат при комнатной температуре до постоянной массы и повторно измельчают до размеров частиц 500 мкм.
Заявляемый способ иллюстрируется следующим примером. В данном примере в качестве темплата используется фенилпирацетам. 0,25 г фенилпирацетама и 1,25 г акриламида (Sigma-Aldrich), растворяют в 25 мл воды очищенной при температуре 40°С. К полученному раствору прибавляют 0,25 г метакриловой кислоты (Sigma-Aldrich) и 0,25 г диаллиламина (Sigma-Aldrich). К полученной смеси прибавляют 0,25 г N,N'-метилен-бис-акриламида (Sigma-Aldrich), 0,1 г персульфата аммония (Sigma-Aldrich), 100 мкл N,N,N',N'-тетраметилэтилендиамина (Sigma-Aldrich) и перемешивают в течение 15 мин. Полученную смесь охлаждают до полной полимеризации при температуре +8°С, измельчают, последовательно промывают изопропиловым спиртом и хлороформом для удаления темплата из пор сорбента, сушат при комнатной температуре до постоянной массы и измельчают полученный сорбент до размеров частиц 500 мкм.
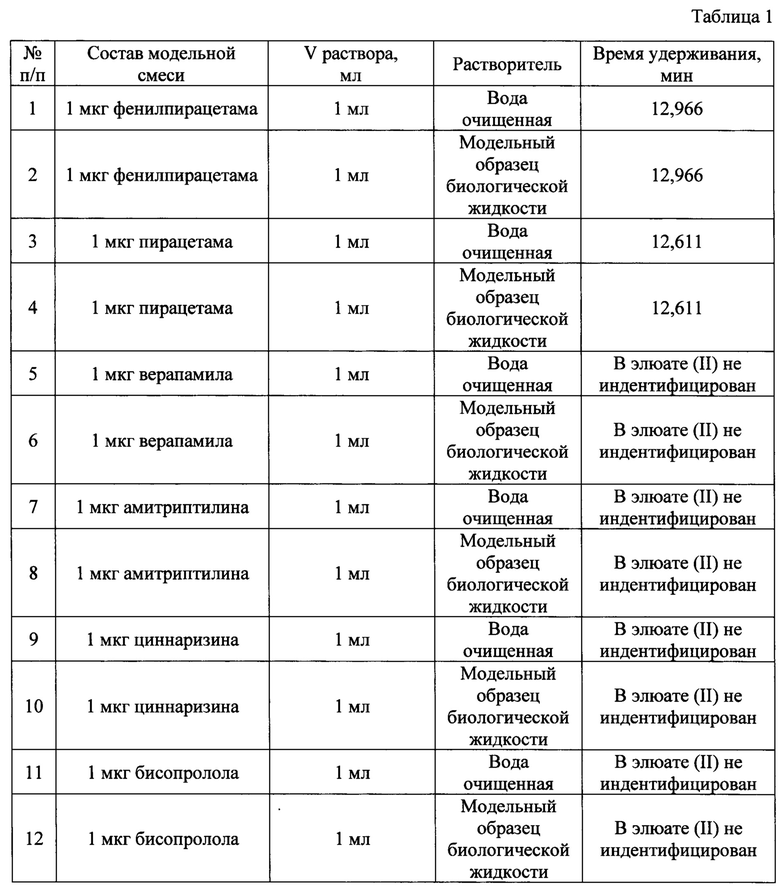
Далее проводили структурные исследования полученного сорбента методом ИК-спектрометрии с Фурье-преобразованием на спектрометре Agilent Technologies Сагу 630 FTIR. ИК - спектрометрию выполняли в соответствии с методикой ОФС.1.2.1.1.0002.15 «Спектрометрия в инфракрасной области» для твердых веществ. Идентификацию компонентов проводили с использованием эталонных спектров [4]. Спектр поглощения представлен на Фиг. 1. Красная линия - спектр поглощения полученного сорбента, синяя линия - библиотечный спектр поглощения карбоксимодифицированного полиакриламида. Наличие выраженных пиков при 1451, 1660, 2934, 3198, 3343 см-1 свидетельствует о наличии карбоксимодифицированной полиакриламидной матрице в образце полученного сорбента.
Далее проводили серию экспериментов по определению селективности полученного сорбента при помощи модельных смесей. Составы модельных смесей представлены в таблице 1. В качестве компонентов модельных смесей были выбраны вещества близкие по химической структуре - пирацетам, и вещества других химических групп - верапамил, циннаризин, бисопролол, амитриптилин. Метод анализа - газовая хроматография с масс-селективным детектированием. Анализ проводили на газовом хроматографе Agilent Technologies 7890 с масс-селективным детектором Agilent Technologies 5975. Хроматографическое разделение компонентов пробы проводили на капиллярной колонке HP-5MS (30 мХ250 ммХ0.25 мм). Газ носитель - гелий с постоянной скоростью потока 1,5 мл/мин. Температурный режим в хроматографической печи: 1 минута 100°С, с дальнейшим нагреванием до 190°С со скоростью 12°С в минуту и поддержанием заданной температуры в течении 9 минут. Энергия ионизации масс-спектрометра 70 eV. Температура источника ионов 280°С. Объем пробы каждой модельной смеси, вводимой в инжектор хроматографа, составлял 1 мкл, режим Split (1:25).
1 мл модельной смеси пропускают через колонку с предварительно подготовленным сорбентом и элюируют 10 мл воды. Полученный элюат (I) отбрасывают, колонку сушат при комнатной температуре. Далее колонку элюируют 2 мл изопропилового спирта, элюат (II) собирают и упаривают. Сухой остаток реконструируют 2 мл этилацетата и вводят в инжектор хроматографа пробу объемом 1 мкл. Результаты эксперимента представлены в таблице 1. В элюате (II) при проведении газохроматографического исследования модельной смеси 1 и 2 производные пирролидона были идентифицированы, время удерживания составило 12,966 мин для фенилпирацетама и 12,611 мин для пирацетама соответственно. При проведении исследований элюатов (II) прочих модельных смесей хроматографические пики компонентов смесей отсутствовали на хроматограммах.
Результат подтверждали путем ГХ-МС исследования образцов биологической жидкости (моча) с добавлением фенилпирацетама, пирацетама, верапамила, циннаризина, бисопролола и амитриптилина по аналогичной методике подготовки проб и условиям проведения исследования.
Полученные данные свидетельствуют о высоком уровне селективности полученного сорбента к целевым анализируемым веществам.
Результатом является получение селективного сорбента для ТФЭ производных пирролидона из биологических жидкостей.
Способ может быть использован для подготовки проб биологических жидкостей к идентификации анализируемых веществ хромато-масс-спектрометрическим методом.
ИСТОЧНИКИ ИНФОРМАЦИИ:
1. Биллинг Юхан Фредрик, Свенссон-Старк Ян Роберт Кристиан, Йильмаз Эсевит, Карлссон Ула Йон Ивар. Селективное отделение нитрозосодержащих соединений. Патент РФ 2622410 С2, 15.06.2017 г. Бюл. 2017. №17.
2. Гривз Эндрю, Манфре Франко, Хаупт Карстен, Тсе Сум Буи Жанна Бернадетт. Молекулярно импринтированный полимер для селективного улавливания молекул пахучих веществ. Патент РФ 2731379 С2, 02.09.2020 г. Бюл. 2020. №25.
3. Нянникурис Александров Еррамредди Тирупати Р., Мартинес Джошуа Дж., Уитерс Джеффри Р. Шаблоны афлатоксина, полимеры с молекулярными отпечатками и способы их получения и применения. Патент РФ №2705210 С2, 06.11.2019 г. Бюл. 2019. №31.
4. Купцов А.Х., Жижин Г.Н. Фурье-КР и Фурье-ИК спектры полимеров - Москва: ООО «Техносфера», 2013. - 696 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ НАНОКОМПОЗИТНОГО СОРБЕНТА ДЛЯ ЗАСУШЛИВЫХ ПОЧВ | 2016 |
|
RU2622430C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСПЕЦИФИЧЕСКОГО ПОЛИМЕРНОГО СОРБЕНТА ДЛЯ ВЫДЕЛЕНИЯ ПРОТЕИНАЗ | 2010 |
|
RU2420739C1 |
| СОСТАВ НАНОКОМПОЗИТНОГО СОРБЕНТА ДЛЯ ЗАСУШЛИВЫХ ПОЧВ | 2016 |
|
RU2623769C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСПЕЦИФИЧЕСКОГО АДСОРБЕНТА | 1979 |
|
SU803193A1 |
| Способ получения селективного сорбента для твердофазной экстракции | 2020 |
|
RU2765188C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОСПЕЦИФИЧЕСКОГО ГИДРОГЕЛЕВОГО СОРБЕНТА ДЛЯ ВЫДЕЛЕНИЯ ПРОТЕИНАЗ | 2012 |
|
RU2484475C1 |
| СПОСОБ ПОЛИМЕРИЗАЦИОННОЙ ИММОБИЛИЗАЦИИ БИОЛОГИЧЕСКИХ МАКРОМОЛЕКУЛ И КОМПОЗИЦИЯ ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2001 |
|
RU2216547C2 |
| СПОСОБ ПОЛУЧЕНИЯ СШИТОГО ГИДРОФИЛЬНОГО ПОЛИМЕРА, ПРОЯВЛЯЮЩЕГО СВОЙСТВА СУПЕРАБСОРБЕНТА | 2011 |
|
RU2467017C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИМЕРОВ С ВЫСОКИМ ВОДОПОГЛОЩЕНИЕМ | 1993 |
|
RU2083596C1 |
| Метод получения суспензии, содержащей частицы микрогеля для закрепления почв и грунтов | 2017 |
|
RU2670968C1 |
Изобретение относится к способу получения селективного сорбента для твердофазной экстракции производных пирролидона из биологических жидкостей методом радикальной полимеризации функционального мономера – метакриловой кислоты – при перемешивании. Для получения сорбента используют комбинацию функциональных мономеров – метакриловую кислоту 0,25 г и диаллиламин 0,25 г; структурный мономер – акриламид 1,25 г. В качестве сшивающего агента используют N,N'-метилен-бис-акриламид 0,25 г. Радикальную полимеризацию проводят в присутствии темплата – производного пирролидона 0,25 г в водной среде с последующим добавлением 0,1 г персульфата аммония, 100 мкл N,N,N',N'-тетраметилэтилендиамина и дальнейшим охлаждением при +8°С. Сорбент измельчают, промывают изопропиловым спиртом и хлороформом для удаления темплата из пор сорбента, сушат при комнатной температуре до постоянной массы и повторно измельчают до размеров частиц 500 мкм. Технический результат: повышенная селективность полученного сорбента. 1 ил., 1 табл., 1 пр.
Способ получения селективного сорбента для твердофазной экстракции производных пирролидона из биологических жидкостей методом радикальной полимеризации функционального мономера - метакриловой кислоты - при перемешивании, отличающийся тем, что для получения сорбента используют комбинацию функциональных мономеров - метакриловую кислоту 0,25 г и диаллиламин 0,25 г; структурный мономер - акриламид 1,25 г, в качестве сшивающего агента используют N,N'-метилен-бис-акриламид 0,25 г; радикальную полимеризацию проводят в присутствии темплата - производного пирролидона 0,25 г в водной среде с последующим добавлением 0,1 г персульфата аммония, 100 мкл N,N,N',N'-тетраметилэтилендиамина и дальнейшим охлаждением при +8°С; сорбент измельчают, промывают изопропиловым спиртом и хлороформом для удаления темплата из пор сорбента, сушат при комнатной температуре до постоянной массы и повторно измельчают до размеров частиц 500 мкм.
| ШАБЛОНЫ АФЛАТОКСИНА, ПОЛИМЕРЫ С МОЛЕКУЛЯРНЫМИ ОТПЕЧАТКАМИ И СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2015 |
|
RU2705210C2 |
| МОЛЕКУЛЯРНО ИМПРИНТИРОВАННЫЙ ПОЛИМЕР ДЛЯ СЕЛЕКТИВНОГО УЛАВЛИВАНИЯ МОЛЕКУЛ ПАХУЧИХ ВЕЩЕСТВ | 2013 |
|
RU2731379C2 |
| СЕЛЕКТИВНОЕ ОТДЕЛЕНИЕ НИТРОЗОСОДЕРЖАЩИХ СОЕДИНЕНИЙ | 2012 |
|
RU2622410C2 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
Авторы
Даты
2021-04-28—Публикация
2020-09-21—Подача