Изобретение относится к области аналитической химии и может быть использовано в фармацевтической, химической и других отраслях промышленности при определении парабенов (эфиров 4-гидроксибензойной кислоты) методом капиллярной газо-жидкостной хроматографии (ГЖХ) в лекарственных препаратах с использованием пламенно-ионизационного детектора.
Известен аналог изобретения – способ хроматографического определения парабенов в жидких и суспензионных фармацевтических препаратах и жидких биологически активных добавках (патент РФ № 2532237). Данное изобретение позволяет в одном анализе проводить качественное и количественное определение метил-, этил-, пропил- и бутилпарабена методом высокоэффективной жидкостной хроматографии на обращенно-фазовом сорбенте с использованием спектрофотометрического или(и) диодно-матричного детекторов в образцах жидких и суспензионных фармацевтических препаратов и биологически активных добавок с предварительной пробоподготовкой (разведение образца и фильтрование через мембранный фильтр с диаметром пор не более 0,5 мкм). К недостаткам этого аналога следует отнести длительность хроматографического анализа (более 30 мин) и относительно высокую себестоимость анализа из-за использования предколонки и реактивов для приготовления подвижной фазы.
Также известен аналог изобретения – газохроматографическое определение парабенов с применением масс-спектрометрического детектора (Bajaj А., John C., Choudhury J., Tripathi R.M. Development and Validation of Gas Chromatography/Mass Spectrometry Method for the Simultaneous Determination of Some Preservatives in Personal Care, Cosmetics and Pharmaceutical Formulations. Research J. Science and Tech. 2017; 9(3): 308–312). Он включает в себя растворение образцов в растворе NaCl (pH 2), выдерживание в ультразвуковой ванне в течение 20 мин, фильтрацию, троектратную экстракцию этилацетатом, обезвоживание, последующую экстракцию метанолом и фильтрацию с последующим газохроматографическим анализом. К недостаткам такого определения парабенов следует отнести длительную пробоподготовку, а также использование масс-спектрометрического детектора, которые существенно увеличивают себестоимость анализа, что осложняет его внедрение в производственную практику в качестве рутинного анализа.
Известен другой способ газохроматографического определения парабенов с применением масс-спектрометрического детектора (Canosa P., Rodriguez I., Rubi E., Cela R. Determination of Parabens and Triclosan in Indoor Dust Using Matrix Solid-Phase Dispersion and Gas Chromatography with Tandem Mass Spectrometry. Anal. Chem. 2007; 79: 1675–1681). Его сущность заключается в получении производных (дериватизации) с N-метил-N-(трет-бутилдиметилсилил)трифторацетамидом и последующем хроматографическом определении. К недостаткам этого аналога следует отнести необходимость контроля полноты получения производных, а также увеличение себестоимости анализа из-за использования дериватизирующих агентов и масс-спектрометрического детектирования.
В качестве прототипа выбран способ количественного определения метилпарабена и пропилпарабена в лекарственном препарате «Лома Люкс Псориасис», сущность которого состоит в экстракции парабенов хлороформом с последующим газохроматографическим определением c использованием насадочной колонки, заполненной частицами диатомитового носителя «Хромосорб AW-HMCS» (основа – кремнезем), модифицированного на 3 % полиэтиленгликоля адипинатом (ПЭГА) и на 1 % ортофосфорной кислотой. К недостаткам прототипа следует отнести низкие чувствительность и разрешающую способность хроматографического метода, а также относительно длительное время анализа.
Технической проблемой является необходимость проведения процесса дериватизации для получения летучих производных парабенов, низкие разрешающая способность и чувствительность хроматографического метода, длительное время анализа.
Техническим результатом изобретения является повышение точности и чувствительности определения в смеси индивидуальных парабенов (эфиров 4-гидроксибензойной кислоты) с высокой разрешающей способностью методом капиллярной ГЖХ в лекарственных препаратах в лекарственных формах «раствор для приема внутрь гомеопатический», «гель для наружного применения», «мазь для наружного применения», «аэрозоль для наружного применения».
Достижение технического результата обеспечивается благодаря следующим техническим решениям:
- использование капиллярной колонки, модифицированной тонкой пленкой гидрофобного полидиметилсилоксана, что позволяет регистрировать на хроматограммах пики с хорошими хроматографическими параметрами (асимметрия пика составляет 1,0, высокие эффективность колонки и разрешение между пиками) и, соответственно, повышает точность получаемых результатов количественного определения;
- выбор хроматографических условий с высокими температурами различных элементов хроматографической системы и скоростью потока газа-носителя, возможных только в системе с капиллярной колонкой, что исключает стадию получения летучих производных парабенов и, как следствие, сокращает время анализа и трудозатраты;
- использование системы деления потока газа-носителя позволяет улучшить симметрию пиков, повысить эффективность хроматографической колонки и снизить уровень шума, что приводит к повышению чувствительности определения парабенов.
В заявляемом изобретении способ определения парабенов (эфиров 4-гидроксибензойной кислоты) методом капиллярной ГЖХ в лекарственных препаратах в лекарственных формах «раствор для приема внутрь гомеопатический», «гель для наружного применения», «мазь для наружного применения», «аэрозоль для наружного применения» реализуется следующим образом.
Пробоподготовка
Для приготовления стандартных растворов точные навески стандартных образцов метилпарабена и пропилпарабена (около 0,02 г каждого) помещают в мерную колбу вместимостью 20 мл, растворяют в хлороформе и доводят объем раствора до метки с целью получения концентрации, соответствующей номинальному количеству парабенов в лекарственном препарате, в котором следует определять их содержание.
Пробоподготовку испытуемого раствора лекарственного препарата осуществляют посредством экстракции. Для этого к 4 мл предварительно полученного испытуемого раствора лекарственного препарата добавляют 5 мл хлороформа и перемешивают на орбитальном шейкере в течение 10 мин при 400 об/мин для увеличения полноты экстракции парабенов в хлороформ.
Получение испытуемого раствора лекарственного препарата зависит от его лекарственной формы:
1. В случае лекарственной формы «раствор для приема внутрь гомеопатический» для экстракции используют сам лекарственный препарат непосредственно (4 мл в соответствии с описанием выше).
2. Испытуемый раствор лекарственного препарата в лекарственной форме «гель для наружного применения» готовят посредством растворения навески около 0,3 г геля в 5 мл воды на вортексе в течение 2 мин со скоростью 1250 об/мин. Отбирают 4 мл полученного раствора и проводят пробоподготовку в соответствии с описанием выше.
3. Испытуемый раствор лекарственного препарата в лекарственной форме «мазь для наружного применения» готовят посредством помещения около 0,6 г мази в 10 мл воды, прогрева при 37 °С на водяной бане в течение 10 мин, перемешивания на вортексе 5 мин со скоростью 2000 об/мин, обработки в ультразвуковой ванне в течение 30 мин и фильтрации полученного раствора через мембранный пористый фильтр из регенерированной целлюлозы с диаметром пор 0,45 мкм. Отбирают 4 мл полученного раствора и проводят пробоподготовку в соответствии с описанием выше. Затем отбирают еще 4 мл полученного раствора лекарственного препарата и готовят испытуемый раствор с добавкой посредством экстракции в 5 мл стандартного раствора метилпарабена и пропилпарабена в хлороформе.
4. Испытуемый раствор лекарственного препарата в лекарственной форме «аэрозоль для наружного применения» готовят следующим образом: извлекают массу лекарственного препарата из флакона под давлением, навеску около 0,5 г помещают в мерную колбу вместимостью 50 мл, растворяют в 35 мл воды на вортексе в течение 2 мин со скоростью 1500 об/мин, затем на ультразвуковой ванне в течение 30 мин, затем хранят при температуре 4 °С для исключения вспенивания раствора в течение 1 ч. Полученный объем раствора при комнатной температуре доводят водой до объема 50 мл. Отбирают 4 мл полученного раствора и проводят пробоподготовку в соответствии с описанием выше. Затем отбирают еще 4 мл полученного раствора лекарственного препарата и готовят испытуемый раствор с добавкой посредством экстракции в 5 мл стандартного раствора метилпарабена в хлороформе.
Количественное определение метилпарабена и пропилпарабена проводят на газовом хроматографе Agilent 7890B с пламенно-ионизационным детектором, оснащенном автосамплером Agilent G4513A (Agilent Technologies, США). Регистрирацию хроматограммы и обработку результатов проводят с помощью программного обеспечения Open Lab версии 2.2.
Колонка (неподвижная фаза): DB-1 (30 м × 0,32 мм, 3,0 мкм), представляющая собой кварцевый капилляр, внутренние стенки которого модифицированы 100 % полидиметилсилоксаном (Agilent Technologies, США).
Газ-носитель (подвижная фаза): гелий.
Хроматографические условия представлены в Таблице 1.
Таблица 1
(30 м × 0,32 мм, 3,0 мкм)
В случае лекарственных форм «раствор для приема внутрь гомеопатический» и «гель для наружного применения» стандартный и испытуемый растворы последовательно инжектируют с помощью шприца автосемплера в инжектор, где происходит испарение пробы. Для лекарственных форм «аэрозоль для наружного применения» и «мазь для наружного применения» инжектируют испытуемый раствор лекарственного препарата и такой же раствор лекарственного препарата с добавленным известным количеством определяемого парабена (с «добавкой»). Идентификацию парабенов проводят по временам удерживания. Время удерживания метилпарабена – около 4,0 мин, время удерживания пропилпарабена – около 6,4 мин.
Аналитический диапазон составляет 0,005–1,450 мг/мл для метилпарабена и пропилпарабена в хлороформе, коэффициенты корреляции полученных зависимостей аналитического сигнала от концентрации парабенов для метилпарабена – 0,9997, для пропилпарабена – 0,9991.
Количественный расчет концентраций парабенов проводят методом внешнего стандарта для гидрофильных лекарственных форм («раствор для приема внутрь гомеопатический», «гель для наружного применения»), используя градуировочную зависимость площади пика парабена от его концентрации в стандартном растворе. Содержание парабена рассчитывают из измеренного аналитического сигнала (площади пика) с помощью обратной функции.
Для лекарственных форм с более сложной матрицей («мазь для наружного применения», «аэрозоль для наружного прменения») используют метод добавок для того, чтобы учесть влияние матрицы на оценку результата. Расчет производят по следующей формуле:
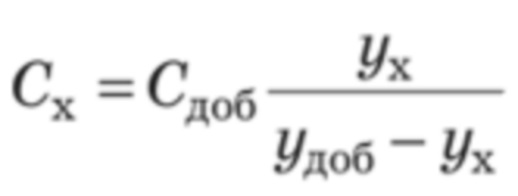
Сх – концентрация определяемого парабена в испытуемом растворе, мг/мл;
Сдоб – концентрация добавки парабена, мг/мл;
ух – площадь пика определяемого парабена на хроматограмме испытуемого раствора;
удоб – площадь пика на хроматограмме испытуемого раствора с «добавкой».
Существенными отличительными признаками заявляемого изобретения являются:
- сокращение времени элюирования парабенов за счет использования капиллярной колонки, модифицированной тонкой пленкой гидрофобного полидиметилсилоксана, вместо использования насадочной колонки, заполненной частицами более гидрофильного сорбента, представляющего собой диатомитовый носитель «Хромосорб AW-HMCS» (основа – кремнезем), модифицированный на 3 % полиэтиленгликоля адипинатом (ПЭГА) и на 1 % ортофосфорной кислотой (время проведения хроматографического анализа заявляемым способом 7 мин);
- повышение точности получаемых результатов количественного определения за счет интегрирования на хроматограммах пиков с лучшими параметрами (асимметрия пика, эффективность, разрешение между пиками);
- сокращение времени анализа и трудозатрат за счет исключения стадии получения летучих производных парабенов с помощью подбора хроматографических условий с высокими температурами различных элементов хроматографической системы и скоростью потока газа-носителя, возможных только в системе с капиллярной колонкой;
- повышение чувствительности определения, за счет уменьшения объема жидкой пробы при использовании специфического свойства системы капиллярной ГЖХ – разделения потока газа-носителя.
Краткое описание чертежей и иных материалов:
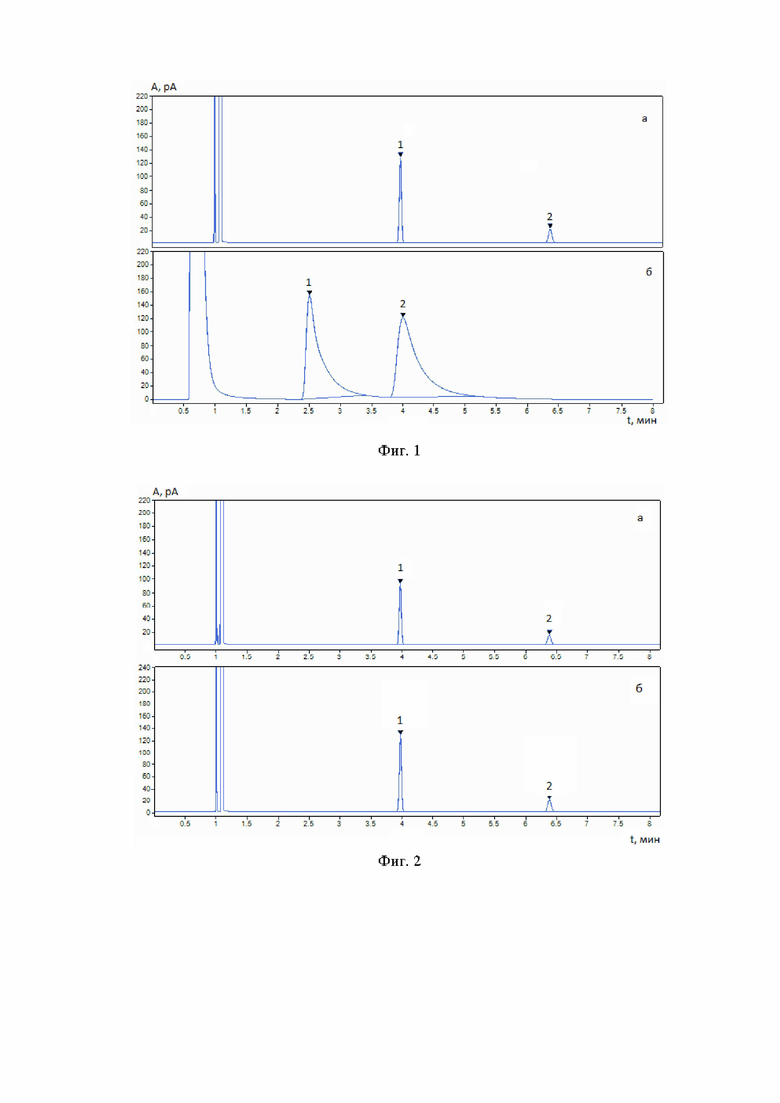
Фиг. 1. Хроматограммы стандартного раствора метилпарабена (1) и пропилпарабена (2), полученные на капиллярной (а) колонке заявляемым способом и на насадочной (б) колонке способом прототипа.
Фиг. 2. Хроматограммы образца лекарственного препарата «Лома Люкс Псориасис» в лекарственной форме «раствор для приема внутрь гомеопатический» (а) и стандартного раствора (б), полученные заявляемым способом: метилпарабен (1) и пропилпарабен (2).
Фиг. 3. Хроматограммы определения метилпарабена в образце лекарственного препарата «Далацин» в лекарственной форме «гель для наружного применения» (а) и стандартного раствора (б), полученные заявляемым способом.
Фиг. 4. Хроматограммы определения метилпарабена в образце лекарственного препарата «Пантенол» в лекарственной форме «аэрозоль для наружного применения» (а) и образца этого же препарата с добавкой метилпарабена (б), полученные заявляемым способом.
Фиг. 5. Хроматограммы образца лекарственного препарата «Офломелид» в лекарственной форме «мазь для наружного применения» (а) и образца этого же препарата с добавкой метилпарабена и пропилпарабена (б), полученные заявляемым способом: метилпарабен (1) и пропилпарабен (2).
Фиг. 6. Хроматограмма тестовой смеси метилпарабена (1), этилпарабена (2), пропилпарабена (3) и бутилпарабена (4).
Возможность осуществления заявляемого изобретения показана следующими примерами.
Пример 1. Сопоставление хроматографических параметров пиков метилпарабена и пропилпарабена на хроматограммах и разрешения между пиками, полученных заявляемым способом и способом прототипа (Таблица 2).
Таблица 2
способом прототипа
Приготовление стандартных растворов с концентрацией каждого определяемого парабена 1,2 мг/мл проводят в соответствии с описанием изобретения.
Полученный стандартный раствор подвергают хроматографированию в условиях заявляемого способа, приведенных в Таблице 1.
Как видно из Фиг. 1, эффективность и разрешающая способность газо-хроматографического разделения парабенов в случае использования насадочной колонки значительно ниже (900 теоретических тарелок, разрешение между пиками 3,4), чем в заявляемом способе (57500 теоретических тарелок, разрешение между пиками 27,3). Факторы асимметрии для метилпарабена и пропилпарабена в случае использования способа прототипа составляют 4,4 и 3,1 соответственно, при использовании заявляемого способа – 1,0 для обоих пиков.
Чувствительность хроматографической системы ниже при использовании колонки прототипа. Высоты пиков сопоставимы с таковыми для капиллярной колонки при одном и том же объеме ввода 1 мкл (но в последнем случае в колонку попадает 1/40 мкл раствора).
При сопоставимой высоте хроматографические пики при использовании колонки прототипа гораздо шире и менее симметричны. В заявляемом способе можно снизить количество инжектируемой пробы и получать симметричные пики, которые можно по-прежнему точно проинтегрировать и получить достоверный результат. Размытые широкие пики, полученные на колонке прототипа, этого сделать не позволяют, и потому требуется инжекция большего количества пробы, т.е. способ прототипа обладает более низкой чувствительностью по сравнению с заявляемым способом.
Данный пример подтверждает повышение эффективности и чувствительности хроматографической системы, благодаря разрешению между пиками и улучшению их симметрии.
Пример 2. Количественное определение метилпарабена и пропилпарабена в лекарственном препарате «Лома Люкс Псориасис» в лекарственной форме «раствор для приема внутрь гомеопатический» заявляемым способом (Фиг. 2).
Приготовление стандартного раствора с концентрацией каждого определяемого парабена 1,4 мг/мл проводят в соответствии с описанием изобретения.
Пробоподготовку испытуемого раствора лекарственного препарата осуществляют в соответствии с описанием изобретения.
Количественное определение метилпарабена и пропилпарабена, а также обработку результатов проводят в соответствии с описанием изобретения. Последовательно инжектируют стандартный и испытуемый раствор соответственно.
Установлено содержание метилпарабена 1,38 мг/мл – 91,7 % от номинального (относительное стандартное отклонение – RSD – составило 1,6 %), содержание пропилпарабена – 0,30 мг/мл – 100,3 % от номинального (RSD – 0,9 %).
Пример 3. Количественное определение метилпарабена в лекарственном препарате «Далацин» в лекарственной форме «гель для наружного применения» заявляемым способом (Фиг. 3).
Приготовление стандартного раствора с концентрацией метилпарабена 0,1 мг/мл проводят в соответствии с описанием изобретения.
Пробоподготовку испытуемого раствора лекарственного препарата осуществляют в соответствии с описанием изобретения.
Количественное определение метилпарабена, а также обработку результатов проводят в соответствии с описанием изобретения. Последовательно инжектируют стандартный и испытуемый раствор соответственно.
Установлено содержание метилпарабена 2,82 мг/г – 94,0 % от номинального (RSD – 1,7 %).
Пример 4. Количественное определение метилпарабена и пропилпарабена в лекарственном препарате «Офломелид» в лекарственной форме «мазь для наружного применения» заявляемым способом (Фиг. 4).
Приготовление стандартного раствора с концентрацией метилпарабена 0,05 мг/мл и пропилпарабена 0,02 мг/мл проводят в соответствии с описанием изобретения.
Пробоподготовку испытуемого раствора лекарственного препарата осуществляют в соответствии с описанием изобретения.
Для приготовления раствора с добавкой 4 мл полученного раствора экстрагируют 5 мл раствора метилпарабена и пропилпарабена в хлороформе с концентрацией 0,05 мг/мл и 0,02 мг/мл соответственно. Расчет содержания парабенов осуществляют по формуле метода добавок в соответствии с описанием изобретения.
Установлено содержание метилпарабена 0,73 мг/г – 91,3 % от номинального (RSD – 1,9 %), пропилпарабена 0,18 мг/г – (RSD – 2,3 %).
Пример 5. Количественное определение метилпарабена в лекарственном препарате «Пантенол» в лекарственной форме «аэрозоль для местного применения» заявляемым способом (Фиг. 5).
Приготовление стандартного раствора с концентрацией метилпарабена 0,02 мг/мл проводят в соответствии с описанием изобретения.
Пробоподготовку испытуемого раствора лекарственного препарата осуществляют в соответствии с описанием изобретения.
Для приготовления раствора с добавкой 4 мл полученного раствора экстрагируют 5 мл раствора метилпарабена в хлороформе с концентрацией 0,02 мг/мл. Расчет содержания метилпарабена осуществляют по формуле метода добавок в соответствии с описанием изобретения.
Установлено содержание метилпарабена 1,82 мг/г – 91,0 % от номинального (RSD – 1,3 %).
Таким образом, примеры 2–5 демонстрируют возможность применения заявляемого способа при определении парабенов в разнообразных лекарственных препаратах в разных лекарственных формах.
Пример 6. Применение заявляемого способа для разделения многокомпонентной смеси парабенов.
Готовят тестовую смесь из метил-, этил-, пропил- и бутилпарабена в хлороформе (концентрация каждого соединения составила 1,25 мг/мл).
Смесь подвергают хроматографированию в условиях заявляемого способа. Парабены разделяют с разрешением до 18,1 за 9 мин (Фиг. 6), при этом фактор асимметрии пиков составляет 1,0, а эффективность системы – до 58900 теоретических тарелок.
Данный пример демонстрирует разделение многокомпонентной смеси из большего количества парабенов заявляемым способом.
Представленные примеры не ограничивают объем притязаний заявляемого изобретения и служат только для цели иллюстрации.


Изобретение относится к области аналитической химии и может быть использовано для определении парабенов в лекарственных препаратах. Способ определения парабенов в лекарственных препаратах методом капиллярной газо-жидкостной хроматографии включает приготовление стандартного раствора парабенов в хлороформе в концентрации, соответствующей ожидаемой концентрации в анализируемом лекарственном препарате, экстракцию 4 мл испытуемого раствора лекарственного препарата добавлением 5 мл хлороформа, последующее перемешивание на орбитальном шейкере в течение 10 мин при 400 об/мин и последующее хроматографирование подготовленных образцов на капиллярной колонке в подобранных хроматографических условиях с использованием пламенно-ионизационного детектора, идентификацию парабенов по временам удерживания и количественный расчет концентраций парабенов методом внешнего стандарта. Техническим результатом является возможность элюировать парабены быстрее и получать на хроматограммах пики с лучшими хроматографическими параметрами. 4 з.п. ф-лы, 6 ил., 2 табл.
1. Способ определения парабенов в лекарственных препаратах методом капиллярной газо-жидкостной хроматографии, включающий приготовление стандартного раствора парабенов в хлороформе в концентрации, соответствующей ожидаемой концентрации в анализируемом лекарственном препарате, экстракцию 4 мл испытуемого раствора лекарственного препарата добавлением 5 мл хлороформа, последующее перемешивание на орбитальном шейкере в течение 10 мин при 400 об/мин и последующее хроматографирование подготовленных образцов на капиллярной колонке в подобранных хроматографических условиях с использованием пламенно-ионизационного детектора, идентификацию парабенов по временам удерживания и количественный расчет концентраций парабенов методом внешнего стандарта.
2. Способ по п. 1, отличающийся тем, что испытуемый раствор лекарственного препарата в лекарственной форме «гель для наружного применения» готовят посредством растворения навески около 0,3 г геля в 5 мл воды на вортексе в течение 2 мин со скоростью 1250 об/мин.
3. Способ по п. 1, отличающийся тем, что испытуемый раствор лекарственного препарата в лекарственной форме «мазь для наружного применения» готовят посредством помещения около 0,6 г мази в 10 мл воды, прогрева при 37 °С на водяной бане в течение 10 мин, перемешивания на вортексе 5 мин со скоростью 2000 об/мин, обработки в ультразвуковой ванне в течение 30 мин, фильтрации полученного раствора через мембранный пористый фильтр из регенерированной целлюлозы с диаметром пор 0,45 мкм с последующим количественным расчетом содержания парабенов методом добавок.
4. Способ по п. 1, отличающийся тем, что испытуемый раствор лекарственного препарата в лекарственной форме «аэрозоль для наружного применения» готовят посредством извлечения массы лекарственного препарата из флакона под давлением, помещения навески около 0,5 г в мерную колбу вместимостью 50 мл, растворения в 35 мл воды на вортексе в течение 2 мин со скоростью 1500 об/мин, затем на ультразвуковой ванне в течение 30 мин, хранения при температуре 4 °С для исключения вспенивания раствора в течение 1 ч, доведения полученного объема раствора при комнатной температуре водой до объема 50 мл с последующим количественным расчетом содержания парабенов методом добавок.
5. Способ по п. 1, отличающийся тем, что капиллярная колонка модифицирована 100% полидиметилсилоксаном, с параметрами 30 м × 0,32 мм, толщиной модифицирующей пленки 3 мкм.
| ОСИПОВ А.С., ПОПОВА О.А., СУЛИМЕНКОВА А.И., НЕЗДОЛЬЕВА М.В | |||
| "ПРИМЕНЕНИЕ ЖИДКОСТНОЙ ХРОМАТОГРАФИИ ГИДРОФИЛЬНЫХ ВЗАИМОДЕЙСТВИЙ ДЛЯ АНАЛИЗА ПАРАБЕНОВ", РАЗРАБОТКА И РЕГИСТРАЦИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ N1, РР.104-107, 2017 | |||
| СПОСОБ ХРОМАТОГРАФИЧЕСКОГО АНАЛИЗА ПАРАБЕНОВ (ЭФИРОВ 4-ГИДРОКСИБЕНЗОЙНОЙ КИСЛОТЫ) В ПРОДУКТАХ ПИТАНИЯ, КОСМЕТИКЕ, ФАРМАЦЕВТИЧЕСКИХ ПРЕПАРАТАХ И БИОЛОГИЧЕСКИ АКТИВНЫХ ДОБАВКАХ | 2013 |
|
RU2532237C1 |
| CN 103115884 A, 22.05.2013 | |||
| КУРАКИНА В.С., МЕДВЕДЕВА О.М., ДМИТРИЕНКО С.Г., ШПИГУН О.А | |||
| "ОПРЕДЕЛЕНИЕ | |||
Авторы
Даты
2021-05-04—Публикация
2020-09-01—Подача