Настоящее техническое решение относится к области химии, фармации, медицине, косметологии и может быть использовано в фармацевтической, косметологической, химической и в смежных отраслях промышленности и научно-исследовательской деятельности для определения летучих компонентов мазей или кремов с использованием капиллярной газожидкостной хроматографии (ГЖХ) с пламенно-ионизационным детектором.
Из уровня техники известен способ хроматографического определения капсаициноидов в перцах методом ультраэффективной жидкостной хроматографии [1], который позволяет проводить количественное определение нордигидрокапсаицина, капсаицина, дигидрокапсаицина, гомокапсаицина и гомодигидрокапсаицина методом ультраэффективной жидкостной хроматографии (УВЭЖХ) на обращенно-фазовом сорбенте с использованием диодно-матричного детектора. Экстракт острого кайенского перца использовали в качестве образца для разработки методики определения. Для получения экстракта свежий перец очищали от кожуры и отделяли стебли и семена. Использовали только околоплодник и плаценту перца. Их измельчали с помощью обычного блендера до получения однородного образца для анализа. Далее проводили микроволновую экстракцию в микроволновой печи, после чего экстракты фильтровали через нейлоновый шприц-фильтр 0,22 мкм и использовали непосредственно для хроматографического анализа. К недостаткам следует отнести узкий класс определяемых соединений (капсаициноиды), что делает его неуниверсальным для работы с мазями, относительно высокую себестоимость анализа из-за оборудования и длительной процедуры получения экстрактов и использования реактивов для приготовления подвижной фазы, невысокие показатели повторяемости (относительное стандартное отклонение (RSD) достигает 3,6%) и воспроизводимости (RSD до 4,3%).
Известен другой способ газохроматографического определения активных компонентов мазей - ментола, камфоры и метилсалицилата - в плазме крови людей, использующих обезболивающие мази, с применением масс-спектрометрического детектора [2]. К его недостаткам следует отнести отдельное определение камфоры и ментола с применением пламенно-ионизационного детектора и метилсалицилата - с применением масс-спектрометрического детектора; необходимость дериватизации метилсалицилата, что приводит к увеличению себестоимости анализа за счет использования дериватизирующих реагентов и масс-спектрометрического детектирования.
Из уровня техники известен также способ определения капсаициноидов, камфоры, ментола, метилсалицилата, этилсалицилата, салицилововй кислоты и 2-гидроксиэтилсалицилата, где методом капиллярной ГЖХ с пламенно-ионизационным детектированием определяют камфору, ментол, метилсалицилат, этилсалицилат, а ВЭЖХ - капсаициноиды, салицилововую кислоту и 2-гидроксиэтилсалицилат [3]. Он включает в себя растворение образцов мази (или искусственно приготовленной мазевой основы в случае растворов сравнения) в гексане на водяной бане, экстракцию в смеси гексан/метанол, центрифугирование, отделение и промывку метанольной фазы с последующим газохроматографическим анализом. К недостаткам такого определения следует отнести длительную пробоподготовку, а также необходимость определять компоненты в два этапа - двумя методами анализа, что удлиняет процедуру количественного определения активных компонентов в лекарственных препаратах (ЛИ).
Прототипом был выбран известный способ количественного определения летучих соединений с температурой кипения меньше 250°С (камфоры, ментола, метилсалицилата, этилсалицилата) и полулетучих соединений с температурой кипения более 250°С (салициловой кислоты, 2-гидроксиэтилсалицилата и капсаицина) методом ГЖХ в составах для местного применения [4], сущность которого состоит в очистке образца мази от главных компонентов мазевой основы с помощью экстракции гексаном и последующем газохроматографическом определении данных компонентов в метанольном растворе методом внутреннего стандарта, в качестве которого выступает 2-феноксиэтанол, с использованием капиллярной колонки DB-5 MS UI (модификатор поверхности - 5% фенилполисилоксан, 95% диметилполисилоксан). К недостаткам прототипа следует отнести длительную пробоподготовку образцов и длительное время анализа, невысокую воспроизводимость аналитического сигнала для некоторых компонентов и применение редкого в рутинном использовании инжектора с программированием температуры.
Таким образом, из уровня техники известны способы для определения летучих компонентов мази, характеризующиеся длительностью проведения пробоподготовки, изготовлением модельных мазевых основ, использованием нескольких аналитических методов, что увеличивает время проведения анализа. Они обладают невысокой чувствительностью для некоторых компонентов мазей, а в некоторых случаях и низкой воспроизводимостью результатов определения. Кроме того, в некоторых известных способах для определения летучих компонентов мазей используют нераспространенное для рутинного анализа оборудование.
Существует явная потребность в разработке способа для определения летучих компонентов в ЛП в виде мази или крема, характеризующегося чувствительностью, воспроизводимостью, и селективностью для активных действующих компонентов по отношению друг к другу и к мазевой основе (матрице), где используют один аналитический метод, доступное оборудование, а также сокращается время проведения пробоподготовки и самого хроматографического цикла.
Описание сущности изобретения
Технической задачей является разработка воспроизводимого, чувствительного и селективного способа для определения летучих компонентов в лекартвенных препаратах в виде мази или крема, и характеризующегося тем, что при определении летучих компонентов используется один аналитический метод, сокращается время проведения пробоподготовки и анализа, используется доступное оборудование.
Техническим результатом заявленного технического решения является то, что оно обладает более высокой чувствительностью, воспроизводимостью при непродолжительном времени всего аналитического цикла, и при использовании одного аналитического метода для определения активных компонентов, обладающих разной степенью летучести.
Достижение технического результата обеспечивается благодаря:
- использованию капиллярной газо-жидкостной хроматографии с пламенно-ионизационным детектированием и выбору хроматографических условий;
- проведению пробоподготовки стандартных растворов летучих активных компонентов (веществ) без использования модельной смеси мазевых основ (матрицы).
Заявленный способ отличается сокращением времени анализа, высокой воспроизводимостью полученных результатов определения и высокой чувствительностью по сравнению с другими известными из уровня техники способами.
Используемые термины и понятия
Метод внутреннего стандарта - способ построения градуировочной кривой. Как и в градуировке по способу внешних стандартов, стандартные растворы сравнения готовят и измеряют отдельно от анализируемого. В этом случае измеряют не один, а одновременно два аналитических сигнала определяемого компонента и какого-либо другого компонента, присутствующего в пробе (либо специально вводимого в нее) и называемого внутренним стандартом. Градуировочная зависимость представляет собой зависимость отношений аналитических сигналов определяемого компонента и внутреннего стандарта от отношения их же концентраций. Содержание внутреннего стандарта либо должно быть точно известно в каждом растворе сравнения и в анализируемой пробе, либо оно должно быть везде одинаково (в этом случае может быть неизвестно). Использование внутреннего стандарта позволяет повысить воспроизводимость результатов и их правильность [5].
Линейность аналитической методики - наличие прямо пропорциональной зависимости аналитического сигнала от концентрации определяемого вещества в образце в пределах аналитического диапазона методики [5].
Аналитический диапазон методики - интервал между наибольшей и наименьшей концентрациями определяемого вещества в образце (включая эти концентрации), для которого показано, что аналитическая методика имеет приемлемый уровень прецизионности, правильности и линейности [5].
Стеклянный вкладыш - вставка для инжектора газового хроматографа, представляющая собой стеклянную трубку с двумя сужениями, пространство между которыми заполнено стекловатой (Фиг. 5) [6].
В газовой хроматографии инжектор - это первая часть прибора, с которой взаимодействует образец. Его основная функция - передать образец на хроматографическую колонку для анализа. Образцы могут быть жидкими или газообразными, они могут содержать высокие концентрации или только следовые количества определяемых соединений. Выбор правильного вкладыша на входе в хроматографическую систему имеет решающее значение для обеспечения эффективного переноса требуемого количества пробы на колонку без негативного воздействия на целевые соединения.
Вкладыши различаются по геометрической конфигурации, дизайну, объему, материалу изготовления и наличию или отсутствию какого-либо материала внутри [7-9].
Способ определения комбинаций летучих компонентов в лекарственных препаратах, характеризующийся тем, что используют капиллярную газожидкостную хроматографию с пламенно-ионизационным детектированием, где используют кварцевый капилляр, внутренние стенки которого покрыты (обработаны) сополимером, вкладыш для инжектора, где скорость потока газа-носителя 1,5 мл/мин, температура инжектора 220°С, температура детектора 320°С, где проводят пробоподготовку стандартного раствора и мази или крема, с использованием внутреннего стандарта, метанола, воды, экстрагируют гексаном и перемешивают смесь со скоростью 3000 об/мин в течение 2 минут, оставляют до расслоения фаз, отбирают метанольный слой, затем проводят количественное определение концентраций летучих компонентов, содержащихся в мази или креме, и где летучие компоненты выбраны из комбинаций камфоры с салициловой кислотой, камфоры с бензилникотинатом и нонивамидом, ментола с метилсалицилатом.
Способ, характеризующийся тем, что используют сополимер, состоящий на 5% из фенилполисилоксана и на 95% из диметилполисилоксана.
Способ, характеризующийся тем, что в качестве газа-носителя используют гелий.
Способ, характеризующийся тем, что в качестве внутреннего стандарта используют 1% раствор 2-феноксиэтанола в метаноле.
Способ, характеризующийся тем, что кварцевый капилляр является неподвижной фазой.
Способ, характеризующийся тем, что температура неподвижной фазы 90°С в течение 5 минут, а затем температуру поднимают со скоростью 10°С/мин до 150°С и выдерживают в течение 2 минут, а затем температуру поднимают со скоростью 40°С/мин до 310°С и выдерживают в течение 2 минут.
Способ, характеризующийся тем, что для проведения пробоподготовки лекарственного препарата в виде мази или крема и стандартного раствора гексан добавляют в объемном соотношении 1:1 к полученной смеси.
Способ, характеризующийся тем, что используют стеклянный вкладыш, с двумя сужениями во второй четверти его высоты, пространство между которыми заполнено стекловатой.
Способ, характеризующийся тем, что для проведения пробоподготовки лекарственного препарата в виде мази или крема внутренний стандарт, метанол и вода взяты в соотношении 1:3,9:0,1 соответственно.
Способ, характеризующийся тем, что для проведения пробоподготовки стандартного образца внутренний стандарт, метанол и вода взяты в соотношении 1:2,9:0,1 соответственно.
Способ, характеризующийся тем, что для камфоры, ментола, метилсалицилата аналитический диапазон составляет от 0,15 мг/мл до 2,30 мг/мл.
Способ, характеризующийся тем, что для салициловой кислоты аналитический диапазон составляет от 0,12 мг/мл до 0,75 мг/мл.
Способ, характеризующийся тем, что для бензилникотината аналитический диапазон составляет от 0,1 мг/мл до 1,5 мг/мл.
Способ, характеризующийся тем, что для нонивамида аналитический диапазон составляет от 0,01 мг/мл до 0,15 мг/мл.
Существенными отличительными признаками заявляемого изобретения являются:
- определение активных компонентов мазей селективно по отношению к компонентам мазевой основы без длительной методики очистки образцов от компонентов основы и, таким образом, сокращение времени пробоподготовки и трудозатрат за счет изучения состава экстракционной смеси, влияния времени экстракции и времени пребывания смеси в покое на степень экстракции и расслоение фаз;
- повышение чувствительности определения хроматографического метода и воспроизводимости получаемых результатов количественного определения за счет подбора соответствующих скорости потока газа-носителя, типа стеклянного вкладыша для инжектора газового хроматографа, высокой температуры инжектора и детектора, что позволяет интегрировать на хроматограммах пики с лучшими хроматографическими параметрами: асимметрия, высокое соотношение сигнал/шум.
- сокращение времени элюирования активных компонентов мазей или кремов за счет подбора скорости газа-носителя и температурного режима колонки их единовременное определение одним аналитическим методом без использования дорогостоящих реактивов и оборудования;
Активные летучие компоненты мазей или кремов, характеризуются определенной температурой кипения. Условно можно разделить их на две группы: летучие вещества с температурой кипения ниже 250°С, такие как камфора - 209°С, ментол - 212°С, метилсалицилат - 222°С, бензилникотинат - 177°С; и полулетучие вещества с температурой кипения выше 250°С, такие как салициловая кислота - 336°С и нонивамид - 493°С (синтетический аналог капсаицина).
Широко распространенными вспомогательными веществами в составе мазей или кремов являются твердый парафин, цетилстеариловый спирт, вазелин, олеил олеат (цетиол), характеризующиеся соответствующими тепрературами кипения. Часть из них - сложные по составу многокомпонентные вещества. Температуры кипения компонентов твердого парафина лежат в диапазоне 330-550°С, вазелина - 280-600°С. Мазевая основа составляет сложную смесь подобных соединений.
Хроматографические методы давно получили широкое распространение среди аналитических методов анализа. Компоненты мазевой основы - в большинстве своем достаточно гидрофобные соединения. Действующие активные летучие компоненты, отличающиеся в некоторой степени по полярности, а значит и по сродству к различным сорбентам, как в газовой хроматографии, так и в жидкостной хроматографии. Отличие в температурах кипения позволяет рассчитывать на большую селективность определения действующих летучих компонентов мазей или кремов, с учетом влияния компонентов мазевой основы, при использовании капиллярной газожидкостной хроматографии в сравнении с высокоэффективной жидкостной хроматографией.
Таким образом, при разработке заявленного способа определения действующих летучих компонентов в мази или креме необходимо исключить на хроматограмме влияние пиков компонентов матрицы на пики действующих летучих веществ, либо убедиться, что влияние отсутствует, и подобрать хроматографические условия, которые позволят элюировать с поверхности сорбента такие разные по свойствам компоненты отдельно друг от друга, но при этом за непродолжительное время.
Для снижения влияния компонентов матрицы использовали жидкостную экстракцию гексаном. Это позволяло удалить большую часть компонентов мазевой основы. Исследованы такие параметры экстракции, как количество экстрагента (гексана), время экстракции и ее интенсивность. Выбраны такие величины этих параметров, которые позволяют достичь наиболее полного и быстрого отделения компонентов мазевой основы в пробе мази или крема и при этом сохранить действующие компоненты в метанольной фазе.
Установлено, что использование модельной смеси, состоящей из вазелина, твердого парафина и цетилстеарилового спирта, при приготовлении стандартного раствора, используемого для сравнения с испытуемым раствором лекарственного препарата, не влияет на результаты определения летучих соединений в мази или креме в заявленном способе. Стандартный раствор готовят с использованием органического растворителя, выбранного таким образом, чтобы определяемые активные летучие компоненты мази или крема хорошо в нем растворялись, и его температура кипения значительно отличалась от температур кипения определяемых активных летучих компонентов мази или крема.
В качестве органического растворителя, обладающего наилучшими свойствами для реализации заявленного способа, был выбран метанол.
При выборе хроматографических условий было важно установить в градиентном температурном режиме колонки исходную температуру достаточно низкой для быстрого испарения метанола, но медленного начала испарения действующих активных веществ с относительно близкими температурами кипения, такими как камфора и ментол, и плавный подъем температуры для того, чтобы соединения успевали элюироваться с поверхности колонки полностью, но не слишком медленно, чтобы исключить размывание пиков на хроматограмме и искажение результатов определения.
Аналогично со скоростью потока газа-носителя: нужен баланс между хорошим разделением компонентов в хроматографической колонке и приемлемое время анализа. При этом температуру инжектора и детектора выбирали достаточно высокой, чтобы высоко кипящие вещества полностью испарялись в инжекторе (и полностью поступали в хроматографическую колонку) и не оседали в детекторе (что в конечном итоге привело бы к искажению полученного аналитического сигнала).
Для повышения точности бы проведен отбор вкладышей для инжектора. Выбирали тот вкладыш, который позволял получить для большого количества компонентов на хроматограмме более высокий аналитический сигнал с хорошей его воспроизводимостью.
Хроматографическую колонку выбрали на основе прототипа, поскольку данная неподвижная фаза, представляющая собой кварцевый капилляр, внутренние стенки которого модифицированы сополимером, состоящим из фенилполисилоксана и диметилполисилоксана, обладает невысокой полярностью. Таким образом, растворитель не имеет к ней высокого родства, а для гидрофобных компонентов матрицы она слишком гидрофильна.
Заявленный способ определения летучих компонентов капиллярной газо-жидкостной хроматографии в лекарственных препаратах в виде мази или крема реализуется следующим образом.
В заявленном способе используют стандартный раствор следующего состава: 0,76% камфоры, 0,76% ментола, 0,76% метилсалицилата, 0,5% бензилникотината, 0,24% салицилововй кислоты и 0,048% нонивамида, приготовленные путем растворения навесок соответствующих стандартных образцов в метаноле.
Для получения концентраций компонентов в области аналитического диапазона хроматографической методики с учетом состава лекарственного препарата, заявленного производителем, стандартный раствор при пробоподготовке необходимо разбавить в 5 раз. Полученные таким образом концентрации определяемых компонентов мази принимают за 100%. Абсолютное количество внутреннего стандарта должно совпадать с таковым для исследуемого образца.
В качестве внутреннего стандарта используют 1% раствор 2-феноксиэтанола в метаноле.
Пробоподготовку мази или крема, содержащих соответствующие активные летучие компоненты, осуществляют следующим образом: к мази или крему добавляют внутренний стандарт, метанол и воду, взятые в соотношении 1:3,9:0,1 соответственно, перемешивают полученную смесь 30 секунд, после чего добавляют гексан в объемном соотношении 1:1 к полученной смеси. Проводят экстракцию полученной смеси в течение 2 минут - перемешивают со скоростью 3000 об/мин, оставляют до расслоения фаз. Отбирают нижний метанольный слой и проводят хроматографический анализ.
Пробоподготовку для стандартного раствора, содержащего активные летучие компоненты, проводят аналогично, получая при разбавлении стандартного раствора в 5 раз концентрации определяемых летучих компонентов мази, принятые за 100%. Поскольку стандартный образец содержит метанол, то внутренний стандарт, метанол и воду берут в соотношении 1:2,9:0,1 соответственно.
Количественное определение камфоры, ментола, метилсалицилата, салицилововй кислоты, бензилникотината и нонивамида проводят на газовом хроматографе с пламенно-ионизационным детектором, оснащенном автосамплером. Регистрацию хроматограмм и обработку результатов проводят с помощью программного обеспечения известного специалисту из области техники.
Колонка (неподвижная фаза): DB-5 (30 м ×0,32 мм, 0,25 мкм), представляющая собой кварцевый капилляр, внутренние стенки которого покрыты (обработаны) сополимером, состоящим из фенилполисилоксана и диметилполисилоксана. Газ-носитель (подвижная фаза): гелий.
Хроматографические условия представлены в Таблице 1.
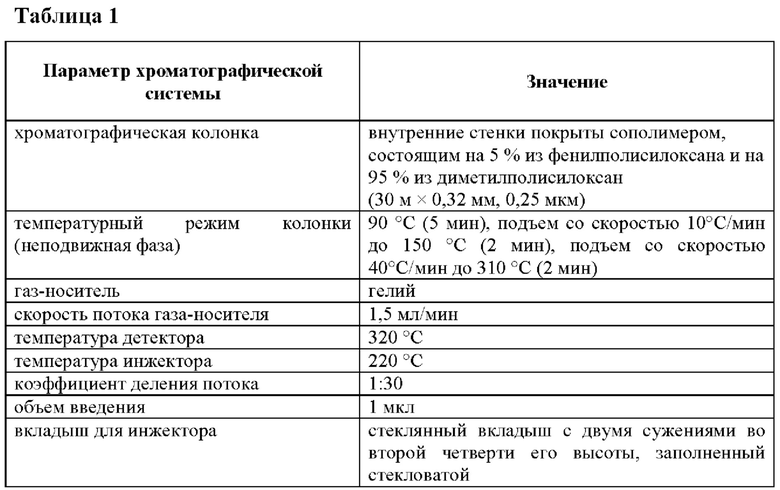
Оценку аналитического диапазона проводили в области концентраций, релевантной содержанию соответствующих компонентов в лекарственных препаратах. Аналитический диапазон составляет от 0,15 мг/мл до 2,30 мг/мл для камфоры, ментола и метилсалицилата, где коэффициенты корреляции R2 составили 0,9998, 0,9998 и 0,9999 соответственно; от 0,12 мг/мл до 0,75 мг/мл для салициловой кислоты, где R2=0,9948; от 0,1 мг/мл до 1,5 мг/мл для бензилникотината, где R2=0,9999; от 0,01 мг/мл до 0,15 мг/мл для нонивамида, где R2=0,9995. Пределы количественного определения составили: 1,5 мкг/мл для камфоры и ментола, 3,7 мкг/мл для метилсалицилата, 0,7 мкг/мл для бензилникотината, 41,5 мкг/мл для салициловой кислоты и 5,2 мкг/мл для нонивамида.
Количественный расчет содержания компонента мази или крема в мг/г рассчитывают из измеренного аналитического сигнала (отношения площадей пиков компонента и внутреннего стандарта) на хроматограммах стандартного раствора и испытуемого раствора образца ЛП с учетом взятых навесок и объемов метанола для растворения:
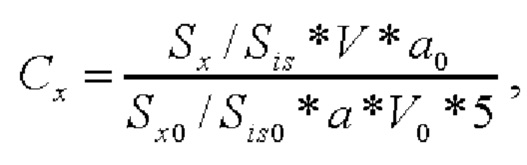 где
где
Сх - концентрация определяемого компонента в лекарственном препарате, мг/г препарата;
Sx - площадь пика определяемого компонента мази на хроматограмме испытуемого раствора;
Sis - площадь пика внутреннего стандарта на хроматограмме испытуемого раствора;
Siso - площадь пика внутреннего стандарта на хроматограмме стандартного раствора;
Sxo - площадь пика определяемого компонента мази на хроматограмме стандартного раствора;
а - навеска ЛП, г;
а0 - навеска стандартного образца компонента мази, используемая для приготовления стандартного раствора, мг;
V - объем метанольной фазы для растворения навески мази, мл;
V0 - объем метанола, используемый для растворения навески стандартного образца, мл;
5 - коэффициент, учитывающий разбавление стандартного раствора в пробирке при пробоподготовке;
Краткое описание чертежей и иных материалов (Приложения 1-5):
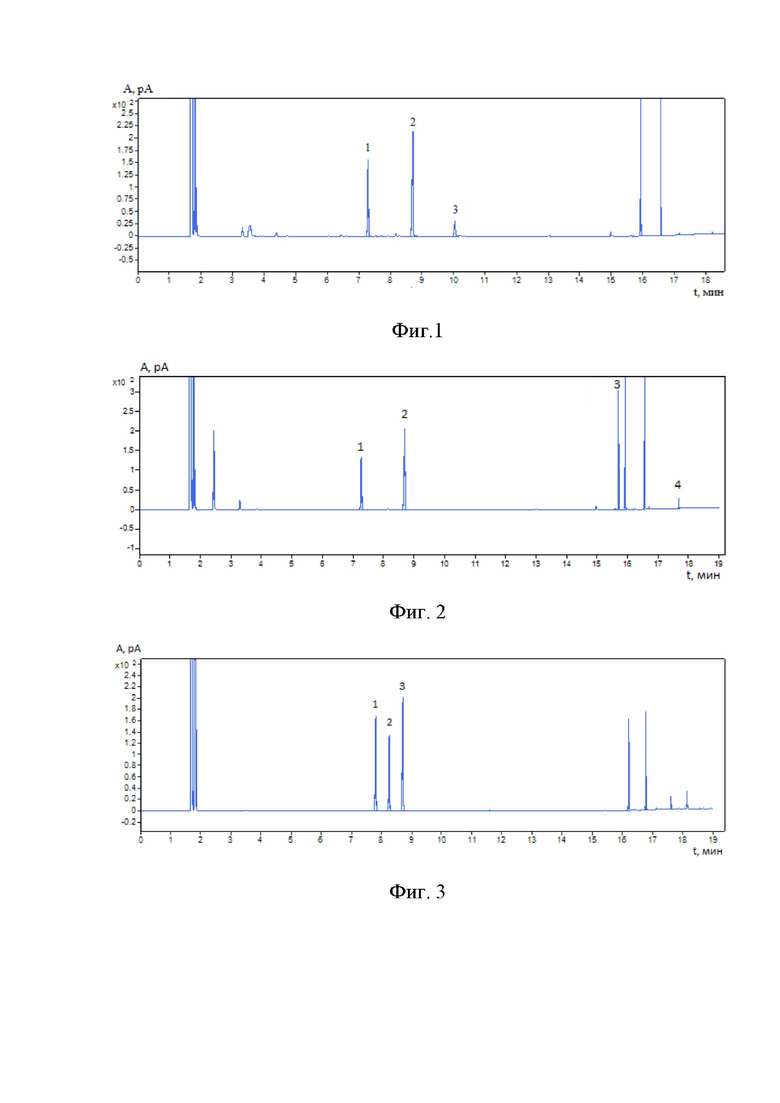
Фиг. 1. Хроматограмма лекарственного препарата в виде мази, содержащего камфору (1) и салициловую кислоту (3) при добавлении внутреннего стандарта 2-феноксиэтанола (2).
Фиг. 2. Хроматограмма лекарственного препарата в виде мази, содержащего камфору (1), бензилникотинат (3) и нонивамид (4) при добавлении внутренного стандарта 2-феноксиэтанола (2).
Фиг. 3. Хроматограмма лекарственного препарата в виде крема, содержащего ментол (1), метилсалицилат (2) при добавлении внутренного стандарта 2-феноксиэтанола (2).
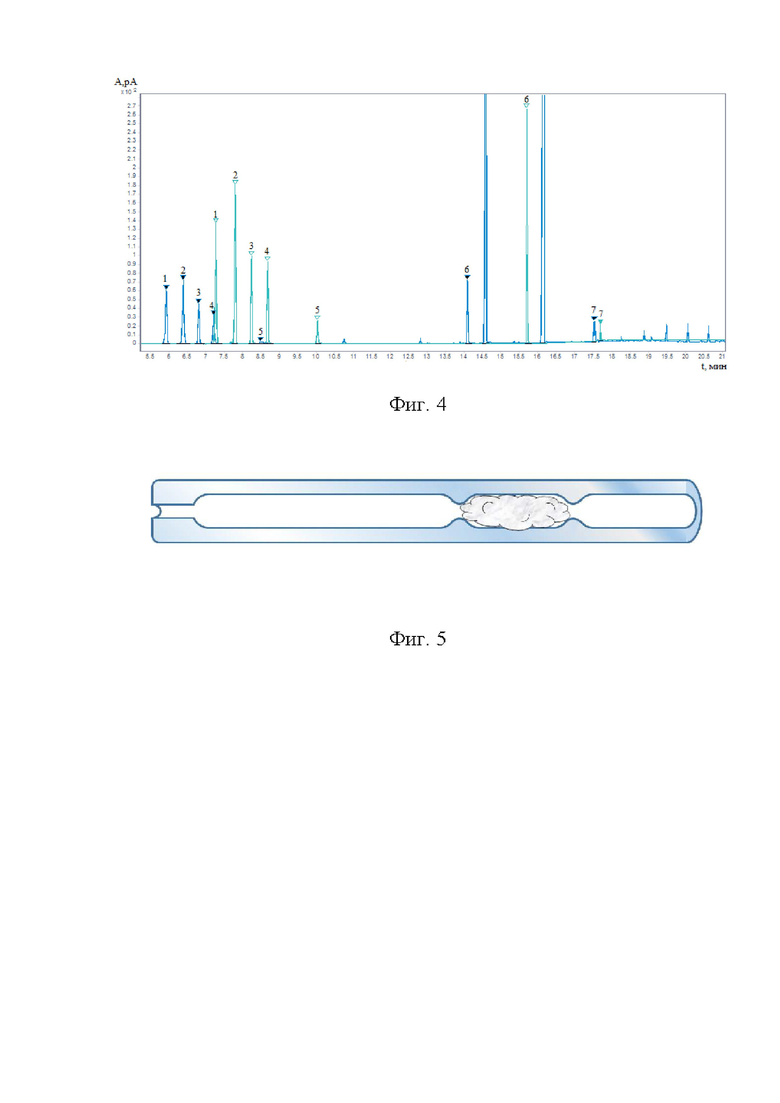
Фиг. 4. Хроматограммы стандартных растворов с сопоставимой концентрацией камфоры (1), ментола (2), метилсалицилата (3), 2-феноксиэтанола (внутренний стандарт) (4), салициловой кислоты (5), бензилникотината (6) и нонивамида (7), полученные заявляемым способом (Δ) и способом прототипа ( ).
).
Фиг. 5. Стеклянный вкладыш, представляющий собой стеклянную трубку с двумя сужениями во второй четверти его высоты, пространство между которыми заполнено стекловатой.
Возможность осуществления заявляемого изобретения раскрыта в следующих примерах.
Пример 1. Количественное определение камфоры и салициловой кислоты, содержащиеся в лекарственном препарате в виде мази, заявляемым способом (Фиг. 1).
Пробоподготовку осуществляют следующим образом. К одной части стандартного раствора, добавляют внутренний стандарт, метанол и воду, взятые в соотношении 1:2,9:0,1 соответственно, перемешивают полученную смесь 30 секунд, после чего добавляют гексан в объемном соотношении 1:1 к полученной смеси. Проводят экстракцию полученной смеси в течение 2 минут - перемешивают со скоростью 3000 об/мин, оставляют на 2 мин до расслоения фаз. Отбирают нижний метанольный слой и проводят хроматографический анализ.
Используют стандартный раствор, приготовленный по методике заявляемого способа, поскольку конечные концентрации компонентов в нем лежат в области аналитических диапазонов концентраций. Для его приготовления используют только те стандартные образцы, которые определяют в конкретном лекарственном препарате - камфору и салициловую кислоту.
Пробоподготовку мази осуществляют аналогично. В пробирку помещают 0,25 г мази, 2,0 мл внутреннего стандарта, 7,8 мл метанола и 0,2 мл воды.
Последовательно инжектируют стандартный раствор и испытуемый раствор.
Содержание камфоры и салициловой кислоты рассчитывают из измеренного аналитического сигнала (отношения площадей пиков компонента и внутреннего стандарта) с помощью обратной функции.
Установлено содержание камфоры 28,1 мг/г мази - 93,8% от номинального значения, где относительное стандартное отклонение - RSD - составило 0,50%, содержание салициловой кислоты - 10,3 мг/г - 103,2% от номинального значения с RSD 1,53%.
Вывод: содержание действующих компонентов в лекарственном препарате соответствует заявленному в Спецификации нормативного документа фирмы производителя.
Пример 2. Количественное определение камфоры, бензилникотината и нонивамида, содержащихся в лекарственном препарате в виде мази, заявляемым способом (Фиг. 2).
Пробоподготовку стандартного раствора и мази осуществляют в соответствии с Примером 1. Последовательно инжектируют стандартный раствор и испытуемый раствор.
Используют стандартный раствор, приготовленный по методике заявляемого способа, поскольку конечные концентрации компонентов в нем лежат в области аналитических диапазонов концентраций. Для его приготовления используют только те стандартные образцы, которые определяют в конкретном лекарственном препарате - камфору, бензилникотинат и нонивамид.
Содержание камфоры, бензилникотината и нонивамида рассчитывают из измеренного аналитического сигнала (отношения площадей пиков компонента и внутреннего стандарта) с помощью обратной функции.
Установлено содержание камфоры 28,2 мг/г - 94,0% от номинального значения с RSD - 0,78%, бензилникотината 19,6 мг/г - 98,1% от номинального значения с RSD - 1,24%, нонивамида 1,81 мг/г - 90,5% от номинального значения с RSD - 1,22%.
Вывод: содержание действующих компонентов в лекарственном препарате соответствует заявленному в Спецификации нормативного документа фирмы производителя.
Пример 3. Количественное определение ментола и метилсалицилата, содержащиеся в лекарственном препарате в виде крема, заявляемым способом (Фиг. 3).
Пробоподготовку стандартного раствора и крема осуществляют в соответствии с Примером 1. Последовательно инжектируют стандартный раствор и испытуемый раствор.
Используют стандартный раствор, приготовленный по методике заявляемого способа, поскольку конечные концентрации компонентов в нем лежат в области аналитических диапазонов концентраций. Для его приготовления используют только те стандартные образцы, которые определяют в конкретном лекарственном препарате - ментол и метилсалицилат.
Содержание ментола и метилсалицилата рассчитывают из измеренного аналитического сигнала (отношения площадей пиков компонента и внутреннего стандарта) с помощью обратной функции.
Установлено содержание ментола 96,2 мг/г - 96,2% от номинального значения с RSD - 0,71%, метилсалицилата 137,8 мг/г - 91,9% от номинального значения с RSD - 0,46%.
Вывод: содержание действующих компонентов в лекарственном препарате соответствует заявленному в Спецификации нормативного документа фирмы производителя.
Таким образом, примеры 1-3 демонстрируют возможность применения заявляемого способа при определении активных компонетов мазей или кремов в разнообразных ЛП в составах для местного применения.
Пример 4.
Сопоставление хроматографических параметров пиков активных компонентов мазей на хроматограммах, полученных заявляемым способом и способом прототипа, и валидационных характеристик хроматографических методик (Таблица 2).
Сравнение проводят для растворов, приготовленных согласно прототипу с концентрациями компонентов мазей, сопоставимыми по величине со 100%-м раствором, приготовленным по методике заявляемого способа.
Полученные стандартные растворы подвергают хроматографированию в условиях заявляемого способа и способа прототипа соответственно.
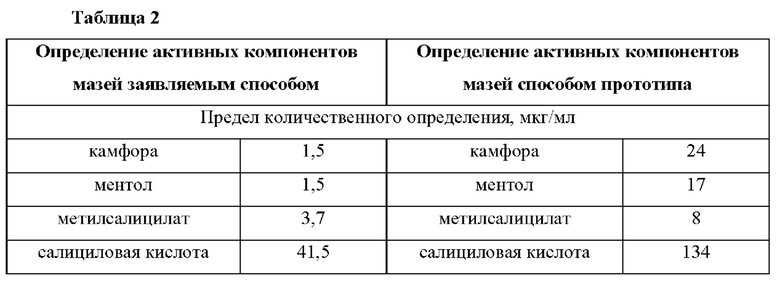
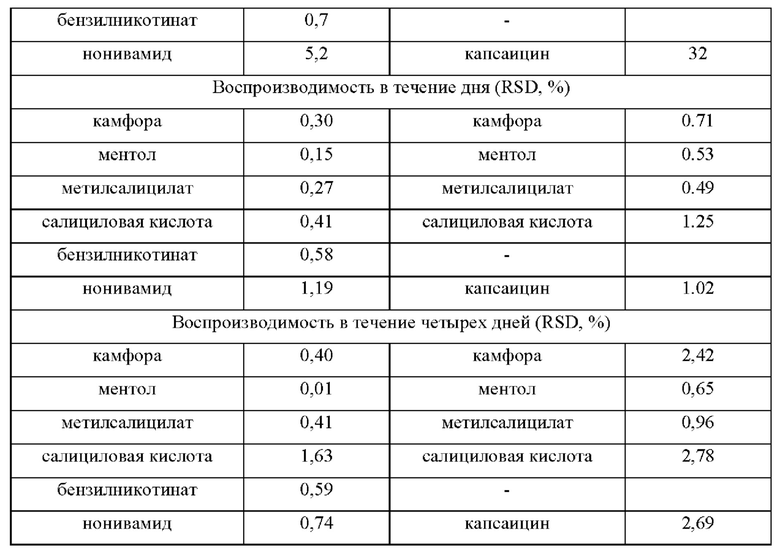
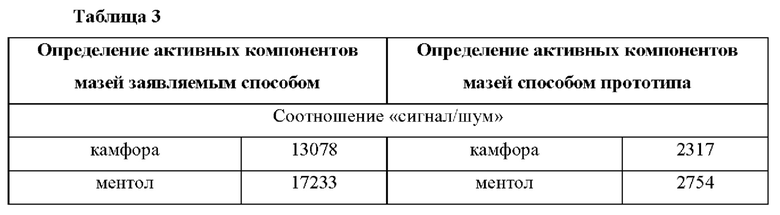
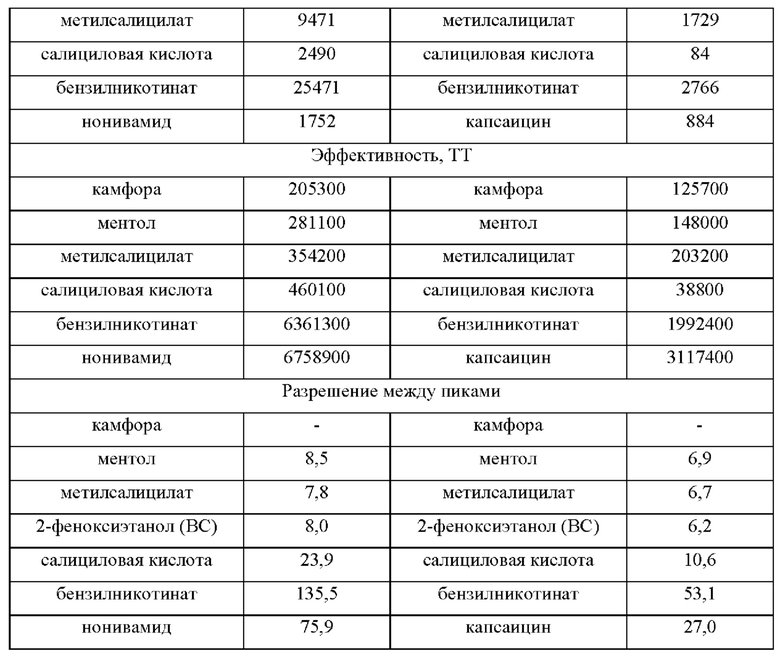
Данные, представленные в таб. 2 демонстрируют, что предел количественного определения одних и тех же компонентов у заявляемого способа в несколько раз, а в случае камфоры и ментола на порядок, ниже, чем у прототипа, что свидетельствует о более высокой чувствительности заявляемого способа. К аналогичному выводу приводят и соотношения сигнал/шум для определяемых компонентов (Таблица 3, Фиг. 4). Высокая температура инжектора и плавный градиент температуры термостата колонки, видимо, позволяют более полно испарять компоненты мазей в инжекторе. Предложенный вариант экстракции позволяет в достаточно высокой степени компонентам мази и 2-феноксиэтанолу перейти в метанольную фазу.
Также из таблицы 2 видна значительная разница в воспроизводимости аналитического сигнала в течение дня и в течение четырех разных дней для заявляемого способа и способа прототипа.
Как видно из Фиг. 4, высота пиков на хроматограмме, полученной заявляемым способом, значительно больше, чем на хроматограмме раствора с такой же концентрацией компонентов, полученной способом прототипа. Стоит отметить, что высота пика нонивамида сопоставима для обоих способов. Но за счет большего дрейфа базовой линии в случае прототипа соотношение сигнал/шум для нонивамида ниже, чем в случае заявляемого способа, где базовая линия отличается меньшим дрейфом.
Особенно заметно отличие в симметрии пиков для салициловой кислоты. Ее пик, принадлежащий хроматограмме, полученной способом прототипа, сильно размыт, его фактор асимметрии составляет 5,4. Для более узкого и высокого пика этого соединения на хроматограмме, полученной заявляемым способом, фактор асимметрии пика составил 1,0. Салициловую кислоту в практике фармацевтического контроля качества и согласно Фармакопее Российской Федерации обычно принято определять методом титрования или методом ВЭЖХ с УФ-детектированием, а метилсалицилат - ВЭЖХ-УФ, что приводит к увеличению числа показателей качества ЛП и более длительному времени экспертизы качества, а так же большим трудозатратам и себестоимости каждого отдельного анализа. Возможность определять все компоненты за один аналитический цикл является очень перспективным направлением по рационализации в этой и не только области промышленности.
Из Таблицы 3 видно, что в случае использования раствора сравнения одной и той же концентрации компонентов эффективность хроматографической системы и разрешающая способность газохроматографического разделения активных компонентов мазей у метода прототипа ниже.
Данный пример подтверждает повышение чувствительности хроматографической системы благодаря улучшению симметрии пиков, разрешению между ними и увеличению эффективности хроматографической системы. А это в свою очередь приводит к повышению воспроизводимости результатов количественного определения, полученных заявляемых способом, по сравнению с таковыми для способа прототипа.
Выше изложенное техническое решение описано довольно подробно с целью ясности понимания и не должно рассматриваться, как ограничивающее объем притязаний.
Представленные примеры не ограничивают объем притязаний настоящего технического решения и служат только для цели иллюстрации и раскрытия заявленного способа.
Промышленная применимость
Все приведенные примеры подтверждают реализацию заявленного способа определения различных летучих компонентов в лекарственных препаратах в виде мази или крема одним аналитическим методом капиллярной газо-жидкостной хроматографии.
Таким образом, поставленная техническая задача, а именно, разработка способа определения летучих компонентов в лекарственных препаратах достигнута, что подтверждается приведенными примерами.
Применение заявленного способа возможно в фармацевтической, химической и в смежных отраслях промышленности и научно-исследовательской деятельности
Список литературы:
1. G.F. Barbero, A. Liazid, М.  М. Palma, C.G. Barroso. Fast separation of capsaicinoids from peppers by reversed phase ultra-performance liquid chromatography: Comparation with traditional high-performance liquid chromatography methods. International Journal of Food Properties. 2016; 19: 984-982.
М. Palma, C.G. Barroso. Fast separation of capsaicinoids from peppers by reversed phase ultra-performance liquid chromatography: Comparation with traditional high-performance liquid chromatography methods. International Journal of Food Properties. 2016; 19: 984-982.
2. J.S. Valdez, D.K. Martin, M. Mayersohn. Sensitive and selective gas chromatographic methods for the quantitation of camphor, menthol and methyl salicylate from human plasma. Journal of Chromatography B. 1999; 729: 163-171.
3. J. Pauwels et al. Optimization and validation of liquid chromatography and headspace-gas chromatography based methods for the quantitative determination of capsaicinoids, salicylic acid, glycol monosalicylate, methyl salicylate, ethyl salicylate, camphor and 1-menthol in a topical formulation. Journal of Pharmaceutical and Biomedical Analysis. 2012; 60: 51-58.
4. Anyakudo F., Adams E., Van Schepdael A. Simultaneous analysis of volatile and semi-volatile components in a topical formulation by gas chromatography using a programmed temperature vaporization inlet and flame ionization detection. Journal of Pharmaceutical and Biomedical Analysis. 2019; 171: 65-72.
5. A.B. Гармаш, H.M. Сорокина. Метрологические основы аналитической химии. Москва. 2012.
6. https://www.agilent.com/store/productDetail.jsp?catalogId=210-4022-5 (дата обращения 10.06.2022 г.)
7. https://www.restek.com/row/technical-literature-library/articles/how-to-choose-a-GC-inlet-liner-simplify-selection-based-on-injection-type/ (дата обращения 10.06.2022 г.)
8. Н.И. Царев, В.И. Царев, И.Б. Катраиов. Практическая газовая хроматография. Барнаул. 2000.
9. К. Хайвер. Б. Ньютон, П. Сандра. Высокоэффективная газовая хроматография. Москва, 1993.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения лозартана, его основного метаболита лозартан карбоновой кислоты и глибенкламида в сыворотке крови и моче человека | 2020 |
|
RU2749567C1 |
| Определение полисорбата 80 в биологических лекарственных препаратах | 2023 |
|
RU2812788C1 |
| Способ количественного определения аскорбиновой кислоты в лекарственных растительных препаратах | 2023 |
|
RU2801885C1 |
| Способ определения арбутина в листьях толокнянки | 2023 |
|
RU2802173C1 |
| Способ определения амиодарона и его основного метаболита дезэтиламиодарона в сыворотке крови человека | 2020 |
|
RU2749566C1 |
| Определение стабилизаторов углеводной природы в биологически активных препаратах | 2023 |
|
RU2816030C1 |
| Способ количественного определения фтивазида | 2024 |
|
RU2828350C1 |
| Способ определения примеси А в лекарственных формах габапентина | 2021 |
|
RU2773851C1 |
| Способ определения алкалоидов в экстракте термопсиса | 2022 |
|
RU2796599C1 |
| Способ количественного определения ионов алюминия атомно-абсорбционной спектрометрией с электротермической атомизацией | 2022 |
|
RU2799235C1 |
Изобретение относится к аналитической химии и может быть использовано в фармацевтической и химической промышленности. Способ определения комбинаций летучих компонентов в лекарственных препаратах характеризуется тем, что используют капиллярную газо-жидкостную хроматографию с пламенно-ионизационным детектированием, где используют кварцевый капилляр, внутренние стенки которого покрыты сополимером, вкладыш для инжектора, где скорость потока газа-носителя 1,5 мл/мин, температура инжектора 220°С, температура детектора 320°С, где проводят пробоподготовку стандартного раствора и мази или крема, с использованием внутреннего стандарта, метанола, воды, экстрагируют гексаном и перемешивают смесь со скоростью 3000 об/мин в течение 2 минут, оставляют до расслоения фаз, отбирают метанольный слой, затем проводят количественное определение концентраций летучих компонентов, содержащихся в мази или креме, и где летучие компоненты выбраны из комбинаций камфоры с салициловой кислотой, камфоры с бензилникотинатом и нонивамидом, ментола с метилсалицилатом. Техническим результатом является повышение чувствительности, воспроизводимости при уменьшении времени аналитического цикла и при использовании одного аналитического метода для определения активных компонентов, обладающих разной степенью летучести. 13 з.п. ф-лы, 5 ил., 3 табл.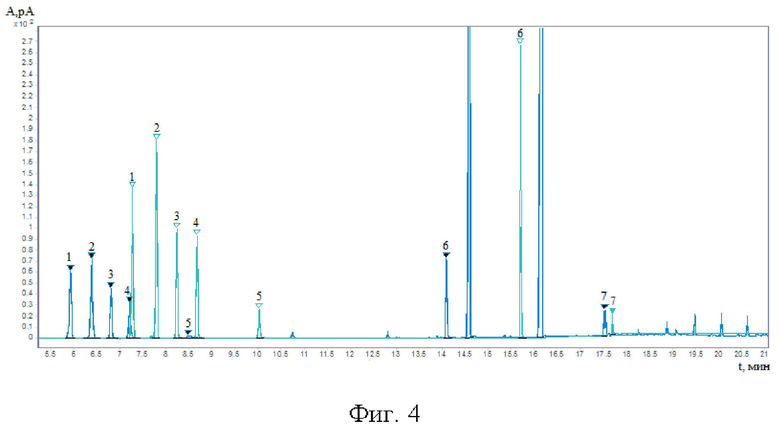
1. Способ определения комбинаций летучих компонентов в лекарственных препаратах, характеризующийся тем, что используют капиллярную газо-жидкостную хроматографию с пламенно-ионизационным детектированием, где используют кварцевый капилляр, внутренние стенки которого покрыты сополимером, вкладыш для инжектора, где скорость потока газа-носителя 1,5 мл/мин, температура инжектора 220°С, температура детектора 320°С, где проводят пробоподготовку стандартного раствора и мази или крема, с использованием внутреннего стандарта, метанола, воды, экстрагируют гексаном и перемешивают смесь со скоростью 3000 об/мин в течение 2 минут, оставляют до расслоения фаз, отбирают метанольный слой, затем проводят количественное определение концентраций летучих компонентов, содержащихся в мази или креме, и где летучие компоненты выбраны из комбинаций камфоры с салициловой кислотой, камфоры с бензилникотинатом и нонивамидом, ментола с метилсалицилатом.
2. Способ по п. 1, дополнительно характеризующийся тем, что используют сополимер, состоящий на 5 % из фенилполисилоксана и на 95 % из диметилполисилоксана.
3. Способ по п. 1, дополнительно характеризующийся тем, что в качестве газа-носителя используют гелий.
4. Способ по п. 1, дополнительно характеризующийся тем, что в качестве внутреннего стандарта используют 1% раствор 2-феноксиэтанола в метаноле.
5. Способ по п. 1, дополнительно характеризующийся тем, что кварцевый капилляр является неподвижной фазой.
6. Способ по п. 5, дополнительно характеризующийся тем, что температура неподвижной фазы 90°С в течение 5 минут, а затем температуру поднимают со скоростью 10°С/мин до 150°С и выдерживают в течение 2 минут, а затем температуру поднимают со скоростью 40°С/мин до 310°С и выдерживают в течение 2 минут.
7. Способ по п. 1, дополнительно характеризующийся тем, что для проведения пробоподготовки лекарственного препарата в виде мази или крема и стандартного раствора гексан добавляют в объемном соотношении 1:1 к полученной смеси.
8. Способ по п. 1, дополнительно характеризующийся тем, что используют стеклянный вкладыш с двумя сужениями во второй четверти его высоты, пространство между которыми заполнено стекловатой.
9. Способ по п. 1, дополнительно характеризующийся тем, что для проведения пробоподготовки лекарственного препарата в виде мази или крема внутренний стандарт, метанол и вода взяты в соотношении 1:3,9:0,1 соответственно.
10. Способ по п. 1, дополнительно характеризующийся тем, что для проведения пробоподготовки стандартного образца внутренний стандарт, метанол и вода взяты в соотношении 1:2,9:0,1 соответственно.
11. Способ по п. 1, дополнительно характеризующийся тем, что для камфоры, ментола, метилсалицилата аналитический диапазон составляет от 0,15 до 2,30 мг/мл.
12. Способ по п. 1, дополнительно характеризующийся тем, что для салициловой кислоты аналитический диапазон составляет от 0,12 до 0,75 мг/мл.
13. Способ по п. 1, дополнительно характеризующийся тем, что для бензилникотината аналитический диапазон составляет от 0,1 до 1,5 мг/мл.
14. Способ по п. 1, дополнительно характеризующийся тем, что для нонивамида аналитический диапазон составляет от 0,01 до 0,15 мг/мл.
| ANYAKUDO FELIX ET AL | |||
| "SIMULTANEOUS ANALYSIS OF VOLATILE AND SEMI-VOLATILE COMPONENTS IN A TOPICAL FORMULATION BY GAS CHROMATOGRAPHY USING A PROGRAMMED TEMPERATURE VAPORIZATION INLET AND FLAME IONIZATION DETECTION", JOURNAL OF PHARMACEUTICAL AND BIOMEDICAL ANALYSIS, V | |||
| Аппарат для передачи изображений на расстояние | 1920 |
|
SU171A1 |
| Разборное приспособление для накатки на рельсы сошедших с них колес подвижного состава | 1920 |
|
SU65A1 |
| PAUWELS JOCHEN ET AL | |||
| "OPTIMIZATION AND VALIDATION OF | |||
Авторы
Даты
2023-02-14—Публикация
2022-06-10—Подача