Изобретение относится к области фармации, в частности к лабораторной экспертизе биологических лекарственных препаратов (далее - БЛП), а именно к количественному определению примесей и вспомогательных веществ, содержащихся в БЛП.
Известен способ определения фенола в аллергенах [1], состоящий в определении фенола при помощи спектрофотометрии. Способ основан на способности фенола поглощать ультрафиолетовое излучение при длине волны 269 нм.
К недостаткам этого способа следует отнести необходимость пробоподготовки (разведение образца), относительную точность и специфичность, поскольку все органические соединения, имеющие в своей структуре ароматическое бензольное кольцо, обладают способностью поглощать излучение в ультрафиолетовой области, в частности, при длине волны 269 нм. Данный способ можно считать специфичным, только допуская, что испытуемый образец не содержит подобных веществ.
Также известен способ количественного определения фенола в крови [2], заключающийся в экстракции фенола из крови и последующем определении его с помощью метода газожидкостной хроматографии (далее - ГЖХ).
К недостаткам этого способа следует отнести необходимость пробоподготовки (экстракция фенола и разведение образца), а также ограниченную область применения: способ разработан для определения содержания фенола в крови и не пригоден для определения содержания фенола в БЛП ввиду различий состава образцов и диапазона концентраций фенола.
Также известен способ, применяемый для определения фенола в иммунных сыворотках и вакцинах [3], состоящий в определении фенола колориметрически. Способ основан на образовании антипиринового красителя при реакции 4-аминоантипирина с фенолами в щелочной среде в присутствии окислителя (феррицианида калия) и последующем измерении интенсивности окраски в анализируемом образце.
К недостаткам этого способа следует отнести необходимость пробоподготовки (разведение образца), длительность, необходимость использования дополнительных реагентов, а также относительную точность и специфичность способа: реакцию с 4-аминоантипирином дают все вещества, относящиеся к классу фенолов.
В качестве прототипа выбран способ количественного определения фенола спектрофотометрическим методом в иммунобиологических лекарственных препаратах [4].
К недостаткам этого способа следует отнести необходимость пробоподготовки (предварительного разведения препаратов в 100 раз), в результате которой концентрация фенола в испытуемом образце соответствует диапазону аналитической области способа. А также относительную точность и специфичность, поскольку все органические соединения, имеющие в своей структуре ароматическое бензольное кольцо, обладают способностью поглощать излучение в ультрафиолетовой области, в частности, при длине волны 269 нм. Данный способ можно считать специфичным, только допуская, что испытуемый образец не содержит подобных веществ.
Техническим результатом изобретения является повышение специфичности и точности количественного определения фенола в БЛП методом ГЖХ.
В данном тексте под терминами специфичность и точность [5, 6] подразумевается следующее.
Специфичность - это способность аналитической методики однозначно оценивать определяемое вещество в присутствии сопутствующих компонентов.
Для описания точности метода измерений используют два термина: «правильность» и «прецизионность». Термин «правильность» характеризует степень близости среднего арифметического значения результатов измерений к истинному или принятому опорному значению, термин «прецизионность» -степень близости результатов измерений друг к другу.
Определение правильности методики непосредственно связано с оценкой линейности. Линейность методики - это наличие линейной зависимости аналитического сигнала от концентрации или количества определяемого вещества в анализируемой пробе в пределах аналитической области. Аналитическая область - это интервал между верхним и нижним значениями аналитических характеристик определяемого компонента в объекте анализа. Для представления прецизионности используют результаты, полученные в условиях «повторяемости (сходимости)» и в условиях «воспроизводимости».
Поставленная задача решается благодаря:
- расширению спектра аналитического оборудования;
- подбору хроматографической колонки, позволяющей обеспечить эффективное отделение фенола от веществ, входящих в состав образца;
- подбору условий ГЖХ: режима подачи несущего газа (гелия); скорости потока несущего газа (гелия); условий деления потока несущего газа (гелия), температуры инжектора, температуры термостата хроматографической колонки; температуры детектора, позволяющих обеспечить эффективное отделение фенола от веществ, входящих в состав образца;
- подбору линейной области концентраций фенола, соответствующей содержанию фенола в БЛП;
- исключению этапа пробоподготовки (разведения образца);
- выбору внутреннего стандарта, позволяющего контролировать эффективность хроматографического разделения.
В заявляемом изобретении способ количественного определения фенола в БЛП осуществляется методом ГЖХ.
Способ количественного определения фенола в БЛП методом ГЖХ реализуется следующим образом.
В качестве внутреннего стандарта используют раствор 2-феноксиэтанола в абсолютном этаноле, концентрацией 5 мг/мл.
В качестве рабочего раствора фенола используют раствор фенола в этаноле концентрацией 5 мг/мл.
Приготовление стандартных растворов с концентрацией фенола 1-5 мг/мл:
0,2 мл рабочего раствора фенола помещают в виалу №1, объемом 1,5 мл для хроматографирования, добавляют воду 0,8 мл, добавляют 0,5 мл внутреннего стандарта, перемешивают. Полученный раствор представляет собой стандартный раствор с концентрацией фенола 1 мг/мл, содержащий внутренний стандарт.
0,6 мл рабочего раствора фенола помещают в виалу №2, объемом 1,5 мл для хроматографирования, добавляют воду 0,4 мл, добавляют 0,5 мл внутреннего стандарта, перемешивают. Полученный раствор представляет собой стандартный раствор с концентрацией фенола 3 мг/мл, содержащий внутренний стандарт.
1,0 мл рабочего раствора фенола помещают в виалу №3, объемом 1,5 мл для хроматографирования, добавляют 0,5 мл внутреннего стандарта, перемешивают. Полученный раствор представляет собой стандартный раствор с концентрацией фенола 5 мг/мл, содержащий внутренний стандарт.
Исследуемый образец: 1,0 мл образца БЛП, содержащий фенол в концентрации 1,5-4 мг/мл, без предварительного разведения, вносят в виалу №4 для хроматографирования объемом 1,5 мл. В ту же виалу добавляют 0,5 мл внутреннего стандарта, перемешивают.
Последовательность ввода образцов соответствует номеру виалы.
Оптимальные условия ГЖХ были подобраны для колонки DB-WAX (размер 30 м × 0,25 мм × 0,25 мкм) фирмы Agilent Technologies; температура инжектора 250°С; деление потока 40:1; объем пробы 0,5 мкл; газ-носитель гелий; режим постоянное давление; скорость потока 1,4 мл/мин; температурный профиль печи: начальная температура 160°С, выдержка 3 мин, градиент 40°С/мин до температуры 200°С выдержка 0,6 мин, градиент 40°С/мин до температуры 220°С; время анализа 7,133 мин; пламенно-ионизационный детектор, температура детектора 250°С.
Критерии пригодности хроматографической системы, установленные в процессе валидации способа:
- число теоретических тарелок не менее 180000;
- разрешение пиков фенола и внутреннего стандарта не менее 15;
- коэффициент асимметрии пика фенола от 0,8 до 1,2;
- время удерживания пика фенола около 5,0 мин;
- время удерживания внутреннего стандарта около 6,0 мин.
Расчет производят относительно внутреннего стандарта, переводя величину полученного аналитического сигнала в относительные единицы.
Оценку результатов производят, используя график регрессионной зависимости относительных площадей пика фенола от концентрации фенола в стандартных растворах.
Существенные отличительные признаки заявляемого изобретения:
1. Повышение специфичности способа за счет подбора хроматографической колонки и условий газохроматографического разделения, позволяющих обеспечить эффективное отделение фенола от веществ, входящих в состав образца.
2. Повышение точности (правильности и прецизионности) способа за счет:
- исключения этапа пробоподготовки;
- проведения анализа с использованием линейной области способа, соответствующей концентрации фенола в БЛП;
- использования внутреннего стандарта, позволяющего контролировать эффективность газохроматографического разделения и проводить расчет в относительных единицах.
3. Расширение спектра аналитического оборудования пригодного для количественного определения фенола в БЛП.
Краткое описание чертежей и иных материалов (Приложения 1-5):
Фиг. 1. Хроматограмма образца препарата «Аллерген Н-ал весенняя смесь ранняя». На хроматограмме обозначены пики фенола (время удерживания 5,202 мин и площадь пика 142,213) и 2-феноксиэтанола (время удерживания 6,304 мин и площадь пика 187,318).
Фиг. 2. Хроматограмма образца вакцины брюшнотифозной полисахаридной «Вианвак». На хроматограмме обозначены пики фенола (время удерживания 5,202 мин и площадь пика 95,2378) и 2-феноксиэтанола (время удерживания 6,302 мин и площадь пика 190,774).
Фиг. 3. Хроматограмма образца вакцины пневмококковой поливалентной полисахаридной «Пневмо 23». На хроматограмме обозначены пики фенола (время удерживания 5,200 мин и площадь пика 156,108) и 2-феноксиэтанола (время удерживания 6,304 мин и площадь пика 176,932).
Фиг. 4. Хроматограмма стандартного раствора фенола с концентрацией 1 мг/мл. На хроматограмме обозначены пики фенола (время удерживания 5,202 мин и площадь пика 124,811) и 2-феноксиэтанола (время удерживания 6,305 мин и площадь пика 181,925).
Фиг. 5. Хроматограмма стандартного раствора фенола с концентрацией 3 мг/мл. На хроматограмме обозначены пики фенола (время удерживания 5,200 мин и площадь пика 259,401) и 2-феноксиэтанола (время удерживания 6,302 мин и площадь пика 170,32).
Фиг. 6. Хроматограмма стандартного раствора фенола с концентрацией 5 мг/мл. На хроматограмме обозначены пики фенола (время удерживания 5,200 мин и площадь пика 367,874) и 2-феноксиэтанола (время удерживания 6,300 мин и площадь пика 196,225).
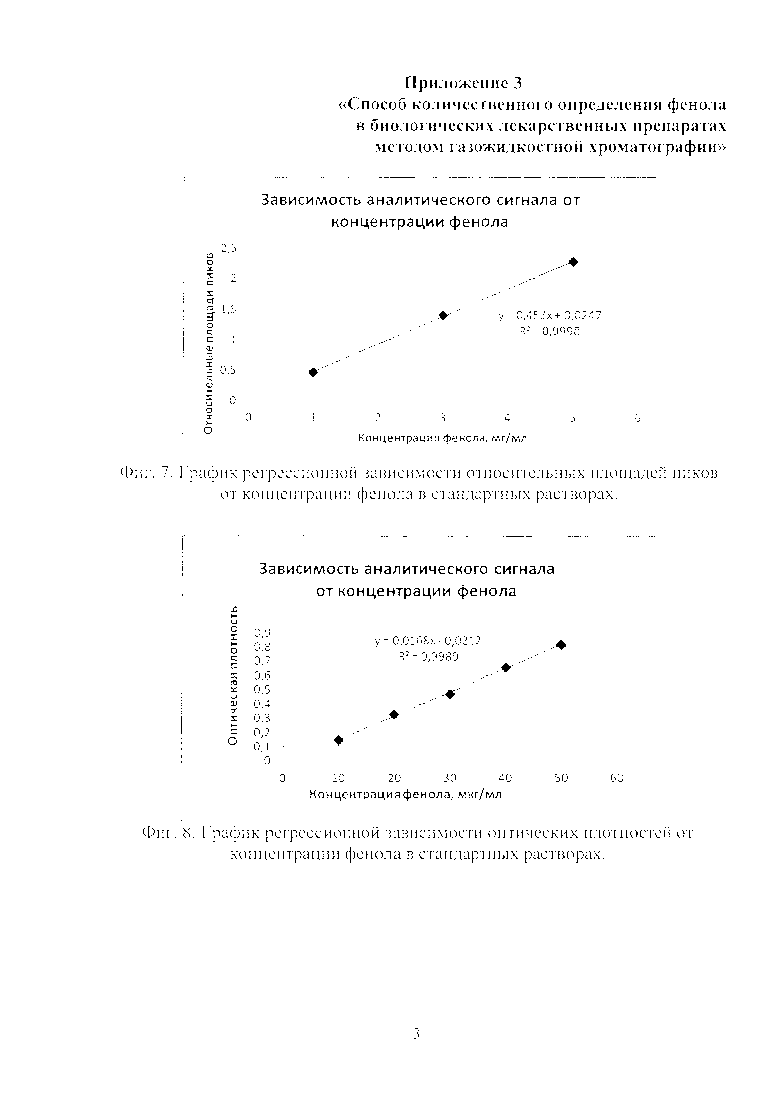
Фиг. 7. График регрессионной зависимости относительных площадей пиков от концентрации фенола в стандартных растворах. На рисунке представлен калибровочный график, полученный при воспроизведении заявляемого способа и отражающий зависимость отношения площади пика фенола к площади пика внутреннего стандарта от концентрации фенола в стандартном растворе.
Фиг. 8. График регрессионной зависимости оптических плотностей от концентрации фенола в стандартных растворах. На рисунке представлен калибровочный график, полученный при воспроизведении способа прототипа и отражающий зависимость оптической плотности от концентрации фенола в стандартном растворе.
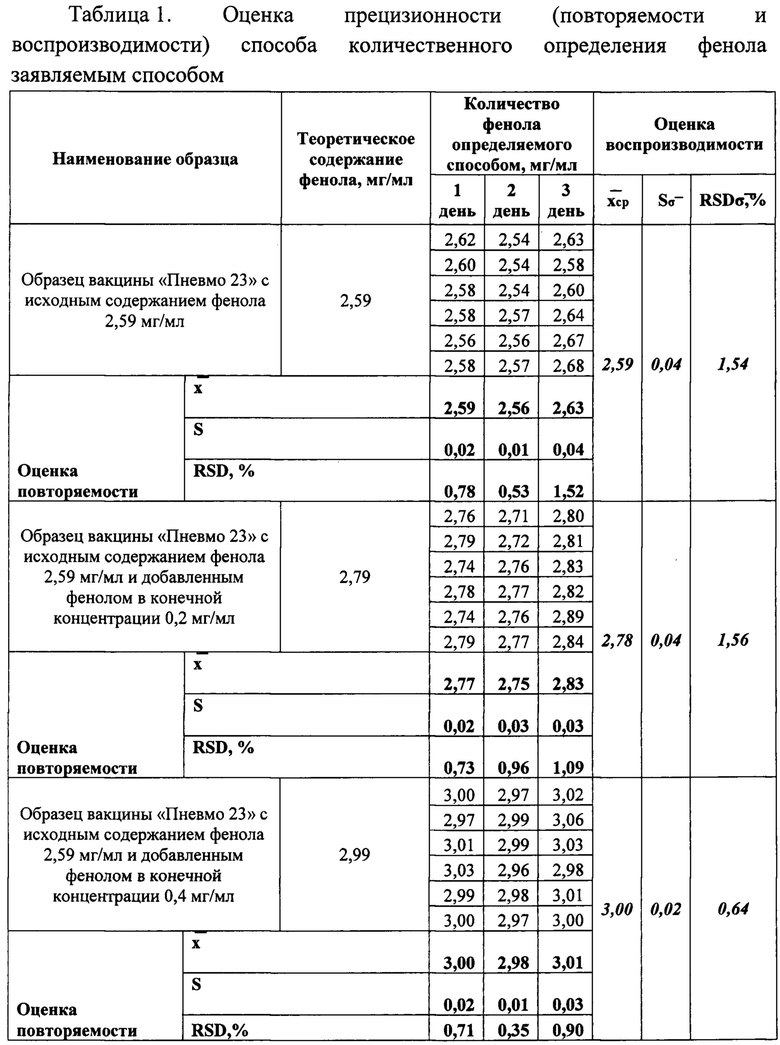
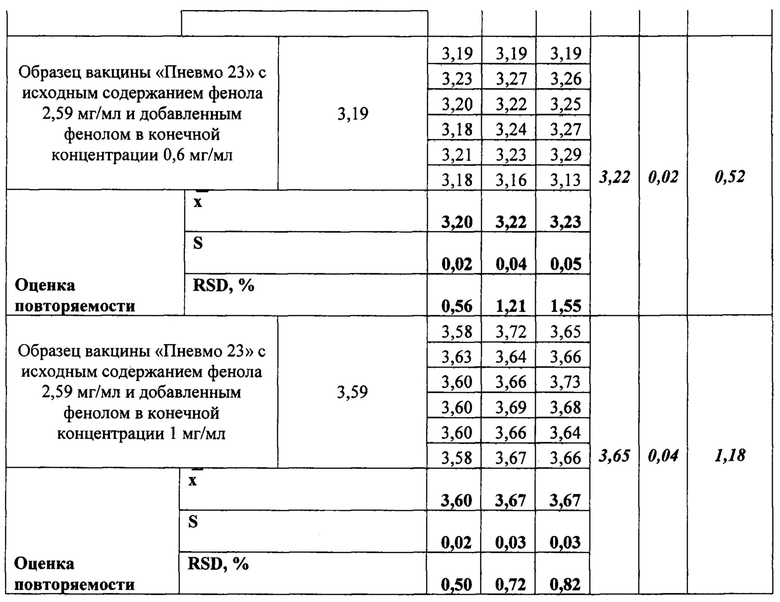
Таблица 1. Оценка прецизионности (повторяемости и воспроизводимости) способа количественного определения фенола заявляемым способом. Исследование проводили с применением метода добавок.
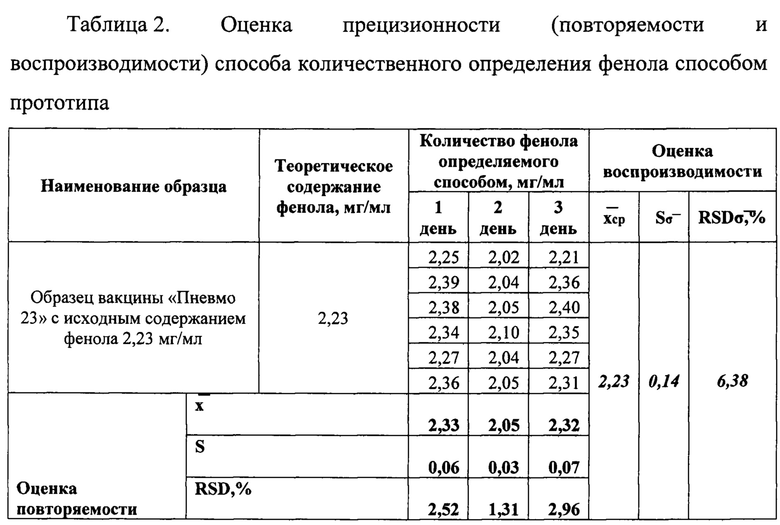
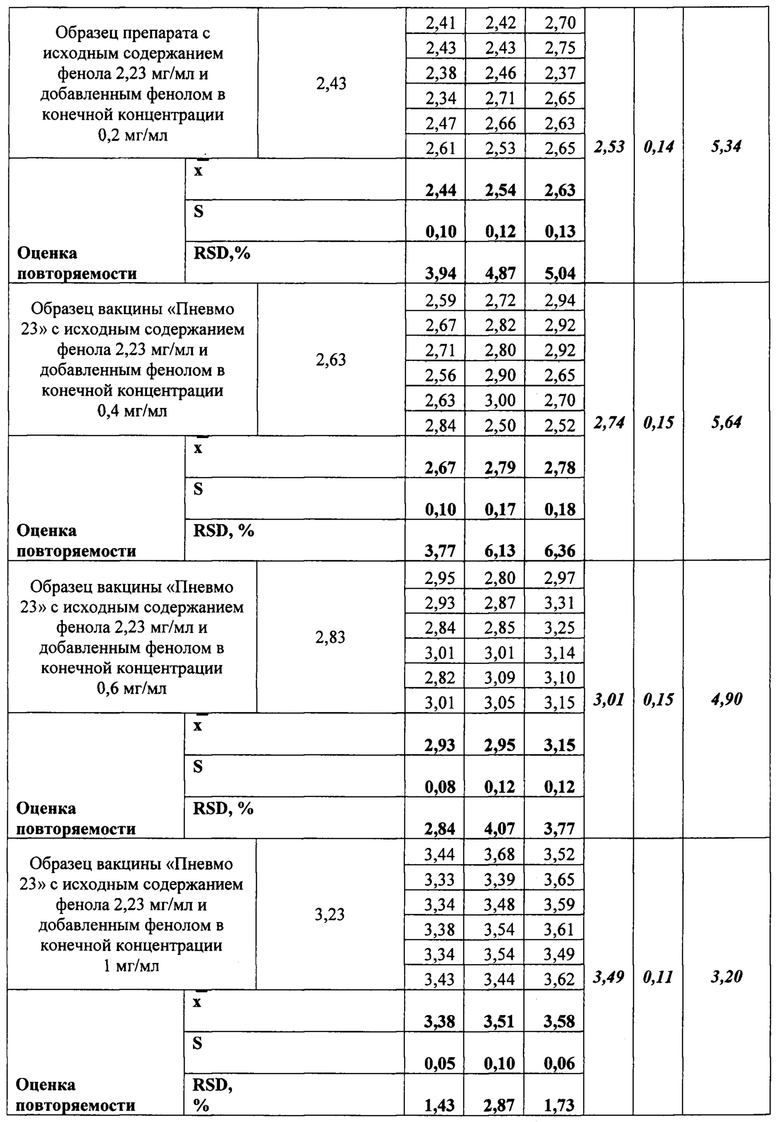
Таблица 2. Оценка прецизионности (повторяемости и воспроизводимости) способа количественного определения фенола способом прототипа. Исследование проводили с применением метода добавок.
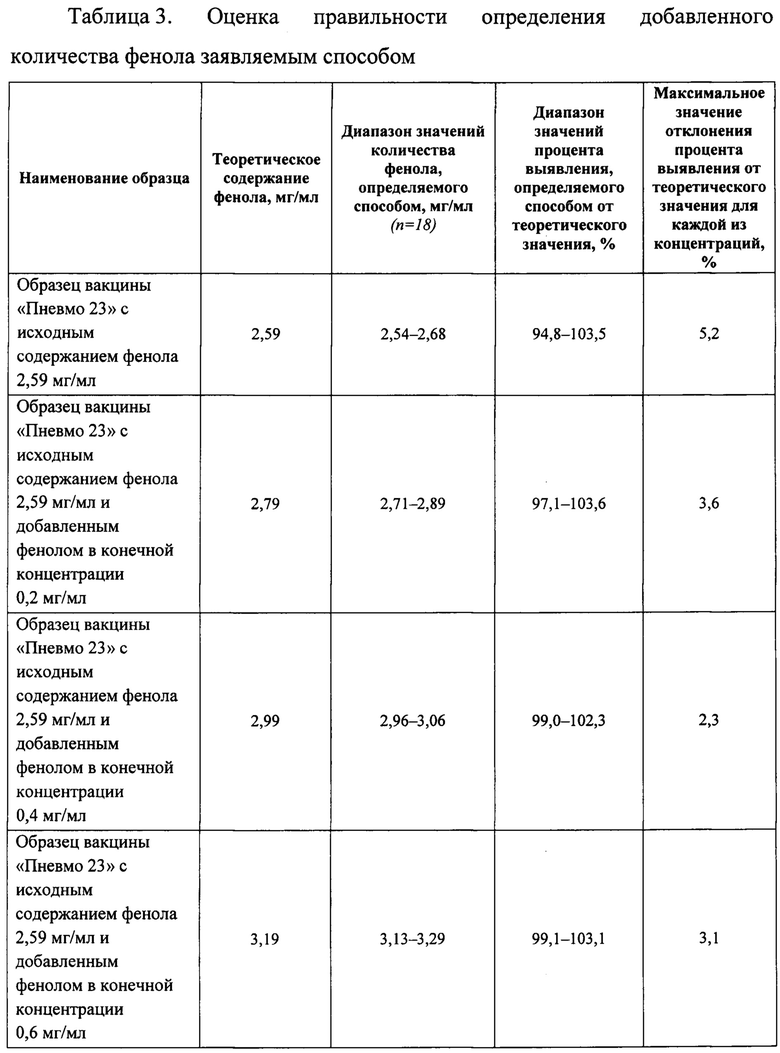
Таблица 3. Оценка правильности способа количественного определения фенола заявляемым способом. Исследование проводили с применением метода добавок.
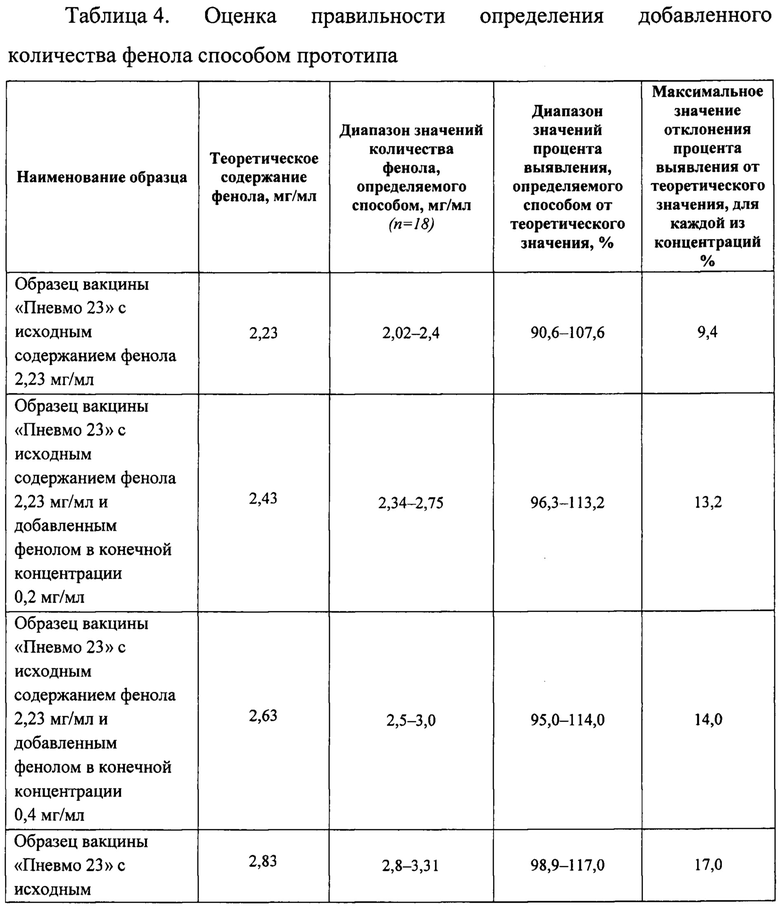
Таблица 4. Оценка правильности способа количественного определения фенола способом прототипа. Исследование проводили с применением метода добавок.
Возможность применения заявляемого изобретения показана следующими примерами:
Пример 1. Определение фенола в препарате «Аллерген Н-ал весенняя смесь ранняя», производство «Севафарма» а.о., Чешская республика (Фиг. 1) заявляемым способом.
Приготовление стандартных растворов с концентрацией фенола 1-5 мг/мл проводят в соответствии с описанием изобретения.
Исследуемый образец: 1,0 мл препарата «Аллерген Н-ал весенняя смесь ранняя», без предварительного разведения, вносят в виалу №4 для хроматографирования объемом 1,5 мл. В ту же виалу добавляют 0,5 мл внутреннего стандарта, перемешивают.
Последовательность ввода образцов соответствует номеру виалы.
Подтверждение критериев пригодности хроматографической системы:
- коэффициент асимметрии пика 0,96;
- число теоретических тарелок 205260;
- разрешение пика 21,3.
Результат: содержание фенола в препарате 1,87 мг/мл. Данный пример показывает возможность использования заявляемого способа для определения фенола в указанном препарате.
Пример 2. Определение фенола в вакцине брюшнотифозной полисахаридной «Вианвак», производства «Гритвак», Россия (Фиг. 2) заявляемым способом.
Приготовление стандартных растворов с концентрацией фенола 1-5 мг/мл проводят в соответствии с описанием изобретения.
Исследуемый образец: 1,0 мл вакцины брюшнотифозной полисахаридной «Вианвак» без предварительного разведения вносят в виалу №4 для хроматографирования объемом 1,5 мл. В ту же виалу добавляют 0,5 мл внутреннего стандарта, перемешивают.
Подтверждение критериев пригодности хроматографической системы:
- коэффициент асимметрии пика 0,98;
- число теоретических тарелок 232452;
- разрешение пика 22,26.
Результат: содержание фенола в препарате 1,29 мг/мл. Данный пример показывает возможность использования заявляемого способа для определения фенола в указанной вакцине.
Пример 3. Определение фенола в вакцине пневмококковой поливалентной полисахаридной «Пневмо 23», производства «Санофи Пастер», Франция. (Фиг. 3) заявляемым способом.
Приготовление стандартных растворов с концентрацией фенола 1-5 мг/мл проводят в соответствии с описанием изобретения.
Исследуемый образец: 1,0 мл вакцины пневмококковой поливалентной полисахаридной «Пневмо 23» без предварительного разведения вносят в виалу №4 для хроматографирования объемом 1,5 мл. В ту же виалу добавляют 0,5 мл внутреннего стандарта, перемешивают.
Подтверждение критериев пригодности хроматографической системы:
- коэффициент асимметрии пика 0,95;
- число теоретических тарелок 232233;
- разрешение пика 21,95.
Результат: содержание фенола в препарате 2,06 мг/мл. Данный пример показывает возможность использования заявляемого способа для определения фенола в указанной вакцине.
Пример 4. Сравнение специфичности способов определения фенола.
В качестве образцов использованы препараты, отличные по составу (Примеры 1-3).
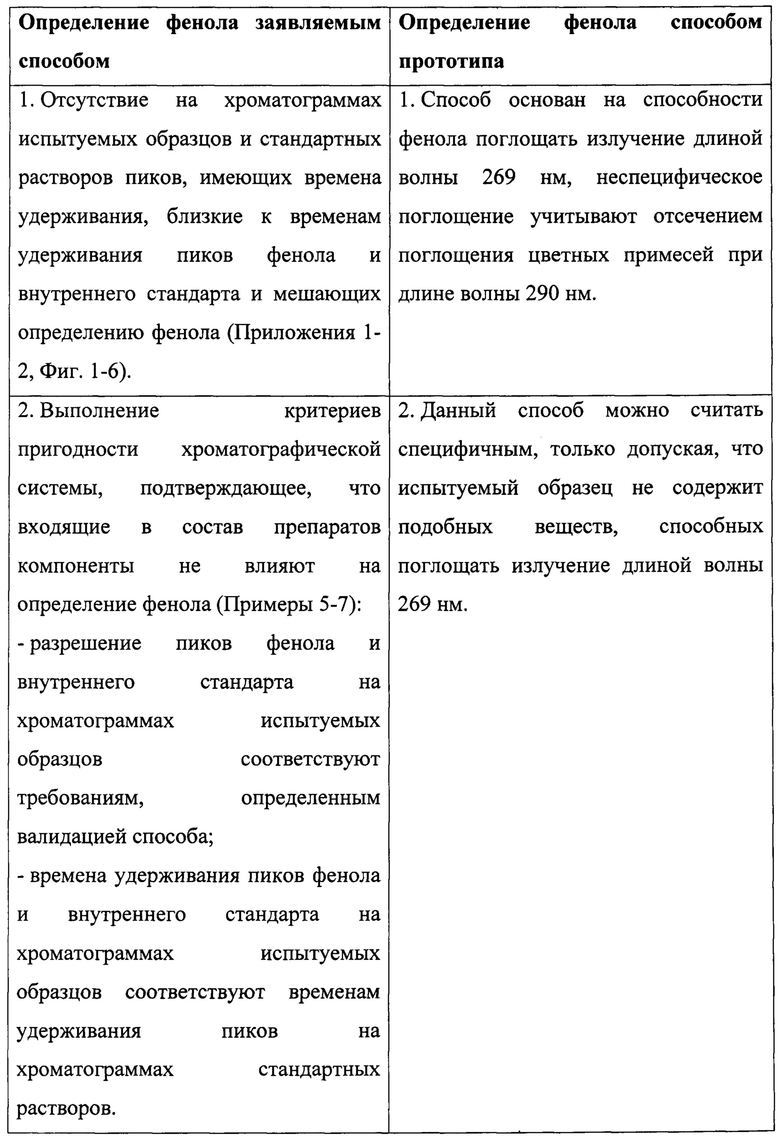
Данный пример показывает, что определение фенола заявляемым способом обладает большей специфичностью за счет возможности разделения компонентов исследуемого образца с последующей идентификацией пика фенола и его количественного определения.
Пример 5. Сравнение линейности способов определения фенола.

Данный пример показывает, что:
1. Аналитическая область заявляемого способа, охватывающая диапазон концентраций допустимого содержания фенола в препаратах БЛП, позволяет исключить стадию пробоподготовки (предварительное разведение образца), что повышает точность количественного определения за счет отсутствия дополнительного источника систематической и/или случайной ошибки определения.
2. Коэффициент детерминации, характеризующий линейность заявляемого способа, ближе к 1, что позволяет сделать вывод о большей точности значений, вычисленных с применением уравнения регрессионной зависимости заявляемого способа.
Пример 6. Сравнение прецизионности (повторяемости и воспроизводимости) способов определения фенола.
Для подтверждения прецизионности (повторяемости и воспроизводимости) заявляемого способа были проведены три независимых серии испытаний исходного образца вакцины пневмококковой поливалентной полисахаридной «Пневмо 23» с исходным содержанием фенола 2,59 мг/мл и 2,23 мг/мл и образцов с добавлением известного количества фенола. Каждый образец готовился в шести повторностях. Результаты определения повторяемости и воспроизводимости способа приведены в Таблице 1 (Приложение 4).
Для сравнительной оценки прецизионности соответствующее количество образцов и измерений было сделано с применением спектрофотометрического способа. Результаты приведены в Таблице 2 (Приложение 4).
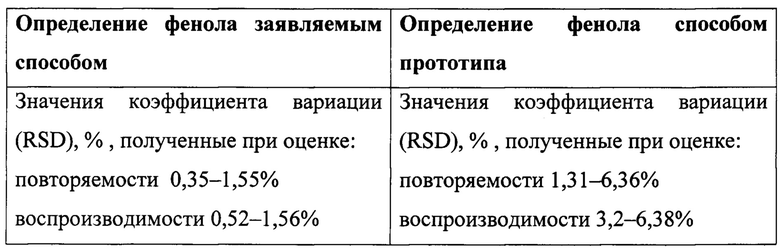
Данный пример показывает, что прецизионность заявляемого способа, характеристикой которой являются величины коэффициентов вариации значений, полученных в условиях повторяемости и воспроизводимости, выше, чем прецизионность способа-прототипа.
Пример 7. Сравнение правильности способов определения фенола.
Правильность способа подтверждают с помощью метода добавок. Вычисляют процент выявления фенола в образце относительно теоретического (истинного) значения. За теоретическое значение принимают сумму исходного количества фенола в препарате и количества фенола внесенного в препарат (добавленного). В качестве образцов использовали вакцину пневмококковую поливалентную полисахаридную «Пневмо 23» с исходным содержанием фенола 2,59 мг/мл и 2,23 мг/мл. Рассчитывали диапазоны значений процентов выявления для каждой из взятых концентраций. Максимальный диапазон значений процентов выявления определяли с учетом наименьшего и наибольшего из всех полученных значений. Результаты приведены в Таблицах 3 и 4 (Приложение 5).
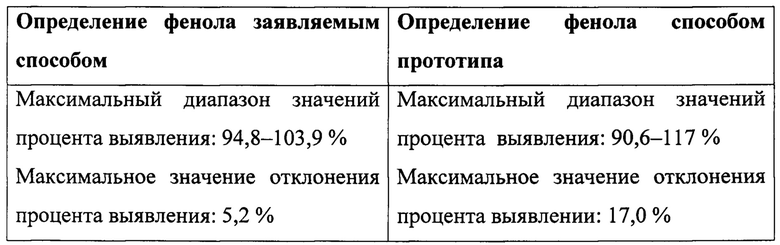
Данный пример показывает, что правильность заявляемого способа определения фенола выше, чем правильность способа прототипа, поскольку максимальное значение отклонения процента выявления определяемого количества фенола от теоретического (истинного) более чем в 3 раза меньше максимального значения отклонения процента выявления способа прототипа.
Источники информации
1. Способ определения фенола в аллергенах (SU, патент 989410, 1983).
2. Способ количественного определения фенола в крови (RU, патент 2188416,2002).
3. European Pharmacopoeia 9.2. Phenol in immunosera and vaccines 01/2008:20515 [Электронный ресурс] http://online6.edqm.eu/ep902/
4. Государственная фармакопея РФ. ГФ XIV. ОФС.1.7.2.0028.15 Количественное определение фенола спектрофотометрическим методом в иммунобиологических лекарственных препаратах [Электронный ресурс] http://femb.ru/femb/pharmacopea.php
5. ГОСТ ИСО 5725-2002 Точность (правильность и прецизионность) методов и результатов измерений.
6. Государственная фармакопея РФ. ГФ XIV. ОФС.1.1.0012.15 Валидация аналитических методик [Электронный ресурс] http://femb.ru/femb/pharmacopea.php
Приложение 4 к заявке на изобретение «Способ количественного определения фенола в биологических лекарственных препаратах методом газожидкостной хроматографии»
Приложение 5 к заявке на изобретение
«Способ количественного определения фенола в биологических лекарственных препаратах методом газожидкостной хроматографии»


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ количественного определения глицина в биологических лекарственных препаратах методом гидрофильной высокоэффективной жидкостной хроматографии | 2019 |
|
RU2700831C1 |
| Определение полисорбата 80 в биологических лекарственных препаратах | 2023 |
|
RU2812788C1 |
| Определение стабилизаторов углеводной природы в биологически активных препаратах | 2023 |
|
RU2816030C1 |
| Способ определения лозартана, его основного метаболита лозартан карбоновой кислоты и глибенкламида в сыворотке крови и моче человека | 2020 |
|
RU2749567C1 |
| Способ определения летучих компонентов в лекарственных препаратах | 2022 |
|
RU2790000C1 |
| Способ определения амиодарона и его основного метаболита дезэтиламиодарона в сыворотке крови человека | 2020 |
|
RU2749566C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПОДЛИННОСТИ И КОЛИЧЕСТВЕННОГО СОДЕРЖАНИЯ БЕНЗЭТОНИЯ ХЛОРИДА В ЛЕКАРСТВЕННЫХ ПРЕПАРАТАХ | 2013 |
|
RU2529814C1 |
| Способ количественного определения фтивазида | 2024 |
|
RU2828350C1 |
| Способ определения дабигатрана в сыворотке крови человека | 2018 |
|
RU2683032C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ 2-ФЕНОКСИЭТАНОЛА В БИОЛОГИЧЕСКИХ СРЕДАХ | 2021 |
|
RU2776730C1 |
Изобретение относится к области здравоохранения, в частности к контролю качества биологических лекарственных препаратов, и может быть использовано для количественного определения фенола в биологических лекарственных препаратах, содержащих фенол в качестве консерванта. Изобретение представляет собой способ количественного определения фенола с помощью газожидкостной хроматографии. Способ предполагает использование исходного препарата без предварительного разведения, автоматический отбор проб, хроматографическое разделение веществ, входящих в состав препарата, и использование внутреннего стандарта, что исключает возможность неспецифического влияния состава образца на количественное определение фенола и снижает вероятность случайной и/или систематической ошибки определения. Предлагаемый способ является более специфичным и точным по сравнению со способами, применяемыми в настоящее время для количественного определения фенола в биологических лекарственных препаратах. 2 з.п. ф-лы, 8 ил., 4 табл.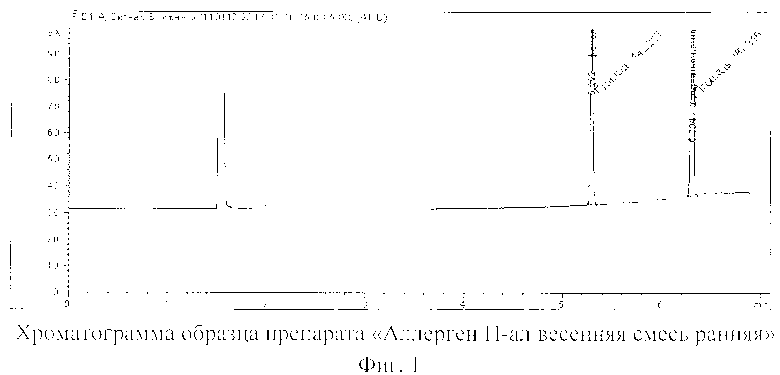
1. Способ количественного определения фенола в биологических лекарственных препаратах с использованием метода газожидкостной хроматографии, характеризующийся тем, что используют хроматографическую колонку, заполненную полиэтиленгликолем, газ-носитель гелий, при температуре инжектора 250°С, в режиме постоянного давления, со скоростью потока 1,4 мл/мин и при температурном профиле печи, в котором начальная температура 160°С, выдержка 3 мин, градиент 40°С/мин до температуры 200°С, выдержка 0,6 мин, градиент 40°С/мин до температуры 220°С, с использованием пламенно-ионизационного детектора при температуре детектора 250°С, в качестве внутреннего стандарта используют 2-феноксиэтанол, далее производят расчет относительно внутреннего стандарта, переводя величину полученного аналитического сигнала в относительные единицы, затем производят оценку результатов с использованием графика регрессионной зависимости относительных площадей пика фенола от концентрации фенола в стандартных растворах.
2. Способ по п. 1, отличающийся тем, что исходный образец биологического лекарственного препарата используют без предварительного разведения.
3. Способ по п. 1, отличающийся тем, что размер хроматографической колонки, заполненной полиэтиленгликолем, 30 м × 0,25 мм × 0,25 мкм.
| Способ определения фенола в аллергенах | 1981 |
|
SU989410A1 |
| СПОСОБ ХРОМАТОГРАФИЧЕСКОГО ОПРЕДЕЛЕНИЯ ФЕНОЛОВ В СТОЧНЫХ ВОДАХ | 2003 |
|
RU2234083C2 |
| JP 2000304665 A, 02.11.2000 | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| XIV, т.2, стр | |||
| Приспособление к ткацкому станку для замены челнока | 1925 |
|
SU2984A1 |
Авторы
Даты
2019-07-03—Публикация
2018-11-26—Подача