Изобретение относится к области фармацевтики и аналитической химии, а именно к способам количественного определения конваллятоксина в лекарственных препаратах, содержащих сердечные гликозиды ландыша, методом высокоэффективной жидкостной хроматографии (ВЭЖХ).
Сердечные гликозиды представляют собой группу биологически активных веществ, обладающих в терапевтических дозах кардиотоническим и антиаритмическим действием. Для обеспечения безопасного использования препаратов на основе ландыша необходимо проводить строгий контроль содержания сердечных гликозидов.
Известна спектрофотометрическая методика количественного определения суммы сердечных гликозидов в пересчете на конваллятоксин (ГФ РФ XV ФС.3.4.0003.18 Ландыша травы настойка). Однако при применении известной методики наблюдается недостаточная селективность в связи с тем, что спектры родственных соединений могут накладываться друг на друга в результате образования хромогенного комплекса при взаимодействии сердечных гликозидов с пикриновой кислотой и давать завышенные результаты, а также метод недостаточно точный, так как не предусмотрено использование стандартного образца в аналогичных условиях испытания.
В качестве прототипа выбран способ количественное определение конваллятоксина методом ВЭЖХ (Agrawal P, Akhade M, Laddha K, Narkhede S, Mirgal A, Salunke C. Quantification of convallatoxin in Antiaris toxicaria Leusch seeds by RP-HPLC. Analytical Chemistry Letters. 2014;4(3):172-7. https://doi.org/10.1080/22297928.2014.925821), который включает разделение соединений на колонке с подвижной фазой, состоящей из растворителя А (ацетронитрила) и растворителя В (вода) в соотношении 20:80 с изократическим элюированием при скорости потока 1,0 мл/мин при комнатной температуре при длине волны детектирования 220 нм. Однако условия хроматографирования, описанные в способе, не позволяют достичь эффективного разделения веществ. При применении известного способа наблюдается перекрывание и пересечение пиков на хроматограммах, это затрудняет корректное интегрирование и количественный анализ конваллятоксина, а также не позволяет определить содержание конваллятоксина в многокомпонентных препаратах ландыша. Также был получен негативный результат оценки спектральной чистоты пика конваллятоксина.
В связи с этим остается актуальной техническая задача поиска наиболее оптимальных условий проведения хроматографического разделения методом высокоэффективной жидкостной хроматографии при создании более селективного и более точного способа количественного определения сердечных гликозидов (конваллятоксина) в лекарственных растительных препаратах на основе ландыша.
Техническим результатом, наблюдаемым при осуществлении предлагаемого авторами способа, является повышение селективности определения конваллятоксина и повышение точности определения его количественного содержания в лекарственном средстве, содержащем сердечные гликозиды ландыша.
Технический результат достигается способом количественного определения конваллятоксина в лекарственных препаратах, содержащих сердечные гликозиды ландыша, который включает осаждение балластных веществ в испытуемом растворе 1-1,5 мл 10 % раствором ацетата свинца, экстракцию сердечных гликозидов 30 мл смеси 96 % спирта и хлороформа в соотношении 2:8, отгонку и фильтрацию, хроматографирование растворов методом ВЭЖХ с использованием обращенно-фазовой колонки с октадецилсилилсиликагельным сорбентом в условиях градиентного элюирования, детектирование с помощью спектрофотометрического детектора при длине волны 220 нм, где подвижная фаза А 0,1 % раствор ортофосфорной кислоты в воде, подвижная фаза Б - ацетонитрил, вычисление количества конваллятоксина в исследуемом препарате по формуле:
Х = 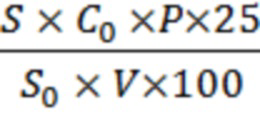 (1),
(1),
где S - площадь пика конваллятоксина на хроматограмме испытуемого раствора; S0 - площадь пика конваллятоксина на хроматограмме стандартного раствора; Р - содержание конваллятоксина в стандартном образце, %; V - объем испытуемого образца; С0 - концентрация конваллятоксина в растворе стандартного образца, мг/мл.
В ходе выбора наиболее оптимальных хроматографических условий авторами проанализированы и выбраны несколько вариантов на основе научных зарубежных публикаций (например, описанный выше способ, выбранный за прототип). При количественном определении конваллятоксина в лекарственных препаратах, содержащих сердечные гликозиды ландыша в условиях проведения ВЭЖХ-методик, раскрытых в источнике информации (Agrawal P, Akhade M, Laddha K, Narkhede S, Mirgal A, Salunke C. Quantification of convallatoxin in Antiaris toxicaria Leusch seeds by RP-HPLC. Analytical Chemistry Letters. 2014;4(3):172-7. https://doi.org/10.1080/22297928.2014.925821). Сравнительные результаты, полученные при применении способа прототипа и способа, предложенного авторами, представлены в таблице 1.
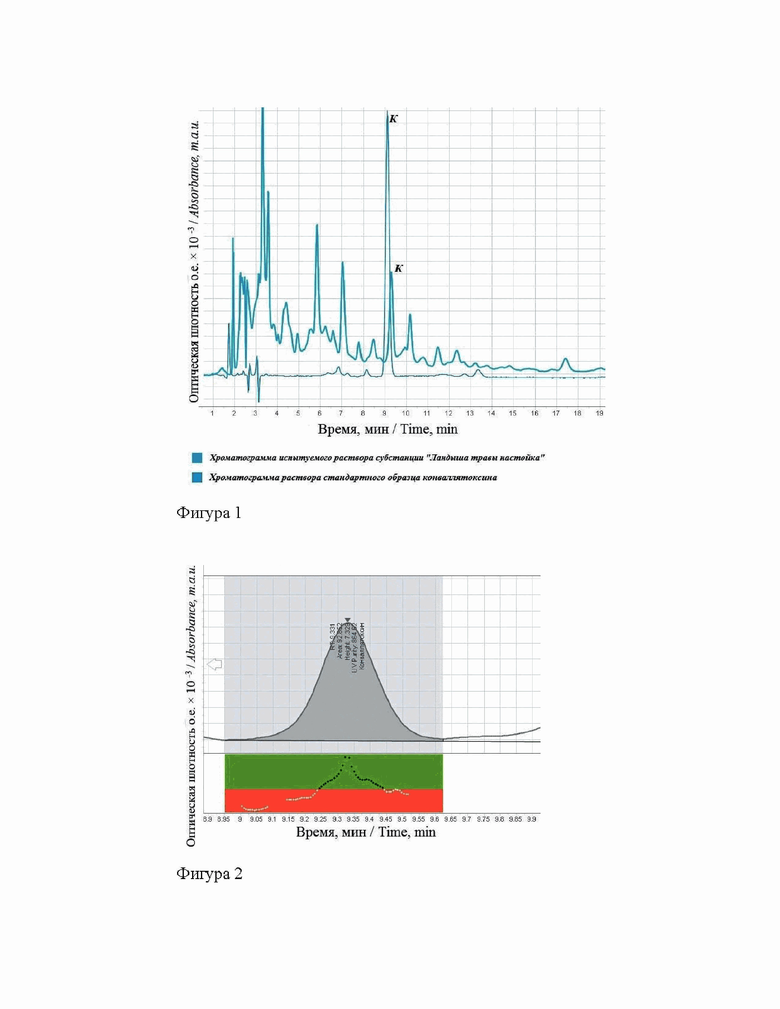
Условия хроматографирования методом ВЭЖХ известного способа (прототипа) не позволили достичь эффективного разделения веществ - разрешение (RS) между пиком конваллятоксина и ближайшим пиком на хроматограмме испытуемого раствора составило 2,5 (фигура 1).
На фигуре 2 представлена типичная хроматограмма испытуемого раствора и раствора стандартного образца конваллятоксина (К - пик конваллятоксина) (оценка спектральной чистоты пика конваллятоксина компьютерной программой Agilent в условиях способа, выбранного за прототип). При осуществлении способа прототипа получен негативный результат оценки спектральной чистоты пика конваллятоксина (864,62).
Все эти факторы затруднили корректное интегрирование, в результате было получено высокое значение относительного стандартного отклонения (RSD) - 2,57 % и 2,67 % соответственно, что повлияло на точность количественного определения. В предлагаемом авторами способе подобраны оптимальные условия хроматографирования, включающие использование обращенно-фазовой колонки с октадецилсилилсиликагельным сорбентом, значение рН подвижной фазы (рН около 2,10 устанавливается с помощью подвижной фазы А - 0,1 % раствор ортофосфорной кислоты в воде), а также использован градиентный режим элюирования, позволяющий полностью разделить пики, повысив селективность способа - разрешение (RS) между пиком конваллятоксина и ближайшим пиком на хроматограмме испытуемого раствора составило 4,40. При оценке спектральной чистоты пиков конваллятоксина коэффициент подобия составил 999,91. Совокупность подобранных авторами условий позволяет достичь наилучшего хроматографического разделения и повысить эффективность способа количественного определения конваллятоксина в лекарственных препаратах, содержащих сердечные гликозиды ландыша с помощью предложенной формулы (1) расчета количества конваллятоксина в лекарственном препарате.
Пробоподготовка включала в себя стадию очистки испытуемых растворов от балластных веществ 10 % раствором ацетата свинца и последующую экстракцию сердечных гликозидов 30 мл смеси 96 % спирта и хлороформа в соотношении 2:8. Из-за разницы в полярности, сердечные гликозиды переходят в органическую фазу, тогда как большинство балластных веществ остаются в водной фазе. Использование таких способов очистки позволило уменьшить содержание нежелательных компонентов пробы, снизить уровень фона на хроматограмме испытуемого раствора, улучшило разрешение и облегчило идентификацию и количественное определение целевого соединения - конваллятоксина.
В таблице 1 представлены количественные данные конваллятоксина, полученные в результате осуществления способа, выбранного за прототип и предлагаемого авторами способа в лекарственном препарате «Ландыша травы настойка» (RSD - относительное стандартное отклонение).
Таблица 1
(RSD = 0,18 %)
(RSD = 2,57 %)
(RSD = 0,67 %)
(RSD = 2,67 %)
Пример 1. Определение количественного содержания конваллятоксина в лекарственном препарате «Ландыша травы настойка» предлагаемым способом
Для приготовления испытуемых растворов было использовано два образца субстанции «Ландыша травы настойка». Испытуемые растворы готовились в трех повторностях. 5,0 мл помещали в круглодонную колбу, прибавляли 5 мл воды очищенной и упаривали на роторном испарителе до объема около 7 мл. Объем испытуемого раствора доводили водой очищенной до 10 мл, прибавляли 1 мл 10 % раствора свинца ацетата и тщательно перемешивали. Затем испытуемый раствор фильтровали через бумажный складчатый фильтр «черная лента», смоченный водой, в делительную воронку. Фильтр промывали 5 мл воды. В делительную воронку к испытуемому раствору прибавляли 30 мл смеси спирт 96 % - хлороформ (2:8) и взбалтывали на орбитальном шейкере в течение 5 мин. После расслаивания нижний хлороформный слой фильтровали через бумажный фильтр, содержащий 3 г натрия сульфата безводного, смоченного 5 мл хлороформа, в колбу для отгона. Операцию извлечения спирто-хлороформной смесью повторяли еще 2 раза, используя по 30 мл смеси того же состава и фильтровали хлороформные извлечения в ту же колбу. Фильтр с натрия сульфатом безводным, смоченный 5 мл хлороформа, промывали 10 мл спирто-хлороформной смесью, промывную жидкость сливали в ту же колбу.
Полученный фильтрат отгоняли на роторном испарителе под вакуумом, при температуре 45°С. Сухие остатки растворяли в 10 мл спирта 25 %. Испытуемый раствор переносили в мерную колбу вместимостью 25 мл. Колбы для отгона промывали дважды по 5 мл тем же спиртом, испытуемый раствор переносили в ту же мерную колбу. Объем испытуемого раствора в мерной колбе доводили тем же спиртом до метки и перемешивали. Фильтровали полученный испытуемый раствор через мембранный фильтр из регенерированной целлюлозы. Дополнительная хроматографическая очистка испытуемого раствора от сопутствующих веществ с применением полиамида для колоночной хроматографии была признана нецелесообразной.
Для приготовления стандартного раствора 10,15 мг СО конваллятоксина помещали в мерную колбу объемом 100 мл, прибавляли 50 мл 70 % этанола, помещали на 5 минут на УЗ баню, доводили объем раствора тем же растворителем до метки, перемешивали. 1,0 мл полученного раствора переносили в мерную колбу объемом 10 мл, доводили объем раствора 25 % спиртом до метки, перемешивали.
Испытание проводили в условиях градиентного элюирования (таблица 2) на обращено-фазовой колонке Luna 5 μm C18(2) 250 × 4,6 мм. Детектирование осуществляли с помощью спектрофотометрического детектора при длине волны 220 нм. Скорость потока составляла 1 мл/мин, температура колонки - 25°С, температура термостата автосамплера - 5°С, объем вводимой пробы - 20 мкл. Время удерживания конваллятоксина в описанных условиях составило 24 минуты.
Результаты были признаны достоверными, так как выполнялись требования теста «Проверка пригодности хроматографической системы»: значение фактора асимметрии пика конваллятоксина - 1,07; относительное стандартное отклонение площади пика конваллятоксина для 6 определений - 0,21 %.
Хроматографировали испытуемые растворы
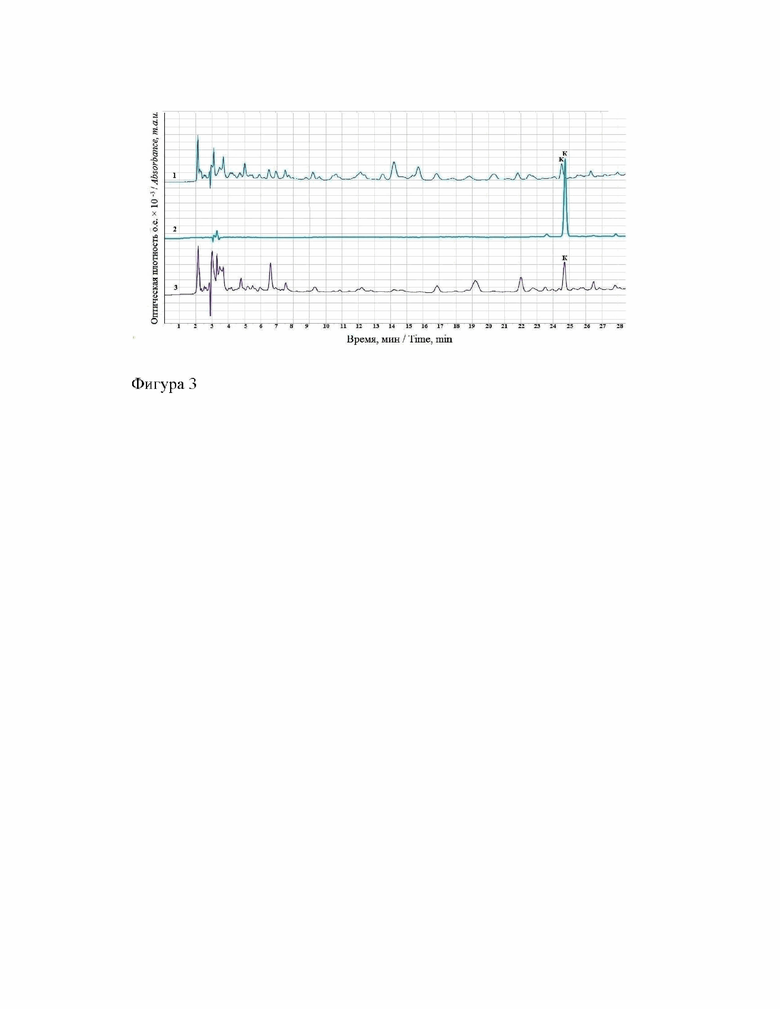
На фигуре 3 представлена типичная хроматограмма испытуемых растворов и раствора стандартного образца конваллятоксина (1 - испытуемый раствор «Зеленина капли»; 2 - СО конваллятоксина, 3 - испытуемый раствор субстанции «Ландыша травы настойка»; К - пик конваллятоксина).
Таблица 2
Содержание конваллятоксина в препарате «Ландыша настойка», мг/мл, расчитывали по формуле:
Х = 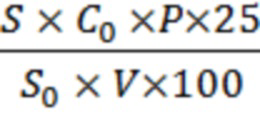 ,
,
где S - площадь пика конваллятоксина на хроматограмме испытуемого раствора; S0 - площадь пика конваллятоксина на хроматограмме стандартного раствора; Р - содержание конваллятоксина в стандартном образце, %; V - объем испытуемого образца; С0 - концентрация конваллятоксина в растворе стандартного образца, мг/мл,
где Х1, Х2, Х3 - содержание конваллятоксина в испытуемом образце; в расчетах использовали средние значения площадей пиков.
Образец 1
Х1 = 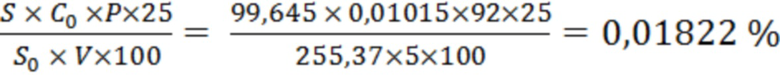 ;
;
Х2 = 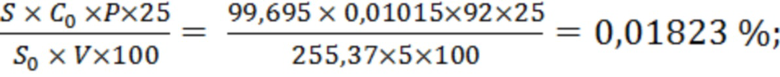
Х3 = 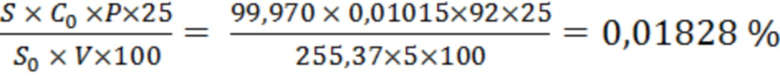 ;
;
Образец 2
Х1 = 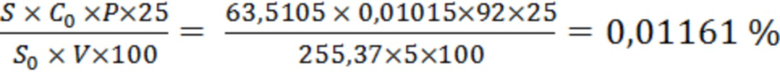 ;
;
Х2 = 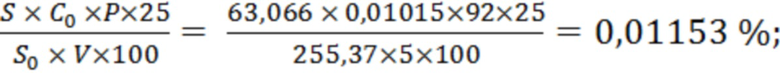
Х3 = 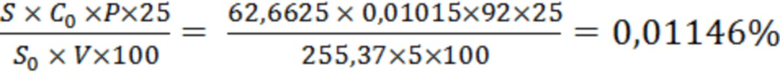 .
.
Таблица 3
субстанция «Ландыша травы настойка»
255,36
255,49
255,21
255,49
256,18
Среднее значение:
255,37
99,71
63,658
100,22
63,438
100,23
62,344
0,01823
0,01828
0,01153
0,01146
Пример 2. Определение количественного содержания конваллятоксина в лекарственном препарате «Зеленина капли» предлагаемым способом
Испытуемые растворы готовились в трех повторностях. 12,5 мл лекарственного препарата «Зеленина капли» (авторами экспериментально доказано, что условия предлагаемого способа, раскрытые в примере 2 подходят также для лекарственных препаратов «Валокормид»/ «Стабикардин» / «Карниланд») помещали в круглодонную колбу и упаривали до объема 5 мл на роторном испарителе. К полученному раствору добавляли 1,5 мл 10 % раствора свинца ацетата. Объем раствора доводили до первоначального объема (12,5 мл) водой очищенной и фильтровали через бумажный складчатый фильтр «черная лента», смоченный водой, в делительную воронку. Фильтр промывали 5 мл воды. В делительную воронку прибавляли 30 мл смеси спирт 96 % - хлороформ (2:8) и взбалтывали на орбитальном шейкере в течение 5 мин. После расслаивания нижний хлороформный слой фильтровали через бумажный фильтр, содержащий 3 г натрия сульфата безводного, смоченного 5 мл хлороформа, в колбу для отгона. Операцию извлечения спирто-хлороформной смесью повторяли еще 2 раза, используя по 30 мл смеси того же состава и фильтровали хлороформные извлечения в ту же колбу. Фильтр с натрия сульфатом безводным, промывали 10 мл спирто-хлороформной смесью, промывную жидкость сливали в ту же колбу.
Полученный фильтрат отгоняли на роторном испарителе под вакуумом, при температуре 45°С. Сухие остатки растворяли в 10 мл спирта 25 %. Испытуемый раствор переносили в мерную колбу вместимостью 25 мл. Колбы для отгона промывали дважды по 5 мл тем же спиртом, испытуемый раствор переносили в ту же мерную колбу. Объем испытуемого раствора в мерной колбе доводили тем же спиртом до метки и перемешивали. Фильтровали полученный испытуемый раствор через мембранный фильтр из регенерированной целлюлозы. испытуемый раствор через мембранный фильтр из регенерированной целлюлозы. Дополнительно проводили хроматографическая очистка испытуемого раствора от сопутствующих веществ с применением полиамида для колоночной хроматографии была признана нецелесообразной.
Для приготовления стандартного раствора 10,15 мг СО конваллятоксина помещали в мерную колбу объемом 100 мл, прибавляли 50 мл 70 % этанола, помещали на 5 минут на УЗ баню, доводили объем раствора тем же растворителем до метки, перемешивали. 1,0 мл полученного раствора переносили в мерную колбу объемом 10 мл, доводили объем раствора 25 % спиртом до метки, перемешивали.
Испытание проводили в условиях градиентного элюирования (табл. 2) на обращено-фазовой колонке Luna 5 μm C18(2) 250 × 4,6 мм. Детектирование осуществляли с помощью спектрофотометрического детектора при длине волны 220 нм. Скорость потока составляла 1 мл/мин, температура колонки - 25°С, температура термостата автосамплера - 5°С, объем вводимой пробы - 20 мкл. Время удерживания конваллятоксина в описанных условиях составило 24 минуты.
Результаты были признаны достоверными, так как выполнялись требования теста «Проверка пригодности хроматографической системы»: значение фактора асимметрии пика конваллятоксина - 1,04; относительное стандартное отклонение площади пика конваллятоксина для 6 определений - 0,08 %.
Хроматографировали испытуемые растворы
Хроматограмма испытуемого раствора показана на фигуре 1 (цифра 1).
Содержание конваллятоксина в препарате «Зеленина Капли», мг/мл, расчитывали по формуле:
Х = 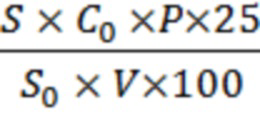 ,
,
где S - площадь пика конваллятоксина на хроматограмме испытуемого раствора; S0 - площадь пика конваллятоксина на хроматограмме стандартного раствора; Р - содержание конваллятоксина в стандартном образце, %; V - объем испытуемого образца; С0 - концентрация конваллятоксина в растворе стандартного образца, мг/мл
Х1 = 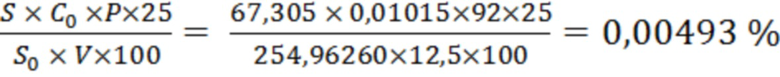 ;
;
Х2 = 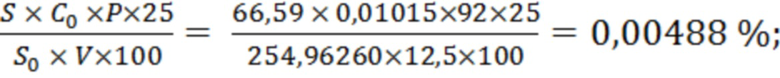
Х3 = 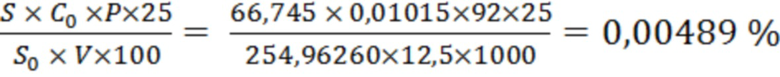 ;
;
Таблица 3
Зеленина капли
254,91600
254,89500
255,17000
255,18100
255,18100
Среднее значение:
254,999
67,16
67,91
66,97
0,00488
0,00489
Пример 3. Подтверждающий, что применение разработанного авторами способа позволяет получать достоверные и воспроизводимые результаты.
Экспериментальная часть исследования включала идентификацию и количественное определение конваллятоксина в лекарственных растительных препаратах на основе ландыша методом ВЭЖХ. В качестве объектов исследования были использованы образцы: субстанция «Ландыша настойка», лекарственные препараты: «Зеленина капли», «Валокормид», «Стабикардин®», «Карниланд®», «Экстракт ландыша - стандартный образец», стандартный образец конваллятоксина, Sigma-Aldrich, CAS-No. 508-75-8, серия BCCF2229, содержание основного вещества 92,0 %.
Для подтверждения специфичности в многокомпонентных препаратах ландыша были приготовлены растворы плацебо, содержащие настойку пустырника, настойку валерианы, настойку боярышника, левоментол и натрия бромид. На хроматограммах растворов плацебо пики со временем удерживания, совпадающим со временем удерживания пика конваллятоксина, отсутствовали.
Была проведена оценка пригодности хроматографической системы на хроматограмме СО конваллятоксина по следующим параметрам:
- значение асимметрии пика конваллятоксина - 1,07;
- относительное стандартное отклонение площади пика конваллятоксина для 6 определений - 0,21 %;
В ходе проведения валидационных исследований методики получены результаты, соответствующие критериям приемлемости (табл. 5). Разработанный способ количественного определения конваллятоксина в препаратах ландыша позволяет получать достоверные, воспроизводимые результаты. Результаты валидационных исследований способа определения конваллятоксина в лекарственном растительном препарате «Ландыша травы настойка» приведены в таблице 4.
Таблица 4
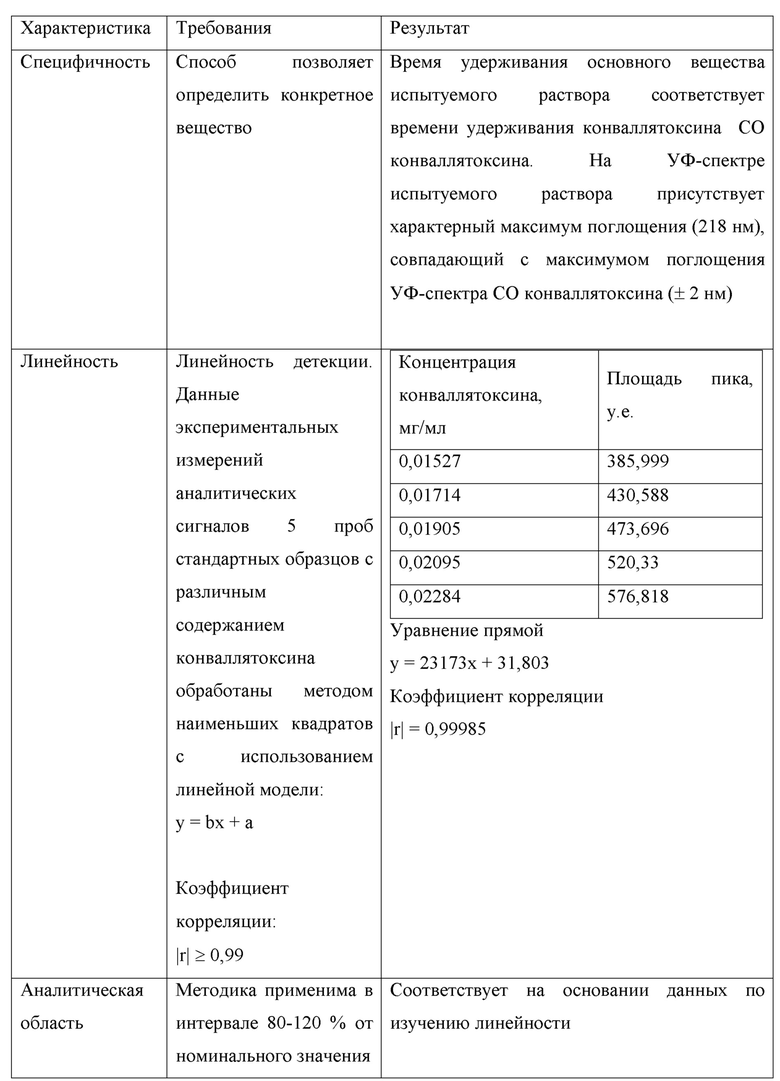
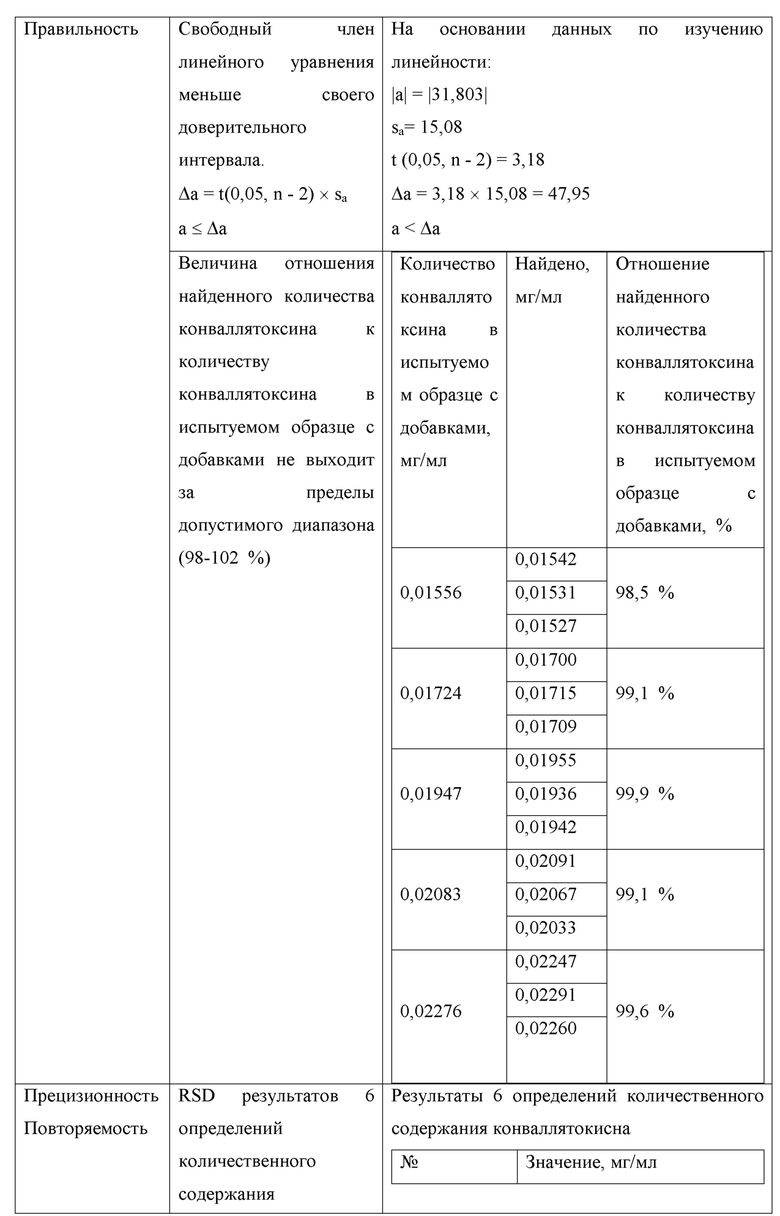
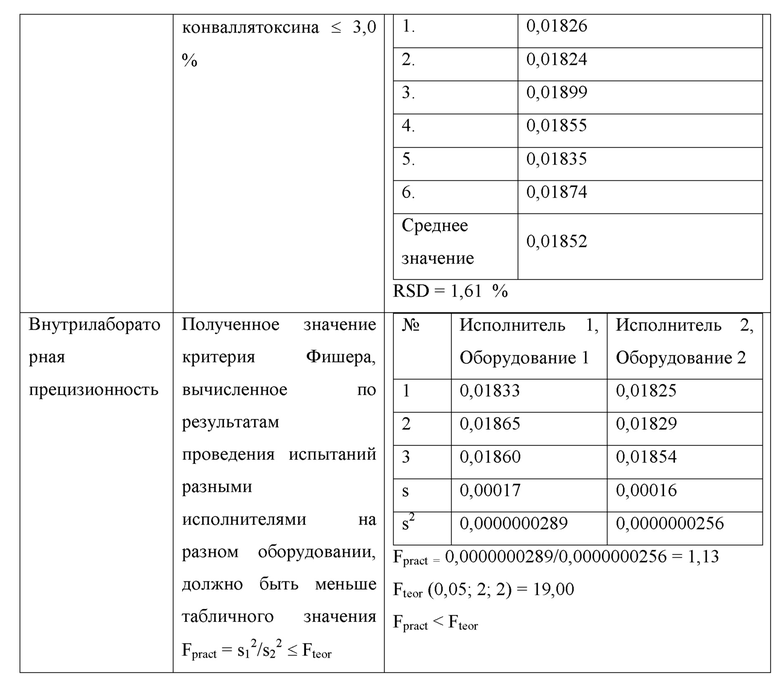
Таким образом, применение разработанного авторами способа количественного определения конваллятоксина в лекарственных препаратах, содержащих сердечные гликозиды ландыша, позволяет получать достоверные и воспроизводимые результаты, в сравнении с выбранным за прототип способом при осуществлении предлагаемого авторами способа наблюдается повышение селективности определения конваллятоксина и повышение точности определения его количественного содержания в лекарственном средстве, содержащем сердечные гликозиды ландыша.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ определения суммы сесквитерпеновых кислот в пересчете на валереновую кислоту методом ВЭЖХ в лекарственных средствах | 2020 |
|
RU2744231C1 |
| Способ количественного определения флавоноидов в плодах и настойке боярышника | 2024 |
|
RU2838184C1 |
| Способ количественного определения аскорбиновой кислоты в лекарственных растительных препаратах | 2023 |
|
RU2801885C1 |
| Способ количественного определения папаверина гидрохлорида и его родственных примесей в лекарственных средствах | 2021 |
|
RU2772608C1 |
| Способ количественного определения глицина в биологических лекарственных препаратах методом гидрофильной высокоэффективной жидкостной хроматографии | 2019 |
|
RU2700831C1 |
| Способ определения парабенов методом ГЖХ в лекарственных препаратах | 2020 |
|
RU2747370C1 |
| Способ количественного определения фтивазида | 2024 |
|
RU2828350C1 |
| Способ определения флавоноидов в траве горца перечного и траве горца птичьего | 2024 |
|
RU2839147C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ НАРЦИССИНА В ЦВЕТКАХ КАЛЕНДУЛЫ ЛЕКАРСТВЕННОЙ | 2015 |
|
RU2599016C1 |
| Способ определения арбутина в листьях толокнянки | 2023 |
|
RU2802173C1 |
Использование: для количественного определения конваллятоксина в лекарственных препаратах, содержащих сердечные гликозиды ландыша. Сущность изобретения заключается в том, что количественное определение конваллятоксина в лекарственных препаратах, содержащих сердечные гликозиды ландыша, осуществляется посредством жидкостной хроматографии. Технический результат: обеспечение возможности повышения точности определения конваллятоксина в лекарственных препаратах. 3 ил., 5 табл.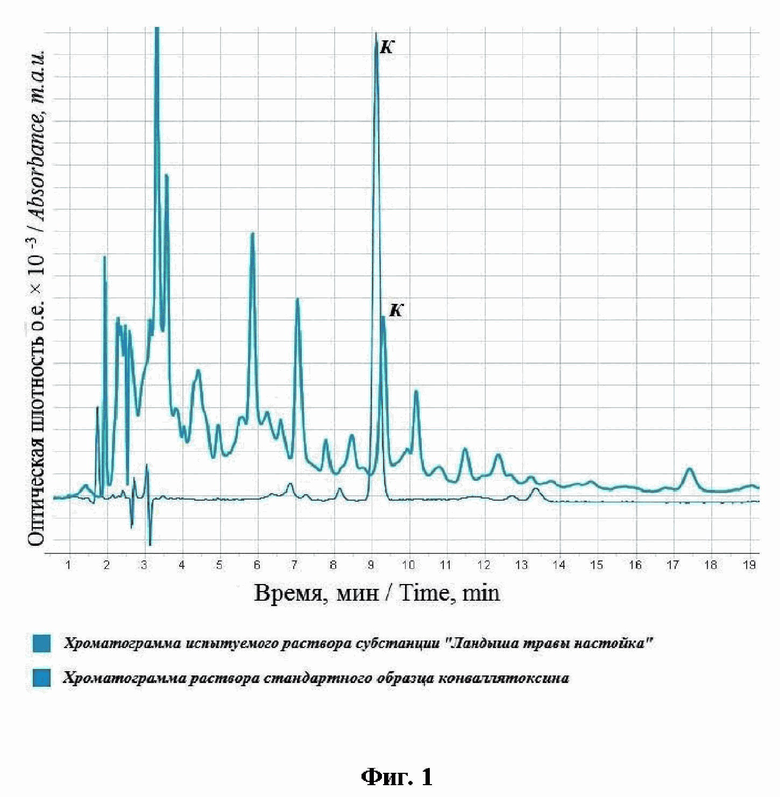
Способ количественного определения конваллятоксина в лекарственных препаратах, содержащих сердечные гликозиды ландыша, характеризующийся тем, что осаждают балластные вещества в растворе испытуемого лекарственного препарата 10 % раствором ацетата свинца в количестве 1-1,5 мл, осуществляют экстракцию сердечных гликозидов 30 мл смеси 96 % спирта и хлороформа в соотношении 2:8, затем проводят отгонку и фильтрацию, хроматографируют раствор испытуемого лекарственного препарата методом ВЭЖХ с использованием обращенно-фазовой колонки с октадецилсилилсиликагельным сорбентом в условиях градиентного элюирования, детектирование проводят с помощью спектрофотометрического детектора при длине волны 220 нм, где подвижная фаза А 0,1 % раствор ортофосфорной кислоты в воде, подвижная фаза Б – ацетонитрил, вычисляют количество конваллятоксина в исследуемом препарате по формуле:
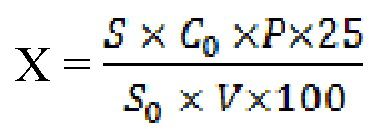 ,
,
где S – площадь пика конваллятоксина на хроматограмме испытуемого раствора; S0 – площадь пика конваллятоксина на хроматограмме стандартного раствора; Р – содержание конваллятоксина в стандартном образце, %; V – объем испытуемого образца; С0 – концентрация конваллятоксина в растворе стандартного образца, мг/мл.
| Agrawal P, Akhade M, Laddha K, Narkhede S, Mirgal A, Salunke C | |||
| Quantification of convallatoxin in Antiaris toxicaria Leusch seeds by RP-HPLC, Analytical Chemistry Letters, 2014, pp | |||
| Приспособление для воспроизведения изображения на светочувствительной фильме при посредстве промежуточного клише в способе фотоэлектрической передачи изображений на расстояние | 1920 |
|
SU172A1 |
| JP H03111758 A, 13.05.1991 | |||
| CN 101972292 A, 16.02.2011 | |||
| CN 107589206 A, 16.01.2018 | |||
| CN 108680695 A, 19.10.2018 | |||
| Способ определения концентрации сердечных гликозидов в растворе | 1986 |
|
SU1352368A1 |
Авторы
Даты
2025-03-31—Публикация
2024-12-19—Подача