ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Область, к которой относится изобретение
В настоящем изобретении представлены терапевтические способы лечения больного злокачественным новообразованием при помощи TG02 и второго терапевтического средства, например, TG02 и ингибитора контрольной точек иммунного ответа, TG02 и ингибитора COX-2, и TG02 и ингибитора контрольных точек иммунного ответа и ингибитора COX-2.
Уровень техники
TG02 представляет собой мультитаргетный ингибитор киназ на основе пиримидина, который ингибирует CDK 1, 2, 5, 7 и 9 вместе с JAK2 и FLT3. Он дозозависимым образом ингибирует нисходящие сигнальные пути CDKs, JAK2 и FLT3 в раковых клетках, при этом основными мишенями являются CDK. TG02 является антипролиферативным в широком ряде опухолевых клеточных линий, индуцируя остановку клеточного цикла G1 и апоптоз. Первичные культуры клеток-предшественников, полученные от пациентов с острым миелоидным лейкозом (AML) и истинной полицитемией, очень чувствительны к TG02. Сравнение с референсными ингибиторами, которые блокируют только одну из основных мишеней TG02, демонстрируют преимущества совместного ингибирования CDK и JAK2/FLT3 в клеточных линиях, а также в первичных клетках. См. Goh et al., Leukemia 26:236-43 (2012). TG02 также известен как SB1317 и под его химическим названием: (16E)-14-метил-20-окса-5,7,14,26-тетраазатетрацикло[19.3.1.1(2,6).1(8,12)]гептакоза-1(25),2(26),3,5,8(27),9,11,16,21,23-декаен. TG02 раскрыт как Соединение 1 в US 8143255. US 9120815 раскрывает различные соли, например, TG02 цитрат, и кристаллические формы TG02. Химическая структура TG02 представляет собой:
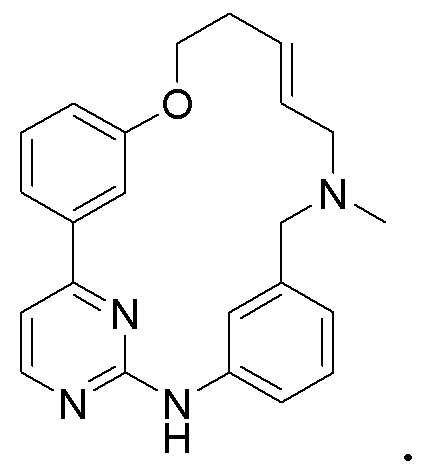
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В одном аспекте в настоящем изобретении представлены терапевтические способы лечения больного злокачественным новообразованием, которые включают введение пациенту терапевтически эффективного количества TG02. В другом аспекте злокачественное новообразование у пациента характеризуется как сверхэкспрессирующий MYC, MCL1 или оба.
В другом аспекте в настоящем изобретении представлены терапевтические способы лечения больного злокачественным новообразованием, включающие введение пациенту терапевтически эффективных количеств TG02 и ингибитора контрольных точек иммунного ответа, например, ингибитора PD-1, ингибитора PD-L1, ингибитора CTLA-4, ингибитора LAG3, ингибитора TIM3 или ингибитора cd47.
В другом аспекте в настоящем изобретении представлены терапевтические способы лечения больного злокачественным новообразованием, включающие введение пациенту терапевтически эффективных количеств TG02 и ингибитора COX, например, априкоксиба или 6-бром-8-(метил-D3)-2-(трифторметил)-2H-хромен-3-карбоновой кислоты.
В другом аспекте в настоящем изобретении представлены терапевтические способы лечения больного злокачественным новообразованием, включающие введение пациенту терапевтически эффективных количеств TG02, ингибитора контрольных точек иммунного ответа и ингибитора COX-2.
В другом аспекте в настоящем изобретении представлены терапевтические способы лечения больного злокачественным новообразованием, у которого есть опухоли, которые сверхэкспрессируют MYC, MCL1 или оба.
В другом аспекте в настоящем изобретении представлены наборы, включающие TG02, TG02 и ингибитор контрольных точек иммунного ответа, TG02 и ингибитор COX-2, и TG02 и ингибитор контрольных точек иммунного ответа и ингибитор COX-2.
В другом аспекте в настоящем изобретении представлены фармацевтическую композицию, включающую TG02, ингибитор COX-2, например, априкоксиб или 6-бром-8-(метил-D3)-2-(трифторметил)-2H-хромен-3-карбоновую кислоту и фармацевтически приемлемый эксципиент.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг. 1 представляет гистограмму, показывающую активность in vitro TG02, TMZ (темозоломида) и TG02+TMZ в клетках GSC923.
Фиг. 2 представляет гистограмму, показывающую активность in vitro TG02, TMZ и TG02+TMZ в клетках LN18.
Фиг. 3 представляет гистограмму, показывающую активность in vitro TG02, TMZ и TG02+TMZ в клетках T98G.
Фиг. 4 представляет гистограмму, показывающую активность in vitro TG02, TMZ и TG02+TMZ в клетках U251.
Фиг. 5 представляет гистограмму, показывающую активность in vitro TG02, TMZ и TG02+TMZ в клетках U87.
Фиг. 6 представляет гистограмму, показывающую активность in vitro TG02, TMZ и TG02+TMZ в клетках LN299.
Фиг. 7 представляет гистограмму, показывающую активность in vitro TG02, TMZ и TG02+TMZ в клетках GSC827.
Фиг. 8 представляет гистограмму, показывающую цитотоксичность in vitro TG02, TMZ и TG02+TMZ (T+T) в клетках GSC923.
Фиг. 9 представляет гистограмму, показывающую цитотоксичность in vitro TG02, TMZ и TG02+TMZ (T+T) в клетках U251.
Фиг. 10 представляет гистограмму, показывающую отсутствие активности in vitro TG02, TMZ и TG02+TMZ (T+T) в клетках эндотелия легочной артерии человека.
Фиг. 11 представляет гистограмму, показывающую отсутствие активности in vitro TG02, TMZ и TG02+TMZ (T+T) в астроцитах человека.
Фиг. 12 представляет кривую зависимости доза-ответ, показывающую активность in vitro TG02 и TG02+TMZ в клетках GSC923.
Фиг. 13 представляет кривую зависимости доза-ответ, показывающую активность in vitro TMZ и TG02+TMZ в клетках GSC923.
Фиг. 14 представляет кривую зависимости доза-ответ, показывающую активность in vitro TG02 и TG02+TMZ в клетках U251.
Фиг. 15 представляет кривую зависимости доза-ответ, показывающую активность in vitro TMZ и TG02+TMZ в клетках U251.
Фиг. 16 схематически иллюстрирует введение TG02 и TMZ в мышиной модели с аллотрансплантатом клеток глиомы GL261.
Фиг. 17 представляет линейный график, показывающий процент выживаемости после введения TG02, TMZ и TG02+TMZ в мышиной модели с аллотрансплантатом клеток глиомы GL261.
Фиг. 18 представляет линейный график, показывающий опухолевую нагрузку после введения TG02, TMZ и TG02+TMZ в мышиной модели с аллотрансплантатом клеток глиомы GL261.
Фиг. 19 является иллюстрацией, показывающей эффект TG02 на уровни белка MYC в клетках гепатоцеллюлярной карциномы (HCC).
Фиг. 20 представляет кривую зависимости доза-ответ, показывающую эффект TG02 на уровни белка MYC в клетках HCC.
Фиг. 21 является иллюстрацией, показывающей эффект TG02 на уровни белка MYC в опухолевых клетках HCC.
Фиг. 22 представляет линейный график, показывающий активность in vivo TG02 и TG02+ сорафениб в ортотопической модели HepG2 HCC ксенотрансплантатов.
Фиг. 23 представляет гистограмму, показывающую экспрессию PD-L1 после лечения при помощи TG02 в трансгенной мышиной модели MYC-индуцированного острого Т-клеточного лимфобластного лейкоза.
Фиг. 24 представляет гистограмму, показывающую экспрессию CD47 после лечения при помощи TG02 в трансгенной мышиной модели MYC-индуцированного острого Т-клеточного лимфобластного лейкоза.
Фиг. 25 представляет гистограмму, показывающую экспрессию BCL-xL после лечения при помощи TG02 в трансгенной мышиной модели MYC-индуцированного острого Т-клеточного лимфобластного лейкоза.
Фиг. 26 представляет гистограмму, показывающую экспрессию MYC после лечения при помощи TG02 в трансгенной мышиной модели MYC-индуцированного острого Т-клеточного лимфобластного лейкоза.
Фиг. 27 представляет линейный график, показывающий эффективность TG02 в комбинации с анти-PD-1 в мышиной сингенной ортотопической модели глиобластомы GL261.
Фиг. 28 является иллюстрацией, показывающей, что опухолевые клетки BT245, на которые воздействует TG02, демонстрируют ингибирование экспрессии MYC и MCL-1.
Фиг. 29 представляет гистограмму, показывающую площадь под кривой (AUC) для TG02-индуцированного ингибирования в клетках глиобластомы (GBM).
Фиг. 30 представляет диаграмму рассеяния, показывающую, что высокая экспрессия MYC коррелирует с низкой AUC в клетках GBM.
Фиг. 31 представляет серию из шести линейных графиков, показывающих активность TG02 в комбинации с облучением в клеточных линиях глиобластомы.
Фиг. 32 представляет гистограмму, показывающую активность TG02 на 26 полученных от пациентов линиях стволовых клеток GBM.
Фиг. 33 является иллюстрацией, показывающей уровень экспрессии CDK9, MYC и Mcl-1 в полученных от пациентов линиях стволовых клеток GBM после лечения при помощи TG02.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В одном из вариантов осуществления в настоящем изобретении представлены терапевтические способы лечения пациента со злокачественным новообразованием, при этом способ включает введение пациенту терапевтически эффективного количества TG02, где один или несколько генов, перечисленных в Таблице 1, см. ниже, дифференцированно присутствуют в биологическом образце, взятом у пациента, по сравнению с биологическим образцом, взятым у индивида другого фенотипического статуса. В другом варианте осуществления сверхэкспрессия MYC дифференцированно присутствует в образце, взятом у пациента. В другом варианте осуществления сверхэкспрессия MCL1 дифференцированно присутствует в образце, взятом у пациента.
В другом варианте осуществления в настоящем изобретении представлены терапевтические способы лечения пациента со злокачественным новообразованием, при этом способ включает введение пациенту терапевтически эффективных количеств TG02 и ингибитора контрольных точек иммунного ответа, где один или несколько генов, перечисленных в Таблице 1, см. ниже, дифференцированно присутствуют в биологическом образце, взятом у пациента, по сравнению с биологическим образцом, взятым у индивида другого фенотипического статуса. В другом варианте осуществления сверхэкспрессия MYC дифференцированно присутствует в образце, взятом у пациента. В другом варианте осуществления сверхэкспрессия MCL1 дифференцированно присутствует в образце, взятом у пациента. В другом варианте осуществления TG02 вводят пациенту перед ингибитором контрольных точек иммунного ответа. В другом варианте осуществления TG02 вводят пациенту после ингибитора контрольных точек иммунного ответа. В другом варианте осуществления TG02 вводят пациенту одновременно с ингибитором контрольных точек иммунного ответа.
В другом варианте осуществления в настоящем изобретении представлены терапевтические способы лечения пациента со злокачественным новообразованием, при этом способ включает введение пациенту терапевтически эффективных количеств TG02, ингибитора контрольных точек иммунного ответа и ингибитора COX-2, где один или несколько генов, перечисленных в Таблице 1, см. ниже, дифференцированно присутствует в биологическом образце, взятом у пациента, по сравнению с биологическим образцом, взятым у индивида другого фенотипического статуса. В другом варианте осуществления сверхэкспрессия MYC дифференцированно присутствует в образце, взятом у пациента. В другом варианте осуществления сверхэкспрессия MCL1 дифференцированно присутствует в образце, взятом у пациента. В другом варианте осуществления TG02 вводят пациенту перед ингибитором COX-2. В другом варианте осуществления TG02 вводят пациенту после ингибитора COX-2. В другом варианте осуществления TG02 вводят пациенту одновременно с ингибитором COX-2.
В другом варианте осуществления в настоящем изобретении представлены терапевтические способы лечения пациента со злокачественным новообразованием, при этом способ включает введение пациенту терапевтически эффективных количеств TG02 и ингибитора контрольных точек иммунного ответа. В другом варианте осуществления TG02 вводят пациенту перед ингибитором контрольных точек иммунного ответа. В другом варианте осуществления TG02 вводят пациенту после ингибитора контрольных точек иммунного ответа. В другом варианте осуществления TG02 вводят пациенту одновременно с ингибитором контрольных точек иммунного ответа.
В другом варианте осуществления в настоящем изобретении представлены терапевтические способы лечения пациента со злокачественным новообразованием, при этом способ включает введение пациенту терапевтически эффективных количеств TG02, ингибитора контрольных точек иммунного ответа и ингибитора COX-2. В другом варианте осуществления TG02 вводят пациенту перед ингибитором COX-2. В другом варианте осуществления TG02 вводят пациенту после ингибитора COX-2. В другом варианте осуществления TG02 вводят пациенту одновременно с ингибитором COX-2.
В другом варианте осуществления в настоящем изобретении представлены наборы, включающие TG02 и ингибитор контрольных точек иммунного ответа, и инструкции по введению TG02 и ингибитора контрольных точек иммунного ответа пациенту больному раком. В другом варианте осуществления набор дополнительно включает ингибитор COX-2.
В другом варианте осуществления в настоящем изобретении представлены наборы, включающие TG02 и ингибитор COX-2 и инструкции по введению TG02 и ингибитора COX-2 пациенту больному раком.
В другом варианте осуществления набор упакован таким образом, чтобы облегчить его использование для осуществления способов по настоящему изобретению.
В другом варианте осуществления набор включает TG02 (или композицию, включающую TG02), упакованный в контейнер, такой как герметичная бутыль или сосуд, с этикеткой, прикрепленной к контейнеру или включенной в набор, которая описывает применение TG02 или композиции для осуществления способа по настоящему раскрытию. В одном из вариантов осуществления TG02 упакован в виде единичной лекарственной формы. Набор может дополнительно включать устройство, подходящее для введения композиции в соответствии с предполагаемым путем введения.
В настоящем изобретении представлены различные терапевтические способы, наборы и композиции, относящиеся к лечению рака. В одном из вариантов осуществления рак представляет собой солидную опухоль. В другом варианте осуществления рак представляет собой гематологическое злокачественное заболевание. В другом варианте осуществления рак выбран из группы, состоящей из рака надпочечников, ацинарно-клеточной карциномы, акустической невриномы, акральной лентигинозной меланомы, акроспиромы, острого эозинофильного лейкоза, острого эритроидного лейкоза, острого лимфобластного лейкоза, острого мегакарибластного лейкоза, острого моноцитарного лейкоза, острого промиелоцитарного лейкоза, аденокарциномы, аденокистозной карциномы, аденомы, аденоматоидной одонтогенной опухоли, аденосквамозной карциномы, новообразования жировой ткани, адренокортикальной карциномы, Т-клеточного лейкоза/лимфомы взрослых, агрессивного NK-клеточного лейкоза, СПИД-ассоциированной лимфомы, альвеолярной рабдомиосаркомы, альвеолярной саркомы мягких тканей, амелобластической фибромы, анапластической крупноклеточной лимфомы, анапластического рака щитовидной железы, ангиоиммунобластной Т-клеточной лимфомы, ангиомиолипомы, ангиосаркомы, астроцитомы, атипичной тератоидно-рабдоидной опухоли, В-клеточного хронического лимфоцитарного лейкоза, В-клеточного пролимфоцитарного лейкоза, В-клеточной лимфомы, базально-клеточной карциномы, рака желчных путей, рака мочевого пузыря, бластомы, рака кости, опухоли Бреннера, опухоли Брауна, лимфомы Беркитта, рака молочной железы, рака головного мозга, карциномы, карциномы in situ, карциносаркомы, опухоли хряща, цементомы, миелоидной саркомы, хондромы, хордомы, хориокарциномы, папилломы хориоидного сплетения, светлоклеточной саркомы почек, краниофарингиомы, кожной Т-клеточной лимфомы, рака шейки матки, колоректального рака, болезни Дегоса, десмопластической мелкокруглоклеточной опухоли, диффузной В-клеточной крупноклеточной лимфомы, дизэмбриопластической нейроэпителиальной опухоли, дисгерминомы, эмбриональной карциномы, новообразования эндокринных желез, опухоли эндодермального синуса; Т-клеточной лимфомы, ассоциированной с энтеропатией; рака пищевода, включенного плода, фибромы, фибросаркомы, фолликулярной лимфомы, фолликулярного рака щитовидной железы, ганглионевромы, рака желудочно-кишечного тракта, эмбрионально-клеточной опухоли, гестационной хориокарциномы, гигантоклеточной фибробластомы, гигантоклеточной опухоли кости, глиальной опухоли, глиобластомы, глиомы, церебрального глиоматоза, глюкагономы, гонадобластомы, гранулезоклеточной опухоли, гинандробластомы, рака желчного пузыря, рака желудка, волосистоклеточного лейкоза, гемангиобластомы, рака головы и шеи, гемангиоперицитомы, гематологического злокачественного заболевания, гепатобластомы, гепатоцеллюлярной карциномы, гепатолиенальной Т-клеточной лимфомы, лимфомы Ходжкина, не-ходжкинской лимфомы, инвазивной лобулярной карциномы, рака кишечника, рака почек, рака гортани, злокачественного лентиго, смертельной срединной карциномы, лейкоза, опухоли из клеток Лейдига, липосаркомы, рака легкого, лимфангиомы, лимфангиосаркомы, лимфоэпителиомы, лимфомы, острого лимфоцитарного лейкоза, острого миелогенного лейкоза, хронического лимфоцитарного лейкоза, рака печени, мелкоклеточного рака легкого, немелкоклеточного рака легкого, MALT лимфомы, злокачественной фиброзной гистиоцитомы, злокачественной опухоли оболочек периферических нервов, злокачественной тритон-опухоли, лимфомы из клеток мантийной зоны, B-клеточной лимфомы из клеток краевой зоны, тучноклеточного лейкоза, медиастинальной эмбрионально-клеточной опухоли, медуллярной карциномы молочной железы, медуллярного рака щитовидной железы, медуллобластомы, меланомы, менингиомы, рака из клеток Меркеля, мезотелиомы, метастатической уротелиальной карциномы, смешанной опухоли Мюллера, муцинозной опухоли, множественной миеломы, новообразования мышечной ткани, фунгоидного микоза, миксоидной липосаркомы, миксомы, миксосаркомы, нозофарингеальной карциномы, нейриномы, нейробластомы, нейрофибромы, нейромы, нодулярной меланомы, окулярного рака, олигоастроцитомы, олигодендроглиомы, онкоцитомы, менингиомы волокон зрительного нерва, опухоли зрительного нерва, рака полости рта, остеосаркомы, рака яичников, опухоли Панкоста, папиллярного рака щитовидной железы, параганглиомы, пинеалобластомы, пинеоцитомы, питуицитомы, аденомы гипофиза, опухоли гипофиза, плазмоцитомы, полиэмбриомы, Т-лимфобластной лимфомы из клеток-предшественников, первичной лимфомы центральной нервной системы, первичной эффузионной лимфомы, первичного перитонеального рака, рака предстательной железы, рака поджелудочной железы, фарингеального рака, псевдомиксомы брюшины, почечно-клеточной карциномы, медуллярной карциномы почки, ретинобластомы, рабдомиомы, рабдомиосаркомы, трансформации Рихтера, рака прямой кишки, саркомы, шванноматоза, семиномы, опухоли из клеток Сертоли, опухоли стромы полового тяжа яичников, перстневидно-клеточного рака, рака кожи, мелко-сине-круглоклеточных опухолей, мелкоклеточного рака, саркомы мягких тканей, соматостатиномы, эпителиомы мошонки, опухоли спинного мозга, лимфомы маргинальной зоны селезенки, плоскоклеточной карциномы, синовиальной саркомы, синдрома Сезари, рака тонкой кишки, плоскоклеточной карциномы, рака желудка, Т-клеточной лимфомы, тестикулярного рака, текомы, рака щитовидной железы, переходно-клеточного рака, рака горла, рака мочеточника, урогенитального рака, уротелиальной карциномы, увеальной меланомы, рака матки, бородавчатой карциномы, глиомы зрительного пути, рака вульвы, рака влагалища, макроглобулинемии Вальденстрема, опухоли Уортина и опухоли Вильмса.
В другом варианте осуществления рак выбран из группы, состоящей из плоскоклеточного рака головы и шеи, аденокарциномы и плоскоклеточного рака пищевода, аденокарциномы желудка, аденокарциномы толстой кишки, гепатоцеллюлярной карциномы, холангиокарциномы желчевыделительной системы, аденокарциномы желчного пузыря, аденокарциномы поджелудочной железы, протоковой карциномы in situ молочной железы, аденокарциномы молочной железы, аденокарциномы легких, плоскоклеточного рака легких, переходно-клеточного рака мочевого пузыря, плоскоклеточного рака мочевого пузыря, плоскоклеточного рака шейки матки, аденокарциномы шейки матки, эндометриального рака, плоскоклеточного рака полового члена и плоскоклеточного рака кожи.
В другом варианте осуществления предраковая опухоль выбрана из группы, состоящей из лейкоплакии головы и шеи, пищевода Барретта, метаплазии желудка, аденомы толстой кишки, хронического гепатита, гиперплазии желчных протоков, интраэпителиальной неоплазии поджелудочной железы, атипичной аденоматозной гиперплазии легких, дисплазии мочевого пузыря, интраэпителиальной цервикальной неоплазии, интраэпителиальной неоплазии полового члена и актинического кератоза кожи.
В другом варианте осуществления у пациента есть опухоли, которые сверхэкспрессируют MYC, MCL1 или оба. Опухоли могут быть определены как сверхэкспрессирующие MYC, MCL1 или оба способами, известными в данной области.
В другом варианте осуществления рак выбран из группы, состоящей из гепатоцеллюлярной карциномы, глиобластомы, рака легких, рака молочной железы, рака головы и шеи, рака предстательной железы, меланомы и колоректального рака.
В другом варианте осуществления рак выбран из группы, состоящей из глиобластомы, гепатоцеллюлярной карциномы, немелкоклеточного и мелкоклеточного рака легких, рака головы и шеи, колоректальной карциномы и трижды негативного рака молочной железы.
В другом варианте осуществления рак стал резистентным к традиционным методам лечения рака. Термин "традиционные методы лечения рака" в контексте настоящей заявки относится к любым противораковым лекарственным средствам или биологическим препаратам или комбинациям противораковых лекарственных средств и/или биологических препаратов, которые были протестированы и/или одобрены для терапевтического применения для людей Управлением США по санитарному надзору за качеством пищевых продуктов и медикаментов, Европейским агентством по лекарственным средствам или аналогичным регулирующим органом.
В другом варианте осуществления пациент ранее получал лечение ингибитором контрольных точек иммунного ответа без TG02. Например, предшествующая терапия иммунных контрольных точек может представлять собой анти-PD-1 терапию.
В другом варианте осуществления пациент ранее получал лечение ингибитором COX-2 без TG02.
В другом варианте осуществления в настоящем изобретении представлены фармацевтическую композицию, содержащую TG02, ингибитор COX-2 и фармацевтически приемлемый эксципиент.
В другом варианте осуществления в настоящем изобретении представлены терапевтические способы лечения пациента со злокачественным новообразованием, при этом способ включает введение пациенту терапевтически эффективного количества TG02, где фенотипический статус пациента представляет собой сверхэкспрессию MYC, сверхэкспрессию MCL1 или сверхэкспрессию MYC и MCL1. В другом варианте осуществления рак выбран из группы, состоящей из гепатоцеллюлярной карциномы, глиобластомы, рака легких, рака молочной железы, рака головы и шеи, рака предстательной железы, меланомы и колоректального рака.
В другом варианте осуществления в настоящем изобретении представлены терапевтические способы лечения пациента со злокачественным новообразованием, при этом способ включает введение пациенту терапевтически эффективных количеств TG02 и второго терапевтического средства, где второе терапевтическое средство не является ни ингибитором контрольных точек иммунного ответа, ни ингибитором COX-2.
В другом варианте осуществления в настоящем изобретении представлены терапевтические способы лечения пациента со злокачественным новообразованием, включающие введение пациенту терапевтически эффективных количеств TG02, ингибитора контрольных точек иммунного ответа и третьего терапевтического средства, где третье терапевтическое средство не является ингибитором COX-2.
В другом варианте осуществления в настоящем изобретении представлены терапевтические способы лечения пациента со злокачественным новообразованием, включающие введение пациенту терапевтически эффективных количеств TG02, ингибитора COX-2 и третьего терапевтического средства, где третье терапевтическое средство не является ингибитором контрольных точек иммунного ответа.
В другом варианте осуществления в настоящем изобретении представлены терапевтические способы лечения пациента со злокачественным новообразованием, включающие введение пациенту терапевтически эффективных количеств TG02, ингибитора контрольных точек иммунного ответа, ингибитора COX-2 и четвертого терапевтического средства, где четвертое терапевтическое средство не является ни ингибитором контрольных точек иммунного ответа, ни ингибитором COX-2.
В другом варианте осуществления в настоящем изобретении представлены индивидуально подобранную терапию для больных раком и охватывает выбор вариантов лечения с наивысшей вероятностью успешного исхода для отдельных больных раком пациентов. В другом аспекте настоящее раскрытие относится к использованию анализа(ов) для прогнозирования результата лечения, например, вероятности благоприятных ответов или успеха лечения у пациентов больных раком.
В другом варианте осуществления в настоящем изобретении представлены способы выбора пациента, например, человека для лечения рака при помощи TG02 и, необязательно, ингибитора контрольных точек иммунного ответа и/или ингибитора COX-2, включающие получение биологического образца, например, клеток крови от пациента, исследование биологического образца от пациента на присутствие биомаркера, например, сверхэкспрессии MYC, сверхэкспрессии MCL1 или обеих, и выбора пациента для лечения, если биологический образец содержит этот биомаркер. В другом варианте осуществления способы дополнительно включают введение терапевтически эффективного количества TG02 и, необязательно, ингибитора контрольных точек иммунного ответа и/или ингибитора COX-2 пациенту, если биологический образец содержит биомаркер. Примеры биомаркеров рака представлены в Таблице 1. В другом варианте осуществления рак представляет собой солидную опухоль. В другом варианте осуществления рак представляет собой гематологическое злокачественное заболевание. В другом варианте осуществления рак выбран из группы, состоящей из гепатоцеллюлярной карциномы, глиобластомы, рака легких, рака молочной железы, рака головы и шеи, рака предстательной железы, меланомы и колоректального рака.
В другом варианте осуществления в настоящем изобретении представлены способы прогнозирования результатов лечения у больного раком пациента, включающие получение биологического образца от пациента, исследование биологического образца от пациента на присутствие биомаркера, например, сверхэкспрессии MYC, сверхэкспрессии MCL1 или обоих, где обнаружение биомаркера указывает, что пациент будет благоприятно реагировать на введение терапевтически эффективного количества TG02 и, необязательно, ингибитора контрольных точек иммунного ответа и/или ингибитора COX-2. Благоприятные ответы включают, но не ограничиваются этим, уменьшение размера опухоли и увеличение выживаемости без прогрессирования заболевания или общей выживаемости.
В другом варианте осуществления в настоящем изобретении представлены способы лечения рака, включающие введение терапевтически эффективного количества TG02 и, необязательно, ингибитора контрольных точек иммунного ответа и/или ингибитора COX-2 пациенту, например, человеку больному раком, у которого клетки содержат биомаркер. В другом варианте осуществления пациент выбран для лечения при помощи TG02 и, необязательно, ингибитора контрольных точек иммунного ответа и/или ингибитора COX-2 после того, как было определено, что клетки пациента содержат сверхэкспрессию MYC. В другом варианте осуществления пациент выбран для лечения при помощи TG02 и, необязательно, ингибитора контрольных точек иммунного ответа и/или ингибитора COX-2 после того, как было определено, что клетки пациента содержат сверхэкспрессию MCL1. В другом варианте осуществления пациент выбран для лечения при помощи TG02 и, необязательно, ингибитора контрольных точек иммунного ответа и/или ингибитора COX-2 после того, как было определено, что клетки пациента содержат сверхэкспрессию MYC и сверхэкспрессию MCL1.
В другом варианте осуществления способ лечения пациента со злокачественным новообразованием, включает получение биологического образца от пациента, определение, содержит или нет биологический образец биомаркер, например, сверхэкспрессию MYC, сверхэкспрессию MCL1 или обоих, и введение пациенту терапевтически эффективного количества TG02 и, необязательно, ингибитора контрольных точек иммунного ответа и/или ингибитора COX-2, если биологический образец содержит биомаркер. В другом варианте осуществления способы, представленные в настоящей заявке, включают определение того, содержат или нет клетки пациента сверхэкспрессию MYC. В другом варианте осуществления способы, представленные в настоящей заявке, включают определение того, содержат или нет клетки пациента сверхэкспрессию MCL1. В другом варианте осуществления способы, представленные в настоящей заявке, включают определение того, содержат или нет клетки пациента сверхэкспрессию MYC и MCL1.
В другом варианте осуществления в настоящем изобретении представлены способ лечения больного злокачественным новообразованием индивида, при этом способ включает получение биологического образца от индивида, определение уровня экспрессии MYC, MCL1 или обоих в биологическом образце; и введение субъекту терапевтически эффективного количества TG02 и второго терапевтического средства, например, темозоломида, карфилзомиба, сорафениба, бортезомиба, доксорубицина, цисплатина, леналидомида, дексаметазона или Ara-C, если биологический образец показывает сверхэкспрессию MYC, MCL1 или обе.
В другом варианте осуществления пациент ранее получал лечение только ингибитором контрольных точек иммунного ответа. Например, предшествующая терапия иммунных контрольных точек может представлять собой анти-PD-1 терапию.
В другом варианте осуществления пациент ранее получал лечение только ингибитором COX-2.
I. Ингибиторы контрольных точек иммунного ответа
Ингибиторы контрольных точек иммунного ответа представляют собой терапии, которые блокируют ингибиторные контрольные точки иммунной системы. Контрольные точки иммунного ответа могут быть стимулирующими или ингибирующими. Блокада ингибирующей иммунной контрольной точки активирует функцию иммунной системы и может быть использована для иммунотерапии рака. Pardoll, Nature Reviews. Cancer 12:252-64 (2012). Опухолевые клетки отключают активированные Т-клетки, когда они присоединяются к специфическим Т-клеточным рецепторам. Ингибиторы контрольных точек иммунного ответа препятствуют присоединению опухолевых клеток к T-клеткам, то приводит к тому, что Т-клетки остаются активированными. Фактически, скоординированное действие клеточных и растворимых компонентов противостоит патогенам и вызываемым раком поражениям. Модуляция путей иммунной системы может включать изменение экспрессии или функциональной активности по меньшей мере одного компонента пути для последующей модуляции ответа иммунной системой. США 2015/0250853. Примеры ингибиторов контрольных точек иммунного ответа включают ингибиторы PD-1, ингибиторы PD-L1, ингибиторы CTLA-4, ингибиторы LAG3, ингибиторы TIM3, ингибиторы cd47 и ингибиторы B7-H1. Таким образом, В одном из вариантов осуществления ингибитор контрольных точек иммунного ответа выбран из группы, состоящей из ингибитора PD-1, ингибитора PD-L1, ингибитора CTLA-4, ингибитора LAG3, ингибитора TIM3 и ингибитора cd47.
В другом варианте осуществления ингибитор контрольных точек иммунного ответа представляет собой ингибитор запрограммированной гибели клеток (PD-1). PD-1 представляет собой коингибирующий Т-клеточный рецептор, который играет ключевую роль в способности опухолевых клеток уклоняться от иммунной системы хозяина. Блокада взаимодействий между PD-1 и PD-L1, лигандом PD-1, усиливает иммунную функцию и опосредует противоопухолевую активность. Примеры ингибиторов PD-1 включают антитела, которые специфически связываются с PD-1. Конкретные анти-PD-1 антитела включают, но не ограничиваются этим, ниволумаб, пембролизумаб, STI-1014 и пидилизумаб. Общее обсуждение доступности, способов получения, механизма действия и клинических исследований анти-PD-1 антител см. США 2013/0309250, США 6808710, США 7595048, США 8008449, США 8728474, США 8779105, США 8952136, США 8900587, США 9073994, США 9084776 и Naido et al., British Journal of Cancer 111:2214-19 (2014).
В другом варианте осуществления ингибитор контрольных точек иммунного ответа представляет собой ингибитор PD-L1 (также известен как B7-H1 или CD274). Примеры ингибиторов PD-L1 включают антитела, которые специфически связываются с PD-L1. Конкретные анти-PD-L1 антитела включают, но не ограничиваются этим, авелумаб, атезолизумаб, дурвалумаб и BMS-936559. Общее обсуждение доступности, способов получения, механизма действия и клинических исследований см. в США 8217149, США 2014/0341917, США 2013/0071403, WO 2015036499 и Naido et al., British Journal of Cancer 111:2214-19 (2014).
В другом варианте осуществления ингибитор контрольных точек иммунного ответа представляет собой ингибитор CTLA-4. CTLA-4, также известный как антиген 4 цитотоксических Т-лимфоцитов, является белковым рецептором, который негативно регулирует иммунную систему. CTLA-4 характеризуется как "тормоз", который связывает костимуляторные молекулы на антигенпрезентирующих клетках, что предотвращает взаимодействие с CD28 на Т-клетках, а также генерирует явно ингибирующий сигнал, который ограничивает активацию Т-клеток. Примеры ингибиторов CTLA-4 включают антитела, которые специфически связываются с CTLA-4. Конкретные анти-CTLA-4 антитела включают, но не ограничиваются этим, ипилимумаб и тремелимумаб. Общее обсуждение доступности, способов получения, механизма действия и клинических исследований см. в США 6984720, США 6207156 и Naido et al., British Journal of Cancer 111:2214-19 (2014).
В другом варианте осуществления ингибитор контрольных точек иммунного ответа представляет собой ингибитор LAG3. LAG3, ген активации лимфоцитов-3, представляет собой отрицательный костимулирующий рецептор, который модулирует гомеостаз, пролиферацию и активацию Т-клеток. Кроме того, сообщалось о том, что LAG3 участвует в супрессивной функции регуляторных Т-клеток (Tregs). Большая часть молекул LAG3 удерживается в клетке близко к центру организации микротрубочек и индуцируется только после активации антигенспецифических Т-клеток. США 2014/0286935. Примеры ингибиторов LAG3 включают антитела, которые специфически связываются с LAG3. Конкретные анти-LAG3 антитела включают, но не ограничиваются этим, GSK2831781. Общее обсуждение доступности, способов получения, механизма действия и исследований см. в США 2011/0150892, США 2014/0093511, США 20150259420 и Huang et al., Immunity 21:503-13 (2004).
В другом варианте осуществления ингибитор контрольных точек иммунного ответа представляет собой ингибитор TIM3. TIM3, домен Т-клеточный иммуноглобулин и муцина 3, представляет собой рецептор иммунной контрольной точки, который функционирует как ограничивающий продолжительность и величину TH1 и TC1 Т-клеточных ответов. Путь TIM3 считается мишенью для противораковой иммунотерапии из-за его экспрессии на дисфункциональных CD8+ T-клетках и Tregs, которые являются двумя подтвержденными популяциями иммунных клеток, которые создают иммуносупрессию в опухолевой ткани. Anderson, Cancer Immunology Research 2:393-98 (2014). Примеры ингибиторов TIM3 включают антитела, которые специфически связываются с TIM3. Общее обсуждение доступности, способов получения, механизма действия и исследований ингибиторов TIM3 см. в США 20150225457, США 20130022623, США 8522156, Ngiow et al., Cancer Res 71: 6567-71 (2011), Ngiow, et al., Cancer Res 71:3540-51 (2011), и Anderson, Cancer Immunology Res 2:393-98 (2014).
В другом варианте осуществления ингибитор контрольных точек иммунного ответа представляет собой ингибитор cd47. См. Unanue, E.R., PNAS 110:10886-87 (2013).
Термин "антитело" предусматривает включение интактных моноклональных антител, поликлональных антител, мультиспецифических антител, образованных из по меньшей мере двух интактных антител, и фрагментов антитела, при условии, что они проявляют желаемую биологическую активность. В другом варианте осуществления "антитело" предусматривает включение растворимыз рецепторов, которые не содержат Fc часть антитела. В одном из вариантов осуществления антитела представляют собой гуманизированные моноклональные антитела и их фрагменты, полученные методами рекомбинантной генной инженерии.
Другой класс ингибиторов контрольных точек иммунного ответа включает полипептиды, которые связываются с PD-1 рецепторами на T-клетках и блокируют их, на вызывая передачу сигнала ингибитора. Такие пептиды включают B7-DC полипептиды, B7-H1 полипептиды, B7-1 полипептиды и B7-2 полипептиды и их растворимые фрагменты, как раскрыто в патенте США 8114845.
Другой класс ингибиторов контрольных точек иммунного ответа включает соединения с пептидными фрагментами, которые ингибируют передачу сигнала PD-1. Примеры таких соединений раскрыты в патенте США 8907053, и они имеют структуру:
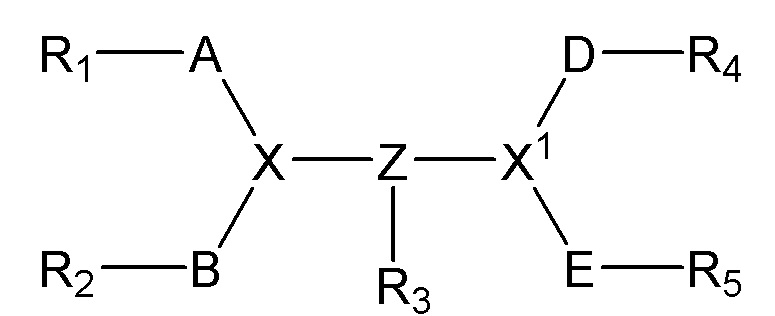
или фармацевтически приемлемая соль такого соединения, где соединение включает по меньшей мере 5 аминокислот, полезных в качестве терапевтических средств, способных ингибировать PD-1 сигнальный путь.
Другой класс ингибиторов контрольных точек иммунного ответа включают ингибиторы некоторых метаболических ферментов, таких как индоламин 2,3-диоксигеназа (IDO), которая экспрессируется инфильтрирующими миелоидными клетками и опухолевыми клетками. Фермент IDO ингибирует иммунные ответы путем истощения аминокислот, которые необходимы для анаболических функций в Т-клетках, или путем синтеза определенных природных лигандов для цитозольных рецепторов, которые способны изменять функции лимфоцитов. Pardoll, Nature Reviews. Cancer 12:252-64 (2012); Löb, Cancer Immunol Immunother 58:153-57 (2009). Конкретные IDO блокирующие агенты включают, но не ограничиваются этим, лево-1-метилтриптофан (L-1MT) и 1-метил-триптофан (1MT). Qian et al., Cancer Res 69:5498-504 (2009); и Löb et al., Cancer Immunol Immunother 58:153-7 (2009).
В одном из вариантов осуществления ингибитор контрольных точек иммунного ответа представляет собой ниволумаб, пембролизумаб, пидилизумаб, STI-1110, авелумаб, атезолизумаб, дурвалумаб, STI-1014, ипилимумаб, тремелимумаб, GSK2831781, BMS-936559 или MED14736.
II. Ингибиторы COX-2
Циклооксигеназа-2 (COX-2) представляет собой фермент, который способствует воспалению и играет роль в прогрессировании опухоли. Ингибиторы COX-2 включают неселективные ингибиторы, такие как аспирин, ибупрофен, сулиндаксульфон, сулиндаксульфид, диклофенак, набуметон, напроксен, индометацин и пироксикам, селективные ингибиторы, такие как целекоксиб, рофекоксиб, валдекоксиб, ANS-398, Cay10404, SC-236 и DUP697, и преимущественные ингибиторы, такие как мелоксикам и нимесулид. Другие ингибиторы COX-2 включают априкоксиб, тилмакоксиб и цимикоксиб. Любой ингибитор COX-2 предусматривается для использования в терапевтических способах по настоящему изоретению. См. Sobolewski et al., "The Role of Cyclooxygenase-2 in Cell Proliferation and Cell Death in Human Malignancies," International Journal of Cell Biology, vol. 2010, Article ID 215158, 21 pages, 2010. doi:10.1155/2010/215158.
В другом варианте осуществления ингибитор COX-2 представляет собой априкоксиб. См. Kirane et al., Clin. Cancer Res. 18:5031-5042 (2012).
В другом варианте осуществления ингибитор COX-2 выбран из группы, состоящей из:
8-(этил-D5)-6-(трифторметокси)-2-(трифторметил)-2H-хромен-3-карбоновой кислоты;
6-хлор-8-(метил-D3)-2-(трифторметил)-2H-хромен-3-карбоновой кислоты;
6-бром-8-(метил-D3)-2-(трифторметил)-2H-хромен-3-карбоновой кислоты;
8-хлор-6-(метил-D3)-2-(трифторметил)-2H-хромен-3-карбоновой кислоты;
6,8-дибром-5,7-(диметил-D6)-2-(трифторметил)-2H-хромен-3-карбоновой кислоты;
8-(1-метилгексил-D15)-2-(трифторметил)-2H-хромен-3-карбоновой кислоты;
6-хлор-8-(1-метилгексил-D15)-2-(трифторметил)-2H-хромен-3-карбоновой кислоты;
8-(гексил-D13)-2-(трифторметил)-2H-хромен-3-карбоновой кислоты;
7,8-(диметил-D6)-2-(трифторметил)-2H-хромен-3-карбоновой кислоты; и
6-хлор-8-(гексил-D13)-2-(трифторметил)-2H-хромен-3-карбоновой кислоты.
См. US 2015/0133538.
В другом варианте осуществления ингибитор COX-2 представляет собой 6-бром-8-(метил-D3)-2-(трифторметил)-2H-хромен-3-карбоновую кислоту.
III. Необязательные терапевтические средства
В некоторых терапевтических способах настоящего раскрытия второе терапевтическое средство вводят больному раком в комбинации с TG02, третье терапевтическое средство вводят больному раком в комбинации с TG02 и ингибитором контрольных точек иммунного ответа или в комбинации с TG02 и ингибитором COX-2, или четвертое терапевтическое средство вводят больному раком в комбинации с TG02, ингибитором контрольных точек иммунного ответа и ингибитором COX-2. Второе, третье и четвертое терапевтические средства, используемые в терапевтических способах настоящего раскрытия, указаны как "необязательные терапевтические средства". Такие необязательные терапевтические средства, полезные в лечении раковых пациентов, известны в данной области. В одном из вариантов осуществления необязательное терапевтическое средство в комбинации с TG02 представляет собой противораковое средство, которое не является ни ингибитором контрольных точек иммунного ответа, ни ингибитором COX-2.
Необязательные терапевтические средства вводят в таком количестве, чтобы обеспечить желаемый терапевтический эффект. Эффективный диапазон доз для каждого необязательного терапевтического средства известен в данной области, и необязательное терапевтическое средство вводят нуждающемуся индивидууму в таких установленных пределах.
TG02, ингибитор контрольных точек иммунного ответа, ингибитор COX-2 и/или необязательное терапевтическое средство можно вводить совместно в виде единичной стандартной дозы или раздельно в виде нескольких доз и в любом порядке, например, когда TG02 вводят перед ингибитором контрольных точек иммунного ответа, ингибитором COX-2 и/или необязательным терапевтическим средством, или наоборот. Пациенту можно вводить одну или несколько доз TG02, ингибитора контрольных точек иммунного ответа, ингибитора COX-2 и/или необязательного терапевтического средства.
В одном из вариантов осуществления необязательное терапевтическое средство представляет собой эпигенетическое лекарственное средство. Как используется в настоящей заявке, термин "эпигенетическое лекарственное средство" относится к терапевтическому средству, которое направленно действует на эпигенетический регулятор. Примеры эпигенетических регуляторов включают гистонлизинметилтрансферазы, гистонаргининметилтрансферазы, гистондеметилазы, гистондеацетилазы, гистонацетилазы и ДНК-метилтрансферазы. Ингибиторы гистондеацетилазы включают, но не ограничиваются этим, вориностат.
В другом варианте осуществления необязательное терапевтическое средство представляет собой хемотерапевтическое средство или другое антипролиферативное средство, которое можно вводить в комбинации с TG02 или его фармацевтически приемлемой солью, для лечения рака. Примеры терапий и противораковых средств, которые можно использовать в комбинации с TG02 или его фармацевтически приемлемой солью, включают хирургическое вмешательство, лучевую терапию (например, гамма-излучение, нейтронную терапию, электронную радиотерапию, протонную терапию, брахитерапию и системные радиоактивные изотопы), эндокринную терапию, модификатор биологического ответа (например, интерферон, интерлейкин, фактор некроза опухоли (TNF), гипертермию и криотерапию, средство для ослабления любого неблагоприятного эффекта (например, противорвотное средство) и любое другое одобренное химиотерапевтическое средство.
Неограничивающие примеры антипролиферативных соединений включают ингибитор ароматазы; антиэстроген; антиандроген; агонист гонадорелина; ингибитор топоизомеразы I; ингибитор топоизомеразы II; активный агент, действующий на микротрубочки; алкилирующий агент, например, темозоломид; ретиноид, каротеноид или токоферол; ингибитор циклооксигеназы; ингибитор MMP; ингибитор mTOR; антиметаболит; соединение платины; ингибитор метионинаминопептидазы; бисфосфонат; антипролиферативное антитело; ингибитор гепараназы; ингибитор онкогенных изоформ Ras; ингибитор теломеразы; ингибитор протеасомы; соединение, применяемое в лечении гематологических злокачественных опухолей; ингибитор Flt-3; ингибитор Hsp90; ингибитор кинезинового моторного белка; ингибитор MEK; противоопухолевый антибиотик; нитрозомочевину; соединение, направленно воздействующее/снижающее активность протеин- или липидкиназы, соединение, направленно воздействующее/снижающее активность протеин- или липидфосфатазы, или любое дополнительное антиангиогенное соединение.
Неограничивающие примеры ингибиторов ароматазы включают стероиды, такие как атаместан, экземестан и формастан, и нестероидные средства, такие как аминоглутетимид, роглитимид, пиридоглутетимид, трилостан, тестолактон, кетоконазол, ворозол, фадрозол, анастрозол и летрозол.
Неограничивающие антиэстрогены включают тамоксифен, фулвестрант, ралоксифен и ралоксифен гидрохлорид. Антиандрогены включают, но не ограничиваются этим, бикалутамид. Агонисты гонадорелина включают, но не ограничиваются этим, абареликс, гозерелин и гозерелинацетат.
Неограничивающие примеры ингибиторов топоизомеразы I включают топотекан, галимкан, иринотекан, камптотецин и его аналоги, 9-нитрокамптотецин и макромолекулярный конъюгат камптотецина PNU-166148. Ингибиторы топоизомеразы II включают, но не ограничиваются этим, антрациклины, такие как доксорубицин, даунорубицин, эпирубицин, идарубицин и неморубицин; антрахиноны, такие как митоксантрон и лосоксантрон; и подофиллотоксины, такие как этопозид и тенипозид.
Активные агенты, действующие на микротрубочки, включают стабилизирующие микротрубочки соединения, дестабилизирующие микротрубочки соединения и ингибиторы полимеризации микротубулина, включая, но не ограничиваясь этим, таксаны, такие как паклитаксел и доцетаксел; алкалоиды барвинка, такие как винбластин, винбластинсульфат, винкристин и винкристинсульфат и винорелбин; дискодермолиды; кохицин и эпотилоны, и их производные.
Неограничивающие примеры алкилирующих агентов включают циклофосфамид, ифосфамид, мелфалан и нитрозомочевины, такие как кармустин и ломустин.
Неограничивающие примеры ингибиторов металлопротеиназы матрикса ("MMP ингибиторы") включают пептидомиметические и пептидомиметические ингибиторы коллагена, тетрациклиновые производные, батимастат, маримастат, приномастат, метастат, BMS-279251, BAY 12-9566, TAA211, MMI270B и AAJ996.
Неограничивающие примеры ингибиторов mTOR включают соединения, которые ингибируют мишень рапамицина в клетках млекопитающих (mTOR) и обладают антипролиферативной активностью, такие как сиролимус, эверолимус, CCI-779 и ABT578.
Неограничивающие примеры антиметаболитов включают 5-фторурацил (5-FU), капецитабин, гемцитабин, ДНК деметилирующие соединения, такие как 5-азацитидин и децитабин, метотрексат и эдатрексат, и антагонисты фолиевой кислоты, такие как пеметрексед.
Неограничивающие примеры соединений платины включают карбоплатин, цисплатин, цисплатин и оксалиплатин.
Неограничивающие примеры ингибиторов метионинаминопептидазы включают бенгамид или его производное и PPI-2458.
Неограничивающие примеры бисфосфонатов включают этидроновую кислоту, клодроновую кислоту, тилудроновую кислоту, памидроновую кислоту, алендроновую кислоту, ибандроновую кислоту, ризедроновую кислоту и золедроновую кислоту.
Неограничивающие примеры ингибиторов гепараназы включают соединения, которые направленно воздействуют, уменьшают или ингибируют деградацию гепаринсульфата, такие как PI-88 и OGT2115.
Неограничивающие примеры соединений, которые направленно воздействуют, уменьшают или ингибируют онкогенную активность Ras, включают ингибиторы фарнезилтрансферазы, такие как L-744832, DK8G557, типифарниб и лонафарниб.
Неограничивающие примеры ингибиторов теломеразы включают соединения, которые направленно воздействуют, уменьшают или ингибируют активность теломеразы, такие как соединения, которые ингибируют рецептор теломеразы, такие как теломестатин.
Неограничивающие примеры ингибиторов протеасомы включают соединения, которые направленно воздействуют, уменьшают или ингибируют активность протеасомы, включая, но не ограничиваясь этим, бортезомиб. В некоторых вариантах осуществления ингибитор протеасомы представляет собой карфилзомиб.
Неограничивающие примеры ингибиторов FMS-подобной тирозинкиназы, которые являются соединениями, направленно воздействующими, снижающими или ингибирующими активность рецепторов FMS-подобной тирозинкиназы (Flt-3R), включают интерферон, Ι-β-D-арабинофуранозилцитозин (ara-c) и бисульфан; и ингибиторы ALK, которые являются соединениями, которые направленно воздействуют, уменьшают или ингибируют киназу анапластической лимфомы.
Неограничивающие примеры ингибиторов Flt-3 включают PKC412, мидостаурин, стауроспориновое производное, SU11248 и MLN518.
Неограничивающие примеры ингибиторов HSP90 включают соединения, направленно воздействующие, снижающие или ингибирующие внутреннюю АТФазную активность HSP90; или разрушающие, таргетирующие, снижающие или ингибирующие белки-клиенты HSP90 через убиквитин-протеасомный путь. Соединения, направленно воздействующие, снижающие или ингибирующие внутреннюю АТФазную активность HSP90, главным образом представляют собой соединения, белки или антитела, которые ингибируют АТФазную активность HSP90, такие как 17-аллиламино,17-деметоксигелданамицин (17AAG), гелданамициновое производное; другие связанные с гелданамицином соединения; радикикол и ингибиторы HDAC.
Неограничивающие примеры ингибиторов протеинтирозинкиназы и/или серин- и/или треонинкиназы или ингибиторов липидкиназы, включают a) соединение, направленно воздействующее, снижающее или ингибирующее активность рецепторов тромбоцитарного фактора роста (PDGFR), такое как соединение, которое направленно воздействует, уменьшает или ингибирует активность PDGFR, такое как производные N-фенил-2-пиримидин-амина, такое как иматиниб, SUlOl, SU6668 и GFB-111; b) соединение, направленно воздействующее, снижающее или ингибирующее активность рецепторов фактора роста фибробластов (FGFR); c) соединение, направленно воздействующее, снижающее или ингибирующее активность рецепторов инсулиноподобного фактора роста I (IGF-IR), такое как соединение, которое направленно воздействует, уменьшает или ингибирует активность IGF-IR; d) соединение, направленно воздействующее, снижающее или ингибирующее активность ингибиторов Trk семейства рецепторных тирозинкиназ, или ингибиторы эфрина B4; e) соединение, направленно воздействующее, снижающее или ингибирующее активность семейства Axl рецепторных тирозинкиназ; f) соединение, направленно воздействующее, снижающее или ингибирующее активность рецепторной тирозинкиназы Ret; g) соединение, направленно воздействующее, снижающее или ингибирующее активность Kit/SCFR рецепторных тирозинкиназ, такое как иматиниб; h) соединение, направленно воздействующее, снижающее или ингибирующее активность рецепторных тирозинкиназ c-Kit, такое как иматиниб; i) соединение, направленно воздействующее, снижающее или ингибирующее активность членов c-Abl семейства, продуктов слияния их генов (например, Bcr-Abl киназы) и мутантов, такое как производное N-фенил-2-пиримидин-амина, такое как иматиниб или нилотиниб; PD180970; AG957; NSC 680410; PD173955; или дазатиниб; j) соединение, направленно воздействующее, снижающее или ингибирующее активность членов семейства протеинкиназ C (PKC) и Raf серин/треонинкиназ, членов семейства MEK, SRC, JAK, FAK, PDK1, PKB/Akt и Ras/MAPK и/или членов семейства циклин-зависимых киназ (CDK), такое как производное стауроспорина, раскрытое в патенте США №5093330, такое как мидостаурин; примеры дополнительных соединений включают UCN-01, сафингол, BAY 43-9006, бриостатин 1, перифозин; илмофозин; RO 318220 и RO 320432; GO 6976; Isis 3521; LY333531/LY379196; изохинолиновое соединение; ингибитор фарнезилтрансферазы; PD184352 или QAN697 или AT7519; k) соединение, направленно воздействующее, снижающее или ингибирующее активность протеинтирозинкиназы, такое как иматинибмезилат или тирфостин, такое как Тирфостин A23/RG-50810; AG 99; Тирфостин AG 213; Тирфостин AG 1748; Тирфостин AG 490; Тирфостин B44; Тирфостин B44 (+) энантиомер; Тирфостин AG 555; AG 494; Тирфостин AG 556, AG957 и адафостин (адамантиловый эфир 4-{[(2,5-дигидроксифенил)метил]амино}-бензойной кислоты; NSC 680410, адафостин); l) соединение, направленно воздействующее, снижающее или ингибирующее активность семейства тирозинкиназных рецепторов эпидермального фактора роста (EGFR, ErbB2, ErbB3, ErbB4 в виде гомо- или гетеродимеров) и их мутантов, такое как CP 358774, ZD 1839, ZM 105180; трастузумаб, цетуксимаб, гефитиниб, эрлотиниб, OSI-774, Cl-1033, EKB-569, GW-2016, антитела El.l, E2.4, E2.5, E6.2, E6.4, E2.11, E6.3 и E7.6.3 и 7H-пирроло-[2,3-d]пиримидиновые производные; и m) соединение, направленно воздействующее, снижающее или ингибирующее активность рецептора c-Met.
Неограничивающие примеры соединений, которые направленно воздействуют, уменьшают или ингибируют активность протеин- или липидфосфатазы, включают ингибиторы фосфатазы 1, фосфатазы 2A или CDC25, такие как окадаиковая кислота или ее производное.
Следующие антиангиогенные соединения включают соединения, имеющие иной механизм их действия, не связанный с ингибированием протеин- или липидкиназы, например, талидомид и TNP-470.
Дополнительные неограничивающие примеры химиотерапевтических соединений, одно или несколько из которых можно использовать в комбинации с TG02 или его фармацевтически приемлемой солью, включают следующие: авастин, даунорубицин, адриамицин, Ara-C, VP-16, тенипозид, митоксантрон, идарубицин, карбоплатин, PKC412, 6-меркаптопурин (6-MP), флударабина фосфат, октреотид, SOM230, FTY720, 6-тиогуанин, кладрибин, 6-меркаптопурин, пентостатин, гидроксимочевина, производные 2-гидрокси-1H-изоиндол-1,3-диона, 1-(4-хлоранилино)-4-(4-пиридилметил)фталазин или его фармацевтически приемлемая соль, 1-(4-хлоранилино)-4-(4-пиридилметил)фталазин сукцинат, ангиостатин, эндостатин, амиды антраниловой кислоты, ZD4190, ZD6474, SU5416, SU6668, бевацизумаб, rhuMAb, rhuFab, макугон; ингибиторы FLT-4, ингибиторы FLT-3, VEGFR-2 IgGI антитело, RPI 4610, бевацизумаб, порфимер натрия, анекортав, триамцинолон, гидрокортизон, 11-а-эпигидрокотизол, кортексолон, 17a-гидроксипрогестерон, кортикостерон, дезоксикортикостерон, тестостерон, эстрон, дексаметазон, флуоцинолон, растительный алкалоид, гормональное соединение и/или антагонист, модификатор биологического ответа, такой как лимфокин или интерферон, антисмысловой олигонуклеотид или олигонуклеотидное производное, короткая шпилечная РНК и короткая интерферирующая РНК.
Множество различных подходящих необязательных терапевтических, например, противораковых средств предназначены для применения в терапевтических способах, представленных в настоящей заявке. Действительно, способы, представленные в настоящей заявке, могут включать, но не ограничиваются этим, введение различных необязательных терапевтических средств, таких как: агенты, которые индуцируют апоптоз; полинуклеотиды (например, антисмысловые, рибозимы, короткая интерферирующая РНК); полипептиды (например, ферменты и антитела); биологические миметики (например, госсипол или BH3 миметики); агенты, которые связываются (например, путем олигомеризации или комплексообразования) с белком Bcl-2 семейства, таким как Bax; алкалоиды; алкилирующие агенты; противоопухолевые антибиотики; антиметаболиты; гормоны; соединения платины; моноклональные или поликлональные антитела (например, антитела, конъюгированные с противораковыми лекарственными средствами, токсинами, дефенсинами), токсины; радионуклиды; модификаторы биологического ответа (например, интерфероны (например, IFN-α) и интерлейкины (например, IL-2)); средства адоптивной иммунотерапии; гематопоэтические факторы роста; агенты, которые индуцируют дифференцировку опухолевых клеток (например, полностью транс-ретиноевая кислота); реагенты для генной терапии (например, реагенты для антисмысловой терапии и нуклеотиды); опухолевые вакцины; ингибиторы ангиогенеза; ингибиторы протеосомы: модуляторы NF-КB; анти-CDK соединения; ингибиторы HDAC; и т.п. Специалистам в данной области известны другие многочисленные примеры необязательных терапевтических средств, таких как химиотерапевтические соединения и противораковые терапии, подходящие для совместного введения с раскрываемыми соединениями.
В некоторых вариантах осуществления противораковые средства включают средства, которые индуцируют или стимулируют апоптоз. Средства, которые индуцируют или стимулируют апоптоз, включают, например, средства, которые взаимодействуют с ДНК или модифицируют ДНК, например, путем интеркалирования, поперечной сшивки, алкилирования, или иным образом повреждая или химически модифицируя ДНК. Средства, которые индуцируют апоптоз, включают, но не ограничиваются этим, облучение (например, рентгеновские лучи, гамма-лучи, УФ); факторы, связанные с фактором некроза опухоли (TNF) (например, рецепторные белки семейства TNF, лиганды семейства TNF, TRAIL, антитела к TRAIL-R1 или TRAIL-R2); ингибиторы киназ (например, ингибитор киназы рецептора эпидермального фактора роста (EGFR). Дополнительные противораковые средства включают: ингибитор киназы рецептора васкулярного фактора роста (VGFR), ингибитор киназы рецептора фактора роста фибробластов (FGFR), ингибитор киназы рецептора тромбоцитарного фактора роста (PDGFR) и ингибиторы киназы Bcr-Abl (такие как ГЛИВЕК)); антисмысловые молекулы; антитела (например, ГЕРЦЕПТИН, РИТУКСАН, ЗЕВАЛИН и АВАСТИН); антиэстрогены (например, ралоксифен и тамоксифен); антиандрогены (например, флутамид, бикалутамид, финастерид, аминоглутамид, кетоконазол и кортикостероиды); ингибиторы циклооксигеназы 2 (COX-2) (например, целекоксиб, мелоксикам, NS-398 и нестероидные противовоспалительные лекарственные средства (NSAID)); противовоспалительные лекарственные средства (например, бутазолидин, ДЕКАДРОН, ДЕЛЬТАСОН, дексаметазон, дексаметазон интенсол, ДЕКСОНА, ГЕКСАДРОЛ, гидроксихлорохин, МЕТИКОРТЕН, ОРАДЕКСОН, ОРАЗОН, оксифенбутазон, ПЕДИАПРЕД, фенилбутазон, ПЛАКВЕНИЛ, преднизолон, преднизон, ПРЕЛОН и ТАНДЕАРИЛ); и противораковые химиотерапевтические средства (например, иринотекан (CAMPTOSAR), CPT-11, флударабин (FLUDARA), дакарбазин (DTIC), дексаметазон, митоксантрон, MYLOTARG, VP-16, цисплатин, карбоплатин, оксалиплатин, 5-FU, доксорубицин, гемцитабин, бортезомиб, гефинитиб, бевацизумаб, ТАКСОТЕР или ТАКСОЛ); клеточные сигнальные молекулы; церамиды и цитокины; стауроспорин и т.п.
В других вариантах осуществления терапевтические способы, представленные в настоящей заявке, включают введение больному раком терапевтически эффективного количества TG02 и по меньшей мере одного дополнительного анти-гиперпролиферативного или противоопухолевого средства, выбранного из алкилирующих агентов, антиметаболитов и натуральных продуктов (например, трав и других соединений растительного и/или животного происхождения).
Алкилирующие агенты, подходящие для применения в способах по настоящему изобретению, включают, но не ограничиваются этим: 1) азотистый иприт (например, мехлорэтамин, циклофосфамид, ифосфамид, мелфалан (L-сарколизин); и хлорамбуцил); 2) этиленимины и метилмеламины (например, гексаметилмеламин и тиотепа); 3) алкилсульфонаты (например, бусульфан); 4) нитрозомочевины (например, кармустин (BCNU); ломустин (CCNU); семистин (метил-CCNU); и стрептозоцин (стрептозотоцин)); и 5) триазены (например, дакарбазин (DTIC; диметилтриазеноимид-азолкарбоксамид).
В некоторых вариантах осуществления антиметаболиты, подходящие для применения в способах по настоящему изобретению, включают, но не ограничиваются этим: 1) аналоги фолиевой кислоты (например, метотрексат (аметоптерин)); 2) пиримидиновые аналоги (например, фторурацил (5-фторурацил; 5-FU), флоксуридин (фтордеоксиуридин, FudR) и цитарабин (цитозин-арабинозид)); и 3) пуриновые аналоги (например, меркаптопурин (6-меркаптопурин; 6-MP), тиогуанин (6-тиогуанин; TG) и пентостатин (2'-дезоксикоформицин)).
В других вариантах осуществления хемотерапевтические средства, подходящие для применения в способах настоящего раскрытия, включают, но не ограничиваются этим: 1) алкалоиды барвинка (например, винбластин (VLB), винкристин); 2) эпиподофиллотоксины (например, этопозид и тенипозид); 3) антибиотики (например, дактиномицин (актиномицин D), даунорубицин (дауномицин, рубидомицин), доксорубицин, блеомицин, плекамицин (митрамицин) и митомицин (митомицин С)); 4) ферменты (например, L-аспарагиназа); 5) модификаторы биологического ответа (например, интерферон-альфа); 6) платиновые координационные комплексы (например, цисплатин (cis-DDP) и карбоплатин); 7) антрацендионы (например, митоксантрон); 8) замещенные мочевины (например, гидроксимочевина); 9) метилгидразиновые производные (например, прокарбазин (N-метилгидразин; MIH)); 10) адренокортикальные супрессанты (например, митотан (o,p'-DDD) и аминоглутетимид); 11) адренокортикостероиды (например, преднизон); 12) прогестины (например, гидроксипрогестерон капроат, медроксипрогестерон ацетат и мегестролацетат); 13) эстрогены (например, диэтилстилбестрол и этинилэстрадиол); 14) антиэстрогены (например, тамоксифен); 15) андрогены (например, тестостеронпропионат и флуоксиместерон); 16) антиандрогены (например, флутамид): и 17) аналоги гонадотропин-высвобождающего гормона (например, лейпролид).
Любое онколитическое средство, которое обычно используют в контексте терапии рака, находит применение в терапевтических способах настоящего раскрытия. Например, Управление США по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) придерживается фармакологического справочника онколитических средств, одобренных для применения в Соединенных Штатах. Международные партнерские агентства FDA поддерживают аналогичные фармакологические справочники. Специалистам в данной области техники будет понятно, что «инструкции по медицинскому применению препарата», требуемые для всех одобренных в США химиотерапевтических средств, описывают утвержденные показания, информацию о дозировках, данные о токсичности и тому подобное для приведенных в качестве примера средств.
Противораковое средства дополнительно включают соединения, которые были идентифицированы как обладающие противораковой активностью. Примеры включают, но не ограничиваются этим, 3-AP, 12-О-тетрадеканоилфорбол-13-ацетат, 17AAG, 852A, ABI-007, ABR-217620, ABT-751, ADI-PEG 20, AE-941, AG-013736, AGRO100, аланозин, AMG 706, антитело G250, антинеопластоны, AP23573, апазиквон, APC8015, атипримод, АТН-161, атрацентен, азацитидин, BB-10901, BCX-1777, бевацизумаб, BG00001, бикалутамид, BMS 247550, бортезомиб, бриостатин-1, бусерелин, калцитриол, CCI-779, CDB-2914, цефиксим, цетуксимаб, CG0070, циленгитид, клофарабин, комбретастатин А4 фосфат, CP-675,206, CP-724,714, CpG 7909, куркумин, децитабин, DENSPM, доксеркальциферол, E7070, E7389, эктеинасцидин 743, эфапроксирал, эфлорнитин, EKB-569, энзастаурин, эрлотиниб, экзисулинд, фенретинид, флавопиридол, флударабин, флутамид, фотемустин, FR901228, G17DT, галиксимаб, гефинитиб, генистеин, глуфосфамид, ГТИ-2040, гистрелин, HKI-272, гомогаррингтонин, HSPPC-96, hu14.18-интерлейкин-2 белок слияния, HuMax-CD4, илопрост, имиквимод, инфликсимаб, интерлейкин-12, IPI-504, ирофулвен, иксабепилон, лапатиниб, леналидомид, лестартиниб, лейпролид, иммунотоксин LMB-9, лонафарниб, луниликсимаб, мафосфамид, MB07133, MDX-010, MLN2704, моноклональное антитело 3F8, моноклональное антитело J591, мотексафин, MS-275, MVA-MUC1-IL2, нилутамид, нитрокамптотецин, нолатрексед дигидрохлорид, нолвадекс, NS-9, O6-бензилгуанин, облимренсен натрия, ONYX-015, ореговомаб, OSI-774, панитумумаб, параплатин, PD-0325901, пеметрексед, PHY906, пиоглитазон, пирфенидон, пиксантрон, PS-341, PSC 833, PXD101, пиразолоакридин, R115777, RAD001, ранпирназа, аналог ребеккамицина, белок rhuАнгиостатин, rhuMab 2C4, розиглитазон, рубитекан, S-1, S-8184, сатраплатин, SB-, 15992, SGN-0010, SGN-40, сорафениб, SR31747A, ST1571, SU011248, субероиланилид гидроксасаминовой кислоты, сурамин, талабостат, талампанел, тариквидар, темсиролимус, иммунотоксин TGFa-PE38, талидомид, тималфазин, типифарниб, тирапазамин, TLK286, трабектедин, триметрексат глюкуронат, TroVax, UCN-1, вальпроевая кислота, винфлунин, VNP40101M, волоциксимаб, вориностат, VX-680, ZD1839, ZD6474, зилейтон и зосуквидар тригидрохлорид.
Более подробное описание противораковых средств и других необязательных терапевтических средств специалисты в данной области могут найти в любом из большого количества справочников, включая, но не ограничиваясь этим, Physician's Desk Reference и в Goodman and Gilman's "Pharmaceutical Basis of Therapeutics" tenth edition, Eds. Hardman et al., 2002.
В некоторых вариантах осуществления способы, представленные в настоящей заявке, включают введение TG02 больному раком в комбинации с лучевой терапией. Способы, представленные в настоящей заявке, не ограничиваются типами, количествами или системами доставки и введения, используемыми для доставки терапевтической дозы облучения пациенту. Например, пациент может получать фотонную лучевую терапию, лучевую терапию пучком частиц, другие виды лучевой терапии и их комбинации. В некоторых вариантах осуществления пациента подвергают облучению с использованием линейного ускорителя. В других вариантах осуществления облучение осуществляют с использованием гамма-ножа.
Источник излучения может быть внешним или внутренним для пациента. Внешняя лучевая терапия является наиболее распространенной и включает направление луча излучения высокой энергии на участок опухоли через кожу с использованием, например, линейного ускорителя. В то время как луч излучения локализуется на участке опухоли, практически невозможно избежать воздействия на нормальную здоровую ткань. Однако внешнее излучение обычно хорошо переносится пациентами. Внутренняя лучевая терапия включает внедрение источника излучения, такого как шарики, проволоки, гранулы, капсулы, частицы и т.п., внутри тела на участке опухоли или вблизи него, включая использование систем доставки, которые конкретно нацелены на раковые клетки (например, используя частицы, прикрепленные к лигандам, связывающим раковые клетки). Такие имплантаты можно удалить после лечения или оставить в организме инактивированными. Типы внутренней лучевой терапии включают, но не ограничиваются этим, брахитерапию, интерстициальное облучение, внутриполостное облучение, радиоиммунотерапию и подобные.
Пациент необязательно может получать радиосенсибилизаторы (например, метронидазол, мезинидазол, внутриартериальный Budr, внутривенный йоддезоксиуридин (IudR), нитроимидазол, 5-замещенные-4-нитроимидазолы, 2H-изоиндолдионы, [[(2-бромэтил)-амино]метил]-нитро-1H-имидазол-1-этанол, нитроанилиновые производные, ДНК-аффинные гипоксия-селективные цитотоксины, галогенированный ДНК-лиганд, 1,2,4-бензотриазин оксиды, производные 2-нитроимидазола, фторсодержащие производные нитроазола, бензамид, никотинамид, акридиновый интеркалятор, производное 5-тиотретразола, 3-нитро-1,2,4-триазол, производное 4,5-динитроимидазола, гидроксилированные тексафрины, цисплатин, митомицин, тирипазамин, нитрозомочевину, меркаптопурин, метотрексат, фторурацил, блеомицин, винкристин, карбоплатин, эпирубицин, доксорубицин, циклофосфамид, виндезин, этопозид, паклитаксел, тепло (гипертермия) и подобные), радиопротекторы (например, цистеамин, аминоалкилдигидрофосфоротиоат, амифостин (WR 2721), IL-1, IL-6 и подобные). Радиосенсибилизаторы усиливают гибель опухолевых клеток. Радиопротекторы защищают здоровую ткань от вредного воздействия радиации.
Любой тип облучения можно применять для пациента, если доза облучения переносится пациентом без неприемлемых отрицательных побочных эффектов. Подходящие типы радиотерапии включают, например, ионизирующую (электромагнитную) радиотерапию (например, рентгеновские лучи или гамма-лучи) или лучевую терапию пучком частиц (например, излучение с высокой линейной энергией). Ионизирующее излучение определяется как излучение, содержащее частицы или фотоны, которые обладают достаточной энергией для получения ионизации, то есть увеличение или потерю электронов (как описано, например, в патенте США 5770581, включенном в настоящую заявку посредством ссылки во всей полноте). Эффекты облучения могут, по меньшей мере частично, контролироваться клиницистом. В одном из вариантов осуществления дозу облучения фракционируют для максимального воздействия на клетку-мишень и снижения токсичности.
В одном из вариантов осуществления суммарная доза облучения, вводимая пациенту, составляет от около 0,01 Грей (Гр) до около 100 Гр. В другом варианте осуществления курс лечения включает введение от около 10 Гр до около 65 Гр (например, около 15 Гр, 20 Гр, 25 Гр, 30 Гр, 35 Гр, 40 Гр, 45 Гр, 50 Гр, 55 Гр или 60 Гр). Хотя в некоторых вариантах осуществления полную дозу облучения можно вводить в течение одного дня, идеально, когда общую дозу фракционируют и вводят в течение нескольких дней. Оптимально, радиотерапию проводят курсом по меньшей мере около 3 дней, например, по меньшей мере 5, 7, 10, 14, 17, 21, 25, 28, 32, 35, 38, 42, 46, 52 или 56 дней (около 1-8 недель). Следовательно, суточная доза облучения будет включать приблизительно 1-5 Гр (например, около 1 Гр, 1,5 Гр, 1,8 Гр, 2 Гр, 2,5 Гр, 2,8 Гр, 3 Гр, 3,2 Гр, 3,5 Гр, 3,8 Гр, 4 Гр, 4,2 Гр или 4,5 Гр) или 1-2 Гр (например, 1,5-2 Гр). Суточная доза облучения должна быть достаточной для индукции разрушения клеток-мишеней. Если распределить на определенный период, В одном из вариантов осуществления облучение не вводят каждый день, тем самым позволяя животному отдыхать, реализовать эффекты терапии. Например, желательно использовать лучевую терапию в течение 5 последовательных дней и не вводить в течение 2 дней в течение каждой недели лечения, давая, таким образом, 2 дня отдыха в неделю. Однако облучение можно вводить 1 день/неделя, 2 дня/неделя, 3 дня/неделя, 4 дня/неделя, 5 дней/неделя, 6 дней/неделя или все 7 дней/неделя, в зависимости от чувствительности животного и любых потенциальных побочных эффектов. Лучевую терапию можно начинать в любое время периода лечения. В одном из вариантов осуществления облучение начинают на 1 или 2 неделе и вводят в течение оставшегося времени терапевтического периода. Например, облучение вводят в недели 1-6 или в недели 2-6 терапевтического периода, включающего 6 недель для лечения, например, солидной опухоли. Альтернативно, облучение вводят в недели 1-5 или недели 2-5 терапевтического периода, включающего 5 недель. Однако эти иллюстративные графики введения радиотерапии не предназначены для ограничения способов, представленных в настоящей заявке.
IV. Терапевтические способы
В терапевтических способах, представленных в настоящей заявке, TG02, ингибитор контрольных точек иммунного ответа, ингибитор COX-2 и/или необязательное терапевтическое, например, противораковое средство можно вводить больному раком при одном или нескольких из следующих условий: с разной периодичностью, с разной длительностью, в разных концентрациях, разными путями введения и т.д.
В некоторых вариантах осуществления TG02 вводят до ингибитора контрольных точек иммунного ответа, ингибитора COX-2 и/или необязательного терапевтического средства, например, за 0,5, 1, 2, 3, 4, 5, 10, 12 или 18 часов, 1, 2, 3, 4, 5 или 6 дней или 1, 2, 3 или 4 недель до введения ингибитора контрольных точек иммунного ответа, ингибитора COX-2 и/или необязательного терапевтического средства.
В некоторых вариантах осуществления TG02 вводят после ингибитора контрольных точек иммунного ответа, ингибитора COX-2 и/или необязательного терапевтического средства, например, через 0,5, 1, 2, 3, 4, 5, 10, 12 или 18 часов, 1, 2, 3, 4, 5 или 6 дней или 1, 2, 3 или 4 недель после введения ингибитора контрольных точек иммунного ответа, ингибитора COX-2 и/или необязательного терапевтического средства.
В некоторых вариантах осуществления TG02, ингибитор контрольных точек иммунного ответа, ингибитор COX-2 и/или необязательное терапевтическое средство вводят одновременно, но по разным схемам введения, например, TG02 вводят ежедневно, в то время как ингибитор контрольных точек иммунного ответа вводят один раз в неделю, один раз каждые две недели, один раз каждые три недели или один раз каждые четыре недели. В других вариантах осуществления TG02 вводят один раз в день, в то время как ингибитор контрольных точек иммунного ответа, ингибитор COX-2 и/или необязательное терапевтическое средство вводят один раз в неделю, один раз каждые две недели, один раз каждые три недели или один раз каждые четыре недели.
Терапевтические способы, представленные в настоящей заявке, включают введение TG02 больному раком в количестве, которое эффективно для достижения целевого назначения. Несмотря на то, что индивидуальные потребности различаются, определение оптимальных диапазонов эффективных количеств каждого компонента входит в компетенцию специалиста в данной области. Как правило, TG02 можно вводить в количестве от около 1 мг/кг до около 500 мг/кг, от около 1 мг/кг до около 100 мг/кг или от около 1 мг/кг до около 50 мг/кг. Дозировка композиции могут быть любой, включая, но не ограничиваясь этим, 30-600 мг/день. Конкретные дозы включают 50, 100, 200, 250, 300, 400, 500 и 600 мг/день. В одном из вариантов осуществления TG02 вводят один раз в день в течение 3-7 последовательных дней до введения ингибитора контрольных точек иммунного ответа. В другом варианте осуществления вводят 250 мг/день TG02. В другом варианте осуществления 250 мг/день TG02 вводят два раза в неделю. В другом варианте осуществления введение TG02 продолжают в день введения ингибитора контрольных точек иммунного ответа и продолжают в течение дополнительных дней до тех пор, пока заболевание не начнет прогрессировать, или до тех пор, пока введение TG02 больше не будет полезным. Эти дозы являются примерными для среднего случая, но могут быть отдельные случаи, в которых заслуживают внимания более высокие или более низкие дозы, и таковые входят в объем настоящего раскрытия. На практике лечащий врач определяет фактический режим дозирования, наиболее подходящий для отдельного пациента, который может варьироваться в зависимости от возраста, массы тела и ответа конкретного пациента.
Стандартная доза для перорального приема TG02 может включать от около 0,01 до около 1000 мг, например, от около 10 до около 500 мг TG02. В одном из вариантов осуществления стандартная доза для перорального приема TG02 составляет 10 мг, 20 мг, 30 мг, 40 мг, 50 мг, 60 мг, 70 мг 80 мг, 90 мг, 100 мг, 110 мг, 120 мг, 130 мг, 140 мг, 150 мг, 160 мг, 170 мг, 180 мг, 190 мг, 200 мг, 210 мг, 220 мг, 230 мг, 240 мг, 250 мг, 260 мг, 270 мг, 280 мг, 290 мг или 300 мг. Стандартную дозу можно вводить один или несколько раз ежедневно, например, в виде одной или нескольких таблеток или капсул.
В дополнение к введению TG02 как отдельного химического вещества, его можно вводить как часть фармацевтического препарата или композиции. В некоторых вариантах осуществления фармацевтический препарат или композиция может включать один или несколько фармацевтически приемлемых носителей, эксципиентов и/или вспомогательных веществ. В некоторых вариантах осуществления один или несколько носителей, эксципиентов и вспомогательных веществ облегчают переработку TG02 в препарат или композицию, которые можно использовать фармацевтически. Препараты, в частности те препараты, которые можно вводить перорально или местно и которые можно использовать для одного типа введения, такие как таблетки, драже, пастилки и капсулы с медленным высвобождением, ополаскиватели и средства для полоскания рта, гели, жидкие суспензии, ополаскиватели для волос, гели для волос, шампуни, а также препараты, которые можно вводить ректально, такие как суппозитории, а также подходящие растворы для введения путем внутривенной инфузии, инъекции, для местного или перорального введения содержат от около 0,01 до 99 процентов, В одном из вариантов осуществления от около 0,25 до 75 процентов активного соединения(соединений), вместе с одним или несколькими из носителей, эксципиентов и/или вспомогательных веществ.
Фармацевтические композиции, представленные в настоящей заявке, можно вводить любому пациенту, который может испытывать положительные эффекты TG02. Главными среди таких пациентов являются млекопитающие, например, люди, хотя способы и композиции, представленные в настоящей заявке, не должны этим ограничиваться. Другие пациенты включают ветеринарных животных (коров, овец, свиней, лошадей, собак, кошек и подобных).
Фармацевтические препараты, представленные в настоящей заявке, получают при помощи обычных процессов смешивания, гранулирования, дражирования, растворения или лиофилизации. Таким образом, фармацевтические препараты для перорального применения можно получить путем комбинирования активных соединений с твердыми эксципиентами, измельчения полученной смеси и обработки смеси гранул, после добавления подходящих вспомогательных веществ, если желательно или необходимо, для получения таблеток или драже.
Подходящими эксципиентами являются, в частности, наполнители такие как сахариды, например, лактоза или сахароза, маннит или сорбит, препараты целлюлозы и/или фосфаты кальция, например, трикальций фосфат или гидрофосфат кальция, а также связующие, такие как крахмальная паста, с использованием, например, кукурузного крахмала, пшеничного крахмала, рисового крахмала, картофельного крахмала, желатина, трагаканта, метилцеллюлозы, гидроксипропилметилцеллюлозы, натрийкарбоксиметилцеллюлозы и/или поливинилпирролидона. Если требуется, можно добавить вещества для улучшения распадаемости таблеток, такие как вышеуказанные крахмалы, а также карбоксиметил-крахмал, сшитый поливинилпирролидон, агар или альгиновая кислота или ее соль, такая как альгинат натрия. Вспомогательные вещества могут представлять собой подходящие регулирующие текучесть и смазывающие вещества. Подходящие вспомогательные вещества включают, например, диоксид кремния, тальк, стеариновую кислоту или ее соли, такие как стеарат магния или стеарат кальция, и/или полиэтиленгликоль. На сердцевину драже наносят подходящие покрытия, которые, если требуется, устойчивы к желудочному соку. Для этой цели можно использовать концентрированные сахаридные растворы, которые могут необязательно содержать гуммиарабик, тальк, поливинилпирролидон, полиэтиленгликоль и/или диоксид титана, лакирующие растворы и подходящие органические растворители или смеси растворителей. Для получения покрытий, устойчивых к желудочному соку, используют растворы подходящих целлюлозных препаратов, таких как фталат ацетилцеллюлозы или фталат гидроксипропилметилцеллюлозы. Красящие вещества или пигменты можно добавить к покрытиям таблеток или драже, например, для идентификации или для характеристики комбинаций доз активных веществ.
Другие фармацевтические препараты, которые можно использовать перорально, включают твердые капсулы, полученные из желатина, а также мягкие герметичные капсулы, полученные из желатина и пластификатора, такого как глицерин или сорбит. Твердые капсулы могут содержать активные соединения в форме гранул, которые могут быть смешаны с наполнителями, такими как лактоза, связующими, такими как крахмалы, и/или смазывающими веществами, такими как тальк или стеарат магния, и необязательно стабилизаторами. В мягких капсулах активные соединения, В одном из вариантов осуществления, растворены или суспендированы в подходящих жидкостях, таких как жирные масла или жидкий парафин. Кроме того, могут быть добавлены стабилизаторы.
Возможные фармацевтические препараты, которые можно использовать ректально, включают, например, суппозитории, которые состоят из комбинации одного или нескольких активных соединений с основой для суппозиториев. Подходящими основами для суппозиториев являются, например, природные или синтетические триглицериды или парафиновые углеводороды. Кроме того, можно также использовать желатиновые ректальные капсулы, которые состоят из комбинации активных соединений с основой. Возможные материалы основы включают, например, жидкие триглицериды, полиэтиленгликоли или парафиновые углеводороды.
Подходящие лекарственные формы для парентерального введения включают водные растворы активных соединений в водорастворимой форме, например, водорастворимые соли и щелочные растворы. Кроме того, можно вводить суспензии активных соединений в виде подходящих масляных инъекционных суспензий. Подходящие липофильные растворители или носители включают жирные масла, например, кунжутное масло или синтетические эфиры жирных кислот, например, этилолеат или триглицериды, или полиэтиленгликоль-400. Водные инъекционные суспензии могут содержать вещества, которые увеличивают вязкость суспензии, включая, например, карбоксиметилцеллюлозу натрия, сорбит и/или декстран. Необязательно, суспензия может также содержать стабилизаторы.
Настоящее раскрытие охватывает использование сольватов TG02. Сольваты, как правило, не оказывают существенного влияния на физиологическую активность или токсичность соединения и как таковые могут функционировать как фармакологические эквиваленты. Термин "сольват", как он используется в настоящей заявке, включает комбинацию, физическую ассоциацию и/или сольватацию TG02 с молекулой растворителя, такую как, например, дисольват, моносольват или гемисольват, где отношение молекулы растворителя к TG02 составляет около 2:1, около 1:1 или около 1:2, соответственно. Эта физическая ассоциация включает различные степени ионного и ковалентного связывания, включая образование водородных связей. В некоторых случаях сольват может быть выделен, например, когда одна или несколько молекул растворителя включены в кристаллическую решетку кристаллического твердого вещества. Таким образом, "сольват" охватывает как фазу раствора, так и выделяемые сольваты. TG02 может присутствовать в виде сольватированных форм с фармацевтически приемлемым растворителем, таким как вода, метанол, этанол и подобные, и предполагается, что настоящее раскрытие включает как сольватированные, так и несольватированные формы TG02. Один тип сольвата представляет собой гидрат. "Гидрат" относится к определенной подгруппе сольватов, где молекула растворителя представляет собой воду. Сольваты, как правило, могут функционировать как фармакологические эквиваленты. Получение сольватов известно в данной области техники. См., например, M. Caira et al, J. Pharmaceut. Sci., 93(3):601-611 (2004), который описывает получение сольватов флуконазола с этилацетатом и с водой. Аналогичное получение сольватов, гемисольватов, гидратов и т.п. описано E.C. van Tonder et al., AAPS Pharm. Sci. Tech., 5(1): Article 12 (2004) и A.L. Bingham et al., Chem. Commun. 603-604 (2001). Типичный, неограничивающий, способ получения сольвата включает растворение TG02 в желаемом растворителе (органическом, воде или их смеси) при температурах выше 20°C до около 25°C, затем охлаждение раствора со скоростью, достаточной для образования кристаллов, и выделение кристаллов известными способами, например фильтрацией. Аналитические методы, такие как инфракрасная спектроскопия, можно использовать для подтверждения присутствия растворителя в кристалле сольвата.
Терапевтически эффективные количества TG02 и/или ингибитора контрольных точек иммунного ответа и/или ингибитора COX-2 и/или необязательного терапевтического средства, сформулированных в соответствии со стандартной фармацевтической практикой, вводят пациенту, нуждающемуся в этом. Показано ли такое лечение, зависит от конкретного случая, и это определяют на основании медицинской оценки (диагноза), которая учитывает признаки, симптомы и/или нарушения функций, которые присутствуют, риски развития определенных признаков, симптомов и/или нарушения функций и другие факторы.
TG02, ингибитор контрольных точек иммунного ответа, ингибитор COX-2 и/или необязательное терапевтическое средство можно вводить любым подходящим путем, например, путем перорального, буккального, ингаляционного, сублингвального, ректального, вагинального, внутрикожного или интратекального через поясничную пункцию, трансуретрального, назального, чрескожного, то есть трансдермального или парентерального (включая внутривенную, внутримышечную, подкожную, внутрикоронарную, внутрикожную, внутримышечную, внутрибрюшинную, внутрисуставную, интратекальную, ретробульбарную, внутрилегочную инъекцию и/или хирургическую имплантацию на конкретном участке) введения. Парентеральное введение можно осуществить с использованием иглы и шприца или с использованием техники высокого давления.
Фармацевтические композиции включают такие, в которых TG02, ингибитор контрольных точек иммунного ответа, ингибитор COX-2 и/или необязательное терапевтическое средство вводят в эффективном количестве для достижения намеченной цели. Конкретную композицию, путь введение и дозировку определяет лечащий врач с учетом диагностированного состояния или заболевания. Количество и интервал дозирования можно регулировать индивидуально для обеспечения уровней TG02, ингибитора контрольных точек иммунного ответа, ингибитора COX-2 и/или необязательного терапевтического средства, достаточного для поддержания терапевтического эффекта.
Токсичность и терапевтическую эффективность TG02, ингибитора контрольных точек иммунного ответа, ингибитора COX-2 и/или необязательного терапевтического средства можно определить с использованием стандартных фармацевтических процедур в клеточных культурах или экспериментальных животных, например, для определения максимально переносимой дозы (MTD) соединения, которую определяют как самую высокую дозу, которая не вызывает токсичности у пациента. Соотношение доз между максимальной переносимой дозой и терапевтическим эффектом (например, ингибирование роста опухоли) представляет собой терапевтический индекс. Доза может варьироваться в пределах этого диапазона в зависимости от используемой лекарственной формы и используемого пути введения. Определение терапевтически эффективного количества входит в компетентность специалиста в данной области техники, особенно в свете подробного раскрытия, представленного в настоящей заявке.
Терапевтически эффективное количество TG02, ингибитора контрольных точек иммунного ответа, ингибитора COX-2 и/или необязательного терапевтического средства, необходимое для использования в терапии, варьируется в зависимости от природы состояния, подлежащего лечению, продолжительности времени, в течение которого желательна активность, и возраста и состояния пациента, и в конечном счете определяется лечащим врачом. Например, дозируемые количества и интервалы можно регулировать индивидуально для обеспечения уровней в плазме TG02 и ингибитора контрольных точек иммунного ответа, которые достаточны для поддержания желаемых терапевтических эффектов. Желаемую дозу удобно вводить в виде разовой дозы или в виде нескольких доз, вводимых с подходящими интервалами, например, в виде одной, двух, трех, четырех или больше дробных доз в день. Часто желательно или требуется несколько доз. Например, TG02 и ингибитор контрольных точек иммунного ответа можно вводить с частотой: одна доза в день; четыре дозы, доставляемые в виде одной дозы в день с четырехдневными интервалами (q4d×4); четыре дозы, доставляемые в виде одной дозы в день с трехдневными интервалами (q3d×4); одна доза в день с пятидневными интервалами (qd×5); одна доза в неделю в течение трех недель (qwk3); пять ежедневных доз, с двухдневным перерывом, а затем снова пять ежедневных доз (5/2/5); или любой режим дозирования, определенный как подходящий в конкретных обстоятельствах.
Ингибитор контрольных точек иммунного ответа вводят в терапевтически эффективных количествах. Когда ингибитор контрольных точек иммунного ответа представляет собой моноклональное антитело, 1-20 мг/кг вводят в виде внутривенной инфузии каждые 2-4 недели. Например, можно вводить 50 мг, 60 мг, 70 мг, 80 мг, 90 мг, 100 мг, 200 мг, 300 мг, 400 мг, 500 мг, 600 мг, 700 мг, 800 мг, 900 мг, 1000 мг, 1100 мг, 1200 мг, 1300 мг, 1400 мг, 1500 мг, 1600 мг, 1700 мг, 1800 мг, 1900 мг и 2000 мг антитела.
Например, когда ингибитор контрольных точек иммунного ответа представляет собой анти-PD-1 антитело ниволумаб, 3 мг/кг можно вводить путем внутривенной инфузии в течение 60 минут каждые две недели. Когда ингибитор контрольных точек иммунного ответа представляет собой анти-PD-1 антитело пембролизумаб, 2 мг/кг можно вводить путем внутривенной инфузии в течение 30 минут каждые две или три недели. Когда ингибитор контрольных точек иммунного ответа представляет собой анти-PD-L1 антитело авелумаб, 10 мг/кг можно вводить путем внутривенной инфузии каждые 2 недели. Disis et al., J. Clin Oncol. 33 (2015) (suppl; abstr 5509). Когда ингибитор контрольных точек иммунного ответа представляет собой анти-PD-L1 антитело MPDL3280A, 20 мг/кг можно вводить путем внутривенной инфузии каждые 3 недели. Herbst et al., Nature 515:563-80 (2014). Когда ингибитор контрольных точек иммунного ответа представляет собой анти-CTLA-4 антитело ипилумумаб, 3 мг/кг можно вводить путем внутривенной инфузии в течение 90 минут каждые 3 недели. Когда ингибитор контрольных точек иммунного ответа представляет собой анти-CTLA-4 антитело тремелимумаб, 15 мг/кг можно вводить путем внутривенной инфузии каждые 12 недель. Naido et al., British Journal of Cancer 111:2214-19 (2014); Drugs R D, 10:123-32 (2010). Когда ингибитор контрольных точек иммунного ответа представляет собой анти-LAG3 антитело GSK2831781, от 1,5 до 5 мг/кг можно вводить путем внутривенной инфузии в течение 120 минут каждые 2-4 недели. Когда ингибитор контрольных точек иммунного ответа представляет собой анти-TIM3 антитело, 1-5 мг/кг можно вводить путем внутривенной инфузии в течение 30-90 минут каждые 2-4 недели. Когда ингибитор пути индоламин-2,3-диоксигеназы (IDO) представляет собой ингибитор индоксимод в комбинации с темозоломидом, используют 18,5 мг/кг/доза BID с повышением до 27,7 мг/кг/доза BID индоксимода с 200 мг/м2 каждые 5 дней темозоломида.
Ингибитор COX-2 также вводят в терапевтически эффективных количествах, например, от около 1 мг/кг до около 500 мг/кг, от около 1 мг/кг до около 100 мг/кг или от около 1 мг/кг до около 50 мг/кг. Стандартная доза для перорального приема ингибитора COX-2 может включать от около 0,01 до около 1000 мг, например, от около 1 до около 250 мг ингибитора COX-2. В одном из вариантов осуществления стандартная доза для перорального приема ингибитора COX-2 составляет 5 мг, 10 мг, 20 мг, 30 мг, 40 мг, 50 мг, 60 мг, 70 мг 80 мг, 90 мг, 100 мг, 110 мг, 120 мг, 130 мг, 140 мг, 150 мг, 160 мг, 170 мг, 180 мг, 190 мг, 200 мг, 210 мг, 220 мг, 230 мг, 240 мг или 250 мг. Стандартную дозу можно вводить один или несколько раз ежедневно, например, в виде одной или нескольких таблеток или капсул.
В одном из вариантов осуществления ингибитор контрольных точек иммунного ответа представляет собой антитело, и 1-20 мг/кг вводят путем внутривенной инфузии каждые 2-4 недели. В другом варианте осуществления 50-2000 мг антитела вводят путем внутривенной инфузии каждые 2-4 недели. В другом варианте осуществления TG02 вводят до введения антитела. В другом варианте осуществления TG02 вводят за 3-7 дней до дня введения антитела. В другом варианте осуществления TG02 также вводят в день введения антитела и в последующие дни после этого до тех пор, пока заболевание не начнет прогрессировать, или до тех пор, пока введение TG02 больше не будет эффективным.
В одном из вариантов осуществления больной раком имеет опухоли с биомаркером, например, сверхэкспрессией MYC и/или MCL1, и принимает 2 мг/кг пембролизумаба, вводимого путем внутривенной инфузии один раз каждые три недели, и 30-600 мг TG02, вводимого в течение 3-7 дней до введения пембролизумаба, в день введения пембролизумаба и после этого до тех пор, пока заболевание не начнет прогрессировать, или до тех пор, пока больше не будет терапевтической пользы.
В другом варианте осуществления больной раком имеет опухоли с биомаркером, например, сверхэкспрессией MYC и/или MCL1, и принимает 3 мг/кг ниволумаба, вводимого путем внутривенной инфузии каждые 2 недели, и 30-600 мг TG02, вводимого перорально в течение 3-7 дней до введения ниволумаба, в день введения ниволумаба и после этого до тех пор, пока заболевание не начнет прогрессировать, или до тех пор, пока больше не будет терапевтической пользы.
В другом варианте осуществления больной раком имеет опухоли с биомаркером, например, сверхэкспрессией MYC и/или MCL1, и принимает 3 мг/кг ниволумаба, вводимого путем внутривенной инфузии каждые 2 недели, и 30-600 мг TG02, вводимого перорально два раза в неделю до введения ниволумаба, в день введения ниволумаба и после этого до тех пор, пока заболевание не начнет прогрессировать, или до тех пор, пока больше не будет терапевтической пользы.
В другом варианте осуществления лечение больного раком ингибитором контрольных точек иммунного ответа и TG02 индуцирует антипролиферативный ответ быстрее, чем когда ингибитор контрольных точек иммунного ответа вводят отдельно.
В другом варианте осуществления лечение больного раком ингибитором COX-2 и TG02 индуцирует антипролиферативный ответ быстрее, чем когда ингибитор COX-2 вводят отдельно.
V. Биомаркеры
Термин "биомаркер", как он используется в настоящей заявке, относится к любому биологическому соединению, такому как ген, белок, фрагмент белка, пептид, полипептид, нуклеиновая кислота и т.д., которое можно определить и/или количественно охарактеризовать у больного раком in vivo или в биологическом образеце, полученном от больного раком. Биомаркер может представлять собой полную интактную молекулу или ее часть или фрагмент. В одном из вариантов осуществления измеряют уровень экспрессии биомаркера. Уровень экспрессии биомаркера можно измерить, например, путем определения уровня белка или РНК, например, мРНК, биомаркера. В некоторых вариантах осуществления части или фрагменты биомаркеров можно определить или измерить, например, при помощи антитела или другого специфического связывающего агента. В некоторых вариантах осуществления измеряемый аспект биомаркера ассоциирован с данным состоянием пациента, таким как конкретная стадия рака. Для биомаркеров, которые определяют на уровне белка или РНК, такие измеряемые аспекты могут включать, например, присутствие, отсутствие или концентрацию, т.е. уровень экспрессии, биомаркера у больного раком или в биологическом образце, полученном от больного раком. Для биомаркеров, которые определяют на уровне нуклеиновой кислоты, такие измеряемые аспекты могут включать, например, аллельные варианты биомаркера или тип, скорость и/или степень мутации биомаркера, также называемые в настоящей заявке как мутационный статус.
Для биомаркеров, которые определяют на уровне экспрессии белка или РНК, уровень экспрессии, измеренный между разными фенотипическими статусами, может считаться разным, например, если средний или медианный уровень экспрессии биомаркера в разных группах рассчитан как статистически значимый. Обычные критерии определения статистической значимости включают, среди прочего, t-критерий, ANOVA, Kruskal-Wallis, Wilcoxon, Mann-Whitney, Анализ Значимости Микромассивов, отношение шансов и т.д. Биомаркеры, отдельно или в комбинации, обеспечивают оценку относительной вероятности принадлежности индивида к тому или иному фенотипическому статусу. Поэтому они являются полезными, среди прочего, как маркеры заболевания и как индикаторы того, что конкретные схемы терапевтического лечения скорее всего приведут к благоприятным для пациента результатам.
Биомаркеры включают, но не ограничиваются этим, гены, перечисленные в Таблице 1. В одном из вариантов осуществления измеряемым аспектом биомаркера является его статус экспрессии. В одном из вариантов осуществления измеряемым аспектом биомаркера является его мутационный статус.
В одном из вариантов осуществления биомаркер представляет собой MYC. В одном из вариантов осуществления измеряемым аспектом MYC является его статус экспрессии. В одном из вариантов осуществления биомаркер представляет собой сверхэкспрессию MYC.
Таким образом, в некоторых аспектах настоящего раскрытия, биомаркер представляет собой MYC, который дифференцированно присутствует у индивида одного фенотипического статуса, например, у пациента, имеющего рак, например, гепатоцеллюлярную карциному (HCC), глиобластомы (GBM), рак легких, рак молочной железы, рак головы и шеи, рак предстательной железы, меланому или колоректальный рак, по сравнению с другим фенотипическим статусом, например, со здоровым незаболевшим субъектом или с пациентом, имеющим рак без сверхэкспрессии MYC.
Биомаркерные стандарты могут заранее определяться, определяться одновременно или определяться после получения биологического образца от индивида. Биомаркерные стандарты для использования со способами, описанными в настоящей заявке, могут, например, включать данные из образцов от субъектов без рака; данные из образцов от субъектов с раком, например, GBM, который не является прогрессирующим, рецидивирующим и/или метастатическим раком; и данные из образцов от субъектов с раком, например, GBM, который является прогрессирующим, рецидивирующим и/или метастатическим раком. Можно осуществить сравнения, чтобы установить предопределенные пороговые биомаркерные стандарты для разных классов субъектов, например, болеющих vs. неболеющих субъектов. Стандарты могут быть выработаны в этом же анализе, или это могут быть известные стандарты из предыдущего анализа.
В одном из вариантов осуществления биомаркер представляет собой MCL1. В одном из вариантов осуществления измеряемым аспектом MCL1 является его статус экспрессии. В одном из вариантов осуществления биомаркер представляет собой сверхэкспрессию MCL1.
Биомаркер дифференцированно присутствует между группами с разным фенотипическим статусом, если средние или медианные уровни экспрессии или мутации биомаркера рассчитаны как разные, т.е. выше или ниже, между этими группами. Таким образом, биомаркеры указывают на принадлежность индивида, например, больного раком, к тому или иному фенотипическому статусу.
Таким образом, в некоторых аспектах настоящего раскрытия, биомаркер представляет собой MCL1, который дифференцированно присутствует, т.е. сверхэкспрессируется у индивида одного фенотипического статуса, например, у пациента, имеющего рак, например, гепатоцеллюлярную карциному (HCC), глиобластомы (GBM), рак легких, рак молочной железы, рак головы и шеи, рак предстательной железы, меланому, колоректальный рак, медуллобластому или обычные опухоли головного мозга, по сравнению с другим фенотипическим статусом, например, неболеющим пациентом или имеющим рак без сверхэкспрессии MCL1.
Помимо отдельных биологических соединений, например, MYC или MCL1, термин "биомаркер" в контексте настоящей заявки предусматривает включение групп, серий или последовательностей из множества биологических соединений. Например, комбинация MYC и MCL1 может включать биомаркер. Термин "биомаркер" может включать одно, два, три, четыре, пять, шесть, семь, восемь, девять, десять, пятнадцать, двадцать двадцать пять, тридцать или больше биологических соединений.
Определение уровня экспрессии или мутационного статуса биомаркера у пациента можно осуществить с использованием любого из множества способов, известных из уровня техники. Любой способ, известный из уровня техники для количественного определения специфических белков и/или детекции экспрессии MYC и/или MCL1 или уровней экспрессии или мутации любого другого биомаркера у пациента или в биологическом образце, можно использовать в способах по настоящему изобретению. Примеры включают, но не ограничиваются этим, ПЦР (полимеразная цепная реакция) или ОТ-ПЦР, Нозерн-блот, Вестерн-блот, ELISA (твердофазный иммуно-ферментный анализ), RIA (радиоиммуноанализ), анализ экспрессии РНК с использованием генных чипов, иммуногистохимию или иммунофлуоресценцию. См., например, Slagle et al. Cancer 83:1401 (1998). Некоторые варианты осуществления настоящего изобретения включают способы, в которых определяют экспрессию (транскрипцию) РНК биомаркеров. Другие варианты осуществления настоящего изобретения включают способы, в которых определяют экспрессию белка в биологическом образеце. См., например, Harlow et al., Antibodies: A Laboratory Manual, Cold Spring Harbor Laboratory, Cold Spring Harbor, NY, (1988), и Ausubel et al., Current Protocols in Molecular Biology, John Wiley & Sons, New York 3rd Edition, (1995). Для нозерн-блоттинга или ОТ-ПЦР анализа из образца опухолевой ткани выделяют РНК с использованием методов в отсутствие РНКазы. Такие методы хорошо известны из уровня техники.
В одном из вариантов осуществления настоящего изобретения биологический образец получают от пациента и клетки в биопсии анализируют для определения статуса экспрессии или мутационного статуса биомаркера.
В одном из вариантов осуществления настоящего изобретения используют ПЭТ-изображение для определения экспрессии биомаркера.
В другом варианте осуществления настоящего изобретения осуществляют нозерн-блот анализ транскрипции биомаркера в образце опухолевых клеток. Нозерн-анализ представляет собой стандартный способ детекции и/или количественного определения уровней мРНК в образце. Сначала РНК выделяют из образца, который анализируют методом Нозерн-блоттинга. В этом анализе образцы РНК сначала разделяют по размеру при помощи электрофореза в агарозном геле в денатурирующих условиях. РНК затем переносят на мембрану, подвергают сшивке и гибридизации с меченым зондом. Как правило, нозерн гибридизация включает полимеризацию меченной радиоактивным изотопом или не-изотопно меченной ДНК in vitro или образование олигонуклеотидов в виде гибридизационных зондов. Как правило, мембрану, удерживающую РНК образец, предварительно гибридизуют или блокируют до гибридизации с зондом, чтобы предотвратить покрытие мембраны зондом и, таким образом, уменьшить неспецифический фоновый сигнал. После гибридизации, как правило, негибридизованный зонд удаляют путем промывки с несколькими заменами буфера. Жесткость условий промывки и гибридизации может рассчитать, выбрать и осуществить любой средний специалист в данной области. Детекцию осуществляют с использованием обнаруживаемо-меченных зондов и подходящего способа детекции. Радиоактивно меченные и не-радиоактивно меченные зонды и их использование хорошо известны из уровня техники. Присутствие и/или относительные уровни экспрессии биомаркера, который анализируют, можно определить количественно с использованием, например, денситометри.
В другом варианте осуществления настоящего изобретения статус экспрессии и/или мутационный статус биомаркера определяют с использованием ОТ-ПЦР. ОТ-ПЦР обеспечивает возможность детекции развития ПЦР амплификации целевого гена в режиме реального времени. Конструирование праймеров и зондов, необходимых для определения статуса экспрессии и/или мутационного статуса биомаркера по настоящему изобретению, сможет осуществить средний специалист в данной области на основании своих профессиональных знаний. ОТ-ПЦР можно использовать для определения уровня РНК, кодирующей биомаркер по настоящему изобретению в образце опухолевой ткани. В одном из вариантов осуществления настоящего изобртения РНК выделяют из биологического образца, в условиях отсутствия РНКазы, затем преобразовывают в ДНК путем обработки обратной транскриптазой. Способы преобразования РНК в ДНК при помощи обратной транскриптазы хорошо известны из уровня техники. Описание ПЦР представлено в следующих ссылочных документах: Mullis et al., Cold Spring Harbor Symp. Quant. Biol. 51:263 (1986); EP 50,424; EP 84,796; EP 258,017; EP 237,362; EP 201,184; Патенты США №№.4683202; 4582788; 4683194.
ОТ-ПЦР зонды зависят от 5'-3' нуклеазной активности ДНК полимеразы, используемой для ПЦР для гидролиза олигонуклеотида, который гибридизуется с целевым ампликоном (биомаркерный ген). ОТ-ПЦР зонды представляют собой олигонуклеотиды, которые содержат флуоресцентнный репортерный краситель, присоединенный к 5' концу, и гасящий фрагмент, связанный с 3' концом (или наоборот). Эти зонды сконструированы для гибридизации с внутренней областью ПЦР продукта. В негибридизованном состоянии близость флуорофора и гасящих молекул препятствует детекции флуоресцентного сигнала от зонда. При ПЦР амплификации, когда полимераза реплицирует матрицу, на которой связан ОТ-ПЦР зонд, 5'-3' нуклеазная активность полимеразы расщепляет зонд. Это отделяет флуоресцентные и гасящие красители, и FRET больше не происходит. Таким образом, флуоресценция увеличивается в каждом цикле пропорционально количеству расщепления зонда. Сигнал флуоресценции, исходящий из реакции, можно измерить или отслеживать в течение некоторого времени с использованием оборудования, которое коммерчески доступно, рутинными и традиционными методами.
В другом варианте осуществления настоящего изобретения экспрессию белков, кодируемых биомаркерами, определяют при помощи вестерн-блот анализа. Вестерн-блоттинг (также известный как иммуноблоттинг) представляет собой способ определения белка в данном образце тканевого гомогената или экстракта. В этом методе используют гель-электрофорез для разделения денатурированных белков по массе. Белки затем переносят из геля на мембрану (например, нитроцеллюлозную или из поливинилиденфторида (PVDF)), где осуществляют их детекцию с использованием первичного антитела, которое специфически связывается с белком. Связанное антитело затем можно определить при помощи вторичного антитела, которое конъюгировано с детектируемой меткой (например, биотин, пероксидаза хрена или щелочная фосфатаза). Детекция сигнала вторичной метки указывает на присутствие белка.
В другом варианте осуществления настоящего изобретения экспрессию белка, кодируемого биомаркером, определяют при помощи твердофазного имменоферментного анализа (ELISA). В одном из вариантов осуществления настоящего изобретения "сэндвич-метод" ELISA включает покрытие планшета иммобилизованным антителом; добавление образца, в котором любой присутствующий антиген связывается с иммобилизованным антителом; добавление детекторного антитела, которое также связывается с антигеном; добавление связанного с ферментом вторичного антитела, которое связывается с детекторным антителом; и добавление субстрата, который преобразуется ферментом на вторичном антителе в детектируемую форму. Детекция сигнала от вторичного антитела указывает на присутствие биомаркерного антигенного белка.
В другом варианте осуществления настоящего изобретения экспрессию биомаркера оценивают с испоьзованием генного чипа или микрочипа. Такие методы хорошо известны средним специалистам в данной области.
VI. Определения
В настоящем изобретении представлены различные терапевтические способы, наборы и фармацевтические композиции, включающие TG02. Термин "TG02" в контексте настоящей заявки относится к (16E)-14-метил-20-окса-5,7,14,26-тетраазатетрацикло[19.3.1.1(2,6).1(8,12)]гептакоза-1(25),2(26),3,5,8(27),9,11,16,21,23-декаену в любой кристаллической или аморфной форме в виде свободного основания или в виде фармацевтически приемлемой соли или сольвата. В одном из вариантов осуществления TG02 относится к свободному основанию (16E)-14-метил-20-окса-5,7,14,26-тетраазатетрацикло[19.3.1.1(2,6).1(8,12)]гептакоза-1(25),2(26),3,5,8(27),9,11,16,21,23-декаена. В другом варианте осуществления TG02 относится к фармацевтически приемлемой соли (16E)-14-метил-20-окса-5,7,14,26-тетраазатетрацикло[19.3.1.1(2,6).1(8,12)]гептакоза-1(25),2(26),3,5,8(27),9,11,16,21,23-декаена. Фармацевтически приемлемую соль TG02 можно получить в процессе конечного выделения и очистки TG02 или отдельно путем взаимодействия TG02 с фармацевтически приемлемыми кислотами. Примеры кислот, которые можно использовать для получения фармацевтически приемлемых солей, включают неорганические кислоты, такие как азотная, борная, хлористоводородная, бромистоводородная, серная и фосфорная, и органические кислоты, такие как щавелевая, малеиновая, янтарная и лимонная. Неограничивающие примеры солей TG02 включают, но не ограничиваются этим, гидрохлорид, гидробромид, гидроиодид, сульфат, бисульфат, 2-гидроксиэтансульфонат, фосфат, гидрофосфат, ацетат, адипат, альгинат, аспартат, бензоат, бисульфат, бутират, камфорат, камфорсульфонат, диглюконат, глицеролсульфат, гемисульфат, гептаноат, гексаноат, формиат, сукцинат, фумарат, малеат, аскорбат, изетионат, салицилат, метансульфонат, мезитиленсульфонат, нафтиленсульфонат, никотинат, 2-нафталинсульфонат, оксалат, памоат, пектинат, персульфат, 3 фенилпропионат, пикрат, пивалат, пропионат, трихлорацетат, трифторацетат, фосфат, глутамат, бикарбонат, пара-толуолсульфонат, ундеканоат, лактат, цитрат, тартрат, глюконат, метансульфонат, этандисульфонат, бензолсульфонат и п-толуолсульфонат.
В другом варианте осуществления TG02 относится к цитратной соли (16E)-14-метил-20-окса-5,7,14,26-тетраазатетрацикло[19.3.1.1(2,6).1(8,12)]гептакоза-1(25),2(26),3,5,8(27),9,11,16,21,23-декаена. Она указана как TG02 цитрат или (16E)-14-метил-20-окса-5,7,14,26-тетраазатетрацикло[19.3.1.1(2,6).1(8,12)]гептакоза-1(25),2(26),3,5,8(27),9,11,16,21,23-декаен - лимонная кислота.
Термин "биологический образец" в контексте настоящей заявки относится к любой ткани или жидкости от пациента, которая является подходящей для детекци биомаркера, такого как статус экспрессии MYC и/или MCL1. Примеры полезных биологических образцов включают, но не ограничиваются этим, полученные путем биопсии образцы ткани и/или клетки, например, солидной опухоли, лимфатической железы, воспаленной ткани, ткани и/или клеток, вовлеченных в состояние или заболевание, крови, плазмы, серозной жидкости, слюны, мочи, лимфы, цереброспинальной жидкости и т.п. Другие подходящие биологические образцы будут хорошо известны специалистам в соответствующих областях. Биологический образец можно анализировать на экспрессию и/или мутацию биомаркера с использованием любого метода, известного в данной области, и его можно получить с использованием методов, которые должны быть хорошо известны клиницистам. В одном из вариантов осуществления изобретения биологический образец включает клетки крови.
Указание диапазонов значений просто предназначено для использования в качестве сокращенного метода индивидуальной ссылки на каждое отдельное значение, попадающее в диапазон, если не указано иное, и каждое отдельное значение включено в описание, как если бы оно было индивидуально указано в настоящем описании. Использование любых примеров или выражений, например, «такой как», приведенных в настоящей заявке, предназначено для лучшей иллюстрации раскрытия и не является ограничением объема раскрытия, если не заявлено иное. Никакие фразы в настоящем описании не должны быть истолкованы как указание любого не заявленного элемента как существенного для осуществления на практике настоящего изобретения.
Термин "около" в контексте настоящей заявки включает указанное число ±10%. Таким образом, "около 10" означает от 9 до 11.
Как используется в настоящей заявке, термины "лечить", "лечение", "лечащий" и т.п. относятся к устранению, уменьшению тяжестви или облегчению заболевания или состояния и/или симптомов, связанных с ним. Хотя это не исключено, лечение заболевания или состояния не требует полного устранения заболевания, состояния или симптомов, связанных с ним. Однако В одном из вариантов осуществления введение TG02 и/или ингибитора иммунных контрольных точек и/или ингибитора СОХ-2 приводит к полной ремиссии рака.
Термин "терапевтически эффективное количество", как он используется в настоящей заявке, относится к такому количеству терапевтического средства, которое достаточно для улучшения одного или нескольких симптомов расстройства или предотвращения развития расстройства или которое вызывает регрессию расстройства. Например, в отношении лечения рака, В одном из вариантов осуществления терапевтически эффективное количество будет относиться к количеству терапевтического средства, которое вызывает терапевтический ответ, например, нормализацию анализа крови, снижение скорости роста опухоли, уменьшение массы опухоли, уменьшении числа метастазов, увеличение времени до прогрессирования опухоли и/или увеличении времени выживания пациентов на по меньшей мере около 2%, по меньшей мере около 5%, по меньшей мере около 10%, по меньшей мере около 15%, по меньшей мере около 20%, по меньшей мере около 25%, по меньшей мере около 30%, по меньшей мере около 35%, по меньшей мере около 40%, по меньшей мере около 45%, по меньшей мере около 50%, по меньшей мере около 55%, по меньшей мере около 60%, по меньшей мере около 65%, по меньшей мере около 70%, по меньшей мере около 75%, по меньшей мере около 80%, по меньшей мере около 85%, по меньшей мере около 90%, по меньшей мере около 95% или по меньшей мере около 100% или больше.
Термин "фармацевтически приемлемый носитель" или "фармацевтически приемлемый наполнитель" охватывает любой из стандартных фармацевтических носителей, растворителей, поверхностно-активных веществ или наполнителей. Подходящие фармацевтически приемлемые носители включают водные носители и не-водные носители. Стандартные фармацевтические носители и их композиции описаны в Remington's Pharmaceutical Sciences, Mack Publishing Co., Easton, PA, 19th ed. 1995.
Термин "контейнер" означает любую закрываемую емкость и поэтому является подходящим для хранения, транспортирования, распределения фармацевтического продукта и/или обращения с ним.
Термин "инструкция по применению" означает информацию, прилагаемую к фармацевтическому продукту, содержащую описание, как вводить продукт, вместе с данными по безопасности и эффективности, которые необходимы, чтобы позволить лечащему врачу, фармацевту и пациенту принять обоснованное решение относительно использования продукта. Содержащуюся в упаковке инструкцию обычно рассматривают как "этикетку" для фармацевтического продукта.
"Параллельное введение", "вводимые в комбинации", "одновременное введение" и аналогичные фразы означают, что одновременно два или более средства вводят одновременно субъекту, принимающему лечение. Под "параллельно" подразумевается, что каждое средство вводят либо одновременно, либо последовательно в любом порядке в разные моменты времени. Однако, если они не вводятся одновременно, подразумевается, что они вводятся субъекту последовательно и достаточно близко по времени, чтобы обеспечить желаемый терапевтический эффект, и могут действовать сообща. Например, TG02 можно вводить одновременно или последовательно в любом порядке в разных точках времени с ингибитором контрольных точек иммунного ответа и/или ингибитором COX-2 и/или необязательным терапевтическим средством. TG02 и ингибитор контрольных точек иммунного ответа и/или ингибитор COX-2 и/или необязательное терапевтическое средство можно вводить раздельно, в любой подходящей форме и любым подходящим путем. Когда TG02 и ингибитор контрольных точек иммунного ответа и/или ингибитор COX-2 и/или необязательное терапевтическое средство вводят не одновременно, должно быть понятно, что их можно вводить в любом порядке пациенту, нуждающемуся в этом. Например, TG02 можно вводить до (например, за 5 минут, 15 минут, 30 минут, 45 минут, 1 час, 2 часа, 4 часа, 6 часов, 12 часов, 24 часа, 48 часов, 72 часа, 96 часов, 1 неделю, 2 недели, 3 недели, 4 недели, 5 недель, 6 недель, 8 недель или 12 недель до), одновременно с, или после (например, через 5 минут, 15 минут, 30 минут, 45 минут, 1 час, 2 часа, 4 часа, 6 часов, 12 часов, 24 часа, 48 часов, 72 часа, 96 часов, 1 неделю, 2 недели, 3 недели, 4 недели, 5 недель, 6 недель, 8 недель или 12 недель после) ингибитора контрольных точек иммунного ответа и/или ингибитора COX-2 субъекту, нуждающемуся в этом. В различных вариантах осуществления TG02 и ингибитор контрольных точек иммунного ответа и/или ингибитор COX-2 вводят с интервалом 1 минута, с интервалом 10 минут, с интервалом 30 минут, с интервалом меньше чем 1 час, с интервалом 1 час, с интервалом 1 час - 2 часа, с интервалом 2 часа - 3 часа, с интервалом 3 часа - 4 часа, с интервалом 4 часа - 5 часов, с интервалом 5 часов - 6 часов, с интервалом 6 часов - 7 часов, с интервалом 7 часов - 8 часов, с интервалом 8 часов - 9 часов, с интервалом 9 часов - 10 часов, с интервалом 10 часов - 11 часов, с интервалом 11 часов - 12 часов, с интервалом не больше чем 24 часа apart или с интервалом не больше чем 48 часов. В одном из вариантов осуществления компоненты комбинированной терапии вводят с интервалом от около 1 минуты до около 24 часов. В одном из вариантов осуществления TG02 вводят за 3-7 дней до дня введения ингибитора контрольных точек иммунного ответа. В другом варианте осуществления TG02 также вводят в день введения ингибитора контрольных точек иммунного ответа и продолжают введение до тех пор, пока заболевание не начнет прогрессировать, или до тех пор, пока TG02 терапия больше не будет приносить пользу.
ПРИМЕРЫ
ПРИМЕР 1
Это исследование осуществляют для сравнения выживаемости без прогрессирования заболевания или общей выживаемости с использованием пембролизумаба (p) или ниволумаба (n) с p или n в комбинации с TG02 для участников с раком, которые не принимали лечение или у которых было прогрессирование после предшествующей терапии и которые были выбраны как имеющие статус сверхэкспрессии MYC и/или MCL1. Участников будут рандомизировать в группы приема либо стандартной анти-PD-1 терапии плюс плацебо, либо стандартной анти-PD-1 терапии плюс TG02.
Первичные критерии эффективности: Выживаемость без прогрессирования заболевания (PFS) и/или общая выживаемость (OS)
Вторичные критерии эффективности: общая частота ответа (ORR) и/или продолжительность ответа
Право на участие
Возраст, подходящий для участия в исследовании: Обычно - 18 лет и старше. Для пациентов с медуллобластомой - 6 месяцев или старше
Пол, подходящий для участия в исследовании: оба
Критерии включения:
Гистологически или цитологически подтвержденный диагноз рака, который не лечится локальной терапией
Должны дать согласие на сравнительные исследования; должны обеспечить недавно полученный образец ткани/биопсии (или образец, полученный в течение 60 дней после согласия)
Радиографически измеряемое заболевание
Оценка общего состояния больного по шкале ECOG (Восточная бъединенная онколоническая группа) 0 или 1
Пациент имеет заболевание со сверхэкспрессируемым MYC и/или MCL1
Критерии исключения:
Химиотерапия, лучевая терапия или биологическая терапия в течение четырех недель до первой дозы исследуемого лекарственного средства, или не восстановились от AEs в результате противораковой терапии, введенной больше чем за четыре недели до начала исследования
Участвует или участвовал в исследовании экспериментального препарата или использует экспериментальное устройство в течение 30 дней до первой дозы исследуемого лекарственного средства
Ожидается, что во время исследования потребуется любая другая форма системной или локализованной противоопухолевой терапии
Хроническая системная терапия стероидами в течение двух недель до запланированной даты первой дозы рандомизированного лечения, или любая другая форма лечения иммунодепрессантами
Известная история любого другого, кроме текущего, злокачественного новообразования, за исключением адекватно пролеченной карциномы базально- или плоскоклеточной карциномы кожи, поверхностного рака мочевого пузыря, рака шейки матки in situ, рака молочной железы или других злокачественных опухолей in situ
Известные активные метастазы в центральной нервной системе (ЦНС) и/или карциноматозный менингит
Активное аутоиммунное заболевание или документально подтвержденная история аутоиммунного заболевания или синдрома, требующих системного лечения стероидами или иммунодепрессантами
Предшествующее лечение любым другим средством против запрограммированной клеточной гибели (PD)
Активная инфекция, требующая системной терапии
Известная история вируса иммунодефицита человека (ВИЧ)
Активный Гепатит B или Гепатит C
Регулярно использует (включая использование в рекреационных целях) запрещенные лекарственные средства или имел недавнюю историю (в течение последнего года) злоупотребления запрещенными веществами (включая алкоголь)
Беременная или кормящая женщина, или предполагающая беременность и роды, в течение планируемого срока исследования.
Протоколы:
Первая группа пациентов получает 2-10 мг/кг пембролизумаб (или эквивалент базовой дозы), вводимый путем внутривенной инфузии один раз каждые три недели, и TG02, вводимый перорально при 100, 200 или 300 мг один раз ежедневно до тех пор, пока заболевание не начнет прогрессировать, или до тех пор, пока больше не будет приносить пользу. Введение TG02 начинают за 3-7 дней до начала лечения пембролизумабом, продолжают в день введения пембролизумаба и продолжают до тех пор, пока заболевание не начнет прогрессировать, или до тех пор, пока TG02 терапия больше не будет приносить пользу. Контрольные пациенты получают 2-10 мг/кг пембролизумаба (или эквивалент базовой дозы), вводимого путем внутривенной инфузии один раз каждые три недели.
Вторая группа пациентов получает 3 мг/кг ниволумаба, вводимого в течение 60 минут путем внутривенной инфузии каждые 2 недели, и TG02, вводимый перорально при 100, 200 или 300 мг один раз ежедневно. Введение TG02 начинают за 3-7 дней до начала лечения ниволумабом, продолжают в день введения ниволумаба и продолжают до тех пор, пока заболевание не начнет прогрессировать, или до тех пор, пока TG02 терапия больше не будет приносить пользу. Контрольные пациенты получают 3 мг/кг ниволумаба, вводимого в течение 60 минут путем внутривенной инфузии каждые 2 недели.
Результаты:
TG02 в комбинации с пембролизумабом или ниволумабом приводит к лучшей противоопухолевой клинической активности по сравнению с ингибиторами контрольных точек иммунного ответа отдельно у пациентов, у которых опухоли сверхэкспрессируют MYC и/или MCL1. Получают неожиданные объективные ответы, связанные с отсутствием прогрессирования опухоли и продлением срока длительного выживания по сравнению с историческими контролями с использованием (антитела) отдельно. В одном из вариантов осуществления пациенты, принимающие TG02 и ингибитор контрольных точек иммунного ответа, достигают продления времени до прогрессирования (или выживаемости без прогрессирования заболевания) по меньшей мере на 2 месяца, по меньшей мере на 4 месяца, по меньшей мере на 6 месяцев, по меньшей мере на 8 месяцев, по меньшей мере на 10 месяцев или по меньшей мере на 12 месяцев. В другом варианте осуществления по меньшей мере некоторые пациенты, принимающие TG02 и ингибитор контрольных точек иммунного ответа, достигают продления длительности ответа по меньшей мере на 2 месяца, по меньшей мере на 4 месяца, по меньшей мере на 6 месяцев, по меньшей мере на 8 месяцев, по меньшей мере на 10 месяцев или по меньшей мере на 12 месяцев.
ПРИМЕР 2
Фаза 2 открытого исследования, оценивающего комбинацию иммунотерапии, блокирующей контрольные точки, и TG02 у пациентов, имеющих рецидив или резистентных к стандартой анти-PD-1 терапи (p) или (n).
Первичная конечная точка: ORR
Вторичные конечные точки: PFS, OS, продолжительность ответа, безопасность
Критерии включения:
Гистологически подтвержденный диагноз рака, который не лечится локальной терапией
Оценка общего состояния больного по шкале ECOG (Восточная объединенная онколоническая группа) 0 или 1
По меньшей мере одно измеряемое поражение
Адекватная функция органов
Предшествующая терапия с использованием анти-PD-1 или анти-PD-L1 антитела
Пациент имеет заболевание со сверхэкспрессируемым MYC и/или MCL1
Критерии исключения:
Химиотерапия, таргетная низкомолекулкулярная терапия, радиотерапия или биологическая терапия рака (включая моноклональные антитела) в течение 4 недель до первой дозы испытываемого лечения, или не восстановился (<= Степень 1 или базовый уровень) от нежелательных явлений из-за ранее вводимого средства.
Ожидается, что во время исследования потребуется любая другая форма системной или локализованной противоопухолевой терапии.
Известные активные метастазы в центральной нервной системе (ЦНС) и/или карциноматозный менингит.
Документально подтвержденная история клинически тяжелого аутоиммунного заболевания или синдрома, требующих системного лечения стероидами или иммунодепрессантами.
Принимает системную стероидную терапию или любую другую форму иммуносупрессивной терапии в течение 1 недели до первой дозы исследуемого лечения.
Принимал живую вакцину в течение 4 недель до первой дозы испытываемого лечения.
История или подтверждение активного пневмонита.
Вирус иммунодефицита человека (ВИЧ)-положительный.
Активный гепатит B или C.
Беременная или кормящая женщина или предполагающая забеременеть или рожать детей в течение планируемого срока исследования вплоть до 120 дней после последней дозы исследуемого лечения.
Протокол дозирования:
Дозы & Схемы введения
*TG02 вводят еженедельно (50-400 мг), начиная по меньшей мере за 5 дней до начала лечения ингибитором контрольных точек терапии и продолжая до тех пор, пока заболевание не начнет прогрессировать, или решения исследователя
Результаты
Комбинирование TG02 с по меньшей мере одним ингибитором контрольных точек у пациентов с опухолями, сверхэкспрессирующими MYC и/или MCL1, задает обратный ход иммунной эфазии и индуцирует клинически релевантные ответы у пациентов, ранее не отвечавших на терапию ингибитором контрольных точек или не получавшим от нее пользы, или у de novo раковых пациентов. Получают неожиданные объективные ответы, связанные с отсутствием прогрессирования опухоли и продлением срока длительного выживания по сравнению с историческими контролями с использованием (антитело) отдельно. В одном из вариантов осуществления пациенты, принимающие TG02 и по меньшей мере один ингибитор контрольных точек иммунного ответа, достигают продления времени до прогрессирования (или выживаемости без прогрессирования заболевания) по меньшей мере на 2 месяца, по меньшей мере на 4 месяца, по меньшей мере на 6 месяцев, по меньшей мере на 8 месяцев, по меньшей мере на 10 месяцев или по меньшей мере на 12 месяцев. В другом варианте осуществления по меньшей мере некоторые пациенты, принимающие TG02 и по меньшей мере один ингибитор контрольных точек иммунного ответа, достигают продления длительности ответа по меньшей мере на 2 месяца, по меньшей мере на 4 месяца, по меньшей мере на 6 месяцев, по меньшей мере на 8 месяцев, по меньшей мере на 10 месяцев или по меньшей мере на 12 месяцев.
ПРИМЕР 3
Фаза 2 плацебо-контролируемого рандомизированного исследования пембролизумаб + TG02 vs. пембролизумаб + плацебо у участников с ранее леченным местно распространенным неоперабельным или метастатическим колоректальным раком, демонстрирующим статус сверхэкспрессии MYC и/или MCL1.
Первичная конечная точка: PFS
Вторичная конечная точка: ORR, продолжительность ответа
Критерии включения:
Гистологически подтвержденный местно распространенная неоперабельная или метастатическая колоректальная карцинома высокой степени
Ранее леченная с использованием по меньшей мере двух линий одобренной стандартной терапии, которые должны включать фторпиримидин, оксалиплатин, иринотекан, бевацизумаб и цетуксимаб или панитумумаб
Оценка общего состояния больного по шкале ECOG (Восточная объединенная онколоническая группа) 0 или 1
Пациент имеет заболевание со сверхэкспрессируемым MYC и/или MCL1
Ожидаемая продолжительность жизни больше 3 месяцев
По меньшей мере одно измеряемое поражение
Участники женского пола с потенциалом деторождения должны быть готовы использовать 2 метода контрацепции или быть хирургически стерильными или воздерживаться от гетеросексуальной активности на протяжении исследования вплоть до 120 дней после последней дозы исследуемого лечения.
Участники мужского пола должны согласиться использовать адекватный метод контрацепции, начиная с первой дозы исследуемой терапии, вплоть до 120 дней после последней дозы исследуемого лечения.
Адекватная функция органов
Критерии исключения:
Участвует в это время в другом исследовании и принимает испытываемое лечение, участвовал в исследовании экспериментального препарата и получал испытываемое лечение в течение 4 недель до первой дозы лекарственного средства в этом исследовании или использовал экспериментальное устройство в течение 4 недель до первой дозы лекарственного средства в этом исследовании
Активное аутоиммунное заболевание, для которого потребовалось системное лечение в последние 2 года
Диагноз иммунодефицита, или принимает системнную стероидную терапию или любую другую форму иммуносупрессивной терапии в течение 7 дней до первой дозы исследуемого лечения
Известные активные метастазы в центральной нервной системе (ЦНС) и/или карциноматозный менингит
Предшествующее лечение с использованием моноклонального антитела(mAb), химиотерапии, таргетной низкомолекулкулярной терапии или лучевой терапии в течение 2 недель до дня 1 исследования, или не восстановился (т.е. ≤ Степень 1 или на базовом уровне) от нежелательных явлений из-за ранее вводимого средства
Предшествующая терапия с использованием средства против запрограммированной клеточной гибели (PD)-1, анти-PD-L1 или анти-PD-L2, или участник ранее участвовал в клиническом испытании пембролизумаба (MK-3475) Merck
Известное дополнительное злокачественное заболевание, которое прогрессирует или требует активного лечения, за исключением адекватно пролеченной карциномы базальноклеточной карциномы кожи или плоскоклеточной карциномы кожи, которая подвергалась потенциально радикалному лечению, или рака шейки матки in situ
Принимал живую вакцину в течение 30 дней до запланированного начала исследуемого лечения
Известная история вируса иммунодефицита человека (ВИЧ)
Известный активный гепатит B или C
Известная история или любое подтверждение интерстициального легочного заболевания или активного неинфекционного пневмонита
Активная инфекция, требующая системн терапи
Известные психиатрические расстройства или злоупотребление запрещенными веществами, которые могут помешать соблюдению требований испытания
Беременная или кормящая женщина или предполагающая забеременеть или рожать детей в течение планируемого срока исследования, начиная со скринингового визита вплоть до 120 дней после последней дозы испытываемого лечения
Протокол дозирования:
Пациенты получают 2-10 мг/кг пембролизумаба, вводимого путем внутривенной инфузии один раз каждые три недели, и TG02, вводимого перорально при 1, 2 или 3 мг/кг за 3-7 дней до введения пембролизумаба, в день введения пембролизумаба и непрерывно после этого до тех пор, пока заболевание не начнет прогрессировать, или до тех пор, пока это больше не будет приносить пользу. Контрольные пациенты получают 2 мг/кг пембролизумаба, вводимого путем внутривенной инфузии один раз каждые три недели.
Результаты:
При использовании для пациентов с опухолями, сверхэкспрессирующими MYC и/или MCL1, TG02 в комбинации с пембролизумабом обеспечивает более высокую клиническую активность, чем пембролизумаб отдельно у этих же пациентов. Получают неожиданные объективные ответы у пациентов, связанные с отсутствием прогрессирования опухоли и продлением срока длительного выживания по сравнению с историческими контролями с использованием (антитело) отдельно. В одном из вариантов осуществления пациенты, принимающие TG02 и пембролизумаб, достигают продления времени до прогрессирования (или выживаемости без прогрессирования заболевания) по меньшей мере на 2 месяца, по меньшей мере на 4 месяца, по меньшей мере на 6 месяцев, по меньшей мере на 8 месяцев, по меньшей мере на 10 месяцев или по меньшей мере на 12 месяцев. В другом варианте осуществления по меньшей мере некоторые пациенты, принимающие TG02 и пембролизумаб, достигают продления длительности ответа по меньшей мере на 2 месяца, по меньшей мере на 4 месяца, по меньшей мере на 6 месяцев, по меньшей мере на 8 месяцев, по меньшей мере на 10 месяцев или по меньшей мере на 12 месяцев.
ПРИМЕР 4
TG02 в комбинации с карфилзомибом у пациентов с карфилзомиб (CFZ)-резистентной множественной миеломой (MM)
Способы
Фаза 1b открытого исследования, включающего MM пациентов, которые ранее получали ≥2 линии терапии. Первичной целью было определение максимально переносимой дозы (MTD) TG02 в комбинации с карфилзомибом (TG02/CFZ). Вторичные цели включали оценку противоопухолевой активности и безопасности. TG02 вводили один раз в день в дни 1, 4, 8, 11, 15, 18 28-дневного режима (BIW). Начальная доза TG02 была 150 мг. Дозу TG02 наращивали с 50 мг приращениями до 300 мг. CFZ дозировали в соответствии с инструкцией по применению препарата. Ответы оценивали с использованием стандартных критериев.
Результаты
Четырнадцать пациентов были отобраны для повышения дозы, и 10 пациентов были отобраны для расширения MTD когорты. Пациентов предварительно интенсивно лечили: в среднем 6 предыдущих лечений [мин. 3; макс. 15], и 92% пациентов получали CFZ в предыдущем режиме. Наилучшим ответом на предыдущую терапию было прогрессирующее заболевание у 46% пациентов. MTD составляла 250 мг TG02 в комбинации с CFZ. Наблюдали два случая дозо-ограничивающей токсичности (включая Степень (Gr) 4 сепсиса и Gr 4 нейтропения), оба в 300 мг когорте. Наиболее типичными связанными с лекарственным средством нежелательными явлениями (AEs) были диарея (Gr 1-2: 71% Gr 3: 17%), тошнота (Gr 1-2: 79%), рвота (Gr 1-2: 50%), слабость (Gr 1-2: 38%, Gr 3: 4%), анорексия (Gr 1: 21%), анемия (Gr 1-2: 4%, Gr 3: 17%) и тромбоцитопения (Gr 3: 8%, Gr 4: 13%). Шесть пациентов(25%) прекратили лечение из-за AE. Серьезные AE были у 50% пациентов; только остая почечная недостаточность и фебрильная нейтропения были у >1 пациента (8% каждая). Тяжесть AE была такой же, как при отдельном введении TG02. Случаев диареи было больше при TG02/CFZ введении (88% vs 67%), но число случаев других AE было таким же, как при отдельном введении TG02. Четырнадцать пациентов, которым вводили TG02 при MTD, оценивали на их ответ. Общая частота ответа (≥PR) составила 27%; уровень клинической пользы (≥MR) составил 45% (1 очень хороший частичный ответ, 2 частичный ответ и 2 минимальный ответ). Все отвечающие на лечение (MR или лучше) были CFZ-резистентыми в предыдущем режиме лечения. Продолжительное стабильное заболевание наблюдали у 27% пациентов.
Заключение
Профиль безопасности TG02 BIW/CFZ был таким же, как для TG02 отдельно. Наиболее типичными AE, связанными с лекарственным средством, были диарея, тошнота и рвота; AE 4 степени были нечастыми. Объективные ответы наблюдали у CFZ-резистентных пациентов.
ПРИМЕР 5
Активность TG02 в клетках глиомы и модели аллотрасплантата
Несколько стандартных клеточных линий мультиформной глиобластомы (GBM) и одну стволовую клеточную линию, экспрессирующую O6-метилгуанин ДНК метилтрансферазу (МГМТ), обрабатывали TG02, темозоломидом (TMZ) или комбинацией TG02 и TMZ в 72-часовом анализе клеточной пролиферации. См. Фиг. 1-3. TG02, TMZ и комбинацию TG02+TMZ также испытывали в клеточных линиях без MGMT экспрессии. См. Фиг. 4-7. Клетки высевали в 12-луночные планшеты и обрабатывали при помощи 50 нМ TG02, 100 мкМ TMZ или TG02+TMZ в течение 72 часов. Жизнеспособность клеток определяли путем подсчета клеток.
Цитотоксический эффект TG02, TMZ и комбинации TG02 и TMZ исследовали при помощи анализа колониеобразования в GSC923 и U251 клетках. См. Фиг. 8 и 9.
Клетки эндотелия легочной артерии и человеческие астроциты испытывали с 50 нМ TG02, 100 мкМ TMZ или TG02+TMZ в течение 72 часов. Клетки затем переносили в нормальную среду и культивировали tit в течение 7 дней. Жизнеспособность клеток определяли путем подсчета клеток. См. Фиг. 10 и 11.
GSC923 (Фиг. 12 и 13) и U251 (Фиг. 14 и 15) клетки обрабатывали различными концентрациями TG02, TMZ и TG02+ TMZ в течение 72 часов и жизнеспособность клеток исследовали путем подсчета клеток. Синергический эффект TG02+TMZ определяли по показателю аддитивности (CI). CI значения рассчитывали с использованием программы COMPUSYN, и они показаны в Таблице 2 для GSC923 клеток и в Таблице 3 для U251 клеток. CI < 1 означает синергический эффект, CI=1 означает аддитивный эффект, и CI > 1 означает антагонистический эффект двух используемых в комбинации соединений.
Фиг. 16 представляет схематическую иллюстрацию введения лекарственного средства мышиной модели с аллотрансплантатом клеток глиомы GL261. Клетки мышиной глиомы GL261 вводили путем стереотаксической инъекции в полосатое тело самкам C57BL/6 мышей альбиносов (n=5-7 на когорту), затем вводили носитель, TG02, TMZ и TG02+TMZ комбинированное лечение. Наблюдали среднюю общую выживаемость 24, 24,5, 27,5 и 32 дня, соответственно. См. Фиг. 17. Результат анализировали с использованием логрангового критерия в программе GraphPad Prism (хи-квадрат = 9,063, df=1, P значение = 0,0026 **). Опухолевую нагрузку определяли методом биолюминесцентной визуализации (BLI) с использованием PerkinElmer IVIS® Spectrum. Интенсивность BLI рассчитывали и нормализовали к исходной интенсивности в день 5. См. Фиг. 18.
ПРИМЕР 6
Активность TG02 в клетках гепатоцеллюлярной карциномы (HCC) и модели ксенотрансплантата
Исследовали влияние TG02 на экспрессию MYC в HCC клеточных линиях. Пять HCC клеточных линий с разными уровнями MYC экспрессии обрабатывали при помощи 0,5 мкМ TG02 в течение 24 часов и экспрессию MYC оценивали методом вестерн-блоттинга. См. Фиг. 19. Уровни MYC экспрессии уменьшались при TG02 обработке в HepG2, SNU398 и HUH-1 клеточных линиях, но не в JHH-5 линии. Hep3B клетки не экспрессировали MYC.
Восемь HCC клеточных линий либо с высокой, либо с низкой экспрессией MYC затем обрабатывали при помощи TG02 in vitro. TG02 обработка приводила к ингибированию клеточной пролиферации во всех испытываемых HCC клеточных линиях. TG02 является селективно более эффективным в клеточных линиях с высокими уровнями MYC экспрессии по сравнению с клетками с низкими уровнями MYC экспрессии, при средних IC50 значениях 84 нМ и 524 нМ, соответственно. См. Фиг. 20.
Ингибирование MYC экспрессии также измеряли in vivo. Ксенотрансплантаты HepG2 гепатоцеллюлярной карциномы выращивали ортотопически у Balb/c бестимусных мышей. TG02 или носитель вводили перорально каждый при 50 мг/кг 5 мышам; опухоли собирали через 8 часов после обработки и уровни экспрессии MYC белка измеряли методом вестерн-блоттинга. MYC экспрессию наблюдали в каждой из контрольных опухолей. В группе TG02 обработки уровни экспрессии MYC уменьшались у 4 из 5 животных, с существенным истощением MYC у двух животных и частичным уменьшением у двух других животных. См. Фиг. 21.
Терапевтическую эффективность TG02 как отдельного средства или в комбинации с сорафенибом в лечении с использованием модели ксенотрансплантата ортотопического HepG2 рака печени человека оценивали у BALB/c бестимусных мышей. В день 19 после инокуляции мышей рандомизировали в группы лечения в соответствии с базовыми уровнями AFP в сыворотке, на основании которых прослеживают объем опухоли в печени. TG02 вводили перорально два раза в неделю при 50 мг/кг и дозу уменьшали до 40 мг/кг. Сорафениб вводили перорально ежедневно при 15 мг/кг. TG02 как отдельное средство имел незначительный эффект на объем опухоли. TG02 в комбинации с сорафенибом приводил к существенной пртивоопухолевой активности. См. Фиг. 22.
ПРИМЕР 7
TG02-опосредованное ингибирование CDK9
Использовали Tet-off трансгенную мышиную модель MYC-индуцированного острого Т-клеточного лимфобластного лейкоза (MYC T-ALL), который сверхэеспрессирует и является зависимым от MYC, для введения TG02 при 100 или 500 мкМ.
MYC представляет собой транскрипционный фактор, который регулирует экспрессию множества генных продуктов, вовлеченных в клеточную пролиферацию, рост, дифференциацию и апоптоз. MYC ген генетически активируется и сверхэкспрессируется во многих типах рака человека, и эта сверхэкспрессия причинно связана с онкогенезом, стимулированием злокачественного роста и иммунной эфазией. См., например, Álvarez-Fernández et al., Clin. Cancer Res. Off. J. Am. Assoc. Cancer Res. 19:2677-2687 (2013); Carter et al., Blood 105:4043-4050 (2005); Casey et al., Science 352:227-231 (2016); Hannah, A.L., Curr. Mol. Med. 5:625-642 (2005); и Parcells et al., Stem Cells Dayt. Ohio 24:1174-1184 (2006).
Как показано на Фиг. 23-26, когда MYC был "включен", PD-L1 экспрессировался, как было пределено при помощи ОТ-ПЦР (t=0 час.). Но когда MYC был "отключен", как CD47, так и PD-L1 экспрессия существенно снижалась зависимым от времени образом. TG02 приводил к время- и дозо-зависимой даунрегуляции экспрессии как PD-L1, так и CD47 мРНК в MYC T-ALL клетках (Фиг. 23 и 24, соответственно), и экспрессии как BCL-xL, так и MYC подавлялась (Фиг. 25 и 26, соответственно). Пониженная экспрессия CD47 и PD-L1 на опухолевых клетках может приводить к уменьшенной иммунной эфазии и повышенной гибели опухолевых клеток.
ПРИМЕР 8
TG02 в комбинации с анти-PD-1
Комбинацию TG02 и PD-1 mAb (анти-PD-1) испытывали в модели ортотопической GL261 глиомы. GL261 аллотрансплантаты устанавливали в течение 3 дней и мышей затем рандомизировали в 6 когорт лечения (n=8) на основании определенных биолюминесцентным методом объемов опухолей.
Мышей обрабатывали носителем, TG02 отдельно (20 или 40 мг/кг), PD-1 mAb отдельно (500 мкг) и комбинацией TG02 и анти-PD-1. Среднее время выживания мышей составляло 27,5, 26,5, 33, 32, 78 и >95 дней, соответственно (Фиг. 27).
Получали существенную пользу для выживания мышей, которых обрабатывали TG02 отдельно при 40 мг/кг (0,009), PD-1 mAb отдельно (0,003), TG02 20 мг/кг+PD-1 mAb (0,0001) и TG02 40 мг/кг+PD-1 mAb (0,0001), по сравнению с группой обработки носителем.
ПРИМЕР 9
TG02 индуцирует клеточную гибель и показывает синергизм с облучение в MYC-управляемой глиобластоме
Взаимосвязь между TG02 противоопухолевой активностью и MYC экспрессией исследовали в панели полученных от пациентов GBM клеточных линий (PDCL). TG02 ингибировал шесть из двенадцати PDCL при IC50 меньше чем 0,2 мкМ. См. Таблицу 4.
Даунрегуляцию MYC и Mcl-1 наблюдали в MYC-амплифицированной BT245 клеточной линии уже через 6 часов, тогда как полную даунрегуляцию наблюдали через 24 часа, что совпадало с существенным увеличением апоптоза (Фиг. 28). AUC TG02-индуцируемого ингибирования жизнеспособности клеток рассчитывали в этой панели клеточных линий для соотнесения с уровнями экспрессии MYC (Фиг. 29). TG02 был более сильным ингибитором PDCL, демонстрирующих высокую экспрессию MYC (Фиг. 30). Чувствительность in vitro (AUC) отрицательно коррелировала с MYC экспрессией в GBM клетках (P значение=0,02)
ПРИМЕР 10
Облучение является эффективным лечением для глиобластомы. Но резистентность опухоли и рецидив развиваются у всех пациентов.
Панель из GBM PDCLs, см. Пример 9, была выбрана для оценки комбинации TG02 и лучевой терапии для лечения глиобластомы (Фиг. 31). Клетки обрабатывали сначала при помощи TG02 при увеличивающихся концентрациях. В течение 30 минут клетки подвергали увеличивающимся дозам облучения и клеточную пролиферацию измеряли через 72 часа после обработки. TG02 отдельно имел антипролиферативную активность в этих клеточных линиях. Добавление TG02 синергически усиливало эффекты облучения. Комбинация TG02 и облучения превышает предсказанную Блиссом модель (изменение больше чем 10% от предсказанной Блиссом модели), демонстрируя синергизм между TG02 и облучением во многих PDCL.
ПРИМЕР 11
Активность TG02 коррелирует с экспрессией MYC в клеточных линиях глиобластомы
Действие TG02 на пролиферацию GBM стволовых клеток оценивали в панели из 26 полученных от пациентов GBM стволовых клеточных линий (Фиг. 32). TG02 был эффективным в этой панели, с достижением IC50 меньше чем 250 нМ в шестнадцати клеточных линиях.
Уровень экспрессии CDK9 и маркеров на пути ниже, включая MYC и Mcl-1, измеряли определения, существует ли корреляция между экспрессией белка и IC50 значениями в этой GBM панели. Было обнаружено, что экспрессия MYC коррелирует с большей чувствительностью к TG02 лечению (Фиг. 33).
Имея теперь полное описание способов, соединений и композиций, представленных в настоящей заявке, специалистам в данной области будет понятно, что это же можно осуществить в пределах широкого и эквивалентного диапазона условий, способов составления композиций и других параметров без изменения объема способов, соединений и композиций, представленных в настоящей заявке, или любого варианта их осуществления. Все патенты, патентные заявки и публикации, на которые ссылаются в настоящей заявке, все включены в настоящую заявку посредством ссылки во всей их полноте.
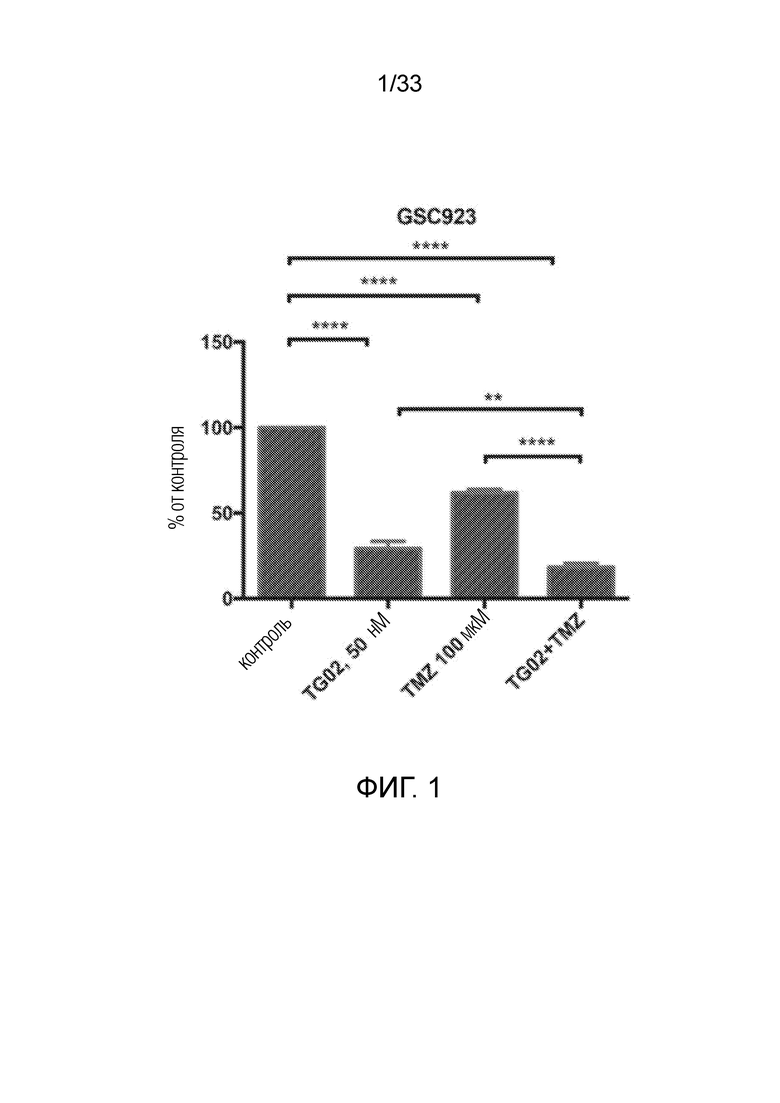
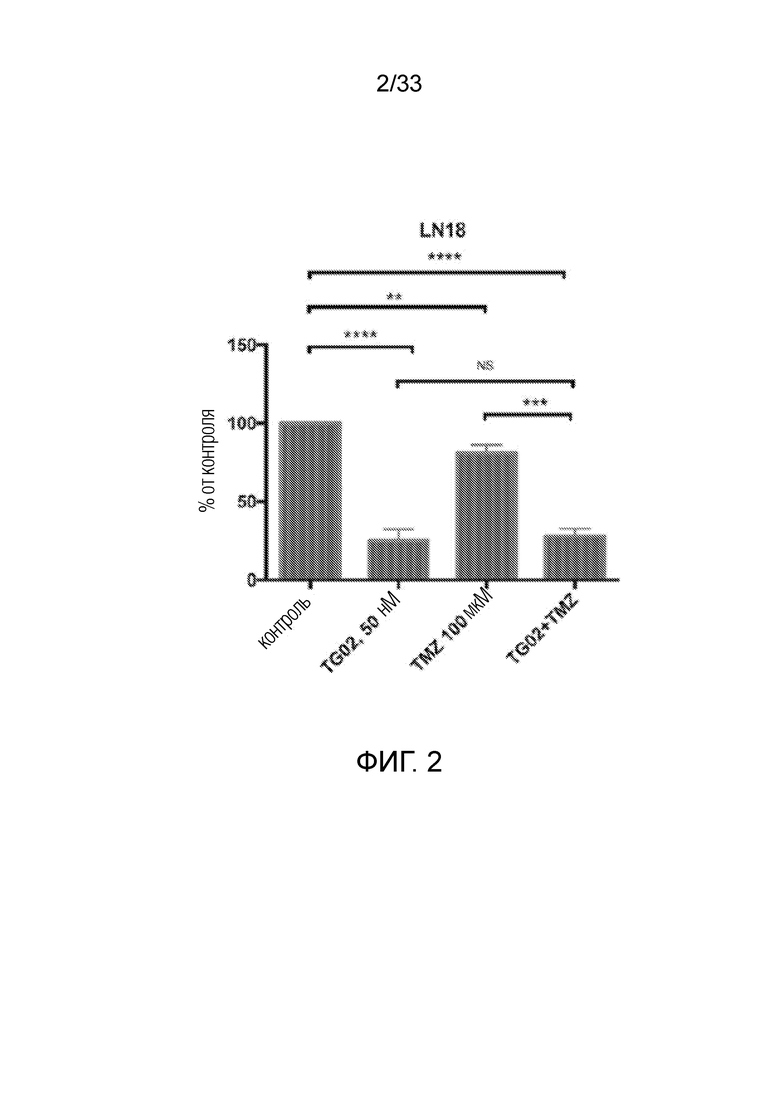
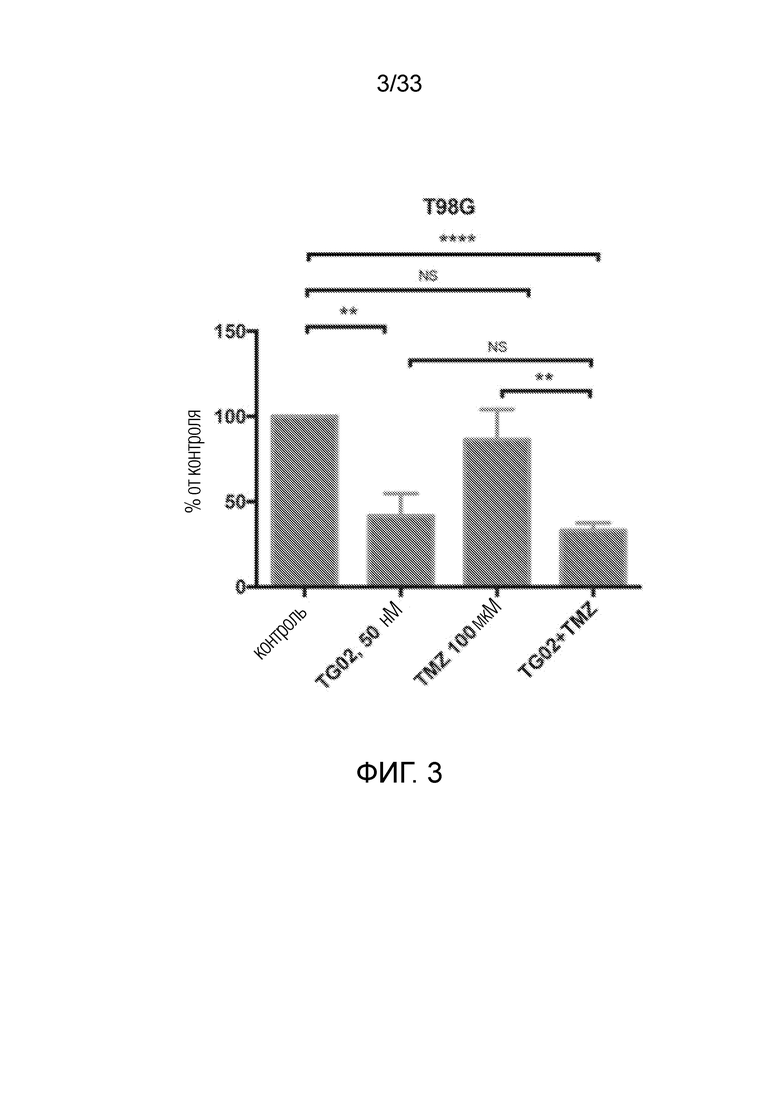
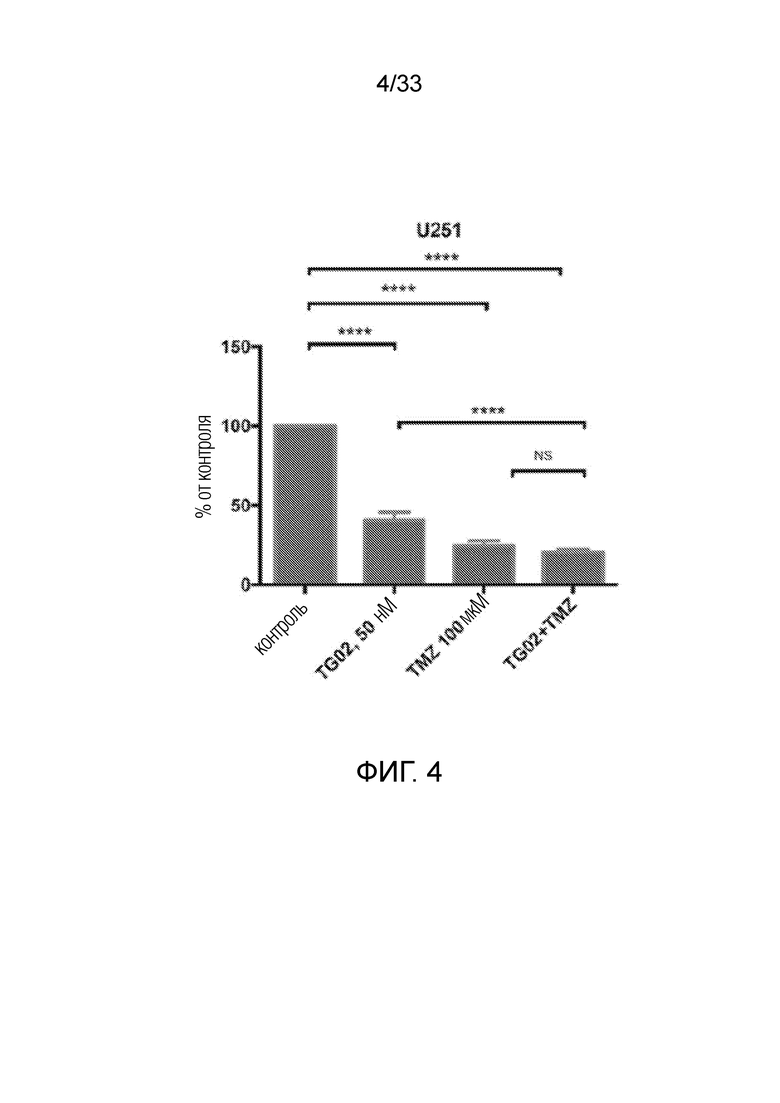
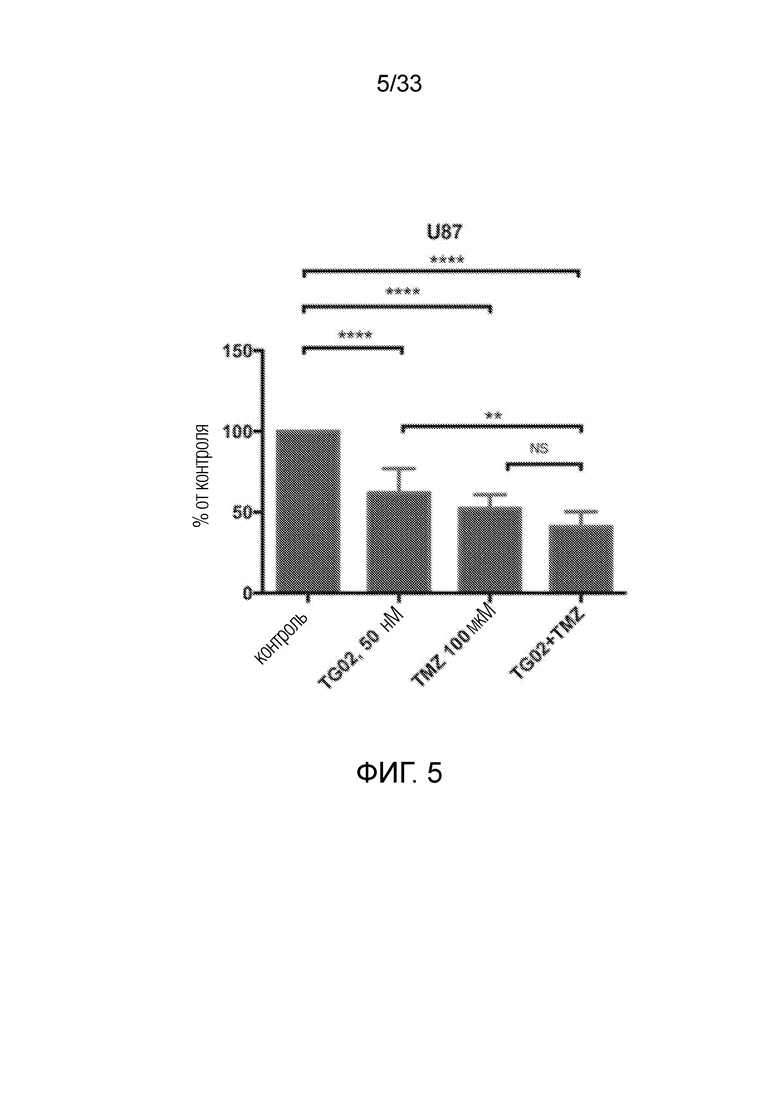
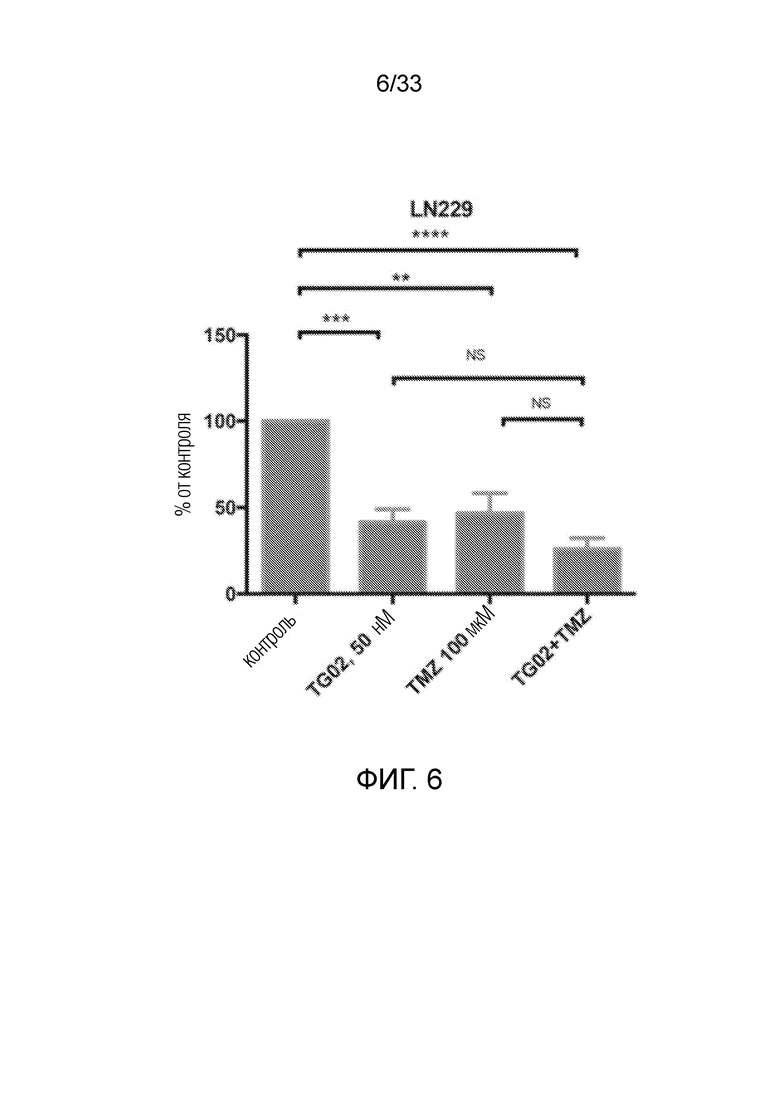
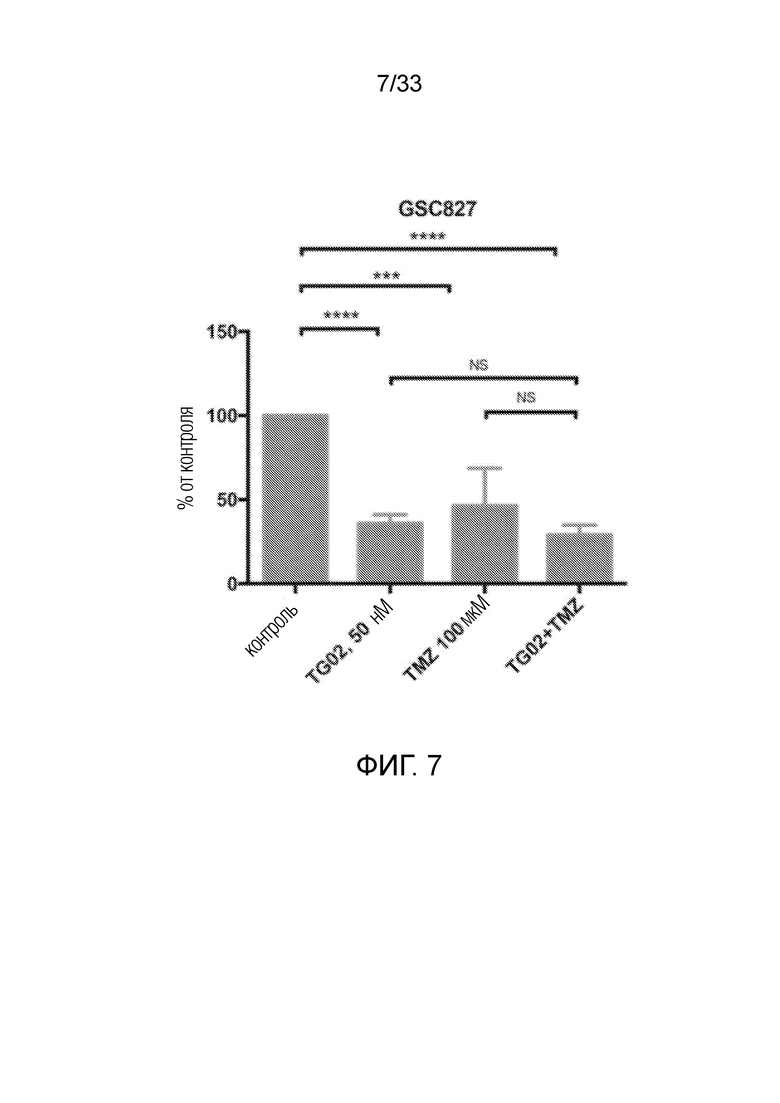
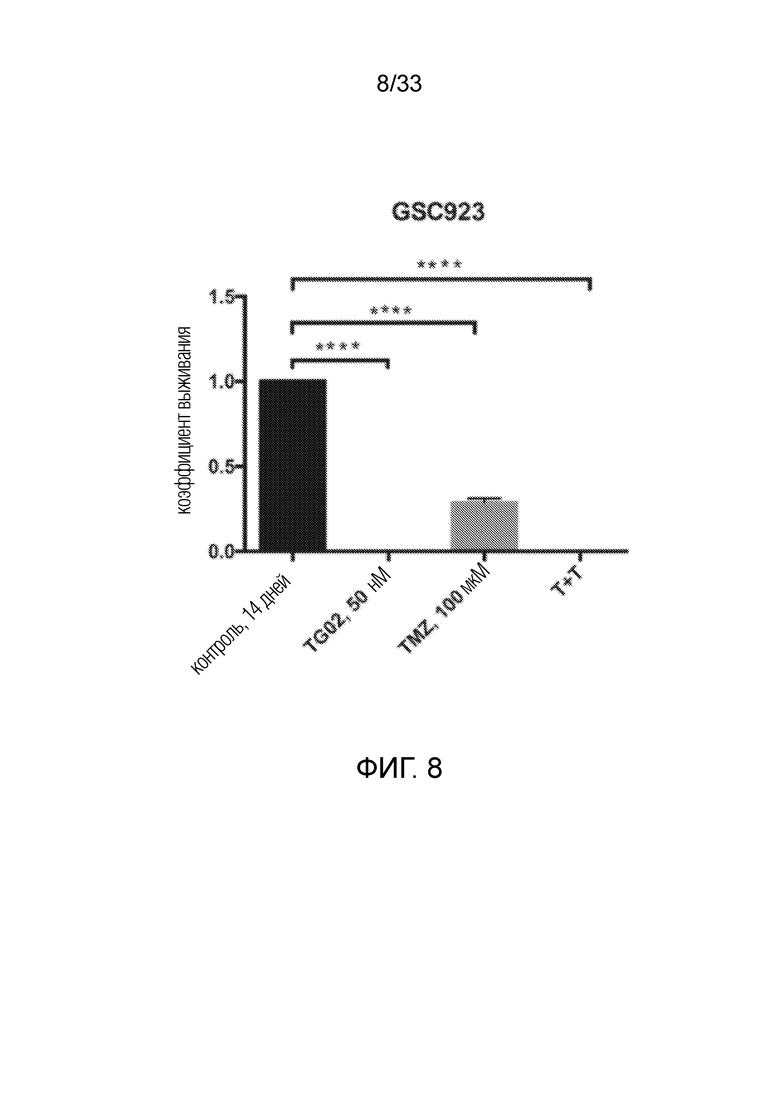
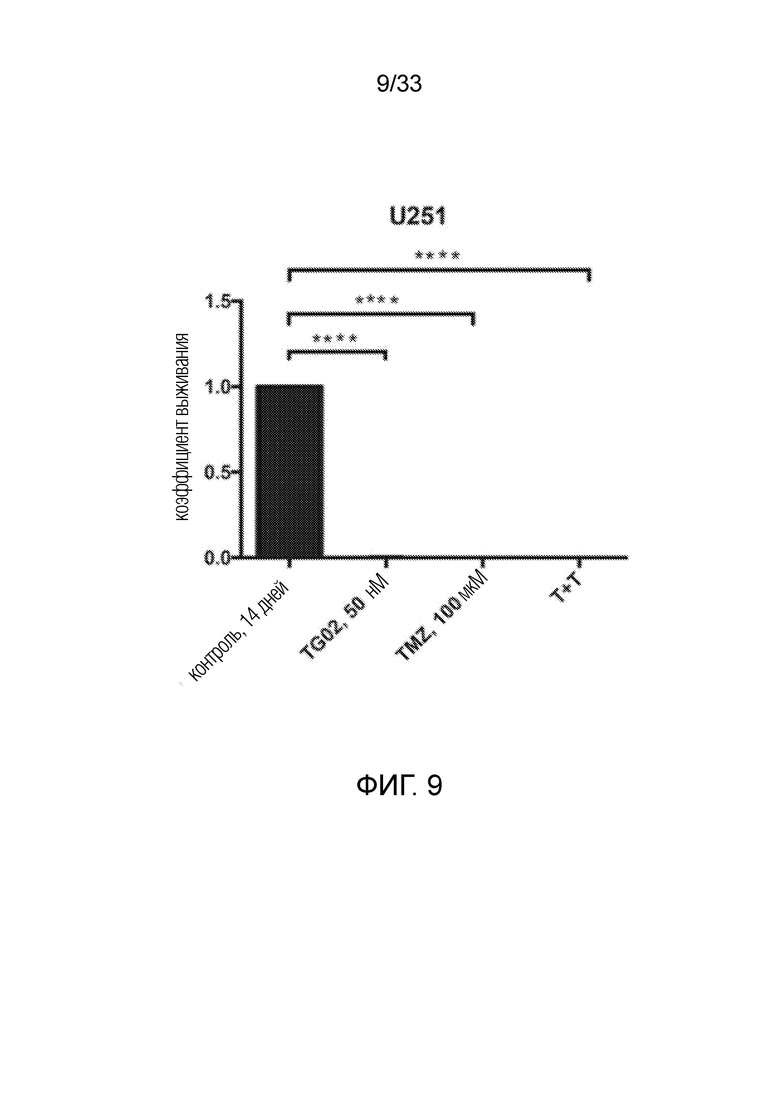
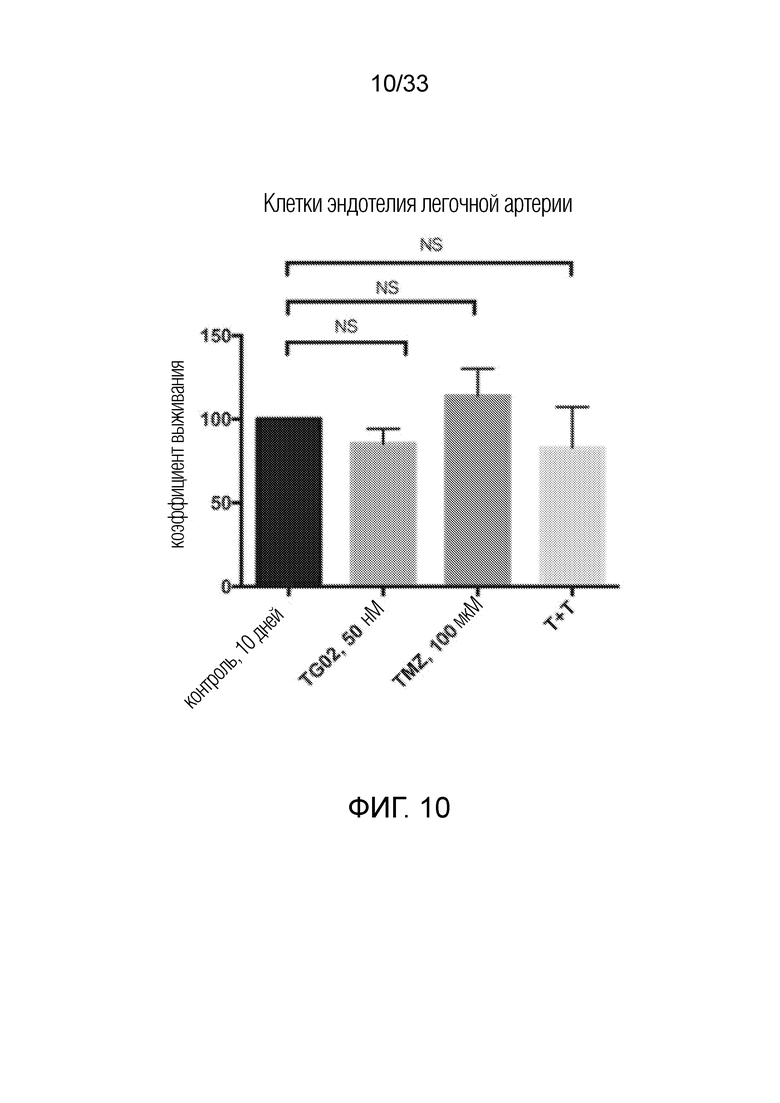
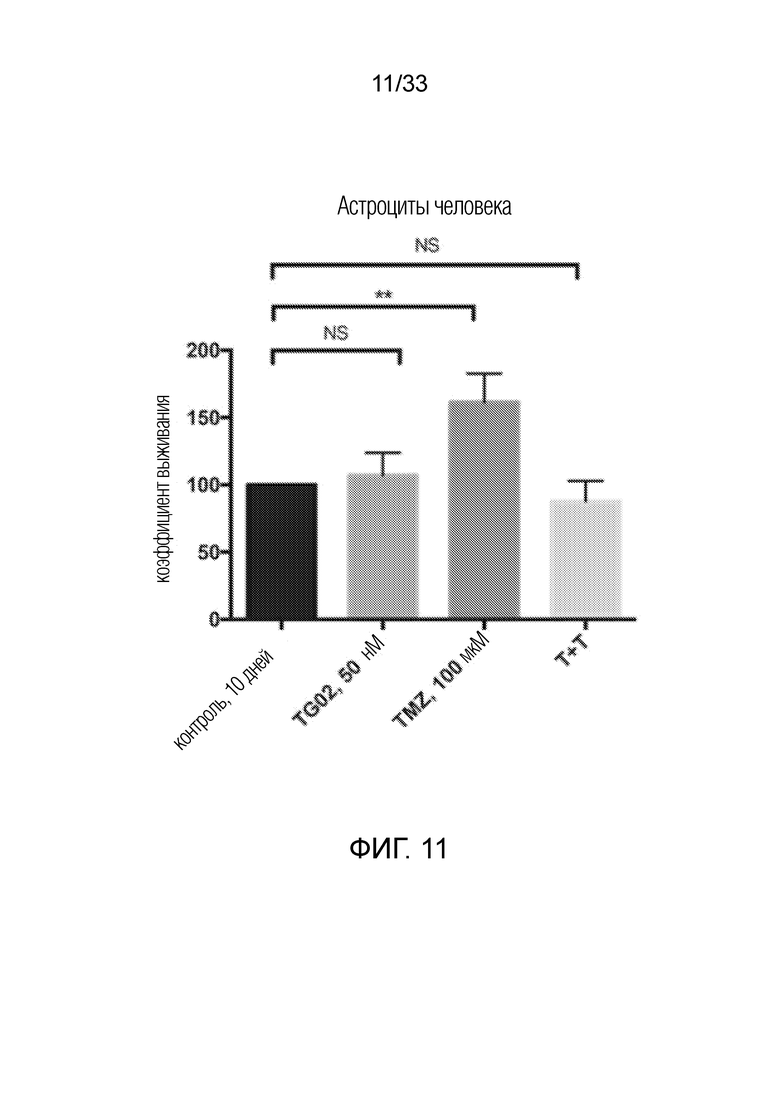
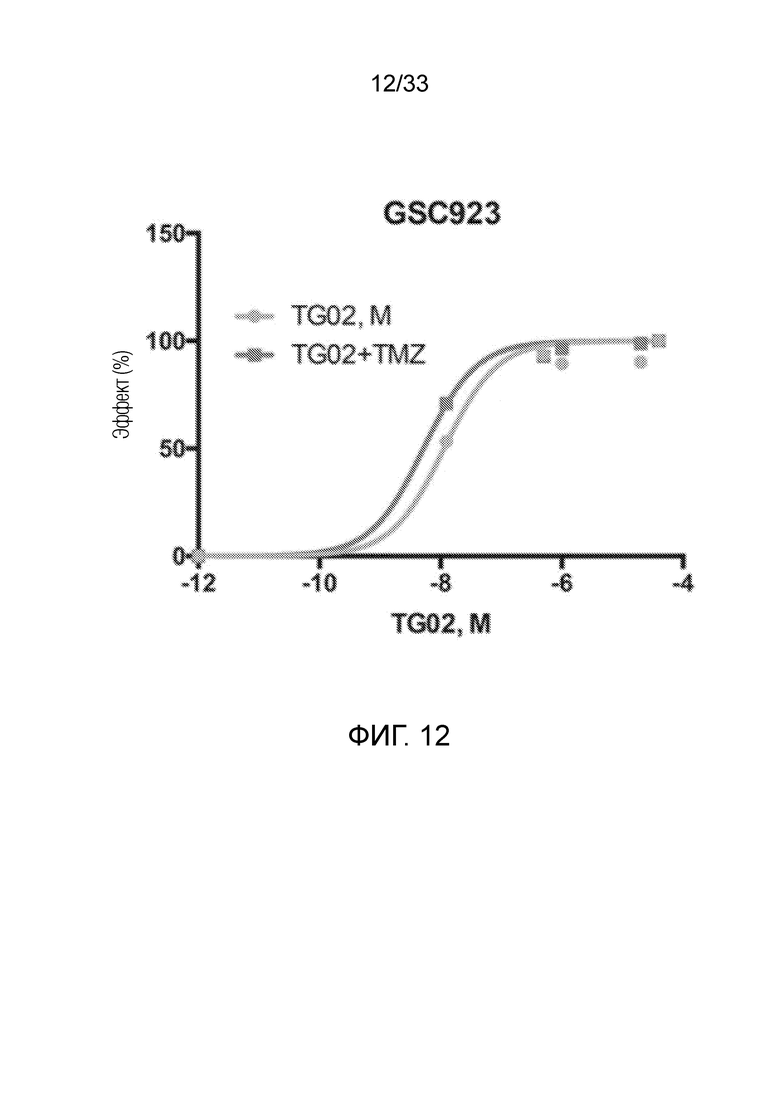
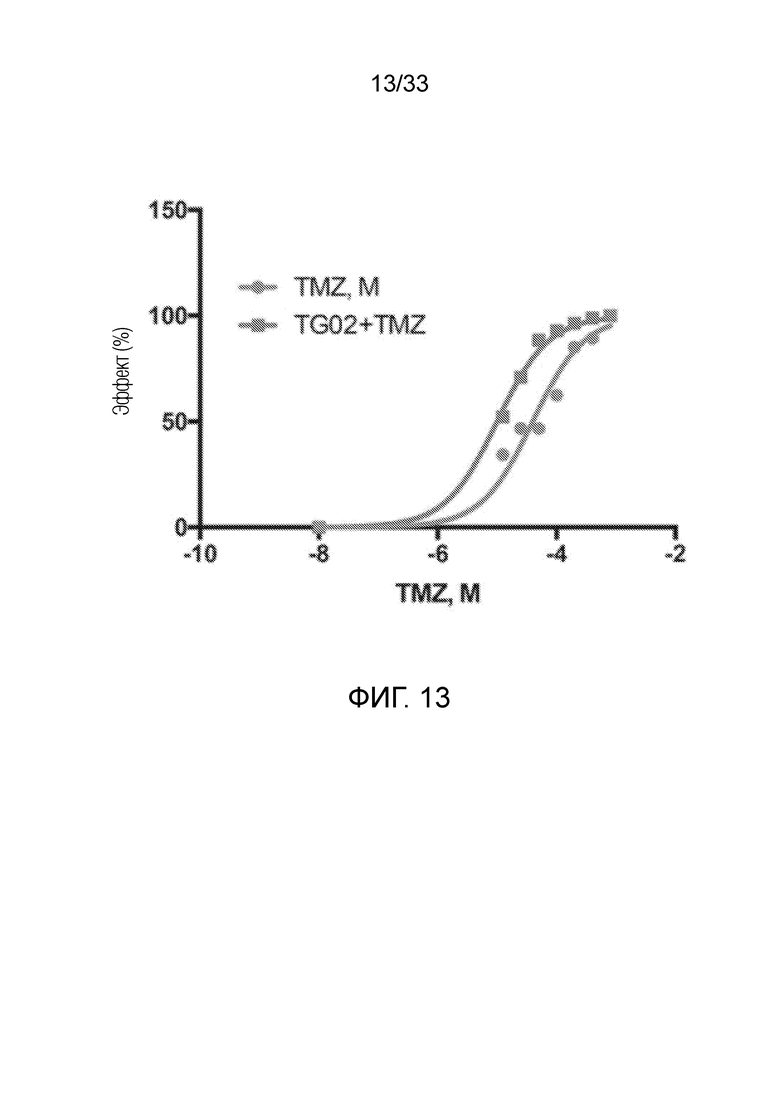
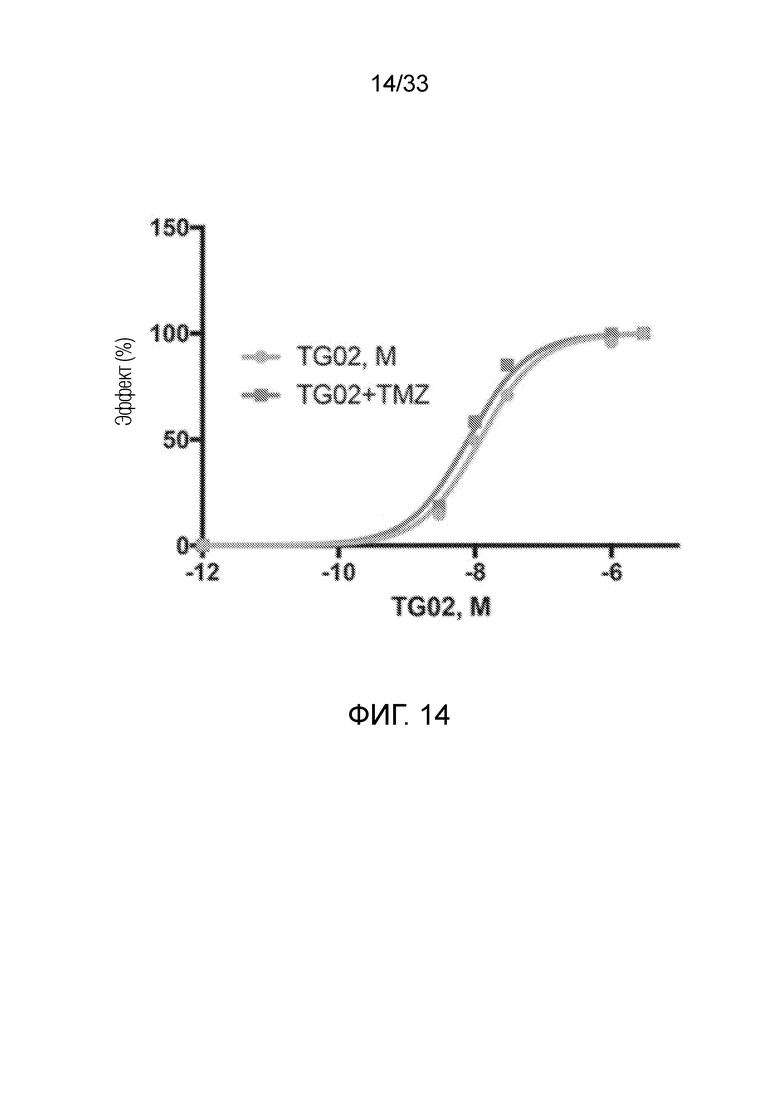
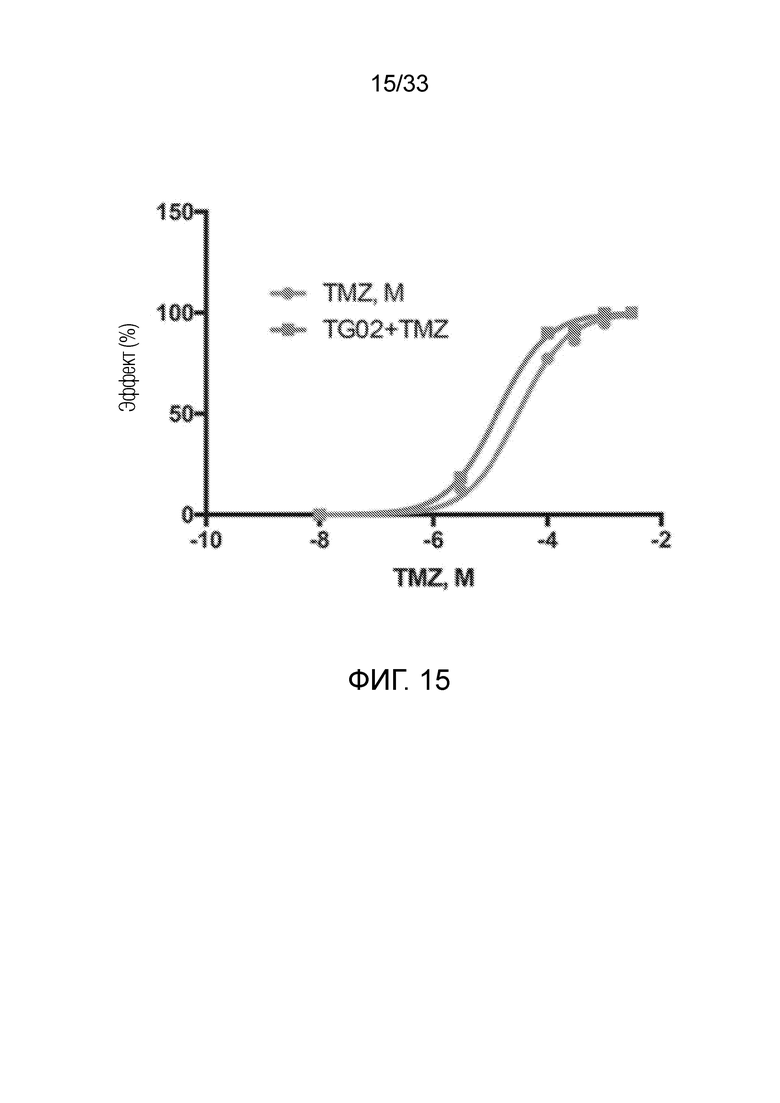
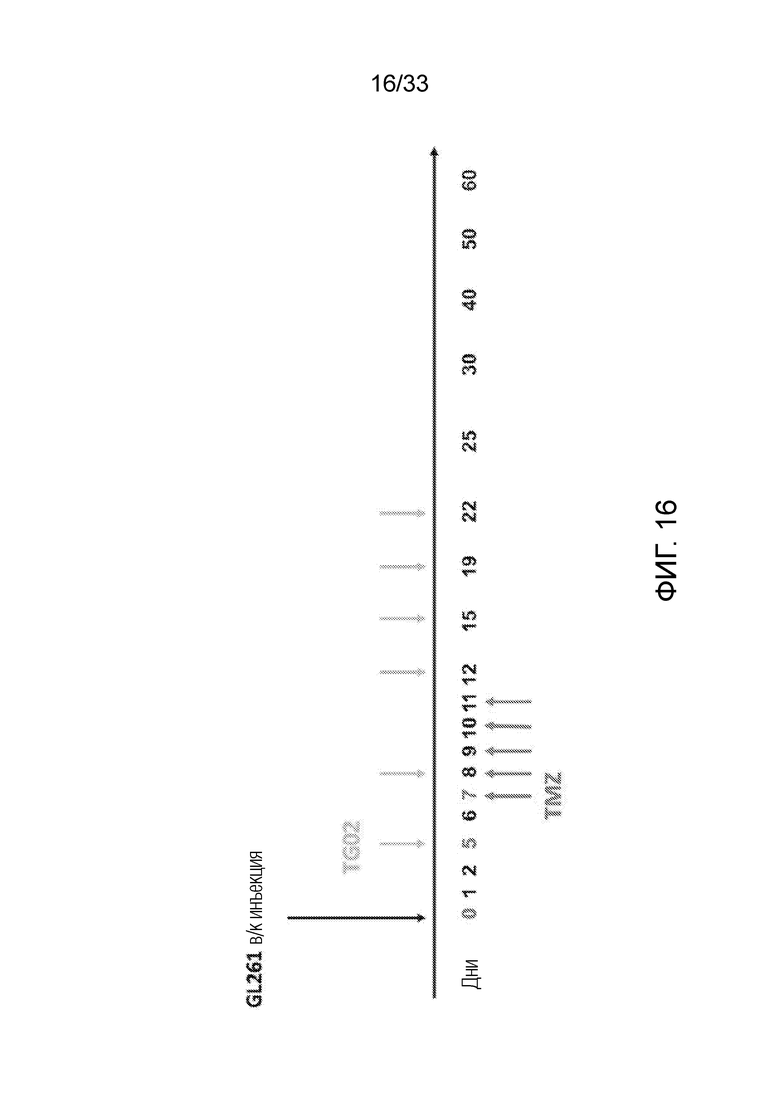
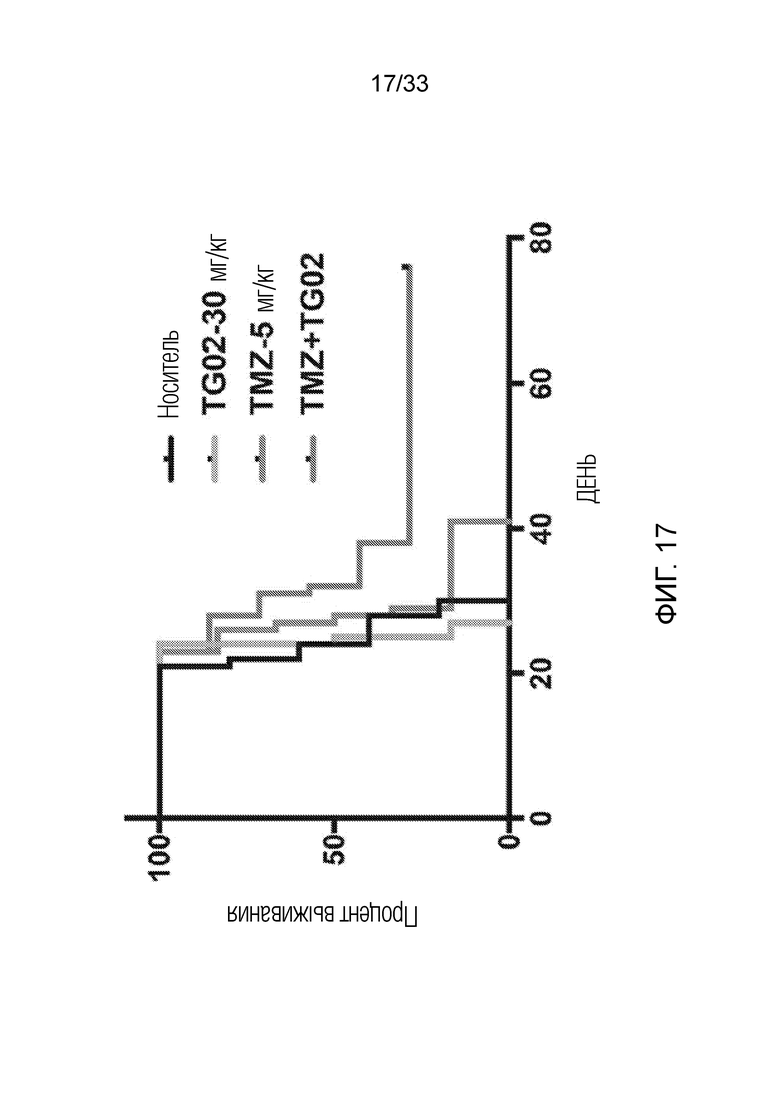
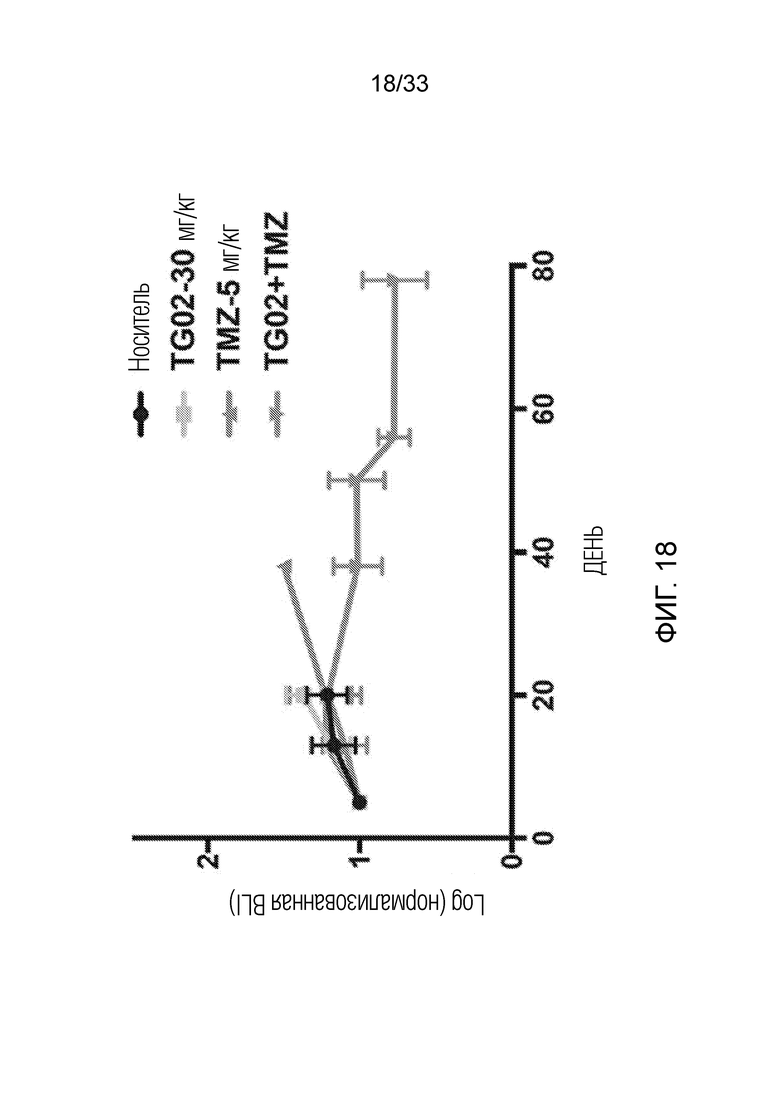
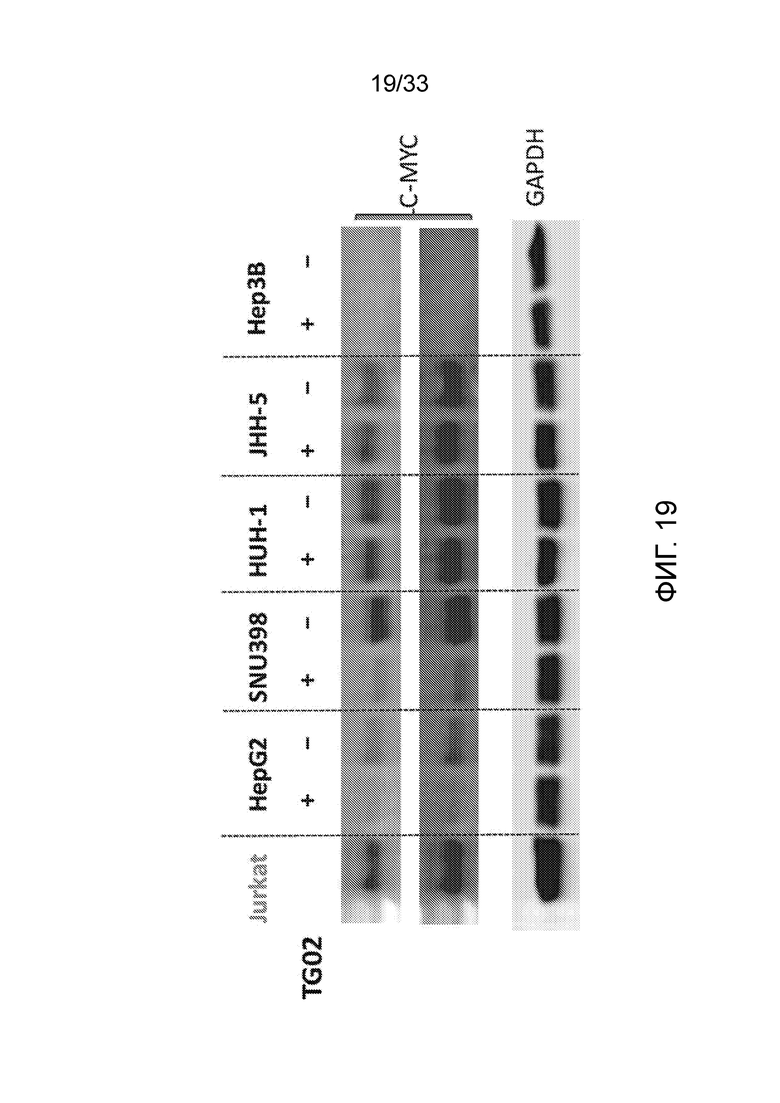
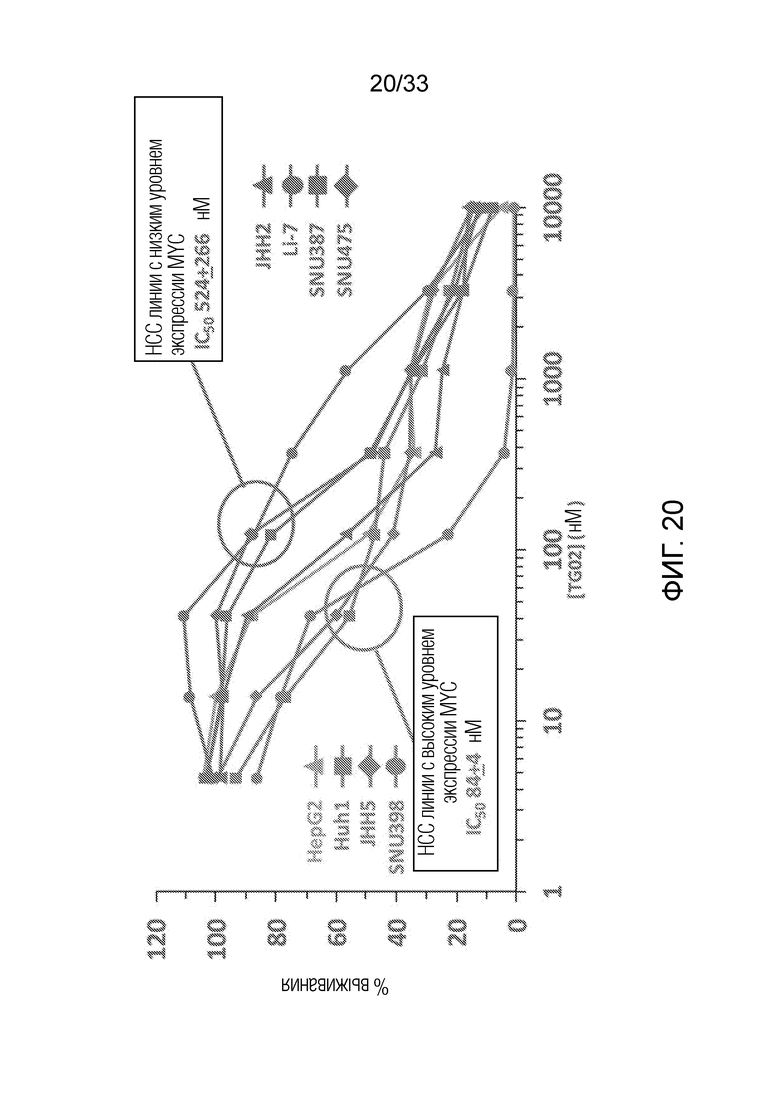
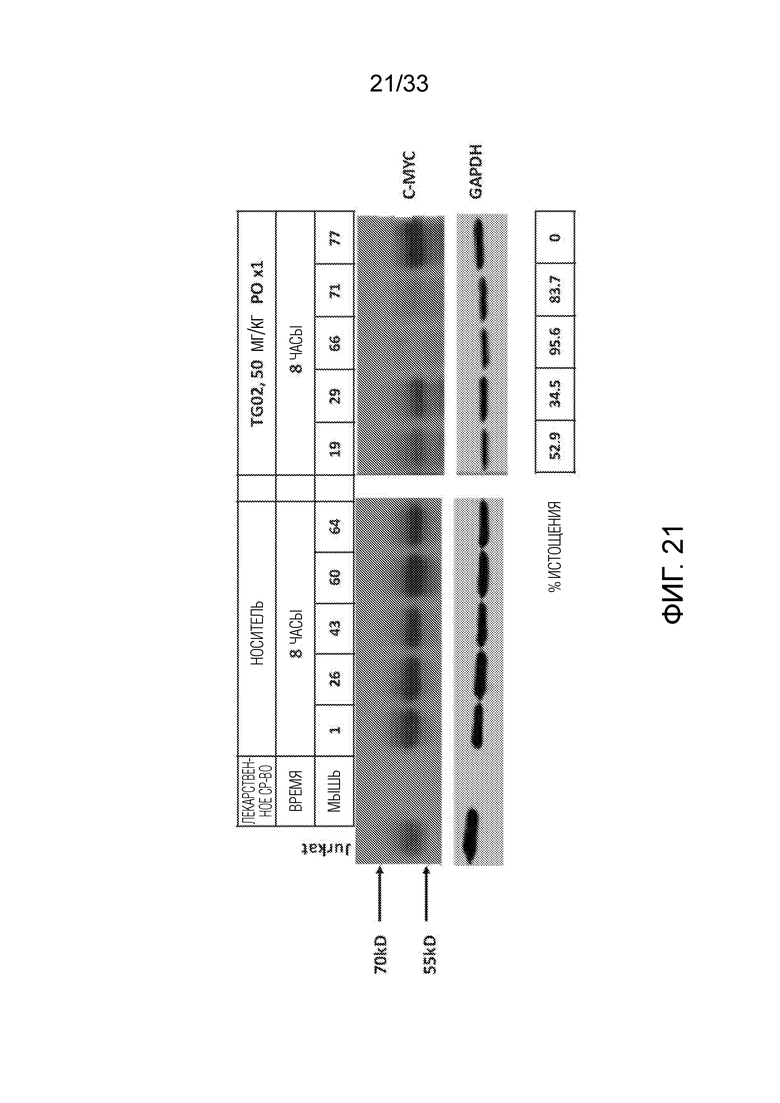
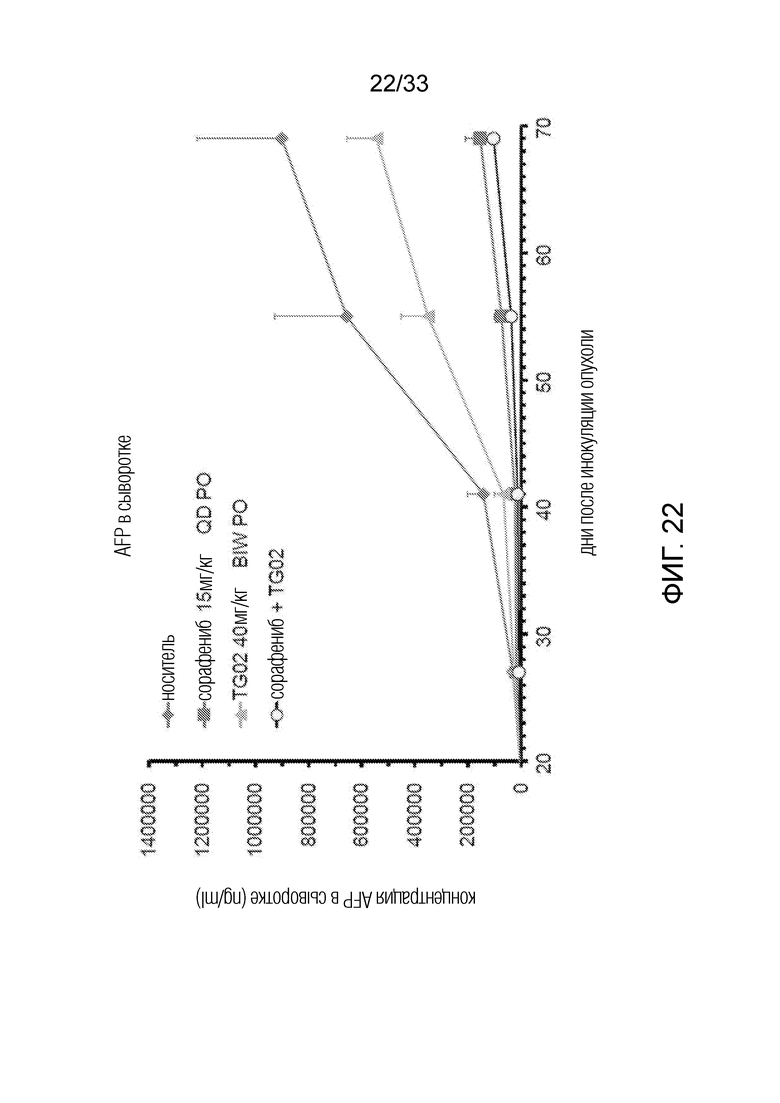
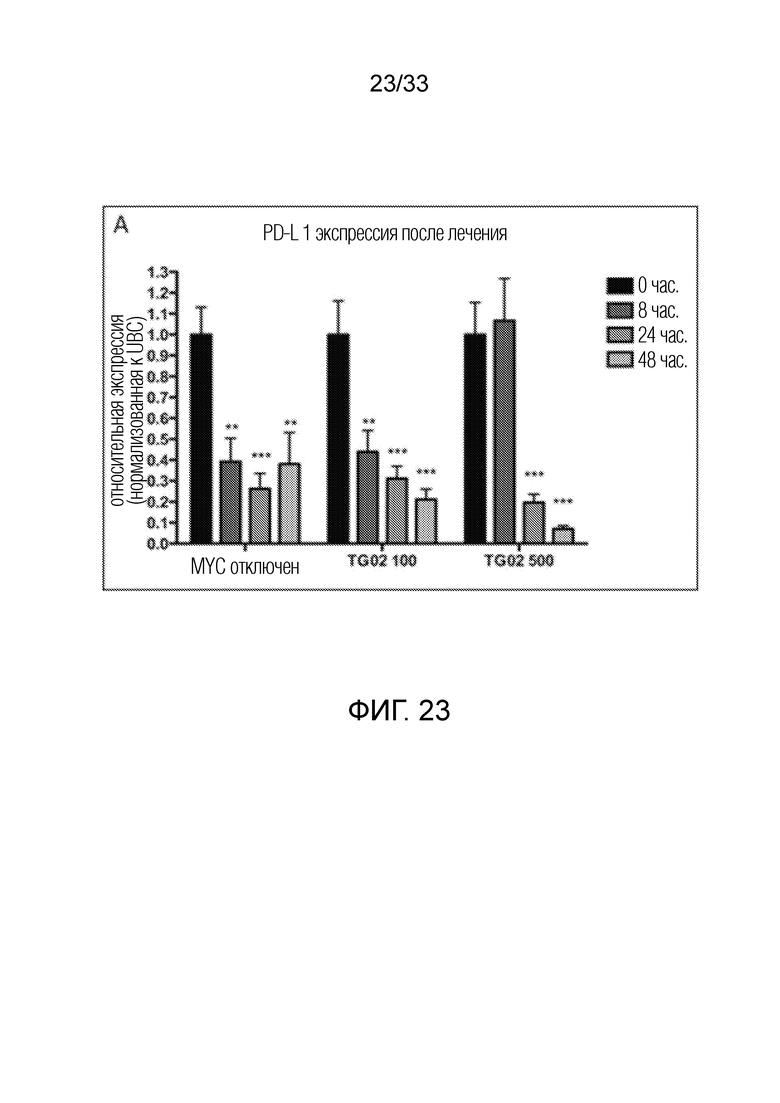
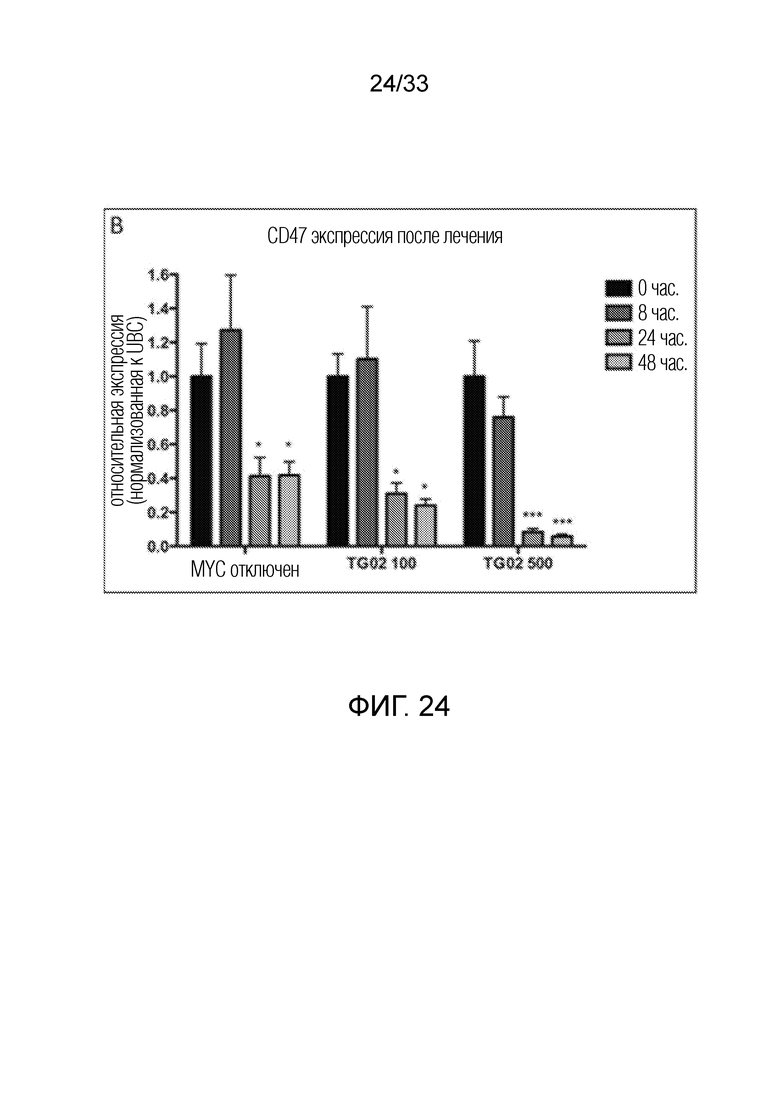
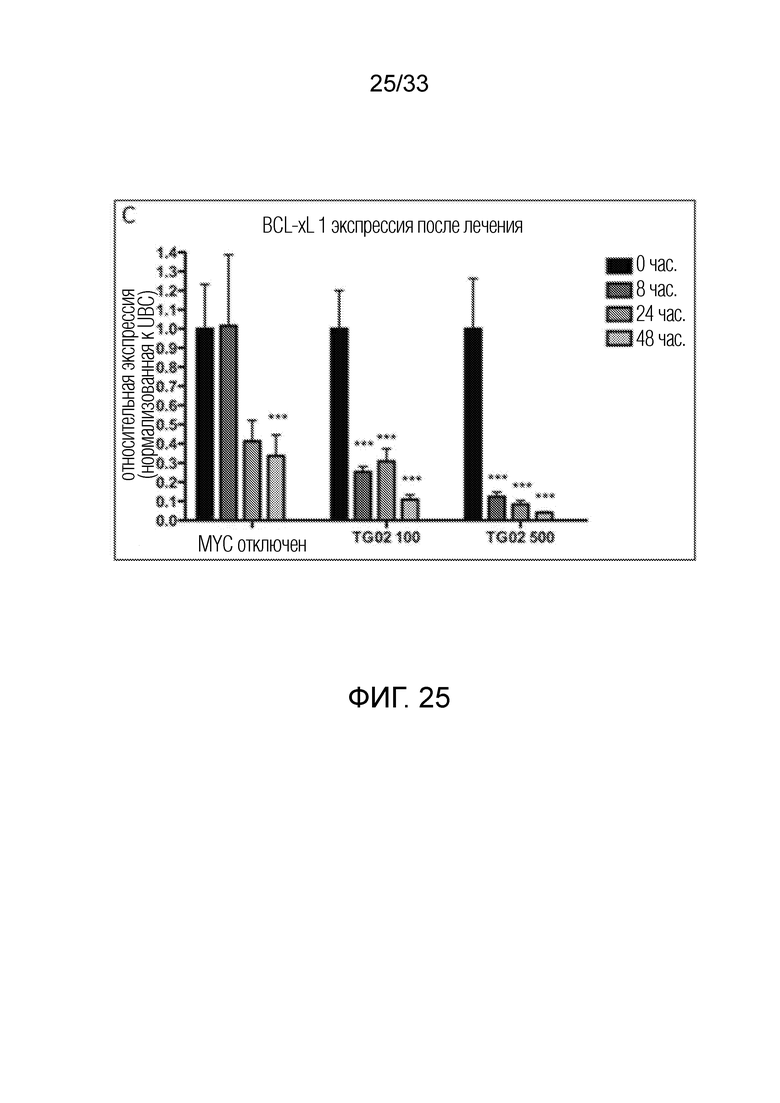
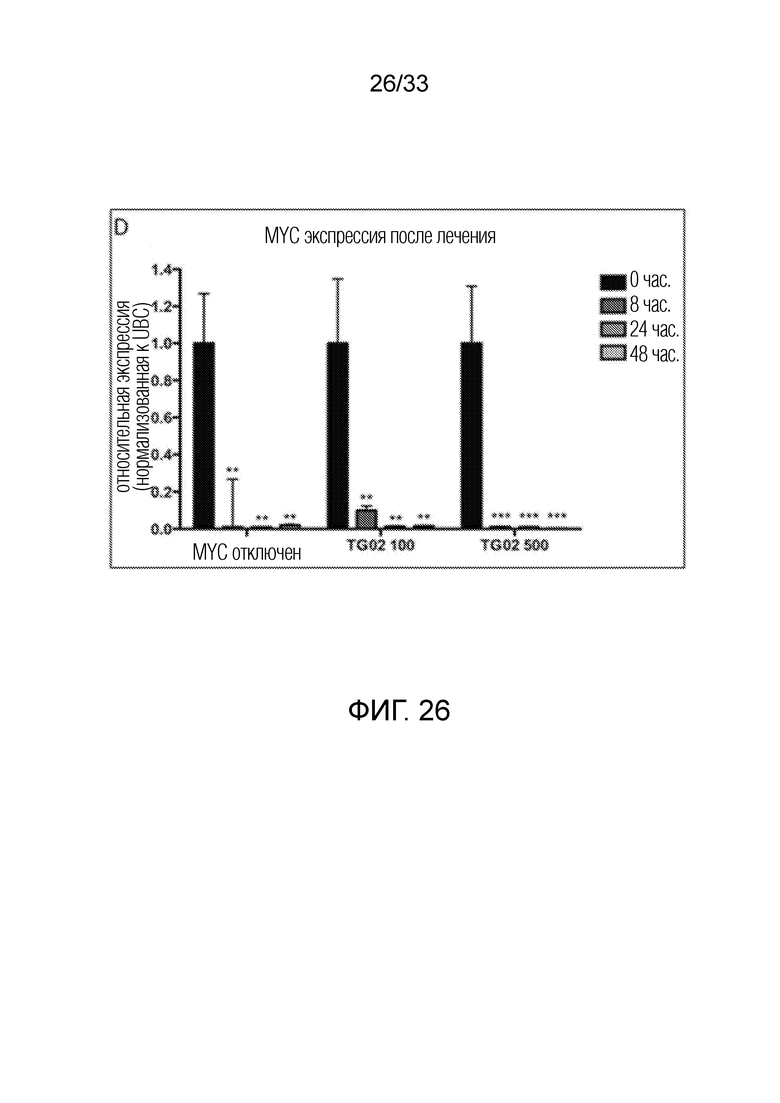
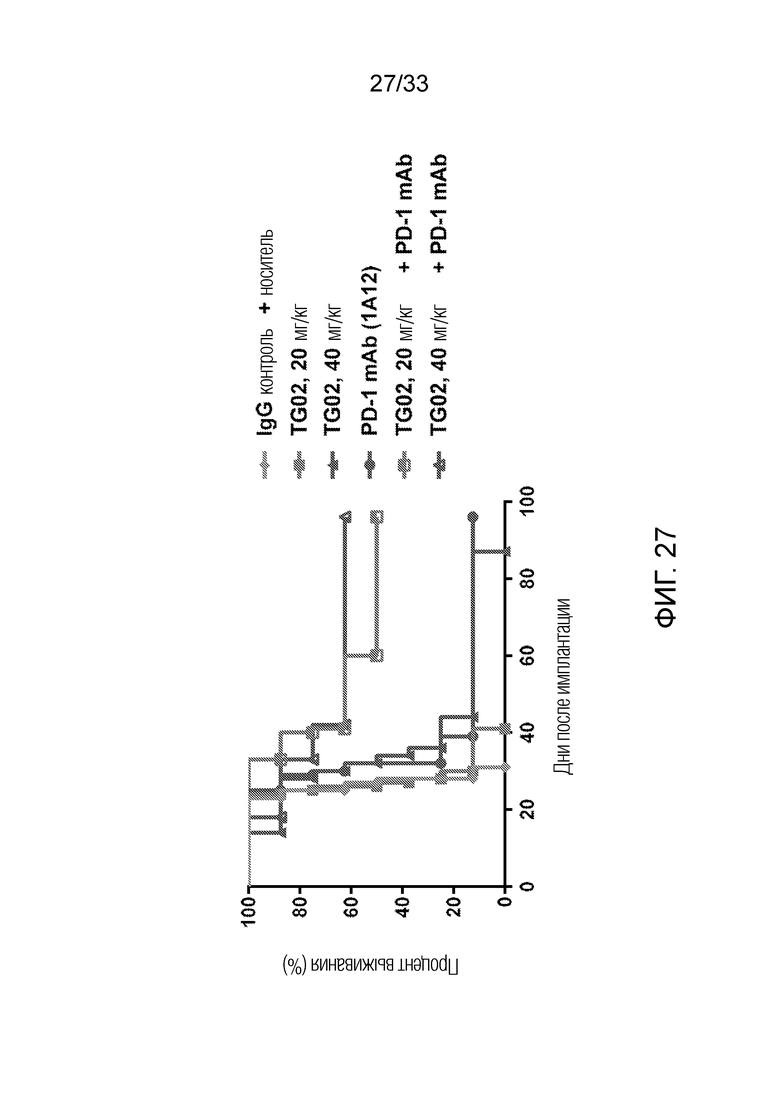
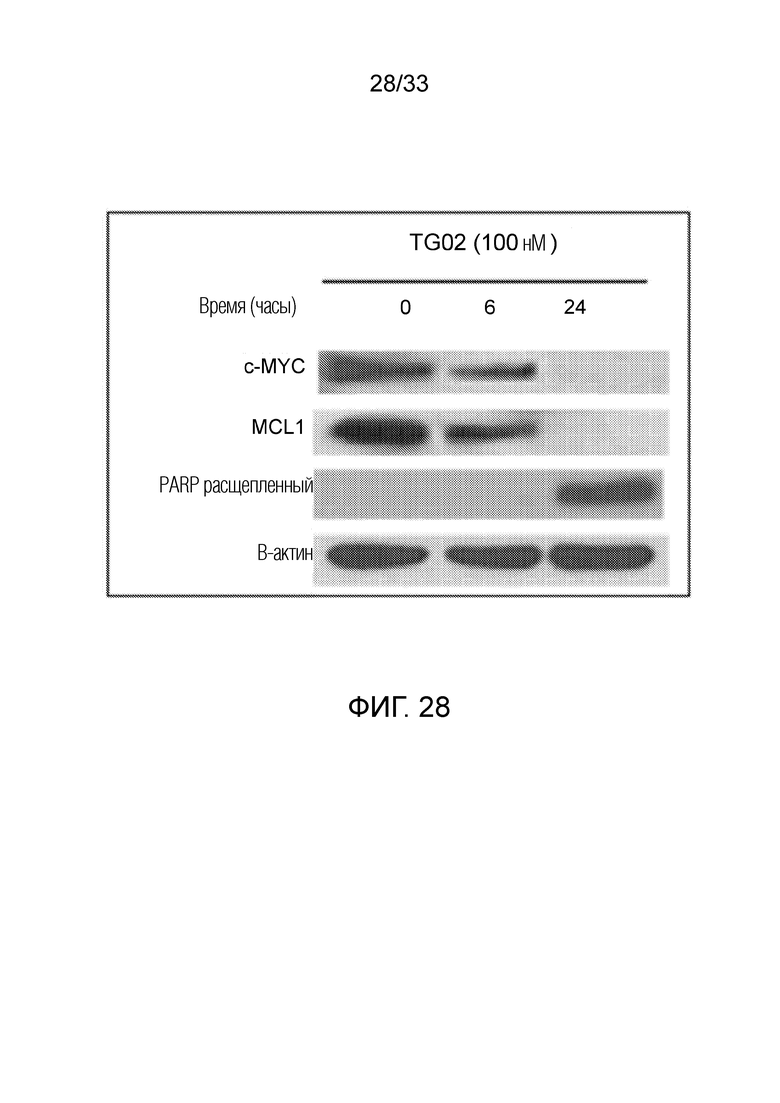
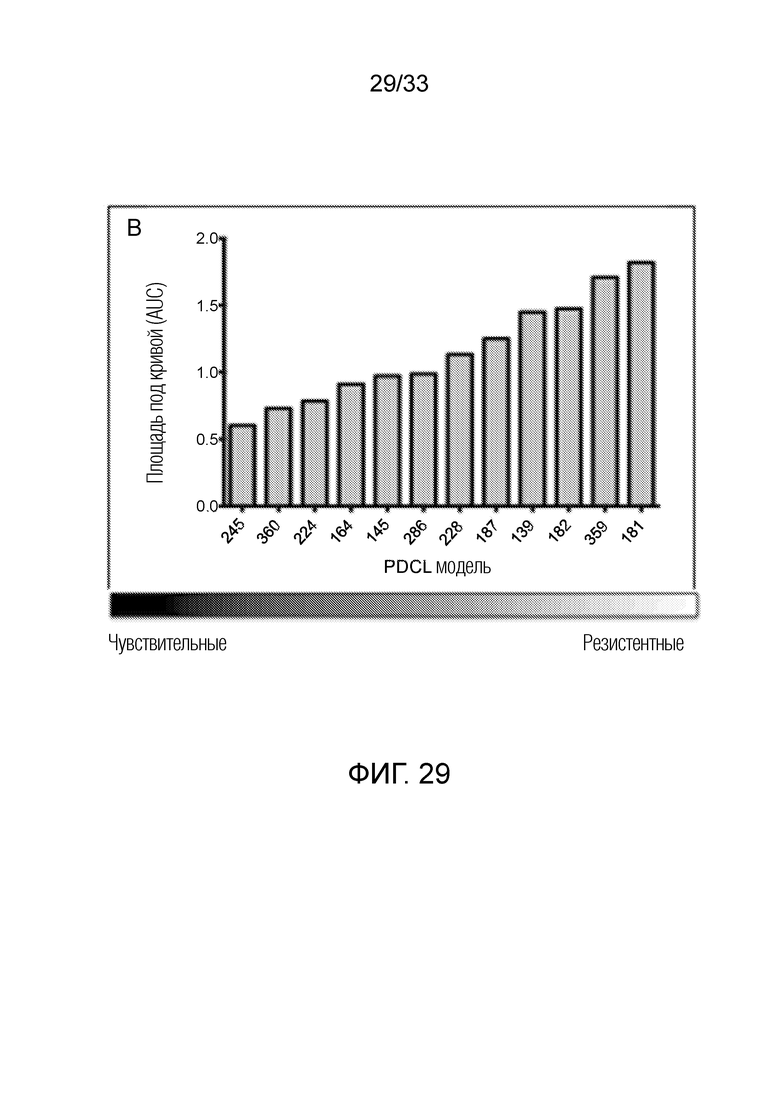
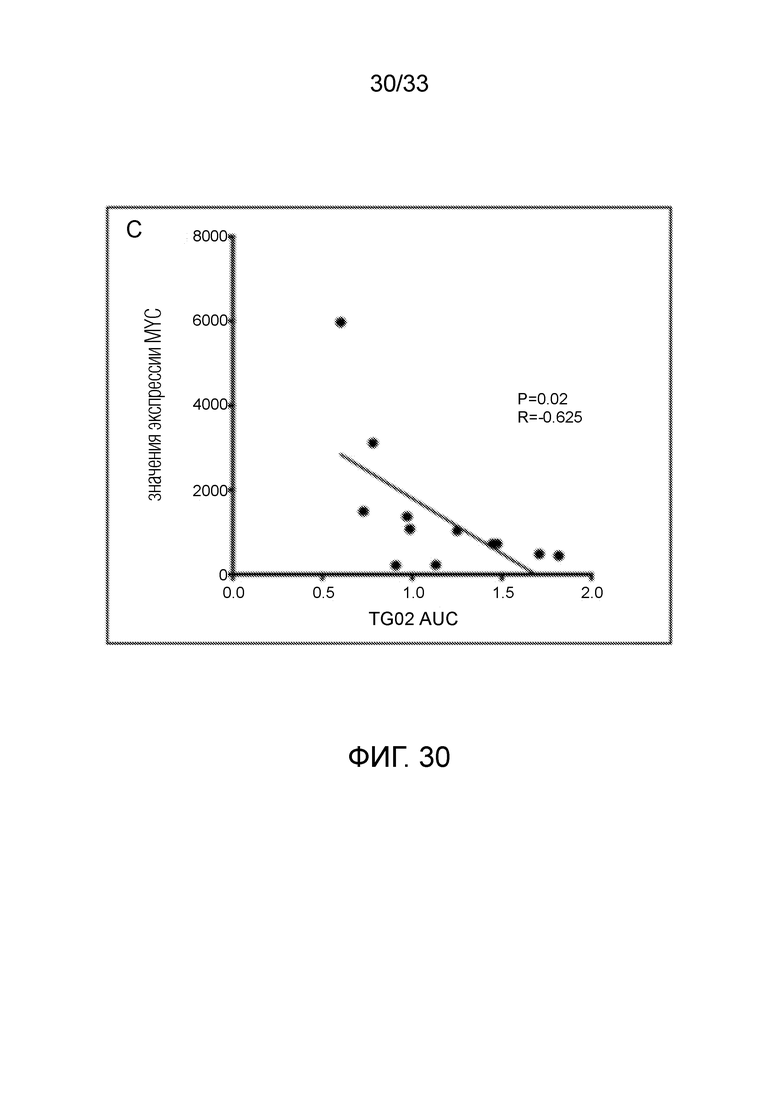
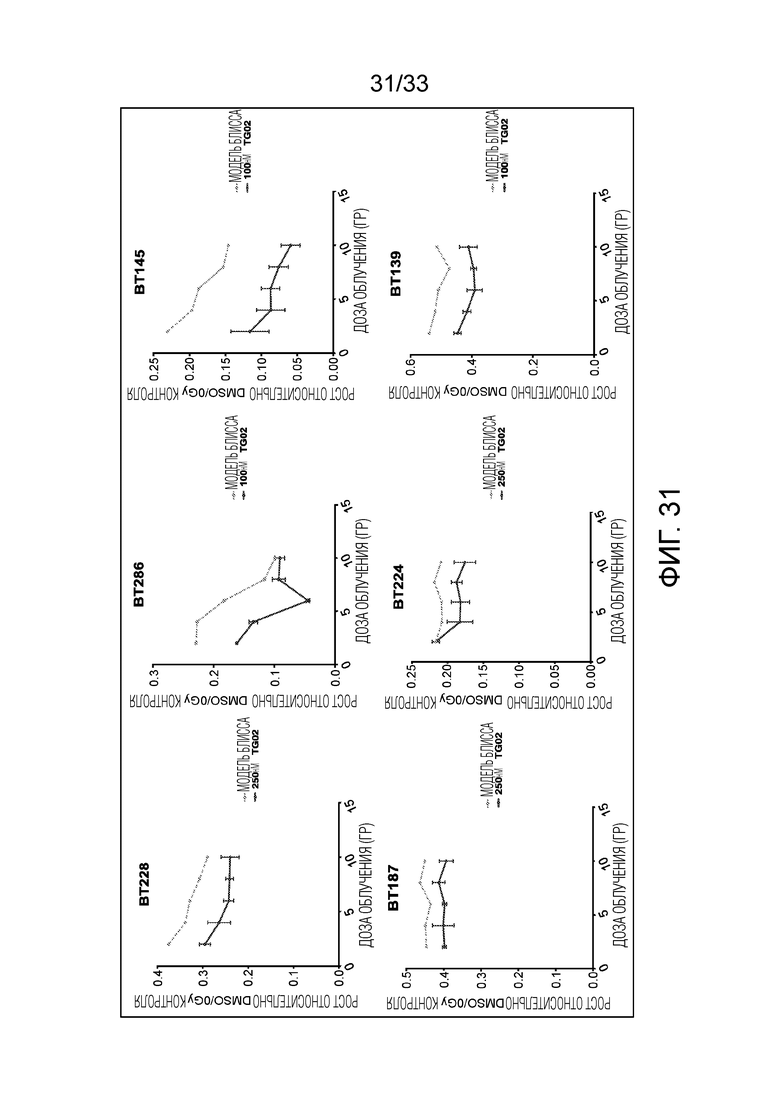
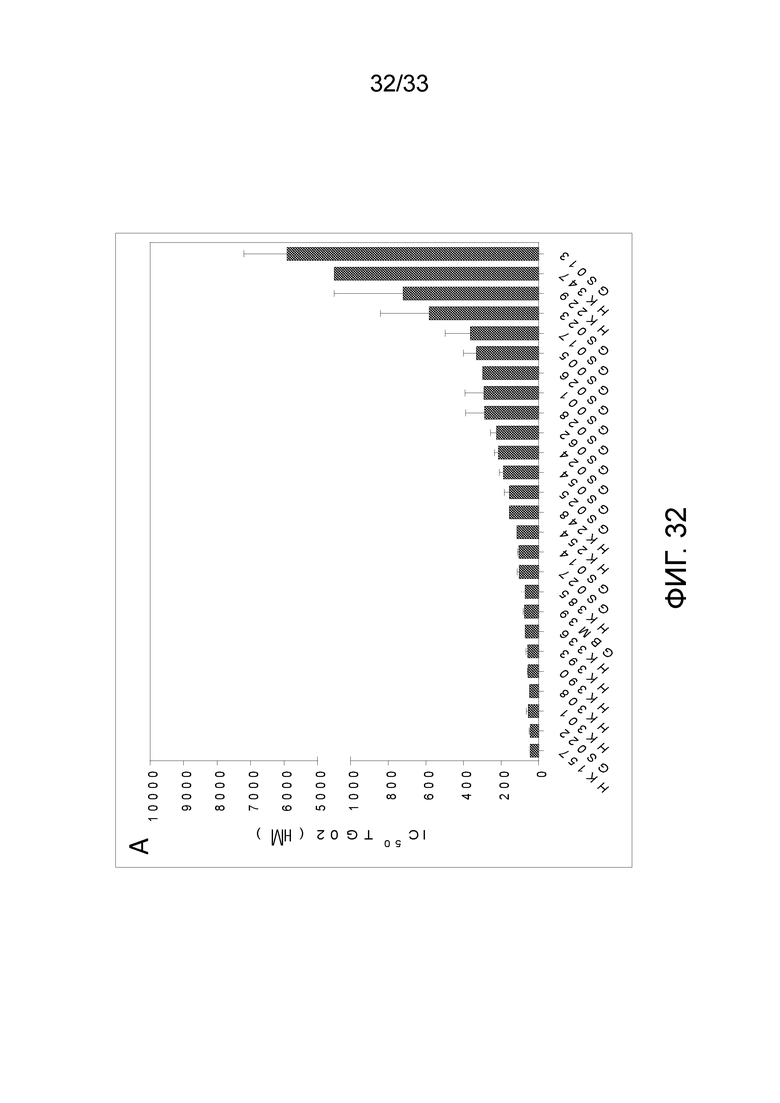
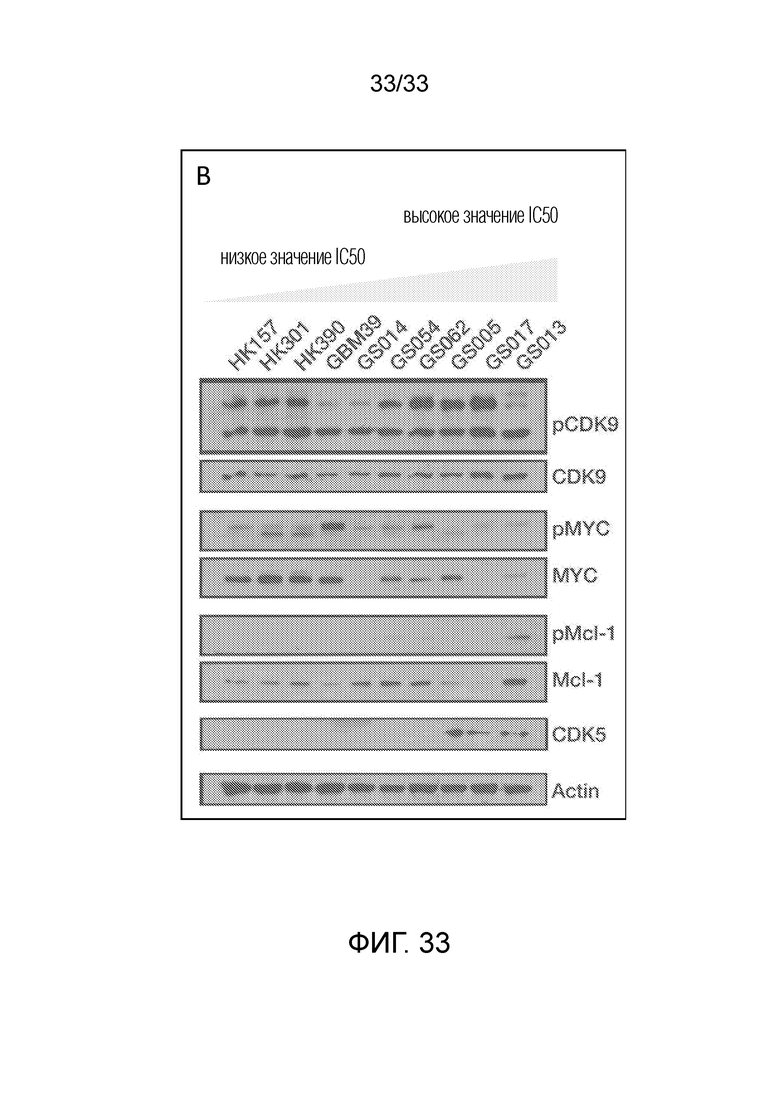
Изобретение относиться к медицине, а именно к онкологии, и может быть использовано для лечения пациента со злокачественным новообразованием. Способ включает введение пациенту терапевтически эффективных количеств (16E)-14-метил-20-окса-5,7,14,26-тетраазатетрацикло[19.3.1.1(2,6).1(8,12)]гептакоза-1(25),2(26),3,5,8(27),9,11,16,21,23-декаена (TG02) или его фармацевтически приемлемой соли в комбинации с лучевой терапией, где общая доза радиации, которую получает пациент, составляет от 0,01 Гр до 100 Гр. Использование изобретения позволяет повысить антипролиферативную активность за счет синергетического действия комбинации. 9 з.п. ф-лы, 4 табл., 33 ил., 11 пр.
1. Способ лечения пациента со злокачественным новообразованием, включающий введение пациенту терапевтически эффективных количеств (16E)-14-метил-20-окса-5,7,14,26-тетраазатетрацикло[19.3.1.1(2,6).1(8,12)]гептакоза-1(25),2(26),3,5,8(27),9,11,16,21,23-декаен или его фармацевтически приемлемая соль в комбинации с лучевой терапией, где общая доза радиации, которую получает пациент, составляет от 0,01 Гр до 100 Гр.
2. Способ по п.1, где пациент за курс лечения получает 15 Гр, 20 Гр, 25 Гр, 30 Гр, 35 Гр, 40 Гр, 45 Гр, 50 Гр, 55 Гр или 60 Гр.
3. Способ по п.1 или 2, где злокачественным новообразованием является солидная опухоль.
4. Способ по любому из пп.1-3, где злокачественное новообразование выбрано из группы, состоящей из рака надпочечников, ацинарно-клеточной карциномы, акустической невриномы, акральной лентигинозной меланомы, акроспиромы, острого эозинофильного лейкоза, острого эритроидного лейкоза, острого лимфобластного лейкоза, острого мегакарибластного лейкоза, острого моноцитарного лейкоза, острого промиелоцитарного лейкоза, аденокарциномы, аденокистозной карциномы, аденомы, аденоматоидной одонтогенной опухоли, аденосквамозной карциномы, новообразования жировой ткани, адренокортикальной карциномы, Т-клеточного лейкоза/лимфомы взрослых, агрессивного NK-клеточного лейкоза, СПИД-ассоциированной лимфомы, альвеолярной рабдомиосаркомы, альвеолярной саркомы мягких тканей, амелобластической фибромы, анапластической крупноклеточной лимфомы, анапластического рака щитовидной железы, ангиоиммунобластной Т-клеточной лимфомы, ангиомиолипомы, ангиосаркомы, астроцитомы, атипичной тератоидно-рабдоидной опухоли, В-клеточного хронического лимфоцитарного лейкоза, В-клеточного пролимфоцитарного лейкоза, В-клеточной лимфомы, базальноклеточной карциномы, рака желчных путей, рака мочевого пузыря, бластомы, рака кости, опухоли Бреннера, опухоли Брауна, лимфомы Беркитта, рака молочной железы, рака головного мозга, карциномы, карциномы in situ, карциносаркомы, опухоли хряща, цементомы, миелоидной саркомы, хондромы, хордомы, хориокарциномы, папилломы хориоидного сплетения, светлоклеточной саркомы почек, краниофарингиомы, кожной Т-клеточной лимфомы, рака шейки матки, колоректального рака, болезни Дегоса, десмопластической мелкокруглоклеточной опухоли, диффузной В-клеточной крупноклеточной лимфомы, дизэмбриопластической нейроэпителиальной опухоли, дисгерминомы, эмбриональной карциномы, новообразования эндокринных желез, опухоли эндодермального синуса; Т-клеточной лимфомы, ассоциированной с энтеропатией; рака пищевода, включенного плода, фибромы, фибросаркомы, фолликулярной лимфомы, фолликулярного рака щитовидной железы, ганглионевромы, рака желудочно-кишечного тракта, эмбрионально-клеточной опухоли, гестационной хориокарциномы, гигантоклеточной фибробластомы, гигантоклеточной опухоли кости, глиальной опухоли, глиобластомы, глиомы, церебрального глиоматоза, глюкагономы, гонадобластомы, гранулезоклеточной опухоли, гинандробластомы, рака желчного пузыря, рака желудка, волосистоклеточного лейкоза, гемангиобластомы, рака головы и шеи, гемангиоперицитомы, гематологического злокачественного заболевания, гепатобластомы, гепатоцеллюлярной карциномы, гепатолиенальной Т-клеточной лимфомы, лимфомы Ходжкина, не-ходжкинской лимфомы, инвазивной лобулярной карциномы, рака кишечника, рака почек, рака гортани, злокачественного лентиго, смертельной срединной карциномы, лейкоза, опухоли из клеток Лейдига, липосаркомы, рака легкого, лимфангиомы, лимфангиосаркомы, лимфоэпителиомы, лимфомы, острого лимфоцитарного лейкоза, острого миелогенного лейкоза, хронического лимфоцитарного лейкоза, рака печени, мелкоклеточного рака легкого, немелкоклеточного рака легкого, MALT лимфомы, злокачественной фиброзной гистиоцитомы, злокачественной опухоли оболочек периферических нервов, злокачественной тритон-опухоли, лимфомы из клеток мантийной зоны, B-клеточной лимфомы из клеток краевой зоны, тучноклеточного лейкоза, медиастинальной эмбрионально-клеточной опухоли, медуллярной карциномы молочной железы, медуллярного рака щитовидной железы, медуллобластомы, меланомы, менингиомы, рака из клеток Меркеля, мезотелиомы, метастатической уротелиальной карциномы, смешанной опухоли Мюллера, муцинозной опухоли, множественной миеломы, новообразования мышечной ткани, фунгоидного микоза, миксоидной липосаркомы, миксомы, миксосаркомы, нозофарингеальной карциномы, нейриномы, нейробластомы, нейрофибромы, нейромы, нодулярной меланомы, окулярного рака, олигоастроцитомы, олигодендроглиомы, онкоцитомы, менингиомы волокон зрительного нерва, опухоли зрительного нерва, рака полости рта, остеосаркомы, рака яичников, опухоли Панкоста, папиллярного рака щитовидной железы, параганглиомы, пинеалобластомы, пинеоцитомы, питуицитомы, аденомы гипофиза, опухоли гипофиза, плазмоцитомы, полиэмбриомы, Т-лимфобластной лимфомы из клеток-предшественников, первичной лимфомы центральной нервной системы, первичной эффузионной лимфомы, первичного перитонеального рака, рака предстательной железы, рака поджелудочной железы, фарингеального рака, псевдомиксомы брюшины, почечно-клеточной карциномы, медуллярной карциномы почки, ретинобластомы, рабдомиомы, рабдомиосаркомы, трансформации Рихтера, рака прямой кишки, саркомы, шванноматоза, семиномы, опухоли из клеток Сертоли, опухоли стромы полового тяжа яичников, перстневидно-клеточного рака, рака кожи, мелко-сине-круглоклеточных опухолей, мелкоклеточного рака, саркомы мягких тканей, соматостатиномы, эпителиомы мошонки, опухоли спинного мозга, лимфомы маргинальной зоны селезенки, плоскоклеточной карциномы, синовиальной саркомы, синдрома Сезари, рака тонкой кишки, плоскоклеточной карциномы, рака желудка, Т-клеточной лимфомы, тестикулярного рака, текомы, рака щитовидной железы, переходно-клеточного рака, рака горла, рака мочеточника, урогенитального рака, уротелиальной карциномы, увеальной меланомы, рака матки, бородавчатой карциномы, глиомы зрительного пути, рака вульвы, рака влагалища, макроглобулинемии Вальденстрема, опухоли Уортина и опухоли Вильмса.
5. Способ по п.4, где злокачественное новообразование выбрано из группы, состоящей из гепатоцеллюлярной карциномы, глиобластомы, рака легких, рака молочной железы, рака головы и шеи, рака предстательной железы, меланомы и колоректального рака.
6. Способ по п.4, где злокачественное новообразование является множественной миеломой.
7. Способ по п.4, где злокачественное новообразование является глиобластомой.
8. Способ по п.4, где злокачественным новообразованием является глиома.
9. Способ по любому из пп.1-8, где злокачественное новообразование является резистентным к лечению лекарственным средством или комбинацией лекарственных средств, которые были одобрены для терапевтического применения человеком.
10. Способ по любому из пп.1-9, включающий введение цитратной соли (16E)-14-метил-20-окса-5,7,14,26-тетраазатетрацикло[19.3.1.1(2,6).1(8,12)]гептакоза-1(25),2(26),3,5,8(27),9,11,16,21,23-декаена пациенту.
| US 8143255, 27.03.2012 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Ударно-вращательная врубовая машина | 1922 |
|
SU126A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2021-06-03—Публикация
2017-03-24—Подача