Настоящее изобретение относится к области медицины, к области получения лекарственного средства, обладающего антикоагулянтной активностью, а именно к способу получения гепарина натрия из слизистой оболочки тонкого кишечника сельскохозяйственных парнокопытных животных.
Гепарин натрия представляет собой вещество, содержащее натриевую соль сульфатированного гликозаминогликана из тканей млекопитающих. При полном гидролизе вещества образуется D-глюкозамин, D-глюкуроновая кислота, L-идуроновая кислота, уксусная кислота и серная кислота (Onishi A, St Ange K, Dordick JS, Linhardt RJ. Heparin and anticoagulation. Front Biosci (Landmark Ed). 2016 Jun 1; 21: 1372-92).
Антикоагуляционный эффект гепарина связан с прямым действием на систему свертывания крови за счет образования комплексов с многими факторами гемокоагуляции и проявляется в торможении I, II и III фаз свертывания. Сам гепарин активируется только в присутствии антитромбина III.
Гепарин натрия широко используется в медицине в качестве лекарственного средства, при этом являясь сырьем для производства низкомолекулярных гепаринов. Показаниями к применению гепарина натрия являются тромбозы, тромбоэмболии (профилактика и лечение), предупреждение свертывания крови (в сердечно-сосудистой хирургии), тромбозы коронарных сосудов, диссеминированное внутрисосудистое свертывание крови, послеоперационный период у больных с тромбоэмболиями в анамнезе. Профилактика свертывания крови во время операций с использованием экстракорпоральных методов кровообращения, заболевания поверхностных вен: варикозное расширение вен, хроническая венозная недостаточность и связанные с ней осложнения (тромбофлебит, перифлебит), тупые травмы и ушибы мягких тканей, подкожные гематомы, в том числе гематомы после операций на венах, флебэктомии, локализованные инфильтраты и отеки мягких тканей.
Изобретение может использоваться при получении лекарственного средства гепарина натрия в промышленных масштабах, в том числе для использования в качестве исходного сырья для производства лекарственных средств из группы низкомолекулярных гепаринов.
Гепарин получают из различных органов сельскохозяйственных животных - печень, легкие, но предпочтительно получают из слизистой оболочки тонкого кишечника свиней, ввиду отсутствия риска контаминации инфекционными агентами, вызывающими нейродегенеративные прионные болезни.
Наиболее близким к предлагаемому изобретению является способ получения гепарина из слизистой оболочки тонкого кишечника (мукозы) свиней (RU 2612813, опубл. 13.03.2017). Способ получения гепарина заключается в следующем. Замороженную слизистую оболочку тонкого кишечника свиней (мукозу), которая хранится не более 6 месяцев при температуре -20°С, размораживают, гомогенизируют, заливают 0,6 М раствором натрия хлорида, добавляют протеолитический фермент - алкалазу до конечной концентрации 0,1-0,5% и ведут ферментативный гидролиз при температуре 65°С и рН 8,5-8,6 в течение 6 часов, по истечении ферментативного гидролиза проводят инактивацию фермента при температуре 90°С в течение 15 минут, гидролизат охлаждают до температуры 15-20°С и центрифугируют, для дополнительной очистки гидролизата от балластных веществ белковой природы к надосадочной жидкости добавляют концентрированную соляную кислоту до рН 3,0, нагревают до температуры 70°С и выдерживают в течение 30 минут, образовавшийся осадок удаляют центрифугированием, после этого ведут сорбцию целевого продукта в динамическом режиме из надосадочной жидкости на анионите YMC-BioPro Q75, анионит предварительно уравновешивают 0,6 М раствором натрия хлорида, после завершения сорбции анионит промывают 0,6 М раствором натрия хлорида, удаление балластных веществ с анионита проводят 0,9 М раствором натрия хлорида, гепарин с анионита десорбируют раствором натрия хлорида с концентрацией 1,4 М с последующей ультрафильтрацией.
Недостатком указанного способа получения гепарина является присутствие родственных примесей антикоагулятно неактивного гепарина, что существенно повышает суммарную антикоагулятную активность на единицу массы вещества и, в свою очередь, не позволяет его использование его в качестве сырья для производства низкомолекулярных гепаринов, без проведения дополнительных операций очистки. Таким образом, данный способ позволяет получить гепарин натрия, который, тем не менее, не соответствует требованиям, предъявляемым к активной фармацевтической субстанции. Также к существенным недостаткам указанного способа получения гепарина является использование дорогостоящего фермента Alcalase® 2,5L. Вышеуказанные недостатки значительно сокращают эффективность и экономичность технологического процесса.
Задача настоящего изобретения заключается в том, чтобы предложить способ получения лекарственного средства гепарина натрия из слизистой оболочки тонкого кишечника сельскохозяйственных парнокопытных животных с использованием высокоэффективного и недорогого бактериального фермента субтилизин на стадии экстракции, редукции антикоагулянтно неактивных фракций гепарина натрия путем добавления ацетата натрия в пермеат с последующим осаждением метанолом и получением активной фармацевтической субстанции гепарина натрия.
Техническим результатом настоящего изобретения является: увеличение выхода фракций гепарина натрия, обладающих абсолютной антикоагулятной активностью, и, таким образом, в том числе, возможностью использования его в качестве сырья для производства лекарственных средств из группы низкомолекулярных гепаринов.
Согласно настоящему изобретению предложен способ получения гепарина с использованием бактериальной сериновой протеиназы - субтилизина, хроматографической очисткой на сильном анионообменном сорбенте. На финальных стадиях получения концентрируют элюат ультрафильтрацией с добавлением ацетата натрия. Раствор полупродукта после ультрафильтрации подвергают стерилизующей фильтрации и осаждению метанолом с выдерживанием смеси на холоде, центрифугированием и высушиванием осадка полупродукта в вакуум-сушильном шкафу.
С целью достижения указанного результата предложен способ, который включает следующие стадии:
Замороженную или жидкую слизистую оболочку тонкого кишечника сельскохозяйственных парнокопытных животных гомогенизируют и экстрагируют 0,5-0,6 М раствором натрия хлорида, добавление бактериального субтилизина до конечной концентрации 0,2-0,4% по объему. Ведут ферментативный гидролиз при температуре 50-70°С и рН 7,0-9,0 в течение 4-6 часов, после чего фермент инактивируют при температуре 90°С в течение 15-30 минут. Экстракт центрифугируют. Балластные примеси из осветленного экстракта удаляют осаждением при рН 2,5-4,0 и температуре 50-70°С в течение 30 минут. Образовавшийся осадок удаляют сепарацией. После этого ведут сорбцию целевого продукта из освобожденного от балластных примесей осветленного экстракта на анионообменном хроматографическом сорбенте. Могут быть использованы любые коммерчески доступные аниониты. Сорбент предварительно уравновешивают 0,6 М раствором натрия хлорида. После завершения сорбции сорбент промывают 0,6 М раствором натрия хлорида, удаляют балластные вещества с сорбента 0,9 М раствором натрия хлорида, гепарин с сорбента десорбируют раствором натрия хлорида с концентрацией 1,4 М. Элюат диафильтруют водой для инъекций и концентрируют ультрафильтрацией с добавлением ацетата натрия до содержания последнего 3,0-6,0% по массе. Раствор полупродукта после ультрафильтрации подвергают стерилизующей фильтрации и осаждению метанолом до окончательной массовой доли последнего - 35-38%. После чего смесь выдерживается при температуре 5±3°С в течение 18±0,5 часов и центрифугируется. Полученный полупродукт высушивается в вакуум-сушильном шкафу.
Использование бактериальной сериновой протеиназы - субтилизина, хроматографического разделения на анионообменном сорбенте и дополнительных стадий очистки элюата осаждением метанолом при добавлении ацетата натрия позволяют эффективно фракционировать полупродукт от родственных примесей антикоагулятно неактивного гепарина, что существенно повышает суммарную антикоагулятную активность на единицу массы вещества, тем самым позволяя снизить себестоимость готового продукта и получить лекарственное средство гепарин натрия высокой степени чистоты, полностью соответствующее требованиям Государственной Фармакопеи Российской Федерации.
Настоящее изобретение иллюстрируется следующими примерами
Пример 1
297,2 кг измельченной слизистой оболочки тонкого кишечника свиней, экстрагируют 0,5 М раствором натрия хлорида с рН 7,0, гомогенизируют и добавляют порошок субтилизина до конечной концентрации 0,2 об.%. Ферментативный гидролиз ведут 6 ч при температуре 50°С. По завершении гидролиза смесь нагревают до 90°С и выдерживают в течение 30 минут. Гидролизат центрифугируют. Получают 1033,4 л экстракта. В экстракт добавляют концентрированную хлористоводородную кислоту до достижения раствором экстракта рН=2,5, нагревают до 70°С и выдерживают 30 минут. Выпавший осадок отделяют центрифугированием. Фугат пропускают через хроматографический сорбент TOSOH TOYOPEARL GigaCap Q-650, уравновешенный 0,6 М раствором натрия хлорида. По завершении сорбции анионит промывают 0,6 М раствором натрия хлорида. Для удаления балластных примесей анионит промывают 0,9 М раствором натрия хлорида. Элюцию гепарина проводят раствором натрия хлорида с концентрацией 1,4 М. Элюат отбирают фракциями. Фракции, содержащие гепарин, объединяют. Получают 21,25 л элюата.
Элюат очищают от низкомолекулярных примесей, включая избыток натрия хлорида, в режиме диаультрафильтрации с добавлением ацетата натрия до содержания последнего 3,0 мас. % на кассетах с пределом отсечения по молекулярной массе 5 кДа.
Раствор полупродукта после ультрафильтрации подвергают стерилизующей фильтрации и осаждению метанолом до окончательной массовой доли последнего - 35%. После чего смесь выдерживается при температуре 4°С в течение 18±0.5 часов и центрифугируется. Полученный полупродукт высушивается в вакуум-сушильном шкафу.
Получают 0,063 кг активной фармацевтической субстанции гепарина натрия с антикоагулянтной активностью 262 МЕ/мг.
Пример 2
265,1 кг измельченной слизистой оболочки тонкого кишечника свиней, экстрагируют 0,56 М раствором натрия хлорида с рН 8,1, гомогенизируют и добавляют порошок субтилизина до конечной концентрации 0,3 об.%. Ферментативный гидролиз ведут 6 ч при температуре 60°С. По завершении гидролиза смесь нагревают до 90°С и выдерживают в течение 30 минут. Гидролизат центрифугируют. Получают 924,3 л экстракта. В экстракт добавляют концентрированную хлористоводородную кислоту до достижения раствором экстракта рН=3,5, нагревают до 70°С и выдерживают 30 минут. Выпавший осадок отделяют центрифугированием. Фугат пропускают через хроматографический сорбент Bio Rad UNOsphere™ Q Media, уравновешенный 0,6 M раствором натрия хлорида. По завершении сорбции анионит промывают 0,6 М раствором натрия хлорида. Для удаления балластных примесей анионит промывают 0,9 М раствором натрия хлорида. Элюцию гепарина проводят раствором натрия хлорида с концентрацией 1,4 М. Элюат отбирают фракциями. Фракции, содержащие гепарин, объединяют. Получают 20,73 л элюата.
Элюат очищают от низкомолекулярных примесей, включая избыток натрия хлорида, в режиме диаультрафильтрации с добавлением ацетата натрия до содержания последнего 4,4 мас.% на кассетах с пределом отсечения по молекулярной массе 5 кДа.
Раствор полупродукта после ультрафильтрации подвергают стерилизующей фильтрации и осаждению метанолом до окончательной массовой доли последнего - 36%. После чего смесь выдерживается при температуре 6°С в течение 18±0,5 часов и центрифугируется. Полученный полупродукт высушивается в вакуум-сушильном шкафу.
Получают 0,0586 кг активной фармацевтической субстанции гепарина натрия с антикоагулянтной активностью 279 МЕ/мг.
Пример 3
284,5 кг измельченной слизистой оболочки тонкого кишечника свиней, экстрагируют 0,6 М раствором натрия хлорида с рН 9,0, гомогенизируют и добавляют порошок субтилизина до конечной концентрации 0,4 об.%. Ферментативный гидролиз ведут 6 ч при температуре 70°С. По завершении гидролиза смесь нагревают до 90°С и выдерживают в течение 30 минут. Гидролизат центрифугируют. Получают 990,7 л экстракта. В экстракт добавляют концентрированную хлористоводородную кислоту до достижения раствором экстракта рН=4,5, нагревают до 70°С и выдерживают 30 минут. Выпавший осадок отделяют центрифугированием. Фугат пропускают через хроматографический сорбент TOSOH TOYOPEARL GigaCap Q-650, уравновешенный 0,6 М раствором натрия хлорида. По завершении сорбции анионит промывают 0,6 М раствором натрия хлорида. Для удаления балластных примесей анионит промывают 0,9 М раствором натрия хлорида. Элюцию гепарина проводят раствором натрия хлорида с концентрацией 1,4 М. Элюат отбирают фракциями. Фракции, содержащие гепарин, объединяют. Получают 21,13 л элюата.
Элюат очищают от низкомолекулярных примесей, включая избыток натрия хлорида, в режиме диаультрафильтрации с добавлением ацетата натрия до содержания последнего 6,0 мас.% на кассетах с пределом отсечения по молекулярной массе 5 кДа.
Раствор полупродукта после ультрафильтрации подвергают стерилизующей фильтрации и осаждению метанолом до окончательной массовой доли последнего - 38%. После чего смесь выдерживается при температуре 5°С в течение 18±0,5 часов и центрифугируется. Полученный полупродукт высушивается в вакуум-сушильном шкафу.
Получают 0,062 кг активной фармацевтической субстанции гепарина натрия с антикоагулянтной активностью 268 МЕ/мг.
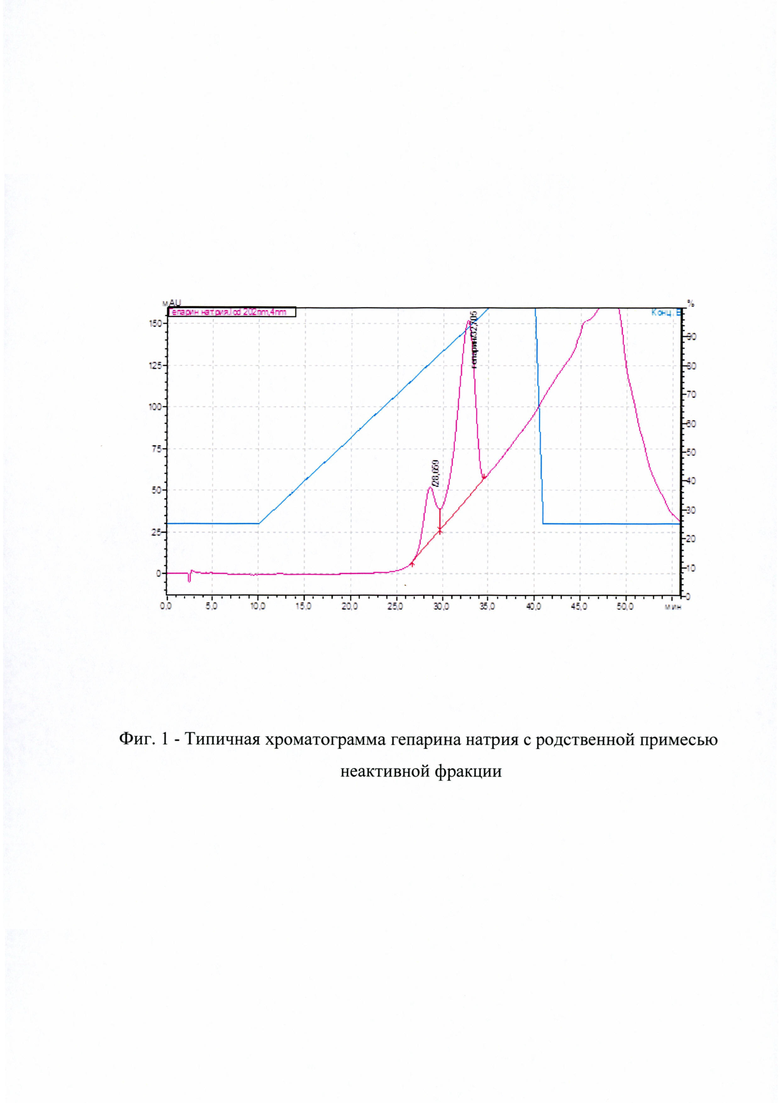
На фиг. 1 представлена типичная хроматограмма гепарина натрия с родственной примесью антикоагулянтно неактивной фракции; на фиг. 2 представлена типичная хроматограмма лекарственного средства гепарин натрия, полученного по способу, предложенному в настоящем изобретении.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ГЕПАРИНА | 2023 |
|
RU2828847C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕПАРИНА | 2015 |
|
RU2612813C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО АНТИГИПОКСИЧЕСКОЙ, РЕГЕНЕРАТИВНОЙ АКТИВНОСТЬЮ | 2020 |
|
RU2745443C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФАРМАЦЕВТИЧЕСКОЙ СУБСТАНЦИИ ГИАЛУРОНИДАЗЫ | 2018 |
|
RU2703108C1 |
| Способ хроматографического выделения и очистки иммуноглобулинов | 2018 |
|
RU2694620C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРЕПАРАТА "ИНГИПРОЛ" | 2001 |
|
RU2197252C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИНСУЛИНА | 1992 |
|
RU2027444C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОСНОВНОГО ИНГИБИТОРА ПРОТЕИНАЗ | 2001 |
|
RU2195316C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОСНОВНОГО ИНГИБИТОРА ПРОТЕАЗ ИЗ ОРГАНОВ КРУПНОГО РОГАТОГО СКОТА | 2002 |
|
RU2229888C2 |
| ПЕПТИДСОДЕРЖАЩАЯ ФРАКЦИЯ ИЗ СЕЛЕЗЕНКИ МЛЕКОПИТАЮЩИХ, ОБЛАДАЮЩАЯ ИММУНОСТИМУЛИРУЮЩЕЙ АКТИВНОСТЬЮ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1993 |
|
RU2033796C1 |

Изобретение относится к способу получения активной фармацевтической субстанции гепарина натрия. Способ включает экстракцию измельченной слизистой оболочки тонкого кишечника свиней 0,5-0,6 М раствором натрия хлорида, добавление субтилизина до конечной концентрации 0,2-0,4 об.%, ферментативный гидролиз при 50-70°С и рН 7,0-9,0 в течение 6 ч с последующей инактивацией фермента при 90°С в течение 30 мин. Осуществляют центрифугирование экстракта и осаждение балластных примесей при рН 2,5-4,5 и 70°С в течение 30 мин. Осуществляют сепарацию и сорбцию полупродукта гепарина из осветленного экстракта на анионообменном хроматографическом сорбенте, предварительно уравновешенном 0,6 М раствором натрия хлорида, промывку 0,6 М раствором натрия хлорида, удаление балластных веществ с сорбента 0,9 М раствором натрия хлорида и десорбцию раствором натрия хлорида с концентрацией 1,4 М. Элюат диафильтруют водой для инъекций, ультрафильтруют на кассетах с пределом отсечения 5 кДа с добавлением ацетата натрия до содержания последнего 3,0-6,0 мас.%. Раствор полупродукта после ультрафильтрации подвергают стерилизующей фильтрации и осаждению метанолом до окончательной массовой доли последнего - 35-38%. Полупродукт выдерживают при температуре 5±3°C в течение 18±0,5 ч, центрифугируют и сушат в вакуум-сушильном шкафу. Изобретение позволяет увеличить выход фракций гепарина натрия, обладающих антикоагулятной активностью. 3 пр., 2 ил.
Способ получения активной фармацевтической субстанции гепарина натрия, включающий экстракцию измельченной слизистой оболочки тонкого кишечника свиней 0,5-0,6 М раствором натрия хлорида, добавление субтилизина до конечной концентрации 0,2-0,4 об.%, ферментативный гидролиз при температуре 50-70°С и рН 7,0-9,0 в течение 6 часов с последующей инактивацией фермента при температуре 90°С в течение 30 минут, центрифугирование экстракта и осаждение балластных примесей при рН 2,5-4,5 и температуре 70°С в течение 30 минут, сепарацию и сорбцию полупродукта гепарина из осветленного экстракта на анионообменном хроматографическом сорбенте, предварительно уравновешенном 0,6 М раствором натрия хлорида, промывку 0,6 М раствором натрия хлорида, удаление балластных веществ с сорбента 0,9 М раствором натрия хлорида и десорбцию раствором натрия хлорида с концентрацией 1,4 М, диафильтрацию водой для инъекций, ультрафильтрацию на кассетах с пределом отсечения 5 кДа с добавлением ацетата натрия до содержания последнего 3,0-6,0 мас.%, стерилизующую фильтрацию, осаждение метанолом до окончательной массовой доли последнего - 35-38%, выдерживание при температуре 5±3°C в течение 18±0,5 часов, центрифугирование и сушку в вакуум-сушильном шкафу.
| СПОСОБ ПОЛУЧЕНИЯ ГЕПАРИНА | 2015 |
|
RU2612813C1 |
| CN 105237657 A, 13.01.2016 | |||
| CN 102040671 A, 04.05.2011 | |||
| VAN DER MEER J.Y | |||
| ET AL | |||
| From Farm to Pharma: An Overview of Industrial Heparin Manufacturing Methods | |||
| Molecules | |||
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| Автомобиль-сани, движущиеся на полозьях посредством устанавливающихся по высоте колес с шинами | 1924 |
|
SU2017A1 |
| VOLPI N | |||
| Purification of heparin, dermatan sulfate and chondroitin sulfate from mixtures by sequential | |||
Авторы
Даты
2021-06-10—Публикация
2020-06-10—Подача