ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к соединению пиридазинона или его соли. Точнее, оно относится к новому соединению пиризадинона или его соли, которые применимы в качестве активного ингредиента гербицида, и гербициду, содержащему указанные соединения.
УРОВЕНЬ ТЕХНИКИ
В Патентном документе 1 раскрывается соединение пиридазинона конкретной химической структуры. Соединение содержит -O-A группу в положении 4 бензольного кольца, замещенного пиридазиноновым кольцом, и его химическая структура отличается от химической структуры соединения по настоящему изобретению.
В Патентном документе 2 раскрывается гетероароматическое соединение конкретной химической структуры. Соединение не содержит пиридазинонового кольца в качестве заместителей в м-положениях (заместители R3 и R4 в Патентном документе 2) фенильного кольца, присоединенного к пиридиновому кольцу через L1, и его структура отличается от химической структуры соединения по настоящему изобретению.
В Патентном документе 3 раскрывается соединение пиридазинона конкретной химической структуры. Соединение содержит фенильную группу или гетероароматическую группу, непосредственно соединенную с заместителем G (бензольное кольцо) на пиридазиноновом кольце, и его химическая структура отличается от химической структуры соединения по настоящему изобретению.
В Патентном документе 4 раскрывается соединение пиридазинона конкретной химической структуры. Соединение содержит заместитель (заместитель R1 в Патентном документе 4), соответствующий заместителю Q в упомянутой выше формуле (I) по настоящему изобретению, который представляет собой группу NR10R11 или гетероциклоалкильную кольцевую группу, и его химическая структура отличается от химической структуры соединения по настоящему изобретению.
ДОКУМЕНТЫ ПРЕДШЕСТВУЮЩЕГО УРОВНЯ
ПАТЕНТНЫЕ ДОКУМЕНТЫ
Патентный документ 1: WO2014/119770
Патентный документ 2: WO2014/207601
Патентный документ 3: WO2009/086041
Патентный документ 4: WO2008/013838
РАСКРЫТИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
ТЕХНИЧЕСКАЯ ЗАДАЧА
Предметом настоящего изобретения является предоставление гербицида, обладающего превосходными гербицидными активностями в отношении сорной растительности, для экономии трудозатрат в борьбе с сорной растительностью и для повышения продуктивности сельскохозяйственных и садовых растений.
РЕШЕНИЕ ПРОБЛЕМЫ
Заявители настоящего изобретения провели обширные исследования для достижения вышеуказанной цели и в результате обнаружили, что соединение пиридазинона конкретной химической структуры обладает высокой гербицидной активностью в отношении широкого спектра сорной растительности в низкой дозе, и оформили настоящее изобретение.
Таким образом, настоящее изобретение относится к соединению пиридазинона, представленному формулой (I), или его соли:
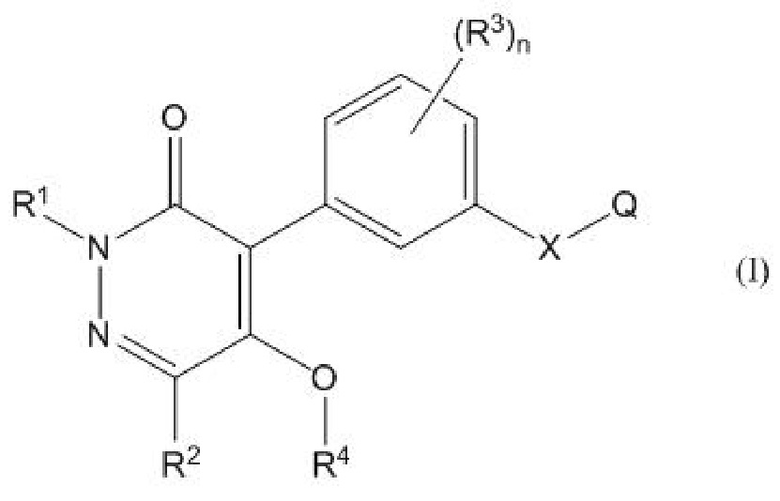
где X представляет собой -O-, -S-, -SO-, -SO2- или -N(Y)-;
Q представляет собой моноциклический арил, который может быть замещен Z, моноциклический гетероарил, который может быть замещен Z, бициклический арил, который может быть замещен Z, или бициклический гетероарил, который может быть замещен Z;
Y представляет собой атом водорода или алкил;
R1 представляет собой алкил, алкенил, алкинил, циклоалкил, циклоалкилалкил, галогеналкил, моноциклический арил, который может быть замещен Z, моноциклический арилалкил, который может быть замещен Z, алкилтиоалкил, алкилсульфинилалкил, алкилсульфонилалкил, диалкиламиноалкил, алкоксиалкил, амино, нитро, алкилкарбонилалкил, алкоксикарбонилалкил или гидроксикарбонилалкил;
R2 представляет собой атом водорода, алкил, галогеналкил, циклоалкил, галоген, алкокси, алкилтио, алкилсульфинил, алкилсульфонил или циано;
R3 представляет собой галоген, гидроксильную группу, алкил, галогеналкил, алкенил, галогеналкенил, алкинил, галогеналкинил, алкокси, галогеналкокси, нитро, амино, алкилкарбонил или циклоалкил;
R4 представляет собой атом водорода, алкил, -C(O)R6, -C(S)R6, -SR7, -SOR7, -SO2R7, моноциклический арилалкил, который может быть замещен Z, алкоксиалкил, -CH(J1)OCOOJ2, алкилкарбонилалкил, моноциклический арил, который может быть замещен Z, моноциклический арилкарбонилалкил, который может быть замещен Z, алкенил, алкоксиалкоксиалкил, алкоксикарбонилалкил, алкинил, цианоалкил, галогеналкоксиалкил или диалкиламиноалкил;
R6 представляет собой алкил, алкокси, морфолино, диалкиламино, (моноциклический арил, который может быть замещен Z)(алкил)амино, циклоалкил, алкоксиалкил, алкилтиоалкил, галогеналкил, алкилтио, алкенил, алкинил, алкоксикарбонилалкил, циклоалкилалкил, цианоалкил, алкоксиалкоксиалкил, моноциклический арил, который может быть замещен Z, моноциклический гетероарил, который может быть замещен Z, моноциклический арилалкил, который может быть замещен Z, моноциклический арилокси, который может быть замещен Z, моноциклический арилтио, который может быть замещен Z, моноциклический арилоксиалкил, который может быть замещен Z, моноциклический арилтиоалкил, который может быть замещен Z, алкоксикарбонил, алкоксиалкокси, галогеналкокси, галогеналкоксиалкокси, алкилтиоалкокси, циклоалкоксиалкокси, моноциклический арилалкокси, который может быть замещен Z, моноциклический арилоксиалкокси, который может быть замещен Z, моноциклический гетероарилоксиалкокси, который может быть замещен Z, алкенилоксиалкокси, алкоксиалкоксиалкокси, алкинилокси, алкенилокси, галогеналкенил, диалкиламиноалкил, алкилтиоалкоксиалкокси, циклоалкилалкокси, циклоалкилалкоксиалкокси, моноциклический арилалкоксиалкокси, который может быть замещен Z, моноциклический гетероарилалкоксиалкокси, который может быть замещен Z, или циклоалкокси, который может быть замещен Z;
R7 представляет собой алкил, галогеналкил, циклоалкил или моноциклический арил, который может быть замещен Z;
Z представляет собой галоген, алкил, галогеналкил, алкокси, галогеналкокси, циклоалкил, циано, нитро, -C(O)OR5, формил, алкилтио, алкилсульфинил, алкилсульфонил, -CH=NOJ3 или диалкиламинокарбонил;
R5 представляет собой атом водорода или алкил;
J1 представляет собой атом водорода или алкил;
J2 представляет собой алкил или циклоалкил;
J3 представляет собой атом водорода, алкилкарбонил или алкоксиалкил; и
n представляет собой целое число от 0 до 4.
Предпочтительно, настоящее изобретение относится к соединению пиридазинона, представленному формулой (I), или его соли:

где X представляет собой -O-, -S-, -SO-, -SO2- или -N(Y)-;
Q представляет собой моноциклический арил, который может быть замещен Z, моноциклический гетероарил, который может быть замещен Z, бициклический арил, который может быть замещен Z, или бициклический гетероарил, который может быть замещен Z;
Y представляет собой атом водорода или алкил;
Z представляет собой галоген, алкил, галогеналкил, циано, нитро или -C(O)OR5;
R1 представляет собой алкил, алкенил, алкинил или циклоалкил;
R2 представляет собой атом водорода, алкил, галогеналкил или циклоалкил;
R3 представляет собой галоген, алкил, галогеналкил, алкенил, галогеналкенил, алкинил, галогеналкинил, алкокси, галогеналкокси или циклоалкил;
R4 представляет собой атом водорода, алкил, -C(O)R6 или -SO2R7;
R5 представляет собой атом водорода или алкил;
R6 представляет собой алкил, алкокси или морфолино;
R7 представляет собой алкил; и
n представляет собой целое число от 1 до 4.
Настоящее изобретение также относится к соединению пиридазинона формулы (I) или его соли, гербициду, содержащему указанное соединение в качестве активного ингредиента, и к способу борьбы с нежелательными растениями или ингибирования их роста, который включает нанесение гербицидноэффективного количества соединения пиридазинона или его соли на нежелательные растения или на место их произрастания.
ПОЛЕЗНЫЕ ЭФФЕКТЫ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Соединение пиридазинона формулы (I) или его соль по настоящему изобретению обеспечивает значительное повышение гербицидных активностей в отношении нежелательных растений (сорной растительности) по сравнению с подобными обычными соединениями.
ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Атом галогена или атом галогена в качестве заместителя в формуле (I) может представлять собой атом фтора, хлора, брома или йода. Число атомов галогена в качестве заместителей может составлять 1 или по меньшей мере 2, и в случае по меньшей мере 2 соответствующие атомы галогена могут быть одинаковыми или отличаться друг от друга. Кроме того, положения замещения таких атомов галогенов могут быть любыми положениями.
Алкил или алкильный фрагмент в формуле (I) может представлять собой, например, линейную или разветвленную C1-C12 группу, такую как метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, неопентил, н-гексил, н-гептил, н-октил, н-нонил, н-децил, н-ундецил или н-додецил.
Алкокси или алкоксильный фрагмент в формуле (I) может представлять собой, например, линейную или разветвленную C1-C12 группу, такую как метокси, этокси, пропокси, изопропокси, бутокси, пентилокси, гексилокси, гептилокси, октилокси, нонилокси, децилокси, ундецилокси или додецилокси.
Алкенил или алкенильный фрагмент в формуле (I) может представлять собой, например, линейную или разветвленную C2-C6 группу, такую как винил, 1-пропенил, 2-пропенил, изопропенил, 2-метил-1-пропенил, 1-метил-1-пропенил, 2-метил-2-пропенил, 1-метил-2-пропенил, 1-бутенил, 2-бутенил, 3-бутенил, 1-пентенил, 2-пентенил, 2-метил-2-бутенил, 3-метил-2-бутенил, 1-гексенил или 2,3-диметил-2-бутенил.
Алкинил или алкинильный фрагмент в формуле (I) может представлять собой, например, линейную или разветвленную C2-C6 группу, такую как этинил, 1-пропинил, 2-пропинил, 1-бутинил, 2-бутинил, 3-бутинил, 1-метил-2-пропинил, 2-метил-3-бутинил, 1-гексинил, 2-гексинил, 3-гексинил, 4-гексинил или 5-гексинил.
Циклоалкил или циклоалкильный фрагмент в формуле (I) может представлять собой, например, C3-C7 группу, такую как циклопропил, циклобутил, циклопентил, циклогексил или циклогептил.
Циклоалкилокси или циклоалкилокси-фрагмент в формуле (I) может представлять собой, например, C3-C7 группу, такую как циклопропилокси, циклобутилокси, циклопентилокси, циклогексилокси или циклогептилокси.
Моноциклический арил в формуле (I) может представлять собой, например, фенил. Кроме того, моноциклический гетероарил может представлять собой, например, 3-6-членный гетероарил, содержащий от одного до четырех атомов O, S или N, в частности тиенил, фурил, пирролил, оксазолил, изоксазолил, изоксазолинил, тиазолил, изотиазолил, пиразолил, имидазолил, 1,3,4-оксадиазолил, 1,2,4-оксадиазолил, 1,3,4-тиадиазолил, 1,2,4-тиадиазолил, 1,2,4-триазолил, 1,2,3-триазолил, 1,2,3-тиадиазолил, 1,2,3,4-тетразолил, пиридил, пиримидил, пиразинил, пиридазинил, 1,3,5-триазинил, 1,2,4-триазинил, имидазолинил, имидазолидинил, пиразолинил или пиразолидинил.
Бициклический арил в формуле (I) может представлять собой, например, нафтил или инденил. Кроме того, бициклический гетероарил может представлять собой, например, конденсированный гетероарил 5-6-членного гетероциклического кольца, содержащий один или два атома O, S или N, и бензольного кольца, в частности бензотиенил, бензофурил, индолил, бензотиазолил, бензоимидазолил, бензоизоксазолил, бензоизотиазолил, индазолил, бензоксазолил, хинолил, изохинолил, хиноксалинил, фталазинил, циннолинил, хиназолинил, нафтиридинил, пиридопиримидил, пиридопиразинил, имидазолопиридил, тиазолопиридил, пиразолопиримидил, имидазолопиразинил, имидазолопиридазинил, триазолопиридил, пиразинопиразинил, пиразинопиридазинил, пиримидопиридазинил, пиримидопиримидил, пиридопиридазинил, пирролопиридил, тиенопиридил, оксазолопиридил, пиразолопиридил, изоксазолопиридил, изотиазолопиридил, пирролопиримидил, тиенопиримидил, имидазолопиримидил, оксазолопиримидил, тиазолопиримидил, изоксазолопиримидил, изотиазолопиримидил, пирролопиразинил, тиенопиразинил, оксазолопиразинил, тиазолопиразинил, пиразолопиразинил, изоксазолопиразинил, изотиазолопиразинил, пирролопиридазинил, тиенопиридазинил, оксазолопиридазинил, тиазолопиридазинил, пиразолопиридазинил, изоксазолопиридазинил, изотиазолопиридазинил, пуринил или птеридинил.
В формуле (I) термин «который может быть замещен Z» означает, что когда каждая группа замещена Z, заместитель Z может быть одним или количество заместителей может быть большим, и в случае, когда количество заместителей может составлять два или более, такие заместители могут быть одинаковыми или разными. Положение(я) замещения такого(их) заместителя(ей) может(гут) быть любым(ми) положением(ями).
Термин «соль соединения пиридазинона формулы (I)» включает все виды солей при условии, что они являются сельскохозяйственно приемлемыми, и, например, могут быть упомянуты соли щелочных металлов, такие как натриевая соль и калиевая соль; соли щелочно-земельных металлов, такие как магниевая соль и кальциевая соль; аминные соли, такие как диметиламинная соль и триэтиламинная соль; соли неорганических кислот, такие как гидрохлорид, перхлорат, сульфат и нитрат; и соли органических кислот, такие как ацетат и метансульфонат.
В качестве соединений пиридазинона формулы (I) иногда могут присутствовать изомеры, такие как диастереоизомеры и оптические изомеры, и настоящее изобретение включает соответствующие изомеры и смеси изомеров. В настоящем описании изомеры описываются как смесь, если не указано иное. Кроме того, в настоящем изобретении в область общих знаний данной области техники включены различные изомеры, отличные от вышеупомянутых типов изомеров. Далее, химическая структура изомера в зависимости от его типа может отличаться от представленной выше структуры формулы (I), но специалисту в данной области техники достаточно хорошо известно, что такая химическая структура является изомером формулы (I), и такой изомер, несомненно, входит в объем настоящего изобретения.
Соединение пиридазинона формулы (I) или его соль (далее - соединение по настоящему изобретению) может быть получено(а) в соответствии с описанным далее способом, в соответствии с обычным способом получения соли или в соответствии с представленными далее примерами получения. Однако способ получения соединения по настоящему изобретению не ограничивается представленными примерами.
[Способ получения 1]
Соединение формулы (I-1), которое представляет собой соединение по настоящему изобретению, может быть получено взаимодействием соединения, представленного формулой (I-2), и соединения, представленного формулой (II), в присутствии основания.
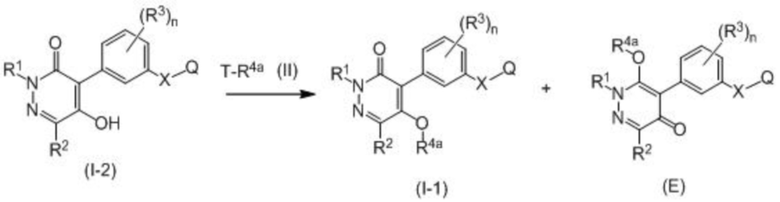
В формулах T представляет собой атом хлора, брома или йода, R4a представляет собой алкил, -C(O)R6, -C(S)R6, -SR7, -SOR7, -SO2R7, моноциклический арилалкил, который может быть замещен Z, алкоксиалкил, -CH(J1)OCOOJ2, алкилкарбонилалкил, моноциклический арил, который может быть замещен Z, моноциклический арилкарбонилалкил, который может быть замещен Z, алкенил, алкоксиалкоксиалкил, алкоксикарбонилалкил, алкинил, цианоалкил, галогеналкоксиалкил или диалкиламиноалкил, и X, Q, R1, R2, R3, R6, R7, Z, J1, J2 и n принимают значения, описанные выше.
Основание, используемое в данной реакции, может представлять собой, например, органическое основание, такое как триэтиламин или пиридин. Количество основания обычно составляет от 0,5 до 10 молярных эквивалентов, предпочтительно от 1 до 5 молярных эквивалентов, относительно соединения формулы (I-2).
Данную реакцию обычно проводят в присутствии растворителя. Растворитель конкретно не ограничен при условии, что он является инертным по отношению к реакции, и может представлять собой, например, простой эфир, такой как диэтиловый эфир, диоксан, тетрагидрофуран (ТГФ) или диметоксиэтан или их смесь.
Количество соединения формулы (II), используемое в данной реакции, обычно составляет от 0,5 до 10 молярных эквивалентов, предпочтительно от 1 до 3 молярных эквивалентов, относительно соединения формулы (I-2).
Температура данной реакции обычно составляет от -30 до 180°C, предпочтительно от -10 до 80°C. Продолжительность данной реакции обычно составляет от 10 минут до 30 часов.
В результате данной реакции образуется смесь соединения формулы (I-1) и его изомера, т.е. соединения, представленного формулой (E). Реакционную смесь, полученную в результате данной реакции, например, смешивают с водой и экстрагируют органический растворителем, полученный органический слой сушат, концентрируют и очищают колоночной хроматографией на силикагеле и т.п., с помощью чего может быть выделено соединение формулы (I-1).
Соединение формулы (II) является известным соединением или может быть получено хорошо известным способом из известного соединения.
[Способ получения 2]
Соединение формулы (I-2), которое представляет собой соединение по настоящему изобретению, может быть получено взаимодействием соединения, представленного формулой (I-3), и морфолина.
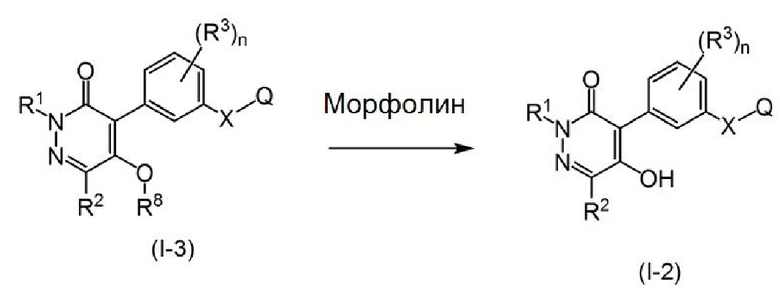
В формулах R8 представляет собой алкил или моноциклический арилалкил, который может быть замещен Z, такой как C1-3 алкил или бензил, и X, Q, R1, R2, R3, Z и n принимают значения, описанные выше.
Количество морфолина, используемое в данной реакции, обычно составляет от 1 до 20 молярных эквивалентов относительно соединения формулы (I-3).
Температура данной реакции обычно составляет от 30 до 180°C, предпочтительно от 50 до 130°C. Продолжительность данной реакции обычно составляет от 10 минут до 30 часов.
Кроме того, данная реакция может проводиться при облучении микроволнами, с помощью которых в некоторых случаях реакция может быть ускорена.
После завершения данной реакции реакционную смесь, например, смешивают с водой, подкисляют кислотой и экстрагируют органическим растворителем, полученный органический слой сушат, концентрируют, очищают колоночной хроматографией на силикагеле и т.п., посредством чего может быть выделено соединение формулы (I-2).
Кроме того, соединение формулы (I-2) может быть получено, например, в соответствии со способом, раскрытым в публикации Heterocycles, vol. 26, pages 1 to 4 (1987), или аналогичным способом.
[Способ получения 3]
Соединение формулы (I-3), которое представляет собой соединение по настоящему изобретению, может быть получено взаимодействием соединения, представленного формулой (III), и соединения, представленного формулой (IV), в присутствии основания или катализатора.
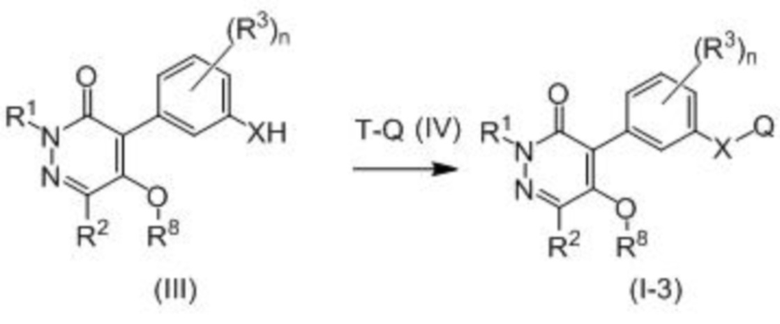
В формулах X, Q, R1, R2, R3, R8, T и n принимают значения, описанные выше.
Основание, используемое в данной реакции, может представлять собой, например, алкоксид металла, такой как трет-бутоксид калия; или неорганическое основание, такое как карбонат калия, карбонат цезия или гидрид натрия. Количество основания обычно составляет от 1 до 10 молярных эквивалентов, предпочтительно от 1 до 3 молярных эквивалентов, относительно соединения формулы (III).
Катализатор, используемый в данной реакции, может представлять собой, например, палладиевый катализатор, такой как ацетат палладия(II), тетракис(трифенилфосфин)палладий, трис(дибензилденацетон)дипалладий или дихлорид [1,1'-бис(дифенилфосфино)ферроцен]палладия; или медный катализатор, такой как дихлорид меди или йодид меди. Количество катализатора обычно составляет от 0,001 до 0,5 молярного эквивалента, предпочтительно от 0,01 до 0,2 молярного эквивалента, относительно соединения формулы (IV).
Данную реакцию обычно проводят в присутствии растворителя. Растворитель конкретно не ограничен при условии, что он является инертным по отношению к реакции, и может представлять собой, например, ароматический углеводород, такой как бензол, толуол или ксилол; простой эфир, такой как диэтиловый эфир, диоксан, ТГФ или диметоксиэтан; амид, такой как диметилформамид (ДМФА); сульфоксид, такой как диметилсульфоксид (DMSO); нитрил, такой как ацетонитрил; кетон, такой как ацетон; или их смесь.
Количество соединения формулы (IV), используемое в данной реакции, обычно составляет от 0,5 до 3 молярных эквивалентов, предпочтительно от 1 до 2 молярных эквивалентов, относительно соединения формулы (III).
Температура данной реакции обычно составляет от 0 до 200°C, предпочтительно от 20 до 100°C. Продолжительность данной реакции обычно составляет от 10 минут до 30 часов.
После завершения данной реакции реакционную смесь, например, нейтрализуют кислотой, смешивают с водой и экстрагируют органическим растворителем, полученный органический слой сушат, концентрируют, очищают колоночной хроматографией на силикагеле и т.п., посредством чего может быть выделено соединение формулы (I-3).
Соединение формулы (IV) является известным соединением или может быть получено хорошо известным способом из известного соединения.
[Способ получения 4]
Соединение представленной выше формулы (III) может быть получено взаимодействием соединения формулы (V) и кислоты.
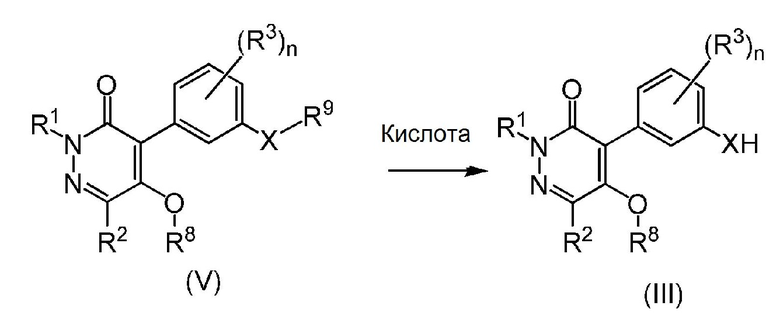
В формулах R9 представляет собой моноциклический арилалкил, который может быть замещен Z, такой как бензил или 4-метоксибензил, и X, R1, R2, R3, R8, Z и n принимают значения, описанные выше.
Кислота, используемая в данной реакции, может представлять собой, например, трифторуксусную кислоту. Количество кислоты обычно составляет от 1 до 20 молярных эквивалентов относительно соединения формулы (V).
Данную реакцию проводят в присутствии растворителя, когда это необходимо. Растворитель конкретно не ограничен при условии, что он является инертным по отношению к реакции, и может представлять собой, например, органическую кислоту, такую как уксусная кислота или пропионовая кислота; воду; или их смесь.
Температура данной реакции обычно составляет от 30 до 180°C, предпочтительно от 50 до 130°C. Продолжительность данной реакции обычно составляет от 10 минут до 30 часов.
После завершения данной реакции реакционную смесь, например, смешивают с водой и экстрагируют органическим растворителем, полученный органический слой сушат, концентрируют, очищают колоночной хроматографией на силикагеле и т.п., посредством чего может быть выделено соединение формулы (III).
[Способ получения 5]
Соединение формулы (V) может быть получено взаимодействием соединения, представленного формулой (VI), и соединения, представленного формулой (VII) или (VIII), в присутствии основания и катализатора.
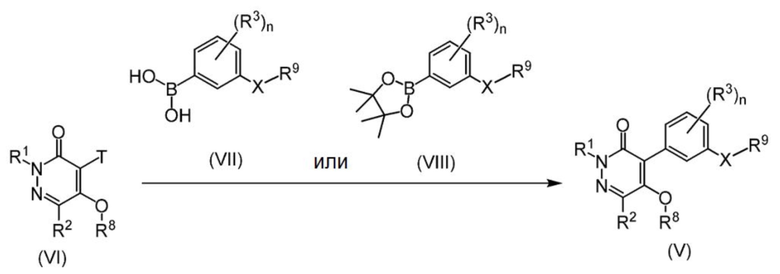
В формулах X, R1, R2, R3, R8, R9, T и n принимают значения, описанные выше.
Основание, используемое в данной реакции, может представлять собой, например, неорганическое основание, такое как карбонат натрия, карбонат калия, гидрокарбонат натрия, карбонат цезия или фосфат калия. Количество основания обычно составляет от 1 до 10 молярных эквивалентов, предпочтительно от 1 до 5 молярных эквивалентов, относительно соединения формулы (VI).
Катализатор, используемый в данной реакции, может представлять собой, например, палладиевый катализатор, такой как ацетат палладия(II), тетракис(трифенилфосфин)палладий, трис(дибензилденацетон)дипалладий или дихлорид [1,1'-бис(дифенилфосфино)ферроцен]палладия. Количество катализатора обычно составляет от 0,001 до 0,5 молярного эквивалента, предпочтительно от 0,01 до 0,2 молярного эквивалента, относительно соединения формулы (VI). Кроме того, в качестве катализатора может использоваться катализатор фазового переноса. Катализатор фазового переноса, используемый в реакции, может представлять собой, например, четвертичную алкиламмониевую соль, такую как бромид тетрабутиламмония или хлорид тетрабутиламмония. Количество катализатора фазового переноса обычно составляет от 0,001 до 1,0 молярного эквивалента, предпочтительно от 0,01 до 0,7 молярного эквивалента, относительно соединения формулы (VI).
Данную реакцию обычно проводят в присутствии растворителя. Растворитель конкретно не ограничен при условии, что он является инертным по отношению к реакции, и может представлять собой, например, ароматический углеводород, такой как бензол или толуол; спирт, такой как метанол, этанол или пропанол; простой эфир, такой как диэтиловый эфир, диоксан, ТГФ или диметоксиэтан; кетон, такой как ацетон или метилэтилкетон; амид, такой как ДМФА; сульфоксид, такой как ДМСО; воду; или их смесь.
В данной реакции при необходимости может использоваться лиганд. Лиганд может представлять собой, например, 2-дициклогексилфосфино-2',6'-диметоксибифенил. Количество лиганда обычно составляет от 0,002 до 1 молярного эквивалента, предпочтительно от 0,02 до 0,4 молярного эквивалента, относительно соединения формулы (VI).
Количество соединения формулы (VII) или (VIII), используемое в данной реакции, обычно составляет от 0,5 до 2 молярных эквивалентов, предпочтительно от 1 до 1,5 молярных эквивалентов, относительно соединения формулы (VI).
Температура данной реакции обычно составляет от 0 до 180°C, предпочтительно от 30 до 150°C. Продолжительность данной реакции обычно составляет от 10 минут до 100 часов.
После завершения данной реакции реакционную смесь, например, смешивают с водой и экстрагируют органическим растворителем, полученный органический слой сушат, концентрируют, очищают колоночной хроматографией на силикагеле и т.п., посредством чего может быть выделено соединение формулы (V).
Соединение формулы (VII) является известным соединением или может быть получено хорошо известным способом из известного соединения.
Соединение формулы (VI) является известным соединением или может быть получено хорошо известным способом из известного соединения. Например, соединение формулы (VI) может быть получено в соответствии со способом, раскрытым в публикации Journal of Heterocyclic Chemistry, vol. 33, pages 1579 to 1582 (1996), или аналогичным способом.
[Способ получения 6]
Соединение формулы (VIII) может быть получено взаимодействием соединения, представленного формулой (IX), и соединения, представленного формулой (X), в присутствии основания и катализатора.
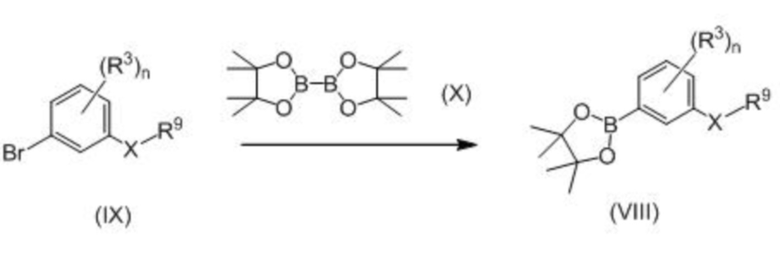
В формулах X, R3, R9 и n принимают значения, описанные выше.
Основание, используемое в данной реакции, может представлять собой, например, неорганическое основание, такое как карбонат натрия, карбонат калия, гидрокарбонат натрия, карбонат цезия, фосфат калия или ацетат калия. Количество основания обычно составляет от 1 до 10 молярных эквивалентов, предпочтительно от 1 до 5 молярных эквивалентов, относительно соединения формулы (IX).
Катализатор, используемый в данной реакции, может представлять собой, например, палладиевый катализатор, такой как ацетат палладия(II), тетракис(трифенилфосфин)палладий или трис(дибензилденацетон)дипалладий. Количество катализатора обычно составляет от 0,001 до 0,5 молярного эквивалента, предпочтительно от 0,01 до 0,2 молярного эквивалента, относительно соединения формулы (IX).
Данную реакцию обычно проводят в присутствии растворителя. Растворитель конкретно не ограничен при условии, что он является инертным по отношению к реакции, и может представлять собой, например, ароматический углеводород, такой как бензол или толуол; спирт, такой как метанол, этанол или пропанол; простой эфир, такой как диэтиловый эфир, диоксан, ТГФ или диметоксиэтан; кетон, такой как ацетон или метилэтилкетон; амид, такой как ДМФА; сульфоксид, такой как ДМСО; воду; или их смесь.
В данной реакции при необходимости может использоваться лиганд. Лиганд может представлять собой, например, трициклогексилфосфин или 2-дициклогексилфосфино-2',6'-диметоксибифенил. Количество лиганда обычно составляет от 0,002 до 1 молярного эквивалента, предпочтительно от 0,02 до 0,4 молярного эквивалента, относительно соединения формулы (IX).
Количество соединения формулы (X), используемое в данной реакции, обычно составляет от 0,5 до 2 молярных эквивалентов, предпочтительно от 1 до 1,5 молярных эквивалентов, относительно соединения формулы (IX).
Температура данной реакции обычно составляет от 0 до 180°C, предпочтительно от 30 до 150°C. Продолжительность данной реакции обычно составляет от 10 минут до 100 часов.
Кроме того, данная реакция может проводиться при облучении микроволнами, с помощью которых в некоторых случаях реакция может быть ускорена.
После завершения данной реакции реакционную смесь, например, смешивают с водой и экстрагируют органическим растворителем, полученный органический слой сушат, концентрируют, очищают колоночной хроматографией на силикагеле и т.п., посредством чего может быть выделено соединение формулы (VIII).
[Способ получения 7]
Соединение формулы (IX) может быть получено взаимодействием соединения, представленного формулой (XI), и соединения, представленного формулой (XII), в присутствии основания и катализатора.
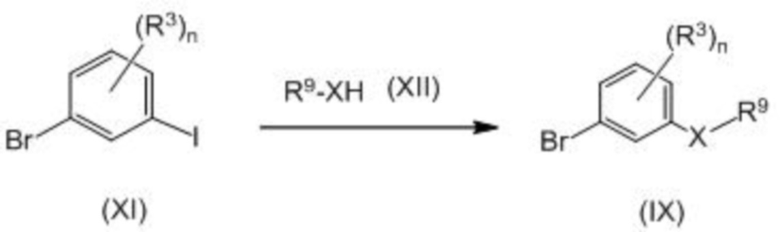
В формулах X, R3, R9 и n принимают значения, описанные выше.
Основание, используемое в данной реакции, может представлять собой, например, неорганическое основание, такое как карбонат натрия, карбонат калия, гидрокарбонат натрия, карбонат цезия или фосфат калия; или органическое основание, такое как триэтиламин или диизопропилэтиламин. Количество основания обычно составляет от 1 до 10 молярных эквивалентов, предпочтительно от 1 до 5 молярных эквивалентов, относительно соединения формулы (XI).
Катализатор, используемый в данной реакции, может представлять собой, например, палладиевый катализатор, такой как ацетат палладия(II), тетракис(трифенилфосфин)палладий или трис(дибензилденацетон)дипалладий. Количество катализатора обычно составляет от 0,001 до 0,5 молярного эквивалента, предпочтительно от 0,01 до 0,2 молярного эквивалента, относительно соединения формулы (XI).
Данную реакцию обычно проводят в присутствии растворителя. Растворитель конкретно не ограничен при условии, что он является инертным по отношению к реакции, и может представлять собой, например, ароматический углеводород, такой как бензол или толуол; спирт, такой как метанол, этанол или пропанол; простой эфир, такой как диэтиловый эфир, диоксан, ТГФ или диметоксиэтан; кетон, такой как ацетон или метилэтилкетон; амид, такой как ДМФА; сульфоксид, такой как ДМСО; воду; или их смесь.
В данной реакции при необходимости может использоваться лиганд. Лиганд может представлять собой, например, трициклогексилфосфин, 2-дициклогексилфосфино-2',6'-диметоксибифенил или 4,5-бис(дифенилфосфино)-9,9-диметилксантен. Количество лиганда обычно составляет от 0,002 до 1 молярного эквивалента, предпочтительно от 0,02 до 0,4 молярного эквивалента, относительно соединения формулы (XI).
Количество соединения формулы (XII), используемое в данной реакции, обычно составляет от 0,5 до 2 молярных эквивалентов, предпочтительно от 1 до 1,5 молярных эквивалентов, относительно соединения формулы (XI).
Температура данной реакции обычно составляет от 0 до 180°C, предпочтительно от 30 до 150°C. Продолжительность данной реакции обычно составляет от 10 минут до 100 часов.
После завершения данной реакции реакционную смесь, например, смешивают с водой и экстрагируют органическим растворителем, полученный органический слой сушат, концентрируют, очищают колоночной хроматографией на силикагеле и т.п., посредством чего может быть выделено соединение формулы (IX).
Соединение формулы (XI) является известным соединением или может быть получено хорошо известным способом из известного соединения.
Соединение формулы (XII) является известным соединением.
[Способ получения 8]
Соединение формулы (IX) может быть получено взаимодействием соединения, представленного формулой (XIII), и соединения, представленного формулой (XIV), в присутствии основания.
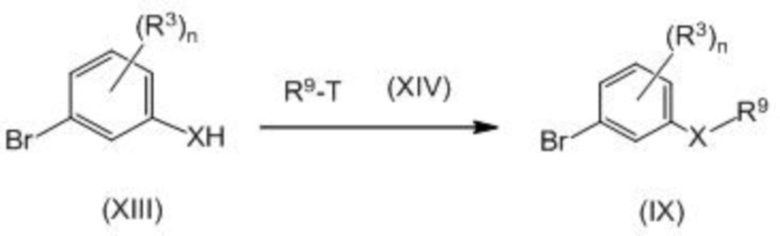
В формулах X, R3, R9, T и n принимают значения, описанные выше.
Основание, используемое в данной реакции, может представлять собой, например, алкоксид металла, такой как трет-бутоксид калия; или неорганическое основание, такое как карбонат калия, карбонат цезия или гидрид натрия. Количество основания обычно составляет от 1 до 10 молярных эквивалентов, предпочтительно от 1 до 3 молярных эквивалентов, относительно соединения формулы (XIII).
Данную реакцию обычно проводят в присутствии растворителя. Растворитель конкретно не ограничен при условии, что он является инертным по отношению к реакции, и может представлять собой, например, ароматический углеводород, такой как бензол, толуол или ксилол; простой эфир, такой как диэтиловый эфир, диоксан, ТГФ или диметоксиэтан; амид, такой как ДМФА; сульфоксид, такой как ДМСО; нитрил, такой как ацетонитрил; кетон, такой как ацетон; или их смесь.
Количество соединения формулы (XIV), используемое в данной реакции, обычно составляет от 0,5 до 3 молярных эквивалентов, предпочтительно от 1 до 2 молярных эквивалентов, относительно соединения формулы (XIII).
Температура данной реакции обычно составляет от 0 до 200°C, предпочтительно от 20 до 100°C. Продолжительность данной реакции обычно составляет от 10 минут до 30 часов.
После завершения данной реакции реакционную смесь, например, нейтрализуют кислотой, смешивают с водой и экстрагируют органическим растворителем, полученный органический слой сушат, концентрируют, очищают колоночной хроматографией на силикагеле и т.п., посредством чего может быть выделено соединение формулы (IX).
Соединение формулы (XIII) является известным соединением или может быть получено хорошо известным способом из известного соединения.
Способы получения промежуточных соединений, предназначенных для использования при получении соединений по настоящему изобретению, не ограничиваются представленными выше примерами способобв получения, и может использоваться любой способ получения. Кроме того, различные исходные вещества также не ограничиваются представленными выше примерами соединений, и могут использоваться любые соединения при условии, что они могут приводить к получению соединений по настоящему изобретению.
Соединения по настоящему изобретению способны бороться с широким спектром нежелательной сорной растительности, такой как однолетние и многолетние сорняки, в частности различные вредные сорняки, например злаковые, такие как просо куриное (Echinochloa crus-qalli L., Echinochloa oryzicola vasing.), росичка (Digitaria sanguinalis L., Digitaria ischaemum Muhl., Digitaria adscendens Henr., Digitaria microbachne Henr., Digitaria horizontalis Willd.), щетинник зеленый (Setaria viridis L.), щетинник большой (Setaria faberi Herrm.), щетинник желтый (Setaria lutescens Hubb.), элевзина индийская (Eleusine indica L.), овсюг (Avena fatua L.), джонсова трава (Sorghum halepense L.), пырей ползучий (Agropyron repens L.), брахиария гусеницевидная (Brachiaria plantaginea), гвинейская трава (Panicum maximum Jacq.), просо пурпуровое (Panicum purpurascens), просо ветвисто-метельчатое (Panicum dichotomiflorum), лептохлоя (Leptochloa chinensis), лептохлоя красная (Leptochloa panicea), мятлик однолетний (Poa annua L.), лисохвост (Alopecurus myosuroides Huds., Alopecurus aequalis Sobol.), бородач колорадский (Agropyron tsukushiense (Honda) Ohwi), брахиария широколистная (Brachiaria platyphylla Nash), ценхрус южный (Cenchrus echinatus L.), плевел многоцветковый (Lolium multiflorum Lam.), плевел жесткий (Lolium rigidum Gaud.), костер кровельный (Bromus tectorum L.) и свинорой пальчатый (Cynodon dactylon Pers.); осоковые, такие как сыть ириа (Cyperus iria L.), циперус пурпурный (Cyperus rotundus L.), чуфа (Cyperus esculentus L.), камыш японский (Scirpus juncoides), сыть вееровидная (Cyperus serotinus), сыть разнородная (Cyperus difformis), ситняг игольчатый (Eleocharis acicularis) и рогульник плавающий (Eleocharis kuroquwai); частуховые, такие как стрелолист японский карликовый (Sagittaria pygmaea), стрелолист трехлистный (Sagittaria trifolia) и частуха желобчатая (Alisma canaliculatum); понтидериевые, такие как монохория (Monochoria vaginalis) и разновидности монохории (Monochoria korsakowii); норичниковые, такие как бедренец ложный (Lindernia pyxidaria); подорожниковые, так как допатриум ситниковый (Dopatrium junceum); дербенниковые, такие как ротала (Rotala india) и аммания мультифлора красная (Ammannia multiflora); повойничковые, такие как повойничек трехтычинковый (Elatine triandra SCHK); мальвовые, такие как канатник Теофраста (Abutilon theophrasti MEDIC) и сида колючая (Sida spinosa L.); сложноцветные, такие дурнишник обыкновенный (Xanthium strumarium L.), амброзия полиннолистная (Ambrosia elatior L.), бодяк щетинистый (Breea setosa (BIEB.) KITAM.), галинзога реснитчатая (Galinsoqa ciliata Blake), ромашка лекарственная (Matricaria chamomilla L.), яснотка стеблеобъемлющая (Lamium amplexicaule L.), одуванчик лекарственный (Taraxacum officinale weber) и мелколепестник канадский (Erigeron canadensis L.); пасленовые, такие как паслен черный (Solanum nigrum L.) и дурман вонючий (Datura stramonium); амарантовые, такие как щирица зеленая (Amaranthus viridis L.), щирица запрокинутая (Amaranthus retroflexus L.), марь белая (Chenopodium album L.) и кохия веничная (Kochia scoparia Schrad.); гречишные, такие как горец развесистый (Polygonum lapathifolium L.), горец почечуйный (Polygonum persicaria L.), горец вьюнковый (Polygonum convolvulus L.) и горец птичий (Polygonum aviculare L.); крестоцветные, такие как сердечник извилистый (Cardamine flexuosa WITH.), пастушья сумка обыкновенная (Capsella bursapastoris Medik.) и горчица сарептская (Brassica juncea Czern.); вьюнковые, такие как ипомея пурпурная (Ipomoea purpurea L.), вьюнок полевой (Convolvulus arvensis L.) и ипомея плющевидная (Ipomoea hederacea Jacq.); портулаковые, такие как портулак обыкновенный (Portulaca oleracea L.); бобовые, такие как кассия туполистная (Cassia obtusifolia L.); гвоздичные, такие как звездчатка обыкновенная (Stellaria media L.); мареновые, такие как подмаренник ложный (Galium spurium L.); молочайные, такие как акалифа южная (Acalypha australis L.); и коммелиновые, такие как коммелина обыкновенная (Commelina communis L.). Таким образом, соединение по настоящему изобретению может эффективно использоваться для селективной борьбы с вредной сорной растительностью или неселективной борьбы с вредной сорной растительностью при выращивании полезных сельскохозяйственных культур, таких как кукуруза (Zea mays L.), соя (Glycine max Merr.), хлопчатник (Gossypium spp.), пшеница(Triticum aestivum L.), рис (Oryza sativa L.), ячмень (Hordeum vulgare L.), рожь (Secale cereale L.), овес (Avena sativa L.), сорго (Sorghum bicolor Moench), рапс (Brassica napus L.), подсолнечник (Helianthus annuus L.), сахарная свекла (Beta vulgaris L.), сахарный тростник (Saccharum officinarum L.), цойсия японская (Zoysia japonica stend), арахис (Arachis hypogaea L.), лен (Linum usitatissimum L.), табак (Nicotiana tabacum L.) и кофе (Coffea spp.).
Соединение по настоящему изобретению можно смешивать с различными сельскохозяйственными добавками и применять в форме различных препаратов, таких как дусты, гранулы, вододиспергируемые гранулы, смачивающиеся порошки, таблетки, пилюли, капсулы (включая препарат, помещенный в растворимую в воде пленку), водные суспензии, масляные суспензии, микроэмульсии, суспоэмульсии, растворимые в воде порошки, эмульгируемые концентраты, растворимые концентраты или пасты. Оно может формоваться в любой препарат, который традиционно используется в данной области техники, при условии, что достигается цель настоящего изобретения.
Добавки, используемые для препарата, включают, например, твердый носитель, такой как диатомовая земля, гашеная известь, карбонат кальция, тальк, белая сажа, каолин, бентонит, каолинит, серицит, глина, карбонат натрия, бикарбонат натрия, мирабилит, цеолит или крахмал; растворитель, такой как вода, толуол, ксилол, сольвент нафта, диоксан, ацетон, изофорон, метилизобутилкетон, хлорбензол, циклогексан, диметилсульфоксид, N,N-диметилформамид, диметилацетамид, N-метил-2-пирролидон или спирт; анионогенное поверхностно-активное вещество или распределяющее вещество, такое как соль жирной кислоты, бензоат, алкилсульфосукцинат, диалкилсульфосукцинат, поликарбоксилат, соль сложного эфира алкилсерной кислоты, алкилсульфат, алкиларилсульфат, сульфат алкилдигликолевого эфира, соль сложного эфира серной кислоты и спирта, алкилсульфонат, алкиларилсульфонат, арилсульфонат, лигнилсульфонат, дисульфонат алкилдифенилэфира, полистиролсульфонат, соль сложного эфира алкилфосфорной кислоты, алкиларилфосфат, стириларилфосфат, соль сложного эфира серной кислоты и простого полиоксиэтиленалкилового эфира, полиоксиэтиленалкиларилэфирсульфат, соль сложного эфира серной кислоты и простого оксиэтиленалкиларилового эфира, полиоксиэтилалкилэфир фосфат, соль сложного эфира полиоксиэтиленалкиларилфосфорной кислоты, соль сложного эфира фосфорной кислоты и простого алкилового эфира полиоксиэтилена, нафталинсульфонат, конденсированный с формальдегидом, или алкилнафталинсульфонат, конденсированный с формальдегидом; неионогенное поверхностно-активное вещество или распределяющее вещество, такое как сложный эфир сорбита и жирной кислоты, сложный эфир глицерина и жирной кислоты, полиглицерид жирной кислоты, полигликолевый эфир спирта жирной кислота, ацетиленгликоль, спирт ацетиленового ряда, оксиалкиленовый блок-сополимер, полиоксиэтиленалкилэфир, полиоксиэтиленалкиларилэфир, полиоксиэтиленстириларилэфир, полиоксиэтиленгликольалкилэфир, полиэтиленгликоль, сложный эфир полиоксиэтилена и жирной кислоты, сложный полиоксиэтиленовый эфир сорбита и жирной кислоты, сложный полиоксиэтиленовый эфир глицерина и жирной кислоты, полиоксиэтиленгидрогенизированное касторовое масло или сложный эфир полиоксипропилена и жирной кислоты; и растительное масло или минеральное масло, такое как оливковое масло, капоковое масло, касторовое масло, пальмовое масло, масло камелии, кокосовое масло, кунжутное масло, кукурузное масло, масло из рисовых отрубей, арахисовое масло, хлопковое масло, соевое масло, рапсовое масло, льняное масло, тунговое масло или жидкие парафины. Эти добавки могут подходящим образом выбираться для применения по отдельности или в комбинации в виде смеси двух или нескольких из них при условии, что достигается цель настоящего изобретения. Кроме того, могут использоваться различные традиционно применяемые добавки, такие как наполнитель, загуститель, вещество, препятствующее осаждению, вещество, предохраняющее от замерзания, стабилизатор дисперсии, антидот, вещество, предохраняющее от плесени, вспенивающая добавка, дезинтегратор и связующее вещество. Массовое соотношение при смешивании соединения по настоящему изобретению и таких различных добавок может составлять от 0,1:99,9 до 95:5, предпочтительно от 0,2:99,8 до 85:15 по массе. Метод смешивания соединения по настоящему изобретению и различных добавок конкретно не ограничен, и они могут подходящим образом смешиваться в соответствии с хорошо известным способом.
Доза гербицида, содержащего соединение по настоящему изобретению (гербицидноэффективное количество соединения по настоящему изобретению), как правило, не может быть определена, поскольку она изменяется в зависимости от погодных условий, состояния почвы, типа препарата, вида нежелательных растений, подлежащих контролю, сезона применения и т.д. Тем не менее, он обычно применяется в количестве, содержащем предпочтительно от 0,1 до 5000 г, более предпочтительно от 0,5 до 3000 г, еще более предпочтительно от 1 до 1,000 г, особенно предпочтительно от 10 до 500 г на гектар соединения по настоящему изобретению (называемое далее количеством активного ингредиента). Настоящее изобретение включает способ борьбы с нежелательными растениями с помощью такого применения гербицида.
Далее, гербицид, содержащий соединение по настоящему изобретению, может применяться сам по себе или в виде смеси или в комбинации с другими сельскохозяйственными химикатами, удобрениями, антидотами или т.п. Когда гербицид применяется в виде смеси или в комбинации, в некоторых случаях может быть получены превосходные эффекты или превосходное действие. Такие другие сельскохозяйственные химикаты включают, например, гербицид, фунгицид, антибиотик, растительный гормон и инсектицид. В частности, со смешанной гербицидной композицией, содержащей соединение по настоящему изобретению и один или несколько активных соединений или более активных соединений других гербицидов либо использующееся в комбинации с ними, спектр сорняков, подлежащих контролю, время применения композиции, гербицидные активности и т.д. могут улучшаться до предпочтительных значений. Соединение по настоящему изобретению и активные соединения других гербицидов могут вводиться в отдельные препараты, чтобы их можно было смешивать для применения во время нанесения, или они могут вводиться в один препарат. Настоящее изобретение включает такую смешанную гербицидную композицию.
Соотношение соединения по настоящему изобретению и активных соединений других гербицидов, как правило, не может быть определено, поскольку оно изменяется в зависимости от погодных условий, состояний почвы, типов препаратов, времени применения, способа применения и т.д., тем не менее, другие гербициды смешиваются в количестве предпочтительно от 0,001 до 10000 частей по массе, более предпочтительно от 0,01 до 1000 частей по массе на один тип активного соединения из расчета на 1 часть по массе соединения по настоящему изобретению. Кроме того, доза применения является такой, что общее количество активных соединений составляет от 0,1 до 10000 г, предпочтительно от 0,2 до 5000 г, более предпочтительно от 10 до 3000 г, на гектар. Настоящее изобретение включает способ борьбы с нежелательной сорной растительностью с помощью применения такой смешанной гербицидной композиции.
Другое гербицидноактивное соединение включает, например, представленные далее соединения (1) - (12) (общие названия, включая поданные на утверждение в ISO (международная организация по стандартизации)). В случае, когда такие соединения образуют соли, сложные алкиловые эфиры и т.д., они, разумеется, включаются в данный перечень, даже если они и не указаны конкретно.
(1) Соединения, которые, как полагают, проявляют гербицидное действие посредством нарушения гормональной активности растений, такие как фенокси-соединения, например 2,4-D, 2,4-D-бутотил, 2,4-D-бутил, 2,4-D-диметиламмоний, 2,4-D-диоламин, 2,4-D-этил, 2,4-D-2-этилгексил, 2,4-D-изобутил, 2,4-D-изоктил, 2,4-D-изопропил, 2,4-D-изопропиламмоний, 2,4-D-натрий, 2,4-D-изопропаноламмоний, 2,4-D-троламин, 2,4-DB, 2,4-DB-бутил, 2,4-DB-диметиламмоний, 2,4-DB-изоктил, 2,4-DB-калий, 2,4-DB-натрий, холиновая соль 2,4-D, дихлорпроп, дихлорпроп-бутотил, дихлорпроп-диметиламмоний, дихлорпроп-изоктил, дихлорпроп-калий, дихлорпроп-P, дихлорпроп-P-диметиламмоний, дихлорпроп-P-калий, дихлорпроп-P-натрий, MCPA, MCPA-бутотил, MCPA-диметиламмоний, MCPA-2-этилгексил, MCPA-калий, MCPA-натрий, MCPA-тиоэтил, MCPB, MCPB-этил, MCPB-натрий, мекопроп, мекопроп-бутотил, мекопроп-натрий, мекопроп-P, мекопроп-P-бутотил, мекопроп-P-диметиламмоний, мекопроп-P-2-этилгексил, мекопроп-P-калий, напроанилид, кломепроп или HIA-1; карбоновые кислоты ароматического ряда, например, 2,3,6-TBA, дикамба, дикамба-бутотил, дикамба-дигликольамин, дикамба-диметиламмоний, дикамба-диоламин, дикамба-изопропиламмоний, дикамба-калий, дикамба-натрий, пиклорам, пиклорам-диметиламмоний, пиклорам-изоктил, пиклорам-калий, пиклорам-триизопропаноламмоний, пиклорам-триизопропиламмоний, пиклорам-троламин, триклопир, триклопир-бутотил, триклопир-триэтиламмоний, клопиралид, клопиралид-оламин, клопиралид-калий, клопиралид-триизопропаноламмоний, аминопиралид, аминоциклопиразлор, галауксифен, галакусифен-метил или DAS-534; и напталам, напталам-натрий, беназолин, беназолин-этил, квинклорак, квинмерак, дифлуфензопир, дифлуфензопир-натрий, флуроксипир, флуроксипир-2-бутокси-1-метилэтил, флуроксипир-мептил, хлорфлуренол или хлорфлуренол-метил.
(2) Соединения, которые, как полагают, проявляют гербицидное действие посредством ингибирования фотосинтеза растений, такие как соединения мочевины, например хлоротолурон, диурон, фторметурон, линурон, изопротурон, метобензурон, тебутиурон, димефурон, изоурон, карбутилат, метабензтиазурон, метоксурон, монолинурон, небурон, сидурон, тербуметон или триэтазин; соединения триазина, например симазин, атразин, атратон, симетрин, прометрин, диметаметрин, гексазинон, метрибузин, тербутилазин, цианазин, аметрин, цибутрин, тербутрин, пропазин, метамитрон или прометон; соединения урацила, например бромацил, бромацил-литий, ленацил или тербацил; соединения анилида, например пропанил или ципромид; карбамат-соединения, например свеп, десмедифам или фенмедифам; соединения гидроксибензонитрила, например бромоксинил, бромоксинил-октаноат, бромоксинил-гептаноат, иоксинил, иоксинил-октаноат, иоксинил-калий или иоксинил-натрий; и пиридат, бентазон, бентазон-натрий, амикарбазон, метазол или пентанохлор или фенмедифам.
(3) Группа солей четвертичного аммониевого основания, например паракват или дикват, которые, как полагают, в организме растения сами по себе превращаются в свободные радикалы с образованием активного кислорода и демонстрируют быструю гербицидную эффективность.
(4) Соединения, которые, как полагают, проявляют гербицидное действие посредством ингибирования биосинтеза хлорофила растениями и избыточного накопления в растительном организме фотосенсибилизирующего пероксидного вещества, такие как соединения дифенилового эфира, например нитрофен, хлорметоксифен, бифенокс, ацилуорфен, ацифлуорфен-натрий, фомесафен, фомесафен-натрий, оксифлуорфен, лактофен, аклонифен, этоксифен-этил, фуорогликофен-этил или флуорогликофен; циклические имиды, например хлорфталим, флумиоксазин, флумиклорак, флумиклорак-пентил, цинидон-этил, флутиацет-метил или EK-5385; и оксадиаргил, оксадиазон, сульфентразон, карфентразон-этил, тиадиазимин, пентоксазон, азафенидин, изопропазол, пирафлуфен-этил, бензфендизон, бутафенацил, сафлуфенацил, флуазолат, профлуазол, флуфенпир-этил, бенкарбазон, тиафенацил, пирахлонил, трифлудимоксазин, HNPC-B4047, IR-6396, EK-5439, EK-5498, SYN-523 или соединения, раскрытые в WO2008/008763 (FMC CORPORATION).
(5) Соединения, которые, как полагают, проявляют гербицидное действие, характеризующееся обесцвечивающей активностью, посредством ингибирования хромогенеза растений, такие как каротиноиды, например соединения пиридазинона, такие как норфлуразон, хлоридазон или метфлуразон; соединения пиразола, например пиразолинат, пиразоксифен, бензофенап, топрамезон, пирасульфотол или толпиралат; и амитрол, флуридон, флуртамон, дифлуфеникан, метоксифенон, кломазон, сулкотрион, мезотрион, темботрион, тефурилтрион, фенквинотрион, циклопириморат, изоксафлутол, дифензокват, дифензокват-метилсульфат, изоксахлортол, бензобициклон, бициклопирон, пиколинафен, бефлутутамид, кетоспирадокс, кетоспирадокс-натрий или соединения, раскрытые в JP2012-2571 (Sumitomo Chemical).
(6) Соединения, которые, как полагают, проявляют гербицидное действие посредством ингибирования липидного биосинтеза растений, такие как соединения арилоксифеноксипропионовой кислоты, например диклофоп-метил, диклофоп, пирифеноп-натрий, флуазифоп-бутил, флуазифоп, флуазифоп-P, флуазифоп-P-бутил, галоксифоп-метил, галоксифоп, галоксифоп-этотил, галоксифоп-P, галоксифоп-P-метил, квизалофоп-этил, квизалофоп-P, квизалофоп-P-этил, квизалофоп-P-тефурил, цигалофоп-бутил, феноксапроп-этил, феноксапроп-P, феноксапроп-P-этил, метамифоп-пропил, метамифоп, клодинафоп-пропаргил, клодинафоп, пропаквизафоп, HNPC-A8169 или SYP-1924; соединения циклогександиона, например аллоксидим-натрий, аллоксидим, клетодим, сетоксидим, тралкоксидим, бутроксидим, тепралоксидим, профоксидим или циклоксидим; соединения фенилпиразолина, например пиноксаден.
(7) Соединения, которые, как полагают, проявляют гербицидное действие посредством ингибирования аминокислотного биосинтеза растений, такие как соединения сульфонилмочевины, например хлоримурон-этил, хлоримурон, сульфометурон-метил, сульфометурон, примисульфурон-метил, примисульфурон, бенсульфурон-метил, бенсульфурон, хлорсульфурон, метсульфурон-метил, метсульфурон, циносульфурон, пиразосульфурон-этил, пиразосульфурон, флазасульфурон, римсульфурон, никосульфурон, имазосульфурон, флуцетосульфурон, циклосульфамурон, просульфурон, флупирсульфурон-метил-натрий, флупирсульфурон, трифлусульфурон-метил, трифлусульфурон, галосульфурон-метил, галосульфурон, трифенсульфурон-метил, трифенсульфурон, этоксисульфурон, оксасульфурон, этаметсульфурон, этаметсульфурон-метил, иодосульфурон, иодосульфурон-метил-натрий, сульфосульфурон, триасульфурон, трибенурон-метил, трибенурон, тритосульфурон, форамсульфурон, трифлоксисульфурон, трифлоксисульфурон-натрий, мезосульфурон-метил, мезосульфурон, ортосульфамурон, амидосульфурон, азимсульфурон, пропирисульфурон, метазосульфурон, метиопирсульфурон, моносульфурон-метил, орсосульфурон, иофенсульфурон или иофенсульфурон-натрий; соединения триазолопиримидинсульфонамида, например флуметсулам, метосулам, диклосулам, клорансулам-метил, флорасулам, пеноксулам или пироксулам; соединения имидазолинона, например имазапир, имазапир-изопропиламмоний, имазетапир, имазетапир-аммоний, имазаквин, имазаквин-аммоний, имазамокс, имазамокс-аммоний, имазаметабенз, имазаметабенз-метил или имазапик; соединения пиримидинилсалициловой кислоты, например пиритиобак-натрий, биспирибак-натрий, пириминобак-метил, пирибензоксим, пирифталид, пиримисульфан или триафамон; соединения сульфониламинокарбонилтриазолинона, например флукарбазон, флукарбазон-натрий, пропоксикарбазон-натрий, пропоксикарбазон или тиенкарбазон-метил; и глифосат, глифосат-натрий, глифосат-калий, глифосат-аммоний, глифосат-диаммоний, глифосат-изопропиламмоний, глифосат-тримезиум, глифосат-сесквинатрий, глюфозинат, глюфозинат-аммоний, глюфозинат-P, глюфозинат-P-аммоний, глюфозинат-P-натрий, биланафос, биланафос-натрий или цинметилин.
(8) Соединения, которые, как полагают, проявляют гербицидное действие посредством ингибирования митоза клеток растений, такие как соединения динитроанилина, например трифлуралин, оризалин, нитралин, пендиметалин, эталфлуралин, бенфлуралин, продиамин, бутралин или динитрамин; соединения амидного типа, например бенсулид, напропамид, напропамид-М, пропизамид или пронамид; фосфорорганические соединения, например амипрофос-метил, бутамифос, анилофос или пиперофос; соединения фенилкарбамата, например профам, хлорпрофам, барбан или карбетамид; соединения кумиламина, например даимурон, кумилурон, бромобутид или метилдимрон; и асулам, асулам-натрий, дитиопир, тиазопир, хлортал-диметил, хлортал, дифенамид, флампроп-М-метил, флампроп-М или флампроп-М-изопропил.
(9) Соединения, которые, как полагают, проявляют гербицидное действие посредством ингибирования биосинтеза белков или биосинтеза липидов растений, такие как соединения хлорацетамида, например алахлор, метазахлор, бутахлор, претилахлор, метолахлор, S-метолахлор, тенилхлор, петоксамид, ацетохлор, пропахлор, диметенамид, диметенамид-P, пропизохлор или диметахлор; соединения тиокарбама, например молинат, димепиперат, пирибутикарб, EPTC, бутилат, вернолат, пебулат, циклоат, просульфокарб, эспрокарб, тиобенкарб, диаллат, три-аллат или орбенкарб; и этобензанид, мефенацет, флуфенацет, тридифан, кафенстрол, фентразамид, оксазикломефон, инданофан, бенфуресат, пироксасульфон, феноксасульфон, метиозолин, далапон, далапон-натрий, TCA-натрий или трихлоруксусная кислота.
(10) Соединения, которые, как полагают, проявляют гербицидное действие посредством ингибирования биосинтеза целлюлозы растений, такие как дихлобенил, триазифлам, индазифлам, флупоксам или изоксабен.
(11) MSMA, DSMA, CMA, эндоталл, эндоталл-дикалий, эндоталл-натрий, эндоталл-моно(N,N-диметилалкиламмоний), этофумезат, хлорат натрия, пеларгоновая кислота (нонановая кислота), фозамин, фозамин-аммоний, ипфенкарбазон, акролеин, сульфамат аммония, бура, хлоруксусная кислота, хлорацетат натрия, цианамид, метиларсоновая кислота, диметиларсиновая кислота, диметиларсинат натрия, динотерб, динотерб-аммоний, динотерб-диоламин, динотерб-ацетат, DNOC, сульфат железа(II), флупропанат, флупропанат-натрий, изоксабен, мефлуидид, мефлуидид-диоламин, метам, метам-аммоний, метам-калий, метам-натрий, метилизотиоцианат, пентахлорофенол, пентахлорфеноксид натрия, пентахлорфенол-лаурат, квинокламин, серная кислота, сульфат мочевины, ксантиносин, гербимицин, унгвинол, метатирозин, сарментин, таксомин А, мевалоцидин, альфа-мимонен, пирибамбенз-пропил, пирибамбенз-изопропил, JS-913, KHG-23844, H-9201, SIOC-0163, SIOC-0171, SIOC-0172, SIOC-0285, SIOC-0426, SIOC-H-057, ZJ-0166, ZJ-1835, ZJ-0453, ZJ-0777, ZJ-0862 и соединения, раскрытые в WO2008/096398 (Kumiai Chemical).
(12) Соединения, которые, как полагают, проявляют гербицидное действие паразитированием на растениях, например Xanthomonas campestris, Epicoccosirus nematosorus, Epicoccosirus nematosperus, Exserohilum monoseras или Drechsrela monoceras.
Одно или несколько соединений могут соответствующим образом выбираться из представленных выше соединений, которые являются активными соединениями других гербицидов. Активные соединения других гербицидов не ограничиваются представленными выше примерами соединений.
ПРИМЕРЫ
Далее настоящее изобретение будет описано более подробно со ссылкой на примеры, но следует иметь в виду, что настоящее изобретение не ограничивается представленными примерами. Сначала будут описаны примеры получения соединений по настоящему изобретению.
ПРИМЕР ПОЛУЧЕНИЯ 1
Получение 4-(5-((3-хлор-5-(трифторметил)пиридин-2-ил)тио)-2-метилфенил)-5-метокси-2,6-диметилпиридазин-3(2H)-она (далее - соединение № 1-32)
(1) В атмосфере азота диизопропилэтиламин (1,2 мл) добавляют к перемешиваемому раствору 2-бром-4-йод-1-метилбензола (1,0 г), (4-метоксифенил)метантиола (520 мг), трис(дибензилденацетон)дипалладия (80 мг), 4,5-бис(дифенилфосфино)-9,9-диметилксантена (100 мг) и 1,4-диоксана (10 мл) и кипятят с обратным холодильником полученную смесь в течение 1 часа. Полученную реакционную смесь охлаждают, смешивают с водой и дважды экстрагируют этилацетатом (30 мл). Органический слой промывают насыщенным раствором соли и сушат над безводным сульфатом натрия, растворитель отгоняют при пониженном давлении и очищают полученный остаток колоночной хроматографией (гептан:этилацетат=20:1, здесь и далее - объемное соотношение) с получением (3-бром-4-метилфенил)(4-метоксибензил)сульфана (1,07 г, выход: 98%) в виде масла коричневого цвета. Данные ЯМР спектра полученного очищенного продукта представлены ниже.
1Н ЯМР (300 МГц, CDCl3): δ м.д.=2,35 (3H, с), 3,79 (3H, с), 4,04 (2H, с), 6,83 (2H, д, J=8,7 Гц), 7,08-7,21 (4H, м), 7,48 (1H, д, J=0,6 Гц).
(2) В атмосфере азота раствор (3-бром-4-метилфенил)(4-метоксибензил)сульфана (1,07 г), бис(пинаколато)дибора (1,26 г), трис(дибензилденацетон)дипалладия (120 мг), трициклогексилфосфина (150 мг), ацетата калия (490 мг) и 1,4-диоксана (15 мл) перемешивают при 120°C в течение 7 часов. Реакционную смесь охлаждают, нерастворимое твердое вещество собирают фильтрацией через целит (Celite) и промывают этилацетатом. Растворитель отгоняют при пониженном давлении и очищают полученный остаток колоночной хроматографией (гептан:этилацетат=20:1) с получением 2-(5-((4-метоксибензил)тио)-2-метилфенил)-4,4,5,5-тетраметил-1,3,2-диоксаборолана (1,07 г, выход: 87%) в виде твердого белого вещества. Данные ЯМР спектра полученного очищенного продукта представлены ниже.
1Н ЯМР (300 МГц, CDCl3): δ м.д.=1,38 (12H, с), 2,48 (3H, с), 3,77 (3H, с), 4,03 (2H, с), 6,80 (2H, д, J=8,4 Гц), 7,04 (1H, д, J=8,1 Гц), 7,17-7,27 (3H, м), 7,76 (1H, дд, J=1,5 Гц, J=6,6 Гц).
(3) Раствор 2-(5-((4-метоксибензил)тио)-2-метилфенил)-4,4,5,5-тетраметил-1,3,2-диоксаборолана (381 мг), 4-бром-5-метокси-2,6-диметилпиридазин-3(2H)-она (200 мг), тетракис(трифенилфосфин)палладия (40 мг), карбоната натрия (200 мг), бромида тетрабутиламмония (144 мг), 1,4-диоксана (6 мл) и воды (4 мл) перемешивают при 120°C в течение 45 минут. Реакционную смесь охлаждают, смешивают с водой и дважды экстрагируют этилацетатом (20 мл). Органический слой промывают насыщенным раствором соли, сушат над безводным сульфатом натрия, растворитель отгоняют при пониженном давлении и очищают полученный остаток колоночной хроматографией (гептан:этилацетат=1:1) с получением 5-метокси-4-(5-((4-метоксибензил)тио)-2-метилфенил)-2,6-диметилпиридазин-3(2H)-она (275 мг, выход: 81%) в виде твердого белого вещества. Данные ЯМР спектра полученного очищенного продукта представлены ниже.
1Н ЯМР (300 МГц, CDCl3): δ м.д.=2,16 (3H, с), 2,27 (3H, с), 3,24 (3H, с), 3,68 (3H, с), 3,77 (3H, с), 4,03 (2H, с), 6,79 (2H, д, J=8,7 Гц), 7,15-7,26 (5H, м).
(4) 5-Метокси-4-(5-((4-метоксибензил)тио)-2-метилфенил)-2,6-диметилпиридазин-3(2H)-он (275 мг) растворяют в трифторуксусной кислоте (2 мл) и выдерживают при 60°C в течение 3 часов. Смесь охлаждают и отгоняют растворитель при пониженном давлении с получением 4-(5-меркапто-2-метилфенил)-5-метокси-2,6-диметилпиридазин-3(2H)-она (190 мг, выход: 99%) в виде твердого вещества коричневого цвета.
(5) Раствор 4-(5-меркапто-2-метилфенил)-5-метокси-2,6-диметилпиридазин-3(2H)-она (190 мг), полученного на предыдущей стадии (4), 2,3-дихлор-5-(трифторметил)пиридина (223 мг), карбоната цезия (336 мг) и диметилформамида (5 мл) перемешивают при 60°C в течение 3 часов. Смесь охлаждают, смешивают с водой и дважды экстрагируют этилацетатом (20 мл). Органический слой промывают насыщенным раствором соли, сушат над безводным сульфатом натрия, растворитель отгоняют при пониженном давлении и очищают полученный остаток колоночной хроматографией (гептан:этилацетат=3:2) с получением целевого продукта (122 мг, выход: 39%) в виде твердого белого вещества. Данные ЯМР спектра очищенного продукта представлены ниже.
1Н ЯМР (300 МГц, CDCl3): δ м.д.=2,24 (3H, с), 2,30 (3H, с), 3,53 (3H, с), 3,73 (3H, с), 7,36-7,38 (2H, м), 7,48 (1H, дд, J=2,1 Гц, J=8,4 Гц), 7,76 (1H, дд, J=0,6 Гц, J=2,1 Гц), 8,33 (1H, дд, J=0,9 Гц, J=1,8 Гц).
ПРИМЕР ПОЛУЧЕНИЯ 2
Получение 4-(5-((3-хлор-5-(трифторметил)пиридин-2-ил)тио)-2-метилфенил)-5-гидрокси-2,6-диметилпиридазин-3(2H)-она (далее -соединение № 1-2)
4-(5-((3-Хлор-5-(трифторметил)пиридин-2-ил)тио)-2-метилфенил)-5-метокси-2,6-диметилпиридазин-3(2H)-он (122 мг) растворяют в морфолине (2 мл), помещают в герметичную пробирку и подвергают обработке микроволновым излучением при 140°C в течение 50 минут. После завершения реакции избыток морфолина отгоняют, остаток подкисляют уксусной кислотой и дважды экстрагируют водный слой этилацетатом (10 мл). Полученный органический слой сушат над сульфатом натрия, растворитель отгоняют при пониженном давлении и очищают полученный остаток колоночной хроматографией (гептан:этилацетат=1:1) с получением целевого продукта (51 мг, выход: 43%) в виде твердого белого вещества. Температура плавления полученного продукта находится в интервале от 99 до 102°C, и данные его ЯМР спектра представлены ниже.
1Н ЯМР (300 МГц, CDCl3): δ м.д.=2,24 (3H, с), 2,30 (3H, с), 3,73 (3H, с), 7,36-7,48 (3H, м), 7,79 (1H, д, J=1,8 Гц), 8,32 (1H, дд, J=0,9 Гц, J=1,8 Гц).
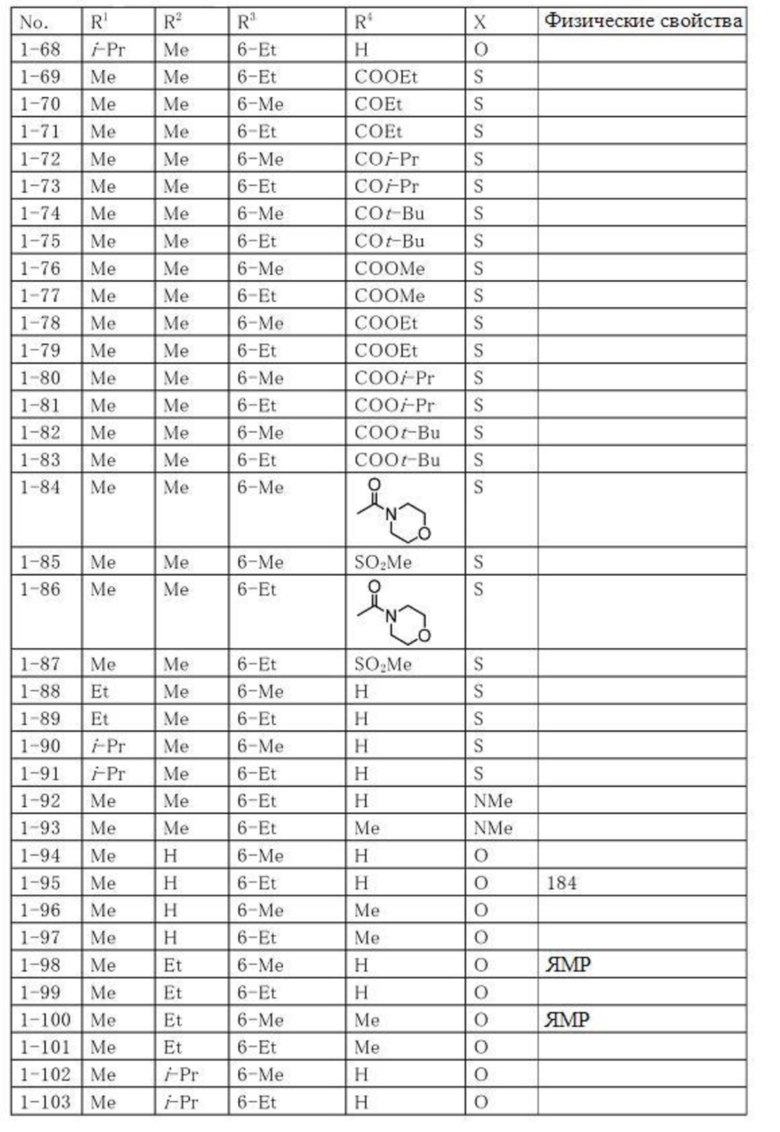
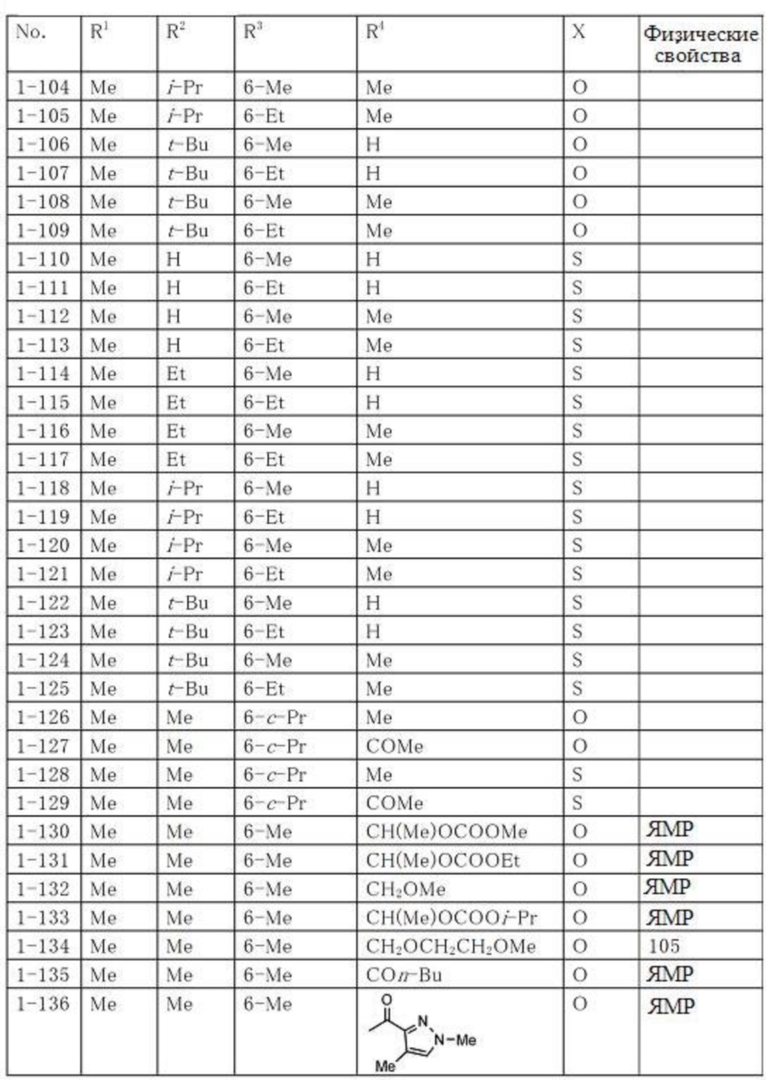
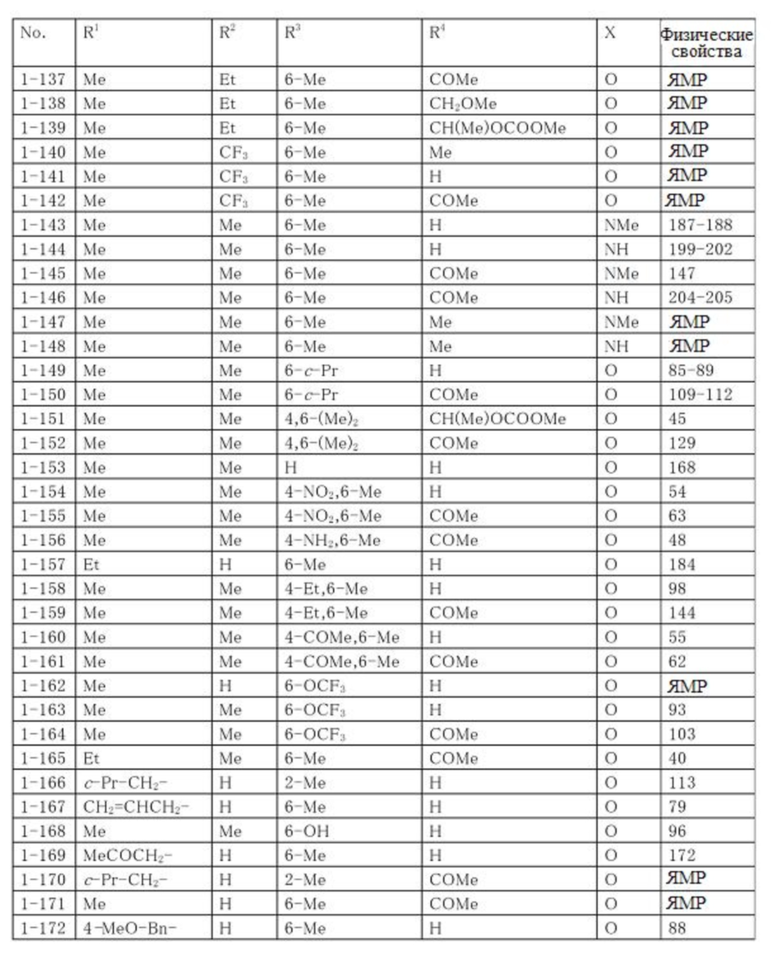
Типичные примеры соединений по настоящему изобретению представлены в таблицах 1-3. Эти соединения могут быть получены в соответствии с представленными примерами получения и способами получения. В таблицах 1- 3 № представляет собой номер соединения, Me представляет собой метильную группу, Et представляет собой этильную группу, Pr представляет собой н-пропильную группу, i-Pr представляет собой изопропильную группу, n-Bu представляет собой н-бутильную группу, t-Bu представляет собой трет-бутильную группу, c-Pr представляет собй циклопропильную группу, c-Hex представляет собой циклогексильную группу, Ph представляет собой фенильную группу, и Bn представляет собой бензильную группу, соответственно. Далее, "2,6-(Me)2" в таблицах означает, что метильные группы в качестве заместителей находятся во 2- и 6-положениях, соответственно, и это применяется далее.
Числовые значения, представленные в колонке «физические свойства» в таблицах 1-3, представляют собой температуры плавления (°C), а 1H-ЯМР спектры соединений, для которых в колонке «физические свойства» указано «ЯМР», представлены в таблице 4.
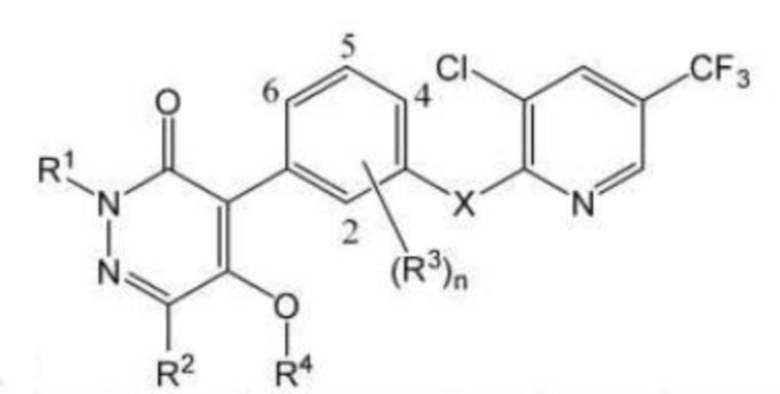
Таблица 1
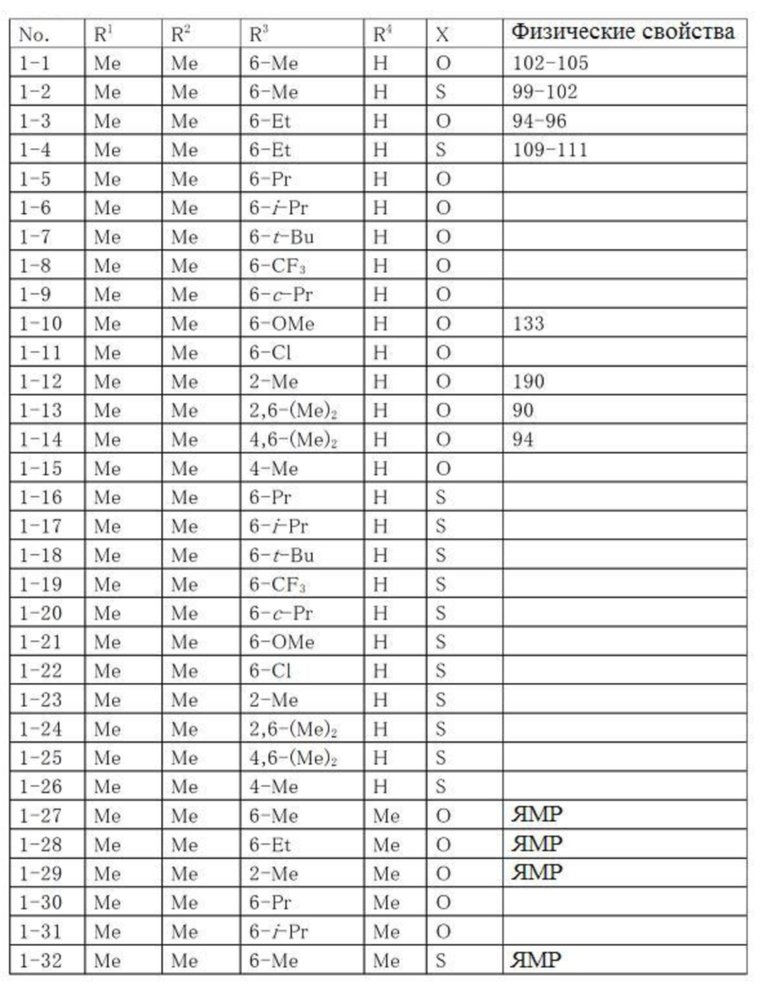
Продолжение таблицы 1
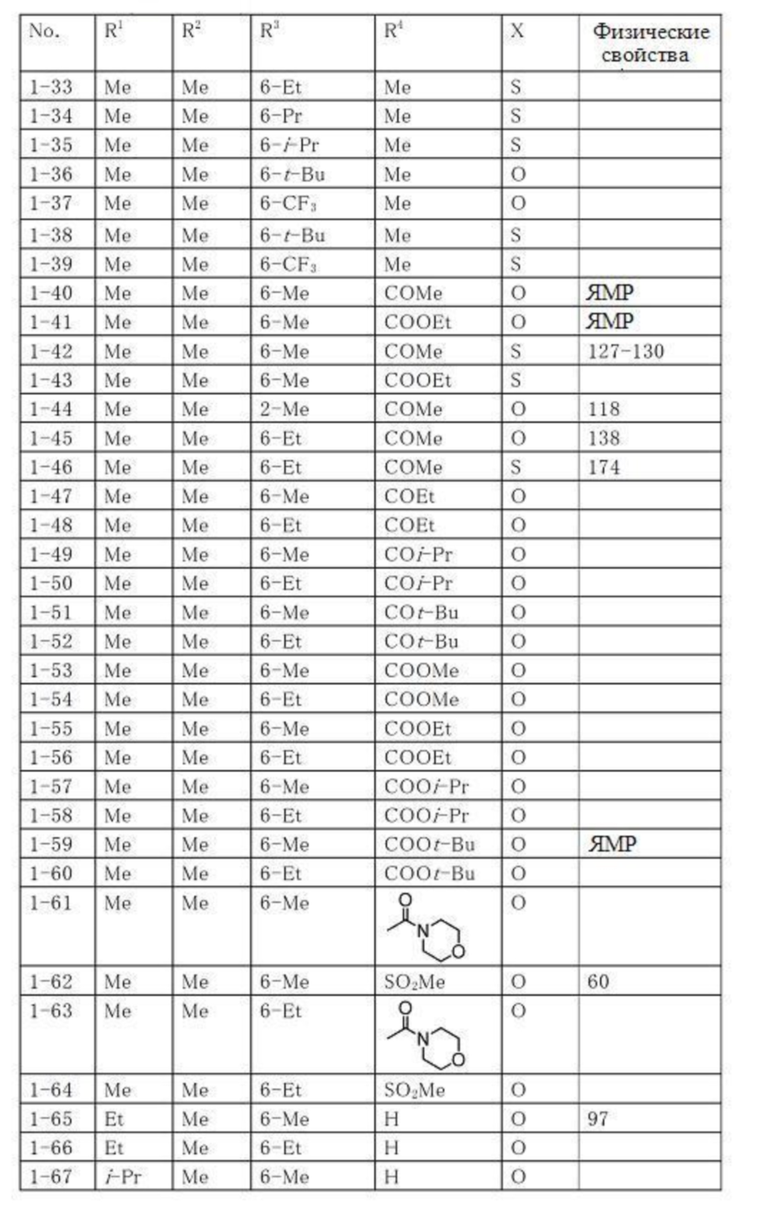
Продолжение таблицы 1
Продолжение таблицы 1
Продолжение таблицы 1
Продолжение таблицы 1
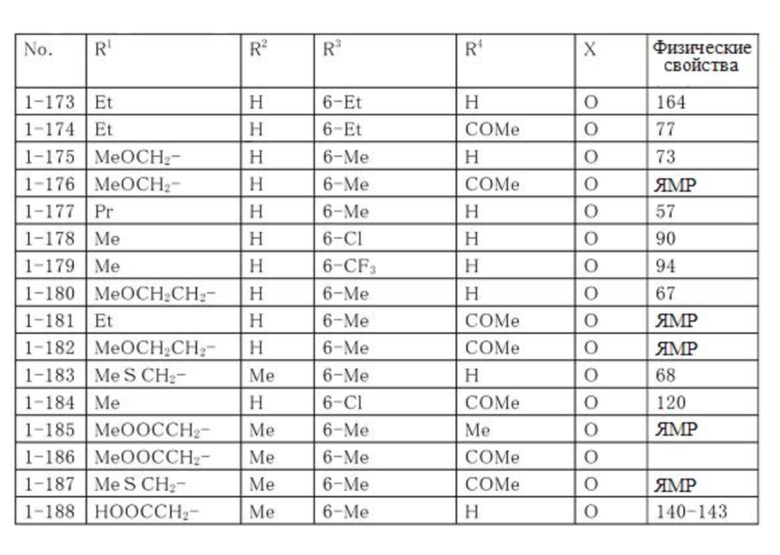
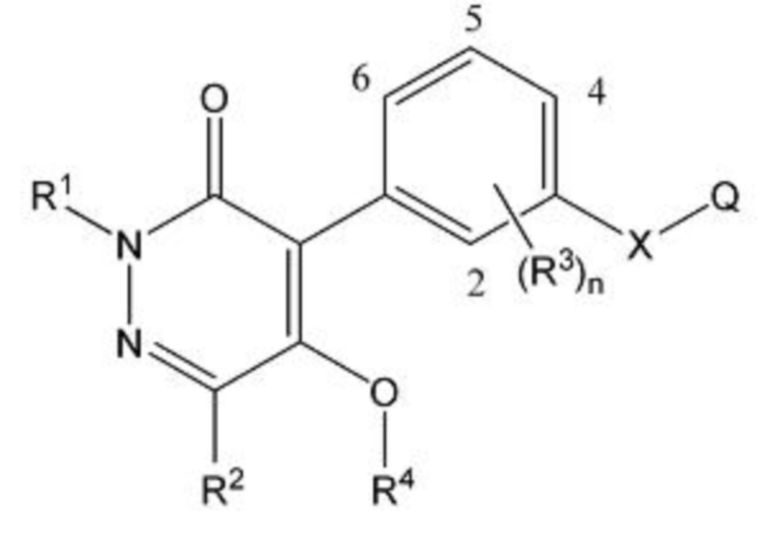
Таблица 2
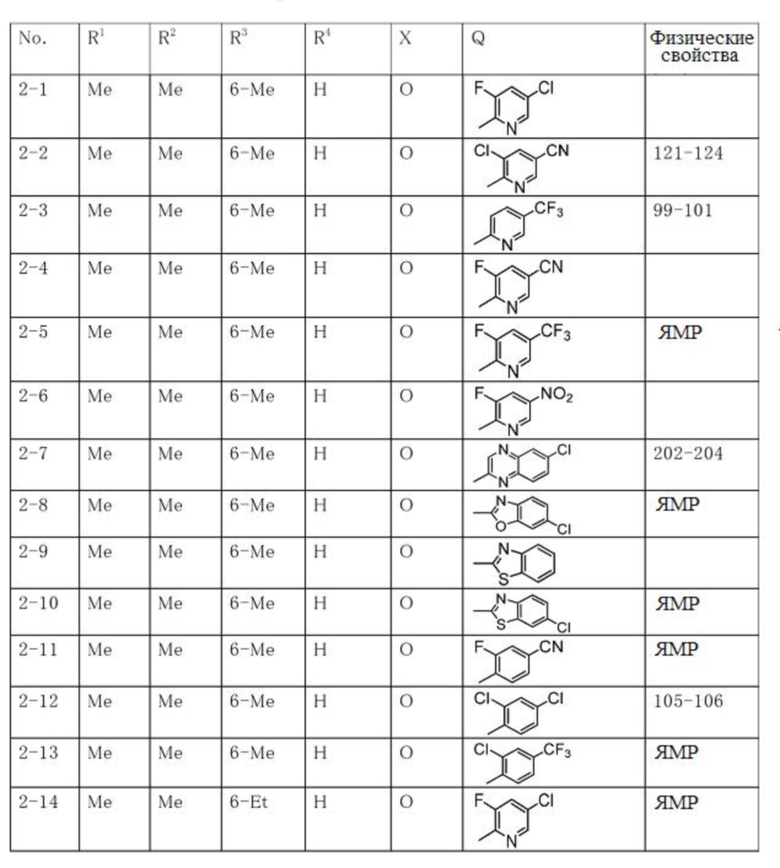
Продолжение таблицы 2
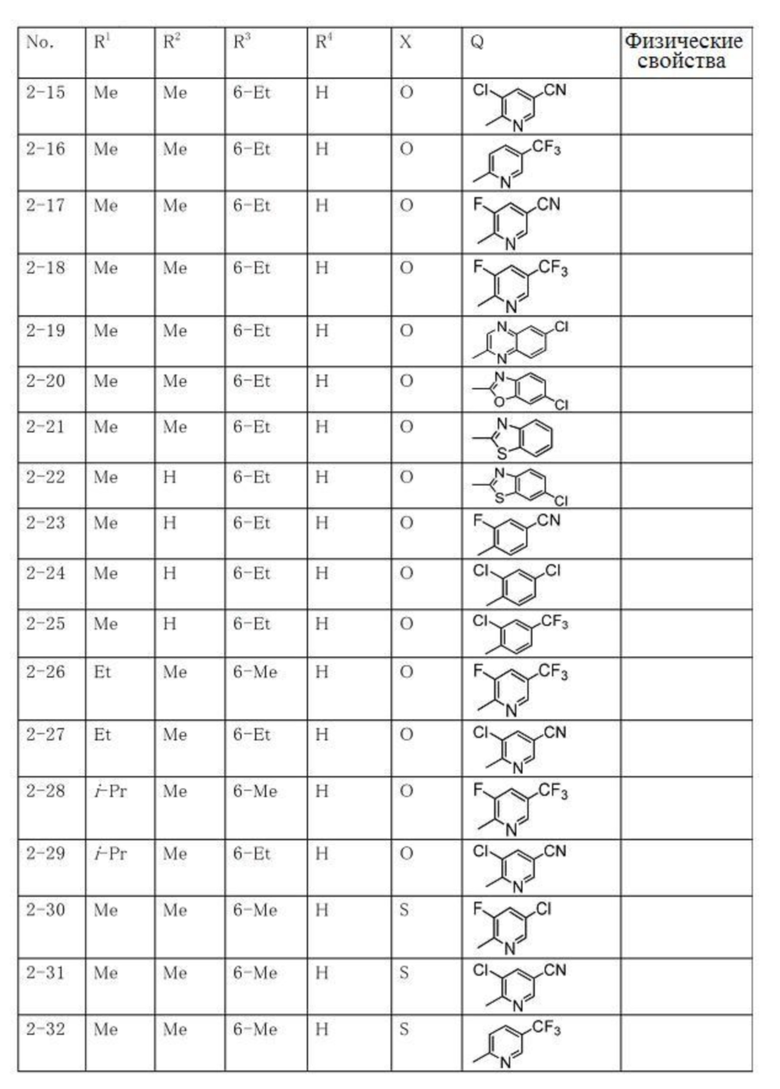
Продолжение таблицы 2
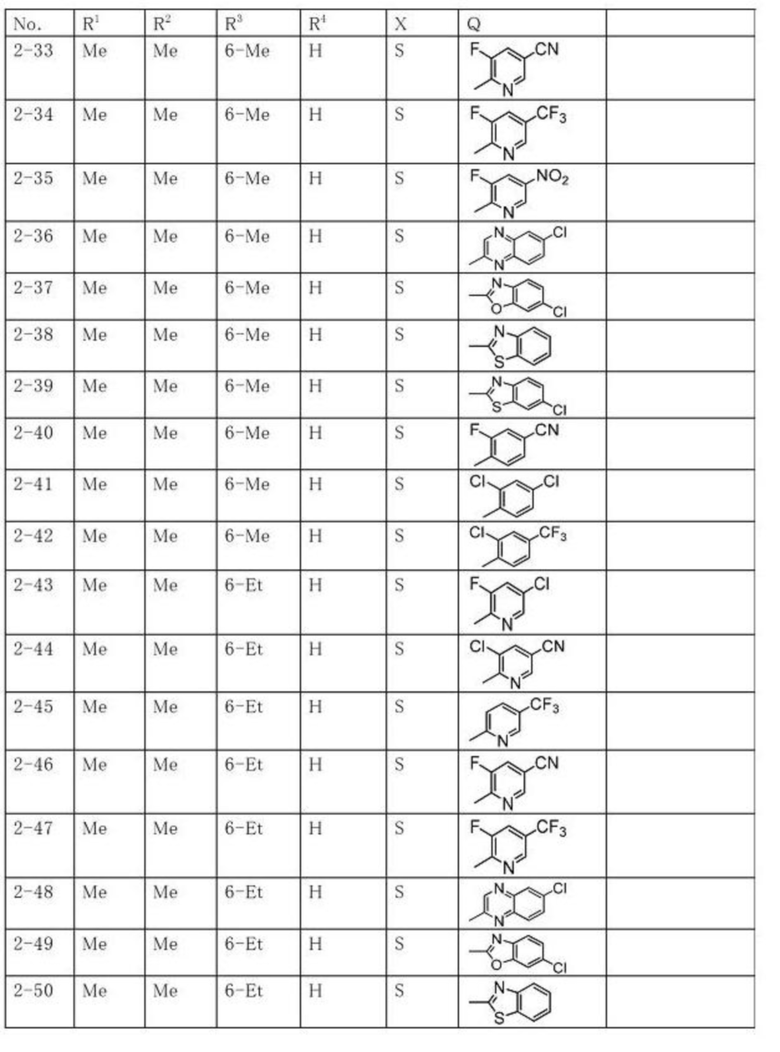
Продолжение таблицы 2
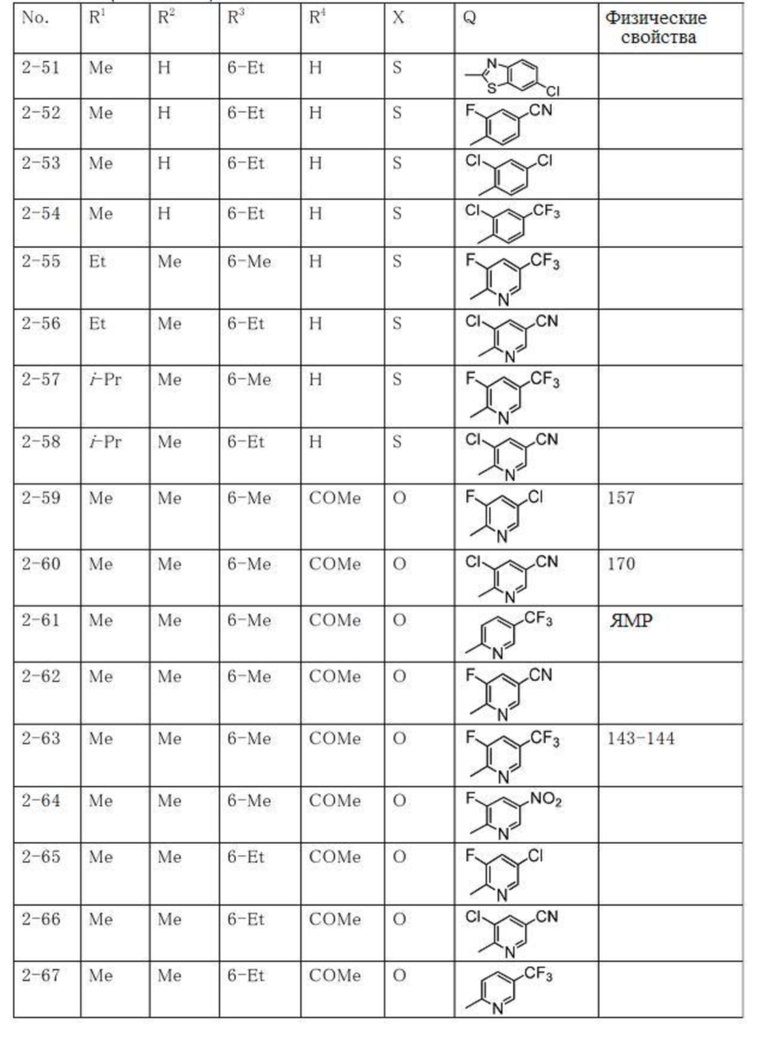
Продолжение таблицы 2
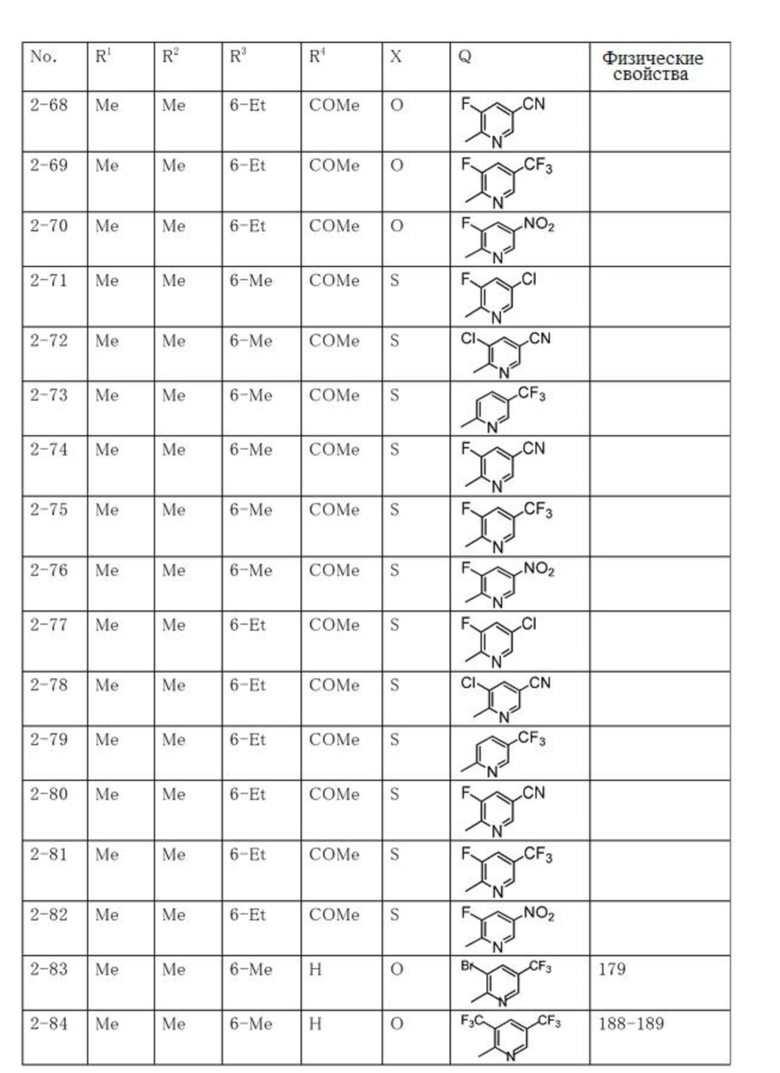
Продолжение таблицы 2
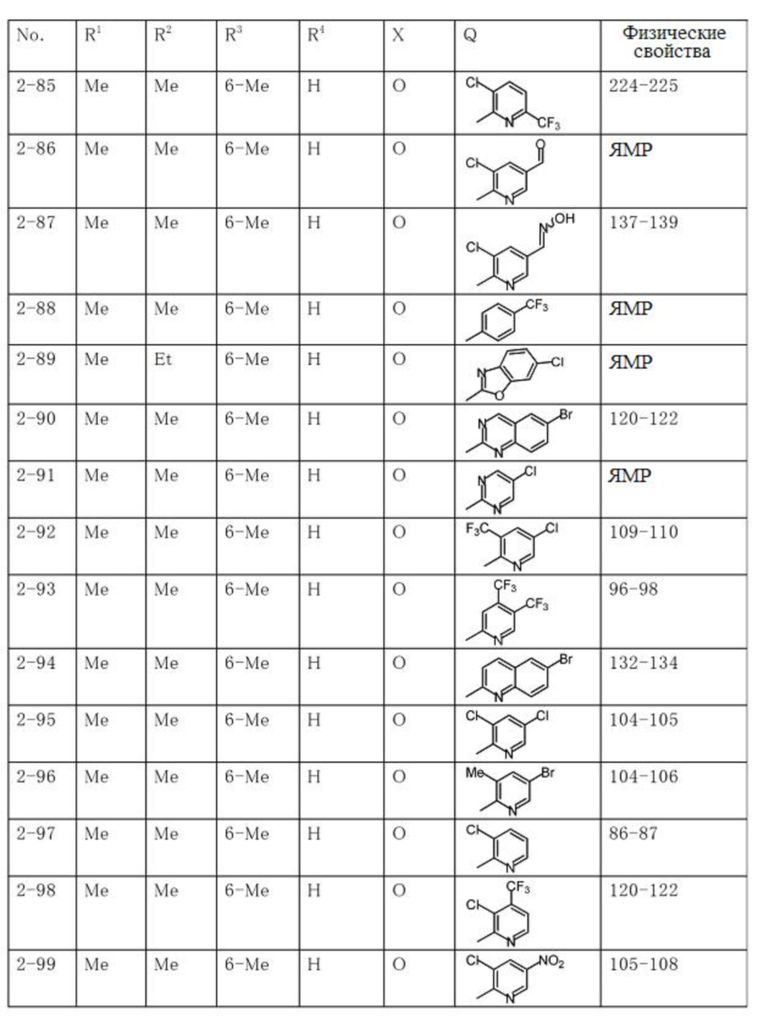
Продолжение таблицы 2
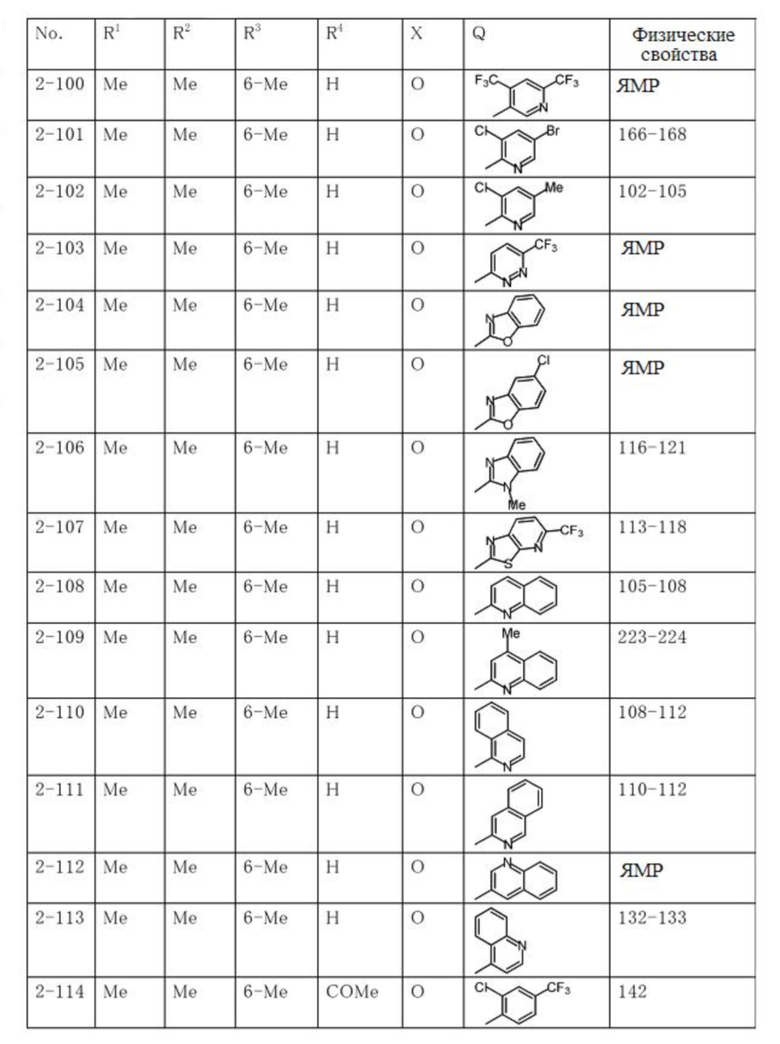
Продолжение таблицы 2
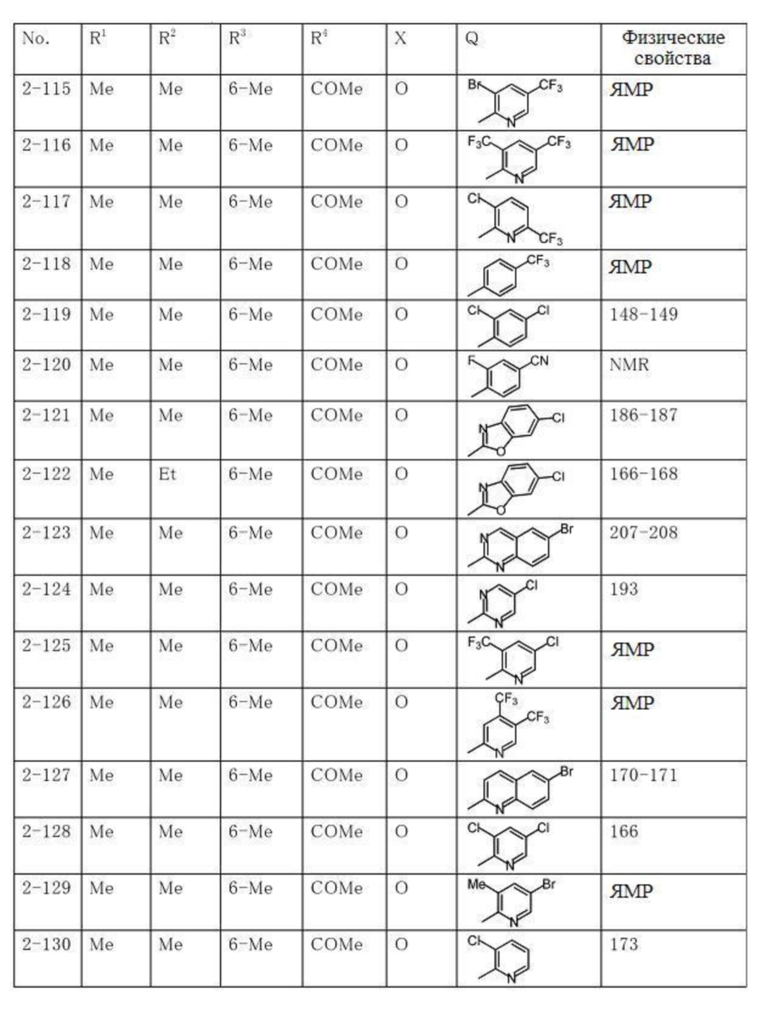
Продолжение таблицы 2
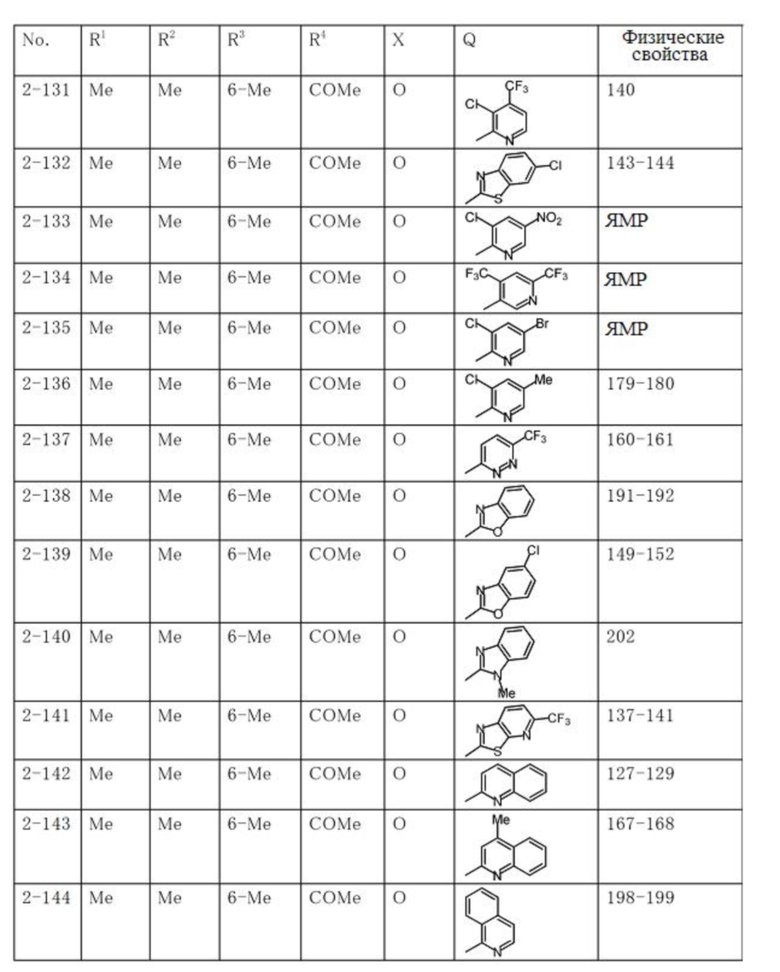
Продолжение таблицы 2
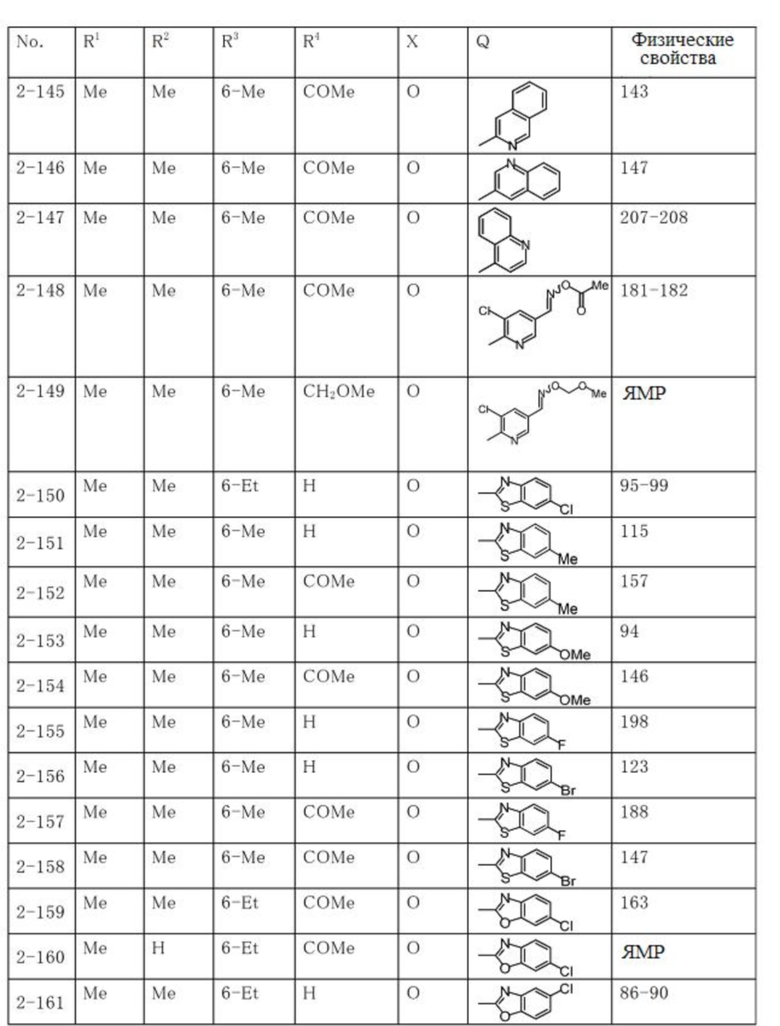
Продолжение таблицы 2
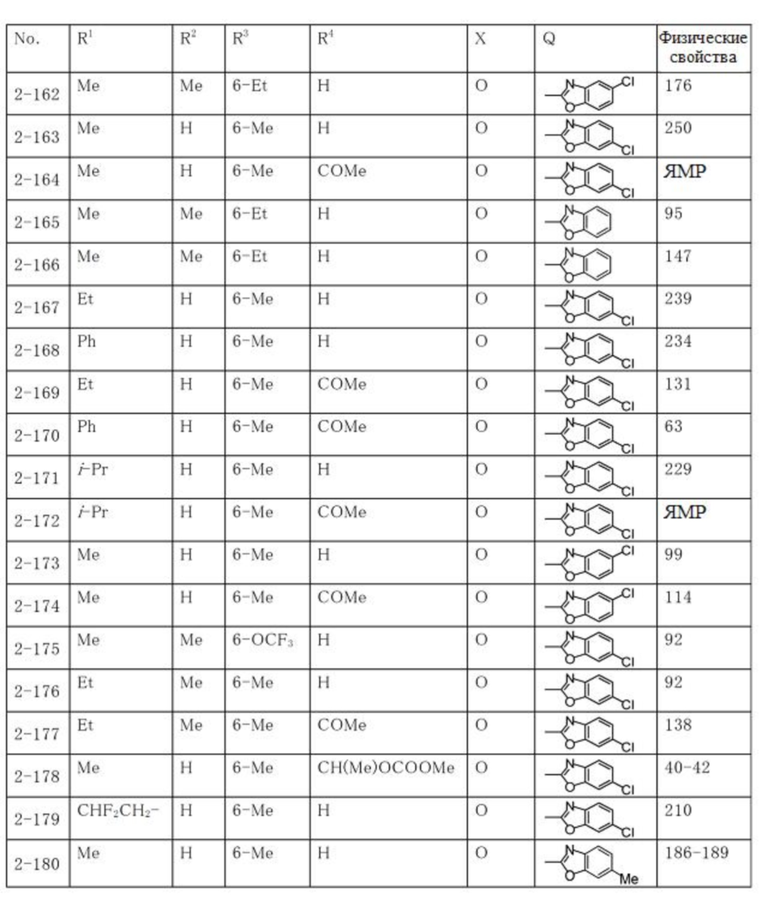
Продолжение таблицы 2
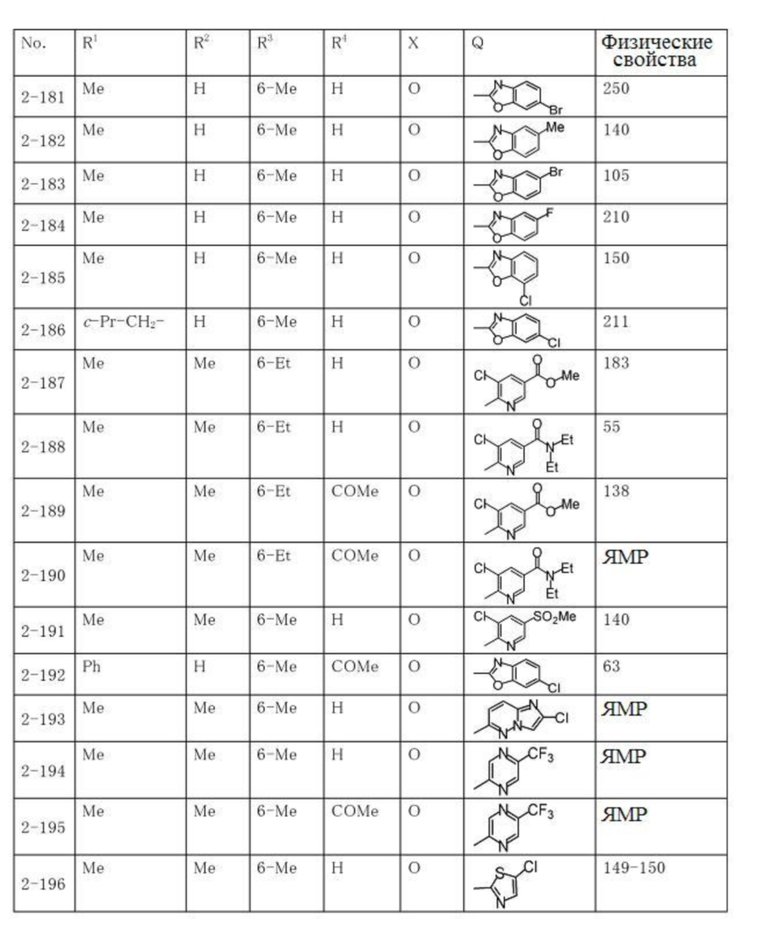
Продолжение таблицы 2
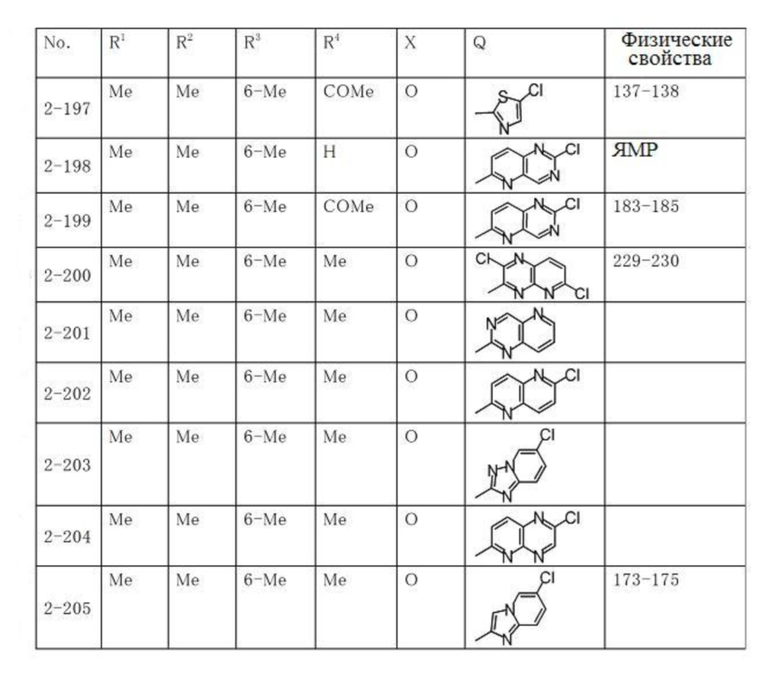
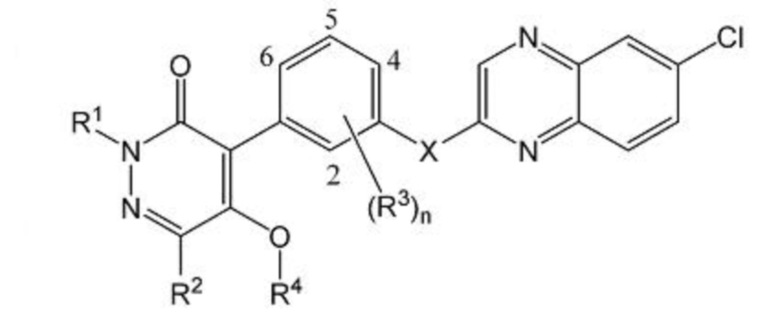
Таблица 3
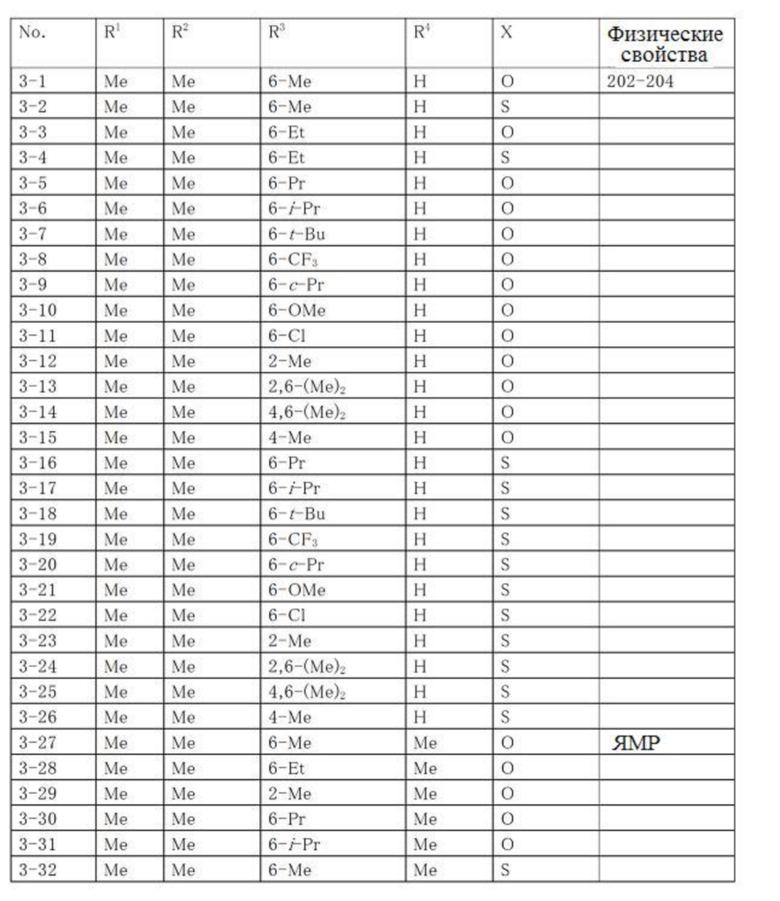
Продолжение таблицы 3
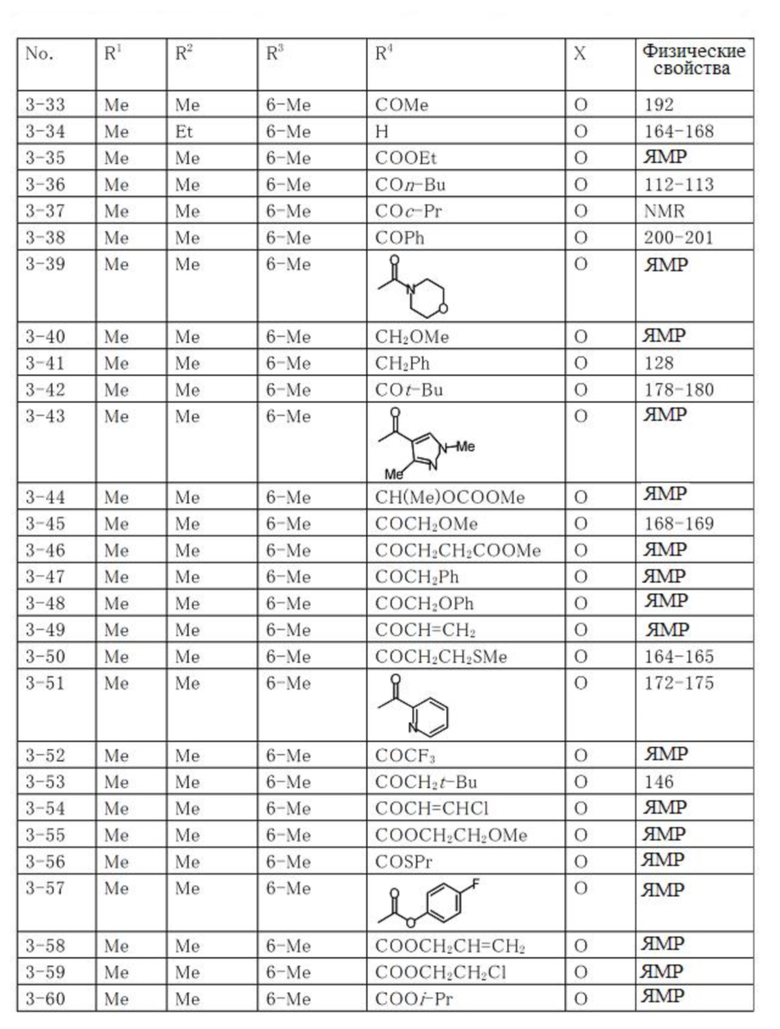
Продолжение таблицы 3
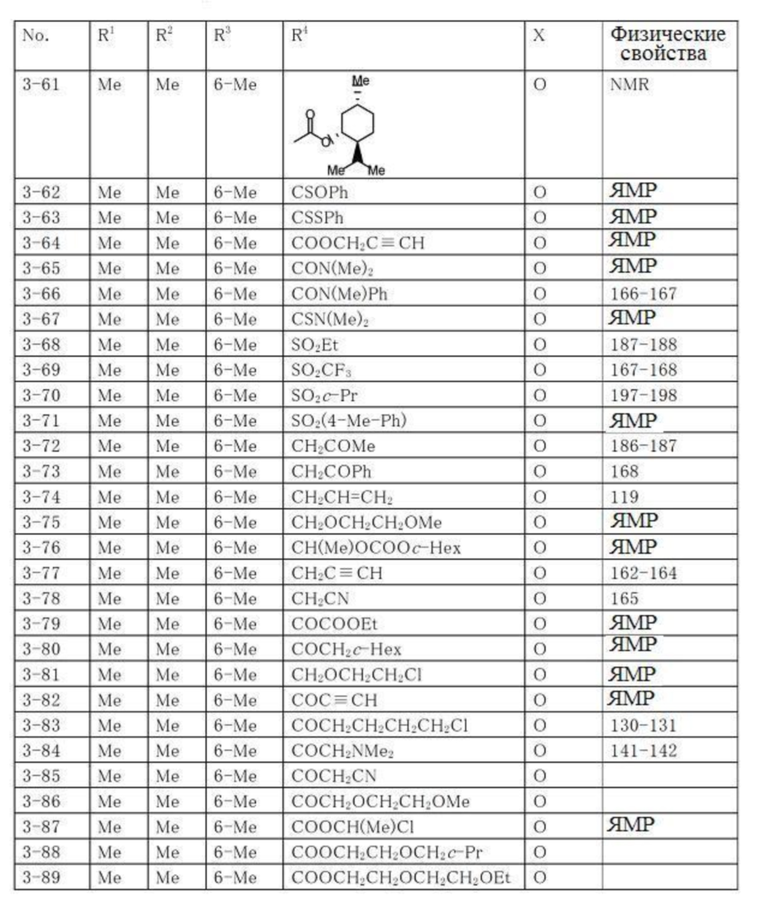
Продолжение таблицы 3
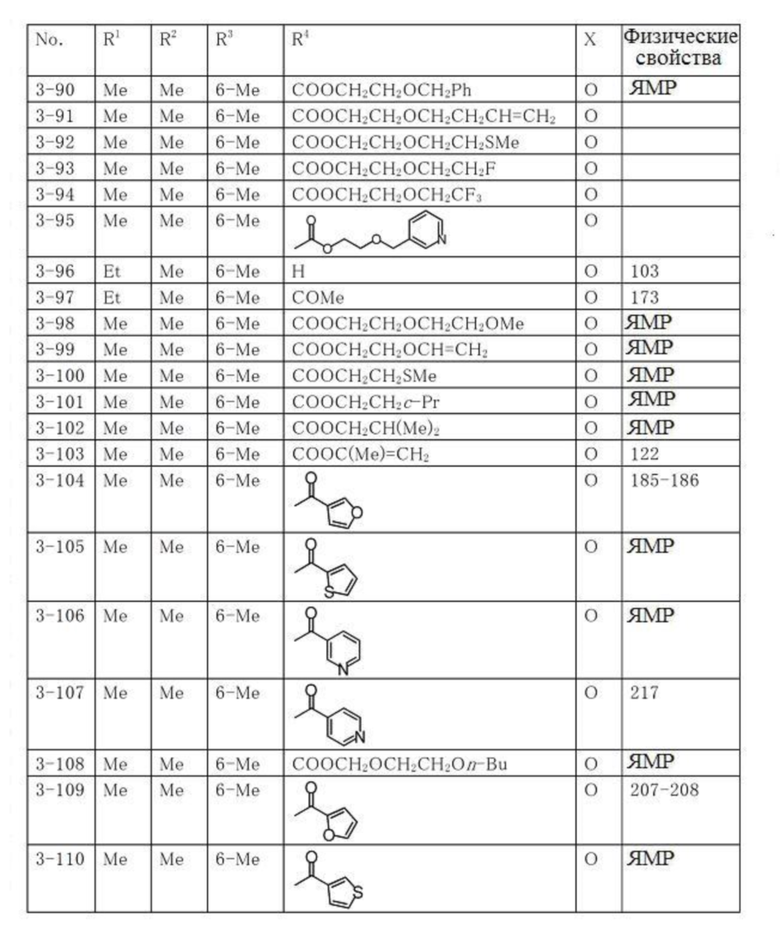
Таблица 4
Далее описаны примеры биологических испытаний соединений по настоящему изобретению.
ПРИМЕР БИОЛОГИЧЕСКОГО ИСПЫТАНИЯ 1
Почву полей высокогорной местности помещают в горшки с площадью поверхности 1/300000 га и высевают в них семена различных растений. Когда соответствующие растения достигают заданной стадии развития листьев ((1) просо куриное (Echinochloa crus-galli L.): стадия развития от 0,5 до 2,9 листьев, (2) росичка (Digitaria sanguinalis L.): стадия развития от 0,5 до 3,0 листьев, (3) щетинник зеленыйй (Setaria viridis L.): стадия развития от 0,5 до 3,2 листьев, (4) овсюг (Avena fatua L.): стадия развития от 0,4 до 1,2 листьев, (5) плевел многоцветковый (Lolium multiflorum Lam.): стадия развития от 0,4 до 2,0 листьев, (6) щирица запрокинутая (Amaranthus retroflexus L.): от семядоли до стадии развития 2,2 листьев, (7) рис (Oryza sativa L): стадия развития от 0,2 до 2,7 листьев, (8) кукуруза (Zea mays L.): стадия развития от 1,7 до 3,6 листьев, (9) пшеница (Triticum aestivum L.): стадия развития от 1,3 до 2,3 листьев, (10) соя (Glycine max Merr.): стадия развития первичного листа), смачивающиеся порошки или эмульгируемые концентраты соединений по настоящему изобретению, полученные в соответствии со стандартным методом получения, взвешивают так, чтобы обеспечить предопределенные количества активных ингредиентов, и разбавляют водой в количестве, соответствующем норме расхода 1000 литров на 1 га (содержащей 0,1% об. сельскохозяйственного распределителя (поверхностно-активное вещество WK производства MARUWA BIOCHEMICAL Co., Ltd.)), и подготовленные таким образом растворы для опрыскиванию применяют лиственной обработкой с помощью небольшого опрыскивателя.
На 14-й день после обработки визуально исследуют состояние роста соответствующих растений, а гербицидный эффект оценивают по степени ингибирования роста (%) от 0 (эквивалентно необработанной площади) до 100 (полное уничтожение). Результаты представлены в таблице 5.
Таблица 5
Продолжение таблицы 5
Продолжение таблицы 5
Продолжение таблицы 5
Продолжение таблицы 5
Продолжение таблицы 5
Продолжение таблицы 5
Продолжение таблицы 5
Продолжение таблицы 5
Продолжение таблицы 5
Продолжение таблицы 5
ПРИМЕР БИОЛОГИЧЕСКОГО ИСПЫТАНИЯ 2
Почву полей высокогорной местности помещают в горшки с площадью поверхности 1/300000 га и высевают в них семена различных растений (просо куриное (Echinochloa crus-galli L.), росичка (Digitaris sanguinalis L.), щетинник зеленыйй (Setaria viridis L.), щирица запрокинутая (Amaranthus retroflexus L.), сида колючая (Sida spinosa L.), канатник Теофраста (Abutilon theophrasti MEDIC), рис ((Oryza sativa L.)), кукуруза (Zea mays L.), пшеница (Triticum aestivum L.), соя (Glycine max Merr.)). На следующий день после высева смачивающиеся порошки или эмульгируемые концентраты соединений по настоящему изобретения, полученные в соответствии со стандартным способом получения, взвешивают так, чтобы получить предопределенные количества активных ингредиентов, и разбавляют водой в количестве, соответствующем норме расхода 1000 литров на 1 га, с последующим применением по почве с помощью небольшого опрыскивателя.
На 14-й день после применения визуально исследуют состояние роста соответствующих растений, а гербицидный эффект оценивают по степени ингибирования роста (%) от 0 (эквивалентно необработанной площади) до 100 (полное уничтожение). Результаты представлены в таблице 6.
Таблица 6
Продолжение таблицы 6
Продолжение таблицы 6
Продолжение таблицы 6
Продолжение таблицы 6
Продолжение таблицы 6
Далее описаны примеры препаратов соединений по настоящему изобретению.
ПРИМЕР ПРЕПАРАТА 1
Указанные выше компоненты с (1) по (4) загружают в высокоскоростной гранулятор смешивания с последующим гранулированием и сушкой для получения диспергируемых в воде гранул.
ПРИМЕР ПРЕПАРАТА 2
Смесь указанных выше компонентов с (1) по (4) и соединение по настоящему изобретению смешивают в массовом соотношении 9:1 с получением смачивающегося порошка.
ПРИМЕР ПРЕПАРАТА 3
Указанные выше компоненты с (1) по (4) смешивают с получением смачивающегося порошка.
ПРИМЕР ПРЕПАРАТА 4
Измельченный компонент (1) и компоненты (2) и (3) предварительно смешивают, затем добавляют компоненты (4) и (5), к полученной смеси добавляют воду и смешивают. Смесь экструдируют и гранулируют с последующей сушкой и просеиванием с получением гранул.
ПРИМЕР ПРЕПАРАТА 5
Компоненты (1), (2) и (3) смешивают и пропускают через мельницу тонкого измельчения и затем к смеси добавляют компонент (4). Смесь замешивают, затем экструдируют и гранулируют с последующей сушкой и просеиванием для получения растворимых в воде гранул.
ПРИМЕР ПРЕПАРАТА 6
Указанные выше компоненты с (1) по (6) смешивают и измельчают в препарате мокрого гранулирования (Дино-мельница) для получения концентрата суспензии на водной основе.
Настоящее изобретение не ограничивается описанными выше вариантами, и возможны различные модификации в рамках заявленного диапазона настоящего изобретения. Кроме того, в настоящее изобретение будут включены варианты, которые могут быть получены посредством надлежащего сочетания технических средств, соответственно раскрытых в различных вариантах. Далее, объединив технические средства, раскрытые соответственно в соответствующих вариантах, можно сформировать новый технический отличительный признак.
ПРОМЫШЛЕННАЯ ПРИМЕНИМОСТЬ
Соединение по настоящему изобретению обеспечивает значительное улучшение гербицидной активности в отношении нежелательных растений по сравнению с аналогичными традиционными соединениями. Кроме того, оно является безопасным для сельскохозяйственных культур. Таким образом, соединение пиридазинона по настоящему изобретению или его соль проявляет превосходные гербицидные активности при применении в качестве активного ингредиента гербицида. Область его применения включает различные поля, включая сельскохозяйственные поля, такие как затопляемое рисовое поле, сухое поле, садовое поле, поле шелковицы и т.д., и несельскохозяйственные поля, такие как горный лес, сельскохозяйственные дороги, земли, производственные участки и т.д. Способ его применения также подходящим образом может быть выбран для использования из почвенной обработки, лественной обработки, обработки при ирригации и т.д.
Полное раскрытие Заявки на Патент Японии № 2016-067797, поданной 30 марта 2016 г., включая спецификацию, формулу изобретения, фигуры и реферат, в полном объеме включено в настоящий документ посредством ссылки.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНГИБИТОРНЫЕ СОЕДИНЕНИЯ | 2013 |
|
RU2673079C2 |
| ПИРИМИДИЛИНДОЛИНОВОЕ СОЕДИНЕНИЕ | 2008 |
|
RU2464269C2 |
| СОЕДИНЕНИЯ | 2019 |
|
RU2800063C2 |
| СОЕДИНЕНИЕ ДИКАРБОНОВОЙ КИСЛОТЫ | 2014 |
|
RU2662817C2 |
| ПРОИЗВОДНЫЕ ТИАЗОЛА | 2005 |
|
RU2367661C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ В ПРОФИЛАКТИКЕ ИЛИ ЛЕЧЕНИИ БАКТЕРИАЛЬНЫХ ИНФЕКЦИЙ | 2017 |
|
RU2783160C2 |
| СЛОЖНЫЕ АРИЛАЛКИЛОВЫЕ ЭФИРЫ 4-АМИНО-6-(ЗАМЕЩЕННЫЙ ФЕНИЛ)ПИКОЛИНАТОВ И 6-АМИНО-2-(ЗАМЕЩЕННЫЙ ФЕНИЛ)-4-ПИРИМИДИНКАРБОКСИЛАТОВ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ГЕРБИЦИДОВ | 2012 |
|
RU2566760C2 |
| ГЕТЕРОЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ | 2006 |
|
RU2382781C2 |
| НОВЫЕ БИЦИКЛИЧЕСКИЕ ДИОКСАНЫ, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ В КАЧЕСТВЕ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ | 2010 |
|
RU2562973C2 |
| СОЕДИНЕНИЯ ПИКОЛИНАМИДА С ФУНГИЦИДНОЙ АКТИВНОСТЬЮ | 2015 |
|
RU2708392C2 |
Изобретение относится к соединениям пиридазинона, представленным формулой (I), гербициду на их основе и способу борьбы с нежелательными растениями. Технический результат: получены новые соединения, обладающие значительной гербицидной активностью в отношении нежелательных растений. 3 н. и 2 з.п. ф-лы, 6 табл., 6 пр.
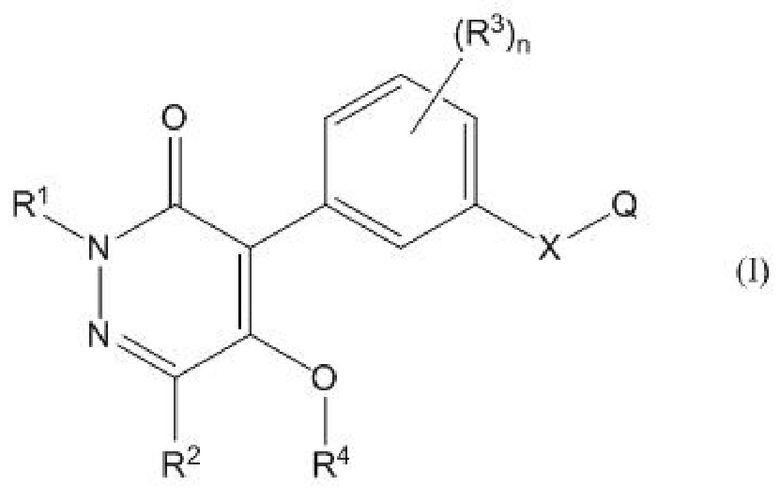
1. Соединение пиридазинона, представленное формулой (I), или его соль, приемлемая в качестве гербицида,
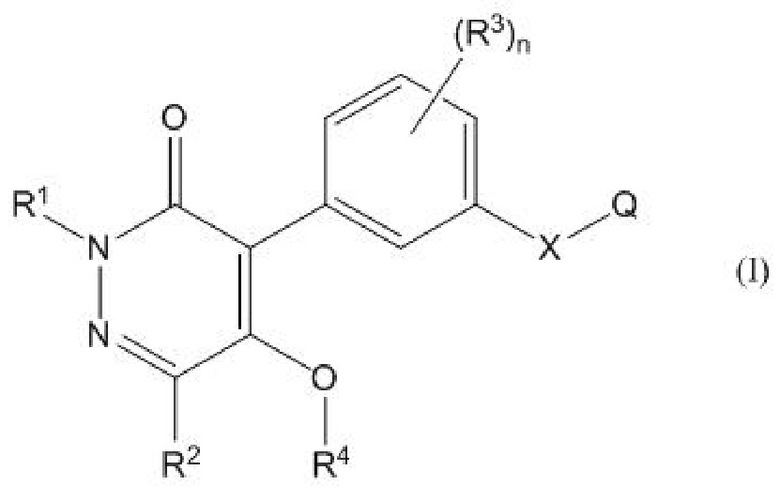
где X представляет собой -O-, -S- или -N(Y)-;
Q представляет собой фенил, который может быть замещен Z, 6-членный гетероарил, содержащий 1-2 атома N, который может быть замещен Z, или 9-10-членный бициклический гетероарил, содержащий 1-3 гетероатома N, O и S, который может быть замещен Z;
Y представляет собой атом водорода или C1-6 алкил;
R1 представляет собой C1-6 алкил, C2-6 алкенил, C3-7 циклоалкил-C1-2 алкил, C2-6 галогеналкил или C1-6 алкилкарбонил-C1-2 алкил;
R2 представляет собой атом водорода, C1-6 алкил или C1-6 галогеналкил;
R3 представляет собой галоген, C1-6 алкил, C1-6 алкокси, C1-6 галогеналкокси или C3-7 циклоалкил;
R4 представляет собой атом водорода, -C(O)R6, -C(S)R6, -SO2R7, Ph-C1-2 алкил, который может быть замещен Z, C1-6 алкокси-C1-2 алкил, -CH(J1)OCOOJ2, C2-6 алкенил, C1-6 алкокси-C1-2 алкокси-C1-2 алкил, C2-6 алкинил, циано-C1-2 алкил или C1-6 галогеналкокси-C1-2 алкил;
R6 представляет собой C1-6 алкил, C1-6 алкокси, морфолино, ди-C1-6 алкиламино, (Ph)(C1-6 алкил)амино, C3-7 циклоалкил, C1-6 алкокси-C1-2 алкил, C1-6 алкилтио-C1-2 алкил, C1-6 галогеналкил, C1-6 алкилтио, C2-6 алкенил, C2-6 алкинил, C1-6 алкоксикарбонил-C1-2 алкил, C3-7 циклоалкил-C1-2 алкил, фенил, который может быть замещен Z, 5-6-членный гетероарил, содержащий 1-2 атома N, который может быть замещен Z, фенил-С1-2 алкил, который может быть замещен Z, фенилокси, который может быть замещен Z, фенилтио, который может быть замещен Z, фенилокси-С1-2 алкил, который может быть замещен Z, С1-6 алкоксикарбонил, С1-6 алкокси-С1-2 алкокси, С1-6 галогеналкокси, С2-6 алкинилокси, С2-6 алкенилокси, С2-6 галогеналкенил или С3-7 циклоалкокси, который может быть замещен Z;
R7 представляет собой С1-6 алкил, С1-6 галогеналкил, С3-7 циклоалкил или фенил, который может быть замещен Z;
Z представляет собой галоген, С1-6 алкил, С1-6 галогеналкил, С1-6 алкокси или циано;
J1 представляет собой С1-6 алкил;
J2 представляет собой С1-6 алкил или С3-7 циклоалкил;
и
n представляет собой целое число от 0 до 4.
2. Соединение пиридазинона или его соль, приемлемая в качестве гербицида, по п.1, где в формуле (I)
X представляет собой -O-, -S- или -N(Y)-;
Q представляет собой фенил, который может быть замещен Z, 6-членный гетероарил, содержащий 1-2 атома N, который может быть замещен Z, или 9-10-членный бициклический гетероарил, содержащий 1-3 гетероатома, выбранных из N, O и S, который может быть замещен Z;
Y представляет собой атом водорода или С1-6 алкил;
Z представляет собой галоген, С1-6 алкил, С1-6 галогеналкил или циано;
R1 представляет собой С1-6 алкил С2-6 алкенил;
R2 представляет собой атом водорода, С1-6 алкил или С1-6 галогеналкил;
R3 представляет собой галоген, С1-6 алкил, С1-6 алкокси, С1-6 галогеналкокси или С3-7 циклоалкил;
R4 представляет собой атом водорода, -C(O)R6 или -SO2R7;
R6 представляет собой С1-6 алкил, С1-6 алкокси или морфолино;
R7 представляет собой С1-6 алкил; и
n представляет собой целое число от 1 до 4.
3. Гербицид, содержащий соединение пиридазинона или его соль по п.1 или 2 в качестве активного ингредиента и сельскохозяйственную добавку.
4. Способ борьбы с нежелательными растениями или ингибирования их роста, который включает нанесение гербицидноэффективного количества соединения пиридазинона или его соли по п.1 или 2 на нежелательные растения или на место их произрастания.
5. Способ по п.4, в котором применяемое количество соединения пиридазинона или его соли составляет от 0,1 до 5000 г/га.
| WO2015177109 A1, 26.11.2015 | |||
| WO2012091156 A1, 05.07.2012 | |||
| СОЕДИНЕНИЯ ПИРИДАЗИНОНА И ГЕРБИЦИД, СОДЕРЖАЩИЙ ДАННОЕ СОЕДИНЕНИЕ | 2008 |
|
RU2463296C2 |
| ПИРИДАЗИНОНОВОЕ ПРОИЗВОДНОЕ И ЕГО ПРИМЕНЕНИЕ В КАЧЕСТВЕ ГЕРБИЦИДА | 2007 |
|
RU2440990C2 |
| WO2014119770 A1, 07.08.2014 | |||
| JP2014210806 A, 13.11.2014 | |||
| TEVENSON, THOMAS M | |||
| et al., "Application of Cross-Coupling and Metalation Chemistry of 3 (2H)-Pyridazinones to Fungicide and Herbicide Discovery", Journal of Heterocyclic Chemistry, | |||
Авторы
Даты
2021-07-07—Публикация
2017-03-29—Подача