ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение относится к белку молока бета-казеину А2 и улучшению антиоксидантной способности у животного за счет увеличения уровней глутатиона в организме животного. В частности, настоящее изобретение относится к молоку и получаемым из молока продуктам питания. Заявитель обнаружил, что употребление молока и молочных продуктов, которые содержат высокие уровни варианта А2 белка бета-казеина, и/или исключение из рациона молока и молочных продуктов, содержащих вариант А1 бета-казеина, помогает увеличить уровни глутатиона в организме. Регулирование уровней глутатиона имеет практическую значимость при осуществелнии контроля ряда нарушений состояния здоровья, связанных с низкими уровнями антиоксидантов и повышенным уровнем окислительного стресса.
УРОВЕНЬ ТЕХНИКИ
Глутатион (GSH) представляет собой антиоксидант, участвующий в нескольких важных биохимических путях. Глутатион представляет собой тиоловый пептид, образованный тремя аминокислотами: глутаминовой кислотой, цистеином и глицином. Сульфгидрильная группа (-SH) остатка цистеина в GSH обеспечивает ключевой сайт для различных конъюгаций и восстановительных реакций между GSH и другими биомолекулами. Окисленная димерная форма GSH (GSSG) может быть обратно преобразована в GSH путем восстановления глутатионредуктазой. Доступность цистеина является лимитирующим фактором для скорости синтеза GSH.
Термин «редокс-состояние» часто используют для описания баланса GSH и GSSG (и других молекул) в биологической системе, такой как клетка или орган. Аномальное редокс-состояние может развиться при ряде различных опасных состояний, таких как гипоксия, шок и сепсис.Окислительно-восстановительные механизмы также контролируют многие клеточные процессы. Основная роль GSH состоит в предотвращении повреждения важных клеточных компонентов, вызываемого активными формами кислорода (АФК). АФК представляют собой химически активные молекулы, содержащие кислород. Примеры включают гидроксильный радикал (-ОН), супероксид (О2-), пероксид водорода (Н2О2) и пероксинитрит (ONOO-). Во время стресса под действием окружающей среды или физиологического стресса уровни АФК могут сильно возрасти Указанное повышение может приводить к значительному повреждению клеточных структур, что широко известно как окислительный стресс.
Редокс-состояние клетки может меняться в зависимости от изменения образования АФК или доступности антиоксидантов. GSH играет важную роль в детоксификации и устранении АФК. Снижение уровней GSH в клетке может приводить к накоплению АФК и окислительному стрессу. Регуляция образования GSH является необходимой для выживания клетки в среде с окислителями.
Состояние окислительного стресса устанавливается при дисбалансе между уровнями или образованием АФК и способностью механизмов антиоксидантной защиты обезвреживать АФК. Существует необходимость в поддержании уровней АФК в физиологически безопасном диапазоне и предупреждении патологических уровней АФК, при которых происходит повреждение ткани. Избыточные уровни АФК приводят к окислительному стрессу, который может вызывать повреждение клеток или смерть, в случае если данный стресс в достаточной степени не компенсирован с помощью механизмов восстановления ткани. Окислительный стресс играет ключевую роль в патогенезе множества заболеваний, включая рак, воспаление, квашиоркор (преимущественно дефицит белка), припадок, аутизм, синдром Дауна, синдром хронической усталости, болезнь Альцгеймера, болезнь Паркинсона, серповидно-клеточную анемию, заболевание печени, муковисцидоз, ВИЧ-СПИД, инфекцию, инфаркт миокарда, инсульт и диабет. Следовательно, GSH играет важную роль в уменьшении проявлений или профилактике этих заболеваний и связанных с ними симптомов. В дополнении к этому, было отмечено, что GSH максимально снижает окислительный стресс, связанный со старением, помогает восстановлению тканей после физиологического стресса в результате, например, физической нагрузки и различных видов спорта, и способствует здоровой фертильности.
Существует множество примеров антиоксидантных пищевых добавок, доступных на рынке. Некоторые реализуются на рынке как добавки глутатиона. Другие реализуются как добавки, стимулирующие повышение уровня GSH. Известно, что сывороточный белок повышает уровни GSH, и поскольку молоко коров содержит сывороточный белок, молоко также может повышать уровни GSH. Однако заявитель обнаружил, что белки бета-казеина, которые также содержатся в молоке коров и молоке других млекопитающих, и в частности, определенные типы бета-казеинов, особенно эффективны для максимального повышения уровней GSH в крови и ткани по сравнению с другими типами бета-казеинов.
Молоко, в особенности молоко коровы, употребляемое населением по всему миру, представляет собой существенный источник белка в рационе питания человека. Молоко коровы, как правило, содержит приблизительно 30-35 грамм белка на литр. Казенны составляют большую часть (80%) данного белка, при этом бета-казеины составляют приблизительно 37% всех казеинов. За последние два десятилетия увеличивается количество данных, подтверждающих участие белков казеина, особенно бета-казеинов, в ряде нарушений состояний здоровья. Бета-казеины можно классифицировать на бета-казеин типа А1 или на бета-казеин типа А2 в зависимости от того, имеют ли они аминокислоту пролин или гистидин в положении 67 аминокислотной последовательности бета-казеина. Данное различие влияет на способность бета-казеина образовывать специфический гептапептидный фрагмент, известный как ВСМ-7, при ферментативном расщеплении. Бета-казеин А1 и бета-казеин А2 представляют собой преобладающие бета-казеины в молоке, употребляемом большинством населения.
Заявитель и другие авторы ранее определили связь между потреблением бета-казеина А1 в молоке и молочных продуктах и частотой возникновения некоторых заболеваний, включая диабет 1 типа (WO 1996/014577), коронарную (ишемическую) болезнь сердца (WO 1996/036239) и неврологические нарушения (WO 2002/019832). Кроме того, Заявитель продемонстрировал связь между бета-казеином А1 и воспалением кишечника (WO 2014/193248), симптомами непереносимости лактозы (WO 2015/005804) и высокими уровнями глюкозы в крови (WO 2015/026245).
Заявитель далее нашел убедительное научное доказательство прямой связи между потреблением бета-казеина А2 и повышенными уровнями GSH в крови и ткани. Таким образом, Заявитель разработал новый способ лечения состояний, упомянутых выше, или управления течением симптомов этих состояний.
Таким образом, целью настоящего изобретения является обеспечение способа улучшения антиоксидантной способности у животного или по меньшей мере обеспечение пригодной для применения альтернативы существующим способам.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В первом аспекте настоящего изобретения предложен способ улучшения антиоксидантной способности у животного путем обеспечения указанного животного композицией, содержащей бета-казеин, где указанный бета-казеин содержит по меньшей мере 75% по массе по меньшей мере от одного бета-казеина, не способного образовывать бета-казоморфин-7 при ферментативном расщеплении.
По меньшей мере один указанный бета-казеин предпочтительно выбран из бета-казеинов типа А2.
В некоторых вариантах реализации настоящего изобретения композицию принимают внутрь для повышения уровня глутатиона в крови или ткани указанного животного.
Кроме того, в некоторых вариантах реализации прием композиции внутрь позволяет избежать или снизить риск заболеваний или нарушений, связанных с окислительным стрессом. Заболевания или нарушения, связанные с окислительным стрессом, могут включать рак, воспаление, квашиоркор (дефицит белка), припадок, аутизм, синдром Дауна, синдром хронической усталости, болезнь Альцгеймера, болезнь Паркинсона, серповидно-клеточную анемию, заболевание печени, муковисцидоз, ВИЧ, СПИД, инфекцию, инфаркт миокарда, инсульт и диабет.
В других вариантах реализации настоящего изобретения прием композиции внутрь позволяет предотвратить или снизить эффекты старения, способствует восстановлению тканей после физической нагрузки или стимулирует фертильность.
В предпочтительных вариантах реализации настоящего изобретения животное представляет собой человека. В качестве альтернативы, животное может представлять собой другое животное, восприимчивое к окислительному стрессу, включая, например, собак или кошек.
Во втором аспекте настоящего изобретения предложена композиция для улучшения антиоксидантной способности у животного путем обеспечения указанного животного композицией, содержащей бета-казеин, где бета-казеин содержит по меньшей мере 75% по массе по меньшей мере одного бета-казеина, не способного образовывать бета-казоморфин-7 при ферментативном расщеплении.
В другом аспекте настоящего изобретения предложено применение композиции для улучшения антиоксидантной способности у животного путем обеспечения указанного животного композицией, содержащей бета-казеин, где указанный бета-казеин содержит по меньшей мере 75% по массе по меньшей мере одного бета-казеина, не способного образовывать бета-казоморфин-7 при ферментативном расщеплении.
В другом аспекте настоящего изобретения предложено применение молока при получении композиции для улучшения антиоксидантной способности у животного, где молоко содержит бета-казеин, и где бета-казеин содержит по меньшей мере 75% по массе по меньшей мере одного бета-казеина, не способного образовывать бета-казоморфин-7 при ферментативном расщеплении.
В другом аспекте настоящего изобретения предложено применение бета-казеина при получении композиции, содержащей бета-казеин для улучшения антиоксидантной способности у животного, где бета-казеин содержит по меньшей мере 75% по массе по меньшей мере одного бета-казеина, не способного образовывать бета-казоморфин-7 при ферментативном расщеплении. Бета-казеин предпочтительно представляет собой компонент молока. Молоко предпочтительно представляет собой молоко коровы.
В другом аспекте настоящего изобретения предложено применение композиции, содержащей бета-казеин, в качестве антиоксиданта, где бета-казеин содержит по меньшей мере 75% по массе по меньшей мере одного бета-казеина, не способного образовывать бета-казоморфин-7 при ферментативном расщеплении.
Количество по меньшей мере одного бета-казеина, не способного образовывать бета-казоморфин-7 при ферментативном расщеплении, может составлять любое количество в диапазоне от 75% до 100% по массе от количества бета-казеина, например, по меньшей мере 90%, по меньшей мере 95%, по меньшей мере 98%, по меньшей мере 99% или даже 100%.
В определенных вариантах реализации настоящего изобретения композиция представляет собой молоко или молочный продукт.Молоко может представлять собой молоко в порошке или жидкое молоко. Молочный продукт может представлять собой сливки, йогурт, творог, сыр, масло, мороженое или любой другой продукт, полученный из молока или содержащий казеин или производное казеина, включая детскую смесь, пищевой продукт для взрослых, белковую добавку или корм для домашних животных.
В некоторых вариантах реализации настоящего изобретения молоко получают путем генотипирования или фенотипирования коров и доения только тех коров, у которых определили, что они производят только бета-казеин типа А2 в своем молоке. Можно сформировать до начала доения стадо коров, содержащее только тех коров, в отношении которых было определено, что они производят только бета-казеин типа А2 в своем молоке.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
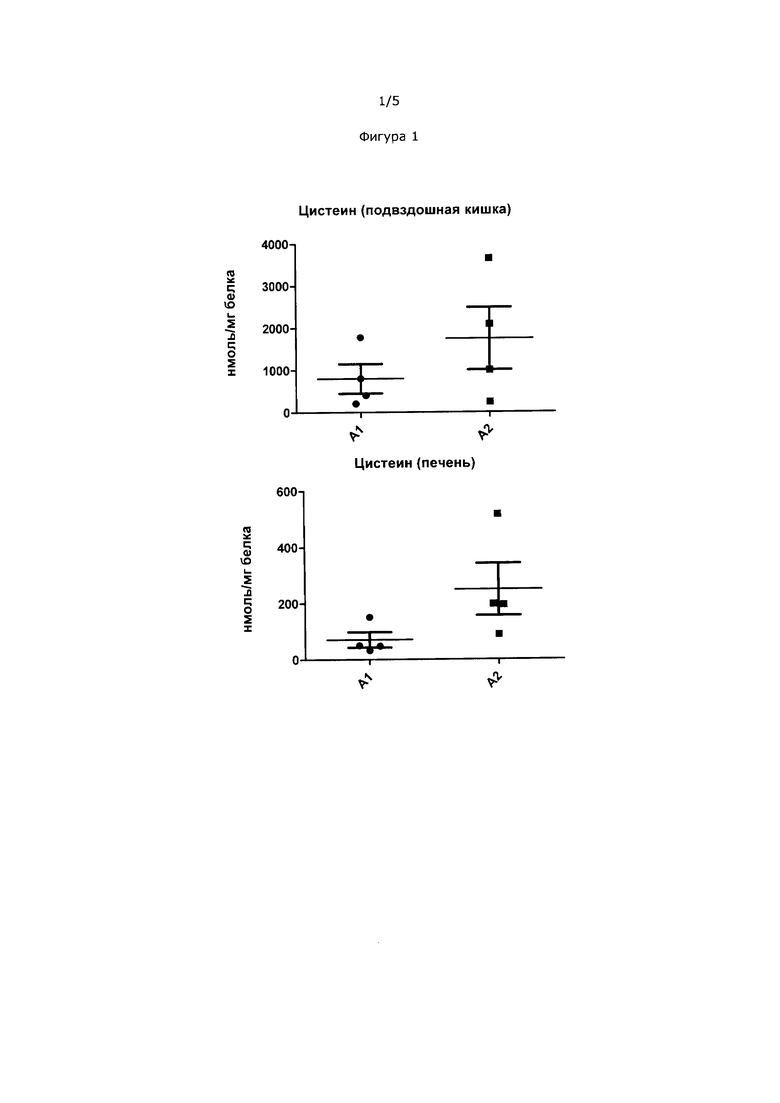
На Фиг. 1 показаны уровни цистеина в подвздошной кишке и печени кроликов, которых кормили кормом с бета-казеином А1 и бета-казеином А2.
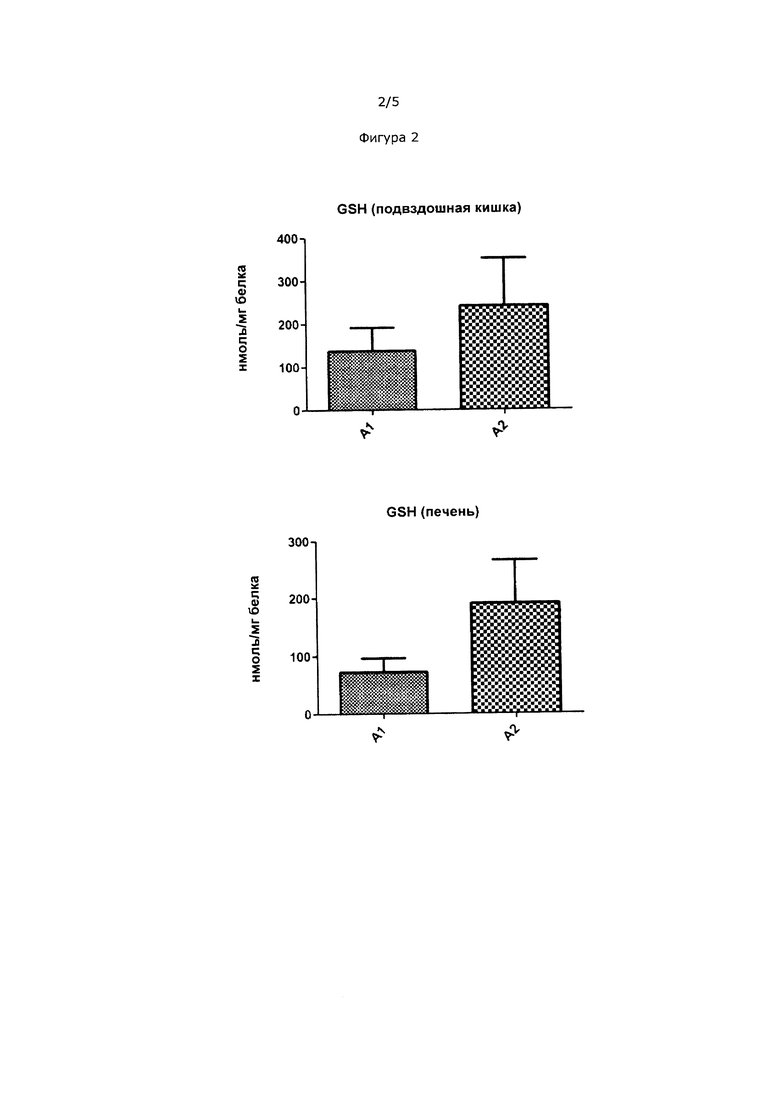
На Фиг. 2 показаны уровни GSH в подвздошной кишке и печени кроликов, которых кормили кормом с бета-казеином А1 и бета-казеином А2.
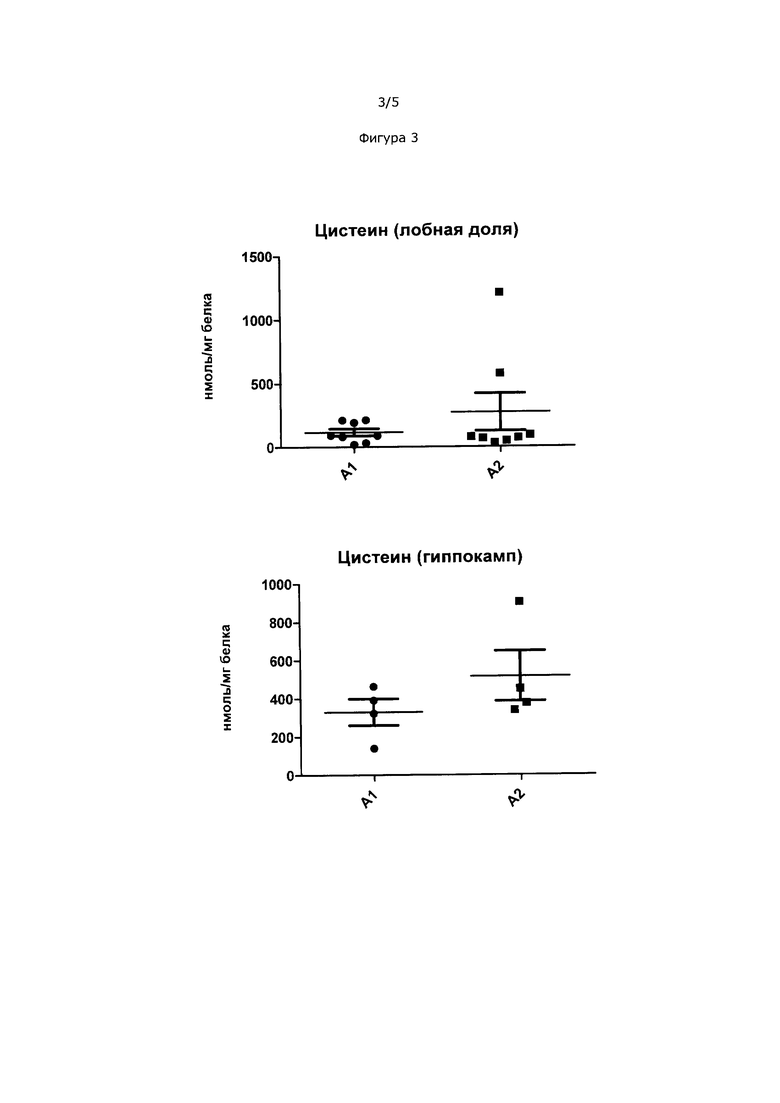
На Фиг. 3 показаны уровни цистеина в лобной доле и гиппокампе кроликов, которых кормили кормом с бета-казеином А1 и бета-казеином А2.
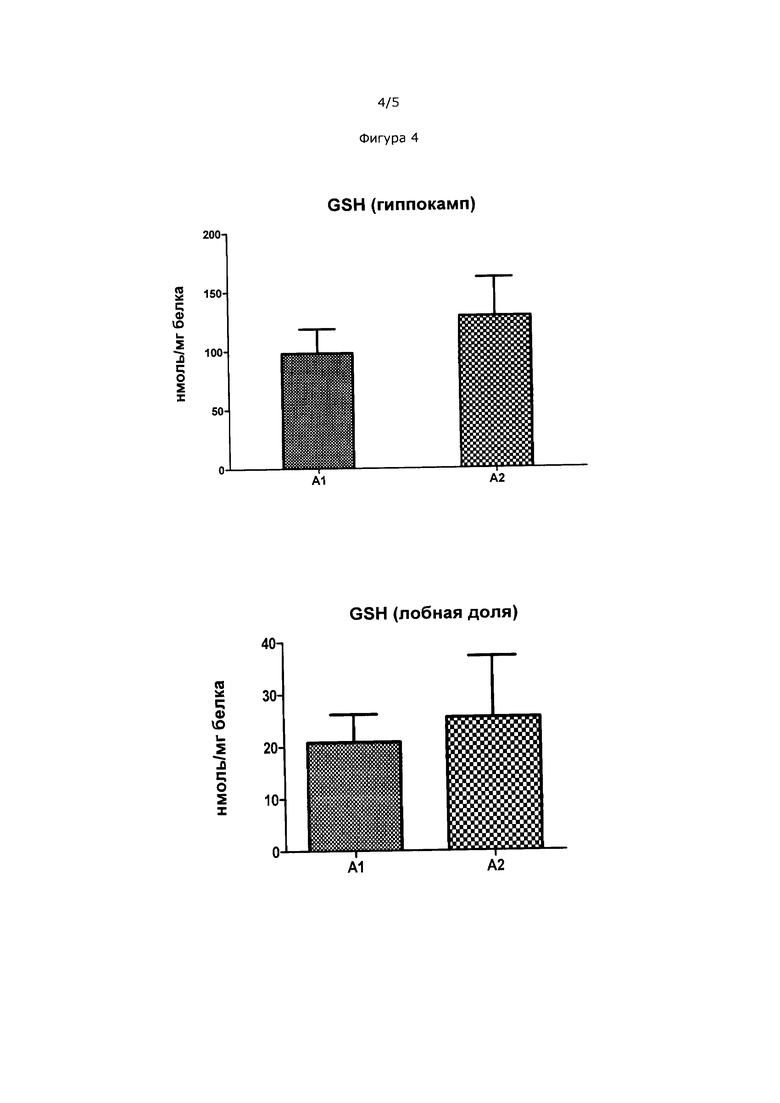
На Фиг. 4 показаны уровни GSH в лобной доле и гиппокампе кроликов, которых кормили кормом с бета-казеином А1 и бета-казеином А2.
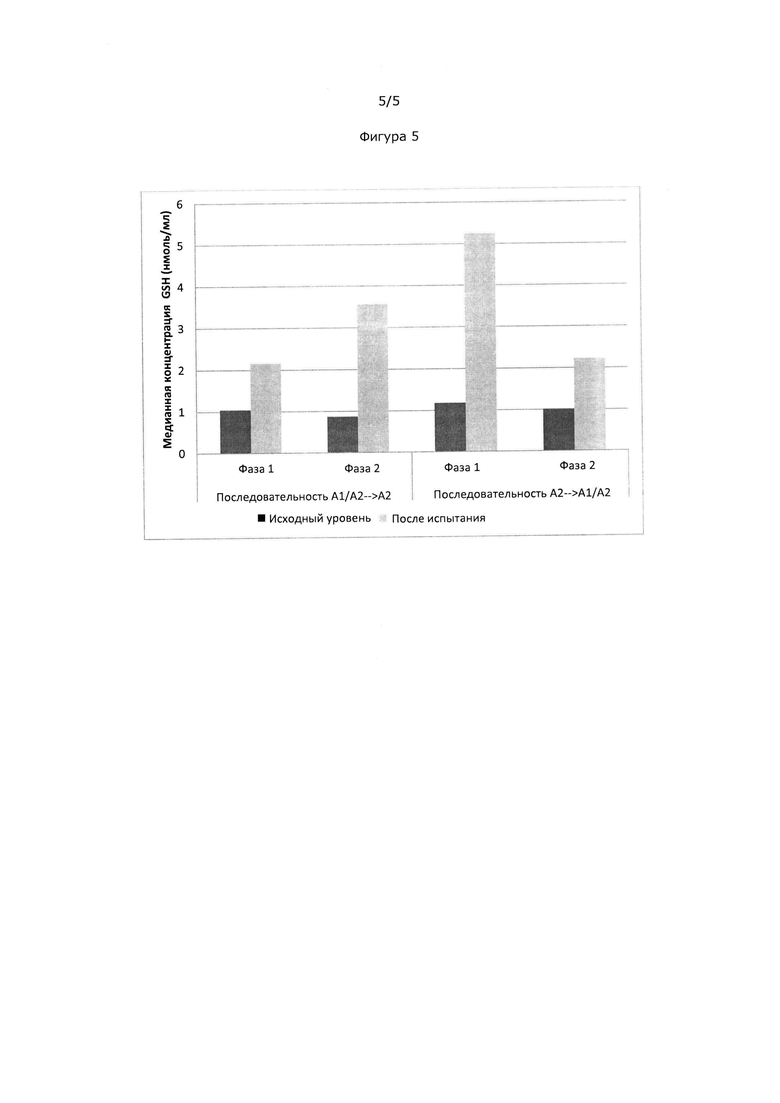
На Фиг. 5 показаны медианные концентрации GSH у людей до и после употребления молока, содержащего только бета-казеин А2 или и бета-казеин А1, и бета-казеин А2.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к композиции, содержащей белок бета-казеин, и его применению для улучшения антиоксидантной способности у животных, особенно у человека. Важным является то, что указанный бета-казеин представляет собой вариант А2 бета-казеина. Бета-казеин в композиции представляет собой 100% бета-казеин А2 или содержит по меньшей мере 75% бета-казеина А2 по массе относительно вариантов бета-казеина, представленных в композиции. Важность преобладания варианта А2 в композиции обусловлена тем фактом, что Заявитель продемонстрировал существование прямой связи между потреблением молока, содержащего только вариант бета-казеина А2, и повышенным содержанием GSH и цистеина (предшественника GSH) у кроликов и людей. Уровни GSH и цистеина оказались более высокими, когда бета-казеин в рационе питания представляет собой бета-казеин А2, а не бета-казеин А1.
Это имеет большое значение для профилактики, лечения или управления течением заболеваний или нарушений, связанных с физиологически высокими уровнями АФК. Антиоксидант GSH помогает регулировать уровни АФК. Следовательно, максимальное увеличение уровней GSH в крови и ткани является полезным для предотвращения или уменьшения симптомов различных заболеваний, включая рак, воспаление, квашиоркор (дефицит белка), припадок, аутизм, синдром Дауна, синдром хронической усталости, болезнь Альцгеймера, болезнь Паркинсона, серповидно-клеточную анемию, заболевание печени, муковисцидоз, ВИЧ, СПИД, инфекцию, инфаркт миокарда, инсульт и диабет, для способствования восстановлению ткани после физиологического стресса, для замедления или снижения до минимума эффектов процесса старения и для улучшения фертильности.
Поскольку основным, если не единственным, источником бета-казеинов в рационе питания большинства населения является молоко или продукты, полученные из молока, и поскольку большая часть потребляемого молока содержит только смесь вариантов А1 и А2 бета-казеина (как объясняется ниже), употребление молока (или продуктов, полученных из такого молока), имеющего высокое содержание варианта А2, будет безусловно означать, что потребление варианта А1 является низким. В соответствии с этим, настоящее изобретение основано на снижении или устранении бета-казеина А1 из рациона питания и повышении бета-казеина А2, и это достигается путем обеспечения того, что бета-казеин в содержащих бета-казеин пищевых композициях, особенно в молоке и молочных продуктах, представляет собой преимущественно бета-казеин А2 или предпочтительно представляет собой исключительно бета-казеин А2.
В идеале бета-казеин в композиции представляет собой 100% бета-казеин А2. Следовательно, полное устранение бета-казеина А1 максимально увеличивает возможность поддержания высоких уровней GSH в крови и ткани и, следовательно, предотвращения неблагоприятных симптомов и последствий, связанных с окислительно-восстановительным дисбалансом и избыточными уровнями АФК. Однако бета-казеин в композиции не обязательно должен представлять собой 100% бета-казеин А2. Благоприятное воздействие высоких уровней GSH наблюдается в любых продуктах, где бета-казеин преимущественно представляет собой бета-казеин А2, например, в любом количестве от 75% по массе до 100% по массе, включая 80%, 90%, 95%, 98% и 99% по массе, но не ограничиваясь только этими количествами.
Композиция согласно настоящему изобретению представляет собой, как правило, молоко, но также может представлять собой любой молочный продукт, такой как сливки, йогурт, творог, сыр, масло, мороженое или любой продукт, содержащий казеин или производное казеина, такое как казеинат натрия. Примеры таких продуктов включают детские смеси, пищевые продукты для взрослых, белковые добавки и корма для домашних животных. Композиция также может представлять собой немолочный продукт, содержащий бета-казеин, который был получен из молока. Композиция также может представлять собой сам бета-казеин или может быть получена из бета-казеина, бета-казеин которой может быть в твердой форме, такой как порошок или гранулы, или в форме твердого сгустка.
Молоко может быть в форме свежего молока, молока в порошке, жидкого молока, восстановленного из порошка, обезжиренного молока, гомогенизированного молока, сгущенного молока, концентрированного молока, пастеризованного молока или непастеризованного молока или в любой другой форме молока.
При том, что молоко может быть получено от любого млекопитающего, включая людей, коз, свиней и буйволов, в предпочтительных вариантах реализации настоящего изобретения молоко представляет собой молоко коровы.
Композиция согласно настоящему изобретению предназначена для употребления в основном человеком, но следует понимать, что польза для здоровья также значима для других видов животных, таких как кошки, собаки и другие домашние животные.
Бета-казеины можно классифицировать в общем случае на бета-казеин типа А1 и типа А2. Бета-казеин А1 и бета-казеин А2 являются преобладающими бета-казеинами в молоке, употребляемом большинством населения. Бета-казеин А1 отличается от бета-казеина А2 по одной аминокислоте. Аминокислота гистидин находится в положении 67 в последовательности из 209 аминокислот бета-казеина А1, тогда как в том же положении у бета-казеина А2 находится пролин. Однако, это различие в одну аминокислоту является критически важным для ферментативного расщепления бета-казеинов в кишечнике. Наличие гистидина в положении 67 обеспечивает возможность образования при ферментативном расщеплении фрагмента белка, содержащего семь аминокислот, известного как бета-казоморфин-7 (ВСМ-7). Таким образом, ВСМ-7 представляет собой продукт расщепления бета-казеина А1. В случае бета-казеина А2 положение 67 занято пролином, который мешает расщеплению аминокислотной связи в этом положении. Таким образом, ВСМ-7 не является продуктом расщепления бета-казеина А2.
Другие варианты бета-казеина, такие как бета-казеин В и бета-казеин С, также имеют гистидин в положении 67, а другие варианты, такие как A3, D, Е и I, имеют пролин в положении 67. Но эти варианты обнаруживаются только в очень низких концентрациях или не обнаруживаются в молоке от коров европейского происхождения. Таким образом, в контексте настоящего изобретения термин «бета-казеин А1» относится к любому бета-казеину, имеющему гистидин в положении 67, и, следовательно, обладающему способностью образовывать ВСМ-7 при ферментативном расщеплении, а термин «бета-казеин А2» относится к любому бета-казеину, имеющему пролин в положении 67, и, следовательно, не обладающему способностью образовывать ВСМ-7 при ферментативном расщеплении.
Молоко коров можно проверить на относительное соотношение бета-казеинов типа А1 и бета-казеинов типа А2. В качестве альтернативы, коровы могут быть проверены генетически на их способность производить молоко, содержащее бета-казеины типа А1 или бета-казеины типа А2 или комбинацию обоих. Данные способы и методики хорошо известны.
Внутриклеточная концентрация GSH в большинстве клеток составляет в среднем 1-2 мМ и может варьировать от приблизительно 10 мМ в гепатоцитах до 0,2 мМ в нейронах. Гепатоциты продуцируют большую часть GSH, обнаруживаемого в плазме крови. По причине относительно низкого содержания GSH в нейронах, восполнение GSH путем восстановления GSSG становится особенно важным процессом в нейронах. GSH может быть транспортирован из клеток и в кровь с использованием опосредованного переносчиком механизма. Некоторая часть GSH, получаемого из пищи и продуцируемого в кишечнике, также может попадать в плазму крови воротной вены. Печень является основным источником GSH плазмы, где GSH синтезируется из цистеина. Мозг, почки, легкие и кишечник являются основными потребителями полученного в печени GSH. Метаболизм GSH внутри органа позволяет транспортировать цистеин и цистин в нетоксичной форме между тканями, а также помогает поддерживать внутриклеточные концентрации GSH и оптимальное редокс-состояние. Субфизиологический уровень GSH может приводить к накоплению АФК и, как следствие, к окислительному стрессу. Наоборот, увеличенный синтез GSH повышает антиоксид антный потенциал и стимулирует метаболическую активность.
Клетки обычно страдают от окислительного стресса по причине одного из трех факторов: 1) увеличение образования оксиданта, 2) снижение антиоксидантной защиты и 3) неспособность осуществить репарацию окислительного повреждения. Окислительное повреждение может происходить в ДНК, белках и липидах. GSH играет центральную роль в нейтрализации практически всех реакций АФК через посредство прямых и косвенных путей. Главное клеточное повреждение, вызываемое АФК, представляет собой окисление макромолекул, таких как полиненасыщенные жирные кислоты в мембранных липидах, незаменимые белки и ДНК.
Доказательства в поддержку настоящего изобретения можно найти в экспериментах, описанных в разделе «Примеры».
Пример 1 представляет собой исследование кроликов, которых кормили кормом с сухим обезжиренным молоком. Использованное сухое обезжиренное молоко получали либо из молока, содержащего только вариант А1 бета-казеина (А1), или из молока, содержащего только вариант А2 бета-казеина (А2). Результаты показаны на Фиг. 1-4. На Фиг. 1 и 2 показано повышенное всасывание как цистеина, так и GSH в подвздошной кишке и печени кроликов, которых кормили кормом А2. Поскольку печень является основным запасающим органом для гомеостаза GSH, увеличение количества GSH печени указывает на общее увеличение уровней GSH в организме. Лобная доля и области гиппокампа из мозга, выделенного из кроликов, которых кормили кормом А2, также имели повышенные уровни GSH по сравнению с теми же областями мозга, выделенными из кроликов на корме А1. Низкие уровни GSH в лобной доле влекут за собой такие нарушения как аутизм, синдром дефицита внимания и гиперактивности (ADHD), синдром Дауна и шизофрению. Низкие уровни в гиппокампе могут влиять на восстановление памяти. Низкие уровни цистеина в гиппокампе были обнаружены у пациентов, страдающих от аутизма и болезни Альцгеймера. Полученные результаты указывают на то, что кролики, которых кормили кормом А2, имели относительно большую антиоксидантную способность в различных органах тела и особенно в мозге по сравнению с кроликами, которых кормили кормом А1.
Пример 2 описывает двойное слепое рандомизированное контролируемое перекрестное исследование 2×2, в котором здоровые участники употребляли каждый день 2×250 мл обычного молока, содержащего оба варианта бета-казеина А1 и А2, или молока, содержащего только вариант бета-казеина А2. Измеряли концентрации глутатиона в плазме. Было обнаружено, что употребление молока, содержащего только бета-казеин А2, связано с большим увеличением концентрации глутатиона в плазме по сравнению с употреблением молока, содержащим оба варианта бета-казеина.
Предварительные исследования показали, что сывороточный белок молока, который не приводит к образованию ВСМ-7 в ходе протеолиза, стимулирует абсорбцию цистеина и синтез GSH, тогда как опиоидные пептиды, полученные из бета-казеина и пшеницы, ингибируют поглощение цистеина, снижают концентрации GSH и снижают антиоксидантный потенциал (то есть снижают отношение GSH/GSSG). Результаты примера 2 согласуются с результатам этих предварительных исследований и свидетельствуют о том, что бета-казеин А1 ограничивает количество цистеина, абсорбирующегося из молока, и следовательно, способность синтезировать GSH. Устранение бета-казеина А1 из молочного рациона обеспечило возможность для большего роста уровней синтеза GSH, возможно, посредством устранения ингибирующего действия ВСМ-7 на всасывание цистеина. Таким образом, ежедневное употребление обычного коммерчески доступного молока связано с увеличением уровней GSH, возможно, как следствия повышенного запаса цистеина в сывороточном белке. Однако величина возросшего уровня антиоксиданта больше в случае употребления молока, содержащего только варианта А2 бета-казеина, по сравнению с употреблением молока, содержащего оба варианта бета-казеина А1 и А2 вместе. Эти результаты подразумевают, что устранение бета-казеина А1 из молока может обеспечить возможность для большего роста уровней GSH и, следовательно, большую антиоксидантную способность.
Все эксперименты, описанные выше, показывают четкую связь между потреблением бета-казеина А2 и высокими уровнями GSH (и его предшественника цистеина) в крови, а также в печени и мозговой ткани по сравнению с употреблением бета-казеина А1. Поскольку GSH представляет собой основную защиту организма против АФК, и известно, что АФК в значительной степени причастны к широкому спектру заболеваний, терапевтическая и профилактическая польза замены получаемого из пищи бета-казеина А1 на бета-казеин А2 очевидна.
Согласно настоящему изобретению предложено решение, которое сравнительно легко воплотить, в частности, путем отказа от молока или молочных продуктов, которые содержат бета-казеин А1, и обеспечения того, чтобы молоко и молочные продукты в рационе питания содержали бета-казеин, который представляет собой преимущественно бета-казеин А2, предпочтительно 100% бета-казеин А2.
Любые ссылки на документы из уровня техники в настоящем описании не следует рассматривать как признание, что такой уровень техники широко известен или составляет часть общедоступных знаний в данной области техники.
Используемые в настоящем описании изобретения термины «содержит/включает», «содержащий/включающий» и схожие слова не следует толковать в исключающем или исчерпывающем смысле. Другими словами, они подразумевают «содержащий/включающий, но не ограничивающийся этим».
Настоящее изобретение дополнительно описано со ссылкой на нижеследующие примеры. Следует понимать, что заявленное изобретение не ограничивается никаким образом этими примерами.
ПРИМЕРЫ
Пример 1: Влияние употребления бета-казеина А1 в сравнении с употреблением бета-казеина А2 на уровни цистеина и GSH у кроликов
В общем количестве 10 самцов кроликов (линия NZW, соответствующего возраста и/или массы) распределяли случайным образом на две группы и назначали кроличий корм с сухим обезжиренным молоком (СОМ) в качестве основного источника белка в течение общего срока 12 недель. Общее содержание белка составляло 16,8%, для 60% этого белка источником было СОМ, то есть 10% рациона состояло из молочного белка. Использованное СОМ было получено либо из молока, содержащего только вариант А1 бета-казеина (А1), или молока, содержащего только вариант А2 бета-казеина (А2). Корм с СОМ проверяли на вкусовую привлекательность, чтобы исключить любые проблемы, связанные с отказом кроликов употреблять корм. К концу 12-недельного периода кроликов умерщвляли. Получали образцы тканей и хранили их при температуре -80°С до дальнейшего применения. Ткани лизировали с использованием 1X лизирующего буфера и лизаты тканей обрабатывали ультразвуком в течение 15 секунд на льду. 100 мкл обработанного ультразвуком образца (сониката) использовали для определения концентрации белка. Оставшийся лизат помещали в микроцентрифужную пробирку и добавляли равный объем 0,4 н. перхлорной кислоты, затем инкубировали на льду в течение 5 мин. Образцы центрифугировали при 13000 об./мин и переносили супернатант в новые микроцентрифужные пробирки. 100 мкл образца добавляли в коническую пробирку микроавтодозатора и хранили при 4°С в штативе автодозатора с охлаждением. 10 мкл этого образца вводили в ВЭЖХ-систему. Достигали разделения метаболитов окислительно-восстановительного пути и метилирования с помощью аналитической колонки Agilent Eclipse XDB-C8 (3×150 мм; 3,5 мкм) и предколонки Agilent Eclipse XDB-С8 (4,6×12,5 мм; 5 мкм). Использовали две мобильные фазы. Мобильная фаза А представляла собой раствор 0% ацетонитрила, 25 мМ натрия фосфата, 1,4 мМ 1-октансульфоной кислоты, подведенный до рН 2,65 ортофосфорной кислотой. Мобильная фаза В представляла собой 50% раствор ацетонитрила. Устанавливали начальную скорость потока 0,6 мл/мин и использовали ступенчатый градиент: 0-9 мин - 0% фазы В, 9-19 мин - 50% фазы В, 19-30 мин - 50% фазы В. Затем уравновешивали колонку 5% фазы В в течение 12 мин перед следующим вводом. Поддерживали температуру 27°С. Электрохимическим детектором был ESA CoulArray с аналитической ячейкой BDD Analytical cell Model 5040, и устанавливали рабочее напряжение 1500 мВ. Концентрации образцов определяли по площадям пиков метаболитов с использованием стандартных калибровочных кривых и поставляемого фирмой ESA программного оборудования для ВЭЖХ. Концентрации образцов нормализовали относительно содержания белка. В некоторых случаях образцы при необходимости разбавляли мобильной фазой или инжектировали до 50 мкл образца, чтобы гарантировать, что уровни тиола находятся в диапазоне калибровочной кривой.
Целевые ткани, включая желудочно-кишечный тракт, печень и две разных части мозга (гиппокамп и лобная доля), собирали и анализировали в них уровни цистеина и уровни GSH. Результаты представлены на Фиг. 1-4.
Пример 2: Влияние бета-казеина А1 в сравнении с бета-казеином А2 на концентрации GSH в образцах плазмы крови у человека
Удовлетворяющие критериям китайские мужчины и женщины включали людей в возрасте 25-68 лет, которые нерегулярно употребляли молоко и обладали согласно собственной оценке непереносимостью коммерческого молока, имели согласно собственной оценке дискомфорт при переваривании пищи после употребления молока и имели соответствующие норме кардиограммы и кровяное давление в ходе спокойного дыхания. В общем количестве 21 мужчина и 24 женщины в возрасте среднее значение ± стандартное отклонение (SD) 46,6±14,0 лет были включены в исследование. У двадцати трех было подтверждена лактозная недостаточность на основе результатов анализов на галактозу в моче.
Участники употребляли обычное коммерчески доступное молоко, содержащее варианты А1 и А2 бета-казеина (А1/А2), в фазе 1 или коммерчески доступное молоко, содержащее только вариант А2 бета-казеина (А2), в фазе 2 (А1/А2→А2; последовательность 1) или наоборот (А2→А1/А2; последовательность 2). Определили отношение бета-казеина А1 к А2 в молоке, содержащем оба варианта бета-казеина, как 42:58 с помощью УВЭЖХ с диодно-матричным детектором и тандемной масс-спектрометрии. Каждая фаза исследования длилась 2 недели с 2-недельными периодами отмывки перед вступлением в фазу 1 и между фазами 1 и 2. Участники согласно указаниям употребляли 250 мл молока после 2 приемов пищи в день каждый день. Им запрещалось употреблять другие молочные продукты, но они могли употреблять немолочные продукты в ходе исследования. Исследование проводилось в соответствии с Хельсинской декларацией с изменениями и дополнения, принятыми в Сеуле в 2008 году, и было одобрено этическим комитетом Шанхайского общества питания (регистрационный номер: SNSIRB#2014[002]). Исследование было зарегистрировано с помощью сайта ClinicalTrials.gov (идентификатор: NCT02406469).
Образцы крови отбирали на исходном уровне и в конце каждой фазы исследования для измерения лабораторных параметров, включая GSH. Плазму хранили при -80°С до возникновения необходимости в проведении анализов. Образцы плазмы размораживали на льду и добавляли 5 мкл 0,4 н. раствора перхлорной кислоты к 200 мкл плазмы для осаждения любых оставшихся белков.
Общие концентрации GSH измеряли при 412 нм с использованием цикличной реакции GSH с дитионитробензоатом в присутствии избытка глутатионредуктазы. Результаты выражали в нмолях образовывающейся 5-тио-2-нитробензойной кислоты (выраженной как мин-1 мг-1 белка). Концентрацию GSH измеряли дважды для каждого образца в ходе независимых анализов.
Концентрации GSH были сильно асимметричны согласно критерию Колмогорова-Смирнова. Следовательно, данные анализировали с использованием двухвыборочного критерия Уилкоксона с фазой и перекрестом в качестве фиксированных эффектов, и брали Р<0,05 для обозначения статистически значимого эффекта фазы или перекреста.
Набор медианных концентраций GSH в начале и конце каждой фазы в обеих последовательностях показан на Фиг. 5 Результаты двухвыборочного критерия Уилкоксона показаны в Таблице 1.
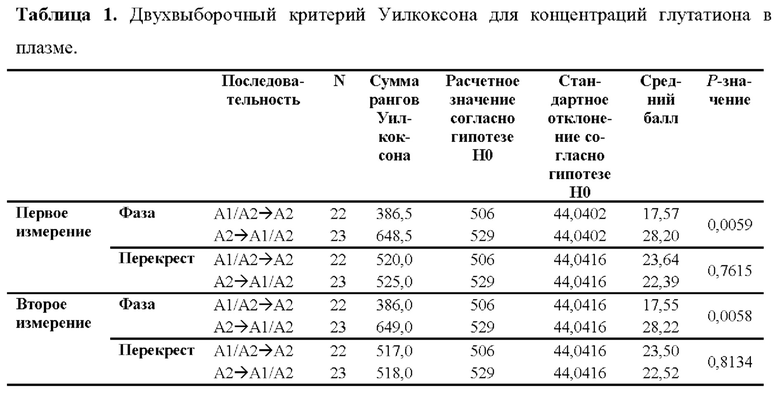
Употребление молока, содержащего только вариант бета-казеина А2, было связано со значительно большим увеличением концентраций GSH в плазме относительно исходного уровня к концу фазы исследования по сравнению с употреблением молока, содержащего оба варианта бета-казеина. Это увеличение происходило в обеих последовательностях в независимости от того, какой молочный продукт употреблялся первым. Изменение среднее значение ± стандартная ошибка среднего (СОС) концентраций GSH относительно исходного уровня составило 4,01±0,61 нмоль/мл для молока, содержащего бета-казеин А2, по сравнению с 1,99±0,50 нмоль/мл для молока, содержащего бета-казеин А1 и бета-казеин А2. Изменение относительно исходных концентраций GSH в случае бета-казеина А2 имело тенденцию быть выше в фазе 1 (последовательность А2→А1/А2), чем в фазе 2 (последовательность А1/А2→А2) (4,07 в сравнении с 2,70 нмоль/мл).
Несмотря на то, что настоящее изобретение было описано с помощью примера, следует понимать, что могут быть осуществлены изменения и модификации без отступления от объема настоящего изобретения, как определено в формуле изобретения. Кроме того, в случае существования известных эквивалентов конкретным признакам, такие эквиваленты включены в настоящее изобретение, как если бы специально цитировались в данном описании изобретения.
Изобретение относится к способу улучшения антиоксидантной способности у животного путем увеличения уровня глутатиона в крови или ткани указанного животного, включающему обеспечение указанного животного композицией для потребления, содержащей бета-казеин, где указанный бета-казеин содержит по меньшей мере 75% по массе по меньшей мере одного бета-казеина, не способного образовывать бета-казоморфин-7 при ферментативном расщеплении. Варианты применения включают применение в качестве оксиданта для лечения или профилактики симптомов рака, воспаления, квашиоркора (дефицита белка), припадка, аутизма, синдрома Дауна, синдрома хронической усталости, болезни Альцгеймера, болезни Паркинсона, серповидно-клеточной анемии, заболевания печени, муковисцидоза, ВИЧ, СПИД, инфекции, инфаркта миокарда, инсульта и диабета, для предотвращения или снижения эффектов старения, стимулирования восстановления ткани после физической нагрузки и стимулирования фертильности. 11 з.п. ф-лы, 5 ил., 1 табл., 2 пр.
1. Способ улучшения антиоксидантной способности у человека путем увеличения уровня глутатиона в крови или ткани указанного человека, указанный способ включает обеспечение указанного человека композицией, содержащей бета-казеин, где указанный бета-казеин содержит по меньшей мере 75% по массе по меньшей мере одного бета-казеина, не способного образовывать бета-казоморфин-7 при ферментативном расщеплении.
2. Способ по п. 1, отличающийся тем, что по меньшей мере один указанный бета-казеин выбран из бета-казеинов типа А2.
3. Способ по любому из пп. 1, 2, отличающийся тем, что прием указанной композиции внутрь предотвращает развитие или снижает риск развития заболеваний или нарушений, связанных с окислительным стрессом.
4. Способ по п. 3, отличающийся тем, что указанные заболевания или нарушения, связанные с окислительным стрессом, выбраны из группы, включающей рак, воспаление, квашиоркор (дефицит белка), припадок, аутизм, синдром Дауна, синдром хронической усталости, болезнь Альцгеймера, болезнь Паркинсона, серповидно-клеточную анемию, заболевание печени, муковисцидоз, ВИЧ, СПИД, инфекцию, инфаркт миокарда, инсульт и диабет.
5. Способ по любому из пп. 1, 2, отличающийся тем, что прием указанной композиции внутрь предотвращает или снижает эффекты старения, стимулирует восстановление ткани после физической нагрузки или стимулирует фертильность.
6. Способ по любому из пп. 1-5, отличающийся тем, что указанный бета-казеин содержит по меньшей мере 90% по массе бета-казеина А2 по массе.
7. Способ по любому из пп. 1-6, отличающийся тем, что указанный бета-казеин содержит 100% бета-казеина А2.
8. Способ по любому из пп. 1-7, отличающийся тем, что указанная композиция представляет собой молоко или молочный продукт.
9. Способ по п. 8, отличающийся тем, что указанное молоко представляет собой свежее молоко, молоко в порошке, жидкое молоко, восстановленное из порошка, обезжиренное молоко, гомогенизированное молоко, сгущенное молоко, концентрированное молоко, пастеризованное молоко или непастеризованное молоко.
10. Способ по п. 8, отличающийся тем, что указанный молочный продукт представляет собой сливки, йогурт, творог, сыр, масло, мороженое, детскую смесь, пищевой продукт для взрослых, белковую добавку или корм для домашних животных.
11. Способ по п. 8 или 9, отличающийся тем, что указанное молоко получают путем тестирования генотипа или фенотипа коров и доения только тех коров, в отношении которых было определено, что указанные коровы в своем молоке вырабатывают только бета-казеин типа А2.
12. Способ по п. 11, отличающийся тем, что указанное молоко получают посредством
(i) формирования стада коров, которое содержит только тех коров, в отношении которых было определено, что указанные коровы вырабатывают только бета-казеин типа А2 в своем молоке; и
(ii) доения по меньшей мере одной коровы из указанного стада.
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Устройство для закрепления лыж на раме мотоциклов и велосипедов взамен переднего колеса | 1924 |
|
SU2015A1 |
| Устройство для остановки поршня при движении паровоза без пара | 1928 |
|
SU14076A1 |
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| ТЕТРАПЕПТИД, ОБЛАДАЮЩИЙ ГЕРОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ, ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО НА ЕГО ОСНОВЕ И СПОСОБ ЕГО ПРИМЕНЕНИЯ | 1999 |
|
RU2157233C1 |
| КОМПОЗИЦИЯ С АНТИОКСИДАНТНЫМИ СВОЙСТВАМИ И СПОСОБ ЛЕЧЕНИЯ БОЛЕЗНЕЙ МЛЕКОПИТАЮЩИХ | 2002 |
|
RU2280448C2 |
Авторы
Даты
2021-07-21—Публикация
2016-05-20—Подача