ОБЛАСТЬ ТЕХНИКИ
Изобретение относится к анализу белков бета-казеина, присутствующих в молоке животных и молочных продуктах, изготовленных из молока животных. В частности, изобретение относится к тестированию на наличие и количественное определение бета-казеинов типа А1 и бета-казеинов типа А2, и родственных вариантов бета-казеина в молоке и молочных продуктах, полученных из молока.
УРОВЕНЬ ТЕХНИКИ
Молоко, главным образом, молоко крупного рогатого скота, которое потребляют популяции по всему миру, является важным источником белка в рационе человека. Обычно молоко крупного рогатого скота содержит приблизительно от 30 до 40 грыамм белка на литр. Казеины составляют самую большую часть (80%) указанного количества белка, а бета-казеины составляют приблизительно 37% казеинов. В течение двух последних десятилетий происходило накопление данных, указывающих на участие казеиновых белков, в частности, бета-казеинов, в различных физиологических или биологических процессах (некоторые из которых связаны с нарушениями здоровья).
Бета-казеины могут быть разделены на бета-казеины типа A1 и бета-казеины типа A2. Бета-казеин A1 и бета-казеин A2 являются преобладающими бета-казеинами в молоке крупного рогатого скота, потребляемом большинством популяций человека. Различные варианты бета-казеина могут быть отнесены к категориям типа А1 или типа А2 на основании аминокислотного остатка в положении 67 в последовательности бета-казеина из 209 аминокислот. Бета-казеин А1 отличается от бета-казеина А2 одной аминокислотой. В положении 67 находится аминокислота гистидин, тогда как в бета-казеине А2 в том же положении находится пролин. Однако это единственное различие в аминокислотах является критически важным для ферментативного расщепления бета-казеинов в кишечнике. Присутствие гистидина в положении 67 при ферментативном расщеплении позволяет продуцировать фрагмент белка, содержащий семь аминокислот, известный как бета-казоморфин-7 (БКМ-7). Таким образом, БКМ-7 является продуктом расщепления бета-казеина A1. В случае бета-казеина A2 в положении 67 находится пролин, который мешает расщеплению аминокислотной связи в этом месте. Таким образом, БКМ-7 не является продуктом расщепления бета-казеина A2.
В других вариантах бета-казеина, таких как варианты B, C, F, G и H1, в положении 67 также находится гистидин, тогда как в вариантах A3, D, E, H2 и I в положении 67, как и во варианте А2, находится пролин. Однако указанные варианты обнаружены только в очень низких концентрациях или вообще не обнаружены в молоке коров европейского происхождения. Таким образом, в контексте настоящего изобретения термин «бета-казеин A1» может относиться к любому бета-казеину с гистидином в положении 67, а термин «бета-казеин А2» может относиться к любому бета-казеину с пролином в положении 67.
BCM-7 представляет собой опиоидный пептид, который может связываться с опиоидными рецепторами и активировать их по всему организму; было продемонстрировано, что он ограничивает производство глутатиона/антиоксидантов, что приводит к изменению функции клеток и экспрессии генов.1 БКМ-7 обладает способностью проникать через стенку желудочно-кишечного тракта и поступать в кровоток, что дает ему возможность влиять на системную и клеточную деятельность через опиоидные рецепторы. Автор настоящего изобретения и другие ранее установили нежелательную связь между потреблением бета-казеина A1, обнаруженного в молоке или молочных продуктах, и диабетом I типа,2 ишемической болезнью сердца,3 неврологическими расстройствами,4 воспалением кишечника,5 симптомами непереносимости лактозы,6 регуляцией концентраций глюкозы в крови,7 когнитивными функциями8 и кишечной микробиотой.9
Все указанные данные относятся к влиянию БКМ-7 или вариантов бета-казеина, которые при расщеплении дают БКM-7, на поведенческие характеристики индивидуумов, страдающих клинически диагностированными заболеваниями или состояниями. Эти данные не касаются здоровых людей. Кроме того, хорошо известно, что результаты исследований, основанных на экспериментах с клеточными культурами, нельзя однозначно экстраполировать на условия in vivo или на эффекты в клинической практике, поскольку существует множество переменных факторов, относящихся к продуцированию, транспорту и метаболизму БКM-7, которые влияют на воздействие на ткани и, следовательно, на биологический ответ. Например, известно, что для клеточного ответа важны концентрации опиоидов и их аффинность к опиоидным рецепторам.
Рост объема научных данных, связывающих варианты бета-казеина с неблагоприятными последствиями употребления молока и молочных продуктов, привели к важности возможности надежного и точного анализа молока и молочных продуктов на присутствие вариантов бета-казеина, в частности, бета-казеина A1 и родственных ему вариантов, содержащих гистидин в положении 67 аминокислотной последовательности.
Определение общих концентраций бета-казеинов в молоке крупного рогатого скота относительно тривиально. Наиболее распространенный подход включает разделение интактных белков посредством жидкостной хроматографии (ЖХ) с последующей детекцией с применением либо ультрафиолетового детектора (УФ), либо масс-спектрометрии (МС). Этот подход недавно применялся Винсентом (Vincent) с соавторами10 для изучения молока в Австралии и Гивенсом (Givens) с соавторами11 для изучения молока в Великобритании. В обоих случаях основные варианты бета-казеина могли быть детектированы по отдельности, но, поскольку очищенные варианты бета-казеина отсутствуют в продаже в виде аналитических стандартов, их невозможно количественно определить по отдельности. Более того, оба способа требовали применения масс-спектрометра высокого разрешения, а также не обладают достаточной чувствительностью, чтобы различать следовые уровни варианта бета-казеина A1 в присутствии избытка варианта бета-казеина A2.
Альтернативный подход включает расщепление молочных белков и количественное определение образованных в результате пептидов. Этот подход был использован Lutter с соавторами12, которые применяли трипсин для расщепления ряда пищевых продуктов для определения концентраций основных молочных белков. Образцы анализировали методом ЖХ-МС/МС с использованием внутренней калибровки. Хотя этот способ более чувствителен и более специфичен, чем способы с использованием интактного белка, он лишен критически важной способности различать варианты бета-казеина.
Хотя вышеперечисленные опубликованные способы могут подходить для анализа свежего молока, не существует способа, который удовлетворял бы всем необходимым аналитическим требованиям для современных отдельных вариантов молочных продуктов. Это, в частности, характерно для таких продуктов, как ультрапастеризованное молоко или детские смеси, где в процессе обработки может происходить существенное изменение белков. Во время анализа казеины в указанных матрицах могут вести себя не так, как казеины «дикого типа» из свежего молока, поэтому аналитические процедуры должны быть адаптированы в соответствии с матрицей. Например, анализ интактных бета-казеинов из образцов сырого молока с использованием ЖХ-УФ выдает отдельные пики для каждого варианта бета-казеина, которые подходят как для качественного, так и для количественного анализа, поскольку их можно легко идентифицировать и интегрировать. Напротив, та же процедура, применяемая к детской смеси, выдает широкие пики, которые не разрешаются и не подходят для качественного или количественного анализа.
Способы анализа, где используется расщепление протеолитическими ферментами, также могут быть сопряжены с проблемами, которые препятствуют их применению при анализе бета-казеина. Наиболее широко применяемой протеазой является трипсин, который при контакте с бета-казеином продуцирует длинный пептид, содержащий 48 остатков. Значительная длина этого пептида означает, что он подвержен множеству модификаций, которые приводят к изменению массы, что, в свою очередь, существенно усложняет детекцию с применением масс-спектрометрии. Кроме того, указанная длина затрудняет синтез этого пептида для применения в качестве аналитического стандарта, что, следовательно, означает, что способы расщепления на основе трипсина не подходят для количественного анализа бета-казеина в определенных молочных продуктах. Таким образом, для анализа бета-казеина необходимо применение альтернативных ферментов.
Автор настоящего изобретения разработал способ абсолютного определения бета-казеина A1 и вариантов бета-казеина A2 в молоке и молочных продуктах на коммерчески значимых уровнях.
Таким образом, цель изобретения заключается в том, чтобы обеспечить способ анализа вариантов бета-казеина в молоке животных и продуктах, полученных из молока животных, или, по меньшей мере, обеспечить полезную альтернативу существующим способам.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Согласно первому аспекту настоящего изобретения предложен способ определения количеств вариантов бета-казеина типа A1 или вариантов бета-казеина типа A2 в композиции с точностью более 80%, где варианты бета-казеина типа A1 представляют собой варианты бета-казеина, содержащие гистидин в положении 67 аминокислотной последовательности бета-казеина, а варианты бета-казеина типа A2 представляют собой варианты бета-казеина, содержащие пролин в положении 67 аминокислотной последовательности бета-казеина, и где указанная композиция представляет собой молоко или продукт, изготовленный из молока, содержащий этапы:
(i) приведение указанной композиции в контакт с химотрипсином в условиях, позволяющих расщепление бета-казеинов в композиции химотрипсином;
(ii) получение водного раствора пептидов, образованных при расщеплении бета-казеина;
(iii) определение концентраций:
a) двух или более пептидов, образованных при расщеплении бета-казеина, присутствующих в растворе, где каждый пептид содержит от 8 до 20 аминокислотных остатков и содержит гистидин в положении, соответствующем положению 67 аминокислотной последовательности бета-казеина; а также
b) двух или более пептидов, образованных при расщеплении бета-казеина, присутствующих в растворе, где каждый пептид содержит от 8 до 20 аминокислотных остатков и содержит пролин в положении, соответствующем положению 67 аминокислотной последовательности бета-казеина;
путем анализа смеси с применением жидкостной хроматографии-масс-спектрометрии; а также
(iv) вычисление концентрации вариантов бета-казеина типа А1 в композиции или концентрации вариантов бета-казеина типа А2 в композиции с использованием концентраций пептидов, образованных при расщеплении бета-казеина, определенных на этапе (iii).
В определенных вариантах реализации настоящего изобретения варианты бета-казеина типа A1 содержат любые одно или более из: бета-казеина А1, бета-казеина В, бета-казеина С, бета-казеина F, бета-казеина G и бета-казеина H1. Например, варианты бета-казеина типа A1 могут содержать только бета-казеин A1.
В определенных вариантах реализации настоящего изобретения варианты бета-казеина типа A2 содержат любые одно или более из: бета-казеина А2, бета-казеина А3, бета-казеина D, бета-казеина E, бета-казеина H2 и бета-казеина I. Например, варианты бета-казеина типа A2 могут содержать только бета-казеин A2.
В некоторых вариантах реализации варианты настоящего изобретения бета-казеина типа A1 включают только бета-казеин A1, а варианты бета-казеина типа А2 включают только бета-казеин А2.
В некоторых вариантах реализации настоящего изобретения определяют концентрации трех или четырех пептидов, образованных при расщеплении бета-казеина, содержащих гистидин в положении, соответствующем положению 67 аминокислотной последовательности бета-казеина. В некоторых вариантах реализации, в которых молоко представляет собой молоко крупного рогатого скота, пептиды, образованные при расщеплении бета-казеина, выбирают из группы, содержащей: VYPFPGPIHN, SLVYPFPGPIHN, VYPFPGPIHNSLPQ и SLVYPFPGPIHNSLPQ.
В некоторых вариантах реализации настоящего изобретения определяют концентрации трех или четырех пептидов, образованных при расщеплении бета-казеина, содержащих пролин в положении, соответствующем положению 67 аминокислотной последовательности бета-казеина. В некоторых вариантах реализации, в которых молоко представляет собой молоко крупного рогатого скота, пептиды, образованные при расщеплении бета-казеина, выбирают из группы, содержащей VYPFPGPIPN, SLVYPFPGPIPN, VYPFPGPIPNSLPQ и SLVYPFPGPIPNSLPQ.
В определенных вариантах реализации настоящего изобретения смесь, анализируемая с применением жидкостной хроматографии-масс-спектрометрии, содержит изотопно-меченые пептиды, соответствующие каждому из пептидов из а) и b). Изотопно-меченые пептиды могут быть добавлены к композиции перед обработкой химотрипсином на этапе (i) или после обработки химотрипсином на этапе (i).
В некоторых вариантах реализации настоящего изобретения, где молоко представляет собой молоко крупного рогатого скота, изотопно-меченые пептиды могут соответствовать следующим пептидам, образованным при расщеплении:
В некоторых вариантах реализации настоящего изобретения, где молоко представляет собой молоко крупного рогатого скота, изотопно-меченые пептиды могут соответствовать следующим пептидам, образованным при расщеплении:
В некоторых вариантах реализации настоящего изобретения, в которых молоко представляет собой молоко крупного рогатого скота, определяют концентрации следующих пептидов на этапе (iii): VYPFPGPIHN, SLVYPFPGPIHN, VYPFPGPIHNSLPQ, SLVYPFPGPIHNSLPQ, VYPFPGPIPN, SLVYPFPGPIPN, VYPFPGPIPNSLPQ и SLVYPFPGPIPNSLPQ.
В некоторых вариантах реализации настоящего изобретения количества вариантов бета-казеина типа А1 и вариантов бета-казеина типа А2 в композиции определяют с точностью более 90%, точностью более 95% или точностью более 99%.
В некоторых вариантах реализации настоящего изобретения композиция представляет собой молоко крупного рогатого скота или молочный продукт, изготовленный из молока крупного рогатого скота.
В некоторых вариантах реализации настоящего изобретения молоко представляет собой свежее молоко, сырое молоко, сухое порошковое молоко, жидкое молоко, восстановленное из порошка, обезжиренное молоко, гомогенизированное молоко, сгущенное молоко, концентрированное молоко, молоко с вкусоароматическими добавками, ультрапастеризованное молоко, пастеризованное молоко или непастеризованное молоко. В некоторых вариантах реализации настоящего изобретения молочный продукт представляет собой детскую смесь, сливки, йогурт, творог, сыр, масло или мороженое.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
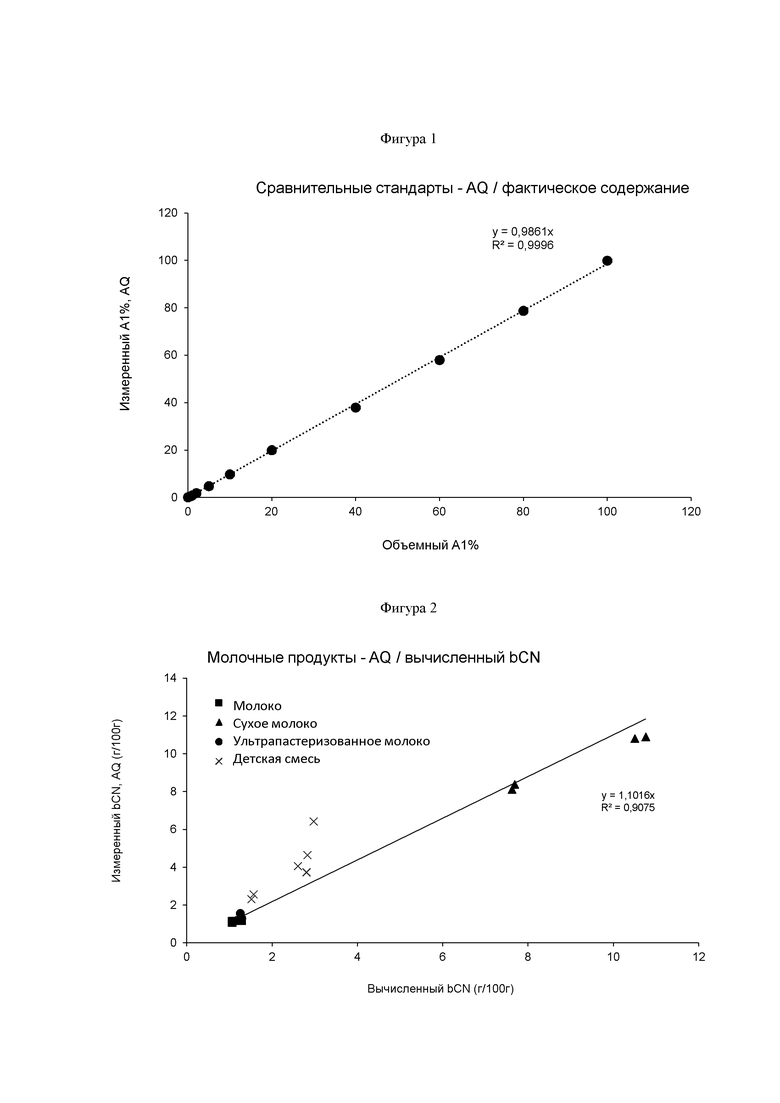
На фигуре 1 представлено относительное содержание бета-казеинов типа A1 в серии сравнительных стандартов молока, проанализированных с применением способа по настоящему изобретению, а также интактного ВЭЖХ-анализа.
На фигуре 2 показано количество бета-казеина в серии образцов молока и молочных продуктов по результатам измерений с применением способа по настоящему изобретению, со сравнением с теоретическим уровнем бета-казеина, определенным по содержанию белка в образцах.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Определения
Термин «бета-казоморфин-7», или «БКМ-7» относится к белковому фрагменту Tyr-Pro-Phe-Pro-Gly-Pro-Ile, гептапептиду, продуцируемому при ферментативном расщеплении вариантов бета-казеина крупного рогатого скота, которые в положении 67 аминокислотной последовательности содержат гистидин, а не пролин.
Термин «вариант бета-казеина типа А1» означает любой вариант бета-казеина, содержащий остаток гистидина в положении 67 аминокислотной последовательности и включает любое одно или более из: бета-казеина А1, бета-казеина В, бета-казеина С, бета-казеина F, бета-казеина G.
Термин «вариант бета-казеина типа А2» означает любой вариант бета-казеина, содержащий остаток пролина в положении 67 его аминокислотной последовательности и включает бета-казеин A2, бета-казеин A3, бета-казеин D, бета-казеин E, бета-казеин H1, бета-казеин H2 и бета-казеин I.
Термин «положение 67» аминокислотной последовательности бета-казеина означает положение с номером 67 при нумерации аминокислотных остатков в последовательности бета-казеина, начиная с N-конца (после удаления сигнального пептида).
Термин «AQ», иногда называемый «AQUA», означает «абсолютное количественное определение» и указывает на то, что способ по настоящему изобретению может применяться для измерения абсолютной концентрации бета-казеинов как фракции образца (т.е. массовой доли), в отличие от других способов, с помощью которых не измеряют абсолютные концентрации, а измеряют содержание бета-казеинов относительно другого компонента в образце, или содержание одного варианта бета-казеина относительно другого.
В тексте настоящего описания, если иное конкретным образом не указано или контекст не требует иного, упоминание одиночного этапа, химического соединения, группы этапов или группы химических соединений следует рассматривать как включающее один и множество (то есть один или более) указанных этапов, химических веществ, групп этапов или групп химических веществ.
Подразумевается, что любое упоминание диапазона чисел в настоящем описании (например, от 1 до 10) также включает упоминание всех связанных чисел в этом диапазоне (например, 1, 1.1, 2, 3, 3.9, 4, 5, 6, 6.5, 7, 8, 9 и 10), а также любой диапазон рациональных чисел в этом диапазоне (например, от 2 до 8, от 1,5 до 5,5 и от 3,1 до 4,7), и, следовательно, все субдиапазоны всех диапазонов, упоминаемых в настоящем описании, раскрыты явным образом. Указанные величины представляют собой исключительно примеры конкретных предполагаемых величин, и все возможные комбинации числовых значений между самым низким и самым высоким значениями, должны, аналогичным образом, рассматриваться как явно оговоренные в настоящем описании.
В тексте настоящего описания термин «содержать», или такие варианты, как «содержит» или «содержащий», следует понимать как подразумевающие включение указанного элемента, целочисленного значения или этапа, или группы элементов, целочисленных значений или этапов, но не исключение любого другого элемента, целочисленного значения или этапа, или группы элементов, целочисленных значений или этапов.
Специалистам в данной области техники будет понятно, что в изобретение, описанное в настоящем документе, могут быть внесены изменения и модификации, помимо конкретным образом описанных. Следует понимать, что настоящее изобретение включает все такие варианты и модификации. Настоящее изобретение также включает все этапы или признаки, упомянутые или указанные в настоящем документе, по отдельности или в совокупности, и любые комбинации или любые два или более из указанных этапов или признаков.
Объем настоящего изобретения не ограничен конкретными описанными в настоящем документе примерами, которые предназначены исключительно для иллюстрации. Функционально эквивалентные продукты, композиции и способы явным образом включены в объем настоящего изобретения.
Никакая ссылка на известные из уровня техники документы в настоящем описании не должна рассматриваться как допущение, что такой уровень техники широко известен или входит в общеизвестные знания в данной области техники.
Методика тестирования
Настоящее изобретение обеспечивает способ определения количеств вариантов бета-казеина типа А1 и вариантов бета-казеина типа А2 в композиции. Важно отметить, что указанный способ позволяет определять количество вариантов бета-казеина этих двух типов с точностью более 80% и даже до 100%. Степень точности стала критически важной, поскольку спрос на молоко и молочные продукты без бета-казеина A1 (и родственных вариантов) резко вырос за последнее десятилетие. Потребителям, а также производителям и поставщикам, необходимо знать, действительно ли продукт по существу не содержит вариантов бета-казеина типа A1.
Указанный способ включает расщепление белков бета-казеина в композиции сериновой протеазой – ферментом химотрипсином. Автор настоящего изобретения установил, что способ расщепления дает специфические поддающиеся идентификации пептиды. Можно определить наличие и количество каждого пептида, получаемого из композиции, а затем использовать эти количества для вычисления процентного количества вариантов бета-казеина типа А1 и вариантов бета-казеина типа А2 в композиции. Количество исследованных пептидов (например, 2, 3, 4 и более) определяет степень точности. Например, анализ всего двух пептидов может обеспечить окончательное определение процентного количества вариантов бета-казеина двух типов в составе с уровнем точности до 80%. Анализ трех пептидов может дать уровень точности около 90%, а анализ четырех пептидов может дать уровень точности около 95%.
Анализируемая композиция может представлять собой молоко любого животного или продукт, изготовленный из молока животного. Композиция также может представлять собой немолочный продукт, содержащий бета-казеин, который получен из молока.
Молоко может быть в форме свежего молока, сырого молока, сухого молока, жидкого молока, восстановленного из порошка, обезжиренного молока, гомогенизированного молока, сгущенного молока, концентрированного молока, пастеризованного молока или не пастеризованного молока, или в любой другой форме молока.
Способ согласно настоящему изобретению лучше всего подходит для анализа молока крупного рогатого скота и продуктов из молока крупного рогатого скота, но может быть легко адаптирован к молоку и молочным продуктам от широкого круга животных, включая человека, овец, коз, лошадей, свиней, буйволов, оленей и любых других млекопитающих, которые продуцируют казеины в молоке.
Композиция также может также представлять собой любой продукт, полученный из молока, такой как детская смесь, сливки, йогурт, творог, сыр, масло или мороженое.
Если анализируемой композицией является молоко, требуется минимальная подготовка образца. Предпочтительнее денатурировать белки, содержащиеся в образце молока, например, путем обработки таким денатурирующим агентом, как гидрохлорид гуанидина или мочевина.
В случае твердых или полутвердых молочных продуктов подготовка образца обычно включает взвешивание некоторого количества гомогенизированного продукта в отдельном сосуде и экстрагирование казеиновых белков в известный объем раствора.
Расщепление бета-казеинов в образце с применением химотрипсина может быть проведено в условиях, подходящих для обеспечения эффективного расщепления. Образец обычно инкубируют при температуре около 37°C в течение нескольких часов перед остановкой реакции таким реагентом, как муравьиная кислота, для дезактивации химотрипсина.
После расщепления образца химотрипсином и любой подготовки образца после расщепления к образцу перед анализом ЖК-МС (жидкостная хроматография - масс-спектрометрия) добавляют определенные изотопно-меченые пептиды. Изотопно-меченые пептиды выбирают на основании предварительного определения автором изобретения того, что химотрипсин разрушает варианты бета-казеина типа А1 с образованием в результате расщепления пептидов:
VYPFPGPIHN, SLVYPFPGPIHN, VYPFPGPIHNSLPQ, и SLVYPFPGPIHNSLPQ
и разрушает варианты бета-казеина типа А2 с образованием в результате расщепления пептидов:
VYPFPGPIPN, SLVYPFPGPIPN, VYPFPGPIPNSLPQ, и SLVYPFPGPIPNSLPQ
Изотопно-меченый пептид может быть из группы:
(*V)YPFPGPIHN, SL(*V)YPFPGPIHN, VYPFPGPIHNS(*L)PQ, SL(*V)YPFPGPIHNSLPQ, (*V)YPFPGPIPN, SL(*V)YPFPGPIPN, VYPFPGPIPNS(*L)PQ, и SL(*V)YPFPGPIPNSLPQ, где *V представляет собой изотопно-меченый остаток валина, а *L представляет собой изотопно-меченый остаток лейцина. Следует понимать, что любой или несколько аминокислотных остатков пептида могут быть изотопно-мечеными. Однако изотопно-меченые валин или лейцин более предпочтительны.
В некоторых вариантах реализации согласно изобретению, применяемые изотопно-меченые пептиды соответствуют пептидам, образованным при расщеплении, согласно таблице 1.
Таблица 1: Пептиды, образованные при расщеплении, и их изотопно-меченые эквиваленты
Способ по настоящему изобретению требует добавления к образцу по меньшей мере двух из указанных выше изотопно-меченых пептидов. Однако для большей точности к образцу добавляют три, четыре или, возможно, большее число изотопно-меченых пептидов.
ЖХ-МС/МС позволяет легко идентифицировать присутствие любого из пептидов, образованных при расщеплении, на основании времени удерживания пептидов и соотношения ионов фрагментов, образованных при анализе в режиме МС/МС. Этот режим, как вариант, называют мониторингом множественных реакций (ММР) или режимом мониторинга выбранной реакции (МВР). Сравнение отклика каждого пептида и изотопно-меченого пептида внутреннего стандарта, присутствующего в смеси, а также сравнение с одновременно получаемой стандартной кривой, позволяет определить концентрацию каждого пептида, на основе которой могут быть вычислены концентрации вариантов бета-казеина типа А1 в композиции и вариантов бета-казеина типа А2.
Обсуждение примеров
Примеры экспериментальных этапов приведены ниже. В примере 1 показано, как образцы могут быть подготовлены для анализа. Обычно подготовка включает экстракцию бета-казеинов в водную среду, где они могут быть развернуты под действием хаотропного денатурирующего агента, такого как мочевина, так что последующее действие химотрипсина на образец будет более эффективным. В случае жидких образцов, таких как цельное молоко или ультрапастеризованное молоко, подготовка включает просто перенос аликвоты образца в сосуд и добавление денатурирующего агента. Для твердых или полутвердых образцов подготовка включает приготовление точного раствора твердого вещества, растворенного в экстракционном буфере, как правило, водном буфере. Затем образцы обрабатывают таким же образом, как и жидкие образцы.
В примере 2 описан этап расщепления химотрипсином. На денатурированные образцы воздействуют раствором химотрипсина в тщательно контролируемых условиях. Эти условия обычно включают буфер для контроля pH раствора, поскольку протеолитические ферменты активны только в узком диапазоне значений pH. Условия обычно также включают механическое перемешивание гидролизата для уменьшения или устранения ограничений переноса массы и нагревание для ускорения реакции. Это приводит к контролируемому расщеплению бета-казеинов и других белков в матрице, с получением набора пептидов, которые могут быть однозначно идентифицированы как происходящие из конкретного белка. По истечении заранее установленного периода времени реакцию останавливают («гасят») добавлением концентрированного раствора кислоты в органическом растворителе, который немедленно останавливает расщепление. Затем образцы обогащают путем добавления изотопно-меченых пептидов внутреннего стандарта, которые впоследствии применяют для вычисления концентраций бета-казеинов.
В примере 3 описан анализ образцов с использованием жидкостной хроматографии с тройной квадрупольной масс-спектрометрической детекцией. Это приводит к пространственному и временному разделению пептидов друг от друга, которое может быть количественно определено индивидуальным образом по прохождению элюента к масс-спектрометру, работающему в режиме мониторинга множественных реакций, или путем настолько же специфической процедуры детекции, такой как мониторинг выбранных ионов с высоким разрешением. Площади пиков целевых пептидов определяют путем интеграции, а также с помощью изотопно-меченых внутренних стандартов. Затем отношения площадей пиков используют для определения концентрации целевых пептидов путем сравнения со стандартной кривой. Чтобы верифицировать корректную идентификацию пептидов, в процедуре используют критерии контроля качества, такие как соответствие времени удерживания и соотношения ионов.
В примере 4 концентрации пептидов используют для вычисления концентраций исходных бета-казеинов. В целом, коэффициенты пересчета выводят на основе отношения массы пептида к массе исходного белка и применяют для преобразования концентрации пептида в концентрацию белка. Поскольку целевые пептиды имеют перекрывающиеся последовательности, указанные концентрации можно суммировать, чтобы найти общее содержание бета-казеина типа A1 и общее содержание бета-казеина типа A2, а также показатели, происходящие из указанных значений, такие как относительное содержание бета-казеина типа A1 в образце в общем количестве бета-казеина.
В примере 5 представлено применение указанного способа для анализа ряда молочных продуктов. Результаты сравнивают и сопоставляют с результатами существующих способов определения процентного содержания бета-казеинов типа A1 в образце молока или молочных продуктах. Для нескольких типов матриц показано, что концентрация бета-казеинов в образце соответствует ожидаемым значениям на основании содержания меченого белка, и, следовательно, относительное содержание бета-казеинов типа A1 в образце определено корректно. Кроме того, относительное содержание бета-казеинов типа A1 согласуется с результатами существующих способов для простых матриц, таких как молоко или сухое молоко, но обеспечивает более точную расчетную оценку для сильно модифицированных продуктов, таких как детские смеси. Результаты представлены в таблице 6.
В столбце 1 таблицы 6 идентифицированы исследованные продукты. В столбце 2 приведено общее содержание белка в каждом образце, определенное с помощью анализа азота по Кьельдалю. Его можно сравнить с данными в столбце 3, где приведено содержание белка, указанное на этикетке продукта. В целом между этими двумя показателями есть удовлетворительное совпадение, указывающее, что содержание белка, указанное на этикетке является точным. В столбце 4 приведено теоретическое содержание бета-казеина в каждом образце, определенное путем умножения содержания белка, указанного на этикетке, на общепринятый коэффициент пересчета 0,32, представляющий собой массовую долю бета-казеина в молочных продуктах относительно общего содержания белка.
В столбце 9 приведено общее содержание бета-казеина, выраженное в г/100 г, как сумма бета-казеинов типа A1 и бета-казеинов типа A2, определенное способом по настоящему изобретению. В целом эти значения на удовлетворительном уровне совпадают со значениями в столбце 4, свидетельствуя, что указанный способ является точным и соответствует своему назначению.
В столбце 10 приведено процентное содержание бета-казеинов типа A1 относительно общего содержания бета-казеина, вычисленное как сумма бета-казеинов типа A1 и бета-казеинов типа A2. Эти результаты можно сравнить с результатами в столбце 5, где представлен A1%, определенный путем анализа интактного белка с применением высокоэффективной жидкостной хроматографии с УФ-детекцией. Для молока и молочных продуктов, которые не претерпели значимых изменений, эти два показателя на удовлетворительном уровне совпадают. Однако существуют значительные расхождения в случае образцов детских смесей, которые в силу характера их производства не пригодны для интактного анализа и дают ошибочные результаты. Аналогичные тенденции наблюдают при сравнении столбца 10 со столбцом 6, где приведено процентное содержание бета-казеинов типа A1, определенное с применением примитивного способа ферментации, задействующего триптическое расщепление образцов с последующей калибровкой по объемным разведениям сравнительных стандартов молока.
На фигуре 1 приведено относительное содержание бета-казеинов типа A1 в серии сравнительных стандартов молока, проанализированных с применением способа по настоящему изобретению, а также интактного ВЭЖХ-анализа. Образцы получали путем объемного разведения молока от двух индивидуальных животных, одно из которых имеет верифицированный генотип A1/A1 и, таким образом, дает молоко, содержащее бета-казеин чистого типа A1, а другое имеет генотип A2/A2, таким образом давая молоко, содержащее бета-казеин чистого типа А2. Плотная кластеризация точек данных вокруг кривой наилучшего соответствия указывает на то, что настоящий способ является прецизионным, на что указывает коэффициент корреляции (R2 = 0,9996). Интерпретация наклона кривой (0,9861) также указывает на точность способа.
На фигуре 2 показано количество бета-казеина в серии образцов молока и молочных продуктов, измеренное с применением способа по настоящему изобретению, со сравнением с теоретическим уровнем бета-казеина, определенным по содержанию белка в образцах. Хорошая кластеризация точек данных около кривой наилучшего соответствия указывает на то, что настоящий способ является прецизионным, на что также указывает коэффициент корреляции (R2 = 0,9075). Наклон кривой (0,9075) также указывает на точность способа.
Настоящее изобретение описано ниже путем отсылок к приведенным примерам. Следует понимать, что заявленное изобретение никоим образом не ограничено указанными примерами.
ПРИМЕРЫ
Пример 1: Подготовка образцов
Жидкие образцы - Для невязких жидких образцов, например, молока, жидкость (40 мкл) переносили в центрифужную пробирку объемом 2 мл. Добавляли раствор мочевины (120 мкл, 500 г/л) для денатурации белков, а затем смесь перемешивали при 2000 об/мин в течение 5 минут.
Твердые образцы - В случае твердых образцов или вязких жидких образцов образец (5,00 ± 0,01 г) взвешивали в пробирке Falcon (50 мл). Добавляли раствор бикарбоната аммония (46,6 мл, 4 г/л) и смесь встряхивали для смачивания всего порошка. После инкубации при 50 °C в течение 15 мин смесь встряхивали до гомогенного состояния. В случае детской смеси образец (100 мкл) переносили в центрифужную пробирку на 2 мл, добавляли осаждающий казеин агент (ацетат аммония 150 г/л, pH 4,2, 1000 мкл), смесь перемешивали при 2000 об/мин в течение 5 минут, а затем центрифугировали при 5000 g в течение 5 минут. После декантации супернатанта к твердому осадку добавляли осаждающий казеин агент (1000 мкл) и смесь перемешивали при 2000 об/мин в течение 5 минут, а затем центрифугировали при 5000 g в течение 5 минут перед декантацией супернатанта. К твердому осадку добавляли воду (1000 мкл), повторяли этапы перемешивания и центрифугирования и декантировали супернатант. Добавляли раствор мочевины (120 мкл, 500 г/л) для денатурации белков, а затем смесь перемешивали при 2000 об/мин в течение 5 минут.
Пример 2: Расщепление химотрипсином
Раствор химотрипсина (1000 мкл) добавляли к образцу, приготовленному в соответствии с примером 1. Смесь инкубировали при 37 °C в течение 8 часов при встряхивании со скоростью 200 об/мин. Добавляли раствор для остановки реакции (120 мкл, 500 г/л раствора муравьиной кислоты), и смесь перемешивали при 2000 об/мин в течение 5 минут и центрифугировали при 10000 g в течение 10 минут. Образец (980 мкл) переносили в сосуд для ЖХ, добавляли раствор стандартов изотопно-меченых пептидов (20 мкл), и смесь перемешивали на вортексе в течение 10 секунд. Раствор стандартов меченых пептидов (Biomatik, индивидуальный заказ, ≥95,0%) готовили путем взвешивания каждого из пептидов (2,00±0,10 мг) из таблицы 1 в полиэтиленовую центрифужную пробирку объемом 2 мл. Пептиды растворяли путем добавления 20% ацетонитрила, содержащего 0,1% муравьиной кислоты. Объем доводили до получения концентрации 1000,0 мг/л. Например, если было взвешено только 1,90 мг, затем добавляли 1,90 мл раствора. Стандарты меченых пептидов в таблице 2 соответствуют целевым пептидам из таблицы 3.
Таблица 2: Стандарты изотопно-меченых пептидов
Ион (m/z)
Таблица 3: Целевые пептиды
Ион (m/z)
Пример 3: Анализ ЖХ-МС/МС
Образцы (1 мкл) вводили в колонку Waters Xselect HSS T3 C18 (2,5 мкм x 2,1 мм x 50 мм) снабженную Phenomenex KrudCatcher с использованием системы жидкостной хроматографии Thermo Vanquish. Параметры разделения обобщены в таблице 4. Вкратце, использовали градиент концентраций ацетонитрила от 20% до 40% для разделения целевых пептидов, в этот момент элюент проходил в масс-спектрометр для детекции. Затем колонку промывали при усиленном потоке перед началом следующего введения. В период промывания нежелательные компоненты образца направляли в слив, а захват данных отключали.
Таблица 4: Градиент и выбранные параметры захвата данных
Захват масс-спектров выполняли с применением масс-спектрометра Thermo TSQ Altis, работающего в режиме положительных ионов ММР. Каждый пептид имеет переходы как квантификатора так и квалификатора, что дает в общей сложности 32 ММР. Все они постоянно отслеживались в течение периода захвата данных без использования планирования. Время выдержки было установлено на 10 мс, разрешение Q1 и Q3 на 2 Да, а давление CID-газа на 2 мТорр. Список переходов и связанных параметров показан в таблице 5.
Таблица 5: Данные ММР для способа мониторинга шестнадцати целевых пептидов
Пример 4: Определение концентрации для вариантов бета-казеина типа A1 и вариантов бета-казеина типа A2
Вычисления производили автоматически с применением заранее разработанной цифровой электронной таблицы, хотя они могут быть выполнены и вручную. Концентрацию вариантов бета-казеина A1 вычисляли путем суммирования произведений концентрации каждого пептида и результата деления массы исходного белка на массу пептида с последующим умножением на коэффициент приготовления:
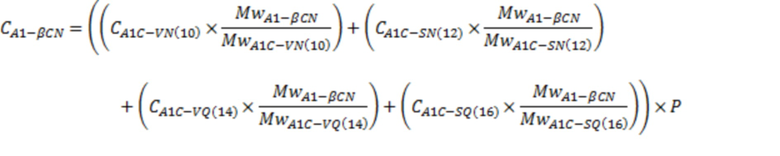
Тот же расчет применяли для вычисления концентрации вариантов бета-казеина A2, но с соответствующей корректировкой масс:
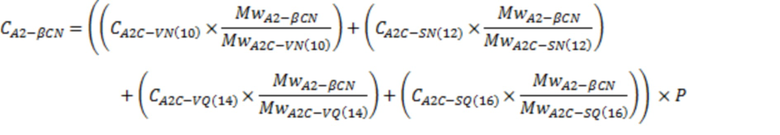
Коэффициент приготовления P вычисляли следующим образом:
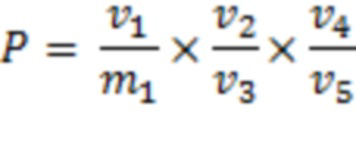
где v1 - конечный объем продукта после экстракции, m1 - масса взвешенного продукта, v2 - объем в пробирке для расщепления после остановки реакции, V3 – объем экстракта, добавленного в пробирку для расщепления, V4 – конечный объем в сосуде для ЖХ, а V5 – объем продукта расщепления, перенесенного в сосуд для ЖХ.
Общую концентрацию бета-казеина вычисляли путем суммирования концентраций двух полиморфов:
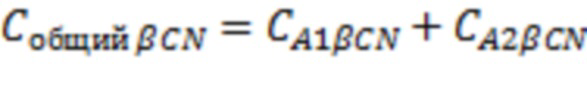
Процент вариантов бета-казеина A1 в продукте вычисляли путем деления концентрации вариантов бета-казеина A1 на сумму концентраций вариантов бета-казеина A1 и A2:
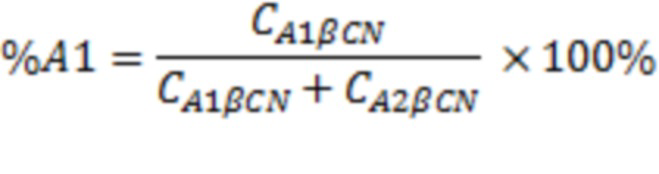
Пример 5: Анализ молока и молочных продуктов
Различные образцы свежего молока, сухого молока, детских смесей и ультрапастеризованного молока были протестированы в соответствии со способом, описанным в примерах 1-4. Также был подготовлен и протестирован ряд стандартов молока. Результаты приведены в таблице 4, где результаты, установленные в соответствии со способом по настоящему изобретению, сравнивают с другими способами определения содержания бета-казеина.
Таблица 6: Данные о концентрации вариантов бета-казеина в молоке и молочных продуктах
Цитируемые источники
1. Trivedi, M.S., Shah, J.S., Al-Mughairy, S., Hodgson, N.W., Simms, B., Trooskens, G., Van Criekinge, W., and Deth, R.C., J. Nutr. Biochem., 2014, 25, 1011-1018.
2. WO 1996/014577.
3. WO 1996/036239.
4. WO 2002/019832.
5. WO 2014/193248.
6. WO 2015/005804.
7. WO 2015/026245.
8. WO 2017/171563.
9. WO 2018/063008.
10. Vincent, D., Elkins, A., Condina, M.R., Ezernieks, V., and Rochfort, S., 2016, PLOS ONE 11, e0163471.
11. Givens, I., Aikman, P., Gibson, T., and Brown, R., Food Chemistry, 2013, 139, 549-552.
12. Lutter, P., Parisod, V., and Weymuth, H., J. AOAC Int., 2011, 94, 1043-1059.
| название | год | авторы | номер документа |
|---|---|---|---|
| БЕТА-КАЗЕИН А2 И УРОВЕНЬ ГЛЮКОЗЫ В КРОВИ | 2014 |
|
RU2698794C2 |
| БЕТА-КАЗЕИН А2 И ПРЕДОТВРАЩЕНИЕ ВОСПАЛЕНИЯ КИШЕЧНИКА | 2014 |
|
RU2784851C2 |
| ОБНАРУЖЕНИЕ И КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ ПРОТЕОЗОПЕПТОНОВ И/ИЛИ СОДЕРЖАНИЯ БЕТА-КАЗЕИНА И ПИТАТЕЛЬНАЯ КОМПОЗИЦИЯ СО СНИЖЕННЫМ СОДЕРЖАНИЕМ ПОЛУЧЕННЫХ ИЗ БЕТА-КАЗЕИНА ПРОТЕОЗОПЕПТОНОВ | 2019 |
|
RU2820927C2 |
| НАБОР ПОСЛЕДОВАТЕЛЬНОСТИ ПРАЙМЕРОВ И АЛЛЕЛЬСПЕЦИФИЧЕСКИХ ЗОНДОВ ДЛЯ ОДНОВРЕМЕННОЙ ГЕНОДИАГНОСТИКИ ЧЕТЫРЕХ АЛЛЕЛЕЙ БЕТА-КАЗЕИНА У КРУПНОГО РОГАТОГО СКОТА | 2022 |
|
RU2798281C1 |
| БЕТА-КАЗЕИН A2 И УРОВЕНЬ ГЛЮКОЗЫ В КРОВИ | 2014 |
|
RU2802806C1 |
| СПОСОБ ОДНОВРЕМЕННОЙ ГЕНОДИАГНОСТИКИ ЧЕТЫРЕХ АЛЛЕЛЕЙ БЕТА-КАЗЕИНА У КРУПНОГО РОГАТОГО СКОТА И ТЕСТ-СИСТЕМА ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 2022 |
|
RU2815238C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НАЛИЧИЯ β-КАЗЕИНА АЛЛЕЛЕЙ А1 И/ИЛИ А2 ГРУППЫ В МОЛОКЕ КРС | 2017 |
|
RU2697248C2 |
| БЕТА-КАЗЕИН И КОГНИТИВНАЯ ФУНКЦИЯ | 2017 |
|
RU2766194C2 |
| Способ определения генотипов бета-казеина крупного рогатого скота путём проведения ПЦР в реальном времени с использованием универсального красителя | 2022 |
|
RU2793465C1 |
| БЕТА-КАЗЕИН А2 И АНТИОКСИДАНТНАЯ СПОСОБНОСТЬ | 2016 |
|
RU2751945C2 |
Изобретение относится к пищевой промышленности, в частности к анализу пищевых продуктов. Описан способ количественного определения вариантов бета-казеина типа A1 или бета-казеина типа A2 в молоке и молочных продуктах, полученных из молока, с применением расщепления химотрипсином с получением водного раствора пептидов, добавлением изотопно-меченых пептидов, соответствующих двум или более из пептидов, последующим анализом ЖХ-МС для определения концентраций этих пептидов и применением указанных концентраций для вычисления количеств присутствующих вариантов бета-казеина типа А1 или вариантов бета-казеина типа А2. Изобретение позволяет обеспечить надежный и точный анализ молока и молочных продуктов на присутствие вариантов бета-казеина. 15 з.п. ф-лы, 2 ил., 6 табл., 5 пр.
1. Способ определения количеств вариантов бета-казеина типа A1 или вариантов бета-казеина типа A2 в композиции с точностью более 80%, где варианты бета-казеина типа A1 представляют собой варианты бета-казеина, содержащие гистидин в положении 67 аминокислотной последовательности бета-казеина, а варианты бета-казеина типа A2 представляют собой варианты бета-казеина, содержащие пролин в положении 67 аминокислотной последовательности бета-казеина, и где композиция представляет собой молоко или продукт, изготовленный из молока, включающий этапы:
(i) приведения в контакт композиции с химотрипсином в условиях, позволяющих расщепление бета-казеинов в композиции химотрипсином;
(ii) получения водного раствора пептидов, образованных при расщеплении бета-казеина;
(iii) добавления изотопно-меченых пептидов, соответствующих двум или более из пептидов:
VYPFPGPIHN;
SLVYPFPGPIHN;
VYPFPGPIHNSLPQ и
SLVYPFPGPIHNSLPQ;
(iv) добавления изотопно-меченых пептидов, соответствующих двум или более из пептидов:
VYPFPGPIPN;
SLVYPFPGPIPN;
VYPFPGPIPNSLPQ; и
SLVYPFPGPIPNSLPQ;
(v) определения концентраций указанных двух или более пептидов из (iii), присутствующих в растворе, а также указанных двух или более пептидов из (iv), присутствующих в растворе, путем анализа смеси с применением жидкостной хроматографии-масс-спектрометрии; и
(vi) вычисления концентрации вариантов бета-казеина типа А1 в композиции или концентрации вариантов бета-казеина типа А2 в композиции с использованием концентраций пептидов, определенных на этапе (v).
2. Способ по п. 1, отличающийся тем, что варианты бета-казеина типа А1 содержат любые один или более из: бета-казеина А1, бета-казеина В, бета-казеина С, бета-казеина F и бета-казеина G.
3. Способ по п. 1 или 2, отличающийся тем, что варианты бета-казеина типа А1 содержат только бета-казеин A1.
4. Способ по любому из пп. 1-3, отличающийся тем, что варианты бета-казеина А2 типа содержат любые один или более из: бета-казеина типа A2, бета-казеина A3, бета-казеина D, бета-казеина E, бета-казеина H1, бета-казеина H2 и бета-казеина I.
5. Способ по любому из пп. 1-4, отличающийся тем, что варианты бета-казеина типа А2 содержат только бета-казеин A2.
6. Способ по любому из пп. 1-5, отличающийся тем, что варианты бета-казеина типа A1 включают только бета-казеин A1 и варианты бета-казеина типа А2 включают только бета-казеин А2.
7. Способ по любому из пп. 1-6, отличающийся тем, что определяют концентрации трех или четырех пептидов, образованных при расщеплении бета-казеина, содержащих гистидин в положении, соответствующем положению 67 аминокислотной последовательности бета-казеина.
8. Способ по любому из пп. 1-7, отличающийся тем, что изотопно-меченые пептиды соответствуют следующим пептидам, образованным при расщеплении:
9. Способ по любому из пп. 1-7, отличающийся тем, что изотопно-меченые пептиды соответствуют следующим пептидам, образованным при расщеплении:
10. Способ по п. 1, отличающийся тем, что на этапе (v) определяют концентрации следующих пептидов:
(i) VYPFPGPIHN;
(ii) SLVYPFPGPIHN;
(iii) VYPFPGPIHNSLPQ;
(iv) SLVYPFPGPIHNSLPQ;
(v) VYPFPGPIPN;
(vi) SLVYPFPGPIPN;
(vii) VYPFPGPIPNSLPQ и
(Viii) SLVYPFPGPIPNSLPQ.
11. Способ по любому из пп. 1-10, отличающийся тем, что количества вариантов бета-казеина типа А1 и вариантов бета-казеина типа А2 в композиции определяют с точностью более 90%.
12. Способ по любому из пп. 1-11, отличающийся тем, что количества вариантов бета-казеина типа А1 и вариантов бета-казеина типа А2 в композиции определяют с точностью более 95%.
13. Способ по любому из пп. 1-12, отличающийся тем, что количества вариантов бета-казеина типа А1 и вариантов бета-казеина типа А2 в композиции определяют с точностью более 99%.
14. Способ по любому из пп. 1-13, отличающийся тем, что композиция представляет собой молоко крупного рогатого скота или молочный продукт, изготовленный из молока крупного рогатого скота.
15. Способ по любому из пп. 1-14, отличающийся тем, что молоко представляет собой свежее молоко, сырое молоко, сухое порошковое молоко, жидкое молоко, восстановленное из порошка, обезжиренное молоко, гомогенизированное молоко, сгущенное молоко, концентрированное молоко, молоко с вкусоароматическими добавками, ультрапастеризованное молоко, пастеризованное молоко или непастеризованное молоко.
16. Способ по любому из пп. 1-14, отличающийся тем, что молочный продукт представляет собой детскую смесь, сливки, йогурт, творог, сыр, масло или мороженое.
| LUTTER P | |||
| et al | |||
| Development and Validation of a Method for the Quantification of Milk Proteins in Food Products Based on Liquid Chromatography with Mass Spectrometric Detection, Journal of AOA C International, 2011, Vol.94, N 4, pp.1043-1059 | |||
| CN 0108519485 A, 11.09.2018 | |||
| WO 2015120036 A1, 13.08.2015 | |||
| WO 2018009571 A1, 11.01.2018 | |||
| КУРБАНОВА М.Г |
Авторы
Даты
2024-11-13—Публикация
2019-10-29—Подача