Изобретение относится к области органической химии, а именно к способу получения новых индивидуальных соединений класса аннелированных по стороне [1,2] гетареновым фрагментом 2-(диалкиламино)-4-арил-7,7а-дигидропирроло[2,3-d][1,3]оксазин-5,6-дионов, которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем и в фармакологии.
Известны структурные аналоги заявленных соединений, получаемые из 4-бензоил-5-фенил-1H-пиррол-2,3-дионов и карбодиимидов (G. Kollenz, G. Perm, W. Ott, K. Peters, E.M. Peters, H.G. von Schnering. Chemische Berichte, 1984, vol. 117, №4, p. 1310-1329). Синтез структурных аналогов осуществляется по следующей схеме:
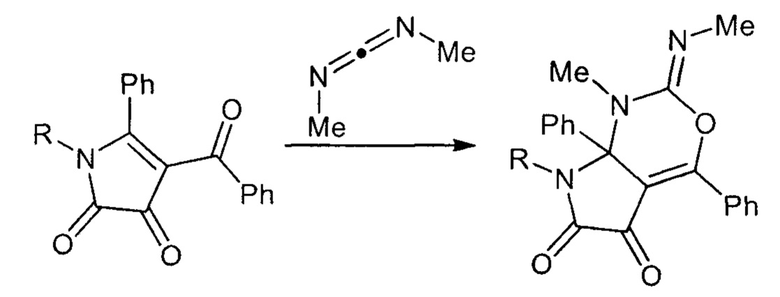
К недостаткам данного способа относится невозможность получения 2-(диалкиламино)-4-арил-7,7а-дигидропирроло[2,3-d][1,3]оксазин-5,6-дионов, аннелированных по стороне [1,2] гетареновым фрагментом.
Задачей изобретения является разработка простого способа синтеза неописанных в литературе 2-(диалкиламино)-4-арил-7,7а-дигидропирроло[2,3-d][1,3]оксазин-5,6-дионов, аннелированных по стороне [1,2] гетареновым фрагментом.
Поставленная задача достигается путем выдерживания гетарено[е]пиррол-2,3-дионов (Ia-в) с замещенными цианамидами (IIa-в) в среде инертных апротонных растворителей по следующей схеме:
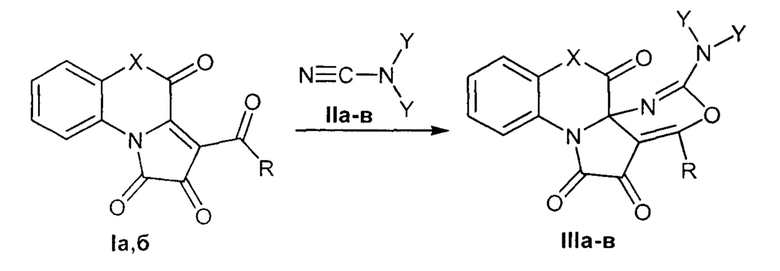
где I: X = NPh, R = Ph (a); X = S, R = Ph (б).
II: Y = CH3 (a); Y+Y = -(СН2)5- (б); Y+Y = -СН2СН2ОСН2СН2- (в).
III: X = NPh, R = Ph, Y = CH3 (a); X = NPh, R = Ph, Y+Y = -(CH2)5- (6); X = S, R = Ph, Y+Y = -CH2CH2OCH2CH2- (в).
Из патентной и технической литературы не были выявлены способы получения 2-(диалкиламино)-4-арил-7,7а-дигидропирроло[2,3-d][1,3]оксазин-5,6-дионов, аннелированных по стороне [1,2] гетареновым фрагментом, имеющие сходные признаки с заявленным способом, а именно, не использовались исходные продукты, растворитель, в котором проходит реакция, на основании чего можно сделать вывод о соответствии заявленного технического решения критерию «новизна» и «изобретательский уровень».
Изобретение иллюстрируется следующими примерами.
Пример 1. 10-(Диметиламино)-8,13-дифенил[1,3]оксазино[4`,5`:2,3]-пирроло[1,2-a]хиноксалин-6,7,12(13H)-трион (IIIa)
К суспензии 0.76 ммоль соединения (Ia) в 5 мл безводного ацетонитрила добавляли 0.76 ммоль N,N-диметилцианамида (IIa), перемешивали при температуре 90°С в течение 9 ч (до исчезновения фиолетовой окраски), выпавший осадок отфильтровывали. Выход 68%, т.пл. 220-221°С (разл.) Соединение (IIIa) C27H20N4O4.
Найдено, %: С 70.03, Н 4.35, N 12.42.
Вычислено, %: С 69.82, Н 4.34, N 12.06.
Соединение (IIIa) - желтое высокоплавкое кристаллическое вещество, плавящееся с разложением, растворимое в ДМСО и ДМФА, ацетоне, хлороформе, 1,2-дихлорэтане, 1,4-диоксане, труднорастворимое в ароматических углеводородах, четыреххлористом углероде, этилацетате, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
В ИК спектре соединения (IIIa), снятого в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний амидных карбонильных групп (С6=O, С12=O) при 1725 см-1, кетонной карбонильной группы (С7=O) при 1692 см-1 и иминогруппы (C10=N11) при 1655 см-1.
В спектре ЯМР 1Н соединения (IIIa), снятом в растворе ДМСО-d6, кроме присутствуют сигналы: 3.01 с (6Н), 6.41 м (1Н), 7.23 м (4Н), 7.51 м (1Н), 7.62 м (4Н), 7.74 м (1Н), 7.81 м (1Н), 8.08 м (2Н).
Пример 2. 10-(Пиперидинил)-8,13-дифенил[1,3]оксазино[4`,5`:2,3]-пирроло[1,2-a]хиноксалин-6,7,12(13H)-трион (IIIб)
К раствору 0.76 ммоль соединения (Ia) в 3 мл сухого ацетонитрила добавляли 0.76 ммоль пиперидин-1-карбонитрил (II6), перемешивали при температуре 90°С в течение 12 ч (до исчезновения фиолетовой окраски), выпавший осадок отфильтровывали. Выход 86,9%, т.пл. 221-224°С (разл.). Соединение (IIIб) C30H24N4O4.
Найдено, %: С 71.21, Н 4.82; N11.10.
Вычислено, %: С 71.42, Н 4.79; N 11.10.
Соединение (IIIб) - желтое высокоплавкое кристаллическое вещество, плавящееся с разложением, растворимое в ДМСО и ДМФА, ацетоне, хлороформе, 1,2-дихлорэтане, 1,4-диоксане, труднорастворимое в ароматических углеводородах, четыреххлористом углероде, этилацетате, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
В ИК спектре соединения (IIIб), снятого в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний амидных карбонильных групп (С6=O, С12=O) при 1726 см-1, кетонной карбонильной группы (С7=O) при 1696 см-1 и иминогруппы (C10=N11) при 1650 см-1.
В спектре ЯМР 1Н соединения (IIIб), снятом в растворе ДМСО-d6, кроме присутствуют сигналы: 1.57 м (6Н), 3.50 с (4Н), 6.41 м (1Н), 7.23 м (4Н), 7.51 м (1Н), 7.62 м (4Н), 7.74 м (1H), 7.82 м (1Н), 8.04 м (2Н).
Пример 3. 10-(Морфолин-4-ил)-8-фенил-12H-[1,3]оксазино[4`,5`:2,3]-пирроло[2,1-с][1,4]бензотиазин-6,7,12-трион (IIIв)
К раствору 0.76 ммоль соединения (Iб) в 3 мл сухого ацетонитрила добавляли 0.76 ммоль морфолин-4-карбонитрила (IIв), перемешивали при температуре 90°С в течение 2 ч (до исчезновения фиолетовой окраски), выпавший осадок отфильтровывали. Выход 87,9%, т.пл. 214-217°С. Соединение (IIIв) C23H17N3O5S.
Найдено, %: С 61.56, Н 3.77; N 9.42.
Вычислено, %: С 61.74, Н 3.83; N 9.39.
Соединение (IIIв) - желтое высокоплавкое кристаллическое вещество, плавящееся с разложением, растворимое в ДМСО и ДМФА, ацетоне, хлороформе, 1,2-дихлорэтане, 1,4-диоксане, труднорастворимое в ароматических углеводородах, четыреххлористом углероде, этилацетате, нерастворимое в алканах и воде. Устойчиво при хранении в обычных условиях.
В ИК спектре соединения (IIIв), снятого в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний амидных карбонильных групп (С6=O, С12=O) при 1730 см-1, кетонной карбонильной группы (С7=O) при 1696 см-1 и иминогруппы (C10=N11) при 1637 см-1.
В спектре ЯМР 1Н соединения (IIIв), снятом в растворе ДМСО-d6, кроме присутствуют сигналы: 3.41 м (4Н), 3.61 м (4Н), 7.46 м (2Н), 7.56 м (1H), 7.66 м (2Н), 7.76 м (1Н), 7.82 м (1Н), 8.04 м (2Н).
Пример 4. Фармакологическое исследование 2-(диалкиламино)-4-арил-7,7а-дигидропирроло[2,3-d][1,3]оксазин-5,6-дионов, аннелированных по стороне [1,2] гетареновым фрагментом (IIIa-в) на наличие противомикробной активности
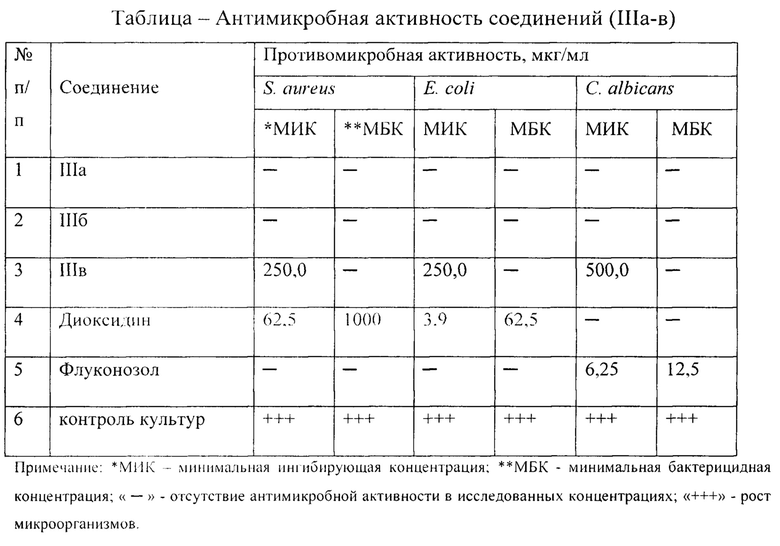
Для исследований использовали общепринятый метод двукратных серийных разведений в жидкой питательной среде микрометодом [А.Н. Миронов, Руководство по проведению доклинических исследований лекарственных средств / Часть первая. - М.: Гриф и К, 2012, с. 509].
В качестве тест-микроорганизмов использовали Staphylococcus aureus (штамм 906), Escherichia coli (штамм 1257), полученных в Федеральном государственном бюджетном учреждении «Научный центр экспертизы средств медицинского применения» (ФГБУ «НЦЭСМП» Минздрава России, г. Москва); Candida albicans, РКПГУ 1353/1277, полученный в НИИ медицинской микологии им. П.Н. Кашкина ФГБОУ ВО СЗГМУ им. И.И. Мечникова Минздрава России.
Культуры выращивали в пробирках на скошенной питательной среде (мясопептонный агар, Сабуро). Для приготовления рабочей взвеси микроорганизмов производили смыв выросшей культуры изотоническим раствором хлорида натрия и устанавливали плотность по стандарту McFarland 0,5 Ед с использованием денситометра. После ряда разведений конечная концентрация клеток в опыте составляла 2,5×105 клеток/мл.
В качестве стандартной навески изучаемых соединений брали 20 мг. Растворяли в 1 мл ДМСО, а затем добавляли 9 мл дистиллированной воды, таким образом, получая концентрацию в 2000,0 мкг/мл испытуемого вещества. Далее в лунках стерильного 96 луночного плоскодонного микропланшета готовили два параллельных ряда двукратных серийных разведений соединений в бульоне МПБ, Сабуро. В каждой лунке содержалось 150 мкл определенной концентрации испытуемого вещества и 150 мкл инокулята культуры. В последних рядах содержалась питательная среда и культуры в равных объемах (контроль). Максимально испытанная концентрация соответствовала 1000,0 мкг/мл, минимальная - 0,5 мкг/мл. Микропланшет помещали в термостат спектрофотометра Epoch и замеряли оптическую плотности (ОП) при длине волны 540 нм. Через 24 часа и 7 суток вновь регистрировали ОП культуральной жидкости.
Анализ полученных данных показал:
- соединение (IIIв) ингибирует рост бактерий и дрожжевых грибков, бактериостатическая активность находится в концентрации 250,0 мкг/мл в отношении культур S. aureus и Е. coli, фунгистатическая - в концентрации 500,0 мкг/мл.
Изобретение относится к области органической химии, а именно к способу получения 2-(диалкиламино)-4-арил-7,7а-дигидропирроло[2,3-d][1,3]оксазин-5,6-дионов, аннелированных по стороне [1,2]гетареновым фрагментом (IIIа-в, где X = NPh, R = Ph, Y = CH3 (a); X = NPh, R = Ph, Y+Y = -(CH2)5- (б); X = S, R = Ph, Y+Y = -CH2CH2OCH2CH2- (в)). Способ осуществляют взаимодействием гетарено[е]пиррол-2,3-дионов (Ia, б, где X = NPh, R = Ph (a); X = S, R = Ph (б).) с замещенными цианамидами (IIa-в, где Y = CH3 (a); Y+Y = -(CH2)5- (б); Y+Y = -CH2CH2OCH2CH2- (в)) в среде инертных апротонных растворителей с последующим выделением целевых продуктов. Технический результат: разработан способ синтеза 2-(диалкиламино)-4-арил-7,7а-дигидропирроло[2,3-d][1,3]оксазин-5,6-дионов, аннелированных по стороне [1,2]гетареновым фрагментом (IIIa-в), которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем и в фармакологии. 1 табл., 4 пр.
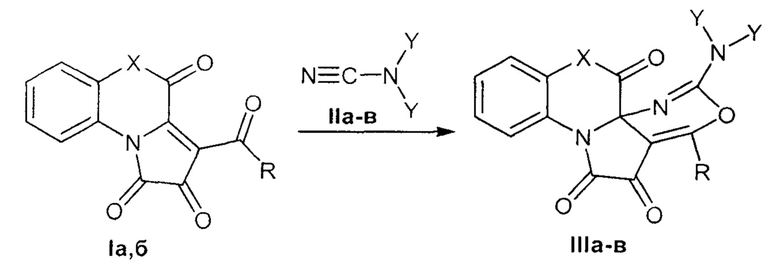
Способ получения 2-(диалкиламино)-4-арил-7,7а-дигидропирроло[2,3-d][1,3]оксазин-5,6-дионов, аннелированных по стороне [1,2] гетареновым фрагментом заключающийся в том, что гетарено[е]пиррол-2,3-дионы (Ia, б) подвергают взаимодействию с замещенными цианамидами (IIa-в) в среде инертных апротонных растворителей с последующим выделением целевых продуктов по следующей схеме
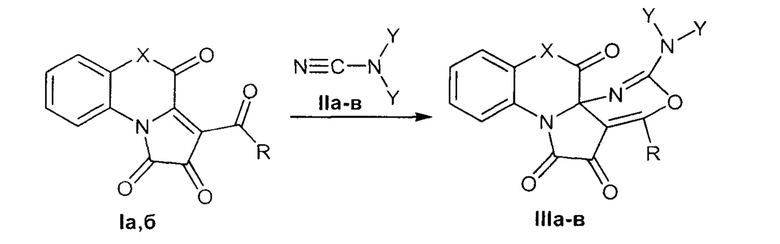
где I: X = NPh, R = Ph (a); X = S, R = Ph (б).
II: Y = CH3 (a); Y+Y = -(CH2)5- (6); Y+Y = -CH2CH2OCH2CH2- (в).
III: X = NPh, R = Ph, Y = CH3 (a); X = NPh, R = Ph, Y+Y = -(CH2)5- (б); X = S, R = Ph, Y+Y = -CH2CH2OCH2CH2- (в).
| Stepanova E.E | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Способ крашения тканей | 1922 |
|
SU62A1 |
| Kasatkina S.O | |||
| et al.: "Hetero-Diels-Alder Reaction of | |||
Авторы
Даты
2021-10-28—Публикация
2021-04-16—Подача