Изобретение относится к области органической химии, а именно к новым биологически активным индивидуальным соединениям класса пиразоло[1,2-a]пирроло[2,3-с]пиразолов, а именно к метил 2,3,8-триоксо-4-фенилтетрагидро-6H-пиразоло[1,2-а]пирроло[2,3-с]пиразол-9а(1H)-карбоксилатам формулы:
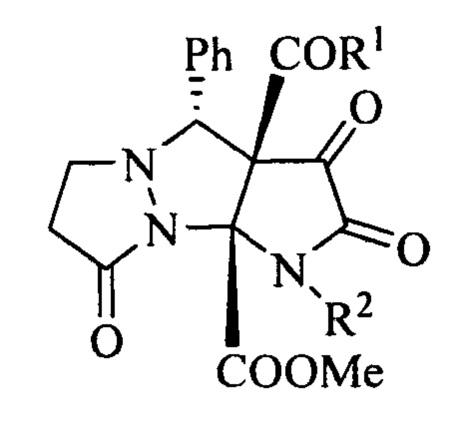
обладающим анальгетической активностью, что позволяет предположить их использование в качестве исходных продуктов для синтеза новых гетероциклических систем, в фармакологии и в медицине в качестве лекарственных средств с анальгетическим эффектом.
Известны структурные аналоги заявленных соединений - 2,3-дигидро-1H,5H-пиразоло[1,2-а]пиразол-1-оны, являющиеся продуктами взаимодействия азометиниминов с диполярофилами, такими как диметил ацетилендикарбоксилат, образующиеся по следующей схеме (Turk С., Svete J., Stanovnik В.,  L.,
L.,  S.,
S.,  A.,
A.,  L. Regioselective 1,3-Dipolar Cycloadditions of (1Z)-1-(Arylmethylidene)-5,5-dimethyl-3-oxopyrazolidin-1-ium-2-ide Azomethine Imines to Acetylenic Dipolarophiles // Helvetica ChimicaActa, 2001, Vol. 84 (1), 146-156):
L. Regioselective 1,3-Dipolar Cycloadditions of (1Z)-1-(Arylmethylidene)-5,5-dimethyl-3-oxopyrazolidin-1-ium-2-ide Azomethine Imines to Acetylenic Dipolarophiles // Helvetica ChimicaActa, 2001, Vol. 84 (1), 146-156):
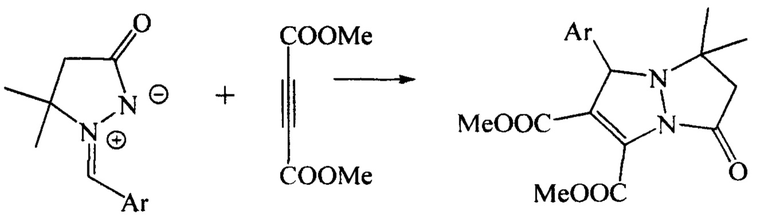
Ar=C6H4NO2-2; C6H4NO2-4; C6H4OMe-2; C6H2(OMe)3-3,4,5; C6H2(OMe)3-2,4,6; C6H3Cl2-2,4; C6H3Cl2-2,6; C6H2Me3-2,4,6.
Задачей изобретения является поиск в ряду производных пиразоло[1,2-a]пирроло[2,3-с]пиразолов веществ с выраженным анальгетическим действием и расширение арсенала средств воздействия на живой организм.
Поставленная задача достигается получением метил 2,3,8-триоксо-4-фенилтетрагидро-6H-пиразоло[1,2-а]пирроло[2,3-с]пиразол-9а(1Н)-карбоксилатов, которые обладают выраженной анальгетической активностью.
Заявляемые соединения синтезируют путем взаимодействия замещенных 1H-пиррол-2,3-дионов (Ia-д) с азометинимином (II) в соотношении 1:1 в среде растворителя с последующим выделением целевых продуктов по следующей схеме:
]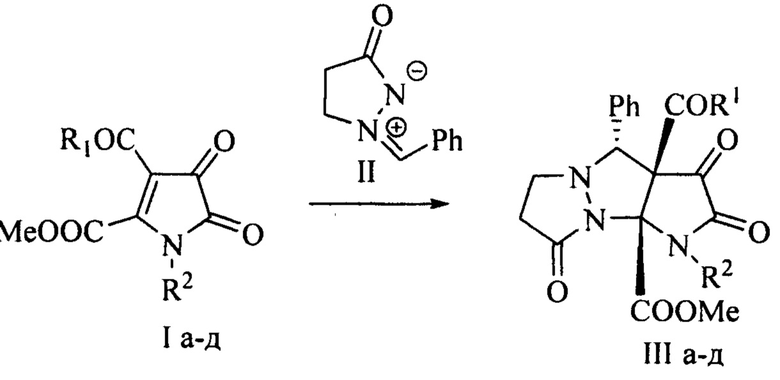
I, III: R1=ОМе, R2=Ph (а), С6Н4Ме-4 (б), C6H4Cl-4 (в), R1=Ph, R2=Ph (г), Bn (д).
Процесс ведут при комнатной температуре, а в качестве растворителя используют абсолютный хлороформ либо другие инертные апротонные растворители.
Изобретение иллюстрируется следующими примерами.
Пример 1. Диметил 2,3,8-триоксо-1,4-дифенилтетрагидро-6H-пиразоло[1,2-a]пиролло[2,3-с]пиразол-3а,9а(1H,4H)-дикарбоксилат (IIIa).
К раствору 1.0 ммоль диметил 4,5-диоксо-1-фенил-4,5-дигидро-1H-пиррол-2,3-дикарбоксилата (Ia) в 10 мл абсолютного хлороформа добавляли 1.0 ммоль азометинимина (II), реакционную смесь оставляли при комнатной температуре на сутки, образовавшийся осадок отфильтровывали и перекристаллизовывали из этанола. Выход 74%, т.пл. 198-200°С. Соединение (IIIa) C24H21,N3O7.
Найдено, %: С 62.31; Н 4.42; N9.16
Вычислено, %: С 62.20; Н 4.57; N 9.07.
Соединение (IIIa) - светло-желтое кристаллическое вещество, легкорастворимое в ДМСО, ДМФА, хлороформе, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях.
В РЖ спектре соединения (IIIa), записанном в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний лактамных и сложноэфирных карбонильных групп при 1777 и 1753 см-1 и кетонной карбонильной группы при 1724 см-1.
Спектр ЯМР 1Н (400 МГц, CDCl3, δ, м.д.): 2.70-2.86 м (2Н, СН2), 3.00 дт (1Н, J=10.9, 9.2 Гц, СН2), 3.62 ддд (1Н, J=10.8, 9.1, 5.6 Гц, СН2), 3.72 с (3Н, ОМе), 3.80 с (3Н, ОМе), 4.86 с (1H, СН), 7.36-7.40 м (3Н, Наром), 7.42-7.50 м (5Н, Наром), 7.53-7.57 м (2Н, Наром).
Пример 2. Диметил 2,3,8-триоксо-4-фенил-1-(4-хлорфенил)тетрагидро-6H-пиразоло[1,2-а]пирроло[2,3-с]пиразол-3а,9а(1H,4H)-дикарбоксилат (IIIв).
К раствору 1.0 ммоль диметил 4,5-диоксо-1-(4-хлорфенил)-4,5-дигидро-1H-пиррол-2,3-дикарбоксилата (Iв) в 10 мл абсолютного хлороформа добавляли 1.0 ммоль азометинимина (II), реакционную смесь оставляли при комнатной температуре на сутки, образовавшийся осадок отфильтровывали и перекристаллизовывали из этанола. Выход 48%, т. пл. 205-207°С. Соединение (IIIв) C24H20ClN3O7.
Найдено, %: С 57.72; Н 4.17; N 8.35.
Вычислено, %: С 57.90; Н 4.05; N 8.44.
Соединение (IIIг) - светло-желтое кристаллическое вещество, легкорастворимое в ДМСО, ДМФА, хлороформе, нерастворимое в воде и алканах. Устойчиво при хранении в обычных условиях.
В ИК спектре соединения (IIIг), записанном в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний лактамных и сложноэфирных карбонильных групп при 1779, 1759 и 1733 см-1 и кетонной карбонильной группы при 1717 см-1.
Спектр ЯМР 1Н (400 МГц, CDCl3, δ, м.д.): 2.70-2.90 м (2Н, СН2), 3.02 дт (1H, J=11.1, 9.3 Гц, СН2), 3.58-3.66 м (1Н, СН2), 3.71 с (3Н, ОМе), 3.80 с (3Н, ОМе), 4.86 с (1Н, СН), 7.35-7.41 м (3Н, Наром), 7.4-7.47 м (4Н, Наром), 7.48-7.53 м (2Н, Наром).
Пример 3. Фармакологическое исследование соединений (IIIa и IIIв) на наличие анальгетической активности.
Оценку анальгетических свойств соединений (IIIa и IIIв) изучали на беспородных мышах массой 18-22 грамм методом термического раздражения «горячая пластинка» по Эдди и Леймбах (Eddy N.B., Leimbarh D.J. Pharmacol and Exper. Gher., 1953, 385-393). В качестве препарата сравнения использовали анальгин (М.Д. Машковский, «Лекарственные средства», т. 1, стр. 184, М., Медицина, 1978).
Проведенные исследования показали (см. табл.), что соединения (IIIa и IIIв) обладают анальгетической активностью. Данные о фармакологической активности аналогов заявляемых соединений в доступной литературе отсутствуют.

Заявляемые ранее неописанные в литературе метил 2,3,8-триоксо-4-фенилтетрагидро-6Я-пиразоло[1,2-a]пирроло[2,3-с]пиразол-9a(1Н)-карбоксилаты могут быть синтезированы с хорошими выходами и могут найти применение в качестве исходных продуктов для синтеза гетероциклических систем и в фармакологии в качестве потенциальных лекарственных средств с анальгетическим действием.
Изобретение относится к области органической химии и фармакологии. Предложены новые биологически активные индивидуальные соединения класса пиразоло[1,2-а]пирроло[2,3-с]пиразолов, а именно метил 2,3,8-триоксо-4-фенилтетрагидро-6H-пиразоло[1,2-а]пирроло[2,3-с]пиразол-9а(1H)-карбоксилаты, которые получают взаимодействием 1H-пиррол-2,3-дионов (I) с азометинимином (II) в соотношении 1:1 в среде растворителя при комнатной температуре, с последующим выделением целевых продуктов. В качестве растворителя используют абсолютный хлороформ либо другие инертные апротонные растворители. Соединения обладают выраженной анальгетической активностью и могут быть использованы в качестве исходных продуктов для синтеза гетероциклических систем и в фармакологии в качестве потенциальных лекарственных средств с анальгетическими свойствами. 1 табл., 3 пр.
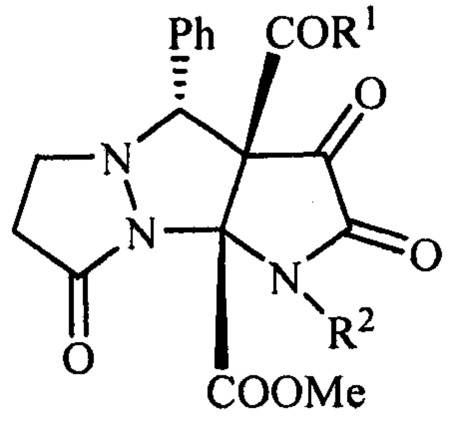
Метил 2,3,8-триоксо-4-фенилтетрагидро-6H-пиразоло[1,2-а]пирроло[2,3-с]пиразол-9a(1H)-карбоксилаты общей формулы
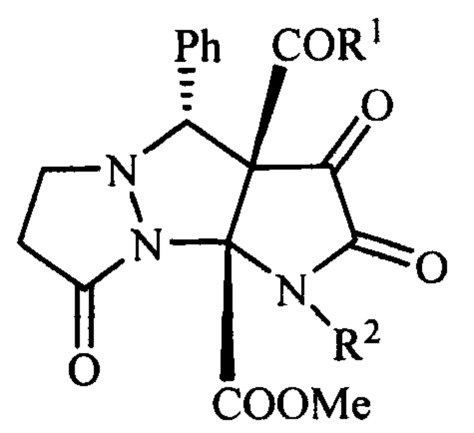
где R1=ОМе, R2=Ph (а), С6Н4Ме-4 (б), С6Н4С1-4 (в), R1=Ph, R2=Ph (г), Bn (д), обладающие анальгетической активностью.
Авторы
Даты
2020-05-21—Публикация
2019-09-06—Подача