Область техники
[0001] Настоящее изобретение относится к амидам гептапептида для использования в медицине, в частности для лечения воспалительных и аутоиммунных заболеваний, зависимых от белка группы высокой подвижности бокс-1 (HMGB1).
Предпосылки изобретения
[0002] Белок группы высокой подвижности бокс-1 (HMGB1) представляет собой ядерный белок, также известный как амфотерин и HMG-1, который в норме обладает многочисленными биологическими активностями. При секреции из клеток во внеклеточное пространство HMGB1 может связываться с множеством рецепторов, включая рецептор конечных продуктов гликирования (RAGE) и толл-подобные рецепторы (TLR2, TLR4 и т. д.), опосредуя тем самым воспалительные и иммунные ответы.Kang et al. Mol. Aspects Med. 2014, 40: 1-116.Yang H et al. FrontImmunol. 2020, 11:484.Внеклеточный HMGB1 вовлечен в широкий спектр воспалительных и аутоиммунных заболеваний, как описано в Harris H E, et al. Nat Rev Rheumatol. 2012, 8:195‐202, и других ссылках, указанных ниже.HMGB1 был идентифицирован как медиатор летальности эндотоксина и мишень в лечении сепсиса.Wang H, etal. Science. 1999, 285(5425):248-51.HMGB1 был идентифицирован как патогенный фактор при многих воспалительных заболеваниях легких, таких как туберкулез легких, хроническая обструктивная болезнь легких (ХОБЛ), фиброз легких, астма, острый респираторный дистресс-синдром (ОРДС), пневмония, тяжелое легочное воспаление и цитокиновый шторм, вызванный вирусом гриппа и COVID-19.Kudo D, et al. Clin Exp Immunol. 2013, 173(2):276-87.Ding J, et al. J Cell Mol Med. 2017, 21(6):1046-1057. Hou C, et al. Mol Med. 2011, 17:807‐815.Andersson U, et al. Mol Med. 2020, 26(1):42. Было показано, что HMGB1 вовлечен в воспалительные заболевания верхних дыхательных путей, такие как воспаление носовых пазух, аллергический ринит, хронический риносинусит с назальными полипами или без них, а воздействие на HMGB1 оказалось полезным для смягчения симптомов воспалительных заболеваний верхних дыхательных путей. Bellussi L M, et al. Int Arch Otorhinolaryngol. 2017, 21(4):390-398. HMGB1 был определен как патогенный фактор и мишень для лечения остеоартрита, дегенеративного заболевания суставов, от которого страдают более 250 миллионов человек во всем мире. Feng Y, et al. Cell Mol Med. 2018, 22(2):1283-1291. HMGB1 вовлечен в развитие диабетических осложнений, таких как диабетическая макроангиопатия, диабетическая ишемическая болезнь сердца, заболевание периферических артерий, диабетическое цереброваскулярное заболевание, диабетическая микроангиопатия, диабетическая нефропатия, диабетическая невропатия, диабетическая ретинопатия, диабетическая кардиомиопатия и диабетическая кардиомиопатия.BiscettiF, et al. Int J Mol Sci. 2019, 20(24):6258.Wu H, et al. Mediators Inflamm. 2016, 2016:3896147.Hafez YM, et al. Diabetes Metab Syndr. 2018, 12(6):1065-1070.HMGB1 был идентифицирован как патогенный фактор и мишень в лечении ревматоидного артрита, аутоиммунного заболевания, встречающегося у 1-2% населения.Kokkola R, et al. Arthritis Rheum. 2002, 46(10):2598-603.Taniguchi N, et al. Arthritis Rheum. 2003, 48(4):971-81.Andersson U, Erlandsson-Harris H. J Intern Med. 2004, 255(3):344-50.Pullerits R, et al. Arthritis Rheum. 2003, 48(6):1693-700.Kokkola R, et al. Arthritis Rheum. 2003, 48(7):2052-8. Sundberg E, et al. Arthritis Res Ther. 2008, 10(2):R33.HMGB1 усугубляет пародонтит, инфекционное заболевание, вызывающее воспаление десен и других тканей пародонта и поражающее более 60% населения во всем мире.Shaddox LM, Walker CB.Clin Cosmet Investig Dent. 2010; 2:79-91. Sun Y, et al. Dose Response. 2020, 18(3):1559325820952660.Yamashiro K, et al. Front Immunol. 2020, 11:1461.HMGB1 участвует в воспалении слизистой оболочки кишечника, а также в возникновении и прогрессировании желудочно-кишечных заболеваний. Sappington PL, et al. Gastroenterology. 2002, 123(3):790-802.Dai S, et al. J Biol Chem 2010, 285(7):4995-5002. Vitali R, et al. PLo S One 2013, 8(6):e66527. HMGB1 участвует в аутоиммунных заболеваниях, таких как васкулит, ассоциированный с антинейтрофильными цитоплазматическими антителами (ANCA), болезнь Бехчета, системная красная волчанка, ревматоидный артрит, анкилозирующий спондилит, синдром Шегрена и миозит, тем самым представляя собой мишень для их лечения.Harris H E, et al. Nat Rev Rheumatol. 2012, 8:195‐202.Magna M, Pisetsky DS. Mol Med. 2014, 20(1):138-46.Zhu B, et al. Medicine (Baltimore). 2018, 97(29):e11531. HMGB1 участвует в заболеваниях глаз, таких как увеит, возрастная дегенерация желтого пятна, глаукома и кератит.Liu Yetal. J Ophthalmol. 2018, 2018:5195290. Таким образом, существует большая потребность в безопасных и эффективных средствах, блокирующих активность внеклеточного HMGB1 или защищающих от высвобождения HMGB1 во внеклеточную среду для лечения или профилактики HMGB1-зависимых воспалительных и аутоиммунных заболеваний.
[0003]В доклинических исследованиях было продемонстрировано несколько фармакологических подходов, нацеленных на внеклеточный HMGB1, включая использование моноклональных антител к HMGB1, ресвератрола, агониста α2-адренорецепторов дексмедетомидина, растворимого тромбомодулина рецептора тромбина, глицирризиновой кислоты и гаптоглобинового белка острой фазы. Однако в настоящее время нет коммерчески доступного эффективного средства против HMGB1 для лечения HMGB1-зависимых воспалительных и аутоиммунных расстройств.Yang H et al. FrontImmunol. 2020, 11:484.
[0004] Известен модифицированный [D-Ala2]-динорфин (1-7), имеющий формулу H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-OH. Chavkin C et al. Proceedings of the National Academy of Sciences of the United States of America, 78(10), 6543-7 1981.Это соединение было получено расщеплением исходного [D-Ala2]-динорфин(1-13)-NH2 трипсином. Однако, амид [D-Ala2]-динорфина (1-7), с формулой H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NH2неизвестен из данной опубликованной работы.
[0005] Патент США 4,707,468 раскрывает полипептид, определяемый приведенной ниже общей формулой, для использования в качестве анальгетика
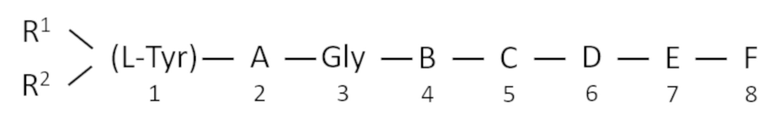
где R1 и R2 могут быть одинаковыми или разными, и каждый представляет собой водород, низший алкил или низший алкенил; A выбран из группы, состоящей из D-Met, D-Ala, D-Ser, D-Cys, D-Thr, Gly и Sar, при условии, что, когда A представляет собой D-Cys, он связан с L-Cys или D -Cys, расположенный в положении 5 через SS-связь, вызывает замыкание внутримолекулярного кольца; B представляет собой L-Phe или D-Phe, в которых бензольное кольцо может быть замещено, или его α-N-алкильное производное; C выбран из группы, состоящей из L-Leu, L-Ile, L-Nle, L-трет.-Leu, L-Met, L-Met (O), L-Ser, L-Cys, L-Val, D-Cys и их α-N-алкильные производные при условии, что, когда A представляет собой D-Cys, C представляет собой L-Cys или D-Cys, и C связан с A через указанную связь SS; D и E, каждый, выбран из группы, состоящей из L-Arg, D-Arg, L-Lys, D-Lys, L-homo-Arg, D-homo-Arg, L-Orn, D-Orn и α-N. их -алкильные производные; F представляет собой OR3,
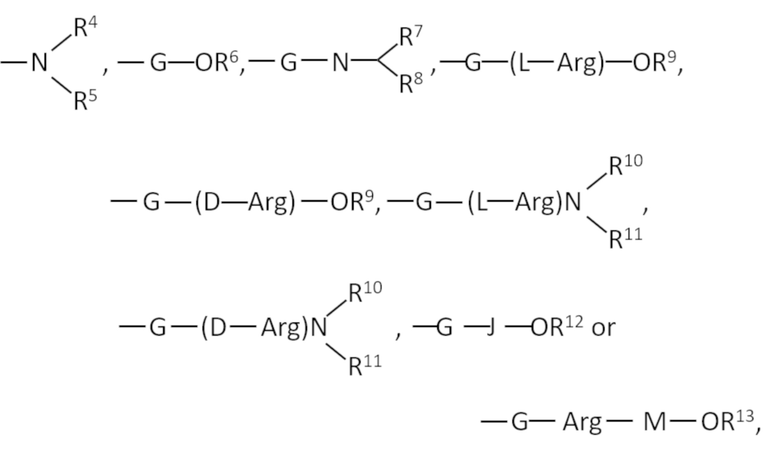
где R3, R4, R5, R6, R7, R8, R9, R10, R11, R12 и R13 одинаковые или разные, и каждый представляет собой водород или низший алкил, G выбран из группы, состоящей из Gly, Ala, Val, Leu, Ile, Ser, Thr, Cys, Met, Asp, Glu, Asn, Gln, Pro, Lys, Orn, Arg, His, Phe, Tyr, Trp, трет-Leu, 2-аминоизомасляная кислота, α-метил- Leu, β-аланин, γ-аминомасляная кислота и ее α-N-алкильные производные, J выбран из группы, состоящей из Gly, Sar, L-Ala, D-Ala, L-Phe, D-Phe, L-Asp. и D-Asp, и M выбран из группы, состоящей из D-Pro, D-ala и D-Glu, при условии, что по крайней мере один из A, B, C, D, E и F содержит D-аминокислоту или N-алкильное производное D-аминокислоты или L-аминокислоты, или фармакологически приемлемая соль указанного полипептида.
[0006] SU 1433415A3 раскрывает способ синтеза пептида для использования анальгетика, определенного общей формулой
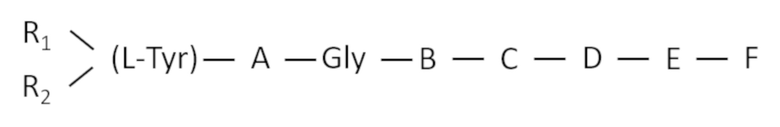
где R1 = R2 - водород или один из R1 и R2 представляет собой водород, другой представляет собой C1-C4-алкил; A - GlyD-Cys, связанный с C, если C -Cys; B - Phe, (n-NO2) Phe; C - Leu, Met (O), Cys, связанный с A, если A - D-Cys; D - Arg, CH3Arg, Lys; E - Arg, CH3Arg; F - NH2, D-Leu-X, где X - OH, NH2, OC2H5, NHC2H5 или D-Leu-Arg-X, где X - NH2, NHC2H5, путем ступенчатого увеличения пептидной цепи, начиная с BOC-защищенного C -концевой аминокислотой с использованием карбодиимидного метода активации карбоксильных групп и метода смешанных ангидридов и удаления защищенных групп из полученного защищенного пептида.
[0007] Хотя патенты US 4,707,468 и SU 1433415A3 раскрывают пептид общей формулы для использования в качестве анальгетика
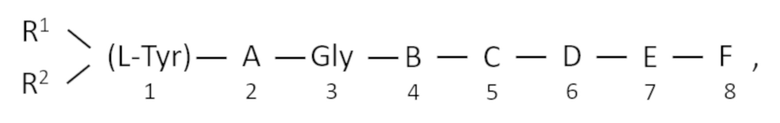
соединение формулы H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NH2 и его алкильные производные по C-концевой амидогруппе являются новыми, поскольку они не были явно упомянуты в US 4,707,468 и SU 1433415A3. Более того, чтобы получить конкретную аминокислотную последовательность соединения формулы H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NH2 и его алкильных производных, необходимо сделать выбор из нескольких списков заместителей, обозначенных цифрами от 1 до 8 в приведенной выше общей формуле, причем R1 = R2 = Hвыбирается из списка 1, A = D-Ala выбирается из списка 2, B = Phe выбирается из списка 4, C = Leuвыбирается из списка 5, D = Argвыбирается из списка 6, E = Argвыбирается из списка 7, и F = NH2выбирается из списка 8.
[0008] Неожиданно мы обнаружили, что введение соединения формулы H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NH2 или его алкильных производных по С-концевой амидогруппе снижает патологически повышенные уровни внеклеточного HMGB1 у млекопитающих. Следовательно, эти соединения можно использовать для профилактики и лечения HMGB1-зависимых воспалительных и аутоиммунных заболеваний. Этот эффект является совершенно неожиданным, поскольку обнаруженный нами анти-HMGB1 эффект никоим образом не связан с обезболиванием, указанным в US 4,707 468 и SU 1433415A3.
Краткое содержание изобретения
[0009] Настоящее изобретение относится к соединению формулы (I):
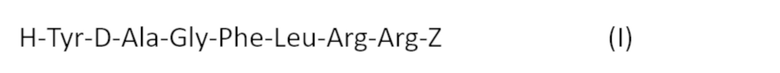
где Z это
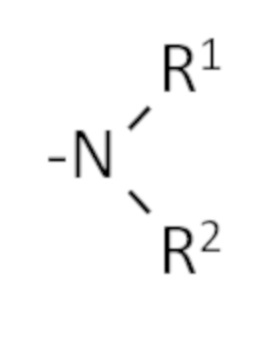
в которой R1 и R2 являются одинаковыми или разными и представляют собой водород или низшую алкильную цепь, содержащую до 4 атомов углерода, или его фармацевтически приемлемой соли для использования при лечении HMGB1-зависимых воспалительных и аутоиммунных заболеваний.
[0010] Первый аспект изобретения относится к соединению формулы (I):
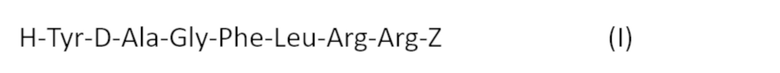
где Z это

в которой R1 и R2 являются одинаковыми или разными и представляют собой водород или низшую алкильную цепь, содержащую до 4 атомов углерода, или его фармацевтически приемлемой соли.
[0011] Согласно другому аспекту, изобретение относится к фармацевтической композиции для лечения HMGB1-зависимого воспалительного или аутоиммунного заболевания, содержащей эффективное количество соединения формулы (I):
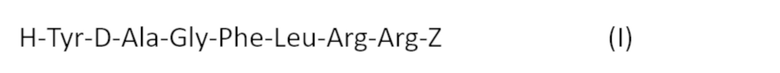
где Z это

в которой R1 и R2 являются одинаковыми или разными и представляют собой водород или низшую алкильную цепь, содержащую до 4 атомов углерода, или его фармацевтически приемлемую соль и фармацевтически приемлемый наполнитель.
[0012] Согласно другому аспекту, изобретение относится к соединению формулы (I):
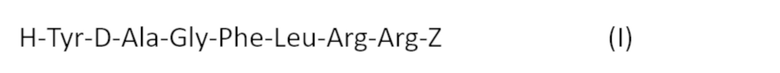
где Z это

в которой R1 и R2 являются одинаковыми или разными и представляют собой водород или низшую алкильную цепь, содержащую до 4 атомов углерода, или его фармацевтически приемлемой соли для использования в качестве лекарственного средства.
[0013] Согласно другому аспекту, изобретение относится к соединению формулы (I):
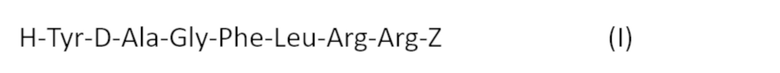
где Z это

в которой R1 и R2 идентичны или различны и представляют собой водород или низшую алкильную цепь, содержащую до 4 атомов углерода, или его фармацевтически приемлемой соли для использования при лечении HMGB1-зависимого воспалительного или аутоиммунного заболевания, выбранного из группы, состоящей из ревматоидного артрита, остеоартрита, анкилозирующего спондилита, пародонтита, аллергического ринита, хронического риносинусита без носовых полипов, хронического риносинусита с носовыми полипами, пневмонии, хронической обструктивной болезни легких, астмы, острого респираторного синдрома взрослых, диабетической макроангиопатии, диабетической болезни коронарных артерий, диабетической болезни периферических артерий, диабетической цереброваскулярной болезни, диабетической микроангиопатии, диабетическая нефропатии, диабетической нейропатии, диабетической ретинопатии, диабетической кардиомиопатии, язвы диабетической стопы, колита, воспалительного заболевания кишечника и заболевания глаз.
[0014] В предпочтительном варианте воплощения изобретения, соединение (I) выбрано из группы, состоящей из H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NH2 ацетата, H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NHC2H5ацетата, H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NHC4H9ацетата иH-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-N(CH3)2ацетата.
[0015] Вболее предпочтительном варианте воплощения изобретения, соединение(I) этоH-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NH2 ацетат.
[0016] В предпочтительном варианте воплощения изобретения, фармацевтически приемлемая соль соединения (I) представляет собой ацетат.
Подробное описание изобретения
[0017] Все термины и определения, объясненные по всему тексту описания изобретения, относятся ко всем аспектам и вариантам осуществления изобретения, если не указано иное.
[0018] Настоящее изобретение относится к соединению формулы (I):
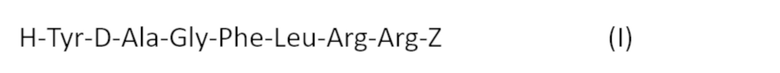
где Z это

в которой R1 и R2 являются одинаковыми или разными и представляют собой водород или низшую алкильную цепь, содержащую до 4 атомов углерода, или его фармацевтически приемлемой соли для использования при лечении HMGB1-зависимого воспалительного или аутоиммунного заболевания.
[0019] Используемый здесь термин «HMGB1» относится к белку бокс-1 группы высокой подвижности (также известному как белок B1 группы высокой подвижности, амфотерин и HMG-1), а также к любым и всем его посттрансляционным модификациям, включая без ограничения ацетилированный HMGB1, фосфорилированный HMGB1, ADP-рибозилированный HMGB1, метилированный HMGB1, гликозилированный HMGB1, частично или полностью восстановленный HMGB1, частично или полностью окисленный HMGB1, полностью тиоловый HMGB1 и дисульфид HMGB1. HMGB1 включает HMGB1 любого вида, включая HMGB1 млекопитающих, таких как HMGB1 человека, HMGB1 грызунов, HMGB1 крупного рогатого скота, HMGB1 свиньи, и их аминокислотные последовательности, раскрытые в базах данных GenBank и UniProtKB/Swiss-Prot, например, UniProtKB/Swiss-Prot Регистрационный номер P09429 для человеческого HMGB1.
[0020] Используемый здесь термин «HMGB1-зависимое воспалительное или аутоиммунное заболевание» относится к воспалительному или аутоиммунному заболеванию, связанному с активностью HMGB1, сверхэкспрессией HMGB1, избыточной продукцией HMGB1 и/или увеличением внеклеточных уровней HMGB1.
[0021] Первый аспект изобретения относится к соединению формулы (I):
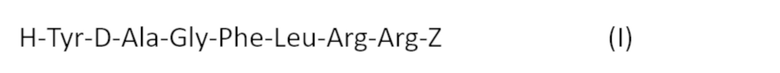
где Z это

в которой R1 и R2 являются одинаковыми или разными и представляют собой водород или низшую алкильную цепь, содержащую до 4 атомов углерода, или его фармацевтически приемлемой соли.
[0022]В предпочтительном варианте, соединение (I) выбрано из группы, состоящей из H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NH2 ацетат,H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NHC2H5 ацетат,H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NHC4H9ацетат иH-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-N(CH3)2 ацетат.
[0023] В более предпочтительном варианте соединение (I) представляет собой H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NH2 ацетат, название L-тирозил-D-аланил-L-глицил-L-фенилаланил-L-лейцил-L-аргинил-L-аргинин амид ацетат.
[0024] Термин «фармацевтически приемлемый» относится к молекулярным объектам и композициям, которые имеют достаточную чистоту и качество для использования в составе композиции по настоящему изобретению и которые при надлежащем введении млекопитающему, например человеку, не производят токсической, неблагоприятной, аллергической или другой нежелательной реакции.
[0025] Настоящее изобретение относится ко всем фармацевтически приемлемым солям соединения (I). Примеры таких фармацевтически приемлемых солей включают, но не ограничиваются, хлоридом, бромидом, сульфатом, ацетатом, пируватом, малатом, фумаратом и цитратом.
[0026] Соединение (I) может быть получено твердофазным синтезом или любым другим методом пептидного синтеза, известным в данной области, как описано, например, в BentonL. Chemistryofpeptidesynthesis. Taylor&Francis, 2006.
[0027] В иллюстративных целях схемы реакций, изображенные ниже, предоставляют потенциальные пути синтеза соединения (I), а также ключевых промежуточных соединений. Более подробное описание отдельных стадий реакции см. в разделе «Примеры» ниже. Специалисты в данной области поймут, что другие пути синтеза, например, указанные в SU 1433415A3, могут быть использованы для синтеза соединений. Хотя конкретные исходные материалы и реагенты изображены на схемах и обсуждаются ниже, другие исходные материалы и реагенты могут быть легко заменены, чтобы обеспечить множество производных и/или условий реакции.
[0028] Общий процесс синтеза соединения (I) включает реакцию N-защищенного, например, с Cbz-группой, метилового эфира (II) с первичным или вторичным амином HNR1R2 в подходящем растворителе, например, метаноле; и последующее снятие защиты с соединения (III) гидрогенолизом в присутствии катализатора, например палладия на угле или никеля Ренея.
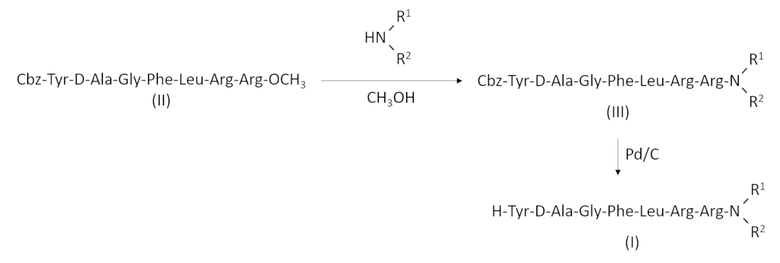
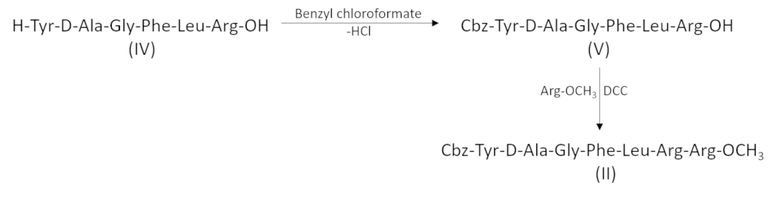
[0029] Процесс синтеза N-защищенного, например, с помощью Cbz-группы, метилового эфира гептапептида (II) включает следующие стадии: защита гексапептида (IV) на N-конце бензилоксикарбонильной группой (Cbz-); и взаимодействие полученного соединения (V) с метиловым эфиром L-аргинина в присутствии дегидратирующего агента, например дициклогексилкарбодиимида (DCC).
[0030]Согласно другому аспекту, изобретение относится к фармацевтической композиции для лечения HMGB1-зависимого воспалительного или аутоиммунного заболевания, содержащей эффективное количество соединения формулы (I):
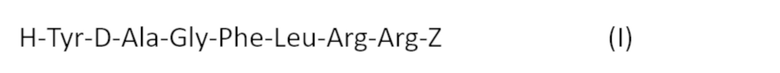
где Z это

в которой R1 и R2 являются одинаковыми или разными и представляют собой водород или низшую алкильную цепь, содержащую до 4 атомов углерода, или его фармацевтически приемлемую соль и фармацевтически приемлемый наполнитель.
[0031] При практическом применении изобретения, фармацевтическая композиция может вводиться любым обычным путем, известным в данной области, например, внутривенно, внутримышечно, внутрибрюшинно, подкожно, внутрисуставно, трансдермально, ректально, местно, интраназально, путем ингаляции, а также перорально в различных дозированных формах, включая, помимо прочего, инъекции, настои, лосьоны, мази, гели, кремы, суспензии, эмульсии, суппозитории, капли, пластыри, аэрозоли или спреи.
[0032] Используемый здесь термин «фармацевтически приемлемый наполнитель» относится к веществу, которое не является терапевтическим агентом, и включает любые и все растворители, дисперсионные среды, покрытия, поверхностно-активные вещества, антиоксиданты, консерванты (например, антибактериальные агенты, противогрибковые агенты), изотонические агенты. агенты, замедляющие абсорбцию, соли, консерванты, лекарственные средства, стабилизаторы лекарственных средств, связующие, эксципиенты, дезинтегрирующие агенты, смазывающие вещества, подсластители, ароматизаторы, красители и т.п. и их комбинации, как известно специалистам в данной области (см., например,Remington'sPharmaceuticalSciences, 18thEd. MackPrintingCompany, 1990, pp. 1289- 1329). Неисключительные примеры вспомогательных веществ, подходящих для использования в жидких лекарственных формах, включают очищенную воду, воду для инъекций, буферные системы для поддержания pH 3,0-8,5, регуляторы тоничности растворов, антимикробные консерванты, поверхностно-активные вещества, такие как неионные и амфифильные поверхностно-активные вещества, стабилизаторы и эмульгаторы. Неисключительные примеры наполнителей, подходящих для использования в твердых лекарственных формах, включают крахмалы, сахара, микрокристаллическую целлюлозу, разбавители, гранулирующие агенты, смазывающие вещества, связующие и разрыхлители, а также основы для суппозиториев, такие как масло какао, натуральные и синтетические триглицериды, полиэтилен. полимеры гликоля, глицериновый желатин и заменители масла какао, такие как Витепсол.
[0033] При практическом применении изобретения композиции могут содержать соединение (I) или его фармацевтически приемлемую соль в количестве от 0,001 до 99,999%.
[0034]При практическом применении настоящего изобретения, композицию можно получить способами, хорошо известными из уровня техники. Такие процедуры включают, но не ограничиваются, смешиванием соединения (I) или его фармацевтически приемлемой соли с другими ингредиентами композиции обычным способом. Руководство по приготовлению композиций можно найти, например, в"Remington: The science and practice of pharmacy" 20th ed. Mack Publishing, Easton PA, 2000 ISBN 0-912734-04-3 and "Encyclopaedia of Pharmaceutical Technology", edited by Swarbrick, J. & J. C. Boylan, Marcel Dekker, Inc., New York, 1988 ISBN 0-8247-2800-9.
[0035]Согласно другому аспекту, изобретение относится к соединению формулы (I):
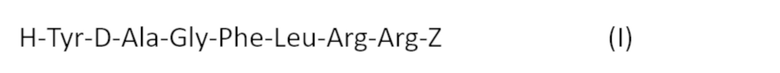
где Z это

в которой R1 и R2 являются одинаковыми или разными и представляют собой водород или низшую алкильную цепь, содержащую до 4 атомов углерода, или его фармацевтически приемлемой соли для использования в качестве лекарственного средства.
[0036]Используемый здесь термин «лекарственное средство» относится к продукту для использования при лечении, предупреждении или облегчении хронического или острого заболевания, расстройства или состояния.
[0037] При практическом применении изобретения, лекарственное средство может быть лиофилизированным порошком соединения (I) или его фармацевтической солью или фармацевтической композицией, содержащей соединение (I) или его фармацевтическую соль и фармацевтически приемлемый наполнитель.
[0038] Согласно другому аспекту, изобретение относится к соединению формулы (I):
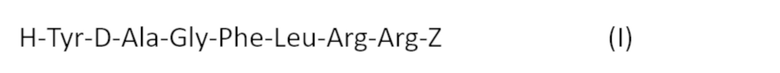
где Z это

в которой R1 и R2 идентичны или различны и представляют собой водород или низшую алкильную цепь, содержащую до 4 атомов углерода, или его фармацевтически приемлемой соли для использования при лечении HMGB1-зависимого воспалительного или аутоиммунного заболевания, выбранного из группы, состоящей из ревматоидного артрита, остеоартрита, анкилозирующего спондилита, пародонтита, аллергического ринита, хронического риносинусита без носовых полипов, хронического риносинусита с носовыми полипами, пневмонии, хронической обструктивной болезни легких, астмы, острого респираторного синдрома взрослых, диабетической макроангиопатии, диабетической болезни коронарных артерий, диабетической болезни периферических артерий, диабетической цереброваскулярной болезни, диабетической микроангиопатии, диабетическая нефропатии, диабетической нейропатии, диабетической ретинопатии, диабетической кардиомиопатии, язвы диабетической стопы, колита, воспалительного заболевания кишечника и заболевания глаз.
[0039] Используемый здесь термин «лечение» относится к ингибированию или предотвращению прогрессирования заболевания, расстройства или состояния или одного или нескольких их симптомов. Термин «лечение» относится как к терапевтическому лечению, так и к профилактическим или превентивным мерам. Лица, нуждающиеся в лечении, включают тех, кто уже страдает этим расстройством, а также тех, кто склонен к заболеванию или диагностирован с расстройством, или тех, у которых расстройство необходимо предотвратить.
[0040] Далее, изобретение обеспечивает способ леченияHMGB1-зависимого воспалительного или аутоиммунного заболевания, включающий введение эффективного количества соединения формулы (I):
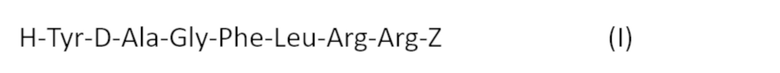
где Z это

в которой R1 и R2 являются одинаковыми или разными и представляют собой водород или низшую алкильную цепь, содержащую до 4 атомов углерода, или его фармацевтически приемлемой соли субъекту, нуждающемуся в этом.
[0041] Используемый здесь термин «субъект» относится к млекопитающему. Неисключительные примеры таких млекопитающих включают приматов (например, человека), коров, овец, коз, свиней, лошадей, собак, кошек, кроликов, крыс, мышей и т.п. В предпочтительном варианте, субъектом является человек.
[0042] В данном контексте, субъект «нуждается» в лечении, если такой субъект получит медицинскую, физиологическую пользу или улучшение качества жизни от такого лечения.
[0043] Термин «терапевтически эффективное количество» относится к количеству соединения (I) или его фармацевтически приемлемой соли, которое будет вызывать биологический или медицинский ответ субъекта или облегчать симптомы, облегчать состояния, замедлять или задерживать прогрессирование заболевания или предотвращать заболевание. В одном варианте осуществления изобретения, термин «терапевтически эффективное количество» относится к количеству соединения (I) или его фармацевтически приемлемой соли, которое при введении субъекту эффективно для (1) по меньшей мере частичного облегчения, ингибирования, предотвращения и/или улучшения состояния или расстройства или заболевания (i), опосредованного HMGB1, или (ii) связанного с количеством HMGB1, или (iii) характеризующегося активностью HMGB1; или (2) снижения активности и/или количества HMGB1.
[0044]При практическом применении изобретения эффективное количество соединения (I) или его фармацевтически приемлемой соли зависит от субъекта, возраста, пола, веса тела, патологического состояния и его тяжести, пути введения и оценки субъекта, выписывающего рецепт. Определение количества на основе таких факторов находится в компетенции среднего специалиста в данной области, при этом суточная доза соединения (I) или его фармацевтически приемлемой соли составляет, например, от 0,001 до 1 мг на кг тела. веса в день, в частности от 0,01 до 0,5 мг на кг веса тела в день, более конкретно от 0,01 до 0,2 мг на кг веса тела в день, более конкретно от 0,02 до 0,2 мг на кг веса тела в день, но не ограничивается этими дозами.
[0045] При практическом применении изобретения, эффективное количество соединения (I) или его фармацевтически приемлемой соли вводится от одного до трех раз в день, но не ограничивается этим режимом.
[0046] При практическом применении изобретения соединение (I) или его фармацевтически приемлемая соль может использоваться для лечения HMGB1-зависимых заболеваний в комбинации с другими активными соединениями, например, с пептидом, определяемым общей формулой патента США 4,707,468.
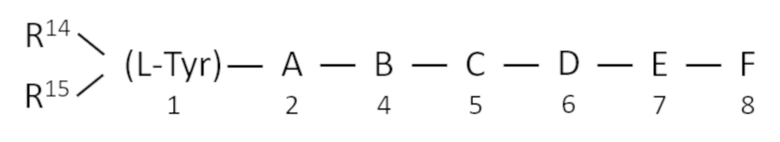
где R1 и R2 могут быть одинаковыми или разными, и каждый представляет собой водород, низший алкил или низший алкенил; A выбран из группы, состоящей из D-Met, D-Ala, D-Ser, D-Cys, D-Thr, Gly и Sar, при условии, что, когда A представляет собой D-Cys, он связан с L-Cys или D -Cys, расположенный в положении 5 через SS-связь, вызывает замыкание внутримолекулярного кольца; B представляет собой L-Phe или D-Phe, в которых бензольное кольцо может быть замещено, или его α-N-алкильное производное; C выбран из группы, состоящей из L-Leu, L-Ile, L-Nle, L-трет.-Leu, L-Met, L-Met (O), L-Ser, L-Cys, L-Val, D-Cys и их α-N-алкильные производные при условии, что, когда A представляет собой D-Cys, C представляет собой L-Cys или D-Cys, и C связан с A через указанную связь SS; D и E, каждый, выбран из группы, состоящей из L-Arg, D-Arg, L-Lys, D-Lys, L-homo-Arg, D-homo-Arg, L-Orn, D-Orn и α-N. их -алкильные производные; F представляет собой OR3,

где R3, R4, R5, R6, R7, R8, R9, R10, R11, R12 и R13 одинаковые или разные, и каждый представляет собой водород или низший алкил, G выбран из группы, состоящей из Gly, Ala, Val, Leu, Ile, Ser, Thr, Cys, Met, Asp, Glu, Asn, Gln, Pro, Lys, Orn, Arg, His, Phe, Tyr, Trp, трет-Leu, 2-аминоизомасляная кислота, α-метил- Leu, β-аланин, γ-аминомасляная кислота и ее α-N-алкильные производные, J выбран из группы, состоящей из Gly, Sar, L-Ala, D-Ala, L-Phe, D-Phe, L-Asp. иD-Asp, и M выбран из группы, состоящей из D-Pro, D-alaиD-Glu, при условии, что по крайней мере один из A, B, C, D, E и F содержит D-аминокислоту или N-алкильное производное D-аминокислоты или L-аминокислоты, или фармакологически приемлемая соль указанного полипептида. Принимая во внимание результаты настоящего изобретения, ожидается, что любой пептид, определенный общей формулой патента США 4,707,468, обязательно будет обладать эффектом против HMGB1 и будет полезен при лечении заболеваний, зависимых от HMGB1.
[0047] Соединение (I) или его фармацевтически приемлемая соль может быть успешно использовано в комбинации по меньшей мере с одним другим активным фармацевтическим агентом для одновременного или последовательного введения, например, при лечении или профилактике ревматоидного артрита, остеоартрита, анкилозирующего спондилита, пародонтита, аллергический ринит, хронического риносинусита без носовых полипов, хронического риносинусита с носовыми полипами, пневмонии, хронической обструктивной болезни легких, астмы, острого респираторного синдрома у взрослых, диабетической макроангиопатии, диабетической ишемической болезни сердца, периферической артериальной болезни, диабетической цереброваскулярной болезни, диабетической микроангиопатии, нефропатии, диабетической нейропатии, диабетической ретинопатии, диабетической кардиомиопатии, язвы диабетической стопы, колита, воспалительных заболеваний кишечника и заболеваний глаз. Такая фармацевтическая комбинация может быть в стандартной лекарственной форме, содержащей заранее определенное количество каждого из по меньшей мере двух активных компонентов. Альтернативно, фармацевтическая комбинация может содержать по меньшей мере два активных компонента по отдельности. Неисключительные примеры такого, по меньшей мере, одного другого активного фармацевтического агента включают гидроксихлорохин, лефлуномид, метотрексат, сульфасалазин, олсалазин, балсалазид, миноциклин, абатацепт, ритуксимаб, тоцилизумаб, анакинра, адалимумаб, этанерцепт, инфликсимаб, цертолизумаб пегол, цертимумаб, этанерцепт, голимумаб, тофацитиниб, барицитиниб, целекоксиб,целекоксиб, ибупрофен, набуметон, напроксен натрия, напроксен, пироксикам, диклофенак, дифлунизал, индометацин, кетопрофен, этодолак, фенопрофен, флурбипрофен, кеторолак, меклофенамат, кортизон, гидрокортизон, метилпреднизолон, преднизолон, циклофосфамид, циклоспорин, азатиоприн, глицирризиновая кислота, гидроксихлорохин, триамцинолона ацетонид, оксиметазолин, фенилэфрин, альбутерол, левалбутерол, беклометазон, будесонид, флунизолид, флутиказон, мометазон, монтелукаст, зафирлукаст, зилеутон, инсулин, обычный инсулин, инсулин аспарт, инсулин глулизин, инсулин лизпро, инсулин изофан, инсулин деглудек, инсулин глезаргирин, инсулин глютаргирин, метформин, бромокриптин, ингибиторы дипептидилпептидазы-4, альбиглутид, дулаглутид, экзенатид, лираглутид, семаглутид, натеглинид, репаглинид, переносчик натрия-глюкозы, ингибиторы натрий-глюкозы (SGLT) 2, сульфонилмочевины, росигалитазон, пиоглитазон, месаламин, токацитиниб, азатиоприн и меркаптопурин.
[0048] Следующие ниже примеры представлены для демонстрации изобретения. Примеры являются только иллюстративными и никоим образом не предназначены для ограничения объема изобретения.
Пример 1
[0049] Этот пример иллюстрирует процесс получения соединения (I).
[0050] Бензилхлорформиат (2,55 г; 15,0 ммоль) добавляли порциями к 50 мл раствора коммерчески доступного диацетата H-Tyr-D-Ala-Gly-Phe-Leu-Arg-OH (10,0 г; 11,8 ммоль; IV) в воде, доведенной до щелочного значения pH добавлением 15 мл 3 н. NaOH, и перемешивали в течение ночи. Затем смесь подкисляли уксусной кислотой, упаривали в вакууме досуха и сухой остаток экстрагировали этанолом. Выпаривание этанольного экстракта дает сухой твердый ацетат Cbz-Tyr-D-Ala-Gly-Phe-Leu-Arg-OH (V) (10,1 г; 11,0 ммоль). Его растворяли в диметилацетамиде и к раствору добавляли дигидрохлорид метилового эфира L-аргинина (3,1 г; 12,0 ммоль; Sigma-Aldrich 11030), дициклогексилкарбодиимид (2,5 г; 12,0 ммоль; DCC) и триэтиламин (1,2 г; 12,0 ммоль). Полученную смесь перемешивали в течение 4 часов при 0 °C, а затем упаривали досуха в вакууме. В полученном веществе остаток кислоты заменяли на ацетат на анионной смоле AG1-X8 (четвертичный аммоний) по стандартной методике. Получили ацетат метилового эфира (II) N-защищенного гептапептида в виде белого твердого вещества, выход примерно 65% в расчете на исходный гексапептид (IV). Cbz-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-OCH3 ацетат (II): HRMS (ESI) m/z [M+H+] вычислено дляC50H71N13O11: 1030.5400, найдено 1030.5409.
[0051]Метиловый эфир (II) превращали в желаемые амиды путем взаимодействия метилового эфира (II) (1,0 г, 0,9 ммоль) с этиламином (90,2 мг, 2,0 ммоль), бутиламином (146,5 мг, 2,0 ммоль) или диметиламином (90,1 мг, 2,0 ммоль) в 25 мл метанола или раствором аммиака, приготовленного путем насыщения 25 мл метанола сухим газообразным аммиаком. Растворы перемешивали в течение двух дней для получения Cbz-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NH2, Cbz-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NHC2H5, Cbz-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NHC4H9 или Cbz-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-N(CH3)2, соответственно. После удаления избытка аминов/аммиака и растворителя выпариванием в вакууме, желаемые продукты были получены в виде сухих твердых веществ. Продукты растворяли в метаноле (20 мл) с уксусной кислотой (0,2 г, 3,3 ммоль) и раствор держали подH2 в присутствии 10% палладия на угле при комнатной температуре до завершения реакции гидрирования. Смеси фильтровали и фильтраты упаривали в вакууме досуха. Сухие остатки очищали с помощью препаративной ВЭЖХ, чтобы получить желаемые амиды в виде твердых веществ белого цвета с выходами 63-81% в расчете на исходный метиловый эфир (II).
H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NH2ацетат, выход74%: 1HNMR (400 MHz, D2O), δ-scale: 0.80 (d, J= 4 Hz, 3H), 0.85 (d, J = 4Hz, 3H), 1.09 (d, J = 8 Hz, 3H), 1.40-1.83 (m, 11H), 1. 87 (s, 9H), 2.89 (m, 1H), 2.95-3.09 (m, 3H),3.14 (m, 4H), 3.80 (m, 3H), 4.09 (m, 1H), 4.25 (m, 3H), 4.54 (m, 1H), 6.83 (m, 2H), 7.07 (m, 2H), 7.19 (m, 2H), 7.28 (m, 3H).HRMS (ESI) m/z [M+H+] вычислено для C41H64N14O8: 881.5032, найдено 881.5039.
H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NHC2H5ацетат, выход 81%: HRMS (ESI) m/z [M+H+] вычислено для C43H68N14O8: 909.5345, найдено909.5351.
H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NHC4H9ацетат, выход 63%: HRMS (ESI) m/z [M+H+] вычислено для C45H72N14O8: 937.5658, найдено 937.5651.
H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-N(CH3)2ацетат, выход 69%: HRMS (ESI) m/z [M+H+] вычислено для C43H68N14O8: 909.5345, найдено 909.5349.
Пример 2
[0052] Этот пример иллюстрирует эффективность соединений по изобретению в ингибировании секреции HMGB1.
[0053] Соединения по изобретению тестировали на мышиной модели острого повреждения легких, индуцированного интратрахеальным введением липополисахарида (LPS), как описано, например, в D'Alessio F R. Mouse Models of Acute LungInjury and ARDS. Methods Mol Biol. 2018, 1809:341-350. Мышей-самцов C57Bl/6 случайным образом разделили на девять групп по 6 животных в каждой. Мышам интратрахеально вводили 1 мкг/мышь α-галактозилцерамида (α-GalCer, KRN7000, Sigma-Aldrich), а через 24 часа - LPS (E. coli; 1 мг/мышь) и 10 мкл/мышь полного адъюванта Фрейнда. Затем мыши получали путем ингаляции физиологический раствор (контроль, 50 мкл),10, 100, или 250 мкг/кгH-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NH2ацетата, 100мкг/кг H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NHC2H5 ацетата,100 мкг/кг H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NHC4H9 ацетата, 100 мкг/кг H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-N(CH3)2 ацетата,10 мкг/кг H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-OH ацетата (ChavkinCetal. 1981), или 250 мкг/кг [D-Ala2, D-Leu5]-энкефалина в 50 мкл физ. раствора. Через 48 часов, концентрации HMGB1 измеряли в бронхоальвеолярной жидкости (BALF) с помощью имеющегося в продаже набора ELISA для HMGB1 (SEA3999Mu, Cloud-Clone corp.). Результаты представлены в таблице 1 как среднее ± SEM (n = 6) уровней HMGB1 в BALF в % от контроля.
[0054] Таблица 1
H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NH2ацетат, 10 мкг/кг
H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NH2ацетат, 100 мкг/кг
H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NH2ацетат, 250мкг/кг
H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NHC2H5ацетат, 100 мкг/кг
H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NHC4H9ацетат, 100 мкг/кг
H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-N(CH3)2ацетат,100 мкг/кг
H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-OHацетат, 10 мкг/кг
D-Ala2-D-Leu5-энкефалин, 250 мкг/кг
60.3 ± 9.0*
31.8 ± 12.4*
34.2 ± 8.0*
35.2 ± 7.2*
40.1 ± 5.0*
42.3 ± 5.9 *
88.67 ± 10.5
92.3 ± 7.2
*Достоверно отличается о контроля (p<0.05;однофакторный анализ ANOVA, Тьюки пост-тест).
[0055] Таблица 1 показывает, что соединения по настоящему изобретению значительно снижают секрецию HMGB1 по сравнению с контролем, тем самым предотвращая позднюю фазу воспаления у мышей, индуцированных LPS,в то время как близкий по строению пептид [D-Ala2, D-Leu5]-энкефалин в дозе 250 мг/кг был неэффективным (p>0,05).Амид H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NH2ацетат (10 мкг/кг) был достоверно эффективнее, чем близкий по строению пептид H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-ОН ацетат в той же дозе (p>0,05). Снижение HMGB1 соединениями настоящего изобретения сопровождалось облегчением симптомов респираторного заболевания, таких как нарушение дыхания, снижение аппетита и угнетение двигательной активности по сравнению с контролем. Таким образом, соединения формулы (I) настоящего изобретения были эффективны в лечении HMGB1-зависимого воспаления легких.
Пример 3
[0056] Этот пример показывает, что соединение (I) полезно для лечения артрита, заболевания, зависимого от HMGB1.
[0057] Эффективность соединения по настоящему изобретению тестировали на модели ревматоидного артрита на мышах, как описано в Brand et al., Nat Protoc. 2007, 2(5):1269-75. Самцов мышей BALB/c случайным образом разделили на две группы по 5 животных в каждой. Артрит вызывали внутрикожной инъекцией в основание хвоста холодной эмульсии (0,05 мл), приготовленной путем эмульгирования раствора куриного коллагена II типа (CII) в уксусной кислоте с полным адъювантом Фрейнда (CFA). Через три недели этим мышам таким же образом вводили вторую инъекцию. После бустерной иммунизации мыши получали 50 мкл физиологического раствора внутрибрюшинно (контроль) или 100 мкг/кг H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NH2ацетата в 50 мкл физиологического раствора внутрибрюшинно один раз в день в течение двух недель. Уровень HMGB1 в сыворотке определяли на 35 день с помощью имеющегося в продаже набора ELISA для HMGB1 (SEA3999Mu, Cloud-Clone corp.). Клиническую тяжесть артрита для каждой лапы определяли количественно по шкале от 0 до 4, как описано в Brand et al., Nat Protoc. 2007, 2(5):1269-75. Результаты представлены в таблице 2 как среднее значение ± SEM (n = 5) уровней HMGB1 в сыворотке в% от контроля и заболеваемость артритом.
[0058] Таблица2
H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NH2ацетат
21.5 ± 5.9*
20
*Достоверно отличается от контроля (p<0.05; непарный двусторонний t-тест).
[0059] Таблица 2 показывает, что соединение (I) значительно снижает секрецию HMGB1 у мышей с артритом, индуцированным коллагеном II типа (p<0,05), и снижает частоту заболеваемости артритом по сравнению с контролем. Таким образом, соединение (I) полезно при лечении HMGB1-зависимого артрита.
Пример 4
[0060] Этот пример иллюстрирует водную фармацевтическую композицию для инъекций, содержащую соединение (I).
[0061] Водную фармацевтическую композицию готовят следующим образом. H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NH2ацетат растворяют в воде для инъекций в количестве, указанном в таблице 3, и раствор доводят до pH 3,0-8,5, используя фосфатный буфер, выход 100%.
[0062] Таблица 3
Вода для инъекций
pH 3.0-8.5
до 100.00
[0063] Раствор фильтруют через фильтр с размером пор 0,22 мкм (Merck Millipore), чтобы приготовить стерильный раствор без консервантов, выход 99,9%. Раствором заполняют стерильные ампулы в потоке азота или любого другого бескислородного инертного газа и запаивают. Полученную водную фармацевтическую композицию в стандартной лекарственной форме можно вводить нуждающемуся в этом субъекту в виде инъекций или внутривенных инфузий для лечения HMGB1-зависимого воспалительного или аутоиммунного заболевания.
Пример 5
[0064] Этот пример иллюстрирует водную фармацевтическую композицию для ингаляций, содержащую соединение (I).
[0065] Водную фармацевтическую композицию готовят следующим образом. H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NH2ацетат растворяют в воде для инъекций в количестве, указанном в таблице 4, с выходом 100%.
[0066] Таблица 4
Вода для инъекций
до 100,00
[0067] Раствор фильтруют через фильтр с размером пор 0,22 мкм (Merck Millipore), чтобы приготовить стерильный раствор без консервантов, выход 99,9%. Раствором заполняют стерильные ампулы в потоке азота или любого другого бескислородного инертного газа и запаивают. Полученную водную фармацевтическую композицию в стандартной лекарственной форме можно вводить нуждающемуся в этом субъекту в виде ингаляций для лечения HMGB1-зависимого воспалительного или аутоиммунного заболевания легких.
Пример 6
[0068] Этот пример иллюстрирует твердую фармацевтическую композицию для ректального введения, содержащую соединение (I).
[0069] Твердая фармацевтическая композиция готовится следующим образом. Для приготовления суппозиторной массы смешивают 1788,9 г Witepsol W35 и 100 г какао-масла и нагревают до 45 °C при перемешивании до полного расплавления, затем расплав охлаждают до 40 °C. В отдельном контейнере 11,1 гH-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NH2ацетата растворяют в 100 г очищенной воды в пропорциях, указанных в таблице 6, до образования прозрачного раствора. Приготовленный водный раствор выливают в нагретый расплав Witepsol W35/масло какао и смесь гомогенизируют. По окончании гомогенизации массу переносят в отдельную емкость, выход 98,5%. Пустую ленту для суппозиториев помещают в держатель машины для наполнения, а температуру контейнера для наполнения суппозиторной массой устанавливают на 40 °C. После наполнения суппозитории оставляют охлаждаться в заполненном отсеком для хранения ленты. Выход стадии 99% (в пересчете на основное вещество). Замороженные суппозитории фиксируются на держателе ленты, запускается процесс запайки и разрезания ленты суппозиториев. Готовый продукт представляет собой суппозиторий массой 2 г с содержанием соединения (I) 10 мг. Состав суппозиториев представлен в таблице 5.
[0070] Таблица 5
Очищенная вода
Масло какао
Witepsol W35
5.0
5.0
до 100
[0071] Полученные суппозитории можно вводить ректально нуждающемуся в этом субъекту для лечения HMGB1-зависимого воспалительного или аутоиммунного заболевания.
Изобретение относится к соединению формулы (I): H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-Z, где Z представляет собой -NR1R2, где R1 и R2 являются одинаковыми или разными и представляют собой водород или низшую алкильную цепь, содержащую до 4 атомов углерода, или его фармацевтически приемлемой соли, а также к фармацевтическим композициям на его основе для применения в лечении HMGB1-зависимого воспалительного или аутоиммунного заболевания. 2 н. и 5 з.п. ф-лы, 5 табл., 6 пр.
1. Соединение формулы (I)

где Z это
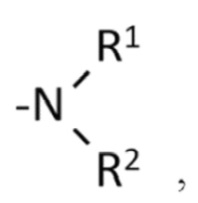
в которой R1 и R2 являются одинаковыми или разными и представляют собой водород или низшую алкильную цепь, содержащую до 4 атомов углерода, или его фармацевтически приемлемая соль.
2. Соединение по п.1, где указанное соединение выбрано из группы, состоящей из H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NH2 ацетат, H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NHC2H5 ацетат, H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NHC4H9 ацетат и H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-N(CH3)2 ацетат.
3. Соединение по любому из пп.1 или 2, где указанное соединение представляет собой H-Tyr-D-Ala-Gly-Phe-Leu-Arg-Arg-NH2 ацетат.
4. Фармацевтическая композиция для лечения HMGB1-зависимого воспалительного или аутоиммунного заболевания, содержащая эффективное количество соединения по любому из пп.1-3 и фармацевтически приемлемый наполнитель.
5. Соединение по любому из пп.1-4 для использования в качестве лекарственного средства.
6. Соединение по любому из пп.1-5 для лечения HMGB1-зависимого воспалительного или аутоиммунного заболевания, выбранного из группы, состоящей из ревматоидного артрита, остеоартрита, анкилозирующего спондилита, пародонтита, аллергического ринита, хронического риносинусита без носовых полипов, хронического риносинусита с носовыми полипами, пневмонии, хронической обструктивной болезни легких, астмы, острого респираторного синдрома взрослых, диабетической макроангиопатии, диабетической ишемической болезни сердца, заболевания периферических артерий, диабетической цереброваскулярной болезни, диабетической микроангиопатии, диабетической нефропатии, диабетической нейропатии, диабетической кардиомиопатии, язвы диабетической стопы, колита, воспалительного заболевания кишечника и заболевания глаз.
7. Соединение по любому из пп.1-6, где фармацевтически приемлемая соль представляет собой ацетат.
| Способ получения пептидов | 1985 |
|
SU1433415A3 |
| US 4707468 A, 17.11.1987 | |||
| Chavkin, Charles; Goldstein, Avram | |||
| Specific receptor for the opioid peptide dynorphin: Structure-activity relationships | |||
| Proceedings of the National Academy of Sciences of the United States of America, 1981, 78(10), 6543-6547. | |||
Авторы
Даты
2021-11-22—Публикация
2021-04-22—Подача