ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Данная заявка испрашивает преимущество и приоритет по предварительной заявке США № 62/555141, поданной 7 сентября 2017 года, 62/657345, поданной 13 апреля 2018 года, и 62/659870, поданной 19 апреля 2018 года, содержание которых включено в данное описание посредством ссылки в полном объеме.
ССЫЛКА НА ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Перечень последовательностей, поданный 6 сентября 2018 года в виде текстового файла с именем "064466.070 sequence listing_ST25.txt", который создан 21 августа 2018 года и имеет размер 10,7 килобайт, включен в данное описание посредством ссылки в соответствии с 37 C.F.R. § 1.52(e)(5).
ОБЛАСТЬ ТЕХНИКИ
Данное изобретение в целом направлено на композиции и способы селективной активации активности Akt3 и способы их применения для модуляции регуляторных Т-клеток.
УРОВЕНЬ ТЕХНИКИ
Регуляторные T-клетки (Treg) представляют собой подмножество CD4+ T-клеток, которые подавляют иммунные ответы и являются важными медиаторами аутотолерантности и иммунного гомеостаза (Sakaguchi, et al., Cell, 133, 775-787 (2008)). Деплетирование или инактивация Treg приводит к развитию тяжелых аутоиммунных реакций (Sakaguchi, et al., J. Immunol., 155, 1151-1164 (1995)), и их накопление ингибирует противоопухолевый иммунитет (Dannull, et al., The Journal of clinical investigation, 115, 3623-3633 (2005)). Treg характеризуются экспрессией Foxp3, являющимся транскрипционным фактором, принадлежащим к семейству транскрипционных факторов Forkhead Box. Foxp3 является основным регулятором клеток Treg, поскольку он необходим для их развития и функционирования (Hori, Science, 299, 1057-1061 (2003); Fontenot, et al., Nat Immunol., 4(4):330-6 (2003). Epub 2003 Mar 3; Khattri, et al., Nat Immunol., 4(4):337-42 (2003). Epub 2003 Mar 3)).
Существует два основных типа клеток Treg: Treg, происходящие из тимуса (или природные Treg (nTreg)), которые составляют 5-10% от общего количества периферических CD4+ T-клеток, и периферические TGFβ-индуцированные Treg (iTreg). Продемонстрировано, что оба типа обладают иммуносупрессивными свойствами, опосредованными несколькими процессами, в которых участвуют иммуносупрессивные растворимые факторы или клеточный контакт (Bluestone, et al., Nat Rev Immunol, 3, 253-257 (2003); Glisic, et al., Cell and Tissue Research, 339, 585-595 (2010); Hori, Science, 299, 1057-1061 (2003); Sakaguchi, Cell, 101, 455-458 (2000); Sakagushi, et al., Curr. Top Microbiol. Immunol., 305, 51-66 (2006); Sakagushi, et al., Immunol., Rev., 212, 8-27 (2006); (Schmidt, et al., Front Immunol., 3:51 (2012)). Однако молекулярные механизмы, с помощью которых nTreg и iTreg развиваются и затем демонстрируют недублирующие свойства для подавления иммунитета, до конца не изучены (Dipica, et al., Immunity, 35 (1): 109-122 (2011)).
Сигналинг PI3K-Akt влияет на многие процессы и является центральным для многих сигнальных путей. Фосфорилирование Akt и активность киназы индуцируются активацией PI3K, которая, в свою очередь, индуцируется несколькими рецепторами факторов роста, TCR, CD28 и ИЛ-2R, среди многих других (Parry, et al., Trends in Immunology, 28, 161-168 (2007)). У млекопитающих есть три изоформы Akt, а именно Akt1, Akt2 и Akt3, кодируемые тремя независимыми генами. In vitro эти изоформы, по-видимому, выполняют дублирующие функции, поскольку различные внеклеточные входы могут индуцировать сходные профили сигналинга Akt (Franke, Science 1, pe29- (2008)). Тем не менее, изоформ-специфические нокауты демонстрируют уникальные особенности, и их участие в развитии заболеваний и физиологических состояниях отличается (Boland, et al., American Journal of Human Genetics, 81, 292-303 (2007); DeBosch, et al., J. Biol. Chem, 281, 32841-32851 (2006); Emamian, et al., Nat Genet, 36, 131-137 (2004); Garofalo, et al., The Journal of clinical investigation, 112, 197-208 (2003); George, et al., Science, 304, 1325-1328 (2004); Nakatani, et al., The Journal of Biological Chemistry, 274, 21528-21532 (1999); Tschopp, et al., Development (Cambridge, England), 132, 2943-2954 (2005); Yang, et al., J. Biol. Chem., 278, 32124-32131 (2003)).
Исследования продемонстрировали, что Akt1 и Akt2 могут негативно регулировать характерные транскрипционные признаки Treg, тем самым избирательно влияя на дифференцировку линии Treg (Sauer, et al., Proceedings of the National Academy of Sciences, 105, 7797-7802 (2008a)). Кроме того, несмотря на то, что было показано, что ингибирование изоформ Akt1 и Akt2 увеличивает экспрессию Foxp3 в индуцированных TGFβ iTregs (Sauer, et al., Proc. Natl. Acad. Sci. USA, 105, 7797-7802 (2008b)), указанный механизм остается неясным. Другое открытие демонстрирует, что делеция Akt2 приводила к дефектной дифференцировке клеток iTh17, но сохраняла развитие клеток nTh17 (Kim, et al., Nat Immunol., 14 (6): 611-8 (2013) Epub 2013 May 5). Кроме того, Akt3 также экспрессируется в иммунных клетках, и в спинном мозге у мышей с нокаутом Akt3, в которых уменьшается количество регуляторных T-клеток Foxp3+ по сравнению с мышами дикого типа (Tsiperson, et al., J Immunol., 190(4):1528-39 (2013) Epub 2013 Jan 18)). Таким образом, несмотря на то, что в некоторых исследованиях изучалась значимость экспрессии изоформ Akt в биологии Т-клеток (Carson, et al., Annals of the New York Academy of Sciences, 1103, 167-178 (2007) , Crellin, et al., Blood, 109, 2014-2022 (2007a); Crellin, et al., Journal of Immunological Methods, 324, 92-104 (2007b); Haxhinasto, J. Exp. Med., 205, 565-574 (2008); Li, et al., Blood, 106, 3068-3073 (2005); Patton, et al., Biochem. Soc. Trans., 35, 167-171 (2007); Patton, et al., J. Immunology 177, 6598-6602 (2006); Sauer, et al., Proc. Natl. Acad. Sci. USA, 105, 7797-7802 (2008b); Walsh, et al., J. Clin. Invest., 116, 2521-2531. (2006)), роли, которые изоформы Akt играют в функции и индукции Treg, все еще остаются неясными.
Следовательно, целью изобретения является создание соединений и композиций для селективной активации Akt3 в иммунных клетках.
Другой целью изобретения является создание способов снижения иммунного ответа у субъекта.
Еще одной целью изобретения является создание способов усиления супрессивного иммунного ответа у субъекта.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В данном изобретении предлагаются композиции и способы селективного активирования Akt3. В одном варианте осуществления данного изобретения предлагается соединение в соответствии с формулой I:
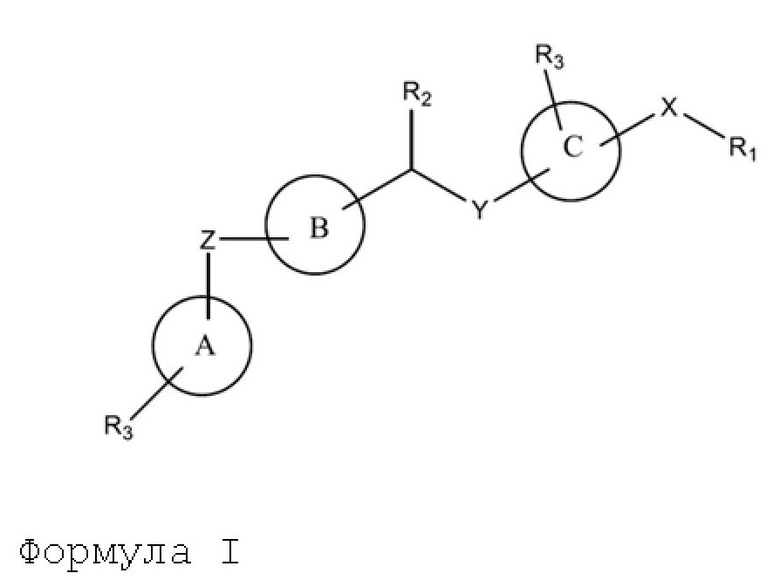
или его фармацевтически приемлемый энантиомер, соль или сольват, где:
кольца A, B и C независимо представляют собой шестичленные арильные или N-содержащие гетероарильные моно- или бициклические кольцевые системы, содержащие ноль или большее количество N-атомов, такие как фенил, пиридин, пиримидин, пиридазин, пиразин, триазин, хинолин, хиназолин, изохинолин, нафталин, нафтиридин, индол, изоиндол, циннолин, фталазин, хиноксалин, птеридин, пурин и бензимидазол.
R1 выбирают из -(C1-C30)-алкила, -(C3-C12)-циклоалкила, -(C3-C12)-гетероциклоалкила, -(C6-C20)-арила, или -(C3-C20)-гетероарильных групп необязательно замещенных одним или большим количеством заместителей, выбранных из -(C1-C12)-алкила, -(C3-C12)-циклоалкила, -(C3-C12)-гетероциклоалкила, -O-(C1-C12)-алкила, -O-(C1-C12)-алкил-(C6-C20)-арила, -O-(C3-C12)-циклоалкила, -S-(C1-C12)-алкила, -S-(C3-C12)-циклоалкила, -COO-(C1-C12)-алкила, -COO-(C3-C12)-циклоалкила, -CONH-(C1-C12)-алкила, -CONH-(C3-C12)-циклоалкила, -CO-(C1-C12)-алкила, -CO-(C3-C12)-циклоалкила, -N-[(C1-C12)-алкил]2, -(C6-C20)-арила, -(C6-C20)-арил-(C1-C12)-алкила, -(C6-C20)-арил-O-(C1-C12)-алкила, -(C3-C20)-гетероарила, -(C3-C20)-гетероарил-(C1-C12)-алкила, -(C3-C20)-гетероарил-O-(C1-C12)-алкила, -COOH, -OH, -SH, -SO3H, -CN, -NH2, или галогена;
X, Y и Z независимо выбирают из =O, -NH, -S, -N-(C1-C30)-алкила или -(C1-C30)-арила;
R2 выбирают из -(C1-C30)-алкила, =O, -OH, -SO2, -SO, или -SOCH3; и
R3 выбирают из -(C1-C30)-алкила, -(C3-C12)-циклоалкила, -(C3-C12)-гетероциклоалкила, -(C6-C20)-арила, или -(C3-C20)-гетероарильных групп, необязательно замещенных одним или большим количеством заместителей, выбранных из -(C1-C12)-алкила, -(C3-C12)-циклоалкила, -(C3-C12)-гетероциклоалкила, -O-(C1-C12)-алкила, -O-(C1-C12)-алкила-(C6-C20)-арила, -O-(C3-C12)-циклоалкила, -S-(C1-C12)-алкила, -S-(C3-C12)-циклоалкила, -COO-(C1-C12)-алкила, -COO-(C3-C12)-циклоалкила, -CONH-(C1-C12)-алкила, -CONH-(C3-C12)-циклоалкила, -CO-(C1-C12)-алкила, -CO-(C3-C12)-циклоалкила, -N-[(C1-C12)-алкил]2, -(C6-C20)-арила, -(C6-C20)-арил-(C1-C12)-алкила, -(C6-C20)-арил-O-(C1-C12)-алкила, -(C3-C20)-гетероарила, -(C3-C20)-гетероарил-(C1-C12)-алкила, -(C3-C20)-гетероарил-O-(C1-C12)-алкила, -COOH, -OH, -SH, -SO3H, -CN, -NH2, или галогена.
В другом варианте осуществления данного изобретения предлагается соединение в соответствии с формулой II:

или его фармацевтически приемлемый энантиомер, соль или сольват, где:
R1 выбирают из -(C1-C30)-алкила, -(C3-C12)-циклоалкила, -(C3-C12)-гетероциклоалкила, -(C6-C20)-арила, или -(C3-C20)-гетероарильных групп необязательно замещенных одним или большим количеством заместителей, выбранных из -(C1-C12)-алкила, -(C3-C12)-циклоалкила, -(C3-C12)-гетероциклоалкила, -O-(C1-C12)-алкила, -O-(C1-C12)-алкил-(C6-C20)-арила, -O-(C3-C12)-циклоалкила, -S-(C1-C12)-алкила, -S-(C3-C12)-циклоалкила, -COO-(C1-C12)-алкила, -COO-(C3-C12)-циклоалкила, -CONH-(C1-C12)-алкила, -CONH-(C3-C12)-циклоалкила, -CO-(C1-C12)-алкила, -CO-(C3-C12)-циклоалкила, -N-[(C1-C12)-алкил]2, -(C6-C20)-арила, -(C6-C20)-арил-(C1-C12)-алкила, -(C6-C20)-арил-O-(C1-C12)-алкила, -(C3-C20)-гетероарила, -(C3-C20)-гетероарил-(C1-C12)-алкила, -(C3-C20)-гетероарил-O-(C1-C12)-алкила, -COOH, -OH, -SH, -SO3H, -CN, -NH2, или галогена;
X, Y и Z независимо выбирают из -O, -NH, -S, -N-(C1-C30)-алкила или -(C1-C30)-арила;
R2 выбирают из -(C1-C30)-алкила, -O, -OH, -SO2, -SO, или -SOCH3; и
R3 выбирают из -(C1-C30)-алкила, -(C3-C12)-циклоалкила, -(C3-C12)-гетероциклоалкила, -(C6-C20)-арила, или -(C3-C20)-гетероарильных групп, необязательно замещенных одним или большим количеством заместителей, выбранных из -(C1-C12)-алкила, -(C3-C12)-циклоалкила, -(C3-C12)-гетероциклоалкила, -O-(C1-C12)-алкила, -O-(C1-C12)-алкила-(C6-C20)-арила, -O-(C3-C12)-циклоалкила, -S-(C1-C12)-алкила, -S-(C3-C12)-циклоалкила, -COO-(C1-C12)-алкила, -COO-(C3-C12)-циклоалкила, -CONH-(C1-C12)-алкила, -CONH-(C3-C12)-циклоалкила, -CO-(C1-C12)-алкила, -CO-(C3-C12)-циклоалкила, -N-[(C1-C12)-алкил]2, -(C6-C20)-арила, -(C6-C20)-арил-(C1-C12)-алкила, -(C6-C20)-арил-O-(C1-C12)-алкила, -(C3-C20)-гетероарила, -(C3-C20)-гетероарил-(C1-C12)-алкила, -(C3-C20)-гетероарил-O-(C1-C12)-алкила, -COOH, -OH, -SH, -SO3H, -CN, -NH2, или галогена.
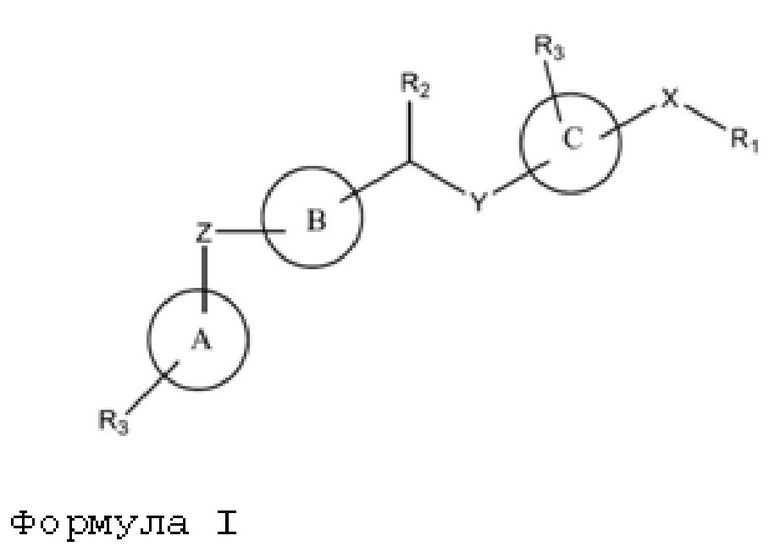
В другом варианте осуществления данного изобретения предлагается соединение в соответствии с формулой III:
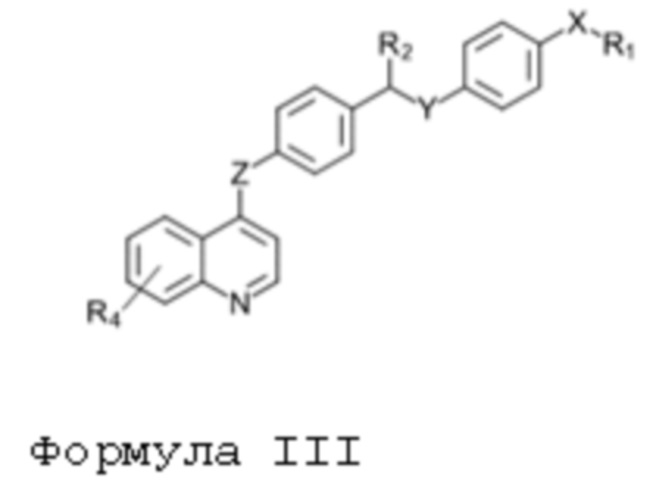
или его фармацевтически приемлемый энантиомер, соль или сольват, где.
R1 выбирают из -(C1-C30)-алкила, -(C3-C12)-циклоалкила, -(C3-C12)-гетероциклоалкила, -(C6-C20)-арила, или -(C3-C20)-гетероарильных групп необязательно замещенных одним или большим количеством заместителей, выбранных из -(C1-C12)-алкила, -(C3-C12)-циклоалкила, -(C3-C12)-гетероциклоалкила, -O-(C1-C12)-алкила, -O-(C1-C12)-алкил-(C6-C20)-арила, -O-(C3-C12)-циклоалкила, -S-(C1-C12)-алкила, -S-(C3-C12)-циклоалкила, -COO-(C1-C12)-алкила, -COO-(C3-C12)-циклоалкила, -CONH-(C1-C12)-алкила, -CONH-(C3-C12)-циклоалкила, -CO-(C1-C12)-алкила, -CO-(C3-C12)-циклоалкила, -N-[(C1-C12)-алкил]2, -(C6-C20)-арила, -(C6-C20)-арил-(C1-C12)-алкила, -(C6-C20)-арил-O-(C1-C12)-алкила, -(C3-C20)-гетероарила, -(C3-C20)-гетероарил-(C1-C12)-алкила, -(C3-C20)-гетероарил-O-(C1-C12)-алкила, -COOH, -OH, -SH, -SO3H, -CN, -NH2, или галогена;
X, Y и Z независимо выбирают из -O, -NH, -S, -N-(C1-C30)-алкила или -(C1-C30)-арила;
R2 выбирают из -(C1-C30)-алкила, =O, -OH, -SO2, -SO, или -SOCH3; и
R4 выбирают из -(C1-C12)-алкила, -(C3-C12)-циклоалкила, -(C3-C12)-гетероциклоалкила, -O-(C1-C12)-алкила, -O-(C1-C12)-алкил-(C6-C20)-арила, -O-(C3-C12)-циклоалкила, -S-(C1-C12)-алкила, -S-(C3-C12)-циклоалкила, -COO-(C1-C12)-алкила, -COO-(C3-C12)-циклоалкила, -CONH-(C1-C12)-алкила, -CONH-(C3-C12)-циклоалкила, -CO-(C1-C12)-алкила, -CO-(C3-C12)-циклоалкила, -N-[(C1-C12)-алкил]2, -(C6-C20)-арила, -(C6-C20)-арил-(C1-C12)-алкила, -(C6-C20)-арил-O-(C1-C12)-алкила, -(C3-C20)-гетероарила, -(C3-C20)-гетероарил-(C1-C12)-алкила, -(C3-C20)-гетероарил-O-(C1-C12)-алкила, -COOH, -OH, -SH, -SO3H, -CN, -NH2, или галогена.
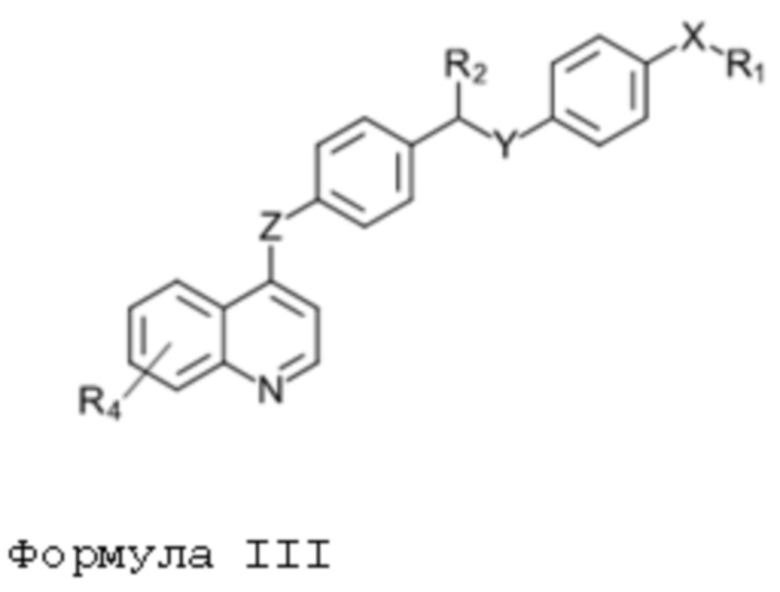
В другом варианте осуществления данного изобретения предлагается соединение в соответствии с формулой IV:
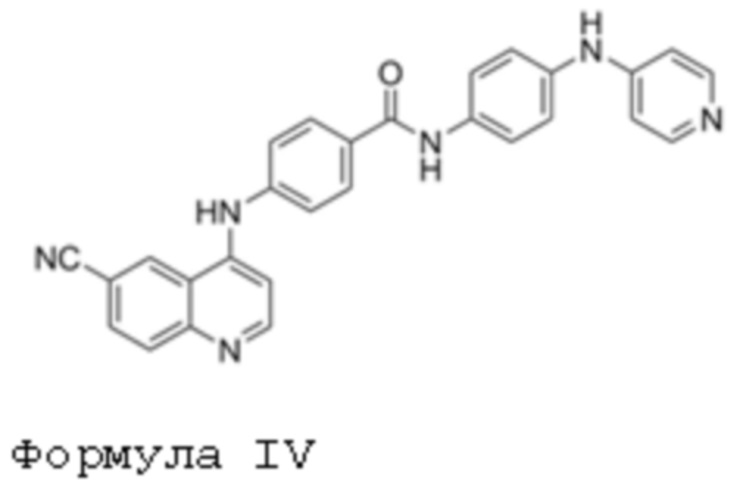
или его фармацевтически приемлемый энантиомер, соль или сольват.
Было обнаружено, что соединение в соответствии с формулой IV (также обозначаемое как mJJ64A) селективно активирует Akt3. Название IUPAC для mJJ64A представляет собой 4-(m-{[p-(4-пиридиламино) фениламино]карбонил}фениламино)-6-хинолинкарбонитрил. Поскольку Akt3 модулирует супрессивную функцию природных Treg и поляризацию индуцированных Treg, соединение формулы IV и родственные соединения формул I-III можно применять для модуляции иммунных ответов.
В одном варианте осуществления данного изобретения предлагается способ усиления иммуносупрессивного ответа у субъекта, нуждающегося в этом, включающий введение указанному субъекту композиции, включающей соединение в соответствии с формулой I, формулой II, формулой III или формулой IV, или его энантиомер, полиморф или фармацевтически приемлемую соль, которые селективно активируют Akt3 посредством количества, эффективного для усиления иммуносупрессивного ответа у указанного субъекта.
Например, в данном изобретении описаны способы повышения иммуносупрессивного ответа, уменьшения иммуностимулирующего ответа или их комбинации у субъекта, нуждающегося в этом. Способы, как правило, включают введение указанному субъекту композиции, включающей соединение в соответствии с формулой I, формулой II, формулой III или формулой IV, или его энантиомер, полиморф или фармацевтически приемлемую соль, которые селективно активируют биоактивность Akt3 в количестве, эффективном для повышения или стимулирования иммуносупрессивного ответа, уменьшения иммуностимулирующего ответа или их комбинации у указанного субъекта.
В некоторых вариантах осуществления данного изобретения иммуносупрессивный ответ, который повышается, выбирают из группы, состоящей из иммуносупрессивной функции природной Treg (nTreg) и содействия превращению типовых T-клеток в индуцированные Treg (iTreg). Иммуносупрессивная функция nTreg может заключаться в секреции одного или большего количества противовоспалительных цитокинов. Противовоспалительным цитокином(ами) может быть ИЛ10, TGFβ или их комбинация.
В некоторых вариантах осуществления данного изобретения указанный субъект имеет аутоиммунное заболевание. Следовательно, в данном документе также описаны способы лечения аутоиммунных заболеваний путем введения субъекту, нуждающемуся в этом, эффективного количества соединения в соответствии с формулой I, формулой II, формулой III или формулой IV или его энантиомера, полиморфа или его фармацевтически приемлемой соли, которое индуцирует или повышает биодоступность или биологическую активность Akt3.
Также описана комбинированная терапия, включающая модуляторы биологической активности Akt3 и способы ее применения.
В одном варианте осуществления данного изобретения предлагается способ усиления иммуносупрессивного ответа у субъекта, нуждающегося в этом, путем введения субъекту композиции, содержащей эффективное количество соединения в соответствии с формулой I, формулой II, формулой III или формулой IV, или его энантиомер, полиморф или фармацевтически приемлемую соль, которые селективно активируют Akt3 посредством количества, эффективного для усиления иммуносупрессивного ответа у указанного субъекта. У указанного субъекта может быть воспалительное нарушение или заболевание, например, аутоиммунное заболевание.
В другом варианте осуществления данного изобретения предлагается способ лечения воспалительного нарушения у субъекта, нуждающегося в этом, путем введения композиции, содержащей соединение в соответствии с формулой I, формулой II, формулой III или формулой IV, или его энантиомер, полиморф или фармацевтически приемлемую соль, которые селективно активируют Akt3 в количестве, эффективном для усиления, индукции или стимуляции иммуносупрессивного ответа у указанного субъекта.
В некоторых вариантах осуществления данного изобретения воспалительное нарушение или заболевание выбирают из группы, состоящей из ревматоидного артрита, системной красной волчанки, гнездной алопеции, анкилозирующего спондилита, антифосфолипидного синдрома, аутоиммунной болезни Аддисона, аутоиммунной гемолитической анемии, аутоиммунного гепатита, аутоиммунного заболевания внутреннего уха, аутоиммунного лимфопролиферативного синдрома (ALPS), аутоиммунной тромбоцитопенической пурпуры (ATP), болезни Бехчета, буллезного пемфигоида, кардиомиопатии, дерматита, ассоциированного со спру-целиакией, синдрома хронической усталости и иммунодефицита, синдрома (CFIDS), хронической воспалительной демиелинизирующей полиневропатии, рубцового пемфигоида, холодовой агглютининовой болезни, синдрома Креста, болезни Крона, болезни Дего, дерматомиозита, дерматомиозита ювенильного, дискоидной волчанки, эссенциальной смешанной криоглобулинемии, фибромиалгии - фибромиозита, болезни Грейвса, болезни Гийена-Барре, тиреоидита Хашимото, идиопатического легочного фиброза, идиопатической тромбоцитопенической пурпуры (ITP), IgA-нефропатии, инсулинозависимого диабета (тип I), ювенильного артрита, болезни Меньера, смешанного заболевания соединительной ткани, рассеяного склероза, миастении, ожирения, пузырчатки обыкновенной, пернициозной анемии, узелкового полиартериита, полихондрита, полигландулярного синдрома, ревматической полимиалгии, полимиозита и дерматомиозита, первичной агаммаглобулинемии, первичного билиарного цирроза, псориаза, феномена Рейно, синдрома Рейтера, ревматической лихорадки, саркоидоза, склеродермии, синдрома Шегрена, синдрома мышечной скованности, артериита Такаясу, височного артериита/гигантоклеточного артериита, язвенного колита, увеита, васкулита, витилиго и гранулематоза Вегенера.
В другом варианте осуществления данного изобретения предлагается способ лечения аутоиммунного заболевания путем введения субъекту, нуждающемуся в этом, композиции, содержащей соединение в соответствии с формулой I, формулой II, формулой III или формулой IV, или его энантиомер, полиморф или фармацевтически приемлемую соль, которые селективно ингибируют Akt3 в количестве, эффективном для стимуляции или усиления иммуносупрессивного ответа у указанного субъекта.
Типовые аутоиммунные заболевания включают, но не ограничиваются ими, ревматоидный артрит, системную красную волчанку, гнездную алопецию, аутоиммунную болезнь Аддисона, аутоиммунную гемолитическую анемию, аутоиммунный гепатит, аутоиммунное заболевание внутреннего уха, аутоиммунный лимфопролиферативный синдром (ALPS), аутоиммунную тромбоцитопеническую пурпуру (ATP), рассеянный склероз, болезнь Крона и миастению.
В некоторых вариантах осуществления данного изобретения иммуносупрессивный ответ, который повышается, выбирают из группы, состоящей из иммуносупрессивной функции природной Treg (nTreg) и индукции превращения типовых T-клеток в индуцированные Treg (iTreg). Иммуносупрессивная функция nTreg может включать секрецию одного или большего количества противовоспалительных цитокинов, например, ИЛ-10, TGFβ или их комбинации.
В другом варианте осуществления данного изобретения предлагается способ лечения субъекта, нуждающегося в этом, путем введения эффективного количества композиции, содержащей соединение в соответствии с формулой I, формулой II, формулой III или формулой IV, или его энантиомер, полиморф или фармацевтически приемлемую соль в комбинации или с чередованием со вторым иммуносупрессивным агентом. Типовые иммуносупрессивные агенты включают, но не ограничиваются ими, преднизон, будесонид, преднизолон, циклоспорин, такролимус, сиролимус, эверолимус, азатиоприн, лефлуномид, микофенолат, абатацепт, адалимумаб, анакинра, цертолизумаб, этанерцепт, голимумаб, инфликсимаб, иксекизумаб, натализумаб, ритуксимаб, секукинумаб, тоцилизумаб, устекинумаб, ведолизумаб, базиликсимаб, даклизумаб, муромонаб или их комбинации.
В некоторых вариантах осуществления данного изобретения соединение в соответствии с формулой I, формулой II, формулой III или формулой IV или его энантиомер, полиморф или фармацевтически приемлемую соль вводят в количестве, эффективном для повышения экспрессии FoxP3 на иммунных клетках, например, Т-клетках, включая, но не ограничиваясь, на клетках Treg, таких как iTreg и nTreg.
В других вариантах осуществления данного изобретения соединение в соответствии с формулой I, формулой II, формулой III или формулой IV или его энантиомер, полиморф или фармацевтически приемлемую соль вводят в количестве, эффективном для повышения пролиферации iTreg и nTreg.
Еще один вариант осуществления данного изобретения предлагается фармацевтическая композиция, содержащая соединение в соответствии с формулой I, формулой II, формулой III или формулой IV или его энантиомер, полиморф или фармацевтически приемлемую соль и вспомогательное вещество. Соединение в соответствии с формулой I, формулой II, формулой III, формулой IV или его энантиомер, полиморф или фармацевтически приемлемая соль обычно находится в количестве, эффективном для усиления супрессивного иммунного ответа при введении субъекту, нуждающемуся в этом.
В другом варианте осуществления данного изобретения предлагается способ усиления иммуного супрессивного ответа у субъекта, нуждающегося в этом, путем приведения в контакт иммунных клеток ex vivo с соединением в соответствии с формулой I, формулой II, формулой III или формулой IV или энантиомером, полиморфом или его фармацевтически приемлемой солью в количестве, эффективном для повышения экспрессии FoxP3 на иммунных клетках, и введения приведенных в контакт иммунных клеток указанному субъекту. В одном варианте осуществления данного изобретения указанные иммунные клетки представляют собой аутологичные иммунные клетки. Указанные иммунные клетки могут включать Т-клетки, включая, но не ограничиваясь этим, nTreg и iTreg.
В другом варианте осуществления данного изобретения предлагается способ ингибирования или уменьшения отторжения трансплантата у субъекта, нуждающегося в этом, путем введения субъекту эффективного количества соединения в соответствии с формулой I, формулой II, формулой III или формулой IV или энантиомера, полиморфа или его фармацевтически приемлемой соли для повышения экспрессии FoxP3 на иммунных клетках указанного субъекта. В некоторых вариантах осуществления данного изобретения повышенная экспрессия FoxP3 на иммунных клетках субъектов индуцирует, стимулирует или повышает супрессивный иммунный ответ у указанного субъекта.
В другом варианте осуществления данного изобретения предлагается способ лечения болезни "трансплантат против хозяина" у субъекта, нуждающегося в этом, путем введения эффективного количества соединения в соответствии с формулой I, формулой II, формулой III или формулой IV или энантиомера, полиморфа или его фармацевтически приемлемой соли для повышения экспрессии FoxP3 на иммунных клетках указанного субъекта.
В другом варианте осуществления данного изобретения предлагается способ лечения хронической инфекции у субъекта, нуждающегося в этом, путем введения эффективного количества соединения в соответствии с формулой I, формулой II, формулой III или формулой IV или энантиомера, полиморфа или его фармацевтически приемлемой соли для повышения экспрессии FoxP3 на иммунных клетках указанного субъекта.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На Фиг. 1 продемонстрирована структура соединения формулы IV (mJJ64A).
Фиг. 2A-2F представляют собой гистограммы FACS-отсортированных iTreg, обработанных указанным количеством mJJ64A. Фиг. 2G представляет собой гистограмму, демонстрирующую процент CD4+ Foxp3+ Т-клеток, обработанных указанным количеством mJJ64A. Фиг. 2Н представляет собой гистограмму средней интенсивности флуоресценции (MFI) (клетки CD4+Foxp3) с обработкой указанным количеством mJJ64A.
Фиг. 3А представляет собой авторадиографию вестерн-блоттинга, демонстрирующую экспрессию Foxp3 при индукции iTreg и обработке указанным количеством mJJ64A. β-актин является контролем. Фиг. 3В представляет собой повторение эксперимента на Фиг. 3A.
Фиг. 4А представляет собой гистограмму, представляющая экспрессию трех изоформ Akt (Akt1, Akt2 и Akt3) в клетках Tconv (серый столбец) и Treg (черный столбец). Фиг. 4В представляет собой вестерн-блот, демонстрирующий экспрессию Akt1, Akt2 и Akt3 в клетках Tconv и Treg. β-актин является контролем нагрузки. Фиг. 4С представляет собой вестерн-блот, демонстрирующий экспрессию pSer при в/бр введении Akt1, Akt2 или Akt3 в нестимулированных или стимулированных клетках Tconv и nTreg. Фиг. 4D представляет собой гистограмму, демонстрирующую супрессивную активность Treg у мышей ДТ (серый столбец) и Akt3 KO (черный столбец). Ось X представляет отношение Tconv к Treg. Ось Y представляет нормализованный процент пролиферации. Фиг. 4E представляет собой гистограмму, демонстрирующую уровни ИЛ-10 (пг/мл) в Treg от мышей ДТ, Akt1 KO, Akt2 KO или Akt3 KO. Фи. 4F представляет собой гистограмму, демонстрирующую уровни TGFβ (пг/мл) в Treg от мышей ДТ, Akt1 KO, Akt2 KO или Akt3 KO.
Фиг. 5А представляет собой линейный график, демонстрирующий процент выживаемости мышей с RAG-колитом, получавших PBS (•), ДТ наивные Т-клетки+PBS ( ), ДТ наивные Т-клетки+ДТ nTreg (
), ДТ наивные Т-клетки+ДТ nTreg ( ) или ДТ наивные Т-клетки+Akt3 nTreg (
) или ДТ наивные Т-клетки+Akt3 nTreg ( ). Фиг. 5В представляет собой линейный график, демонстрирующий объем опухоли (мм 3) в динамике (дни) у мышей с адоптивным переносом EL4 (♦), PC61+EL4 (◊), PC61+EL4+ДТ Treg (
). Фиг. 5В представляет собой линейный график, демонстрирующий объем опухоли (мм 3) в динамике (дни) у мышей с адоптивным переносом EL4 (♦), PC61+EL4 (◊), PC61+EL4+ДТ Treg ( ) или PC61+EL4+Akt3 KO Treg (
) или PC61+EL4+Akt3 KO Treg ( ).
).
Фи. 6А представляет собой вестерн-блот, демонстрирующий экспрессию Akt1, Akt2 и Akt3 в клетках Th и iTreg. β-актин является контролем нагрузки. Фиг. 6В представляет собой гистограмму, демонстрирующую экспрессию РНК Akt1, Akt2 и Akt3 в клетках Th (серый столбец) и iTreg (черный столбец). Фиг. 6С представляет собой вестерн-блот, демонстрирующий экспрессию pSer в клетках Th или Treg после в/бр введения Akt1, Akt2 или Akt3. Фиг. 6D представляет собой гистограмму, демонстрирующую процент клеток FoxP3+ в популяции CD4 Т-клеток в клетках Th (серый столбец) и iTreg (черный столбец) у мышей Akt1 KO, мышей Akt2 KO и мышей Akt3 KO. Фиг.6E представляет собой гистограмму, демонстрирующую индукцию FoxP3 в Tconv в ответ на TGFβ в Th (ДТ) + CV (сплошная линия), iTreg (ДТ) + CV (линия из точек) и iTreg (ДТ) + Akt3 кшРНК (пунктирная линия).
Фиг. 7А представляет собой вестерн-блот, демонстрирующий экспрессию Akt3 и FoxP3 в контроле и в Treg с нокином Akt3. β-актин применяется в качестве нагрузочного контроля. Фиг. 7В представляет собой гистограмму, демонстрирующую экспрессию FoxP3. Фиг. 7C представляет собой гистограмму, демонстрирующую MFI (CD4+FoxP3) в контроле и в Akt3 KI Treg. На Фиг. 7D-I продемонстрированы гистограммы, представляющие экспрессию ИЛ2 и актина в контроле и Akt3 KI Treg. На Фиг. 7D и на Фиг. 7G продемонстрирована экспрессия ИЛ2 в контролях и Akt3 KI соответственно. На Фиг. 7Е и на Фиг. 7Н продемонстрирована экспрессия актина в контроле и Akt3 KI, соответственно. На Фиг. 7F и на Фиг.7I продемонстрировано наложение пиков экспрессии ИЛ2 и актина для контроля и Akt3 KI соответственно.
Фиг. 8 представляет собой гистограмму, демонстрирующую влияние mJJ64A на экспрессию Akt1 pS473, Akt2 pS474, Akt3 pS472 и Akt pan S473,474,472 в клетках A2780 по сравнению с контролем. Ось Y представляет собой значение интегральной плотности.
Фиг. 9А представляет собой вестерн-блот, демонстрирующий экспрессию FoxP3, pAkt3, Akt3, pAkt1 и Akt1 в активированных клетках Tconv, индуцированных TGF-β и обработанных различными концентрациями mJJ64A. Фиг. 9В представляет собой гистограмму, демонстрирующую экспрессию RORγt и FoxP3 в активированных iTreg, индуцированных TGF-β и обработанных различными концентрациями mJJ64A. Фиг. 9С представляет собой вестерн-блот, демонстрирующую экспрессию FoxP3 в активированных iTreg, индуцированных TGF-β и обработанных различными концентрациями mJJ64A.
На Фиг. 10А приведены гистограммы, представляющие пролиферацию активированных iTreg, индуцированных TGF-β и обработанных различными концентрациями mJJ64A. Фиг. 10B представляет собой гистограмму, демонстрирующую процент пролиферации iTreg, обработанных различными концентрациями mJJ64A. Ось X представляет концентрацию mJJ64A. Ось Y представляет процент пролиферации. Фиг. 10С представляет собой гистограмму, демонстрирующую процент живых клеток в iTreg, обработанных различными концентрациями mJJ64A. Ось X представляет обработку, а ось Y представляет процент живых клеток. Фиг. 10D представляет собой набор гистограмм, демонстрирующих пролиферацию активированных nTreg, обработанных различными концентрациями mJJ64A. Фиг. 10Е представляет собой гистограмму, демонстрирующую процент пролиферации nTreg, обработанных различными концентрациями mJJ64A. Ось X представляет обработку, а ось Y представляет процент пролиферации. Фиг. 10F представляет собой гистограмму, демонстрирующую процент живых клеток в nTreg, обработанных различными концентрациями mJJ64A. Ось X представляет обработку, а ось Y представляет процент живых клеток. Фиг. 10G представляет собой набор гистограмм, демонстрирующих пролиферацию CD4 T-клеток, обработанных различными концентрациями mJJ64A. Фиг. 10Н представляет собой гистограмму, демонстрирующую процент пролиферации CD4 T клеток, обработанных различными концентрациями mJJ64A. Ось X представляет концентрацию mJJ64A. Ось Y представляет процент пролиферации. Фиг. 10I представляет собой гистограмму, демонстрирующую процент живых клеток в CD4 T клетках, обработанных различными концентрациями mJJ64A. Ось X представляет обработку, а ось Y представляет процент живых клеток. Фиг. 10J представляет собой набор гистограмм, демонстрирующих пролиферацию CD8 T-клеток, обработанных различными концентрациями mJJ64A. Фиг. 10К представляет собой гистограмму, демонстрирующую процент пролиферации CD8 T-клеток, обработанных различными концентрациями mJJ64A. Ось X представляет концентрацию mJJ64A. Ось Y представляет процент пролиферации. Фиг. 10L представляет собой гистограмму, демонстрирующую процент живых клеток в CD8 Т-клетках, обработанных различными концентрациями mJJ64A. Ось X представляет обработку, а ось Y представляет процент живых клеток.
Фиг. 11А представляет собой набор гистограмм, демонстрирующих супрессивную функцию мышиных iTreg в необработанных и mJJ64A-обработанных iTreg. Соотношение клеток iTreg и Tconv составляло 0:1, 0,5:1, 1:1 и 2:1. Фиг. 11B представляет собой гистограмму, демонстрирующую процент пролиферации в необработанных (черный столбец) и обработанных mJJ64A (серый столбец) клетках при соотношении Treg:Tconv, составляющем 0,5:1. Ось X представляет экспериментальную группу, а ось Y представляет процент пролиферации. Фиг. 11С представляет собой гистограмму, демонстрирующую процент пролиферации в необработанных (черный столбец) и обработанных mJJ64A (серый столбец) клетках при соотношении Treg:Tconv, составляющем 1:1. Ось X представляет экспериментальную группу, а ось Y представляет процент пролиферации. Фиг. 11D представляет собой гистограмму, демонстрирующую процент пролиферации в необработанных (черный столбец) и обработанных mJJ64A (серый столбец) клетках при соотношении Treg:Tconv, составляющем 2:1. Ось X представляет экспериментальную группу, а ось Y представляет процент пролиферации.
Фиг. 12А представляет собой набор гистограмм, демонстрирующих супрессивную функцию необработанных и mJJ64A-обработанных nTreg. Соотношение клеток iTreg и Tconv составляло 0:1, 0.5:1, 1:1, 2:1 и 3:1. Фиг. 12В представляет собой гистограмму, демонстрирующую процент пролиферирующих клеток в необработанных и mJJ64A-обработанных nTreg в смеси nTreg и Tconv (0,5:1). Фиг. 12C представляет собой гистограмму, демонстрирующую процент пролиферирующих клеток в необработанных и mJJ64A-обработанных nTreg в смеси nTreg и Tconv (1:1). Фиг. 12D представляет собой гистограмму, демонстрирующую процент пролиферирующих клеток в необработанных и mJJ64A-обработанных nTreg в смеси nTreg и Tconv (2:1). Фиг. 12E представляет собой гистограмму, демонстрирующую процент пролиферирующих клеток в необработанных и mJJ64A-обработанных nTreg в смеси nTreg и Tconv (3:1). Фиг. 12F представляет собой гистограмму, демонстрирующую пролиферацию nTreg, обработанных различными концентрациями mJJ64A. Фиг. 12G представляет собой гистограмму, демонстрирующую процент пролиферации nTreg, обработанных различными концентрациями mJJ64A. Ось X представляет группу обработки, а ось Y представляет процент пролиферации. Фиг. 12Н представляет собой гистограмму, демонстрирующую процент живых клеток в nTreg, обработанных различными концентрациями mJJ64A. Ось X представляет группу обработки, а ось Y представляет процент пролиферации.
Фиг. 13A представляет собой набор гистограмм, демонстрирующих экспрессию FoxP3 и ИЛ10 в клетках nTreg, обработанных различными концентрациями mJJ64A. Фиг. 13В представляет собой гистограмму, демонстрирующую процент клеток ИЛ-10+ FoxP3+ в nTreg, обработанных различными концентрациями mJJ64A.
Фиг. 14А представляет собой иллюстрацию, демонстрирующую экспериментальный способ и схему лечения для экспериментов с опухолью ТС-1. Фиг. 14В представляет собой линейный график, демонстрирующий объем опухоли (см3) в динамике (дни) для не получавших ( ) и получавших mJJ64A-(♦) мышей с опухолью TC1.
) и получавших mJJ64A-(♦) мышей с опухолью TC1.
Фиг. 15А представляет собой гистограмму, демонстрирующую число клеток CD8+ на 10 6 живых клеток в опухолях от не получавших (черный столбец) и получавших mJJ64A (серый столбец) мышей. Фиг. 15В представляет собой гистограмму, демонстрирующую число клеток CD4+ на 10 6 живых клеток в опухолях от не получавших (черный столбец) и получавших mJJ64A (серый столбец) мышей. Фиг. 15С представляет собой гистограмму, демонстрирующую число клеток FoxP3+ на 106 CD4+ клеток в опухолях от не получавших (черный столбец) и получавших mJJ64A (серый столбец) мышей. Фиг. 15D представляет собой гистограмму, демонстрирующую число клеток CD8+, FoxP3NEG CD4+, и Treg на 10 6 живых клеток в селезенке неполучавших (темно-серый столбец) или получавших mJJ64A (светло-серый столбец) мышей с опухолями. Фиг. 15Е представляет собой гистограмму, демонстрирующую число клеток CD8+, FoxP3NEG CD4+и Treg на 10 6 живых клеток в селезенке не получавших (черный столбец) или получавших mJJ64A (светло-серый столбец) мышей без опухолей.
Фиг. 16А представляет собой схематическую иллюстрацию экспериментального дизайна модели колита. Фиг. 16В представляет собой линейный график, демонстрирующий вес (г) в динамике (дни после инъекции) у мышей с колитом, получавших контроль (•), iTreg ( ), mJJ64A+iTreg (
), mJJ64A+iTreg ( ) и mJJ64A (
) и mJJ64A ( ). Фиг. 16С представляет собой линейный график, демонстрирующий нормализованный вес в динамике (дни после инъекции) у мышей с колитом, получавших контроль (•), iTreg (
). Фиг. 16С представляет собой линейный график, демонстрирующий нормализованный вес в динамике (дни после инъекции) у мышей с колитом, получавших контроль (•), iTreg ( ), mJJ64A+iTreg (
), mJJ64A+iTreg ( ) и mJJ64A (
) и mJJ64A ( ). Фиг. 16D представляет собой линейный график, демонстрирующий процент выживаемости мышей с колитом, не получавших какого-либо соединения (•), получавших iTreg (синий кружок), mJJ64A+iTreg (
). Фиг. 16D представляет собой линейный график, демонстрирующий процент выживаемости мышей с колитом, не получавших какого-либо соединения (•), получавших iTreg (синий кружок), mJJ64A+iTreg ( ) и mJJ64A (красный кружок). Ось X представляет время (дни), а ось Y представляет процент выживаемости. Фиг. 16E-I представляют собой репрезентативные фотографии мышей с колитом, не получавших какого-либо соединения (Фиг. 16E), получавших iTreg (Фиг. 16F), получавших JJa-обработанные iTreg (Фиг. 16G), не получавших какого-либо соединения (Фиг. 16H) и получавших mJJ64A (Фиг. 16I). Нижнее изображение демонстрирует выпадение прямой кишки в группах, не получавших какого-либо соединения.
) и mJJ64A (красный кружок). Ось X представляет время (дни), а ось Y представляет процент выживаемости. Фиг. 16E-I представляют собой репрезентативные фотографии мышей с колитом, не получавших какого-либо соединения (Фиг. 16E), получавших iTreg (Фиг. 16F), получавших JJa-обработанные iTreg (Фиг. 16G), не получавших какого-либо соединения (Фиг. 16H) и получавших mJJ64A (Фиг. 16I). Нижнее изображение демонстрирует выпадение прямой кишки в группах, не получавших какого-либо соединения.
Фиг. 17А представляет собой фотографию, демонстрирующую репрезентативные толстые кишки мышей, не получавших какого-либо соединения (UT), получавших iTreg, получавших mJJ64A-обработанные iTreg, получавших mJJ64A, а также толстые кишки мышей дикого типа (ДТ). На Фиг. 17В представлена гистограмма, представляющая длину и вес толстой кишки у здоровых, не получавших лечения (UT), и получавших iTreg, mJJ64A и mJJ64A+iTreg мышей. Ось X представляет группу обработки, а ось Y представляет вес/длину толстой кишки (мг/мм). На Фиг. 17C-J продемонстрированы репрезентативные гистологические срезы толстой кишки: нормальной толстой кишки мышей ДТ (Фиг. 17C), мышей Rag-/- колит- , не получавших какого-либо соединения (Фиг. 17D), нормальной толстой кишки мышей ДТ (Фиг. 17E), мышей Rag-/- колит- , не получавших какого-либо соединения (Фиг. 17F) ), мышей Rag-/- колит- , получавших iTreg (Фиг. 17G), мышей Rag-/- колит- , получавших mJJ64A (10 мг/кг) (Фиг. 17H), мышей Rag-/- колит- , получавших iTreg (Фиг. 17I) и мышей Rag-/- колит- , получавших mJJ64A (10 мг/кг) (Фиг. 17J).
Фиг. 18А представляет собой гистограмму, демонстрирующую количество CD4+ Т-клеток на 10 6 живых клеток в селезенке Rag - / - мышей ДТ, мышей UT, мышей, получавших iTreg, mJJ64A, а также мышей, получавших mJJ64A-обработанные iTreg. Ось X представляет группу обработки, а ось Y представляет количество клеток CD4+ на 10 6 живых клеток. Фиг. 18В представляет собой гистограмму, демонстрирующую процент клеток FoxP3+ на CD4+ Т-клетках в селезенке Rag-/- мышей ДТ, мышей UT, мышей, получавших iTreg, mJJ64A, а также мышей, получавших mJJ64A-обработанные iTreg. Ось X представляет группу обработки, а ось Y представляет количество клеток FoxP3+на количество клеток CD4 + . Фиг. 18С представляет собой гистограмму, демонстрирующую процент FoxP3 - клеток на количество CD4+ T-клеток в селезенке Rag-/- мышей ДТ, мышей UT, мышей, получавших iTreg, mJJ64A, а также мышей, получавших mJJ64A-обработанные iTreg. Ось X представляет группу обработки, а ось Y представляет количество FoxP3 - клеток на количество CD4+клеток. Фиг. 18D представляет собой гистограмму, демонстрирующую количество CD4+ Т-клеток на 10 6 живых клеток в лимфатическом узле Rag-/- мышей ДТ, мышей UT, мышей, получавших iTreg, mJJ64A, а также мышей, получавших mJJ64A-обработанные iTreg. Ось X представляет группу обработки, а ось Y представляет количество клеток CD4+ на 10 6 живых клеток. Фиг. 18E представляет собой гистограмму, демонстрирующую процент клеток FoxP3+ на CD4+ Т-клетках в лимфатическом узле Rag-/- мышей ДТ, мышей UT, мышей, получавших iTreg, mJJ64A, а также мышей, получавших mJJ64A-обработанные iTreg. Ось X представляет группу обработки, а ось Y представляет количество клеток FoxP3+на количество клеток CD4 + . Фиг. 18F представляет собой гистограмму, демонстрирующую процент FoxP3 - клеток на количество CD4+ T-клеток в лимфатическом узле Rag-/- мышей ДТ, мышей UT, мышей, получавших iTreg, mJJ64A, а также мышей, получавших mJJ64A-обработанные iTreg. Ось X представляет группу обработки, а ось Y представляет количество клеток FoxP3+на количество клеток CD4 + .
Фиг. 19А представляет собой схематическую иллюстрацию индукции экспериментальной модели аутоиммунного энцефаломиелита (EAE). Фиг. 19B представляет собой диаграмму, демонстрирующую критерий градации для бальной оценки тяжести EAE. Фиг. 19С представляет собой линейный график, демонстрирующий бальную оценку EAE в динамике (дни после индукции EAE) для мышей, получавших контроль (•), iTreg (синий кружок) и mJJ64A-10 ( ). Ось X представляет время (дни), а ось Y представляет бальную оценку EAE. Фиг. 19D представляет собой линейный график, демонстрирующий процент выживаемости в динамике (дни) мышей, не получавших какого-либо соединения (
). Ось X представляет время (дни), а ось Y представляет бальную оценку EAE. Фиг. 19D представляет собой линейный график, демонстрирующий процент выживаемости в динамике (дни) мышей, не получавших какого-либо соединения ( ), мышей, получавших iTreg (•), и мышей, получавших mJJ64A-10 (
), мышей, получавших iTreg (•), и мышей, получавших mJJ64A-10 ( ). Ось X представляет время (дни), а ось Y представляет процент выживаемости. Фиг. 19Е представляет собой линейный график, демонстрирующий бальную оценку EAE в динамике (дни после индукции EAE) для мышей EAE, получавших контроль (•), iTreg (♦), mJJ64A-3 (синий кружок), mJJ64A-6 (
). Ось X представляет время (дни), а ось Y представляет процент выживаемости. Фиг. 19Е представляет собой линейный график, демонстрирующий бальную оценку EAE в динамике (дни после индукции EAE) для мышей EAE, получавших контроль (•), iTreg (♦), mJJ64A-3 (синий кружок), mJJ64A-6 ( ) и mJJ64A-10 (
) и mJJ64A-10 ( ). Ось X представляет время (дни после индукции EAE), а ось Y представляет бальную оценку EAE. Фиг. 19F представляет собой линейный график, демонстрирующий процент выживаемости в динамике (дни) мышей EAE, не получавших какого-либо соединения (
). Ось X представляет время (дни после индукции EAE), а ось Y представляет бальную оценку EAE. Фиг. 19F представляет собой линейный график, демонстрирующий процент выживаемости в динамике (дни) мышей EAE, не получавших какого-либо соединения ( ), мышей, получавших iTreg (синий кружок), mJJ64A-3 (
), мышей, получавших iTreg (синий кружок), mJJ64A-3 (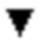 ), mJJ64A-6 (
), mJJ64A-6 ( ) и mJJ64A-10 (♦). Ось X представляет время (дни), а ось Y представляет процент выживаемости.
) и mJJ64A-10 (♦). Ось X представляет время (дни), а ось Y представляет процент выживаемости.
Фиг. 20А-С представляют собой гистограммы, демонстрирующие процент клеток FoxP3+на количество CD4+Т-клеток в селезенке (Фиг. 20А), крови (Фиг. 20В) и мозге (Фиг. 20С) EAE-мышей UT, EAE-мышей, получавших iTreg, mJJ64A-3, mJJ64A-6 и mJJ64A-10. Ось X представляет группу обработки, а ось Y представляет количество клеток FoxP3+на количество клеток CD4 + . Фиг. 20D-F представляют собой гистограммы, демонстрирующие процент клеток FoxP3 - на количество CD4+ Т-клеток в селезенке (Фиг. 20D), крови (Фиг. 20E) и мозге (Фиг. 20F) EAE-мышей UT, EAE-мышей, получавших iTreg, mJJ64A-3, mJJ64A-6 и mJJ64A-10. Ось X представляет группу обработки, а ось Y представляет количество клеток FoxP3 - на количество клеток CD4 + . Фиг. 20G-I представляют собой гистограммы, демонстрирующие процент клеток ROR+ на количество CD4+ T-клеток в селезенке (Фиг. 20G), крови (Фиг. 20H), и мозге (Фиг. 20I) EAE-мышей UT, EAE-мышей, получавших iTreg, mJJ64A-3, mJJ64A-6 и mJJ64A-10. Ось X представляет группу обработки, а ось Y представляет количество клеток ROR+ на количество клеток CD4+ .
Фиг. 21А представляет собой гистограмму, демонстрирующую процент живых iTregs человека в клетках, обработанных различными концентрациями mJJ64A. Ось X представляет группу обработки, а ось Y представляет процент живых клеток. Фиг. 21B представляет собой гистограмму, демонстрирующую процент FoxP3+CD4+ в iTreg человека, обработанных различными концентрациями mJJ64A. Ось X представляет группу обработки, а ось Y представляет процент клеток FoxP3+CD4+ .
ПОДРОБНОЕ ОПИСАНИЕ ДАННОГО ИЗОБРЕТЕНИЯ
I. Определения
Термин "стимулировать экспрессию" означает влиять на экспрессию, например, индуцировать экспрессию или активность, или индуцировать повышенную/более высокую экспрессию или активность по сравнению с нормальными здоровыми контролями.
Термины "иммуноактивирующий ответ", "активирующий иммунный ответ" и "иммуностимулирующий ответ" относятся к ответу, который инициирует, индуцирует, усиливает или повышает активацию или эффективность врожденного или адаптивного иммунитета. Такие иммунные ответы включают, например, развитие полезного гуморального (опосредованного антителами) и/или клеточного (опосредованного антиген-специфическими Т-летками или их продуктами секреции) ответа, направленного против пептида у пациента-реципиента. Такой ответ может быть активным ответом, индуцированным введением иммуногена, или пассивным ответом, индуцированным введением антитела или примированных Т-клеток. Клеточный иммунный ответ вызывается презентацией полипептидных эпитопов в ассоциации с молекулами МНС класса I или класса II с целью активации антиген-специфических CD4+Т-хелперных клеток и/или CD8+ цитотоксических Т-клеток. Ответ может также включать активацию моноцитов, макрофагов, NK-клеток, базофилов, дендритных клеток, астроцитов, клеток микроглии, эозинофилов, активацию или вовлечение нейтрофилов или других компонентов врожденного иммунитета. Наличие клеточного иммунологического ответа можно определить с помощью анализов пролиферации (CD4+ T-клетки) или CTL (цитотоксические T-лимфоциты). Относительный вклад гуморального и клеточного ответов в защитный или терапевтический эффект иммуногена можно различить, отдельно выделяя антитела и Т-клетки из иммунизированного сингенного животного и измеряя защитный или терапевтический эффект у второго субъекта.
Термины "супрессивный иммунный ответ" и "иммуносупрессивный ответ" относятся к ответу, который уменьшает или предотвращает активацию или эффективность врожденного или адаптивного иммунитета.
В данном контексте термин "иммунная толерантность" относится к любому механизму, с помощью которого потенциально вредный иммунный ответ предотвращается, подавляется или смещается к невредному иммунному ответу (Bach et al., N. Eng. J. Med., 347:911-920 (2002)).
В данном контексте термин "толерогенная вакцина", как правило, представляет собой антиген-специфический препарат, применяемый для ослабления аутореактивных Т- и/или В-клеточных ответов, оставляя при этом общую иммунную функцию без изменений.
"Иммуногенный агент" или "иммуноген" способен вызывать иммунологический ответ против себя при введении млекопитающему, необязательно в сочетании с адъювантом.
Термин "иммунная клетка" относится к клеткам врожденной и приобретенной иммунной системы, включая нейтрофилы, эозинофилы, базофилы, моноциты, макрофаги, дендритные клетки, лимфоциты, включая В-клетки, Т-клетки и естественные клетки-киллеры.
В данном контексте "типовые Т-клетки" представляют собой Т-лимфоциты, которые экспрессируют рецептор α-Т-клеток (TCR), а также корецептор CD4 или CD8. Типовые Т-клетки присутствуют в периферической крови, лимфатических узлах и тканях. См. Roberts and Girardi, “Conventional and Unconventional T Cells”, Clinical and Basic Immunodermatology, pp. 85-104, (Gaspari and Tyring (ed.)), Springer London (2008).
В данном контексте "нетиповые Т-клетки" представляют собой лимфоциты, которые экспрессируют γδ TCR и могут обычно находиться в эпителиальной среде, такой как кожа, желудочно-кишечный тракт или мочеполовой тракт. Другой подгруппой нетиповых Т-клеток является инвариантная Т-клетка - естественный киллер (NKT), которая обладает фенотипическими и функциональными возможностями типовой Т-клетки, а также особенностями естественных клеток-киллеров (например, цитолитической активностью). См. Roberts and Girardi, “Conventional and Unconventional T Cells”, Clinical and Basic Immunodermatology, pp. 85-104, (Gaspari and Tyring (ed.)), Springer London (2008).
В данном контексте термин "Treg" относится к регуляторным Т-клеткам или клеткам. Регуляторные Т-клетки представляют собой субпопуляцию Т-клеток, которые модулируют иммунную систему, поддерживают толерантность к аутоантигенам, устраняют аутоиммунные заболевания и иным образом подавляют иммуностимулирующие или активирующие реакции других клеток. Регуляторные Т-клетки бывают разных форм, наиболее изученными из которых являются те, которые экспрессируют CD4, CD25 и Foxp3.
В данном контексте термин "природная Treg" или "nTreg" относится к регуляторным Т-клеткам или клеткам, которые развиваются в тимусе.
В данном контексте термин "индуцированная Treg" или "iTreg" относится к регуляторным T-клеткам или клеткам, которые развиваются из зрелых типовых CD4+T-клеток вне тимуса.
"Биологическая активность" Akt3 относится к биологической функции полипептида Akt3. Биоактивность может быть увеличена или уменьшена путем увеличения или уменьшения активности исходных уровней полипептида, увеличения или уменьшения авидности исходных уровней полипептида, количества полипептида, соотношения Akt3 по отношению к одной или большему количеству других изоформ Akt (например, Akt1 или Akt2) полипептида, увеличивая или уменьшая уровни экспрессии полипептида (в том числе путем увеличения или уменьшения экспрессии мРНК Akt3) или их комбинации. Например, биодоступный полипептид Akt3 представляет собой полипептид, который обладает киназной активностью и может связываться и фосфорилировать субстрат Akt3. Полипептид Akt3, который не является биодоступным, включает полипептид Akt3, который неправильно локализован или неспособен связываться и фосфорилировать субстраты Akt.
В данном контексте фраза о том, что молекула "специфически связывает" или "демонстрирует специфическое связывание" с мишенью, относится к реакции связывания, которая является определяющей для присутствия молекулы в присутствии гетерогенной популяции других биологических препаратов.
При определенных условиях иммуноанализа, указанная молекула связывается преимущественно с конкретной мишенью и не связывается в значительном количестве с другими биологическими веществами, присутствующими в образце. Специфическое связывание антитела с мишенью в таких условиях требует, чтобы антитело было выбрано по его специфичности к мишени. Различные форматы иммуноанализа могут применяться для выбора антител, специфически иммунореактивных с конкретным белком. Например, твердофазный иммуноанализ ИФА обычно применяют для выбора моноклональных антител, специфически иммунореактивных с белком. См., например, Harlow and Lane (1988) Antibodies, A Laboratory Manual, Cold Spring Harbor Publications, Нью-Йорк, для описания форматов и условий иммуноанализа, которые можно применять для определения специфической иммунореактивности.
Термины "олигонуклеотид" и "полинуклеотид" обычно относятся к любому полирибонуклеотиду или полидеоксрибонуклеотиду, который может быть немодифицированной РНК или ДНК или модифицированной РНК или ДНК. Таким образом, например, термин "полинуклеотиды" в данном контексте относятся, среди прочего, к одно- и двухцепочечной ДНК, ДНК, которая представляет собой смесь одно- и двухцепочечных областей, одно- и двухцепочечной РНК, и РНК, которая представляет собой смесь из одно- и двухцепочечных областей, гибридных молекул, содержащих ДНК и РНК, которые могут быть одноцепочечными или, более типично, двухцепочечными или смесью одноцепочечных и двухцепочечных областей. Термин "нуклеиновая кислота" или "последовательность нуклеиновых кислот" также охватывает полинуклеотид, как определено выше.
Кроме того, термин "полинуклеотид" в данном контексте относится к трицепочечным областям, содержащим РНК или ДНК, или как РНК, так и ДНК. Цепи в таких областях могут быть из той же молекулы или из разных молекул. Области могут включать все из одной или большего количества молекул, но, как правило, включают только область некоторых из молекул. Одна из молекул триспиральной области часто является олигонуклеотидом.
В данном контексте термин "полинуклеотид" включает ДНК или РНК, как описано выше, которые содержат одно или большее количество модифицированных оснований. Таким образом, ДНК или РНК с каркасами, модифицированными для стабильности или по другим причинам, представляют собой "полинуклеотиды", при этом этот термин предусмотрен для применения в данном документе. Кроме того, ДНК или РНК, содержащие нетиповые основания, такие как инозин, или модифицированные основания, такие как тритилированные основания, с приведением только двух примеров, являются полинуклеотидами и охватываются этим термином, как определено в данном описании.
В данном контексте термин "полипептид" относится к цепи аминокислот любой длины независимо от модификации (например, фосфорилирование или гликозилирование). Термин полипептид включает белки и их фрагменты. Полипептиды могут быть "экзогенными", что означает, что они "гетерологичны", то есть чужеродны используемой клетке-хозяину, например, полипептид человека, продуцируемый бактериальной клеткой. Полипептиды описаны в данном документе как последовательности аминокислотных остатков. Эти последовательности пишутся слева направо в направлении от амино- к карбоксиконцу. В соответствии со стандартной номенклатурой последовательности аминокислотных остатков обозначаются трехбуквенным или однобуквенным кодом, как указано ниже: аланин (Ala, A), аргинин (Arg, R), аспарагин (Asn, N), аспарагиновая кислота (Asp, D), цистеин (Cys, C), глутамин (Gln, Q), глутаминовая кислота (Glu, E), глицин (Gly, G), гистидин (His, H), изолейцин (Ile, I), лейцин (Leu, L), лизин (Lys, K), метионин (Met, M), фенилаланин (Phe, F), пролин (Pro, P), серин (Ser, S), треонин (Thr, T), триптофан (Trp , W), тирозин (Tyr, Y) и валин (Val, V).
"Вариант" относится к полипептиду или полинуклеотиду, который отличается от эталонного полипептида или полинуклеотида, но сохраняет существенные его свойства. Типовый вариант полипептида отличается по аминокислотной последовательности от другого эталонного полипептида. Обычно различия являются ограниченными, так что последовательности эталонного полипептида и варианта в целом очень похожи и во многих областях идентичны. Вариант и эталонный полипептид могут отличаться по аминокислотной последовательности одной или большим количеством модификаций (например, заменами, добавлениями и/или делециями). Замещенный или вставленный аминокислотный остаток может быть, а может и не быть, кодирован генетическим кодом. Вариант полипептида может встречаться в природе, например, аллельный вариант, или это может быть вариант, который, как известно, не встречается в природе.
Модификации и изменения могут быть внесены в структуру полипептидов по данному изобретению и все же получить молекулу, имеющую характеристики, аналогичные полипептиду (например, консервативная аминокислотная замена). Например, некоторые аминокислоты могут быть заменены другими аминокислотами в последовательности без заметной потери активности. Поскольку именно интерактивная способность и природа полипептида определяют биологическую функциональную активность этого полипептида, некоторые замены аминокислотной последовательности могут быть осуществлены в полипептидной последовательности и, тем не менее, при этом получают полипептид с подобными свойствами.
При внесении таких изменений можно учитывать индекс гидрофобности аминокислот. Специалисты в данной области техники обычно понимают важность индекса гидрофобности аминокислот для придания интерактивной биологической функции полипептиду. Известно, что определенные аминокислоты могут быть заменены другими аминокислотами, обладающими сходным индексом или показателем гидрофобности, но при этом получают полипептид с подобной биологической активностью. Каждой аминокислоте присвоен индекс гидрофобности на основе ее гидрофобности и характеристик заряда. Эти индексы следующие: изолейцин (+4,5); валин (+4,2); лейцин (+3,8); фенилаланин (+2,8); цистеин/цистин (+2,5); метионин (+1,9); аланин (+1,8); глицин (-0,4); треонин (-0,7); серин (-0,8); триптофан (-0,9); тирозин (-1,3); пролин (-1,6); гистидин (-3,2); глутамат (-3,5); глутамин (-3,5); аспартат (-3,5); аспарагин (-3,5); лизин (-3,9) и аргинин (-4,5).
Считается, что природа относительной гидрофобности аминокислоты определяет вторичную структуру полученного полипептида, которая, в свою очередь, определяет взаимодействие полипептида с другими молекулами, такими как ферменты, субстраты, рецепторы, антитела, антигены и кофакторы. В данной области техники известно, что аминокислоту можно заменить другой аминокислотой, имеющей сходный индекс гидрофобности, и при этом получить функционально эквивалентный полипептид. При таких изменениях, замена аминокислот, индексы гидрофобности которых находятся в пределах ± 2, является предпочтительной, те индексы гидрофобности, которые находятся в пределах ± 1, являются особенно предпочтительными, а те индексы гидрофобности, которые находятся в пределах ± 0,5, являются даже более особенно предпочтительными.
Замена аналогичных аминокислот также может быть выполнена на основе гидрофильности, в частности, когда созданный таким образом биологически функциональный эквивалентный полипептид или пептид предназначен для применения в иммунологических вариантах осуществления. Аминокислотным остаткам были присвоены следующие значения гидрофильности: аргинин (+ 3,0); лизин (+ 3,0); аспартат (+ 3,0 ± 1); глутамат (+ 3,0 ± 1); серин (+ 0,3); аспарагин (+ 0,2); глютамин (+ 0,2); глицин (0); пролин (- 0,5 ± 1); треонин (- 0,4); аланин (- 0,5); гистидин (- 0,5); цистеин (- 1,0); метионин (- 1,3); валин (- 1,5); лейцин (- 1,8); изолейцин (- 1,8); тирозин (- 2,3); фенилаланин (- 2,5); триптофан (- 3,4). Специалисту в данной области техники будет понятно, что аминокислоту можно заменить другой аминокислотой, имеющей сходное значение гидрофильности, но при этом получить биологически эквивалентный и, в частности, иммунологически эквивалентный полипептид. При таких изменениях, замена аминокислот, индексы гидрофильности которых находятся в пределах ± 2, является предпочтительной, те индексы гидрофильности, которые находятся в пределах ± 1, являются особенно предпочтительными, а те индексы гидрофильности, которые находятся в пределах ± 0,5, являются даже более особенно предпочтительными.
Как указано выше, аминокислотные замены обычно основаны на относительном сходстве аминокислотных заместителей боковой цепи, например, по их гидрофобности, гидрофильности, заряду, размеру и тому подобное. Типовые замены, которые учитывают различные вышеупомянутые характеристики, хорошо известны специалистам в данной области техники и включают (исходный остаток: типовая замена): (Ala: Gly, Ser), (Arg: Lys), (Asn: Gln, His), (Asp: Glu, Cys, Ser), (Gln: Asn), (Glu: Asp), (Gly; Ala), (His: Asn, Gln), (Ile: Leu, Val), (Leu: Ile, Val), (Lys: Arg), (Met: Leu, Tyr), (Ser: Thr), (Thr: Ser), (Trp: Туr), (Туr: Trp, Phe) и (Val: Ile, Leu). Варианты осуществления данного изобретения, таким образом, предусматривают функциональные или биологические эквиваленты полипептида, как изложено выше. В частности, варианты осуществления полипептидов могут включать варианты, имеющие около 50%, 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98%, 99% или более идентичности последовательности с полипептидом, представляющим интерес.
Термин "процент (%) идентичности последовательности" определяется как процент нуклеотидов или аминокислот в кандидатной последовательности, которые идентичны нуклеотидам или аминокислотам в эталонной последовательности нуклеиновой кислоты после выравнивания последовательностей и введения гэпов, если необходимо, для достижения максимальной процентной идентичности последовательности. Выравнивание для целей определения процента идентичности аминокислотных последовательностей можно осуществить различными способами, известными специалистам в данной области техники, например, применяя общедоступное компьютерное программное обеспечение, например, программное обеспечение BLAST, BLAST-2, ALIGN, ALIGN-2 или Megalign (DNASTAR). Соответствующие параметры для измерения выравнивания, включая любые алгоритмы, необходимые для достижения максимального выравнивания по всей длине сравниваемых последовательностей, могут быть определены с помощью известных способов.
Для целей данного изобретения, % идентичности данной нуклеотидной или аминокислотной последовательности C с, по сравнению с или против данной последовательности нуклеиновой кислоты D (что в альтернативном варианте может быть сформулировано как данная аминокислотная последовательность C, которая имеет или содержит определенный % идентичности последовательности с, по сравнению с или против данной последовательности D) рассчитывается следующим образом:
100-кратное отношение W/Z
где W - количество нуклеотидов или аминокислот, которые были расценены как идентичные совпадения при выравнивании C и D с помощью программы выравнивания последовательностей, и где Z - общее количество нуклеотидов или аминокислот в D. Специалисту в данной области техники будет понятно, что если длина аминокислотной последовательности C не равна длине последовательности D, % идентичности последовательности C по отношению к D не будет равен % идентичности последовательности D по отношению к C.
Термин "носитель" относится к органическому или неорганическому ингредиенту, природному или синтетическому, с которым активный ингредиент комбинируется для облегчения применения.
Термин "фармацевтически приемлемый" означает нетоксичный материал, который не влияет на эффективность биологической активности активных ингредиентов.
Термин "фармацевтически приемлемый носитель" означает один или большее количество совместимых твердых или жидких наполнителей, разбавителей или инкапсулирующих веществ, которые подходят для введения человеку или другому позвоночному животному.
Термин "эффективное количество" или "терапевтически эффективное количество" означает дозу, достаточную для обеспечения лечения нарушения, заболевания или патологического состояния, которое подлежит лечению, или для иного обеспечения желаемого фармакологического и/или физиологического эффекта. Точная доза будет варьироваться в зависимости от множества факторов, таких как переменные, зависимые от субъекта (например, возраст, состояние иммунной системы и т. д.), заболевание и проводимое лечение.
Термины "индивидуум", "субъект" и "пациент" применяются в данном документе взаимозаменяемо и относятся к млекопитающему, включая, но не ограничиваясь ими, людей, грызунов, таких как мыши и крысы, и других лабораторных животных.
II. Композиции для активации Akt 3
В данном изобретении предлагаются композиции и способы их применения для селективной активации Akt3.
В одном варианте осуществления данного изобретения предлагается соединение формулы I:
или его фармацевтически приемлемый энантиомер, соль или сольват, где:
кольца A, B и C независимо представляют собой шестичленные арильные или N-содержащие гетероарильные моно- или бициклические кольцевые системы, содержащие ноль или большее количество N-атомов, такие как фенил, пиридин, пиримидин, пиридазин, пиразин, триазин, хинолин, хиназолин, изохинолин, нафталин, нафтиридин, индол, изоиндол, циннолин, фталазин, хиноксалин, птеридин, пурин и бензимидазол.
R1 выбирают из -(C1-C30)-алкила, -(C3-C12)-циклоалкила, -(C3-C12)-гетероциклоалкила, -(C6-C20)-арила, или -(C3-C20)-гетероарильных групп необязательно замещенных одним или большим количеством заместителей, выбранных из -(C1-C12)-алкила, -(C3-C12)-циклоалкила, -(C3-C12)-гетероциклоалкила, -O-(C1-C12)-алкила, -O-(C1-C12)-алкил-(C6-C20)-арила, -O-(C3-C12)-циклоалкила, -S-(C1-C12)-алкила, -S-(C3-C12)-циклоалкила, -COO-(C1-C12)-алкила, -COO-(C3-C12)-циклоалкила, -CONH-(C1-C12)-алкила, -CONH-(C3-C12)-циклоалкила, -CO-(C1-C12)-алкила, -CO-(C3-C12)-циклоалкила, -N-[(C1-C12)-алкил]2, -(C6-C20)-арила, -(C6-C20)-арил-(C1-C12)-алкила, -(C6-C20)-арил-O-(C1-C12)-алкила, -(C3-C20)-гетероарила, -(C3-C20)-гетероарил-(C1-C12)-алкила, -(C3-C20)-гетероарил-O-(C1-C12)-алкила, -COOH, -OH, -SH, -SO3H, -CN, -NH2, или галогена;
X, Y и Z независимо выбирают из =O, -NH, -S, -N-(C1-C30)-алкила или -(C1-C30)-арила;
R2выбирают из -(C1-C30)-алкила, =O, -OH, -SO2, -SO, или -SOCH3; и
R3 выбирают из -(C1-C30)-алкила, -(C3-C12)-циклоалкила, -(C3-C12)-гетероциклоалкила, -(C6-C20)-арила, или -(C3-C20)-гетероарильных групп, необязательно замещенных одним или большим количеством заместителей, выбранных из -(C1-C12)-алкила, -(C3-C12)-циклоалкила, -(C3-C12)-гетероциклоалкила, -O-(C1-C12)-алкила, -O-(C1-C12)-алкила-(C6-C20)-арила, -O-(C3-C12)-циклоалкила, -S-(C1-C12)-алкила, -S-(C3-C12)-циклоалкила, -COO-(C1-C12)-алкила, -COO-(C3-C12)-циклоалкила, -CONH-(C1-C12)-алкила, -CONH-(C3-C12)-циклоалкила, -CO-(C1-C12)-алкила, -CO-(C3-C12)-циклоалкила, -N-[(C1-C12)-алкил]2, -(C6-C20)-арила, -(C6-C20)-арил-(C1-C12)-алкила, -(C6-C20)-арил-O-(C1-C12)-алкила, -(C3-C20)-гетероарила, -(C3-C20)-гетероарил-(C1-C12)-алкила, -(C3-C20)-гетероарил-O-(C1-C12)-алкила, -COOH, -OH, -SH, -SO3H, -CN, -NH2, или галогена.
В другом варианте осуществления данного изобретения предлагается соединение формулы II:

или его фармацевтически приемлемый энантиомер, соль или сольват, где:
R1 выбирают из -(C1-C30)-алкила, -(C3-C12)-циклоалкила, -(C3-C12)-гетероциклоалкила, -(C6-C20)-арила, или -(C3-C20)-гетероарильных групп необязательно замещенных одним или большим количеством заместителей, выбранных из -(C1-C12)-алкила, -(C3-C12)-циклоалкила, -(C3-C12)-гетероциклоалкила, -O-(C1-C12)-алкила, -O-(C1-C12)-алкил-(C6-C20)-арила, -O-(C3-C12)-циклоалкила, -S-(C1-C12)-алкила, -S-(C3-C12)-циклоалкила, -COO-(C1-C12)-алкила, -COO-(C3-C12)-циклоалкила, -CONH-(C1-C12)-алкила, -CONH-(C3-C12)-циклоалкила, -CO-(C1-C12)-алкила, -CO-(C3-C12)-циклоалкила, -N-[(C1-C12)-алкил]2, -(C6-C20)-арила, -(C6-C20)-арил-(C1-C12)-алкила, -(C6-C20)-арил-O-(C1-C12)-алкила, -(C3-C20)-гетероарила, -(C3-C20)-гетероарил-(C1-C12)-алкила, -(C3-C20)-гетероарил-O-(C1-C12)-алкила, -COOH, -OH, -SH, -SO3H, -CN, -NH2, или галогена;
X, Y и Z независимо выбирают из -O, -NH, -S, -N-(C1-C30)-алкила или -(C1-C30)-арила;
R2 выбирают из -(C1-C30)-алкила, -O, -OH, -SO2, -SO, или -SOCH3; и
R3 выбирают из -(C1-C30)-алкила, -(C3-C12)-циклоалкила, -(C3-C12)-гетероциклоалкила, -(C6-C20)-арила, или -(C3-C20)-гетероарильных групп, необязательно замещенных одним или большим количеством заместителей, выбранных из -(C1-C12)-алкила, -(C3-C12)-циклоалкила, -(C3-C12)-гетероциклоалкила, -O-(C1-C12)-алкила, -O-(C1-C12)-алкила-(C6-C20)-арила, -O-(C3-C12)-циклоалкила, -S-(C1-C12)-алкила, -S-(C3-C12)-циклоалкила, -COO-(C1-C12)-алкила, -COO-(C3-C12)-циклоалкила, -CONH-(C1-C12)-алкила, -CONH-(C3-C12)-циклоалкила, -CO-(C1-C12)-алкила, -CO-(C3-C12)-циклоалкила, -N-[(C1-C12)-алкил]2, -(C6-C20)-арила, -(C6-C20)-арил-(C1-C12)-алкила, -(C6-C20)-арил-O-(C1-C12)-алкила, -(C3-C20)-гетероарила, -(C3-C20)-гетероарил-(C1-C12)-алкила, -(C3-C20)-гетероарил-O-(C1-C12)-алкила, -COOH, -OH, -SH, -SO3H, -CN, -NH2, или галогена.
В другом варианте осуществления данного изобретения предлагается соединение формулы III:
или его фармацевтически приемлемый энантиомер, соль или сольват, где:
R1 выбирают из -(C1-C30)-алкила, -(C3-C12)-циклоалкила, -(C3-C12)-гетероциклоалкила, -(C6-C20)-арила, или -(C3-C20)-гетероарильных групп необязательно замещенных одним или большим количеством заместителей, выбранных из -(C1-C12)-алкила, -(C3-C12)-циклоалкила, -(C3-C12)-гетероциклоалкила, -O-(C1-C12)-алкила, -O-(C1-C12)-алкил-(C6-C20)-арила, -O-(C3-C12)-циклоалкила, -S-(C1-C12)-алкила, -S-(C3-C12)-циклоалкила, -COO-(C1-C12)-алкила, -COO-(C3-C12)-циклоалкила, -CONH-(C1-C12)-алкила, -CONH-(C3-C12)-циклоалкила, -CO-(C1-C12)-алкила, -CO-(C3-C12)-циклоалкила, -N-[(C1-C12)-алкил]2, -(C6-C20)-арила, -(C6-C20)-арил-(C1-C12)-алкила, -(C6-C20)-арил-O-(C1-C12)-алкила, -(C3-C20)-гетероарила, -(C3-C20)-гетероарил-(C1-C12)-алкила, -(C3-C20)-гетероарил-O-(C1-C12)-алкила, -COOH, -OH, -SH, -SO3H, -CN, -NH2, или галогена;
X, Y и Z независимо выбирают из -O, -NH, -S, -N-(C1-C30)-алкила или -(C1-C30)-арила;
R2 выбирают из -(C1-C30)-алкила, -O, -OH, -SO2, -SO, или -SOCH3; и
R4 выбирают из -(C1-C12)-алкила, -(C3-C12)-циклоалкила, -(C3-C12)-гетероциклоалкила, -O-(C1-C12)-алкила, -O-(C1-C12)-алкил-(C6-C20)-арила, -O-(C3-C12)-циклоалкила, -S-(C1-C12)-алкила, -S-(C3-C12)-циклоалкила, -COO-(C1-C12)-алкила, -COO-(C3-C12)-циклоалкила, -CONH-(C1-C12)-алкила, -CONH-(C3-C12)-циклоалкила, -CO-(C1-C12)-алкила, -CO-(C3-C12)-циклоалкила, -N-[(C1-C12)-алкил]2, -(C6-C20)-арила, -(C6-C20)-арил-(C1-C12)-алкила, -(C6-C20)-арил-O-(C1-C12)-алкила, -(C3-C20)-гетероарила, -(C3-C20)-гетероарил-(C1-C12)-алкила, -(C3-C20)-гетероарил-O-(C1-C12)-алкила, -COOH, -OH, -SH, -SO3H, -CN, -NH2, или галогена.
В еще одном варианте осуществления данного изобретения предлагается соединение формулы IV:
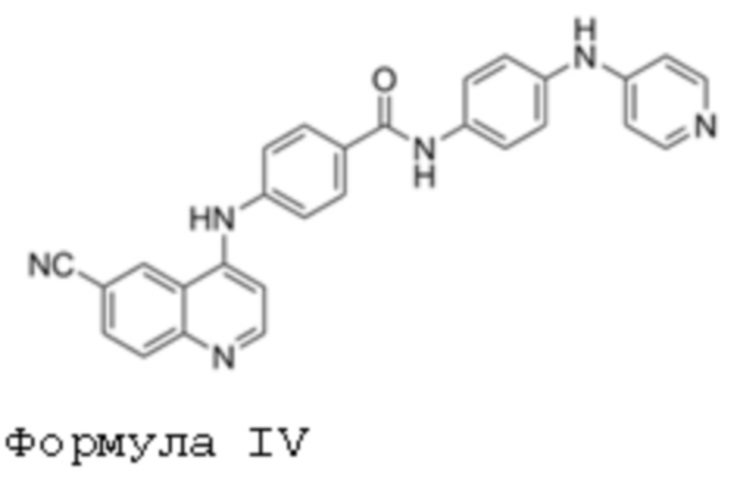
или его фармацевтически приемлемый энантиомер, соль или сольват.
Соединение формулы IV, также называемое mJJ64A, и энантиомеры, полиморфы, фармацевтически приемлемые соли и их производные можно применять для индукции, стимуляции или увеличения биологической активности Akt3 в иммунных клетках.
В некоторых вариантах осуществления данного изобретения активатор Atk3 представляет собой производное формулы I, формулы II, формулы III или формулы IV. В данном контексте термин "производное" или "дериватизированный" включает одну или большее количество химических модификаций формулы I, формулы II, формулы III или формулы IV или их энантиомера, полиморфа или их фармацевтически приемлемой соли. То есть"производное" может представлять собой функциональный эквивалент формулы I, формулы II, формулы III или формулы IV, который способен вызывать улучшенную фармакологическую функциональную активность и/или поведенческий ответ у данного субъекта. Иллюстрацией таких химических модификаций может быть замена водорода галогеновой группой, алкильной группой, ацильной группой или аминогруппой.
Химическая модификация формулы I, формулы II, формулы III или формулы IV, энантиомера, полиморфа или их фармацевтически приемлемой соли может либо усиливать, либо уменьшать водород-связывающее взаимодействие, взаимодействие с зарядом, гидрофобное взаимодействие, ван-дер-ваальсово взаимодействие или дипольное взаимодействие между указанным соединением и его мишенью.
В некоторых вариантах осуществления данного изобретения соединение формулы I, формулы II, формулы III или формулы IV может выступать в качестве модели (например, матрицы) для разработки других производных соединений, которые являются функциональным эквивалентом указанного соединения и которые способны индуцировать улучшенную фармакологическую функциональную активность и/или эффект и/или поведенческий ответ у данного субъекта.
Соединение формулы I, формулы II, формулы III или формулы IV может представлять собой рацемическое соединение и/или его оптически активные изомеры. В связи с этим некоторые из соединений могут иметь асимметричные атомы углерода и, следовательно, могут существовать либо в виде рацемических смесей, либо в виде отдельных оптических изомеров (энантиомеров). Описанные в данном документе соединения, которые содержат хиральный центр, включают все возможные стереоизомеры указанного соединения, включая композиции, включающие рацемическую смесь двух энантиомеров, а также композиции, включающие каждый энантиомер в отдельности, по существу, свободные от другого энантиомера. Так, например, в данном документе рассматривается композиция, включающая S-энантиомер соединения, по существу не содержащий R-энантиомер, или R-энантиомер, по существу не содержащий S-энантиомер. Если названное соединение включает в себя более одного хирального центра, объем данного изобретения также включает композиции, включающие смеси с различными пропорциями между диастереомерами, а также композиции, включающие один или большее количество диастереомеров, по существу не содержащих один или большее количество других диастереомеров. Под термином "по существу не содержащий" подразумевается, что композиция включает менее 25%, 15%, 10%, 8%, 5%, 3% или менее 1% минорного энантиомера или диастереомера (диастереомеров).
Akt3, также называемый RAC-гамма-серин/треонин-протеинкиназой, представляет собой фермент, который у человека кодируется геном Akt3. Известно, что Akt-киназы являются регуляторами клеточного сигналинга в ответ на инсулин и факторы роста и ассоциируются с широким спектром биологических процессов, включая пролиферацию, дифференцировку, апоптоз, онкогенез клеток, а также синтез гликогена и поглощение глюкозы. Было продемонстрировано, что Akt3 стимулируется тромбоцитарным фактором роста (PDGF), инсулином и инсулиноподобным фактором роста 1 (IGF1).
Активность киназы Akt3 опосредует сериновое и/или треониновое фосфорилирование ряда нижеразмещенных субстратов. Последовательности нуклеиновых кислот для Akt3 являются известными в данной области техники. Например, см. номер доступа в GenBank AF124141.1: мРНК протеинкиназы В гамма Homo sapiens, полные cds, что специально включено посредством ссылок в полном объеме и обеспечивает последовательность нуклеиновых кислот:
AGGGGAGTCATCATGAGCGATGTTACCATTGTGAAGGAAGGTTGGGTTCAGAAGAGGGGA
GAATATATAAAAAACTGGAGGCCAAGATACTTCCTTTTGAAGACAGATGGCTCATTCATA
GGATATAAAGAGAAACCTCAAGATGTGGATTTACCTTATCCCCTCAACAACTTTTCAGTG
GCAAAATGCCAGTTAATGAAAACAGAACGACCAAAGCCAAACACATTTATAATCAGATGT
CTCCAGTGGACTACTGTTATAGAGAGAACATTTCATGTAGATACTCCAGAGGAAAGGGAA
GAATGGACAGAAGCTATCCAGGCTGTAGCAGACAGACTGCAGAGGCAAGAAGAGGAGAGAATGAATTGTAGTCCAACTTCACAAATTGATAATATAGGAGAGGAAGAGATGGATGCCTCT
ACAACCCATCATAAAAGAAAGACAATGAATGATTTTGACTATTTGAAACTACTAGGTAAA
GGCACTTTTGGGAAAGTTATTTTGGTTCGAGAGAAGGCAAGTGGAAAATACTATGCTATG
AAGATTCTGAAGAAAGAAGTCATTATTGCAAAGGATGAAGTGGCACACACTCTAACTGAA
AGCAGAGTATTAAAGAACACTAGACATCCCTTTTTAACATCCTTGAAATATTCCTTCCAG
ACAAAAGACCGTTTGTGTTTTGTGATGGAATATGTTAATGGGGGCGAGCTGTTTTTCCAT
TTGTCGAGAGAGCGGGTGTTCTCTGAGGACCGCACACGTTTCTATGGTGCAGAAATTGTC
TCTGCCTTGGACTATCTACATTCCGGAAAGATTGTGTACCGTGATCTCAAGTTGGAGAAT
CTAATGCTGGACAAAGATGGCCACATAAAAATTACAGATTTTGGACTTTGCAAAGAAGGG
ATCACAGATGCAGCCACCATGAAGACATTCTGTGGCACTCCAGAATATCTGGCACCAGAG
GTGTTAGAAGATAATGACTATGGCCGAGCAGTAGACTGGTGGGGCCTAGGGGTTGTCATG
TATGAAATGATGTGTGGGAGGTTACCTTTCTACAACCAGGACCATGAGAAACTTTTTGAA
TTAATATTAATGGAAGACATTAAATTTCCTCGAACACTCTCTTCAGATGCAAAATCATTG
CTTTCAGGGCTCTTGATAAAGGATCCAAATAAACGCCTTGGTGGAGGACCAGATGATGCA
AAAGAAATTATGAGACACAGTTTCTTCTCTGGAGTAAACTGGCAAGATGTATATGATAAA
AAGCTTGTACCTCCTTTTAAACCTCAAGTAACATCTGAGACAGATACTAGATATTTTGAT
GAAGAATTTACAGCTCAGACTATTACAATAACACCACCTGAAAAATATGATGAGGATGGT
ATGGACTGCATGGACAATGAGAGGCGGCCGCATTTCCCTCAATTTTCCTACTCTGCAAGT
GGACGAGAATAAGTCTCTTTCATTCTGCTACTTCACTGTCATCTTCAATTTATTACTGAA
AATGATTCCTGGACATCACCAGTCCTAGCTCTTACACATAGCAGGGGCACCTTCCGACAT
CCCAGACCAGCCAAGGGTCCTCACCCCTCGCCACCTTTCACCCTCATGAAAACACACATA
CACGCAAATACACTCCAGTTTTTGTTTTTGCATGAAATTGTATCTCAGTCTAAGGTCTCA
TGCTGTTGCTGCTACTGTCTTACTATTA
(SEQ ID NO: 1)
Аминокислотные последовательности также известны в данной области техники. См., например, номер доступа UniProtKB/Swiss-Prot. Q9Y243 (Akt3_HUMAN), что специально включено посредством ссылки в полном объеме и обеспечивает аминокислотную последовательность:
MSDVTIVKEGWVQKRGEYIKNWRPRYFLLKTDGSFIGYKEKPQDVDLPYPLNNFSVAKCQ
LMKTERPKPNTFIIRCLQWTTVIERTFHVDTPEEREEWTEAIQAVADRLQRQEEERMNCS
PTSQIDNIGEEEMDASTTHHKRKTMNDFDYLKLLGKGTFGKVILVREKASGKYYAMKILK
KEVIIAKDEVAHTLTESRVLKNTRHPFLTSLKYSFQTKDRLCFVMEYVNGGELFFHLSRE
RVFSEDRTRFYGAEIVSALDYLHSGKIVYRDLKLENLMLDKDGHIKITDFGLCKEGITDA
ATMKTFCGTPEYLAPEVLEDNDYGRAVDWWGLGVVMYEMMCGRLPFYNQDHEKLFELILM
EDIKFPRTLSSDAKSLLSGLLIKDPNKRLGGGPDDAKEIMRHSFFSGVNWQDVYDKKLVP
PFKPQVTSETDTRYFDEEFTAQTITITPPEKYDEDGMDCMDNERRPHFPQFSYSASGRE
(SEQ ID NO: 2).
Доменная структура Akt3 рассматривается в публикации Romano, Scientifica, Volume 2013 (2013), ID статьи 317186, на 12 страницах, и включает в себя N-концевой домен гомологии плекстрина (PH), за которым следует каталитический домен киназы (KD) и С-концевая регуляторная гидрофобная область. Каталитический и регуляторный домены важны для биологических действий, опосредованных протеинкиназами Akt, и проявляют максимальную степень гомологии среди трех изоформ Akt. Домен PH связывает липидные субстраты, такие как фосфатидилинозитол (3,4) дифосфат (PIP2) и фосфатидилинозитол (3,4,5) трифосфат (PIP3). Сайт связывания АТФ расположен приблизительно в середине каталитического домена киназы, который имеет значительную степень гомологии с другими компонентами семейства AGC-киназ, такими как p70 S6 киназа (S6K) и p90 рибосомная S6 киназа (RSK), протеинкиназа A (PKA) и протеинкиназа B (PKB). Гидрофобный регуляторный фрагмент является типовой особенностью семейства AGC-киназ. Со ссылкой на SEQ ID NO: 2, полагают, что Akt 3 обычно имеет следующий процессинг молекулы и доменную структуру, описанную ниже.
Процессинг молекулы:
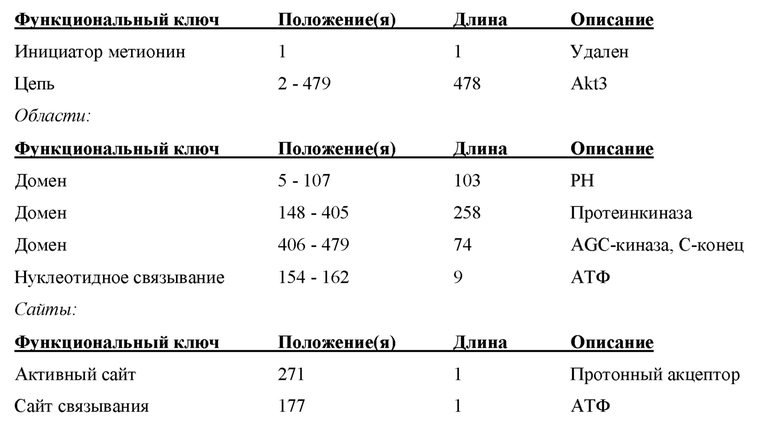
Инициатор метионин SEQ ID NO: 2 является одноразовым для функции Akt3. Следовательно, в некоторых вариантах осуществления данного изобретения указанное соединение прямо или косвенно ингибирует экспрессию или биодоступность Akt3, имеющего аминокислотную последовательность
SDVTIVKEGWVQKRGEYIKNWRPRYFLLKTDGSFIGYKEKPQDVDLPYPLNNFSVAKCQ
LMKTERPKPNTFIIRCLQWTTVIERTFHVDTPEEREEWTEAIQAVADRLQRQEEERMNCS
PTSQIDNIGEEEMDASTTHHKRKTMNDFDYLKLLGKGTFGKVILVREKASGKYYAMKILK
KEVIIAKDEVAHTLTESRVLKNTRHPFLTSLKYSFQTKDRLCFVMEYVNGGELFFHLSRE
RVFSEDRTRFYGAEIVSALDYLHSGKIVYRDLKLENLMLDKDGHIKITDFGLCKEGITDA
ATMKTFCGTPEYLAPEVLEDNDYGRAVDWWGLGVVMYEMMCGRLPFYNQDHEKLFELILM
EDIKFPRTLSSDAKSLLSGLLIKDPNKRLGGGPDDAKEIMRHSFFSGVNWQDVYDKKLVP
PFKPQVTSETDTRYFDEEFTAQTITITPPEKYDEDGMDCMDNERRPHFPQFSYSASGRE
(SEQ ID NO: 3).
Два специфических сайта, один в домене киназы (Thr-305 со ссылкой на SEQ ID NO: 2), а другой в С-концевой регуляторной области (Ser-472 со ссылкой на SEQ ID NO: 2), должны быть фосфорилированы для полной активации Akt3. Взаимодействие между PH-доменом Akt3 и TCL1A усиливает фосфорилирование и активацию Akt3. IGF-1 приводит к активации Akt3, которая может играть роль в регуляции выживания клеток.
А. Составы
В другом вариант осуществления данного изобретения предлагаются составы и фармацевтические композиции, включающие одно или большее количество соединений в соответствии с формулами I, II, III, IV или их энантиомер, полиморф или фармацевтически приемлемую соль. Как правило, уровни дозы для соединений, описанных в данном документе, составляют от около 0,0001 мг/кг веса тела до около 1000 мг/кг, более предпочтительно от 0,001 до 500 мг/кг, более предпочтительно от 0,01 до 50 мг/кг веса тела в сутки для введения млекопитающим.
1. Носитель для доставки
Соединения формул I, II, III и IV можно вводить субъекту, предпочтительно человеку, при этом их вводят в клетки субъекта с помощью или без помощи носителя для доставки. Подходящие носители для доставки описанных активных агентов известны в данной области техники и могут быть выбраны в соответствии с конкретным активным агентом. В некоторых вариантах осуществления данного изобретения указанное соединение вводят или инкапсулируют в наночастицу, микрочастицу, мицеллу, синтетическую липопротеиновую частицу или углеродную нанотрубку. Например, указанные композиции могут быть включены в носитель, такой как полимерные микрочастицы, которые обеспечивают контролируемое высвобождение активного агента (агентов). В некоторых вариантах осуществления данного изобретения высвобождение препарата (препаратов) контролируется посредством диффузии активного агента (агентов) из микрочастиц и/или разложением полимерных частиц путем гидролиза и/или ферментативного разложения. Пригодные полимеры включают этилцеллюлозу и другие природные или синтетические производные целлюлозы. Полимеры, которые медленно растворяются и образуют гель в водной среде, такие как гидроксипропилметилцеллюлоза или полиэтиленоксид, также могут быть пригодными в качестве материалов для микрочастиц, содержащих препарат. Другие полимеры включают, но не ограничиваются ими, полиангидриды, поли (сложноэфирные ангидриды), полигидроксикислоты, такие как полилактид (PLA), полигликолид (PGA), поли(лактид-со-гликолид) (PLGA), поли-3-гидроксибутират (PHB) и его сополимеры, поли-4-гидроксибутират (P4HB) и его сополимеры, поликапролактон и его сополимеры и их комбинации.
В некоторых вариантах осуществления данного изобретения соединения в соответствии с формулой I, формулой II, формулой III или формулой IV или их энантиомер, полиморф или фармацевтически приемлемая соль и второй терапевтический агент включают в одни и те же частицы и составляют для высвобождения в разное время и/или в разные периоды времени. Например, в некоторых вариантах осуществления данного изобретения один из агентов полностью высвобождается из частиц до того, как начинается высвобождение второго агента. В других вариантах осуществления данного изобретения высвобождение первого агента происходит с последующим высвобождением второго агента до того, как все количество первого агента высвободится. В других вариантах осуществления данного изобретения оба агента высвобождаются в одно и то же время в течение одного и того же периода времени или в течение различных периодов времени.
Соединения в соответствии с формулой I, формулой II, формулой III или формулой IV или их энантиомер, полиморф или фармацевтически приемлемая соль могут быть включены в носитель для доставки, полученный из материалов, которые нерастворимы в водном растворе или медленно растворимы в водном растворе , но способны разлагаться в желудочно-кишечном тракте посредством ферментативного расщепления, поверхностно-активного действия желчных кислот, и/или механической эрозии. В данном контексте термин "медленно растворимый в воде" относится к материалам, которые не растворяются в воде в течение 30 минут. Предпочтительные примеры включают жиры, жирные вещества, воски, воскоподобные вещества и их смеси. Пригодные жиры и жирные вещества включают жирные спирты (такие как лаурил, миристилстеарил, цетиловый или цетостеариловый спирт), жирные кислоты и производные, включая, но не ограничиваясь ими, сложные эфиры жирных кислот, глицериды жирных кислот (моно-, ди- и три- глицериды) и гидрогенизированные жиры. Конкретные примеры включают, но не ограничиваются этим, гидрогенизированное растительное масло, гидрогенизированное хлопковое масло, гидрогенизированное касторовое масло, гидрогенизированные масла, доступные под торговым наименованием Стеротекс (Sterotex®), стеариновую кислоту, масло какао и стеариловый спирт. Пригодные воски и воскоподобные материалы включают природные или синтетические воски, углеводороды и обычные воски.
Конкретные примеры восков включают пчелиный воск, гликовоск, касторовый воск, карнаубский воск, парафины и канделильский воск. В данном контексте, термин "воскоподобный материал" определяется как любой материал, который обычно является твердым при комнатной температуре и имеет температуру плавления от около 30 до 300°C. Точка высвобождения и/или период высвобождения могут варьироваться, как обсуждалось выше.
2. Фармацевтические композиции
В данном изобретении предлагаются фармацевтические композиции, включающие соединения в соответствии с формулой I, формулой II, формулой III или формулой IV с носителем для доставки или без него. Фармацевтические композиции могут быть составлены для введения с помощью парентерального (внутримышечного, внутрибрюшинного, внутривенного (в/в) или подкожного введения), энтерального, трансмукозального (назального, вагинального, ректального или сублингвального) или трансдермального (либо пассивного, либо с помощью ионтофореза или электропорации) путей введения или посредством применения биоразлагаемых вставок и могут быть составлены в лекарственных формах, подходящих для каждого пути введения.
В определенных вариантах осуществления данного изобретения указанные композиции вводят местно, например, путем инъекции непосредственно в участок, подлежащий лечению (например, в опухоль). В некоторых вариантах осуществления данного изобретения указанные композиции вводят инъекционно или иным образом непосредственно в сосудистую сеть сосудистой ткани, находящейся около предполагаемого участка лечения или прилегающей к нему (например, прилегающей к опухоли). Как правило, местное введение вызывает повышенную локальную концентрацию композиции, которая больше, чем та, которая может быть достигнута при системном введении.
а. Составы для парентерального введения
Соединения в соответствии с формулой I, формулой II, формулой III или формулой IV или их энантиомер, полиморф или фармацевтически приемлемая соль и их фармацевтические композиции можно вводить в водном растворе с помощью парентеральной инъекции. Указанный состав также может быть в форме суспензии или эмульсии. В общем, фармацевтические композиции предлагаются с эффективными количествами активного агента (агентов) и необязательно включают фармацевтически приемлемые разбавители, консерванты, солюбилизаторы, эмульгаторы, адъюванты и/или носители. Такие композиции включают разбавители, стерильную воду, забуференный солевой раствор с различным содержанием буфера (например, трис-HCl, ацетат, фосфат), pH и различной ионной силой; и, необязательно, добавки, такие как детергенты и солюбилизирующие агенты (например, ТВИН® 20, ТВИН® 80, также называемый полисорбатом 20 или 80), антиоксиданты (например, аскорбиновая кислота, метабисульфит натрия) и консерванты (например, тимерсол, бензиловый спирт) и наполнители (например, лактоза, маннит). Примерами неводных растворителей ли носителей являются пропиленгликоль, полиэтиленгликоль, растительные масла, такие как оливковое масло и кукурузное масло, желатин, и пригодные для инъекционного введения органические сложные эфиры, такие как этилолеат. Указанные составы могут быть лиофилизированы и повторно растворены/ресуспендированы непосредственно перед применением. Указанный состав можно стерилизовать, например, фильтрованием через задерживающий бактерии фильтр, включением стерилизующих агентов в композиции, облучением композиций или нагреванием композиций.
b. Составы для энтерального введения
Соединения в соответствии с формулой I, формулой II, формулой III или формулой IV или их энантиомер, полиморф или фармацевтически приемлемая соль могут быть составлены для энтерального введения. Пригодные пероральные лекарственные формы соединений формулы I, формулы II, формулы III или формулы IV или их энантиомера, полиморфа или фармацевтически приемлемой соли включают таблетки, капсулы, растворы, суспензии, сиропы и пастилки. Таблетки могут быть изготовлены с применением технологий прессования или формования, хорошо известных в данной области техники. Желатиновые или нежелатиновые капсулы могут быть приготовлены в виде капсул с твердой или мягкой оболочкой, которые могут инкапсулировать жидкие, твердые и полутвердые наполнители с помощью способов, хорошо известных в данной области техники.
Составы могут быть приготовлены с применением фармацевтически приемлемого носителя. В данном контексте термин "носитель" обычно включает, но не ограничивается ими, разбавители, консерванты, связующие агенты, смазывающие агенты, дезинтеграторы, агенты, вызывающие набухание, наполнители, стабилизаторы и их комбинации.
Носитель также включает все компоненты композиции для покрытия, которые могут включать пластификаторы, пигменты, красители, стабилизаторы и агенты, обеспечивающие скольжение. Дозированные составы с замедленным высвобождением могут быть приготовлены, как описано в общеизвестных источниках литературы. В этих источниках представлена информация о носителях, материалах, оборудовании и способах приготовления таблеток и капсул и лекарственных формах таблеток, капсул и гранул с замедленным высвобождением.
Примеры пригодных материалов для покрытия включают, но не ограничиваются ими, полимеры целлюлозы, такие как ацетатфталат целлюлозы, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, фталат гидроксипропилметилцеллюлозы и ацетат сукцинат гидроксипропилметилцеллюлозы; поливинилацетатфталат, полимеры и сополимеры акриловой кислоты и метакриловые смолы, которые являются коммерчески доступными под торговым названием Эудрагит (Eudragit®) (Roth Pharma, Westerstadt, Германия), зеин, шеллак и полисахариды.
Кроме того, материал для покрытия может содержать обычные носители, такие как пластификаторы, пигменты, красители, агенты, обеспечивающие скольжение, стабилизаторы, порообразователи и поверхностно-активные вещества.
Необязательные фармацевтически приемлемые вспомогательные вещества включают, но не ограничиваются ими, разбавители, связующие агенты, смазывающие агенты, дезинтегранты, красители, стабилизаторы и поверхностно-активные агенты. Разбавители, также называемые "наполнителями", как правило, необходимы для увеличения массы твердой лекарственной формы, чтобы получить приемлемый размер для прессования таблеток или формирования сфер и гранул. Пригодные разбавители включают, но не ограничиваются ими, дигидрат дикальцийфосфат, сульфат кальция, лактозу, сахарозу, маннит, сорбит, целлюлозу, микрокристаллическую целлюлозу, каолин, хлорид натрия, сухой крахмал, гидролизованные крахмалы, прежелатинизированный крахмал, диоксид кремния, оксид титана, алюмосиликат магния и сахарную пудру.
Связующие агенты применяются для придания связующих качеств твердому дозированному составу и, таким образом, гарантируют, что таблетка, сфера или гранула остаются интактными после формирования лекарственных форм. Пригодные связующие материалы включают, но не ограничиваются ими, крахмал, прежелатинизированный крахмал, желатин, сахара (включая сахарозу, глюкозу, декстрозу, лактозу и сорбит), полиэтиленгликоль, воски, природные и синтетические смолы, такие как аравийская камедь, трагакант, альгинат натрия, целлюлоза, включая гидроксипропилметилцеллюлозу, гидроксипропилцеллюлозу, этилцеллюлозу и вигум, а также синтетические полимеры, такие как сополимеры акриловой кислоты и метакриловой кислоты, сополимеры метакриловой кислоты, сополимеры метилметакрилата, сополимеры аминоалкилметакрилата, полиакриловая кислота/полиметакриловая кислота и поливинилпирролидон.
Смазывающие агенты применяются для облегчения изготовления таблеток. Примеры пригодных смазывающих агентов включают, но не ограничиваются ими, стеарат магния, стеарат кальция, стеариновую кислоту, бегенат глицерина, полиэтиленгликоль, тальк и минеральное масло.
Дезинтегранты применяются для облегчения дезинтеграции лекарственной формы или "распада" после введения и обычно включают, но не ограничиваются ими, крахмал, крахмалгликолят натрия, карбоксиметилкрахмал натрия, карбоксиметилцеллюлозу натрия, гидроксипропилцеллюлозу, прежелатинизированный крахмал, глины, целлюлозу, альгинин, смолы или перекрестно-сшитые полимеры, такие как перекрестно-сшитый PVP (Polyplasdone® XL от компании GAF Chemical Corp).
Стабилизаторы применяются для ингибирования или замедления реакций разложения лекарственного средства, которые включают, например, окислительные реакции. Пригодные стабилизаторы включают, но не ограничиваются ими, антиоксиданты, бутилированный гидрокситолуол (ВНТ); аскорбиновую кислоту, ее соли и сложные эфиры; витамин Е, токоферол и его соли; сульфиты, такие как метабисульфит натрия; цистеин и его производные; лимонную кислоту; пропилгаллат и бутилированный гидроксианизол (BHA).
Пероральные лекарственные формы, такие как капсулы, таблетки, растворы и суспензии, могут быть составлены для контролируемого высвобождения. Например, одно или большее количество соединений и необязательный один или большее количество дополнительных активных агентов могут быть составлены в виде наночастиц, микрочастиц и их комбинаций и заключены в мягкую или твердую желатиновую или нежелатиновую капсулу или диспергированы в диспергирующей среде с образованием пероральной суспензии или сиропа. Указанные частицы могут быть сформированы из препарата и полимера или матрицы с контролируемым высвобождением. В альтернативном варианте, частицы препарта могут быть покрыты одним или большим количеством покрытий с контролируемым высвобождением перед введением в готовую лекарственную форму.
В другом варианте осуществления данного изобретения одно или большее количество соединений и необязательный один или большее количество дополнительных активных агентов диспергируют в матричном материале, который превращается в гель или эмульгируется при контакте с водной средой, такой как физиологические жидкости. В случае гелей, матрица набухает, захватывая активные агенты, которые высвобождаются медленно с течением времени в результате диффузии и/или деградации матричного материала. Такие матрицы могут быть составлены в виде таблеток или наполнителей для твердых и мягких капсул.
В еще одном варианте осуществления данного изобретения одно или большее количество соединений и необязательный один или большее количество дополнительных активных агентов входят в состав проданной/твердой пероральной лекарственной формы, такой как таблетка или капсула, при этом на твердую лекарственную форму наносят одно или большее количество покрытий с контролируемым высвобождением, таких как покрытия с замедленным высвобождением или покрытия с пролонгированным высвобождением. Покрытие или покрытия также могут содержать указанные соединения и/или дополнительные активные агенты.
Лекарственные формы с пролонгированным высвобождением
Композиции с пролонгированным высвобождением обычно готовят в виде диффузионных или осмотических систем, которые известны в данной области техники. Диффузионная система обычно состоит из двух типов устройств, резервуара и матрицы и хорошо известна и описана в данной области техники. Матричные устройства обычно готовят посредством прессования препарата с медленно растворяющимся полимерным носителем в форме таблеток. Три основных типа материалов, применяемых при изготовлении матричных устройств, - это нерастворимые пластики, гидрофильные полимеры и жирные соединения. Пластиковые матрицы включают, но не ограничиваются ими, метилакрилатметилметакрилат, поливинилхлорид и полиэтилен. Гидрофильные полимеры включают, но не ограничиваются ими, целлюлозные полимеры, такие как метил- и этилцеллюлоза, гидроксиалкилцеллюлозы, такие как гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, натрий-карбоксиметилцеллюлоза и Carbopol® 934, полиэтиленоксиды и их смеси. Жирные соединения включают, но не ограничиваются ими, различные воски, такие как карнаубский воск и глицерилтристеарат, и вещества типа воска, включая гидрогенизированное касторовое масло или гидрогенизированное растительное масло, или их смеси.
В некоторых предпочтительных вариантах осуществления данного изобретения пластиковый материал представляет собой фармацевтически приемлемый акриловый полимер, включая, но не ограничиваясь этим, сополимеры акриловой кислоты и метакриловой кислоты, метилметакрилат, метилметакрилатные сополимеры, этоксиэтилметакрилаты, цианоэтилметакрилат, аминоалкилметакрилатный сополимер, поли(акриловую кислоту), поли(метакриловую кислоту), сополимер метилакриловой кислоты и алкиламина, поли(метилметакрилат), поли(метакриловую кислоту) (ангидрид), полиметакрилат, полиакриламид, поли(ангидрид метакриловой кислоты) и глицидилметакрилатные сополимеры. В определенных предпочтительных вариантах осуществления данного изобретения акриловый полимер состоит из одного или большего количества аммонийметакрилатных сополимеров. Аммонийметакрилатные сополимеры хорошо известны в данной области техники и описаны в NF XVII как полностью полимеризованные сополимеры сложных эфиров акриловой и метакриловой кислот с низким содержанием четвертичных аммониевых групп.
В одном предпочтительном варианте осуществления данного изобретения акриловый полимер представляет собой лак на основе акриловой синтетической смолы, такой как тот, который коммерчески доступен от компании Rohm Pharma под торговым названием Эудрагит (Eudragit®). В дополнительных предпочтительных вариантах осуществления данного изобретения акриловый полимер содержит смесь двух лаков на основе акриловой синтетической смолы, коммерчески доступных от компании Rohm Pharma под торговыми названиями Эудрагит RL30D (Eudragit® RL30D) и Эудрагит RS30D (Eudragit®RS30D), соответственно. Эудрагит RL30D (Eudragit® RL30D) и Эудрагит RS30D (Eudragit® RS30D) представляют собой сополимеры акриловых и метакриловых эфиров с низким содержанием четвертичных аммониевых групп, при этом молярное отношение аммониевых групп к оставшимся нейтральным (мет)акриловым эфирам составляет 1:20 в Эудрагит RL30D (Eudragit® RL30D) и 1:40 в Эудрагит RS30D (Eudragit® RS30D). Средний молекулярный вес составляет около 150000. Эудрагит S-100 (Edragit® S-100) и Эудрагит L-100 (Eudragit® L-100) также являются предпочтительными. Обозначения кода RL (высокая проницаемость) и RS (низкая проницаемость) относятся к свойствам проницаемости этих агентов. Смеси Эудрагит RL/RS (Eudragit® RL/RS) являются нерастворимыми в воде и пищеварительных соках. Однако системы, состоящие из множества частиц, образованные так, чтобы включать эти частицы, являются набухающими и проницаемыми в водных растворах и пищеварительных соках. Полимеры, описанные выше, такие как Эудрагит RL/RS (Eudragit® RL/RS), могут быть смешаны вместе в любом желаемом соотношении, чтобы в конечном итоге получить препарат с замедленным высвобождением, имеющий желаемый профиль растворения. Желаемые системы, состоящие из множества частиц, из замедленным высвобождением могут быть получены, например, из 100% Эудрагит RL (Eudragit®RL), 50% Эудрагит RL (Eudragit® RL) и 50% Эудрагит RS (Eudragit®RS), а также 10% Эудрагит RL (Eudragit®RL) и 90% ЭудрагитRS (Eudragit®RS). Специалисту в данной области техники будет понятно, что также можно применять другие акриловые полимеры, такие как, например, Эудрагит L (Eudragit®L).
В альтернативном варианте, композиции с пролонгированным высвобождением могут быть приготовлены с применением осмотических систем или путем нанесения полупроницаемого покрытия на лекарственную форму. В последнем случае желаемый профиль высвобождения препарата может быть достигнут путем комбинирования низкопроницаемых и высокопроницаемых материалов для покрытия в подходящей пропорции.
Устройства с различными механизмами высвобождения препарата, описанные выше, могут быть комбинированы в конечную лекарственную форму, содержащую одну или множество единиц. Примеры множества единиц включают, но не ограничиваются ими, многослойные таблетки и капсулы, содержащие таблетки, сферы или гранулы и т.д.Часть с немедленным высвобождением может быть добавлена в систему с пролонгированным высвобождением посредством нанесения слоя с немедленным высвобождением поверх сердцевины с пролонгированным высвобождением с использованием процесса покрытия или прессования, или в систему из множества единиц, такую как капсула, содержащая сферы с пролонгированным и немедленным высвобождением.
Таблетки с пролонгированным высвобождением, содержащие гидрофильные полимеры, готовят с помощью способов, являющихся широко известными в данной области техники, такими как процессы прямого прессования, влажного гранулирования или сухого гранулирования. Их составы обычно включают полимеры, разбавители, связующие и смазывающие агенты, а также активный фармацевтический ингредиент. Обычные разбавители включают инертные порошкообразные вещества, такие как крахмалы, порошкообразную целлюлозу, особенно кристаллическую и микрокристаллическую целлюлозу, сахара, такие как фруктоза, маннит и сахароза, зерновую муку и аналогичные пищевые порошки. Типичные разбавители включают, например, различные типы крахмала, лактозы, маннита, каолина, фосфата или сульфата кальция, неорганические соли, такие как хлорид натрия и сахарная пудра. Также являются пригодными порошкообразные производные целлюлозы. Типовые связующие агенты для таблеток включают вещества, такие как крахмал, желатин и сахара, такие как лактоза, фруктоза и глюкоза. Также можно применять природные и синтетические смолы, включая аравийскую камедь, альгинаты, метилцеллюлозу и поливинилпирролидон. Полиэтиленгликоль, гидрофильные полимеры, этилцеллюлоза и воски также можно применять в качестве связующих агентов. Смазывающий агент является необходимым в составе таблетки для предотвращения застревания таблетки и пуансона в матрице. Смазывающий агент выбирают из таких скользких твердых веществ, как тальк, стеарат магния и кальция, стеариновая кислота и гидрогенизированные растительные масла.Таблетки с пролонгированным высвобождением, содержащие восковые материалы, обычно готовят с помощью способов, известных в данной области техники, таких как способ прямого смешивания, способ кристаллизации и способ водной дисперсии. Вспособе кристаллизации, препарат смешивают с восковым материалом и либо кристаллизуют распылением, либо кристаллизуют, просеивают и обрабатывают.
Лекарственные формы с замедленным высвобождением
Композиции с замедленным высвобождением могут быть созданы путем покрытия твердой лекарственной формы полимерной пленкой, которая нерастворима в кислой среде желудка и растворима в нейтральной среде тонкой кишки.
Дозированные лекарственные формы с замедленным высвобождением могут быть получены, например, путем покрытия лекарственного средства или композиции, содержащей лекарственное средство, выбранным материалом для покрытия. Указанная лекарственная композиция может представлять собой, например, таблетку для введения в капсулу, таблетку для применения в качестве внутреннего ядра в лекарственной форме с «покрытым ядром» или множество сфер, частиц или гранул, содержащих лекарственное средство, для включения либо в таблетку, либо в капсулу. Предпочтительные материалы для покрытия включают биоразлагаемые, постепенно гидролизуемые, постепенно растворимые в воде и/или ферментативно разлагаемые полимеры и могут быть обычными "кишечнорастворимыми" полимерами. Кишечнорастворимые полимеры, как будет понятно специалистам в данной области техники, становятся растворимыми в среде с более высоким pH нижних отделов желудочно-кишечного тракта или медленно разрушаются, когда лекарственная форма проходит через желудочно-кишечный тракт, в то время как ферментативно разлагаемые полимеры разлагаются бактериальными ферментами, присутствующими в нижних отделах желудочно-кишечного тракта, особенно в толстой кишке. Пригодные материалы для покрытия, применяемые для осуществления замедленного высвобождения, включают, но не ограничиваются ими, целлюлозные полимеры, такие как гидроксипропилцеллюлоза, гидроксиэтилцеллюлоза, гидроксиметилцеллюлоза, гидроксипропилметилцеллюлоза, ацетат сукцинат гидроксипропилметилцеллюлозы, фталат гидроксипропилметилцеллюлозы, метилцеллюлоза, этилцеллюлоза, ацетат целлюлозы, фталат ацетата целлюлозы, тримеллитат ацетата целлюлозы и карбоксиметилцеллюлоза натрия; полимеры и сополимеры акриловой кислоты, предпочтительно образованные из акриловой кислоты, метакриловой кислоты, метилакрилата, этилакрилата, метилметакрилата и/или этилметакрилата и других метакриловых смол, коммерчески доступных под торговым наименованием Эудрагит (Eudragit®) (Rohm Pharma; Westerstadt, Германия) включая Эудрагит (Eudragit®) L30D-55 и L100-55 (растворимый при pH 5,5 и выше), Эудрагит (Eudragit®) L-100 (растворимый при pH 6,0 и выше), Эудрагит (Eudragit®) S (растворимый при pH 7,0 и выше, в результате чего наблюдается более высокая степень этерификации) и Эудрагит (Eudragit®) NE, RL и RS (нерастворимые в воде полимеры, имеющие различные степени проницаемости и расширяемости); виниловые полимеры и сополимеры, такие как поливинилпирролидон, винилацетат, винилацетатфталат, сополимер винилацетата и кротоновой кислоты, а также сополимер этилена и винилацетата; ферментативно разлагаемые полимеры, такие как азополимеры, пектин, хитозан, амилоза и гуаровая смола; зеин и шеллак. Также можно применять комбинации различных материалов для покрытия. Также можно наносить многослойные покрытия с применением разных полимеров.
Специалисты в данной области техники могут легко определить предпочтительный вес покрытия для конкретных материалов для покрытия путем оценки индивидуальных профилей высвобождения для таблеток, сфер и гранул, приготовленных с различными количествами различных материалов для покрытия. Именно комбинация материалов, способа и формыприменения дает желаемые характеристики высвобождения, которые можно определить только из клинических исследований.
Композиция для покрытия может включать обычные добавки, такие как пластификаторы, пигменты, красители, стабилизаторы, агенты, обеспечивающие скольжение, и т.д. Пластификатор обычно присутствует для уменьшения хрупкости покрытия, как правило, составляет от около 10 мас. % до 50 мас. % по отношению к сухой массе полимера. Примеры типичных пластификаторов включают полиэтиленгликоль, пропиленгликоль, триацетин, диметилфталат, диэтилфталат, дибутилфталат, дибутилсебацат, триэтилцитрат, трибутилцитрат, триэтилацетилцитрат, касторовое масло и ацетилированные моноглицериды. Стабилизирующий агент предпочтительно применяется для стабилизации частиц в дисперсии. Типовыми стабилизирующими агентами являются неионогенные эмульгаторы, такие как сложные эфиры сорбита, полисорбаты и поливинилпирролидон. Агенты, обеспечивающие скольжение, рекомендуются для уменьшения эффекта застревания во время формирования и высыхания пленки и, как правило, составляют приблизительно от 25 мас. % до 100 мас. % от массы полимера в растворе для покрытия. Одним из эффективных агентов, обеспечивающих скольжение, является тальк. Также можно применять другие агенты, обеспечивающие скольжение, такие как стеарат магния и моностеараты глицерина. Также могут применяться пигменты, такие как диоксид титана. В композицию для покрытия также можно добавлять небольшие количества пеногасителя, такого как силикон (например, симетикон).
с. Составы для введения в легкие и в слизистые оболочки.
Активный агент (агенты) и его композиции можно применять в составе для введения в легкие и в слизистые оболочки. Введение может включать доставку композиции в легкие, в слизистую оболочку носа, полости рта (сублингвально, буккально), влагалища или прямой кишки.
В одном варианте осуществления данного изобретения указанные соединения составляют для доставки в легкие, например, путем интраназального введения или пероральной ингаляции. Дыхательные пути представляют собой анатомическую структуру, участвующую в обмене газов между атмосферой и кровотоком. Легкие представляют собой ветвящиеся анатомические структуры, в конечном итоге оканчивающиеся альвеолами, в которых происходит обмен газов. Площадь альвеолярной поверхности является самой большой в дыхательной системе и предствляет собой место, где происходит всасывание лекарств. Альвеолы покрыты тонким эпителием без ресничек или слизистым слоем и выделяют поверхностно-активные фосфолипиды. Термин "дыхательные пути" охватывает верхние дыхательные пути, включая ротоглотку и гортань, за которыми следуют нижние дыхательные пути, которые включают трахею с последующей бифуркацией в бронхи и бронхиолы. Верхние и нижние дыхательные пути называются проводящими дыхательными путями. Терминальные бронхиолы затем делятся на дыхательные бронхиолы, которые затем приводят к конечной дыхательной зоне, альвеолам или глубоким легким. Глубокое легкое, или альвеолы, являются основной мишенью для вдыхаемых терапевтических аэрозолей при системной доставке лекарственных средств.
Существует введение в легкие терапевтических композиций, состоящих из низкомолекулярных лекарственных средств, например, бета-андрогенных антагонистов для лечения астмы. Другие терапевтические агенты, которые являются активными в легких, вводятся системно и действуют на мишень посредством легочной абсорбции. Назальная доставка рассматривается как многообещающий способ введения терапевтических средств по следующим причинам: нос имеет большую площадь поверхности, доступную для всасывания лекарственных средств, благодаря покрытию эпителиальной поверхности многочисленными микроворсинками, кроме того, субэпителиальный слой является сильно васкуляризованным, венозная кровь из носа попадает непосредственно в системный кровоток и, таким образом, предотвращает потерю лекарственного средства в результате пресистемного метаболизма в печени; такая доставка предполагает применение более низких доз, наблюдается более быстрое достижение терапевтических уровней в крови, более быстрое начало фармакологической активности, меньшее количество побочных эффектов, высокие показатели общего кровотока на см 3, наличие пористой эндотелиальной базальной мембраны, а также указанная доставка является легко доступной.
В данном контексте термин "аэрозоль" относится к любому приготовлению состава мелкодисперсных частиц, который может находиться в растворе или суспензии, независимо от того, изготавливается ли он с применением пропеллента. Аэрозоли можно изготовить с помощью стандартных способов, таких как ультразвуковая обработка или обработка под высоким давлением.
Носители для легочных композиций можно разделить на носители для сухих порошковых составов и носители для введения в виде растворов. Аэрозоли для доставки терапевтических агентов в дыхательные пути известны в данной области техники. Для введения через верхние дыхательные пути указанный состав может быть составлен в форме раствора, например, воды или изотонического солевого раствора, забуференного или небуферизованного, или в форме суспензии, для интраназального введения в форме капель или спрея. Предпочтительно, такие растворы или суспензии являются изотоническими по отношению к назальному секрету и имеют примерно одинаковое значение рН, например, от около pH 4,0 до около pH 7,4 или от pH 6,0 до pH 7,0. Буферы должны быть физиологически совместимы и включать, например, фосфатные буферы. Например, типивое назальное противоотечное средство описано как забуференное до pH около 6,2. Специалист в данной области техники может легко определить пригодное содержание солевого раствора и pH для получения безвредного водного раствора для назального введения и/или введения в верхние отделы дыхательных путей.
Предпочтительно водный раствор представляет собой воду, физиологически приемлемые водные растворы, содержащие соли и/или буферы, такие как забуференный фосфатом солевой раствор (PBS), или любой другой водный раствор, приемлемый для введения животному или человеку. Такие растворы хорошо известны специалисту в данной области техники и включают, но не ограничиваются ими, дистиллированную воду, деионизированную воду, чистую или сверхчистую воду, солевой раствор, забуференный фосфатом солевой раствор (PBS). Другие пригодные водные носители включают, но не ограничиваются ими, раствор Рингера и изотонический раствор хлорида натрия. Водные суспензии могут включать суспендирующие агенты, такие как производные целлюлозы, альгинат натрия, поливинилпирролидон и трагакантовая камедь, и смачивающий агент, такой как лецитин. Пригодные консерванты для водных суспензий включают этил и n-пропил p-гидроксибензоат.
В другом варианте осуществления данного изобретения для составов можно применять растворители, которые являются низкотоксичными органическими (то есть неводными) остаточными растворителями класса 3, например, этанол, ацетон, этилацетат, тетрагидрофуран, этиловый эфир и пропанол. Указанный растворитель выбирают на основании его способности легко аэрозолизировать состав. Реакция с участием указанного растворителя и соединений не должна иметь пагубных последствий. Следует применять пригодный растворитель, который растворяет соединения или образует суспензию соединений. Указанный растворитель должен быть достаточно летучим для образования аэрозоля раствора или суспензии. Дополнительные растворители или аэрозольные агенты, такие как фреоны, можно добавлять по желанию для повышения летучести раствора или суспензии.
В одном варианте осуществления данного изобретения композиции могут содержать незначительные количества полимеров, поверхностно-активных веществ или других вспомогательных веществ, хорошо известных специалистам в данной области техники. В этом контексте "незначительные количества" означают отсутствие вспомогательных веществ, которые могут влиять или опосредовать поглощение соединений в легких, и что присутствующие наполнители присутствуют присутствуют в количестве, которое не оказывает отрицательного влияния на поглощение соединений в легких.
Сухие липидные порошки могут быть непосредственно диспергированы в этаноле из-за их гидрофобной природы. Для липидов, хранящихся в органических растворителях, таких как хлороформ, желаемое количество раствора помещают во флакон, а хлороформ выпаривают в потоке азота с образованием сухой тонкой пленки на поверхности стеклянного флакона. Пленка легко набухает при восстановлении этанолом. С целью полного диспергирования липидной молекулы в органическом растворителе, суспензию обрабатывают ультразвуком. Неводные суспензии липидов также можно приготовить в абсолютном этаноле с помощью многоразового распылителя PARI LC Jet + (PARI Respiratory Equipment, Монтерей, штат Калифорния).
Сухие порошковые составы ("DPF") с большим размером частиц имеют улучшенные характеристики текучести, такие как меньшая агрегация, более легкая аэрозолизация и потенциально меньший фагоцитоз. Аэрозоли сухого порошка для ингаляционной терапии обычно получают со средними диаметрами, в основном в диапазоне менее 5 микрон, хотя предпочтительный диапазон составляет от одного до десяти микрон в аэродинамическом диаметре. Крупные частицы-"носители" (не содержащие препарат) доставляются вместе с терапевтическими аэрозолями, чтобы способствовать достижению эффективной аэрозолизации среди других возможных преимуществ.
Полимерные частицы можно приготовить с помощью одинарного и двойного испарения легколетучего растворителя в эмульсионной среде, распылительной сушки, экстракции растворителем, выпаривания растворителя, разделения фаз, простой и сложной коацервации, межфазной полимеризации и других способов, хорошо известных специалистам в данной области техники. Частицы могут быть получены с помощью способов изготовления микросфер или микрокапсул, известных в данной области техники. Предпочтительными способами изготовления являются распылительная сушка и сублимационная сушка, что влечет за собой применение раствора, содержащего поверхностно-активное вещество, распыление с образованием капель желаемого размера и удаление растворителя.
Указанные частицы могут быть изготовлены с помощью соответствующего материала, придания поверхности необходимой шероховатости, с определенным диаметром и плотностью утряски для локализованной доставки в выбранные области респираторного тракта, такие как глубокие участки легких или верхние дыхательные пути. Например, частицы более высокой плотности или более крупные частицы могут применяться для доставки в верхние дыхательные пути. Аналогично, смесь частиц разных размеров, снабженных одинаковыми или разными EGS, можно вводить для нацеливания на разные области легкого за одно введение.
Составы для доставки в легкие включают однослойные фосфолипидные везикулы, липосомы или липопротеиновые частицы. Составы и способы изготовления таких составов, содержащих нуклеиновую кислоту, хорошо известны специалисту в данной области техники. Липосомы формируют из коммерчески доступных фосфолипидов, поставляемых различными поставщиками, включая Avanti Polar Lipids, Inc. (Бирмингем, штат Алабама). В одном варианте осуществления данного изобретения липосома может включать молекулу лиганда, специфичную для рецептора на поверхности клетки-мишени, чтобы направлять липосому к клетке-мишени.
d. Трансдермальное введение
Также можно приготовить составы для трансдермального введения. Обычно это мази, лосьоны, спреи или пластыри, которые можно приготовить по стандартной технологии. Составы для трансдермального введения могут включать усилители проникновения.
III. Способы селективной активации Akt3
Описанные композиции для селективной активации Akt3 можно применять для модуляции иммунного ответа путем снижения супрессивной функции nTreg. В некоторых вариантах осуществления данного изобретения соединения в соответствии с формулой I, формулой II, формулой III или формулой IV или их энантиомер, полиморф или фармацевтически приемлемую соль вводят системно. В других вариантах осуществления данного изобретения соединения в соответствии с формулой I, формулой II, формулой III или формулой IV или их энантиомер, полиморф или фармацевтически приемлемую соль вводят местно или регионально. Например, в некоторых вариантах осуществления данного изобретения композиции, содержащие соединения в соответствии с формулой I, формулой II, формулой III или формулой IV, или их энантиомер, полиморф или фармацевтически приемлемая соль доставляют или специфически нацеливают на ткань или органы, нуждающиеся в модуляции. Treg можно модулировать путем нацеливания или доставки композиций в лимфатические узлы. nTreg можно модулировать путем нацеливания или специфической доставки композиций в тимус или селезенке. iTreg можно модулировать путем нацеливания или специфической доставки композиций к типовым Т-клеткам вне тимуса.
В некоторых подходах in vivo, описанные в данном документе композиции вводят субъекту в терапевтически эффективном количестве. В данном контексте термин "эффективное количество" или "терапевтически эффективное количество" означает дозу, достаточную для лечения, подавления или ослабления одного или большего количества симптомов нарушения, которое подлежит лечению, или для иного обеспечения желаемого фармакологического и/или физиологического эффекта. Точная доза будет варьироваться в зависимости от множества факторов, таких как переменные, зависимые от субъекта (например, возраст, состояние иммунной системы и т. д.), заболевание и проводимое лечение. Типовые симптомы, фармакологические и физиологические эффекты обсуждаются более подробно ниже.
В некоторых вариантах осуществления данного изобретения действие композиции на субъекта сравнивают с контролем. Например, влияние композиции на конкретный симптом, фармакологический или физиологический показатель можно сравнить с субъектом, не получавшим лечение, или состоянием субъекта до начала лечения. В некоторых вариантах осуществления данного изобретения, симптом, фармакологический или физиологический показатель оценивают у субъекта до лечения и в дальнейшем один или большее количество раз после начала лечения. В некоторых вариантах осуществления данного изобретения контроль представляет собой эталонный уровень или среднее значение, определяемое на основании измерения симптома, фармакологического или физиологического показателя у одного или большего количества субъектов, у которых нет заболевания или состояния, подлежащего лечению (например, у здоровых субъектов). В некоторых вариантах осуществления данного изобретения эффект лечения сравнивают с обычным лечением, известным в данной области техники. Например, если заболевание, подлежащее лечению, представляет собой рак, обычное лечение может представлять собой применение химиотерапевтического агента.
В некоторых вариантах осуществления данного изобретения иммуномодулирующие композиции, описанные в данном описании, вводят в комбинации с одним или большим количеством дополнительных активных агентов. Комбинированная терапия может включать введение активных агентов вместе в одной и той же смеси или в отдельных смесях. Следовательно, в некоторых вариантах осуществления данного изобретения указанная фармацевтическая композиция включает два, три или большее количество активных агентов. Фармацевтические композиции могут быть составлены в виде фармацевтической стандартной лекарственной форме, называемой стандартной лекарственной формой. Такие составы обычно включают эффективное количество одного или большего количества описанных иммуномодулирующих соединений. Разные активные агенты могут иметь одинаковые или разные механизмы действия. В некоторых вариантах осуществления данного изобретения комбинация приводит к аддитивному эффекту при лечении заболевания или нарушения. В некоторых вариантах осуществления данного изобретения комбинации приводят к более чем аддитивному эффекту при лечении заболевания или нарушения.
Предпочтительно, описанные соединения и способы применения специфически активируют активность Akt3 без увеличения или уменьшения активности Akt1, Akt2, или их комбинации.
А. Усиление иммуносупрессивных реакций и ослабление иммуностимулирующих реакций
1. Способы лечения
Описанные соединения или их энантиомер, полиморф или фармацевтически приемлемая соль являются пригодными в качестве терапевтических агентов. Иммунные клетки, предпочтительно Т-клетки, могут контактировать in vivo или ex vivo с соединениями в соответствии с формулой I, формулой II, формулой III или формулой IV или их энантиомером, полиморфом или фармацевтически приемлемой солью для снижения или ингибирования иммунных реакций, включая воспаление, но не ограничиваясь им. Т-клетки, контактирующие с соединениями в соответствии с формулой I, формулой II, формулой III или формулой IV или их энантиомером, полиморфом или фармацевтически приемлемой солью, могут представлять собой любую иммунную клетку, которая экспрессирует Akt3 или обладает активностью Akt3 и обладает способностью превращаться в Foxp3+. Типовые иммунные клетки, которые можно обрабатывать соединениями в соответствии с формулой I, формулой II, формулой III или формулой IV, или их энантиомером, полиморфом или фармацевтически приемлемой солью, включают, но не ограничиваются этим, регуляторные клетки, такие как клетки ThI, TcI Th25, Tc2, Th3, ThI 7, Th22, Treg, nTreg, iTreg и TrI, а также клетки, которые секретируют или индуцируют секрецию другими клетками воспалительных молекул, включая, но не ограничиваясь этим, ИЛ- Iβ, TNF-α TGF-бета, ИФН-γ, ИЛ-17, ИЛ-6, ИЛ-23, ИЛ-22, ИЛ-21 и MMP. Описанные соединения или их энантиомер, полиморф или фармацевтически приемлемую соль также можно применять для увеличения или стимулирования активности или продукции Treg, увеличения продукции цитокинов, таких как ИЛ-10, из Treg, повышения дифференцировки Treg, увеличения количества Treg, или повышения выживаемости Treg.
Описанные соединения или их энантиомер, полиморф или фармацевтически приемлемую соль можно применять для увеличения экспрессии FoxP3 на иммунных клетках.
В одном варианте осуществления данного изобретения предлагается способ усиления иммуного супрессивного ответа у субъекта, нуждающегося в этом, путем приведения в контакт иммунных клеток ex vivo с описанными соединениями или их энантиомером, полиморфом или фармацевтически приемлемой солью в количестве, эффективном для увеличения экспрессии FoxP3 на иммунных клетках, и введения приведенных в контакт иммунных клеток указанному субъекту. В одном варианте осуществления данного изобретения указанные иммунные клетки представляют собой аутологичные иммунные клетки. Указанные иммунные клетки могут включать Т-клетки, включая, но не ограничиваясь этим, Treg и iTreg.
В некоторых вариантах осуществления данного изобретения описанные соединения или их энантиомер, полиморф или фармацевтически приемлемую соль вводят в комбинации со вторым терапевтическим агентом. При иммунной модуляции комбинированная терапия может оказаться полезной. В некоторых вариантах осуществления данного изобретения описанные соединения или их энантиомер, полиморф или фармацевтически приемлемую соль можно применять для ослабления или реверсии активности провоспалительного препарата и/или ограничения нежелательных эффектов таких препаратов.
B. Способы лечения воспалительных реакций
В одном из вариантов осуществления данного изобретения предлагаются способы лечения или облегчения одного или большего количества симптомов воспаления. В более предпочтительном варианте осуществления данного изобретения композиции в соответствии с формулой I, формулой II, формулой III или формулой IV и описанные способы являются пригодными для лечения хронического и персистирующего воспаления. Воспаление в целом можно лечить с применением соединений в соответствии с формулой I, формулой II, формулой III или формулой IV или их энантиомера, полиморфа или фармацевтически приемлемой соли.
Иммунный ответ, включая воспаление, можно ингибировать или ослабить у субъекта, предпочтительно человека, путем введения эффективного количества описанных соединений или их энантиомера, полиморфа или фармацевтически приемлемой соли, чтобы повысить или стимулировать биологическую активность Akt3 в иммунной клетке, уменьшить количество провоспалительных молекул в месте воспаления, индуцировать или увеличить экспрессию FoxP3, индуцировать или увеличить пролиферацию iTreg, или чтобы достичь комбинаций этих эффектов. Типовые провоспалительные молекулы включают, но не ограничиваются ими, ИЛ- 1 β, TNF-α, TGF-бета, ИФН-γ, ИЛ-17, ИЛ-6, ИЛ-23, ИЛ-22, ИЛ-21 и MMP.
Соединения в соответствии с формулой I, формулой II, формулой III или формулой IV или их энантиомер, полиморф или фармацевтически приемлемая соль могут вызывать усиление супрессивного действия Treg на иммунный ответ. Treg могут супрессировать дифференцировку, пролиферацию, активность и/или продукцию и/или секрецию цитокинов клетками Th1, Th17, Th7, Th22 и/или другими клетками, которые секретируют или индуцируют секрецию другими клетками воспалительных молекул, включая, но не ограничиваясь этим, ИЛ- 1 β, TNF-α TGF-бета, ИФН-γ, ИЛ-17, ИЛ-6, ИЛ-23, ИЛ-22, ИЛ-21 и MMP. Например, соединения в соответствии с формулой I, формулой II, формулой III или формулой IV или их энантиомер, полиморф или фармацевтически приемлемая соль могут вызывать усиление супрессивного действия Treg на клетки Th1 и/или Th 17 для уменьшения продуцируемого уровня ИФН-γ и ИЛ-17, соответственно. Описанные соединения или их энантиомер, полиморф или фармацевтически приемлемая соль также могут действовать непосредственно на Treg, чтобы стимулировать или усиливать продукцию ИЛ-10, супрссировать путь Th1 и Th 17 или увеличивать количество Treg.
1. Заболевания, подлежащие лечению
Композиции, содержащие описанные соединения или их энантиомер, полиморф или фармацевтически приемлемую соль, которые избирательно повышают активность или экспрессию Akt3, могут применяться для снижения иммуностимулирующего ответа у субъекта. В некоторых вариантах осуществления данного изобретения указанные субъекты имеют воспалительное заболевание, включая, но не ограничиваясь этим, аутоиммунное заболевание.
Репрезентативные воспалительные или аутоиммунные заболевания и нарушения, которые можно лечить с помощью описанных соединений или их энантиомера, полиморфа или фармацевтически приемлемой соли или с помощью композиций, содержащих описанные соединения или их энантиомер, полиморф или фармацевтически приемлемую соль, включают, но не ограничиваются ими, ревматоидный артрит, системную красную волчанку, гнездную алопецию, анкилозирующий спондилит, антифосфолипидный синдром, аутоиммунную болезнь Аддисона, аутоиммунную гемолитическую анемию, аутоиммунный гепатит, аутоиммунное заболевание внутреннего уха, аутоиммунный лимфопролиферативный синдром (ALPS), аутоиммунную тромбоцитопеническую пурпуру (ATP), болезнь Бехчета, буллезный пемфигоид, кардиомиопатию, дерматит, ассоциированный со спру-целиакией, синдром хронической усталости и иммунодефицита, синдрома (CFIDS), хроническую воспалительную демиелинизирующую полиневропатию, рубцовый пемфигоид, холодовую агглютининовую болезнь, синдром Креста, болезнь Крона, болезнь Дего, дерматомиозит, дерматомиозит ювенильный, дискоидную волчанку, эссенциальную смешанную криоглобулинемию, фибромиалгию - фибромиозит, болезнь Грейвса, болезнь Гийена-Барре, тиреоидит Хашимото, идиопатический легочной фиброз, идиопатическую тромбоцитопеническую пурпуру (ITP), IgA-нефропатию, инсулинозависимый диабет (тип I), ювенильный артрит, болезнь Меньера, смешанное заболевание соединительной ткани, рассеяный склероз, миастению, ожирение, пузырчатку обыкновенную, пернициозную анемию, узелковый полиартериит, полихондрит, полигландулярный синдром, ревматическую полимиалгию, полимиозит и дерматомиозит, первичную агаммаглобулинемию, первичный билиарный цирроз, псориаз, феномен Рейно, синдром Рейтера, ревматическую лихорадку, саркоидоз, склеродермию, синдром Шегрена, синдром мышечной скованности, артериит Такаясу, височный артериит/гигантоклеточный артериит, язвенный колит, увеит, васкулит, витилиго и гранулематоз Вегенера.
2. Комбинированные терапевтические средства
Описанные соединения или их энантиомер, полиморф или фармацевтически приемлемую соль и их композиции можно применять отдельно или в комбинации с дополнительными терапевтическими агентами. Описанные соединения можно вводить вместе или чередовать с дополнительными терапевтическими агентами. Дополнительные терапевтические агенты включают, но не ограничиваются ими, иммуносупрессивные агенты (например, антитела против других маркеров поверхности лимфоцитов (например, CD40, альфа-4 интегрин) или против цитокинов), другие слитые белки (например, CTLA-4-Ig, абатацепт (Оренция (Orencia®)), блокаторы TNF-α, такие как TNFR-Ig, этанерцепт (Энбрел (Enbrel®)), инфликсимаб (Ремикейд (Remicade®)), цертолизумаб (Симзия (Cimzia®)) и адалимумаб (Хумира (Humira®)), циклофосфамид (CTX) (то есть Эндоксан® (Endoxan®), Цитоксан (Cytoxan®), Неосар (Neosar®), Процитокс (Procytox®), Ревиммун (Revimmune™)), метотрексат (MTX) (то есть Ревматрекс (Rheumatrex®), Трексалл (Trexall®)), белимумаб (то есть Бенлиста (Benlysta®)) или другие иммуносупрессивные препараты (например, циклоспорин А, FK506-подобные соединения, соединения рапамицина или стероиды), антипролиферативные, цитотоксические агенты или другие соединения, которые могут способствовать иммуносупрессии.
Дополнительные иммуносупрессивные агенты включают, но не ограничиваются ими, преднизон, будесонид, преднизолон, циклоспорин, такролимус, сиролимус, эверолимус, азатиоприн, лефлуномид, микофенолат, анакинра, голимумаб, иксекизумаб, натализумаб, ритуксимаб, секукинумаб, тоцилизумаб, устекинумаб, ведолизумаб, базиликсимаб, даклизумаб, муромонаб, или их комбинации.
В одном вариант осуществления данного изобретения предлагается дополнительный терапевтический агент, который функционирует для ингибирования или снижения активации Т-клеток посредством отдельного пути. В одном таком варианте осуществления данного изобретения дополнительный терапевтический агент представляет собой слитый белок CTLA-4, такой как CTLA-4-Ig (абатацепт). Слитые белки CTLA-4-Ig конкурируют с костимуляторным рецептором, CD28, на Т-клетках за связывание с CD80/CD86 (B7-1/B7-2) на антигенпрезентирующих клетках и, таким образом, функционируют для ингибирования активации Т-клеток. В другом варианте осуществления данного изобретения дополнительный терапевтический агент представляет собой слитый белок CTLA-4-Ig, известный как белатацепт. Белатацепт содержит две аминокислотные замены (L104E и A29Y), которые заметно увеличивают его авидность к CD86 in vivo. В другом варианте осуществления данного изобретения дополнительный терапевтический агент представляет собой Maxy-4.
В другом варианте осуществления данного изобретения второй терапевтический агент представляет собой циклофосфамид (CTX). Циклофосфамид (общее название для
Эндоксан (Endoxan®), Цитоксан (Cytoxan®), Неосар (Neosar®), Процитокс (Procytox®), Ревиммун (Revimmune ™)), также известный как цитофосфан, является алкилирующим агентом мустаргена из группы оксазофоринов. Препарат применяется для лечения различных видов рака и некоторых аутоиммунных заболеваний. В другом варианте осуществления данного изобретения соединения формулы I или их энантиомер, полиморф или фармацевтически приемлемую соль и CTX вводят совместно в эффективном количестве для ингибирования, ослабления симптомов или лечения хронического аутоиммунного заболевания или нарушения, такого как системная красная волчанка (SLE) .
В другом варианте осуществления данного изобретения второй терапевтический агент предпочтительно применяют для лечения хронического воспаления, при этом схема лечения нацелена как на острое, так и на хроническое воспаление.
В другом варианте осуществления данного изобретения композиции в соответствии с формулой I, формулой II, формулой III или формулой IV, или их энантиомер, полиморф или фармацевтически приемлемую соль применяют в комбинации, с чередованием или в последовательности с соединениями, которые повышают активность или продукцию Treg. Типовые агенты, усиливающие Treg, включают, но не ограничиваются ими, глюкокортикоид флутиказон, сальметерол, антитела к ИЛ-12, ИФН-γ и ИЛ-4; витамин D3 и дексаметазон, а также их комбинации.
Антитела к другим провоспалительным молекулам также можно применять в комбинации или с чередовании с описанными соединениями в соответствии с формулой I, формулой II, формулой III или формулой IV или их энантиомером, полиморфом или фармацевтически приемлемой солью, слитыми белками или их фрагментами . Предпочтительные антитела связываются с ИЛ-6, ИЛ-23, ИЛ-22 или ИЛ-21.
В другом варианте осуществления данного изобретения предлагается способ лечения отторжения трансплантата путем введения субъекту, нуждающемуся в этом, эффективного количества описанных соединений в соответствии с формулой I, формулой II, формулой III или формулой IV или их энантиомера, полиморфа или фармацевтически приемлемой соли, с целью увеличения экспрессии FoxP3 на иммунных клетках.
В другом варианте осуществления данного изобретения предлагается способ лечения болезни "трансплантат против хозяина" путем введения субъекту, нуждающемуся в этом, эффективного количества описанных соединений в соответствии с формулой I, формулой II, формулой III или формулой IV или их энантиомера, полиморфа или фармацевтически приемлемой соли с целью увеличения экспрессии FoxP3 на иммунных клетках.
В еще одном варианте осуществления данного изобретения предлагается способ ингибирования или уменьшения отторжения трансплантата у нуждающегося в этом хозяина путем введения нуждающемуся в этом субъекту эффективного количества описанных соединений или их энантиомера, полиморфа или фармацевтически приемлемой соли с целью увеличения экспрессии FoxP3 на иммунных клетках.
В другом варианте осуществления данного изобретения предлагается способ лечения хронической инфекции путем введения субъекту, нуждающемуся в этом, эффективного количества описанных соединений в соответствии с формулой I, формулой II, формулой III или формулой IV или их энантиомера, полиморфа или фармацевтически приемлемой соли, с целью увеличения экспрессии FoxP3 на иммунных клетках.
В одном варианте осуществления данного изобретения предлагается способ лечения ожирения путем введения субъекту, нуждающемуся в этом, эффективного количества описанных соединений в соответствии с формулой I, формулой II, формулой III или формулой IV или их энантиомера, полиморфа или фармацевтически приемлемой соли с целью повышения активности Akt3. Не желая быть связанными какой-либо одной теорией, полагают, что Akt3 регулирует адипогенез и что дисрегуляция сигналинга Akt3 может привести к усилению адипогенеза, ожирению и резистентности к инсулину.
IV. Наборы
В данном документе также описаны медицинские наборы. Медицинские наборы могут включать, например, предоставаление дозы описанных соединений или их энантиомера, полиморфа или фармацевтически приемлемой соли или их композиций. Описанные соединения или их энантиомер, полиморф или фармацевтически приемлемая соль или их композиции могут поставляться отдельно (например, лиофилизированными) или в фармацевтической композиции. Описанные соединения или их энантиомер, полиморф или фармацевтически приемлемая соль или их композиции могут быть в стандартной дозе или в объеме, который следует разбавить перед введением. В некоторых вариантах осуществления данного изобретения указанный набор включает в себя предоставление фармацевтически приемлемого носителя. Указанный набор также может включать устройства для введения активного агента (агентов) или композиции (композиций), например, шприцы и иглы. Указанные наборы могут включать печатные инструкции относительно введения описанных соединений при применении, как описано выше.
Примеры
Пример 1: mJJ64A значительно увеличивает экспрессию FoxP3 на iTreg.
Результаты
Полученные данные демонстрируют, что mJJ64A значительно увеличивал экспрессию FoxP3 на iTreg и несущественно увеличивал пролиферацию iTreg (Фиг. 2A-2H).
Пример 2: mJJ64A увеличивает экспрессию FoxP3 при добавлении во время индукции iTreg.
Результаты
Полученные данные демонстрируют, что mJJ64A увеличивает экспрессию FoxP3 при добавлении во время индукции iTreg (Фиг. 3A и 3B).
Пример 3: Akt3 специфически регулирует оба типа Treg: nTreg и iTreg.
Результаты
Полученные данные демонстрируют, что Akt3 является ключевым регулятором nTreg (Фиг. 4A-4F). Супрессирующая активность Treg у мышей Akt3 KO была обусловлена снижением уровней ингибирующих цитокинов ИЛ-10 и TGFβ (Фиг. 4E и 4F). Полученные данные также демонстрируют, что в отсутствие Akt3, но не других изоформ, супрессирующая активность Treg нарушалась in vivo (Фиг. 5A-5B). Treg от мышей Akt3 KO продемонстрировали нарушение супрессивной активности в модели колита RAG (Фиг. 5А). Кроме того, адоптивный перенос Treg от мышей Akt3 KO мышам, имеющим Treg-деплетированную опухоль, демонстрирует нарушение супрессии противоопухолевого иммунитета (Фиг. 5B).
Полученные данные также продемонстрировали, что Akt3 был ключевым регулятором iTreg (Фиг. 6A-6E). РНК Akt3, белок и фосфорилирование Akt3 активировались в iTreg (Фиг. 6А-6С). У мышей Akt3 KO конверсия клеток Tconv в iTreg значительно ингибировалась (Фиг. 6D). Кроме того, нокдаун Akt3 из клеток ДТ Tconv отменяет индукцию FoxP3 в ответ на TGFβ (Фиг. 6 E).
Фиг. 7A-I демонстрируют, что нокина Akt3 было достаточно, чтобы индуцировать Treg, как продемонстрировано активацией FoxP3.
Пример 4: mJJ64A повышает фосфорилирование Akt3 в клетках карциномы яичника человека.
Результаты
Полученные данные демонстрируют, что mJJ64A значительно повышает фосфорилирование Akt3, но не Akt1 или Akt2 в клетках карциномы яичника человека (Фиг. 8)
Пример 5: mJJ64A усиливает FoxP3 и Akt3 в клетках Tconv во время индукции iTreg.
Результаты
Полученные данные демонстрируют, что в результате воздействия mJJ64A увеличивалась экспрессия FoxP3 и Akt3 в клетках Tconv во время индукции iTreg (Фиг. 9A-9B).
Пример 6: mJJ64A увеличивает пролиферацию iTreg и nTreg
Результаты
В результате воздействия mJJ64A увеличивалась пролиферация iTreg (Фиг. 10A - 10C) и nTreg (Фиг. 10D - 10F), но не относящихся к Treg CD4 (Фиг. 10G - 10I) и CD8 (Фиг. 10J - 10L) Т-клеток.
Пример 7: mJJ64A увеличивает супрессивную функцию iTreg и nTreg мыши.
Результаты
На Фиг. 11А - 11D продемонстрировано, что в результате воздействия mJJ64A усиливалась супрессивная функция клеток iTreg мыши in vitro. В результате воздействия mJJ64A также повышалась супрессивная функция клеток nTreg мыши in vitro и увеличивалась пролиферация nTreg, без влияния на их жизнеспособность (Фиг. 12A - 12H).
Пример 8: mJJ64A усиливает продукцию ИЛ-10 посредством nTreg.
Результаты
Полученные данные демонстрируют, что в результате воздействия mJJ64A увеличивалась продукция ИЛ-10 клетками nTreg (Фиг. 13A - 13B).
Пример 9: mJJ64A увеличивает рост опухоли TC-1 и значительно увеличивает количество Treg в опухолях и селезенке пролеченных мышей.
Результаты
Полученные данные демонстрируют, что у мышей с опухолями TC-1, получавших mJJ64A, наблюдался значительно больший рост опухоли по сравнению с контролями, не получавшими лечения (Фиг. 14A и 14B). mJJ64A также увеличивал количество Treg в опухолях и селезенке пролеченных мышей по сравнению с контролями, не получавшими лечения (Фиг. 15D и 15E). Воздействие mJJ64A не влияло на опухолевую инфильтрацию CD8+ и FoxP3NEG CD4 T-клеток (Фиг. 15A - 15C).
Пример 10: mJJ64A защищает от экспериментального колита.
Результаты
Полученные данные демонстрируют, что воздействие mJJ64A защищало от экспериментального колита (Фиг. 16A - 16I и Фиг. 17A - 17J). Кроме того, введение мышам iTreg, обработанных mJJ64A ex vivo , также обеспечивало защиту от экспериментального колита (Фиг. 16A - 16I и Фиг. 17A - 17J).
Пример 11: mJJ64A увеличивает процент Treg у Rag-/- мышей.
Результаты
Полученные данные демонстрируют, что введение Rag-/- мышам mJJ64A увеличивало процент Treg в селезенке и брыжеечных лимфатических узлах по сравнению с Rag-/- мышами, не получавшими лечения (Фиг. 18A - F).
Пример 12. Эффективность mJJ64A в мышиной EAE-модели.
Результаты
mJJ64A замедлял прогрессирование заболевания и увеличивал выживаемость в экспериментальной модели аутоиммунного энцефаломиелита (EAE) у мышей (Фиг. 19A - 19F). Кроме того, mJJ64A-индуцированные iTreg также замедляли прогрессирование заболевания и повышали выживаемость в модели EAE по сравнению с контролями, не получавшими лечения (Фиг. 19).
Пример 13: mJJ64A повышает индукцию iTreg, не влияя на жизнеспособность клеток.
Результаты
Полученные данные демонстрируют, что mJJ64A индуцировал iTreg человека (Фиг. 21B), но не влиял на жизнеспособность клеток (Фиг. 21A).
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> Augusta University Research Institute, Inc
Khleif, Samir N
Mkrtichyan, Mikayel
<120> СПЕЦИФИЧЕСКИЙ АКТИВАТОР AKT3 И ЕГО ПРИМЕНЕНИЕ
<130> 064466.070
<150> 62/555,141
<151> 2017-09-07
<150> 62/657,345
<151> 2018-04-13
<150> 62/659,870
<151> 2018-04-19
<160> 3
<170> PatentIn версия 3.5
<210> 1
<211> 1708
<212> ДНК
<213> Homo sapiens
<400> 1
aggggagtca tcatgagcga tgttaccatt gtgaaggaag gttgggttca gaagagggga 60
gaatatataa aaaactggag gccaagatac ttccttttga agacagatgg ctcattcata 120
ggatataaag agaaacctca agatgtggat ttaccttatc ccctcaacaa cttttcagtg 180
gcaaaatgcc agttaatgaa aacagaacga ccaaagccaa acacatttat aatcagatgt 240
ctccagtgga ctactgttat agagagaaca tttcatgtag atactccaga ggaaagggaa 300
gaatggacag aagctatcca ggctgtagca gacagactgc agaggcaaga agaggagaga 360
atgaattgta gtccaacttc acaaattgat aatataggag aggaagagat ggatgcctct 420
acaacccatc ataaaagaaa gacaatgaat gattttgact atttgaaact actaggtaaa 480
ggcacttttg ggaaagttat tttggttcga gagaaggcaa gtggaaaata ctatgctatg 540
aagattctga agaaagaagt cattattgca aaggatgaag tggcacacac tctaactgaa 600
agcagagtat taaagaacac tagacatccc tttttaacat ccttgaaata ttccttccag 660
acaaaagacc gtttgtgttt tgtgatggaa tatgttaatg ggggcgagct gtttttccat 720
ttgtcgagag agcgggtgtt ctctgaggac cgcacacgtt tctatggtgc agaaattgtc 780
tctgccttgg actatctaca ttccggaaag attgtgtacc gtgatctcaa gttggagaat 840
ctaatgctgg acaaagatgg ccacataaaa attacagatt ttggactttg caaagaaggg 900
atcacagatg cagccaccat gaagacattc tgtggcactc cagaatatct ggcaccagag 960
gtgttagaag ataatgacta tggccgagca gtagactggt ggggcctagg ggttgtcatg 1020
tatgaaatga tgtgtgggag gttacctttc tacaaccagg accatgagaa actttttgaa 1080
ttaatattaa tggaagacat taaatttcct cgaacactct cttcagatgc aaaatcattg 1140
ctttcagggc tcttgataaa ggatccaaat aaacgccttg gtggaggacc agatgatgca 1200
aaagaaatta tgagacacag tttcttctct ggagtaaact ggcaagatgt atatgataaa 1260
aagcttgtac ctccttttaa acctcaagta acatctgaga cagatactag atattttgat 1320
gaagaattta cagctcagac tattacaata acaccacctg aaaaatatga tgaggatggt 1380
atggactgca tggacaatga gaggcggccg catttccctc aattttccta ctctgcaagt 1440
ggacgagaat aagtctcttt cattctgcta cttcactgtc atcttcaatt tattactgaa 1500
aatgattcct ggacatcacc agtcctagct cttacacata gcaggggcac cttccgacat 1560
cccagaccag ccaagggtcc tcacccctcg ccacctttca ccctcatgaa aacacacata 1620
cacgcaaata cactccagtt tttgtttttg catgaaattg tatctcagtc taaggtctca 1680
tgctgttgct gctactgtct tactatta 1708
<210> 2
<211> 479
<212> БЕЛОК
<213> Homo sapiens
<400> 2
Met Ser Asp Val Thr Ile Val Lys Glu Gly Trp Val Gln Lys Arg Gly
1. 5 10 15
Glu Tyr Ile Lys Asn Trp Arg Pro Arg Tyr Phe Leu Leu Lys Thr Asp
20 25 30
Gly Ser Phe Ile Gly Tyr Lys Glu Lys Pro Gln Asp Val Asp Leu Pro
35 40 45
Tyr Pro Leu Asn Asn Phe Ser Val Ala Lys Cys Gln Leu Met Lys Thr
50 55 60
Glu Arg Pro Lys Pro Asn Thr Phe Ile Ile Arg Cys Leu Gln Trp Thr
65 70 75 80
Thr Val Ile Glu Arg Thr Phe His Val Asp Thr Pro Glu Glu Arg Glu
85 90 95
Glu Trp Thr Glu Ala Ile Gln Ala Val Ala Asp Arg Leu Gln Arg Gln
100 105 110
Glu Glu Glu Arg Met Asn Cys Ser Pro Thr Ser Gln Ile Asp Asn Ile
115 120 125
Gly Glu Glu Glu Met Asp Ala Ser Thr Thr His His Lys Arg Lys Thr
130 135 140
Met Asn Asp Phe Asp Tyr Leu Lys Leu Leu Gly Lys Gly Thr Phe Gly
145 150 155 160
Lys Val Ile Leu Val Arg Glu Lys Ala Ser Gly Lys Tyr Tyr Ala Met
165 170 175
Lys Ile Leu Lys Lys Glu Val Ile Ile Ala Lys Asp Glu Val Ala His
180 185 190
Thr Leu Thr Glu Ser Arg Val Leu Lys Asn Thr Arg His Pro Phe Leu
195 200 205
Thr Ser Leu Lys Tyr Ser Phe Gln Thr Lys Asp Arg Leu Cys Phe Val
210 215 220
Met Glu Tyr Val Asn Gly Gly Glu Leu Phe Phe His Leu Ser Arg Glu
225 230 235 240
Arg Val Phe Ser Glu Asp Arg Thr Arg Phe Tyr Gly Ala Glu Ile Val
245 250 255
Ser Ala Leu Asp Tyr Leu His Ser Gly Lys Ile Val Tyr Arg Asp Leu
260 265 270
Lys Leu Glu Asn Leu Met Leu Asp Lys Asp Gly His Ile Lys Ile Thr
275 280 285
Asp Phe Gly Leu Cys Lys Glu Gly Ile Thr Asp Ala Ala Thr Met Lys
290 295 300
Thr Phe Cys Gly Thr Pro Glu Tyr Leu Ala Pro Glu Val Leu Glu Asp
305 310 315 320
Asn Asp Tyr Gly Arg Ala Val Asp Trp Trp Gly Leu Gly Val Val Met
325 330 335
Tyr Glu Met Met Cys Gly Arg Leu Pro Phe Tyr Asn Gln Asp His Glu
340 345 350
Lys Leu Phe Glu Leu Ile Leu Met Glu Asp Ile Lys Phe Pro Arg Thr
355 360 365
Leu Ser Ser Asp Ala Lys Ser Leu Leu Ser Gly Leu Leu Ile Lys Asp
370 375 380
Pro Asn Lys Arg Leu Gly Gly Gly Pro Asp Asp Ala Lys Glu Ile Met
385 390 395 400
Arg His Ser Phe Phe Ser Gly Val Asn Trp Gln Asp Val Tyr Asp Lys
405 410 415
Lys Leu Val Pro Pro Phe Lys Pro Gln Val Thr Ser Glu Thr Asp Thr
420 425 430
Arg Tyr Phe Asp Glu Glu Phe Thr Ala Gln Thr Ile Thr Ile Thr Pro
435 440 445
Pro Glu Lys Tyr Asp Glu Asp Gly Met Asp Cys Met Asp Asn Glu Arg
450 455 460
Arg Pro His Phe Pro Gln Phe Ser Tyr Ser Ala Ser Gly Arg Glu
465 470 475
<210> 3
<211> 478
<212> БЕЛОК
<213> Homo sapiens
<400> 3
Ser Asp Val Thr Ile Val Lys Glu Gly Trp Val Gln Lys Arg Gly Glu
1. 5 10 15
Tyr Ile Lys Asn Trp Arg Pro Arg Tyr Phe Leu Leu Lys Thr Asp Gly
20 25 30
Ser Phe Ile Gly Tyr Lys Glu Lys Pro Gln Asp Val Asp Leu Pro Tyr
35 40 45
Pro Leu Asn Asn Phe Ser Val Ala Lys Cys Gln Leu Met Lys Thr Glu
50 55 60
Arg Pro Lys Pro Asn Thr Phe Ile Ile Arg Cys Leu Gln Trp Thr Thr
65 70 75 80
Val Ile Glu Arg Thr Phe His Val Asp Thr Pro Glu Glu Arg Glu Glu
85 90 95
Trp Thr Glu Ala Ile Gln Ala Val Ala Asp Arg Leu Gln Arg Gln Glu
100 105 110
Glu Glu Arg Met Asn Cys Ser Pro Thr Ser Gln Ile Asp Asn Ile Gly
115 120 125
Glu Glu Glu Met Asp Ala Ser Thr Thr His His Lys Arg Lys Thr Met
130 135 140
Asn Asp Phe Asp Tyr Leu Lys Leu Leu Gly Lys Gly Thr Phe Gly Lys
145 150 155 160
Val Ile Leu Val Arg Glu Lys Ala Ser Gly Lys Tyr Tyr Ala Met Lys
165 170 175
Ile Leu Lys Lys Glu Val Ile Ile Ala Lys Asp Glu Val Ala His Thr
180 185 190
Leu Thr Glu Ser Arg Val Leu Lys Asn Thr Arg His Pro Phe Leu Thr
195 200 205
Ser Leu Lys Tyr Ser Phe Gln Thr Lys Asp Arg Leu Cys Phe Val Met
210 215 220
Glu Tyr Val Asn Gly Gly Glu Leu Phe Phe His Leu Ser Arg Glu Arg
225 230 235 240
Val Phe Ser Glu Asp Arg Thr Arg Phe Tyr Gly Ala Glu Ile Val Ser
245 250 255
Ala Leu Asp Tyr Leu His Ser Gly Lys Ile Val Tyr Arg Asp Leu Lys
260 265 270
Leu Glu Asn Leu Met Leu Asp Lys Asp Gly His Ile Lys Ile Thr Asp
275 280 285
Phe Gly Leu Cys Lys Glu Gly Ile Thr Asp Ala Ala Thr Met Lys Thr
290 295 300
Phe Cys Gly Thr Pro Glu Tyr Leu Ala Pro Glu Val Leu Glu Asp Asn
305 310 315 320
Asp Tyr Gly Arg Ala Val Asp Trp Trp Gly Leu Gly Val Val Met Tyr
325 330 335
Glu Met Met Cys Gly Arg Leu Pro Phe Tyr Asn Gln Asp His Glu Lys
340 345 350
Leu Phe Glu Leu Ile Leu Met Glu Asp Ile Lys Phe Pro Arg Thr Leu
355 360 365
Ser Ser Asp Ala Lys Ser Leu Leu Ser Gly Leu Leu Ile Lys Asp Pro
370 375 380
Asn Lys Arg Leu Gly Gly Gly Pro Asp Asp Ala Lys Glu Ile Met Arg
385 390 395 400
His Ser Phe Phe Ser Gly Val Asn Trp Gln Asp Val Tyr Asp Lys Lys
405 410 415
Leu Val Pro Pro Phe Lys Pro Gln Val Thr Ser Glu Thr Asp Thr Arg
420 425 430
Tyr Phe Asp Glu Glu Phe Thr Ala Gln Thr Ile Thr Ile Thr Pro Pro
435 440 445
Glu Lys Tyr Asp Glu Asp Gly Met Asp Cys Met Asp Asn Glu Arg Arg
450 455 460
Pro His Phe Pro Gln Phe Ser Tyr Ser Ala Ser Gly Arg Glu
465 470 475
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ 3-(5-АМИНО-1-ОКСОИЗОИНДОЛИН-2-ИЛ)ПИПЕРИДИН-2,6-ДИОНА И ИХ ПРИМЕНЕНИЕ В ЛЕЧЕНИИ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С БЕЛКОМ С "ЦИНКОВЫМИ ПАЛЬЦАМИ" 2 СЕМЕЙСТВА IKAROS (IKZF2) | 2019 |
|
RU2815714C2 |
| КОНЬЮГАТЫ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО, ВКЛЮЧАЮЩИЕ АНТИТЕЛО ПРОТИВ ЧЕЛОВЕЧЕСКОГО DLK1, И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2801630C2 |
| ПРОИЗВОДНЫЕ 3-(5-ГИДРОКСИ-1-ОКСОИЗОИНДОЛИН-2-ИЛ) ПИПЕРИДИН-2,6-ДИОНА И ИХ ПРИМЕНЕНИЕ В ЛЕЧЕНИИ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С БЕЛКОМ С "ЦИНКОВЫМИ ПАЛЬЦАМИ" 2 (IKZF2) СЕМЕЙСТВА IKAROS | 2019 |
|
RU2797559C2 |
| КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ РАКА С ПРИМЕНЕНИЕМ АНТАГОНИСТОВ, СВЯЗЫВАЮЩИХСЯ С КОМПОНЕНТОМ СИГНАЛЬНОГО ПУТИ PD-1, И ИНГИБИТОРОВ MEK | 2015 |
|
RU2733735C2 |
| ПРОИЗВОДНЫЕ КАЛИХЕАМИЦИНА И ИХ КОНЪЮГАТЫ "АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО" | 2018 |
|
RU2732568C1 |
| СПОСОБЫ, КОМПОЗИЦИИ И ИМПЛАНТИРУЕМЫЕ ЭЛЕМЕНТЫ, СОДЕРЖАЩИЕ АКТИВНЫЕ КЛЕТКИ | 2018 |
|
RU2826206C2 |
| СПОСОБЫ И МАТЕРИАЛЫ ДЛЯ ПОВЫШЕНИЯ УРОВНЕЙ ПОЛИПЕПТИДА ФАКТОРА ТРАНСКРИПЦИИ EB | 2020 |
|
RU2838857C2 |
| СОЕДИНЕНИЯ АЗАЛАКТАМА В КАЧЕСТВЕ ИНГИБИТОРОВ HPK1 | 2021 |
|
RU2819642C1 |
| ЛЕКАРСТВЕННЫЙ КОНЪЮГАТ ПРОИЗВОДНОГО ЭРИБУЛИНА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ЕГО ПРИМЕНЕНИЕ В МЕДИЦИНЕ | 2021 |
|
RU2830242C1 |
| КОНЪЮГАТЫ СКОНСТРУИРОВАННЫХ АНТИТЕЛ С ЦИСТЕИНОВЫМИ ЗАМЕНАМИ | 2016 |
|
RU2834224C1 |

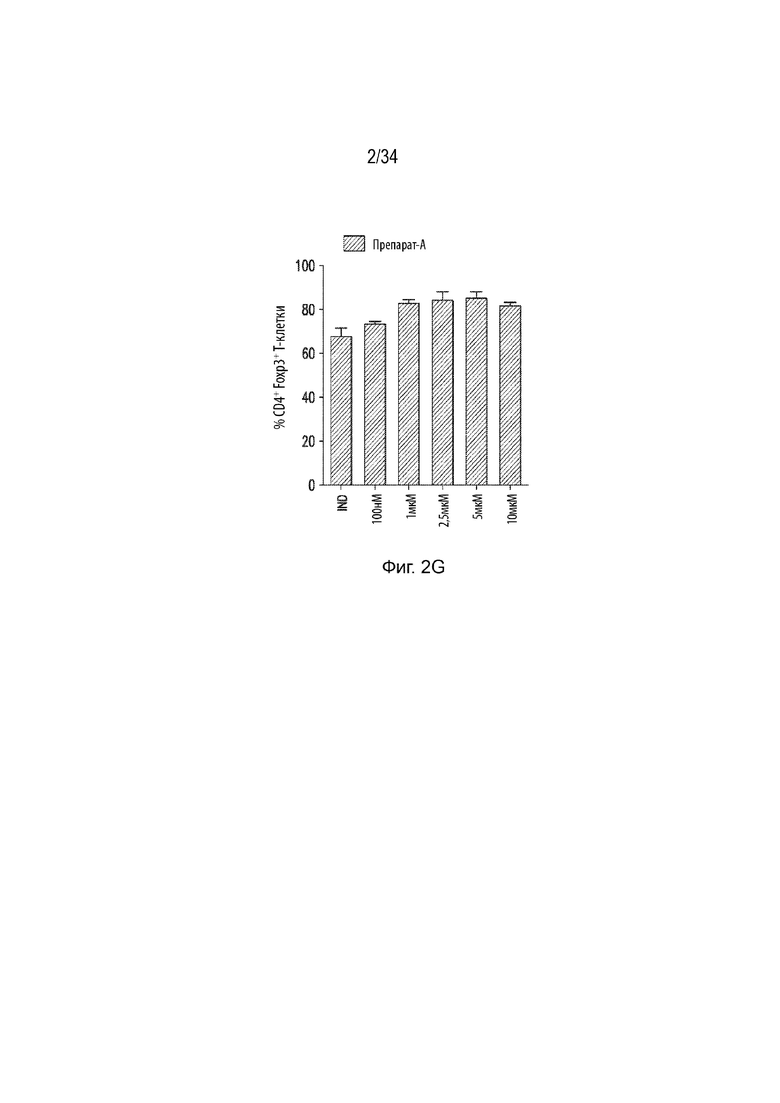
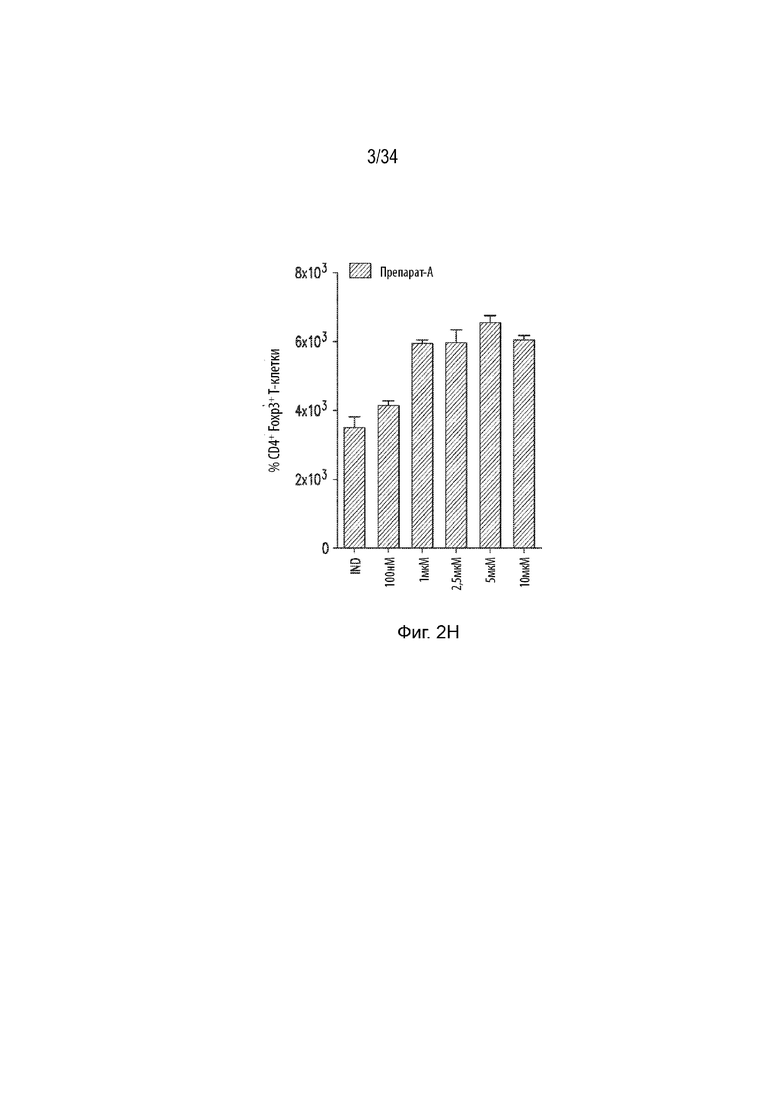
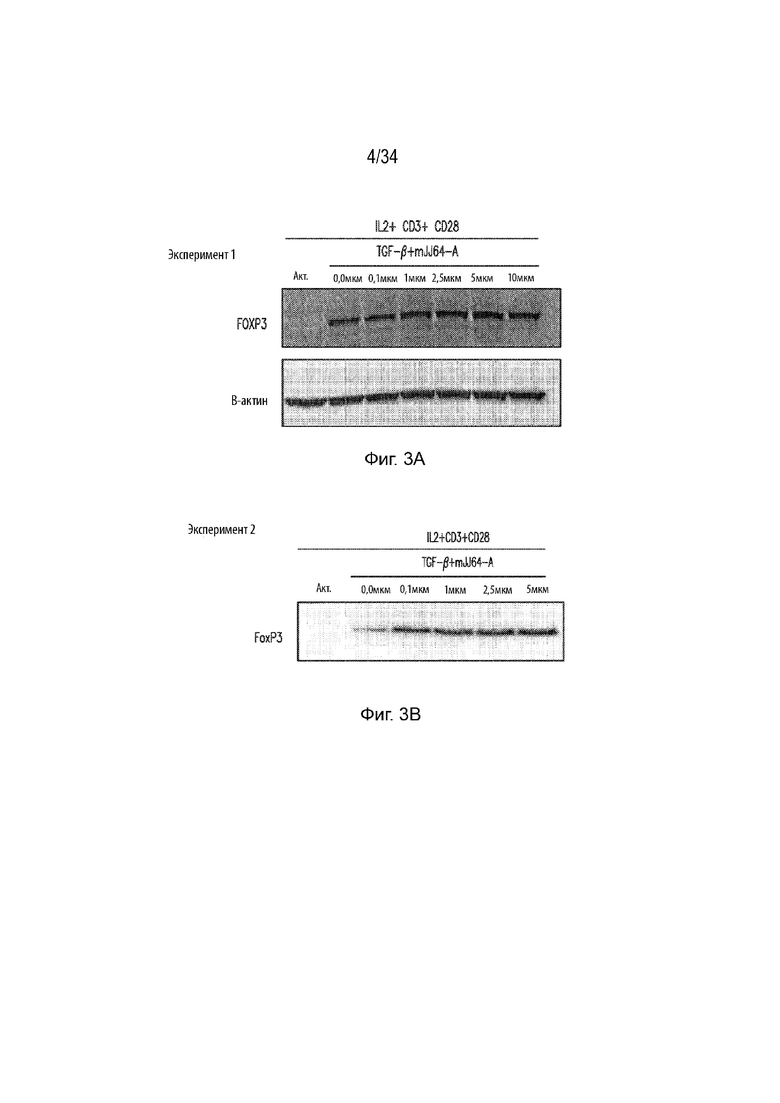
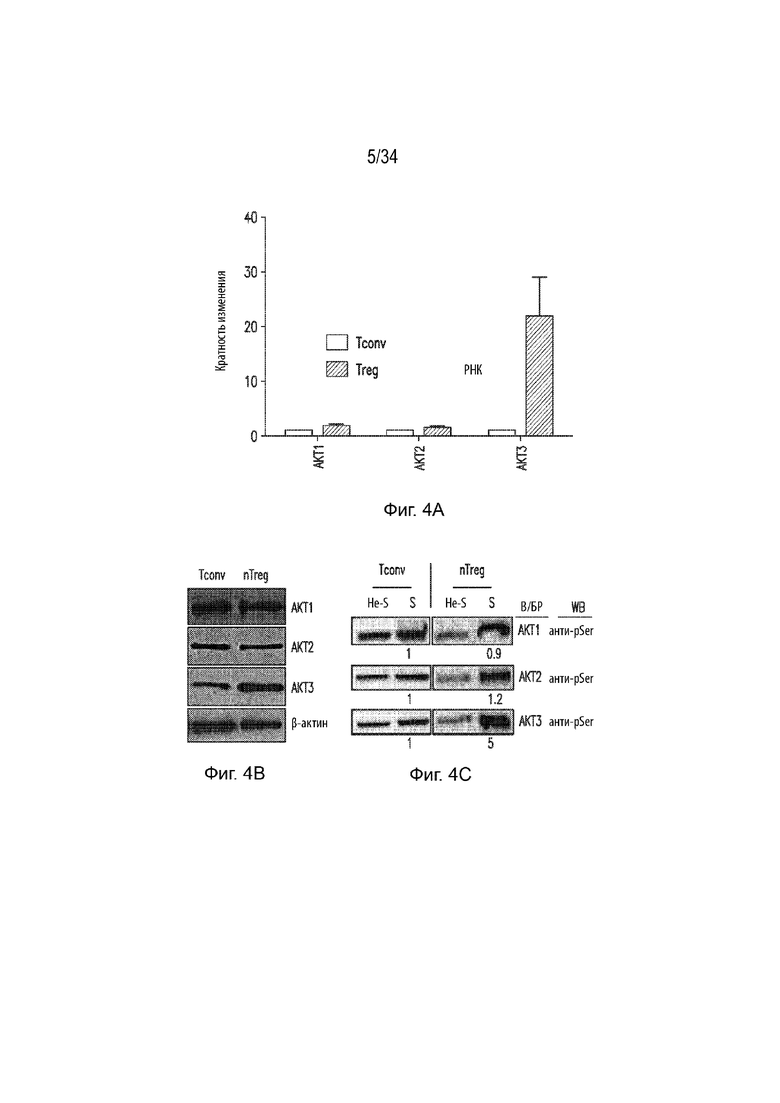
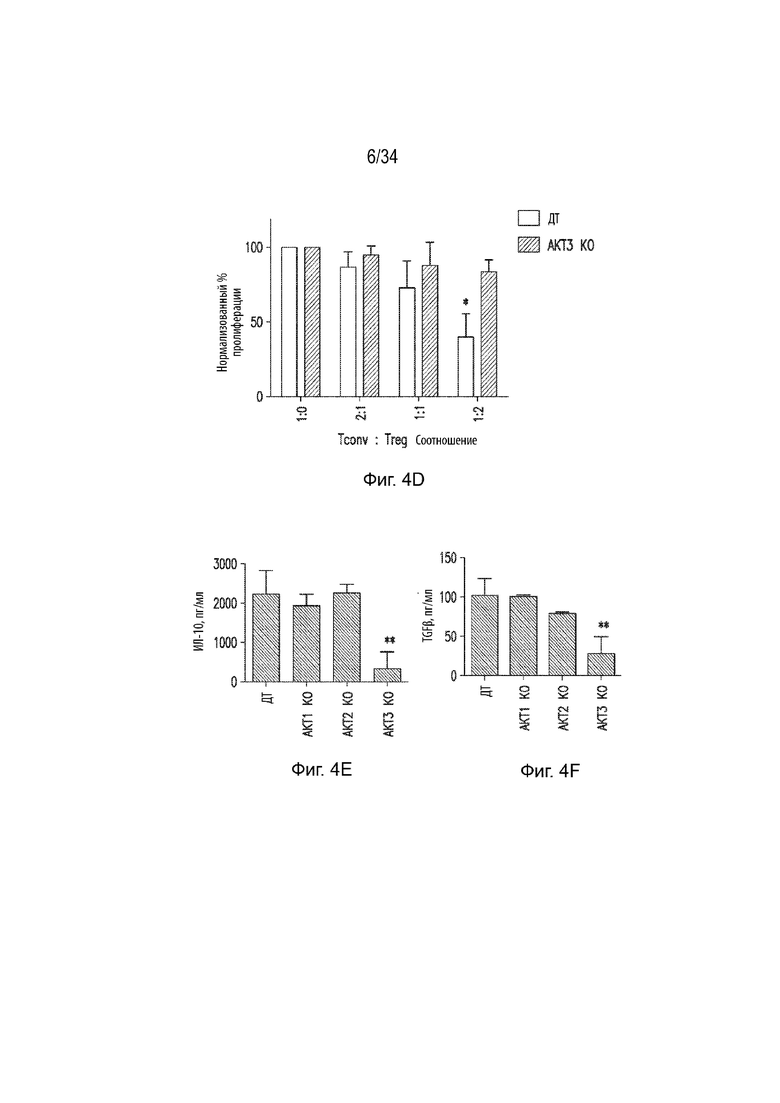

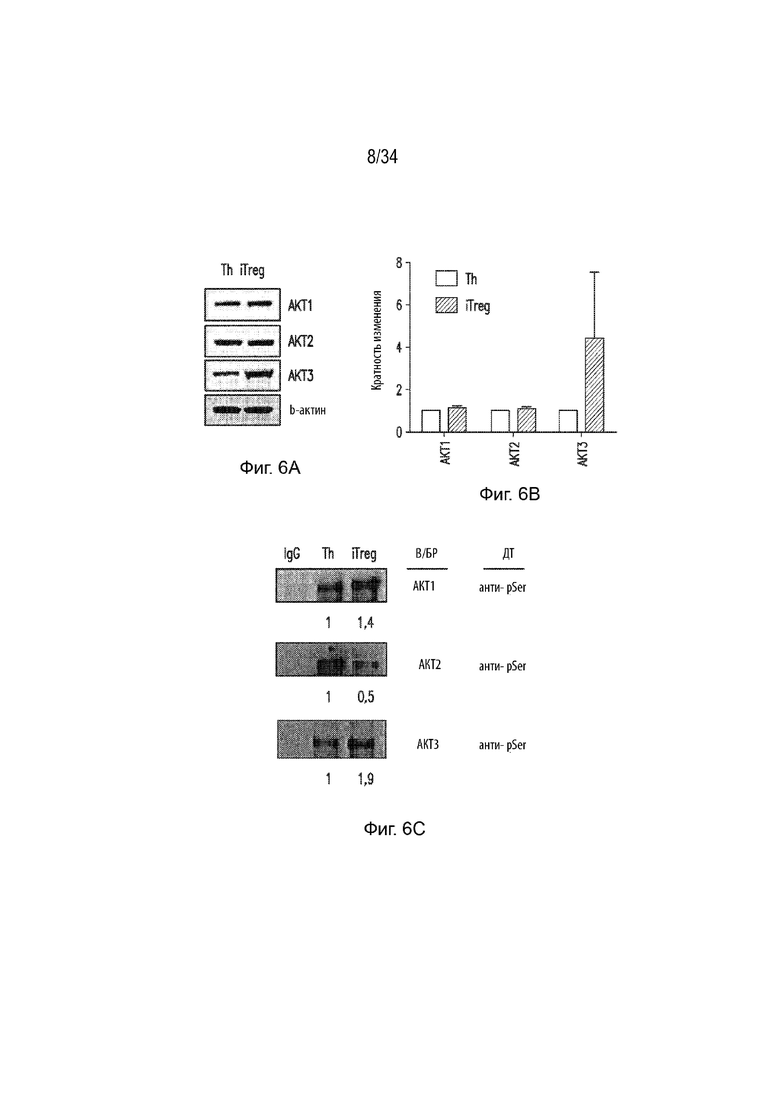

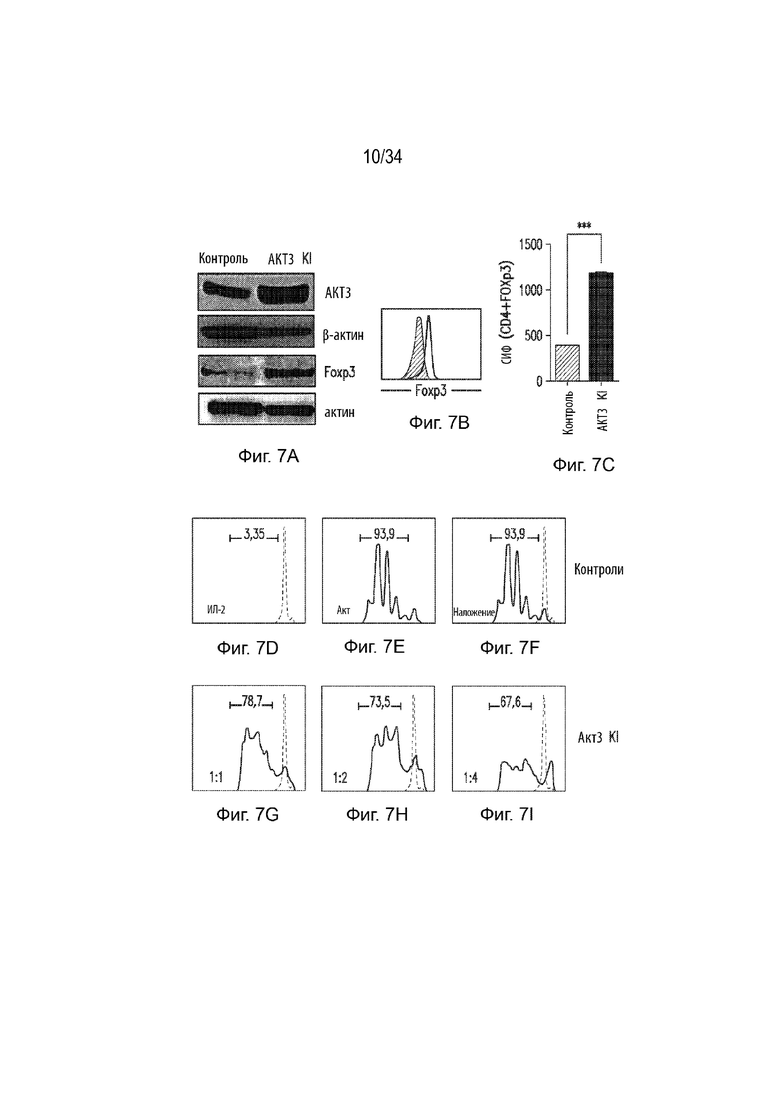
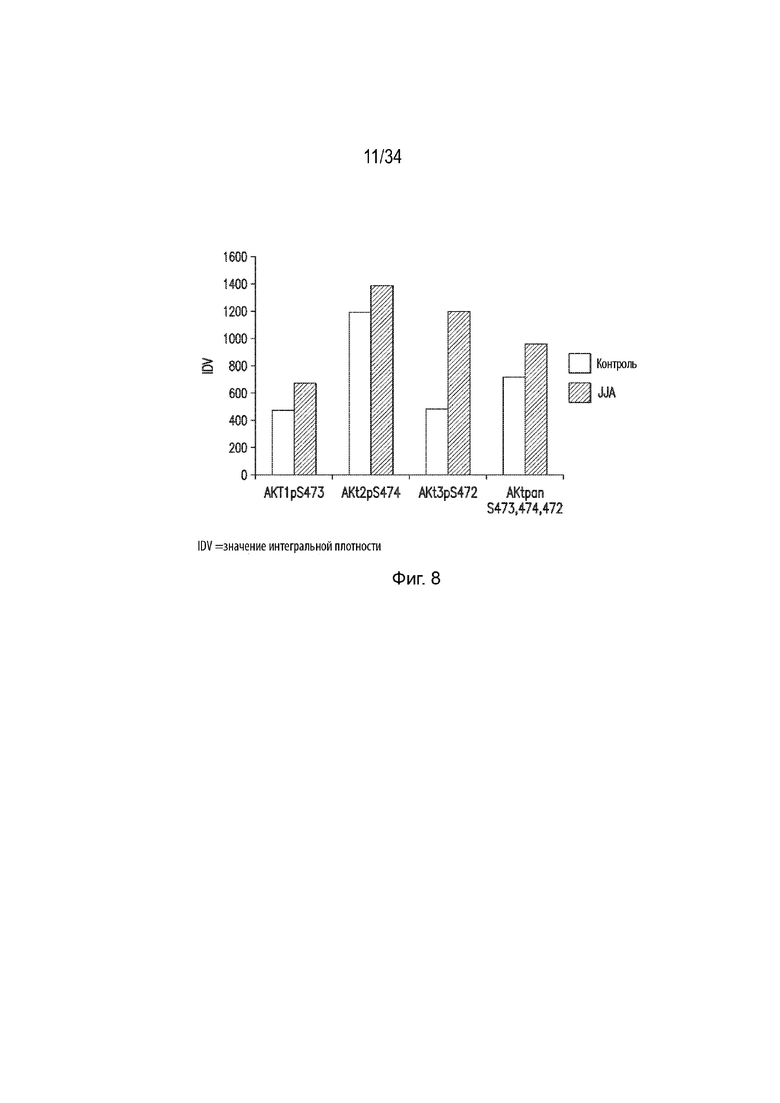

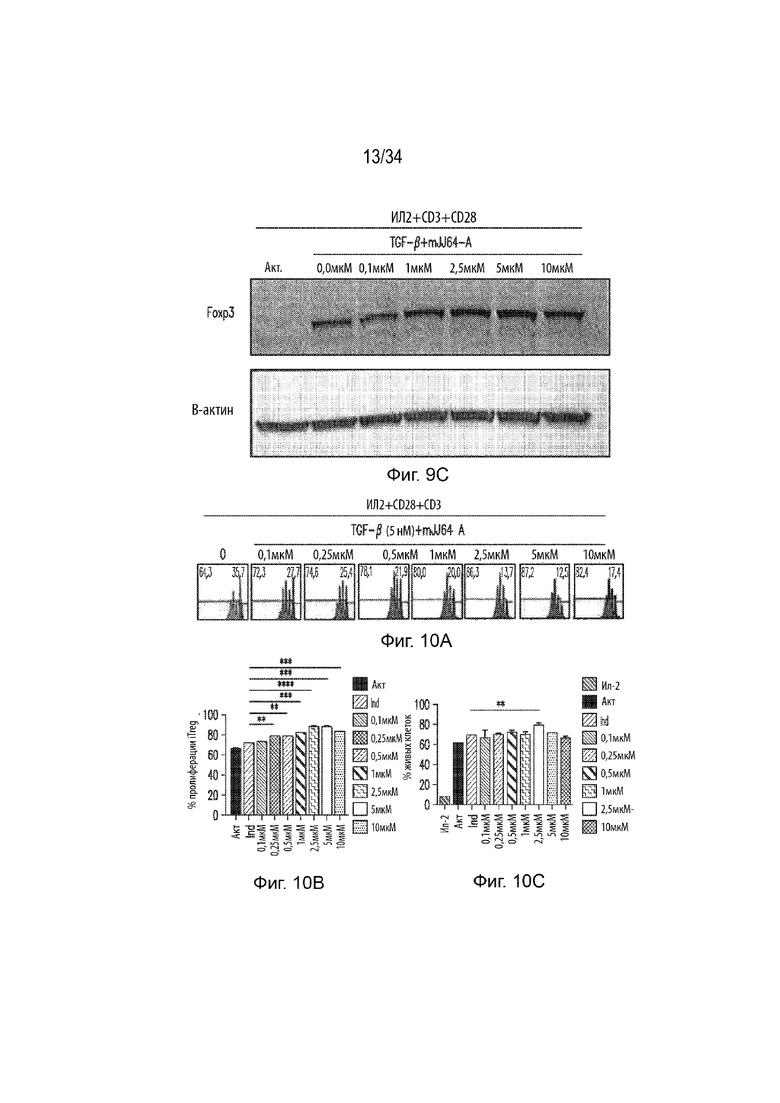

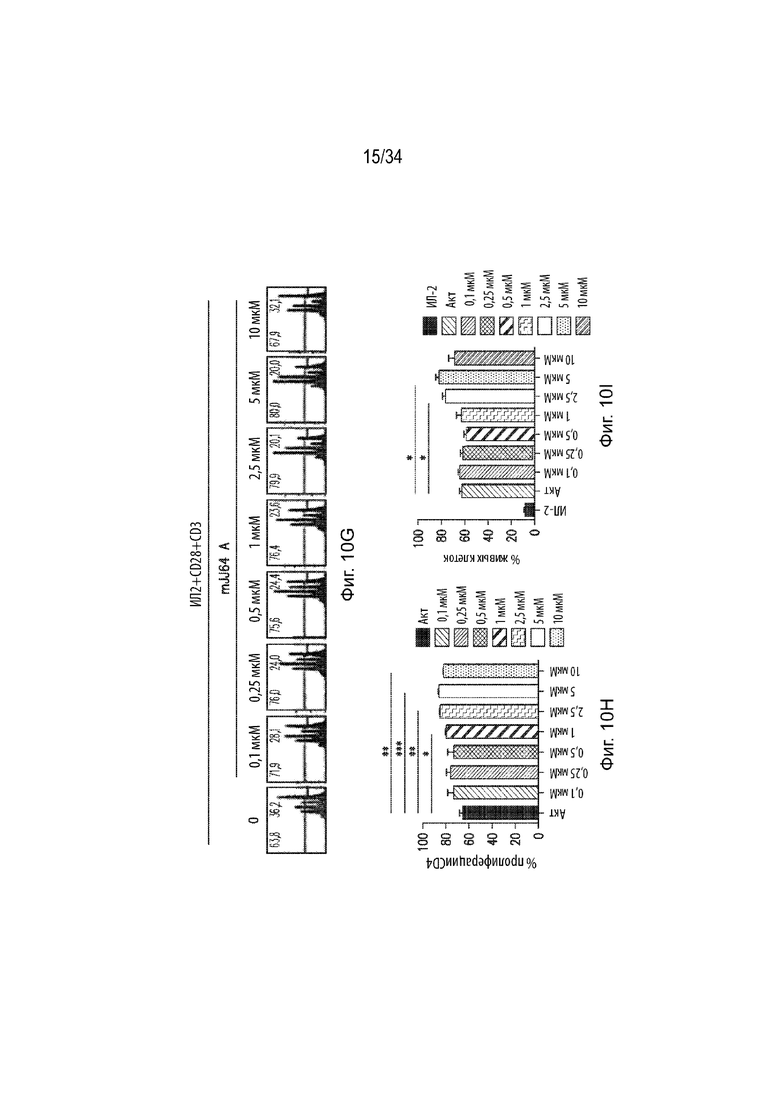

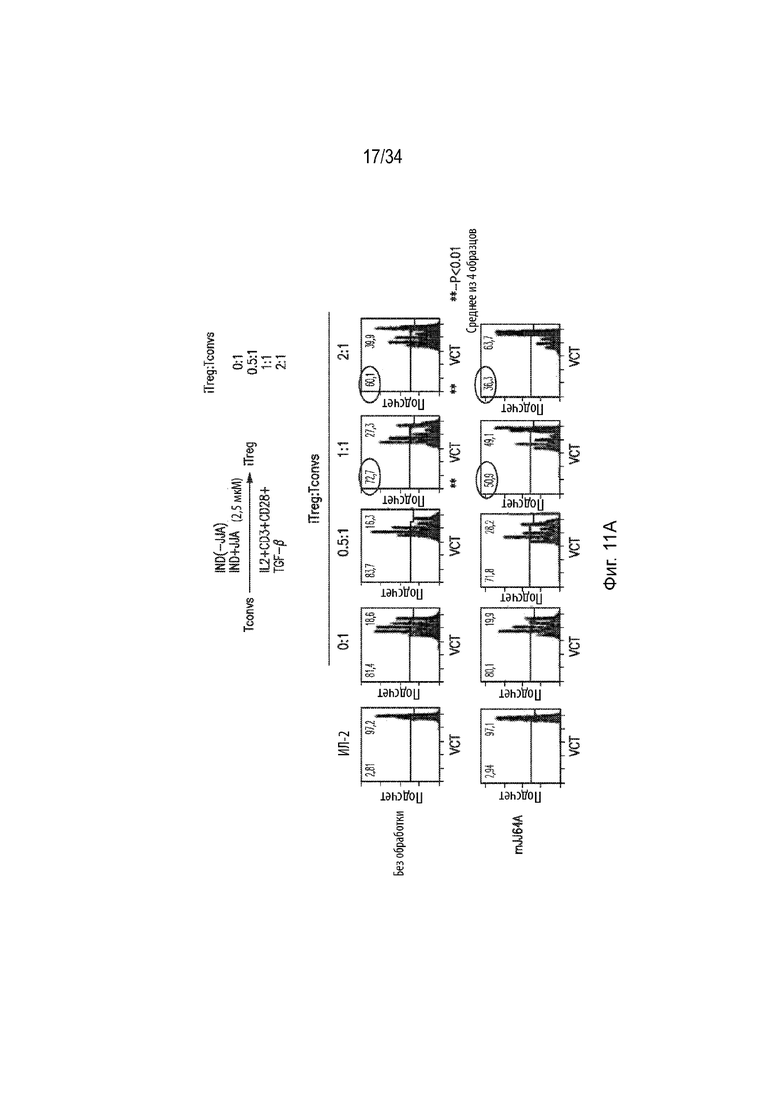

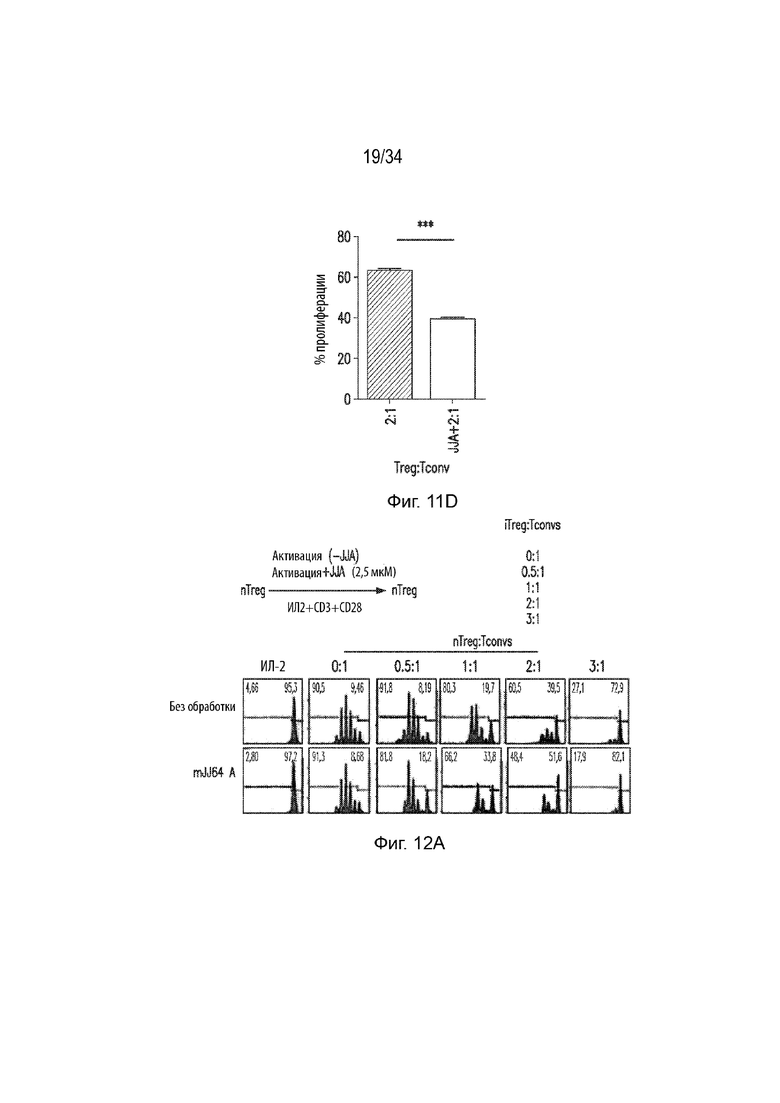

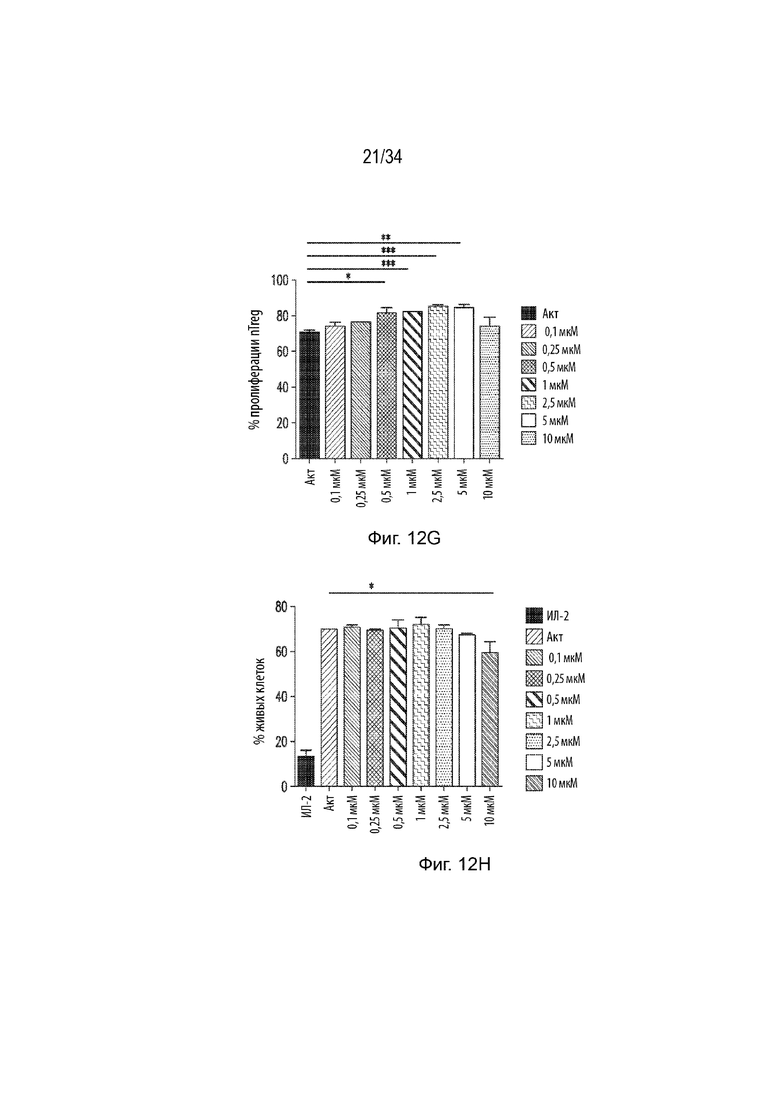

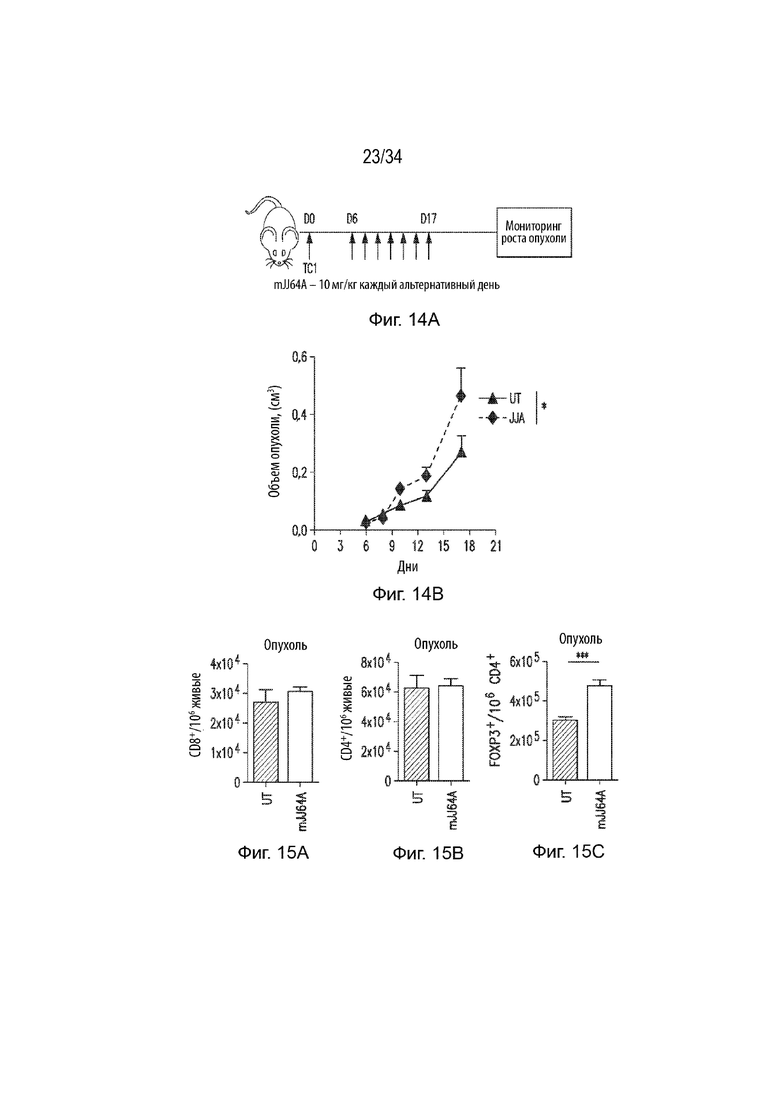

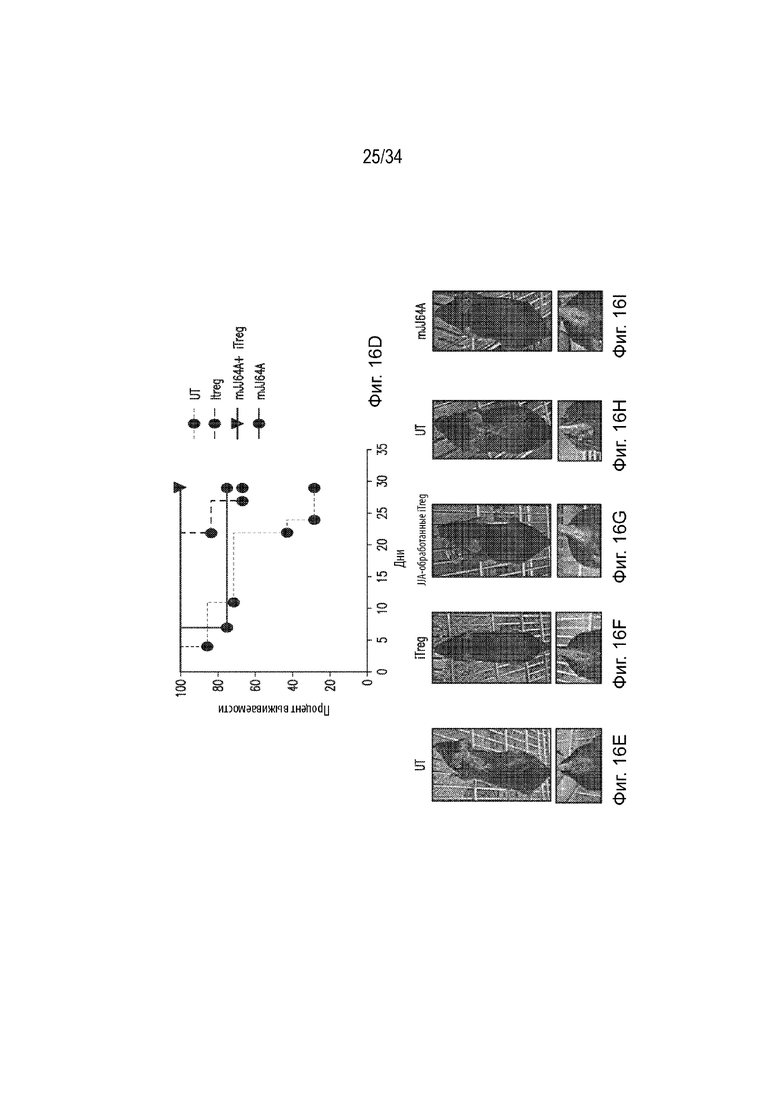


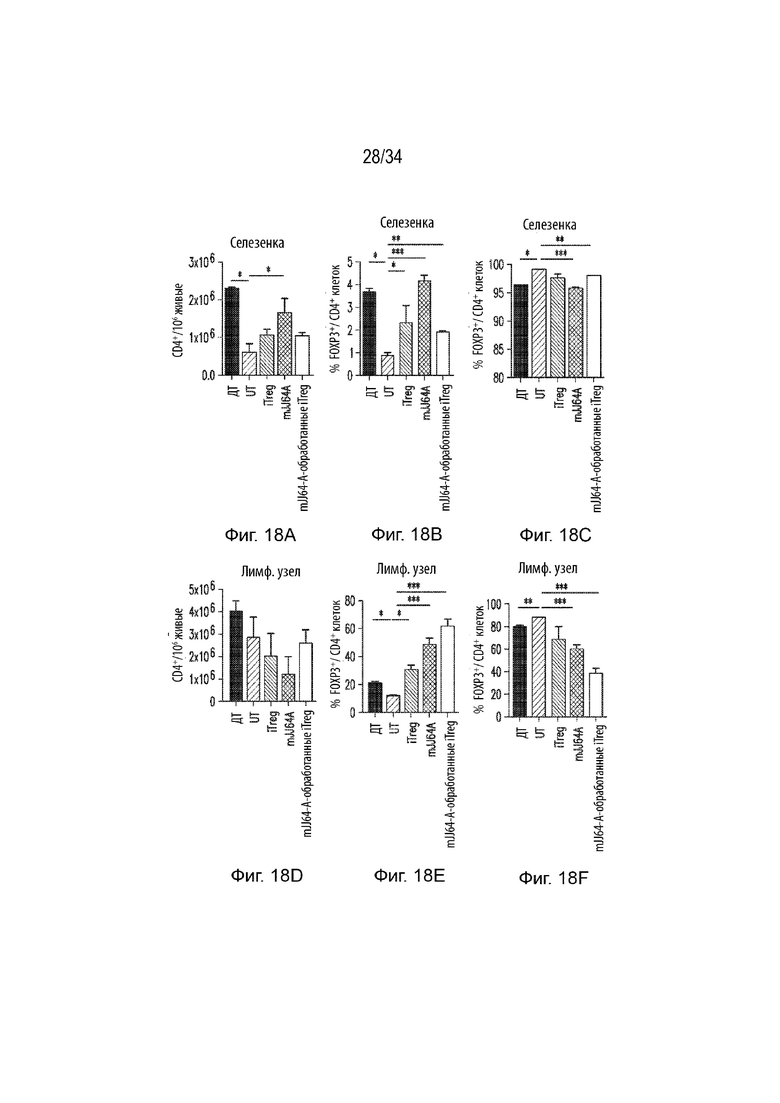
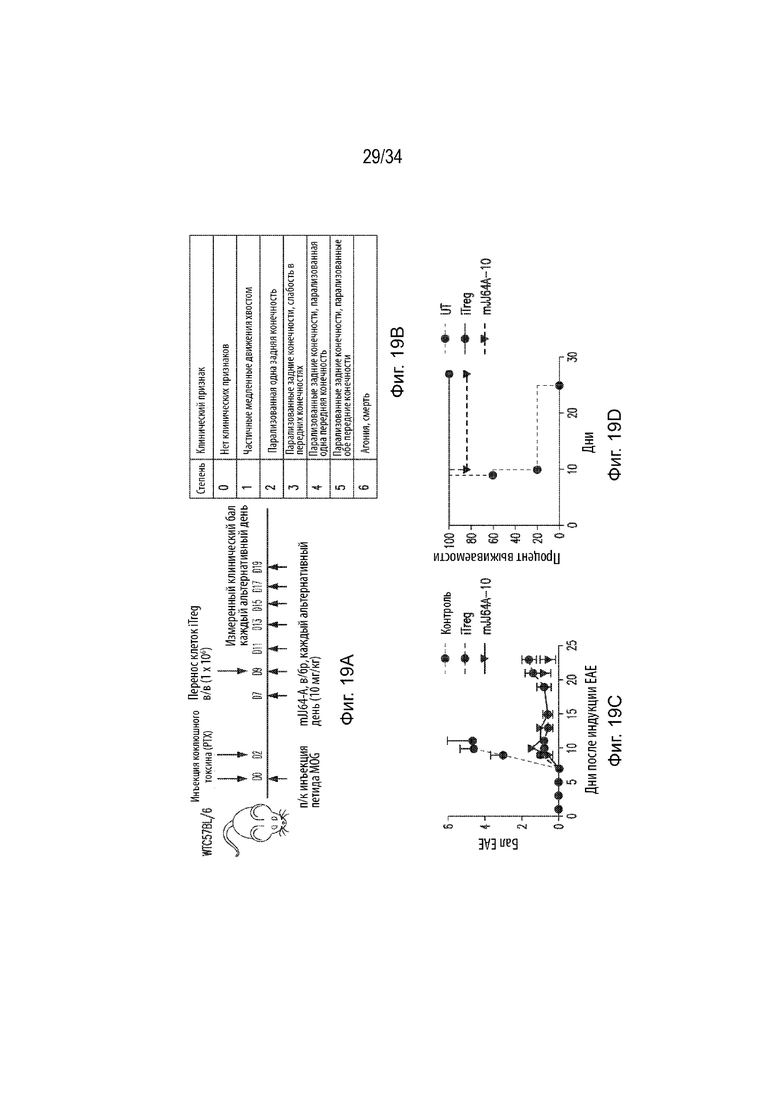
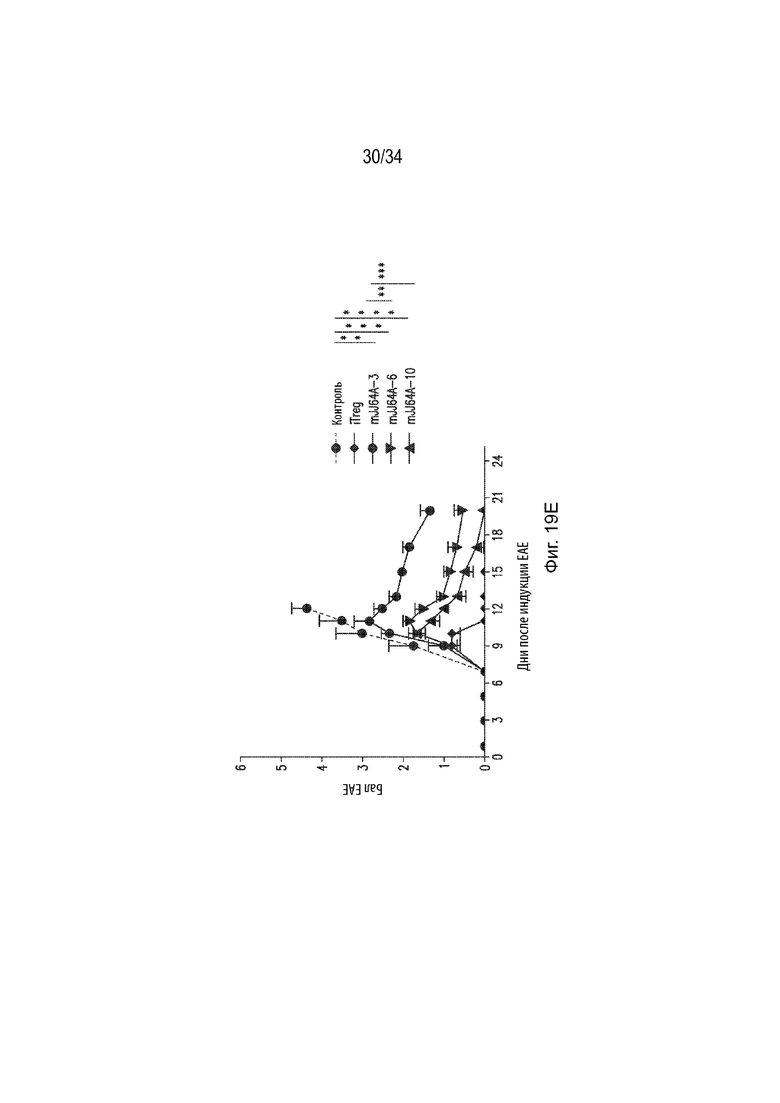
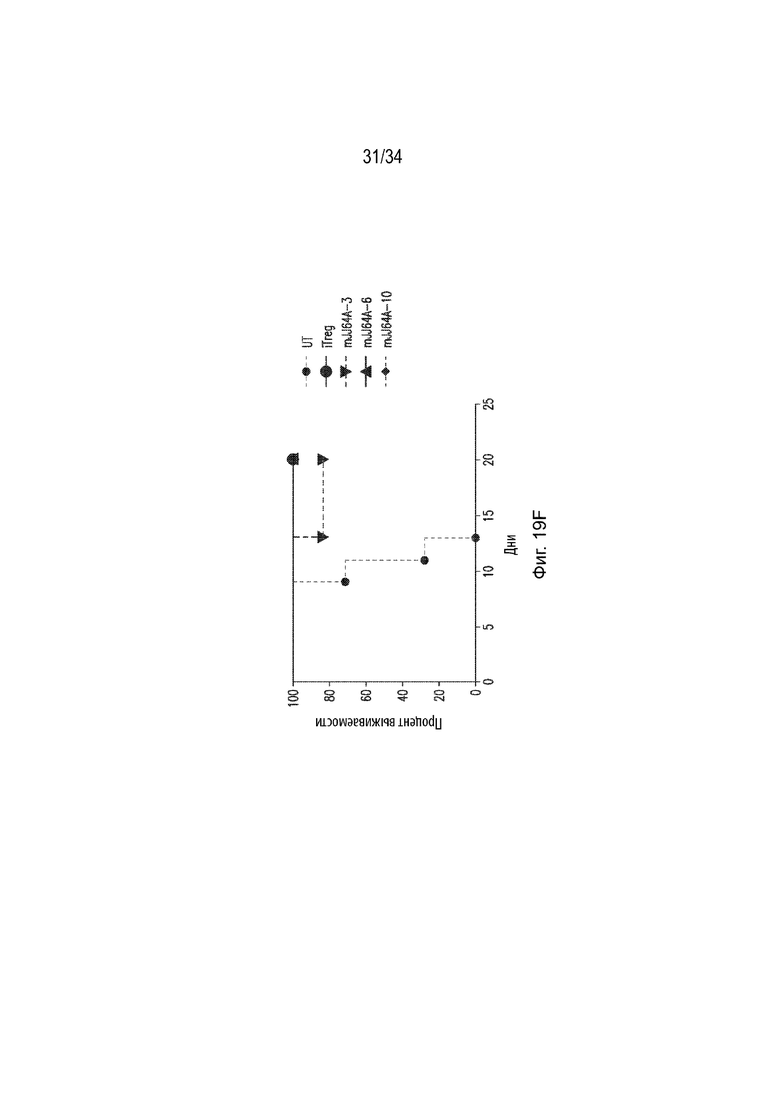
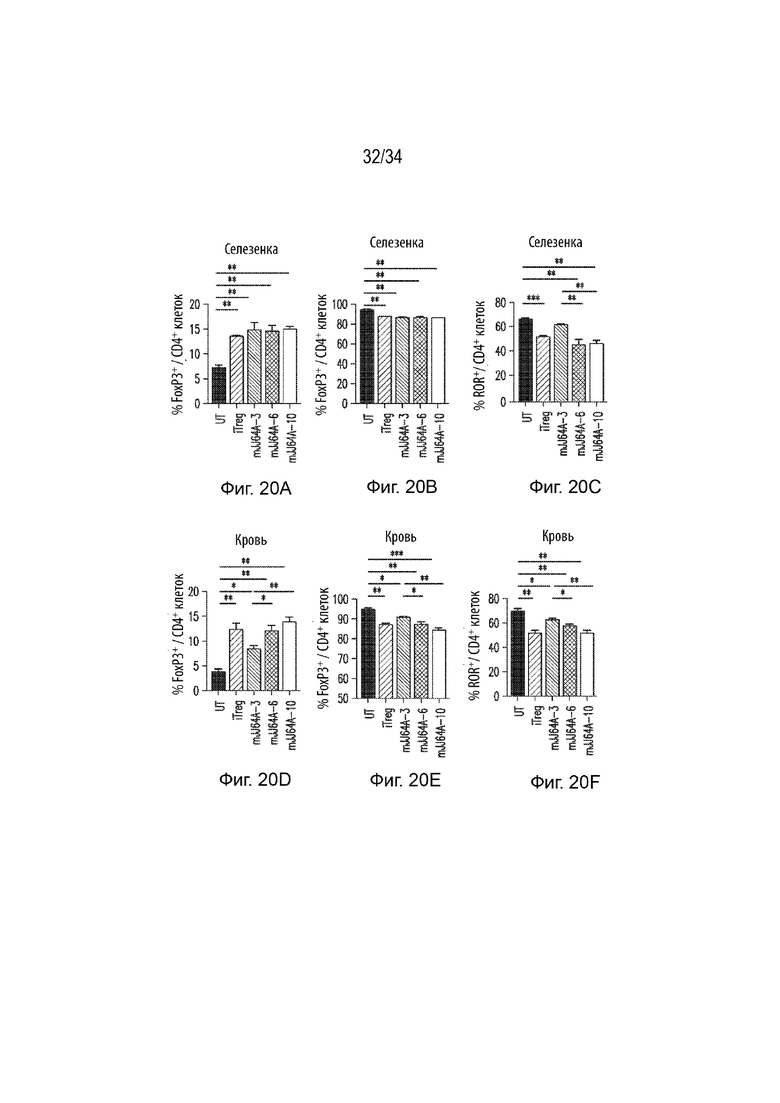
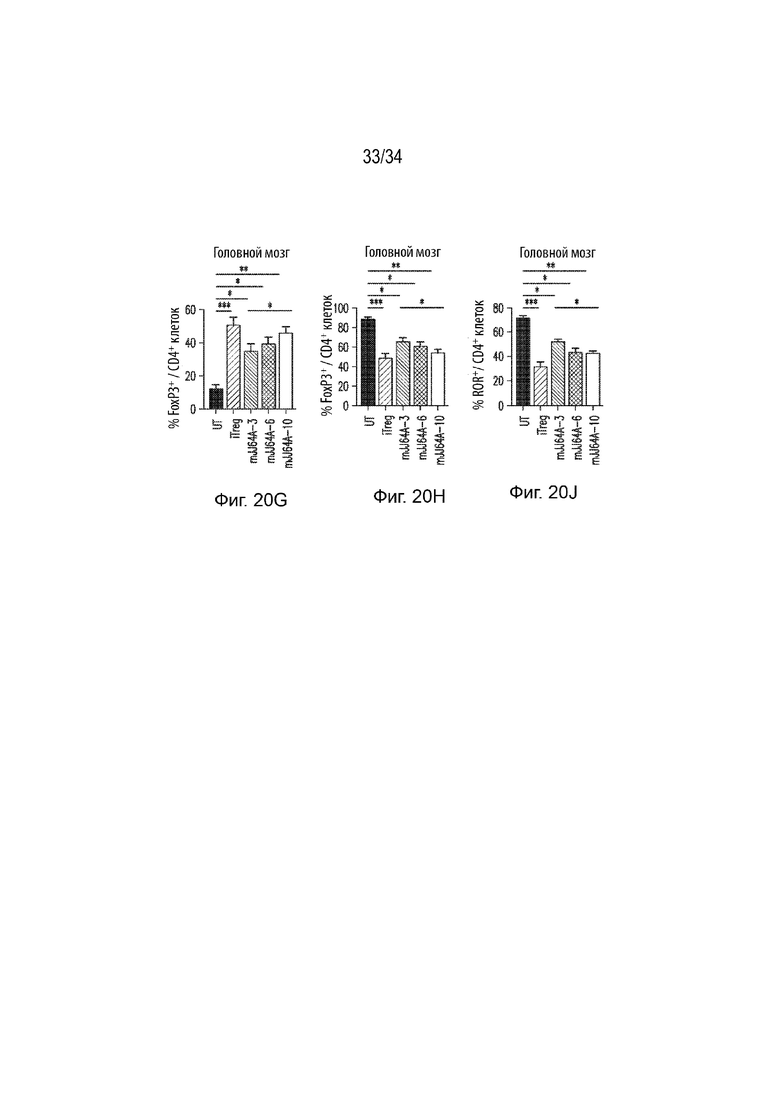
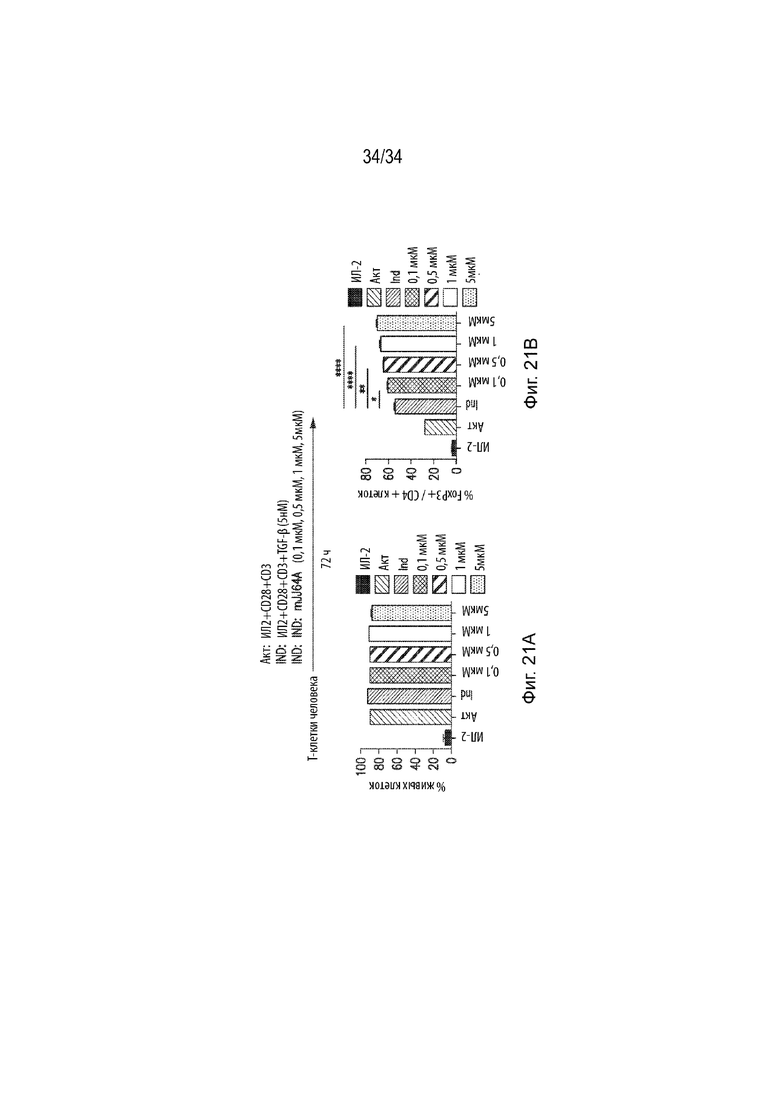
Изобретение относится к соединению формулы I или его фармацевтически приемлемой соли, где кольца A, B и C независимо представляют собой фенил, пиридин и хинолин; R1 представляет собой -(C3-C12)-гетероциклоалкил, -(C6-C20)-арил, или -(C3-C20)-гетероарильные группы, необязательно замещенные одним или большим количеством заместителей, выбранных из -(C1-C12)-алкила или -NH2; X, Y и Z независимо представляют собой -O, -NH, или -N-(C1-C30)-алкил; R2 представляет собой =O; и R3 на кольце А представляет собой -(C1-C30)-алкил, -(C3-C12)-гетероциклоалкил, -(C6-C20)-арил, -O-(C1-C12)-алкил, -N-[(C1-C12)-алкил]2, -COOH, -CN, -NH2 или галоген; R3 на кольце С представляет собой водород, -(C1-C30)-алкил или галоген; при условии, что когда R1 представляет собой незамещенный пиридин или N-замещенный –(С1)-алкилом пиридин, X, Y и Z представляют собой NH, R2 представляет собой =О, А представляет собой хинолин или пиридин, В представляет собой фенил или пиридин, С представляет собой фенил, R3 на кольце С представляет собой водород, тогда R3 на кольце А не является -N-[(C1)-алкил]2, -COOH, -CN и –F; когда соединение имеет структуру формулы III
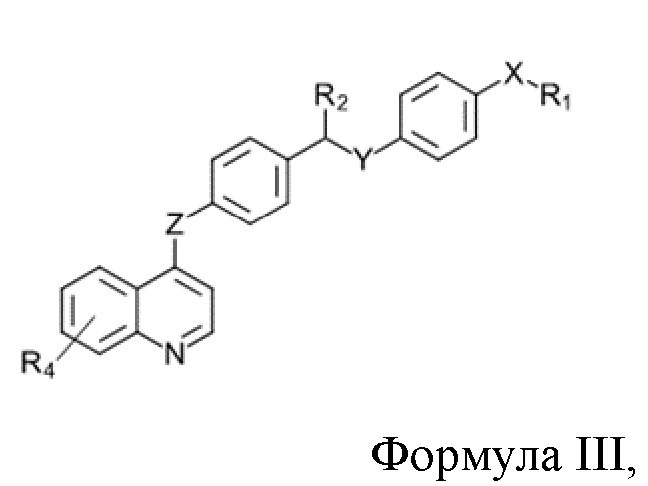
R1 представляет собой незамещенный пиридин, N-замещенный -(C1-С3)-алкилом пиридин или пиримидин, замещенный –(C1)-алкилом и NH2, X, Y, Z представляют собой -NH, R2 представляет собой =O, тогда R4 не является галогеном, –(C1)-алкилом, -O-(C1)-алкилом, -NH2 и -N-[(C1)-алкилом]2; когда R1 представляет собой незамещенный пиридин, незамещенный хинолин или хинолин, замещенный -NH2, -NO2, or -N-[(C1)-алкилом]2, X, Y, Z представляют собой -NH, R2 представляет собой =O, A представляет собой пиридин, B представляет собой фенил, C представляет собой фенил, R3 на кольце C представляет собой водород, тогда R3 на кольце A не является –(C1-C2)-алкилом и -NH2; и когда R1 представляет собой акридин, X, Y, Z представляют собой -NH, R2 представляет собой =O, A представляет собой пиридин, B представляет собой фенил, C представляет собой фенил, R3 на кольце C представляет собой водород, тогда R3 на кольце A не является –(C1)-алкилом. Изобретение также относится к фармацевтической композиции и способам селективного активирования Akt3. Технический результат - получены новые соединения, которые могут найти применение в медицине для эффективного лечения воспалительного, аутоимунного заболеваний, болезни «трансплантант против хозяина», хронической инфекции и ожирения. 12 н. и 18 з.п. ф-лы, 112 ил., 13 пр.
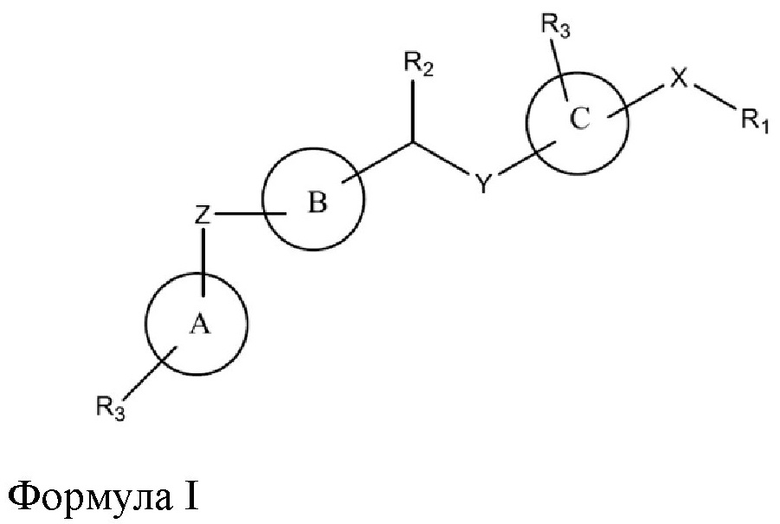
1. Соединение формулы I

или его фармацевтически приемлемая соль,
где:
кольца A, B и C независимо представляют собой фенил, пиридин и хинолин;
R1 представляет собой -(C3-C12)-гетероциклоалкил, -(C6-C20)-арил, или -(C3-C20)-гетероарильные группы, необязательно замещенные одним или большим количеством заместителей, выбранных из -(C1-C12)-алкила или -NH2;
X, Y и Z независимо представляют собой -O, -NH, или -N-(C1-C30)-алкил;
R2 представляет собой =O; и
R3 на кольце А представляет собой -(C1-C30)-алкил, -(C3-C12)-гетероциклоалкил, -(C6-C20)-арил, -O-(C1-C12)-алкил, -N-[(C1-C12)-алкил]2, -COOH, -CN, -NH2 или галоген;
R3 на кольце С представляет собой водород, -(C1-C30)-алкил или галоген;
при условии, что
(i) когда R1 представляет собой незамещенный пиридин или N-замещенный –(С1)-алкилом пиридин, X, Y и Z представляют собой NH, R2 представляет собой =О, А представляет собой хинолин или пиридин, В представляет собой фенил или пиридин, С представляет собой фенил, R3 на кольце С представляет собой водород, тогда R3 на кольце А не является -N-[(C1)-алкил]2, -COOH, -CN и –F;
(ii) когда соединение имеет структуру формулы III,

R1 представляет собой незамещенный пиридин, N-замещенный -(C1-С3)-алкилом пиридин или пиримидин, замещенный –(C1)-алкилом и NH2, X, Y, Z представляют собой -NH, R2 представляет собой =O, тогда R4 не является галогеном, –(C1)-алкилом, -O-(C1)-алкилом, -NH2 и -N-[(C1)-алкилом]2;
(iii) когда R1 представляет собой незамещенный пиридин, незамещенный хинолин или хинолин, замещенный -NH2, -NO2, or -N-[(C1)-алкилом]2, X, Y, Z представляют собой -NH, R2 представляет собой =O, A представляет собой пиридин, B представляет собой фенил, C представляет собой фенил, R3 на кольце C представляет собой водород, тогда R3 на кольце A не является –(C1-C2)-алкилом и -NH2; и
(iv) когда R1 представляет собой акридин, X, Y, Z представляют собой -NH, R2 представляет собой =O, A представляет собой пиридин, B представляет собой фенил, C представляет собой фенил, R3 на кольце C представляет собой водород, тогда R3 на кольце A не является –(C1)-алкилом.
2. Соединение формулы II
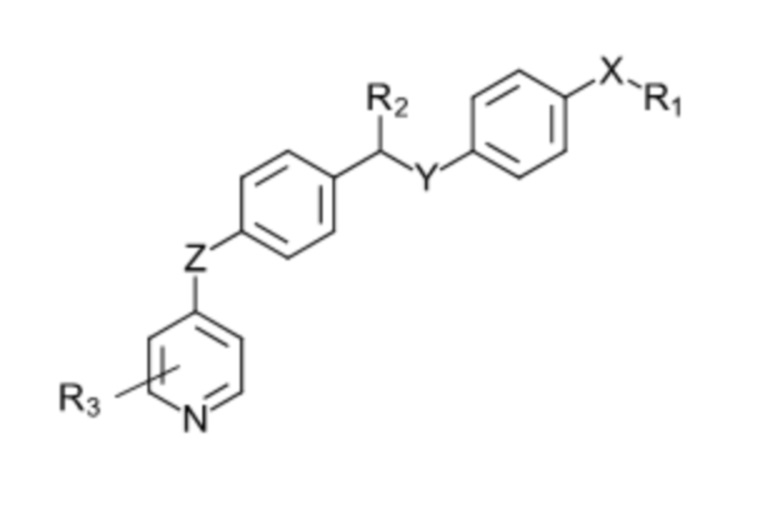
Формула II
или его фармацевтически приемлемая соль, где:
R1 представляет собой -(C6-C20)-арил или -(C3-C20)-гетероарильные группы, необязательно замещенные одним или большим количеством заместителей, выбранных из -(C1-C12)-алкила;
X, Y и Z независимо представляют собой -O или -NH;
R2 представляет собой =O; и
R3 представляет собой -(C1-C30)-алкил, или -NH2,
при условии, что
(i) когда R1 представляет собой хинолин, замещенный -NH2, -NO2, или -N-[(C1)-алкилом]2, X, Y, Z представляют собой -NH, тогда R3 на кольце A не является –(C1-C2)-алкилом и -NH2; и
(ii) когда R1 представляет собой акридин, X, Y, Z представляют собой -NH, тогда R3 на кольце A не является –(C1)-алкилом.
3. Соединение формулы III
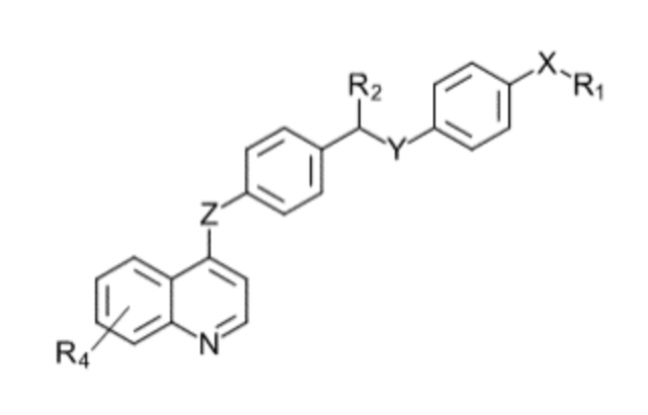
Формула III
или его фармацевтически приемлемая соль, где:
R1 представляет собой -(C3-C12)-гетероциклоалкил, -(C6-C20)-арил или -(C3-C20)-гетероарильные группы, необязательно замещенные одним или большим количеством заместителей, выбранных из -(C1-C12)-алкила и -NH2;
X, Y и Z независимо представляют собой -O, -NH, или -N-(C1-C30)-алкил;
R2 представляет собой =O; и
R4 представляет собой -(C1-C12)-алкил, -(C3-C12)-гетероциклоалкил, -O-(C1-C12)-алкил, -N-[(C1-C12)-алкил]2, -(C6-C20)-арил, -COOH, -CN, -NH2 или галоген,
при условии, что:
когда R1 представляет собой незамещенный пиридин, пиридин N-замещенный -(C1-C3)-алкилом, или пиримидин, замещенный –(C1)-алкилом и -NH2, X, Y, Z представляют собой -NH, R2 представляет собой =O, тогда R4 не является галогеном, -CN, -COOH, –(C1)-алкилом, -O-(C1)-алкилом, -NH2, и -N-[(C1)-алкил] 2.
4. Способ усиления иммуносупрессивного ответа у субъекта, нуждающегося в этом, включающий введение указанному субъекту соединения формулы I
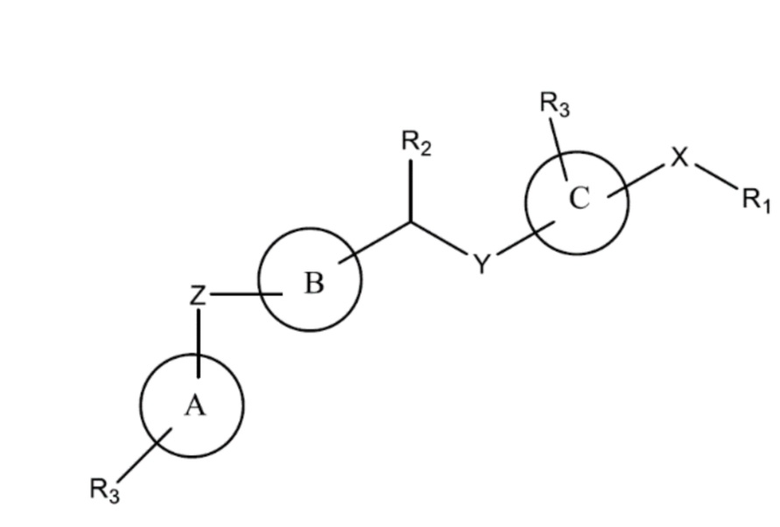
Формула I
или его фармацевтически приемлемой соли,
где
кольца A, B и C независимо представляют собой фенил, пиридин или хинолин;
R1 представляет собой -(C3-C12)-гетероциклоалкил, -(C6-C20)-арил или -(C3-C20)-гетероарильные группы, необязательно замещенные одним или большим количеством заместителей, выбранных из -(C1-C12)-алкила и -NH2;
X, Y и Z независимо представляют собой -O, -NH или -N-(C1-C30)-алкил;
R2 представляет собой =O;
R3 на кольце A представляет собой -(C3-C12)-гетероциклоалкил, -N-[(C1-C12)-алкил]2 или -CN; и
R3 на кольце C представляет собой водород, -(C1-C30)-алкил или галоген;
которое селективно активирует Akt3 в количестве, эффективном для усиления иммуносупрессивного ответа у указанного субъекта.
5. Способ по п. 4, где соединение представляет собой соединение формулы IV:
 .
.
6. Способ по п. 4 или 5, в котором у указанного субъекта имеется воспалительное нарушение или заболевание.
7. Способ лечения воспалительного нарушения, включающий введение субъекту, нуждающемуся в этом, композиции, содержащей соединения формулы I

Формула I
или фармацевтически приемлемую соль,
где
кольца A, B и C независимо представляют собой фенил, пиридин или хинолин;
R1 представляет собой -(C3-C12)-гетероциклоалкил, -(C6-C20)-арил или -(C3-C20)-гетероарильные группы, необязательно замещенные одним или большим количеством заместителей, выбранных из -(C1-C12)-алкила и -NH2;
X, Y и Z независимо представляют собой -O, -NH или -N-(C1-C30)-алкил;
R2 представляет собой =O;
R3 на кольце A представляет собой -(C3-C12)-гетероциклоалкил, -N-[(C1-C12)-алкил]2 или -CN; и
R3 на кольце C представляет собой водород, -(C1-C30)-алкил или галоген,
которые селективно активируют Akt3 в количестве, эффективном для индукции, усиления или стимуляции иммуносупрессивного ответа у указанного субъекта.
8. Способ по п. 6 или 7, в котором указанное воспалительное нарушение или заболевание выбирают из группы, состоящей из ревматоидного артрита, системной красной волчанки, гнездной алопеции, анкилозирующего спондилита, антифосфолипидного синдрома, аутоиммунной болезни Аддисона, аутоиммунной гемолитической анемии, аутоиммунного гепатита, аутоиммунного заболевания внутреннего уха, аутоиммунного лимфопролиферативного синдрома (ALPS), аутоиммунной тромбоцитопенической пурпуры (ATP), болезни Бехчета, буллезного пемфигоида, кардиомиопатии, дерматита, ассоциированного со спру-целиакией, синдрома хронической усталости и иммунодефицита, синдрома (CFIDS), хронической воспалительной демиелинизирующей полиневропатии, рубцового пемфигоида, холодовой агглютининовой болезни, синдрома Креста, болезни Крона, болезни Дего, дерматомиозита, дерматомиозита ювенильного, дискоидной волчанки, эссенциальной смешанной криоглобулинемии, фибромиалгии-фибромиозита, болезни Грейвса, болезни Гийена-Барре, тиреоидита Хашимото, идиопатического легочного фиброза, идиопатической тромбоцитопенической пурпуры (ITP), IgA-нефропатии, инсулинозависимого диабета (тип I), ювенильного артрита, болезни Меньера, смешанного заболевания соединительной ткани, рассеяного склероза, миастении, ожирения, пузырчатки обыкновенной, пернициозной анемии, узелкового полиартериита, полихондрита, полигландулярного синдрома, ревматической полимиалгии, полимиозита и дерматомиозита, первичной агаммаглобулинемии, первичного билиарного цирроза, псориаза, феномена Рейно, синдрома Рейтера, ревматической лихорадки, саркоидоза, склеродермии, синдрома Шегрена, синдрома мышечной скованности, артериита Такаясу, височного артериита/гигантоклеточного артериита, язвенного колита, увеита, васкулита, витилиго и гранулематоза Вегенера.
9. Способ лечения аутоиммунного заболевания, включающий введение субъекту, нуждающемуся в этом, композиции, содержащей любое из соединений по пп. 1-3 или соединение формулы IV, указанное в п. 5, или его фармацевтически приемлемую соль, которые селективно активируют Akt3 в количестве, эффективном для индукции, стимуляции или усиления иммуносупрессивного ответа у указанного субъекта.
10. Способ по п. 9, в котором указанное аутоиммунное заболевание выбирают из группы, состоящей из ревматоидного артрита, системной красной волчанки, гнездной алопеции, аутоиммунной болезни Аддисона, аутоиммунной гемолитической анемии, аутоиммунного гепатита, аутоиммунного заболевания внутреннего уха, аутоиммунного лимфопролиферативного синдрома (ALPS), аутоиммунной тромбоцитопенической пурпуры (ATP), болезни Крона, рассеянного склероза и миастении.
11. Способ по любому из пп. 4-10, в котором иммуносупрессивный ответ, который усиливается, выбирают из группы, состоящей из иммуносупрессивной функции природной Treg (nTreg) и индукции превращения типовой T-клетки в индуцированную Treg (iTreg).
12. Способ по п. 11, в котором иммуносупрессивная функция nTreg представляет собой секрецию одного или большего количества противовоспалительных цитокинов.
13. Способ по п. 12, в котором противовоспалительным цитокином является IL-10, TGFβ или их комбинация.
14. Способ по любому из пп. 4-13, в котором соединение вводят в количестве, повышающем экспрессию FoxP3 на иммунных клетках.
15. Способ по п. 14, в котором иммунные клетки содержат iTreg.
16. Способ по любому из п. 15, в котором соединение вводят в количестве, эффективном для увеличения пролиферации iTreg.
17. Фармацевтическая композиция для селективной активации Akt3 в иммунных клетках, содержащая эффективное количество соединения формулы I
 ,
,
где
кольца A, B и C независимо представляют собой фенил, пиридин или хинолин;
R1 представляет собой -(C3-C12)-гетероциклоалкил, -(C6-C20)-арил или -(C3-C20)-гетероарильные группы, необязательно замещенные одним или большим количеством заместителей, выбранных из -(C1-C12)-алкила и -NH2;
X, Y и Z независимо представляют собой -O, -NH или -N-(C1-C30)-алкил;
R2 представляет собой =O;
R3 на кольце A представляет собой -(C3-C12)-гетероциклоалкил, -N-[(C1-C12)-алкил]2 или -CN; и
R3 на кольце C представляет собой водород, -(C1-C30)-алкил или галоген;
или его фармацевтически приемлемой соли, а также вспомогательное вещество.
18. Фармацевтическая композиция по п. 17, в которой соединение или его фармацевтически приемлемая соль находятся в количестве, эффективном для усиления супрессивного иммунного ответа при введении субъекту, нуждающемуся в этом.
19. Способ усиления иммуносупрессивного ответа у субъекта, нуждающегося в этом, включающий приведение в контакт иммунных клеток ex vivo с соединением формулы I

Формула I
или его фармацевтически приемлемой солью,
где
кольца A, B и C независимо представляют собой фенил, пиридин или хинолин;
R1 представляет собой -(C3-C12)-гетероциклоалкил, -(C6-C20)-арил или -(C3-C20)-гетероарильные группы, необязательно замещенные одним или большим количеством заместителей, выбранных из -(C1-C12)-алкила и -NH2;
X, Y и Z независимо представляют собой -O, -NH или -N-(C1-C30)-алкил;
R2 представляет собой =O;
R3 на кольце A представляет собой -(C3-C12)-гетероциклоалкил, -N-[(C1-C12)-алкил]2 или -CN; и
R3 на кольце C представляет собой водород, -(C1-C30)-алкил или галоген,
в количестве, эффективном для увеличения экспрессии FoxP3 на иммунных клетках, и введения указанных приведенных в контакт иммунных клеток указанному субъекту.
20. Способ по п. 19, в котором указанные иммунные клетки включают аутологичные иммунные клетки.
21. Способ по п. 19 или 20, в котором указанные иммунные клетки включают Т-клетки.
22. Способ по п. 21, в котором указанные Т-клетки включают Treg.
23. Способ по п. 22, в котором указанные Treg включают iTreg.
24. Способ ингибирования или уменьшения отторжения трансплантата у субъекта, нуждающегося в этом, путем введения эффективного количества соединения формулы I

Формула I
или его фармацевтически приемлемой соли,
где
кольца A, B и C независимо представляют собой фенил, пиридин или хинолин;
R1 представляет собой -(C3-C12)-гетероциклоалкил, -(C6-C20)-арил, или -(C3-C20)-гетероарильные группы, необязательно замещенные одним или большим количеством заместителей, выбранных из -(C1-C12)-алкила и -NH2;
X, Y и Z независимо представляют собой -O, -NH или -N-(C1-C30)-алкил;
R2 представляет собой =O;
R3 на кольце A представляет собой -(C3-C12)-гетероциклоалкил, -N-[(C1-C12)-алкил]2 или -CN; и
R3 на кольце C представляет собой водород, -(C1-C30)-алкил или галоген,
для повышения экспрессии FoxP3 на иммунных клетках указанного субъекта.
25. Способ лечения болезни «трансплантат против хозяина» у субъекта, нуждающегося в этом, путем введения указанному субъекту эффективного количества соединения формулы I

Формула I
или его фармацевтически приемлемой соли,
где кольца A, B и C независимо представляют собой фенил, пиридин или хинолин;
R1 представляет собой -(C3-C12)-гетероциклоалкил, -(C6-C20)-арил, или -(C3-C20)-гетероарильные группы, необязательно замещенные одним или большим количеством заместителей, выбранных из -(C1-C12)-алкила и -NH2;
X, Y и Z независимо представляют собой -O, -NH или -N-(C1-C30)-алкил;
R2 представляет собой =O;
R3 на кольце A представляет собой -(C3-C12)-гетероциклоалкил, -N-[(C1-C12)-алкил]2 или -CN; и
R3 на кольце C представляет собой водород, -(C1-C30)-алкил или галоген,
для повышения экспрессии FoxP3 на иммунных клетках указанного субъекта.
26. Способ лечения хронической инфекции у субъекта, нуждающегося в этом, путем введения указанному субъекту эффективного количества соединения формулы I

Формула I
или его фармацевтически приемлемой соли,
где кольца A, B и C независимо представляют собой фенил, пиридин или хинолин;
R1 представляет собой -(C3-C12)-гетероциклоалкил, -(C6-C20)-арил, или -(C3-C20)-гетероарильные группы, необязательно замещенные одним или большим количеством заместителей, выбранных из -(C1-C12)-алкила и -NH2;
X, Y и Z независимо представляют собой -O, -NH или -N-(C1-C30)-алкил;
R2 представляет собой =O;
R3 на кольце A представляет собой -(C3-C12)-гетероциклоалкил, -N-[(C1-C12)-алкил]2 или -CN; и
R3 на кольце C представляет собой водород, -(C1-C30)-алкил или галоген,
для повышения экспрессии FoxP3 на иммунных клетках указанного субъекта.
27. Способ лечения ожирения у субъекта, нуждающегося в этом, путем введения указанному субъекту эффективного количества соединения формулы I

Формула I
или его фармацевтически приемлемой соли,
где кольца A, B и C независимо представляют собой фенил, пиридин или хинолин;
R1 представляет собой -(C3-C12)-гетероциклоалкил, -(C6-C20)-арил, или -(C3-C20)-гетероарильные группы, необязательно замещенные одним или большим количеством заместителей, выбранных из -(C1-C12)-алкила и -NH2;
X, Y и Z независимо представляют собой -O, -NH или -N-(C1-C30)-алкил;
R2 представляет собой =O;
R3 на кольце A представляет собой -(C3-C12)-гетероциклоалкил, -N-[(C1-C12)-алкил]2 или -CN; и
R3 на кольце C представляет собой водород, -(C1-C30)-алкил или галоген.
28. Соединение по любому из пп. 1-3 или фармацевтическая композиция по пп. 17 и 18, или способ по любому из пп. 4-16 и 19-27, где R1 в формуле I и/или III представляет собой фенил, пиридин, пиримидин или пиридазин, необязательно замещенный одним или большим количеством заместителями, выбранными из -(C1-C12)- алкила и NH2, и где R1 в формуле II представляет собой фенил, пиридин, пиримидин или пиридазин, необязательно замещенный одним или большим количеством –(C1-C12)-алкилов.
29. Соединение по любому из пп. 1-3, 28, или фармацевтическая композиция по пп. 17, 18 или способ по любому из пп. 4-16, 19-27, где R3 на кольце А в формуле I и/или R4 в формуле III независимо представляют собой CN, -N-[(C1-C12)-алкил]2 или -(C1-C12)-гетероциклоалкил.
30. Соединение по любому из пп. 1-3, 28, или фармацевтическая композиция по пп. 17, 18, или способ по любому из пп. 9-16, 19-27, где R3 на кольце А в формуле I, R3 в формуле II, и/или R4 в формуле III независимо представляют собой галоген, -(C1-C30)-алкил или NH2.
| US 20170202956 A1, 20.07.2017 | |||
| US 20170202829 A1, 20.07.2017 | |||
| ATWELL et al | |||
| Journal of Medicinal Chemistry, vol | |||
| Устройство для электрической сигнализации | 1918 |
|
SU16A1 |
| Фибровый челнок | 1924 |
|
SU673A1 |
| ИНГИБИТОРЫ АКТИВНОСТИ АКТ | 2006 |
|
RU2421454C2 |
| ИНГИБИТОРЫ АКТИВНОСТИ АКТ | 2010 |
|
RU2579513C2 |
| СОЕДИНЕНИЯ И СПОСОБЫ МОДУЛИРОВАНИЯ КИНАЗ И ПОКАЗАНИЯ К ПРИМЕНЕНИЮ УКАЗАННЫХ СОЕДИНЕНИЙ И СПОСОБОВ | 2008 |
|
RU2487121C2 |
Авторы
Даты
2024-03-13—Публикация
2018-09-06—Подача