ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новым блокаторам калиевых каналов Kv1.3, полинуклеотидам, кодирующим их, и к способам их получения и применения.
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Ионные каналы представляют собой мембранные белки, которые формируют поры в биологических мембранах, позволяя (и регулируя) поток ионов через соответствующую мембрану. Существует множество различных типов ионных каналов, которые могут быть классифицированы по-разному, например, по типу ионов, пропуск которых они осуществляют, по способу, посредством которого пропуск ионов регулируется или ограничивается (например "лиганд-зависимые" или "потенциал-зависимые"), и по их клеточной или субклеточной локализации.
Калиевые каналы относятся к четырем основным классам, а именно: потенциал-зависимые калиевые каналы, кальций-активируемые калиевые каналы, калиевые каналы внутреннего выпрямления и калиевые каналы тандемных поровых доменов.
Потенциалзависимые калиевые каналы, подобно другим потенциалзависимым каналам, открываются или закрываются в ответ на трансмембранный потенциал. Они представляют собой комплексное семейство с разнообразными биологическими функциями, включая регуляцию высвобождения нейротрансмиттеров, частоту сердцебиений, секрецию инсулина, нейрональную возбудимость, эпителиальный транспорт электролитов, сокращение гладких мышц и объем клеток.
Канал Kv1.3 (представитель 3 подсемейства A потенциалзависимых каналов) экспрессируется на T-клетках и участвует в регуляции активации T-клеток. Было показано, что блокаторы Kv1.3 ингибируют пролиферацию активированных T-клеток in vitro (рассмотрено в Cahalan and Chandy, Immunol. Rev. 231:59-87, 2009) и ингибируют зависимое от T клеток прогрессирование заболевания в различных экспериментальных моделях аутоиммунных заболеваний, включая экспериментальный аутоиммунный энцефаломиелит (EAE), экспериментальный артрит, гиперчувствительность замедленного типа (DTH), аллергический контактный дерматит и гломерулонефрит.См., например, Rangaraju et al. (Expert Opin. Ther. Targets 13:909-24, 2009); Beeton et al. (Proc. Natl. Acad. Sci. U S A. 103:17414-9, 2006); Koo et al. (J. Immunol. 158:5120-8, 1997); Hyodo et al. (Am. J. Physiol. Renal Physiol. 299: F1258-69, 2010). В WO 2016/112208 описано местное применение блокаторов Kv1.3 для лечения воспаления кожи и слизистой оболочки.
Таким образом, блокаторы Kv1.3 имеют значительный потенциал для применения для лечения воспалительных нарушений, включая аутоиммунные нарушения.
В WO 2015/013330 предлагается применение пептидов-блокаторов Kv1.3 для лечения офтальмологических состояний, таких как сухость глаза и увеит, включая случаи, когда они вызваны аутоиммунными состояниями, такими как синдром Шегрена.
Блокаторы Kv1.3 также могут иметь благоприятные метаболические эффекты, например, в отношении гомеостаза энергии, регуляции массы тела и контроля уровня глюкозы. Мыши с нокаутом Kv1.3 (Kv1.3(-/-)) имеют сниженный прирост массы тела, более высокую чувствительность к инсулину и сниженные уровни глюкозы в плазме в ответ на рацион с высоким содержанием жиров по сравнению с контрольными однопометными животными (Xu et al., Hum. Mol. Genet. 12:551-9, 2003). Кроме того, было показано, что блокаторы Kv1.3 повышают экспрессию в скелетных мышцах и жировой ткани переносчика глюкозы 4 (GLUT4), повышая чувствительность к инсулину у нормальных мышей и мышей с ожирением ob/ob, и повышая поглощение глюкозы в первичных адипоцитах in vitro (Xu et al., Proc. Natl. Acad. Sci. USA 101:3112-7, 2004). У человека однонуклеотидный полиморфизм (SNP) в гене Kv1.3 также ассоциирован со снижением чувствительности к инсулину и нарушением толерантности к глюкозе (Tschritter, Clin Endocrinol Metab 91: 654-8, 2006).
Kv1.3 также экспрессируется в пролиферирующих гладкомышечных клетках человека и мыши. Блокаторы Kv1.3 могут быть эффективными при гладкомышечных пролиферативных нарушениях, таких как рестеноз, например, у пациентов после сосудистой хирургической операции (например, ангиопластика). Было показано, что блокаторы Kv1.3 ингибируют вхождение кальция, снижают миграцию гладкомышечных клеток и ингибируют гиперплазию неоинтимы в образцах вен человека ex vivo (Cheong et al., Cardiovasc. Res. 89:282-9, 2011).
Дальнейшие данные указывают на то, что каналы Kv1.3 вовлечены в активацию и/или пролиферацию многих типов клеток, включая опухолевые клетки (Bielanska et al., Curr. Cancer Drug Targets 9:904-14, 2009), микроглию (Khanna et al., Am. J. Physiol. Cell Physiol. 280: C796-806, 2001), и дифференцировку нейрональных клеток-предшественников (Wang et al., J. Neurosci. 30:5020-7, 2010). Таким образом, блокаторы Kv1.3 могут быть полезными для лечения нейровоспалительных и нейродегенеративных нарушений и злокачественных опухолей.
Kv1.3 является частью подсемейства близкородственных калиевых каналов, обозначаемых от Kv1.1 до Kv1.8. Когда речь идет о больших гомологичных семействах, всегда является желательным, чтобы блокатор был настолько селективным и специфичным, насколько это возможно, в отношении желаемой мишени, для повышения эффективности и безопасности и избегания нежелательных эффектов вне мишени. Наиболее специфическими блокаторами Kv1.3, идентифицированными на сегодняшний день, являются пептиды ядов, происходящих из различных типов ядовитых организмов, таких как змеи, паукообразные (такие как скорпионы и пауки), морские анемоны и т.д. Такие блокаторы Kv1.3 включают пептиды ShK, Oskl, маргатоксина и калиотоксина, рассмотренные Chandy et al., Trends in Pharmacol. Sci. 25:280-9, 2004. Также см. Abdel-Mottaleb et al., Toxicon 51:1424-30, 2008, и Mouhat et al., Biochem. J. 385(Pt 1):95-104, 2005.
Различные попытки сконструировать пептиды токсинов для конкретных свойств, включая специфичность или эффективность, описаны, например, в WO2006/002850, WO2006/042151, WO2008/088422, WO2006/116156, WO2010/105184 и WO2014/116937.
Однако остается потребность в альтернативных блокаторах Kv1.3. В частности, могут быть желательными блокаторы, имеющие повышенную специфичность по сравнению с известными блокаторами, хотя также может быть пригодным улучшение других свойств, таких как стабильность и эффективность.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Изобретение относится к блокаторам ионных каналов из скорпиона Parabuthus transvaalicus, имеющим аминокислотные последовательности:
QMDMRCSASVECKQKCLKAIGSIFGKCMNKKCKCYPR (PaT1); и
QMDMRCSASVECKQKCLKAIGRGFGKCMNKKCKCYPR (PaT2);
и их варианты.
Было обнаружено, что, среди других желательных свойств, эти молекулы являются чрезвычайно селективными блокаторами Kv1.3 относительно других потенциалзависимых калиевых каналов и, как правило, они также обладают высокой эффективностью в отношении канала Kv1.3.
Таким образом, изобретение относится к блокатору ионного канала, содержащему ингибирующий Kv1.3 компонент, причем указанный ингибирующий Kv1.3 компонент содержит:
последовательность PaT1:
QMDMRCSASVECKQKCLKAIGSIFGKCMNKKCKCYPR;
или ее вариант, который отличается от PaT1 на вплоть до 9 замен, инсерций или делеций, где любые замены или делеции находятся в положениях аминокислот, выбранных из положений 1-5, 7-11, 13-15, 17-23, 25, 28-31, 33 и 35-37; и
где указанный ингибирующий Kv1.3 компонент обладает активностью ингибирования Kv1.3 и является селективным в отношении Kv1.3;
или его фармацевтически приемлемой соли.
Таким образом, ингибирующий Kv1.3 компонент блокатора ионного канала может содержать вплоть до 9 изменений аминокислот по сравнению с последовательностью PaT1. За исключением случаев, когда указано иное, каждое из этих 9 изменений может быть независимо выбрано из одной аминокислотной инсерции, делеции или замены. В одном варианте осуществления ингибирующий Kv1.3 компонент блокатора ионного канала может содержать 9, 8, 7, 6, 5, 4, 3, 2 или 1 изменений аминокислот по сравнению с последовательностью PaT1. В одном варианте осуществления ингибирующий Kv1.3 компонент блокатора ионного канала содержит 6 изменений аминокислот по сравнению с последовательностью PaT1.
Аминокислотные остатки PaT1 пронумерованы от 1 до 33в традиционном направлении от N- к C-концу. На протяжении настоящего описания аминокислотные положения в вариантах PaT1 пронумерованы в соответствии с соответствующим положением в PaT1 при оптимальном выравнивании с ней. Таким образом, в частности, для ингибиторов, которые содержат одну или несколько инсерций или делеций по сравнению с PaT1, нумерация любого данного остатка отражает соответствующий остаток в PaT1 и не обязательно отражает его линейное положение в соответствующей последовательности.
Остаток, присутствующий в конкретном положении, может быть указан посредством номера соответствующего положения вместе с однобуквенным кодом или трехбуквенным кодом для присутствующего остатка. Таким образом, 1Q или Q1 (эти два формата являются взаимозаменяемыми) указывают на остаток глутамина (Q) в положении 1, в то время как 2Nle, 2[Nle], Nle2 или [Nle]2 указывают на остаток норлейцина в положении 2.
Звездочка может использоваться для обозначения положения делеции относительно последовательности PaT1. Например, "1*" указывает на делецию остатка в положении 1 по сравнению с PaT1.
Инсерция может быть указана посредством цепи последовательно расположенных остатков в одном положении, например "1QA" указывает на инсерцию остатка аланина (A) после остатка глутамина (Q) в положении 1.
В некоторых вариантах осуществления может быть желательным, чтобы одно или несколько из положений 28, 31, 34, 35, 36 или 37 были идентичны соответствующим положениям в PaT1, т.е. остаток, присутствующий в соответствующем положении(ях), был идентичен остатку, присутствующему в PaT1 в соответствующем положении. Например, одно или несколько из положений 28, 31, 34 и 35 могут быть идентичны соответствующему положению в PaT1. В некоторых вариантах осуществления все из положений 28, 31, 34 и 35 являются идентичными соответствующим положениям в PaT1, например, все из положений 28, 31, 34, 35, 36 и 37 являются идентичными соответствующим положениям в PaT1.
Может быть желательным, чтобы любые замены по сравнению с PaT1 представляли собой консервативные замены. Однако любая замена, приведенная в любой из генетических формул, описанных ниже, может быть внесена в соответствующее положение.
Ингибирующий Kv1.3 компонент молекулы может содержать последовательность PaT1:
QMDMRCSASVECKQKCLKAIGSIFGKCMNKKCKCYPR
или может отличаться от PaT1 на вплоть до 9 замен, инсерций или делеций, где какие-либо замены или делеции внесены только в соответствующие положения, где в случае, если она отличается от PaT1:
остаток в положении 1 выбран из N, P, I, V, H, Y и S или удален;
остаток в положении 2 выбран из Nle, I, V, L, T, Q и E или удален;
остаток в положении 3 выбран из E, S и N или удален;
остаток в положении 4 выбран из Nle, I, V, L, A, E и S или удален;
остаток в положении 5 выбран из K, Q, A, L, E и D или удален;
остаток в положении 7 выбран из K, R, Q, E, F и A;
остаток в положении 8 выбран из I, H, S, L, Y и G;
остаток в положении 9 выбран из A, Abu, P, F, V и L;
остаток в положении 10 выбран из R, K, P, A, Q и L;
остаток в положении 11 выбран из Q и D;
остаток в положении 13 выбран из L, A, E, Q, I, K, H, D, V и G;
остаток в положении 14 выбран из V, K, E, L, D и 2-амино-5-карбоксипентаноила;
остаток в положении 15 выбран из S, L и P;
остаток в положении 17 выбран из K, Y, R, Q, D, V и E или удален;
остаток в положении 18 выбран из D, A, Y, G, V, Q, hQ и L или удален;
остаток в положении 19 выбран из R, Y и Q или удален;
остаток в положении 20 выбран из Y, E и R или удален;
остаток в положении 21 выбран из R, H, E и D;
остаток в положении 22 выбран из R, M, D, L и C;
остаток в положении 23 выбран из R, K, hK, P, G и H;
остаток в положении 26 представляет собой гомолизин;
остаток в положении 28 выбран из Nle, A и L;
остаток в положении 29 представляет собой V;
остаток в положении 30 выбран из G и D;
остаток в положении 31 выбран из D, Q, E и H;
остаток в положении 33 выбран из H, V, D, Q и R;
остаток в положении 35 выбран из T, F(4-NH2), F(4-F), F(4-NO2) и F(4-CH3);
остаток в положении 36 выбран из Q, S и G или удален;
остаток в положении 37 выбран из K, E, S и C или удален.
Ингибирующий Kv1.3 компонент молекулы может содержать последовательность PaT1:
QMDMRCSASVECKQKCLKAIGSIFGKCMNKKCKCYPR
или может отличаться от PaT1 на вплоть до 9 замен, инсерций или делеций, где какие-либо замены или делеции внесены только в следующих положениях, где в случае, если она отличается от PaT1:
остаток в положении 1 выбран из N, P, I, V, H, Y и S или удален;
остаток в положении 2 выбран из Nle, I, V, L, T, Q и E или удален;
остаток в положении 3 выбран из E, S и N или удален;
остаток в положении 4 выбран из Nle, I, V, L, A, E и S или удален;
остаток в положении 5 выбран из K, Q, A, L, E и D или удален;
остаток в положении 7 выбран из K, R, Q и A;
остаток в положении 8 выбран из I, H и G;
остаток в положении 9 выбран из A, Abu и L;
остаток в положении 10 выбран из R, K, P, A и L;
остаток в положении 11 выбран из Q и D;
остаток в положении 13 выбран из L, A, E, Q, I, K, H, D, V и G;
остаток в положении 14 выбран из V, K, E, L, D и 2-амино-5-карбоксипентаноила;
остаток в положении 15 выбран из S, L и P;
остаток в положении 17 выбран из K, Y, R, Q, D, V и E или удален;
остаток в положении 18 выбран из D, A, Y, G, V, Q, hQ и L или удален;
остаток в положении 19 выбран из R, Y и Q или удален;
остаток в положении 20 выбран из Y, E и R или удален;
остаток в положении 21 выбран из R, H, E и D;
остаток в положении 22 выбран из R, M, D, L и C;
остаток в положении 23 выбран из R, K, hK, P, G и H;
остаток в положении 28 выбран из Nle, A и L;
остаток в положении 29 представляет собой V;
остаток в положении 30 выбран из G и D;
остаток в положении 31 выбран из D, Q, E и H;
остаток в положении 33 выбран из H, V, D, Q и R;
остаток в положении 35 выбран из T, F(4-NH2), F(4-F), F(4-NO2) и F(4-CH3);
остаток в положении 36 выбран из Q, S и G или удален;
остаток в положении 37 выбран из K, E, S и C или удален.
В некоторых вариантах осуществления ингибирующий Kv1.3 компонент может отличаться от PaT1 на вплоть до 9 замен, инсерций или делеций, где какие-либо замены или делеции внесены только в следующих положениях, где в случае, если она отличается от PaT1:
остаток в положении 1 выбран из N, P, I, V, H, Y и S или удален;
остаток в положении 2 выбран из Nle, I, V, L, T, Q и E или удален;
остаток в положении 3 выбран из E, S и N или удален;
остаток в положении 4 выбран из Nle, I, V, L, A, E и S или удален;
остаток в положении 5 выбран из K, Q, A и L или удален;
остаток в положении 7 выбран из K, R и Q;
остаток в положении 8 выбран из I, H, S, L, Y и G;
остаток в положении 9 выбран из A, Abu, P, F, V и L;
остаток в положении 10 выбран из R, K и P;
остаток в положении 11 представляет собой Q;
остаток в положении 13 выбран из L, A, E, Q, I, K, H и G;
остаток в положении 14 выбран из V, K, E, L и 2-амино-5-карбоксипентаноила;
остаток в положении 15 выбран из S и L;
остаток в положении 17 выбран из K, Y, R, Q и D или удален;
остаток в положении 18 выбран из D, A, Y, G, V, Q, hQ и L или удален;
остаток в положении 19 выбран из R, Y и Q или удален;
остаток в положении 20 выбран из Y, E и R или удален;
остаток в положении 21 выбран из R, H и E;
остаток в положении 22 выбран из R, M, D, L и C;
остаток в положении 23 выбран из R, K, hK, P и G;
остаток в положении 28 представляет собой Nle;
остаток в положении 30 выбран из G и D;
остаток в положении 31 выбран из D, Q, E и H;
остаток в положении 33 выбран из H, V, D, Q и R;
остаток в положении 35 выбран из T, F(4-NH2), F(4-F), F(4-NO2) и F(4-CH3);
остаток в положении 36 выбран из Q, S и G или удален;
остаток в положении 37 выбран из K, S и C или удален.
В некоторых вариантах осуществления ингибирующий Kv1.3 компонент может отличаться от PaT1 на вплоть до 9 замен, инсерций или делеций, где какие-либо замены или делеции внесены только в следующих положениях, где в случае, если она отличается от PaT1:
остаток в положении 1 выбран из N, P, I, V, H, Y и S или удален;
остаток в положении 2 выбран из Nle, I, V, L, T, Q и E или удален;
остаток в положении 3 выбран из E, S и N или удален;
остаток в положении 4 выбран из Nle, I, V, L, A, E и S или удален;
остаток в положении 5 выбран из K, Q, A и L или удален;
остаток в положении 7 выбран из K, R и Q;
остаток в положении 8 выбран из I, H и G;
остаток в положении 9 выбран из A, Abu и L;
остаток в положении 10 выбран из R, K и P;
остаток в положении 11 представляет собой Q;
остаток в положении 13 выбран из L, A, E, Q, I, K, H и G;
остаток в положении 14 выбран из V, K, E, L и 2-амино-5-карбоксипентаноила;
остаток в положении 15 выбран из S и L;
остаток в положении 17 выбран из K, Y, R, Q и D или удален;
остаток в положении 18 выбран из D, A, Y, G, V, Q, hQ и L или удален;
остаток в положении 19 выбран из R, Y и Q или удален;
остаток в положении 20 выбран из Y, E и R или удален;
остаток в положении 21 выбран из R, H и E;
остаток в положении 22 выбран из R, M, D, L и C;
остаток в положении 23 выбран из R, K, hK, P и G;
остаток в положении 28 представляет собой Nle;
остаток в положении 30 выбран из G и D;
остаток в положении 31 выбран из D, Q, E и H;
остаток в положении 33 выбран из H, V, D, Q и R;
остаток в положении 35 выбран из T, F(4-NH2), F(4-F), F(4-NO2) и F(4-CH3);
остаток в положении 36 выбран из Q, S и G или удален;
остаток в положении 37 выбран из K, S и C или удален.
Ингибирующий Kv1.3 компонент молекулы может содержать последовательность PaT1:
QMDMRCSASVECKQKCLKAIGSIFGKCMNKKCKCYPR
или может отличаться от PaT1 на вплоть до 9 замен, инсерций или делеций, где какие-либо замены или делеции внесены только в следующих положениях, где в случае, если она отличается от PaT1:
остаток в положении 1 выбран из N, P, V, H, Y и S или удален;
остаток в положении 2 выбран из Nle, I, V и L или удален;
остаток в положении 3 выбран из E и S или удален;
остаток в положении 4 выбран из Nle, I, V, L, E и S или удален;
остаток в положении 5 представляет собой K или удален;
остаток в положении 7 выбран из K и R;
остаток в положении 8 выбран из I и H;
остаток в положении 9 выбран из Abu и L;
остаток в положении 10 выбран из R и K;
остаток в положении 11 представляет собой Q;
остаток в положении 13 выбран из L, A, E, Q, V и G;
остаток в положении 14 выбран из V, K, E, L и 2-амино-5-карбоксипентаноила;
остаток в положении 15 выбран из S и L;
остаток в положении 17 выбран из K, Y и R или удален;
остаток в положении 18 выбран из D, A, Y, G, V, Q, hQ и L или удален;
остаток в положении 19 выбран из R и Y или удален;
остаток в положении 20 выбран из Y, E и R или удален;
остаток в положении 21 выбран из R, H и E;
остаток в положении 22 выбран из R и C;
остаток в положении 23 выбран из R, K, hK, P и G;
остаток в положении 28 представляет собой Nle;
остаток в положении 30 представляет собой G;
остаток в положении 33 выбран из H, V и R;
остаток в положении 35 выбран из F(4-NH2), F(4-F), F(4-NO2) и F(4-CH3);
остаток в положении 36 выбран из Q, S и G или удален;
остаток в положении 37 выбран из S и C или удален.
В некоторых вариантах осуществления ингибирующий Kv1.3 компонент молекулы содержит последовательность PaT1:
QMDMRCSASVECKQKCLKAIGSIFGKCMNKKCKCYPR
или отличается от PaT1 на вплоть до 9 замен, инсерций или делеций, где какие-либо замены или делеции внесены только в следующих положениях, где в случае, если она отличается от PaT1:
остаток в положении 1 выбран из N и P или удален;
остаток в положении 2 представляет собой Nle, I, V и L;
остаток в положении 3 выбран из E и S;
остаток в положении 4 представляет собой Nle, I, V и L;
остаток в положении 8 представляет собой I;
остаток в положении 10 представляет собой R;
остаток в положении 11 представляет собой Q;
остаток в положении 13 представляет собой A;
остаток в положении 14 представляет собой V;
остаток в положении 18 выбран из D, Y и A;
остаток в положении 19 представляет собой R;
остаток в положении 20 представляет собой Y;
остаток в положении 21 представляет собой R;
остаток в положении 22 выбран из R и C;
остаток в положении 23 выбран из R и G;
остаток в положении 28 представляет собой Nle;
остаток в положении 30 представляет собой G;
остаток в положении 33 представляет собой H;
остаток в положении 37 представляет собой C.
В некоторых вариантах осуществления изобретение относится к блокатору ионных каналов, содержащему ингибирующий Kv1.3 компонент, причем указанный ингибирующий Kv1.3 компонент содержит:
последовательность PaT1:
QMDMRCSASVECKQKCLKAIGSIFGKCMNKKCKCYPR;
или последовательность, которая обладает по меньшей мере 75% идентичностью с последовательностью PaT1, где какие-либо отличия от последовательности PaT1 находятся в положениях аминокислот, выбранных из положений 1-5, 7-11, 13-15, 17-23, 25, 28-31, 33 и 35-37; и
где указанный ингибирующий Kv1.3 компонент обладает активностью ингибирования Kv1.3 и является селективным в отношении Kv1.3;
или его фармацевтически приемлемую соль.
В некоторых вариантах осуществления ингибирующий Kv1.3 компонент обладает по меньшей мере 75% идентичностью с последовательностью PaT1. В некоторых вариантах осуществления ингибирующий Kv1.3 компонент обладает по меньшей мере 80% идентичностью с последовательностью PaT1. В некоторых вариантах осуществления ингибирующий Kv1.3 компонент обладает по меньшей мере 85% идентичностью с последовательностью PaT1. В некоторых вариантах осуществления ингибирующий Kv1.3 компонент обладает по меньшей мере 90% идентичностью с последовательностью PaT1. В некоторых вариантах осуществления ингибирующий Kv1.3 компонент обладает по меньшей мере 95% идентичностью с последовательностью PaT1. В некоторых вариантах осуществления ингибирующий Kv1.3 компонент обладает по меньшей мере 97% идентичностью с последовательностью PaT1.
Ингибирующий Kv1.3 компонент может содержать одну или несколько инсерций или делеций по сравнению с последовательностью PaT1.
Как правило, ингибирующий Kv1.3 компонент содержит максимум три инсерции по сравнению с последовательностью PaT1, например, точно 3 инсерции, точно 2 инсерции или точно 1 инсерцию.
Как правило, только одна аминокислота встроена в любой данный участок, хотя могут быть допустимыми инсерции нескольких аминокислот.Во избежание сомнений инсерция двух аминокислот в одном участке считается двумя инсерциями и, таким образом, двумя из допустимых отличий от последовательности PaT1.
Как правило, ингибирующий Kv1.3 компонент содержит не более 7 делеций по сравнению с последовательностью PaT1, например, не более 6, не более 5, не более 5, не более 4, не более 3, не более 2 делеций, не более одной делеции или вообще не содержит делеций.
Для сохранения расстояния между остатками цистеина и, таким образом, паттерна образования дисульфидных связей, может быть желательным, чтобы никакие инсерции и делеции не находились между остатком цистеина в положении 6 (6C) и остатком цистеина в положении 34 (34C). Таким образом, любая инсерция или делеция предпочтительно может находиться с N-концевой стороны от 6C или C-концевой стороны от 34C.
Однако, если ингибирующий Kv1.3 компонент содержит одну или несколько инсерций или делеций между 6C и 34C, тогда может быть желательным включение одного и того же количества обеих инсерций и делеций в эту область, например, для восстановления относительного расстояния между остатками цистеина.
Во многих вариантах осуществления ингибирующий Kv1.3 компонент не имеет инсерций по сравнению с последовательностью PaT1.
Если между 6C и 34C присутствует делеция, может быть желательно, чтобы присутствовала только одна такая делеция. Она может находиться, например, в положении 17, 18, 19 или 20, особенно если молекула не содержит соответствующую инсерцию для сохранения расстояния между остатками цистеина.
Без связи с теорией, полагают, что множественные делеции в большей степени допустимы на N-концевой последовательности (остатки 1-5) и C-концевой последовательности (остатки 36-37). В этих областях могут быть допустимыми множественные делеции. Для делеций в N-концевой последовательности (положения 1-5), если остаток в положении X удален, может быть желательным, чтобы все остатки с N-концевой стороны от этого остатка также были удалены. Таким образом, например, могут быть удалены, например, остатки 1, 1 и 2, 1-3, 1-4 или 1-5. Для делеций на C-конце (положения 36-37), если остаток в положении 36 удален, может быть желательным, чтобы остаток в положении 37 также был удален. Таким образом, например, могут быть удалены остатки 37, или 36 и 37.
Во избежание сомнений, делеция двух последовательно расположенных аминокислот считается двумя аминокислотными делециями и, таким образом, двумя из допустимых отличий от последовательности PaT1.
Остатки глутамина (Q) могут быть нестабильными, как in vivo, так и in vitro, например, в ходе хранения в водном растворе. Это может иметь особое значение, когда остаток глутамина находится на N-конце молекулы, поскольку боковая цепь может быть пространственно способна взаимодействовать со свободной альфа-аминогруппой, что приводит к дегидратации до пироглутамата. Таким образом, может быть желательным, чтобы остаток в положении 1 не являлся Q, в частности, если блокатор ионного канала не содержит никакой дополнительной последовательности с N-концевой стороны ингибитора Kv1.3. Например, остаток в положении 1 может представлять собой N или P, или может быть удален; т.е. ингибитор Kv1.3 может содержать 1N, 1P или 1*.
Дополнительно или альтернативно, может быть желательным, чтобы один, два или все три из остатков в положениях 2, 4 и 28 не являлись M, поскольку остатки метионина (M) подвержены окислению. Предпочтительно один, два или все три остатка метионина либо индивидуально заменены остатком, имеющим не окисляемую боковую цепь, либо удалены. Можно использовать любой подходящий не окисляемый остаток, причем особенно предпочтительными являются Nle, I, V и L.
Подходящие комбинации остатков в некоторых или всех из положений 2, 4 и 28 включают:
2*+4Nle, 4I, 4V или 4L;
2Nle+4Nle, 4I, 4V или 4L;
2I+4Nle, 4I, 4V или 4L;
2V+4Nle, 4I, 4V или 4L;
2L+4Nle, 4I, 4V или 4L.
Любую из указанных выше можно комбинировать с 28Nle.
Особенно предпочтительной может быть 2Nle+4Nle+28Nle.
В некоторых вариантах осуществления ингибирующий Kv1.3 компонент содержит остатки 22S+23I или 22R+23G.
В дополнение к каким-либо отличиям в положениях 1, 2, 4 и 28, может быть желательно, чтобы ингибирующий Kv1.3 компонент содержал только 4 дополнительных отличия, только 3 дополнительных отличия, только 2 дополнительных отличия или только 1 дополнительное отличие от последовательности PaT1.
Ингибирующий Kv1.3 компонент может быть идентичен PaT1 или PaT2 во всех положениях кроме положений 1, 2, 4 и 28.
Дополнительно или альтернативно, ингибирующий Kv1.3 компонент может содержать остатки 13A и/или 18A.
Например, он может содержать
2Nle+13A;
2Nle+18A, или
2Nle+13A+18A.
Например, он может содержать
2Nle+4Nle+13A+28Nle;
2Nle+4Nle+18A+28Nle; или
2Nle+4Nle+13A+18A+28Nle.
Любую из указанных выше комбинаций можно комбинировать с 1*.
Ингибирующий Kv1.3 компонент может быть идентичен PaT1 или PaT2 во всех положениях кроме положений 2, 3 и 4.
Дополнительно или альтернативно, ингибирующий Kv1.3 компонент может содержать остатки 1P и/или 18A.
Например, он может содержать
2Nle+4Nle+28Nle;
2Nle+3E+4Nle+28Nle;
2Nle+3E+4Nle+18A+28Nle;
1P+2Nle+4Nle+28Nle;
1P+2Nle+3E+4Nle+28Nle; или
1P+2Nle+3E+4Nle+18A+28Nle.
Дополнительно или альтернативно, любую из вышеуказанных комбинаций можно комбинировать с 22C+37C, т.е. остатками в положениях 22 и 37, способными образовывать дисульфидную связь.
Блокатор ионного канала может содержать дополнительные аминокислотные последовательности с N-концевой и/или C-концевой стороны от ингибирующего Kv1.3 компонента. Например, блокатор ионного канала может представлять собой слитый белок, содержащий ингибитор Kv1.3 и одну или несколько гетерологичных пептидных или полипептидных последовательностей, которые могут упоминаться как гетерологичные компоненты. Гетерологичные компоненты могут служить, например, для способствования рекомбинантной экспрессии, повышения растворимости или продления времени полужизни in vivo. Подходящие гетерологичные компоненты включают сывороточный альбумин человека (HSA), Fc-домен антитела и т.д.
Другие гетерологичные компоненты включают метки, такие как полигистидиновая метка, FLAG-метка или Myc-метка.
Блокатор ионного канала может содержать линкерный пептид, находящийся между ингибитором Kv1.3 и гетерологичным компонентом.
Различные компоненты могут иметь любую подходящую ориентацию. Например, ингибитор Kv1.3 может находиться с N-концевой стороны от гетерологичного компонента, или гетерологичный компонент может находиться с N-концевой стороны ингибитора Kv1.3 с линкером (когда он присутствует) между ними.
Длина пептидного линкера, как правило, составляет от 3 до 30 аминокислот с большой долей небольших и гидрофильных аминокислотных остатков (например, глицин и серин) для обеспечения требуемой гибкости без нарушения растворимости молекулы в воде. Например, он может содержать по меньшей мере 50% остатков глицина и серина, по меньшей мере 60% остатков глицина и серина, по меньшей мере 70% остатков глицина и серина, по меньшей мере 80% остатков глицина и серина или по меньшей мере 90% остатков глицина и серина. Также он может содержать участок расщепления протеазой для обеспечения разделения ингибитора Kv1.3 и гетерологичного компонента.
Ингибитор Kv1.3 также может быть встроен в гетерологичный полипептид, который может считаться "каркасом" для ингибитора Kv1.3. В таких случаях можно считать, что блокатор ионных содержит гетерологичные компоненты с N- и C-концевой стороны от ингибитора Kv1.3, где гетерологичные компоненты происходят из одной и той же молекулы и взаимодействуют друг с другом, например, укладываясь в каркас, имеющий экспонированный на его поверхности ингибитор Kv1.3. Таким образом, ингибитор Kv1.3 может быть встроен в поверхностную петлю гетерологичного белка, например, в последовательность CDR антитела или его фрагмента, содержащего антигенсвязывающий домен. Было продемонстрировано, что ингибитор Kv1.3 сохраняет активность, когда он встроен в CDR (например CDR3L) гуманизированного иммуноглобулина, обозначаемого как "Syn", направленного против респираторно-синцитиального вируса (Wang et al., Proc. Natl. Acad. Sci. USA 113(41), 11501-11506, 2016.). Таким образом, антитело Syn или его фрагмент, содержащий антигенсвязывающий домен, можно использовать в качестве каркаса. Если каркас антитела содержит Fc-домен, может быть желательно, чтобы он функционально был Fc-нулевым", т.е. неспособным связываться с Fc-рецептором. Такие мутации описаны Wang et al., в цитируемом документе.
В некоторых вариантах осуществления блокатор ионного канала может иметь максимальную длину 200 аминокислот, например 150 аминокислот, 125 аминокислот, 100 аминокислот, 75 аминокислот или 50 аминокислот, например 49, 48, 47, 46, 45, 44, 43, 42, 41, 40, 39, 38 или 37 аминокислот, или может быть даже более коротким, где ингибирующий Kv1.3 компонент содержит одну или несколько делеций по сравнению с последовательностью PaT1.
Блокатор ионного канала, кроме того, может содержать вплоть до 10 дополнительных остатков на N-конце, например 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 дополнительных остатков на N-конце. Дополнительно или альтернативно блокатор ионного канала может, кроме того, содержать вплоть до 10 остатков на C-конце, например 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 дополнительных остатков на C-конце, ограничиваясь тем, что молекула имеет длину не более 50 аминокислот.
Например, дополнительная последовательность на N-конце может содержать или состоять из последовательности GG или SG. Дополнительно или альтернативно, дополнительная последовательность на C-конце может содержать или состоять из последовательности RRTA, HRRK, QSKA, AGPR, RSRT, RHKR, GGKR, PKTA, TDAR, HRQQ, RPRH, ARNA, TGRK, HERT, NTRT, QRNG, AHRN, PRSA, QRQS, QRRK, ARAK, AKRD, RDKT, HRRK, RAKR, QRTR, ATRH, ARRS, AKTR, NRQR, PRNT, например RRTA или HRRK. Было показано, что все из этих последовательностей являются совместимыми с активностью и селективностью ингибитора Kv1.3 при добавлении на C-конец аналогов Odk2 (см. WO 12014/116937).
Таким образом, изобретение также относится к блокатору ионных каналов, имеющему формулу:
R1-Z1-X-Z2-R2
где
R1 представляет собой водород, C1-4 алкил, ацетил, формил, бензоил или трифторацетил;
R2 представляет собой OH, NH2 или CH2OH,
X представляет собой ингибитор Kv1.3, имеющий последовательность PaT1 или ее вариант, как описано выше, и
Z1 и Z2 независимо представляют собой последовательности из вплоть до 10 аминокислотных остатков;
при условии, что блокатор ионного канала имеет максимальную длину 50 аминокислот;
или его фармацевтически приемлемой соли.
Как указано выше, Z1 может содержать или состоять из последовательности GG или SG.
Дополнительно или альтернативно Z2, может содержать или состоять из последовательности RRTA, HRRK, QSKA, AGPR, RSRT, RHKR, GGKR, PKTA, TDAR, HRQQ, RPRH, ARNA, TGRK, HERT, NTRT, QRNG, AHRN, PRSA, QRQS, QRRK, ARAK, AKRD, RDKT, HRRK, RAKR, QRTR, ATRH, ARRS, AKTR, NRQR, PRNT, например, RRTA или HRRK.
Дополнительно или альтернативно, R2 может представлять собой CH2OH и может содержаться в (4-амино-5-гидроксипентил)гуанидине или 4-амино-5-гидроксипентанамиде.
Ингибирующий Kv1.3 компонент молекулы содержит 6 остатков цистеина (C), которые вместе образуют три дисульфидных связи между остатками 6C и 27C, остатками 12C и 32C, и остатками 16C и 34C. Полагают, что эти связи являются важными для конформации и активности ингибитора Kv1.3.
Дисульфидные связи могут быть графически указаны следующим образом относительно PaT1:
QMDMR[C(1)]SASVE[C(2)]KQK[C(3)]LKAIGSIFGK[C(1)]MNKK[C(2)]K[C(3)]YPR
где пара остатков цистеина, которые вместе участвуют в образовании дисульфидной связи, указана одним и тем же числом в скобках. Сходное указание может применяться для любых других последовательностей в настоящей заявке. За исключением случаев, когда контекстом требуется иное, следует понимать, что активное ингибиторное соединение включает наличие соответствующих дисульфидных связей.
Может быть желательным, чтобы никакие другие остатки цистеина не были внесены в ингибирующий Kv1.3 компонент путем замены. Дополнительно или альтернативно, может быть желательно, чтобы никакие остатки цистеина не присутствовали ни в одной из N- или C-концевых дополнительных последовательностей. Таким образом, в некоторых вариантах осуществления молекула не содержит остатков цистеина помимо остатков цистеина в положениях 6, 12, 16, 27, 32 и 34 PaT1.
Однако в некоторых вариантах осуществления ингибиторный компонент содержит 8 остатков цистеина, которые вместе образуют четыре дисульфидных связи между остатками 6C и 27C, остатками 12C и 32C, остатками 16C и 34C, и остатками цистеина в положениях, соответствующих положениям 22 и 37 Pat1. Примером такой молекулы является соединение 87 и образование дисульфидных связей может быть графически показано следующим образом:
H-S[Nle]D[Nle]R[C(1)]SASVE[C(2)]KQK[C(3)]LAAIG[C(4)]IFGK[C(1)][Nle]NKK[C(2)]K[C(3)]YP[C(4)]-NH2
Сходное обозначение может применяться для других соединений, имеющих четыре пары дисульфидных связей.
Таким образом, ингибитор, как правило, имеет остатки цистеина в положениях 22 и 37, или ни одно из положений 22 и 37 не является остатком цистеина (т.е. оба из положений 22 и 37 не являются цистеином).
Ингибирующий Kv1.3 компонент может содержать одну из следующих последовательностей:
Блокаторы ионных каналов могут содержать или состоять из любых из следующих последовательностей:
В некоторых вариантах осуществления блокатор ионного канала не имеет последовательность:
QMDMRCSASVECKQKCLKAIGSIFGKCMNKKCKCYPR
или
QMDMRCSASVECKQKCLKAIGRGFGKCMNKKCKCYPR.
В некоторых вариантах осуществления R1 представляет собой H и R2 представляет собой NH2 или OH. В некоторых вариантах осуществления может быть желательным, чтобы R2 представлял собой OH.
Блокаторы ионных каналов включают следующие:
В одном из вариантов осуществления блокатор ионного канала представляет собой:
H-P[Nle]E[Nle]RCSASVECKQKCLAAIGSIFGKC[Nle]NKKCKCYPR-OH (соединение 97).
В некоторых вариантах осуществления блокатор ионного канала не является:
H-QMDMRCSASVECKQKCLKAIGSIFGKCMNKKCKCYPR-OH (соединение 1)
или
H-QMDMRCSASVECKQKCLKAIGRGFGKCMNKKCKCYPR-OH (соединение 2).
Кроме того, изобретение относится к нуклеиновой кислоте, кодирующей блокатор ионного канала, ингибитор Kv1.3 или пептид Z1-X-Z2, как описано.
Изобретение также относится к экспрессирующему вектору, содержащему нуклеиновую кислоту по изобретению.
Кроме того, изобретение относится к клетке-хозяину, содержащей нуклеиновую кислоту или экспрессирующий вектор по изобретению и способной экспрессировать блокатор ионного канала, ингибитор Kv1.3 или пептид Z1-X-Z2, как описано. Клетка-хозяин может быть способна секретировать блокатор ионного канала, ингибитор Kv1.3 или пептид Z1-X-Z2, как описано.
Кроме того, изобретение относится к способу синтеза блокатора ионного канала по изобретению, причем способ включает:
(a) синтез блокатора ионного канала посредством методологии твердофазного или жидкофазного пептидного синтеза и выделение полученного таким образом пептида;
(b) экспрессию блокатора ионного канала с конструкции нуклеиновой кислоты, которая кодирует блокатор ионного канала, и выделение продукта экспрессии; или
(c) экспрессию пептида-предшественника с конструкции нуклеиновой кислоты, которая кодирует последовательность пептида-предшественника, выделение продукта экспрессии и модификацию пептида-предшественника с получением блокатора ионного канала.
Кроме того, изобретение относится к фармацевтической композиции, содержащей блокатор ионного канала по изобретению или его фармацевтически приемлемую соль в смеси с фармацевтически приемлемым носителем.
Кроме того, изобретение относится к блокатору ионных каналов по изобретению или его фармацевтически приемлемой соли для применения в способе медикаментозного лечения.
Кроме того, изобретение относится к блокатору ионных каналов по изобретению или его фармацевтически приемлемой соли для применения в способе ингибирования или снижения воспаления, особенно для лечения воспалительного состояния или нарушения, в том числе аутоиммунных нарушений.
Воспалительное состояние или нарушение может представлять собой любое состояние или нарушение, при котором является желательным уменьшение воспаления, например, где воспаление участвует в симптомах или патогенезе.
Такие состояния включают аутоиммунные заболевания, аллергию и гиперчувствительность, отторжение аллотрансплантата и реакцию "трансплантат против хозяина".
Конкретные состояния включают сенную лихорадку, астму, анафилаксию, аллергический ринит, крапивницу, экзему, очаговую алопецию, дерматомиозит, миозит с тельцами включения, полимиозит, анкилозирующий спондилит, васкулит, артрит (включая ревматоидный артрит, остеоартрит, псориатический артрит), синдром Шегрена, системную красную волчанку (SLE, или просто "волчанка") и увеит, воспалительный фиброз (например склеродермия, фиброз легких, цирроз), хроническое обструктивное заболевание легких (COPD), гепатит, хроническую воспалительную демиелинизирующую полиневропатию, воспалительное заболевание кишечника, колит (включая болезнь Крона и язвенный колит), эритему, тиреоидит, псориаз, атопический дерматит, аллергический контактный дерматит, склеродермию, гломерулонефрит, воспалительную резорбцию кости, рассеянный склероз, диабет 1 типа, отторжение трансплантата и реакцию "трансплантат против хозяина".
Кроме того, изобретение относится к блокатору ионных каналов по изобретению или его фармацевтически приемлемой соли для применения в способе ингибирования увеличения массы тела, способствования снижению массы тела, снижения избыточной массы тела или лечения ожирения (например, посредством контроля аппетита, питания, приема пищи, употребления калорий и/или потребления энергии) или для лечения связанного с ожирением воспаления, связанного с ожирением заболевания желчного пузыря или индуцируемого ожирением апноэ во сне.
Эффект на массу тела может быть терапевтическим или косметическим.
Кроме того, изобретение относится к блокатору ионных каналов по изобретению или его фармацевтически приемлемой соли для применения для лечения состояния, вызванного или ассоциированного с нарушением контроля уровня глюкозы, такого как метаболический синдром, резистентность к инсулину, нарушение толерантности к глюкозе, преддиабет, повышение уровня глюкозы натощак или диабет 2 типа.
Кроме того, изобретение относится к блокатору ионных каналов по изобретению или его фармацевтически приемлемой соли для применения для лечения гладкомышечного пролиферативного нарушения, такого как рестеноз, например у пациентов после сосудистой хирургической операции (например, ангиопластика).
Кроме того, изобретение относится к блокатору ионных каналов по изобретению или его фармацевтически приемлемой соли для применения для лечения нейровоспалительного или нейродегенеративного нарушения, такого как болезнь Альцгеймера, рассеянный склероз (MS), болезнь Паркинсона или боковой амиотрофический склероз (ALS) (например, после вирусной инфекции).
Кроме того, изобретение относится к блокатору ионных каналов по изобретению или его фармацевтически приемлемой соли для применения для лечения злокачественной опухоли, например, рака молочной железы, рака предстательной железы или лимфомы, такой как неходжкинская лимфома (NHL). NHL включает T-клеточную NHL и B-клеточную NHL.
Формы B-клеточной NHL включают диффузную крупноклеточную B-клеточную лимфому, фолликулярную лимфому, лимфому Беркитта, иммунобластную крупноклеточную лимфому, B-лимфобластную лимфому из клеток-предшественников и лимфому из клеток мантийной зоны. Формы T-клеточной NHL включают фунгоидный микоз, анапластическую крупноклеточную лимфому, периферическую T-клеточную лимфому, T-лимфобластную лимфому из клеток-предшественников и синдром Сезари.
Кроме того, изобретение относится к применению блокатора ионного канала по изобретению или его фармацевтически приемлемой соли для получения лекарственного средства для ингибирования или снижения воспаления, особенно при лечении воспалительного состояния или нарушения, включая аутоиммунные нарушения. Дополнительные детали таких состояний указаны выше.
Кроме того, настоящее изобретение относится к применению блокатора ионного канала по изобретению или его фармацевтически приемлемой соли для получения лекарственного средства для применения для ингибирования увеличения массы тела, способствования снижению массы тела, снижения избыточной массы тела или лечения ожирения (например, посредством контроля аппетита, питания, приема пищи, употребления калорий и/или потребления энергии) или для лечения связанного с ожирением воспаления, связанного с ожирением заболевания желчного пузыря или индуцируемого ожирением апноэ во сне.
Кроме того, изобретение относится к применению блокатора ионного канала по изобретению или его фармацевтически приемлемой соли для получения лекарственного средства для лечения состояния, вызванного или ассоциированного с нарушением контроля уровня глюкозы, такого как метаболический синдром, резистентность к инсулину, нарушение толерантности к глюкозе, преддиабет, повышение уровня глюкозы натощак или диабет 2 типа.
Кроме того, изобретение относится к применению блокатора ионного канала по изобретению или его фармацевтически приемлемой соли для получения лекарственного средства для лечения гладкомышечного пролиферативного нарушения, такого как рестеноз, например у пациентов после сосудистой хирургической операции (например, ангиопластика).
Кроме того, изобретение относится к применению блокатора ионного канала по изобретению или его фармацевтически приемлемой соли для получения лекарственного средства для лечения нейровоспалительного или нейродегенеративного нарушения, такого как болезнь Альцгеймера, рассеянный склероз (MS), болезнь Паркинсона или боковой амиотрофический склероз (ALS) (например, после вирусной инфекции).
Кроме того, изобретение относится к применению блокатора ионного канала по изобретению или его фармацевтически приемлемой соли для получения лекарственного средства для лечения злокачественной опухоли, например, рака молочной железы, рака предстательной железы или лимфомы, такой как неходжкинская лимфома (NHL).
Кроме того, изобретение относится к способу ингибирования или уменьшения воспаления (особенно при лечении воспалительного состояния или нарушения, включая аутоиммунные нарушения), включающему введение блокатора ионного канала по изобретению или его фармацевтически приемлемой соли индивидууму, нуждающемуся в этом. Дополнительные детали таких состояний указаны выше.
Кроме того, изобретение относится к способу ингибирования увеличения массы тела, способствования снижению массы тела, снижения избыточной массы тела или лечения ожирения (например, посредством контроля аппетита, питания, приема пищи, употребления калорий и/или потребления энергии) или для лечения связанного с ожирением воспаления, связанного с ожирением заболевания желчного пузыря или индуцируемого ожирением апноэ во сне, включающему введение блокатора ионного канала по изобретению или его фармацевтически приемлемой соли индивидууму, нуждающемуся в этом.
Кроме того, изобретение относится к способу лечения состояния, вызванного или ассоциированного с нарушением контроля уровня глюкозы, такого как метаболический синдром, резистентность к инсулину, нарушение толерантности к глюкозе, преддиабет, повышение уровня глюкозы натощак или диабет 2 типа, включающему введение блокатора ионного канала по изобретению или его фармацевтически приемлемой соли индивидууму, нуждающемуся в этом.
Кроме того, изобретение относится к способу лечения гладкомышечного пролиферативного нарушения, такого как рестеноз, например у пациентов после сосудистой хирургической операции (например, ангиопластика), включающему введение блокатора ионного канала по изобретению или его фармацевтически приемлемой соли индивидууму, нуждающемуся в этом.
Кроме того, изобретение относится к способу лечения нейровоспалительного или нейродегенеративного нарушения, такого как болезнь Альцгеймера, рассеянный склероз (MS), болезнь Паркинсона или боковой амиотрофический склероз (ALS) (например, после вирусной инфекции), включающему введение блокатора ионного канала по изобретению или его фармацевтически приемлемой соли индивидууму, нуждающемуся в этом.
Кроме того, изобретение относится к способу лечения злокачественной опухоли, например, рака молочной железы, рака предстательной железы или лимфомы, такой как неходжкинская лимфома, включающему введение блокатора ионного канала по изобретению или его фармацевтически приемлемой соли индивидууму, нуждающемуся в этом.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Если в настоящем описании не определено иначе, научные и технические термины, используемые в этой заявке, имеют значения, которые обычно понятны специалистам в данной области. Как правило, номенклатура, используемая применительно к, и способы, химии, молекулярной биологии, клеточной биологии и биологии злокачественной опухоли, иммунологии, микробиологии, фармакологии, и химии белков и нуклеиновых кислот, описанные в настоящем описании, представляют собой номенклатуру и способы, хорошо известные и часто используемые в данной области.
Все патенты, опубликованные патентные заявки и непатентные публикации, упоминаемые в настоящей заявке, конкретно включены в качестве ссылок в настоящее описание. В случае противоречий, настоящее описание, включая его конкретные определения, имеет преимущество.
Каждый вариант осуществления изобретения, описанный в настоящем описании, может применяться отдельно или в комбинации с одним или несколькими другими вариантами осуществления изобретения.
Если нет иных указаний, следующие определения приводятся для конкретных терминов, которые используются в настоящем письменном описании.
На протяжении настоящего описания, слово "содержать", и его грамматические варианты, такие как "содержит" или "содержащий", подразумевают включение указанного целого числа или компонента, или группы целых чисел или компонентов, но не исключение любого другого целого числа или компонента, или группы целых чисел или компонентов.
Форма единственного числа включает множественное число, если контекст явно не определяет иное.
Термин "включая" используют для указания на "включая, но не ограничиваясь ими". "Включая" и "включая, но не ограничиваясь ими" могут использоваться взаимозаменяемо.
Термины "пациент", "субъект" и "индивидуум" могут использоваться взаимозаменяемо. Субъектом может быть млекопитающее, включая человека и не являющееся человеком млекопитающее, такое как не являющийся человеком примат (например, человекообразная обезьяна, старосветская мартышка или новосветская мартышка), сельскохозяйственное животное (например, животное подсемейства бычьих или семейства свиных), животное-компаньон (например, животное семейства собачьих или животное семейства кошачьих) или лабораторное животное, такое как грызун (например, мышь или крыса).
На протяжении настоящего описания и формулы изобретения используются общепринятые трехбуквенные и однобуквенные коды для встречающихся в природе аминокислот, т.е. A (Ala), G (Gly), L (Leu), I (Ile), V (Val), F (Phe), W (Trp), S (Ser), T (Thr), Y (Tyr), N (Asn), Q (Gln), D (Asp), E (Glu), K (Lys), R (Arg), H (His), M (Met), C (Cys) и P (Pro); а также общепризнанные коды для других α-аминокислот, таких как норлейцин (Nle), саркозин (Sar), α-аминоизомасляная кислота (Aib), 2,3-диаминопропионовая кислота (Dap), 2,4-диаминобутановая кислота (Dab), 2,5-диаминопентановая кислота (орнитин; Orn) альфа-аминомасляная кислота (Abu, также известная как гомоаланин), hK, hLys или гомо-Lys (гомолизин), hQ, hGln или гомо-Gln (гомо-глутамин, также известный как 6-оксолизин, L-5-карбамоилнорвалин, 6-амино-6-оксонорлейцин или 5-(аминокарбонил)норвалин), F(4-F) (4-фторфенилаланин), F(4-NH2) (4-аминофенилаланин), F(4-NO2) (4-нитрофенилаланин), F(4-CH3) (4-метилфенилаланин).
Обозначение [2-амино-5-карбоксипентаноил] указывает на пептидный остаток 2-амино-5-карбоксипентановой кислоты:
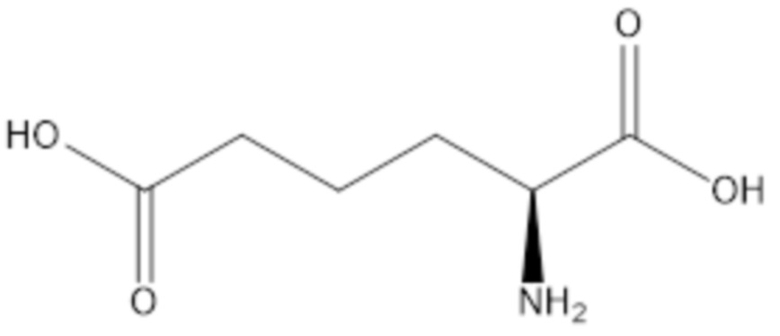
который, таким образом, имеет боковую цепь, сходную с боковой цепью глутаминовой кислоты, но с дополнительной метиленовой группой.
Такие другие α-аминокислоты могут быть показаны в квадратных скобках "[]" (например, "[Nle]") при использовании в общей формуле или последовательности в настоящем описании, особенно когда остальная часть формулы или последовательности показана с использованием однобуквенного кода. 20 "встречающихся в природ" аминокислот, приведенных выше, представляют собой аминокислоты, которые кодируются стандартным генетическим кодом, и также могут называться "протеиногенными" аминокислотами.
Если нет иных указаний, аминокислотные остатки в пептидах по изобретению имеют L-конфигурацию. Однако могут быть включены аминокислоты в D-конфигурации. В настоящем контексте код аминокислоты, указанный строчной буквой, указывает на D-конфигурацию указанной аминокислоты, например "k" обозначает D-конфигурацию лизина (K).
Часть "H" (или "Hy-") на N-конце рассматриваемой последовательности указывает на атом водорода [т.е. R1=водород], соответствующий присутствию свободной первичной или вторичной аминогруппы на N-конце, в то время как часть "-OH" или "-NH2" на C-конце последовательности [т.е. R2=OH или NH2] указывает на присутствие карбоксигруппы (COOH) или амидогруппы (CONH2) на C-конце молекулы. Часть "CH2OH" на C-конце [т.е. R2=CH2OH] указывает на присутствие гидроксильной группы, связанной с алкильной группой, на C-конце молекулы. Часть CH2OH может находиться в (4-амино-5-гидроксипентил)гуанидине или 4-амино-5-гидроксипентанамиде. Обозначения других групп R1 и R2 должны быть интерпретированы соответствующим образом.
БЛОКАТОРЫ KV1.3
Термин Kv1.3 используют для указания на представителя 3 подсемейства A потенциалзависимых калиевых каналов, также обозначаемого как KCNA3, HPCN3, HGK5, HuKIII и HLK3. "Подсемейство A" также может упоминаться как "shaker-родственное подсемейство". Аминокислотная последовательность человека приведена под номером доступа UniProt P22001, версия P22001.3 (Q5VWN2).
Канал Kv1.3 экспрессируется на T- и B-лимфоцитах и вовлечен в активацию T-клеток. Ряд групп стремится разработать блокаторы Kv1.3 для ингибирования иммунного ответа, для различных других показаний. Однако канал Kv1.3 является частью комплексного семейства родственных ионных каналов, также включающего каналы Kv1.1, Kv1.2 и Kv1.6, которые имеют разные физиологические роли. Следовательно, является желательным, чтобы ингибиторы Kv1.3 были настолько селективными, насколько это возможно, предпочитая Kv1.3 другим ионным каналам, особенно другим потенциалзависимым калиевым каналам, таким как Kv1.1, Kv1.2, Kv1.4, Kv1.5, Kv1.6, Kv1.7 и Kv1.8.
Термин "блокатор ионного канала" используется просто для указания на соединение, имеющее активность ингибитора (или блокатора) ионного канала, т.е. способное ингибировать или устранять ток ионов через соответствующий ионный канал, как правило, путем связывания с ионным каналом. Аналогично, термины "ингибитор Kv1.3" и "ингибирующий Kv1.3 компонент" относятся к пептиду, способному ингибировать или устранять ток ионов через ионный канал Kv1.3, как правило, путем связывания с каналом Kv1.3. Однако термины "блокатор" и "ингибитор" не следует считать подразумевающими какой-либо конкретный механизм действия или какой-либо конкретный способ взаимодействия с самим ионным каналом.
Блокатор ионного канала (и отдельно ингибирующий Kv1.3 компонент) по изобретению обладает ингибирующей или блокирующей активностью в отношении ионного канала Kv1.3, т.е. он способен ингибировать ток ионов через канал Kv1.3.
Значения IC50 могут использоваться в качестве меры ингибиторной (или блокирующей) активности или эффективности. Величина IC50 является показателем концентрации ингибитора, требуемой для достижения половины максимального ингибирования этим соединением активности ионного канала в данном анализе. Соединение, которое имеет более низкую IC50 в отношении конкретного ионного канала, чем эталонное соединение, может считаться более активным ингибитором или более мощным ингибитором, чем эталонное соединение. Термины "активность" и "эффективность" используются взаимозаменяемо.
Значения IC50 могут быть определены с использованием любого подходящего анализа, такого как способы анализа на основе флуоресценции, измеряющие ток ионов (например, ток ионов талия), и способы анализа фиксации потенциала. Они могут проводиться, как описано в примерах ниже. Предпочтительными могут быть способы анализа фиксации потенциала, например, с использованием системы QPatch®.
Блокатор ионного канала (или ингибитор Kv1.3) по изобретению может иметь IC50 ниже 10нМ, но в идеальном случае IC50 составляет менее 5 нМ, менее 2 нМ или менее 1 нМ. В некоторых случаях она может составлять только 0,5 нМ, 0,1 нМ или даже ниже.
Блокаторы ионных каналов по изобретению могут включать соединения 1-5, 7, 11-42, 44-48, 50-53, 55-60, 62-68, 70-73, 75-81, 83- 88, 90-98, 101, 104-108, 116, 122, 129, 131, 132, 134 и 137, как описано в настоящем описании. В примере 2 настоящего описания эти соединения имеют IC50 0,3 нМ или менее.
Блокаторы ионных каналов по изобретению могут включать соединения 7, 14-35, 37, 39, 40-48, 50-53, 55-60, 62-68, 70-73, 75-80, 83-97, 90, 91, 93-98, 101, 104-108, 116, 129 и 131, как описано в настоящем описании. В примере 2 настоящего описания показано, что эти соединения имеют IC50 0,2 нМ или менее.
Блокаторы ионных каналов по изобретению могут включать соединения 7, 15-17, 19-28, 30-35, 37, 39-42, 44, 46-48, 51-53, 55-60, 62-67, 70, 71, 73, 75-80, 83-85, 87, 91, 93, 96-98, 104, 106, 107, 108 и 129, как описано в настоящем описании. В примере 2 настоящего описания показано, что эти соединения имеют IC50 0,15 нМ или менее.
Блокаторы ионных каналов по изобретению могут включать соединения 1, 3, 17, 19, 21, 23, 26-33, 37, 41-43, 46-49, 52, 62, 63, 66-68, 70-73, 75, 76, 78, 82-84, 87, 91, 94, 97-102, 105-108, 115 и 116, как описано в настоящем описании. В примере 5 настоящего описания показано, что эти соединения имеют IC50 1 нМ или менее для ингибирования активации T-клеток в цельной крови крысы.
Блокаторы ионных каналов по изобретению являются селективными в отношении Kv1.3. В одном из вариантов осуществления блокаторы ионных каналов по изобретению являются селективными относительно Kv1.1, Kv1.2, Kv1.4, Kv1.5, Kv1.6, Kv1.7 и Kv1.8. В частности, блокаторы ионных каналов по изобретению являются селективными в отношении Kv1.3 относительно одного или нескольких из Kv1.1, Kv1.2 и Kv1.6.
Например, они могут быть:
селективными в отношении Kv1.3 относительно Kv1.1;
селективными в отношении Kv1.3 относительно Kv1.2;
селективными в отношении Kv1.3 относительно Kv1.6;
селективными в отношении Kv1.3 относительно Kv1.1 и Kv1.2;
селективными в отношении Kv1.3 относительно Kv1.1 и Kv1.6;
селективными в отношении Kv1.3 относительно Kv1.2 и Kv1.6; или
селективными в отношении Kv1.3 относительно Kv1.1, Kv1.2 и Kv1.6.
Как правило, блокаторы ионных каналов являются селективными в отношении Kv1.3 относительно Kv1.1.
Кроме того, они могут быть селективными в отношении Kv1.3 относительно Kv1.2 и/или Kv1.6.
Под "селективным" в этом контексте подразумевают, что блокаторы ионных каналов обладают более высокой ингибиторной активностью против Kv1.3, чем против соответствующих каналов Kv1.1, Kv1.2 и Kv1.6. Таким образом, их IC50 против Kv1.3, как правило, является более низкой, чем в отношении соответствующего другого ионного канала или каналов.
Селективность в отношении Kv1.3 относительно другого ионного канала X, таким образом, может быть выражена в качестве соотношения соответствующих величин IC50, например в качестве IC50[X] / IC50[Kv1.3].
Блокаторы ионных каналов по изобретению, таким образом, могут обладать селективностью в отношении Kv1.3 относительно Kv1.1, составляющей по меньшей мере 10, по меньшей мере 100, по меньшей мере 1000, или по меньшей мере 10000, и она может составлять вплоть до 100000 или даже выше. Как правило, они обладают селективностью в отношении Kv1.3 относительно Kv1.1, составляющей по меньшей мере 100 или по меньшей мере 1000.
Блокаторы ионных каналов по изобретению могут включать соединения 1-3, 5, 8, 12, 16-23, 25-31, 34-37, 40-42, 45-49, 52-54, 56, 58, 62, 63, 70, 71, 76, 79, 83, 94-98, 101, 103-108 и 117, как описано в настоящем описании. В примере 3 настоящего описания показано, что эти соединения обладают селективностью в отношении Kv1.3 относительно Kv1.1, составляющей по меньшей мере 1000.
Блокаторы ионных каналов по изобретению могут включать соединения 3, 12, 16, 18-22, 25-28, 30, 31, 35, 37, 40-42, 52, 53, 62, 70, 71, 76, 79, 94, 95, 98 и 105, как описано в настоящем описании. В примере 3 настоящего описания показано, что эти соединения обладают селективностью в отношении Kv1.3 относительно Kv1.1, составляющей по меньшей мере 10000.
Таким образом, блокаторы ионных каналов по изобретению могут обладать селективностью в отношении Kv1.3 относительно Kv1.2, составляющей по меньшей мере 10, по меньшей мере 100, по меньшей мере 1000, или по меньшей мере 10000, и она может составлять вплоть до 100000 или даже выше. Как правило, они обладают селективностью в отношении Kv1.3 относительно Kv1.2, составляющей по меньшей мере 10 и предпочтительно по меньшей мере 50, или по меньшей мере 100, или по меньшей мере 1000.
Блокаторы ионных каналов по изобретению могут включать соединения 1-3, 5, 8, 16-23, 25-31, 34-37, 40-42, 45-49, 52-54, 56, 58, 62, 63, 70, 71, 76, 79, 83, 94-98, 101, 103-108 и 117, как описано в настоящем описании. В примере 3 настоящего описания показано, что эти соединения обладают селективностью в отношении Kv1.3 относительно Kv1.2, составляющей по меньшей мере 50.
Блокаторы ионных каналов по изобретению могут включать соединения 1, 3, 5, 8, 12, 18, 25, 29, 30, 36, 37, 41, 46-48, 52, 62, 70, 71, 79, 83, 94-98, 101, 103-106 и 117, как описано в настоящем описании. В примере 3 настоящего описания показано, что эти соединения обладают селективностью в отношении Kv1.3 относительно Kv1.2, составляющей по меньшей мере 700.
Блокаторы ионных каналов по изобретению могут включать соединения 1, 3, 12, 18, 29, 30, 36, 37, 41, 47, 48, 62, 70, 71, 79, 94-98, 101 и 103-105, как описано в настоящем описании. В примере 3 настоящего описания показано, что эти соединения обладают селективностью в отношении Kv1.3 относительно Kv1.2, составляющей по меньшей мере 1000.
Таким образом, блокаторы ионных каналов по изобретению могут обладать селективностью в отношении Kv1.3 относительно Kv1.6, составляющей по меньшей мере 10, по меньшей мере 100, по меньшей мере 1000, или по меньшей мере 10000, и она может составлять вплоть до 100000 или даже выше. Как правило, они обладают селективностью в отношении Kv1.3 относительно Kv1.6, составляющей по меньшей мере 100, или по меньшей мере 400, или по меньшей мере 1000.
Блокаторы ионных каналов по изобретению могут включать соединения 1, 2, 3, 5, 8, 12, 16-23, 25-31, 34-37, 40-42, 45-49, 52-54, 56, 58, 62, 63, 70, 71, 76, 79, 83, 94-98, 101, 103-108 и 117, как описано в настоящем описании. В примере 3 настоящего описания показано, что эти соединения обладают селективностью в отношении Kv1.3 относительно Kv1.6, составляющей по меньшей мере 400.
Блокаторы ионных каналов по изобретению могут включать соединения 3, 12, 16, 18, 20, 22, 26, 30, 31, 37, 41, 52, 53, 70, 71, 76, 79, 94, 95, 98 и 105, как описано в настоящем описании. В примере 3 настоящего описания показано, что эти соединения обладают селективностью в отношении Kv1.3 относительно Kv1.6, составляющей по меньшей мере 10000.
Блокаторы ионных каналов по изобретению могут иметь более высокую селективность, чем известные блокаторы ионных каналов, такие как ShK, мокатоксин (Moka1), Vm24, Odk2 или Osk1. Таким образом, блокаторы ионных каналов по изобретению могут обладать более высокой селективностью в отношении Kv1.3 относительно ионного канала X, т.е. IC50[X] / IC50[Kv1.3], которая превышает селективность молекулы для сравнения. Селективность этих двух блокаторов ионных каналов определяют в одних и тех же условиях для каждого ионного канала для обеспечения прямого сравнения. Как упоминалось выше, можно использовать любые подходящие способы анализа, такие как способы анализа потока ионов на основе флуоресценции и способы анализа фиксации потенциала.
Блокаторы ионных каналов по изобретению могут иметь более низкую абсолютную ингибирующую активность (т.е. превышающую IC50), чем известные блокаторы ионных каналов (такие как Odk2 или Osk1), в отношении любого или всех из Kv1.1, Kv1.2 и/или Kv1.6. Однако для них может быть приемлемым, чтобы они обладали более высокой абсолютной ингибирующей активностью в отношении любого или всех из этих ионных каналов при условии, что их селективность в отношении Kv1.3 является более высокой, чем селективность соединения для сравнения. Хотя, как правило, соединения по изобретению сочетают в себе высокую специфичность в отношении Kv1.3 с высокой эффективностью.
СИНТЕЗ И РЕКОМБИНАНТНАЯ ЭКСПРЕССИЯ
Блокаторы ионных каналов, описанные в настоящем описании, могут быть синтезированы с использованием методологии твердофазного или жидкофазного синтеза пептидов. В этом контексте может быть упомянута WO 98/11125 и, среди многих других, Fields, G.B. et al., 2002, "Principles and practice of solid-phase peptide synthesis", Synthetic Peptides (2nd Edition), и в примерах настоящего описания.
Альтернативно блокаторы ионных каналов, описанные в настоящем описании, могут быть синтезированы посредством рекомбинантных способов или посредством комбинирования рекомбинантных способов и химии пептидов.
Например, пептид-блокатор ионных каналов можно синтезировать способом, который включает:
(a) синтез пептида посредством методологии твердофазного или жидкофазного пептидного синтеза и выделение полученного таким образом пептида;
(b) экспрессию пептида с конструкции нуклеиновой кислоты, которая кодирует пептид, и выделение продукта экспрессии; или
(c) экспрессию пептида-предшественника с конструкции нуклеиновой кислоты, которая кодирует последовательность пептида-предшественника, выделение продукта экспрессии и модификацию пептида-предшественника с получением блокатора ионных каналов по изобретению.
Пептид-предшественник может быть модифицирован путем внесения одной или нескольких непротеиногенных аминокислот (например, Nle), внесения соответствующих концевых групп R1 и R2, и т.д.
Экспрессию пептида или пептида-предшественника с нуклеиновой кислоты, кодирующей пептид или пептид-предшественник, можно проводить в клетке или бесклеточной системе экспрессии, содержащей такую нуклеиновую кислоту. Такая экспрессия, как правило, требует, чтобы пептид или пептид-предшественник состоял полностью из протеиногенных аминокислот (т.е. 20 аминокислот, кодируемых стандартным генетическим кодом).
Для рекомбинантной экспрессии фрагменты нуклеиновых кислот, кодирующие пептид-предшественник, в норме встраивают в подходящие векторы для формирования клонирующих или экспрессирующих векторов. Векторы могут быть, в зависимости от назначения и типа применения, в форме плазмид, фагов, космид, минихромосом или вируса, но также важным вектором может быть голая ДНК, которая экспрессируется только временно в определенных клетках. Предпочтительные клонирующие и экспрессирующие векторы (плазмидные векторы) способны к автономной репликации, таким образом, обеспечивая высокое количество копий для целей экспрессии на высоком уровне или репликации на высоком уровне для последующего клонирования.
В общем, экспрессирующий вектор содержит следующие элементы в направлении 5'→3' и в функциональной связи: промотор для запуска экспрессии фрагмента нуклеиновой кислоты, необязательно последовательность нуклеиновой кислоты, кодирующую лидерный пептид, обеспечивающий секрецию (во внеклеточную фазу или, когда это применимо, в периплазму), фрагмент нуклеиновой кислоты, кодирующий пептид-предшественник, и необязательно последовательность нуклеиновой кислоты, кодирующую терминатор. Он может содержать дополнительные элементы, такие как селективные маркеры и ориджины репликации. Когда имеют дело с экспрессирующими векторами в продуцирующих штаммах или клеточных линиях, может быть предпочтительным, чтобы вектор был способен встраиваться в геном клетки-хозяина. Специалисту в данной области хорошо известны подходящие векторы, и он способен сконструировать их в соответствии конкретными потребностями.
Векторы по изобретению используют для трансформации клеток-хозяев для продуцирования пептида или пептида-предшественника. Такие трансформированные клетки могут представлять собой культивируемые клетки или клеточные линии для увеличения в количестве фрагментов нуклеиновой кислоты и векторов, и/или могут использоваться для рекомбинантного продуцирования пептидов-предшественников.
Предпочтительными трансформированными клетками являются микроорганизмы, такие как бактерии [такие как виды Escherichia (например, E.coli), Bacillus (например, Bacillus subtilis), Salmonella или Mycobacterium (предпочтительно непатогенные, например BCG M. bovis), дрожжи (например, Saccharomyces cerevisiae и Pichia pastoris) и простейшие. Альтернативно трансформированные клетки могут происходить из многоклеточного организма, т.е. они могут представлять собой клетку грибов, клетку насекомых, клетку водорослей, клетку растений или клетку животных, такую как клетка млекопитающих. Для целей клонирования и/или оптимизированной экспрессии предпочтительно, чтобы трансформированная клетка была способна реплицировать фрагмент нуклеиновой кислоты по изобретению. Клетки, экспрессирующие фрагмент нуклеиновой кислоты, можно использовать для мелкомасштабного или крупномасштабного получения пептидов по изобретению.
При продуцировании пептида или пептида-предшественника посредством трансформированных клеток является удобным, хотя и совсем не обязательным, чтобы продукт экспрессии секретировался в культуральную среду.
ТЕРАПЕВТИЧСКИЕ ПОКАЗАНИЯ
Как рассмотрено выше, было показано, что блокаторы Kv1.3 ингибируют пролиферацию активированных T-клеток и имеют благоприятный эффект в различных экспериментальных моделях заболевания. Без связи с теорией полагают, что клеточный выходящий поток калия через канал Kv1.3 является необходимым для поддержания входящего потока калия, требуемого для активации T-клеток.
Kv1.3 сверхэкспрессируется в Gad5/инсулин-специфических T-клетках от пациентов с впервые выявленным диабетом 1 типа, в миелин-специфических T-клетках от пациентов с MS и в T-клетках синовиальной оболочки пациентов с ревматоидным артритом (Beeton et al., Proc Natl Acad Sci USA 103:17414-9, 2006), в образцах рака молочной железы (Abdul et al., Anticancer Res 23:3347, 2003) и клеточных линиях рака предстательной железы (Fraser et al., Pflugers Arch 446:559, 2003).
Положительные исходы в моделях на животных с блокаторами Kv1.3 описаны в моделях гиперчувствительности к овальбумину и столбнячному токсоиду (Beeton et al., Mol Pharmacol 67:1369, 2005; Koo et al., Clin Immunol 197:99, 1999), в моделях рассеянного склероза, таких как модель экспериментального аутоиммунного энцефаломиелита с адоптивным переносом (AT-EAE) на крысах (Beeton et al., Proc Natl Acad Sci USA 103:17414-9, 2006), модель воспалительной резорбции кости (Valverde et al., J Bone Mineral Res 19:155, 2004), модели артрита (Beeton et al., Proc Natl Acad Sci 103: 17414, 2006; Tarcha et al., J. Pharmacol. Exp.Ther. 342: 642, 2012) и ожирения, диабета и метаболических нарушений (Xu et al., Hum Mol Genet 12:551, 2003; Xu et al., Proc Natl Acad Sci 101: 3112, 2004).
Местное применение блокаторов Kv1.3 было предложено для лечения воспаления кожи и слизистых оболочек.
Таким образом, блокаторы ионных каналов, описанные в настоящем описании, имеют значительный потенциал к применению для ингибирования или снижения воспаления, особенно при лечении воспалительного состояния или нарушения, включая аутоиммунные нарушения.
Воспалительное состояние или нарушение может представлять собой любое состояние или нарушение, при котором является желательным снижение воспаления, например, где воспаление вносит вклад в симптомы или патогенез.
Такие состояния включают аутоиммунные нарушения, аллергию и гиперчувствительность, отторжение аллотрансплантата и реакцию "трансплантат против хозяина".
Более конкретно, состояния включают сенную лихорадку, астму, анафилаксию, аллергический ринит, крапивницу, экзему, очаговую алопецию, дерматомиозит, миозит с тельцами включения, полимиозит, анкилозирующий спондилит, васкулит, артрит (включая ревматоидный артрит, остеоартрит, псориатический артрит), синдром Шегрена, системную красную волчанку (SLE, или просто "волчанка") и увеит, воспалительный фиброз (например склеродермия, фиброз легких, цирроз), хроническое обструктивное заболевание легких (COPD), гепатит, хроническую воспалительную демиелинизирующую полиневропатию, воспалительное заболевание кишечника, колит (включая болезнь Крона и язвенный колит), эритему, тиреоидит, псориаз, атопический дерматит, аллергический контактный дерматит, склеродермию, гломерулонефрит, воспалительную резорбцию кости, рассеянный склероз, диабет 1 типа, отторжение трансплантата и реакцию "трансплантат против хозяина".
Блокаторы Kv1.3 также могут иметь благоприятные метаболические эффекты, например, в отношении гомеостаза энергии, регуляции массы тела и контроля уровня глюкозы.
Таким образом, блокаторы ионных каналов, описанные в настоящем описании, могут использоваться для ингибирования увеличения массы тела, способствования снижению массы тела, снижения избыточной массы тела или лечения ожирения (например, посредством контроля аппетита, питания, приема пищи, употребления калорий и/или потребления энергии) или для лечения связанных с ними нарушений и состояний здоровья, включая связанное с ожирением воспаление, связанное с ожирением заболевание желчного пузыря или индуцируемое ожирением апноэ во сне.
Эффект на массу тела может быть терапевтическим или косметическим.
Блокаторы ионных каналов также можно использовать для лечения состояний, вызванных или ассоциированного с нарушением контроля уровня глюкозы, включая метаболический синдром, резистентность к инсулину, нарушение толерантности к глюкозе, преддиабет, повышение уровня глюкозы натощак или диабет 2 типа. Некоторые из этих состояний могут быть ассоциированы с ожирением. Их эффекты на эти состояния могут опосредоваться целиком или частично эффектом на массу тела, или они могут быть независимыми от них.
Kv1.3 также экспрессируется в пролиферирующих гладкомышечных клетках человека и мыши. Блокаторы Kv1.3 могут быть эффективны при гладкомышечных пролиферативных нарушениях, таких как рестеноз, например, у пациентов после сосудистой хирургической операции (например, ангиопластика).
Дальнейшие данные указывают на то, что каналы Kv1.3 вовлечены в активацию и/или пролиферацию многих типов клеток, включая опухолевые клетки (Bielanska et al., Curr. Cancer Drug Targets 9:904-14, 2009), микроглию (Khanna et al., Am. J. Physiol. Cell Physiol. 280: C796-806, 2001) и дифференцировку нейрональных клеток-предшественников (Wang et al., J. Neurosci. 30:5020-7, 2010). Таким образом, блокаторы Kv1.3 могут быть благоприятными для лечения нейровоспалительных и нейродегенеративных нарушений, таких как болезнь Альцгеймера, рассеянный склероз (MS), болезнь Паркинсона и боковой амиотрофический склероз (ALS) (например, после вирусных инфекций), и злокачественных опухолей, включая рак молочной железы, рак предстательной железы и лимфому, такую как неходжкинская лимфома (NHL). Неходжкинские лимфомы включают T-клеточную NHL и B-клеточную NHL. Формы B-клеточной NHL включают диффузную крупноклеточную B-клеточную лимфому, фолликулярную лимфому, лимфому Беркитта, иммунобластную крупноклеточную лимфому, B-лимфобластную лимфому из клеток-предшественников и лимфому из клеток мантийной зоны. Формы T-клеточной NHL включают фунгоидный микоз, анапластическую крупноклеточную лимфому, периферическую T-клеточную лимфому, T-лимфобластную лимфому из клеток-предшественников и синдром Сезари.
ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ И ВВЕДЕНИЕ
Один из аспектов настоящего изобретения относится к композиции, содержащей блокатор ионных каналов по изобретению или его соль вместе с носителем, эксципиентом или наполнителем. В определенных вариантах осуществления композиция представляет собой фармацевтическую композицию, какая-либо соль представляет собой фармацевтически приемлемую соль и носитель представляет собой фармацевтически приемлемый носитель, эксципиент или наполнитель.
Таким образом, соединения по настоящему изобретению или их соли, особенно их фармацевтически приемлемые соли, могут быть составлены в качестве композиций или фармацевтических композиций, полученных для хранения или введения, и которые содержат терапевтически эффективное количество соединения по изобретению или его соли.
Подходящие соли, образованные с основаниями, включают соли металлов, такие как соли щелочных металлов или соли щелочноземельных металлов, например, соли натрия, калия или магния; соли аммиака и соли органических аминов, такие как соли, образованные с морфолином, тиоморфолином, пиперидином, пирролидином, низшим моно-, ди- или триалкиламином (например, этил-трет-бутил-, диэтил-, диизопропил-, триэтил-, трибутил- или диметилпропиламин) или низшим моно-, ди- или три-(гидроксиалкил)амином (например, моно-, ди- или триэтаноламин). Также могут быть получены внутренние соли. Аналогично, когда соединение по настоящему изобретению содержит основную часть, соли могут быть получены с использованием органических или неорганических кислот. Например, соли могут быть получены из следующих кислот: муравьиная, уксусная, пропионовая, масляная, валериановая, капроновая, щавелевая, молочная, лимонная, виннокаменная, янтарная, фумаровая, малеиновая, малоновая, миндальная, яблочная, фталевая, хлористоводородная, бромистоводородная, фосфорная, азотная, серная, бензойная, карбоновая, мочевая, метансульфоновая, нафталинсульфоновая, бензолсвльфоновая, толуолсульфоновая, п-толуолсульфоновая (т.е. 4-метилбензолсульфоновая), камфорсульфоновая, 2-аминоэтансульфоновая, аминометилфосфоновая и трифторметансульфоновая кислота (последнюю также называют трифлатной кислотой), а также другие известные фармацевтически приемлемые кислоты. Аддитивные соли аминокислот также могут быть образованы с аминокислотами, такими как лизин, глицин или фенилаланин.
В некоторых вариантах осуществления фармацевтическая композиция по изобретению представляет собой композицию, где соединение имеет форму фармацевтически приемлемой кислотно-аддитивной соли.
Как будет понятно специалисту в данной области, "терапевтически эффективное количество" соединения или фармацевтической композиции по настоящему изобретению варьируется в зависимости, среди прочих, от возраста, массы тела и/или пола индивидуума (пациента), подвергаемого лечению. Другие факторы, которые могут иметь значение, включают физические характеристики конкретного рассматриваемого пациента, режим питания пациента, природу какого-либо сопутствующего лекарственного средства, конкретное используемое соединение(я), конкретный способ введения, желаемый фармакологический эффект(ы) и конкретное терапевтическое показание. Поскольку эти факторы и их взаимосвязь при определении этого количества хорошо известны в области медицины, специалист в данной области способен определить терапевтически эффективные дозировки для достижения желаемого терапевтического эффекта.
Как используют в рамках изобретения, термин "терапевтически эффективное количество" относится к количеству, которое уменьшает симптомы данного состояния или патологии и предпочтительно которое нормализует физиологический ответ у индивидуума с этим состоянием или патологией. Уменьшение симптомов или нормализацию физиологических ответов можно определять с использованием стандартных способов в данной области, и они могут варьироваться в зависимости от данного состояния или патологии. В одном аспекте терапевтически эффективное количество соединения по изобретению или фармацевтической композиции представляет собой количество, которое восстанавливает поддающийся измерению физиологический параметр по существу до той же величины (предпочтительно в пределах 30%, более предпочтительно в переделах 20%, и еще более предпочтительно в пределах 10% от этой величины) параметра, что и у индивидуума без рассматриваемого состояния или патологии.
В одном варианте осуществления изобретения введение соединения или фармацевтической композиции по настоящему изобретению начинают при более низких дозировках, причем дозировки повышают до тех пор, ока не достигнут желаемого эффекта предупреждения/лечения соответствующего медицинского показания. Это определяет терапевтически эффективное количество. Для соединений по настоящему изобретению, отдельно или в качестве части фармацевтической композиции, такие дозировки активного соединения для человека могут составлять приблизительно от 0,01 пмоль/кг до 500 мкмоль/кг массы тела, приблизительно от 0,01 пмоль/кг до 300 мкмоль/кг массы тела, от 0,01 пмоль/кг до 100 мкмоль/кг массы тела, от 0,1 пмоль/кг до 50 мкмоль/кг массы тела, от 1 пмоль/кг до 10 мкмоль/кг массы тела, от 5 пмоль/кг до 5 мкмоль/кг массы тела, от 10 пмоль/кг до 1 мкмоль/кг массы тела, от 50 пмоль/кг до 0,1 мкмоль/кг массы тела, от 100 пмоль/кг до 0,01 мкмоль/кг массы тела, от 0,001 мкмоль/кг до 0,5 мкмоль/кг массы тела, от 0,05 мкмоль/кг до 0,1 мкмоль/кг массы тела.
Эффективная дозировка и протокол лечения могут быть определены общепринятыми способами, начиная с низкой дозы у лабораторных животных, а затем повышая дозировку, одновременно осуществляя мониторинг эффектов, а также систематически варьируя режим дозирования. Многочисленные факторы могут быть учтены врачом при определении оптимальной дозировки для данного индивидуума. Такие факторы известны специалисту в данной области.
ПРИМЕРЫ
Пример 1: Общий пептидный синтез
Перечень сокращенных обозначений и поставщиков приведен в таблице ниже
Устройство и стратегия синтеза
Пептиды синтезировали партиями на устройстве для синтеза пептидов, таком как устройство CEM Liberty Peptide Synthesizer или Symphony X Synthesizer, в соответствии с методиками твердофазного пептидного синтеза с использованием 9-флуоренилметилоксикарбонила (Fmoc) в качестве N-α-амино-защитной группы и подходящих распространенных защитных групп для функциональных групп боковых цепей.
Использовали смолы на основе полимерной подложки, например, такие как TentaGel™. Устройство для синтеза нагружали смолой, которую перед применением подвергали набуханию в DMF.
Реакция сочетания
Устройство для синтеза пептидов CEM Liberty Peptide Synthesizer
Раствор Fmoc-защищенной аминокислоты (4 экв.) добавляли к смоле вместе с раствором реагента для присоединения (4 экв.) и раствором основания (8 экв.). Смесь либо нагревали с использованием микроволнового блока до 70-75°C и подвергали присоединению в течение 5 минут, либо подвергали присоединению без нагревания в течение 60 минут.В ходе присоединения через смесь барботировали азот.
Symphony X Synthesizer
Растворы для присоединения переносили в реакционные емкости в следующем порядке: аминокислота (4 экв.), HATU (4 экв.) и DIPEA (8 экв.). Время присоединения составляло 10 мин при комнатной температуре (к.т.), если нет иных указаний. Смолу промывали DMF (5×0,5 мин). В случае повторяющихся присоединений время присоединения во всех случаях составляло 45 мин при к.т.
Удаление защитной группы
CEM Liberty Peptide Synthesizer
Удаление защитной группы Fmoc проводили с использованием пиперидина в DMF или других подходящих растворителей. Раствор для удаления защитной группы добавляли в реакционную емкость и смесь нагревали в течение 30 с, достигая приблизительно 40°C. Из реакционной емкости сливали жидкость и добавляли свежий раствор для удаления защитной группы, а затем нагревали до 70-75°C в течение 3 мин. Из реакционной емкости сливали жидкость, а затем смолу промывали DMF или другими подходящими растворителями.
Symphony X Synthesizer
Удаление защитной группы Fmoc проводили в течение 2,5 минут с использованием 40% пиперидина в DMF, и его повторяли с использованием тех же условий. Смолу промывали DMF (5×0,5 мин).
Расщепление
Высушенную пептидную смолу обрабатывали TFA и подходящими улавливателями в течение приблизительно 2 часов. Объем фильтрата уменьшали и неочищенный пептид преципитировали после добавления диэтилового эфира. Неочищенный пептидный преципитат промывали несколько раз диэтиловым эфиром и в конце сушили.
Очистка неочищенного пептида посредством ВЭЖХ
Неочищенный пептид очищали посредством препаративной обращено-фазовой ВЭЖХ с использованием общепринятого устройства для ВЭЖХ, такого как Gilson GX-281, с комбинацией насосов 331/332 для двойного применения градиента, оборудованного колонкой, такой как колонка Gemini NX 5u C18 110A 5×25 см, и коллектором фракций с использованием скорости потока 20-40 мл/мин с подходящим градиентом буфера A (0,1% муравьиная кислота, водн.) или A (0,1% TFA, водн.) и буфера B (0,1% муравьиная кислота, 90% MeCN, водн.) или B (0,1% TFA, 90% MeCN, водн.). Фракции анализировали посредством аналитической ВЭЖХ и MS и отдельные фракции объединяли и лиофилизировали. Конечный продукт охарактеризовывали посредством ВЭЖХ и MS.
Образование дисульфидной связи
Неочищенный или частично очищенный линейный пептид с шестью остатками цистеина растворяли в буфере, таком как гидрокарбонат натрия (NaHCO3) или ацетат аммония (NH4Ac) до конечной концентрации приблизительно 0,1 мг/мл или 25 мкМ. pH буфера доводили до pH 8,0 и раствор перемешивали при комнатной температуре при перемешивании магнитной мешалкой и открытым доступом для атмосферы. За ходом реакции следили посредством ВЭЖХ, и визуально было оценено, что она завершилась в течение ночи. Раствор гасили путем снижения pH раствора органической кислотой, такой как уксусная кислота или трифторуксусная кислота (pH<4). Раствор фильтровали и загружали непосредственно в колонку для препаративной ВЭЖХ для очистки.
Аналитическая ВЭЖХ
Конечную чистоту определяли с использованием устройства для аналитической ВЭЖХ (Agilent 1100/1200 series), оборудованного автоматическим пробоотборником, дегазатором, 20-мкл проточной ячейкой и программным обеспечением Chromeleon. ВЭЖХ использовалась со скоростью потока 1,2 мл/мин при 40°C с использованием аналитической колонки, такой как колонка Kinetex 2,6 μm XB-C18 100A 100×4,6 мм. Детекцию и количественное определение соединения проводили при 215 нм. Использовали буфер A (0,1% TFA, водн.) и буфер B (0,1% TFA, 90% MeCN, водн.).
Масс-спектроскопия
Конечный анализ посредством MS проводили на общепринятом масс-спектрометре, например, Waters Xevo G2 Tof, оборудованном электрораспылительным детектором с калибровкой с фиксированной массой и программным обеспечением MassLynx. Он действовал в положительном режиме с использованием прямого инжектирования и напряжения на конусе 15 В (1 TOF), 30 В (2 TOF) или 45 В (3 TOF), как указано на хроматограмме. Точность составляла 5 м.д. с типичным разрешением 15000-20000.
Синтезированные соединения представлены в таблице 1.
Пример 2: Активность блокирования Kv1.3 в анализе FLIPR с талием
Клеточную линию с потенциалзависимым K+каналом Kv1.3 человека приобретали от Perkin Elmer (TDS-AX-010-C-1). Клеточная линия основана на клетках CHO-DUKX, стабильно трансфицированных потенциалзависимым K+каналом человека Kv1.3.
Клеточную линию выращивали в MEMα с нуклеотидами, GlutaMAX (Gibco, каталожный номер 32571028), 10% эмбриональной бычьей сывороткой (FBS), 0,4 мг/мл генетицина, 100 единиц/мл пенициллина и 100 мкг/мл стрептомицина, и высевали в количестве 10000 клеток/лунка в черные покрытые поли-D-лизином 96-луночные планшеты.
Анализ калиевых ионных каналов FluxOR™ (Invitrogen, каталожный номер №F10016) использовали для количественного определения потока ионов калия в клетки в ответ на активацию Kv1.3 стимулирующим буфером, вызывающим деполяризацию клеточной мембраны, генерируя флуоресцентный сигнал, пропорциональный активности канала. Анализ проводили, как описано производителем набора для анализа. Флуоресцентные ответы регистрировали и количественно определяли с использованием высокопроизводительной системы скрининга FLIPR® Tetra (Molecular Devices, Inc.).
Данные тестируемых соединений, индуцирующих потока талия в клетку, приводили к данным для положительного (ShK) и отрицательного контроля (носитель) для вычисления IC50 из кривой концентрация-ответ.Результаты представлены в таблице 2. IC50 может считаться мерой эффективности ингибирования для соответствующего соединения. Величина IC50 является показателем концентрации ингибитора, требуемой для достижения половины максимального ингибирования для этого соединения активности ионного канала в данном анализе. Соединение, которое имеет более низкую IC50 в отношении конкретного ионного канала, чем эталонное соединение, может считаться более активным ингибитором или более мощным ингибитором, чем эталонное соединение.
Пример 3: Селективность в отношении Kv1.3 в анализе фиксации потенциала
Линии клеток китайского хомячка (CHO), стабильно экспрессировавшие экзогенные α-субъединицы человека каждого калиевого ионного канала, выращивали и пассировали в стандартных условиях культивирования.
Автоматизированное плоское устройство для фиксации потенциала QPatch® использовали для количественного определения ионного тока. Всю регистрацию проводили в общепринятой конфигурации целых клеток после установления перемычек с гигаомным сопротивлением. Внешний раствор для регистрации содержал (150 мМ NaCl, 10 мМ KCl, 10 мМ HEPES, 1 мМ MgCl2, 3 мМ CaCl2, 10 мМ глюкоза, значение pH, доведенное до 7,4 посредством NaOH) и внутренний раствор для регистрации содержал (20 мМ KCl, 120 мМ KF, 10 мМ HEPES, 10 мМ EGTA, 5 мМ NaATP, значение pH, доведенное до 7,2 посредством KOH). В ходе экспериментов 0,1% (об./об.) BSA был включен в качестве носителя во все внешние растворы для регистрации. Ток индуцировали путем удержания напряжения -80 мВ с использованием протокола напряжения, который сдвигал напряжение до 30 мВ на 500 мс каждые 15 с.
Взаимосвязь концентрация-ответ определяли путем использования в совокупности семи возрастающих концентраций тестируемого образца для индивидуальной клетки с периодом регистрации 2 мин на применение соединения.
Эффективность определяли в качестве среднего заряда на протяжении последних трех перемещений в конце каждого периода применения концентрации, исходя из трех положений курсора. Процентное ингибирование для каждого периода применения тестируемой дозы вычисляли в качестве уменьшения среднего курсорного значения (заряда) относительно курсорного значения, измеренного в конце периода носителя, и использовали для вычисления IC50, исходя из кривой концентрация-ответ.
Результаты представлены в таблице 3.
Kv1.3
Kv1.3
Kv1.3
Сравнение данных, приведенных в примерах 2 и 3, показывает, что существует хорошая корреляция между величинами IC50 при измерении в этих двух способах анализа.
Пример 4a: Ингибиторная активность блокаторов Kv1.3 в отношении PBMC человека
Мононуклеарные клетки периферической крови (PBMC) человека использовали для оценки эффектов блокаторов Kv1.3 на активацию T-клеток при определении по высвобождению IL-2 (цитокин) после стимуляции, направленной против CD3.
PBMC человека получали от Precision for Medicine (Frederick, MD). Использовали клетки от 5 доноров. Связанное с планшетом антитело против CD3 использовали для стимуляции тотальных T-клеток в препаратах PBMC. В кратком изложении, 96-луночные планшеты покрывали антителом против CD3 в течение 2 ч при 37°C с использованием 50 мкл раствора антитела против CD3 в концентрации 0,5 мкг/мл, разведенного в 1×PBS. После этого планшеты промывали два раза.
Блокаторы Kv1.3, как показано в таблице 4a, разбавляли в среде (RPMI 1640 с Glutamax-I, содержавшая 10% об./об. эмбриональную телячью сыворотку, 1% об./об. раствор пенициллин-стрептомицин) и добавляли в объеме 100 мкл в концентрациях в диапазоне от 0,01 пМ до 100 нМ (десятикратные разведения). В качестве положительных контролей использовали циклоспорин A (1 мкг/мл) и пептид Vm24 (100 нМ). Наконец, 1×105 PBMC добавляли в каждую лунку в объеме 100 мкл до конечного объема 200 мкл на лунку. Планшеты инкубировали в течение 20-24 часов в инкубаторе с 37°C/5% CO2. После центрифугирования планшетов 25 мкл супернатанта переносили в планшеты для детекции IL-2 (MSD Human IL-2 Tissue Culture Kit, каталожный номер №K151AHB-2) и IL-2 измеряли, как описано производителем (Meso Scale Discovery, Rockville, Maryand, США).
Результаты представлены в таблице 4a в качестве геометрического среднего значения величин IC50, полученного в анализах на стимулированных антителом против CD3 PBMC человека. Все величины получали на основе по меньшей мере 4 повторений.
Инкубация с антителом против CD3 активировала hPBMC и добавление блокаторов Kv1.3 приводило к дозозависимому уменьшению секреции IL-2. В среднем, величины IC50 (как вычислено из высвобождения IL-2) тестируемых соединений находились в диапазоне от 0,05 нМ до 0,4 нМ. Это было сравнимо с IC50, наблюдаемой для ShK186 (IC50 составляет 0,07 нМ) и было приблизительно в 10-100 раз более низким, чем IC50 Moka1, который был менее эффективным в отношении ингибирования секреции IL-2.
Отсутствуют значимые различия между тестируемыми соединениями и ShK186. Показатели всех из ShK186 и тестируемых соединений были значимо более низкими, чем у Moka1.
Циклоспорин блокировал индуцируемое CD3 высвобождение IL-2 полностью во всех экспериментах.
Пример 4b: Ингибиторная активность блокаторов Kv1.3 в отношении PBMC человека
Мононуклеарные клетки периферической крови (PBMC) человека использовали для оценки эффектов блокаторов Kv1.3 на активацию T-клеток при определении по высвобождению IL-2 после стимуляции, направленной против CD3.
PBMC человека получали от Precision for Medicine (Frederick, MD). Использовали клетки от 5 доноров. Связанное с планшетом антитело против CD3 использовали для стимуляции тотальных T-клеток в препаратах PBMC. В кратком изложении, 96-луночные планшеты покрывали антителом против CD3 в течение 2 ч при 37°C с использованием 50 мкл раствора антитела против CD3 в концентрации 1,0 мкг/мл, разведенного в 1×PBS. После этого планшеты промывали два раза.
Затем блокаторы Kv1.3 разбавляли в среде (RPMI 1640 с Glutamax-I, содержавшая 10% об./об. эмбриональную телячью сыворотку, 1% об./об. раствором пенициллин-стрептомицин) и добавляли в объеме 50 мкл. Соединения, указанные в таблице 4b, использовали в концентрациях в диапазоне от 0,3 пМ до 1000 нМ (половинные логарифмические разведения с варьирующими начальными концентрациями). В качестве положительных контролей использовали циклоспорин A (1 мкг/мл) и пептид Vm24 (100 нМ).
Наконец, 50000 PBMC в той же среде добавляли в каждую лунку в объеме 50 мкл, обеспечивая конечный объем 100 мкл на лунку. Планшеты инкубировали в течение 20-24 часов в инкубаторе при 37°C/5% CO2. После центрифугирования планшетов 25 мкл супернатанта переносили в планшеты для детекции IL-2 (MSD Human IL-2 Tissue Culture Kit, каталожный номер K151AHB-2) и IL-2 измеряли, как описано производителем (Meso Scale Discovery, Rockville, Maryand, США).
Результаты представлены в таблице 4b в качестве геометрического среднего значения величин IC50, полученного в анализах на стимулированных антителом против CD3 PBMC человека. Все величины получали на основе по меньшей мере 6 повторений.
Инкубация с антителом против CD3 активировала hPBMC, и добавление соединений по настоящему изобретению приводило к дозозависимому снижению секреции IL-2.
Средние величины IC50 (при вычислении по высвобождению IL-2) тестируемых соединений находились в диапазоне от 0,01 нМ до 0,09 нМ, как показано в таблице 4b. Это было сравнимо с IC50, наблюдаемой в случае ShK186 (IC50 составляет 0,05 нМ). Этот анализ проводили с использованием доноров, отличающихся от доноров, использованных для примера 4a, таким образом, идентичные величины для Shk-186 в этих двух наборах экспериментов не ожидались.
Циклоспорин полностью блокировал индуцируемое антителом против CD3 высвобождение IL-2 во всех экспериментах.
Пример 5: Ингибиторная активность блокаторов Kv1.3 в цельной крови крысы
Цельную кровь крысы использовали для оценки эффективности блокаторов Kv1.3 в отношении активации T-клеток при определении по высвобождению IL-17A после стимуляции тапсигаргином. Добавление тапсигаргина приводит к активации каскада передачи сигнала, оканчивающегося активацией пролиферации T-клеток и продуцированием цитокинов, где ионный канал Kv1.3 играет ключевую роль, так что в этой экспериментальной системе может быть измерена активность блокаторов Kv1.3 в первичных клетках.
Цельную кровь крысы получали от здоровых наивных крыс Lewis или Sprague-Dawley, которым проводили терминальное кровопускание из сердца с использованием пробирок для взятия крови с гепарином натрия для сбора. Тестируемые соединения разбавляли до 4x конечных тестируемых концентраций в буфере для анализа (DMEM+GlutaMAX). GlutaMAX представляет собой среду, содержащую 3,97 мМ L-аланин-L-глутамин (Gibco, каталожный номер №61965026), дополненную 25 мМ буфером HEPES, 1 мМ пируватом натрия, 100 единицами/мл пенициллина, 100 мкг/мл стрептомицина и 0,05% казеином из коровьего молока (Sigma-Aldrich)) и 25 мкл добавляли в лунки 96-луночного планшета. Затем добавляли 50 мкл цельной крови крысы и инкубировали в течение минимум 5 минут при комнатной температуре для обеспечения связывания соединений. Затем во все лунки планшетов для анализа добавляли 25 мкл 40 мкМ тапсиаргина, разбавленного в буфере для анализа, для активации клеток с последующей инкубацией в течение 24 ч при 37°C/5% CO2 в боксе с увлажнением. Планшеты для анализа центрифугировали в течение 10 мин при 300g при 4°C и супернатанты переносили в новые планшеты. Концентрации IL-17A, высвободившегося в супернатанты, измеряли с использованием набора ELISA для IL-17A крысы (Abcam, каталожный номер №ab214028) в соответствии с рекомендацией изготовителя. Образцы разбавляли в 2,5 раза путем переноса 20 мкл супернатантов в лунки планшетов для ELISA, содержавшие 30 мкл буфера 75BS из набора для детекции.
Данные тестируемых соединений, обеспечивающих ингибирование IL-17A, нормализовывали к данным контролей с полной активацией тапсиаргином (без добавления блокатора) и без активации (добавление буфера для анализа вместо тапсиаргина) для вычисления IC50 на основе кривой концентрация-ответ.
Результаты представлены в таблице 5, выраженные в качестве IC50 со стандартным отклонением (IC50_SD). Все величины получены на основе по меньшей мере 2 повторений. Биологические эффекты ex vivo демонстрируют корреляцию с эффективностью соединений.
Пример 6: Охарактеризация фармакокинетики
Способ
Крысам Sprague Dawley или Wistar (самцы с массой тела приблизительно 250-350 г) проводили однократную подкожную (п/к) инъекцию каждого пептида, подлежащего тестированию.
После п/к введения выбранных соединений (доза 70 нмоль/кг, объем дозирования либо 2, либо 5 мл/кг), проводили взятие образцов крови через 15 мин, 30 мин, 45 мин, 60 мин, 90 мин, 2 ч, 3 ч, 4 ч после введения дозы. В каждый момент времени взятия образца проводили взятие образцов от крыс посредством сублингвального отбора крови или разреза хвоста. После последнего взятия образца крыс умерщвляли посредством анестезии O2/CO2. Носитель для дозирования представлял собой 10 мМ фосфат, 0,8% NaCl, 0,05% полисорбат 20 (pH 6,0).
Образцы плазмы анализировали после твердофазной экстракции (SPE) посредством жидкостной хроматографии-масс-спектрометрии (LC-MS/MS). Средние концентрации в плазме использовали для вычисления фармакокинетических параметров с использованием некомпартментного подхода в Phoenix WinNonlin 6.4 или более поздней версии. Терминальное время полувыведения в плазме (T½) определяли в качестве ln(2)/λz, где λz представляет собой величину наклона логарифмической линейной регрессии профиля логарифма концентрации против времени в ходе терминальной фазы. AUCinf представляет собой площадь под кривой концентрация-время, экстраполированную на бесконечность (AUCinf=AUClast+Clast/ λz, где Clast представляет собой последнюю наблюдаемую концентрацию в плазме). Cmax представляет собой максимальную наблюдаемую концентрацию, соответствующую моменту времени Tmax. Результаты для выбранных соединений представлены в таблице 6.
Пример 7: Эффект лечения блокатором Kv1.3 в модели воспаления уха с гемоцианином лимфы улитки (KLH) у крыс
Классическую реакцию гиперчувствительности замедленного типа (DTH) индуцировали в одном ухе крыс.В кратком изложении, самцов крыс Lewis в возрасте 8-10 недель иммунизировали на сутки -7 посредством 200 мкл гемоцианина лимфы улитки (KLH) (от Sigma, каталожный номер №H7017) (4 мг/мл), эмульгированного в полном адъюванте Фрейнда (CFA) (Difco, каталожный номер №263810) подкожно (п/к) в основание хвоста. На 0 сутки крысам внутрикожно вводили 40 мкл KLH/ NaCl 0,9% (2 мг/мл) в левое ухо. После нагрузки KLH в левом ухе у крыс развивалось зависимое от T-клеток воспаление. Правое ухо оставалось невоспаленным и служило в качестве контроля.
Способность лечения блокатором Kv1.3 снижать ответ DTH в виде опухания уха исследовали путем сравнения ответа у крыс (n=8-10/г), которым вводили носитель, с ответом у крыс, которым вводили блокатор Kv1.3. Носитель или блокатор Kv1.3, растворенный в носителе, вводили п/к (2 мл/кг) за 24 ч до нагрузки уха посредством KLH. Тестируемая доза блокатора Kv1.3 составляла 50, 70 или 100 нмоль/кг.Тестируемый носитель представлял собой 10 мМ фосфат, 0,8% масс./об. NaCl, 0,05% масс./об. полисорбат20, pH 6. Во всех экспериментах в качестве положительного контроля в испытании включали циклоспорин (CsA). Циклоспорин (пероральный раствор Sandimmune Neooral® 100 мг/мл, Novartis) вводили перорально (10 мг/кг) за один час до нагрузки KLH и вновь через 6 часов после нагрузки KLH.
В качестве первичного результата эффективности вычисляли площадь под кривой (AUC) для Δ толщины уха (мм) для каждого животного через 0-48 часов после индукции реакции DTH в ухе, где изменение (D) вычисляли как: толщина левого уха - толщина правого уха. Затем эти результаты использовали для вычисления % ингибирования толщины уха посредством обработки блокатором Kv1.3: % ингибирование: ((1-(индивидуальная Δ AUC блокатора Kv1.3 /средняя ΔAUC в группе носителя)) × 100. Результаты вычисляли в качестве % ингибирования+/-стандартное отклонение (SD), и они представлены в таблице 7 и таблице 8.
кг)
(нмоль/кг)
(+/-8,3)
(+/-7,9)
(+/-14,0)
(+/-5,2)
(+/-5,5)
(+/-8,6)
(+/-5,4)
(+/-10,0)
(+/-2,8)
Работа, описанная в настоящем описании, получила финансирование от European Communities Seventh Framework Program FP7/2007-2013 по соглашению о субсидировании Venomics_CA_20111021.
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ:
--->
<110>Zealand Pharma A/S
<120>БЛОКАТОРЫ Kv1.3
<130>P120765PCT
<150>111-EP-NOR-03
<151>2019-09-20
<150>111-EP-NOR-04
<151>2020-05-04
<160>180
<170>PatentIn version 3.5
<210>1
<211>37
<212>БЕЛОК
<213>Неизвестный
<220>
<223>Токсин Parabuthus transvaalicus (PaT1)
<400>1
Gln Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>2
<211>37
<212>БЕЛОК
<213>Неизвестный
<220>
<223>Токсин Parabuthus transvaalicus (PaT2)
<400>2
Gln Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Arg Gly Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>3
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>3
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>4
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>4
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Arg Gly Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>5
<211>36
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>5
Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys Leu
1 5 10 15
Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys Lys
20 25 30
Cys Tyr Pro Arg
35
<210>6
<211>35
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>6
Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys Leu Lys
1 5 10 15
Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys Lys Cys
20 25 30
Tyr Pro Arg
35
<210>7
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>7
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>8
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>8
Asn Ile Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>9
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>9
Asn Met Asp Val Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>10
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>10
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Lys Asp Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>11
<211>39
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>11
Gly Gly Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln
1 5 10 15
Lys Cys Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys
20 25 30
Lys Cys Lys Cys Tyr Pro Arg
35
<210>12
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>12
Asn Met Glu Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>13
<211>39
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>13
Ser Gly Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln
1 5 10 15
Lys Cys Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys
20 25 30
Lys Cys Lys Cys Tyr Pro Arg
35
<210>14
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<400>14
Asn Xaa Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>15
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<400>15
Asn Met Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>16
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>16
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>17
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>17
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Val Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>18
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>18
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Leu Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>19
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>19
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Lys Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>20
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>20
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Asp Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>21
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>21
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Arg Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>22
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>22
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Glu Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>23
<211>41
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>23
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg Arg Arg Thr Ala
35 40
<210>24
<211>41
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>24
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg His Arg Arg Lys
35 40
<210>25
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>25
Asn Met Asp Met Arg Cys Lys Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>26
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>26
Asn Met Asp Met Arg Cys Ser Ile Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>27
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>27
Asn Met Asp Met Arg Cys Ser Ala Ser Arg Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>28
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>28
Asn Met Asp Met Arg Cys Ser Ala Ser Val Gln Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>29
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>29
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Leu Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>30
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>30
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Ala Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>31
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>31
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Glu Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>32
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>32
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Leu Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>33
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>33
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile His Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>34
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>34
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Lys Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>35
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>35
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Arg Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>36
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>36
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Gly Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>37
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>37
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
His Cys Tyr Pro Arg
35
<210>38
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>38
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Val Cys Tyr Pro Arg
35
<210>39
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<400>39
Asn Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>40
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>40
Asn Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>41
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>41
Pro Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>42
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>42
Asn Xaa Asp Xaa Arg Cys Arg Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>43
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>43
Asn Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Glu Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>44
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>44
Asn Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Gln Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>45
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>45
Asn Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Lys Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>46
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>46
Asn Xaa Ser Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>47
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>47
Asn Xaa Asp Xaa Arg Cys Ser His Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>48
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>48
Asn Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Ser Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>49
<211>36
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(27)..(27)
<223>Xaa представляет собой норлейцин
<400>49
Asn Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys Lys
20 25 30
Cys Tyr Pro Arg
35
<210>50
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>50
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Tyr Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>51
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>51
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Arg Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>52
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>52
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>53
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>53
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Tyr Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>54
<211>36
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>54
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys Lys
20 25 30
Cys Tyr Pro Arg
35
<210>55
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>55
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Tyr Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>56
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>56
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Arg Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>57
<211>36
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>57
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys Lys
20 25 30
Cys Tyr Pro Arg
35
<210>58
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>58
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Tyr Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>59
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>59
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Glu Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>60
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>60
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Arg Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>61
<211>36
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>61
Asn Met Asp Met Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys Lys
20 25 30
Cys Tyr Pro Arg
35
<210>62
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>62
Asn Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Pro Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>63
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>63
Asn Xaa Asp Xaa Arg Cys Ser Ala Ser Lys Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>64
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>64
His Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>65
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>65
Tyr Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>66
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>66
Ser Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>67
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>67
Val Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>68
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(9)..(9)
<223>Xaa представляет собой альфа-аминомасляную кислоту (гомоаланин)
<400>68
Ser Xaa Asp Xaa Arg Cys Ser Ala Xaa Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>69
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(26)..(26)
<223>Xaa представляет собой гомолизин
<400>69
Ser Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Xaa Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>70
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(35)..(35)
<223>Xaa представляет собой 4-аминофенилаланин
<400>70
Ser Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Xaa Pro Arg
35
<210>71
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<400>71
Ser Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Gly Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>72
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<400>72
Ser Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Val Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>73
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(14)..(14)
<223>Xaa представляет собой 2-амино-5-карбоксипентаноил
<400>73
Ser Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Xaa Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>74
<211>36
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<400>74
Ser Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Gln
35
<210>75
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<400>75
Ser Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Arg Cys Tyr Pro Arg
35
<210>76
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<400>76
Ser Xaa Asp Glu Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>77
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<400>77
Ser Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Gly Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>78
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<400>78
Ser Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Val Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>79
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<400>79
Ser Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Ala Gln Ser Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>80
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<400>80
Ser Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Ala Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>81
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<400>81
Ser Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Ala Gln Leu Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>82
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>82
Ser Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>83
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>83
Pro Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Cys Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Cys
35
<210>84
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>84
Ser Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Glu Lys Cys
1 5 10 15
Leu Gln Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>85
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(18)..(18)
<223>Xaa представляет собой гомоглутамин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>85
Pro Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Glu Lys Cys
1 5 10 15
Leu Xaa Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>86
<211>32
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(23)..(23)
<223>Xaa представляет собой норлейцин
<400>86
Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys Leu Lys Ala Ile Gly
1 5 10 15
Cys Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys Lys Cys Tyr Pro Cys
20 25 30
<210>87
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>87
Ser Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Cys Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Cys
35
<210>88
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>88
Pro Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Cys Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Cys
35
<210>89
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<400>89
Ser Xaa Asp Xaa Arg Cys Ser Ala Leu Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>90
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<400>90
Ser Xaa Asp Xaa Arg Cys Ser Ala Val Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>91
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(35)..(35)
<223>Xaa is 4-fluoro-phenylalanine
<400>91
Ser Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Xaa Pro Arg
35
<210>92
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(35)..(35)
<223>Xaa представляет собой 4-нитрофенилаланин
<400>92
Ser Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Xaa Pro Arg
35
<210>93
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(35)..(35)
<223>Xaa представляет собой 4-метилфенилаланин
<400>93
Ser Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Xaa Pro Arg
35
<210>94
<211>36
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(1)..(1)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(3)..(3)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(27)..(27)
<223>Xaa представляет собой норлейцин
<400>94
Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys Leu
1 5 10 15
Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys Lys
20 25 30
Cys Tyr Pro Arg
35
<210>95
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>95
Asn Ile Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>96
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>96
Pro Ile Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Lys Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>97
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>97
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>98
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>98
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>99
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>99
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Leu Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>100
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>100
Pro Ile Asp Glu Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>101
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>101
Pro Ile Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>102
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<400>102
Pro Xaa Asp Xaa Arg Cys Ser Ala Ser Val Glu Cys Ala Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>103
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>103
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Ala Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>104
<211>32
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(23)..(23)
<223>Xaa представляет собой норлейцин
<400>104
Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys Leu Lys Ala Ile Gly
1 5 10 15
Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys Lys Cys Tyr Pro Arg
20 25 30
<210>105
<211>32
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>МОДИФИЦИРОВАННЫЙ ОСТАТОК
<222>(1)..(1)
<223>АЦЕТИЛИРОВАНИЕ
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(23)..(23)
<223>Xaa представляет собой норлейцин
<400>105
Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys Leu Lys Ala Ile Gly
1 5 10 15
Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys Lys Cys Tyr Pro Arg
20 25 30
<210>106
<211>33
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(24)..(24)
<223>Xaa представляет собой норлейцин
<400>106
Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys Leu Lys Ala Ile
1 5 10 15
Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys Lys Cys Tyr Pro
20 25 30
Arg
<210>107
<211>34
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>МОДИФИЦИРОВАННЫЙ ОСТАТОК
<222>(1)..(1)
<223>АЦЕТИЛИРОВАНИЕ
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(25)..(25)
<223>Xaa представляет собой норлейцин
<400>107
Ser Lys Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys Leu Lys Ala
1 5 10 15
Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys Lys Cys Tyr
20 25 30
Pro Arg
<210>108
<211>34
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>МОДИФИЦИРОВАННЫЙ ОСТАТОК
<222>(1)..(1)
<223>АЦЕТИЛИРОВАНИЕ
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(25)..(25)
<223>Xaa представляет собой норлейцин
<400>108
Leu Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys Leu Lys Ala
1 5 10 15
Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys Lys Cys Tyr
20 25 30
Pro Arg
<210>109
<211>32
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>МОДИФИЦИРОВАННЫЙ ОСТАТОК
<222>(1)..(1)
<223>АЦЕТИЛИРОВАНИЕ
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(23)..(23)
<223>Xaa представляет собой норлейцин
<400>109
Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys Leu Lys Ala Ile Gly
1 5 10 15
Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys Lys Cys Tyr Pro Ser
20 25 30
<210>110
<211>31
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>МОДИФИЦИРОВАННЫЙ ОСТАТОК
<222>(1)..(1)
<223>АЦЕТИЛИРОВАНИЕ
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(23)..(23)
<223>Xaa представляет собой норлейцин
<400>110
Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys Leu Lys Ala Ile Gly
1 5 10 15
Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys Lys Cys Tyr Ser
20 25 30
<210>111
<211>31
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>МОДИФИЦИРОВАННЫЙ ОСТАТОК
<222>(1)..(1)
<223>АЦЕТИЛИРОВАНИЕ
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(23)..(23)
<223>Xaa представляет собой норлейцин
<400>111
Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys Leu Lys Ala Ile Gly
1 5 10 15
Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys Lys Cys Tyr Gly
20 25 30
<210>112
<211>30
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>МОДИФИЦИРОВАННЫЙ ОСТАТОК
<222>(1)..(1)
<223>АЦЕТИЛИРОВАНИЕ
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(23)..(23)
<223>Xaa представляет собой норлейцин
<400>112
Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys Leu Lys Ala Ile Gly
1 5 10 15
Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys Lys Cys Tyr
20 25 30
<210>113
<211>33
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>МОДИФИЦИРОВАННЫЙ ОСТАТОК
<222>(1)..(1)
<223>АЦЕТИЛИРОВАНИЕ
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(24)..(24)
<223>Xaa представляет собой норлейцин
<400>113
Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys Leu Lys Ala Ile
1 5 10 15
Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys Lys Cys Tyr Pro
20 25 30
Arg
<210>114
<211>34
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(25)..(25)
<223>Xaa представляет собой норлейцин
<400>114
Leu Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys Leu Lys Ala
1 5 10 15
Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys Lys Cys Tyr
20 25 30
Pro Arg
<210>115
<211>34
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>МОДИФИЦИРОВАННЫЙ ОСТАТОК
<222>(1)..(1)
<223>АЦЕТИЛИРОВАНИЕ
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(25)..(25)
<223>Xaa представляет собой норлейцин
<400>115
Leu Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys Leu Ala Ala
1 5 10 15
Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys Lys Cys Tyr
20 25 30
Pro Arg
<210>116
<211>34
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>МОДИФИЦИРОВАННЫЙ ОСТАТОК
<222>(1)..(1)
<223>АЦЕТИЛИРОВАНИЕ
<400>116
Leu Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys Leu Ala Ala
1 5 10 15
Ile Gly Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys Lys Cys Tyr
20 25 30
Pro Arg
<210>117
<211>32
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<400>117
Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys Leu Lys Ala Ile Gly
1 5 10 15
Ser Ile Phe Gly Lys Cys Met Asn Lys Lys Cys Lys Cys Tyr Pro Arg
20 25 30
<210>118
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>118
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Glu Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>119
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(1)..(1)
<223>D-пролин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>119
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>120
<211>36
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>120
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Arg
35
<210>121
<211>36
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(1)..(1)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(3)..(3)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(27)..(27)
<223>Xaa представляет собой норлейцин
<400>121
Xaa Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys Leu
1 5 10 15
Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys Lys
20 25 30
Cys Tyr Pro Arg
35
<210>122
<211>38
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>122
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg Arg
35
<210>123
<211>38
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>123
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg Tyr
35
<210>124
<211>38
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>124
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg Leu
35
<210>125
<211>38
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>125
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg His
35
<210>126
<211>38
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>126
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg Glu
35
<210>127
<211>39
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>127
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg Lys Ser
35
<210>128
<211>39
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>128
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg Phe Glu
35
<210>129
<211>39
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>129
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg His Arg
35
<210>130
<211>39
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>130
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg Ala Lys
35
<210>131
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(37)..(37)
<223>Xaa представляет собой (4-amino-5-гидроксипентил)гуанидин
<400>131
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Xaa
35
<210>132
<211>38
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(38)..(38)
<223>Xaa представляет собой 4-амино-5-гидроксипентанамид
<400>132
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg Xaa
35
<210>133
<211>39
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>133
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg Ser Thr
35
<210>134
<211>39
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>134
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg Arg Tyr
35
<210>135
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>135
Pro Xaa Glu Xaa Arg Cys Ser Ser Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>136
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>136
Pro Xaa Glu Xaa Arg Cys Ser Leu Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>137
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>137
Pro Xaa Glu Xaa Arg Cys Ser Ala Pro Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>138
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>138
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Pro Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>139
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>139
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Gln Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>140
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>140
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Leu Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>141
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>141
Pro Xaa Glu Xaa Arg Cys Ser Ala Ser Val Glu Cys Lys Gln Pro Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>142
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>142
Pro Xaa Glu Xaa Arg Cys Glu Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>143
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>143
Pro Xaa Glu Xaa Arg Cys Phe Ala Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>144
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>144
Pro Xaa Glu Xaa Arg Cys Ser Tyr Ser Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>145
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 1
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(4)..(4)
<223>Xaa представляет собой норлейцин
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(28)..(28)
<223>Xaa представляет собой норлейцин
<400>145
Pro Xaa Glu Xaa Arg Cys Ser Ala Phe Val Glu Cys Lys Gln Lys Cys
1 5 10 15
Leu Ala Ala Ile Gly Ser Ile Phe Gly Lys Cys Xaa Asn Lys Lys Cys
20 25 30
Lys Cys Tyr Pro Arg
35
<210>146
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>146
Arg Arg Thr Ala
1
<210>147
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>147
His Arg Arg Lys
1
<210>148
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>148
Gln Ser Lys Ala
1
<210>149
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>149
Ala Gly Pro Arg
1
<210>150
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>150
Arg Ser Arg Thr
1
<210>151
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>151
Arg His Lys Arg
1
<210>152
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>152
Gly Gly Lys Arg
1
<210>153
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>153
Pro Lys Thr Ala
1
<210>154
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>154
Thr Asp Ala Arg
1
<210>155
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>155
His Arg Gln Gln
1
<210>156
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>156
Arg Pro Arg His
1
<210>157
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>157
Ala Arg Asn Ala
1
<210>158
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>158
Thr Gly Arg Lys
1
<210>159
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>159
His Glu Arg Thr
1
<210>160
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>160
Asn Thr Arg Thr
1
<210>161
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>161
Gln Arg Asn Gly
1
<210>162
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>162
Ala His Arg Asn
1
<210>163
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>163
Pro Arg Ser Ala
1
<210>164
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>164
Gln Arg Gln Ser
1
<210>165
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>165
Gln Arg Arg Lys
1
<210>166
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>166
Ala Arg Ala Lys
1
<210>167
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>167
Ala Lys Arg Asp
1
<210>168
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>168
Arg Asp Lys Thr
1
<210>169
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>169
His Arg Arg Lys
1
<210>170
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>170
Arg Ala Lys Arg
1
<210>171
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>171
Gln Arg Thr Arg
1
<210>172
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>172
Ala Thr Arg His
1
<210>173
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>173
Ala Arg Arg Ser
1
<210>174
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>174
Ala Lys Thr Arg
1
<210>175
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>175
Asn Arg Gln Arg
1
<210>176
<211>4
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Дополнительная C-концевая последовательность
<400>176
Pro Arg Asn Thr
1
<210>177
<211>35
<212>БЕЛОК
<213>Stichodactyla helianthus
<400>177
Arg Ser Cys Ile Asp Thr Ile Pro Lys Ser Arg Cys Thr Ala Phe Gln
1 5 10 15
Cys Lys His Ser Met Lys Tyr Arg Leu Ser Phe Cys Arg Lys Thr Cys
20 25 30
Gly Thr Cys
35
<210>178
<211>37
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Модифицированная SEQ ID NO 177 (ShK-186)
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(1)..(1)
<223>Xaa представляет собой фосфотирозил
<220>
<221>ДОПОЛНИТЕЛЬНЫЙ ПРИЗНАК
<222>(2)..(2)
<223>Xaa представляет собой 8-амино-3,6-диоксаоктаноил
<400>178
Xaa Xaa Arg Ser Cys Ile Asp Thr Ile Pro Lys Ser Arg Cys Thr Ala
1 5 10 15
Phe Gln Cys Lys His Ser Met Lys Tyr Arg Leu Ser Phe Cys Arg Lys
20 25 30
Thr Cys Gly Thr Cys
35
<210>179
<211>34
<212>БЕЛОК
<213>Искусственная последовательность
<220>
<223>Мокатоксин 1 (Moka1)
<400>179
Ile Asn Val Lys Cys Ser Leu Pro Gln Gln Cys Ile Lys Pro Cys Lys
1 5 10 15
Asp Ala Gly Met Arg Phe Gly Lys Cys Met Asn Lys Lys Cys Arg Cys
20 25 30
Tyr Ser
<210>180
<211>36
<212>БЕЛОК
<213>Неизвестный
<220>
<223>Токсин Vaejovis mexicanus (Vm24)
<400>180
Ala Ala Ala Ile Ser Cys Val Gly Ser Pro Glu Cys Pro Pro Lys Cys
1 5 10 15
Arg Ala Gln Gly Cys Lys Asn Gly Lys Cys Met Asn Arg Lys Cys Lys
20 25 30
Cys Tyr Tyr Cys
35
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| ПЛАТФОРМА НА ОСНОВЕ КАРКАСА ЦИСТИНОВОГО УЗЛА | 2016 |
|
RU2770384C2 |
| КОНСТРУКЦИИ, ИМЕЮЩИЕ SIRP-АЛЬФА ДОМЕН ИЛИ ЕГО ВАРИАНТ | 2016 |
|
RU2740672C2 |
| ПЕПТИД, ОБЛАДАЮЩИЙ АКТИВНОСТЬЮ БЕЛКА SLURP-1 ЧЕЛОВЕКА, И ЕГО ПРИМЕНЕНИЕ ДЛЯ ПОДАВЛЕНИЯ РОСТА КАРЦИНОМ И ГЛИОМ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПОДАВЛЕНИЯ РОСТА КАРЦИНОМ И ГЛИОМ, И СПОСОБ ПОДАВЛЕНИЯ РОСТА КАРЦИНОМ И ГЛИОМ С ИСПОЛЬЗОВАНИЕМ УКАЗАННОГО ПЕПТИДА | 2022 |
|
RU2792364C1 |
| СУБСТРАТЫ МАТРИКСНОЙ МЕТАЛЛОПРОТЕИНАЗЫ И ДРУГИЕ РАСЩЕПЛЯЕМЫЕ ФРАГМЕНТЫ И СПОСОБЫ ИХ ИСПОЛЬЗОВАНИЯ | 2014 |
|
RU2832636C2 |
| ВАРИАНТЫ СВИНОГО G-CSF И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2823074C2 |
| ВАРИАНТНЫЕ МОЛЕКУЛЫ IL-10 И СПОСОБ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННОЙ ОПУХОЛИ | 2020 |
|
RU2836849C2 |
| ИСКУССТВЕННЫЕ НЕИЗБИРАТЕЛЬНЫЕ ЭПИТОПЫ КЛЕТОК Т-ХЕЛПЕРОВ КАК ИММУННЫЕ СТИМУЛЯТОРЫ ДЛЯ СИНТЕТИЧЕСКИХ ПЕПТИДНЫХ ИММУНОГЕНОВ | 2019 |
|
RU2839585C2 |
| ИММУНОЦИТОКИНЫ НА ОСНОВЕ IL-15 И IL-15Rα ДОМЕНА SUSHI | 2012 |
|
RU2763298C2 |
| МОЛЕКУЛЫ, СВЯЗЫВАЮЩИЕ ADAM9, И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2017 |
|
RU2783619C2 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ ЖЕЛУДОЧНО-КИШЕЧНЫХ РАССТРОЙСТВ | 2014 |
|
RU2763796C2 |
Группа изобретений относится к химии и фармацевтической промышленности, а именно: к блокатору ионного канала (или его фармацевтически приемлемой соли), выбранному из 145 соединений, имеющих аминокислотные последовательности SEQ ID NO: 1-145 в перечне последовательностей; к способу его синтеза; к композиции для лечения воспалительного состояния или нарушения, содержащей предложенный блокатор ионного канала и носитель, эксципиент или наполнитель; к применениям указанного блокатора ионного канала для ингибирования или уменьшения воспаления и для лечения воспалительного состояния или нарушения. Также предложены варианты блокатора ионного канала, имеющего аминокислотную последовательность SEQ ID NO: 3, 30, 95, 97, 101 или 103, в которой пары остатков цистеина (С) такие, как 6С и 27С, 12С и 32С, 16С и 34С, участвуют в образовании дисульфидной связи. Группа изобретений обеспечивает новые блокаторы ионных каналов Kv1.3. 11 н. и 2 з.п. ф-лы, 11 табл., 8 пр.
1. Блокатор ионного канала или его фармацевтически приемлемая соль, выбранный из:
2. Блокатор ионного канала, который представляет собой H-NMDMRC(1)SASVEC(2)KQKC(3)LKAIGSIFGKC(1)MNKKC(2)KC(3)YPR-OH (SEQ ID NO. 3) (соединение 3), или его фармацевтически приемлемая соль, где пара остатков цистеина, которые вместе участвуют в образовании дисульфидной связи, указана одним и тем же числом в скобках.
3. Блокатор ионного канала, который представляет собой H-NMDMRC(1)SASVEC(2)AQKC(3)LKAIGSIFGKC(1)MNKKC(2)KC(3)YPR-NH2(SEQ ID NO. 30) (соединение 30), или его фармацевтически приемлемая соль, где пара остатков цистеина, которые вместе участвуют в образовании дисульфидной связи, указана одним и тем же числом в скобках.
4. Блокатор ионного канала, который представляет собой H-NID[Nle]RC(1)SASVEC(2)KQKC(3)LKAIGSIFGKC(1)[Nle]NKKC(2)KC(3)YPR-OH (SEQ ID NO. 95) (соединение 95), или его фармацевтически приемлемая соль, где пара остатков цистеина, которые вместе участвуют в образовании дисульфидной связи, указана одним и тем же числом в скобках.
5. Блокатор ионного канала, который представляет собой H-P[Nle]E[Nle]RC(1)SASVEC(2)KQKC(3)LAAIGSIFGKC(1)[Nle]NKKC(2)KC(3)YPR-OH (SEQ ID NO. 97) (соединение 97), или его фармацевтически приемлемая соль, где пара остатков цистеина, которые вместе участвуют в образовании дисульфидной связи, указана одним и тем же числом в скобках.
6. Блокатор ионного канала, который представляет собой H-PIE[Nle]RC(1)SASVEC(2)KQKC(3)LAAIGSIFGKC(1)[Nle]NKKC(2)KC(3)YPR-OH (SEQ ID NO. 101) (соединение 101), или его фармацевтически приемлемая соль, где пара остатков цистеина, которые вместе участвуют в образовании дисульфидной связи, указана одним и тем же числом в скобках.
7. Блокатор ионного канала, который представляет собой H-P[Nle]E[Nle]RC(1)SASVEC(2)AQKC(3)LAAIGSIFGKC(1)[Nle]NKKC(2)KC(3)YPR-OH (SEQ ID NO. 103) (соединение 103), или его фармацевтически приемлемая соль, где пара остатков цистеина, которые вместе участвуют в образовании дисульфидной связи, указана одним и тем же числом в скобках.
8. Способ синтеза блокатора ионного канала по любому из пп.1-7, причем способ включает:
(a) синтез блокатора ионного канала посредством методологии твердофазного или жидкофазного синтеза пептидов и выделение полученного таким образом пептида;
(b) экспрессию блокатора ионного канала с конструкции нуклеиновой кислоты, которая кодирует блокатор ионного канала и выделение продукта экспрессии; или
(c) экспрессию пептида-предшественника с конструкции нуклеиновой кислоты, которая кодирует последовательность пептида-предшественника, выделение продукта экспрессии и модификацию пептида-предшественника с получением блокатора ионного канала.
9. Композиция для лечения воспалительного состояния или нарушения, содержащая блокатор ионного канала или его фармацевтически приемлемую соль по любому из пп.1-7 и носитель, эксципиент или наполнитель.
10. Применение блокатора ионного канала или его фармацевтически приемлемой соли по любому из пп.1-7 для ингибирования или уменьшения воспаления.
11. Применение блокатора ионного канала или его фармацевтически приемлемой соли по любому из пп.1-7 для лечения воспалительного состояния или нарушения.
12. Применение по п.11, где воспалительное состояние или нарушение представляет собой аутоиммунное нарушение, аллергию или гиперчувствительность, отторжение аллотрансплантата или реакцию "трансплантат против хозяина".
13. Применение по п.11 или 12, где воспалительное состояние или заболевание представляет собой сенную лихорадку, астму, анафилаксию, аллергический ринит, крапивницу, экзему, очаговую алопецию, дерматомиозит, миозит с тельцами включения, полимиозит, анкилозирующий спондилит, васкулит, артрит (включая ревматоидный артрит, остеоартрит, псориатический артрит), синдром Шегрена, системную красную волчанку (SLE), увеит, воспалительный фиброз (например склеродермия, фиброз легких, цирроз), хроническое обструктивное заболевание легких (COPD), гепатит, хроническую воспалительную демиелинизирующую полиневропатию, воспалительное заболевание кишечника, колит (включая болезнь Крона и язвенный колит), эритему, тиреоидит, псориаз, атопический дерматит, аллергический контактный дерматит, склеродермию, гломерулонефрит, воспалительную резорбцию кости, рассеянный склероз, диабет 1 типа, отторжение трансплантата или реакцию "трансплантат против хозяина".
| WO 2008088422 A2, 24.07.2008 | |||
| Adam Bartok et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Вулканизационная форма | 1927 |
|
SU18397A1 |
| US 20140255401 A1, 11.09.2014 | |||
| КЛЕТКА-ХОЗЯИН, СОДЕРЖАЩАЯ ВЕКТОР ДЛЯ ПРОДУЦИРОВАНИЯ БЕЛКОВ, ТРЕБУЮЩИХ ГАММА-КАРБОКСИЛИРОВАНИЯ | 2006 |
|
RU2415934C2 |
| Steve Reynaud et al | |||
| A Venomics Approach Coupled to High-Throughput Toxin | |||
Авторы
Даты
2024-08-28—Публикация
2020-09-18—Подача