Заявленная группа изобретений относится к медицине и медицинским эндопротезам, предназначена для использования в эндоваскулярной и сердечно-сосудистой хирургии при лечении аневризм (АА) и расслоения аорты (РА).
Сердечно-сосудистые заболевания (ССЗ) лидируют в структуре общей смертности во всем мире, в т.ч. в России и составляют 57,1%. По данным ВОЗ, каждый год от ССЗ умирает 17,5 миллиона человек. Это составляет примерно 31% всех случаев смерти в мире. 85% этих смертей происходит в результате сердечного приступа и/или инсульта. Мировая статистика здравоохранения регистрирует неуклонный рост заболеваемости аневризмами аорты (АА) (особенно в последние десятилетия), и к настоящему времени эта патология уже перестала являться казуистикой, занимая одно из ведущих позиций среди сердечно-сосудистых заболеваний.
В современной сосудистой хирургии аневризмы дуги аорты, грудной и брюшной аорты, а также расслоение представляют собой сложную клиническую и техническую проблему, так как они отличаются особой опасностью в связи с осложнениями, которые нередко сопровождают эти заболевания и создают реальную опасность летального исхода или тяжелой инвалидизации из-за высокого риска разрыва.
Несмотря на существенный риск побочных интра- и послеоперационных осложнений, а также значительного риска смертности, на протяжении более 40 лет хирургическая резекция с установкой сосудистого протеза, а также хирургическое восстановление с полной заменой дуги аорты были первым методом выбора. К сожалению, более 40% пациентов считаются непригодными для выполнения таких процедур из-за их возраста и сердечно-легочного статуса. (Is it time for total endovascular aortic arch replacement? VEITHsymposium Bulletin July 2020). Метаанализ Urbanski et al. показал среднюю 30-дневную смертность в 11% среди 1232 пациентов, получавших лечение на дуге аорты, со значительной разностью в показателях смертности (от 2% до 19%), которая зависела от опыта центра, возраста пациента, предшествующей стернотомии и потребности в сопутствующей реконструкции. (Multicentre analysis of current strategies and outcomes in open aortic arch surgery: heterogeneity is still an issue. Eur J Cardiothorac Surg. 2016;50(2):249-255.).
Ввиду этого, в последнее десятилетие эндоваскулярная реконструкция становится все более популярной и заключается в помещении стент-графта (СГ) в аневризматический мешок с проксимальной и дистальной фиксацией на здоровых сегментах артерии. Такой подход является альтернативой открытой операции и методом выбора для больных с тяжелой сопутствующей патологией, с высоким риском интра- и послеоперационных осложнений.
СГ представляет собой трубку из синтетического или биологического материала, соединенного с металлическим компонентом, обеспечивающим опорную функцию. Современные СГ - самораскрывающиеся, их составными частями являются: металлический каркас и искусственный тканый материал покрытия. В настоящее время доступны несколько моделей СГ для лечения АБА, которые различаются по дизайну, количеству модулей, основе и структуре стента, толщине, порозности, методам прикрепления ткани протеза к стенту и наличию или отсутствию возможности активной фиксации устройства к стенке аорты.
Также к СГ предъявляется множество требований, в основном связанных либо с тканным компонентом (проницаемость, биосовместимость, атромбогенность, гибкость, прочность и износостойкость), либо с каркасным (развиваемое радиальное усилие, радиальная жесткость, эластичность, рентгенконтрастность и износостойкость). Кроме требований к компонентам, дизайн стент-графта также должен решать поставленные проблемы, в особенности связанных с анатомией аорты и ее ветвей. Тем не менее, для эндоваскулярного стентирования также характерно появление ряда специфических осложнений, таких как эндолики (затеки в пространство между протезом и аневризматическим мешком), переломы стента или стент-графта, смещение трансплантата, разрыв подвздошных артерий, ретроградное расслоение, микроэмболизация, аортоэзофагеальный (аортопищеводный) свищ и локальные осложнения в месте доставки (например, инфекция паховой области, лимфоцеле, серома).
Наиболее часто используемые в мире для лечения АА являются СГ Endurant II, Excluder С3, Zenith и их аналоги. Все эти СГ представляют собой модульные конструкции цилиндрической или конической формы, выполненные из синтетического материала (дакрон, политетрафторэтилен (ПТФЭ)) с подшитым к нему металлическим каркасом различной формы (нитиноловый стент). Применение данных СГ у ряда пациентов ограничено особенностями сосудистой анатомии и типом аневризм. А также для установки таких СГ обязательным условием является наличие неизмененной стенки аорты в проксимальной и дистальной зонах имплантации для надежной фиксации. В связи с этим, только 70% пациентам с АА возможно предложить данный вид лечения. В остальных 30% случаях наличие короткой шейки аневризмы или ее отсутствие, вовлечение в аневризматический мешок крупных магистральных артерий (брахиоцефальные, висцеральные) является абсолютным противопоказанием к эндоваскулярному лечению.
Известны специальные персонифицированные модели СГ, такие как фенестрированные (Zenith Fenestrated) или браншированные СГ (E-xtra DESIGN ENGINEERING). Появление таких СГ фенестрированных и браншированных графтом заводским методом продемонстрировало оптимистичные результаты, однако техническая сложность выполнения процедуры и высокая стоимость расходного материалы не позволяет внедрить эту методику в широкую клиническую практику, тем более включить в рамки оказания высокотехнологической медицинской помощи. В связи с этим были предложены различные варианты выполнения фенестрации (так называемого отверстия) в только что имплантированный стент-графт: устройства для лазерной и радиочастотной фенестрации, выполнение фенестрации жесткой стороной проводника или с помощью специального катетера с пункционной иглой на его кончике. Однако, применяемые на практике такие методы требуют ретроградного проведения проводника с инструментом для фенестрации с использованием дополнительного хирургического доступа. Это приводит к дополнительной травматизации и риску возникновения осложнений. Проведение проводника в антеградном направлении сопряжено с трудностями визуализации перерытых сосудов и невозможности обеспечения навигации для эндоваскулярной реваскуляризации, что, в свою очередь, может привести к ятрогенному повреждению артериальной стенки и массивному кровотечению. А также наличие эндоликов компрометирует предложенные методы фенестрации в виду того, что сохраняется сообщение с полостью аневризмы имеющейся модели.
Для устранения указанных недостатков были разработаны некоторые специальные эндоваскулярные устройства, которые могут использоваться при наличии сложных аневризм с включением в процесс основных боковых ветвей внутри или около аневризматического мешка. Наиболее известными из них являются стенты с многослойным модулятором потока (ММП) [Stenting complex aorta aneurysms with the Cardiatis multilayer flow modulator: first impressions. Eur J Vasc Endovasc Surg. 2014. A Single- Center Experience of Aortic and Iliac Artery Aneurysm Treated with Multilayer Flow Modulator. Ann Vasc Surg. 2016. Evidence of use of multilayer flow modulator stents in treatment of thoracoabdominal aortic aneurysms and dissections. Journal of Vascular Surgery April 2017]. Такие стенты представляют собой саморасширяющиеся, трехслойные, радиально-прочные и эластичные стенты, содержащие хромкобальтовый сплав, и стенты с открытой структурой, не покрытые каким-либо материалом. Они были разработаны для лечения аневризм аорты и периферических артерий. Эти многослойные стенты изменяют динамику потока вдоль сосуда, преобразовывая турбулентный поток в мешочке аневризмы в ламинарный поток, и в то же время действуют как пассивный барьер, значительно уменьшая поток крови в сторону стенки аневризмы (>90%). Они обеспечивают образование тромба в аневризматическом мешке, и размер аневризмы со временем уменьшается [The combined use of multilayer flow modulator stent and conventional stent grafts in complex thoracoabdominal aortic aneurysms and Type 3 dissections accompanying aneurysms. Turk Gogus Kalp Damar Cerrahisi Derg. 2018 Apr.]. Однако, и такие стенты не лишены ряда недостатков. Во-первых, длительное время сохраняется кровоток в полость аневризмы с возможностью известных осложнений данного заболевания. Во-вторых, через 12 месяцев и более, как правило, конструкция становится непроницаемой для крови за счет тромбообразования. Что ведет к ишемии жизненно-важных органов и даже к летальным исходам.
В настоящее время для лечения АА стали активно применять модульные системы бифуркационных стент-графтов (патенты US 7887576, US 9687337). Известные системы как правило состоят из трех модулей: раздвоенного основного корпуса с супраренальной фиксацией (аортально-бифуркационный сегмент, содержащий основное трубчатое тело с разветвленными ножками на дистальном конце и стентом, без тканного материала, но с фиксирующими цапками для зацепления со стенкой аорты проксимальнее почечных артерий, на проксимальном конце) и двух ножных модулей (два подвздошных трубчатых сегмента). Основной корпус и ножные модули представляют собой трубчатые тела, выполненные из биосовместимого тканного материала, прикрепленного к стентам и поддерживаемого ими. Основной корпус располагается в аорте. Ножные модули располагаются в подвздошных артериях и соединяются с основным корпусом.
Однако со временем в результате физиологического процесса заболевания артерии и роста аневризмы как фиксация, так и герметизация могут быть нарушены. Например, шейка аорты может еще больше расширяться из-за прогрессирования атеросклеротической болезни или механического воздействия стента. Таким образом, стент-графт может потерять свое уплотнение по отношению в стенки аорты, что приведет к образованию эндоликов. Естественно, эндолики могут быть серьезной проблемой, мешающей стент-графту выполнять свою функцию. Эндолик, даже относительно небольшой, может привести к увеличению аневризмы, увеличивая риск разрыва. Потеря посадки также может снизить силы трения, которые удерживают стент-графт на месте. Кроме того, фиксация, обеспеченная цапками, может быть под угрозой из-за отказа фиксации цапками или локального разрыва стенки аорты. Потеря фиксации крайне нежелательна и может также способствовать смертности и заболеваемости пациентов. Кроме того, миграция стент-графта может вызвать эндолик типа I и увеличить необходимость хирургического вмешательства для устранения эндолика.
Наиболее близкой по технической сути является система бифуркационного стент-графта для лечения аневризмы брюшной аорты, описанная в патенте RU 2742451, которая выбрана нами в качестве прототипа.
Прототип представляет собой систему СГ, состоящую из аортально-бифуркационного сегмента, двух подвздошных сегментов и дополнительного внутреннего сегмента.
Аортально-бифуркационный сегмент содержит основное трубчатое тело с разветвленными ножками на дистальном конце, выполненное из биосовместимого тканного материала, прикрепленного к стентам и поддерживаемого ими.
Проксимальный конец аортально-бифуркационного сегмента выполнен с возможностью входить в зацепление с частью аорты без аневризматического расширения, проксимальной от почечных артерий, и содержит только металлический, выполненный с возможностью расширения, каркас (например, стент), без тканного материала, но с фиксирующими цапками для зацепления со стенкой аорты проксимальнее почечных артерий. Часть аортально-бифуркационного сегмента, размещаемая в проксимальной шейке аневризмы брюшной аорты, выполнена только из стента/стентов, без биосовместимого тканного материала, но с фиксирующими разнонаправленными (например, каудально и краниально) цапками на внешней поверхности для зацепления со стенкой аорты.
Каждый из подвздошных сегментов содержит трубчатое тело, выполненное из биосовместимого тканного материала, прикрепленного к стентам и поддерживаемого ими, при этом проксимальный конец каждого подвздошного сегмента выполнен с возможностью соединения с просветом ножки аортально-бифуркационного сегмента.
Дополнительный внутренний сегмент выполнен с возможностью плотного прилегания к части аортально-бифуркационного сегмента, размещаемой в проксимальной шейке аневризмы брюшной аорты, и содержит трубчатое тело из биосовместимого тканного материала и стенты, прикрепленные к биосовместимому тканному материалу вдоль длины трубчатого тела и поддерживающие его.
Для обеспечения герметичности при наличии неблагоприятной анатомии проксимальной шейки аневризмы (например, короткая или дилатированная шейка, трапецивидная шейка и т.п.) система для лечения аневризмы брюшной аорты может включать в себя дополнительный внешний сегмент, содержащий тело из биосовместимого тканного материала. Дополнительный внешний сегмент выполнен с возможностью размещения вокруг части брюшной аорты ниже отхождения почечных артерий и обеспечения плотного прижатия проксимальной шейки аневризмы брюшной аорты к части аортально-бифуркационного сегмента, размещаемой в проксимальной шейке аневризмы брюшной аорты. Дополнительный внешний сегмент представляет собой ремень или ленту шириной от 10 до 30 мм замыкаемую в кольцо и снабженную застежкой или пряжкой, или нитями для завязывания на узел.
Способ лечения аневризмы брюшной аорты с использованием ранее упомянутой системы - прототипа, включает этапы на которых: вводят аортально-бифуркационный сегмент в брюшную аорту; размещают аортально-бифуркационный сегмент в контакте с тканями аорты так, чтобы расположенный на его проксимальном конце металлический каркас был сцеплен со стенкой аорты проксимальнее почечных артерий, а часть аортально-бифуркационного сегмента, размещенная в проксимальной шейке аневризмы брюшной аорты, была сцеплена со стенкой проксимальной шейки аневризмы брюшной аорты; вводят первый подвздошный сегмент в левую или правую подвздошную артерию; размещают первый подвздошный сегмент в контакте с тканями соответственно левой или правой подвздошной артерии и соединяют проксимальный конец указанного подвздошного сегмента с просветом одной из ножек аортально-бифуркационного сегмента; вводят второй подвздошный сегмент в другую правую или левую подвздошную артерию; размещают второй подвздошный сегмент в контакте с тканями соответственно другой правой или левой подвздошной артерии и соединяют проксимальный конец указанного подвздошного сегмента с просветом другой ножки аортально-бифуркационного сегмента; вводят баллонный катетер и выполняют дополнительную баллонную дилатацию части аортально-бифуркационного сегмента, размещенной в проксимальной шейке аневризмы брюшной аорты; вводят дополнительный внутренний сегмент внутрь аортально-бифуркационного сегмента; размещают дополнительный внутренний сегмент в плотном контакте с частью аортально-бифуркационного сегмента, размещенной в проксимальной шейке аневризмы брюшной аорты.
Несмотря на очевидные достоинства представленного прототипа, он имеет ряд объективных недостатков и ограничений. Во-первых, возникают трудности введения проводника в контралатеральную ножку основного ствола на фоне аневризматического расширения подвздошных артерий. Во-вторых, возникает опасность травматизации истонченной стенки аорты цапками для фиксации. В прототипе фиксирующие цапки проксимального аортально-бифуркационного сегмента выполнены в виде элементов «короны», что создает препятствие для стентирования почечных артерий и повышает тромбообразование. В-третьих, для обеспечения герметичности аневризматического мешка, как указано прототипе, устанавливают дополнительный внешний сегмент лапароскопическим или открытым хирургическим доступом вокруг брюшной аорты ниже отхождения почечных артерий. Однако, известно, что опыт внешнего бандажа аневризмы аорты не является положительным, т.к. аневризма склонна к прогрессированию, что исключает стойкую профилактику ее разрыва. А имплантация внешнего элемента лапароскопическим или открытым хирургическим доступом вызывает дополнительную травматизацию и повышает опасность перфорации мешка аорты, а также может привести к разрыву аневризмы аорты. Так же, система, описанная в прототипе, не является универсальной и применима только в определенной анатомической области аорты.
Таким образом, несмотря на совершенствование хирургической техники операций, разработки новых устройств с применением качественных материалов для протезирования аорты, лечение больных с АА и РА является актуальной проблемой сосудистой хирургии.
Технический результат, обеспечиваемый заявленной группой изобретений, заключается в создании универсальной (без ограничений типов и локализации аневризм) и безопасной для имплантации системы стент-графта для лечения аневризм и расслоений аорты.
Технический результат обеспечивается предложенной системой бифуркационного стент-графта для лечения аневризм и расслоения аорты, которая включает в себя аорто-бифуркационный сегмент, два подвздошных сегмента в виде «ножек» и от 1 до 4х дополнительных сегмента для проксимальных отделов аорты.
Аортально-бифуркационный сегмент содержит основное трубчатое тело, выполненное из металлического стента с возможностью расширения и прикрепленного к нему на всем его протяжении биосовместимого тканного материала. Дополнительно, по сагиттальному диаметру выполняется стяжка дистального конца для формирования левого и правого отверстий дистального конца сегмента. Проксимальный и дистальный концы сегмента отмечены рентгенконтрастными маркерами.
Каждый из подвздошных сегментов содержит трубчатое тело, выполненное из металлического стента с возможностью расширения и прикрепленного к нему биосовместимого тканного материала на всём его протяжении. Проксимальный и дистальный концы сегментов отмечены рентгенконтрастными маркерами. При этом каждый проксимальный конец подвздошных сегментов за счет расширения металлического стента (каркаса) имеет возможность герметичной фиксации в соответствующий просвет левого и/или правого отверстий дистального конца аортально-бифуркационного сегмента.
Каждый из дополнительных сегментов (от 1 до 4х) для проксимальных отделов аорты содержит трубчатое тело, выполненное из металлического стента с возможностью расширения и прикрепленного к нему биосовместимого тканного материала на всем его протяжении, причем проксимальный и дистальный концы сегмента отмечены рентгенконтрастными маркерами. Дистальный конец сегментов, за счет возможности расширения металлического стента (каркаса), имеет возможность герметичной фиксации в просвете проксимального конца аортально-бифуркационного сегмента, а также, при необходимости, в просвете проксимального конца 2го и последующих дополнительных сегментов для проксимальных отделов аорты.
Также технический результат обеспечивается предложенным способом лечения аневризмы и расслоения аорты с использованием системы ранее упомянутой ССГ, включающим этапы, на которых вводят аортально-бифуркационный сегмент в брюшную аорту, вводят первый подвздошный сегмент в левую или правую подвздошную артерию, вводят второй подвздошный сегмент в другую левую или правую подвздошную артерию и вводят дополнительный сегмент, согласно изобретению, при введении аотально-бифуркационного сегмента в брюшную аорту, дистальный конец его размещают на бифуркации аорты, после чего сегмент саморасширяется, затем вводят первый подвздошный сегмент в левую или правую подвздошную артерию, размещая при этом его проксимальный конец на 5-8 мм в просвете соответствующего левого или правого отверстия профиля-двустволки аортально-бифуркационного сегмента, после чего первый подвздошный сегмент саморасширяется, затем вводят второй подвздошный сегмент в другую левую или правую подвздошную артерию, размещая при этом его проксимальный конец на 5-8 мм в просвете соответствующего левого или правого отверстия дистального конца аортально-бифуркационного сегмента, после чего второй подвздошный сегмент саморасширяется, затем через просвет установленного первого или второго подвздошного сегмента и через просвет установленного аортально-бифуркационного сегмента на проводнике вводят первый дополнительный сегмент для проксимальных отделов аорты, размещая его дистальный конец на 5-8 мм в просвете проксимального конца аортально-бифуркационного сегмента, после чего первый дополнительный сегмент саморасширяется, а установку второго, третьего и четвёртого дополнительных сегменток для проксимальных отделов аорты осуществляют при необходимости способом аналогичным установке первого дополнительного сегмента. Способ лечения аневризмы и расслоения аорты характеризуется тем, что после установки всех сегментов системы стент-графта (ССГ) для лечения аневризмы и расслоения аорты для эндопротезировании перекрытых ССГ необходимых ветвей аорты, выполняют фенестрацию проводником биосовместимого тканного материала необходимого сегмента ССГ напротив устья соответствующей ветви аорты и удаляют направляющий катетер, после чего для каждой из ветвей заводят по проводнику в артерию на баллоне через фенестрированный биосовместимый тканный материал периферический стент-графт (СГ), за счёт раздувания баллона фиксируют периферический СГ в артерии, при этом его проксимальным концом деформируют соответствующую ячейку металлического стента необходимого сегмента ССГ и удаляют баллон и проводник.
Сущность предложенной группы изобретений отражена на чертежах.
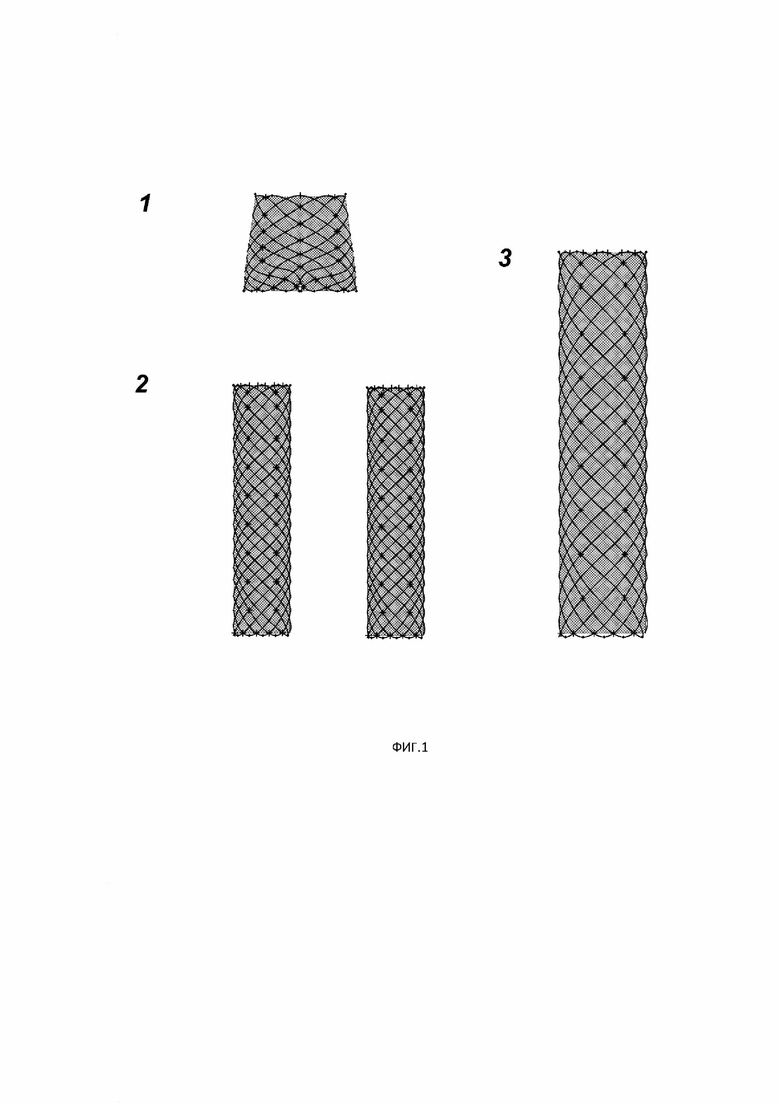
Фиг.1 - система стент-графта, где:
1- аортально-бифуркационный сегмент;
2 - два подвздошных сегмента в виде «ножек»;
3 - дополнительный сегмент для проксимальных отделов аорты (от 1 до 4х).
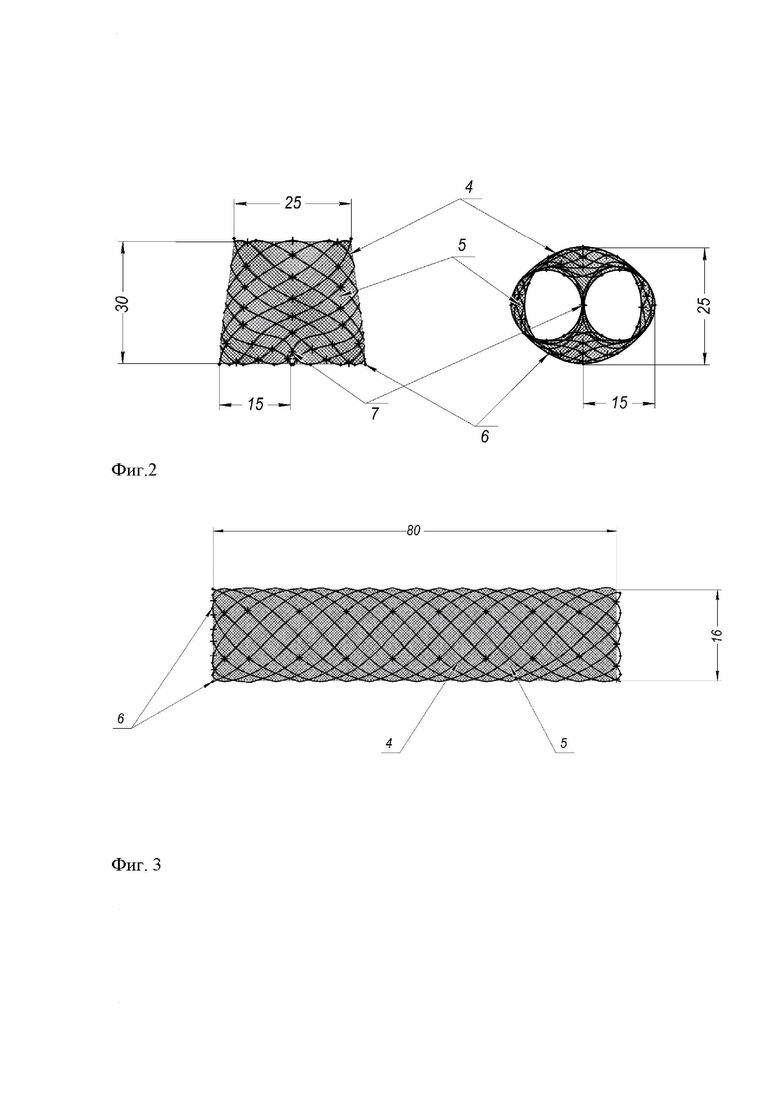
Фиг.2 - аортально-бифуркационный сегмент, где:
4 - металлический стент;
5 - биосовместимый тканный материал;
6 - рентгенконтрастные маркеры;
7 - стяжка дистального конца с формированием восьмиобразного профиля-двустволки.
Фиг.3 – подвздошный сегмент, где:
4 - металлический стент;
5 - биосовместимый тканный материал;
6- рентгенконтрастные маркеры.
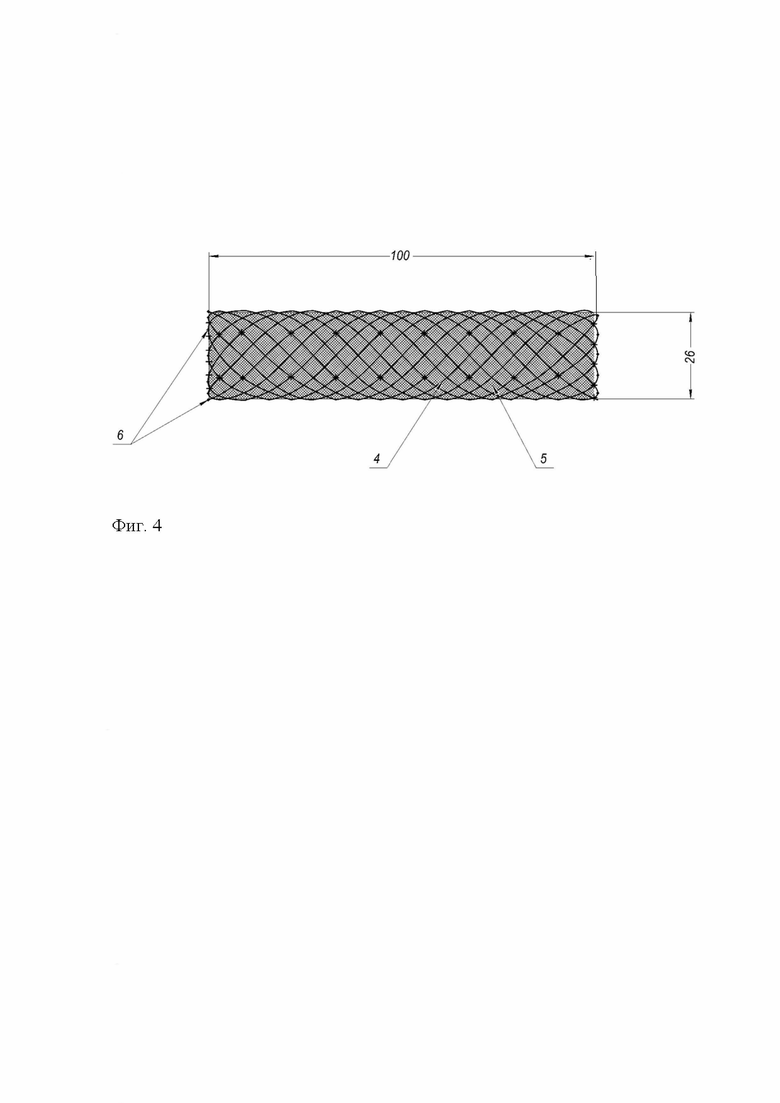
Фиг.4 - дополнительный сегмент для проксимальных отделов аорты (от 1 до 4х), где:
4 - металлический стент;
5 - биосовместимый тканный материал;
6- рентгенконтрастные маркеры
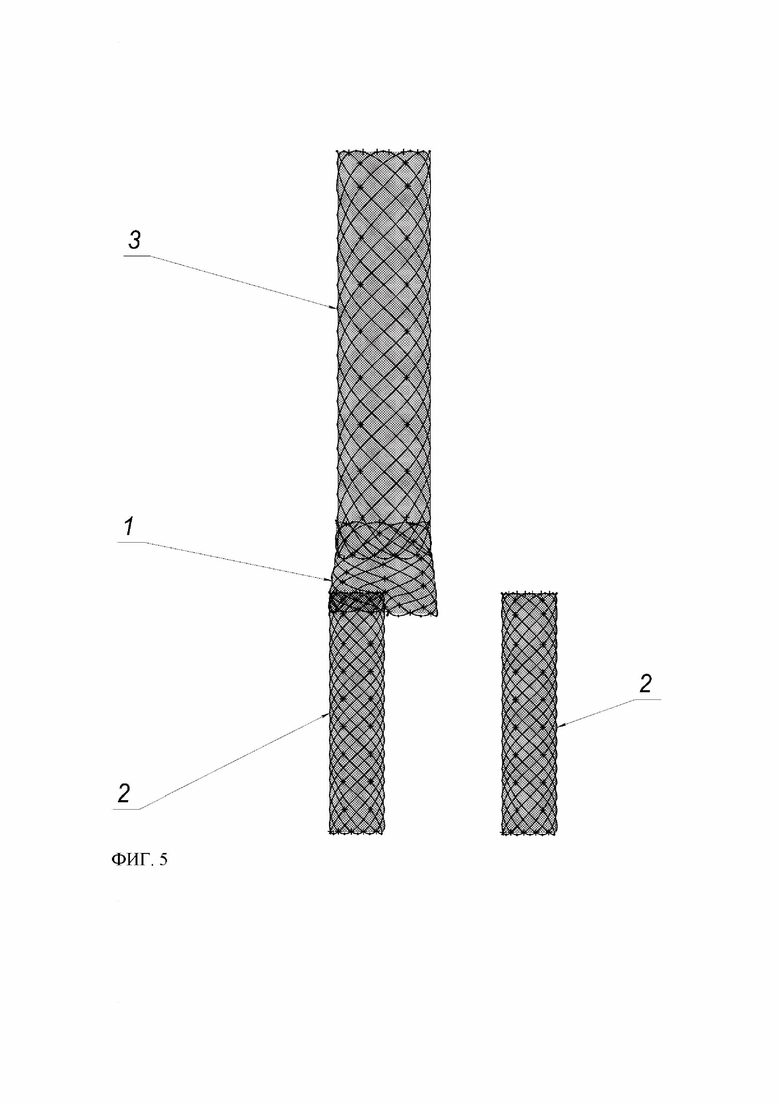
Фиг. 5 – фиксация сегментов ССГ, где:
1 - аорто-бифуркационный сегмент;
2 - подвздошный сегмент в рабочем положении и контрлатеральный подвздошный сегмент;
3 - проксимальный аортальный сегмент, установленный в рабочее положение.
Для лучшего понимания приводим описание осуществления предлагаемой группы изобретений.
Предложенная система стент-графта (ССГ) для лечения аневризм и расслоения аорты, включает в себя аортально-бифуркационный сегмент (Фиг.1(1), Фиг. (2)), два подвздошных сегмента (Фиг 1(2), Фиг. (3)) и от 1 до 4х дополнительных сегментов для проксимальных отделов аорты (Фиг. 1 (3)), Фиг.4).
Аортально-бифуркационный сегмент содержит основное трубчатое тело, выполненное из металлического стента (каркаса) (Фиг.2(4)) с возможностью расширения и прикрепленного к нему на всем его протяжении биосовместимого тканного материала (Фиг.2(5)). Биосовместимый тканный материал может быть дакроном, политетрафторэтиленом или лавсаном. Биосовместимый тканный материал может представлять собой один материал или может быть смесью, переплетением или композитом из двух или более материалов, а также может также включать другие добавки, такие как пластификаторы, модификаторы поверхности, биологические материалы, такие как пептиды и ферменты, и терапевтические агенты, такие как лекарства или другие медикаменты. Биосовместимый материал располагается внутри металлического стента и прикреплен на всем его протяжении.
Для прикрепления биосовместимого материала к металлическим стентам предпочтительно использование стандартных хирургических узловых швов нерассасывающейся хирургической нитью. Такой порядок фиксации биосовместимого тканного материала к металлическому стенту позволяет избежать отслойки парусности, что уменьшает опасность тромбообразования и минимизирует возможность возникновение эндоликов при имплантации.
Стенты (каркасы) (Фиг.2(4)) могут быть изготовлены из металла, такого как нитинол, кобальт и других биосовместимых сплавов в виде саморасширяющейся сетки с мобильными ячейками. Саморасширяющаяся сетка позволяет изменять конфигурацию сегмента (стент с прикрепленным к нему биосовместимым тканным материалом) в соответствии с диаметром аорты (изменение длины сегмента в зависимости от изменения диаметра при расширении). Наличие ячеек обеспечивает мобильность стенок стента и возможность их плотного прилегания в зоне здоровой стенки аорты, что усиливает каркасные свойства конструкции, а также препятствует распространению аневризматической деформации сосуда с последующим его расслоением. Кроме того, обеспечивает свободное прохождение инструмента для антеградной фенестрации при перекрытии гемодинамически значимых артерий (в т.ч. отходящих внеанатомично), что предупреждает образование эндоликов без создания препятствия кровотоку внутри просвета основного трубчатого тела сегмента.
Проксимальный и дистальный концы сегмента отмечены рентгенконтрастными маркерами (Фиг. 2(6)). В качестве рентгеноконтрастных маркеров может быть использован любой биосовместимый рентгеноконтрастный материал. Это обеспечивает визуализацию и облегчение позиционирования сегмента при имплантации.
Дополнительно, по сагиттальному диаметру дистального конца аортально-бифуркационного сегмента выполняется стяжка из материала (Фиг. 2(7)), аналогичного материалу металлического стента. Это обеспечивает разделение дистального конца сегмента на две равные части с формированием левого или правого отверстия дистального конца аортально-бифуркационного сегмента для последующей фиксации в сформированных просветах профиля подвздошных сегментов.
Диаметр проксимального конца при максимальном расширении составляет до 25 мм. Диаметр каждого восьмиобразного профиля-двустволки дистального конца после выполнения стяжки составляет до 15 мм при максимальном расширении. Длина аортально-бифуркационного сегмента, как сказано выше, изменяется в зависимости от расширения диаметра, и при максимальном расширении сегмента длина его составляет до 30 мм.
Предложенная система ССГ включает в себя 2 подвздошных сегмента в виде «ножек» (Фиг.3). Каждый сегмент фиксируется в просвет восьмиобразного профиля-двустволки аортально-бифуркационного сегмента для отсечения магистрального кровотока от скомпрометированных стенок подвздошных артерий (Фиг.5). Каждый подвздошный сегмент в виде «ножек» содержит трубчатое тело, выполненное из металлического стента с возможностью расширения (в виде саморасширяющейся сетки с мобильными ячейками) и прикрепленного к нему биосовместимого тканного материала, аналогично материалам, используемым в аорто-бифуркационном сегменте, на всём его протяжении. Проксимальный и дистальный концы сегментов отмечены рентгенконтрастными маркерами аналогично материалам, используемым в аорто-бифуркационном сегменте. Стенты, содержащиеся в подвздошных сегментах, могут быть выполнены из тех же материалов, что и стенты основного аортально-бифуркационного сегмента.
Диаметр каждого подвздошного сегмента при максимальном расширении составляет до 16 мм, длина изменяется в зависимости от расширения диаметра, и при максимальном расширении сегмента длина его составляет до 80 мм.
Дополнительно, ССГ включает в себя от 1 до 4х дополнительных сегментов (ДС) для проксимальных отделов аорты (Фиг.4). Каждый ДС содержит трубчатое тело, выполненное из металлического стента (Фиг.4 (4)) с возможностью расширения и прикрепленного к нему биосовместимого тканного материала (Фиг.4(5)) на всем его протяжении, причем проксимальный и дистальный концы сегмента отмечены рентгенконтрастными маркерами (Фиг.4(6)). Как отмечено ранее, все материалы, в т.ч. биосовместимый тканый материал, рентгеноконтрастные маркеры могут быть выполнены из аналогичных материалов, используемых в аортально-бифуркационном сегменте и двух подвздошных сегментах. Кроме того, стенты ДС могут быть выполнены аналогично стентам аортально-бифуркационного сегмента и двух подвздошных сегментов из аналогичных материалов. Диаметр каждого ДС составляет при максимальном расширении до 26 мм, длина изменяется в зависимости от расширения диаметра, и при максимальном расширении сегмента длина его составляет до 100 мм.
Анатомические особенности человека не позволяют подходить одинаково к каждому пациенту, так как не представляется возможным точно определить уровень отхождения крупных ветвей брюшной и грудной аорты для каждого конкретного случая. А имплантация каждого отдельного ДС напрямую зависит клинических показаний, типа и размера аневризм в брюшном и грудном отделах аорты. Именно поэтому ССГ включает в себя от 1 до 4х ДС, которые перекрывают необходимое внутреннее пространство.
Лечение аневризмы аорты с использованием вышеописанной системой стент-графта включает следующие основные этапы. Выполняют латеральный доступ на бедренных артериях с двух сторон длинной по 10 см, затем хирургическое выделение бедренных артерий с двух сторон. Пункционно вводят проводник в правую или левую бедренную артерию до дуги аорты, после чего по проводнику вводят катетер и выполняют ангиографию для определения «дорожной карты». По проводнику в аорту вводят стандартную систему доставки с расположенным внутри аортально-бифуркационным сегментом, дистальный конец его размещают на бифуркации аорты, после чего сегмент саморасширяется. Затем через ту же артерию по проводнику при помощи стандартной системы доставки вводят первый подвздошный сегмент в соответствующую доступу левую или правую подвздошную артерию, размещая при этом его проксимальный конец на 5-8 мм (Фиг.5(3)) внутри просвета соответствующего левого или правого отверстия дистального конца аортально-бифуркационного сегмента. После чего первый подвздошный сегмент саморасширяется.
Через другую бедренную артерию вводят второй подвздошный сегмент в другую соответствующую левую или правую подвздошную артерию, размещая при этом его проксимальный конец на 5-8 мм в просвете соответствующего левого или правого отверстия левого или правого отверстия дистального конца аортально-бифуркационного сегмента, после чего второй подвздошный сегмент саморасширяется. Затем по проводнику при помощи стандартной системы доставки через просвет установленного соответствующего первого или второго подвздошного сегмента и через просвет установленного аортально-бифуркационного сегмента вводят первый дополнительный сегмент для проксимальных отделов аорты перекрывая юкстаренальный и супраренальный отделы аорты. Размещают его дистальный конец на 5-8 мм внутри просвета проксимального конца аортально-бифуркационного сегмента (Фиг. 5), после чего первый дополнительный сегмент саморасширяется. При необходимости выполняют установку второго, третьего и четвёртого дополнительных сегментов для проксимальных отделов аорты аналогичным первому дополнительному сегменту способом до здорового участка аорты.
Размещение конца одного сегмента в соответствующем просвете другого сегмента на 5-8 мм (Фиг.5) с последующим расширением обеспечивает фиксацию и герметичность ССГ (всех ее сегментов между собой).
После имплантации всех необходимых сегментов ССГ, выполняют ангиографию с визуализацией устьев магистральных ветвей аорты. Затем для эндопротезирования перекрытых сегментами ССГ необходимых ветвей аорты, заводят катетер под углом и выполняют фенестрацию биосовместимого тканного материала необходимого сегмента ССГ напротив устья соответствующей ветви аорты и удаляют направляющий катетер. После чего для каждой из ветвей заводят по проводнику в артерию на баллоне через фенестрированный биосовместимый тканный материал периферический стент-графт (СГ), за счёт раздувания баллона фиксируют периферический СГ в артерии, при этом его проксимальным концом деформируют соответствующую ячейку металлического стента (каркаса) необходимого сегмента ССГ и удаляют баллон и проводник.
Таким образом, предложенная ССГ является универсальной для каждого пациента и пригодна для применения при любом типе аневризм, а также при любой ее распространённости. А за счет выполнения сегментов из металлического стента (каркаса) с возможностью расширения и прикрепленного к нему биосовместимого тканного материала из вышеперечисленных материалов, позволяет провести антеградную фенестрацию в каждом сегменте напротив устья перекрытой сегментами ССГ жизненно-важных артерий аорты без выполнения дополнительных хирургических доступов у пациента в периферические отделы вовлеченных сосудов, что существенно снижает риск возникновения интраоперационных и постоперацинонных осложнений, в т.ч. разрыва аневризмы при ее выделении.
Система стент-графта для лечения аневризм и расслоения аорты и способ лечения аневризмы и расслоения аорты с ее использованием разработаны в отделении сердечно-сосудистой хирургии ФГБУ «РНЦРХТ им. акад. А.М. Гранова».
| название | год | авторы | номер документа |
|---|---|---|---|
| Стент-графт для лечения аневризм и расслоения аорты | 2021 |
|
RU2764189C1 |
| Способ протезирования магистральных ветвей аорты | 2023 |
|
RU2814372C1 |
| СИСТЕМА БИФУРКАЦИОННОГО СТЕНТ-ГРАФТА ДЛЯ ЛЕЧЕНИЯ АНЕВРИЗМЫ БРЮШНОЙ АОРТЫ И СПОСОБ ЛЕЧЕНИЯ АНЕВРИЗМЫ БРЮШНОЙ АОРТЫ С ЕЕ ИСПОЛЬЗОВАНИЕМ | 2020 |
|
RU2742451C1 |
| СПОСОБ ЭНДОВАСКУЛЯРНОГО ВОССТАНОВЛЕНИЯ ПРОСВЕТА АОРТЫ ПРИ ДИССЕКЦИИ ТОРАКОАБДОМИНАЛЬНОГО ОТДЕЛА | 2015 |
|
RU2599346C1 |
| СПОСОБ ЭНДОВАСКУЛЯРНОЙ ПРОФИЛАКТИКИ И КОРРЕКЦИИ ЭНДОЛИКОВ I ТИПА ПРИ ЭНДОПРОТЕЗИРОВАНИИ АОРТЫ | 2020 |
|
RU2752029C1 |
| Стент-графт для шунтирования и протезирования висцеральных артерий | 2022 |
|
RU2790931C1 |
| Способ имплантации бифуркационного стент-графта в инфраренальный отдел аорты | 2019 |
|
RU2730983C1 |
| Способ дебранчинга левой почечной и верхней брыжеечной артерий при резекции торакоабдоминальной аневризмы аорты | 2023 |
|
RU2811657C1 |
| Способ определения комплекса показателей функционального состояния нисходящего грудного и брюшного отделов аорты у пациентов после гибридного оперативного лечения, включающего протезирование восходящего отдела аорты синтетическим протезом, с применением компьютерной томографии | 2024 |
|
RU2841599C1 |
| УЗЕЛ СТЕНТА ДЛЯ ЛЕЧЕНИЯ ТОРАКОАБДОМИНАЛЬНОЙ БИФУРКАЦИОННОЙ АНЕВРИЗМЫ | 2015 |
|
RU2671073C2 |
Группа изобретений относится к медицине, а именно к сердечно-сосудистой хирургии. Система стент-графта для лечения аневризм и расслоения аорты, включает аортально-бифуркационный сегмент, содержащий основное трубчатое тело, выполненное из металлического стента с возможностью расширения и прикрепленного к нему биосовместимого тканного материала, два подвздошных сегмента, содержащих трубчатое тело, выполненные из металлического стента с возможностью расширения и прикрепленного к нему биосовместимого тканного материала. Биосовместимый тканный материал прикреплен к металлическому стенту аортально-бифуркационного сегмента на всем его протяжении, причем проксимальный и дистальный концы сегмента отмечены рентгенконтрастными маркерами. Дополнительно, по сагиттальному диаметру аортально-бифуркационного сегмента выполнена стяжка дистального конца для формирования восьмиобразного профиля. Два подвздошных сегмента в виде «ножек», содержащих трубчатое тело, выполнены из металлического стента с возможностью расширения и прикрепленного к нему биосовместимого тканного материала на всем его протяжении, причем проксимальный и дистальный концы сегментов отмечены рентгенконтрастными маркерами. При этом система содержит от 1 до 4х дополнительных сегментов для проксимальных отделов аорты, каждый из которых содержит трубчатое тело, выполненное из металлического стента с возможностью расширения и прикрепленного к нему биосовместимого тканного материала на всем его протяжении, причем проксимальный и дистальный концы сегмента отмечены рентгенконтрастными маркерами. Способ реализует посредством имплантации заявленного устройства. Заявленная группа изобретений позволяет провести антеградную фенестрацию в каждом сегменте напротив устья перекрытой сегментами системы стент-графта жизненно-важных артерий аорты без выполнения дополнительных хирургических доступов у пациента в периферические отделы вовлеченных сосудов, что существенно снижает риск возникновения интраоперационных и постоперацинонных осложнений, в т.ч. разрыва аневризмы при ее выделении. 2 н. и 1 з.п. ф-лы, 5 ил.
1. Система бифуркационного стент-графта для лечения аневризм и расслоения аорты, включающая аортально-бифуркационный сегмент, содержащий основное трубчатое тело, выполненное из металлического стента с возможностью расширения и прикрепленного к нему биосовместимого тканного материала, два подвздошных сегмента, содержащих трубчатое тело, выполненные из металлического стента с возможностью расширения и прикрепленного к нему биосовместимого тканного материала; отличающаяся тем, что биосовместимый тканный материал прикреплен к металлическому стенту аортально-бифуркационного сегмента на всем его протяжении, причем проксимальный и дистальный концы сегмента отмечены рентгенконтрастными маркерами, и, дополнительно, по сагиттальному диаметру аортально-бифуркационного сегмента выполнена стяжка дистального конца для формирования левого и правого отверстий дистального конца сегмента, два подвздошных сегмента в виде «ножек», содержащих трубчатое тело, выполнены из металлического стента с возможностью расширения и прикрепленного к нему биосовместимого тканного материала на всём его протяжении, причем проксимальный и дистальный концы сегментов отмечены рентгенконтрастными маркерами, при этом система содержит от 1 до 4-х дополнительных сегментов для проксимальных отделов аорты, каждый из которых содержит трубчатое тело, выполненное из металлического стента с возможностью расширения и прикрепленного к нему биосовместимого тканного материала на всем его протяжении, причем проксимальный и дистальный концы сегмента отмечены рентгенконтрастными маркерами.
2. Способ лечения аневризмы и расслоения аорты с использованием системы стент-графта по п.1, включающий этапы, на которых вводят аортально-бифуркационный сегмент в брюшную аорту, вводят первый подвздошный сегмент в левую или правую подвздошную артерию, вводят второй подвздошный сегмент в другую левую или правую подвздошную артерию и вводят дополнительный сегмент, отличающийся тем, что при введении аотально-бифуркационного сегмента в брюшную аорту, дистальный конец его размещают на бифуркации аорты, после чего сегмент саморасширяется, затем вводят первый подвздошный сегмент в левую или правую подвздошную артерию, размещая при этом его проксимальный конец на 5-8 мм внутри просвета соответствующего левого или правого отверстия дистального конца аортально-бифуркационного сегмента, после чего первый подвздошный сегмент саморасширяется, затем вводят второй подвздошный сегмент в другую левую или правую подвздошную артерию, размещая при этом его проксимальный конец на 5-8 мм внутри просвета соответствующего левого или правого отверстия дистального конца аортально-бифуркационного сегмента, после чего второй подвздошный сегмент саморасширяется, затем через просвет установленного первого или второго подвздошного сегмента и через просвет установленного аортально-бифуркационного сегмента на проводнике вводят первый дополнительный сегмент для проксимальных отделов аорты, размещая его дистальный конец на 5-8 мм в просвете проксимального конца аортально-бифуркационного сегмента, после чего первый дополнительный сегмент саморасширяется, а установку второго, третьего и четвёртого дополнительных сегментов для проксимальных отделов аорты осуществляют способом аналогичным установке первого дополнительного сегмента.
3. Способ лечения аневризмы и расслоения аорты по п.2, характеризующийся тем, что после установки всех сегментов системы стент-графта (ССГ) для лечения аневризмы и расслоения аорты для эндопротезировании перекрытых ССГ необходимых ветвей аорты, выполняют фенестрацию проводником биосовместимого тканного материала необходимого сегмента ССГ напротив устья соответствующей ветви аорты и удаляют направляющий катетер, после чего для каждой из ветвей заводят по проводнику в артерию на баллоне через фенестрированный биосовместимый тканный материал периферический стент-графт (СГ), за счёт раздувания баллона фиксируют периферический СГ в артерии, при этом его проксимальным концом деформируют соответствующую ячейку металлического стента необходимого сегмента ССГ и удаляют баллон и проводник.
| СИСТЕМА БИФУРКАЦИОННОГО СТЕНТ-ГРАФТА ДЛЯ ЛЕЧЕНИЯ АНЕВРИЗМЫ БРЮШНОЙ АОРТЫ И СПОСОБ ЛЕЧЕНИЯ АНЕВРИЗМЫ БРЮШНОЙ АОРТЫ С ЕЕ ИСПОЛЬЗОВАНИЕМ | 2020 |
|
RU2742451C1 |
| КОМБИНИРОВАННЫЙ ГИБРИДНЫЙ ПРОТЕЗ С БЕСШОВНЫМИ СОЕДИНЕНИЯМИ ДЛЯ ПРОТЕЗИРОВАНИЯ ГРУДНОЙ АОРТЫ И ЕЕ ВЕТВЕЙ (ВАРИАНТЫ) И СПОСОБ ЕГО ИМПЛАНТАЦИИ (ВАРИАНТЫ) | 2020 |
|
RU2754769C1 |
| УСТРОЙСТВО ДЛЯ СТЕНТИРОВАНИЯ И НАБОР ДЛЯ СТЕНТИРОВАНИЯ АОРТЫ | 2016 |
|
RU2721137C2 |
| СПОСОБ ЗАЩИТБ1 ОТ АТМОСФЕРНОЙ КОРРОЗИИ ИЗДЕЛИЙ ИЗ ЧУГУНА И УГЛЕРОДИСТОЙ СТАЛИ | 0 |
|
SU165631A1 |
| Кудринский А | |||
| В | |||
| Результаты эндоваскулярного протезирования при расслоении аорты III типа, автореферат, М., 2020, 23 с | |||
| Iannelli G., Tommaso L., Cirillo P | |||
| et al | |||
| Treatment of residual type A aortic dissection with implantation of the | |||
Авторы
Даты
2022-01-18—Публикация
2021-03-16—Подача