Изобретение относится к медицине, хирургии, паразитологии и позволяет улучшить непосредственные и отдаленные показатели лечения больных с паразитарным поражением печени, а в особенности больных с кистозным эхинококкозом.
Эхинококкоз является одним из самых распространенных паразитарных заболеваний в мире и Российской Федерации [1]. На его долю приходится более 1% от всех биогельминтозов. В последние голы отмечается рост заболеваемости эхинококкозом в Российской Федерации и мире за последние 25 лет более чем в три раза (с 0,1 в 1990 г до 0,35 на 100 тыс. населения в 2015 г) [2].
«Золотым» стандартом лечения эхинококкоза печения принято считать хирургический способ. За долгие годы у хирургов накоплен огромный арсенад различных методов лечения. Хирургические опции на сегодняшний день включают в себя: перицистэктомию, частичную гепатэктомию или лобэктомию, открытую цистэктомию (с или без оментопластики) или дренирование кист [3]. «Открытая» эхинококкэктомия в течение десятилетий занимала свое ведущее место в лечении больных кистозным эхинококкозом печени, однако неуклонный рост количества осложнений, в том числе билиарных фистул, а также неудовлетворительные результаты в плане рецидивов побудили хирургов искать более совершенные методы лечения [4].
Существующие варианты лапаротомных перицистэктомий и резекций печени при высокой эффективности сопряжены с риском тяжелых послеоперационных осложнений [5].
Прямых прототипов предлагаемому нами способу лечения на сегодняшний день нет, однако одним из наиболее современных вариантов миниинвазивного лечения эхинококковых кист печени является PAIR (чрескожная пункция, аспирация, инъекция и реаспирация) - это менее инвазивный подход в лечении эхинококковых кист печени, выполняющий под контролем У3-исследования [6]. Однако, PAIR применим не для всех типов кист. Предварительное определение количества, стадии развития, наличия дочерних кист имеет решающее значение для успешного лечения с помощью данной методики. Показаниями к PAIR являются кисты по классификации ВОЗ СЕ1 и СЕ3а (однокомпонентные кисты) <5 см, которые плохо реагируют на медикаментозную терапию, и в сочетании с медикаментозной терапией для кист >5 см. Противопоказания для проведения PAIR включают отсутствие чрескожного доступа к кисте, поверхностные субкапсулярные кисты из-за высокого риска разрыва, наличие цистобилиарных свищей, неактивные кисты, и сложные мультисептальные кисты.
Процедура PAIR включает пункцию кисты, аспирацию, инъекцию сколицидного средства и повторную аспирацию содержимого. Жидкость, которая первоначально аспирируется, оценивается на наличие жизнеспособных протосколексов, что подтверждает диагноз эхинококкоза. Также оценивается наличие цисто-билиарного свища путем тестирования на наличие билирубина в жидкости, который также может быть определен перед PAIR с помощью МР-холангиографии. Вводимый гермицид оставляют примерно на 15 минут, после чего происходит отделение зародышевой мембраны от окружающей кисты. В настоящее время наиболее часто используются три раствора: 70-95% этанол, 15-20% гипертонический физиологический раствор или раствор цетримида. Процедура также включает в себя тщательное наблюдение за пациентом с целью предотвращения развития осложнений по типу анафилаксии. Лечение альбендазолом или мебендазолом за четыре часа до процедуры следует продолжать в течение одного месяца после операции (альбендазол)либо в течение трех месяцев (мебендазол). Такое предварительное и последующее лечение снижает риск рецидива и вторичного внутрибрюшинного отсева. После процедуры PAIR выполняются несколько контрольных УЗИ гепатопанкреатобилиарной области. Хороший ответ определяется присутствием следующих факторов: уменьшение размеров полости, увеличение степени кальцификации стенки, уменьшение жидкостного компонента кисты и повышение эхогенности кисты (что согласуется с появлением псевдомассы). В мета-анализе,в котором сравнивались результаты лечения 769 пациентов, перенесших PAIR в сочетании с терапией мебендазолом или альбендазолом, и 952 пациентов, основным методом лечения которых было хирургическое вмешательство, лучшие результаты наблюдались в группе пациентов, перенесших PAIR в сочетании с медикаментозной терапией. В данной группе отмечены более низкие показатели осложнений, значительно меньшее количество дней госпитализации (2,4 дня против 15 дней) и более низкие показатели рецидива заболевания. Группа больных, перенесших хирургическое лечение, отличалась более высокими показателями осложнений. Несмотря на полученные при данном мета-анализе результаты, следует помнить о том, что PAIR имеет довольно узкие показания к использованию и не применим к большей части кист, при которых проводится хирургическое лечение.
Таким образом, неудовлетворительные результаты лечения пациентов с кистозным эхинококкозом печени, обуславливают поиск новых вариантов лечения. Мы считаем, что вышеуказанные варианты лечения паразитарных кисты при своей достаточной радикальности не отвечают тенденциям малоинвазивности и органосбережения. Вариант радиочастотной аблации эхинококковых кист печени позволяет достигать лучших непосредственных и отдаленных хирургических показателей.
Задачей, на решение которой направлено заявляемое изобретение, является расширение возможностей хирургического способа лечения, путем сохранения анатомической целостности органа, использования современного малоинвазивного вмешательства.
Предлагаемый способ лечения. Для улучшения результатов лечения пациентов с эхинококкозом печени в хирургической клинике Боткинской Больницы был разработан и внедрен следующий протокол вмешательства.
Процедура проводилась под общей анестезией в условиях операционной. Положение пациента на операционном столе определялось локализацией кисты и наличием ультразвукового окна для безопасной траектории пункционной иглы и в последующем антенны. Процедура проводилась аппаратом СВЧ CovidienEvident MWA AblationSystem с набором антенн Covidien. Аппарат состоит из генератора мощностью 60 Вт (45 Вт на антенне) с частотой колебаний до 915 МГц, перистальтического насоса, подающего по замкнутому контуру охлажденную воду (хладогентом служит заранее приготовленный замороженный физиологический раствор) и антенны для СВЧ-аблации. Нами использовались одиночные антенны.
Пункция очага производилась под ультразвуковым контролем (аппарат Logic9, GE, конвексный датчик 3,5 МГц с пункционным адаптером). Параллельно в кисту устанавливался дренаж Resolve (MeritMedical) диаметром 12-14 Fr для частичной эвакуации жидкой части эхинококковой кисты и антенна СВЧ. Затем осуществлялся контроль положения антенны для прецизионного позиционирования в центре эхинококковой кисты. Затем включалась подача жидкости перистальтическим насосом и начиналась работа генератора. При этом проводились ультразвуковой контроль формирования зоны аблации и наблюдение за окружающими анатомическими структурами. После того, как гиперэхогенная зона полностью охватывала очаг, генератор отключали. Время воздействия составляло 11 минут. После отключения генератора прекращалась подача охлаждающей жидкости и измерялась температура, достигнутая в центре очага. При нормальной работе генератора она составляла более 100°С. Электрод извлекался из паренхимы печени при работающем в ручном режиме на максимальной мощности генераторе. Таким образом достигалась термообработка пункционного канала, что препятствовало кровотечению и паразитарной диссеминации.
После процедуры больного переводили в палату, через 4 часа после операции проводился лабораторный контроль. В течение нескольких суток проводилась консервативная терапия, включая антибиотикопрофилактику. В течение первых суток выполняли УЗИ и МСКТ/МРТ для определения адекватности СВЧ и выявления возможных осложнений вмешательства.
Для подтверждения эффективности предлагаемого способа лечения предлагается анализ результатов его применения.
Пациентам с эхинококкозом печени с 2019 года начали применяться методики физического воздействия на паразитарные кисты. Были оценены следующие показатели: длительность операции, объем кровопотери, послеоперационные осложнения по Clavien-Dindo, послеоперационные осложнения по ISGLS, послеоперационный койко-день, рецидив в течение первого года после хирургического вмешательства.
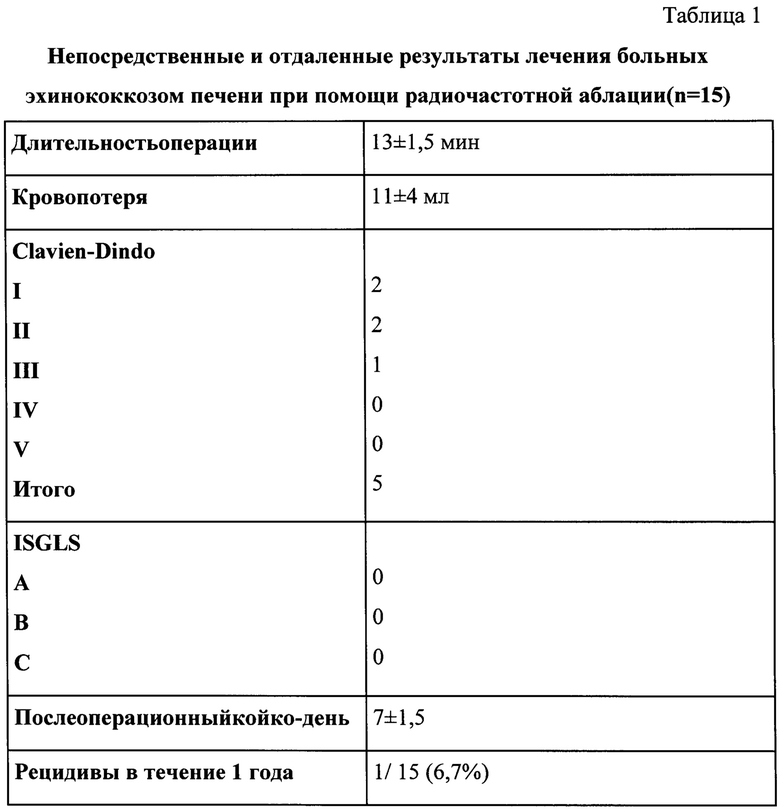
Таким образом, предлагаемый современный способ лечения больных эхинококкозом печени позволяет достигать удовлетворительных непосредственных и отдаленных результатов.
Список литературы.
1. Мусаев Г.Х., Фатьянова А.С., Левкин В.В. Принципы и современные тенденции лечения эхинококкоза печени. Хирургия. Журнал им. Н.И. Пирогова. 2017;(12):90-94. https://doi.org/l0.17116/hirurgia20171290-94
2. Шабунин А.В. Роль перицистэктомии в лечении больных эхинококкозом печени / А.В. Шабунин, М.М. Тавобилов, А.А. Карпов, П.А. Дроздов, С.С. Лебедев, Д.С. Озерова, О.С.Журавель // Вестник хирургической гастроэнтерологии. - 2019. - №. 1. - С. 35-40.
3. Tuxun Т. World review of laparoscopic treatment of liver cystic echinococcosis-914 patients/ T. Tuxun, J.H. Zhang, J.M. Zhao, Q.W. Tai, M. Abudurexti, H.Z. Ma, H. Wen // International Journal of Infectious Diseases. -2014. - T. 24. - C. 43-50. doi: 10.1016/j.ijid.2014.01.012
4. Greco S. Complications of hepatic echinococcosis: multimodality imaging approach/ S. Greco, R. Cannella, D. Giambelluca, G. Pecoraro, E. Battaglia, M. Midiri, F. Vernuccio // Insights into Imaging. - 2019. - T. 10. - №. 1. - C. 113. doi: 10.1186/s13244-019-0805-8.
5. Castillo S. et al. Infected Hepatic Echinococcosis. Clinical, Therapeutic, and Prognostic Aspects. A Systematic Review / S. Castillo, C. Manterola, L. Grande, C. Rojas // Annals of Hepatology. - 2020. - T. 21. - C. 30142-3 PMID: 32835861 doi: 10.1016/j.aohep.2020.07.009
6. Naar L.Management of Cystic Echinococcosis Complications and Dissemination L. Naar, L. Hatzaras, N. Arkadopoulos // The Surgical Management of Parasitic Diseases. - Springer, Cham, 2020. - C. 209-228.DOI: 10.1007/s00268-009-9982-9
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ радиочастной аблации эхинококковых кист печени | 2021 |
|
RU2767275C1 |
| СПОСОБ ПЕРСОНИФИЦИРОВАННОГО ПОДБОРА ПРОТИВОПАРАЗИТАРНОЙ ТЕРАПИИ У БОЛЬНЫХ ЭХИНОКОККОЗОМ ПЕЧЕНИ | 2023 |
|
RU2810944C1 |
| Способ органосберегающей резекции селезенки | 2024 |
|
RU2831985C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ЭХИНОКОККОЗА ПЕЧЕНИ | 2008 |
|
RU2355436C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ МНОГОКАМЕРНОГО ЭХИНОКОККОЗА ПЕЧЕНИ | 2011 |
|
RU2478345C1 |
| СПОСОБ ТРЕХЭТАПНОГО МИНИ-ИНВАЗИВНОГО ЛЕЧЕНИЯ ОСЛОЖНЕНИЙ ЦИРРОЗА ПЕЧЕНИ | 2023 |
|
RU2816786C1 |
| СПОСОБ РЕГЕНЕРАТИВНОЙ КЛЕТОЧНОЙ ТЕРАПИИ ДЛЯ ЛЕЧЕНИЯ ГЕПАТОЦЕЛЛЮЛЯРНОЙ НЕДОСТАТОЧНОСТИ ПРИ ЦИРРОЗЕ ПЕЧЕНИ | 2023 |
|
RU2822653C1 |
| СПОСОБ ОБРАБОТКИ ПУНКЦИОННО-ДРЕНАЖНОГО КАНАЛА У БОЛЬНЫХ С ПАРАЗИТАРНЫМ ПОРАЖЕНИЕМ ПЕЧЕНИ ПОСЛЕ ДРЕНИРОВАНИЯ ПОЛОСТИ РАСПАДА | 2023 |
|
RU2811279C1 |
| Способ комплексного лечения осложнений цирроза печени через один хирургический доступ | 2024 |
|
RU2838304C1 |
| СПОСОБ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ЭХИНОКОККОЗА ПЕЧЕНИ | 2001 |
|
RU2195192C1 |
Изобретение относится к медицине, хирургии, паразитологии. Процедура проводилась под общей анестезией в условиях операционной. Положение пациента на операционном столе определялось локализацией кисты и наличием ультразвукового окна для безопасной траектории пункционной иглы и в последующем антенны. Процедура проводится аппаратом для сверхвысокочастотной аблации с набором антенн. Аппарат состоит из генератора мощностью 60 Вт с частотой колебаний до 915 МГц, перистальтического насоса, подающего по замкнутому контуру охлажденную воду и антенны для СВЧ-аблации. Для проведения процедуры используют одиночные антенны. Пункция очага производится под ультразвуковым контролем. Параллельно в кисту устанавливался дренаж для частичной эвакуации жидкой части эхинококковой кисты и антенна СВЧ. Затем осуществляется контроль положения антенны для прецизионного позиционирования в центре эхинококковой кисты. Затем включалась подача жидкости перистальтическим насосом и начиналась работа генератора. При этом проводились ультразвуковой контроль формирования зоны аблации и наблюдение за окружающими анатомическими структурами. Способ позволяет улучшить непосредственные и отдаленные показатели лечения больных с паразитарным поражением печени, больных с кистозным эхинококкозом. 1 з.п. ф-лы, 1 табл.
1. Способ лечения эхинококкоза печени, заключающийся в том, что производят одномоментную пункцию и дренирование эхинококковой кисты и введение антенны для СВЧ-аблации с последующей сверхвысокочастотной аблацией эхинококковой кисты в течение 11 минут при мощности 60 Вт и частотой колебаний 915 МГц.
2. Способ по п. 1, отличающийся тем, что в аблируемой полости оставляют страховой дренаж.
| СПОСОБ ЛЕЧЕНИЯ ПАЦИЕНТОВ С МЕТАСТАТИЧЕСКИМ РАКОМ ПЕЧЕНИ | 2013 |
|
RU2554794C1 |
| СПОСОБ ЛЕЧЕНИЯ ЭХИНОКОККОВОЙ КИСТЫ ПЕЧЕНИ ТИПА СЕ2В, СЕ3В | 2018 |
|
RU2695007C1 |
| Способ бескровной резекции селезенки | 2018 |
|
RU2675355C1 |
| ЗАГАЙНОВ В | |||
| Е | |||
| и др | |||
| Экспериментальное обоснование нового метода термического разрушения опухолей паренхиматозных органов местным воздействием энергии сверхвысоких частот //Медицинский альманах | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| N | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
| ЗАГАЙНОВ В | |||
| Е | |||
| и др | |||
| Новый метод микроволновой термоаблации | |||
Авторы
Даты
2022-03-17—Публикация
2021-05-19—Подача