Изобретение относится к медицине, а именно к инфекционным болезням и болезням кровообращения взрослого населения, может быть использовано в качестве объективного прогностического критерия риска развития сердечно-сосудистых осложнений и, следовательно, связанной с этим степени тяжести течения заболевания у пациентов с COVID-19, находящихся на амбулаторном или стационарном лечении. Способ может быть применен также у пациентов, перенесших заболевание и находящихся на этапе выздоровления с целью оценки эффективности проведенной терапии и необходимости продолжения лечения или коррекции схемы лечения.
Несмотря на широкий охват населения вакцинопрофилактикой против COVID-19, проблема распространения SARS-CoV-2 не теряет своей актуальности [1]. С февраля 2020 года по настоящее время в мире непрерывно растет число заболевших и умерших. Наиболее высокая заболеваемость с максимальным числом летальных исходов зарегистрирована в Индии и США. В России общая заболеваемость коронавирусной инфекцией, вызванной SARS-CoV-2, также остается на высоком уровне [2].
В настоящее время регистрируется большое число тяжелых форм COVID-19 за счет взрослого населения с затяжным течением, часто регистрируются сердечно-сосудистые осложнения, что является одной из особенностей новой коронавирусной инфекции. В связи с этим высоко актуальна проблема прогноза течения заболевания и возможности определения степени сердечно-сосудистого риска у больных на раннем этапе с целью своевременного предупреждения неблагоприятных исходов [3]. Практикующему врачу амбулаторного и стационарного звена важно выделить группу пациентов, которым необходимо более быстрое дополнительное обследование и назначение активной профилактической терапии.
На сегодняшний день известно, что SARS-CoV-2 проникает в клетку посредством взаимодействия с рецепторами ангиотензинпревращающего фермента 2 типа (АПФ-2). Вместе с тем рецепторы к АПФ-2 представлены в большинстве органов и систем организма, особенно - в сосудистом русле, что позволяет вирусу наносить системное повреждение. Существенной прогрессии эндотелиальной дисфункции способствует активация воспаления, приводящая к повышению активности рецепторов АПФ-2 на поверхности эндотелия, что в свою очередь приводит к выбросу эндотелина-1 - основной вазоконстрикторной субстанции. За счет выраженной вазоконстрикции нарушается тканевая перфузия, что ведет к фокальным некрозам с повреждением интимы сосудов и гиперкоагуляции. Это стимулирует усиление выброса провоспалительных цитокинов. Таким образом, неконтролируемая продукция эндотелина-1 приводит к прогрессированию системного воспаления и тромбообразованию, высокие значения его могут быть маркером неблагоприятного прогноза, а снижение может коррелировать с положительной динамикой.
В настоящее время отсутствуют достоверные показатели, характеризующие степень поражения сосудов при COVID-19. Широко используемое определение уровня Д-димера как маркера тромбообразования не может применяться на практике для своевременного прогнозирования исхода и пересмотра тактики терапии, поскольку представляет собой продукт разрушения уже образовавшегося тромба и характеризует поздние процессы, происходящие в сосудах у пациентов с коронавирусной инфекцией [4-7].
Наиболее близким аналогом заявленного изобретения можно считать «Способ оценки эффективности сосудистой терапии по выраженности эндотелиальной дисфункции» (патент RU №2455641, автор - Инжутова А.И.) [8]. Согласно предложенной методике, для определения степени дисфункции эндотелия определяется количество эндотелиоцитов, меченных аннексином-V. Недостаток этого способа заключается в его трудоемкости. Кроме этого, он ориентирован на пациентов с соматической патологией.
Также близким аналогом является «Способ определения риска развития сердечно-сосудистых осложнений у женщин с гипертонической болезнью (патент RU №2530621 авторов Радаевой О.А. и Новиковой Л.В.), согласно которому риск развития сердечно-сосудистых осложнений оценивается на основании уровней интерлейкина-1, интерлейкина-1α, фактора ингибирования лейкозных клеток и количества CD34 [9]. Основными недостатками способа является необходимость определения 4 показателей и применимость только для случаев с эссенциальной артериальной гипертензией.
Из патентной литературы известно определение состояния сосудистой стенки у больных артериальной гипертензией с помощью математической модели на основании результатов определения в сыворотке крови общего холестерина, липопротеинов высокой плотности, эндотелина-1, гомоцистеина и С-реактивного белка реализовано в «Способе определения диагностического показателя жесткости сосудистой стенки у больных артериальной гипертонией с абдоминальным ожирением (патент RU №2567606 авторов Петелиной Т.И., Гапон Л.И., Авдеевой К.С., Мусихиной Н.А. и Дьячкова С.М.) [10]. Как и по предыдущим способам, недостатком его является трудоемкость и ограниченность применения для пациентов с соматической патологией.
Похожий результат может быть достигнут и другими методами. Известен «Способ выявления дисфункции эндотелия коронарных артерий» (патент RU №2199266, авторов Парнес Е.Я., Парнес М.Е., Парнес М.Е., Красносельского М.Я.). Согласно этому методу, заключение о наличии или отсутствии дисфункции эндотелия коронарных артерий дается на основании результатов анализа мощности спектральных составляющих вариабельности ритма сердца на зарегистрированной ритмокардиограмме [11]. Недостатком данного способа является, в первую очередь, оценка только определенного участка сосудистого русла - коронарных артерий, а также возможность влияния на вариабельность ритма электролитных, биохимических и наследственных нарушений.
Еще одним близким к рассматриваемым изобретениям является «Способ прогнозирования варианта артериальной гипертонии у пациентов пожилого и старческого возраста» (патент RU №2266702 авторов Кательницкой Л.И., Хаишева Л.А., Иванченко Д.Н., Джагессар Р.К., Кициева А.А., Лужецкой И.В.). Согласно этому методу у пациентов группы риска пожилого и старческого возраста определяют величину эндотелий-зависимой вазодилатации - ЭЗВД, как разность диаметров плечевой артерии при реактивной гиперемии и в покое, соотнесенной к ее диаметру в покое, и эндотелий-независимой вазодилатации - ЭНВД, рассчитанную аналогичным образом на фоне приема нитроглицерина. Кроме того, определяют уровень эндотелина-1 и по всем указанным величинам прогнозируют развитие систолодиастолической или изолированной артериальной гипертонии [12]. Недостатком данного способа является то, что прогнозирование артериальной гипертонии связано с приемом нитроглицерина, который может проявлять нежелательные действия: в первую очередь, существенно снижать артериальное давление с вероятностью развития обморочного состояния. Кроме того, оценка может быть проведена только в указанной возрастной категории.
Еще одним близким к представленному нами изобретению является результат работы Сенчихина В.Н. и Лямина С.В. «Вазомоторная и секреторная функции эндотелия у больных артериальной гипертонией молодого возраста» (Материалы конгресса «Перспективы Российской кардиологии», Москва, 2005). Авторы для оценки вазомоторной и секреторной функции эндотелия определяли уровень оксида азота, концентрацию эндотелина-1, величину эндотелий-зависимой вазодилатации. В данной работе указано, что у здоровых лиц молодого возраста уровень продукции оксида азота составляет 19,1±4,5 мкмоль/дл, содержание эндотелина-1 в плазме крови - 8,8 фмоль/мл [13]. Однако этот способ ориентирован на применение у лиц с определенной патологией - артериальной гипертензией, а не при инфекционной патологии.
Таким образом, ни один из имеющихся способов не ориентирован на оценку состояния сосудов у пациентов с COVID-19.
Технической проблемой, на решение которой направлено предлагаемое изобретение, является разработка способа определения степени риска развития сердечнососудистых осложнений у пациентов с COVID-19, широко используемого в повседневной клинической практике первичного звена и в условиях стационарного лечения.
Указанная проблема решается путем определения уровня эндотелина-1 в сыворотке крови у заболевших COVID-19, в том числе, в раннем периоде, и в периоде реконвалесценции с последующей оценкой полученных результатов для установления степени риска развития сердечно-сосудистых осложнений.
Предлагаемый метод основан на том, что у пациентов при COVID-19 за счет особенностей действия вируса отмечается поражение сосудов с повреждением сосудистой стенки и выходом в кровоток эндотелина-1. При этом степень поражения сосудов может зависеть от количества рецепторов, с которыми взаимодействует вирус. Эндотелин-1 вызывает вазоконстрикцию с последующим тромбообразованием и усилением воспалительной реакции, что отражается на функции сердечной мышцы и других органов. Эти проявления напрямую зависят от количества высвобожденного эндотелина-1. Выброс этого вещества происходит на самых ранних этапах повреждения эндотелия, когда другие маркеры (МВ-креатинкиназа, трансаминазы, натрий-уретический пептид, Д-димер) еще остаются не задействованы. Таким образом, определение уровня эндотелина-1 имеет важное значение для определения прогноза сердечно-сосудистого риска в различные периоды COVID-19. Очевидно, что этот показатель может повышаться в ответ и на повреждение сосудистой стенки другой этиологии, что может быть изучено в последующим и не противоречит поставленной технической задаче.
Сущность изобретения заключается в том, что при осуществлении предлагаемого способа проводится лабораторное определение концентрации эндотелина-1 иммуноферментным способом в сыворотке крови заболевших COVID-19 с последующей оценкой степени риска развития сердечно-сосудистых осложнений в зависимости от полученных значений.
Преимуществами предлагаемого способа являются возможность быстрой оценки степени риска сердечно-сосудистых осложнений на ранних стадиях поражения сосудов, объективность и точность результата, возможность определения уровня эндотелина-1 известным методом иммуноферментного анализа при наличии набора реагентов, как в амбулаторных условиях, так и на стационарном этапе.
Техническим результатом способа является установление степеней риска развития сердечно-сосудистых осложнений: низкой, средней, высокой, очень высокой, независимо от наличия или отсутствия хронической соматической патологии системы кровообращения в анамнезе. Способ позволяет существенно снизить неблагоприятные исходы заболевания, как на этапе первичного звена, так и на стационарном этапе за счет своевременной коррекции схемы терапии. Кроме того, своевременный прогноз сердечно-сосудистого риска позволит снизить количество госпитализаций, оптимизировать работу первичного звена. Оценка степени сердечно-сосудистого риска позволяет выделять группу пациентов, нуждающихся в срочной госпитализации (при высоком и очень высоком риске) и активной терапии; группу лиц, нуждающихся в дополнительном обследовании, но с возможным амбулаторным наблюдением и лечением (при средней степени риска), а также группу с низким сердечно-сосудистым риском, в которой необходим минимальный объем контроля и терапии.
Способ определения эндотелина-1 в сыворотке крови:
1-й этап. У пациента, больного COVID-19 натощак берется венозная кровь в объеме не менее 1 мл в пробирку для серологических исследований.
2-й этап. Взятая цельная кровь центрифугируется в стандартном режиме, сыворотка с помощью пипетки перемещается в пробирку для аликвотирования.
3-й этап. С помощью набора реагентов для определения эндотелина-1 количественным методом и анализатора иммуноферментным способом проводится определения концентрации эндотелина-1. При невозможности определения в течение суток после взятия биоматериала сыворотка крови может быть заморожена при температуре -20°С.
После получения результата определяется соответствие установленного значения степени риска:
- менее 0,16 пмоль/л - низкий риск;
- от 0,16 до 0,5 пмоль/л - средний риск;
- от 0,5 до 2,0 пмоль/л - высокий риск;
- более 2,0 пмоль/л - очень высокий риск развития сердечно-сосудистых осложнений.
Степени риска были установлены путем сопоставления полученных значений эндотелина-1 в сыворотке крови пациентов и результатов последующего наблюдения (жалоб, общего состояния, данных ЭКГ, результатов биохимического исследования с дополнительным анализом на уровни Д-димера и кардиоспецифичных маркеров в динамике, МРТ головного мозга) с оценкой развившихся осложнений и исходов.
Изобретение поясняется следующими материалами.
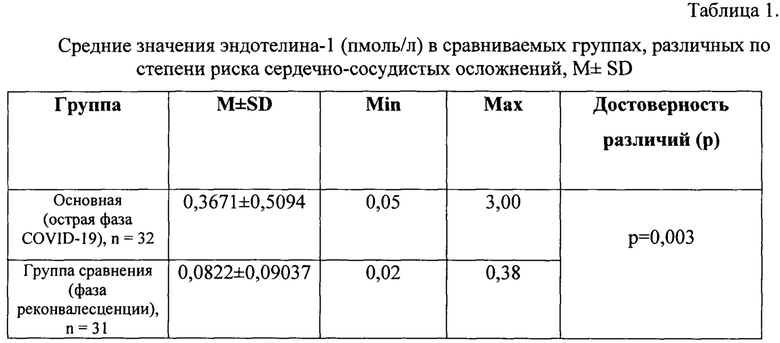
В таблице 1 представлены лабораторные данные исследования 63 пациентов, где основную группу составили 32 пациента в острой фазе COVID-19, до начала терапии, а 31 пациент - с выздоровлением или наличием минимальных изменений, не ограничивающих повседневную привычную активность (0 или 1 балл по шкале клинического улучшения ВОЗ). после проведенного курса терапии, на 28-е сутки от момента начала комплексного (противовирусного, противосвертывающего и другого, при необходимости) лечения. Дополнительно проведена оценка наиболее распространенных кардиоспецифичных маркеров повреждения сердечно-сосудистой системы, применяемых традиционно в рутинной клинической практике, оценена их значимость по сравнению с энотелином-1 в сравниваемых группах. Пациенты обеих групп сопоставимы по возрасту, тендерному составу и сопутствующей патологии. Верификация диагноза COVID-19 проведена методом полимеразной цепной реакции (ПЦР, тест-система «Амплисенс», РФ). Все пациенты дали информированное согласие на участие в исследовании и использование обезличенных данных их медицинской документации в научных целях и в публикациях. Исследование было одобрено локальным этическим комитетом. Критерии включения в исследование: мужчины и женщины в возрасте от 18 до 85 лет, лабораторно подтвержденный диагноз коронавирусной инфекции, вызванной вирусом SARS-CoV-2.
К критериям невключения отнесли состояния, которые независимо от других указывают на тяжелое течение и высокий риск неблагоприятного исхода: госпитализация пациента в отделение реанимации на момент включения в исследование, необходимость искусственной вентиляции легких, снижение уровня сознания, ажитация, установленная нестабильная гемодинамика, субтотальное диффузное уплотнение легочной ткани по типу «матового стекла» и консолидации в сочетании с ретикулярными изменениями; вовлечение паренхимы легкого ≥75% (КТ-картина, соответствующая КТ-4), гидроторакс. В исследование не включали пациентов, имеющих сопутствующие заболевания, которые существенно ухудшают прогноз заболевания (онкологическая патология, острый инфаркт миокарда, ВИЧ, туберкулез и другие).
Статистический анализ полученных данных проводили с использованием стандартного набора статистического пакета программы IBM SPSS Statistics Version 23 с помощью однофакторного дисперсионного анализа для оценки разницы средних с учетом стандартного отклонения (M±SD) у двух и более выборок. Статистическая достоверность различий при расчете методом однофакторного дисперсионного анализа для двух и более выборок считалась достигнутой при значении р менее 0,05.
В таблицах 2, 3, 4 представлены данные о результатах исследования традиционно используемых на практике кардиоспецифичных маркеров.
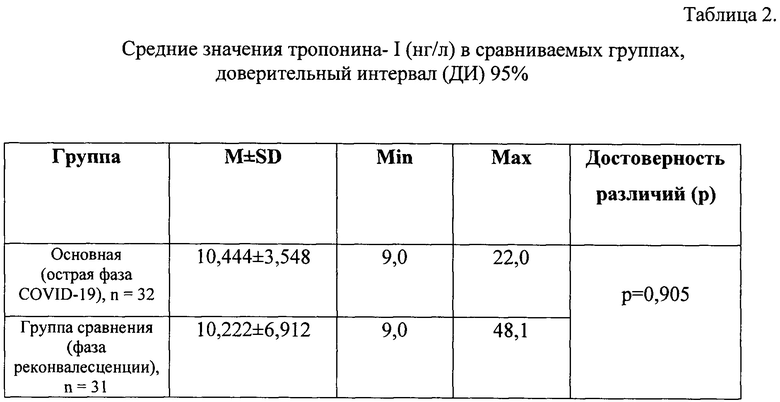
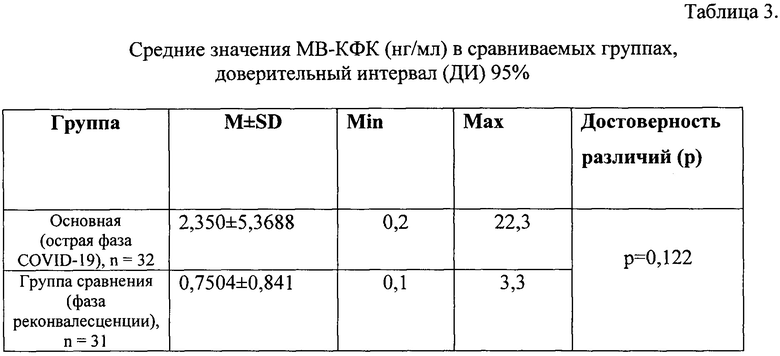
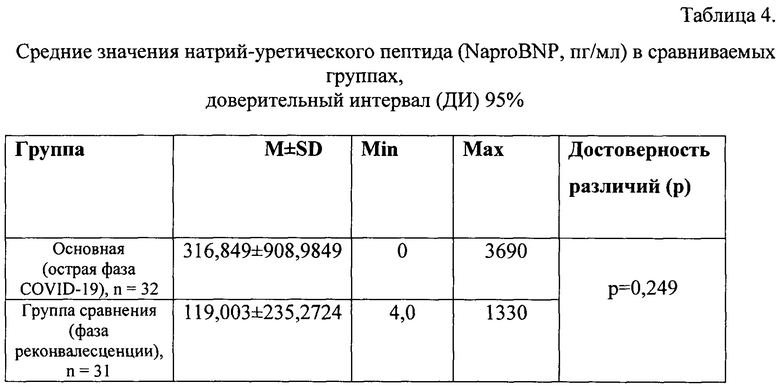
Таким образом, полученные результаты по оценке уровня эндотелина-1 демонстрируют существенные различия между группами до лечения и после курса эффективной терапии, приведшей к выздоровлению или значительному улучшению состояния. По уровню других маркеров, используемых в рутинной практике, различий выявлено не было, хотя они были повышены у некоторых пациентов в острой фазе.
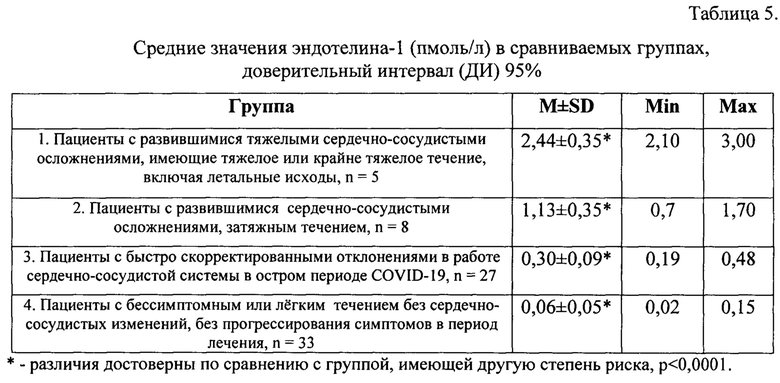
При выделении групп пациентов, различных по прогнозу, мы получили результаты, представленные в таблице 5. Как из нее видно, наиболее высокий риск развития осложнений был у пациентов с высокими значениями эндотелина-1: от 2,1 до 3,0 (верхний предел определения для применявшегося набора реагентов), а наименьший соответствовал значениям от 0,02 (- нижний предел чувствительности применявшегося набора реагентов) до 0,15, что подтверждает выбранные значения. При этом достоверность различий между группами имеет высокую степень. Определенные максимальные и минимальные показатели позволили выделить границы значений между группами с соответствующими степенями риска.
Среди этих пациентов наиболее ярко подтверждают необходимость использования предложенного способа следующие примеры. Для исследования уровня эндотелина-1 дополнительно к показателям, рутинно определяемым лабораторией, в связи с отсутствием соответствующего набора реагентов на тот момент, сыворотка крови аликвотировалась и замораживалась. Уровень эндотелина-1 был определен позднее, одновременно для всех взятых проб крови, после завершения острого периода у представленных в примерах пациентов.
Пример 1.
Мужчина 79 лет обратился за амбулаторной помощью в связи с диагностированной коронавирусной инфекцией, вызванной SARS-CoV-2.
Жалобы на слабость, утомляемость, отсутствие аппетита. Болен в течение 2 дней, неделю назад был контакт с больным, инфицированным вирусом SARS-CoV-2. В анамнезе: аденома предстательной железы, хронический гастрит, другую патологию отрицает. Объективно: на момент осмотра состояние средней степени тяжести, температура тела - 37,5°С, сатурация кислородом - 95-96%, артериальное давление - 110/70 мм рт. ст., ЧСС=68 ударов в минуту, ЧДД=18. Аускультативно определено жесткое дыхание, тоны сердца приглушены. По данным проведенной компьютерной томографии органов грудной клетки, поражения легких нет, КТ-0. Осуществлен лабораторный контроль: общий анализ крови, Д-димера, коагулограммы, взята проба крови на уровень эндотелина-1. По результатам обследования: уровень эндотелина-1 - 3 пмоль/л, что определяется в соответствии с разработанным методом как очень высокий риск. Изменения других показателей, в целом, соответствовали острой фазе COVID-19. Больному было назначено лечение в соответствии с действующими рекомендациями Минздрава РФ. В течение следующих суток состояние больного ухудшилось, в связи с чем он был госпитализирован в реанимационное отделение. На фоне гиперкоагуляции, подтвержденной лабораторно, неэффективности проводимой терапии больной скончался.
Таким образом, на момент первого осмотра пациента никакие данные, за исключением уровня эндотелина-1, не свидетельствовали о вероятности критического ухудшения состояния. Своевременная оценка риска могла бы стать обоснованием для раннего назначения наиболее эффективной противосвертывающей терапии с обеспечением интенсивного мониторинга показателей гемостаза и сердечно-сосудистой деятельности, чего не было сделано из-за отсутствия данных о значимости уровня эндотелина-1 на тот момент.
Пример 2.
Мужчина 83 лет, обратился за помощью с жалобами на ощущение перебоев в работе сердца, повышение температуры тела до 37,5°С. По результатам ПЦР диагностики установлено инфицирование коронавирусной инфекцией, вызванной SARS-CoV-2. Болен в течение 3 дней. Объективно: температура 37,5°С, уровень Д-димера - 594 нг/л. Уровень эндотелина-1 - 0,8 пмоль/л, что соответствует высокому риску развития сердечно-сосудистых осложнений. По данным компьютерной томографии органов грудной клетки, поражения легких нет, картина соответствует возрастной норме, КТ-0. По данным ЭКГ, нарушение проводимости, нарушение реполяризации, единичные вентрикулярные экстрасистолы, изменения миокарда по ишемическому типу в передне-боковом отделе. Среди рекомендованных Минздравом РФ для лечения COVID-19 препаратов было выбрано наиболее активное сочетание. Назначена противовирусная (фавипиравир с нагрузочной дозой 1800 мг 2 раза в первые сутки, затем по 800 мг 2 раза в сутки) и антикоагулянтная (ривароксабан 20 мг - максимальная доза из рекомендуемых для профилактики тромбоэмболических осложнений) терапия. Дополнительно рекомендован прием антибиотика (левофлоксацин 500 мг 2 раза в сутки) и противовоспалительного ингибитора янус киназ (барицитиниб 4 мг в сутки). Пациент наблюдался амбулаторно с ежедневным дистанционным контролем и, при необходимости, осмотром на 5-й, 10-й и 14-й дни. На фоне терапии в течение 2 недель отмечена постепенная положительная динамика, госпитализация не требовалась.
Таким образом, своевременно определенная высокая степень риска могла бы стать убедительным обоснованием для применения активного варианта терапии с частым контролем. В данном случае, в отсутствии результатов исследования на эндотелии-1, это было сделано на основании предположений по возрасту и высокому уровню Д-димера, который повышается при уже имеющемся образовании тромба. Лечение прошло амбулаторно, пациент выздоровел, без развития осложнений. В то же время изменения на ЭКГ наряду с отсутствием поражения легких не могли быть обоснованием для назначения максимальной профилактической дозы ривароксабана и ингибитора янус киназ.
Пример 3.
Мужчина 39 лет обратился за амбулаторной помощью в связи с диагностированной коронавирусной инфекцией, вызванной SARS-CoV-2, и жалобами на выраженную слабость, лихорадку, одышку. Из анамнеза: болен 7 дней. В течение этого времени лечился самостоятельно народными и общепринятыми для лечения ОРВИ средствами, без эффекта. К концу недели почувствовал удушение: нарастание слабости, ломоты во всем теле, стойкое повышение температуры тела до 38,5°С, снижение сатурации кислородом до 93-92%. По данным компьютерной томографии органов грудной клетки, отмечено поражение легких - по 25% с каждой стороны, КТ-2, присутствует перикардиальный выпот. По лабораторным данным, увеличение Д-димера до 1000 нг/л, С-реактивного белка до 80 нг/л, уровень эндотелина-1 - 0,38 ммоль/л, что соответствует средней степени риска развития сердечно-сосудистых осложнений. Пациенту назначили противовирусную (фавипиравир), антикоагулянтную (ривароксабан в средней используемой для профилактики дозе - 10 мг в сутки), антибактериальную (левофлоксацин), и противовоспалительную терапию (ингибиторы янус киназ). На фоне приема препаратов отмечалось устойчивое улучшение, общий курс лечения составил 14 дней, госпитализации не потребовалось.
Таким образом, пример подтверждает наличие средней степени риска, по данным анализа на уровень эндотелина-1, несмотря на большой срок от начала заболевания и наличие поражения легких могло бы объективно подтвердить выбор средней дозы ривароксабана и амбулаторного лечения. В отсутствии результата анализа на эндотелии-1 выбор средних доз терапии и возможностей амбулаторной терапии был сделан на основании возраста пациента, что не является надежным критерием.
Пример 4.
Женщина 62 лет обратилась с жалобами на повышение температуры тела до 37,8°С, ломоту в суставах и мышцах, потерю обоняния в течение 3 дней. По результатам диагностики методом ПЦР установлено инфицирование коронавирусной инфекцией, вызванной вирусом SARS-CoV-2. Оценены лабораторные показатели клинического анализа крови, Д-димера, коагулограммы, сделан анализ крови на уровень эндотелина-1. Уровень эндотелина-1 - 0,10 пмоль/л, что соответствует низкому риску развития сердечно-сосудистых осложнений. Изменения других показателей, в целом, соответствовали острой фазе COVID-19. По данным компьютерной томографии органов грудной клетки, картина соответствует возрастной норме, поражения легких нет, КТ-0. Среди рекомендованных Минздравом РФ для лечения COVID-19 препаратов выбрана наиболее легкая схема терапии. Назначен противовирусный препарат умифеновир 200 мг 4 раза в день и антикоагулянт ривароксабан в минимальной дозе - 2,5 мг. В связи с выздоровлением курс лечения через 7 дней был завершен.
Таким образом, определение уровня эндотелина-1 могло бы объективно подтвердить низкую степень риска сердечно-сосудистых осложнений и возможность использования минимальной терапии с низким риском развития побочных действий от применяемых препаратов. В отсутствии данных об уровне эндотелина-1 это было сделано на основании небольшого срока от появления первых симптомов и невысокой температуры тела, что не является надежными критериями.
Вывод. Разработанный способ определения степени риска развития сердечно-сосудистых осложнений позволяет объективно определить вероятность неблагоприятного исхода COVID-19, своевременно назначить более эффективную терапию и обеспечить активный контроль за состоянием пациента при выявлении высокого риска, как на амбулаторном, так и на стационарном этапе. В то же время в ряде случаев оценка риска позволяет избежать больших доз препаратов и применения активных схем, что позволяет избежать побочных действий и снизить стоимость лечения.
Список литературы
1. Giannis D., Ziogas I.A., Gianni P. Coagulation disorders in coronavirus infected patients: COVID-19, SARS-CoV-1, MERS-CoV and lessons from the past. J. Clin. Virol. 2020; 127. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7195278/.
2. Han H, Yang L, Liu R, et al. Prominent changes in blood coagulation of patients with SARS-CoV-2 infection. Clin Chem Lab Med. 2020. https://doi.org/10.1515/cclm-2020-0188.
3. Levi M. COVID-19 coagulopathy vs disseminated intravascular coagulation. Blood Adv. 2020; 4(12). https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7322961/
4. Tang N, Bai H, Chen X, et al. Anticoagulant treatment is associated with decreased mortality in severe coronavirus disease 2019 patients with coagulopathy. J Thromb Haemost. 2020; 18(5): 1094-1099. https://doi.org/10.1111/jth.14817.
5. Lillicrap D. Disseminated intravascular coagulation in patients with 2019-nCoV pneumonia. J Thromb Haemost. 2020; 18(4):786-787. https://doi.org/10.1111/jth.14781.
6. Ruzhentsova T.A., Chukhliaev P.V., Khavkina D.A., Garbuzov A.A., Akimkin V.G., Zhundrikova V.Iu., Tivanova E.V. The Role of Endothelin-I in Cardiovascular Disease in Patients With COVID-19. Available at SSRN: http://dx.doi.org/10.2139/ssrn.3831110.
7. Шабров A.B., Апресян А.Г., Добкес А.Л., Ермолов С.Ю., Ермолова Т.В., Манасян С.Г., Сердюков С.В. Современные методы оценки эндотелиальной дисфункции и возможности их применения в практической медицине. Рациональная фармакотерапия в кардиологии 2016; 12(6):733-742. DOI: http://dx.doi.org/10.20996/1819-6446-2016-12-6-733-742.
8. Инжутова А.И. Способ оценки эффективности сосудистой терапии по выраженности эндотелиальной дисфункции. 2012. RU2455641.
9. Радаева О.A., Новикова Л.В. Способ определения риска развития сердечно-сосудистых осложнений у женщин с гипертонической болезнью. 2014. RU2530621.
10. Петелина Т.И., Гапон Л.И., Авдеева К.С, Мусихина Н.А., Дьячков С.М. Способ определения диагностического показателя жесткости сосудистой стенки у больных артериальной гипертензией с абдоминальным ожирением. 2015. RU2567606.
11. Кательницкая Л.И., Хаишева Л.А., Иванченко Д.Н., Джагессар Р.К., Кициева А.А., Лужецкая И.В. Способ прогнозирования варианта артериальной гипертонии у пациентов пожилого и старческого возраста. 2003. RU2266702 С2.
12. Парнес Е.Я., Парнес М.Е., Парнес М.Е., Красносельский М.Я. Способ выявления дисфункции эндотелия коронарных артерий. 2003. RU2199266.
13. Сенчихина В.Н., Лямина С.В. «Вазомоторная и секреторная функции эндотелия у больных артериальной гипертонии молодого возраста». Материалы конгресса «Перспективы Российской кардиологии». М.: 2005.
Изобретение относится к медицине, а именно к инфектологии и кардиологии, и может быть использовано для определения степени риска развития сердечно-сосудистых осложнений при COVID-19. В сыворотке крови пациента с подтвержденным COVID-19 проводят лабораторное определение содержания эндотелина-1 с помощью количественного иммуноферментного метода. В зависимости от полученного значения устанавливают степень риска развития сердечно-сосудистых осложнений в соответствии со следующим разделением: менее 0,16 пмоль/л - низкий риск; от 0,16 до 0,5 пмоль/л - средний риск; от 0,5 до 2,0 пмоль/л - высокий риск; более 2,0 пмоль/л - очень высокий риск. Способ обеспечивает возможность установления степеней риска развития сердечно-сосудистых осложнений при COVID-19: низкой, средней, высокой, очень высокой, независимо от наличия или отсутствия хронической соматической патологии системы кровообращения в анамнезе, за счет определения эндотелина-1 в сыворотке крови, являющегося маркером дисфункции эндотелия. 5 табл., 4 пр.
Способ определения степени риска развития сердечно-сосудистых осложнений при COVID-19, отличающийся тем, что в сыворотке крови пациента с подтвержденным COVID-19 проводят лабораторное определение содержания эндотелина-1 с помощью количественного иммуноферментного метода и в зависимости от полученного значения устанавливают степень риска развития сердечно-сосудистых осложнений в соответствии со следующим разделением:
- менее 0,16 пмоль/л - низкий риск;
- от 0,16 до 0,5 пмоль/л - средний риск;
- от 0,5 до 2,0 пмоль/л - высокий риск;
- более 2,0 пмоль/л - очень высокий риск.
| FARHANGRAZI Z.S | |||
| et al | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Precis | |||
| Nanomed | |||
| Способ восстановления спиралей из вольфрамовой проволоки для электрических ламп накаливания, наполненных газом | 1924 |
|
SU2020A1 |
| БУБНОВА М.Г | |||
| и др | |||
| Способ изготовления электрических сопротивлений посредством осаждения слоя проводника на поверхности изолятора | 1921 |
|
SU19A1 |
| Пульмонология | |||
| Способ восстановления спиралей из вольфрамовой проволоки для электрических ламп накаливания, наполненных газом | 1924 |
|
SU2020A1 |
| ПОЛОНСКАЯ Я.В | |||
| и др | |||
| Способ изготовления электрических сопротивлений посредством осаждения слоя проводника на поверхности изолятора | 1921 |
|
SU19A1 |
Авторы
Даты
2022-03-24—Публикация
2021-09-22—Подача