Изобретение относится к медицине, а именно к кардиологии и может быть использовано в лечении пациентов, перенесших инфаркт миокарда.
Известен способ прогнозирования риска жизнеугрожающих желудочковых аритмий, основанный на оценке фракции выброса левого желудочка [1]. Исходя из этого, снижение фракции выброса левого желудочка менее 35% является основным показанием для имплантации кардиовертера-дефибриллятора у больных с ишемической кардиомиопатией, а в частности перенесших инфаркт миокарда, в целях первичной профилактики внезапной сердечной смерти. Это отражено в современных российских и международных рекомендациях [1].
Фракция выброса левого желудочка оказывает наибольшее влияние на риск развития внезапной сердечной смерти в течение первых 6 месяцев после развития острого инфаркта миокарда [2]. Однако по другим исследованиям, у пациентов в ранние сроки после инфаркта миокарда не отмечается улучшения выживаемости в течение 30 месяцев после имплантации кардиовертера-дефибриллятора [3]. Этот парадокс говорит о несовершенстве современных подходов к прогнозированию развития жизнеугрожающих желудочковых тахиаритмий у пациентов, перенесших инфаркт миокарда и планирующихся на имплантацию кардиовертера-дефибриллятора в целях первичной профилактики внезапной сердечной смерти. Это связано с изменчивостью факторов риска по прошествии времени после инфаркта миокарда и изменению клинического состояния больного (улучшается систолическая функция левого желудочка и уменьшаются проявления сердечной недостаточности) [4].
Недостатком данного способа является то, что изолированное использование фракции выброса левого желудочка для селекции пациентов на имплантацию кардиовертера-дефибриллятора с целью первичной профилактики внезапной сердечной смерти не приводит к желаемому результату, так как количество жизнеугрожающих аритмий и как следствие число срабатываний устройств в данной группе больных остается относительно небольшим [5, 6]. Соответственно растет количество имплантированных устройств, вероятность срабатывания которых низкая. А рост нерационально имплантированных кардиовертеров-дефибрилляторов может отразиться на качестве жизни пациентов и на экономическую составляющую системы здравоохранения.
Известен способ прогнозирования желудочковой экстрасистолии высоких градаций у пациентов с хронической сердечной недостаточностью и сохранной фракцией выброса левого желудочка, который является наиболее близким по значению. При данном способе проводят эхокардиографию и определяют толщину межжелудочковой перегородки, индекс конечно-диастолического объема и степень диастолической дисфункции левого желудочка. Прогноз желудочковой экстрасистолии высоких градаций у данной категории пациентов осуществляют с помощью разработанной формулы, используя вышеуказанные предикторы. При значении прогностического коэффициента 0,4 и более прогнозируют желудочковые экстрасистолии высоких градаций у данной категории пациентов. Способ позволяет с высокой точностью осуществить прогнозирование желудочковой экстрасистолии высоких градаций у пациентов с хронической сердечной недостаточностью и сохраненной фракцией выброса левого желудочка.
Недостатками данного способа является то, что используется только один диагностический критерий - показатели эхокардиографии, в то время как для полноценного прогноза можно дополнительно анализировать показатели других неинвазивных методов диагностики, таких как определение уровня ST-2.
В проанализированной патентной и научно-медицинской литературе адекватного прототипа не обнаружено.
Задача изобретения - создание способа прогнозирования риска развития желудочковых тахикардий у пациентов с постинфарктным кардиосклерозом и фракцией выброса левого желудочка менее 35%.
Поставленную задачу решают следующим образом: пациентам определяют уровень концентрации ST-2 в сыворотке крови, после чего проводится расчет прогностического коэффициента. Если прогностический коэффициент по данным определения уровня концентрации ST-2 в сыворотке крови составляет более 0,1502, то у пациента имеется высокий риск развития желудочковой тахикардии.
Техническим результатом является возможность оптимизировать селекцию пациентов с высоким риском развития желудочковой тахикардии и внезапной сердечной смерти, тем самым минимизировать количество нерационально имплантированных кардиовертеров-дефибрилляторов.
Существенные признаки, характеризующие изобретение, проявили в заявляемой совокупности новые свойства, явным образом не вытекающие из уровня техники в данной области и не являющиеся очевидными для специалиста.
Идентичной совокупности признаков не обнаружено при изучении патентной и научно-медицинской литературы.
Данное изобретение может быть использовано в практическом здравоохранении для повышения качества лечения пациентов с постинфарктным кардиосклерозом, фракцией выброса левого желудочка менее 35% и показаниями к имплантации кардиовертера-дефибриллятора.
Исходя из вышеизложенного, следует считать предлагаемое изобретение соответствующим условиям патентоспособности «Новизна», «Изобретательский уровень», «Промышленная применимость».
Способ осуществляют следующим образом:
Первым этапом определяют уровень ST-2. Проводят забор крови натощак из локтевой вены методом венопункции в специальную стерильную вакуумную систему «BD Vacutainer®» с активатором свертывания. Полученный образец инкубируют при комнатной температуре 30 - 45 минут, после чего в течение 15 минут центрифугируют при скорости 3000 оборотов в минуту. Полученную сыворотку декантируют в одноразовые пластиковые пробирки и подвергают заморозке и хранению в температурных условиях при - 40°С. Для количественного измерения концентрации стимулирующего фактора роста ST-2 в сыворотке крови используют набор «Presage® ST2 Assay» (Critical Diagnostics, США), основанный на «сэндвич» иммуноферментном анализе в микропланшетном формате. Результаты измерения выражают в нг/мл. Измерение оптических плотностей, построение калибровочных графиков, оценку и учет результатов количественного содержания всех определяемых показателей проводят с помощью микропланшетного ридера Infinite F50 и программного обеспечения Magellan Tracker (Австрия). Рассчитывают прогностический коэффициент по следующей формуле 1:
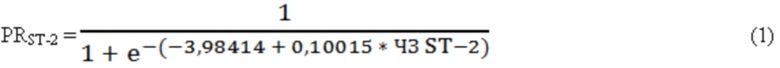
Где, PRST-2 - прогностический коэффициент по данным определения уровня ST-2 в сыворотке крови, е - основание натурального логарифма (е=2,7182818284), ЧЗ ST-2 - числовое значение уровня ST-2 в сыворотке крови. Если прогностический коэффициент по данным определения уровня ST-2 в сыворотке крови более 0,1502, то прогнозируют высокий риск развития желудочковых тахикардий (фиг. 1).
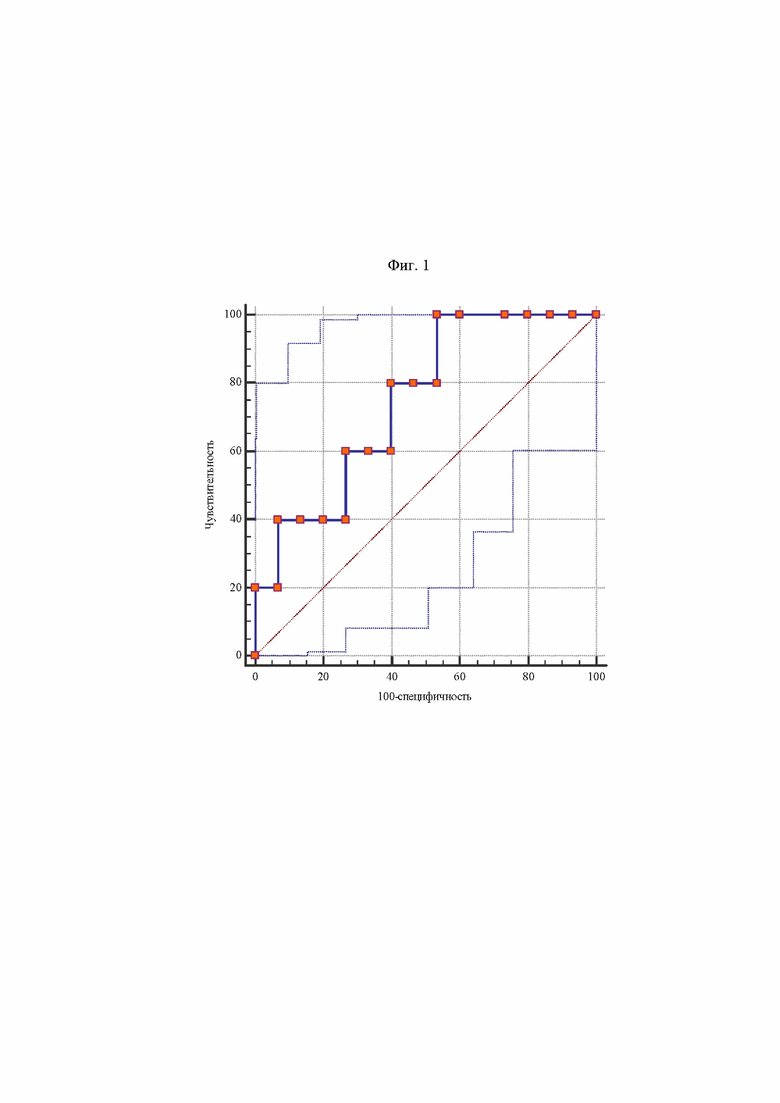
Изобретение будет понятно из следующего описания и приложенных к нему фигур. На фиг. 1 изображена ROC-кривая прогностического коэффициента по результатам определения уровня концентрации ST-2 в сыворотке крови с площадью под кривой 0,747, уровнем достоверности 0,003. Чувствительность данной модели составила 100,00, при специфичности 46,67.
Клинические примеры:
Пример 1. Пациент Г. 64 года, находился на обследовании и лечении в НИИ Кардиологии с 01.08.2017 г. по 11.08.2017 г. с диагнозом: Ишемическая болезнь сердца. Постинфарктный кардиосклероз от 2015 г. Нестенозирующий атеросклероз коронарных артерий (коронароангиография от 02.08.2017 г.). Желудочковая экстрасистолия. Хроническая сердечная недостаточность 1 стадии, функциональный класс II (по классификации New-York Heart Association). Из данных анамнеза было выявлено, что пациент перенес инфаркт миокарда в 2015 году. За прошедшее время чувствовал себя удовлетворительно. В ходе обследования выявлены показания для имплантации кардиовертера-дефибриллятора, с целью первичной профилактики внезапной сердечной смерти. По предлагаемому способу первым этапом проведена эхокардиография, документирована низкая фракция выброса левого желудочка - 29%. Вторым этапом выполнено определение уровня ST-2 в сыворотке крови, по результатам которой прогностический коэффициент составил 0,1637. Следовательно, у пациента выявлен высокий риск развития желудочковой тахикардии и внезапной сердечной смерти. Соответственно проведен следующий этап, а именно имплантация кардиовертера-дефибриллятора. На следующий день после операции проведено программирование кардиовертера-дефибриллятора. Пациент выписан в удовлетворительном состоянии. В ходе 24 месячного наблюдения по данным программирования кардиовертера-дефибриллятора в четыре контрольные точки (1-й, 6-й, 12-й и 18-й месяц после имплантации кардиовертера-дефибриллятора) у пациента документированы 2 пароксизма желудочковой тахикардии, купированный антитахикардийной стимуляцией желудочков. Нарушений в работе устройств выявлено не было.
Пример 2. Пациент С. 48 лет, находился на обследовании и лечении в НИИ Кардиологии с 02.10.2017 г. по 13.10.2017 г. с диагнозом: Ишемическая болезнь сердца: стенокардия напряжения, функциональный класс I. Постинфарктный кардиосклероз от 2014 г. Нестенозирующий атеросклероз коронарных артерий (коронароангиография от 04.10.2017 г.). Хроническая сердечная недостаточность IIБ стадии, функциональный класс II (по классификации New-York Heart Association). Из анамнеза было выявлено, что пациент перенес инфаркт миокарда в 2014 году. В ходе обследования выявлены показания для имплантации кардиовертера-дефибриллятора, с целью первичной профилактики внезапной сердечной смерти. По предлагаемому способу первым этапом проведена эхокардиография, документирована низкая фракция выброса левого желудочка - 34%. Вторым этапом выполнено определение уровня ST-2 в сыворотке крови, по результатам которой прогностический коэффициент составил 0,2531. Следовательно, у пациента выявлен высокий риск развития желудочковой тахикардии и внезапной сердечной смерти. Соответственно проведен следующий этап, а именно имплантация кардиовертера-дефибриллятора. На следующий день после операции проведено программирование кардиовертера-дефибриллятора. Пациент выписан в удовлетворительном состоянии. В ходе 18 месячного наблюдения по данным программирования кардиовертера-дефибриллятора в четыре контрольные точки (1-й, 6-й, 12-й и 18-й месяц после имплантации кардиовертера-дефибриллятора) у пациента документировано 2 пароксизма желудочковой тахикардии, которые были купированы антитахикардийной стимуляцией желудочков, 1 пароксизм желудочковой тахикардии купирован шоковым срабатыванием кардиовертера-дефибриллятора. Нарушений в работе устройств выявлено не было.
Пример 3. Пациент Р. 63 года, находился на обследовании и лечении в НИИ Кардиологии с 04.12.2017 г. по 15.12.2017 г. с диагнозом: Ишемическая болезнь сердца. Постинфарктный кардиосклероз от 2013 г. Нестенозирующий атеросклероз коронарных артерий (коронароангиография от 06.12.2017 г.). Хроническая сердечная недостаточность IIА стадии, функциональный класс II (по классификации New-York Heart Association). Из данных анамнеза было выявлено, что пациент перенес инфаркт миокарда в 2013 г. Отмечает прогрессирование одышки в течение последних трех лет. По данным эхокардиографии от декабря 2016 года выявлено снижение фракции выброса левого желудочка до 28%. За прошедшее время чувствовал себя удовлетворительно. В ходе обследования выявлены показания для имплантации кардиовертера-дефибриллятора, с целью первичной профилактики внезапной сердечной смерти. По предлагаемому способу первым этапом проведена эхокардиография, документирована низкая фракция выброса левого желудочка - 30%. Вторым этапом выполнено определение уровня ST-2 в сыворотке крови, по результатам которой прогностический коэффициент составил 0,1825. Следовательно, у пациента выявлен высокий риск развития желудочковой тахикардии и внезапной сердечной смерти. Соответственно проведен следующий этап, а именно имплантация кардиовертера-дефибриллятора. На следующий день после операции проведено программирование кардиовертера-дефибриллятора. Пациент выписан в удовлетворительном состоянии. В ходе 18 месячного наблюдения по данным программирования кардиовертера-дефибриллятора в четыре контрольные точки (1-й, 6-й, 12-й и 18-й месяц после имплантации кардиовертера-дефибриллятора) у пациента документировано 3 пароксизма желудочковой тахикардии, два пароксизма устойчивой желудочковой тахикардии купированы антитахикардийной стимуляцией желудочков, один пароксизм желудочковой тахикардии носил неустойчивый характер и купировался самостоятельно. Нарушений в работе устройств выявлено не было.
Пример 4. Пациент Д. 47 лет, находился на обследовании и лечении в НИИ Кардиологии с 07.02.2018 г. по 20.02.2018 г. с диагнозом: Ишемическая болезнь сердца: стенокардия напряжения, функциональный класс I. Постинфарктный кардиосклероз от 2013 г. и 2015 г. Нестенозирующий атеросклероз коронарных артерий (коронароангиография от 12.02.2018 г.). Хроническая сердечная недостаточность IIБ стадии, функциональный класс II (по классификации New-York Heart Association). Из данных анамнеза было выявлено, что пациент дважды перенес инфаркт миокарда в 2013 и 2015 году. Отмечает прогрессирование одышки в течение последних четырех лет. Впервые снижение фракции выброса левого желудочка менее 35% документировано в 2014 году. В ходе обследования выявлены показания для имплантации кардиовертера-дефибриллятора, с целью первичной профилактики внезапной сердечной смерти. По предлагаемому способу первым этапом проведена эхокардиография, документирована низкая фракция выброса левого желудочка - 31%. Вторым этапом выполнено определение уровня ST-2 в сыворотке крови, по результатам которой прогностический коэффициент составил 0,2591. Следовательно, у пациента выявлен высокий риск развития желудочковой тахикардии и внезапной сердечной смерти. Соответственно проведен следующий этап, а именно имплантация кардиовертера-дефибриллятора. На следующий день после операции проведено программирование кардиовертера-дефибриллятора. Пациент выписан в удовлетворительном состоянии. В ходе 18 месячного наблюдения по данным программирования кардиовертера-дефибриллятора в четыре контрольные точки (1-й, 6-й, 12-й и 18-й месяц после имплантации кардиовертера-дефибриллятора) у пациента документировано 5 пароксизмов желудочковой тахикардии, 3 пароксизма устойчивой желудочковой тахикардии купированы антитахикардийной стимуляцией желудочка, 2 пароксизма желудочковой тахикардии носили неустойчивый характер и купировались самостоятельно. Нарушений в работе устройств выявлено не было.
Пример 5. Пациент Ю. 71 год, находился на обследовании и лечении в НИИ Кардиологии с 16.01.2018 г. по 29.01.2018 г. с диагнозом: Ишемическая болезнь сердца: стенокардия напряжения, функциональный класс I. Постинфарктный кардиосклероз от 2012, 2014 и 2015 года. Нестенозирующий атеросклероз коронарных артерий (коронароангиография от 18.01.2018 г.). Желудочковая экстрасистолия. Хроническая сердечная недостаточность IIБ стадии, функциональный класс II (по классификации New-York Heart Association). Из данных анамнеза было выявлено, что пациента стенокардия напряжения беспокоит более пяти лет, по данным эхокардиографии выявлено локальное нарушения сокращения миокарда левого желудочка и снижение фракции выброса левого желудочка менее 35% с 2012 года. В ходе обследования выявлены показания для имплантации кардиовертера-дефибриллятора, с целью первичной профилактики внезапной сердечной смерти. По предлагаемому способу первым этапом проведена эхокардиография, документирована низкая фракция выброса левого желудочка - 29%. Вторым этапом выполнено определение уровня ST-2 в сыворотке крови, по результатам которой прогностический коэффициент составил 0,1385. Следовательно, у пациента по данным эхокардиографии выявлен высокий риск развития желудочковой тахикардии и внезапной сердечной смерти. А по данным расчёта прогностического коэффициента по результатам определения концентрации ST-2 в сыворотке крови, риск развития желудочковой тахикардии и внезапной сердечной смерти оказался низким. Но в соответствии с действующими рекомендациями в целях первичной профилактики внезапной сердечной смерти (снижение фракции выброса левого желудочка менее 35%) проведен следующий этап, а именно имплантация кардиовертера-дефибриллятора [1]. На следующий день после операции проведено программирование кардиовертера-дефибриллятора. Пациент выписан в удовлетворительном состоянии. В ходе 18 месячного наблюдения по данным программирования кардиовертера-дефибриллятора в четыре контрольные точки (1-й, 6-й, 12-й и 18-й месяц после имплантации кардиовертера-дефибриллятора) у пациента пароксизмов желудочковой тахикардии не документировано. Нарушений в работе устройств выявлено не было.
Стоит отметить, что у пациентов с пароксизмами желудочковой тахикардии помимо снижения фракции выброса левого желудочка менее 35%, были повышенные показатели концентрации ST-2 в сыворотке крови и прогностический коэффициент по данному показателю составил более 0,1502 (фиг. 1). В то время как у пациентов без пароксизмов желудочковой тахикардии был снижен только один показатель - фракция выброса левого желудочка составила во всех случаях ниже 35%, а показатели концентрации ST-2 в сыворотке крови, были невысокими.
Предлагаемый способ апробирован у 40 пациентов, перенесших инфаркт миокарда, фракцией выброса левого желудочка менее 35% и показаниями для имплантации кардиовертера-дефибриллятора в целях первичной профилактики внезапной сердечной смерти в соответствии с рекомендациями [1]. Все пациенты живы. Осложнений в раннем и позднем послеоперационном периоде не было. По истечении 18 месяцев наблюдения у 10 пациентов документированы пароксизмы желудочковой тахикардии, которые купированы ИКД-терапией, у остальных 30 пациентов пароксизмов желудочковой тахикардии выявлено не было. Клиническая характеристика пациентов по группам представлена в таблице 1.
Таблица 1. Клиническая характеристика пациентов по группам.
(n=10)
(n=30)
Примечание: АРА II - антагонисты рецепторов ангиотензина II, ГГП - гипогликемические препараты, иАПФ - ингибиторы ангиотензинпревращающего фермента, ИМ - инфаркт миокарда, СКА - стентирование коронарных артерий, СКФ - скорость клубочковой фильтрации, ФК - функциональный класс, ФП - фибрилляция предсердий.
Основные клинико-инструментальные показатели по группам представлены в таблице 2.
Таблица 2. Клинико-инструментальные и лабораторные показатели.
(n=10)
Me [Q1; Q3]
(n=30)
Me [Q1; Q3]
Примечание: ИММ - индекс массы миокарда, КДИ - конечно-диастолический индекс, КДО - конечно-диастолический объем, КДР - конечно-диастолический размер, КСИ - конечно-систолический индекс, КСО - конечно-систолический объем, КСР - конечно-систолический размер, ЛЖ - левый желудочек, ЛПИ - индекс левого предсердия, МЖП - межжелудочковая перегородка, ППИ - индекс правого предсердия, СДПЖ - систолическое давление в правом желудочке, ТШХ - тест 6-минутной ходьбы.
Статистический анализ результатов проводили с помощью пакета программ Statistica 10.0, StatSoft, USA. Для оценки нормальности распределения признака использовали критерий Шапиро-Уилка. Для оценки достоверности межгрупповых различий использовали непараметрический критерий Манна-Уитни для независимых выборок. Для оценки корреляционных связей между парами количественных признаков использовали ранговый непараметрический коэффициент Спирмена. Для сравнительной оценки информативности неинвазивных методов диагностики проводился однофакторный (с расчетом индекса Юдена), многофакторный ROC-анализ и логистическая регрессия с помощью пакета программ MedCalc stastical software. При уровне значимости p меньше 0,05 считалось, что исследуемый показатель в сравниваемых группах имел статистически значимые различия.
Предлагаемый в качестве изобретения способ апробирован на 40 больных и позволяет повысить точность прогнозирования риска развития желудочковых тахикардий, своевременно решить вопрос оптимизации отбора пациентов-кандидатов на имплантацию кардиовертера-дефибриллятора, и тем самым повысить эффективность лечения больных с постинфарктным кардиосклерозом и фракцией выброса левого желудочка менее 35%.
Источники информации:
1. Рекомендации ESC по лечению пациентов с желудочковыми нарушениями ритма и профилактике внезапной сердечной смерти. Рабочая группа Европейского Общества Кардиологов (ESC) по лечению пациентов с желудочковыми нарушениями ритма и профилактике внезапной сердечной смерти / S.G. Priori, C. Blomstrom-Lundqvist, A. Mazzanti et al. // Российский кардиологический журнал. - 2016. - №7 (135). - С. 5-86.
2. Valsartan, Captopril, or both in myocardial infarction complicated by heart failure, left ventricular dysfunction, or both / M.A. Pfeffer, J.V. John, McMurray et al. // N. Engl. J. Med. - 2003. - Vol. 349. - P. 1893-1906.
3. Mechanisms underlying the lack of effect of implantable cardioverter-defibrillator therapy on mortality in high-risk patients with recent myocardial infarction: insights from the defibrillation in acute myocardial infarction trial (DINAMIT) / P. Dorian, S.H. Hohnloser, K.E. Thorpe et al. // Circulation. - 2010. - Vol. 122, N 25. - P. 2645-2652.
4. Predictors of sudden cardiac death change with time after myocardial infarction: results from the VALIANT trial / J.P. Piccini, M. Zhang, K. Pieper et al. // Eur. Heart J. - 2010. - Vol. 31. - P. 211-221.
5. Incidence of defibrillator shocks after elective generator exchange following uneventful first battery life / F.M. Merchant, P. Jones, S. Wehrenberg et al. // J. Am. Heart. Assoc. - 2014. - Vol. 3. - P. 1-7.
6. Incidence of implantable cardioverter defibrillator therapy and mortality in primary and secondary prevention of sudden cardiac death / Y. Konstantino, T. Shafat, V. Novack et al. // Isr. Med. Assoc. J. - 2015. - Vol. 17, N 12. - P. 760-763.
7. Cardiac 123I-mIBG scintigraphy is associated with freedom of appropriate ICD therapy in stable chronic heart failure patients / D.O. Verschure, J.R. de Groot, S. Mirzaei et al. // International Journal of Cardiology. - 2017. - Vol. 248. - P. 403-408.
Изобретение относится к медицине, а именно к кардиологии. Пациентам определяют уровень ST-2 в сыворотке крови. Затем рассчитывают прогностический коэффициент риска развития желудочковых тахикардий по формуле. Формула рассчитывается с использованием показателей уровня ST-2 в крови. Если прогностический коэффициент по данным определения уровня ST-2 в сыворотке крови составляет более 0,1502, то у пациента имеется высокий риск развития пароксизмов желудочковой тахикардии. Способ позволяет повысить эффективность антиаритмической терапии у больных с высоким риском развития желудочковых тахикардий, а также позволяет оптимизировать отбор пациентов-кандидатов на имплантацию кардиовертера-дефибриллятора, что уменьшит количество нерационально имплантируемых устройств, тем самым улучшит качество жизни пациентов и оптимизирует экономические затраты. 5 пр., 2 табл., 1 ил.
Способ прогнозирования риска развития желудочковых тахикардий у пациентов с постинфарктным кардиосклерозом и фракцией выброса левого желудочка менее 35%, характеризующийся тем, что определяют уровень ST-2 в сыворотке крови и рассчитывают прогностический коэффициент по формуле
PRST-2 = 1/(1 + e^(-(-3,98414 + 0,10015 * ЧЗ ST-2))),
где PRST-2 – прогностический коэффициент риска развития желудочковой тахикардии, рассчитанный по уровню ST-2 в сыворотке крови;
е – основание натурального логарифма (е=2,7182818284);
-3,98414 – коэффициент постоянной;
0,10015 – коэффициент переменной;
ЧЗ ST-2 – числовое значение уровня ST-2 в сыворотке крови;
и при значении PRST-2 более 0,1502 прогнозируют высокий риск развития желудочковых тахикардий.
| Атабеков Т | |||
| А | |||
| ПРОГНОСТИЧЕСКАЯ ОЦЕНКА РАЗВИТИЯ ЖЕЛУДОЧКОВЫХ ТАХИАРИТМИЙ И ОПТИМИЗАЦИЯ ИМПЛАНТАЦИИ КАРДИОВЕРТЕРА ДЕФИБРИЛЛЯТОРА У ПАЦИЕНТОВ С ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА, Томск, 2020, 103 с | |||
| Способ прогнозирования риска развития желудочковых тахиаритмий у пациентов, перенесших инфаркт миокарда, с фракцией выброса левого желудочка менее 35% | 2019 |
|
RU2722656C1 |
| Супергетеродинный радиоприемник | 1930 |
|
SU20157A1 |
| AТAБЕКОВ Т | |||
| A | |||
| и др | |||
| Неинвазивные методы диагностики в оценке развития желудочковых тахиаритмий у | |||
Авторы
Даты
2022-04-15—Публикация
2021-10-21—Подача