Изобретение относится к медицине, а именно к кардиологии, и может быть использовано в лечении пациентов с ишемической болезнь сердца и высоким риском развития желудочковой тахикардии.
Известен способ стратификации риска жизнеугрожающих желудочковых нарушений ритма сердца, основанный на оценке систолической функции левого желудочка и функционального класса хронической сердечной недостаточности (по классификации Нью-Йоркской ассоциации сердца), у пациентов с ишемической болезнью сердца [1]. Так, имплантация кардиовертера-дефибриллятора в целях вторичной профилактики показана пациентам с устойчивой желудочковой тахикардией, при умеренно выраженной дисфункции левого желудочка (фракция выброса левого желудочка менее 45%), вне зависимости от возможности выполнения катетерной абляции и результатов процедуры (класс показаний I, уровень доказанности C) [1]. А снижение фракции выброса левого желудочка менее 35% и наличие сердечной недостаточности II или III функционального класса по классификации Нью-Йоркской ассоциации сердца, вследствие перенесенного, не менее чем 40 дней назад, инфаркта миокарда, является показанием для имплантации кардиовертера-дефибриллятора в целях первичной профилактики внезапной сердечной смерти [1].
Согласно исследованиям, фракция выброса левого желудочка оказывает наибольшее влияние на риск развития внезапной сердечной смерти в течение первых 6 месяцев после развития острого инфаркта миокарда [2]. Однако по другим исследованиям, у пациентов в ранние сроки после инфаркта миокарда не отмечается улучшения выживаемости в течение 30 месяцев после имплантации кардиовертера-дефибриллятора [3]. Этот парадокс говорит о несовершенстве современных подходов к прогнозированию развития жизнеугрожающих желудочковых тахикардий у пациентов с ишемической болезнью сердца и планирующихся на имплантацию кардиовертера-дефибриллятора в целях первичной и вторичной профилактики внезапной сердечной смерти.
Недостатком данного способа является то, что использование фракции выброса левого желудочка и функционального класса сердечной недостаточности для селекции пациентов на имплантацию кардиовертера-дефибриллятора с целью первичной и вторичной профилактики внезапной сердечной смерти не приводит к желаемому результату, так как количество жизнеугрожающих аритмий и как следствие число срабатываний устройств в данной группе больных остается относительно небольшим [4, 5]. Соответственно растет количество имплантированных устройств, вероятность срабатывания которых низкая.
Известен способ прогнозирования желудочковой экстрасистолии высоких градаций у пациентов с хронической сердечной недостаточностью и сохранной фракцией выброса левого желудочка. При данном способе проводят эхокардиографию и определяют толщину межжелудочковой перегородки, индекс конечно-диастолического объема и степень диастолической дисфункции левого желудочка. Прогноз желудочковой экстрасистолии высоких градаций у данной категории пациентов осуществляют с помощью разработанной формулы, используя вышеуказанные предикторы. При значении прогностического коэффициента 0,4 и более прогнозируют желудочковые экстрасистолии высоких градаций у данной категории пациентов. Способ позволяет с высокой точностью осуществить прогнозирование желудочковой экстрасистолии высоких градаций у пациентов с хронической сердечной недостаточностью и сохраненной фракцией выброса левого желудочка.
Основным недостатком данного способа является использование только показателей эхокардиографии, что не дает достаточной точности прогноза желудочковых тахикардий у больных ишемической болезнью сердца.
В проанализированной патентной и научно-медицинской литературе адекватного прототипа не обнаружено.
Задача изобретения является создание способа прогнозирования риска развития желудочковых тахикардий у пациентов с ишемической болезнью сердца c учетом показателя активности симпатико-адреналовой системы такого, как бета-адренореактивность мембран эритроцитов.
Поставленную задачу решают следующим образом: пациентам определяют уровень бета-адренореактивности мембран эритроцитов в крови. Затем рассчитывают прогностический коэффициент риска развития желудочковых тахикардий по формуле
ПК = 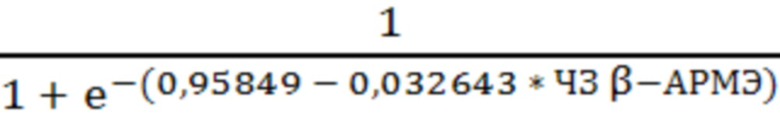
Если прогностический коэффициент составляет 0,304 и более, то у пациента определяют высокий риск развития желудочковой тахикардии.
Изобретение будет понятно из следующего описания и приложенных к нему фигуры.
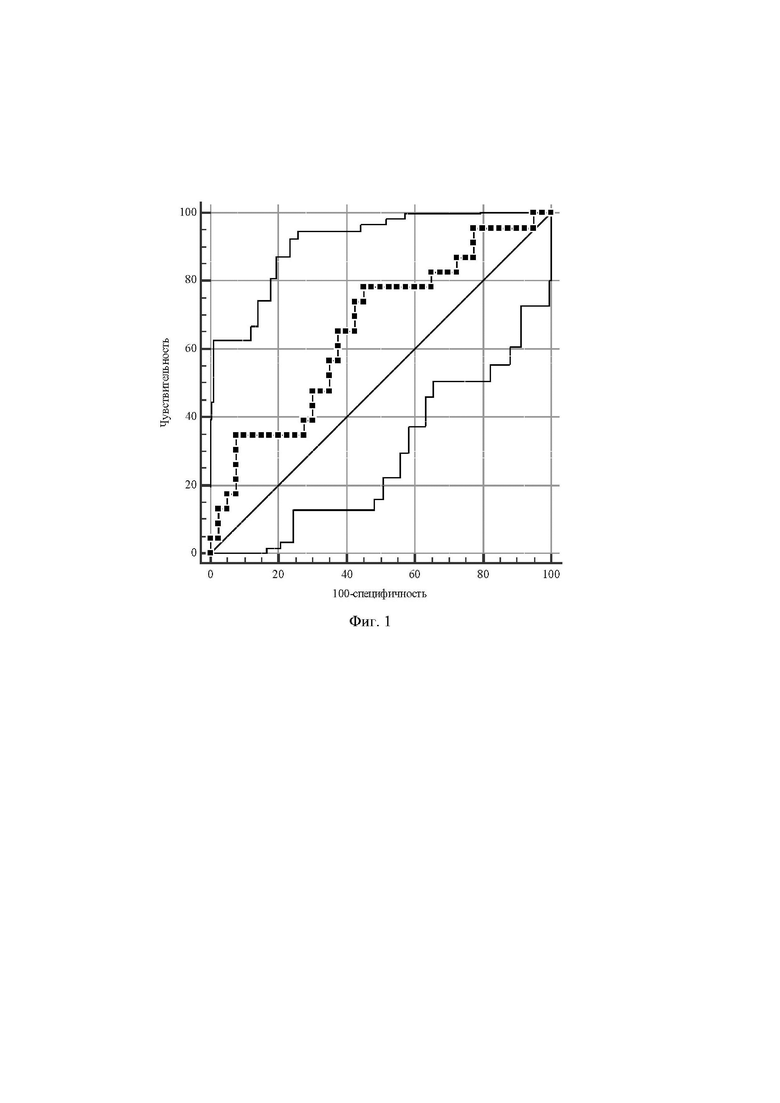
На фиг. 1 изображена ROC-кривая прогностического коэффициента риска развития желудочковых тахикардий по результатам определения показателя уровня бета-адренореактивности мембран эритроцитов в крови с площадью под кривой 0,657, уровнем достоверности 0,031. Чувствительность данной прогностической модели составила 78,26, при специфичности 55,00.
Способ осуществляют следующим образом.
Определение бета-адренореактивности организма по изменению осморезистентности эритроцитов под влиянием бета-адреноблокатора осуществляли с помощью набора реактивов «БЕТА-АРМ АГАТ» (ООО «Агат-Мед», Россия) по предлагаемому протоколу. Для этого проводился забор крови из локтевой вены методом венопункции в специальную стерильную вакуумную систему «BD Vacutainer®» с антикоагулянтом K2 ЭДТА. После 0,2 мл цельной крови добавляли к 0,2 мл физиологического раствора и перемешивали, избегая пенообразования. В центрифужные пробирки (по две контрольные и две опытные пробы на каждый анализируемый образец крови) вносили буфер, в контрольные пробы - 0,1 мл дистиллированной воды, в опытные пробы - 0,1 мл раствора адренореактивного вещества, перемешивали, вносили образец крови в объеме 0,05 мл, перемешивали без пенообразования и инкубировали 15 мин при комнатной температуре. Затем опять перемешивали и инкубировали 15 мин при комнатной температуре. Далее пробы центрифугировали 10 мин при 1500 об/мин на центрифуге «Eppendorf» (Германия). Надосадочный слой переносили в кювету и измеряли величину оптической плотности проб против физиологического раствора при длине волны 540 нм на спектрофотометре Biochrom WPA Biowave II (Великобритания).
Величину бета-адренореактивности мембран эритроцитов в крови рассчитывали по предлагаемой фирмой формуле 1
β-АРМЭ = (Е01+ Е02)/(Ек1+Ек2)*100%, (1)
где β-АРМЭ - величина показателя адренореактивности мембран эритроцитов в крови, усл. ед.; Е01 и Е02 - оптические плотности опытных проб, ед. опт. плотн.; Ек1 и Ек2 - оптические плотности контрольных проб, ед. опт. плотн.
Принцип действия
Метод основан на факте торможения гемолиза эритроцитов, помещенных в гипоосмотическую среду, в присутствии бета-адреноблокатора - 1-(1-изопропиламино)-3-(1-нафталенил-окси)-2-пропанола гидрохлорида. Эритроциты человека, помещенные в гипоосмотическую среду, подвергаются гемолизу, степень которого определяют по величине оптической плотности надосадочной жидкости при длине волны 540 нм (контроль). В опытную пробу с аналогичным раствором гипоосмотического буфера добавляют раствор бета-адреноблокатора, который связывается с бета-рецепторами клеточной мембраны, снижая степень гемолиза.
Следующим этапом рассчитывают прогностический коэффициент риска развития желудочковых тахикардий по предложенной нами формуле 2
ПК = 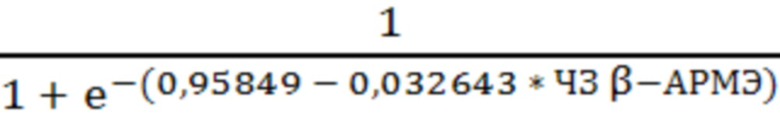 , (2)
, (2)
где ПК - прогностический коэффициент риска развития желудочковой тахикардии, рассчитанный по уровню бета-адренореактивности мембран эритроцитов в крови, е - основание натурального логарифма (е=2,7182818284), 0,95849 - коэффициент постоянной, - 0,032643 - коэффициент переменной, ЧЗ β-АРМЭ - числовое значение уровня бета-адренореактивности мембран эритроцитов в крови. Если прогностический коэффициент риска развития желудочковой тахикардии по уровню бета-адренореактивности мембран эритроцитов в крови 0,304 и более, то прогнозируют высокий риск развития желудочковых тахикардий (фиг. 1).
Статистический анализ результатов проводили с помощью пакета программ Statistica 10.0, StatSoft, USA. Для оценки нормальности распределения признака использовали критерий Шапиро-Уилка. Для оценки достоверности межгрупповых различий использовали непараметрический критерий Манна-Уитни для независимых выборок. Для сравнительной оценки информативности неинвазивных методов диагностики проводился однофакторный (с расчетом индекса Юдена), многофакторный ROC-анализ и логистическая регрессия с помощью пакета программ MedCalc stastical software. При уровне значимости p меньше 0,05 считалось, что исследуемый показатель в сравниваемых группах имел статистически значимые различия.
Техническим результатом является возможность оптимизировать антиаритмическую терапию у пациентов с высоким риском развития желудочковой тахикардии.
Существенные признаки, характеризующие изобретение, проявили в заявляемой совокупности новые свойства, явным образом не вытекающие из уровня техники в данной области и не являющиеся очевидными для специалиста.
Идентичной совокупности признаков не обнаружено при изучении патентной и научно-медицинской литературы.
Данное изобретение может быть использовано в практическом здравоохранении для повышения качества лечения пациентов с ишемической болезнью сердца и показаниями для имплантации кардиовертера-дефибриллятора.
Исходя из вышеизложенного, следует считать предлагаемое изобретение соответствующим условиям патентоспособности «Новизна», «Изобретательский уровень», «Промышленная применимость».
Предлагаемый способ апробирован у 63 пациентов с ишемической болезнью сердца и показаниями для имплантации кардиовертера-дефибриллятора в целях профилактики внезапной сердечной смерти в соответствии с рекомендациями [1].
Все пациенты живы. Осложнений в раннем и позднем послеоперационном периоде не было. За период наблюдения (27,0 [14,0; 53,0] месяцев) у 23 пациентов документированы пароксизмы желудочковой тахикардии по данным записи эндограмм кардиовертера-дефибриллятора, они составили первую группу. У остальных 40 пациентов пароксизмов желудочковой тахикардии выявлено не было, они составили вторую группу. Клиническая характеристика пациентов по группам представлена в таблице 1.
Таблица 1. Клиническая характеристика пациентов по группам
(n=23)
(n=40)
Примечание: АРА II - антагонисты рецепторов ангиотензина II, ГГП - гипогликемические препараты, ГМЛЖ - гипертрофия миокарда левого желудочка, иАПФ - ингибиторы ангиотензинпревращающего фермента, ИКМП - ишемическая кардиомиопатия, ИМ - инфаркт миокарда, ИММЛЖ - индекс массы миокарда левого желудочка, ИМТ - индекс массы тела, КСД - калийсберегающий диуретик, СКА - стентирование коронарных артерий, ФВЛЖ - фракция выброса левого желудочка, ФЖ - фибрилляция желудочков, ФК - функциональный класс, ФП - фибрилляция предсердий.
Основные клинико-инструментальные показатели пациентов по группам представлены в таблице 2.
Таблица 2. Лабораторно-инструментальные показатели
(n=23)
Me [Q1; Q3]
(n=40)
Me [Q1; Q3]
Примечание: ЗСЛЖ - задняя стенка левого желудочка, ИСЛЖ - левого желудочка, КДИЛЖ - конечно-диастолический индекс левого желудочка, КДОЛЖ - конечно-диастолический объем левого желудочка, КДРЛЖ - конечно-диастолический размер левого желудочка, КСИЛЖ - конечно-систолический индекс левого желудочка, КСОЛЖ - конечно-систолический объем левого желудочка, КСРЛЖ - конечно-систолический размер левого желудочка, МЖП - межжелудочковая перегородка, СДПЖ - систолическое давление в правом желудочке, СИ (В) - сердечный индекс (В-режим), β-АРМЭ - бета-адренореактивность мембран эритроцитов в крови.
У пациентов с пароксизмами желудочковой тахикардии (первая группа) показатель бета-адренореактивности мембран эритроцитов в крови был статистически значимо ниже, чем у пациентов без эпизодов желудочковой тахикардии (вторая группа). Прогностический коэффициент риска развития желудочковой тахикардии, рассчитанный по уровню бета-адренореактивности мембран эритроцитов в крови у пациентов с желудочковой тахикардией составил 0,304 и более (фиг. 1). В то время как у пациентов без пароксизмов желудочковой тахикардии данный прогностический коэффициент был 0,303 и менее.
Пример 1. Пациент В.Я. 66 лет, находился на обследовании и лечении в НИИ Кардиологии с 08.09.2017 г. по 18.09.2017 г. с диагнозом: Ишемическая болезнь сердца. Нестенозирующий атеросклероз коронарных артерий. Пароксизмальная устойчивая желудочковая тахикардия. Синдром Морганьи-Эдамса-Стокса. Хроническая сердечная недостаточность 1 стадии, функциональный класс II (по классификации New-York Heart Association). В ходе обследования выявлены показания для имплантации кардиовертера-дефибриллятора с целью вторичной профилактики внезапной сердечной смерти. Фракция выброса левого желудочка по данным эхокардиографии составила 63%. 13.09.2017 выполнена имплантация кардиовертера-дефибриллятора, проведено программирование устройства. Пациент выписан в удовлетворительном состоянии. В ходе 26 месячного наблюдения по данным программирования кардиовертера-дефибриллятора у пациента документированы 18 пароксизмов устойчивой желудочковой тахикардии, купированные антитахикардийной стимуляцией желудочков. Нарушений в работе устройств выявлено не было. По предлагаемому способу проведено определение уровня бета-адренореактивности мембран эритроцитов в крови, который составил 27,15%. Проведен расчет прогностического коэффициента риска развития желудочковой тахикардии по данным определения показателя уровня бета-адренореактивности мембран эритроцитов в крови, который составил 0,518. Следовательно, у пациента высокий риск развития желудочковой тахикардии. Соответственно, имплантация кардиовертера-дефибриллятора была оправданной.
Пример 2. Пациент И.Я. 67 лет, находился на обследовании и лечении в НИИ Кардиологии с 03.09.2015 г. по 16.09.2015 г. с диагнозом: Ишемическая болезнь сердца. Нестенозирующий атеросклероз коронарных артерий. Пароксизмальная устойчивая желудочковая тахикардия. Синдром Морганьи-Эдамса-Стокса. Хроническая сердечная недостаточность 1 стадии, функциональный класс I (по классификации New-York Heart Association). В ходе обследования выявлены показания для имплантации кардиовертера-дефибриллятора с целью вторичной профилактики внезапной сердечной смерти. Фракция выброса левого желудочка по данным эхокардиографии составила 67%. 08.09.2015 выполнена имплантация кардиовертера-дефибриллятора, проведено программирование устройства. Пациент выписан в удовлетворительном состоянии. В ходе 52 месячного наблюдения по данным программирования кардиовертера-дефибриллятора у пациента документированы 2 пароксизма устойчивой желудочковой тахикардии, купированные шоком. Нарушений в работе устройств выявлено не было. По предлагаемому способу проведено определение уровня бета-адренореактивности мембран эритроцитов в крови, который составил 19,5%. Проведен расчет прогностического коэффициента риска развития желудочковой тахикардии по данным определения показателя уровня бета-адренореактивности мембран эритроцитов в крови, который составил 0,579. Следовательно, у пациента высокий риск развития желудочковой тахикардии. Соответственно, имплантация кардиовертера-дефибриллятора была оправданной.
Пример 3. Пациент И.И. 57 лет, находился на обследовании и лечении в НИИ Кардиологии с 12.12.2016 г. по 23.12.2016 г. с диагнозом: Ишемическая болезнь сердца. Постинфарктный кардиосклероз от 2014 года. Атеросклероз коронарных артерий. Ишемическая кардиомиопатия. Пароксизмальная устойчивая желудочковая тахикардия. Синдром Морганьи-Эдамса-Стокса. Хроническая сердечная недостаточность I стадии, функциональный класс II (по классификации New-York Heart Association). В ходе обследования выявлены показания для имплантации кардиовертера-дефибриллятора с целью вторичной профилактики внезапной сердечной смерти. Фракция выброса левого желудочка по данным эхокардиографии составила 34%. 19.12.2016 выполнена имплантация кардиовертера-дефибриллятора, проведено программирование устройства. Пациент выписан в удовлетворительном состоянии. В ходе 28 месячного наблюдения по данным программирования кардиовертера-дефибриллятора у пациента документированы 3 пароксизма неустойчивой желудочковой тахикардии, купированные самостоятельно, и 3 эпизода устойчивой желудочковой тахикардии, купированные антитахикардийной стимуляцией желудочков. Нарушений в работе устройств выявлено не было. По предлагаемому способу проведено определение уровня бета-адренореактивности мембран эритроцитов в крови, который составил 11,77%. Проведен расчет прогностического коэффициента риска развития желудочковой тахикардии по данным определения показателя уровня бета-адренореактивности мембран эритроцитов в крови, который составил 0,639. Следовательно, у пациента высокий риск развития желудочковой тахикардии. Соответственно, имплантация кардиовертера-дефибриллятора была оправданной.
Пример 4. Пациент А.С. 58 лет, находился на обследовании и лечении в НИИ Кардиологии с 13.01.2017 г. по 23.01.2017 г. с диагнозом: Ишемическая болезнь сердца. Постинфарктный кардиосклероз от 1995, 2005 и 2006 года. Атеросклероз коронарных артерий. Стентирование коронарных артерий. Ишемическая кардиомиопатия. Хроническая сердечная недостаточность IIБ стадии, функциональный класс III (по классификации New-York Heart Association). В ходе обследования выявлены показания для имплантации кардиовертера-дефибриллятора с целью первичной профилактики внезапной сердечной смерти. Фракция выброса левого желудочка по данным эхокардиографии составила 22%. 18.01.2017 выполнена имплантация кардиовертера-дефибриллятора, проведено программирование устройства. Пациент выписан в удовлетворительном состоянии. В ходе 30 месячного наблюдения по данным программирования кардиовертера-дефибриллятора у пациента документированы 17 пароксизмов неустойчивой желудочковой тахикардии, купированные самостоятельно и 1 эпизод желудочковой тахикардии, купированный антитахикардийной стимуляцией желудочков. Нарушений в работе устройств выявлено не было. По предлагаемому способу проведено определение уровня бета-адренореактивности мембран эритроцитов в крови, который составил 41,54%. Проведен расчет прогностического коэффициента риска развития желудочковой тахикардии по данным определения показателя уровня бета-адренореактивности мембран эритроцитов в крови, который составил 0,402. Следовательно, у пациента высокий риск развития желудочковой тахикардии. Соответственно, имплантация кардиовертера-дефибриллятора была оправданной.
Пример 5. Пациент А.Д. 79 лет, находился на обследовании и лечении в НИИ Кардиологии с 03.02.2017 г. по 14.02.2017 г. с диагнозом: Ишемическая болезнь сердца. Постинфарктный кардиосклероз от 2016 года. Атеросклероз коронарных артерий. Ишемическая кардиомиопатия. Хроническая сердечная недостаточность IIБ стадии, функциональный класс II (по классификации New-York Heart Association). В ходе обследования выявлены показания для имплантации кардиовертера-дефибриллятора с целью первичной профилактики внезапной сердечной смерти. Фракция выброса левого желудочка по данным эхокардиографии составила 32%. 08.02.2017 выполнена имплантация кардиовертера-дефибриллятора, проведено программирование устройства. Пациент выписан в удовлетворительном состоянии. В ходе 28 месячного наблюдения по данным программирования кардиовертера-дефибриллятора у пациента документирован 1 пароксизм неустойчивой желудочковой тахикардии, купированный самостоятельно. Нарушений в работе устройств выявлено не было. По предлагаемому способу проведено определение уровня бета-адренореактивности мембран эритроцитов в крови, который составил 27,26%. Проведен расчет прогностического коэффициента риска развития желудочковой тахикардии по данным определения показателя уровня бета-адренореактивности мембран эритроцитов в крови, который составил 0,517. Следовательно, у пациента высокий риск развития желудочковой тахикардии. Соответственно, имплантация кардиовертера-дефибриллятора была оправданной.
Пример 6. Пациент Г.В. 66 лет, находился на обследовании и лечении в НИИ Кардиологии с 22.09.2017 г. по 02.10.2017 г. с диагнозом: Ишемическая болезнь сердца. Постинфарктный кардиосклероз 2004 года. Атеросклероз коронарных артерий. Стентирование коронарных артерий. Ишемическая кардиомиопатия. Хроническая сердечная недостаточность I стадии, функциональный класс II (по классификации New-York Heart Association). В ходе обследования выявлены показания для имплантации кардиовертера-дефибриллятора с целью первичной профилактики внезапной сердечной смерти. Фракция выброса левого желудочка по данным эхокардиографии составила 33%. 27.09.2017 выполнена имплантация кардиовертера-дефибриллятора, проведено программирование устройства. Пациент выписан в удовлетворительном состоянии. В ходе 24 месячного наблюдения по данным программирования кардиовертера-дефибриллятора у пациента срабатываний устройства и пароксизмов желудочковой тахикардии выявлено не было. По предлагаемому способу проведено определение уровня бета-адренореактивности мембран эритроцитов в крови, который составил 80,62%. Проведен расчет прогностического коэффициента риска развития желудочковой тахикардии по данным определения показателя уровня бета-адренореактивности мембран эритроцитов в крови, который составил 0,157. Следовательно, у пациента низкий риск развития желудочковой тахикардии. Однако, у пациента по данным эхокардиографии выявлен высокий риск развития желудочковой тахикардии, и в соответствии с действующими рекомендациями, в целях первичной профилактики внезапной сердечной смерти (снижение фракции выброса левого желудочка менее 35%, II или III функциональный класс хронической сердечной недостаточности, вследствие перенесенного инфаркта миокарда давностью более 40 дней) пациенту проведена имплантация кардиовертера-дефибриллятора, при этом из антиаритмических лекарств была назначена только поддерживающая доза бета-адреноблокатора.
Таким образом, прогностический коэффициент риска развития желудочковой тахикардии по уровню бета-адренореактивности мембран эритроцитов в крови позволяет повысить точность оценки риска развития желудочковых тахикардий, своевременно решить вопрос оптимизации отбора пациентов-кандидатов на имплантацию кардиовертера-дефибриллятора, а также подбора антиаритмической терапии и тем самым повысить эффективность лечения больных ишемической болезнью сердца.
Источники информации
1. Рекомендации ESC по лечению пациентов с желудочковыми нарушениями ритма и профилактике внезапной сердечной смерти. Рабочая группа Европейского Общества Кардиологов (ESC) по лечению пациентов с желудочковыми нарушениями ритма и профилактике внезапной сердечной смерти / S.G. Priori, C. Blomstrom-Lundqvist, A. Mazzanti et al. // Российский кардиологический журнал. - 2016. - №7 (135). - С. 5-86.
2. Valsartan, Captopril, or both in myocardial infarction complicated by heart failure, left ventricular dysfunction, or both / M.A. Pfeffer, J.V. John, McMurray et al. // N. Engl. J. Med. - 2003. - Vol. 349. - P. 1893-1906.
3. Mechanisms underlying the lack of effect of implantable cardioverter-defibrillator therapy on mortality in high-risk patients with recent myocardial infarction: insights from the defibrillation in acute myocardial infarction trial (DINAMIT) / P. Dorian, S.H. Hohnloser, K.E. Thorpe et al. // Circulation. - 2010. - Vol. 122, N 25. - P. 2645-2652.
4. Incidence of defibrillator shocks after elective generator exchange following uneventful first battery life / F.M. Merchant, P. Jones, S. Wehrenberg et al. // J. Am. Heart. Assoc. - 2014. - Vol. 3. - P. 1-7.
5. Incidence of implantable cardioverter defibrillator therapy and mortality in primary and secondary prevention of sudden cardiac death / Y. Konstantino, T. Shafat, V. Novack et al. // Isr. Med. Assoc. J. - 2015. - Vol. 17, N 12. - P. 760-763.
Изобретение относится к медицине, а именно к кардиологии. Пациентам определяют уровень бета-адренореактивности мембран эритроцитов в крови. Затем рассчитывают прогностический коэффициент риска развития желудочковых тахикардий по оригинальной формуле. Формула рассчитывается с использованием показателя уровня бета-адренореактивности мембран эритроцитов в крови. Если прогностический коэффициент по результатам определения уровня бета-адренореактивности мембран эритроцитов в крови составляет 0,304 и более, то у пациента прогнозируют высокий риск развития желудочковой тахикардии. Способ позволяет повысить эффективность антиаритмической терапии у больных с высоким риском развития желудочковых тахикардий, тем самым улучшит качество жизни пациентов. 1 ил., 2 табл., 6 пр.
Способ прогнозирования риска развития желудочковых тахикардий у пациентов с ишемической болезнью сердца, характеризующийся тем, что определяют уровень бета-адренореактивности мембран эритроцитов в крови и рассчитывают прогностический коэффициент по формуле
ПК = 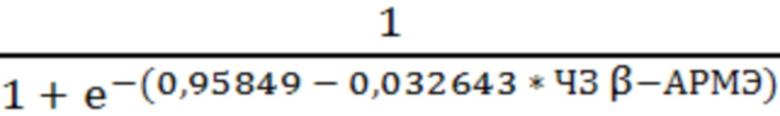
где ПК - прогностический коэффициент риска развития желудочковой тахикардии,
е - основание натурального логарифма - е=2,7182818284,
0,95849 - коэффициент постоянной,
- 0,032643 - коэффициент переменной,
ЧЗ β-АРМЭ - числовое значение уровня бета-адренореактивности мембран эритроцитов в крови;
и при значении данного коэффициента равным 0,304 и более прогнозируют высокий риск развития желудочковых тахикардий.
| Способ прогнозирования прогрессирования хронической сердечной недостаточности в течение года после перенесенного инфаркта миокарда | 2019 |
|
RU2716749C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ РИСКА РАЗВИТИЯ ПАРОКСИЗМОВ ЖЕЛУДОЧКОВОЙ ТАХИКАРДИИ У БОЛЬНЫХ В ПЕРВЫЕ СУТКИ ИНФАРКТА МИОКАРДА | 2017 |
|
RU2650039C1 |
| АЛЕКСАНДРЕНКО В.А | |||
| ПРОГНОЗИРОВАНИЕ ИНДИВИДУАЛЬНОГО РИСКАНЕБЛАГОПРИЯТНЫХ СЕРДЕЧНО-СОСУДИСТЫХ СОБЫТИЙ В ТЕЧЕНИЕ ГОДА ПОСЛЕ ПЕРЕНЕСЕННОГО ИНФАРКТА МИОКАРДА С УЧЕТОМ МОЛЕКУЛЯРНО-ГЕНЕТИЧЕСКИХ ФАКТОРОВ, диссертация, Томск, 2020, 172 с | |||
| Гарганеева А.А | |||
| и др | |||
| Бета-адренореактивность эритроцитов и | |||
Авторы
Даты
2021-07-26—Публикация
2021-04-01—Подача