Данная заявка испрашивает преимущество по предварительной заявке на патент США № 62/456 609, поданной 8 февраля 2017 года, которая тем самым включена посредством ссылки во всей своей полноте.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Настоящая заявка содержит перечень последовательностей, который был подан в электронном виде в формате ASCII и включен в данный документ посредством ссылки во всей своей полноте. Указанная копия в формате ASCII, созданная 19 января 2018 года, имеет название PAT057578-WO-PCT_SL.txt и размер 80 531 байт.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к антителам-миметикам фактора роста фибробластов 21 (FGF21). Также раскрыты способы лечения FGF21-ассоциированных нарушений, таких как ожирение, сахарный диабет 1 типа и 2 типа, панкреатит, дислипидемия, неалкогольный стеатогепатит (NASH), инсулинорезистентность, гиперинсулинемия, нарушение толерантности к глюкозе, гипергликемия, метаболический синдром и другие метаболические нарушения, а также снижения смертности и инвалидности критически больных пациентов.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Семейство факторов роста фибробластов (FGF) характеризуется 22 генетически отличающимися гомологичными лигандами, которые классифицируются на семь подсемейств. В соответствии с опубликованными литературными источниками, семейство FGF в настоящее время состоит из по меньшей мере двадцати трех членов, от FGF-1 до FGF-23 (Reuss et al. (2003) Cell Tissue Res. 313:139-157).
Фактор роста фибробластов 21 (FGF21) был выделен из мышиных эмбрионов и является наиболее близким к FGF19 и FGF23. Данное подсемейство FGF регулирует различные физиологические процессы, нетипичные для классических FGF, а именно, энергетический гомеостаз и гомеостаз желчных кислот, метаболизм глюкозы и липидов и гомеостаз фосфора, а также витамина D. Кроме того, в отличие от классических FGF, данное подсемейство действует эндокринным образом (Moore, D.D. (2007) Science 316, 1436-8). Сообщалось, что FGF21 предпочтительно экспрессируется в печени (Nishimura et al. (2000) Biochimica et Biophysica Acta, 1492:203-206; публикация патента WO01/36640 и публикация патента WO01/18172) и описан в качестве средства лечения ишемической сосудистой болезни, при заживлении ран и при лечении заболеваний, ассоциированных с потерей функции клеток легких, бронхов и альвеол, а также многочисленными другими нарушениями.
FGF21 был идентифицирован в качестве эффективного метаболического регулятора. Системное введение FGF21 грызунам и макакам-резусам с алиментарным или генетическим ожирением и диабетом приводит к выраженным антигипергликемическим и обеспечивающим снижение уровня триглицеридов эффектам и снижению веса тела (Coskun,T, et al. (2008) Endocrinology 149:6018-6027; Kharitonenkov, A. et al. (2005) Journal of Clinical Investigation 115:1627-1635; Kharitonenkov, A., et al. (2007) Endocrinology 148:774-781; Xu, J, et al. (2009) Diabetes 58:250-259). FGF21 представляет собой полипептид из 209 аминокислот, содержащий лидерную последовательность из 28 аминокислот. FGF21 человека характеризуется приблизительно 79% аминокислотной идентичностью по отношению к FGF21 мыши и приблизительно 80% аминокислотной идентичностью по отношению к FGF21 крысы.
У млекопитающих FGF опосредуют свое действие с помощью совокупности из четырех рецепторов FGF, FGFR1-4, которые, в свою очередь, экспрессируются в многочисленных сплайс-вариантах. Каждый рецептор FGF содержит внутриклеточный тирозинкиназный домен, который активируется при связывании лиганда, приводя к нисходящим сигнальным путям, включающим MAPK (Erk1/2), RAF1, AKT1 и STAT. (Kharitonenkov, A. et al. (2008) BioDrugs 22:37-44). В нескольких отчетах сделано предположение, что "c"-репортерные сплайс-варианты FGFR1-3 характеризуются специфической аффинностью по отношению к β-клото и могли выступать в качестве эндогенных рецепторов FGF21 (Kurosu et al., 2007 J. Biol. Chem. 282:26687-26695); Ogawa et al., 2007 Proc. Natl. Acad. Sci. USA 104:7432-7437; Kharitonenkov et al., 2008 J. Cell Physiol. 215, 1-7). В клетках 3T3-L1 и белой жировой ткани FGFR1 представляет собой, по всей видимости, наиболее многочисленный рецептор, и, таким образом, наиболее вероятно, что основными функциональными рецепторами FGF21 в этой ткани являются комплексы β-клото-FGFR1c.
Несмотря на то, что FGF21 активирует рецепторы FGF и молекулы нисходящего сигнального пути, в том числе FRS2a и киназу, регулируемую внеклеточными сигналами (ERK), непосредственное взаимодействие FGFR и FGF21 не было выявлено. Кроме того, различные клетки, отличные от адипоцитов, не отвечают на FGF21, даже несмотря на то, что они экспрессируют многочисленные изоформы FGFR. Все эти данные свидетельствуют о том, что кофактор должен опосредовать передачу сигнала FGF21 с помощью FGFR. В исследованиях идентифицирован бета-клото (β-клото), который в значительной степени экспрессируется в печени, адипоцитах и в поджелудочной железе, в качестве детерминанты клеточного ответа на FGF21 (Kurosu, H. et al. (2007) J Biol Chem 282, 26687-95). Комплекс β-клото-FGFR, но не FGFR отдельно, связывается с FGF21 in vitro (Kharitonenkov, A., et al. (2008) J Cell Physiol 215, 1-7). FGF21 связывается с β-клото в комплексе с FGFR1c, 2c или 3c; но не с β-клото в комплексе с FGFR4 (Owen et al., 2015 Trends in Endocrinology 26: 22-29). Аналогичный механизм был идентифицирован в системе FGF23-клото-FGFR (Urakawa, I. et al. (2006) Nature 444, 770-4).
Биоактивность FGF21 впервые была идентифицирована в анализе захвата глюкозы адипоцитами 3T3-L1 у мышей (Kharitonenkov, A. et al. (2005) J Clin Invest 115, 1627-35). Впоследствии было показано, что FGF21 индуцирует инсулиннезависимый захват глюкозы и экспрессию GLUT1. Также было показано, что FGF21 обеспечивает снижение тяжести гипергликемии в ряде моделей сахарного диабета у грызунов. Помимо этого, было обнаружено, что трансгенные мыши, сверхэкспрессирующие FGF21, являются невосприимчивыми к алиментарным метаболическим нарушениям, включая сниженный вес тела и массу жировой ткани, а также повышение чувствительности к инсулину (Badman, M.K. et al. (2007) Cell Metab 5, 426-37). Введение FGF21 отличным от человека приматам (NHP), страдающим диабетом, вызывало снижение уровней глюкозы, триглицеридов, инсулина и глюкагона в плазме крови натощак и приводило к значительным улучшениям липопротеиновых профилей, в том числе около 80% повышению уровня холестерина HDL (Kharitonenkov, A. et al. (2007) Endocrinology 148, 774-81). Важно, что гипогликемия не наблюдалась ни в какой точке во время данного исследования с участием NHP. В других исследованиях FGF21 идентифицирован в качестве важного эндокринного гормона, который способствует контролю адаптации к состоянию голодания. Это представляет отсутствующую ранее связь по нисходящей от PPARα, с помощью которой печень устанавливает связь с оставшейся частью организма в регуляции биологических процессов энергетического гомеостаза. Объединенные наблюдения того, что FGF21 обеспечивает регуляцию жировой ткани (липолиз), печени (окисление жирных кислот и кетогенез) и головного мозга (неактивность), определяют его в качестве основного эндокринного регулятора ответа на голодание (Kharitonenkov, A. & Shanafelt, A.B. (2008) BioDrugs 22, 37-44).
Проблема применения FGF21 непосредственно в качестве биотерапевтического препарата заключается в том, что его период полужизни является очень коротким. У мышей период полужизни FGF21 человека составляет от 0,5 до 1 часа, а у яванских макаков период полужизни составляет от 2 до 3 часов. Кроме того, при применении FGF21 дикого типа в фармацевтических составах или препаратах в отношении его стабильности отрицательно влияют консерванты, например, м-крезол.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к антителам-миметикам FGF21, т. е. моноклональным антителам, которые связываются с бета-клото (β-клото) и активируют рецепторный комплекс фактора роста фибробластов 21 человека (далее в данном документе иногда обозначаемого как "FGF21") и опосредованную FGF21 передачу сигнала (например, зависимую от рецептора FGF21 передачу сигнала), их антигенсвязывающим фрагментам и предусматривающим их фармацевтическим композициям и способам лечения.
В конкретных аспектах антигенсвязывающие фрагменты (антитела-миметики FGF21, связывающие β-клото) по настоящему изобретению могут представлять собой молекулы с FGF21-подобной активностью и селективностью, но с добавленными терапевтически необходимыми характеристиками, такими как стабильность белков, низкая иммуногенность, легкость получения и необходимый период полужизни in vivo.
Моноклональные антитела-миметики FGF21 по настоящему изобретению, их антигенсвязывающие фрагменты и содержащие их фармацевтические композиции пригодны для лечения FGF21-ассоциированных нарушений, таких как ожирение, сахарный диабет 2 типа, сахарный диабет 1 типа, панкреатит, дислипидемия, неалкогольный стеатогепатит (NASH), инсулинорезистентность, гиперинсулинемия, нарушение толерантности к глюкозе, гипергликемия, метаболический синдром, гипертензия, сердечно-сосудистое заболевание, атеросклероз, периферическая артериальная болезнь, инсульт, сердечная недостаточность, ишемическая болезнь сердца, заболевание почек, диабетические осложнения, нейропатия, гастропарез и другие метаболические нарушения, а также в снижении смертности и инвалидности критически больных пациентов.
В конкретных аспектах выделенные антитела-миметики FGF21 или их антигенсвязывающие фрагменты, описанные в данном документе, связывают β-клото с равновесной константой диссоциации (KD), составляющей менее чем или равной 500 пM или 400 пM, например, определенной с помощью анализа связывания BIACORE™, а также могут активировать рецепторный комплекс FGFR1c_β-клото яванского макака с EC50, составляющей менее чем или равной 50 нМ, например, измеренной с помощью клеточных анализов фосфорилирования (pERK или фосфо-ERK) киназы, регулируемой внеклеточными сигналами (ERK). В конкретных аспектах выделенные антитела-миметики FGF21 или их антигенсвязывающие фрагменты, описанные в данном документе, связывают β-клото с равновесной константой диссоциации (KD), составляющей менее чем или равной 300 пM или 400 пM, например, определенной с помощью анализа связывания BIACORE™, а также могут активировать рецепторный комплекс FGFR1c_β-клото яванского макака с EC50, составляющей менее чем или равной 50 нМ, например, измеряемой с помощью клеточных анализов pERK.
В конкретных аспектах выделенные антитела-миметики FGF21 или антигенсвязывающие фрагменты, описанные в данном документе, связывают β-клото с равновесной константой диссоциации (KD), составляющей менее чем или равной 100 пM или 50 пM. Например, выделенные антитела или антигенсвязывающие фрагменты, описанные в данном документе, могут связываться с β-клото человека с KD, составляющей менее чем или равной 100 пM, составляющей менее чем или равной 50 пM, составляющей менее чем или равной 45 пM, составляющей менее чем или равной 40 пM, составляющей менее чем или равной 35 пM, составляющей менее чем или равной 25 пM или составляющей менее чем или равной 15 пM. Более конкретно, выделенные антитела или антигенсвязывающие фрагменты, описанные в данном документе, также могут связываться с β-клото человека с KD, составляющей менее чем или равной 10 пM, измеренной с помощью связывающего анализа BIACORE™ или анализа титрования при равновесии в растворе (SET); а также могут активировать рецепторный комплекс FGFR1c_β-клото яванского макака с EC50, составляющей менее чем или равной 50 нМ, например, измеренной с помощью клеточных анализов pERK.
Настоящее изобретение относится к выделенному антителу или его антигенсвязывающим фрагментам, которые связываются с β-клото человека и яванского макака. Настоящее изобретение также относится к выделенному антителу или его антигенсвязывающим фрагментам, которые связываются с β-клото и активируют рецепторный комплекс FGF21 и опосредованную FGF21 передачу сигнала (например, зависимую от рецептора FGF21 передачу сигнала). В конкретных аспектах выделенное антитело или его антигенсвязывающий фрагмент, описанные в данном документе, не активируют рецепторные комплексы FGFR2c_β-клото, FGFR3c_β-клото или FGFR4_β-клото человека.
Настоящее изобретение также относится к выделенному антителу или его антигенсвязывающим фрагментам, которые связывают β-клото и дополнительно конкурируют за связывание с антителом, описанным в таблице 1, например, антителом NOV005 или NOV006. Настоящее изобретение также дополнительно относится к выделенному антителу или его антигенсвязывающим фрагментам, которые связывают тот же самый эпитоп, что и антитело, описанное в таблице 1, например, антитело NOV005 или NOV006.
Описанное в данном документе "конкурирование" между антителами и/или их антигенсвязывающими фрагментами означает, что оба антитела (или их антигенсвязывающие фрагменты) связываются с тем же самым эпитопом β-клото (например, как определено с помощью анализа конкурентного связывания, с помощью любых способов, известных специалистам в данной области техники). Антитело или его антигенсвязывающий фрагмент также "конкурирует" с антителом к β-клото или антигенсвязывающим фрагментом по настоящему изобретению (например, NOV005 или NOV006), если указанное конкурирующее антитело или его антигенсвязывающий фрагмент связываются с тем же самым эпитопом β-клото или перекрывающимся эпитопом β-клото, что и антитело или антигенсвязывающий фрагмент по настоящему изобретению. При использовании в данном документе конкурирующее антитело или его антигенсвязывающий фрагмент также могут включать таковые, которые (i) стерически блокируют антитело или антигенсвязывающий фрагмент по настоящему изобретению от связывания со своей мишенью (например, если указанное конкурирующее антитело связывается с расположенным рядом неперекрывающимся эпитопом β-клото и/или эпитопом β-клото и физически препятствует связыванию антитела или его антигенсвязывающего фрагмента со своей мишенью); и/или (ii) связываются с другим неперекрывающимся эпитопом β-клото и индуцируют конформационное изменение белка β-клото, в результате чего указанный белок больше не может связываться антителом к β-клото или антигенсвязывающим фрагментом по настоящему изобретению таким образом, как это происходило бы при отсутствии указанного конформационного изменения.
Аффинность связывания выделенных антител и антигенсвязывающих фрагментов, описанных в данном документе, может быть определена с помощью титрования при равновесии в растворе (SET). Способы SET известны в данной области техники и описаны более подробно ниже. В качестве альтернативы, аффинность связывания выделенных антител или фрагментов, описанных в данном документе, может быть определена с помощью анализа Biacore. Способы кинетических анализов Biacore известны в данной области техники и описаны более подробно ниже.
Выделенные антитела-миметики FGF21 или их антигенсвязывающие фрагменты можно применять для повышения активации рецепторного комплекса FGF21 и, таким образом, сигнального пути с участием FGF21. В конкретном аспекте выделенные антитела-миметики FGF21 или их антигенсвязывающие фрагменты можно применять для повышения активации рецепторного комплекса FGF21 и, тем самым, сигнального пути с участием FGF21 на по меньшей мере приблизительно 15%, 20%, 25%, 30%, 35%, 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, или 95%.
Выделенные антитела-миметики FGF21 или их антигенсвязывающие фрагменты, описанные в данном документе, могут представлять собой моноклональные антитела, человеческие или гуманизированные антитела, химерные антитела, Fab-фрагменты, Fv-фрагменты, F(ab')2-фрагменты или scFv-фрагменты, и/или изотипы IgG (например, IgG1, IgG2 или IgG4).
Выделенные антитела-миметики FGF21 или их антигенсвязывающие фрагменты, описанные в данном документе, также могут содержать каркасную область, в которой аминокислота была замещена на каркасную область антитела из соответствующих последовательностей зародышевых линий VH или VL.
Другой аспект настоящего изобретения включает выделенное антитело или его антигенсвязывающие фрагменты, имеющие полноразмерные последовательности тяжелой и легкой цепей Fab, описанных в таблице 1, например, антитела NOV005 или NOV006. Более конкретно, выделенное антитело или его антигенсвязывающие фрагменты могут иметь последовательности тяжелой и легкой цепей Fab NOV005 или NOV006.
Дополнительный аспект настоящего изобретения включает выделенное антитело или его антигенсвязывающие фрагменты, содержащие последовательности вариабельных доменов тяжелой и легкой цепей Fab, описанных в таблице 1, например, NOV005 или NOV006. Более конкретно, выделенное антитело или его антигенсвязывающий фрагмент содержит последовательность вариабельного домена тяжелой и легкой цепей Fab NOV005 или NOV006.
Настоящее изобретение также относится к композициям (например, фармацевтическим композициям), содержащим выделенное антитело или его антигенсвязывающие фрагменты, описанные в данном документе (например, NOV005 или NOV006), а также композициям антител в комбинации с фармацевтически приемлемым носителем. В частности, настоящее изобретение дополнительно включает фармацевтические композиции, содержащие антитело или его антигенсвязывающие фрагменты из таблицы 1, такие как, например, антитело NOV005 или NOV006. Настоящее изобретение также относится к фармацевтическим композициям, содержащим комбинацию из двух или более выделенных антител или их антигенсвязывающих фрагментов из таблицы 1, например, антитела NOV005 или NOV006.
Настоящее изобретение также относится к выделенной молекуле нуклеиновой кислоты, кодирующей вариабельную область тяжелой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 15. В конкретных аспектах молекула нуклеиновой кислоты содержит последовательность, которая характеризуется по меньшей мере 90% идентичностью последовательности по отношению к последовательности, выбранной из группы, состоящей из SEQ ID NO: 16, 36 или 38. В дополнительном аспекте настоящего изобретения молекула нуклеиновой кислоты, предусмотренная в данном документе, содержит последовательность нуклеиновой кислоты под SEQ ID NO: 16, 36 или 38.
Настоящее изобретение также относится к выделенной молекуле нуклеиновой кислоты, кодирующей вариабельную область легкой цепи, имеющую аминокислотную последовательность под SEQ ID NO: 26 или 32. В конкретных аспектах молекула нуклеиновой кислоты содержит последовательность, которая характеризуется по меньшей мере 90% идентичностью последовательности по отношению к последовательности нуклеиновой кислоты под SEQ ID NO: 27, 54, 33 или 40. В дополнительном аспекте настоящего изобретения молекула нуклеиновой кислоты, предусмотренная в данном документе, содержит последовательность нуклеиновой кислоты под SEQ ID NO: 27, 54, 33 или 40.
Настоящее изобретение также относится к вектору, который содержит одну или несколько молекул нуклеиновых кислот, описанных в данном документе. В конкретных аспектах первый вектор кодирует вариабельную область тяжелой цепи или тяжелую цепь антитела, предусмотренного в данном документе, такого как NOV005 или NOV006, второй вектор кодирует вариабельную область легкой цепи или легкую цепь антитела, предусмотренного в данном документе, такого как NOV005 или NOV006. Первый вектор и второй вектор трансдуцируют в клетку-хозяина для коэкспрессии с образованием антител, содержащих такие тяжелые цепи и такие легкие цепи.
Настоящее изобретение также относится к выделенной клетке-хозяину, которая содержит последовательность рекомбинантной ДНК, кодирующую тяжелую цепь антитела, описанного выше, и вторую последовательность рекомбинантной ДНК, кодирующую легкую цепь антитела, описанного выше, при этом указанные последовательности ДНК функционально связаны с промотором и способны экспрессироваться в клетке-хозяине. Предполагается, что антитело может представлять собой человеческое моноклональное антитело. Также предполагается, что клетка-хозяин представляет собой клетку млекопитающего, отличного от человека, например, клетку CHO или HEK293.
Настоящее изобретение также относится к рецептору фактора роста фибробластов 21 (FGF21) и, таким образом, опосредованной FGF21 передаче сигнала (например, зависимой от FGF21 передаче сигнала), при этом способ предусматривает стадию приведения клетки в контакт с эффективным количеством композиции, содержащей выделенное антитело или его антигенсвязывающие фрагменты, описанные в данном документе.
В одном конкретном аспекте предполагается, что клетка представляет собой клетку человека. Дополнительно предполагается, что клетка находится в организме субъекта. В одном варианте осуществления предполагается, что клетка представляет собой адипоцит. В других вариантах осуществления клетка может представлять собой одно или несколько из гепатоцитов, клеток поджелудочной железы, эндотелиальных клеток, мышечных клеток или клеток почечного эпителия. В конкретных аспектах, более того, предполагается, что субъект представляет собой человека.
Настоящее изобретение также относится к способу лечения, контроля, улучшения или предупреждения FGF21-ассоциированного нарушения у субъекта, при этом указанный способ предусматривает стадию введения эффективного количества композиции, содержащей антитело или его антигенсвязывающие фрагменты, описанные в данном документе (например, NOV005 или NOV006). В одном аспекте FGF21-ассоциированное нарушение представляет собой ожирение. В одном аспекте FGF21-ассоциированное нарушение представляет собой диабет 2 типа. Предполагается, что субъект представляет собой человека.
Любое из вышеизложенных выделенных антител или их антигенсвязывающих фрагментов может представлять собой моноклональное антитело или его антигенсвязывающие фрагменты.
Неограничивающие варианты осуществления описаны в следующих аспектах.
1. Выделенное антитело или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото, при этом антитело или его антигенсвязывающий фрагмент содержат:
CDR1 тяжелой цепи (HCDR1), содержащую аминокислотную последовательность под SEQ ID NO: 6, 9, 10 или 12;
CDR2 тяжелой цепи (HCDR2), содержащую аминокислотную последовательность под SEQ ID NO: 7, 11 или 13;
CDR3 тяжелой цепи (HCDR3), содержащую аминокислотную последовательность под SEQ ID NO: 8 или 14;
CDR1 легкой цепи (LCDR1), содержащую аминокислотную последовательность под SEQ ID NO: 19, 31, 22 или 25;
CDR2 легкой цепи (LCDR2), содержащую аминокислотную последовательность под SEQ ID NO: 20 или 23; и
CDR3 легкой цепи (LCDR3), содержащую аминокислотную последовательность под SEQ ID NO: 21 или 24.
2. Выделенное антитело или его антигенсвязывающий фрагмент в соответствии с аспектом 1, при этом антитело или его антигенсвязывающий фрагмент содержат:
CDR1 тяжелой цепи (HCDR1), содержащую аминокислотную последовательность под SEQ ID NO: 6, 9, 10 или 12;
CDR2 тяжелой цепи (HCDR2), содержащую аминокислотную последовательность под SEQ ID NO: 7, 11 или 13;
CDR3 тяжелой цепи (HCDR3), содержащую аминокислотную последовательность под SEQ ID NO: 8
или 14;
CDR1 легкой цепи (LCDR1), содержащую аминокислотную последовательность под SEQ ID NO: 31, 22 или 25;
CDR2 легкой цепи (LCDR2), содержащую аминокислотную последовательность под SEQ ID NO: 20 или 23; и
CDR3 легкой цепи (LCDR3), содержащую аминокислотную последовательность под SEQ ID NO: 21 или 24.
3. Выделенное антитело или его антигенсвязывающий фрагмент в соответствии с аспектом 1, при этом антитело или его антигенсвязывающий фрагмент содержат:
CDR1 тяжелой цепи (HCDR1), содержащую аминокислотную последовательность под SEQ ID NO: 6, 9, 10 или 12;
CDR2 тяжелой цепи (HCDR2), содержащую аминокислотную последовательность под SEQ ID NO: 7, 11 или 13;
CDR3 тяжелой цепи (HCDR3), содержащую аминокислотную последовательность под SEQ ID NO: 8 или 14;
CDR1 легкой цепи (LCDR1), содержащую аминокислотную последовательность под SEQ ID NO: 19, 31, 22 или 25;
CDR2 легкой цепи (LCDR2), содержащую аминокислотную последовательность под SEQ ID NO: 20 или 23; и
CDR3 легкой цепи (LCDR3), содержащую аминокислотную последовательность под SEQ ID NO: 21 или 24.
4. Выделенное антитело или его антигенсвязывающий фрагмент в соответствии с аспектом 1, при этом антитело или его антигенсвязывающий фрагмент содержат:
(i) HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 6, HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 7, HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 8, LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 31, LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 20, и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 21;
(ii) HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 9, HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 7, HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 8, LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 31, LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 20, и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 21;
(iii) HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 10, HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 11, HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 8, LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 22, LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 23, и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 24; или
(iv) HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 12, HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 13, HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 14, LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 25, LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 23, и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 21.
5. Выделенное антитело или его антигенсвязывающий фрагмент в соответствии с аспектом 1, при этом антитело или его антигенсвязывающий фрагмент содержат:
(i) HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 6, HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 7, HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 8, LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 19, LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 20, и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 21;
(ii) HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 9, HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 7, HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 8, LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 19, LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 20, и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 21;
(iii) HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 10, HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 11, HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 8, LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 22, LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 23, и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 24; или
(iv) HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 12, HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 13, HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 14, LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 25, LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 23, и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 21.
6. Выделенное антитело или его антигенсвязывающий фрагмент в соответствии с аспектом 1, при этом антитело или его антигенсвязывающий фрагмент содержат: HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 6, HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 7, HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 8, LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 19 или 31, LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 20, и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 21.
7. Выделенное антитело или его антигенсвязывающий фрагмент в соответствии с аспектом 1, при этом антитело или его антигенсвязывающий фрагмент содержат: HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 9, HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 7, HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 8, LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 19 или 31, LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 20, и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 21.
8. Выделенное антитело или его антигенсвязывающий фрагмент в соответствии с аспектом 1, при этом антитело или его антигенсвязывающий фрагмент содержат: HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 10, HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 11, HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 8, LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 22, LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 23, и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 24.
9. Выделенное антитело или его антигенсвязывающий фрагмент в соответствии с аспектом 1, при этом антитело или его антигенсвязывающий фрагмент содержат: HCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 12, HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 13, HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 14, LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 25, LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 23, и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 21.
10. Антитело или его антигенсвязывающий фрагмент в соответствии с любым из аспектов 1-9, при этом указанные антитело или фрагмент повышают активность β-клото и FGFR1c.
11. Антитело или его антигенсвязывающий фрагмент в соответствии с любым из аспектов 1-9, которые связываются с белком β-клото человека с KD, составляющей менее чем или равной 450 пМ, измеренной с помощью анализа связывания BIACORE™.
12. Выделенное антитело или его антигенсвязывающий фрагмент в соответствии с любым из аспектов 1-9, при этом указанный эпитоп содержит (i) одну или несколько аминокислот из остатков 246-265, 536-550, 834-857 и 959-986 последовательности β-клото (SEQ ID NO:52) или (ii) один, два, три, четыре, пять или более аминокислотных остатков из каждого из следующих отрезков остатков 246-265, 536-550, 834-857 и 959-986 последовательности β-клото (SEQ ID NO:52) или по существу состоит из них.
13. Выделенное антитело или его антигенсвязывающий фрагмент в соответствии с любым из аспектов 1-9, при этом указанный эпитоп содержит (i) одну или несколько аминокислот из остатков 646-670, 696-700 и 646-689 последовательности β-клото (SEQ ID NO:52) или (ii) один, два, три, четыре, пять или более аминокислотных остатков из каждого из следующих отрезков остатков 646-670, 696-700 и 646-689 последовательности β-клото (SEQ ID NO:52) или по существу состоит из них.
14. Выделенное антитело или его антигенсвязывающий фрагмент в соответствии с любым из аспектов 1-13, которые способны активировать рецепторный комплекс FGFR1c-β-клото яванского макака с EC50, составляющей менее чем или равной 50 нМ, измеренной с помощью клеточных анализов pERK.
15. Выделенное антитело или антигенсвязывающий фрагмент в соответствии с любым из аспектов 1-14, при этом указанное антитело или фрагмент не контактируют с остатками 701 (Tyr) или 703 (Arg) β-клото человека (SEQ ID NO: 52).
16. Выделенное антитело или антигенсвязывающий фрагмент в соответствии с любым из аспектов 1-15, при этом антитело или фрагмент содержат вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 15 или аминокислотную последовательность, характеризующуюся по меньшей мере 90% или 95% идентичностью по отношению к ней; и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 26 или 32 или аминокислотную последовательность, характеризующуюся по меньшей мере 90% или 95% идентичностью по отношению к ней.
17. Выделенное антитело или антигенсвязывающий фрагмент в соответствии с любым из аспектов 1-16, при этом антитело или фрагмент содержат VH, содержащую аминокислотную последовательность под SEQ ID NO: 15.
18. Выделенное антитело или антигенсвязывающий фрагмент в соответствии с любым из аспектов 1-17, при этом антитело или фрагмент содержат VL, содержащую аминокислотную последовательность под SEQ ID NO: 26 или 32.
19. Выделенное антитело или антигенсвязывающий фрагмент в соответствии с аспектом 17, при этом антитело или фрагмент содержат (i) VH, содержащую аминокислотную последовательность под SEQ ID NO: 15, и VL, содержащую аминокислотную последовательность под SEQ ID NO: 26, или (ii) VH, содержащую аминокислотную последовательность под SEQ ID NO: 15, и VL, содержащую аминокислотную последовательность под SEQ ID NO: 32.
20. Выделенное антитело или антигенсвязывающий фрагмент в соответствии с любым из аспектов 1-19, при этом антитело содержит (i) тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 17, и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 28, или (ii) тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 17, и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 34.
21. Выделенное антитело или его антигенсвязывающий фрагмент, при этом антитело или фрагмент связываются с тем же эпитопом, что и выделенное антитело или фрагмент в соответствии с любым из аспектов 1-20, где антитело или его антигенсвязывающий фрагмент не содержат (i) CDR согласно комбинированной системе нумерации или CDR согласно Kabat из антитела NOV004, изложенного в таблице 2; и/или (ii) вариабельный домен тяжелой цепи, содержащий аминокислотную последовательность под SEQ ID NO: 43 или 55, и вариабельную область легкой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 47 или 57.
22. Выделенное антитело или его антигенсвязывающий фрагмент, при этом антитело или фрагмент конкурируют за связывание с β-клото с выделенным антителом или фрагментом в соответствии с любым из аспектов 1-20, при этом антитело или антигенсвязывающий фрагмент не содержат (i) CDR согласно комбинированной системе нумерации или CDR согласно Kabat из антитела NOV004, изложенного в таблице 2; и/или (ii) вариабельный домен тяжелой цепи, содержащий аминокислотную последовательность под SEQ ID NO: 43 или 55, и вариабельную область легкой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 47 или 57.
23. Выделенное антитело или антигенсвязывающий фрагмент в соответствии с любым из аспектов 1-20, при этом антитело или фрагмент не содержат (i) CDR согласно комбинированной системе нумерации или CDR согласно Kabat из антитела NOV004, изложенного в таблице 2; и/или (ii) вариабельный домен тяжелой цепи, содержащий аминокислотную последовательность под SEQ ID NO: 43 или 55, и вариабельную область легкой цепи, содержащую аминокислотную последовательность под SEQ ID NO: 47 или 57.
24. Фармацевтическая композиция, содержащая антитело или его антигенсвязывающий фрагмент в соответствии с любым из вышеуказанных аспектов и фармацевтически приемлемый носитель.
25. Способ лечения метаболического нарушения, предусматривающий введение субъекту, страдающему метаболическим нарушением, эффективного количества фармацевтической композиции, содержащей антитело или антигенсвязывающий фрагмент в соответствии с любым из аспектов 1-23.
26. Способ в соответствии с аспектом 25, при этом субъект страдает одним или несколькими из ожирения, сахарного диабета 1 типа и 2 типа, панкреатита, дислипидемии, неалкогольного стеатогепатита (NASH), инсулинорезистентности, гиперинсулинемии, нарушения толерантности к глюкозе, гипергликемии, гипертриглицеридемии и метаболического синдрома.
27. Способ в соответствии с аспектом 25, при этом субъект страдает одним или несколькими из ожирения, диабета и дислипидемии.
28. Способ лечения сердечно-сосудистого нарушения, предусматривающий введение субъекту, страдающему сердечно-сосудистым нарушением, эффективного количества фармацевтической композиции, содержащей антитело или фрагмент в соответствии с любым из предыдущих аспектов.
29. Способ в соответствии с аспектом 28, при этом субъект страдает одним или несколькими из атеросклероза, периферической артериальной болезни, инсульта, сердечной недостаточности и ишемической болезни сердца.
30. Антитело или его антигенсвязывающий фрагмент в соответствии с любым из аспектов 1-23 для применения в качестве лекарственного препарата.
31. Способ снижения веса тела, предусматривающий введение субъекту, нуждающемуся в этом, эффективного количества фармацевтической композиции, содержащей антитело или антигенсвязывающий фрагмент в соответствии с любым из аспектов 1-23.
32. Способ уменьшения аппетита или потребления пищи, предусматривающий введение субъекту, нуждающемуся в этом, эффективного количества фармацевтической композиции, содержащей антитело или антигенсвязывающий фрагмент в соответствии с любым из аспектов 1-23.
33. Способ уменьшения концентраций триглицеридов (TG) в плазме крови или концентраций общего холестерина в плазме крови (ТС) у субъекта, предусматривающий введение субъекту, нуждающемуся в этом, эффективного количества фармацевтической композиции, содержащей антитело или антигенсвязывающий фрагмент в соответствии с любым из аспектов 1-23.
34. Способ в соответствии с аспектами 31, 32 или 33, при этом субъект страдает метаболическим нарушением.
35. Способ в соответствии с аспектом 34, при этом субъект страдает одним или несколькими из следующего: ожирение, сахарный диабет 1 типа и 2 типа, панкреатит, дислипидемия, неалкогольный стеатогепатит (NASH), инсулинорезистентность, гиперинсулинемия, нарушение толерантности к глюкозе, гипергликемия и метаболический синдром.
36. Нуклеиновая кислота, кодирующая одно или несколько антител в соответствии с любым из предыдущих аспектов или VL и/или VH любого из антител.
37. Нуклеиновая кислота, содержащая последовательность, характеризующуюся по меньшей мере 90% идентичностью по отношению к последовательностям, изложенным в таблице 1.
38. Нуклеиновая кислота, содержащая последовательность, характеризующуюся по меньшей мере 95% идентичностью по отношению к последовательностям, изложенным в таблице 1.
39. Нуклеиновая кислота, содержащая последовательность, изложенную в таблице 1.
40. Вектор, содержащий нуклеиновую кислоту в соответствии с аспектами 36, 37, 38 или 39.
41. Клетка-хозяин, содержащая вектор в соответствии с аспектом 40.
42. Фармацевтическая композиция, содержащая антитело или антигенсвязывающий фрагмент в соответствии с любым из аспектов 1-23 для применения в лечении метаболического нарушения.
43. Способ получения антитела или его антигенсвязывающего фрагмента, которые связывают β-клото, предусматривающий стадию культивирования клетки-хозяина в соответствии с аспектом 41 в условиях, подходящих для экспрессии антитела или его фрагмента.
44. Фармацевтическая композиция в соответствии с аспектом 42, при этом метаболическое нарушение представляет собой ожирение, диабет, гипертриглицеридемию или дислипидемию.
45. Фармацевтическая композиция, содержащая антитело или антигенсвязывающий фрагмент в соответствии с любым из аспектов 1-23 для применения в лечении сердечно-сосудистого нарушения.
46. Фармацевтическая композиция, содержащая антитело или антигенсвязывающий фрагмент в соответствии с любым из аспектов 1-23 для применения в способе снижения веса тела, способе уменьшения аппетита или потребления пищи, способе уменьшения концентраций триглицеридов (TG) в плазме крови или концентраций общего холестерина (TC) в плазме крови у субъекта.
47. Применение антитела или его антигенсвязывающего фрагмента в соответствии с любым из аспектов 1-23 для получения лекарственного препарата, предназначенного для лечения метаболического нарушения, для лечения сердечно-сосудистого нарушения, для снижения веса тела, для уменьшения аппетита или потребления пищи, для уменьшения концентраций TG в плазме крови или концентраций TC в плазме крови у субъекта.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фигура 1. Активация pERK в клетках FGFR1c_β-клото_HEK293 человека (фиг. 1A) и яванского макака (фиг. 1B) с помощью NOV004, NOV005 и NOV006. Данные по активации pERK свидетельствуют о том, что (i) NOV004 обеспечивал активацию рецепторного комплекса FGFR1c_β-клото человека и яванского макака с EC50, составляющей приблизительно 3 нМ и 20 нМ соответственно; (ii) NOV005 обеспечивал активацию рецепторного комплекса FGFR1c_β-клото человека и яванского макака с EC50, составляющей приблизительно 3 нМ и 16 нМ соответственно; и (iii) NOV006 обеспечивал активацию рецепторного комплекса FGFR1c_β-клото человека и яванского макака с EC50, составляющей приблизительно 4 нМ и 18 нМ соответственно.
Фигура 2. Получение профилей NOV004, NOV005 и NOV006 в отношении активации pERK в клетках HEK293 FGFR2c_β-клото (фиг. 2A), FGFR3c_β-клото (фиг. 2B) и FGFR4_β-клото (фиг. 2C). FGF21 использовали в качестве положительного контроля в отношении активации FGFR2c_β-клото или FGFR3c_β-клото. FGF19 использовали в качестве положительного контроля в отношении активации FGFR4_β-клото.
Фигура 3. Получение профилей NOV004, NOV005 и NOV006 в отношении активности FGF23 с помощью клеток HEK293, трансфицированных α-клото, Egr1-люциферазой и люциферазой Renilla. FGF23 использовали в качестве положительного контроля.
Фигура 4. Активность NOV005 и NOV006 при конкурентном связывании по сравнению с NOV004 в случае β-клото человека. Биосенсорную систему Forte Bio® применяли для определения активности при конкурентном связывании с β-клото человека. На стадии 1 рекомбинантный β-клото человека загружали на сенсор, затем выполняли загрузку NOV004 до насыщения на стадии 2. Потом загружали NOV005 или NOV006 и выявляли активность относительно NOV004 при конкурентном связывании. Отсутствие второго сигнала связывания свидетельствует о том, что антитела конкурируют за связывание с β-клото человека. Неродственное антитело использовали в качестве отрицательного контроля, а NOV004 использовали в качестве положительного контроля для самоконкуренции.
Фигура 5. Профили концентрация-время NOV004, NOV005 и NOV006 после IV инъекции у крыс. Животные характеризовались средним значением Cmax примерно 200 мкг/мл через 1 ч. после IV введения NOV004 (фиг. 5A), NOV005 (фиг. 5B) или NOV006 (фиг. 5C), при этом все три антитела характеризовались сопоставимыми PK-профилями.
Фигура 6A. Через одну неделю две подкожные дозы 1 мг/кг NOV005 (n=5 животных) или среды-носителя (n=3 животных) вводили нормогликемическим самцам яванских макаков, страдающим ожирением (дни введения дозы обозначены стрелками). Данные о потреблении пищи в стандартном корме нормализовали в виде процента исходного уровня с групповым средним ± SEM. Обезьяны потребляли фрукты, овощи и арахис в качестве лакомств в течение всего исследования.
Фигура 6B. Через одну неделю две подкожные дозы 1 мг/кг NOV005 (n=5 животных) или среды-носителя (n=3 животных) вводили нормогликемическим самцам яванских макаков, страдающим ожирением (дни введения дозы обозначены стрелками). Вес тела исходного уровня в случае животных, обработанных NOV005 и средой-носителем, составлял 11,3+1,2 и 11,4+1,3 кг соответственно. Данные о весе тела нормализовали в виде процента от исходного уровня с (A) групповым средним ± SEM и (B) показанными данными отдельных животных.
ПОДРОБНОЕ ОПИСАНИЕ
Настоящее изобретение основано отчасти на обнаружении молекул антител, которые специфически связываются с β-клото и приводят к активации рецепторов FGF, например, FGFR1c, а также активации опосредованной FGF21 передачи сигнала (например, зависимой от FGF21 передачи сигнала). Настоящее изобретение относится как к полноразмерному формату антител IgG, так и к их антигенсвязывающим фрагментам, таким как Fab-фрагменты (например, антитела NOV005 или NOV006).
Соответственно, в настоящем изобретении предусмотрены антитела, которые специфически связываются с β-клото (напрмер, β-клото человека и яванского макака), фармацевтическим композициям, способам получения и способам применения таких антител и композиций.
ТЕРМИНОЛОГИЯ
Если не указано иное, все технические и научные термины, используемые в данном документе, имеют то же значение, которое обычно понимают специалисты в данной области техники, к которой относится настоящее изобретение.
Используемый в данном документе термин "FGF21" относится к члену семейства белков фактора роста фибробластов (FGF). Иллюстративная аминокислотная последовательность FGF21 (номер доступа в GenBank NP_061986.1) приведена под SEQ ID NO: 1; соответствующая ей полинуклеотидная последовательность приведена под SEQ ID NO:2 (номер эталонной последовательности в NCBI NM_019113.2).
Используемый в данном документе термин "рецептор FGF21" относится к рецептору FGF21 (Kharitonenkov,A, et al. (2008) Journal of Cellular Physiology 215:1-7; Kurosu,H, et al. (2007) JBC 282:26687-26695; Ogawa, Y, et al. (2007) PNAS 104:7432-7437).
Термин "полипептид FGF21" относится к встречающемуся в природе полипептиду, экспрессирующемуся у людей. Для целей настоящего изобретения термин "полипептид FGF21" можно применять взаимозаменяемо для обозначения любого полноразмерного полипептида FGF21, например, SEQ ID NO:1, который состоит из 209 аминокислотных остатков и который кодируется нуклеотидной последовательностью под SEQ ID NO:2; любой зрелой формы указанного полипептида, которая состоит из 181 аминокислотного остатка, и в которой 28 аминокислотных остатков на аминоконце полноразмерного полипептида FGF21 (т. е. которые составляют сигнальный пептид) были удалены, и их вариантов.
Термин "антитело", используемый в данном документе, означает полное антитело и любой его антигенсвязывающий фрагмент (т. е. "антигенсвязывающую часть") или одну цепь. Полное антитело представляет собой гликопротеин, содержащий по меньшей мере две тяжелые (H) цепи и две легкие (L) цепи, соединенные между собой посредством дисульфидных связей. Каждая тяжелая цепь состоит из вариабельной области тяжелой цепи (сокращено в данном документе как VH) и константной области тяжелой цепи. Константная область тяжелой цепи состоит из трех доменов, CH1, CH2 и CH3. Каждая легкая цепь состоит из вариабельной области легкой цепи (сокращено в данном документе как VL) и константной области легкой цепи. Константная область легкой цепи состоит из одного домена, CL. VH- и VL-области могут быть дополнительно подразделены на гипервариабельные области, называемые определяющими комплементарность областями (CDR), которые чередуются с более консервативными областями, называемыми каркасными областями (FR). Каждая VH и VL состоит из трех CDR и четырех FR, расположенных от аминоконца до карбоксиконца в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4. Вариабельные области тяжелых и легких цепей содержат связывающий домен, который взаимодействует с антигеном. Константные области антител могут опосредовать связывание иммуноглобулина с тканями или факторами хозяина, которые включают различные клетки иммунной системы (например, эффекторные клетки) и первый компонент (Clq) классической системы комплемента.
Термин "антигенсвязывающая часть" или "антигенсвязывающий фрагмент" антитела, используемый в данном документе, относится к одному или нескольким фрагментам интактного антитела, которые сохраняют способность специфически связываться с заданным антигеном (например, β-клото). Антигенсвязывающие функции антитела могут выполняться фрагментами интактного антитела. Примеры связывающих фрагментов, охватываемых термином "антигенсвязывающая часть" или "антигенсвязывающий фрагмент" антитела, включают в себя Fab-фрагмент, моновалентный фрагмент, состоящий из доменов VL, VH, CL и CH1; F(ab)2-фрагмент, бивалентный фрагмент, содержащий два Fab-фрагмента, связанных посредством дисульфидного мостика в шарнирной области; Fd-фрагмент, состоящий из доменов VH и CH1; Fv-фрагмент, состоящий из доменов VL и VH одного плеча антитела; фрагмент однодоменного антитела (dAb) (Ward et al., 1989 Nature 341:544-546), который состоит из домена VH или домена VL; и выделенную определяющую комплементарность область (CDR).
Кроме того, хотя два домена Fv-фрагмента, VL и VH, кодируются отдельными генами, они могут быть объединены с применением рекомбинантных способов с помощью искусственного пептидного линкера, который позволяет преобразовать их в единую белковую цепь, в которой области VL и VH спариваются с образованием моновалентных молекул (известных как одноцепочечные Fv (scFv); см., например, Bird et al., 1988 Science 242:423-426; и Huston et al., 1988 Proc. Natl. Acad. Sci. 85:5879-5883). Такие одноцепочечные антитела включают в себя одну или несколько антигенсвязывающих частей или фрагментов антитела. Эти фрагменты антител получают с помощью традиционных методик, известных специалистам в данной области техники, и фрагменты подвергают скринингу на пригодность таким же способом, как и интактные антитела.
Антигенсвязывающие фрагменты также могут быть включены в однодоменные антитела, макситела, минитела, интратела, диатела, триатела, тетратела, v-NAR и бис-scFv (см., например, Hollinger and Hudson, 2005, Nature Biotechnology, 23, 9, 1126-1136). Антигенсвязывающие части антител могут быть привиты на остовы на основе полипептидов, таких как фибронектин типа III (Fn3) (см. патент США № 6703199, в котором описаны монотела на основе полипептида фибронектина).
Антигенсвязывающие фрагменты антител могут быть встроены в одноцепочечные молекулы, содержащие пару тандемных Fv-сегментов (VH-CH1-VH-CH1), которые вместе с комплементарными полипептидами легкой цепи образуют пару антиген-связывающих областей (Zapata et al. (1995) Protein Eng. 8(10):1057-1062; и патент США. № 5641870).
Используемый в данном документе термин "аффинность" относится к силе взаимодействия между антителом и антигеном в отдельных антигенных сайтах. В пределах каждого антигенного сайта вариабельная область "плеча" антитела взаимодействует с антигеном посредством слабых нековалентных сил во многочисленных сайтах; чем больше взаимодействий, тем сильнее аффинность. Используемый в данном документе термин "высокая аффинность" в отношении антитела или его антигенсвязывающих фрагментов (например, Fab-фрагмента), как правило, относится к антителу или антигенсвязывающему фрагменту, имеющим KD 10-9M или меньше.
Термин "аминокислота" относится к встречающимся в природе и синтетическим аминокислотам, а также к аналогам аминокислот и миметикам аминокислот, которые функционируют подобно встречающимся в природе аминокислотам. Встречающиеся в природе аминокислоты представляют собой аминокислоты, закодированные в генетическом коде, а также такие аминокислоты, которые были впоследствии модифицированы, например, гидроксипролин, γ-карбоксиглутамат и O-фосфосерин. Аналоги аминокислот относятся к соединениям, которые имеют такую же основную химическую структуру, что и встречающаяся в природе аминокислота, т. е. альфа-углерод, который связан с водородом, карбокисльной группой, аминогруппой и R-группой, например, гомосерин, норлейцин, метионинсульфоксид, метионинметилсульфоний. Такие аналоги имеют модифицированные R-группы (например, норлейцин) или модифицированные пептидные остовы, но сохраняют такую же основную химическую структуру, что и встречающаяся в природе аминокислота. Миметики аминокислот относятся к химическим соединениям, которые имеют структуру, отличающуюся от общей химической структуры аминокислоты, но которые функционируют подобно встречающейся в природе аминокислоте.
Используемый в данном документе термин "специфичность связывания" относится к способности отдельного антигенсвязывающего активного центра антитела реагировать только с одной антигенной детерминантой.
Фраза "специфически (или селективно) связывается" с антителом (например, антителом, связывающим β-клото) относится к реакции связывания, которая определяется наличием узнаваемого антигена (например, β-клото человека или яванского макака) в гетерогенной популяции белков и других биологических материалов. Фразы "антитело, распознающее антиген" и "антитело, специфичное в отношении антигена" используются в данном документе взаимозаменяемо с термином "антитело, которое специфически связывается с антигеном".
Термин "опосредованный FGF21" или подобный относится к тому факту, что рецептор FGF21 и/или антитела по настоящему изобретению опосредуют клеточный ответ и сигнальный путь с участием FGF21 при связывании с β-клото, тем самым активируя ряд физиологических эффектов, в том числе без ограничения снижение одного или нескольких из следующего: уровня триглицеридов в плазме крови, уровня инсулина в плазме крови, уровня глюкозы в плазме крови, потребления пищи и веса тела.
"FGF21-ассоциированное нарушение", "FGF21-ассоциированное состояние", "заболевание или состояние, ассоциированное с FGF21" или аналогичные термины, используемые в данном документе, относятся к любому количеству состояний или заболеваний, в отношении которых осуществляют предупреждение, диагностику и/или лечение с помощью активации сигнального пути с участием FGF21 (например, с помощью активации передачи сигнала с участием рецептора FGF21). Они могут включать в себя состояния, заболевания или нарушения, характеризующиеся аберрантной передачей сигнала с участием FGF21 (например, аберрантной активацией опосредованной FGF21 передачи сигнала и/или передачи сигнала с участием рецептора FGF21). Эти состояния включают в себя без ограничения метаболические, эндокринные и сердечно-сосудистые нарушения, такие как ожирение, сахарный диабет 1 типа и 2 типа, панкреатит, дислипидемия, неалкогольная жировая болезнь печени (NAFLD), неалкогольный стеатогепатит (NASH), инсулинорезистентность, гиперинсулинемия, нарушение толерантности к глюкозе, гипергликемия, метаболический синдром, острый инфаркт миокарда, гипертензия, сердечно-сосудистое заболевание, атеросклероз, периферическая артериальная болезнь, инсульт, сердечная недостаточность, ишемическая болезнь сердца, заболевание почек, диабетические осложнения, нейропатия, гастропарез, нарушения, ассоциированные с тяжелыми инактивирующими мутациями инсулинового рецептора, и другие метаболические нарушения, а также в снижении смертности и инвалидности критически больных пациентов.
"Сахарный диабет 2 типа" представляет собой состояние, характеризующееся избыточным продуцированием глюкозы, несмотря на доступность инсулина, а циркулирующие уровни глюкозы остаются чрезвычайно высокими в результате недостаточного выведения глюкозы.
"Сахарный диабет 1 типа" представляет собой состояние, характеризующееся высокими уровнями глюкозы в крови, вызванными полным отсутствием инсулина. Это происходит, когда иммунная система организма атакует продуцирующие инсулин бета-клетки в поджелудочной железе и разрушает их. Впоследствии поджелудочная железа продуцирует мало или не продуцирует инсулина.
"Панкреатит" представляет собой воспаление поджелудочной железы.
"Дислипидемия" представляет собой нарушение метаболизма липопротеинов, в том числе сверхпродукцию или дефицит липопротеинов. Разновидности дислипидемии могут проявляться повышением концентраций общего холестерина, холестерина липопротеинов низкой плотности (LDL) и триглицеридов, а также снижением концентрации липопротеинов холестерина высокой плотности (HDL) в крови.
"Неалкогольный стеатогепатит (NASH)" представляет собой заболевание печени, не связанное с потреблением алкоголя, характеризующееся жировым изменением гепатоцитов, сопровождающимся внутридольковым воспалением и фиброзом.
"Нарушение толерантности к глюкозе" или нарушенная толерантность к глюкозе (IGT) представляет собой преддиабетическое состояние, которое ассоциировано с повышенным риском сердечно-сосудистой патологии. Преддиабетическое состояние препятствует эффективному перемещению глюкозы в клетки и утилизации ее в качестве эффективного источника топлива у субъекта, приводя к повышенным уровням глюкозы в крови и некоторой степени инсулинорезистентности.
"Гипергликемия" определяется как избыток сахара (глюкозы) в крови.
"Гипогликемия", также называемая низким уровнем сахара в крови, имеет место, если уровень глюкозы в крови падет до слишком низкого уровня, чтобы обеспечивать достаточное количество энергии для путей активности организма человека.
"Гиперинсулинемия" определяется как более превышающий нормальный уровень инсулина в крови.
"Инсулинорезистентность" определяется как состояние, при котором нормальное количество инсулина приводит к субнормальному биологическому ответу.
"Ожирение" с точки зрения субъекта-человека может быть определено как вес тела на более 20 процентов выше идеального веса тела для данной популяции (R. H. Williams, Textbook of Endocrinology, 1974, p. 904-916). Он также может быть определен в виде индекса массы тела (BMI, определенного как вес индивидуума в килограммах, деленный на квадрат его роста в метрах (кг/м2)), составляющего более или равного 30.
"Метаболический синдром" может быть определен как кластер из по меньшей мере трех следующих признаков: абдоминальный жир - у большинства мужчин объем талии 40 дюймов или больше; высокий уровень сахара в крови - по меньшей мере 110 миллиграмм на децилитр (мг/дл) натощак; высокий уровень триглицеридов - по меньшей мере 150 мг/дл в кровотоке; низкий уровень HDL - менее 40 мг/дл; и кровяное давление 130/85 мм рт. ст. или выше.
"Гипертензия", или высокое кровяное давление, которое представляет собой временное или длительное повышение системного артериального кровяного давления до уровня, который, вероятно, индуцирует сердечно-сосудистое повреждение или другие неблагоприятные последствия. Гипертензия была произвольным образом определена как систолическое давление крови выше 140 мм рт. ст. или диастолическое давление крови выше 90 мм. рт. ст.
"Сердечно-сосудистые заболевания" представляют собой заболевания, связанные с сердцем или кровеносными сосудами.
"Периферическая артериальная болезнь" возникает, если в артериях, которые несут кровь к голове, органам или конечностям, образуется бляшка. Со временем бляшка может затвердевать и обеспечивать сужение артерий, что ограничивает поток обогащенной кислородом крови к органам и другим частям организма.
"Атеросклероз" представляет собой сосудистое заболевание, характеризующееся беспорядочным образом распределенными липидными отложениями в интиме артерий большого и среднего размера, вызывая сужение просвета артерий и приводя в конечном итоге к фиброзу и кальцификации. Поражения обычно являются очаговыми и прогрессируют медленно и спорадически. Ограничение кровотока является причиной большинства клинических проявлений, которые варьируются в отношении распространения и тяжести поражений.
"Инсульт" представляет собой любое острое клиническое явление, связанное с нарушением мозгового кровообращения, которое продолжается дольше 24 часов. Инсульт включает в себя необратимое повреждение головного мозга, при этом тип и тяжесть симптомов зависят от расположения и степени поражения ткани головного мозга, кровоток в которой был нарушен.
"Сердечная недостаточность", также называемая застойной сердечной недостаточностью, представляет собой состояние, при котором сердце дольше не может накачивать достаточное количество крови к остальной части тела.
"Ишемическая болезнь сердца", также называемая заболеванием коронарной артерии, представляет собой сужение малых кровеносных сосудов, которые снабжают кровью и кислородом сердце.
"Заболевание почек", или нефропатия, представляет собой любое заболевание почки. Диабетическая нефропатия представляет собой основную причину инвалидности и смертности у людей с сахарным диабетом 1 типа или 2 типа.
"Диабетические осложнения" представляют собой проблемы, вызванные высокими уровнями глюкозы в крови, в отношении других функций организма, например, почек, нервов (нейропатии), стоп (язвы стоп и недостаточный кровоток) и глаз (например, ретинопатии). Диабет также повышает риск заболеваний сердца и нарушений костей и суставов. Другие отдаленные осложнения диабета включают в себя проблемы с кожей, проблемы с пищеварительной системой, половую дисфункцию и проблемы с зубами и деснами.
"Нейропатии" представляют собой любые заболевания, в которых задействованы черепно-мозговые нервы или периферическая или автономная нервная система.
"Гастропарез" представляет собой слабость перистальтики желудка, которая приводит к замедленному высвобождению кишечника.
Критически больные пациенты, охваченные настоящим изобретением, как правило, испытывают неустойчивое гиперметаболическое состояние. Указанное неустойчивое метаболическое состояние связано с изменениями метаболизма субстратов, которые могут приводить к параметрам относительного дефицита некоторых питательных веществ. Как правило, имеет место повышенное окисление как жировой, так и мышечной ткани.
Кроме того, критически больные пациенты представляют собой предпочтительно пациентов, которые испытывают синдром системного воспалительного ответа или респираторный дистресс. Снижение инвалидности означает снижение вероятности того, что у критически больного пациента будут развиваться дополнительные заболевания, состояния или симптомы, или снижение тяжести дополнительных заболеваний, состояний или симптомов. Например, снижение инвалидности может соответствовать снижению частоты бактериемии, или сепсиса, или осложнений, ассоциированных с полиорганной недостаточностью.
Термин "консервативно модифицированный вариант" применяется как к аминокислотным последовательностям, так и к последовательностям нуклеиновой кислоты. Применительно к конкретным последовательностям нуклеиновой кислоты консервативно модифицированные варианты относятся к тем нуклеиновым кислотам, которые кодируют идентичные или по существу идентичные аминокислотные последовательности, или в случае, когда нуклеиновая кислота не кодирует аминокислотную последовательность, они относятся к по существу идентичным последовательностям. Вследствие вырожденности генетического кода любой заданный белок кодируется большим числом функционально идентичных нуклеиновых кислот. Например, все из кодонов GCA, GCC, GCG и GCU кодируют аминокислоту аланин. Таким образом, в каждом положении, где аланин определяется кодоном, кодон может быть изменен на любой из описанных соответствующих кодонов без изменения кодируемого полипептида. Такие вариации нуклеиновой кислоты представляют собой "молчащие вариации", которые представляют собой один вид консервативно модифицированных вариаций. Каждая последовательность нуклеиновой кислоты, которая кодирует полипептид, также описывает в данном документе каждую возможную молчащую вариацию нуклеиновой кислоты. Специалист поймет, что каждый кодон в нуклеиновой кислоте (за исключением AUG, который обычно является единственным кодоном для метионина, и TGG, который обычно является единственным кодоном для триптофана) может быть модифицирован с получением функционально идентичной молекулы. Соответственно, каждая молчащая вариация нуклеиновой кислоты, которая кодирует полипептид, подразумевается в каждой описанной последовательности.
В случае полипептидных последовательностей "консервативно модифицированные варианты" включают отдельные замены, делеции или добавления в полипептидной последовательности, которые приводят в результате к замене аминокислоты на сходную по химическим свойствам аминокислоту. Таблицы консервативных замен, обеспечивающие функционально сходные аминокислоты, являются хорошо известными из уровня техники. Такие консервативно модифицированные варианты дополняют, а не исключают, полиморфные варианты, межвидовые гомологи и аллели по настоящему изобретению. Следующие восемь групп содержат аминокислоты, которые являются консервативными заменами друг для друга: 1) аланин (A), глицин (G); 2) аспарагиновая кислота (D), глутаминовая кислота (E); 3) аспарагин (N), глутамин (Q); 4) аргинин (R), лизин (K); 5) изолейцин (I), лейцин (L), метионин (M), валин (V); 6) фенилаланин (F), тирозин (Y), триптофан (W); 7) серин (S), треонин (T); и 8) цистеин (C), метионин (M) (см., например, Creighton, Proteins (1984)). В некоторых вариантах осуществления термин "консервативные модификации последовательности" используется для обозначения аминокислотных модификаций, которые не оказывают значительного влияния на характеристики связывания у антитела, содержащего аминокислотную последовательность, или не изменяют их.
Термин "эпитоп" означает белковую детерминанту, способную специфически связываться с антителом. Эпитопы обычно состоят из химически активных поверхностных групп молекул, таких как аминокислоты или боковые цепи сахаров, и обычно обладают специфическими характеристиками трехмерной структуры, а также специфическими характеристиками заряда. Конформационные и неконформационные эпитопы отличаются тем, что связывание первого, но не последнего, утрачивается в присутствии денатурирующих растворителей.
Подразумевается, что термин "человеческое антитело", используемый в данном документе, включает в себя антитела, имеющие вариабельные области, в которых как каркасные, так и области CDR получены из последовательностей, происходящих от человека. Кроме того, если антитело содержит константную область, константная область также получена из таких последовательностей человека, например, последовательностей зародышевой линии человека или мутированных вариантов последовательностей зародышевой линии человека. Человеческие антитела по настоящему изобретению могут включать в себя аминокислотные остатки, не кодируемые последовательностями человека (например, мутации, введенные за счет случайного или сайт-специфического мутагенеза in vitro или за счет соматической мутации in vivo).
Термин "человеческое моноклональное антитело" относится к антителам, проявляющим одну специфичность связывания, которые имеют вариабельные области, в которых как каркасные, так и области CDR получены из последовательностей человека. В одном варианте осуществления моноклональные антитела человека продуцируются гибридомой, которая предусматривает B-клетку, полученную из трансгенного животного, отличного от человека, например, трансгенной мыши, с геномом, содержащим трансген тяжелой цепи и трансген легкой цепи человека, слитую с иммортализованной клеткой.
"Гуманизированное" антитело представляет собой антитело, которое сохраняет реактивность антитела, отличного от человеческого, при этом является менее иммуногенным у людей. Этого можно достичь, например, посредством сохранения CDR-областей, отличных от человеческих, и замены остальных частей антитела на соответствующие им части человеческих антител (т. е. константная область, а также каркасные части вариабельной области). См., например, Morrison et al., Proc. Natl. Acad. Sci. USA, 81:6851-6855, 1984; Morrison and Oi, Adv. Immunol., 44:65-92, 1988; Verhoeyen et al., Science, 239:1534-1536, 1988; Padlan, Molec. Immun., 28:489-498, 1991; и Padlan, Molec. Immun., 31:169-217, 1994. Другие примеры технологии конструирования с молекулами человека включают без ограничения технологию Xoma, раскрытую в патенте США 5766886.
Термины "идентичный" или процентная "идентичность" в контексте двух или более нуклеиновых кислот или полипептидных последовательностей относятся к двум или более последовательностям или подпоследовательностям, которые являются одинаковыми. Две последовательности являются "по существу идентичными", если две последовательности имеют указанную процентную долю аминокислотных остатков или нуклеотидов, которые являются одинаковыми (т. е. 60% идентичность, необязательно 65%, 70%, 75%, 80%, 85%, 90%, 95% или 99% идентичность на протяжении указанной области или, если не указано, на протяжении всей последовательности), при сравнении и выравнивании для обеспечения максимального соответствия на протяжении окна сравнения или обозначенной области, как измерено с применением одного из следующих алгоритмов сравнения последовательности или посредством ручного выравнивания и визуального просмотра. Необязательно идентичность существует в области, которая имеет длину по меньшей мере приблизительно 50 нуклеотидов (или 10 аминокислот), или более предпочтительно в области, которая имеет длину 100-500 или 1000 или более нуклеотидов (или 20, 50, 200 или более аминокислот).
Для сравнения последовательностей обычно одна последовательность выступает в качестве эталонной последовательности, с которой сравнивают тестируемые последовательности. При использовании алгоритма сравнения последовательностей тестируемую и эталонную последовательности вводят в компьютер, если необходимо, устанавливают координаты подпоследовательностей, и устанавливают программные параметры алгоритма для анализа последовательности. Можно использовать программные параметры по умолчанию или можно установить альтернативные параметры. Алгоритм сравнения последовательностей затем рассчитывает значения процентной идентичности последовательностей для тестируемых последовательностей по сравнению с эталонной последовательностью, исходя из программных параметров.
"Окно сравнения", как используется в данном документе, включает ссылку на сегмент с любым из ряда смежных положений, выбранных из группы, состоящей из от 20 до 600, обычно от приблизительно 50 до приблизительно 200, чаще от приблизительно 100 до приблизительно 150, в котором последовательность может сравниваться с эталонной последовательностью с таким же числом смежных положений после осуществления оптимального выравнивания двух последовательностей. Способы выравнивания последовательностей для сравнения являются хорошо известными из уровня техники. Оптимальное выравнивание последовательностей для сравнения можно проводить, например, с помощью алгоритма поиска локальной гомологии согласно Smith and Waterman (1970) Adv. Appl. Math. 2:482c, с помощью алгоритма выравнивания гомологичных участков согласно Needleman and Wunsch, J. Mol. Biol. 48:443, 1970, с помощью способа поиска сходства согласно Pearson and Lipman, Proc. Nat'l. Acad. Sci. USA 85:2444, 1988, с помощью компьютерных реализаций этих алгоритмов (GAP, BESTFIT, FASTA и TFASTA в составе пакета программного обеспечения Wisconsin Genetics Software Package, Genetics Computer Group, 575 Science Dr., Мэдисон, Висконсин) или с помощью выравнивания в ручном режиме и визуального осмотра (см., например, Brent et al., Current Protocols in Molecular Biology, John Wiley & Sons, Inc. (Ringbou ed., 2003)).
Два примера алгоритмов, которые подходят для определения процента идентичности последовательностей и сходства последовательностей, представляют собой алгоритмы BLAST и BLAST 2.0, которые описаны в Altschul et al., Nuc. Acids Res. 25:3389-3402, 1977; и Altschul et al., J. Mol. Biol. 215:403-410, 1990, соответственно. Программное обеспечение для осуществления анализов BLAST является общедоступным от Национального центра биотехнологической информации. Этот алгоритм предусматривает вначале идентификацию пар последовательностей с высокими баллами (HSP) посредством идентификации коротких слов длиной W в запрашиваемой последовательности, которые либо совпадают, либо удовлетворяют некоторому положительно оцениваемому пороговому баллу T при выравнивании со словом такой же длины в последовательности из базы данных. T известен под названием пороговый балл соседних слов (Altschul et al., выше). Эти первоначальные совпадения для соседних слов выступают в качестве "затравок" для начала поисков, чтобы найти более длинные HSP, содержащие их. Совпадения для слов продлеваются в обоих направлениях вдоль каждой последовательности настолько, насколько может быть увеличен суммарный балл выравнивания. В случае нуклеотидных последовательностей суммарные баллы рассчитывают с применением параметров M (вознаграждающий балл за пару совпадающих остатков; всегда >0) и N (штрафной балл за несовпадающие остатки; всегда <0). В случае аминокислотных последовательностей оценочную матрицу используют для расчета суммарного балла. Продление совпадений для слов в каждом направлении останавливается, когда суммарный балл выравнивания уменьшается на величину X относительно его максимального достигнутого значения; суммарный балл стремится к нулю или ниже вследствие накопления отрицательно оцениваемых выравниваний одного или нескольких остатков; или достигается конец любой из последовательностей. Параметры W, T и X алгоритма BLAST определяют чувствительность и скорость выравнивания. В программе BLASTN (для нуклеотидных последовательностей) в качестве параметров по умолчанию применяется длина слова (W), составляющая 11, ожидание (E), составляющее 10, M=5, N=-4, и сравнение обеих нитей. В случае аминокислотных последовательностей, в программе BLASTP в качестве параметров по умолчанию используются длина слова 3, и ожидание (E) 10, и оценочная матрица BLOSUM62 (см. Henikoff and Henikoff, Proc. Natl. Acad. Sci. USA 89:10915, 1989), выравнивания (B) 50, ожидание (E) 10, M=5, N=-4 и сравнение обеих цепей.
Алгоритм BLAST также осуществляет статистический анализ сходства между двумя последовательностями (см., например, Karlin and Altschul, Proc. Natl. Acad. Sci. USA 90:5873-5787, 1993). Одной мерой сходства, предусмотренной в алгоритме BLAST, является наименьшая суммарная вероятность (P (N)), которая указывает на вероятность, с которой совпадение между двумя нуклеотидными или аминокислотными последовательностями возникло случайно. Например, нуклеиновая кислота считается схожей с эталонной последовательностью, если наименьшая суммарная вероятность при сравнении тестируемой нуклеиновой кислоты с эталонной нуклеиновой кислотой составляет менее приблизительно 0,2, более предпочтительно менее приблизительно 0,01 и наиболее предпочтительно менее приблизительно 0,001.
Процентную идентичность между двумя аминокислотными последовательностями также можно определить с использованием алгоритма согласно E. Meyers and W. Miller (Comput. Appl. Biosci., 4:11-17, 1988), который был включен в программу ALIGN (версия 2.0) при использовании таблицы веса остатков PAM120, штрафа за продолжение гэпа 12 и штрафа за открытие гэпа 4. Кроме того, процентная идентичность между двумя аминокислотными последовательностями может быть определена с применением алгоритма Нидлмана-Вунша (J. Mol. Biol. 48:444-453, 1970), который был включен в программу GAP в составе пакета программного обеспечения GCG (доступного во всемирной компьютерной сети по адресу gcg.com), с использованием либо матрицы Blossom 62, либо матрицы PAM250, а также штрафа за открытие гэпа, составляющего 16, 14, 12, 10, 8, 6 или 4, и штрафа за продление гэпа, составляющего 1, 2, 3, 4, 5 или 6.
Помимо процентной идентичности последовательности, упомянутой выше, еще одним показателем того, что две последовательности нуклеиновой кислоты или полипептидов являются по существу идентичными, является то, что полипептид, кодируемый первой нуклеиновой кислотой, является иммунологически перекрестно реактивным с антителами, выработка которых индуцирована полипептидом, кодируемым второй нуклеиновой кислотой, как описано ниже. Таким образом, полипептид, как правило, является по существу идентичным второму полипептиду, например, если два пептида отличаются только консервативными заменами. Другим показателем того, что две последовательности нуклеиновой кислоты являются по существу идентичными, является то, что две молекулы или их комплементарные цепи гибридизируются друг с другом в жестких условиях, как описано ниже. Еще одним показателем того, что две последовательности нуклеиновой кислоты являются по существу идентичными, является то, что для амплификации последовательности могут применяться одни и те же праймеры.
Термин "выделенное антитело" относится к антителу, которое по существу не содержит других антител, обладающих отличающейся антигенной специфичностью (например, выделенное антитело, которое специфически связывает β-клото, по существу не содержит других антител, которые специфически связывают другие антигены кроме β-клото). Однако выделенное антитело, которое специфически связывается с β-клото, может характеризоваться перекрестной реактивностью в отношении других антигенов. Более того, выделенное антитело может по существу не содержать другого клеточного материала и/или химических веществ.
Термин "изотип" относится к классу антитела (например, IgM, IgE, IgG, такой как IgG1 или IgG4), который обеспечивается генами константной области тяжелой цепи. Изотип также включает модифицированные варианты одного из этих классов, в которых были осуществлены модификации с целью изменения функции Fc, например, для усиления или снижения эффекторных функций или связывания с Fc-рецепторами.
Предполагается, что термины "kassoc" или "ka", используемые в данном документе, относятся к скорости ассоциации для конкретного взаимодействия антитело-антиген, тогда как термины "kdis" или "kd", используемые в данном документе, как предполагается, относятся к скорости диссоциации для конкретного взаимодействия антитело-антиген. Предполагается, что термин "KD", используемый в данном документе, относится к константе диссоциации, которую получают из отношения kd к ka (т. е. kd/ka) и которая выражена в виде молярной концентрации (M). Значения KD для антител можно определить с помощью способов, хорошо известных из уровня техники. Способы определения KD антитела предусматривают измерение поверхностного плазмонного резонанса с помощью биосенсорной системы, такой как Biacore®, или измерения аффинности в растворе с помощью титрования при равновесии в растворе (SET).
Используемые в данном документе термины "моноклональное антитело" или "композиция на основе моноклональных антител" относятся к препарату из молекул антитела одного молекулярного состава. Композиция на основе моноклонального антитела проявляет одну специфичность и аффинность связывания в отношении конкретного эпитопа.
Термин "нуклеиновая кислота" используется в данном документе взаимозаменяемо с термином "полинуклеотид" и относится к дезоксирибонуклеотидам или рибонуклеотидам и полимерам на их основе в одно- либо в двух-цепочечной форме. Термин охватывает нуклеиновые кислоты, содержащие известные аналоги нуклеотидов или модифицированные остатки или связи в остове, которые являются синтетическими, встречающимися в природе и не встречающимися в природе, которые характеризуются свойствами связывания, подобными эталонной нуклеиновой кислоте, и которые метаболизируются подобно эталонным нуклеотидам. Примеры таких аналогов включают без ограничения фосфоротиоаты, фосфорамидаты, метилфосфонаты, хиральные метилфосфонаты, 2-O-метилрибонуклеотиды, пептидонуклеиновые кислоты (PNA).
Если не указано иное, конкретная последовательность нуклеиновой кислоты также потенциально охватывает ее консервативно модифицированные варианты (например, замены вырожденными кодонами) и комплементарные последовательности, а также непосредственно указанную последовательность. В частности, как подробно описано ниже, замены вырожденными кодонами могут быть достигнуты посредством создания последовательностей, в которых третье положение в одном или нескольких выбранных (или всех) кодонах заменено любым из канонических нуклеозидов и/или дезоксиинозиновыми остатками (Batzer et al., Nucleic Acid Res. 19:5081, 1991; Ohtsuka et al., J. Biol. Chem. 260:2605-2608, 1985; и Rossolini et al., Mol. Cell. Probes 8:91-98, 1994).
Термин "функционально связанный" относится к функциональной взаимосвязи между двумя или более сегментами полинуклеотида (например, ДНК). Как правило, данный термин относится к функциональной взаимосвязи регулирующей транскрипцию последовательности с транскрибируемой последовательностью. Например, промоторная или энхансерная последовательность является функционально связанной с кодирующей последовательностью, если она стимулирует или модулирует транскрипцию кодирующей последовательности в соответствующей клетке-хозяине или другой системе экспрессии. В целом, регулирующие транскрипцию промоторные последовательности, которые являются функционально связанными с транскрибируемой последовательностью, являются физически смежными с транскрибируемой последовательностью, т. е. они являются цис-действующими. Тем не менее, некоторые регулирующие транскрипцию последовательности, такие как энхансеры, не обязательно должны быть физически смежными или располагаться в непосредственной близости с кодирующими последовательностями, транскрипцию которых они усиливают.
Используемый в данном документе термин "оптимизированный" означает, что нуклеотидная последовательность была изменена таким образом, чтобы она кодировала аминокислотную последовательность с использованием кодонов, которые являются предпочтительными в продуцирующей клетке или организме, обычно в эукариотической клетке, например, клетке Pichia, клетке яичника китайского хомячка (CHO) или клетке человека. Оптимизированную нуклеотидную последовательность конструируют таким образом, чтобы полностью или насколько это возможно сохранить аминокислотную последовательность, первоначально кодируемую исходной нуклеотидной последовательностью, которая также известна как "первичная" последовательность. Оптимизированные последовательности в контексте данного документа были сконструированы так, чтобы они имели кодоны, которые являются предпочтительными в клетках млекопитающих. Тем не менее, оптимизированная экспрессия этих последовательностей в других эукариотических клетках или прокариотических клетках также предполагается в контексте данного документа. Аминокислотные последовательности, кодируемые оптимизированными нуклеотидными последовательностями, также называются оптимизированными.
Термины "полипептид" и "белок" используются в данном документе взаимозаменяемо для обозначения полимера из аминокислотных остатков. Термины применяются к полимерам из аминокислот, в которых один или несколько аминокислотных остатков представляют собой искусственный химический миметик соответствующей встречающейся в природе аминокислоты, а также к полимерам из встречающихся в природе аминокислот и полимеру из не встречающихся в природе аминокислот. Если не указано иное, конкретная полипептидная последовательность также потенциально охватывает ее консервативно модифицированные варианты.
Термин "рекомбинантное человеческое антитело", используемый в данном документе, включает все человеческие антитела, которые получают, экспрессируют, создают или выделяют посредством рекомбинантных способов, такие как антитела, выделенные из животного (например, мыши), которое является трансгенным или трансхромосомным по генам иммуноглобулинов человека, или гибридомы, полученные из него, антитела, выделенные из клетки-хозяина, трансформированной для экспрессии человеческого антитела, например, из трансфектомы, антитела, выделенные из рекомбинантной комбинаторной библиотеки человеческих антител, и антитела, полученные, экспрессированные, созданные или выделенные с помощью любых других способов, которые включают сплайсинг всего гена иммуноглобулина человека или его части, последовательностей в другие последовательности ДНК. Такие рекомбинантные антитела человека имеют вариабельные области, в которых каркасные и CDR-области получены из последовательностей иммуноглобулина зародышевой линии человека. Однако в определенных вариантах осуществления такие рекомбинантные человеческие антитела могут быть подвергнуты мутагенезу in vitro (или, в случае применения животного, трансгенного по последовательностям Ig человека, соматическому мутагенезу in vivo), и, таким образом, аминокислотные последовательности областей VH и VL рекомбинантных антител представляют собой последовательности, которые, хотя и получены из последовательностей VH и VL зародышевой линии человека или родственны им, могут не существовать в естественных условиях в репертуаре антител зародышевой линии человека in vivo.
Термин "рекомбинантная клетка-хозяин" (или просто "клетка-хозяин") относится к клетке, в которую был введен рекомбинантный вектор экспрессии. Следует понимать, что такие термины, как предполагается, относятся не только к конкретной клетке-субъекту, но и к потомству такой клетки. Поскольку определенные модификации могут происходить в последующих поколениях вследствие либо мутации, либо воздействий окружающей среды, такое потомство может, в действительности, не быть идентичным родительской клетке, но при этом оно включено в объем термина "клетка-хозяин", который используется в данном документе.
Термин "субъект" включает человека и животных, отличных от человека. Отличные от человека животные охватывают всех позвоночных (например, млекопитающих и отличных от млекопитающих животных), таких как отличные от человека приматы (например, яванский макак), овца, собака, корова, куры, амфибии и рептилии. За исключением случаев, когда на это обращают внимание, термины "пациент" или "субъект" используются в данном документе взаимозаменяемо. Используемые в данном документе термины "макак-крабоед" или "яванский макак" относятся к яванскому макаку (Macaca fascicularis).
Используемый в данном документе термин "осуществление лечение" или "лечение" любого заболевания или нарушения (например, FGF21-ассоциированного нарушения) относится в одном варианте осуществления к снижению тяжести заболевания или нарушения (т. е. замедлению, или остановке, или снижению развития заболевания или по меньшей мере одного из его клинических симптомов). В другом варианте осуществления "осуществление лечения" или "лечение" относится к облегчению или снижению тяжести в отношении по меньшей мере одного физического параметра, в том числе таких, которые могут быть неявными для пациента. В еще одном варианте осуществления "осуществление лечения" или "лечение" означает модулирование заболевания или нарушения либо физически (например, стабилизацию явного симптома), либо физиологически (например, стабилизацию физического параметра), либо включая и то и другое. В еще одном варианте осуществления "осуществление лечения" или "лечение" относится к предупреждению или задержке возникновения, или развития, или прогрессирования заболевания или нарушения.
"Предупреждение", если оно относится к показаниям, описанным в данном документе, в том числе, например, FGF21-ассоциированному нарушению, означает любое действие, которое обеспечивает предупреждение или замедление ухудшения, например, параметров FGF21-ассоциированного заболевания, описанных ниже, у пациента, характеризующегося риском указанного ухудшения.
Предполагается, что термин "вектор" относится к молекуле полинуклеотида, способной транспортировать другой полинуклеотид, с которым она была связана. Одним типом вектора является "плазмида", которая относится к кольцевой двухцепочечной петле ДНК, в которую могут быть лигированы дополнительные сегменты ДНК. Другим типом вектора является вирусный вектор, такой как аденоассоциированный вирусный вектор (AAV или AAV2), в котором дополнительные сегменты ДНК могут быть лигированы в вирусный геном. Определенные векторы способны к автономной репликации в клетке-хозяине, в которую они введены (например, бактериальные векторы, имеющие бактериальную точку начала репликации, и эписомные векторы млекопитающих). Другие векторы (например, неэписомные векторы млекопитающих) могут интегрироваться в геном клетки-хозяина после введения в клетку-хозяина, и благодаря этому реплицируются вместе с геномом хозяина. Более того, определенные векторы способны управлять экспрессией генов, с которыми они функционально связаны. Такие векторы называются в данном документе "рекомбинантными векторами экспрессии" (или просто "векторами экспрессии").
В целом, векторы экспрессии, применимые в методиках рекомбинантной ДНК, часто имеют форму плазмид. В данном описании "плазмида" и "вектор" могут использоваться взаимозаменяемо, поскольку плазмида является наиболее широко применяемой формой вектора. Тем не менее, предполагается, что настоящее изобретение включает такие другие формы векторов экспрессии, такие как вирусные векторы (например, ретровирусы с дефектной репликацией, аденовирусы и аденоассоциированные вирусы), которые выполняют эквивалентные функции.
Термин "модуляция активности FGF21", используемый в данном документе, относится к повышению или снижению активности FGF21, что может представлять собой результат, например, взаимодействия средства с полинуклеотидом или полипептидом FGF21, активации сигнального пути с участием FGF21 и/или активации опосредованной FGF21 передачи сигнала (например, зависимой от рецептора FGF21 передачи сигнала) и т. п. Например, модуляция биологической активности относится к повышению или снижению биологической активности. Активность FGF21 может быть оценена с помощью средств, в том числе без ограничения определения уровней глюкозы, инсулина, триглицеридов или холестерина в крови у субъекта; с помощью оценки полипептидных уровней бета-клото и/или рецепторов FGF (например, FGFR-1c); или с помощью оценки активации опосредованной FGF21 передачи сигнала (например, зависимой от рецептора FGF21 передачи сигнала).
Сравнения активности FGF21 также могут быть выполнены с помощью, например, измерения уровней нижерасположенного биомаркера FGF21 и измерения значений повышения передачи сигнала с участием FGF21. Активность также может быть оценена с помощью измерения передачи сигнала в клетке; активности киназ; захвата глюкозы в адипоциты; колебаний уровней инсулина, триглицеридов или холестерина в крови; изменений уровней липидов печени или триглицеридов печени; взаимодействий между FGF21 и/или бета-клото и рецептором FGF21; или фосфорилирования рецептора FGF21. В некоторых вариантах осуществления фосфорилирование рецептора FGF21 может представлять собой фосфорилирование тирозина. В некоторых вариантах осуществления модуляция активности FGF21 может вызывать модуляцию связанного с FGF21 фенотипа.
Термин "нижерасположенный биомаркер FGF21", используемый в данном документе, представляет собой ген или продукт гена или измеряемые признаки гена или продукта гена. В некоторых вариантах осуществления ген или активность, которые представляют собой нижерасположенный маркер FGF21, характеризуются измененным уровнем экспрессии или уровнем в сосудистой ткани. В некоторых вариантах осуществления активность нижерасположенного маркера изменяется в присутствии модулятора FGF21. В некоторых вариантах осуществления нижерасположенные маркеры характеризуются измененными уровнями экспрессии, если FGF21 подвержен нарушению в результате действия модулятора FGF21 по настоящему изобретению. Нижераположенные маркеры FGF21 включают в себя без ограничения захват глюкозы или 2-дезоксиглюкозы, уровни pERK и других фосфорилированных или ацетилированных белков или NAD.
Используемый в данном документе термин "повышает регуляцию" относится к повышению, активации или стимуляции активности или количества. Например, в контексте настоящего изобретения модуляторы FGF21 могут повышать активность бета-клото и/или рецептора FGF21. В одном варианте осуществления регуляция FGFR-1c может быть повышена в ответ на модулятор FGF21. Повышение регуляции также может относиться к связанной с FGF21 активности, такой как, например, способности снижать уровни глюкозы, инсулина, триглицеридов или холестерина в крови; снижать уровни липидов печени или триглицеридов печени; снижать вес тела; повышать толерантность к глюкозе, расход энергии или чувствительность к инсулину; или вызывать фосфорилирование рецептора FGF21; или повышать уровень нижерасположенного маркера FGF21. Рецептор FGF21 может представлять собой β-клото и FGFR-1c. Повышение регуляции может составлять по меньшей мере 25%, по меньшей мере 50%, по меньшей мере 75%, по меньшей мере 100%, по меньшей мере 150%, по меньшей мере 200%, по меньшей мере 250%, по меньшей мере 400% или по меньшей мере 500% по сравнению с контролем.
Используемый в данном документе термин "модулятор" относится к композиции, которая обеспечивает модуляцию одного или нескольких физиологических или биохимических явлений, связанных с FGF21-ассоциированным нарушением, таким как сахарный диабет 1 типа или 2 типа или метаболическое состояние, например, ожирение. Указанные явления включают в себя без ограничения способность снижать уровни глюкозы, инсулина, триглицеридов или холестерина в крови; снижать уровни липидов печени или триглицеридов печени; снижать вес тела и повышать толерантность к глюкозе, расход энергии или чувствительность к инсулину.
Белки FGF21
В настоящем изобретении предусмотрены антитела-миметики FGF21 (например, моноклональные антитела, которые связываются с бета-клото (β-клото)), которые индуцируют опосредованную FGF21 передачу сигнала (например, опосредованную рецептором FGF21 передачу сигнала), определенную в данном документе. In vivo зрелая форма FGF21 представляет собой активную форму молекулы. Иллюстративная последовательность FGF21 человека дикого типа имеет номер эталонной последовательности в NCBI NP_061986.1, и ее можно найти в таких выданных патентах, как, например, US 6716626 B1, например, как изложенная ниже (SEQ ID NO:1).
Met Asp Ser Asp Glu Thr Gly Phe Glu His Ser Gly Leu Trp Val Ser
1 5 10 15
Val Leu Ala Gly Leu Leu Leu Gly Ala Cys Gln Ala His Pro Ile Pro
20 25 30
Asp Ser Ser Pro Leu Leu Gln Phe Gly Gly Gln Val Arg Gln Arg Tyr
35 40 45
Leu Tyr Thr Asp Asp Ala Gln Gln Thr Glu Ala His Leu Glu Ile Arg
50 55 60
Glu Asp Gly Thr Val Gly Gly Ala Ala Asp Gln Ser Pro Glu Ser Leu
65 70 75 80
Leu Gln Leu Lys Ala Leu Lys Pro Gly Val Ile Gln Ile Leu Gly Val
85 90 95
Lys Thr Ser Arg Phe Leu Cys Gln Arg Pro Asp Gly Ala Leu Tyr Gly
100 105 110
Ser Leu His Phe Asp Pro Glu Ala Cys Ser Phe Arg Glu Leu Leu Leu
115 120 125
Glu Asp Gly Tyr Asn Val Tyr Gln Ser Glu Ala His Gly Leu Pro Leu
130 135 140
His Leu Pro Gly Asn Lys Ser Pro His Arg Asp Pro Ala Pro Arg Gly
145 150 155 160
Pro Ala Arg Phe Leu Pro Leu Pro Gly Leu Pro Pro Ala Leu Pro Glu
165 170 175
Pro Pro Gly Ile Leu Ala Pro Gln Pro Pro Asp Val Gly Ser Ser Asp
180 185 190
Pro Leu Ser Met Val Gly Pro Ser Gln Gly Arg Ser Pro Ser Tyr Ala
195 200 205
Ser
209
Соответствующая последовательность mRNA, кодирующая полноразмерный полипептид FGF21 (номер эталонной последовательности в NCBI NM_019113.2), показана ниже (SEQ ID NO:2).
1 ctgtcagctg aggatccagc cgaaagagga gccaggcact caggccacct gagtctactc
61 acctggacaa ctggaatctg gcaccaattc taaaccactc agcttctccg agctcacacc
121 ccggagatca cctgaggacc cgagccattg atggactcgg acgagaccgg gttcgagcac
181 tcaggactgt gggtttctgt gctggctggt cttctgctgg gagcctgcca ggcacacccc
241 atccctgact ccagtcctct cctgcaattc gggggccaag tccggcagcg gtacctctac
301 acagatgatg cccagcagac agaagcccac ctggagatca gggaggatgg gacggtgggg
361 ggcgctgctg accagagccc cgaaagtctc ctgcagctga aagccttgaa gccgggagtt
421 attcaaatct tgggagtcaa gacatccagg ttcctgtgcc agcggccaga tggggccctg
481 tatggatcgc tccactttga ccctgaggcc tgcagcttcc gggagctgct tcttgaggac
541 ggatacaatg tttaccagtc cgaagcccac ggcctcccgc tgcacctgcc agggaacaag
601 tccccacacc gggaccctgc accccgagga ccagctcgct tcctgccact accaggcctg
661 ccccccgcac tcccggagcc acccggaatc ctggcccccc agccccccga tgtgggctcc
721 tcggaccctc tgagcatggt gggaccttcc cagggccgaa gccccagcta cgcttcctga
781 agccagaggc tgtttactat gacatctcct ctttatttat taggttattt atcttattta
841 tttttttatt tttcttactt gagataataa agagttccag aggagaaaaa aaaaaaaaaa
901 aaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa
Зрелая последовательность FGF21 не имеет лидерной последовательности и может также предусматривать другие модификации полипептида, такие как протеолитический процессинг аминоконца (с лидерной последовательностью или без нее) и/или карбоксильного конца, отщепление меньшего полипептида от более крупного предшественника, N-связанное и/или O-связанное гликозилирование и другие посттрансляционные модификации, понятные специалистам в данной области техники. Иллюстративный пример зрелой последовательности FGF21 характеризуется следующей последовательностью (SEQ ID NO:53, которая представляет положения аминокислот 29-209 полноразмерной последовательности белка FGF21 (номер эталонной последовательности в NCBI NP_061986.1)):
His Pro Ile Pro Asp Ser Ser Pro Leu Leu Gln Phe Gly Gly Gln Val
5 10 15
Arg Gln Arg Tyr Leu Tyr Thr Asp Asp Ala Gln Gln Thr Glu Ala His
20 25 30
Leu Glu Ile Arg Glu Asp Gly Thr Val Gly Gly Ala Ala Asp Gln Ser
35 40 45
Pro Glu Ser Leu Leu Gln Leu Lys Ala Leu Lys Pro Gly Val Ile Gln
50 55 60
Ile Leu Gly Val Lys Thr Ser Arg Phe Leu Cys Gln Arg Pro Asp Gly
65 70 75 80
Ala Leu Tyr Gly Ser Leu His Phe Asp Pro Glu Ala Cys Ser Phe Arg
85 90 95
Glu Leu Leu Leu Glu Asp Gly Tyr Asn Val Tyr Gln Ser Glu Ala His
100 105 110
Gly Leu Pro Leu His Leu Pro Gly Asn Lys Ser Pro His Arg Asp Pro
115 120 125
Ala Pro Arg Gly Pro Ala Arg Phe Leu Pro Leu Pro Gly Leu Pro Pro
130 135 140
Ala Leu Pro Glu Pro Pro Gly Ile Leu Ala Pro Gln Pro Pro Asp Val
145 150 155 160
Gly Ser Ser Asp Pro Leu Ser Met Val Gly Pro Ser Gln Gly Arg Ser
165 170 175
Pro Ser Tyr Ala Ser
180
Соответствующая кодирующая последовательность cDNA зрелого полипептида FGF21 (SEQ ID NO:53) показана ниже (SEQ ID NO:63):
1 caccccatcc ctgactccag tcctctcctg caattcgggg gccaagtccg gcagcggtac
61 ctctacacag atgatgccca gcagacagaa gcccacctgg agatcaggga ggatgggacg
121 gtggggggcg ctgctgacca gagccccgaa agtctcctgc agctgaaagc cttgaagccg
181 ggagttattc aaatcttggg agtcaagaca tccaggttcc tgtgccagcg gccagatggg
240 gccctgtatg gatcgctcca ctttgaccct gaggcctgca gcttccggga gctgcttctt
301 gaggacggat acaatgttta ccagtccgaa gcccacggcc tcccgctgca cctgccaggg
360 aacaagtccc cacaccggga ccctgcaccc cgaggaccag ctcgcttcct gccactacca
421 ggcctgcccc ccgcactccc ggagccaccc ggaatcctgg ccccccagcc ccccgatgtg
481 ggctcctcgg accctctgag catggtggga ccttcccagg gccgaagccc cagctacgct
541 tcctga
Антитела и антигенсвязывающие фрагменты, являющиеся миметиками FGF21
В настоящем изобретении предусмотрены антитела, которые специфически связываются с β-клото (например, β-клото человека). В некоторых вариантах осуществления в настоящем изобретении предусмотрены антитела, которые специфически связываются с β-клото человека и яванского макака. Антитела по настоящему изобретению включают в себя без ограничения человеческие моноклональные антитела и Fab, выделенные, как описано в примерах.
Последовательность дикого типа β-клото имеет номер эталонной последовательности в NCBI NP_783864.1, и ее можно найти в таких литературных источниках, как Xu, et al. (2007) J Biol Chem. 282(40):29069-72, и Lin, et al. (2007) J Biol Chem. 282(37):27277-84. Полноразмерная cDNA, кодирующая β-клото человека, имеет номер доступа к GenBank NM_175737. Последовательность белка представлена ниже (SEQ ID NO:52).
1 mkpgcaagsp gnewiffstd eittryrntm sngglqrsvi lsalillrav tgfsgdgrai
61 wsknpnftpv nesqlflydt fpknffwgig tgalqvegsw kkdgkgpsiw dhfihthlkn
121 vsstngssds yiflekdlsa ldfigvsfyq fsiswprlfp dgivtvanak glqyystlld
181 alvlrniepi vtlyhwdlpl alqekyggwk ndtiidifnd yatycfqmfg drvkywitih
241 npylvawhgy gtgmhapgek gnlaavytvg hnlikahskv whnynthfrp hqkgwlsitl
301 gshwiepnrs entmdifkcq qsmvsvlgwf anpihgdgdy pegmrkklfs vlpifseaek
361 hemrgtadff afsfgpnnfk plntmakmgq nvslnlreal nwikleynnp riliaengwf
421 tdsrvktedt taiymmknfl sqvlqairld eirvfgytaw slldgfewqd aytirrglfy
481 vdfnskqker kpkssahyyk qiirengfsl kestpdvqgq fpcdfswgvt esvlkpesva
541 sspqfsdphl yvwnatgnrl lhrvegvrlk trpaqctdfv nikkqlemla rmkvthyrfa
601 ldwasvlptg nlsavnrqal ryyrcvvseg lklgisamvt lyypthahlg lpepllhadg
661 wlnpstaeaf qayaglcfqe lgdlvklwit inepnrlsdi ynrsgndtyg aahnllvaha
721 lawrlydrqf rpsqrgavsl slhadwaepa npyadshwra aerflqfeia wfaeplfktg
781 dypaamreyi askhrrglss salprlteae rrllkgtvdf calnhfttrf vmheqlagsr
841 ydsdrdiqfl qditrlsspt rlavipwgvr kllrwvrrny gdmdiyitas giddqaledd
901 rlrkyylgky lqevlkayli dkvrikgyya fklaeekskp rfgfftsdfk akssiqfynk
961 vissrgfpfe nsssrcsqtq entectvclf lvqkkplifl gccffstlvl llsiaifqrq
1021 krrkfwkakn lqhiplkkgk rvvs
В настоящем изобретении предусмотрены антитела и их антигенсвязывающие фрагменты, которые специфически связываются с белком β-клото (например, β-клото человека и/или яванского макака) и способны активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность, при этом указанное антитело описано в таблице 1, например, NOV005 или NOV006. В конкретных аспектах антитела и их антигенсвязывающие фрагменты, предусмотренные в данном документе, которые специфически связываются с белком β-клото (например, β-клото человека и/или яванского макака) и способны активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность, не представляют собой антитело, описанное в таблице 2, например, NOV001, NOV002, NOV003 или NOV004. Антитела, описанные в таблице 2, были описаны в международной заявке на патент согласно PCT № PCT/IB2016/054660, поданной 2 августа 2016 года, которая включена в данный документ посредством ссылки в полном объеме.
В настоящем изобретении предусмотрены антитела, которые специфически связываются с белком β-клото (например, β-клото человека и/или яванского макака), при этом антитела содержат домен VH, имеющий аминокислотную последовательность под SEQ ID NO: 15. В настоящем изобретении также предусмотрены антитела, которые специфически связываются с белком β-клото, при этом указанные антитела содержат CDR VH, имеющую аминокислотную последовательность любой из CDR VH, приведенных в таблице 1 ниже. В частности, в настоящем изобретении предусмотрены антитела, которые специфически связываются с белком β-клото (например, β-клото человека и/или яванского макака), при этом указанные антитела содержат одну, две, три или больше CDR VH (или в качестве альтернативы состоят из них), имеющих аминокислотную последовательность любой из CDR VH, приведенных в таблице 1 ниже.
В настоящем изобретении предусмотрены антитела, которые специфически связываются с белком β-клото, при этом указанные антитела содержат домен VL, имеющий аминокислотную последовательность под SEQ ID NO: 26 или 32. В настоящем изобретении также предусмотрены антитела, которые специфически связываются с белком β-клото (например, β-клото человека и/или яванского макака), при этом указанные антитела содержат CDR VL, имеющую аминокислотную последовательность любой из CDR VL, приведенных в таблице 1 ниже. В частности, в настоящем изобретении предусмотрены антитела, которые специфически связываются с белком β-клото (например, β-клото человека и/или яванского макака), при этом указанные антитела содержат одну, две, три или больше CDR VL (или в качестве альтернативы состоят из них), имеющих аминокислотную последовательность любой из CDR VL, приведенных в таблице 1 ниже.
Другие антитела по настоящему изобретению содержат аминокислоты, которые были подвергнуты мутации, и при этом характеризуются по меньшей мере 60, 70, 80, 85, 90 или 95 процентной идентичностью областей CDR по отношению к областям CDR, показанным в последовательностях, описанных в таблице 1. В некоторых вариантах осуществления они содержат мутантные аминокислотные последовательности, в которых не более 1, 2, 3, 4 или 5 аминокислот были подвергнуты мутации в областях CDR при сравнении с областями CDR, показанными в последовательности, описанной в таблице 1.
В настоящем изобретении также предусмотрены молекулы нуклеиновой кислоты или полинуклеотиды, содержащие последовательности нуклеиновой кислоты, которые кодируют VH, VL, полноразмерную тяжелую цепь и полноразмерную легкую цепь антител, которые специфически связываются с белком β-клото (например, β-клото человека и яванского макака). Такие последовательности нуклеиновой кислоты могут быть оптимизированы для экспрессии в клетках млекопитающих (например, в таблице 1 показаны оптимизированные последовательности нуклеиновой кислоты для тяжелой цепи и легкой цепи антител по настоящему изобретению).
Таблица 1. Примеры антител- и Fab-миметиков FGF21
Таблица 2 Антитела-миметики FGF21
Другие антитела по настоящему изобретению включают в себя антитела, в которых аминокислоты или нуклеиновые кислоты, кодирующие аминокислоты, были подвергнуты мутации, но при этом они характеризуются по меньшей мере 60, 65, 70, 75, 80, 85, 90 или 95 идентичностью по отношению к последовательностям, описанным в таблице 1. В некоторых вариантах осуществления предусмотрены мутантные аминокислотные последовательности, в которых не более 1, 2, 3, 4 или 5 аминокислот были подвергнуты мутации в вариабельных областях при сравнении с вариабельными областями, показанными в последовательности, описанной в таблице 1, при этом они сохраняют по существу такую же антигенсвязывающую активность.
Другие антитела по настоящему изобретению включают в себя антитела, в которых аминокислоты или нуклеиновые кислоты, кодирующие аминокислоты, были подвергнуты мутации, но при этом они характеризуются по меньшей мере 60, 65, 70, 75, 80, 85, 90 или 95 идентичностью по отношению к последовательностям, описанным в таблице 1. В некоторых вариантах осуществления предусмотрены мутантные аминокислотные последовательности, в которых не более 1, 2, 3, 4 или 5 аминокислот были подвергнуты мутации в вариабельных областях при сравнении с вариабельными областями, показанными в последовательности, описанной в таблице 1, при этом они сохраняют по существу такую же антигенсвязывающую активность.
Поскольку каждое из данных антител может связываться с β-клото, последовательности (аминокислотные последовательности и нуклеотидные последовательности, кодирующие аминокислотные последовательности) VH, VL, полноразмерной легкой цепи и полноразмерной тяжелой цепи можно подвергать "смешиванию и подбору" для создания других β-клото-связывающих антител по настоящему изобретению. Такие подвергнутые "смешиванию и подбору" β-клото-связывающие антитела можно тестировать с применением анализов связывания, известных из уровня техники (например, разновидностей ELISA и других анализов, описанных в разделе "Примеры"). Если эти цепи подвергаются смешиванию и подбору в пары, последовательность VH из конкретной пары VH/VL следует заменить на структурно подобную последовательность VH. Аналогичным образом, последовательность полноразмерной тяжелой цепи из конкретной пары полноразмерная тяжелая цепь/полноразмерная легкая цепь следует заменить структурно подобной последовательностью полноразмерной тяжелой цепи. Аналогичным образом последовательность VL из конкретной пары VH/VL следует заменить на структурно подобную последовательность VL. Аналогичным образом последовательность полноразмерной легкой цепи из конкретной пары полноразмерная тяжелая цепь/полноразмерная легкая цепь следует заменить на структурно подобную последовательность полноразмерной легкой цепи.
Соответственно, в одном аспекте в настоящем изобретении предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, имеющие: вариабельный домен тяжелой цепи, содержащий аминокислотную последовательность под SEQ ID NO: 15, и вариабельный домен легкой цепи, содержащий аминокислотную последовательность под SEQ ID NO: 26 или 32, при этом антитело специфически связывается с β-клото (например, β-клото человека или яванского макака).
В другом аспекте настоящего изобретения предусмотрены (i) выделенное антитело, имеющее: полноразмерную тяжелую цепь, содержащую аминокислотную последовательность, которая была оптимизирована для экспрессии в клетке млекопитающего, под SEQ ID NO: 17, и полноразмерную легкую цепь, содержащую аминокислотную последовательность, которая была оптимизирована для экспрессии в клетке млекопитающего, под SEQ ID NO: 28 или 34; или (ii) функциональный белок, содержащий его антигенсвязывающую часть. Более конкретно, в определенных аспектах в настоящем изобретении предусмотрено выделенное антитело или его антигенсвязывающая часть, содержащие тяжелую цепи и легкую цепь, содержащие аминокислотные последовательности, выбранные из SEQ ID NO: 17 и 28 или 17 и 34 соответственно.
В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом антитело или фрагмент содержат вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 15 или аминокислотную последовательность, характеризующуюся по меньшей мере 90% или 95% идентичностью по отношению к ней; и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 26 или 32 или аминокислотную последовательность, характеризующуюся по меньшей мере 90% или 95% идентичностью по отношению к ней.
В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом антитело или фрагмент содержат VH, содержащую аминокислотную последовательность под SEQ ID NO: 15.
В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом антитело или фрагмент содержат VL, содержащую аминокислотную последовательность под SEQ ID NO: 26 или 32.
В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом антитело или фрагмент содержат (i) VH, содержащую аминокислотную последовательность под SEQ ID NO: 15, и VL, содержащую аминокислотную последовательность под SEQ ID NO: 26, или (ii) VH, содержащую аминокислотную последовательность под SEQ ID NO: 15, и VL, содержащую аминокислотную последовательность под SEQ ID NO: 32.
В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом антитело содержит (i) тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 17, и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 28, или (ii) тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 17, и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 34.
В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом антитело или антигенсвязывающий фрагмент не содержат CDR согласно комбинированной системе нумерации или CDR согласно Kabat из антитела NOV004, изложенного в таблице 2.
Термины "определяющая комплементарность область" и "CDR", используемые в данном документе, относятся к последовательностям аминокислот в вариабельных областях антитела, которые придают антигенную специфичность и аффинность связывания. Как правило, в каждой вариабельной области тяжелой цепи присутствуют три CDR (HCDR1, HCDR2, HCDR3), и в каждой вариабельной области легкой цепи присутствуют три CDR (LCDR1, LCDR2, LCDR3).
Точные границы аминокислотной последовательности указанной CDR могут быть легко определены с использованием любой из ряда широко известных схем, в том числе описанных в Kabat et al. (1991), "Sequences of Proteins of Immunological Interest," 5th Ed. Public Health Service, National Institutes of Health, Bethesda, MD (схема нумерации согласно Kabat), Al-Lazikani et al., (1997) JMB 273,927-948 (схема нумерации по "Chothia"), а также нумерация ImMunoGenTics (IMGT) (Lefranc, M.-P., The Immunologist, 7, 132-136 (1999); Lefranc, M.-P. et al., Dev. Comp. Immunol., 27, 55-77 (2003) (схема нумерации "IMGT"). Например, в случае классических форматов согласно Kabat аминокислотные остатки CDR в домене тяжелой вариабельной цепи (VH) нумеруют 31-35 (HCDR1), 50-65 (HCDR2) и 95-102 (HCDR3); а аминокислотные остатки CDR в домене легкой вариабельной цепи (VL) нумеруют 24-34 (LCDR1), 50-56 (LCDR2) и 89-97 (LCDR3). Согласно Chothia аминокислоты CDR в VH нумеруют 26-32 (HCDR1), 52-56 (HCDR2) и 95-102 (HCDR3); а аминокислотные остатки в VL нумеруют 26-32 (LCDR1), 50-52 (LCDR2) и 91-96 (LCDR3). Объединяя определения CDR согласно Kabat и согласно Chothia, CDR состоят из аминокислотных остатков 26-35 (HCDR1), 50-65 (HCDR2) и 95-102 (HCDR3) в человеческой VH и аминокислотных остатков 24-34 (LCDR1), 50-56 (LCDR2) и 89-97 (LCDR3) в человеческой VL. Согласно IMGT аминокислотные остатки CDR в VH нумеруют примерно 26-35 (CDR1), 51-57 (CDR2) и 93-102 (CDR3), а аминокислотные остатки CDR в VL нумеруют примерно 27-32 (CDR1), 50-52 (CDR2) и 89-97 (CDR3) (нумерация в соответствии с "Kabat"). Согласно IMGT области CDR антитела можно определять с применением программы IMGT/DomainGap Align. Объединяя определения CDR согласно Kabat и согласно Chothia, CDR согласно комбинированной системе нумерации могут состоять из аминокислотных остатков 26-35 (HCDR1), 50-65 (HCDR2) и 99-108 (HCDR3) в человеческой VH и аминокислотных остатков 24-39 (LCDR1), 55-61 (LCDR2) и 94-102 (LCDR3) в человеческой VL.
В другом аспекте в настоящем изобретении предусмотрены β-клото-связывающие антитела, которые содержат CDR1, CDR2 и CDR3 тяжелой цепи и легкой цепи, описанные в таблице 1, или их комбинации. В конкретных аспектах эти CDR обозначены с помощью системы Kabat. В других конкретных аспектах эти CDR обозначены с помощью комбинированной системы нумерации.
С учетом того, что каждое из этих антител может связываться с β-клото, и что специфичность связывания с антигеном обеспечивается преимущественно областями CDR1, 2 и 3, последовательности CDR1, 2 и 3 VH и последовательности CDR1, 2 и 3 VL можно подвергнуть "смешиванию и подбору" (т. е. CDR из различных антител можно подвергнуть смешиванию и подбору, хотя каждое антитело предпочтительно содержит CDR1, 2 и 3 VH и CDR1, 2 и 3 VL для создания других β-клото-связывающих молекул по настоящему изобретению. Такие подвергнутые "смешиванию и подбору" β-клото-связывающие антитела можно тестировать с применением анализов связывания, известных из уровня техники и описанных в примерах (например, анализов связывания ELISA, SET, Biacore®). Когда последовательности CDR VH подвергают смешиванию и подбору, последовательность CDR1, CDR2 и/или CDR3 из конкретной последовательности VH следует заменить структурно подобной(-ыми) последовательностью(-ями) CDR. Аналогичным образом, когда последовательности CDR VL подвергают смешиванию и подбору, последовательность CDR1, CDR2 и/или CDR3 из конкретной последовательности VL следует заменить структурно подобной(-ыми) последовательностью(-ями) CDR. Специалисту в данной области техники будет совершенно очевидно, что новые последовательности VH и VL можно создавать путем замены одной или нескольких последовательностей областей CDR VH и/или VL структурно подобными последовательностями из последовательностей CDR, показанных в данном документе для моноклональных антител по настоящему изобретению. Помимо вышеуказанного, в одном варианте осуществления антигенсвязывающие фрагменты антител, описанных в данном документе, могут содержать CDR1, 2 и 3 VH или CDR 1, 2 и 3 VL, при этом фрагмент связывается с β-клото в виде одного вариабельного домена.
В определенных вариантах осуществления настоящего изобретения антитела или их антигенсвязывающие фрагменты могут иметь последовательности тяжелой и легкой цепей Fab, описанных в таблице 1. Более конкретно, антитело или его антигенсвязывающие фрагменты могут иметь последовательность тяжелой и легкой цепей Fab NOV005 или NOV006.
В определенных вариантах осуществления настоящего изобретения антитело или антигенсвязывающий фрагмент, которые специфически связываются с β-клото, содержат CDR1, CDR2 и CDR3 вариабельной области тяжелой цепи Fab NOV005 или NOV006, и CDR1, CDR2 и CDR3 вариабельной области легкой цепи Fab NOV005 или NOV006, например, изложенные в таблице 1.
В других вариантах осуществления настоящего изобретения антитело или антигенсвязывающий фрагмент, которые специфически связываются с β-клото, содержат CDR1 вариабельной области тяжелой цепи, CDR2 вариабельной области тяжелой цепи, CDR3 вариабельной области тяжелой цепи, CDR1 вариабельной области легкой цепи, CDR2 вариабельной области легкой цепи и CDR3 вариабельной области легкой цепи, определенные согласно Kabat и описанные в таблице 1. В еще одних вариантах осуществления настоящего изобретения антитело или антигенсвязывающий фрагмент, которые специфически связываются с β-клото, содержат CDR1 вариабельной области тяжелой цепи, CDR2 вариабельной области тяжелой цепи, CDR3 вариабельной области тяжелой цепи, CDR1 вариабельной области легкой цепи, CDR2 вариабельной области легкой цепи и CDR3 вариабельной области легкой цепи, определенные согласно Chothia и описанные в таблице 1. В еще одних вариантах осуществления настоящего изобретения антитело или антигенсвязывающий фрагмент, которые специфически связываются с β-клото, содержат CDR1 вариабельной области тяжелой цепи, CDR2 вариабельной области тяжелой цепи, CDR3 вариабельной области тяжелой цепи, CDR1 вариабельной области легкой цепи, CDR2 вариабельной области легкой цепи и CDR3 вариабельной области легкой цепи, определенные согласно комбинированной системе нумерации, Kabat и Chothia, и описанные в таблице 1. В еще одних вариантах осуществления настоящего изобретения антитело или антигенсвязывающий фрагмент, которые специфически связываются с β-клото, содержат CDR1 вариабельной области тяжелой цепи, CDR2 вариабельной области тяжелой цепи, CDR3 вариабельной области тяжелой цепи, CDR1 вариабельной области легкой цепи, CDR2 вариабельной области легкой цепи и CDR3 вариабельной области легкой цепи, определенные согласно IMGT и описанные в таблице 1.
В определенных вариантах осуществления в настоящем изобретении предусмотрены антитела или антигенсвязывающие фрагменты, которые специфически связываются с β-клото, описанные в таблице 1, например, антитело NOV005 или NOV006. В предпочтительном варианте осуществления антитело или антигенсвязывающий фрагмент, которые связывают β-клото и активируют рецепторный комплекс FGF21, представляют собой Fab NOV005 или NOV006.
В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом антитело или его антигенсвязывающий фрагмент содержат:
(i) CDR1 тяжелой цепи (HCDR1), содержащую аминокислотную последовательность под SEQ ID NO: 6, 9, 10 или 12;
(ii) CDR2 тяжелой цепи (HCDR2), содержащую аминокислотную последовательность под SEQ ID NO: 7, 11 или 13;
(iii) CDR3 тяжелой цепи (HCDR3), содержащую аминокислотную последовательность под SEQ ID NO: 8 или 14;
(iv) CDR1 легкой цепи (LCDR1), содержащую аминокислотную последовательность под SEQ ID NO: 19, 31, 22 или 25;
(v) CDR2 легкой цепи (LCDR2), содержащую аминокислотную последовательность под SEQ ID NO: 20 или 23; и
(vi) CDR3 легкой цепи (LCDR3), содержащую аминокислотную последовательность под SEQ ID NO: 21 или 24.
В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом антитело или его антигенсвязывающий фрагмент содержат:
(i) CDR1 тяжелой цепи (HCDR1), содержащую аминокислотную последовательность под SEQ ID NO: 6, 9, 10 или 12;
(ii) CDR2 тяжелой цепи (HCDR2), содержащую аминокислотную последовательность под SEQ ID NO: 7, 11 или 13;
(iii) CDR3 тяжелой цепи (HCDR3), содержащую аминокислотную последовательность под SEQ ID NO: 8 или 14;
(iv) CDR1 легкой цепи (LCDR1), содержащую аминокислотную последовательность под SEQ ID NO: 31, 22 или 25;
(v) CDR2 легкой цепи (LCDR2), содержащую аминокислотную последовательность под SEQ ID NO: 20 или 23; и
(vi) CDR3 легкой цепи (LCDR3), содержащую аминокислотную последовательность под SEQ ID NO: 21 или 24.
В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом антитело или его антигенсвязывающий фрагмент содержат:
(i) CDR1 тяжелой цепи (HCDR1), содержащую аминокислотную последовательность под SEQ ID NO: 6, 9, 10 или 12;
(ii) CDR2 тяжелой цепи (HCDR2), содержащую аминокислотную последовательность под SEQ ID NO: 7, 11 или 13;
(iii) CDR3 тяжелой цепи (HCDR3), содержащую аминокислотную последовательность под SEQ ID NO: 8 или 14;
(iv) CDR1 легкой цепи (LCDR1), содержащую аминокислотную последовательность под SEQ ID NO: 19, 31, 22 или 25;
(v) CDR2 легкой цепи (LCDR2), содержащую аминокислотную последовательность под SEQ ID NO: 20 или 23; и
(vi) CDR3 легкой цепи (LCDR3), содержащую аминокислотную последовательность под SEQ ID NO: 21 или 24.
В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом антитело или его антигенсвязывающий фрагмент содержат VH, содержащую HCDR1, HCDR2 и HCDR3, и VL, содержащую LCDR1, LCDR2 и LCDR3, где:
HCDR1 содержит аминокислотную последовательность под SEQ ID NO: 6, HCDR2 содержит аминокислотную последовательность под SEQ ID NO: 7, HCDR3 содержит аминокислотную последовательность под SEQ ID NO: 8, LCDR1 содержит аминокислотную последовательность под SEQ ID NO: 31, LCDR2 содержит аминокислотную последовательность под SEQ ID NO: 20, и LCDR3 содержит аминокислотную последовательность под SEQ ID NO: 21.
В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом антитело или его антигенсвязывающий фрагмент содержат VH, содержащую HCDR1, HCDR2 и HCDR3, и VL, содержащую LCDR1, LCDR2 и LCDR3, где:
HCDR1 содержит аминокислотную последовательность под SEQ ID NO: 9, HCDR2 содержит аминокислотную последовательность под SEQ ID NO: 7, HCDR3 содержит аминокислотную последовательность под SEQ ID NO: 8, LCDR1 содержит аминокислотную последовательность под SEQ ID NO: 31, LCDR2 содержит аминокислотную последовательность под SEQ ID NO: 20, и LCDR3 содержит аминокислотную последовательность под SEQ ID NO: 21.
В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом антитело или его антигенсвязывающий фрагмент содержат VH, содержащую HCDR1, HCDR2 и HCDR3, и VL, содержащую LCDR1, LCDR2 и LCDR3, где:
HCDR1 содержит аминокислотную последовательность под SEQ ID NO: 10, HCDR2 содержит аминокислотную последовательность под SEQ ID NO: 11, HCDR3 содержит аминокислотную последовательность под SEQ ID NO: 8, LCDR1 содержит аминокислотную последовательность под SEQ ID NO: 22, LCDR2 содержит аминокислотную последовательность под SEQ ID NO: 23, и LCDR3 содержит аминокислотную последовательность под SEQ ID NO: 24.
В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом антитело или его антигенсвязывающий фрагмент содержат VH, содержащую HCDR1, HCDR2 и HCDR3, и VL, содержащую LCDR1, LCDR2 и LCDR3, где:
HCDR1 содержит аминокислотную последовательность под SEQ ID NO: 12, HCDR2 содержит аминокислотную последовательность под SEQ ID NO: 13, HCDR3 содержит аминокислотную последовательность под SEQ ID NO: 14, LCDR1 содержит аминокислотную последовательность под SEQ ID NO: 25, LCDR2 содержит аминокислотную последовательность под SEQ ID NO: 23, и LCDR3 содержит аминокислотную последовательность под SEQ ID NO: 21.
В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом антитело или его антигенсвязывающий фрагмент содержат VH, содержащую HCDR1, HCDR2 и HCDR3, и VL, содержащую LCDR1, LCDR2 и LCDR3, где:
(i) HCDR1 содержит аминокислотную последовательность под SEQ ID NO: 6, HCDR2 содержит аминокислотную последовательность под SEQ ID NO: 7, HCDR3 содержит аминокислотную последовательность под SEQ ID NO: 8, LCDR1 содержит аминокислотную последовательность под SEQ ID NO: 19, LCDR2 содержит аминокислотную последовательность под SEQ ID NO: 20, и LCDR3 содержит аминокислотную последовательность под SEQ ID NO: 21 или
(ii) HCDR1 содержит аминокислотную последовательность под SEQ ID NO: 9, HCDR2 содержит аминокислотную последовательность под SEQ ID NO: 7, HCDR3 содержит аминокислотную последовательность под SEQ ID NO: 8, LCDR1 содержит аминокислотную последовательность под SEQ ID NO: 19, LCDR2 содержит аминокислотную последовательность под SEQ ID NO: 20, и LCDR3 содержит аминокислотную последовательность под SEQ ID NO: 21.
В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом антитело или его антигенсвязывающий фрагмент содержат VH, содержащую HCDR1, HCDR2 и HCDR3, и VL, содержащую LCDR1, LCDR2 и LCDR3, где:
HCDR1 содержит аминокислотную последовательность под SEQ ID NO: 10, HCDR2 содержит аминокислотную последовательность под SEQ ID NO: 11, HCDR3 содержит аминокислотную последовательность под SEQ ID NO: 8, LCDR1 содержит аминокислотную последовательность под SEQ ID NO: 22, LCDR2 содержит аминокислотную последовательность под SEQ ID NO: 23, и LCDR3 содержит аминокислотную последовательность под SEQ ID NO: 24.
В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом антитело или его антигенсвязывающий фрагмент содержат VH, содержащую HCDR1, HCDR2 и HCDR3, и VL, содержащую LCDR1, LCDR2 и LCDR3, где:
HCDR1 содержит аминокислотную последовательность под SEQ ID NO: 12, HCDR2 содержит аминокислотную последовательность под SEQ ID NO: 13, HCDR3 содержит аминокислотную последовательность под SEQ ID NO: 14, LCDR1 содержит аминокислотную последовательность под SEQ ID NO: 25, LCDR2 содержит аминокислотную последовательность под SEQ ID NO: 23, и LCDR3 содержит аминокислотную последовательность под SEQ ID NO: 21.
В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом антитело или его антигенсвязывающий фрагмент содержат VH, содержащую CDR HCDR1, HCDR2 и HCDR3, и VL, содержащую CDR LCDR1, LCDR2 и LCDR3, где антитело или его антигенсвязывающий фрагмент содержат: HCDR1, содержащую аминокислотную последовательностью под SEQ ID NO: 6, HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 7, HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 8, LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 19 или 31, LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 20, и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 21.
В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом антитело или его антигенсвязывающий фрагмент содержат VH, содержащую CDR HCDR1, HCDR2 и HCDR3, и VL, содержащую CDR LCDR1, LCDR2 и LCDR3, где антитело или его антигенсвязывающий фрагмент содержат: HCDR1, содержащую аминокислотную последовательностью под SEQ ID NO: 9, HCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 7, HCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 8, LCDR1, содержащую аминокислотную последовательность под SEQ ID NO: 19 или 31, LCDR2, содержащую аминокислотную последовательность под SEQ ID NO: 20, и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 21.
В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом указанное антитело или фрагмент повышают активность β-клото и/или FGFR1c. В конкретных аспектах указанное антитело или его фрагмент повышают активность β-клото и/или FGFR1c, например, определенной с помощью активности фосфо-ERK, на по меньшей мере приблизительно 10% или 20%. В конкретных аспектах указанное антитело или его фрагмент повышают активность β-клото и/или FGFR1c, например, определенной с помощью активности фосфо-ERK, на по меньшей мере приблизительно 30% или 40%. В конкретных аспектах указанное антитело или его фрагмент повышают активность β-клото и/или FGFR1c, например, определенной с помощью активности фосфо-ERK, на по меньшей мере приблизительно 50% или 60%. В конкретных аспектах указанное антитело или его фрагмент повышают активность β-клото и/или FGFR1c, например, определенной с помощью активности фосфо-ERK, на по меньшей мере приблизительно 70% или 80%. В конкретных аспектах указанное антитело или его фрагмент повышают активность β-клото и/или FGFR1c, например, определенной с помощью активности фосфо-ERK, на по меньшей мере приблизительно 90% или 95%.
В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом антитело или антигенсвязывающий фрагмент связываются с белком β-клото человека с KD, составляющей менее чем или равной 500 пM или 450 пM, например, определенной с помощью анализов связывания BIACORE™. В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом антитело или антигенсвязывающий фрагмент связываются с белком β-клото человека с KD, составляющей менее чем или равной 450 пM или 400 пM, например, определенной с помощью анализов связывания BIACORE™.
В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом антитело или антигенсвязывающий фрагмент связываются с белком β-клото человека с KD, составляющей менее чем или равной 10 пM или 20 пM, например, определенной с помощью анализов связывания BIACORE™.
В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом указанный эпитоп β-клото содержит одну или несколько аминокислот из остатков 246-265, 536-550, 834-857 и 959-986 последовательности β-клото (SEQ ID NO:52).
В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом указанные эпитопы содержат одну или несколько аминокислот из остатков 646-670, 696-700 и 646-689 последовательности β-клото (SEQ ID NO:52).
В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом указанное антитело или антигенсвязывающий фрагмент обеспечивают защиту одной или нескольких аминокислот из остатков 246-265, 536-550, 834-857 и 959-986 β-клото человека (SEQ ID NO:52), как определено с помощью водородно-дейтериевого обмена (HDx).
В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом указанное антитело или антигенсвязывающий фрагмент обеспечивают защиту одной или нескольких аминокислот из остатков 646-670, 696-700 и 646-689 последовательности β-клото (SEQ ID NO:52).
В конкретных вариантах осуществления в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом указанное антитело или фрагмент не контактируют с остатками 701 (Tyr) или 703 (Arg) β-клото человека (SEQ ID NO: 52).
В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом указанное антитело или его антигенсвязывающий фрагмент способны активировать рецепторный комплекс FGFR1c_β-клото человека, например, с EC50, составляющей менее чем или равной 50 нM, измеренной с помощью клеточных анализов pERK.
В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом указанное антитело или его антигенсвязывающий фрагмент способны активировать рецепторный комплекс FGFR1c_β-клото человека, например, с EC50, составляющей менее чем или равной 100 нM, измеренной с помощью клеточных анализов pERK.
В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом указанное антитело или его антигенсвязывающий фрагмент способны активировать рецепторный комплекс FGFR1c_β-клото человека, например, с EC50, составляющей менее чем или равной 40 нM или 30 нМ, измеренной с помощью клеточных анализов pERK.
В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом указанное антитело или его антигенсвязывающий фрагмент способны активировать рецепторный комплекс FGFR1c_β-клото человека, например, с EC50, составляющей менее чем или равной 50 нM, измеренной с помощью клеточных анализов pERK, и при этом антитело или его антигенсвязывающий фрагмент не способны активировать рецепторный комплекс FGFR2c-β-клото, рецепторный комплекс FGFR3c-β-клото и/или рецепторный комплекс FGFR4-β-клото.
В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом указанное антитело или его антигенсвязывающий фрагмент способны активировать рецепторный комплекс FGFR1c_β-клото яванского макака с EC50, составляющей менее чем или равной 50 нM, измеренной с помощью клеточных анализов pERK.
В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом указанное антитело или его антигенсвязывающий фрагмент способны активировать рецепторный комплекс FGFR1c_β-клото яванского макака с EC50, составляющей менее чем или равной 40 нM или 30 нМ, измеренной с помощью клеточных анализов pERK.
В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, моноклональное антитело) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото и индуцируют активность рецепторного комплекса FGF21, например, рецепторного комплекса FGFR1c-β-клото, при этом указанное антитело или его антигенсвязывающий фрагмент способны активировать рецепторный комплекс FGFR1c_β-клото яванского макака с EC50, составляющей менее чем или равной 20 нM, измеренной с помощью клеточных анализов pERK. При использовании в данном документе человеческое антитело содержит вариабельные области тяжелых и легких цепей или полноразмерные тяжелые или легкие цепи, которые представляют собой "продукт из" определенной последовательности зародышевой линии или "происходят из" нее, если вариабельные области или полноразмерные цепи антитела получены из системы, в которой применяют гены зародышевой линии иммуноглобулинов человека. Такие системы включают иммунизацию трансгенной мыши, несущей гены иммуноглобулинов человека, антигеном, представляющим интерес, или скрининг библиотеки генов иммуноглобулинов человека, отображенных на фаге, с использованием антигена, представляющего интерес. Антитело человека, которое является "продуктом" или "полученным из" последовательности зародышевой линии иммуноглобулина человека, может быть идентифицировано как таковое посредством сравнения аминокислотной последовательности антитела человека с аминокислотными последовательностями зародышевой линии иммуноглобулинов человека и выбора последовательности зародышевой линии иммуноглобулина человека, которая является наиболее близкой по последовательности (т. е. имеет наибольший % идентичности) к последовательности антитела человека.
Антитело человека, которое является "продуктом" или "полученным из" конкретной последовательности зародышевой линии иммуноглобулина человека, может содержать аминокислотные отличия по сравнению с последовательностью зародышевой линии вследствие, например, естественных соматических мутаций или преднамеренного введения сайт-направленных мутаций. Тем не менее, в каркасных областях VH или VL выбранное антитело человека, как правило, является на по меньшей мере 90% идентичным по аминокислотам последовательности аминокислотной последовательности, кодируемой геном зародышевой линии иммуноглобулина человека, и содержит аминокислотные остатки, которые идентифицируют антитело человека как человеческое по сравнению с аминокислотными последовательностями зародышевой линии иммуноглобулина других видов (например, последовательностями зародышевой линии мыши). В определенных случаях, антитело человека может быть на по меньшей мере 60%, 70%, 80%, 90%, или на по меньшей мере 95%, или даже на по меньшей мере 96%, 97%, 98% или 99% идентичным по аминокислотной последовательности аминокислотной последовательности, кодируемой геном зародышевой линии иммуноглобулина.
Как правило, рекомбинантное антитело человека будет проявлять отличия не более чем 10 аминокислотами от аминокислотной последовательности, кодируемой геном зародышевой линии иммуноглобулина человека, в каркасных областях VH или VL. В определенных случаях антитело человека может проявлять отличие не более чем 5, или даже не более чем 4, 3, 2 или 1 аминокислотой от аминокислотной последовательности, кодируемой геном зародышевой линии иммуноглобулина. Примеры генов зародышевой линии человека иммуноглобулинов включают в себя без ограничения фрагменты зародышевой линии вариабельных доменов, описанных ниже, а также DP47 и DPK9.
Гомологичные антитела
В еще одном варианте осуществления в настоящем изобретении предусмотрено антитело или его антигенсвязывающий фрагмент, содержащие аминокислотные последовательности, которые гомологичны последовательностям, описанным в таблице 1, и антитело связывается с белком β-клото (например, β-клото человека и яванского макака) и сохраняет необходимые функциональные свойства (например, активацию или повышение активности рецепторного комплекса β-клото/FGFR1c и/или один или несколько видов активности FGF21) этих антител, описанных в таблице 1.
Например, в настоящем изобретении предусмотрено выделенное антитело (например, антитело, способное активировать или повышать активность рецепторного комплекса β-клото/FGFR1c) или его функциональный антигенсвязывающий фрагмент, содержащие вариабельный домен тяжелой цепи и вариабельный домен легкой цепи, при этом вариабельный домен тяжелой цепи содержит аминокислотную последовательность, которая на по меньшей мере 80%, по меньшей мере 90%, 95%, 96%, 97%, 98%, или по меньшей мере 99% идентична аминокислотной последовательности под SEQ ID NO: 15; вариабельный домен легкой цепи содержит аминокислотную последовательность, которая на по меньшей мере 80%, по меньшей мере 90%, 95%, 96%, 97%, 98%, или по меньшей мере 99% идентична аминокислотной последовательности под SEQ ID NO: 26 или 32; при этом антитело специфически связывается с β-клото (например, β-клото человека или яванского макака) и индуцирует активность β-клото, и при этом вариабельный домен тяжелой цепи не содержит аминокислотную последовательность, изложенную в таблице 2, например, аминокислотную последовательность под SEQ ID NO: 43 или 55, и вариабельный домен легкой цепи не содержит аминокислотную последовательность, изложенную в таблице 2, например, аминокислотную последовательность под SEQ ID NO: 47 или 57. В определенных аспектах настоящего изобретения последовательности тяжелых и легких цепей дополнительно содержат последовательности HCDR1, HCDR2, HCDR3, LCDR1, LCDR2 и LCDR3, определенных согласно Kabat, например, изложенных в таблице 1. В определенных других аспектах настоящего изобретения последовательности тяжелых и легких цепей дополнительно содержат последовательности HCDR1, HCDR2, HCDR3, LCDR1, LCDR2 и LCDR3, определенных согласно Chothia, например, изложенных в таблице 1 соответственно. В определенных других аспектах настоящего изобретения последовательности тяжелых и легких цепей дополнительно содержат последовательности HCDR1, HCDR2, HCDR3, LCDR1, LCDR2 и LCDR3, определенных согласно комбинированной системе нумерации, например, изложенных в таблице 1 соответственно. В определенных других аспектах настоящего изобретения последовательности тяжелых и легких цепей дополнительно содержат последовательности HCDR1, HCDR2, HCDR3, LCDR1, LCDR2 и LCDR3, определенных согласно IMGT, например, изложенных в таблице 1 соответственно.
Например, в настоящем изобретении предусмотрено выделенное антитело (например, антитело, способное активировать или повышать активность рецепторного комплекса β-клото/FGFR1c) или его функциональный антигенсвязывающий фрагмент, содержащие вариабельный домен тяжелой цепи и вариабельный домен легкой цепи, при этом вариабельный домен тяжелой цепи содержит аминокислотную последовательность, которая на по меньшей мере 80%, по меньшей мере 90%, 95%, 96%, 97%, 98%, или по меньшей мере 99% идентична аминокислотной последовательности под SEQ ID NO: 15; вариабельный домен легкой цепи содержит аминокислотную последовательность, которая на по меньшей мере 80%, по меньшей мере 90%, 95%, 96%, 97%, 98%, или по меньшей мере 99% идентична аминокислотной последовательности под SEQ ID NO: 26 или 32; при этом антитело специфически связывается с β-клото (например, β-клото человека или яванского макака), и при этом вариабельный домен тяжелой цепи не содержит аминокислотную последовательность, изложенную в таблице 2, например, аминокислотную последовательность под SEQ ID NO: 43 или 55, и вариабельный домен легкой цепи не содержит аминокислотную последовательность, изложенную в таблице 2, например, аминокислотную последовательность под SEQ ID NO: 47 или 57. В определенных аспектах настоящего изобретения последовательности тяжелых и легких цепей дополнительно содержат последовательности HCDR1, HCDR2, HCDR3, LCDR1, LCDR2 и LCDR3, определенных согласно Kabat, например, изложенных в таблице 1. В определенных других аспектах настоящего изобретения последовательности тяжелых и легких цепей дополнительно содержат последовательности HCDR1, HCDR2, HCDR3, LCDR1, LCDR2 и LCDR3, определенных согласно Chothia, например, изложенных в таблице 1. В определенных других аспектах настоящего изобретения последовательности тяжелых и легких цепей дополнительно содержат последовательности HCDR1, HCDR2, HCDR3, LCDR1, LCDR2 и LCDR3, определенных согласно комбинированной системе нумерации, например, изложенных в таблице 1. В определенных других аспектах настоящего изобретения последовательности тяжелых и легких цепей дополнительно содержат последовательности HCDR1, HCDR2, HCDR3, LCDR1, LCDR2 и LCDR3, определенных согласно IMGT, например, изложенных в таблице 1.
В других вариантах осуществления аминокислотные последовательности VH и/или VL могут быть на 50%, 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98% или 99% идентичны последовательностям, изложенным в таблице 1, при этом вариабельный домен тяжелой цепи не содержит аминокислотную последовательность, изложенную в таблице 2, например, аминокислотную последовательность под SEQ ID NO: 43 или 55, и вариабельный домен легкой цепи не содержит аминокислотную последовательность, изложенную в таблице 2, например, аминокислотную последовательность под SEQ ID NO: 47 или 57. В других вариантах осуществления аминокислотные последовательности VH и/или VL могут быть идентичными, за исключением аминокислотной замены в не более чем 1, 2, 3, 4 или 5 аминокислотных положениях. Антитело, имеющее области VH и VL, характеризующиеся высокой (т. е. 80% или большей) идентичностью с областями VH и VL антител, описанных в таблице 1, можно получить посредством мутагенеза (например, сайт-направленного или ПЦР-опосредованного мутагенеза) молекул нуклеиновой кислоты, кодирующих SEQ ID NO: 10, 30, 50 или 70 и SEQ ID NO: 20, 40, 60 или 80 соответственно, с последующим исследованием кодируемого измененного антитела в отношении сохраненной функции с помощью функциональных анализов, описанных в данном документе, при этом вариабельный домен тяжелой цепи не содержит аминокислотную последовательность, изложенную в таблице 2, например, аминокислотную последовательность под SEQ ID NO: 43 или 55, и вариабельный домен легкой цепи не содержит аминокислотную последовательность, изложенную в таблице 2, например, аминокислотную последовательность под SEQ ID NO: 47 или 57.
В других вариантах осуществления аминокислотные последовательности полноразмерной тяжелой цепи и/или полноразмерной легкой цепи могут быть на 50% 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98% или 99% идентичны последовательностям, изложенным в таблице 1, при этом тяжелая цепь не содержит аминокислотную последовательность тяжелой цепи, изложенную в таблице 2, например, аминокислотную последовательность под SEQ ID NO: 45, 56, 59 или 61, и легкая цепь не содержит аминокислотную последовательность легкой цепи, изложенную в таблице 2, например, аминокислотную последовательность под SEQ ID NO: 49, 58, 60 или 62. Антитело, имеющее полноразмерную тяжелую цепь и полноразмерную легкую цепь, характеризующиеся высокой (т. е. 80% или большей) идентичностью полноразмерной тяжелой цепи под SEQ ID NO: 17 и полноразмерной легкой цепи под SEQ ID NO: 28 или 34, может быть получено с помощью мутагенеза (т. е. сайт-направленного или ПЦР-опосредованного мутагенеза) молекул нуклеиновой кислоты, кодирующих такие полипептиды, с последующим исследованием кодируемого измеренного антитела в отношении сохраненной функции с помощью функциональных анализов, описанных в данном документе, при этом тяжелая цепь не содержит аминокислотную последовательность тяжелой цепи, изложенную в таблице 2, например, аминокислотную последовательность под SEQ ID NO: 45, 56, 59 или 61, и легкая цепь не содержит аминокислотную последовательность легкой цепи, изложенную в таблице 2, например, аминокислотную последовательность под SEQ ID NO: 49, 58, 60 или 62. Антитело, имеющее полноразмерную тяжелую цепь и полноразмерную легкую цепь, характеризующиеся высокой (т. е. 80% или большей) идентичностью полноразмерной тяжелой цепи под SEQ ID NO: 17 и полноразмерной легкой цепи под SEQ ID NO: 28 или 34, может быть получено с помощью мутагенеза (т. е. сайт-направленного или ПЦР-опосредованного мутагенеза) молекул нуклеиновой кислоты, кодирующих такие полипептиды, с последующим исследованием кодируемого измеренного антитела в отношении сохраненной функции с помощью функциональных анализов, описанных в данном документе, при этом тяжелая цепь не содержит аминокислотную последовательность тяжелой цепи, изложенную в таблице 2, например, аминокислотную последовательность под SEQ ID NO: 45, 56, 59 или 61, и легкая цепь не содержит аминокислотную последовательность легкой цепи, изложенную в таблице 2, например, аминокислотную последовательность под SEQ ID NO: 49, 58, 60 или 62.
В других вариантах осуществления нуклеотидные последовательности полноразмерной тяжелой цепи и/или полноразмерной легкой цепи могут быть на 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98% или 99% идентичны последовательностям, изложенным в таблице 1, при этом тяжелая цепь не содержит аминокислотную последовательность тяжелой цепи, изложенную в таблице 2, например, аминокислотную последовательность под SEQ ID NO: 45, 56, 59 или 61, и легкая цепь не содержит аминокислотную последовательность легкой цепи, изложенную в таблице 2, например, аминокислотную последовательность под SEQ ID NO: 49, 58, 60 или 62.
В других вариантах осуществления нуклеотидные последовательности вариабельных областей тяжелой цепи и/или вариабельных областей легкой цепи могут быть на 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98% или 99% идентичны последовательностям, изложенным в таблице 1, при этом тяжелая цепь не содержит аминокислотную последовательность тяжелой цепи, изложенную в таблице 2, например, аминокислотную последовательность под SEQ ID NO: 45, 56, 59 или 61, и легкая цепь не содержит аминокислотную последовательность легкой цепи, изложенную в таблице 2, например, аминокислотную последовательность под SEQ ID NO: 49, 58, 60 или 62.
При использовании в данном документе процентная идентичность двух последовательностей зависит от числа идентичных положений, общих для последовательностей (т. е. % идентичность равняется числу идентичных положений/общее число положений x 100), при этом учитывается число гэпов и длина каждого гэпа, которые необходимо ввести для оптимального выравнивания двух последовательностей. Сравнение последовательностей и определение процентной идентичности двух последовательностей можно осуществлять с применением математического алгоритма, описанного в неограничивающих примерах ниже.
В качестве дополнения или альтернативы, последовательности белка по настоящему изобретению также можно применять в качестве "запрашиваемой последовательности" для проведения поиска в общедоступных базах данных, например, для идентификации родственных последовательностей. Например, такие поиски можно проводить с применением программы BLAST (версия 2.0) Altschul, et al., 1990 J.Mol. Biol. 215:403-10.
Антитела с консервативными модификациями
В определенных вариантах осуществления антитело по настоящему изобретению имеет вариабельную область тяжелой цепи, содержащую последовательности CDR1, CDR2 и CDR3, и вариабельную область легкой цепи, содержащую последовательности CDR1, CDR2 и CDR3, при этом одна или несколько из этих последовательностей CDR имеют определенные аминокислотные последовательности, основанные на антителах, описанных в данном документе, или их консервативные модификации, и при этом антитела сохраняют требуемые функциональные свойства β-клото-связывающих антител по настоящему изобретению.
Соответственно, в настоящем изобретении предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1с или повышать его активность) или его антигенсвязывающий фрагмент, состоящие из вариабельной области тяжелой цепи, содержащей последовательности CDR1, CDR2 и CDR3, и вариабельной области легкой цепи, содержащей последовательности CDR1, CDR2 и CDR3, при этом аминокислотные последовательности CDR1 вариабельной области тяжелой цепи выбраны из группы, состоящей из SEQ ID NO: 6 и ее консервативных модификаций; аминокислотные последовательности CDR2 вариабельной области тяжелой цепи выбраны из группы, состоящей из SEQ ID NO: 7 и ее консервативных модификаций; аминокислотные последовательности CDR3 вариабельной области тяжелой цепи выбраны из группы, состоящей из SEQ ID NO: 8 и ее консервативных модификаций; аминокислотные последовательности CDR1 вариабельной области легкой цепи выбраны из группы, состоящей из SEQ ID NO: 19 и 31 и их консервативных модификаций; аминокислотные последовательности CDR2 вариабельной области легкой цепи выбраны из группы, состоящей из SEQ ID NO: 20 и ее консервативных модификаций; аминокислотные последовательности CDR3 вариабельной области легкой цепи выбраны из группы, состоящей из SEQ ID NO: 21 и ее консервативных модификаций; и антитело или его антигенсвязывающие фрагменты специфически связываются с β-клото.
Соответственно, в настоящем изобретении предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1с или повышать его активность) или его антигенсвязывающий фрагмент, состоящие из вариабельной области тяжелой цепи, содержащей последовательности CDR1, CDR2 и CDR3, и вариабельной области легкой цепи, содержащей последовательности CDR1, CDR2 и CDR3, при этом аминокислотные последовательности CDR1 вариабельной области тяжелой цепи выбраны из группы, состоящей из SEQ ID NO: 6, 9, 10 и 12 и их консервативных модификаций; аминокислотные последовательности CDR2 вариабельной области тяжелой цепи выбраны из группы, состоящей из SEQ ID NO: 7, 11 и 13 и их консервативных модификаций; аминокислотные последовательности CDR3 вариабельной области тяжелой цепи выбраны из группы, состоящей из SEQ ID NO: 8 и 14 и их консервативных модификаций; аминокислотные последовательности CDR1 вариабельной области легкой цепи выбраны из группы, состоящей из SEQ ID NO: 19, 31, 22 и 25 и их консервативных модификаций; аминокислотные последовательности CDR2 вариабельной области легкой цепи выбраны из группы, состоящей из SEQ ID NO: 20 и 23 и их консервативных модификаций; аминокислотные последовательности CDR3 вариабельной области легкой цепи выбраны из группы, состоящей из SEQ ID NO: 21 или 24 и их консервативных модификаций; и антитело или его антигенсвязывающие фрагменты специфически связываются с β-клото.
В одном аспекте в настоящем изобретении предусмотрено выделенное антитело, оптимизированное для экспрессии в клетке млекопитающего, содержащее вариабельную область тяжелой цепи и вариабельную область легкой цепи, при этом вариабельная область тяжелой цепи имеет аминокислотные последовательности, выбранные из группы из SEQ ID NO: 15 и их консервативных модификаций; и полноразмерная легкая цепь имеет аминокислотные последовательности, выбранные из группы из SEQ ID NO: 26 или 32 и их консервативных модификаций; и антитело специфически связывается с β-клото (например, β-клото человека и яванского макака), и при этом вариабельная область тяжелой цепи не содержит аминокислотную последовательность вариабельной области тяжелой цепи, изложенную в таблице 2, например, аминокислотную последовательность под SEQ ID NO: 43 или 55, и вариабельный домен легкой цепи не содержит аминокислотную последовательность вариабельной области легкой цепи, изложенную в таблице 2, например, аминокислотную последовательность под SEQ ID NO: 47 или 57.
В других вариантах осуществления антитело по настоящему изобретению, оптимизированное для экспрессии в клетке млекопитающего, имеет последовательность полноразмерной тяжелой цепи и последовательность полноразмерной легкой цепи, при этом одна или несколько из этих последовательностей имеют определенные аминокислотные последовательности на основе антител, описанных в данном документе, или их консервативные модификации, и при этом антитела сохраняют требуемые функциональные свойства β-клото-связывающих антител по настоящему изобретению. Соответственно, в настоящем изобретении предусмотрено выделенное антитело, оптимизированное для экспрессии в клетке млекопитающего, состоящее из полноразмерной тяжелой цепи и полноразмерной легкой цепи, где полноразмерная тяжелая цепь имеет аминокислотные последовательности, выбранные из группы из SEQ ID NO: 17 и ее консервативных модификаций; и полноразмерная легкая цепь имеет аминокислотные последовательности, выбранные из группы из SEQ ID NO: 28 или 34 и их консервативных модификаций; и антитело специфически связывается с β-клото (например, β-клото человека и яванского макака), и при этом тяжелая цепь не содержит аминокислотную последовательность тяжелой цепи, изложенную в таблице 2, например, аминокислотную последовательность под SEQ ID NO: 45, 56, 59 или 61, и легкая цепь не содержит аминокислотную последовательность легкой цепи, изложенную в таблице 2, например, аминокислотную последовательность под SEQ ID NO: 49, 58, 60 или 62.
Антитела, которые связываются с одним и тем же эпитопом(эпитопами) или которые конкурируют за один и тот же эпитоп(эпитопы)
В настоящем изобретении предусмотрены антитела (например, антитела, способные активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность), которые связываются с тем же эпитопом, что и β-клото-связывающие антитела, описанные в таблице 1 (например, NOV005 или NOV006). В определенном аспекте такие антитела и антигенсвязывающие фрагменты способны повышать активность β-клото и FGFR1c. Таким образом, дополнительные антитела могут быть идентифицированы на основании их способности конкурировать (например, конкурентно подавлять связывание статистически значимым образом) с другими антителами по настоящему изобретению в анализах связывания β-клото (таких, как описанные в примерах). Способность исследуемого антитела подавлять связывание антител по настоящему изобретению с белком β-клото демонстрирует, что исследуемое антитело может конкурировать с этим антителом за связывание с β-клото; такое антитело может в соответствии с неограничивающей теорией связываться с тем же самым или родственным (например, структурно аналогичным или пространственно проксимальным) эпитопом белка β-клото, что и антитело, с которым оно конкурирует. В определенном варианте осуществления антитело, которое связывается с тем же эпитопом на β-клото, что и антитела по настоящему изобретению, представляет собой человеческое моноклональное антитело. Такие моноклональные антитела человека можно получать и выделять, как описано в данном документе. При использовании в данном документе антитело "конкурирует" за связывание, когда конкурирующее антитело подавляет связывание с β-клото антитела или антигенсвязывающего фрагмента по настоящему изобретению на более чем 50% (например, 80%, 85%, 90%, 95%, 98% или 99%) в присутствии эквимолярной концентрации конкурирующего антитела. В определенном варианте осуществления антитело, которое связывается с тем же эпитопом на β-клото, что и антитела по настоящему изобретению, представляет собой гуманизированное моноклональное антитело. Такие гуманизированные моноклональные антитела можно получать и выделять, как описано в данном документе.
В определенном аспекте в настоящем изобретении предусмотрены антитела (например, антитела, способные активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность), которые связываются с тем же эпитопом, что и β-клото-связывающее антитело NOV005 или NOV006.
В определенном аспекте в настоящем изобретении предусмотрены антитела (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность), которые связываются с тем же эпитопом, что и β-клото-связывающее антитело, которое содержит вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 15, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 26 или 32.
В определенном аспекте в настоящем изобретении предусмотрены антитела (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность), которые связываются с тем же эпитопом, что и β-клото-связывающее антитело, которое содержит вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 15, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 26.
В определенном аспекте в настоящем изобретении предусмотрены антитела, которые связываются с тем же эпитопом, что и β-клото-связывающее антитело, которое содержит вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 15, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 32.
В определенном аспекте в настоящем изобретении предусмотрены антитела (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность), которые связываются с тем же перекрывающимся эпитопом, что и β-клото-связывающее антитело NOV005 или NOV006.
В определенном аспекте в настоящем изобретении предусмотрены антитела (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность), которые связываются с тем же перекрывающимся эпитопом, что и β-клото-связывающее антитело, которое содержит вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 15, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 26 или 32.
В определенном аспекте в настоящем изобретении предусмотрены антитела (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность), которые связываются с тем же перекрывающимся эпитопом, что и β-клото-связывающее антитело, которое содержит вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 15, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 26.
В определенном аспекте в настоящем изобретении предусмотрены антитела (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность), которые связываются с тем же перекрывающимся эпитопом, что и β-клото-связывающее антитело, которое содержит вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 15, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 32.
В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото, при этом указанный эпитоп содержит одну или несколько аминокислот из остатков 246-265 последовательности β-клото (SEQ ID NO: 52). В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото, при этом указанный эпитоп содержит одну или несколько аминокислот из остатков 536-550 последовательности β-клото (SEQ ID NO:52). В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото, при этом указанный эпитоп содержит одну или несколько аминокислот из остатков 834-857 последовательности β-клото (SEQ ID NO:52). В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото, при этом указанный эпитоп содержит одну или несколько аминокислот из остатков 959-986 последовательности β-клото (SEQ ID NO:52).
В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото, при этом указанный эпитоп содержит одну или несколько аминокислот из остатков 246-265, 536-550, 834-857 и 959-986 последовательности β-клото (SEQ ID NO:52). В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото, при этом указанный эпитоп содержит две или более аминокислот из остатков 246-265, 536-550, 834-857 и 959-986 последовательности β-клото (SEQ ID NO:52). В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото, при этом указанный эпитоп содержит три или более аминокислот из остатков 246-265, 536-550, 834-857 и 959-986 последовательности β-клото (SEQ ID NO:52). В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото, при этом указанный эпитоп содержит аминокислоты из остатков 246-265, 536-550, 834-857 и 959-986 последовательности β-клото (SEQ ID NO:52). В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с эпитопом β-клото, при этом указанный эпитоп содержит по меньшей мере один аминокислотный остаток из каждого из следующих отрезков аминокислотных остатков: 246-265, 536-550, 834-857 и 959-986 последовательности β-клото (SEQ ID NO:52).
В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с одним или несколькими эпитопами β-клото, при этом указанные эпитопы содержат одну или несколько аминокислот из остатков 646-670 последовательности β-клото (SEQ ID NO:52). В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с одним или несколькими эпитопами β-клото, при этом указанные эпитопы содержат одну или несколько аминокислот из остатков 696-700 последовательности β-клото (SEQ ID NO:52). В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с одним или несколькими эпитопами β-клото, при этом указанные эпитопы содержат одну или несколько аминокислот из остатков 646-689 последовательности β-клото (SEQ ID NO:52).
В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с одним или несколькими эпитопами (например, прерывистыми эпитопами) β-клото, при этом указанные эпитопы содержат одну, или две, или три, или четыре, или пять, или более аминокислот из остатков 646-670, 696-700 и 646-689 последовательности β-клото (SEQ ID NO:52). В определенном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с двумя или более эпитопами (например, прерывистыми эпитопами) β-клото, при этом указанные эпитопы содержат одну или несколько аминокислот из остатков 646-670, 696-700 и 646-689 последовательности β-клото (SEQ ID NO:52). В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с тремя или более эпитопами (например, прерывистыми эпитопами) β-клото, при этом указанные эпитопы содержат одну или более аминокислот из остатков 646-670, 696-700 и 646-689 последовательности β-клото (SEQ ID NO:52). В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с тремя или более эпитопами (например, прерывистыми эпитопами) β-клото, при этом указанные эпитопы содержат аминокислоты из остатков 646-670, 696-700 и 646-689 последовательности β-клото (SEQ ID NO:52). В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с тремя или более эпитопами (например, прерывистыми эпитопами) β-клото, при этом указанные эпитопы содержат аминокислотные остатки из каждого из следующих диапазонов аминокислотных остатков: 646-670, 696-700 и 646-689 последовательности β-клото (SEQ ID NO:52).
В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые обеспечивают защиту, определенную с помощью водородно-дейтериевого обмена (HDx), одного, двух, трех, четырех, пяти или более из следующих пептидов β-клото (SEQ ID NO: 52): аминокислотные остатки 245-266, 246-265, 343-349, 344-349, 421-429, 488-498, 509-524, 536-550, 568-576, 646-669, 646-670, 696-700, 773-804, 834-857, и 959-986.
В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые обеспечивают защиту, определенную с помощью водородно-дейтериевого обмена (HDx), следующих пептидов β-клото (SEQ ID NO: 52): аминокислотные остатки 246-265, 536-550, 834-857 и 959-986.
В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые обеспечивают защиту, определенную с помощью водородно-дейтериевого обмена (HDx), следующих пептидов β-клото (SEQ ID NO: 52): аминокислотные остатки 245-266, 246-265, 343-349, 344-349, 421-429, 488-498, 509-524, 536-550, 568-576, 646-669, 646-670, 696-700, 773-804, 834-857, и 959-986.
В определенных аспектах в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые повышают активность β-клото и FGFR1c, при этом антитело или его антигенсвязывающий фрагмент не контактируют с остатками 701 (Tyr) или 703 (Arg) β-клото человека (SEQ ID NO: 52).
В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с β-клото, при этом указанное антитело или его антигенсвязывающий фрагмент контактируют с одной или несколькими аминокислотами из остатков 246-265 последовательности β-клото (SEQ ID NO: 52), например, как определено с помощью рентгеноструктурной кристаллографии, анализа водородно-дейтериевого обмена или сканирующего мутагенеза. В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с β-клото, при этом указанное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент контактируют с одной или несколькими аминокислотами из остатков 536-550 последовательности β-клото (SEQ ID NO:52), например, как определено с помощью рентгеноструктурной кристаллографии, анализа водородно-дейтериевого обмена или сканирующего мутагенеза. В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с β-клото, при этом указанное антитело или его антигенсвязывающий фрагмент контактируют с одной или несколькими аминокислотами из остатков 834-857 последовательности β-клото (SEQ ID NO:52), например, как определено с помощью рентгеноструктурной кристаллографии, анализа водородно-дейтериевого обмена или сканирующего мутагенеза. В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с β-клото, при этом указанное антитело или его антигенсвязывающий фрагмент контактируют с одной или несколькими аминокислотами из остатков 959-986 последовательности β-клото (SEQ ID NO:52), например, как определено с помощью рентгеноструктурной кристаллографии, анализа водородно-дейтериевого обмена или сканирующего мутагенеза.
В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с β-клото, при этом указанное антитело или его антигенсвязывающий фрагмент контактируют с одной или несколькими аминокислотами из остатков 246-265, 536-550, 834-857 и 959-986 последовательности β-клото (SEQ ID NO:52), например, как определено с помощью рентгеноструктурной кристаллографии, анализа водородно-дейтериевого обмена или сканирующего мутагенеза. В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с β-клото, при этом указанное антитело или его антигенсвязывающий фрагмент контактируют с двумя или более аминокислотами из остатков 246-265, 536-550, 834-857 и 959-986 последовательности β-клото (SEQ ID NO:52), например, как определено с помощью рентгеноструктурной кристаллографии, анализа водородно-дейтериевого обмена или сканирующего мутагенеза. В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с β-клото, при этом указанное антитело или его антигенсвязывающий фрагмент контактируют с тремя или более аминокислотами из остатков 246-265, 536-550, 834-857 и 959-986 последовательности β-клото (SEQ ID NO:52), например, как определено с помощью рентгеноструктурной кристаллографии, анализа водородно-дейтериевого обмена или сканирующего мутагенеза. В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с β-клото, при этом указанное антитело или его антигенсвязывающий фрагмент контактируют с аминокислотами из остатков 246-265, 536-550, 834-857 и 959-986 последовательности β-клото (SEQ ID NO:52), например, как определено с помощью рентгеноструктурной кристаллографии, анализа водородно-дейтериевого обмена или сканирующего мутагенеза. В конкретных аспектах в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с β-клото, при этом указанное антитело или его антигенсвязывающий фрагмент контактируют с по меньшей мере одним аминокислотным остатком из каждого из следующих отрезков аминокислотных остатков: 246-265, 536-550, 834-857 и 959-986 последовательности β-клото (SEQ ID NO:52), например, как определено с помощью рентгеноструктурной кристаллографии, анализа водородно-дейтериевого обмена или сканирующего мутагенеза.
В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с β-клото, при этом указанное антитело или его антигенсвязывающий фрагмент контактируют с одной или несколькими аминокислотами из остатков 646-670 последовательности β-клото (SEQ ID NO:52), например, как определено с помощью рентгеноструктурной кристаллографии, анализа водородно-дейтериевого обмена или сканирующего мутагенеза. В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с β-клото, при этом указанное антитело или его антигенсвязывающий фрагмент контактируют с одной или несколькими аминокислотами из остатков 696-700 последовательности β-клото (SEQ ID NO:52), например, как определено с помощью рентгеноструктурной кристаллографии, анализа водородно-дейтериевого обмена или сканирующего мутагенеза. В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с β-клото, при этом указанное антитело или его антигенсвязывающий фрагмент контактируют с одной или несколькими аминокислотами из остатков 646-689 последовательности β-клото (SEQ ID NO:52), например, как определено с помощью рентгеноструктурной кристаллографии, анализа водородно-дейтериевого обмена или сканирующего мутагенеза.
В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с β-клото, при этом указанное антитело или его антигенсвязывающий фрагмент контактируют с одной, или двумя, или тремя, или четырьмя, или пятью или более аминокислотами из остатков 646-670, 696-700 и 646-689 последовательности β-клото (SEQ ID NO:52), например, как определено с помощью рентгеноструктурной кристаллографии, анализа водородно-дейтериевого обмена или сканирующего мутагенеза. В определенном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с β-клото, при этом указанное антитело или его антигенсвязывающий фрагмент контактируют с одним или несколькими аминокислотными остатками из каждого из следующих отрезков аминокислотных остатков 646-670, 696-700 и 646-689 последовательности β-клото (SEQ ID NO:52), например, как определено с помощью рентгеноструктурной кристаллографии, анализа водородно-дейтериевого обмена или сканирующего мутагенеза. В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с β-клото, при этом указанное антитело или его антигенсвязывающий фрагмент контактируют с одним или несколькими аминокислотными остатками из каждого из отрезков аминокислотных остатков 646-670, 696-700 и 646-689 последовательности β-клото (SEQ ID NO:52), например, как определено с помощью рентгеноструктурной кристаллографии, анализа водородно-дейтериевого обмена или сканирующего мутагенеза. В конкретном аспекте в данном документе предусмотрено выделенное антитело (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность) или его антигенсвязывающий фрагмент, которые связываются с β-клото, при этом указанное антитело или его антигенсвязывающий фрагмент контактируют с аминокислотными остатками 646-670, 696-700 и 646-689 последовательности β-клото (SEQ ID NO:52), например, как определено с помощью рентгеноструктурной кристаллографии, анализа водородно-дейтериевого обмена или сканирующего мутагенеза.
В конкретном аспекте в настоящем изобретении предусмотрены антитела (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность), которые конкурируют с антителом NOV005 или NOV006 за связывание с β-клото.
В конкретном аспекте в настоящем изобретении предусмотрены антитела (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность), которые конкурируют за связывание с β-клото с β-клото-связывающим антителом, которое содержит вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 15, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 26 или 32.
В конкретном аспекте в настоящем изобретении предусмотрены антитела (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность), которые конкурируют за связывание с β-клото с β-клото-связывающим антителом, которое содержит вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 15, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 26.
В конкретном аспекте в настоящем изобретении предусмотрены антитела (например, антитело, способное активировать рецепторный комплекс β-клото/FGFR1c или повышать его активность), которые конкурируют за связывание с β-клото с β-клото-связывающим антителом, которое содержит вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность под SEQ ID NO: 15, и вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность под SEQ ID NO: 32.
Сконструированные и модифицированные антитела
Антитело (например, NOV005 или NOV006) по настоящему изобретению также можно получить с применением антитела, имеющего одну или несколько из последовательностей VH и/или VL, показанных в данном документе, в качестве исходного материала для конструирования модифицированного антитела, причем данное модифицированное антитело может иметь измененные свойства исходного антитела. Антитело может быть сконструировано посредством модификации одного или нескольких остатков в пределах одной или обоих вариабельных областей (т. е. VH и/или VL), например, в пределах одной или нескольких CDR-областей и/или в пределах одной или нескольких каркасных областей. Дополнительно или в качестве альтернативы, антитело может быть сконструировано посредством модификации остатков в константной(константных) области(областях), например, для изменения эффекторной (эффекторных) функции(функций) антитела.
Один тип конструирования вариабельной области, который можно осуществлять, представляет собой прививку CDR. Антитела взаимодействуют с целевыми антигенами преимущественно посредством аминокислотных остатков, которые расположены в шести определяющих комплементарность областях (CDR) тяжелой и легкой цепей. По этой причине аминокислотные последовательности в пределах CDR являются более разнообразными у отдельных антител, чем последовательности за пределами CDR. Поскольку последовательности CDR отвечают за большинство взаимодействий антитело-антиген, можно экспрессировать рекомбинантные антитела, которые имитируют свойства конкретных встречающихся в природе антител, посредством конструирования векторов экспрессии, которые содержат последовательности CDR из конкретного встречающегося в природе антитела, привитые на каркасные последовательности из отличающегося антитела с отличающимися свойствами (см., например, Riechmann, L. et al., 1998 Nature 332:323-327; Jones, P. et al., 1986 Nature 321:522-525; Queen, C. et al., 1989 Proc. Natl. Acad., U.S.A. 86:10029-10033; патент США № 5225539 за авторством Winter, и патенты США №№ 5530101; 5585089; 5693762 и 6180370 за авторством Queen et al.).
Соответственно, другой вариант осуществления настоящего изобретения относится к выделенному антителу или его антигенсвязывающему фрагменту, содержащим вариабельную область тяжелой цепи, которая содержит последовательности CDR1, имеющие аминокислотную последовательность, выбранную из последовательностей HCDR1, изложенных в таблице 1; последовательности CDR2, имеющие аминокислотную последовательность, выбранную из последовательностей HCDR2, изложенных в таблице 1; последовательности CDR3, имеющие аминокислотную последовательность, выбранную из последовательностей HCDR3, изложенных в таблице 1; и вариабельную область легкой цепи, которая содержит последовательности CDR1, имеющие аминокислотную последовательность, выбранную из последовательностей LCDR1, изложенных в таблице 1; последовательности CDR2, имеющие аминокислотную последовательность, выбранную из последовательностей LCDR2, изложенных в таблице 1; последовательности CDR3, имеющие аминокислотную последовательность, выбранную из последовательностей LCDR3, изложенных в таблице 1. Таким образом, такие антитела содержат последовательности CDR VH и VL моноклональных антител, но могут содержать и различные каркасные последовательности из этих антител.
Соответственно, другой вариант осуществления настоящего изобретения относится к выделенному антителу или его антигенсвязывающему фрагменту, предусматривающим вариабельную область тяжелой цепи, которая содержит последовательности CDR1, содержащие аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 6 и 9; последовательности CDR2, содержащие аминокислотную последовательность под SEQ ID NO: 7; последовательности CDR3, содержащие аминокислотную последовательность под SEQ ID NO: 8; и вариабельную область легкой цепи, которая содержит последовательности CDR1, содержащие аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 19 и 31; последовательности CDR2, содержащие аминокислотную последовательность под SEQ ID NO: 20; и последовательности CDR3, содержащие аминокислотную последовательность под SEQ ID NO: 21. Таким образом, такие антитела содержат последовательности CDR VH и VL моноклональных антител, но могут содержать и различные каркасные последовательности из этих антител.
Такие каркасные последовательности можно получить из общедоступных баз данных ДНК или опубликованных источников, которые включают последовательности генов зародышевой линии антител. Например, последовательности ДНК зародышевой линии для генов вариабельной области тяжелой и легкой цепей человека можно найти в базе данных последовательностей зародышевой линии человека "VBase" (доступной во всемирной сети по адресу mrc-cpe.cam.ac.uk/vbase), а также в Kabat, E. A., et al., 1991 Sequences of Proteins of Immunological Interest, Fifth Edition, U.S. Department of Health and Human Services, NIH Publication No. 91-3242; Tomlinson, I. M., et al., 1992 J. Mol. Biol. 227:776-798; и Cox, J. P. L. et al., 1994 Eur. J Immunol. 24:827-836; содержание каждого из которых прямо включено в данный документ посредством ссылки.
Примером каркасных последовательностей для применения в антителах по настоящему изобретению являются последовательности, которые являются структурно подобными каркасным последовательностям, применяемым в выбранных антителах по настоящему изобретению, например, консенсусные последовательности и/или каркасные последовательности, применяемые в моноклональных антителах по настоящему изобретению. Последовательности CDR1, 2 и 3 VH и последовательности CDR1, 2 и 3 VL могут быть привиты на каркасные области, которые имеют последовательность, идентичную той, что обнаруживается в гене зародышевой линии иммуноглобулина, из которого получена каркасная последовательность, или последовательности CDR могут быть привиты на каркасные области, которые содержат одну или несколько мутаций по сравнению с последовательностями зародышевой линии. Например, было обнаружено, что в определенных случаях благоприятным является мутирование остатков в пределах каркасных областей для сохранения или повышения способности к связыванию антигена антителом (см., например, патенты США №№ 5530101; 5585089; 5693762 и 6180370 за авторством Queen et al). Каркасные области, которые можно применять в качестве остовов для построения антител и антигенсвязывающих фрагментов, описанных в данном документе, включают в себя без ограничения VH1A, VH1B, VH3, Vk1, Vl2 и Vk2. Дополнительные каркасные области известны в данной области техники, и их можно найти, например, в базе данных vBase во всемирной сети по адресу vbase.mrc-cpe.cam.ac.uk/index.php?&MMN_position=1:1.
Соответственно, вариант осуществления настоящего изобретения относится к выделенным β-клото-связывающим антителам или их антигенсвязывающим фрагментам, содержащим вариабельную область тяжелой цепи, которая содержит аминокислотную последовательность под SEQ ID NO: 15 или аминокислотную последовательность, имеющую одну, две, три, четыре или пять аминокислотных замен, делеций или добавлений в каркасной области таких последовательностей, и дополнительно содержащим вариабельную область легкой цепи, которая имеет аминокислотную последовательность, выбранную из группы, состоящей из SEQ ID NO: 26 или 32, или аминокислотную последовательность, имеющую одну, две, три, четыре или пять аминокислотных замен, делеций или добавлений в каркасной области таких последовательностей, при этом вариабельная область тяжелой цепи не содержит аминокислотную последовательность вариабельной области тяжелой цепи, изложенную в таблице 2, например, аминокислотную последовательностью под SEQ ID NO: 43 или 55, и вариабельный домен легкой цепи не содержит аминокислотную последовательность вариабельной области легкой цепи, изложенную в таблице 2, например, аминокислотную последовательность под SEQ ID NO: 47 или 57.
Другой тип модификации вариабельной области заключается в мутировании аминокислотных остатков в пределах областей CDR1, CDR2 и/или CDR3 VH и/или VL с улучшением таким образом одного или нескольких свойств связывания (например, аффинности) антитела, представляющего интерес, известном как "созревание аффинности". Для введения мутации(-й) можно осуществлять сайт-направленный мутагенез или ПЦР-опосредованный мутагенез, и эффект в отношении связывания антитела или другого функционального свойства, представляющего интерес, можно оценивать в анализах in vitro или in vivo, описанных в данном документе и представленных в примерах. Можно вводить консервативные модификации (которые обсуждаются выше). Мутации могут представлять собой замены, добавления или делеции аминокислот. Более того, как правило, изменяют не более одного, двух, трех, четырех или пяти остатков в пределах CDR-области.
Известно, что некоторые мотивы аминокислотных последовательностей подвергали посттрансляционной модификации (PTM), такой как гликозилирование (т. е. NxS/T, x любой, кроме P), окисление свободных цистеиновых остатков, дезамидирование (например NG) или изомеризация (например, DG). В случае присутствия в областях CDR такие мотивы идеально удаляются посредством сайт-направленного мутагенеза с целью повышения гомогенности продукта.
Способ созревания аффинности хорошо описан в уровне техники. Среди многих систем дисплея фаговый дисплей (Smith GP (1985) Science 228:1315-1317) и дисплей на эукариотических клетках, таких как дрожжевые грибы (Boder ET and Wittrup KD (1997) Nature Biotechnology 15: 553-557), по видимому, являются наиболее широко применяемыми системами для отбора при взаимодействии антиген-антитело. Преимущества таких дисплейных систем заключаются в том, что они подходят для широкого диапазона антигенов и что строгость условий отбора можно легко регулировать. При фаговом дисплее можно проводить дисплей фрагментов scFv или Fab, а при дрожжевом дисплее, кроме того, полноразмерных IgG. Данные широко применяемые способы позволяют осуществлять отбор требуемых вариантов антитела из больших библиотек с разнообразием, составляющим более 10E7. Для библиотек с меньшим разнообразием, например, 10E3, можно проводить скрининг посредством микроэкспрессии и ELISA.
Библиотеки с нецелевыми или случайными вариантами антител можно получать, например, с помощью ПЦР сниженной точности (Cadwell RC and Joyce GF (1994) Mutagenic PCR. PCR Methods Appl. 3: S136-S140), и она обеспечивает очень простой, но иногда ограниченный подход. Другой стратегией является CDR-направленная диверсификация антитела-кандидата. На одно или несколько положений в одной или нескольких CDR можно специфически целенаправленно воздействовать с помощью, например, вырожденных олигонуклеотидов (Thompson J et al. (1996) J.Mol.Biol. 256: 77-88), тринуклеотидного мутагенеза (TRIM) (Kayushin AL et al. (1996) Nucleic Acids Res. 24: 3748-3755) или любого другого подхода, известного в данной области техники.
Соответственно, в другом варианте осуществления в настоящем изобретении предусмотрены выделенные β-клото-связывающие антитела или их антигенсвязывающие фрагменты, состоящие из вариабельной области тяжелой цепи, имеющей область CDR1 VH, состоящую из аминокислотной последовательности, выбранной из группы, содержащей SEQ ID NO: 6 и 9, или аминокислотной последовательности, имеющей одну, две, три, четыре или пять аминокислотных замен, делеций или добавлений по сравнению с SEQ ID NO: 6 и 9; область CDR2 VH, характеризующуюся аминокислотной последовательностью под SEQ ID NO: 7 или аминокислотной последовательностью, имеющей одну, две, три, четыре или пять аминокислотных замен, делеций или добавлений по сравнению с SEQ ID NO: 7; область CDR3 VH, характеризующуюся аминокислотной последовательностью под SEQ ID NO: 8 или аминокислотной последовательностью, имеющей одну, две, три, четыре или пять аминокислотных замен, делеций или добавлений по сравнению с SEQ ID NO: 8; область CDR1 VL, характеризующуюся аминокислотной последовательностью, выбранной из группы, состоящей из SEQ ID NO: 19 или 31, или аминокислотной последовательностью, имеющей одну, две, три, четыре или пять аминокислотных замен, делеций или добавлений по сравнению с SEQ ID NO: 19 или 31; область CDR2 VL, характеризующуюся аминокислотной последовательностью под SEQ ID NO: 20 или аминокислотной последовательностью, имеющей одну, две, три, четыре или пять аминокислотных замен, делеций или добавлений по сравнению с SEQ ID NO: 20; область CDR3 VL, характеризующуюся аминокислотной последовательностью под SEQ ID NO: 21 или аминокислотной последовательностью, имеющей одну, две, три, четыре или пять аминокислотных замен, делеций или добавлений по сравнению с SEQ ID NO: 21.
Прививка антигенсвязывающих доменов на альтернативные каркасы или остовы
Можно применять широкий спектр каркасов или остовов антитела/иммуноглобулина при условии, что полученный в результате полипептид содержит по меньшей мере одну связывающую область, которая специфически связывается с β-клото. Такие каркасы или остовы включают 5 основных идиотипов иммуноглобулинов человека или их фрагментов и включают иммуноглобулины других видов животных, предпочтительно имеющие гуманизированные составляющие. Антитела с одной тяжелой цепью, такие как идентифицированные у верблюдовых, представляют особый интерес в этом отношении. Специалисты в данной области техники продолжают открывать и разрабатывать новые каркасы, остовы и фрагменты.
В одном аспекте настоящее изобретение относится к получению антител, отличных от иммуноглобулинов, с применением остовов, отличных от иммуноглобулинов, на которые можно привить CDR по настоящему изобретению. Можно применять известные или будущие каркасы и остовы, отличные от иммуноглобулинов, при условии, что они содержат связывающую область, специфичную в отношении целевого белка β-клото. Известные каркасы или остовы, отличные от иммуноглобулинов, включают без ограничения фибронектин (Compound Therapeutics, Inc., Уолтем, Массачусетс), анкирин (Molecular Partners AG, Цюрих, Швейцария), доменные антитела (Domantis, Ltd., Кембридж, Массачусетс и Ablynx nv, Звейнарде, Бельгия), липокалин (Pieris Proteolab AG, Фрайзинг, Германия), небольшие модульные иммунофармацевтические средства (Trubion Pharmaceuticals Inc., Сиэтл, Вашингтон), макситела (Avidia, Inc., Маунтин-Вью, Калифорния), белок A (Affibody AG, Швеция) и аффилин (гамма-кристаллин или убиквитин) (SciI Proteins GmbH, Галле, Германия).
Фибронектиновые остовы имеют в основе домен фибронектина типа III (например, десятый модуль фибронектина типа III (10 домен Fn3)). Домен фибронектина типа III имеет 7 или 8 бета-тяжей, которые распределены между двумя складчатыми бета-слоями, которые сами располагаются между друг другом, образуя сердцевину белка, и дополнительно содержит петли (аналогичные CDR), которые соединяют бета-тяжи друг с другом и являются доступными для растворителя. По меньшей мере три такие петли присутствуют на каждом краю сэндвича из складчатых бета-слоев, где край представляет собой границу белка, перпендикулярную направлению складчатых бета-слоев (см. патент США № 6818418). Эти остовы на основе фибронектина не являются иммуноглобулином, хотя общая укладка очень напоминает таковую у наименьшего функционального фрагмента антитела, вариабельной области тяжелой цепи, которая содержит полную единицу распознавания антигена в IgG верблюда и ламы. Благодаря этой структуре антитело, отличное от иммуноглобулина, имитирует свойства связывания антигена, которые являются подобными по своей природе и аффинности свойствам антител. Эти остовы можно применять в стратегии рандомизации и шаффлинга петель in vitro, которая является подобной процессу созревания аффинности антител in vivo. Эти молекулы на основе фибронектина можно применять в качестве остовов, при этом области петель молекулы могут быть заменены на CDR по настоящему изобретению с применением стандартных методик клонирования.
Анкириновая технология основывается на применении белков с полученными из анкириновых повторов модулями в качестве остовов для переноса вариабельных участков, которые можно применять для связывания с различными мишенями. Модуль с анкириновым повтором представляет собой полипептид из 33 аминокислот, состоящий из двух антипараллельных α-спиралей и β-изгиба. Связывание вариабельных областей в основном оптимизируют путем применения рибосомного дисплея.
Авимеры получают из природного белка, содержащего A-домен, такого как LRP-1. Эти домены используются по своей природе для белок-белковых взаимодействий, и у человека более 250 белков имеют в основе структуры A-домены. Авимеры состоят из ряда различных мономеров (2-10) "A-домена", связанных посредством аминокислотных линкеров. Авимеры, которые могут связываться с целевым антигеном, можно создавать с применением методики, описанной, например, в публикациях заявок на патент США №№ 20040175756; 20050053973; 20050048512 и 20060008844.
Аффинные лиганды, аффитела, представляют собой небольшие простые белки, состоящие из трехспирального пучка на основе остова из одного из связывающих IgG доменов белка A. Белок A представляет собой поверхностный белок бактерии Staphylococcus aureus. Этот домен остова состоит из 58 аминокислот, 13 из которых рандомизируют для создания библиотек аффител с большим количеством вариантов лигандов (см., например, патент США № 5831012). Молекулы аффител имитируют антитела, они имеют молекулярную массу 6 кДа в сравнении с молекулярной массой антител, которая составляет 150 кДа. Несмотря на свой небольшой размер, сайт связывания в молекулах аффител является подобным таковому у антитела.
Антикалины представляют собой продукты, разработанные компанией Pieris ProteoLab AG. Их получают из липокалинов, распространенной группы небольших и устойчивых белков, которые обычно вовлечены в физиологический транспорт или запасание химически чувствительных или нерастворимых соединений. Несколько природных липокалинов встречаются в тканях или биологических жидкостях человека. Структура белка напоминает иммуноглобулины с гипервариабельными петлями сверху на жестком каркасе. Тем не менее, в противоположность антителам или их рекомбинантным фрагментам липокалины состоят из одной полипептидной цепи с 160-180 аминокислотными остатками, при этом они лишь незначительно больше, чем один домен иммуноглобулина. Набор из четырех петель, которые образуют связывающий карман, проявляет выраженную структурную пластичность и допускает наличие ряда боковых цепей. Таким образом, сайт связывания можно видоизменить в запатентованном способе для того, чтобы распознавать заданные целевые молекулы различной формы с высокой аффинностью и специфичностью. Один белок семейства липокалинов, белок, связывающий билин (BBP), из Pieris Brassicae применяли для разработки антикалинов посредством осуществления мутагенеза набора из четырех петель. Одним примером патентной заявки, в которой описываются антикалины, является публикация согласно PCT № WO 199916873.
Молекулы аффилина представляют собой небольшие белки, отличные от иммуноглобулина, которые сконструированы с конкретными видами аффинности в отношении белков и малых молекул. Новые молекулы аффилина можно очень быстро выбрать из двух библиотек, каждая из которых имеет в основе отличающийся каркасный белок, происходящий от человека. Молекулы аффилина не проявляют какой-либо структурной гомологии с белками, представляющими собой иммуноглобулины. В настоящее время применяют два аффилиновых остова, один из которых представляет собой гамма-кристаллин, структурный белок хрусталика глаза человека, а другой представляет собой белок суперсемейства "убиквитинов". Оба остова человека являются весьма небольшими, проявляют стабильность при высокой температуре и являются наиболее устойчивыми к изменениям pH и денатурирующим средствам. Эта высокая стабильность в основном обусловлена развернутой бета-складчатой структурой белков. Примеры белков, полученных из гамма-кристаллина, описаны в WO200104144, а примеры "убиквитин-подобных" белков описаны в WO2004106368.
Миметики эпитопов белков (PEM) представляют собой циклические пептидоподобные молекулы среднего размера (MW 1-2 кДа), имитирующие бета-шпилечные вторичные структуры белков, основную вторичную структуру, вовлеченную в белок-белковые взаимодействия.
В настоящем изобретении предусмотрены полностью человеческие антитела, которые специфически связываются с белком β-клото. В определенных аспектах, по сравнению с химерными или гуманизированными антителами, β-клото-связывающие антитела человека по настоящему изобретению дополнительно характеризуются пониженной антигенностью при введении субъектам-людям.
Антитела верблюдовых
Белки, представляющие собой антитела, полученные из представителей семейства, к которому относятся двугорбые верблюды и одногорбые верблюды (Camelus bactrianus и Calelus dromaderius), в том числе представителей из видов Нового Света, таких как виды лам (Lama paccos, Lama glama и Lama vicugna), были охарактеризованы в отношении размера, сложности структуры и антигенности в отношении субъектов-людей. У определенных антител IgG этого семейства млекопитающих, которые обнаруживаются в природе, отсутствуют легкие цепи, и, следовательно, они отличаются в плане структуры от типичной четырехцепочечной четвертичной структуры, характеризующейся двумя тяжелыми и двумя легкими цепями, у антител от других животных. См. PCT/EP93/02214 (WO 94/04678, опубликованную 3 марта 1994 года).
Область антитела верблюдовых, которая представляет собой небольшой отдельный вариабельный домен, идентифицированный как VHH, можно получить с помощью генной инженерии с получением небольшого белка, характеризующегося высокой аффинностью в отношении мишени, что приводит в результате к полученному из антитела белку с низкой молекулярной массой, известному как "нанотело верблюдовых". См. патент США № 5759808, выданный 2 июня 1998 года; см. также Stijlemans, B. et al., 2004 J Biol Chem 279: 1256-1261; Dumoulin, M. et al., 2003 Nature 424: 783-788; Pleschberger, et al. 2003 Bioconjugate Chem 14: 440-448; Cortez-Retamozo, V. et al. 2002 Int J Cancer 89: 456-62; и Lauwereys, M. et al. 1998 EMBO J 17: 3512-3520. Сконструированные библиотеки антител верблюдовых и фрагментов антител являются коммерчески доступными, например, от Ablynx, Гент, Бельгия. Как и в случае других антител, происходящих из организма, отличного от человека, аминокислотную последовательность антитела верблюдовых можно изменить рекомбинантным способом с получением последовательности, которая более точно напоминает последовательность человека, т. е. нанотело можно "гуманизировать". Таким образом можно дополнительно снизить природную низкую антигенность антител верблюдовых у людей.
Нанотело верблюдовых имеет молекулярную массу, составляющую примерно одну десятую от массы молекулы IgG человека, и белок имеет физический диаметр лишь несколько нанометров. Одним следствием небольшого размера является способность нанотел верблюдовых связываться с сайтами антигенов, которые являются функционально невидимыми для белков, представляющих собой антитела большего размера, т. е. нанотела верблюдовых являются применимыми в качестве реагентов для выявления антигенов, которые в ином случае являются скрытыми при использовании классических иммунологических методик, и в качестве возможных терапевтических средств. Таким образом, еще одним следствием небольшого размера является то, что нанотело верблюдовых может осуществлять ингибирование в результате связывания с конкретным сайтом в бороздке или узком углублении целевого белка и, следовательно, может служить в качестве, которое более точно походит на функцию классического низкомолекулярного лекарственного средства, чем таковую у классического антитела.
Низкая молекулярная масса и компактный размер дополнительно приводят к тому, что нанотела верблюдовых являются чрезвычайно термостабильными, устойчивыми к экстремальным значениям pH и к протеолитическому расщеплению и характеризуются слабой антигенностью. Другим следствием является то, что нанотела верблюдовых легко перемещаются из кровеносной системы в ткани и даже пересекают гематоэнцефалический барьер и могут обеспечивать лечение нарушений, которые поражают нервную ткань. Нанотела могут дополнительно способствовать транспорту лекарственного средства через гематоэнцефалический барьер. См. заявку на патент США 20040161738, опубликованную 19 августа 2004 года. Эти признаки в сочетании с низкой антигенностью у людей указывают на большой терапевтический потенциал. Кроме того, эти молекулы можно полностью экспрессировать в прокариотических клетках, таких как E. coli, и они экспрессируются в виде слитых белков с использованием бактериофага и являются функциональными.
Соответственно, признаком настоящего изобретения является антитело или нанотело верблюдовых, характеризующееся специфической аффинностью в отношении β-клото (например, β-клото человека). В определенных вариантах осуществления в данном документе антитело или нанотело верблюдовых продуцируется в естественных условиях у животного семейства верблюдовых, т. е. оно продуцируется верблюдовыми после иммунизации с помощью β-клото или фрагмента его пептида при применении методик, описанных в данном документе для других антител. В качестве альтернативы β-клото-связывающее нанотело верблюдовых конструируют, т. е. получают посредством отбора, например, из библиотеки фагов, на которых проявляются подвергнутые соответствующему мутагенезу белки, представляющие собой нанотела верблюдовых, с применением процедур пэннинга с β-клото в качестве мишени, как описано в примерах в данном документе. Сконструированные нанотела можно дополнительно адаптировать к конкретным требованиям с помощью генной инженерии так, чтобы они имели период полужизни у субъекта-реципиента от 45 минут до двух недель. В конкретном варианте осуществления антитело или нанотело верблюдовых получают посредством прививки последовательностей CDR тяжелой или легкой цепи антител человека по настоящему изобретению на каркасные последовательности нанотела или однодоменного антитела, как описано, например, в PCT/EP93/02214.
БИСПЕЦИФИЧЕСКИЕ МОЛЕКУЛЫ И МУЛЬТИВАЛЕНТНЫЕ АНТИТЕЛА
В другом аспекте в настоящем изобретении описаны биспецифические или мультиспецифические молекулы, содержащие β-клото-связывающее антитело или его фрагмент по настоящему изобретению, например, антитело NOV005 или NOV006. Антитело по настоящему изобретению или его антигенсвязывающие области можно дериватизировать или связать с другой функциональной молекулой, например, с другим пептидом или белком (например, другим антителом или лигандом рецептора) с получением биспецифической молекулы, которая связывается с по меньшей мере двумя различными сайтами связывания или целевыми молекулами. Антитело по настоящему изобретению, по существу, можно дериватизировать или связать с более чем одной другой функциональной молекулой с получением мультиспецифических молекул, которые связываются с более чем двумя различными сайтами связывания и/или целевыми молекулами; также предполагается, что такие мультиспецифические молекулы охватываются используемым в данном документе термином "биспецифическая молекула". Для создания биспецифической молекулы по настоящему изобретению антитело по настоящему изобретению можно функционально связать (например, посредством химического связывания, генетического слияния, нековалентного соединения или иным образом) с одной или несколькими другими связывающими молекулами, как, например, другое антитело, фрагмент антитела, пептид или связывающий миметик, в результате чего получают биспецифическую молекулу.
Соответственно, настоящее изобретение включает биспецифические молекулы, содержащие по меньшей мере один первый элемент, обеспечивающий специфичность связывания в отношении β-клото, и второй элемент, обеспечивающий специфичность связывания в отношении второго целевого эпитопа. Например, второй целевой эпитоп представляет собой другой эпитоп β-клото, отличающийся от первого целевого эпитопа.
Кроме того, в случае настоящего изобретения, в котором биспецифическая молекула является мультиспецифической, молекула может дополнительно включать третий элемент, обеспечивающий специфичность связывания, в дополнение к таковым в отношении первого и второго целевых эпитопов.
В одном аспекте биспецифические молекулы по настоящему изобретению содержат в качестве элемента, обеспечивающего специфичность связывания, по меньшей мере одно антитело или его фрагмент антитела, в том числе, например, Fab, Fab', F(ab')2, Fv или одноцепочечный Fv. Антитело также может представлять собой димер легких цепей или тяжелых цепей или любой их минимальный фрагмент, такой как Fv или одноцепочечная конструкция, которая описана в Ladner et al., патент США № 4946778.
Диатела представляют собой бивалентные биспецифические молекулы, в которых домены VH и VL экспрессируются на одной полипептидной цепи, соединенные линкером, который является слишком коротким для того, чтобы обеспечить возможность спаривания между двумя доменами на одной и той же цепи. Домены VH и VL образуют пары с комплементарными доменами другой цепи, таким образом образуя два сайта связывания антигена (см., например, Holliger et al., 1993 Proc. Natl. Acad. Sci. USA 90:6444-6448; Poljak et al., 1994 Structure 2:1121-1123). Диатела можно получать посредством экспрессии двух полипептидных цепей либо со структурой VHA-VLB и VHB-VLA (конфигурация VH-VL), либо VLA-VHB и VLB-VHA (конфигурация VL-VH) в одной и той же клетке. Большинство из них могут экспрессироваться в растворимой форме в бактериях. Одноцепочечные диатела (scDb) получают путем соединения двух образующих диатело полипептидных цепей с линкером из примерно 15 аминокислотных остатков (см. Holliger and Winter, 1997 Cancer Immunol. Immunother., 45(3-4):128-30; Wu et al., 1996 Immunotechnology, 2(1):21-36). scDb могут экспрессироваться в бактериях в растворимой активной мономерной форме (см. Holliger and Winter, 1997 Cancer Immunol. Immunother., 45(34): 128-30; Wu et al., 1996 Immunotechnology, 2(1):21-36; Pluckthun and Pack, 1997 Immunotechnology, 3(2): 83-105; Ridgway et al., 1996 Protein Eng., 9(7):617-21). Диатело можно сливать с Fc с получением "ди-диатела" (см. Lu et al., 2004 J. Biol. Chem., 279(4):2856-65).
Другие антитела, которые могут применяться в биспецифических молекулах по настоящему изобретению, представляют собой мышиные, химерные и гуманизированные моноклональные антитела.
Биспецифические молекулы можно получить посредством конъюгирования составляющих элементов, обеспечивающих специфичность связывания, с помощью способов, известных в данной области техники. Например, каждый элемент, обеспечивающий специфичность связывания, в биспецифической молекуле можно получить отдельно, а затем конъюгировать друг с другом. Если элементы, обеспечивающие специфичность связывания, представляют собой белки или пептиды, ряд связывающих или сшивающих средств можно применять для ковалентного конъюгирования. Примеры сшивающих средств включают белок A, карбодиимид, N-сукцинимидил-S-ацетилтиоацетат (SATA), 5,5'-дитиобис(2-нитробензойную кислоту) (DTNB), о-фенилендималеимид (oPDM), N-сукцинимидил-3-(2-пиридилдитио)пропионат (SPDP) и сульфосукцинимидил-4-(N-малеимидометил)циклогексан-1-карбоксилат (сульфо-SMCC) (см., например, Karpovsky et al., 1984 J. Exp. Med. 160:1686; Liu, MA et al., 1985 Proc. Natl. Acad. Sci. USA 82:8648). Другие способы включают способы, описанные в Paulus, 1985 Behring Ins. Mitt. No. 78,118-132; Brennan et al., 1985 Science 229:81-83), и Glennie et al., 1987 J. Immunol. 139: 2367-2375). Конъюгирующие средства представляют собой SATA и сульфо-SMCC, оба из них доступны от Pierce Chemical Co. (Рокфорд, Иллинойс).
Если элементы, обеспечивающие специфичность связывания, представляют собой антитела, их можно конъюгировать путем связывания посредством сульфгидрильной группы C-концевых шарнирных областей двух тяжелых цепей. В конкретном варианте осуществления шарнирную область модифицируют таким образом, чтобы она содержала нечетное количество остатков с сульфгидрильной группой, например, один, перед конъюгированием.
В качестве альтернативы оба элемента, обеспечивающие специфичность связывания, могут быть закодированы в одном векторе и могут экспрессироваться и собираться в одной клетке-хозяине. Этот способ является особенно применимым в случае, когда биспецифическая молекула представляет собой слитый белок mAb x mAb, mAb x Fab, Fab x F(ab')2 или лиганд x Fab. Биспецифическая молекула по настоящему изобретению может представлять собой одноцепочечную молекулу, содержащую одно одноцепочечное антитело и связывающую детерминанту, или одноцепочечную биспецифическую молекулу, содержащую две связывающие детерминанты. Биспецифические молекулы могут содержать по меньшей мере две одноцепочечные молекулы. Способы получения биспецифических молекул описаны, например, в патенте США № 5260203; патенте США № 5455030; патенте США № 4881175; патенте США № 5132405; патенте США № 5091513; патенте США № 5476786; патенте США № 5013653; патенте США № 5258498 и патенте США № 5482858.
Связывание биспецифических молекул со своими специфическими мишенями можно подтвердить, например, с помощью твердофазного иммуноферментного анализа (ELISA), радиоиммунологического анализа (REA), FACS-анализа, биологического анализа (например, подавления роста) или анализа посредством вестерн-блоттинга. В каждом из этих анализов обычно выявляют наличие комплексов белок-антитело, представляющих особый интерес, путем использования меченого реагента (например, антитела), специфичного в отношении комплекса, представляющего интерес.
В другом аспекте настоящее изобретение предусматривает мультивалентные соединения, содержащие по меньшей мере две идентичные или отличающиеся антигенсвязывающие части антител по настоящему изобретению, связывающиеся с β-клото. Антигенсвязывающие части могут быть связаны вместе посредством слияния белков или ковалентной или нековалентной связи. В качестве альтернативы способы связывания были описаны для биспецифических молекул. Тетравалентные соединения можно получить, например, путем сшивания антител из антител по настоящему изобретению с антителом, которое связывается с константными областями антител по настоящему изобретению, например, Fc или шарнирной областью.
Тримеризующий домен описан, например, в патенте EP 1012280B1, принадлежащем Borean. Пентамеризующие модули описаны, например, в PCT/EP97/05897.
Антитела с увеличенным периодом полужизни
В настоящем изобретении предусмотрены антитела (например, NOV005 или NOV006), которые специфически связываются с белком β-клото, что характеризуются увеличенным периодом полужизни in vivo.
Многие факторы могут влиять на период полужизни белка in vivo. Например, фильтрация в почках, метаболизм в печени, разрушение посредством протеолитических ферментов (протеаз) и иммунные ответы (например, нейтрализация белка посредством антител и поглощение макрофагами и дендритными клетками). Для увеличения периода полужизни антител по настоящему изобретению можно применять ряд стратегий. Например, химическое связывание с полиэтиленгликолем (PEG), reCODE PEG, остовом антитела, полисиаловой кислотой (PSA), гидроксиэтилкрахмалом (HES), альбуминсвязывающими лигандами и углеводными защитными фрагментами; генетическое слияние с белками, связывающимися с белками сыворотки крови, такими как альбумин, IgG, FcRn, и перенос; соединение (генетическое или химическое) с другими связывающими фрагментами, которые связываются с белками сыворотки крови, такими как нанотела, молекулы Fab, молекулы DARPin, авимеры, аффитела и антикалины; генетическое слияние с rPEG, альбумином, доменом альбумина, альбуминсвязывающими белками и Fc; или включение в наноносители, составы с медленным высвобождением или медицинские устройства.
Для продления циркуляции антител в сыворотке крови in vivo молекулы инертного полимера, такого как высокомолекулярный PEG, могут быть присоединены к антителам или их фрагментам с помощью многофункционального линкера или без него посредством сайт-специфической конъюгации PEG с N- или С-концом антител либо посредством эпсилон-аминогрупп, присутствующих в лизиновых остатках. Для пегилирования антитела антитело или его фрагмент, как правило, вводят в реакцию с полиэтиленгликолем (PEG), таким как реакционноспособный сложный эфир или альдегидное производное PEG, в условиях, при которых одна или несколько групп PEG присоединяются к антителу или фрагменту антитела. Пегилирование можно осуществлять посредством реакции ацилирования или реакции алкилирования с реакционноспособной молекулой PEG (или аналогичным реакционноспособным водорастворимым полимером). Предполагается, что используемый в данном документе термин "полиэтиленгликоль" охватывает любую из форм PEG, которые применяли для дериватизации других белков, как, например, моно(C1-C10)алокси- или арилоксиполиэтиленгликоль или полиэтиленгликоль-малеимид. В определенных вариантах осуществления антитело, подлежащее пегилированию, представляет собой агликозилированное антитело. Будет применяться дериватизация с помощью линейного или разветвленного полимера, которая приводит к минимальной потере биологической активности. Степень конъюгации можно тщательно контролировать посредством SDS-PAGE и масс-спектрометрии для обеспечения надлежащей конъюгации молекул PEG с антителами. Непрореагировавший PEG можно отделить от конъюгатов антитело-PEG посредством эксклюзионной или ионообменной хроматографии. PEG-дериватизированные антитела можно тестировать в отношении связывающей активности, а также в отношении эффективности in vivo с применением способов, хорошо известных специалистам в данной области техники, например, посредством иммуноанализов, описанных в данном документе. Способы пегилирования белков известны в данной области техники и могут применяться по отношению к антителам по настоящему изобретению. См., например, EP 0154316 за авторством Nishimura et al. и EP 0401384 за авторством Ishikawa et al.
Другие модифицированные технологии пегилирования включают технологию направленного конструирования, которая обеспечивает химическую ортогональность с использованием преобразованной системы биосинтеза (ReCODE PEG), при которой химически специфические боковые цепи включаются в биосинтетические белки посредством преобразованной системы, которая включает синтетазу tRNA и tRNA. Данная технология позволяет включать более чем 30 новых аминокислот в биосинтетические белки в E. coli, дрожжах и клетках млекопитающих. tRNA включает не встречающуюся в природе аминокислоту в любом месте, где расположен терминирующий кодон, преобразовывая кодон из терминирующего в такой, который передает сигнал о включении химически специфической аминокислоты.
Технология рекомбинантного пегилирования (rPEG) также может применяться для увеличения периода полужизни в сыворотке крови. Данная технология предусматривает генетическое слияние хвоста белка из 300-600 аминокислот произвольной структуры с существующим фармацевтическим белком. Поскольку кажущаяся молекулярная масса такой белковой цепи произвольной структуры в приблизительно 15 раз превышает ее фактическую молекулярную массу, период полужизни белка в сыворотке крови значительно увеличивается. В отличие от традиционного пегилирования, для которого требуется химическая конъюгация и повторная очистка, способ изготовления значительно упрощается, и продукт является однородным.
Полисиалирование представляет собой другую технологию, в которой используется природный полимер, полисиаловая кислота (PSA), для продления срока действия и улучшения стабильности терапевтических пептидов и белков. PSA представляет собой полимер сиаловой кислоты (сахар). При применении для доставки лекарственного средства на основе белка и терапевтического пептида полисиаловая кислота обеспечивает защитную микросреду при конъюгации. Это увеличивает срок действия терапевтического белка в кровотоке и предотвращает его распознавание иммунной системой. Полимер, представляющий собой PSA, в естественных условиях обнаруживается в организме человека. Он был усвоен некоторыми бактериями, которые эволюционировали на протяжении миллионов лет с покрытием их стенок им. Данные полисиалированные в естественных условиях бактерии затем были способны благодаря молекулярной мимикрии противодействовать защитной системе организма. PSA, которую можно отнести к совершенной природной технологии малозаметности, можно с легкостью получить из таких бактерий в больших количествах и с заданными физическими характеристиками. Бактериальная PSA является полностью неимуногенной, даже когда связана с белками, так как она является химически идентичной PSA в организме человека.
Другая технология предусматривает применение производных гидроксиэтилкрахмала ("HES"), связанных с антителами. HES представляет собой модифицированный природный полимер, полученный из крахмала восковой кукурузы, и может быть метаболизирован посредством ферментов организма. Растворы HES обычно вводят для восполнения недостающего объема крови и улучшения реологических свойств крови. Модифицирование антитела с помощью HES позволяет продлить период полужизни в кровотоке за счет увеличения стабильности молекулы, а также за счет уменьшения почечного очищения, что приводит к увеличению биологической активности. Изменяя различные параметры, такие как молекулярная масса HES, можно адаптировать к конкретным требованиям широкий спектр конъюгатов HES-антитело.
Антитела, характеризующиеся увеличенным периодом полужизни in vivo, также можно получить путем введения одной или нескольких аминокислотных модификаций (т. е. замен, вставок или делеций) в константный домен IgG или его связывающий FcRn фрагмент (предпочтительно Fc или шарнирный фрагмент Fc домена). См., например, международную публикацию № WO 98/23289; международную публикацию № WO 97/34631 и патент США № 6277375.
Кроме того, антитела можно конъюгировать с альбумином (например, сывороточным альбумином человека; HSA), чтобы сделать антитело или фрагмент антитела более стабильными in vivo или чтобы они характеризовались более длительным периодом полужизни in vivo. Методики являются хорошо известными из уровня техники, см., например, международные публикации №№ WO 93/15199, WO 93/15200 и WO 01/77137 и европейский патент № EP 413622. Кроме того, в контексте биспецифического антитела, описанного выше, элементы, обеспечивающие специфичность антител, могут быть сконструированы таким образом, что один связывающий домен антитела связывается с FGF21, в то время как второй связывающий домен антитела связывается с сывороточным альбумином, предпочтительно HSA.
Стратегии по увеличению периода полужизни являются особенно применимыми для нанотел, связующих молекул на основе фибронектина и других антител или белков, для которых требуется увеличенный период полужизни in vivo.
КОНЪЮГАТЫ АНТИТЕЛ
В настоящем изобретении предусмотрены антитела или их фрагменты, которые специфически связываются с белком β-клото, слитые с помощью рекомбинантного способа или химически конъюгированные (в том числе посредством как ковалентного, так и нековалентного способов конъюгирования) с гетерологичным белком или полипептидом (или его фрагментом, предпочтительно с полипептидом из по меньшей мере 10, по меньшей мере 20, по меньшей мере 30, по меньшей мере 40, по меньшей мере 50, по меньшей мере 60, по меньшей мере 70, по меньшей мере 80, по меньшей мере 90 или по меньшей мере 100 аминокислот) с получением слитых белков. В частности, в настоящем изобретении предусмотрены слитые белки, содержащие антигенсвязывающий фрагмент (например, Fab-фрагмент, Fd-фрагмент, Fv-фрагмент, F(ab)2-фрагмент, VH-домен, CDR VH, VL-домен или CDR VL) антитела, описанного в данном документе, например, NOV005 или NOV006, и гетерологичный белок, полипептид или пептид. Способы слияния или конъюгирования белков, полипептидов или пептидов с антителом или фрагментом антитела известны из уровня техники. См., например, патенты США №№ 5336603, 5622929, 5359046, 5349053, 5447851 и 5112946; европейские патенты №№ EP 307434 и EP 367166; международные публикации №№ WO 96/04388 и WO 91/06570; Ashkenazi et al., 1991, Proc. Natl. Acad. Sci. USA 88: 10535-10539; Zheng et al., 1995, J. Immunol. 154:5590-5600; и Vil et al., 1992, Proc. Natl. Acad. Sci. USA 89:11337- 11341.
Дополнительные слитые белки можно создать посредством методик шаффлинга генов, шаффлинга мотивов, шаффлинга экзонов и/или шаффлинга кодонов (совокупно называемых "шаффлингом ДНК"). Шаффлинг ДНК можно применять для изменения активности антител по настоящему изобретению или их фрагментов (например, получения антител или их фрагментов с более высокими уровнями аффинности и более низкими значениями скорости диссоциации). См., в целом, патенты США №№ 5605793, 5811238, 5830721, 5834252 и 5837458; Patten et al., 1997, Curr. Opinion Biotechnol. 8:724-33; Harayama, 1998 Trends Biotechnol. 16(2):76-82; Hansson et al., 1999, J. Mol. Biol. 287:265-76; и Lorenzo and Blasco, 1998, Biotechniques 24(2):308-313 (каждый из данных патентов и публикаций тем самым включен посредством ссылки во всей своей полноте). Антитела или их фрагменты, или кодируемые антитела или их фрагменты можно изменять путем воздействия на них случайного мутагенеза с помощью ПЦР с внесением ошибок, случайной вставки нуклеотидов или других способов до проведения рекомбинации. Полинуклеотид, кодирующий антитело или его фрагмент, которые специфически связываются с белком β-клото, может быть подвергнут рекомбинации с одним или несколькими компонентами, мотивами, секциями, частями, доменами, фрагментами и т. д. одной или нескольких гетерологичных молекул.
Более того, антитела или их фрагменты можно слить с маркерными последовательностями, таким как пептид, для облегчения очистки. В предпочтительных вариантах осуществления маркерная аминокислотная последовательность представляет собой гексагистидиновый пептид (SEQ ID NO: 64), такой как метка, предусмотренная в векторе pQE (QIAGEN, Inc., 9259 Eton Avenue, Чатсворт, Калифорния, 91311), среди прочих, многие из которых являются коммерчески доступными. Как описано в Gentz et al., 1989, Proc. Natl. Acad. Sci. USA 86:821-824, например, гексагистидин (SEQ ID NO: 64) обеспечивает удобную очистку слитого белка. Другие пептидные метки, применимые для очистки, включают без ограничения гемагглютининовую ("HA") метку, которая соответствует эпитопу, полученному из белка гемагглютинина вируса гриппа (Wilson et al., 1984, Cell 37:767), и метку "flag".
В других вариантах осуществления антитела по настоящему изобретению или их фрагменты конъюгированы с диагностическим или выявляемым средством. Такие антитела могут быть применимыми для контроля или прогнозирования начала проявления, развития, прогрессирования и/или степени тяжести заболевания или нарушения в рамках процедуры клинического тестирования, такой как определение эффективности конкретной терапии. Такую диагностику и выявление можно осуществлять посредством связывания антитела с выявляемыми веществами, в том числе без ограничения с различными ферментами, такими как без ограничения пероксидаза хрена, щелочная фосфатаза, бета-галактозидаза или ацетилхолинтрансфераза; простетическими группами, такими как без ограничения стрептавидин/биотин и авидин/биотин; флуоресцентными материалами, такими как без ограничения умбеллиферон, флуоресцеин, флуоресцеин-изотиоцианат, родамин, дихлортриазиниламин-флуоресценин, дансил-хлорид или фикоэритрин; люминесцентными материалами, такими как без ограничения люминол; биолюминесцентными материалами, такими как без ограничения люцифераза, люциферин и экворин; радиоактивными материалами, такими как без ограничения йод (131I, 125I, 123I и 121I), углерод (14C), сера (35S), тритий (3H), индий (115In, 113In, 112In и 111In), технеций (99Tc), таллий (201Ti), галлий (68Ga, 67Ga), палладий (103Pd), молибден (99Mo), ксенон (133Xe), фтор (18F), 153Sm, 177Lu, 159Gd, 149Pm, 140La, 175Yb, 166Ho, 90Y, 47Sc, 186Re, 188Re, 142Pr, 105Rh, 97Ru, 68Ge, 57Co, 65Zn, 85Sr, 32P, 153Gd, 169Yb, 51Cr, 54Mn, 75Se, 113Sn и 117Олово; и позитронно-активными металлами, применяющимися в различных методах позитронно-эмиссионной томографии, и ионами нерадиоактивных парамагнитных металлов.
В настоящем изобретении дополнительно охвачены пути применения антител и их фрагментов, конъюгированных с терапевтическим фрагментом. Антитело или его фрагмент могут быть конъюгированы с терапевтическим фрагментом, таким как цитотоксин, например, цитостатическое или цитоцидное средство, терапевтическое средство или ион радиоактивного металла, например, излучатели альфа-частиц. Цитотоксин или цитотоксическое средство включает любое средство, которое является пагубным для клеток.
Кроме того, антитело или его фрагмент могут быть конъюгированы с терапевтическим фрагментом или фрагментом, представляющим собой лекарственное средство, который модифицирует заданный биологический ответ. Терапевтические фрагменты или фрагменты, представляющие собой лекарственные средства, не следует рассматривать как ограниченные классическими химическими терапевтическими средствами. Например, фрагмент, представляющий собой лекарственное средство, может представлять собой белок, пептид или полипептид, обладающие требуемой биологической активностью. Такие белки могут включать, например, токсин, такой как абрин, рицин A, экзотоксин Pseudomonas, холерный токсин или дифтерийный токсин; белок, такой как фактор некроза опухоли, α-интерферон, β-интерферон, фактор роста нервов, фактор роста тромбоцитов, тканевой активатор плазминогена, апоптическое средство, антиангиогенное средство; или модификатор биологического ответа, такой как, например, лимфокин.
Более того, антитело можно конъюгировать с терапевтическими фрагментами, такими как ион радиоактивного металла, такого как излучатели альфа-частиц, как например, 213Bi, или с макроциклическими хелаторами, пригодными для конъюгирования ионов радиоактивных металлов, в том числе без ограничения 131In, 131LU, 131Y, 131Ho, 131Sm, с полипептидами. В некоторых вариантах осуществления макроциклический хелатор представляет собой 1,4,7,10-тетраазациклододекан-N,N',N'',N'''-тетрауксусную кислоту (DOTA), которая может быть прикреплена к антителу через линкерную молекулу. Такие линкерные молекулы широко известны из уровня техники и описаны в Denardo et al., 1998, Clin Cancer Res. 4(10):2483-90; Peterson et al., (1999) Bioconjug. Chem. 10(4):553-7; и Zimmerman et al., 1999, Nucl. Med. Biol. 26(8):943-50, каждый из которых включен посредством ссылки во всей своей полноте.
Методики конъюгирования терапевтических фрагментов с антителами являются хорошо известными, см., например, Amon et al., "Monoclonal Antibodies For Immunotargeting Of Drugs In Cancer Therapy", в Monoclonal Antibodies And Cancer Therapy, Reisfeld et al. (eds.), pp. 243-56 (Alan R. Liss, Inc. 1985); Hellstrom et al., "Antibodies For Drug Delivery", в Controlled Drug Delivery (2nd Ed.), Robinson et al. (eds.), pp. 623-53 (Marcel Dekker, Inc. 1987); Thorpe, "Antibody Carriers Of Cytotoxic Agents In Cancer Therapy: A Review", в Monoclonal Antibodies 84: Biological And Clinical Applications, Pinchera et al. (eds.), pp. 475-506 (1985); "Analysis, Results, And Future Prospective Of The Therapeutic Use Of Radiolabeled Antibody In Cancer Therapy", в Monoclonal Antibodies For Cancer Detection And Therapy, Baldwin et al. (eds.), pp. 303-16 (Academic Press 1985), и Thorpe et al., 1982, Immunol. Rev. 62:119-58.
Антитела также могут быть прикреплены к твердым подложкам, которые являются особенно применимыми для иммунологических анализов или очистки целевого антигена. Такие твердые подложки включают без ограничения стекло, целлюлозу, полиакриламид, нейлон, полистирол, поливинилхлорид или полипропилен.
Способы получения антител
Нуклеиновые кислоты, кодирующие антитела
В настоящем изобретении предусмотрены по существу очищенные молекулы нуклеиновой кислоты, которые кодируют полипептиды, содержащие вышеописанные сегменты или домены цепей β-клото-связывающего антитела. Некоторые из нуклеиновых кислот по настоящему изобретению содержат нуклеотидную последовательность, кодирующую вариабельную область тяжелой цепи, показанную в SEQ ID NO: 15, и/или нуклеотидную последовательность, кодирующую вариабельную область легкой цепи, показанную в SEQ ID NO: 26 или 32. В конкретном аспекте молекулы нуклеиновой кислоты, предусмотренные в данном документе, представляют собой молекулы, определенные в таблице 1, например, молекулы нуклеиновой кислоты, содержащие последовательность под SEQ ID NO: 16, 36 или 38, кодирующую VH, или молекулы нуклеиновой кислоты, содержащие последовательность под SEQ ID NO: 27, 54, 33 или 40, кодирующую VL. Некоторые другие молекулы нуклеиновой кислоты по настоящему изобретению содержат нуклеотидные последовательности, которые являются по существу идентичными (например, на по меньшей мере 65, 80%, 95% или 99%) нуклеотидным последовательностям, определенным в таблице 1, например, молекулы нуклеиновой кислоты, содержащие последовательность под SEQ ID NO: 16, 36 или 38, кодирующую VH, или молекулы нуклеиновой кислоты, содержащие последовательность под SEQ ID NO: 27, 54, 33 или 40, кодирующую VL. При экспрессии с соответствующих векторов экспрессии полипептиды, кодируемые этими полинуклеотидами, способны проявлять способность к связыванию антигена FGF21.
В данном документе также предусмотрены полинуклеотиды, которые кодируют все или по существу все из последовательности вариабельной области тяжелой цепи и/или легкой цепи β-клото-связывающего антитела, изложенного в данном документе, например, полинуклеотиды, изложенные в таблице 1. В конкретных аспектах в настоящем изобретении предусмотрены полинуклеотиды, которые кодируют все или по существу все из VH и/или VL β-клото-связывающего антитела NOV005. В конкретных аспектах в настоящем изобретении предусмотрены полинуклеотиды, которые кодируют все или по существу все из тяжелой цепи и/или легкой цепи β-клото-связывающего антитела NOV005. В конкретных аспектах в настоящем изобретении предусмотрены полинуклеотиды, которые кодируют все или по существу все из VH и/или VL β-клото-связывающего антитела NOV006. В конкретных аспектах в настоящем изобретении предусмотрены полинуклеотиды, которые кодируют все или по существу все из тяжелой цепи и/или легкой цепи β-клото-связывающего антитела NOV006.
Вследствие вырожденности кода ряд последовательностей нуклеиновой кислоты будут кодировать каждую из аминокислотных последовательностей иммуноглобулина. Например, SEQ ID NO: 16 и 36 представляют собой две последовательности нуклеиновой кислоты, которые кодируют VH NOV005, и SEQ ID NO: 27 и 54 представляют собой две последовательности нуклеиновой кислоты, которые кодируют VL NOV005.
Молекулы нуклеиновой кислоты по настоящему изобретению могут кодировать как вариабельную область, так и константную область антитела. Некоторые из последовательностей нуклеиновой кислоты по настоящему изобретению содержат нуклеотиды, кодирующие последовательность тяжелой цепи, которая является по существу идентичной (например, на по меньшей мере 80%, 90% или 99%) последовательности тяжелой цепи, изложенной в SEQ ID NO: 17. Некоторые другие последовательности нуклеиновой кислоты содержат нуклеотиды, кодирующие последовательность легкой цепи, которая является по существу идентичной (например, на по меньшей мере 80%, 90% или 99%) последовательности легкой цепи, изложенной в SEQ ID NO: 28 или 34. В конкретных аспектах молекулы нуклеиновой кислоты, предусмотренные в данном документе, представляют собой молекулы, определенные в таблице 1, например, молекулы нуклеиновой кислоты, содержащие последовательность под SEQ ID NO: 18, 37, 30 или 39, кодирующую тяжелую цепь, или молекулы нуклеиновой кислоты, содержащие последовательность под SEQ ID NO: 29, 51, 35 или 41, кодирующую легкую цепь.
В конкретном аспекте в данном документе предусмотрен полинуклеотид, содержащий последовательность нуклеиновой кислоты под SEQ ID NO: 16, кодирующую VH. В конкретном аспекте в данном документе предусмотрен полинуклеотид, содержащий последовательность нуклеиновой кислоты под SEQ ID NO: 36, кодирующую VH. В конкретном аспекте в данном документе предусмотрен полинуклеотид, содержащий последовательность нуклеиновой кислоты под SEQ ID NO: 38, кодирующую VH. В конкретном аспекте в данном документе предусмотрен полинуклеотид, содержащий последовательность нуклеиновой кислоты под SEQ ID NO: 27, кодирующую VL. В конкретном аспекте в данном документе предусмотрен полинуклеотид, содержащий последовательность нуклеиновой кислоты под SEQ ID NO: 54, кодирующую VL. В конкретном аспекте в данном документе предусмотрен полинуклеотид, содержащий последовательность нуклеиновой кислоты под SEQ ID NO: 29, кодирующую VL. В конкретном аспекте в данном документе предусмотрен полинуклеотид, содержащий последовательность нуклеиновой кислоты под SEQ ID NO: 51, кодирующую VL.
В конкретном аспекте в данном документе предусмотрен полинуклеотид, содержащий последовательность нуклеиновой кислоты под SEQ ID NO: 18, кодирующую тяжелую цепь. В конкретном аспекте в данном документе предусмотрен полинуклеотид, содержащий последовательность нуклеиновой кислоты под SEQ ID NO: 37, кодирующую тяжелую цепь. В конкретном аспекте в данном документе предусмотрен полинуклеотид, содержащий последовательность нуклеиновой кислоты под SEQ ID NO: 30, кодирующую тяжелую цепь. В конкретном аспекте в данном документе предусмотрен полинуклеотид, содержащий последовательность нуклеиновой кислоты под SEQ ID NO: 39, кодирующую тяжелую цепь.
В конкретном аспекте в данном документе предусмотрен полинуклеотид, содержащий последовательность нуклеиновой кислоты под SEQ ID NO: 29, кодирующую легкую цепь. В конкретном аспекте в данном документе предусмотрен полинуклеотид, содержащий последовательность нуклеиновой кислоты под SEQ ID NO: 51, кодирующую легкую цепь. В конкретном аспекте в данном документе предусмотрен полинуклеотид, содержащий последовательность нуклеиновой кислоты под SEQ ID NO: 35, кодирующую легкую цепь. В конкретном аспекте в данном документе предусмотрен полинуклеотид, содержащий последовательность нуклеиновой кислоты под SEQ ID NO: 41, кодирующую легкую цепь.
Полинуклеотидные последовательности можно получать с помощью твердофазного синтеза ДНК de novo или с помощью ПЦР-мутагенеза существующей последовательности (например, последовательностей, которые описаны в примерах ниже), кодирующей β-клото-связывающее антитело или его связывающий фрагмент. Прямой химический синтез нуклеиновых кислот можно осуществлять с помощью способов, известных из уровня техники, таких как фосфотриэфирный способ из Narang et al., 1979, Meth. Enzymol. 68:90; фосфодиэфирный способ из Brown et al., Meth. Enzymol. 68:109, 1979; диэтилфосфорамидитный способ из Beaucage et al., Tetra Lett., 22:1859, 1981; и способ с использованием твердой подложки из патента США № 4458066. Введение мутаций в последовательность полинуклеотида с помощью ПЦР можно осуществлять, как описано, например, в PCR Technology: Principles and Applications for DNA Amplification, H.A. Erlich (Ed.), Freeman Press, NY, NY, 1992; PCR Protocols: A Guide to Methods and Applications, Innis et al. (Ed.), Academic Press, San Diego, CA, 1990; Mattila et al., Nucleic Acids Res. 19:967, 1991; и Eckert et al., PCR Methods and Applications 1:17, 1991.
Также в настоящем изобретении предусмотрены векторы экспрессии и клетки-хозяева для получения β-клото-связывающих антител, описанных в данном документе, например, NOV005 или NOV006. Различные векторы экспрессии можно применять для экспрессии полинуклеотидов, кодирующих цепи или связывающие фрагменты β-клото-связывающих антител. Как вирусные, так и невирусные векторы экспрессии можно применять для продуцирования антител в клетке-хозяине млекопитающего. Невирусные векторы и системы включают плазмиды, эписомные векторы, как правило, с кассетой экспрессии для экспрессии белка или РНК, а также искусственные человеческие хромосомы (см., например, Harrington et al., Nat Genet. 15:345, 1997). Например, невирусные векторы, применимые для экспрессии полинуклеотидов и полипептидов, связывающих FGF21, в клетках млекопитающих (например, человека), включают pThioHis A, B и C, pcDNA3.1/His, pEBVHis A, B и C (Invitrogen, Сан-Диего, Калифорния), векторы MPSV и многочисленные другие векторы, известные из уровня техники для экспрессии других белков. Применимые вирусные векторы включают векторы на основе ретровирусов, аденовирусов, аденоассоциированных вирусов, вирусов герпеса, векторы на основе SV40, папилломавируса, вируса Эпштейна-Барра HBP, векторы на основе вируса коровьей оспы и вируса леса Семлики (SFV). См., Brent et al., выше; Smith, Annu. Rev. Microbiol. 49:807, 1995; и Rosenfeld et al., Cell 68:143, 1992.
Выбор вектора экспрессии зависит от предполагаемых клеток-хозяев, в которых должен экспрессироваться вектор. Как правило, векторы экспрессии содержат промотор и другие регуляторные последовательности (например, энхансеры), которые функционально связаны с полинуклеотидами, кодирующими цепь или фрагмент β-клото-связывающего антитела. В некоторых вариантах осуществления индуцируемый промотор применяют для предотвращения экспрессии встроенных последовательностей в условиях, отличающихся от индуцирующих. Индуцируемые промоторы включают, например, арабинозный, lacZ, металлотионеиновый промотор или промотор белка теплового шока. Культуры трансформированных организмов можно размножать в неиндуцирующих условиях, не оказывая влияния на популяцию кодирующими последовательностями, продукты экспрессии которых лучше переносятся клетками-хозяевами. Для эффективной экспрессии цепи или фрагмента β-клото-связывающего антитела кроме промоторов также могут быть необходимы или желательны другие регуляторные элементы. Эти элементы, как правило, включают инициирующий кодон ATG и смежный сайт связывания рибосомы или другие последовательности. Кроме того, эффективность экспрессии можно повысить за счет включения энхансеров, соответствующих применяемой клеточной системе (см., например, Scharf et al., Results Probl. Cell Differ. 20:125, 1994; и Bittner et al., Meth. Enzymol., 153:516, 1987). Например, энхансер SV40 или энхансер CMV можно применять для повышения экспрессии в клетках-хозяевах млекопитающего.
Векторы экспрессии также могут предусматривать положение сигнальной последовательности секреции с образованием слитого белка с полипептидами, кодируемыми вставленными последовательностями антитела, связывающего FGF21. Чаще вставляемые последовательности β-клото-связывающего антитела соединяют с сигнальными последовательностями до включения в вектор. Векторы, подлежащие применению для получения последовательностей, кодирующих вариабельные домены легкой и тяжелой цепей β-клото-связывающего антитела, иногда также кодируют константные области или их части. Такие векторы обеспечивают возможность экспрессии вариабельных областей в виде слитых белков с константными областями, приводя тем самым к получению интактных антител или их фрагментов. Как правило, такие константные области являются человеческими.
Клетки-хозяева, несущие и экспрессирующие цепи β-клото-связывающего антитела, могут быть либо прокариотическими, либо эукариотическими. E. coli является одним прокариотическим хозяином, применимым для клонирования и экспрессии полинуклеотидов по настоящему изобретению. Другие микробные хозяева, подходящие для применения, включают бациллы, такие как Bacillus subtilis, и другие энтеробактерии, такие как Salmonella, Serratia и различные виды Pseudomonas. Для этих прокариотических хозяев также можно создать векторы экспрессии, которые, как правило, содержат последовательности для управления экспрессией, совместимые с клеткой-хозяином (например, точку начала репликации). Кроме того, будет присутствовать любое количество разнообразных хорошо известных промоторов, как, например, лактозная промоторная система, триптофановая (trp) промоторная система, бета-лактамазная промоторная система или промоторная система из фага лямбда. Промоторы, как правило, управляют экспрессией, необязательно с операторной последовательностью, и имеют последовательности сайта связывания рибосомы и т. п. для инициации и завершения транскрипции и трансляции. Для экспрессии полипептидов, связывающих FGF21, по настоящему изобретению также можно применять другие микроорганизмы, такие как дрожжи. Также можно применять клетки насекомых в сочетании с бакуловирусными векторами.
В некоторых предпочтительных вариантах осуществления для экспрессии и продуцирования β-клото-связывающих полипептидов по настоящему изобретению применяют клетки-хозяева, представляющие собой клетки млекопитающих. Например, они могут представлять собой либо линию клеток гибридомы, экспрессирующую эндогенные гены иммуноглобулинов (например, клон 1D6.C9 гибридомы из миеломы, который описан в примерах), либо линию клеток млекопитающего, несущую экзогенный вектор экспрессии (например, клетки миеломы SP2/0, приведенные в качестве примера ниже). Они включают любую нормальную мортальную или нормальную или аномальную иммортальную клетку животного или человека. Например, был разработан ряд подходящих линий клеток-хозяев, способных секретировать интактные иммуноглобулины, в том числе линии клеток CHO, различные линии клеток Cos, клетки HeLa, линии клеток миеломы, трансформированные B-клетки и гибридомы. Применение тканевой культуры клеток млекопитающего для экспрессии полипептидов в общем обсуждается, например, в Winnacker, FROM GENES TO CLONES, VCH Publishers, N.Y., N.Y., 1987. Векторы экспрессии для клеток-хозяев, представляющих собой клетки млекопитающих, могут включать последовательности для управления экспрессией, такие как точка начала репликации, промотор и энхансер (см., например, Queen et al., Immunol. Rev. 89:49-68, 1986), и необходимые сайты, несущие информацию для процессинга, такие как сайты связывания рибосом, сайты сплайсинга РНК, сайты полиаденилирования и последовательности терминатора транскрипции. Эти векторы экспрессии обычно содержат промоторы, полученные из генов млекопитающих или из вирусов млекопитающих. Подходящие промоторы могут быть конститутивными, специфическими в отношении типа клеток, специфическими в отношении стадии развития и/или модулируемыми или регулируемыми. Применимые промоторы включают без ограничения металлотионеиновый промотор, конститутивный большой поздний промотор аденовируса, индуцируемый дексаметазоном промотор MMTV, промотор SV40, промотор polIII MRP, конститутивный промотор MPSV, индуцируемый тетрациклином промотор CMV (такой как немедленно-ранний промотор CMV человека), конститутивный промотор CMV и комбинации промотор-энхансер, известные из уровня техники.
Способы введения векторов экспрессии, содержащих последовательности полинуклеотидов, представляющие интерес, изменяются в зависимости от типа клетки-хозяина. Например, трансфекцию с использованием хлорида кальция обычно используют для прокариотических клеток, тогда как обработку фосфатом кальция или электропорацию можно применять для других клеток-хозяев. (См., в целом, Sambrook, et al., выше). Другие способы включают, например, электропорацию, обработку фосфатом кальция, трансформацию, опосредованную липосомами, инъекцию и микроинъекцию, баллистические способы, виросомы, иммунолипосомы, конъюгаты поликатион:нуклеиновая кислота, депротеинизированную ДНК, искусственные вирионы, слияние со структурным белком VP22 вируса герпеса (Elliot and O'Hare, Cell 88:223, 1997), усиленное средством поглощение ДНК и трансдукцию ex vivo. Для длительного продуцирования рекомбинантных белков с высоким выходом часто будет требоваться стабильная экспрессия. Например, линии клеток, которые стабильно экспрессируют цепи или связывающие фрагменты β-клото-связывающего антитела, можно получить с применением векторов экспрессии по настоящему изобретению, которые содержат вирусные точки начала репликации или эндогенные экспрессионные элементы и ген селектируемого маркера. После введения вектора можно обеспечивать рост клеток в течение 1-2 дней в обогащенной среде перед их переносом на селективную среду. Целью селектируемого маркера является придание устойчивости к факторам отбора, и его присутствие обеспечивает возможность роста клеток, которые успешно экспрессируют введенные последовательности в селективных средах. Пролиферация устойчивых стабильно трансфицированных клеток может обеспечиваться с применением методик тканевой культуры, соответствующих типу клеток.
Получение моноклональных антител
Моноклональные антитела (mAb) можно получать с помощью ряда методик, в том числе традиционного способа моноклональных антител, например, стандартной методики гибридизации соматических клеток по Kohler and Milstein, 1975 Nature 256: 495. Можно использовать множество методик получения моноклонального антитела, например, вирусную или онкогенную трансформацию B-лимфоцитов.
Системы с применением животных для получения гибридом включают в себя мышиные, крысиные и кроличьи системы. Получение гибридомы у мыши является хорошо отработанной процедурой. Протоколы иммунизации и методики выделения иммунизированных спленоцитов для слияния известны из уровня техники. Партнеры по слиянию (например, клетки миеломы мыши) и процедуры слияния также являются известными.
Химерные или гуманизированные антитела по настоящему изобретению можно получить на основе последовательности мышиного моноклонального антитела, полученного, как описано выше. ДНК, кодирующую тяжелую и легкую цепи иммуноглобулинов, можно получить из представляющей интерес мышиной гибридомы и подвергнуть конструированию таким образом, чтобы она содержала последовательности иммуноглобулина, отличные от мышиных (например, человеческие), с применением стандартных методик молекулярной биологии. Например, для создания химерного антитела вариабельные области мыши можно связать с константными областями человека с применением способов, известных из уровня техники (см., например, патент США № 4816567 за авторством Cabilly et al.). Для создания гуманизированного антитела CDR-области мыши можно вставить в каркас человека с применением способов, известных из уровня техники. См., например, патент США № 5225539 за авторством Winter, и патенты США №№ 5530101; 5585089; 5693762 и 6180370 за авторством Queen et al.
В определенном варианте осуществления антитела по настоящему изобретению представляют собой человеческие моноклональные антитела. Такие человеческие моноклональные антитела, направленные против β-клото, можно получать с применением трансгенных или трансхромосомных мышей, несущих части иммунной системы человека вместо мышиной системы. Эти трансгенные и трансхромосомные мыши включают мышей, называемых в данном документе соответственно мыши HuMAb и мыши KM, и их совокупно называют в данном документе "мышами с Ig человека".
Мышь HuMAb® (Medarex, Inc.) содержит минилокусы генов иммуноглобулинов человека, которые кодируют не подвергшиеся перегруппировке последовательности тяжелых цепей (μ и γ) и легкой цепи κ иммуноглобулина человека, вместе с целенаправленными мутациями, которые инактивируют эндогенные локусы цепей μ и κ (см., например, Lonberg, et al., 1994 Nature 368 (6474): 856-859). Соответственно, мыши проявляют пониженную экспрессию IgM или κ мыши, и в ответ на иммунизацию введенные трансгены тяжелой и легкой цепей человека подвергаются переключению класса и соматической мутации с получением высокоаффинного моноклонального IgGκ человека (Lonberg, N. et al., 1994 выше; обзор в Lonberg, N., 1994 Handbook of Experimental Pharmacology 113:49-101; Lonberg, N. and Huszar, D., 1995 Intern. Rev. Immunol.13: 65-93, и Harding, F. and Lonberg, N., 1995 Ann. N. Y. Acad. Sci. 764:536-546). Получение и применение мышей HuMAb и геномные модификации, которые несут такие мыши, дополнительно описаны в Taylor, L. et al., 1992 Nucleic Acids Research 20:6287-6295; Chen, J. et al., 1993 International Immunology 5: 647-656; Tuaillon et al., 1993 Proc. Natl. Acad. Sci. USA 94:3720-3724; Choi et al., 1993 Nature Genetics 4:117-123; Chen, J. et al., 1993 EMBO J. 12: 821-830; Tuaillon et al., 1994 J. Immunol. 152:2912-2920; Taylor, L. et al., 1994 International Immunology 579-591; и Fishwild, D. et al., 1996 Nature Biotechnology 14: 845-851, содержание всех из которых конкретно включено в данный документ посредством ссылки во всей их полноте. См. дополнительно патенты США №№ 5545806; 5569825; 5625126; 5633425; 5789650; 5877397; 5661016; 5814318; 5874299; и 5770429; все за авторством Lonberg и Kay; патент США № № 5545807 за авторством Surani et al.; публикации согласно PCT №№ WO 92103918, WO 93/12227, WO 94/25585, WO 97113852, WO 98/24884 и WO 99/45962, все за авторством Lonberg и Kay; и публикацию согласно PCT № WO 01/14424 за авторством Korman et al.
В другом варианте осуществления человеческие антитела по настоящему изобретению можно получать с помощью мыши, которая несет последовательности иммуноглобулина человека на трансгенах и трансхромосомах, как, например, мыши, которая несет трансген тяжелой цепи человека и трансхромосому легкой цепи человека. Такие мыши, называемые в данном документе "мышами KM", подробно описаны в публикации согласно PCT WO 02/43478 за авторством Ishida et al.
Более того, альтернативные системы на основе трансгенных животных, экспрессирующих гены иммуноглобулинов человека, являются доступными из уровня техники, и их можно применять для получения β-клото-связывающих антител по настоящему изобретению. Например, можно применять альтернативную трансгенную систему, называемую Xenomouse (Abgenix, Inc.). Такие мыши описаны, например, в патентах США №№ 5939598; 6075181; 6114598; 6150584 и 6162963 за авторством Kucherlapati et al.
Более того, альтернативные системы на основе трансхромосомных животных, экспрессирующих гены иммуноглобулинов человека, являются доступными из уровня техники, и их можно применять для получения β-клото-связывающих антител по настоящему изобретению. Например, можно применять мышей, несущих как трансхромосому тяжелой цепи человека, так и трансхромосому легкой цепи человека, называемых "мышами TC"; такие мыши описаны в Tomizuka et al., 2000 Proc. Natl. Acad. Sci. USA 97:722-727. Кроме того, коровы, несущие трансхромосомы тяжелой и легкой цепей человека, были описаны в уровне техники (Kuroiwa et al., 2002 Nature Biotechnology 20:889-894), и их можно применять для получения антител, связывающих FGF21, по настоящему изобретению.
Человеческие моноклональные антитела по настоящему изобретению также можно получать с применением способов фагового дисплея для скрининга библиотек генов иммуноглобулинов человека. Такие способы фагового дисплея для выделения антител человека определены в уровне техники или описаны в примерах ниже. См., например, патенты США №№ 5223409; 5403484 и 5571698 за авторством Ladner et al.; патенты США №№ 5427908 и 5580717 за авторством Dower et al.; патенты США №№ 5969108 и 6172197 за авторством McCafferty et al.; и патенты США №№ 5885793; 6521404; 6544731; 6555313; 6582915 и 6593081 за авторством Griffiths et al.
Человеческие моноклональные антитела по настоящему изобретению также можно получить с применением мышей SCID, в которых были перенесены иммунные клетки человека таким образом, что после иммунизации может генерироваться ответ в виде продуцирования человеческих антител. Такие мыши описаны, например, в патентах США №№ 5476996 и 5698767 за авторством Wilson et al.
Конструирование каркаса или Fc
Сконструированные антитела по настоящему изобретению включают таковые, в которых были осуществлены модификации в каркасных остатках в пределах VH и/или VL, например, для улучшения свойств антитела. Как правило, такие модификации каркаса осуществляют для снижения иммуногенности антитела. Например, один подход заключается в "мутировании к первоначальному виду" одного или нескольких каркасных остатков в соответствующую последовательность зародышевой линии. Более конкретно, антитело, которое подверглось соматической мутации, может содержать каркасные остатки, которые отличаются от последовательности зародышевой линии, из которой получено антитело. Такие остатки могут быть идентифицированы посредством сравнения каркасных последовательностей антитела с последовательностями зародышевой линии, из которых получено антитело. Для возвращения последовательностей каркасной области в их конфигурацию зародышевой линии соматические мутации можно ввести для "мутирования к первоначальному виду" в последовательности зародышевой линии, например, с помощью сайт-направленного мутагенеза. Также предполагается, что такие "мутированные к первоначальному виду" антитела охватываются настоящим изобретением.
Другой тип модификации каркаса предусматривает мутацию одного или нескольких остатков в пределах каркасной области или даже в пределах одной или нескольких областей CDR, чтобы удалить T-клеточные эпитопы, со снижением тем самым потенциальной иммуногенности антитела. Этот подход также называется "деиммунизацией" и более подробно описан в публикации заявки на патент США № 20030153043 за авторством Carr et al.
Дополнительно или в качестве альтернативы модификациям, осуществляемым в пределах каркасных или CDR-областей, антитела по настоящему изобретению можно конструировать таким образом, чтобы они включали модификации в пределах Fc-области, как правило, для изменения одного или нескольких функциональных свойств антитела, таких как период полужизни в сыворотке крови, фиксация комплемента, связывание с Fc-рецептором и/или антигензависимая клеточная цитотоксичность. Кроме того, антитело по настоящему изобретению может быть модифицировано химически (например, к антителу можно присоединять один или несколько химических фрагментов), или оно может быть модифицировано с изменением характера его гликозилирования, чтобы, опять-таки, изменить одно или несколько функциональных свойств антитела. Каждый из этих вариантов осуществления более подробно описан ниже. Нумерация остатков в Fc-области производится согласно EU-индексу по Kabat.
В одном варианте осуществления шарнирную область CH1 модифицируют таким образом, что число цистеиновых остатков в шарнирной области изменяется, например, увеличивается или уменьшается. Данный подход дополнительно описан в патенте США № 5677425 за авторством Bodmer et al. Число цистеиновых остатков в шарнирной области CH1 изменяют, например, чтобы облегчить сборку легкой и тяжелой цепей или чтобы увеличить или уменьшить стабильность антитела.
В другом варианте осуществления область Fc-шарнир антитела подвергают мутации для снижения биологического периода полужизни антитела. Более конкретно, одну или несколько аминокислотных мутаций вводят в область на границе раздела доменов CH2-CH3 во фрагменте Fc-шарнир таким образом, чтобы антитело характеризовалось нарушенным связыванием с белком A стафилококка (SpA) по сравнению со связыванием нативного домена Fc-шарнир с SpA. Данный подход более подробно описан в патенте США № 6165745 за авторством Ward et al.
В другом варианте осуществления антитело модифицируют для увеличения его биологического периода полужизни. Различные подходы являются возможными. Например, можно вводить одну или несколько из следующих мутаций: T252L, T254S, T256F, как описано в патенте США № 6277375 за авторством Ward. В качестве альтернативы для увеличения биологического периода полужизни антитело можно изменять в пределах области CH1 или CL таким образом, чтобы оно содержало эпитоп для связывания с рецептором реутилизации, взятый из двух петель домена CH2 из области Fc IgG, как описано в патентах США №№ 5869046 и 6121022 за авторством Presta et al.
В других вариантах осуществления область Fc изменяют путем замены по меньшей мере одного аминокислотного остатка на отличающийся аминокислотный остаток для изменения эффекторных функций антитела. Например, одну или несколько аминокислот можно заменить на отличный аминокислотный остаток таким образом, чтобы антитело характеризовалось измененной аффинностью в отношении эффекторного лиганда, но сохраняло способность к связыванию антигена первичного антитела. Эффекторный лиганд, аффинность в отношении которого изменяют, может представлять собой, например, Fc-рецептор или компонент C1 комплемента. Данный подход подробно описан, например, в патентах США №№ 5624821 и 5648260, оба за авторством Winter et al.
В другом варианте осуществления одну или несколько аминокислот, выбранных из аминокислотных остатков, можно заменить на отличающийся аминокислотный остаток таким образом, чтобы антитело характеризовалось измененным связыванием C1q и/или пониженной или устраненной комплементзависимой цитотоксичностью (CDC). Данный подход более подробно описан в патенте США № 6 194 551 за авторством Idusogie et al.
В другом варианте осуществления один или несколько аминокислотных остатков изменяют для изменения таким образом способности антитела к фиксации комплемента. Этот подход дополнительно описан в публикации согласно PCT WO 94/29351 за авторством Bodmer et al.
В еще одном варианте осуществления Fc-область модифицируют для повышения способности антитела опосредовать антителозависимую клеточную цитотоксичность (ADCC) и/или для повышения аффинности антитела в отношении Fcγ-рецептора посредством модификации одной или нескольких аминокислот. Этот подход дополнительно описан в публикации согласно PCT WO 00/42072 за авторством Presta. Более того, сайты связывания на IgG1 человека для FcγRI, FcγRII, FcγRIII и FcRn были картированы, и были описаны варианты с улучшенным связыванием (см. Shields, R. L. et al., 2001 J. Biol. Chen. 276:6591-6604).
В еще одном варианте осуществления характер гликозилирования антитела является модифицированным. Например, можно получить агликозилированное антитело (т. е. антитело без гликозилирования). Характер гликозилирования может быть изменен, например, для повышения аффинности антитела в отношении "антигена". Такие модификации углеводов можно осуществлять, например, посредством изменения одного или нескольких сайтов гликозилирования в пределах последовательности антитела. Например, можно произвести одну или несколько аминокислотных замен, которые приводят к исключению одного или нескольких сайтов гликозилирования в каркасе вариабельной области с устранением за счет этого гликозилирования в этом сайте. Такое агликозилирование может повышать аффинность антитела к антигену. Такой подход подробно описан, например, патентах США №№ 5714350 и 6350861 за авторством Co et al.
В качестве дополнения или альтернативы может быть получено антитело, которое характеризуется измененным типом гликозилирования, как, например, гипофукозилированное антитело, имеющее уменьшенные количества фукозильных остатков, или антитело, имеющее повышенное содержание структур с дополнительным остатком GlcNac в точке ветвления. Было продемонстрировано, что такой измененный характер гликозилирования повышает способность антител к ADCC. Такие модификации углеводов можно осуществлять, например, посредством экспрессии антитела в клетке-хозяине с измененным механизмом гликозилирования. Клетки с измененным механизмом гликозилирования были описаны в уровне техники, и их можно применять в качестве клеток-хозяев, в которых экспрессируются рекомбинантные антитела по настоящему изобретению, с получением таким образом антитела с измененным характером гликозилирования. Например, в EP 1176195 за авторством Hang et al. описывается линия клеток с функциональным нарушением гена FUT8, который кодирует фукозилтрансферазу, в результате чего антитела, экспрессируемые в такой линии клеток, проявляют гипофукозилирование. В публикации согласно PCT WO 03/035835 за авторством Presta описан вариант линии клеток CHO, клетки Lecl3 с пониженной способностью к прикреплению фукозы к связанным посредством Asn (297) углеводам, что также приводит к гипофукозилированию антител, экспрессирующихся в такой клетке-хозяине (см. также Shields, R.L. et al., 2002 J. Biol. Chem. 277:26733-26740). В публикации согласно PCT WO 99/54342 за авторством Umana et al. описываются линии клеток, сконструированные для экспрессии модифицирующих гликопротеин гликозилтрансфераз (например, бета-(1,4)-N-ацетилглюкозаминилтрансферазы III (GnTIII)), в результате чего антитела, экспрессирующиеся в сконструированных линиях клеток, характеризуются повышенным содержанием структур с дополнительным остатком GlcNac в точке ветвления, что приводит к повышенной активности ADCC у антител (см. также Umana et al., 1999 Nat. Biotech. 17:176-180).
СПОСОБЫ КОНСТРУИРОВАНИЯ ИЗМЕНЕННЫХ АНТИТЕЛ
Как описано выше, β-клото-связывающие антитела, имеющие последовательности VH и VL или последовательности полноразмерных тяжелых и легких цепей, показанные в данном документе, можно применять для создания новых β-клото-связывающих антител путем модификации последовательностей полноразмерных тяжелых цепей и/или легких цепей, последовательностей VH и/или VL или константной(константных) области(областей), прикрепленной(прикрепленных) к ним. Таким образом, в другом аспекте настоящего изобретения структурные свойства β-клото-связывающего антитела по настоящему изобретению применяют для создания структурно родственных β-клото-связывающих антител, которые сохраняют по меньшей мере одно функциональное свойство антител по настоящему изобретению, например, связывание с β-клото человека, а также активация одного или нескольких функциональных свойств рецепторного комплекса FGF21 (например, активация передачи сигнала с участием рецептора FGF21).
Например, одну или несколько областей CDR антител по настоящему изобретению или их мутантных вариантов можно объединить с помощью методик рекомбинации с известными каркасными областями и/или другими CDR с созданием дополнительных сконструированных с применением методик рекомбинации β-клото-связывающих антител по настоящему изобретению, как описано выше. Другие типы модификаций включают модификации, описанные в предыдущем разделе. Исходным материалом для способа конструирования является одна или несколько из последовательностей VH и/или VL, представленных в данном документе, или одна или несколько их CDR-областей. Для создания сконструированного антитела не обязательно фактически получать (т. е. экспрессировать в виде белка) антитело, имеющее одну или несколько последовательностей VH и/или VL, представленных в данном документе, или одну или несколько их CDR-областей. Скорее, информацию, содержащуюся в последовательности(последовательностях), применяют в качестве исходного материала для создания последовательности(последовательностей) "второго поколения", полученной(полученных) из исходной(исходных) последовательности(последовательностей), а затем последовательность(последовательности) "второго поколения" получают и экспрессируют в виде белка.
Соответственно, в другом варианте осуществления в настоящем изобретении предусмотрен способ получения β-клото-связывающего антитела (например, NOV005 или NOV006), содержащего последовательность вариабельной области тяжелой цепи антитела, имеющую последовательность CDR1 под SEQ ID NO: 6 или 9, последовательность CDR2 под SEQ ID NO: 7 и/или последовательность CDR3 под SEQ ID NO: 8; и последовательность вариабельной области легкой цепи антитела, имеющую последовательность CDR1 под SEQ ID NO: 19 или 31, последовательность CDR2 под SEQ ID NO: 20 и/или последовательность CDR3 под SEQ ID NO: 21; необязательно изменения по по меньшей мере одному аминокислотному остатку в пределах последовательности вариабельной области тяжелой цепи антитела и/или последовательности вариабельной области легкой цепи антитела с созданием по меньшей мере одной измененной последовательности антитела и экспрессирования последовательности антитела в виде белка.
Соответственно, в другом варианте осуществления в настоящем изобретении предусмотрен способ получения β-клото-связывающего антитела, оптимизированного в отношении экспрессии в клетке млекопитающего, состоящего из последовательности полноразмерной тяжелой цепи антитела, содержащей последовательность под SEQ ID NO: 17; и последовательности полноразмерной легкой цепи антитела, содержащей последовательность под SEQ ID NO: 28 или 34; необязательно изменения по меньшей мере одному аминокислотному остатку в пределах последовательности полноразмерной тяжелой цепи антитела и/или последовательности полноразмерной легкой цепи антитела с созданием по меньшей мере одной измененной последовательности антитела и экспрессирования последовательности антитела в виде белка. В одном варианте осуществления изменение тяжелой или легкой цепи осуществляется в каркасной области тяжелой или легкой цепи.
Измененную последовательность антитела также можно получить посредством скрининга библиотек антител, имеющих фиксированные последовательности CDR3 или минимальные необходимые связывающие детерминанты, описанные в US2005/0255552, и различающиеся последовательности CDR1 и CDR2. Скрининг можно осуществлять согласно любой технологии скрининга, подходящей для скрининга антител из библиотек антител, как, например, технология фагового дисплея.
Стандартные методики молекулярной биологии можно применять для получения и экспрессии измененной последовательности антитела. Антитело, кодируемое измененной(измененными) последовательностью(последовательностями) антитела, является антителом, которое сохраняет одно, некоторые или все из функциональных свойств β-клото-связывающих антител, описанных в данном документе, при этом функциональные свойства включают без ограничения специфическое связывание с β-клото человека, яванского макака, крысы и/или мыши; и антитело активирует опосредованную FGF21 передачу сигнала, например, зависимую от рецептора FGF21 передачу сигнала, в клеточном анализе FGFR1c_ β-клото_HEK293 pERK.
В определенных вариантах осуществления способов конструирования антител по настоящему изобретению мутации можно вводить случайным образом или селективно по всей кодирующей последовательности β-клото-связывающего антитела или ее части, и полученные модифицированные β-клото-связывающие антитела можно подвергнуть скринингу в отношении активности связывания и/или других функциональных свойств, как описано в данном документе. Способы введения мутаций были описаны в уровне техники. Например, в публикации согласно PCT WO 02/092780 за авторством Short описываются способы создания и скрининга мутантных вариантов антител с применением насыщающего мутагенеза, сборки с лигированием синтезированных фрагментов или их комбинации. В качестве альтернативы в публикации согласно PCT WO 03/074679 за авторством Lazar et al. описываются способы применения способов компьютерного скрининга для оптимизации физико-химических свойств антител.
В определенных вариантах осуществления настоящего изобретения антитела были сконструированы с удалением сайтов дезамидирования. Как известно, дезамидирование вызывает структурные и функциональные изменения в пептиде или белке. Дезамидирование может приводить к снижению биоактивности, а также изменениям фармакокинетики и антигенности фармацевтического белка. (Anal Chem. 2005 Mar 1;77(5):1432-9).
В определенных вариантах осуществления настоящего изобретения антитела были сконструированы с повышением pI и улучшением их свойств, подобных лекарственным средствам. Значение pI белка представляет собой основную детерминанту общих биофизических свойств молекулы. Было известно, что антитела, которые характеризуются низкими значениями pI, являются менее растворимыми, менее стабильными и подверженными агрегации. Кроме того, очистка антител с низкими значением pI является сложной и может быть проблематичной, особенно во время масштабного перехода для клинического применения. Повышение значения pI антител или Fab к β-клото по настоящему изобретению приводило к повышению их растворимости, что обеспечивает составление антител при более высоких концентрациях (>100 мг/мл). Составление антител при высоких концентрациях (например, >100 мг/мл) обеспечивает преимущество возможности введения более высоких доз антител в глаза пациентов с помощью интравитреальных инъекций, что, в свою очередь, может способствовать снижению частоты введения дозы, которое представляет собой существенное преимущество для лечения хронических заболеваний, в том числе сердечно-сосудистых нарушений. Более высокие значения pI также могут приводить к FcRn-опосредованному рециклингу версии IgG антитела, тем самым способствуя тому, что лекарственное средство сохраняется в организме в течение более длительного периода, при этом требуется меньшее количество инъекций. В конечном итоге общая стабильность антител является значительно повышенной вследствие более высокого значения pI, что приводит к более длительному сроку хранения и биоактивности in vivo. Предпочтительно значение pI составляет более или равняется 8,2.
Функциональные свойства измененных антител можно оценить с применением стандартных анализов, доступных из уровня техники и/или описанных в данном документе, таких как анализы, изложенные в примерах (например, разновидности ELISA).
ПРОФИЛАКТИЧЕСКИЕ И ТЕРАПЕВТИЧЕСКИЕ ПУТИ ПРИМЕНЕНИЯ
Антитела, которые связываются с β-клото, описанные в данном документе (например, NOV005 или NOV006), и их антигенсвязывающие фрагменты, можно применять в терапевтически пригодной концентрации для лечения заболевания или нарушения, ассоциированного с аберрантной передачей сигнала с участием FGF21 (например, аберрантной активацией опосредованной FGF21 передачи сигнала и/или передачей сигнала с участием рецептора FGF21), с помощью введения субъекту, нуждающемуся в этом, эффективного количества антител или антигенсвязывающих фрагментов по настоящему изобретению, например, NOV005 или NOV006. В настоящем изобретении предусмотрен способ лечения FGF21-ассоциированных метаболических нарушений с помощью введения субъекту, нуждающемуся в этом, эффективного количества антител по настоящему изобретению, например, NOV005 или NOV006. В настоящем изобретении предусмотрен способ лечения FGF21-ассоциированных сердечно-сосудистых нарушений с помощью введения субъекту, нуждающемуся в этом, эффективного количества антител по настоящему изобретению, например, NOV005 или NOV006.
Антитела по настоящему изобретению (например, NOV005 или NOV006) можно применять, в числе прочего, для предупреждения, лечения, предупреждения и улучшения в отношении FGF21-ассоциированных состояний и нарушений, в том числе без ограничения метаболических, эндокринных и сердечно-сосудистых нарушений, таких как ожирение, сахарный диабет 1 типа и 2 типа, панкреатит, дислипидемия, неалкогольная жировая болезнь печени (NAFLD), неалкогольный стеатогепатит (NASH), инсулинорезистентность, гиперинсулинемия, нарушение толерантности к глюкозе, гипергликемия, гипертриглицеридемия, метаболический синдром, острый инфаркт миокарда, гипертензия, сердечно-сосудистое заболевание, атеросклероз, периферическая артериальная болезнь, инсульт, сердечная недостаточность, ишемическая болезнь сердца, заболевание почек, диабетические осложнения, нейропатия, гастропарез, нарушения, ассоциированные с тяжелыми инактивирующими мутациями инсулинового рецептора, и другие метаболические нарушения, а также в снижении смертности и инвалидности критически больных пациентов.
Антитела по настоящему изобретению (например, NOV005 или NOV006) можно применять, в числе прочего, для лечения, диагностики, снижения тяжести, улучшения или предупреждения ряда заболеваний, нарушений или состояний, в том числе без ограничения метаболических заболеваний, ассоциированных с инсулинорезистентностью, таких как сахарный диабет 2 типа, сахарный диабет 1 типа, нарушения, связанные с мутацией инсулинового рецептора (нарушения INSR, например, инсулинорезистентность B типа), неалкогольная жировая болезнь печени (NAFLD) и различные формы частичной липодистрофии, в том числе семейная частичная липодистрофия и индуцированная высокоактивной антиретровирусной терапией HIV частичная липодистрофия (HIV-HAART), а также заболевания, ассоциированные с продуцированием инсулина (например, сахарный диабет 1 типа), и в снижении смертности и инвалидности критически больных пациентов.
Многочисленные инактивирующие мутации INSR были описаны при варьирующихся фенотипах. Пациенты, как правило, проявляют сильную устойчивость к действию инсулина, что прогрессирует до гипергликемии во время пубертатного периода. Современный стандарт лечения представляет собой лечение с помощью очень высоких доз инсулина, когда субъекты начинают испытывать гипергликемию, что, как правило, является недостаточным при контроле гипергликемии.
В конкретных аспектах антитела по настоящему изобретению (например, NOV005 или NOV006) можно применять, в числе прочего, для лечения или контроля сахарного диабета 1 типа, дислипидемии, гипергликемии, гипогликемии, нарушения толерантности к глюкозе, гипертриглицеридемии или индуцированной HIV-HAART частичной липодистофии.
Антитела по настоящему изобретению также можно применять в комбинации с другими средствами для предупреждения, лечения или улучшения в отношении FGF21-ассоциированных нарушений. Например, средства терапии на основе статинов можно применять в комбинации с антителами-миметиками FGF21 и антигенсвязывающими фрагментами по настоящему изобретению для лечения пациентов с сердечно-сосудистыми или метаболическими нарушениями.
В конкретных аспектах в данном документе предусмотрен способ снижения веса тела (например, на по меньшей мере 4%, по меньшей мере 5%, по меньшей мере 6%, по меньшей мере 7%, по меньшей мере 8%, по меньшей мере 9%, по меньшей мере 10%, по меньшей мере 12%, по меньшей мере 15% или по меньшей мере 20%) у субъекта, предусматривающий введение субъекту, нуждающемуся в этом, эффективного количества фармацевтической композиции, содержащей антитело или антигенсвязывающий фрагмент, описанные в данном документе (например, NOV005 или NOV006), которые связывают β-клото и способны повышать активность рецепторного комплекса β-клото/FGFR1c.
В конкретных аспектах в данном документе предусмотрен способ уменьшения аппетита или потребления пищи (например, на по меньшей мере 4%, по меньшей мере 5%, по меньшей мере 6%, по меньшей мере 7%, по меньшей мере 8%, по меньшей мере 9%, по меньшей мере 10%, по меньшей мере 12%, по меньшей мере 15% или по меньшей мере 20%) у субъекта, предусматривающий введение субъекту, нуждающемуся в этом, эффективного количества фармацевтической композиции, содержащей антитело или антигенсвязывающий фрагмент, описанные в данном документе (например, NOV005 или NOV006), которые связывают β-клото и способны повышать активность рецепторного комплекса β-клото/FGFR1c.
В конкретных аспектах в данном документе предусмотрен способ снижения (например, на по меньшей мере 4%, по меньшей мере 5%, по меньшей мере 6%, по меньшей мере 7%, по меньшей мере 8%, по меньшей мере 9%, по меньшей мере 10%, по меньшей мере 12%, по меньшей мере 15%, по меньшей мере 20%, по меньшей мере 30%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80% или по меньшей мере 90%) концентраций триглицеридов (TG) в плазме крови или общего холестерина (TC) в плазме крови у субъекта, предусматривающий введение субъекту, нуждающемуся в этом, эффективного количества фармацевтической композиции, содержащей антитело или антигенсвязывающий фрагмент, описанные в данном документе (например, NOV005 или NOV006), которые связывают β-клото и способны повышать активность рецепторного комплекса β-клото/FGFR1c.
В конкретных аспектах способов, предусмотренных в данном документе, субъект страдает метаболическим нарушением, таким как ожирение, сахарный диабет 1 типа и 2 типа, панкреатит, дислипидемия, неалкогольный стеатогепатит (NASH), инсулинорезистентность, гиперинсулинемия, нарушение толерантности к глюкозе, гипергликемия, гипертриглицеридемия и метаболический синдром. В конкретных аспектах способов, предусмотренных в данном документе, субъект страдает сердечно-сосудистым нарушением. В конкретных аспектах субъект представляет собой человека.
В определенных аспектах в данном документе предусмотрен способ лечения или контроля ожирения у субъекта, предусматривающий введение субъекту, нуждающемуся в этом, эффективного количества фармацевтической композиции, содержащей антитело или антигенсвязывающий фрагмент, описанные в данном документе (например, NOV005 или NOV006), которые связывают β-клото и способны повышать активность рецепторного комплекса β-клото/FGFR1c.
В определенных аспектах в данном документе предусмотрен способ лечения или контроля диабета 2 типа у субъекта, предусматривающий введение субъекту, нуждающемуся в этом, эффективного количества фармацевтической композиции, содержащей антитело или антигенсвязывающий фрагмент, описанные в данном документе (например, NOV005 или NOV006), которые связывают β-клото и способны повышать активность рецепторного комплекса β-клото/FGFR1c.
В определенных аспектах в данном документе предусмотрен способ лечения или контроля диабета 1 типа у субъекта, предусматривающий введение субъекту, нуждающемуся в этом, эффективного количества фармацевтической композиции, содержащей антитело или антигенсвязывающий фрагмент, описанные в данном документе (например, NOV005 или NOV006), которые связывают β-клото и способны повышать активность рецепторного комплекса β-клото/FGFR1c.
В определенных аспектах в данном документе предусмотрен способ лечения или контроля липодистрофии, такой как индуцированная HIV-HAART частичная липодистрофия, у субъекта, предусматривающий введение субъекту, нуждающемуся в этом, эффективного количества фармацевтической композиции, содержащей антитело или антигенсвязывающий фрагмент, описанные в данном документе (например, NOV005 или NOV006), которые связывают β-клото и способны повышать активность рецепторного комплекса β-клото/FGFR1c.
В определенных аспектах в данном документе предусмотрен способ лечения или контроля NASH у субъекта, предусматривающий введение субъекту, нуждающемуся в этом, эффективного количества фармацевтической композиции, содержащей антитело или антигенсвязывающий фрагмент, описанные в данном документе (например, NOV005 или NOV006), которые связывают β-клото и способны повышать активность рецепторного комплекса β-клото/FGFR1c.
В определенных аспектах в данном документе предусмотрен способ лечения или контроля нарушения, связанного с мутацией инсулинового рецептора, у субъекта, предусматривающий введение субъекту, нуждающемуся в этом, эффективного количества фармацевтической композиции, содержащей антитело или антигенсвязывающий фрагмент, описанные в данном документе (например, NOV005 или NOV006), которые связывают β-клото и способны повышать активность рецепторного комплекса β-клото/FGFR1c.
ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ
В настоящем изобретении предусмотрены фармацевтические композиции, содержащие β-клото-связывающие антитела (интактные или связывающие фрагменты), составленные вместе с фармацевтически приемлемым носителем. Композиции могут дополнительно содержать один или несколько других терапевтических средств, которые являются подходящими для лечения или предупреждения, например, сердечно-сосудистых нарушений. Фармацевтически приемлемые носители усиливают или стабилизируют композицию, или их можно применять для облегчения получения композиции. Фармацевтически приемлемые носители включают растворители, дисперсионные среды, средства для покрытия, антибактериальные и противогрибковые средства, изотонические и замедляющие абсорбцию средства и т. п., которые являются физиологически совместимыми.
Фармацевтическая композиция по настоящему изобретению может быть введена с помощью ряда способов, известных в данной области техники. Путь и/или способ введения меняются в зависимости от требуемых результатов. Предпочтительно, чтобы введение было внутривенным, внутримышечным, внутрибрюшинным или подкожным, или введение осуществляют вблизи участка мишени. Фармацевтически приемлемый носитель должен быть подходящим для интравитреального, внутривенного, внутримышечного, подкожного, парентерального, позвоночного или эпидермального введения (например, посредством инъекции или инфузии). В зависимости от пути введения активное соединение, т. е. антитело, биспецифическая и мультиспецифическая молекула, может быть покрыто материалом для защиты соединения от действия кислот и других естественных условий, которые могут инактивировать соединение. В конкретном аспекте фармацевтическую композицию, содержащую β-клото-связывающее антитело, описанное в данном документе, такое как антитело NOV005 или NOV006, для применения в способах, предусмотренных в данном документе, вводят подкожно. В конкретном аспекте фармацевтическую композицию, содержащую β-клото-связывающее антитело, описанное в данном документе, такое как антитело NOV005 или NOV006, для применения в способах, предусмотренных в данном документе, вводят внутривенно.
Композиция должна быть стерильной и текучей. Надлежащую текучесть можно поддерживать, например, посредством применения покрытия, такого как лецитин, посредством поддержания необходимого размера частиц в случае дисперсии и посредством применения поверхностно-активных веществ. Во многих случаях предпочтительным является включение в композицию изотонических средств, например, сахаров, полиспиртов, таких как маннит или сорбит, и хлорида натрия. Длительная абсорбция инъекционых композиций может быть обеспечена включением в композицию средства, которое замедляет абсорбцию, например, моностеарата алюминия или желатина.
Фармацевтические композиции по настоящему изобретению можно получить в соответствии со способами, хорошо известными и обычно осуществляемыми в данной области техники. См., например, Remington: The Science and Practice of Pharmacy, Mack Publishing Co., 20th ed., 2000; и Sustained and Controlled Release Drug Delivery Systems, J.R. Robinson, ed., Marcel Dekker, Inc., New York, 1978. Фармацевтические композиции предпочтительно изготовляют в соответствии с положениями GMP. Как правило, терапевтически эффективную дозу или эффективную дозу β-клото-связывающего антитела применяют в фармацевтических композициях по настоящему изобретению. β-Клото-связывающие антитела составляют в фармацевтически приемлемые лекарственные формы с помощью традиционных способов, известных специалистам в данной области техники. Схемы дозирования корректируют для обеспечения оптимального требуемого ответа (например, терапевтического ответа). Например, можно вводить один болюс, можно вводить несколько разделенных доз в течение некоторого времени, или дозу можно пропорционально уменьшать или увеличивать, как показано согласно потребностям терапевтической ситуации. Особенно преимущественным является составление композиций для парентерального применения в единичной дозированной форме для удобства введения и однородности дозирования. Единичная дозированная форма, как используется в данном документе, относится к физически дискретным единицам, подходящим в качестве единичных доз для субъектов, подлежащих лечению; при этом каждая единица содержит предварительно определенное количество активного соединения, рассчитанное для получения требуемого терапевтического эффекта, в сочетании с необходимым фармацевтическим носителем.
Фактические уровни дозы активных ингредиентов в фармацевтических композициях по настоящему изобретению можно изменять для того, чтобы получить количество активного ингредиента, которое является эффективным для достижения требуемого терапевтического ответа для конкретного пациента, эффективным в отношении композиции и способа введения, не являясь токсичным для пациента. Выбранный уровень дозы зависит от ряда факторов, в том числе активности конкретных используемых композиций по настоящему изобретению или их присутствия в форме сложного эфира, соли или амида, пути введения, времени введения, скорости выведения конкретного используемого соединения, длительности лечения, других лекарственных средств, соединений и/или материалов, применяемых в комбинации с конкретными используемыми композициями, возраста, пола, веса, состояния, общего состояния здоровья и анамнеза пациента, подлежащего лечению, и подобных факторов.
Врач или ветеринар может начинать введение доз антител по настоящему изобретению, применяемых в фармацевтической композиции, с уровней ниже, чем уровни, которые необходимы для достижения требуемого терапевтического эффекта, и постепенно повышать дозу до тех пор, пока не будет достигнут требуемый эффект. В целом, эффективные дозы композиций по настоящему изобретению для лечения сердечно-сосудистых нарушений, описанных в данном документе, меняются в зависимости от многих разных факторов, в том числе от способов введения, участка мишени, физиологического состояния пациента, от того, является ли пациентом человек или животное, от других вводимых лекарственных препаратов и от того, является ли лечение профилактическим или терапевтическим. Дозы для лечения необходимо подбирать для оптимизации безопасности и эффективности. В конкретном варианте осуществления в случае системного введения антитела доза находится в диапазоне от приблизительно 0,0001 до 100 мг/кг или от 0,01 до 15 мг/кг веса тела хозяина. Иллюстративный режим лечения предусматривает системное введение один раз в две недели, или один раз в месяц, или один раз в 3-6 месяцев. Иллюстративный режим лечения предусматривает системное введение один раз в две недели, или один раз в месяц, или один раз в 3-6 месяцев, или по мере необходимости (PRN).
Антитело обычно вводят по несколько раз. Интервалы между отдельными дозами могут составлять недели, месяцы или года. Интервалы также могут быть нерегулярными, на что указывает измерение уровней β-клото-связывающего антитела в крови у пациента. Кроме этого, альтернативные интервалы введения доз могут быть определены врачом, и их можно вводить ежемесячно или по мере необходимости для оказания эффекта. В некоторых способах системного введения дозировку корректируют для достижения концентрации антитела в плазме крови, составляющей 1-1000 мкг/мл, и в некоторых способах - 25-500 мкг/мл. В качестве альтернативы антитело можно вводить в виде состава с замедленным высвобождением, в этом случае требуется менее частое введение. Доза и частота меняются в зависимости от периода полужизни антитела у пациента. В целом, гуманизированные антитела проявляют более длительный период полужизни, чем химерные антитела и антитела, отличные от человеческих. Доза и частота введения могут меняться в зависимости от того, является ли лечение профилактическим или терапевтическим. В профилактических применениях относительно низкую дозу вводят с относительно большими интервалами в течение длительного периода времени. Некоторые пациенты продолжают получать лечение до конца своей жизни. В терапевтических применениях иногда необходимо введение относительно высокой дозы с относительно короткими интервалами до тех пор, пока прогрессирование заболевания не уменьшится или завершится, и предпочтительно до тех пор, пока у пациента не будет наблюдаться частичное или полное облегчение симптомов заболевания. После этого пациенту можно осуществлять введение по профилактической схеме.
ПРИМЕРЫ
Следующие примеры предусмотрены для дополнительной иллюстрации настоящего изобретения, а не для ограничения его объема. Другие варианты настоящего изобретения будут полностью очевидны специалисту в данной области техники и охвачены прилагаемой формулой изобретения.
Пример 1. Скрининг и получение антител
Получение клеток 300.19 с FGFR1c-β-клото человека для их применения в качестве антигена
Клетки 300.19, которые стабильно экспрессировали FGFR1c (aa 1-386) и β-клото человека, получали для применения в качестве цельноклеточного антигена. Полноразмерную cDNA, кодирующую β-клото человека (номер доступа в GenBank NM_175737), клонировали в сайты EcoRI и EcoRV в pEF1/Myc-His B (Invitrogen, каталожный № V92120). cDNA, кодирующую аминокислоты 1-386 из FGFR1c человека (номер доступа в GenBank NM_023106), клонировали в сайты BamHI и NotI в pEF6/Myc-His B (Invitrogen, каталожный номер V96220). В обе конструкции непосредственно перед старт кодоном вводили последовательность Козак (CACC), а стоп кодон добавляли в вектор перед меткой Myc-His. Мышиные пре-В-клетки 300-19 котрансфицировали плазмидами с β-клото и FGFR1c посредством электропорации с применением устройства Amaxa Nucleofector и набора Nucleofector (Lonza, каталожный № VCA-1003). Стабильные клоны отбирали с применением 1 мг/мл генетицина (Invitrogen, каталожный № 10131) и 8 мг/мл бластицидина (Invitrogen, каталожный № 46-1120) на протяжении 3 недель.
Получение клеток HEK293, экспрессирующих FGFR/β-клото, для применения в клеточных анализах
Для тестирования антител к β-клото в отношении специфичности связывания, функциональной активности или перекрестной реактивности с ортологами получали клетки HEK293, стабильно экспрессирующие FGFR1c_β-клото человека, FGFR2c_β-клото человека, FGFR3c_β-клото человека, FGFR4_β-клото человека или FGFR1c_β-клото яванского макака с применением стандартной трансфекции липофектамином 2000 и методов отбора клеточных клонов.
Применяли следующие плазмиды для экспрессии в клетках млекопитающих, которые кодировали полноразмерную cDNA β-клото человека (NM_175737), FGFR1c человека (NM_023106), FGFR2c человека (NP_001138387), FGFR3c человека (NP_000133) или FGFR4 человека (NP_998812); в случае β-клото яванского макака полноразмерную последовательность получали с помощью ПЦР-амплификации из cDNA жировой ткани яванского макака (BioChain, каталожный № C1534003-Cy) с праймерами, разработанными на основе на последовательностей β-клото человека и макака-резуса, и клонировали. cDNA FGFR1c яванского макака клонировали из cDNA жировой ткани яванского макака (BioChain, каталожный № C1534003-Cy) с применением праймеров, разработанных на основе последовательности FGFR1c человека (№ NM_023106), и было показано, что на аминокислотному уровне он на 100% идентичен FGFR1c человека. Следовательно, конструкцию с cDNA FGFR1c человека, описанную выше, применяли для создания клеток HEK293 которые стабильно экспрессируют β-клото яванского макака и FGFR1c человека (№ NM_023106), поскольку аминокислотные последовательности FGFR1с человека и яванского макака являются идентичными.
Определение аффинности связывания антител с β-клото
Аффинности связывания антител определяли с применением кинетического анализа Biacore. Сенсорный чип CM5 серии S (GE Healthcare, каталожный № BR-1005-30) уравновешивали при комнатной температуре в течение приблизительно 30 минут. Систему заполняли 1x буфером HBS-EP+ (10x раствор, GE Healthcare, каталожный № BR-1006-69) и чип загружали в прибор Biacore. Чип подвергали нормализации с помощью раствора BIAnormalizing (GE Healthcare, каталожный № BR-1006-51) и чип кондиционировали с помощью 50 мМ NaOH с применением скорости потока 60 мкл/минута для всех проточных каналов. 30 секундное введение повторяли трижды с временем выдержки в 60 секунд. 10 мМ ацетат натрия с pH 5,0 вводили при скорости 60 мкл/минута в течение 120 секунд и повторяли дважды. Затем начинали новый цикл путем иммобилизации антитела к Fc IgG человека с применением набора для захвата антител человека (GE Healthcare, каталожный № BR-1008-39). Ab к Fc человека разводили до 50 мг/мл в буфере для иммобилизации (10 мМ ацетат натрия, pH 5,0). Реагенты для иммобилизации по аминогруппе смешивали 1:1 (EDC и NHS) и вводили в течение 7 минут при скорости 10 мкл/минута. Затем Ab к Fc человека вводили в течение 6 минут при скорости 10 мкл/минута. В последнюю очередь вводили этаноламин в течение 7 минут при скорости 10 мкл/минута с временем выдержки в 60 секунд. Это должно было приводить к иммобилизации на уровне приблизительно 8000-10000 RU. Затем проводили тестовые введения NOV004, NOV005 и NOV006 для получения Rmax, составляющего 10 RU (уровни захвата=~28 RU). Их выполняли с применением скорости потока, равной 10 мкл/мл, и буфера для регенерации на основе 3 M MgCl2. Каждый раз оценивали каждую проточную ячейку вследствие изменений поверхности чипа, аффинности IgG, качества белка IgG и отличий в разведениях. Начинали с концентрации IgG, составляющей 0,5 мкг/мл, и концентрацию увеличивали (или уменьшали) в зависимости от результатов введений образца. Например, если 100 RU наблюдали за 15 секунд, тогда раствор Ab разводили до 0,25 мкг/мл и повторяли введения. После определения параметров захвата для каждого антитела в каждой проточной ячейке β-клото человека при различных концентрациях пропускали над чипом и ka (1/Mс), kd (1/с), KD (M) и Rmax (RU) рассчитывали на основе кинетических показателей Biacore.
Определение того, проявляют ли разные антитела конкурентное связывание с β-клото
Forte Bio применяли для определения того, проявляют ли антитела конкурентное связывание с β-клото человека. Все образцы и реагенты разводили в 10x буфере для кинетических анализов (Forte Bio, каталожный № 18-1092) с PBS-буфером в отношении 1/10 (объем/объем). β-клото человека (R and D Systems, 5889-KB-050) разводили буфером для кинетических анализов до требуемой концентрации (5 мкг/мл). β-клото человека загружали на сенсор с антителом к his-метке (Forte Bio, каталожный № 18-5114) на 20 секунд, затем на 400 секунд на сенсор загружали антитело 1, пока не достигались условия насыщения (200 нM). В последнюю очередь на сенсор на 100 секунд загружали конкурентное антитело при концентрации 200 нМ в присутствии 200 нМ антитела 1. Отсутствие второго сигнала связывания обозначает, что антитела конкурируют за связывание с β-клото человека.
Измерение активации рецептора FGFR_β-клото с применением клеточного анализа pERK
Стандартные методики применяли для культивирования клеток и измерения уровня фосфо-ERK 1/2 (pERK). Вкратце, клетки HEK293, стабильно экспрессирующие FGFR1c_β-клото человека, FGFR2c_β-клото человека, FGFR3c_β-клото человека, FGFR4_β-клото человека или FGFR1c_β-клото яванского макака поддерживали в среде DMEM (Invitrogen, 11995), содержащей 10% FBS (Hyclone, SH30071), бластицидин (Invitrogen, A1113902) и генетицин (Invitrogen, 10131035), при 37°C в 5% CO2. Клетки высевали в 384-луночные планшеты, покрытые поли-D-лизином (BD Biosciences, 354663), и инкубировали на протяжении ночи при 37°C и 5% CO2, а затем подвергали сывороточному голоданию.
Супернатанты гибридом или антитела к β-клото разводили в среде Freestyle 293 и различные концентрации антител добавляли в планшет. После инкубации клетки промывали, затем лизировали с помощью лизирующего буфера. Клеточные лизаты переносили в 384-луночный планшет для анализа (PerkinElmer, каталожный № 6008280) и применяли набор AlphaScreen SureFire™ pERK 1/2 (Perkin Elmer, TGRES10K) для измерения уровня фосфо-ERK 1/2. Планшеты считывались на многоканальном ридере EnVision 2104 (Perkin Elmer) с применением стандартных настроек AlphaScreen. Данные доза-эффект наносили на график в виде кратного повышения активности pERK относительно базальной активности в зависимости от концентрации белка для определения значений EC50 с применением уравнения Y=Нижнее значение+(Верхнее значение-Нижнее значение)/(1+10^((LogEC50-X) x Наклон кривой)) и программного обеспечения GraphPad Prism 5.
Получение моноклональных антител
Антитела к-β-клото человека получали в мышах Balb/c (Jackson Laboratory, линия: BALB/cJ) или Bcl2 22 wehi (Jackson Laboratory, линия: C.Cg-Tg(BCL2)22Wehi/J) посредством иммунизаций цельными клетками, как описано в общем в Dreyer et al (2010) (Dreyer AM et.al. (2010) BMC Biotechnology 10:87).
Вкратце, 1×107 клеток 300.19 с FGFR1c_β-клото человека инъецировали мышам Balb/c шесть раз с интервалом от 10 до 30 дней. Первые инъекции цельных клеток выполняли с полным адъювантом Фрейнда (Sigma-Aldrich, F5881). Клетки и адъювант не смешивали, а инъецировали раздельно в два близко расположенных, но отдельных, подкожных участка. Позже за ними следовали внутрибрюшинные инъекции тех же клеток либо с адъювантной системой Sigma (Sigma-Aldrich S6322) или без адъюванта.
В случае мышей Bcl2 22 wehi по 1×107 клеток 300.19 с FGFR1c_β-клото человека инъецировали этим животным четыре раза с интервалами в семь дней. Первые инъекции выполняли с полным адъювантом Фрейнда (Sigma-Aldrich F5881). Клетки и адъювант инъецировали отдельно двумя сериями в два близко расположенных, но отдельных, подкожных участка. Последующие инъекции клеток выполняли подкожно без адъюванта.
Иммунные ответы у иммунизированных мышей измеряли с помощью анализа сортировки клеток с активированной флуоресценцией (FACS). Сыворотку крови иммунизированных мышей, разведенную в 1000 или 10000 раз, применяли для окрашивания клеток HEK с FGFR1c_β-клото человека и клеток 300.19 с FGFR1c_ β-клото человека, а затем применяли вторичное детекторное антитело к IgG мыши, конъюгированное с аллофикоцианином (APC)(Jackson ImmunoResearch, каталожный № 115-136-071). Флуоресценцию считывали на Becton Dickinson LSRII или проточном цитометре Foressa. Для проведения электрослияний отбирали четырех мышей с наивысшим титром.
Скрининг, субклонирование и отбор гибридом
2×108 спленоцитов и 5×107 клеток F0 (ATCC, CRL-1646), служащих партнерами по слиянию, промывали в среде Cytofusion (LCM-C, Cyto Pulse Sciences) и подвергали слиянию с применением генератора сигналов Hybrimune (Cyto Pulse Sciences, модель CEEF-50B) согласно инструкциям производителя с пиковым импульсом, составляющим 600 вольт. Клетки высевали в 384-луночные планшеты при расчетной плотности 3000 клеток F0 на лунку и культивировали в среде для отбора HAT (Sigma-Aldrich, каталожный № H0262).
Первичный скрининг осуществляли с применением платформы FACS с высокой пропускной способностью (Anderson, Paul. Automated Hybridoma Screening, Expansion, Archiving and Antibody Purification. В: 3rd Annual 2014 SLAS Conference. Jan. 18-22, 2014, San Diego, CA). Вкратце, супернатанты гибридом инкубировали с линиями клеток, стабильно экспрессирующих и не экспрессирующих FGFR1c_β-клото человека, и связывание антител определяли с помощью вторичного антитела к IgG мыши, конъюгированного с APC (Jackson ImmunoReseach, каталожный № 115-136-071).
Антитела из супернатанта каждой гибридомы тестировали в отношении связывания одновременно с четырьмя ʺштрих-кодированнымиʺ линиями клеток: исходными клетками 300.19, клетками 300.19 с FGFR1c_β-клото человека, исходными клетками HEK 293 и клетки HEK 293 с FGFR1c_β-клото человека. В первичном скрининге отобрали 348 вариантов. Первичные варианты размножали в 96-луночных планшетах, и связывание вновь подтверждали на клетках HEK 293 FGFR1c_β-клото человека с помощью FACS, что дало 122 подтвержденных варианта. Супернатанты, содержащие среду HАТ (гипоксантин-аминоптерин-тимидин), полученные от 115 вариантов со связыванием, переподтвержденным с помощью FACS, подвергали анализу профиля в отношении клеточной активации рецепторного комплекса FGFR1c_β-клото человека с применением анализа фосфо-ERK 1/2, описанного в данном документе.
Гибридомы, супернатанты которых обусловливали наивысшую клеточную активность фосфо-ERK 1/2, размножали и из их супернатантов очищали IgG. Очищенные IgG из 74 гибридом подвергали анализу профиля в отношении клеточной активации рецепторного комплекса FGFR1c_β-клото человека с применением анализа фосфо-ERK 1/2, описанного в примере 2. IgG от гибридом с наилучшей эффективностью в отношении активации фосфо-ERK 1/2 за счет рецепторного комплекса FGFR1c_β-клото человека подвергали анализу профиля в отношении перекрестной реактивности с ортологами с помощью рецепторного комплекса FGFR1c_β-клото яванского макака и селективности для рецепторных комплексов FGFR2c_β-клото человека и FGFR3c_β-клото человека с применением анализа фосфо-ERK 1/2, описанного в примере 2. На основании результатов данного анализа профиля для дальнейших анализов профиля отбирали несколько клонов гибридом, например 127F19. В частности, наиболее эффективные очищенные IgG, как, например, продуцируемые клоном 127F19, подвергали анализу профиля в отношении перекрестной реактивности, и показано, что они активировали FGFR1c_β-клото яванского макака, но не FGFR2c_β-клото, FGFR3c_β-клото, FGFR4_β-клото или клото-FGFR человека. Отобранные IgG, например, продуцируемые клоном 127F19, связывались с клетками, экспрессирующими β-клото или FGFR1c_β-клото, но не с клетками, экспрессирующими только FGFR1.
Для оценки передачи сигнала под действием 127F19 в клетках, экспрессирующих α-клото, клетки HEK293 трансфицировали с помощью α-клото, люциферазы Egr1 и люциферазы Renilla. Вкратце, клетки HEK293 культивировали в DMEM, 10% FBS, высевали из расчета 30000 клеток/лунка и трансфицировали с помощью клото, Egr-1-luc и TK-Rennilla с применением липофектамина 2000. На следующий день FGF23, FGF21 и 127F19 разбавляли до указанной концентрации в DMEM, дополненной 0,1% FBS, и добавляли к трансфицированным клеткам на ночь. Активность люциферазы обнаруживали с помощью набора для люциферазного анализа Dual-Glo (Promega, E2920) согласно инструкции производителя. Как и ожидалось, FGF23, для передачи сигнала с помощью которого требуется экспрессия α-клото, демонстрировал сильную экспрессию люциферазы. При этом, ни FGF21, ни 127F19 не демонстрировали какой-либо значительной экспрессии люциферазы, что позволяет предположить, что α-клото не выступает в качестве корецептора для FGF21 или данных антител-миметиков FGF21.
Гуманизация и созревание аффинности моноклональных антител
Гуманизация
Способ гуманизации хорошо описан в уровне техники (Jones PT et al. (1986) Nature 321: 522-525; Queen C et al. (1989) PNAS USA 86: 10029-10033; Riechmann L et al. (1988) Nature 33:323-327; Verhoeyen M et al. (1988) Science 239: 1534-1536). Термин "гуманизация" описывает перенос антигенсвязывающего участка из антитела, отличного от человеческого, например, мышиного антитела, в человеческую акцепторную каркасную область, например, последовательность зародышевого типа (Retter I et al. (2005). Nucleic Acids Res. 33:D671-D674.).
Считается, что главная цель гуманизации антитела заключается в минимизация риска развития иммунного ответа на антитело у человека (Rebello PR et al. (1999) Transplantation 68: 1417-1420). Антигенсвязывающий участок содержит определяющие комплементарность области (CDR) (Chothia C and Lesk AM (1987) Journal of Molecular Biology 196: 901-917; Kabat E et al. (1991) Anon. 5th Edition ed; NIH Publication No. 91: 3242) и положения за пределами CDR, т. е. в каркасной области вариабельных доменов (VL и VH), которые прямо или опосредовано влияют на связывание. Остатки каркасных областей, которые могут непосредственно влиять на связывание, могут находиться, например, в так называемой области "внешней" петли, расположенной между CDR2 и CDR3. Остатки, которые опосредовано влияют на связывание, например, находятся в так называемых зонах Вернье (Foote J, Winter G. (1992) Journal of Molecular Biology 224:4 87-499). Считается, что они поддерживают конформацию CDR. Такие положения за пределами CDR принимают во внимание при выборе подходящей акцепторной каркасной области, чтобы свести к минимуму число отклонений конечного гуманизированного антитела от акцепторной последовательности зародышевой линии человека в каркасных областях.
Множество акцепторных каркасных областей зародышевой линии человека тестировали в отношении гуманизации как легкой цепи, так и тяжелой цепи. Например, человеческие каркасные области VBase_VH4_4-30.1 и VBase_VH3_3-21 тестировали в отношении гуманизации тяжелой цепи, а человеческие каркасные области VBase_VK1_O18 и VBase_VK3_L25 тестировали в отношении гуманизации легкой цепи.
Оптимизация последовательно за счет созревания аффинности
Известно, что определенные мотивы аминокислотной последовательности подвергаются посттрансляционной модификации (PTM), как, например, гликозилированию (т. е. NxS/T, x является любым, кроме P), окислению свободных цистеиновых остатков, дезамидированию (например, NG) или изомеризации (например, DG). В случае их присутствия в областях CDR, такие мотивы предпочтительно удалить с помощью сайт-направленного мутагенеза, чтобы увеличить гомогенности продукта.
Способ созревания аффинности хорошо описан в уровне техники. Среди большого числа дисплейных систем фаговый дисплей (Smith GP, 1985, Filamentous fusion phage: novel expression vectors that display cloned antigens on the virion surface. Science 228:1315-1317) и дисплей на эукариотических клетках, таких как дрожжи (Boder ET and Wittrup KD, 1997, Yeast surface display for screening combinatorial polypeptide libraries. Nature Biotechnology 15: 553-557), по видимому, являются наиболее широко применяемыми системами для отбора при взаимодействии антиген-антитело. Преимущества таких дисплейных систем заключаются в том, что они подходят для широкого диапазона антигенов и что строгость условий отбора можно легко регулировать. При фаговом дисплее можно проводить дисплей фрагментов scFv или Fab, а при дрожжевом дисплее, кроме того, полноразмерных IgG. Данные широко применяемые способы позволяют осуществлять отбор требуемых вариантов антитела из больших библиотек с разнообразием, составляющим более 10E7. Для библиотек с меньшим разнообразием, например, 10E3, можно проводить скрининг посредством микроэкспрессии и ELISA. Библиотеки с нецелевыми или случайными вариантами антител можно получать, например, с помощью ПЦР сниженной точности (Cadwell RC and Joyce GF, 1994, Mutagenic PCR. PCR Methods Appl. 3: S136-S140), и она обеспечивает очень простой, но иногда ограниченный подход. Другой стратегией является CDR-направленная диверсификация антитела-кандидата. На одно или несколько положений в одной или нескольких CDR можно осуществлять специфическое нацеливание с применением, например, вырожденных олигонуклеотидов (Thompson J et al., 1996, Affinity maturation of a high-affinity human monoclonal antibody against the third hypervariable loop of human immunodeficiency virus: use of phage display to improve affinity and broaden strain reactivity. J.Mol.Biol. 256: 77-88), тринуклеотидного мутагенеза (TRIM) (Kayushin AL et al., 1996, A convenient approach to the synthesis of trinucleotide phosphoramidites--synthons for the generation of oligonucleotide/peptide libraries. Nucleic Acids Res. 24: 3748-3755) или любого другого подхода, известного в данной области техники. Аминокислотные модификации проводили у гуманизированных кандидатов для устранения PTM.
Получение плазмид экспрессии
Последовательности ДНК, кодирующие гуманизированные домены VL и VH, заказывали в GeneArt™ (Life Technologies Inc. Регенсбург, Германия), включая оптимизацию кодонов для Homo sapiens. Последовательности, кодирующие домены VL и VH, субклонировали посредством вырезания из векторов, полученных в GeneArt, и вставки в векторы экспрессии, подходящие для секреции в клетках млекопитающих. Тяжелые и легкие цепи клонировали в отдельные векторы экспрессии для обеспечения возможности котрансфекции. К элементам вектора экспрессии относятся промотор (энхансер-промотор цитомегаловируса (CMV)), сигнальная последовательность для облегчения секреции, сигнал полиаденилирования и терминатор транскрипции (ген бычьего гормона роста (BGH)), элемент, обеспечивающий возможность эписомальной репликации и репликации у прокариот (например, точка начал репликации SV40 и ColE1 или другие, известные из уровня техники), и элементы для обеспечения возможности отбора (ген устойчивости к ампициллину и зеоциновый маркер).
Экспрессия и очистка гуманизированных антител-кандидатов
Клетки эмбриональной почки человека, конститутивно экспрессирующие большой T-антиген SV40 (HEK293-T, ATCC11268), являются одной из широко применяемых линий клеток-хозяев для транзиентной экспрессии гуманизированных и/или оптимизированных белков IgG. Трансфекции осуществляли с применением PEI (полиэтиленимин, MW 25000, линейный, Polysciences, USA, каталожный № 23966) в качестве реагента для трансфекции.
Первую очистку осуществляли с помощью аффинности на колонке HiTrap MabSelect®SuRe с белком A. Элюат тестировали в отношении агрегации (SEC-MALS) и чистоты (SDS-PAGE, LAL и MS). При необходимости пулы, полученные в первой очистке, загружали в SPX (Hi Load 16/60 Superdex, класс 200, 120 мл (GE-Helthcare). NOV004, NOV005 и NOV006 представляют собой гуманизированные mAb, происходящие из мышиной гибридомы 127F19. Изотипические IgG1 с L234A/L235A (LALA) или IgG1κ с D265A/P329A (DAPA) выбрали в качестве профилактических мер для снижения способности антитела к стимуляции антителозависимой клеточноопосредованной цитотоксичности (ADCC) и комплементзависимой цитотоксичности (CDC) (см., например, Hezareh M et al. (2001) Journal of Virology 75: 12161-12168). Гуманизированные кандидаты NOV004, NOV005 и NOV006, которые относятся к изотипам IgG1 (DAPA), экспрессировали и очищали, как описано.
Пример 2. In vitro определение характеристик моноклональных антител
In vitro исследование выполняли, чтобы продемонстрировать свойства связывания и клеточной активности у NOV004, NOV005 и NOV006. Biacore, как описано в примере 1, применяли для оценки KD у mAb к β-клото человека. Рассчитанные KD для NOV004, NOV005 и NOV006 составляли приблизительно 3xE-10M, 3xE-10M и 4xE-10M, соответственно.
Анализ pERK, как описано в примере 1, применяли для анализа профиля mAb в отношении активации рецептора FGFR_β-клото. NOV004 активировало рецепторный комплекс FGFR1c_β-клото человека и яванского макака, при этом рассчитанная EC50 составляла приблизительно 3 нМ и 20 нМ соответственно (фигура 1). NOV005 активировало рецепторный комплекс FGFR1c_β-клото человека и яванского макака, при этом рассчитанная EC50 составляла приблизительно 3 нМ и 16 нМ соответственно (фигура 1). NOV006 активировало рецепторный комплекс FGFR1c_β-клото человека и яванского макака, при этом рассчитанная EC50 составляла приблизительно 4 нМ и 18 нМ соответственно (фигура 1). NOV005, NOV006 и NOV006 не активировали рецепторные комплексы FGFR2c_β-клото, FGFR3c_β-клото или FGFR4_β-клото человека (фигура 2). mAb подвергали анализу профиля в отношении активации FGF23, как описано в примере 1. NOV005, NOV006 и NOV004 не проявляли активацию FGF23 (фигура 3). Данные Forte Bio демонстрируют, что NOV005 и NOV006 конкурируют с NOV004 за связывание с β-клото человека (фигура 4).
Исследования по картированию эпитопов с помощью водородно-дейтериевого обмена с применением внеклеточного домена β-клото человека с вариантом NOV004, который относится к изотипу IgG1-LALA человека, демонстрируют, что следующие пептиды являются в значительной степени защищенными в комплексе mAb-ECD β-клото: aa 246-265, 343-349, 421-429, 488-498, 509-524, 536-550, 568-576, 646-669, 773-804, 834-857 и 959-986; и что следующие области являются наиболее сильно защищенными: aa 246-265, 536-550, 834-857 и 959-986 (данные не показаны; см. публикацию международной PCT-заявки № WO 2017/021893, которая включена в данный документом посредством ссылки во всей своей полноте). Данные исследования, в сочетании с данными по связыванию, активности и конкуренции, указывают на то, что NOV005 и NOV006 также могли в значительной степени защищать такие области ECD β-клото.
Пример 3. Фармакокинетические профили моноклональных антител в крысах
Животные и условия содержания
Уход за животными и условия содержания животных обеспечивали в соответствии с Руководством по содержанию и использованию лабораторных животных (Institute of Laboratory Animal Resources, National Research Council). Все процедуры регулировались стандартами, установленными Министерством здравоохранения и социальных служб США, и их выполняли в соответствии с протоколом, одобренным Комитетом по уходу и использованию животных Института биомедицинских исследований Novartis (NIBR). Самцов крыс линии Sprague-Dawley (n=3/группа) содержали в клетках с твердым дном на стеллажах, оборудованных для автоматической подачи воды ad libitum, их содержали при цикле 12 ч света/темноты (от 6 утра до 6 вечера) и обеспечивали свободный доступ к стандартному корму для крыс (Harlan-Teklad; Фредерик, Мэриленд; каталожный № 8604). В виварии поддерживали температуру 68-76°F при влажности 30-70%.
Подготовка и введение доз NOV004, NOV005 или NOV006
Исходные растворы NOV004, NOV005 и NOV006 в 10 мМ His/His-HCl, 220 мМ сахарозы, оттаивали в условиях холодильника перед использованием. Утром в день введения дозы все три антитела разводили до приблизительно в 3 мг/мл в PBS и соответствующими объемами заполняли дозировочные шприцы (3 мл/кг) и держали при комнатной температуре до проведения введения. Животных помещали в трубчатую камеру для обездвиживания и вводили одно из NOV004, NOV005 или NOV006 путем внутривенной (IV) инъекции в хвостовую вену (10 мг/кг).
Сбор образцов крови
Образцы крови собирали в день -3 (исходный уровень), день 0 (1 и 6 ч после введения дозы) и дни 1, 2, 3, 4, 8, 16 и 28 после введения дозы. Все моменты времени рассчитывали от конца введения дозы, вводимой в день 0. В каждый момент времени приблизительно 70 мкл крови собирали в пробирки для сбора/разделения с EDTA BD Microtainer (Becton, Dickinson, and Company; Франклин-Лейкс, Нью-Джерси; каталожный № 365973). Для остановки кровотечения применяли давящую марлевую повязку. Образцы центрифугировали в течение 10 мин при 20817 x g, а затем ~30 мкл плазмы крови перемещали в 0,2-мл пробирки Thermo-strip (Thermo-Scientific; Питтсбург, Пенсильвания; каталожный № AB-0451) и замораживали при 80°C. После каждого сбора крыс возвращали в их домашние клетки.
Измерение общих концентраций NOV004, NOV005 или NOV006 в плазме крови
Содержание человеческого IgG (например, NOV004, NOV005 или NOV006) в плазме крови крыс оценивали количественно с применением оригинального иммунологического "сэндвич"-анализа с применением антитела козы к Fc-гамма человека (KPL, № 109-005-098) в качестве антитела захвата и антитела козы к IgG человека с HRP-меткой в качестве детекторного антитела. Антителом захвата (2 мкг/мл в PBS, 30 мкл/лунка) покрывали 384-луночные белые титрационные микропланшеты (Greiner Bio-One; Монро, Северная Каролина; каталожный № 781074). Планшеты инкубировали на протяжении ночи при комнатной температуре (RT) без встряхивания. После аспирации раствора для нанесения покрытия без промывки в каждую лунку добавляли по 90 мкл 1х молочного разбавителя/блокирующего раствора (KPL; Гейтерсбург, Мэриленд; каталожный № 50-82-01) и планшеты инкубировали в течение 2 ч при RT. В конце инкубации раствор аспирировали и планшеты хранили в саше из фольги с влагопоглотителем при -80°C.
В день анализа шестнадцать стандартных концентраций NOV004, NOV005 и NOV006 в диапазоне 0,244-4000 пМ готовили путем серийного разведения в казеиновом буфере, включая буферный отрицательный контроль. Все исследуемые образцы разводили вручную из расчета 1:50 в казеиновом буфере, а затем последовательно разводили в 5 раз с применением Biomek Fx, получая в общей сложности три разведения. Планшеты инкубировали в течение 2 ч при RT и затем 3 раза промывали промывочным фосфатным буфером (90 мкл/лунка). В каждый планшет добавляли меченное пероксидазой хрена антитело козы к IgG человека (400 нг/мл в казеиновом буфере, 30 мкл/лунка) и планшеты инкубировали в течение 1 ч при RT. Планшеты промывали 3 раза промывочным фосфатным буфером (90 мкл/лунка) и затем добавляли хемилюминесцентный субстрат KPL LumiGLO (30 мкл/лунка; каталожный № 54-61-00). Хемилюминесценцию считывали незамедлительно на планшет-ридере SpectraMax M5 (Molecular Devices) при всех длинах волн с временем интегрирования 50 мс. Концентрации Fc человека (пМ) в образцах плазмы крови интерполировали на основании стандартных кривых для NOV004, NOV005 или NOV006, умножали на коэффициенты разбавления и переводили в концентрации в нМ.
Среднюю Cmax, составляющую приблизительно 200 мкг/мл, наблюдали у животных через 1 ч после IV введения NOV004, NOV005 или NOV006. NOV004, NOV005 и NOV006 проявляли эквивалентные PK-профили у крыс линии Sprague-Dawley (фигура 5).
Пример 4. Возможность получения и оценки состава
Выполняли исследования, касающиеся способа получения и состава NOV004, NOV005 и NOV006. Образование высокомолекулярных разновидностей (HMW), наблюдаемое в ходе предыдущих оценок NOV004, свидетельствовало о высокой степени его агрегации в растворе и привело к разработке и оценке других антител-миметиков FGF21, которые характеризуются сопоставимой функциональной активностью, но имеют лучшие характеристики получения и состава, например, малое (например, менее 20%, менее 15%, менее 10% или менее 5%) наблюдаемое образование HMW или его отсутствие.
Последовательности ДНК, кодирующие антитела NOV005 и NOV006, включая оптимизацию кодонов для Homo sapiens, заказывали в GeneArt™ (Life Technologies Inc., Регенсбург, Германия) и ATUM (Менло-Парк, Калифорния). Векторы, экспрессирующие NOV004, NOV005 и NOV006, линеаризовали и трансфицировали в клеточную линию CHO. Пулы отбирали с применением 10 нМ метотрексата (MTX) до восстановления до >95% жизнеспособности. Для получения в биореакторе WAVE и масштабировали до соответствующих размеров отбирали по одному пулу для каждой молекулы. Супернатант культур, получаемых в биореакторе WAVE, собирали через 13 дней и фильтровали.
Материал NOV005 и NOV006, собранный из биореактора WAVE, обрабатывали с применением двух способов очистки с помощью колоночной хроматографии для стандартных антител - захвата с применением аффинной хроматографии (смола - GE Healthcare MabSelect SuRe) и окончательной очистки с применением катионообменной хроматографии (CEC) (смола - Fractogel EMD SO3-). Перед обработкой с помощью CEC захваченный материал подвергали вирусной инактивации (доведение рН до 3,5, инкубация при данном рН при комнатной температуре в течение 70 мин с последующим доведением pH до 5,0) и стерилизующей фильтрации. После проведения CEC осуществляли диафильтрацию материала с заменой буфера на 10 мМ гистидин/гистидин-HCl, pH 5,0, с применением тангенциальной поточной фильтрации. Затем материал концентрировали до приблизительно 200 мг/мл с обеспечением материала для исследований состава. Например, антитела оценивали в буферах для получения состава и определяли некоторые параметры, в частности, образование HMW после 4 недель хранения при 40°C. В таблице 3 ниже обобщены данные из иллюстративного эксперимента, оценивающего образования HMW, наблюдаемое в образцах NOV004, NOV005 и NOV006 после 4 недель хранения при 40°C.
Таблица 3 Образование высокомолекулярных разновидностей (HMW)
LOQ=нижняя граница количественного определения
Отличия последовательностей NOV005 и NOV006 в сравнении с NOV004, обеспечили значительное улучшение с точки зрения образования HMW при хранении. Оба NOV005 и NOV006 проявляли образование HMW на уровне приблизительно менее 1% в случае хранения при 40°C в течение 4 недель, тогда как NOV004 проявляло намного более высокий уровень образования HMW, составляющий приблизительно 64% образования HMW в случае хранения при 40°C в течение 4 недель.
Ниже приведено выравнивание последовательностей VH и VL у NOV005 и NOV004.
VH
Идентичность: 79,2
Сходство: 88,3%
NOV005 1 QVQLQESGPGLVKPSQTLSLTCTVSGYSITSGYTWHWIRQHPGKGLEWIG 50
:|||.|||.|||||..:|.|:|.||||||||||||||:||.|||||||:.
NOV004 1 EVQLVESGGGLVKPGGSLRLSCAVSGYSITSGYTWHWVRQAPGKGLEWLS 50
NOV005 51 YIHYSVYTNYNPSLKSRVTISRDTSKNQFSLKLSSVTAADTAVYYCARRT 100
|||||||||||||:|.|.||||||:||.|.|:::|:.|.|||||||||||
NOV004 51 YIHYSVYTNYNPSVKGRFTISRDTAKNSFYLQMNSLRAEDTAVYYCARRT 100
NOV005 101 TSLERYFDVWGQGTLVTVSS 120
||||||||||||||||||||
NOV004 101 TSLERYFDVWGQGTLVTVSS 120
VL
Идентичность: 99,1%
Сходство: 100,0%
NOV005 1 DIQMTQSPSSLSASVGDRVTITCQASQDISNYLNWYQQKPGKAPKLLIYY 50
||||||||||||||||||||||||||||||||||||||||||||||||||
NOV004 1 DIQMTQSPSSLSASVGDRVTITCQASQDISNYLNWYQQKPGKAPKLLIYY 50
NOV005 51 TSRLQSGVPSRFSGSGSGADYTFTISSLQPEDIATYFCQQGNTLPYTFGQ 100
||||||||||||:|||||||||||||||||||||||||||||||||||||
NOV004 51 TSRLQSGVPSRFTGSGSGADYTFTISSLQPEDIATYFCQQGNTLPYTFGQ 100
NOV005 101 GTKLEIK 107
|||||||
NOV004 101 GTKLEIK 107
Эти данные показывают, что NOV005 и NOV006 неожиданно проявили минимальные тенденции к агрегации, на что указывает образование HMW, в отличие от NOV004, и можно предположить, что NOV005 и NOV006 проявляют подходящие характеристики, и они будут более предпочтительными для получения фармацевтического состава.
Пример 5. Исследование на яванских макаках с ожирением
Изучали эффекты mAb-миметиков FGF21, таких как NOV004, NOV005 или NOV006, на потребление пищи, вес тела и биомаркеры плазмы крови у яванских макаков с ожирением.
Иллюстративные протоколы
Пять самцов яванских макаков обрабатывали с помощью двух подкожных (s.c.) доз mAb-миметиков FGF21, таких как NOV004, NOV005 или NOV006, из расчета 1 мг/кг, которые вводили с интервалом в одну неделю (дни исследования 0 и 7); а потребление пищи, вес тела и биомаркеры плазмы крови оценивали в течение более 100 дней после введения дозы. При введении каждой дозы животных обездвиживали в их домашней клетке, собирали образцы крови, а затем каждому животному вводили подкожно дозу из расчета 1 мг/кг mAb-миметиков FGF21, таких как NOV004, NOV005 или NOV006. Измерения потребления пищи начинали за 1 неделю до введения первой дозы и продолжали на протяжении всего исследования. Рацион исследования взвешивали перед кормлением и каждый день делили на две равные порции. На следующее утро оставшуюся пищу собирали и взвешивали. Число гранул (по 1 г каждая), упавших в поддон-ловушку, подсчитывали и прибавляли к массе оставшейся пищи. Суточное потребление пищи рассчитывали в виде масса предоставленной пищи минус масса собранной пищи. Потребление фруктов и овощей не измеряли. Вес тела до принятия пищи измеряли в двух повторностях по утрам три раза в неделю (до сбора крови или введения дозы) с применением динамической характеристики на весах.
Измерение концентраций mAb-миметиков FGF21 в плазме крови
Содержание Fc IgG человека в плазме крови яванских макаков оценивали количественно с применением иммунологического "сэндвич"-анализа на основе ELISA. IgG1 мыши к IgG человека, моноклональное антитело мыши против IgG человека, применяли в качестве антитела захвата. 384-луночные белые планшеты Greiner покрывали IgG1 мыши к IgG человека при концентрации 2 мкг/мл (30 мкл/лунка) и инкубировали в течение ночи при комнатной температуре (RT). Покрывающее антитело аспирировали и добавляли 1x молочный блокирующий раствор (KPL, № 50-82-01) из расчета 90 мкл/лунку на 2 ч при RT. Блокирующий раствор аспирировали и планшеты хранили при -80°C в пакетах для планшетов с влагопоглотителем до проведения анализа. В день проведения анализа, планшеты и реагенты нагревали до RT. Стандарты получали путем разбавления очищенного IgG от 4000 до 16 пM в оригинальном казеиновом разбавителе для образцов и включали буферный контроль. Образцы разбавляли 1:50, 1:250, 1:1250 и 1: 6250 в двух повторностях в таком же разбавителе, что и стандарты, и затем стандарты, разбавленные образцы и контроли добавляли в планшет на 2 ч при RT (рабочий объем на всех стадиях составлял 30 мкл/лунка). Затем планшеты промывали 3 раза промывочным фосфатным буфером. Меченное пероксидазой хрена (HRP) антитело к Fc-гамма человека добавляли в планшет на 1 час при RT, а затем планшеты промывали 3 раза промывочным фосфатным буфером. В планшет добавляли хемилюминесцентный субстрат и планшеты незамедлительно считывали на люминесцентном планшет-ридере.
Стандарты mAb-миметиков FGF21, например, NOV004, NOV005 или NOV006, анализировали в трех повторностях на планшет. Разбавленные образцы плазмы крови анализировали в двух повторностях. Образцы с неизвестной концентрацией интерполировали на основании стандартной кривой IgG. Аппроксимацию кривой, обратное расчисление, % восстановления и интерполяцию концентраций образцов осуществляли с применением программного обеспечения SoftMax Pro, версии 5.4.1. Сигнал, генерируемый стандартами IgG, наносили на график и аппроксимировали с применением функции аппроксимации к 4-параметрической логистической кривой. Концентрации Fc (пМ) в образцах плазмы крови интерполировали на основании стандартной кривой для mAb-миметиков FGF21 и умножали на коэффициенты разбавления. Анализ установил нижний предел количественного определения (LLOQ) и верхний предел количественного определения(ULOQ). LLOQ и ULOQ определяли как нижнюю и верхнюю концентрацию стандарта со 100% восстановлением ± 20% и CV < 20%, и затем умножали на коэффициенты разбавления.
Обнаружение антител к лекарственному средству
Образцы плазмы крови разбавляли 1:5 в буфере LowCross (Boca Scientific; Бока-Ратон, Флорида; каталожный № 100 500). Готовили реакционную смесь, содержащую 0,6 мкг/мл меченного биотином mAb-миметика FGF21 и 0,6 мкг/мл меченных дигоксигенином mAb-миметика FGF21 в буфере LowCross. Разбавленную плазму крови (80 мкл) смешивали с 160 мкл реакционной смеси в 96-луночных планшетах с U-образным дном (BD Falcon; Биллерика, Массачусетс; каталожный № 351177). Края планшетов герметизировали парафильмом и планшеты инкубировали на качающейся платформе при 37°С в течение 2 ч (150 об/мин, в защищенном от света месте). Затем аликвоту каждой смеси (100 мкл) переносили в двух повторностях в лунки 96-луночных планшетов, покрытых стрептавидином (Roche; каталожный № 11734776001), которые сначала 3 раза промывали промывочным буфером, состоящим из 1X PBS, содержащего 0,05% (объем/объем) Tween-20 (300 мкл на лунку). Планшеты герметизировали и затем инкубировали при RT на качающейся платформе в течение 1 ч (300 об/мин, в защищенном от света месте). Планшеты 3 раза промывали промывочным буфером (300 мкл на лунку), а затем в каждую лунку добавляли по 100 мкл конъюгированного с пероксидазой POD фрагмента Fab к дигоксигенину (Roche; каталожный № 11633716001), разбавленного 1:2500 в буфере LowCross. Планшеты герметизировали, инкубировали при RT на качающейся платформе в течение 45 минут (300 об/мин, в защищенном от света месте), а затем промывали 3 раза промывочным буфером (300 мкл на лунку). В каждую лунку добавляли субстрат TMB One Component HRP Microwell (Bethyl Laboratories; Монтгомери, Техас; каталожный № Е102; 100 мкл/лунка) и синий цвет проявлялся в течение 9-10 мин в защищенном от света месте. Цветовую реакцию останавливали добавлением в каждую лунку по 100 мкл 0,18 н. H2SO4, планшеты подвергали недолгому встряхиванию и желтый цвет измеряли при OD450.
Измерение концентраций глюкозы в плазме крови
Концентрации глюкозы в плазме крови измеряли с применением анализа на уровень глюкозы Autokit (WAKO Chemicals; Ричмонд, Вирджиния; каталожный № 439-90901). Стандартною кривую получали путем разведения калибровочного раствора до стандартов с концентрацией 500, 200, 100, 50, 20 и 0 мг/дл. Реагент для анализа (300 мкл), предварительно нагретый до 37°С, добавляли к 2 мкл плазмы, стандартов и контрольных образцов в 96-луночном прозрачном плоскодонном планшете (Thermo Scientific; каталожный № 269620). Содержимое планшета смешивали на встряхивателе для планшетов в течение 30 с, а затем инкубировали при 37°С в течение 5 мин. После перемешивания в течение 20 с планшет считывали при 505/600 нм с применением устройства Molecular Devices SPECTRAmax PLUS 384 (Саннивейл, Калифорния). Концентрации глюкозы в образцах рассчитывали путем сравнения со стандартной кривой.
Измерение концентраций инсулина в плазме крови
Концентрации инсулина в плазме крови определяли с применением набора для RIA, специфического в отношении инсулина человека, от Millipore (Биллерика, Массачусетс; каталожный № HI-14K) согласно инструкциям производителя.
Соответствующие количества буфера для анализа, стандартов или разбавленных образцов плазмы крови смешивали с
125I-инсулином и антителом к инсулину в 5-мл пробирках PP SARSTEDT размером 75×12 мм(каталожный №
55.526). Содержимое пробирок перемешивали на вортексе, их закрывали и инкубировали в течение 20 ч при RT. После инкубации добавляли 1 мл осаждающего реагента, охлажденного до 4°С, содержимое пробирок перемешивали на вортексе и инкубировали в течение 30 мин при 4°C. Все пробирки центрифугировали в течение 30 мин (3000 об/мин при 4°С), супернатанты сливали, а осадки подсчитывали на автоматическом счетчике гамма-излучения PerkinElmer WIZARD2 (№ модели 2470; PerkinElmer; Волтгем, Массачусетс). Концентрации инсулина рассчитывали путем сравнения со стандартной кривой, полученной с применением известных количеств инсулина.
Измерение концентраций триглицеридов в плазме крови
Концентрации триглицеридов (TG) в плазме крови измеряли с применением набора реагентов для определения уровня триглицеридов (GPO) (Pointe Scientific; Кантон, Мичиган; каталожный № T7532-500). Предварительно подогретый реагент для анализа (300 мкл, 37°C) добавляли к 5 мкл плазмы крови в 96-луночном прозрачном плоскодонном планшете (Thermo Fisher Scientific; Тьюксбери, Массачусетс; каталожный № 269620). Содержимое планшета смешивали на встряхивателе для планшетов в течение 30 с, а затем помещали в инкубатор при 37°С на 5 мин. После перемешивания в течение 20 с измеряли поглощение при 500 нм с помощью планшет-ридера SPECTRAmax PLUS. Концентрации TG рассчитывали путем сравнения с калибровочной кривой, полученной с применением известных количеств стандарта TG (Pointe Scientific; каталожный № T7531-STD).
Измерение концентраций холестерина в плазме крови
Общий холестерин (TC) в плазме крови оценивали количественно с применением набора (жидких) реагентов для определения уровня холестерина (Pointe Scientific; каталожный № C7510-500). Предварительно подогретый реагент для анализа (200 мкл, 37°C) добавляли к 10 мкл плазмы в 96-луночном прозрачном плоскодонном планшете для анализа (Thermo Fisher Scientific; каталожный № 269620). Содержимое планшета смешивали на встряхивателе для планшетов в течение 30 с, а затем инкубировали при 37°С в течение 5 мин. После перемешивания в течение 20 с измеряли поглощение при 500 нм на планшет-ридере SPECTRAmax PLUS. Концентрации холестерина рассчитывали путем сравнения с калибровочной кривой, полученной с применением известных количеств стандарта холестерина (Stanbio Laboratory; Берне, Техас; каталожный № 1012-030).
Измерение концентраций холестерина липопротеинов высокой плотности в плазме крови
Для определения концентраций холестерина липопротеинов высокой плотности (HDL) образец плазмы крови объемом 50 мкл смешивали с 50 мкл реагента для осаждения холестерина (WAKO Chemicals; Ричмонд, Вирджиния; каталожный № 431-52501) в микроцентрифужной пробирке объемом 0,5 мл и недолго перешивали на вортексе. Пробирку оставляли при комнатной температуре на 10 мин и затем центрифугировали при 2000 хg в течение 10 мин при 4°С. После центрифугирования отбирали примерно половину супернатанта (содержащего часть холестерина HDL исходного образца плазмы крови) и 10 мкл использовали для анализа на холестерин, описанного выше.
Измерение концентраций β-гидроксибутирата в плазме крови
Концентрации β-гидроксибутирата (β-HB) в плазме крови измеряли с применением набора для теста на β-гидроксибутират LiquiColor (Stanbio Laboratory; каталожный № 2440-058). Реагент для анализа R1 (215 мкл, предварительно нагретый до 37°C) добавляли к 20 мкл образца для контроля качества или образца плазмы крови в 96-луночном прозрачном плоскодонном планшете (Thermo Fisher Scientific; каталожный № 269620). Содержимое планшета смешивали на встряхивателе для планшетов в течение 30 с, а затем помещали в инкубатор при 37°С на 5 мин. Предварительное считывание поглощения проводили при 505 нм на планшет-ридере SPECTRAmax PLUS. Реагент для анализа R2 (35 мкл, предварительно нагретый до 37°C) добавляли в каждую лунку и содержимое планшета снова перемешивали на встряхивателе для планшетов в течение 30 с и инкубировали при 37°С в течение 5 мин. После перемешивания в течение 20 с определяли конечное поглощение при 505 нм, из которого вычитали предварительно считанное значение. Концентрации β-HB рассчитывали путем сравнения с калибровочной кривой, полученной с применением известных количеств калибровочного раствора β-HB (Wako Diagnostics; Ричмонд, Вирджиния; каталожный № 412-73791).
Статистические анализы
Статистические анализы проводили с применением Graphpad Prism (версия 6.05; GraphPad Software; Ла-Хойя, Калифорния). Данные о поглощенной пище для каждого животного стандартизовали как процент от исходного уровня (рассчитанного как среднее для дней от - 6 до 0), а затем рассчитывали групповые средние ± стандартные ошибки среднего (SEM); при этом каждый день сравнивали с днем 0 с помощью непараметрического критерия Фридмана с использованием апостериорного критерия Данна для множественных сравнений. Значения веса тела представляли в виде групповых средних ± стандартные ошибки среднего (SEM), рассчитанные как процент от исходного уровня (рассчитанного как среднее для дней -7, -5, -3 и 0). Первичные данные веса тела и биомаркеров плазмы крови также анализировали с помощью непараметрического критерия Фридмана с использованием апостериорного критерия Данна для множественных сравнений. Значимым считали Р < 0,05.
Пример 6. Исследование на яванских макаках с ожирением
Для оценки эффектов NOV005 у самцов яванских макаков с нормогликемическим ожирением им вводили две подкожные дозы NOV005 из расчета 1 мг/кг (n=5 животных) или среду-носитель (n=3 животных) с промежутком в одну неделю. Предварительные результаты исследования обобщены ниже.
• NOV005 снижал потребление пищи в виде стандартного рациона, при этом максимальное среднее уменьшение составляло приблизительно 60% по сравнению с исходным уровнем (фигура 6А), а максимальное среднее уменьшение массы составляло примерно 10% по сравнению с исходным уровнем у животных, обрабатываемых с помощью NOV005 (фигура 6B).
• Плазму крови животных, взятую в состоянии не натощак, анализировали на изменения биомаркеров липидного и углеводного обмена:
o среднее снижение уровней TG в плазме крови составляло приблизительно 65% по сравнению с исходным уровнем у животных, обрабатываемых с помощью NOV005, ко дню 35;
o NOV005 также снижал уровни общего холестерина и инсулина по сравнению с исходным уровнем ко дню 35, но эти изменения не были статистически значимыми;
o другие биомаркеры, которые будут измеряться в конце исследования, включают профили адипонектина, β-гидроксибутирата, ApoCIII, HDL-C и липопротеинов.
Таблица 4. NOV005 нормализовал уровни биомаркеров в плазме крови у яванских макаков с ожирением
1Для измерений биомаркеров кровь у животных собирали в состоянии не натощак.
2Значения исходного уровня отражают среднее для дней -7, -3 и 0.
3Процентное изменение рассчитывали для каждой особи и затем усредняли для группового среднего ± SEM.
*P < 0,05 в сравнении с исходным уровнем на основании непараметрического критерия Фридмана с апостериорным критерием Данна.
Включение посредством ссылки
Все литературные источники, процитированные в данном документе, включая патенты, заявки на патенты, рукописи, учебные пособия и т. п., а также литературные источники, процитированные в них, в тех случаях, когда они еще не упоминались, настоящим включены в данный документ посредством ссылки во всей своей полноте.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> NOVARTIS AG
<120> АНТИТЕЛА-МИМЕТИКИ FGF21 И ПУТИ ИХ ПРИМЕНЕНИЯ
<130> PAT057578-WO-PCT
<140>
<141>
<150> 62/456,609
<151> 2017-02-08
<160> 64
<170> PatentIn версия 3.5
<210> 1
<211> 209
<212> БЕЛОК
<213> Homo sapiens
<400> 1
Met Asp Ser Asp Glu Thr Gly Phe Glu His Ser Gly Leu Trp Val Ser
1 5 10 15
Val Leu Ala Gly Leu Leu Leu Gly Ala Cys Gln Ala His Pro Ile Pro
20 25 30
Asp Ser Ser Pro Leu Leu Gln Phe Gly Gly Gln Val Arg Gln Arg Tyr
35 40 45
Leu Tyr Thr Asp Asp Ala Gln Gln Thr Glu Ala His Leu Glu Ile Arg
50 55 60
Glu Asp Gly Thr Val Gly Gly Ala Ala Asp Gln Ser Pro Glu Ser Leu
65 70 75 80
Leu Gln Leu Lys Ala Leu Lys Pro Gly Val Ile Gln Ile Leu Gly Val
85 90 95
Lys Thr Ser Arg Phe Leu Cys Gln Arg Pro Asp Gly Ala Leu Tyr Gly
100 105 110
Ser Leu His Phe Asp Pro Glu Ala Cys Ser Phe Arg Glu Leu Leu Leu
115 120 125
Glu Asp Gly Tyr Asn Val Tyr Gln Ser Glu Ala His Gly Leu Pro Leu
130 135 140
His Leu Pro Gly Asn Lys Ser Pro His Arg Asp Pro Ala Pro Arg Gly
145 150 155 160
Pro Ala Arg Phe Leu Pro Leu Pro Gly Leu Pro Pro Ala Leu Pro Glu
165 170 175
Pro Pro Gly Ile Leu Ala Pro Gln Pro Pro Asp Val Gly Ser Ser Asp
180 185 190
Pro Leu Ser Met Val Gly Pro Ser Gln Gly Arg Ser Pro Ser Tyr Ala
195 200 205
Ser
<210> 2
<211> 938
<212> ДНК
<213> Homo sapiens
<400> 2
ctgtcagctg aggatccagc cgaaagagga gccaggcact caggccacct gagtctactc 60
acctggacaa ctggaatctg gcaccaattc taaaccactc agcttctccg agctcacacc 120
ccggagatca cctgaggacc cgagccattg atggactcgg acgagaccgg gttcgagcac 180
tcaggactgt gggtttctgt gctggctggt cttctgctgg gagcctgcca ggcacacccc 240
atccctgact ccagtcctct cctgcaattc gggggccaag tccggcagcg gtacctctac 300
acagatgatg cccagcagac agaagcccac ctggagatca gggaggatgg gacggtgggg 360
ggcgctgctg accagagccc cgaaagtctc ctgcagctga aagccttgaa gccgggagtt 420
attcaaatct tgggagtcaa gacatccagg ttcctgtgcc agcggccaga tggggccctg 480
tatggatcgc tccactttga ccctgaggcc tgcagcttcc gggagctgct tcttgaggac 540
ggatacaatg tttaccagtc cgaagcccac ggcctcccgc tgcacctgcc agggaacaag 600
tccccacacc gggaccctgc accccgagga ccagctcgct tcctgccact accaggcctg 660
ccccccgcac tcccggagcc acccggaatc ctggcccccc agccccccga tgtgggctcc 720
tcggaccctc tgagcatggt gggaccttcc cagggccgaa gccccagcta cgcttcctga 780
agccagaggc tgtttactat gacatctcct ctttatttat taggttattt atcttattta 840
tttttttatt tttcttactt gagataataa agagttccag aggagaaaaa aaaaaaaaaa 900
aaaaaaaaaa aaaaaaaaaa aaaaaaaaaa aaaaaaaa 938
<210> 3
<400> 3
000
<210> 4
<400> 4
000
<210> 5
<400> 5
000
<210> 6
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 6
Gly Tyr Ser Ile Thr Ser Gly Tyr Thr Trp His
1 5 10
<210> 7
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 7
Tyr Ile His Tyr Ser Val Tyr Thr Asn Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 8
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 8
Arg Thr Thr Ser Leu Glu Arg Tyr Phe Asp Val
1 5 10
<210> 9
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 9
Ser Gly Tyr Thr Trp His
1 5
<210> 10
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 10
Gly Tyr Ser Ile Thr Ser Gly Tyr
1 5
<210> 11
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 11
His Tyr Ser Val Tyr
1 5
<210> 12
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 12
Gly Tyr Ser Ile Thr Ser Gly Tyr Thr
1 5
<210> 13
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 13
Ile His Tyr Ser Val Tyr Thr
1 5
<210> 14
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 14
Ala Arg Arg Thr Thr Ser Leu Glu Arg Tyr Phe Asp Val
1 5 10
<210> 15
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 15
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Tyr Ser Ile Thr Ser Gly
20 25 30
Tyr Thr Trp His Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Tyr Ile His Tyr Ser Val Tyr Thr Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Thr Thr Ser Leu Glu Arg Tyr Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 16
<211> 360
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полинуклеотид"
<400> 16
caagtgcagc tgcaggaatc tggccctggc ctggtcaagc ctagccagac cctgtccctg 60
acctgcaccg tgtccggcta ctccatcacc tccggctaca cctggcactg gatccggcag 120
caccccggca agggcctgga atggatcggc tacatccact actccgtgta caccaactac 180
aaccccagcc tgaagtccag agtgaccatc tcccgggaca cctccaagaa ccagttctcc 240
ctgaagctgt cctccgtgac cgccgctgac accgccgtgt actactgcgc cagacggacc 300
acctccctgg aacggtactt cgacgtgtgg ggccagggca ccctggtcac cgtgtcctct 360
<210> 17
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 17
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Gln
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Tyr Ser Ile Thr Ser Gly
20 25 30
Tyr Thr Trp His Trp Ile Arg Gln His Pro Gly Lys Gly Leu Glu Trp
35 40 45
Ile Gly Tyr Ile His Tyr Ser Val Tyr Thr Asn Tyr Asn Pro Ser Leu
50 55 60
Lys Ser Arg Val Thr Ile Ser Arg Asp Thr Ser Lys Asn Gln Phe Ser
65 70 75 80
Leu Lys Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Thr Thr Ser Leu Glu Arg Tyr Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Ala Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Ala Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 18
<211> 1350
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полинуклеотид"
<400> 18
caagtgcagc tgcaggaatc tggccctggc ctggtcaagc ctagccagac cctgtccctg 60
acctgcaccg tgtccggcta ctccatcacc tccggctaca cctggcactg gatccggcag 120
caccccggca agggcctgga atggatcggc tacatccact actccgtgta caccaactac 180
aaccccagcc tgaagtccag agtgaccatc tcccgggaca cctccaagaa ccagttctcc 240
ctgaagctgt cctccgtgac cgccgctgac accgccgtgt actactgcgc cagacggacc 300
acctccctgg aacggtactt cgacgtgtgg ggccagggca ccctggtcac cgtgtcctct 360
gcttccacca aggggccctc cgtgttccct ctggcccctt ccagcaagtc cacctctggc 420
ggcaccgccg ctctgggctg cctcgtgaag gactacttcc ccgagcccgt gaccgtgtcc 480
tggaactctg gcgccctgac ctccggcgtg cacaccttcc ctgccgtgct gcagtcctcc 540
ggcctgtact ccctgtccag cgtcgtgacc gtgccctcca gctctctggg cacccagacc 600
tacatctgca acgtgaacca caagccctcc aacaccaaag tggacaagcg ggtggaaccc 660
aagtcctgcg acaagaccca cacctgtcct ccctgccctg cccctgagct gctgggcgga 720
ccttccgtgt tcctgttccc tccaaagccc aaggacaccc tgatgatctc ccggacccct 780
gaagtgacct gcgtggtggt ggccgtgtcc cacgaggatc ccgaagtgaa gttcaattgg 840
tacgtggacg gcgtggaagt gcacaacgcc aagaccaagc ccagagagga acagtacaac 900
tccacctacc gggtggtgtc cgtgctgacc gtgctgcacc aggactggct gaacggcaaa 960
gagtacaagt gcaaagtgtc caacaaggcc ctggccgctc ccatcgaaaa gaccatctcc 1020
aaggccaagg gccagccccg cgagccccaa gtgtacacac tgcctcccag ccgggaagag 1080
atgaccaaga atcaagtgtc cctgacatgt ctggtcaagg gcttctaccc tagcgatatc 1140
gccgtggaat gggagtccaa cggccagcct gagaacaact acaagaccac ccctcccgtg 1200
ctggactccg acggctcatt cttcctgtac tccaagctga ccgtggacaa gtcccggtgg 1260
cagcagggca acgtgttctc ctgctccgtg atgcacgagg ccctgcacaa ccactacacc 1320
cagaagtccc tgagcctgtc ccctggcaag 1350
<210> 19
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 19
Gln Ala Ser Gln Asp Ile Ser Asn Tyr Leu Asn
1 5 10
<210> 20
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 20
Tyr Thr Ser Arg Leu Gln Ser
1 5
<210> 21
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 21
Gln Gln Gly Asn Thr Leu Pro Tyr Thr
1 5
<210> 22
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 22
Ser Gln Asp Ile Ser Asn Tyr
1 5
<210> 23
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 23
Tyr Thr Ser
1
<210> 24
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 24
Gly Asn Thr Leu Pro Tyr
1 5
<210> 25
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 25
Gln Asp Ile Ser Asn Tyr
1 5
<210> 26
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 26
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Arg Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Ala Asp Tyr Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 27
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полинуклеотид"
<400> 27
gacatccaga tgacccagag cccgtcgtcc ctctccgctt ccgtgggaga tagagtgacc 60
atcacctgtc aagccagcca ggatatttca aactacctga attggtacca gcagaagccg 120
gggaaggctc ccaagttgct catctactac acatcgaggc tgcagtccgg cgtgcccagc 180
cggttctccg ggtccggatc aggcgccgac tataccttca ccatttcctc cctgcaaccg 240
gaggacattg ccacttactt ctgccaacaa gggaacaccc tgccctacac tttcggacaa 300
ggaactaagc tggaaatcaa g 321
<210> 28
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 28
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Arg Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Ala Asp Tyr Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 29
<211> 642
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полинуклеотид"
<400> 29
gacatccaga tgacccagag cccctccagc ctgtccgcct ccgtgggcga cagagtgacc 60
atcacctgtc aggcctccca ggacatctcc aactacctga actggtatca gcagaagccc 120
ggcaaggccc ctaagctgct gatctactac acctcccggc tgcagtccgg cgtgccctcc 180
agattctccg gctctggctc tggcgccgac tacaccttca ccatctccag cctgcagccc 240
gaggatatcg ctacctactt ctgtcagcaa ggcaacaccc tgccctacac cttcggccag 300
ggcaccaagc tggaaatcaa gcgtacggtg gccgctccct ccgtgttcat cttcccaccc 360
tccgacgagc agctgaagtc cggcaccgcc tccgtcgtgt gcctgctgaa caacttctac 420
cctcgcgagg ccaaagtgca gtggaaagtg gacaacgccc tgcagagcgg caactcccag 480
gaatccgtca ccgagcagga ctccaaggac agcacctact ccctgtcctc caccctgacc 540
ctgtccaagg ccgactacga gaagcacaaa gtgtacgcct gcgaagtgac ccaccagggc 600
ctgtccagcc ccgtgaccaa gtccttcaac cggggcgagt gc 642
<210> 30
<211> 1350
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полинуклеотид"
<400> 30
caagtgcagc tgcaggaatc tggccctggc ctggtcaagc ctagccagac cctgtccctg 60
acctgcaccg tgtccggcta ctccatcacc tccggctaca cctggcactg gatccggcag 120
caccccggca agggcctgga atggatcggc tacatccact actccgtgta caccaactac 180
aaccccagcc tgaagtccag agtgaccatc tcccgggaca cctccaagaa ccagttctcc 240
ctgaagctgt cctccgtgac cgccgctgac accgccgtgt actactgcgc cagacggacc 300
acctccctgg aacggtactt cgacgtgtgg ggccagggca ccctggtcac cgtgtcctct 360
gcttccacca aggggccctc cgtgttccct ctggcccctt ccagcaagtc cacctctggc 420
ggcaccgccg ctctgggctg cctcgtgaag gactacttcc ccgagcccgt gaccgtgtcc 480
tggaactctg gcgccctgac ctccggcgtg cacaccttcc ctgccgtgct gcagtcctcc 540
ggcctgtact ccctgtccag cgtcgtgacc gtgccctcca gctctctggg cacccagacc 600
tacatctgca acgtgaacca caagccctcc aacaccaaag tggacaagcg ggtggaaccc 660
aagtcctgcg acaagaccca cacctgtcct ccctgccctg cccctgagct gctgggcgga 720
ccttccgtgt tcctgttccc tccaaagccc aaggacaccc tgatgatctc ccggacccct 780
gaagtgacct gcgtggtggt ggccgtgtcc cacgaggatc ccgaagtgaa gttcaattgg 840
tacgtggacg gcgtggaagt gcacaacgcc aagaccaagc ccagagagga acagtacaac 900
tccacctacc gggtggtgtc cgtgctgacc gtgctgcacc aggactggct gaacggcaaa 960
gagtacaagt gcaaagtgtc caacaaggcc ctggccgctc ccatcgaaaa gaccatctcc 1020
aaggccaagg gccagccccg cgagccccaa gtgtacacac tgcctcccag ccgggaagag 1080
atgaccaaga atcaagtgtc cctgacatgt ctggtcaagg gcttctaccc tagcgatatc 1140
gccgtggaat gggagtccaa cggccagcct gagaacaact acaagaccac ccctcccgtg 1200
ctggactccg acggctcatt cttcctgtac tccaagctga ccgtggacaa gtcccggtgg 1260
cagcagggca acgtgttctc ctgctccgtg atgcacgagg ccctgcacaa ccactacacc 1320
cagaagtccc tgagcctgtc ccctggcaag 1350
<210> 31
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 31
Arg Ala Ser Gln Asp Ile Ser Asn Tyr Leu Asn
1 5 10
<210> 32
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 32
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Arg Leu Gln Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Ala Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 33
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полинуклеотид"
<400> 33
gagatcgtga tgacccagtc ccctgccacc ctgtccctga gccctggcga gagagccacc 60
ctgagctgcc gggcctccca ggacatctcc aactacctga actggtatca gcagaagccc 120
ggccaggccc ctcggctgct gatctactac acctcccggc tgcagtccgg catccctgcc 180
agattctccg gctctggctc tggcgccgac tacaccctga ccatctccag cctgcagccc 240
gaggacttcg ccgtgtactt ctgtcagcaa ggcaacaccc tgccctacac cttcggccag 300
ggcaccaagc tggaaatcaa g 321
<210> 34
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 34
Glu Ile Val Met Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Arg Leu Gln Ser Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Ala Asp Tyr Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 35
<211> 642
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полинуклеотид"
<400> 35
gagatcgtga tgacccagtc ccctgccacc ctgtccctga gccctggcga gagagccacc 60
ctgagctgcc gggcctccca ggacatctcc aactacctga actggtatca gcagaagccc 120
ggccaggccc ctcggctgct gatctactac acctcccggc tgcagtccgg catccctgcc 180
agattctccg gctctggctc tggcgccgac tacaccctga ccatctccag cctgcagccc 240
gaggacttcg ccgtgtactt ctgtcagcaa ggcaacaccc tgccctacac cttcggccag 300
ggcaccaagc tggaaatcaa gcgtacggtg gccgctccct ccgtgttcat cttcccaccc 360
tccgacgagc agctgaagtc cggcaccgcc tccgtcgtgt gcctgctgaa caacttctac 420
cctcgcgagg ccaaagtgca gtggaaagtg gacaacgccc tgcagagcgg caactcccag 480
gaatccgtca ccgagcagga ctccaaggac agcacctact ccctgtcctc caccctgacc 540
ctgtccaagg ccgactacga gaagcacaaa gtgtacgcct gcgaagtgac ccaccagggc 600
ctgtccagcc ccgtgaccaa gtccttcaac cggggcgagt gc 642
<210> 36
<211> 360
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полинуклеотид"
<400> 36
caagtccagc tgcaagaatc cggacccggc ctcgtcaagc cgtcccagac tctgtctctc 60
acttgcacgg tgtcaggcta cagcatcacc agcggttaca cctggcactg gatcaggcag 120
catcctggaa aggggctgga atggattggg tacattcact actcggtgta caccaactac 180
aacccatcgc tcaagtcgag agtcaccatt tcccgggaca cctccaagaa ccagttcagc 240
ctcaagctgt cctctgtgac cgccgctgat actgccgtgt actattgcgc acgccggact 300
acttccctgg agcgctactt cgacgtctgg ggccagggca ctttggtcac cgtcagctcc 360
<210> 37
<211> 1350
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полинуклеотид"
<400> 37
caagtccagc tgcaagaatc cggacccggc ctcgtcaagc cgtcccagac tctgtctctc 60
acttgcacgg tgtcaggcta cagcatcacc agcggttaca cctggcactg gatcaggcag 120
catcctggaa aggggctgga atggattggg tacattcact actcggtgta caccaactac 180
aacccatcgc tcaagtcgag agtcaccatt tcccgggaca cctccaagaa ccagttcagc 240
ctcaagctgt cctctgtgac cgccgctgat actgccgtgt actattgcgc acgccggact 300
acttccctgg agcgctactt cgacgtctgg ggccagggca ctttggtcac cgtcagctcc 360
gccagcacta agggccccag cgtgtttccg ctggccccct cctccaaaag cacctccggc 420
ggaactgccg cgctcggatg tctcgtgaag gactatttcc ccgagcctgt gacagtgtca 480
tggaactcgg gagcactgac cagcggagtg catacttttc ccgcggtcct gcagtcctcc 540
ggattgtaca gcctgtcatc ggtcgtgacc gtgccgtcct catcgctggg cacccagacc 600
tacatctgca acgtgaacca caaacctagc aacaccaaag tggataagcg ggtggaacct 660
aagtcctgcg acaagactca cacttgtccg ccatgcccag cgcctgaact cctgggtggt 720
ccttcggtgt tcctgttccc gccaaagccg aaggacaccc tgatgatctc ccggacgcct 780
gaagtgacct gtgtggtggt ggctgtgtca catgaggacc ctgaagtcaa gttcaattgg 840
tacgtggacg gcgtggaggt gcacaacgcc aagaccaagc ctagagagga acagtacaac 900
tccacctacc gcgtcgtgtc ggtgctgacc gtgttgcacc aagactggct gaatggaaag 960
gagtataagt gcaaagtgtc caacaaggcc ctggccgcac caattgagaa aaccatctcc 1020
aaggccaagg gacagccgcg cgaaccccaa gtgtacaccc ttcccccgtc ccgggaggaa 1080
atgaccaaga atcaagtctc cctgacttgc cttgtgaagg gtttctaccc ctccgacatc 1140
gccgtggagt gggagtcaaa cgggcagccg gaaaacaact acaagaccac acctccggtg 1200
ctggattccg acggctcctt cttcttgtac tcgaagctga ccgtggataa gagcaggtgg 1260
cagcagggaa acgtgttctc ctgctccgtg atgcacgaag ctctgcacaa ccactacact 1320
cagaagtcgc tctcgctgag ccccgggaag 1350
<210> 38
<211> 360
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полинуклеотид"
<400> 38
caagtccagc tgcaagaatc cggacccggc ctcgtcaagc cgtcccagac tctgtctctc 60
acttgcacgg tgtcaggcta cagcatcacc agcggttaca cctggcactg gatcaggcag 120
catcctggaa aggggctgga atggattggg tacattcact actcggtgta caccaactac 180
aacccatcgc tcaagtcgag agtcaccatt tcccgggaca cctccaagaa ccagttcagc 240
ctcaagctgt cctctgtgac cgccgctgat actgccgtgt actattgcgc acgccggact 300
acttccctgg agcgctactt cgacgtctgg ggccagggca ctttggtcac cgtcagctcc 360
<210> 39
<211> 1350
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полинуклеотид"
<400> 39
caagtccagc tgcaagaatc cggacccggc ctcgtcaagc cgtcccagac tctgtctctc 60
acttgcacgg tgtcaggcta cagcatcacc agcggttaca cctggcactg gatcaggcag 120
catcctggaa aggggctgga atggattggg tacattcact actcggtgta caccaactac 180
aacccatcgc tcaagtcgag agtcaccatt tcccgggaca cctccaagaa ccagttcagc 240
ctcaagctgt cctctgtgac cgccgctgat actgccgtgt actattgcgc acgccggact 300
acttccctgg agcgctactt cgacgtctgg ggccagggca ctttggtcac cgtcagctcc 360
gccagcacta agggccccag cgtgtttccg ctggccccct cctccaaaag cacctccggc 420
ggaactgccg cgctcggatg tctcgtgaag gactatttcc ccgagcctgt gacagtgtca 480
tggaactcgg gagcactgac cagcggagtg catacttttc ccgcggtcct gcagtcctcc 540
ggattgtaca gcctgtcatc ggtcgtgacc gtgccgtcct catcgctggg cacccagacc 600
tacatctgca acgtgaacca caaacctagc aacaccaaag tggataagcg ggtggaacct 660
aagtcctgcg acaagactca cacttgtccg ccatgcccag cgcctgaact cctgggtggt 720
ccttcggtgt tcctgttccc gccaaagccg aaggacaccc tgatgatctc ccggacgcct 780
gaagtgacct gtgtggtggt ggctgtgtca catgaggacc ctgaagtcaa gttcaattgg 840
tacgtggacg gcgtggaggt gcacaacgcc aagaccaagc ctagagagga acagtacaac 900
tccacctacc gcgtcgtgtc ggtgctgacc gtgttgcacc aagactggct gaatggaaag 960
gagtataagt gcaaagtgtc caacaaggcc ctggccgcac caattgagaa aaccatctcc 1020
aaggccaagg gacagccgcg cgaaccccaa gtgtacaccc ttcccccgtc ccgggaggaa 1080
atgaccaaga atcaagtctc cctgacttgc cttgtgaagg gtttctaccc ctccgacatc 1140
gccgtggagt gggagtcaaa cgggcagccg gaaaacaact acaagaccac acctccggtg 1200
ctggattccg acggctcctt cttcttgtac tcgaagctga ccgtggataa gagcaggtgg 1260
cagcagggaa acgtgttctc ctgctccgtg atgcacgaag ctctgcacaa ccactacact 1320
cagaagtcgc tctcgctgag ccccgggaag 1350
<210> 40
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полинуклеотид"
<400> 40
gaaatcgtga tgactcagtc ccccgccact ctctccctgt cccctggcga acgggccacc 60
ctgtcgtgcc gggcgtcgca ggacatctca aactatctga actggtacca gcagaagcct 120
ggacaggcac ccaggctcct gatctactac acctcgcgcc tgcaatccgg aatcccagcc 180
cgcttctccg gttccggctc cggcgctgat tacaccctca ccattagcag cctgcagccg 240
gaggacttcg ccgtgtactt ctgtcaacaa ggaaacaccc tcccgtacac atttgggcag 300
ggaaccaagc tggagattaa g 321
<210> 41
<211> 642
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полинуклеотид"
<400> 41
gaaatcgtga tgactcagtc ccccgccact ctctccctgt cccctggcga acgggccacc 60
ctgtcgtgcc gggcgtcgca ggacatctca aactatctga actggtacca gcagaagcct 120
ggacaggcac ccaggctcct gatctactac acctcgcgcc tgcaatccgg aatcccagcc 180
cgcttctccg gttccggctc cggcgctgat tacaccctca ccattagcag cctgcagccg 240
gaggacttcg ccgtgtactt ctgtcaacaa ggaaacaccc tcccgtacac atttgggcag 300
ggaaccaagc tggagattaa gcgtacggtg gccgcgccgt ccgtgttcat cttccctcct 360
tctgacgagc agctcaagag cggcaccgcg tcggtggtct gcctgctgaa caacttctac 420
ccacgggagg ccaaggtcca gtggaaagtg gataacgcat tgcagtcggg aaactcacag 480
gagtcggtga ccgaacagga ctccaaagac tcaacctact ccctgtcctc cactcttacc 540
ctgtccaagg cggactacga aaagcacaag gtctacgcct gcgaagtgac ccatcagggt 600
ctgagcagcc ctgtgactaa gagctttaac cgcggcgaat gc 642
<210> 42
<211> 16
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
пептид"
<400> 42
Tyr Ile His Tyr Ser Val Tyr Thr Asn Tyr Asn Pro Ser Val Lys Gly
1 5 10 15
<210> 43
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 43
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Tyr Ser Ile Thr Ser Gly
20 25 30
Tyr Thr Trp His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
35 40 45
Leu Ser Tyr Ile His Tyr Ser Val Tyr Thr Asn Tyr Asn Pro Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Thr Ala Lys Asn Ser Phe Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Thr Thr Ser Leu Glu Arg Tyr Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 44
<211> 360
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полинуклеотид"
<400> 44
gaagtccaac tcgtcgaatc cggcggcgga ctggtcaagc cgggaggatc gctgagactg 60
tcgtgcgcag tgtcagggta cagcatcacc tccggttaca cctggcactg ggtcagacag 120
gcgccgggaa aaggcctgga atggctgtcc tacattcatt actccgtgta cactaactac 180
aacccctcag tgaaggggcg gttcaccatc tcccgggaca ctgccaagaa tagcttctat 240
ctgcaaatga actccctgcg ggccgaggat accgccgtgt actactgcgc gaggcgcacc 300
acgtccctgg agcgctactt tgacgtgtgg ggccagggta ccctcgtgac tgtgtcctcg 360
<210> 45
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 45
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Tyr Ser Ile Thr Ser Gly
20 25 30
Tyr Thr Trp His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
35 40 45
Leu Ser Tyr Ile His Tyr Ser Val Tyr Thr Asn Tyr Asn Pro Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Thr Ala Lys Asn Ser Phe Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Thr Thr Ser Leu Glu Arg Tyr Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Ala Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Ala Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 46
<211> 1350
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полинуклеотид"
<400> 46
gaagtccaac tcgtcgaatc cggcggcgga ctggtcaagc cgggaggatc gctgagactg 60
tcgtgcgcag tgtcagggta cagcatcacc tccggttaca cctggcactg ggtcagacag 120
gcgccgggaa aaggcctgga atggctgtcc tacattcatt actccgtgta cactaactac 180
aacccctcag tgaaggggcg gttcaccatc tcccgggaca ctgccaagaa tagcttctat 240
ctgcaaatga actccctgcg ggccgaggat accgccgtgt actactgcgc gaggcgcacc 300
acgtccctgg agcgctactt tgacgtgtgg ggccagggta ccctcgtgac tgtgtcctcg 360
gctagcacca agggcccctc cgtgttccct ctggcccctt ccagcaagtc tacctccggc 420
ggcacagctg ctctgggctg cctggtcaag gactacttcc ctgagcctgt gacagtgtcc 480
tggaactctg gcgccctgac ctctggcgtg cacaccttcc ctgccgtgct gcagtcctcc 540
ggcctgtact ccctgtcctc cgtggtcaca gtgccttcaa gcagcctggg cacccagacc 600
tatatctgca acgtgaacca caagccttcc aacaccaagg tggacaagcg ggtggagcct 660
aagtcctgcg acaagaccca cacctgtcct ccctgccctg ctcctgaact gctgggcggc 720
ccttctgtgt tcctgttccc tccaaagccc aaggacaccc tgatgatctc ccggacccct 780
gaagtgacct gcgtggtggt ggccgtgtcc cacgaggatc ctgaagtgaa gttcaattgg 840
tacgtggacg gcgtggaggt gcacaacgcc aagaccaagc ctcgggagga acagtacaac 900
tccacctacc gggtggtgtc cgtgctgacc gtgctgcacc aggactggct gaacggcaaa 960
gagtacaagt gcaaagtctc caacaaggcc ctggccgccc ctatcgaaaa gacaatctcc 1020
aaggccaagg gccagcctag ggaaccccag gtgtacaccc tgccacccag ccgggaggaa 1080
atgaccaaga accaggtgtc cctgacctgt ctggtcaagg gcttctaccc ttccgatatc 1140
gccgtggagt gggagtctaa cggccagcct gagaacaact acaagaccac ccctcctgtg 1200
ctggactccg acggctcctt cttcctgtac tccaaactga ccgtggacaa gtcccggtgg 1260
cagcagggca acgtgttctc ctgctccgtg atgcacgagg ccctgcacaa ccactacacc 1320
cagaagtccc tgtccctgtc tcccggcaag 1350
<210> 47
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 47
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Arg Leu Gln Ser Gly Val Pro Ser Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Ala Asp Tyr Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 48
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полинуклеотид"
<400> 48
gatattcaga tgactcagag cccctcctcg ctctccgcct ccgtggggga tcgcgtgaca 60
atcacctgtc aagcgtccca ggacatctca aactacctga actggtatca gcagaagcca 120
gggaaggccc cgaagctgct gatctactac acttcgcggc tgcagtccgg cgtgccgtca 180
cggttcactg gctcgggctc cggagcagac tacaccttca ccattagcag cctgcagccc 240
gaggacatcg ctacctactt ttgccaacaa ggaaacaccc tgccttacac cttcggacag 300
ggtactaagc tggaaatcaa a 321
<210> 49
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 49
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Arg Leu Gln Ser Gly Val Pro Ser Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Ala Asp Tyr Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 50
<211> 642
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полинуклеотид"
<400> 50
gatattcaga tgactcagag cccctcctcg ctctccgcct ccgtggggga tcgcgtgaca 60
atcacctgtc aagcgtccca ggacatctca aactacctga actggtatca gcagaagcca 120
gggaaggccc cgaagctgct gatctactac acttcgcggc tgcagtccgg cgtgccgtca 180
cggttcactg gctcgggctc cggagcagac tacaccttca ccattagcag cctgcagccc 240
gaggacatcg ctacctactt ttgccaacaa ggaaacaccc tgccttacac cttcggacag 300
ggtactaagc tggaaatcaa acgtacggtg gccgctccca gcgtgttcat cttccccccc 360
agcgacgagc agctgaagag cggcaccgcc agcgtggtgt gcctgctgaa caacttctac 420
ccccgggagg ccaaggtgca gtggaaggtg gacaacgccc tgcagagcgg caacagccag 480
gagagcgtca ccgagcagga cagcaaggac tccacctaca gcctgagcag caccctgacc 540
ctgagcaagg ccgactacga gaagcataag gtgtacgcct gcgaggtgac ccaccagggc 600
ctgtccagcc ccgtgaccaa gagcttcaac aggggcgagt gc 642
<210> 51
<211> 642
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полинуклеотид"
<400> 51
gacatccaga tgacccagag cccgtcgtcc ctctccgctt ccgtgggaga tagagtgacc 60
atcacctgtc aagccagcca ggatatttca aactacctga attggtacca gcagaagccg 120
gggaaggctc ccaagttgct catctactac acatcgaggc tgcagtccgg cgtgcccagc 180
cggttctccg ggtccggatc aggcgccgac tataccttca ccatttcctc cctgcaaccg 240
gaggacattg ccacttactt ctgccaacaa gggaacaccc tgccctacac tttcggacaa 300
ggaactaagc tggaaatcaa gcgtacggtg gccgcgccgt ccgtgttcat cttccctcct 360
tctgacgagc agctcaagag cggcaccgcg tcggtggtct gcctgctgaa caacttctac 420
ccacgggagg ccaaggtcca gtggaaagtg gataacgcat tgcagtcggg aaactcacag 480
gagtcggtga ccgaacagga ctccaaagac tcaacctact ccctgtcctc cactcttacc 540
ctgtccaagg cggactacga aaagcacaag gtctacgcct gcgaagtgac ccatcagggt 600
ctgagcagcc ctgtgactaa gagctttaac cgcggcgaat gc 642
<210> 52
<211> 1044
<212> БЕЛОК
<213> Homo sapiens
<400> 52
Met Lys Pro Gly Cys Ala Ala Gly Ser Pro Gly Asn Glu Trp Ile Phe
1 5 10 15
Phe Ser Thr Asp Glu Ile Thr Thr Arg Tyr Arg Asn Thr Met Ser Asn
20 25 30
Gly Gly Leu Gln Arg Ser Val Ile Leu Ser Ala Leu Ile Leu Leu Arg
35 40 45
Ala Val Thr Gly Phe Ser Gly Asp Gly Arg Ala Ile Trp Ser Lys Asn
50 55 60
Pro Asn Phe Thr Pro Val Asn Glu Ser Gln Leu Phe Leu Tyr Asp Thr
65 70 75 80
Phe Pro Lys Asn Phe Phe Trp Gly Ile Gly Thr Gly Ala Leu Gln Val
85 90 95
Glu Gly Ser Trp Lys Lys Asp Gly Lys Gly Pro Ser Ile Trp Asp His
100 105 110
Phe Ile His Thr His Leu Lys Asn Val Ser Ser Thr Asn Gly Ser Ser
115 120 125
Asp Ser Tyr Ile Phe Leu Glu Lys Asp Leu Ser Ala Leu Asp Phe Ile
130 135 140
Gly Val Ser Phe Tyr Gln Phe Ser Ile Ser Trp Pro Arg Leu Phe Pro
145 150 155 160
Asp Gly Ile Val Thr Val Ala Asn Ala Lys Gly Leu Gln Tyr Tyr Ser
165 170 175
Thr Leu Leu Asp Ala Leu Val Leu Arg Asn Ile Glu Pro Ile Val Thr
180 185 190
Leu Tyr His Trp Asp Leu Pro Leu Ala Leu Gln Glu Lys Tyr Gly Gly
195 200 205
Trp Lys Asn Asp Thr Ile Ile Asp Ile Phe Asn Asp Tyr Ala Thr Tyr
210 215 220
Cys Phe Gln Met Phe Gly Asp Arg Val Lys Tyr Trp Ile Thr Ile His
225 230 235 240
Asn Pro Tyr Leu Val Ala Trp His Gly Tyr Gly Thr Gly Met His Ala
245 250 255
Pro Gly Glu Lys Gly Asn Leu Ala Ala Val Tyr Thr Val Gly His Asn
260 265 270
Leu Ile Lys Ala His Ser Lys Val Trp His Asn Tyr Asn Thr His Phe
275 280 285
Arg Pro His Gln Lys Gly Trp Leu Ser Ile Thr Leu Gly Ser His Trp
290 295 300
Ile Glu Pro Asn Arg Ser Glu Asn Thr Met Asp Ile Phe Lys Cys Gln
305 310 315 320
Gln Ser Met Val Ser Val Leu Gly Trp Phe Ala Asn Pro Ile His Gly
325 330 335
Asp Gly Asp Tyr Pro Glu Gly Met Arg Lys Lys Leu Phe Ser Val Leu
340 345 350
Pro Ile Phe Ser Glu Ala Glu Lys His Glu Met Arg Gly Thr Ala Asp
355 360 365
Phe Phe Ala Phe Ser Phe Gly Pro Asn Asn Phe Lys Pro Leu Asn Thr
370 375 380
Met Ala Lys Met Gly Gln Asn Val Ser Leu Asn Leu Arg Glu Ala Leu
385 390 395 400
Asn Trp Ile Lys Leu Glu Tyr Asn Asn Pro Arg Ile Leu Ile Ala Glu
405 410 415
Asn Gly Trp Phe Thr Asp Ser Arg Val Lys Thr Glu Asp Thr Thr Ala
420 425 430
Ile Tyr Met Met Lys Asn Phe Leu Ser Gln Val Leu Gln Ala Ile Arg
435 440 445
Leu Asp Glu Ile Arg Val Phe Gly Tyr Thr Ala Trp Ser Leu Leu Asp
450 455 460
Gly Phe Glu Trp Gln Asp Ala Tyr Thr Ile Arg Arg Gly Leu Phe Tyr
465 470 475 480
Val Asp Phe Asn Ser Lys Gln Lys Glu Arg Lys Pro Lys Ser Ser Ala
485 490 495
His Tyr Tyr Lys Gln Ile Ile Arg Glu Asn Gly Phe Ser Leu Lys Glu
500 505 510
Ser Thr Pro Asp Val Gln Gly Gln Phe Pro Cys Asp Phe Ser Trp Gly
515 520 525
Val Thr Glu Ser Val Leu Lys Pro Glu Ser Val Ala Ser Ser Pro Gln
530 535 540
Phe Ser Asp Pro His Leu Tyr Val Trp Asn Ala Thr Gly Asn Arg Leu
545 550 555 560
Leu His Arg Val Glu Gly Val Arg Leu Lys Thr Arg Pro Ala Gln Cys
565 570 575
Thr Asp Phe Val Asn Ile Lys Lys Gln Leu Glu Met Leu Ala Arg Met
580 585 590
Lys Val Thr His Tyr Arg Phe Ala Leu Asp Trp Ala Ser Val Leu Pro
595 600 605
Thr Gly Asn Leu Ser Ala Val Asn Arg Gln Ala Leu Arg Tyr Tyr Arg
610 615 620
Cys Val Val Ser Glu Gly Leu Lys Leu Gly Ile Ser Ala Met Val Thr
625 630 635 640
Leu Tyr Tyr Pro Thr His Ala His Leu Gly Leu Pro Glu Pro Leu Leu
645 650 655
His Ala Asp Gly Trp Leu Asn Pro Ser Thr Ala Glu Ala Phe Gln Ala
660 665 670
Tyr Ala Gly Leu Cys Phe Gln Glu Leu Gly Asp Leu Val Lys Leu Trp
675 680 685
Ile Thr Ile Asn Glu Pro Asn Arg Leu Ser Asp Ile Tyr Asn Arg Ser
690 695 700
Gly Asn Asp Thr Tyr Gly Ala Ala His Asn Leu Leu Val Ala His Ala
705 710 715 720
Leu Ala Trp Arg Leu Tyr Asp Arg Gln Phe Arg Pro Ser Gln Arg Gly
725 730 735
Ala Val Ser Leu Ser Leu His Ala Asp Trp Ala Glu Pro Ala Asn Pro
740 745 750
Tyr Ala Asp Ser His Trp Arg Ala Ala Glu Arg Phe Leu Gln Phe Glu
755 760 765
Ile Ala Trp Phe Ala Glu Pro Leu Phe Lys Thr Gly Asp Tyr Pro Ala
770 775 780
Ala Met Arg Glu Tyr Ile Ala Ser Lys His Arg Arg Gly Leu Ser Ser
785 790 795 800
Ser Ala Leu Pro Arg Leu Thr Glu Ala Glu Arg Arg Leu Leu Lys Gly
805 810 815
Thr Val Asp Phe Cys Ala Leu Asn His Phe Thr Thr Arg Phe Val Met
820 825 830
His Glu Gln Leu Ala Gly Ser Arg Tyr Asp Ser Asp Arg Asp Ile Gln
835 840 845
Phe Leu Gln Asp Ile Thr Arg Leu Ser Ser Pro Thr Arg Leu Ala Val
850 855 860
Ile Pro Trp Gly Val Arg Lys Leu Leu Arg Trp Val Arg Arg Asn Tyr
865 870 875 880
Gly Asp Met Asp Ile Tyr Ile Thr Ala Ser Gly Ile Asp Asp Gln Ala
885 890 895
Leu Glu Asp Asp Arg Leu Arg Lys Tyr Tyr Leu Gly Lys Tyr Leu Gln
900 905 910
Glu Val Leu Lys Ala Tyr Leu Ile Asp Lys Val Arg Ile Lys Gly Tyr
915 920 925
Tyr Ala Phe Lys Leu Ala Glu Glu Lys Ser Lys Pro Arg Phe Gly Phe
930 935 940
Phe Thr Ser Asp Phe Lys Ala Lys Ser Ser Ile Gln Phe Tyr Asn Lys
945 950 955 960
Val Ile Ser Ser Arg Gly Phe Pro Phe Glu Asn Ser Ser Ser Arg Cys
965 970 975
Ser Gln Thr Gln Glu Asn Thr Glu Cys Thr Val Cys Leu Phe Leu Val
980 985 990
Gln Lys Lys Pro Leu Ile Phe Leu Gly Cys Cys Phe Phe Ser Thr Leu
995 1000 1005
Val Leu Leu Leu Ser Ile Ala Ile Phe Gln Arg Gln Lys Arg Arg
1010 1015 1020
Lys Phe Trp Lys Ala Lys Asn Leu Gln His Ile Pro Leu Lys Lys
1025 1030 1035
Gly Lys Arg Val Val Ser
1040
<210> 53
<211> 181
<212> БЕЛОК
<213> Homo sapiens
<400> 53
His Pro Ile Pro Asp Ser Ser Pro Leu Leu Gln Phe Gly Gly Gln Val
1 5 10 15
Arg Gln Arg Tyr Leu Tyr Thr Asp Asp Ala Gln Gln Thr Glu Ala His
20 25 30
Leu Glu Ile Arg Glu Asp Gly Thr Val Gly Gly Ala Ala Asp Gln Ser
35 40 45
Pro Glu Ser Leu Leu Gln Leu Lys Ala Leu Lys Pro Gly Val Ile Gln
50 55 60
Ile Leu Gly Val Lys Thr Ser Arg Phe Leu Cys Gln Arg Pro Asp Gly
65 70 75 80
Ala Leu Tyr Gly Ser Leu His Phe Asp Pro Glu Ala Cys Ser Phe Arg
85 90 95
Glu Leu Leu Leu Glu Asp Gly Tyr Asn Val Tyr Gln Ser Glu Ala His
100 105 110
Gly Leu Pro Leu His Leu Pro Gly Asn Lys Ser Pro His Arg Asp Pro
115 120 125
Ala Pro Arg Gly Pro Ala Arg Phe Leu Pro Leu Pro Gly Leu Pro Pro
130 135 140
Ala Leu Pro Glu Pro Pro Gly Ile Leu Ala Pro Gln Pro Pro Asp Val
145 150 155 160
Gly Ser Ser Asp Pro Leu Ser Met Val Gly Pro Ser Gln Gly Arg Ser
165 170 175
Pro Ser Tyr Ala Ser
180
<210> 54
<211> 321
<212> ДНК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полинуклеотид"
<400> 54
gacatccaga tgacccagag cccctccagc ctgtccgcct ccgtgggcga cagagtgacc 60
atcacctgtc aggcctccca ggacatctcc aactacctga actggtatca gcagaagccc 120
ggcaaggccc ctaagctgct gatctactac acctcccggc tgcagtccgg cgtgccctcc 180
agattctccg gctctggctc tggcgccgac tacaccttca ccatctccag cctgcagccc 240
gaggatatcg ctacctactt ctgtcagcaa ggcaacaccc tgccctacac cttcggccag 300
ggcaccaagc tggaaatcaa g 321
<210> 55
<211> 119
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 55
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile His Pro Gly Ser Gly Asn Thr Tyr Tyr Asn Glu Lys Phe
50 55 60
Gln Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ile Leu Leu Leu Arg Ser Tyr Gly Met Asp Asp Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 56
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 56
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile His Pro Gly Ser Gly Asn Thr Tyr Tyr Asn Glu Lys Phe
50 55 60
Gln Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ile Leu Leu Leu Arg Ser Tyr Gly Met Asp Asp Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 57
<211> 112
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 57
Asp Val Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Ile Val His Ser
20 25 30
Ser Gly Asn Thr Tyr Leu Glu Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Phe Gln Gly
85 90 95
Ser His Ile Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 58
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 58
Asp Val Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Ile Val His Ser
20 25 30
Ser Gly Asn Thr Tyr Leu Glu Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Phe Gln Gly
85 90 95
Ser His Ile Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 59
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 59
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Val Ser Gly Tyr Ser Ile Thr Ser Gly
20 25 30
Tyr Thr Trp His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
35 40 45
Leu Ser Tyr Ile His Tyr Ser Val Tyr Thr Asn Tyr Asn Pro Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Thr Ala Lys Asn Ser Phe Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Arg Thr Thr Ser Leu Glu Arg Tyr Phe Asp Val Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 60
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 60
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Gln Ala Ser Gln Asp Ile Ser Asn Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Tyr Thr Ser Arg Leu Gln Ser Gly Val Pro Ser Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Ala Asp Tyr Thr Phe Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Ile Ala Thr Tyr Phe Cys Gln Gln Gly Asn Thr Leu Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 61
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 61
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Ile Asn Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Arg Ile His Pro Gly Ser Gly Asn Thr Tyr Tyr Asn Glu Lys Phe
50 55 60
Gln Gly Arg Val Thr Leu Thr Ala Asp Lys Ser Thr Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ile Leu Leu Leu Arg Ser Tyr Gly Met Asp Asp Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe
115 120 125
Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu
130 135 140
Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp
145 150 155 160
Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu
165 170 175
Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser
180 185 190
Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro
195 200 205
Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp Lys
210 215 220
Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro
225 230 235 240
Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser
245 250 255
Arg Thr Pro Glu Val Thr Cys Val Val Val Ala Val Ser His Glu Asp
260 265 270
Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn
275 280 285
Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val
290 295 300
Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu
305 310 315 320
Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Ala Ala Pro Ile Glu Lys
325 330 335
Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr
340 345 350
Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr
355 360 365
Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu
370 375 380
Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu
385 390 395 400
Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys
405 410 415
Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu
420 425 430
Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
Lys
<210> 62
<211> 219
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: синтетический
полипептид"
<400> 62
Asp Val Val Met Thr Gln Thr Pro Leu Ser Leu Ser Val Thr Pro Gly
1 5 10 15
Gln Pro Ala Ser Ile Ser Cys Lys Ser Ser Gln Ser Ile Val His Ser
20 25 30
Ser Gly Asn Thr Tyr Leu Glu Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Phe Gln Gly
85 90 95
Ser His Ile Pro Tyr Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 63
<211> 546
<212> ДНК
<213> Homo sapiens
<400> 63
caccccatcc ctgactccag tcctctcctg caattcgggg gccaagtccg gcagcggtac 60
ctctacacag atgatgccca gcagacagaa gcccacctgg agatcaggga ggatgggacg 120
gtggggggcg ctgctgacca gagccccgaa agtctcctgc agctgaaagc cttgaagccg 180
ggagttattc aaatcttggg agtcaagaca tccaggttcc tgtgccagcg gccagatggg 240
gccctgtatg gatcgctcca ctttgaccct gaggcctgca gcttccggga gctgcttctt 300
gaggacggat acaatgttta ccagtccgaa gcccacggcc tcccgctgca cctgccaggg 360
aacaagtccc cacaccggga ccctgcaccc cgaggaccag ctcgcttcct gccactacca 420
ggcctgcccc ccgcactccc ggagccaccc ggaatcctgg ccccccagcc ccccgatgtg 480
ggctcctcgg accctctgag catggtggga ccttcccagg gccgaagccc cagctacgct 540
tcctga 546
<210> 64
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности: Синтетическая
6xHis метка"
<400> 64
His His His His His His
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ ЛЕЧЕНИЯ РАССТРОЙСТВ, СВЯЗАННЫХ С FGF21 | 2016 |
|
RU2752530C2 |
| ВИДЫ КОМБИНИРОВАННОЙ ТЕРАПИИ РАКА, НАЦЕЛИВАЮЩИЕСЯ НА CD38 И TGF-БЕТА | 2019 |
|
RU2808632C2 |
| СЛИТЫЕ С FGF21 БЕЛКИ ДЛИТЕЛЬНОГО ДЕЙСТВИЯ И СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2016 |
|
RU2741087C2 |
| АНТИТЕЛО ПРОТИВ БЕТА-АМИЛОИДА, ЕГО АНТИГЕНСВЯЗЫВАЮЩИЙ ФРАГМЕНТ И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2777844C1 |
| КОМБИНАЦИИ АНТИТЕЛ К STAPHYLOCOCCUS AUREUS | 2019 |
|
RU2804815C2 |
| АНТИ-PD-1 АНТИТЕЛА | 2019 |
|
RU2788095C2 |
| АНТИТЕЛА, НАПРАВЛЕННЫЕ ПРОТИВ ЛЕЙКОТОКСИНОВ STAPHYLOCOCCUS AUREUS | 2019 |
|
RU2805969C2 |
| ТЕРАПЕВТИЧЕСКИЕ АНТИТЕЛА ПРОТИВ ЛИГАНДА CD40 | 2018 |
|
RU2770209C2 |
| АМАТОКСИНОВЫЕ КОНЪЮГАТЫ АНТИТЕЛА С ЛЕКАРСТВЕННЫМ СРЕДСТВОМ И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2826004C2 |
| АНТИТЕЛА, СВЯЗЫВАЮЩИЕСЯ С GPRC5D | 2020 |
|
RU2841523C2 |
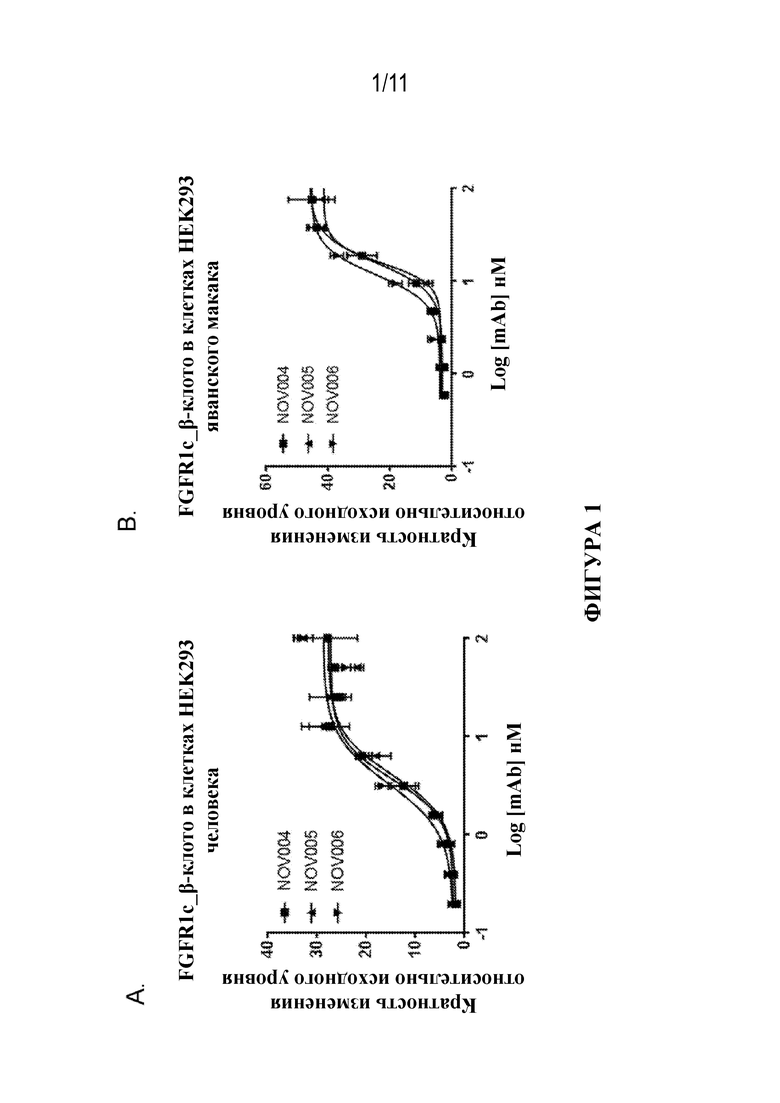
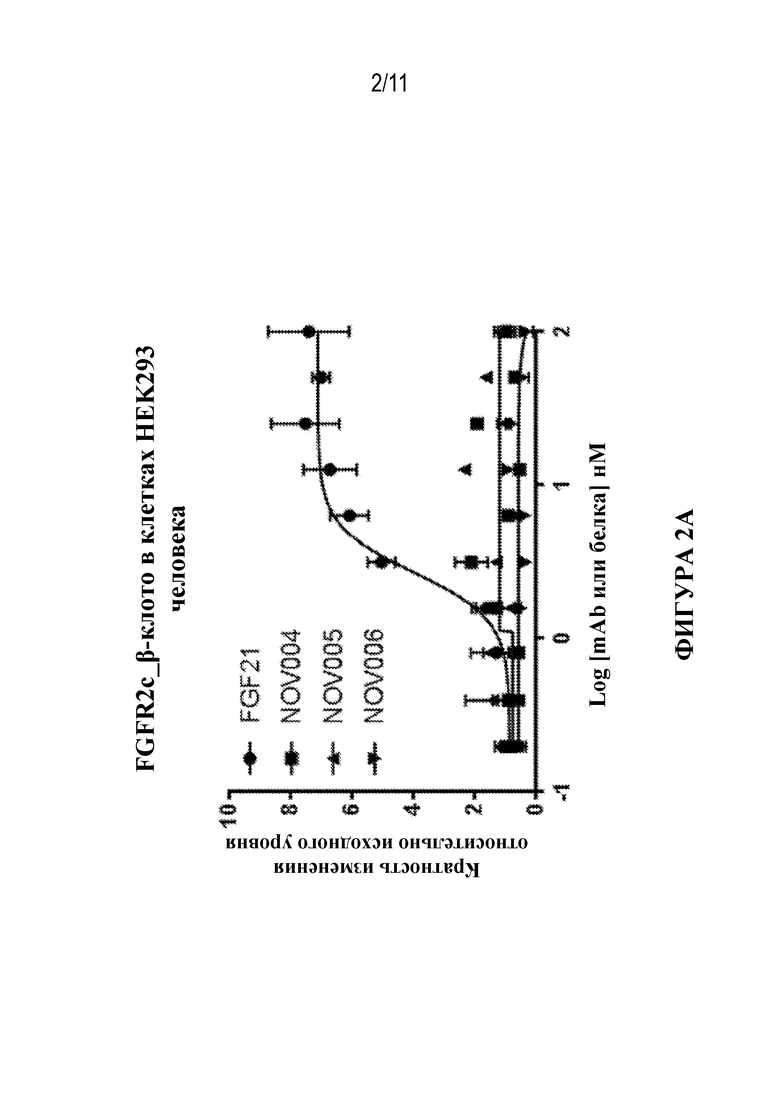
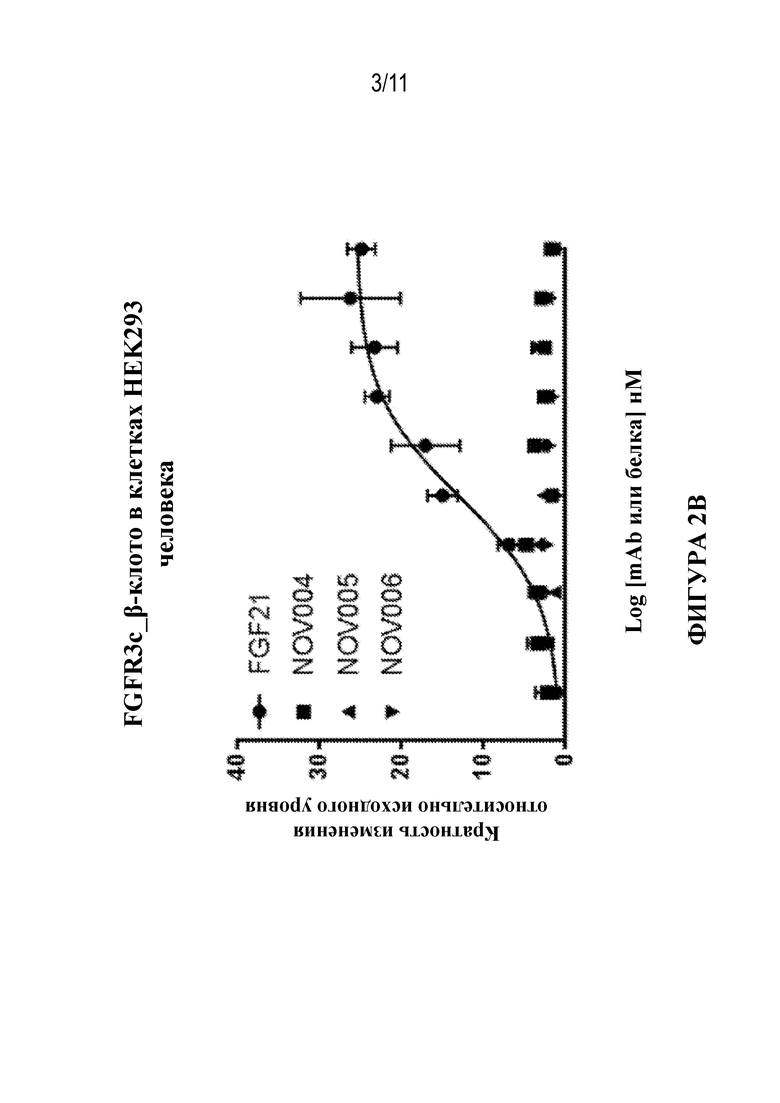
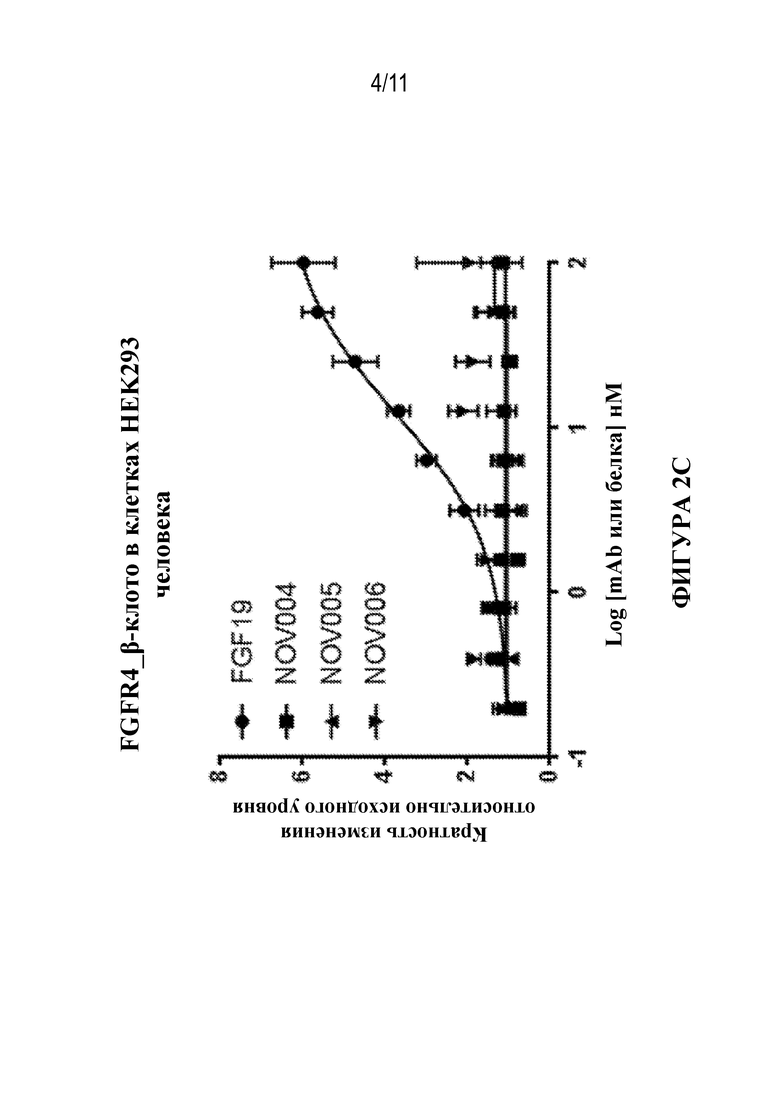

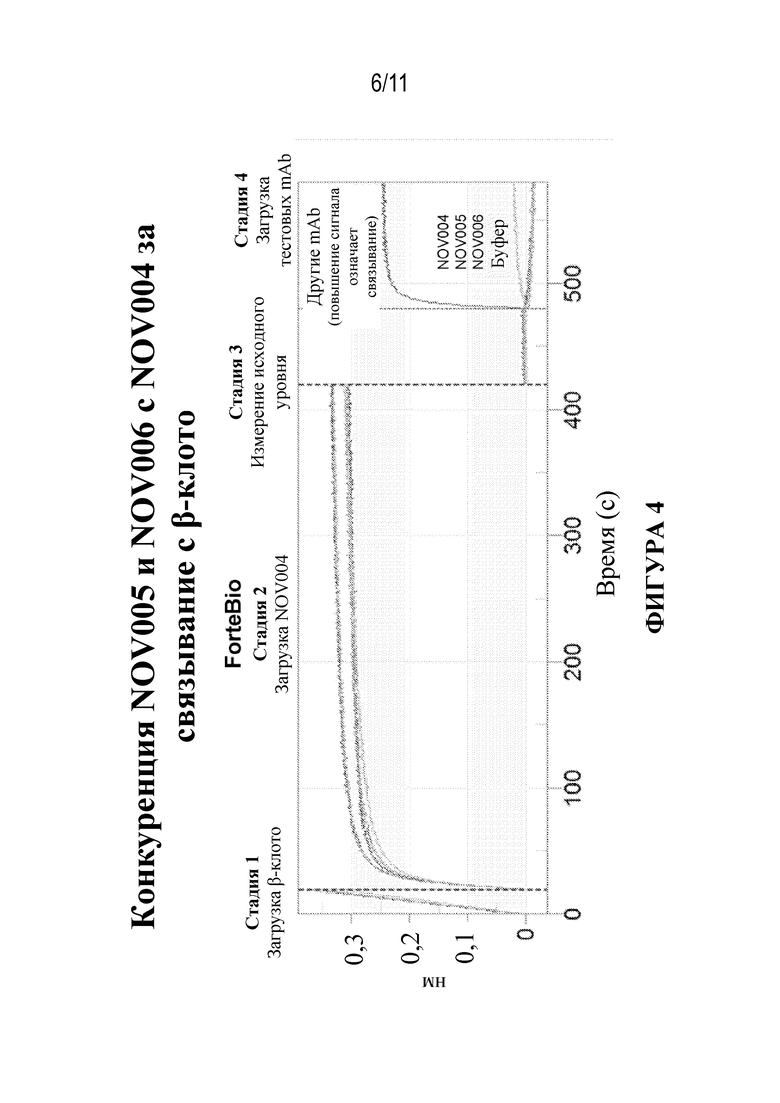
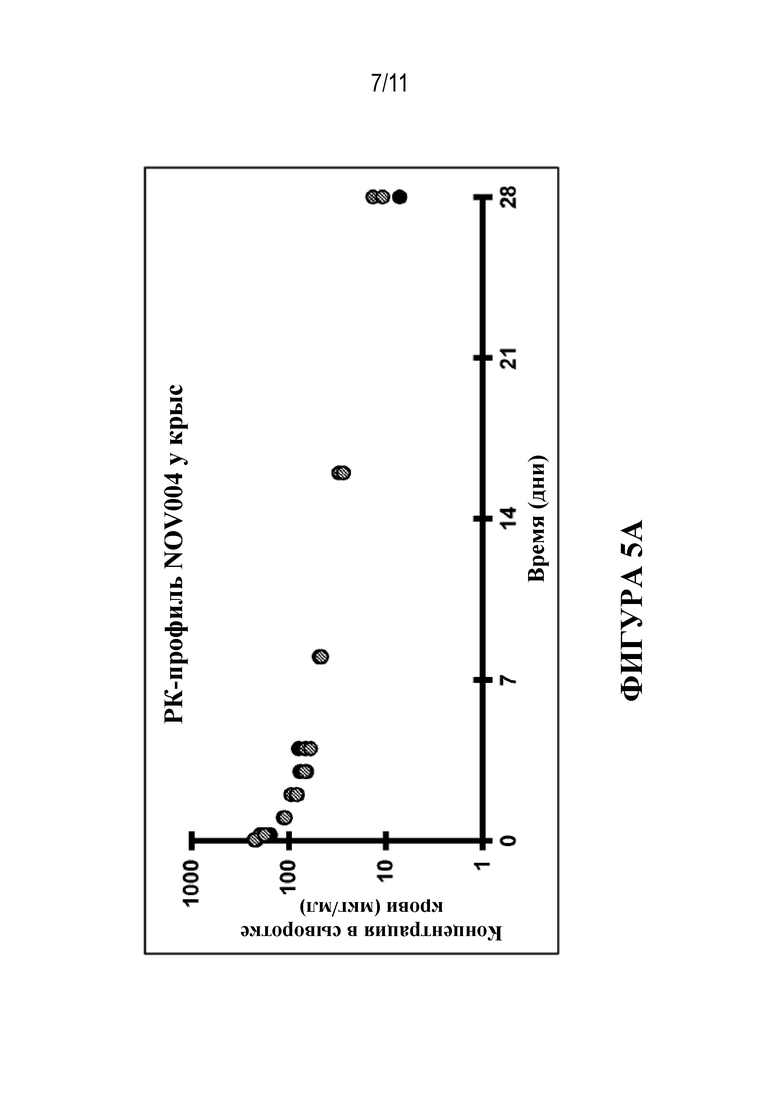
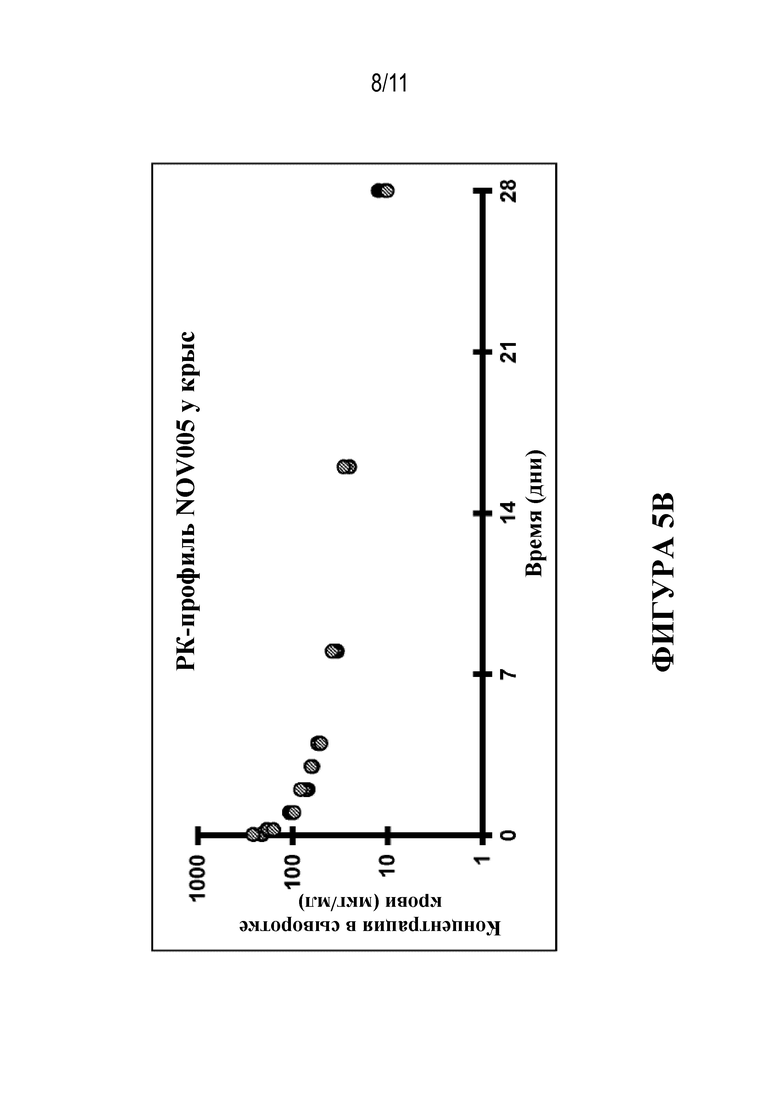
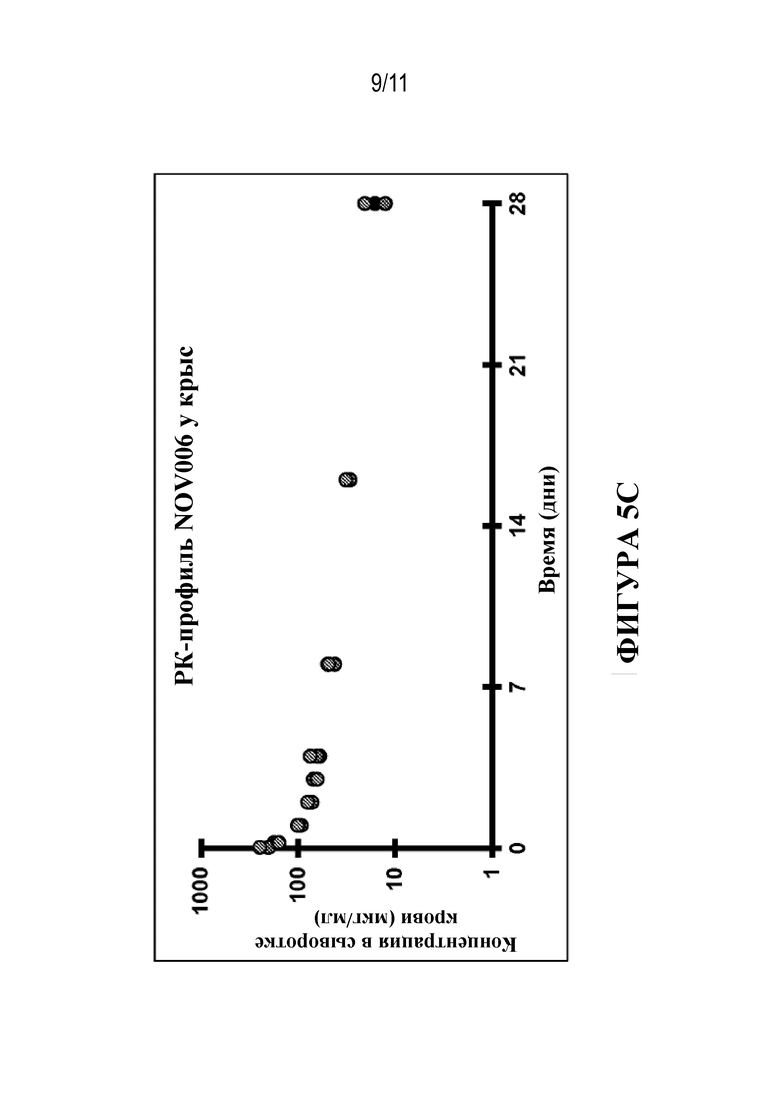

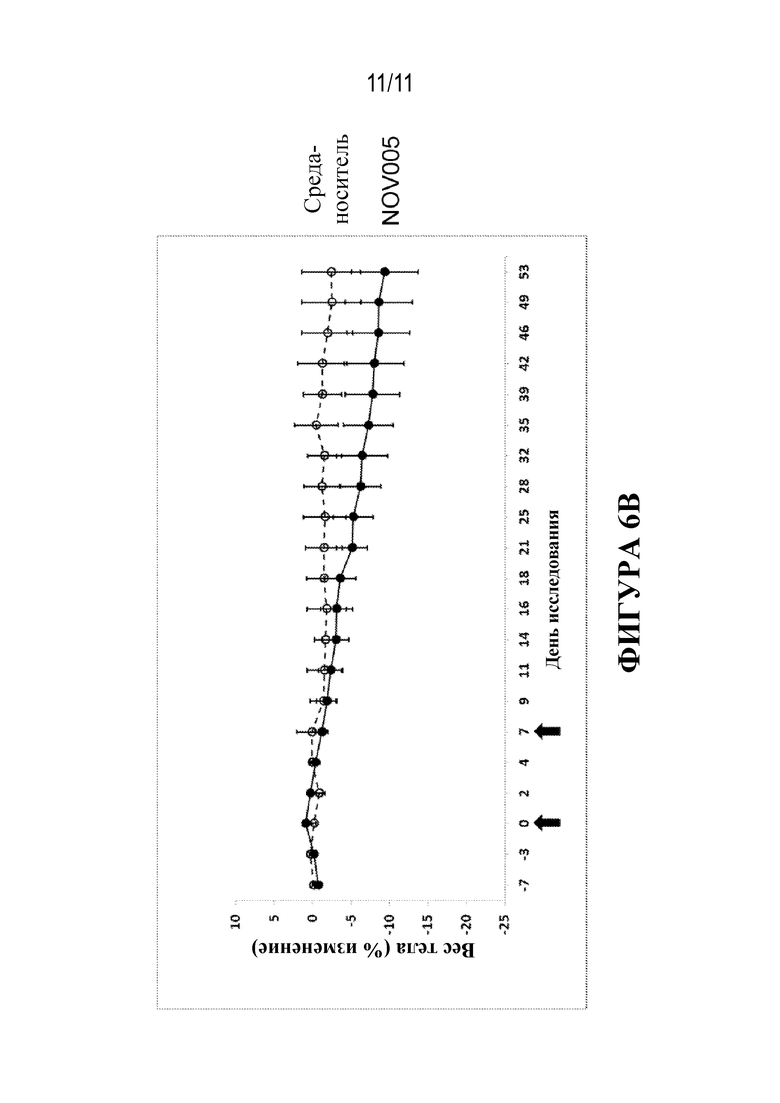
Изобретение относится к области биотехнологии. Предложено моноклональное антитело или его антигенсвязывающий фрагмент, которые связываются с β-клото человека. Также предложены кодирующие указанное антитело нуклеиновые кислоты, вектор экспрессии и клетка-хозяин, которые используются в способе получения антитела. Кроме того, представлены фармацевтические композиции и способы снижения веса тела, уменьшения аппетита или потребления пищи, уменьшения концентраций TG в плазме крови или концентраций TC в плазме крови у индивида, лечения метаболического FGF21-ассоциированного нарушения, атеросклероза, периферической артериальной болезни, инсульта, сердечной недостаточности или ишемической болезни сердца. Изобретение обеспечивает активацию рецепторного комплекса фактора роста фибробластов 21 человека (FGF21) и опосредованную FGF21 передачу сигнала с помощью антител-миметиков FGF21, обладающих улучшенными характеристиками стабильности. 18 н. и 11 з.п. ф-лы, 11 ил., 4 табл., 6 пр.
1. Выделенное антитело, или его антигенсвязывающий фрагмент, которое связывается с β-клото, где антитело, или его антигенсвязывающий фрагмент, содержит:
(i) HCDR1, содержащую аминокислотную последовательность SEQ ID NO: 6, HCDR2, содержащую аминокислотную последовательность SEQ ID NO: 7, HCDR3, содержащую аминокислотную последовательность SEQ ID NO: 8, LCDR1, содержащую аминокислотную последовательность SEQ ID NO: 19, LCDR2, содержащую аминокислотную последовательность SEQ ID NO: 20, и LCDR3, содержащую аминокислотную последовательность SEQ ID NO: 21;
(ii) HCDR1, содержащую аминокислотную последовательность SEQ ID NO: 9, HCDR2, содержащую аминокислотную последовательность SEQ ID NO: 7, HCDR3, содержащую аминокислотную последовательность SEQ ID NO: 8, LCDR1, содержащую аминокислотную последовательность SEQ ID NO: 19, LCDR2, содержащую аминокислотную последовательность SEQ ID NO: 20, и LCDR3, содержащую аминокислотную последовательность под SEQ ID NO: 21;
(iii) HCDR1, содержащую аминокислотную последовательность SEQ ID NO: 10, HCDR2, содержащую аминокислотную последовательность SEQ ID NO: 11, HCDR3, содержащую аминокислотную последовательность SEQ ID NO: 8, LCDR1, содержащую аминокислотную последовательность SEQ ID NO: 22, LCDR2, содержащую аминокислотную последовательность SEQ ID NO: 23, и LCDR3, содержащую аминокислотную последовательность SEQ ID NO: 24;
(iv) HCDR1, содержащую аминокислотную последовательность SEQ ID NO: 12, HCDR2, содержащую аминокислотную последовательность SEQ ID NO: 13, HCDR3, содержащую аминокислотную последовательность SEQ ID NO: 14, LCDR1, содержащую аминокислотную последовательность SEQ ID NO: 25, LCDR2, содержащую аминокислотную последовательность SEQ ID NO: 23, и LCDR3, содержащую аминокислотную последовательность SEQ ID NO: 21;
(v) HCDR1, содержащую аминокислотную последовательность SEQ ID NO: 6, HCDR2, содержащую аминокислотную последовательность SEQ ID NO: 7, HCDR3, содержащую аминокислотную последовательность SEQ ID NO: 8, LCDR1, содержащую аминокислотную последовательность SEQ ID NO: 31, LCDR2, содержащую аминокислотную последовательность SEQ ID NO: 20, и LCDR3, содержащую аминокислотную последовательность SEQ ID NO: 21;
(vi) HCDR1, содержащую аминокислотную последовательность SEQ ID NO: 9, HCDR2, содержащую аминокислотную последовательность SEQ ID NO: 7, HCDR3, содержащую аминокислотную последовательность SEQ ID NO: 8, LCDR1, содержащую аминокислотную последовательность SEQ ID NO: 31, LCDR2, содержащую аминокислотную последовательность SEQ ID NO: 20, и LCDR3, содержащую аминокислотную последовательность SEQ ID NO: 21.
2. Выделенное антитело, или его антигенсвязывающий фрагмент, по п.1, где антитело, или его антигенсвязывающий фрагмент, содержит
(i) вариабельную область тяжелой цепи (VH), содержащую аминокислотную последовательность SEQ ID NO: 15 или аминокислотную последовательность, которая по меньшей мере на 90 или 95% идентична ей; и
(ii) вариабельную область легкой цепи (VL), содержащую аминокислотную последовательность SEQ ID NO: 26 или 32 или аминокислотную последовательность, которая по меньшей мере на 90 или 95% идентична ей.
3. Выделенное антитело, или его антигенсвязывающий фрагмент, по п.1 или 2, где антитело, или его антигенсвязывающий фрагмент, содержит VH, содержащую аминокислотную последовательность SEQ ID NO: 15.
4. Выделенное антитело, или его антигенсвязывающий фрагмент, по любому из пп.1-3, где антитело, или его антигенсвязывающий фрагмент, содержит VL, содержащую аминокислотную последовательность SEQ ID NO: 26 или 32.
5. Выделенное антитело, или его антигенсвязывающий фрагмент, по п.3, где антитело или его антигенсвязывающий фрагмент, содержит
(i) VH, содержащую аминокислотную последовательность SEQ ID NO: 15, и VL, содержащую аминокислотную последовательность SEQ ID NO: 26, или
(ii) VH, содержащую аминокислотную последовательность SEQ ID NO: 15, и VL, содержащую аминокислотную последовательность SEQ ID NO: 32.
6. Выделенное антитело, или его антигенсвязывающий фрагмент, по любому из пп.1-5, где антитело, или его антигенсвязывающий фрагмент, содержит
(i) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 17, и легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 28, или
(ii) тяжелую цепь, содержащую аминокислотную последовательность SEQ ID NO: 17, и легкую цепь, содержащую аминокислотную последовательность SEQ ID NO: 34.
7. Выделенное антитело, или его антигенсвязывающий фрагмент, по любому из пп.1-6, где антитело или его антигенсвязывающий фрагмент, не содержит
(i) CDR по комбинированной системе нумерации или по Kabat антитела NOV004, как указано в таблице 2; и/или
(ii) вариабельную область тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 43 или 55, и вариабельную область легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 47 или 57.
8. Фармацевтическая композиция для лечения метаболического FGF21-ассоциированного нарушения, содержащая антитело, или его антигенсвязывающий фрагмент, по любому из пп.1-7 и фармацевтически приемлемый носитель.
9. Способ лечения метаболического FGF21-ассоциированного нарушения, включающий введение индивиду, страдающему метаболическим FGF21-ассоциированным нарушением, эффективного количества фармацевтической композиции, содержащей антитело, или его антигенсвязывающий фрагмент, по любому из пп.1-7.
10. Способ по п.9, где индивид страдает одним или несколькими из следующего: ожирение, сахарный диабет 1 типа и 2 типа, панкреатит, дислипидемия, неалкогольный стеатогепатит (NASH), инсулинорезистентность, гиперинсулинемия, нарушение толерантности к глюкозе, гипергликемия и метаболический синдром.
11. Способ по п.9, где индивид страдает одним или несколькими из следующего: ожирение, диабет, гипертриглицеридемия и дислипидемия.
12. Способ лечения сердечно-сосудистого нарушения, где сердечно-сосудистое нарушение представляет собой одно или несколько из следующего: атеросклероз, периферическая артериальная болезнь, инсульт, сердечная недостаточность и ишемическая болезнь сердца, где способ включает введение индивиду, страдающему указанным сердечно-сосудистым нарушением, эффективного количества фармацевтической композиции, содержащей антитело, или его антигенсвязывающий фрагмент, по любому из пп.1-7.
13. Применение антитела, или его антигенсвязывающего фрагмента, по любому из пп.1-7 в качестве лекарственного препарата для лечения метаболического FGF21-ассоциированного нарушения или сердечно-сосудистого нарушения, где сердечно-сосудистое нарушение представляет собой одно или несколько из следующего: атеросклероз, периферическая артериальная болезнь, инсульт, сердечная недостаточность и ишемическая болезнь сердца.
14. Способ снижения веса тела, включающий введение индивиду эффективного количества фармацевтической композиции, содержащей антитело, или его антигенсвязывающий фрагмент, по любому из пп.1-7.
15. Способ уменьшения аппетита или потребления пищи, включающий введение индивиду эффективного количества фармацевтической композиции, содержащей антитело, или его антигенсвязывающий фрагмент, по любому из пп.1-7.
16. Способ уменьшения концентраций триглицеридов (TG) в плазме крови или концентраций общего холестерина (ТС) в плазме крови у индивида, включающий введение индивиду эффективного количества фармацевтической композиции, содержащей антитело, или его антигенсвязывающий фрагмент, по любому из пп.1-7.
17. Способ по п.14, 15 или 16, где индивид страдает метаболическим нарушением.
18. Способ по п.17, где индивид страдает одним или несколькими из: ожирения, сахарного диабета 1 типа и 2 типа, панкреатита, дислипидемии, неалкогольного стеатогепатита (NASH), инсулинорезистентности, гиперинсулинемии, нарушения толерантности к глюкозе, гипергликемии и метаболического синдрома.
19. Нуклеиновая кислота, кодирующая одно или несколько антител по любому из пп.1-7.
20. Нуклеиновая кислота, кодирующая область CDR антитела, или его антигенсвязывающего фрагмента, которое специфически связывается с белком β-клото, где нуклеиновая кислота содержит последовательность, выбранную из SEQ ID NO: 16, 36 или 38, и последовательность, выбранную из SEQ ID NO: 54, 27, 33 или 40.
21. Нуклеиновая кислота, кодирующая область CDR антитела, или его антигенсвязывающего фрагмента, которое специфически связывается с белком β-клото, где нуклеиновая кислота содержит последовательность, выбранную из SEQ ID NO: 18, 37, 30 или 39, и последовательность, выбранную из SEQ ID NO: 29, 51, 35 или 41.
22. Вектор экспрессии, содержащий нуклеиновую кислоту по п.19, 20 или 21.
23. Клетка-хозяин для получения антитела, или его антигенсвязывающего фрагмента, которое специфически связывается с белком β-клото, содержащая вектор экспрессии по п.22.
24. Фармацевтическая композиция для лечения метаболического FGF21-ассоциированного нарушения, содержащая эффективное количество антитела, или его антигенсвязывающего фрагмента, по любому из пп.1-7.
25. Способ получения антитела, или его антигенсвязывающего фрагмента, которое связывается с β-клото, включающий стадию культивирования клетки-хозяина по п.23 в условиях, подходящих для экспрессии антитела, или его антигенсвязывающего фрагмента.
26. Фармацевтическая композиция по п.24, где метаболическое нарушение представляет собой ожирение, диабет, гипертриглицеридемию и дислипидемию.
27. Фармацевтическая композиция для лечения сердечно-сосудистого нарушения, содержащая эффективное количество антитела, или его антигенсвязывающего фрагмента, по любому из пп.1-7, где сердечно-сосудистое нарушение представляет собой одно или несколько из: атеросклероза, периферической артериальной болезни, инсульта, сердечной недостаточности и ишемической болезни сердца.
28. Фармацевтическая композиция для применения в способе снижения веса тела, в способе уменьшения аппетита или потребления пищи, в способе уменьшения концентраций триглицеридов (TG) в плазме крови или концентраций общего холестерина (TC) в плазме крови у индивида,
где композиция содержит эффективное количество антитела, или его антигенсвязывающего фрагмента, по любому из пп.1-7.
29. Применение антитела, или его антигенсвязывающего фрагмента, по любому из пп.1-7 для получения лекарственного препарата для лечения метаболического FGF21-ассоциированного нарушения, для лечения сердечно-сосудистого нарушения, где сердечно-сосудистое нарушение представляет собой одно или несколько из: атеросклероза, периферической артериальной болезни, инсульта, сердечной недостаточности и ишемической болезни сердца, для снижения веса тела, для уменьшения аппетита или потребления пищи, для уменьшения концентраций TG в плазме крови или концентраций TC в плазме крови у индивида.
| WO 2015148708 A1, 01.10.2015 | |||
| US 9284378 B2, 15.03.2016 | |||
| REITMAN M.L., FGF21 Mimetic Shows Therapeutic Promise, CELL METABOLISM, 2013, vol | |||
| Способ использования делительного аппарата ровничных (чесальных) машин, предназначенных для мериносовой шерсти, с целью переработки на них грубых шерстей | 1921 |
|
SU18A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| МАКСИМОВ М.Л | |||
| и др., Современные лекарственные средства для фармакотерапии ожирения и метаболического синдрома (Обзор), Сеченовский вестник, 2016, Номер 4(26), с.64-75. | |||
Авторы
Даты
2022-06-20—Публикация
2018-02-06—Подача