ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящая заявка испрашивает приоритет по предварительной заявке на патент США №62/696198, поданной 10 июля 2018 года. Раскрытие данной заявки включено в данный документ посредством ссылки во всей своей полноте.
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
[0002] Настоящая заявка содержит перечень последовательностей, который был подан в электронном виде в формате с кодировкой ASCII и настоящим включен посредством ссылки во всей своей полноте. Копия перечня последовательностей в электронном виде, созданная 9 марта 2019 года, имеет название 022548_WO025_SL.txt, а ее размер составляет 52428 байт.
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
[0003] Трансформирующий фактор роста бета (TGF-β) представляет собой цитокин, который регулирует различные биологические процессы, такие как образование внеклеточного матрикса, заживление ран, эмбриональное развитие, развитие кости, гемопоэз, иммунные и воспалительные ответы и злокачественная трансформация. Дерегуляция TGF-β приводит к патологическим состояниям, например, врожденным аномалиям развития, раку, хроническому воспалению и аутоиммунным и фиброзным заболеваниям.
[0004] TGF-β имеет три известных изоформы - TGF-β1, 2 и 3. Эти три изоформы являются плейотропными по своей функции и характеризуются различными профилями экспрессии в разных типах клеток и тканей. Они характеризуются аналогичной активностью in vitro, но нокауты индивидуальных молекул в специфических типах клеток позволяют предположить неидентичную роль in vivo, несмотря на их общую способность связываться с одним и тем же рецептором (Akhurst et al., Nat Rev Drug Discov 11(10):790-811 (2012)).
[0005] После связывания TGF-β с TGFβRII конститутивная киназная активность рецептора обеспечивает фосфорилирование и активацию TGFβRI, который фосфорилирует SMAD2/3, что обеспечивает возможность его ассоциации с SMAD4, которая приводит к дальнейшей локализации в ядре и транскрипции генов, отвечающих на TGF-β. Там же. В дополнение к этому каноническому сигнальному каскаду, по неканоническому сигнальному пути сигналы передаются через другие факторы, в том числе MAPK p38, PI3K, AKT, JUN, JNK и NF-κB. Передача сигнала от TGF-β также модулируется другими сигнальными путями, в том числе WNT, Hedgehog, Notch, INF, TNF и RAS. Таким образом, конечным результатом передачи сигнала от TGF-β является перекрестное взаимодействие всех этих сигнальных путей, которые интегрируют состояние клетки и ее окружение. Там же.
[0006] CD38 представляет собой трансмембранный гликопротеин типа II массой 45 кДа с длинным С-концевым внеклеточным доменом и коротким N-концевым цитоплазматическим доменом. Белок CD38 представляет собой бифункциональный, выделяемый во внешнюю среду фермент, который катализирует превращение NAD+ в циклическую ADP-рибозу (cADPR), а также гидролизует cADPR до ADP-рибозы. В процессе онтогенеза CD38 появляется на CD34-положительных коммитированных стволовых клетках и коммитированных по линиям дифференцировки предшественниках лимфоидных, эритроидных и миелоидных клеток. Экспрессия CD38 сохраняется в основном в лимфоидной линии с различными уровнями экспрессии на разных стадиях развития Т- и В-клеток.
[0007] Уровень экспрессии CD38 повышен при многих гемопоэтических злокачественных новообразованиях и у клеточных линий, происходящих из различных гемопоэтических злокачественных новообразований, включая неходжкинскую лимфому (NHL), лимфому Беркитта (BL), множественную миелому (MM), хронический B-лимфоцитарный лейкоз (B-CLL), острый B- и T-лимфоцитарный лейкоз (ALL), Т-клеточную лимфому (TCL), острый миелоидный лейкоз (AML), злокачественный ретикулоэндотелиоз (HCL), лимфому Ходжкина (HL) и хронический миелоидный лейкоз (CML). С другой стороны, большинство примитивных плюрипотентных стволовых клеток гемопоэтической системы являются CD38-отрицательными. Экспрессия CD38 при гемопоэтических злокачественных новообразованиях и ее корреляция с прогрессированием заболевания делают CD38 привлекательной мишенью для терапии посредством антител.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0008] В данном документе представлены виды комбинированной терапии, нацеливающиеся на CD38 и TGF-β. Авторы настоящего изобретения обнаружили, что антитело к TGF-β может блокировать способность TGF-β ослаблять противоопухолевый эффект антитела к CD38 (например, TGF-β может ингибировать опосредованную NK-клетками ADCC, вызываемую антителом к CD38). По сравнению с доступными в настоящее время видами лечения рака, в том числе видами лечения посредством антител, предлагаемые в данном документе виды комбинированной терапии могут обеспечивать более высокую клиническую эффективность.
[0009] Соответственно, в данном документе представлен способ повышения эффективности средства, которое специфически связывается с CD38, с помощью средства, которое специфически связывается с TGF-β. В некоторых вариантах осуществления в данном документе представлен способ лечения рака у пациента (например, пациента-человека) путем введения пациенту средства, которое специфически связывается с CD38 человека, и средства, которое специфически связывается с TGF-β человека. В некоторых вариантах осуществления средство, которое специфически связывается с CD38 человека, представляет собой антитело к CD38 или его антигенсвязывающий фрагмент. В некоторых вариантах осуществления антитело к CD38 способно осуществлять уничтожение CD38-положительной клетки посредством апоптоза, антителозависимой клеточно-опосредованной цитотоксичности (ADCC) и/или комплемент-зависимой цитотоксичности (CDC), при этом уничтожение CD38-положительной клетки посредством апоптоза может происходить в отсутствие клеток стромы или цитокинов, производимых стромой. В некоторых вариантах осуществления средство, которое специфически связывается с TGF-β человека, представляет собой панспецифическое антитело к TGF-β или его антигенсвязывающий фрагмент.
[0010] В некоторых вариантах осуществления в данном документе представлен способ лечения рака у больного человека, заключающийся во введении пациенту антитела к CD38 и антитела к TGF-β или его антигенсвязывающего фрагмента.
[0011] В некоторых вариантах осуществления антитело к CD38:
a) содержит HCDR1-3 и LCDR1-3, содержащие аминокислотные последовательности под SEQ ID NO: 15-20 соответственно;
b) содержит вариабельный домен тяжелой цепи и вариабельный домен легкой цепи, содержащие аминокислотные последовательности под SEQ ID NO: 13 и 14 соответственно; или
c) содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 11, и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 12.
[0012] В некоторых вариантах осуществления антитело к TGF-β:
a) содержит HCDR1-3 и LCDR1-3, содержащие аминокислотные последовательности под SEQ ID NO: 5-10 соответственно;
b) содержит вариабельный домен тяжелой цепи и вариабельный домен легкой цепи, содержащие аминокислотные последовательности под SEQ ID NO: 3 и 4 соответственно, или
c) содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 1, и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 2.
[0013] В некоторых вариантах осуществления антитело к CD38 содержит CDR1 тяжелой цепи (HCDR1), HCDR2, HCDR3, CDR1 легкой цепи (LCDR1), LCDR2 и LCDR3, содержащие аминокислотные последовательности под SEQ ID NO: 15-20 соответственно, а антитело к TGF-β или его антигенсвязывающий фрагмент содержит HCDR1, HCDR2, HCDR3, LCDR1, LCDR2 и LCDR3, содержащие аминокислотные последовательности под SEQ ID NO: 5-10 соответственно. В определенных вариантах осуществления антитело к CD38 содержит вариабельный домен тяжелой цепи (VH) и вариабельный домен легкой цепи (VL), содержащие аминокислотные последовательности под SEQ ID NO: 13 и 14 соответственно; а антитело к TGF-β содержит VH и VL, содержащие аминокислотные последовательности под SEQ ID NO: 3 и 4 соответственно. В конкретных вариантах осуществления антитело к CD38 содержит тяжелую цепь (HC) и легкую цепь (LC), содержащие аминокислотные последовательности под SEQ ID NO: 11 и 12 соответственно; а антитело к TGF-β содержит тяжелую цепь и легкую цепь, содержащие аминокислотные последовательности под SEQ ID NO: 1 и 2 соответственно.
[0014] В любом из вариантов осуществления, представленных в данном документе, антитело к CD38 может содержать Fc-область IgG1 человека, а антитело к TGF-β может содержать Fc-область IgG4 человека.
[0015] В данном документе также представлен способ лечения множественной миеломы у больного человека, предусматривающий введение пациенту антитела к CD38, которое содержит аминокислотную последовательность вариабельного домена тяжелой цепи под SEQ ID NO: 13 и аминокислотную последовательность вариабельного домена легкой цепи под SEQ ID NO: 14, и антитела к TGF-β, которое содержит аминокислотную последовательность вариабельного домена тяжелой цепи под SEQ ID NO: 3 и аминокислотную последовательность вариабельного домена легкой цепи под SEQ ID NO: 4.
[0016] В данном документе также представлен способ лечения множественной миеломы у больного человека, предусматривающий введение пациенту антитела к CD38, которое содержит аминокислотную последовательность тяжелой цепи под SEQ ID NO: 11 и аминокислотную последовательность легкой цепи под SEQ ID NO: 12, и антитела к TGF-β, которое содержит аминокислотную последовательность тяжелой цепи под SEQ ID NO: 1 и аминокислотную последовательность легкой цепи под SEQ ID NO: 2.
[0017] В любом из вариантов осуществления, представленных в данном документе, антитело к CD38 и антитело к TGF-β или его фрагмент можно вводить пациенту последовательно.
[0018] В данном документе также представлено антитело к CD38 для применения в лечении рака у больного человека, в комбинации с антителом к TGF-β, а также применение антитела к CD38 для изготовления лекарственного препарата для лечения рака у больного человека, в комбинации с антителом к TGF-β. В некоторых вариантах осуществления антитело к CD38:
a) содержит HCDR1-3 и LCDR1-3, содержащие аминокислотные последовательности под SEQ ID NO: 15-20 соответственно;
b) содержит вариабельный домен тяжелой цепи и вариабельный домен легкой цепи, содержащие аминокислотные последовательности под SEQ ID NO: 13 и 14 соответственно; или
c) содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 11, и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 12.
[0019] В данном документе также представлено антитело к TGF-β для применения в лечении рака у больного человека, в комбинации с антителом к CD38, а также применение антитела к TGF-β для изготовления лекарственного препарата для лечения рака у больного человека, в комбинации с антителом к CD38. В некоторых вариантах осуществления антитело к TGF-β:
a) содержит HCDR1-3 и LCDR1-3, содержащие аминокислотные последовательности под SEQ ID NO: 5-10 соответственно;
b) содержит вариабельный домен тяжелой цепи и вариабельный домен легкой цепи, содержащие аминокислотные последовательности под SEQ ID NO: 3 и 4 соответственно; или
c) содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 1, и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 2.
[0020] В некоторых вариантах осуществления способов, антител для применения и путей применения антител, описанных в данном документе, рак является CD38-положительным.
[0021] В некоторых вариантах осуществления способов, антител для применения и путей применения антител, описанных в данном документе, рак выбран из группы, состоящей из множественной миеломы, неходжкинской лимфомы, лимфомы Ходжкина, диффузной крупноклеточной B-клеточной лимфомы, периферической Т-клеточной лимфомы, злокачественного ретикулоэндотелиоза, хронического лимфоцитарного лейкоза, хронического миелоидного лейкоза, острого миелоидного лейкоза, острого лимфоцитарного лейкоза, меланомы, глиобластомы, рака легкого, плоскоклеточного рака кожи, колоректального рака, рака молочной железы, рака яичника, рака головы и шеи, гепатоцеллюлярной карциномы, уротелиального рака и почечно-клеточной карциномы.
[0022] В некоторых вариантах осуществления способов, антител для применения и путей применения антител, описанных в данном документе, рак представляет собой гематологическое злокачественное новообразование.
[0023] В некоторых вариантах осуществления способов, антител для применения и путей применения антител, описанных в данном документе, рак представляет собой множественную миелому. В конкретных вариантах осуществления описанные в данном документе способы лечения приводят к меньшему разрушению кости, чем лечение посредством антитела к CD38 отдельно, и/или усиливают образование кости с обеспечением ремоделирования кости и/или заживления кости у пациентов с множественной миеломой.
[0024] Соответственно, в некоторых вариантах осуществления в данном документе представлен способ уменьшения разрушения кости у пациента-человека с множественной миеломой, предусматривающий введение пациенту средства, которое специфически связывается с CD38 человека, описанного в данном документе (например, антитела к CD38), и средства, которое специфически связывается с TGF-β человека, описанного в данном документе (например, антитела к TGF-β). Также в данном документе представлено антитело к TGF-β, описанное в данном документе, для применения в уменьшении разрушения кости у пациента с множественной миеломой человека в комбинации с антителом к CD38, и применение антитела к TGF-β для изготовления лекарственного препарата для уменьшения разрушения кости у пациента-человека с множественной миеломой в комбинации с антителом к CD38.
[0025] В данном документе также представлен способ усиления образования кости, приводящего к ремоделированию кости и/или заживлению кости у пациента с множественной миеломой, предусматривающий введение пациенту средства, которое специфически связывается с CD38 человека, описанного в данном документе (например, антитела к CD38), и средства, которое специфически связывается с TGF-β человека, описанного в данном документе (например, антитела к TGF-β). В данном документе также представлено антитело к TGF-β, описанное в данном документе, для применения в усилении образования кости у пациента с множественной миеломой человека в комбинации с антителом к CD38, а также применение антитела к TGF-β для изготовления лекарственного препарата для усиления образования кости у пациента с множественной миеломой человека в комбинации с антителом к CD38.
[0026] В некоторых вариантах осуществления способов, антител для применения и путей применения антител, описанных в данном документе, рак является рефрактерным к лечению посредством Ab2 или лечению посредством даратумумаба или рефрактерным к обоим видам лечения. В некоторых вариантах осуществления у пациента имеется рецидивирующая или рефрактерная множественная миелома, и он получил по меньшей мере одну предшествующую терапию или по меньшей мере две предшествующих терапии.
[0027] В данном документе также представлено готовое изделие, содержащее антитело к CD38 и антитело к TGF-β, где указанное готовое изделие применимо для лечения рака у пациента, например, согласно способу лечения, описанному в данном документе. В некоторых вариантах осуществления антитело к CD38:
a) содержит HCDR1-3 и LCDR1-3, содержащие аминокислотные последовательности под SEQ ID NO: 15-20 соответственно;
b) содержит вариабельный домен тяжелой цепи и вариабельный домен легкой цепи, содержащие аминокислотные последовательности под SEQ ID NO: 13 и 14 соответственно; или
c) содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 11, и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 12; и
антитело к TGF-β
a) содержит HCDR1-3 и LCDR1-3, содержащие аминокислотные последовательности под SEQ ID NO: 5-10 соответственно;
b) содержит вариабельный домен тяжелой цепи и вариабельный домен легкой цепи, содержащие аминокислотные последовательности под SEQ ID NO: 3 и 4 соответственно; или
c) содержит тяжелую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 1, и легкую цепь, содержащую аминокислотную последовательность под SEQ ID NO: 2.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
[0028] Фиг. 1 представляет собой график, на котором показано высвобождение TGF-β из линий клеток множественной миеломы через один, два или три дня, как количественно определено с помощью ELISA.
[0029] Фиг. 2 представляет собой график, на котором показаны уровни флуоресценции кальцеина (% лизиса) в клетках-мишенях MOLP8, которые инкубировали с Ab2 в концентрации 0, 0,001, 0,1 или 1 мкг/мл и лизировали в течение 1 часа под действием NK-клеток человека, которые инкубировали с 10 нг/мл TGF-β на протяжении ночи, через 24 часа, 48 часов или 72 часа.
[0030] Фиг. 3 представляет собой график, на котором показаны уровни флуоресценции кальцеина (% лизиса) в клетках-мишенях MOLP8, которые инкубировали с Ab2 в концентрации 0, 0,001, 0,01, 0,1 или 1 мкг/мл или контрольным IgG1 и лизировали в течение 1 часа под действием NK-клеток человека, которые инкубировали с 10 нг/мл TGF-β и 50 мкг/мл Ab1 в течение 90 часов.
[0031] Фиг. 4 представляет собой график, на котором показан эффект 0,1, 1 и 10 нг/мл TGF-β на Ab2-опосредованную ADCC клеток NCI-H929.
[0032] Фиг. 5 представляет собой график, на котором показана Ab2-опосредованная ADCC клеток NCI-H929, обработанных 100 мкг/мл IgG4, 100 мкг/мл Ab1, 10 нг/мл TGF-β, TGF-β+IgG4 или TGF-β+Ab1. *=p<0,05 в сравнении с NT; **=p<0,005 в сравнении с NT.
[0033] Фиг. 6 представляет собой график, на котором показана Ab2-опосредованная ADCC клеток NCI-H929, обработанных 200 мкг/мл IgG4, 200 мкг/мл Ab1, 10 нг/мл TGF-β, TGF-β+IgG4 или TGF-β+Ab1. *=p<0,05 в сравнении с NT; **=p<0,005 в сравнении с NT.
[0034] Фиг. 7 представляет собой график, на котором показаны уровни флуоресценции кальцеина (% лизиса) в клетках-мишенях K562, которые лизировали под действием цитолитической активности NK-клеток человека, которые инкубировали с эндогенными TGF-β-высвобождающими клетками JJN3 и 100 мкг/мл Ab1 или изотипическим контролем в течение 90 часов.
[0035] Фиг. 8 представляет собой график, на котором показана Ab2-опосредованная ADCC клеток-мишеней RPMI8226, которые инкубировали с Ab2 в концентрации 0, 0,01 или 0,1 мкг/мл или с контрольным мутантным Ab2 в концентрации 0,1 мкг/мл и лизировали в течение 1 часа под действием NK-клеток человека, которые инкубировали с эндогенными TGF-β-высвобождающими клетками JJN3 и 100 мкг/мл Ab1 или изотипическим контролем в течение 90 часов.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0036] В настоящем описании представлены новые виды комбинированной терапии, нацеливающиеся на TGF-β человека и CD38 человека, например, с применением антител, которые связывают эти мишени. Виды комбинированной терапии можно применять для лечения таких состояний, как рак. Если не указано иное, в данном документе "TGF-β" относится к TGF-β человека. Полипептидные последовательности трех изоформ TGF-β человека (TGF-β1, TGF-β2 и TGF-β3) доступны под номерами доступа в SwissProt P01137, P08112 и P10600 соответственно, которые представлены в данном документе под SEQ ID NO: 21-23. Если не указано иное, в данном документе "CD38" относится к CD38 человека. Полипептидная последовательность CD38 человека доступна под номером доступа в Genbank NP_001766, которая представлена в данном документе под SEQ ID NO: 24.
[0037] Используемый в данном документе термин "антитело" (Ab) или "иммуноглобулин" (Ig) относится к тетрамерному белку, содержащему две тяжелые (Н) цепи (приблизительно 50-70 кДа) и две легкие (L) цепи (приблизительно 25 кДа), связанные между собой дисульфидными связями. Каждая тяжелая цепь состоит из вариабельного домена тяжелой цепи (VH) и константной области тяжелой цепи (CH). Каждая легкая цепь состоит из вариабельного домена легкой цепи (VL) и константной области легкой цепи (CL). Домены VH и VL могут быть дополнительно подразделены на области гипервариабельности, называемые "областями, определяющими комплементарность" (CDR), чередующиеся с более консервативными областями, называемыми "каркасными областями" (FR). Каждый из VH или VL состоит из трех CDR и четырех FR, расположенных от аминоконца к карбоксильному концу в следующем порядке: FR1, CDR1, FR2, CDR2, FR3, CDR3 и FR4. Отнесение аминокислот к каждой из областей можно осуществлять в соответствии с определениями IMGT® (Lefranc et al., Dev Comp Immunol 27(1):55-77 (2003)) или определениями по Kabat, Sequences of Proteins of Immunological Interest (National Institutes of Health, Bethesda, MD (1987 и 1991)); Chothia & Lesk, J. Mol. Biol. 196:901-917 (1987) или Chothia et al., Nature 342:878-883 (1989).
[0038] Термин "аффинность" относится к показателю притяжения между антигеном и антителом. Свойственная антителу сила притяжения к антигену, как правило, выражается как равновесная константа аффинности связывания (KD) конкретного взаимодействия антитело-антиген. Говорится, что антитело специфически связывается с антигеном, когда KD составляет менее 10-7 M, как, например, менее 10-8 M (например, 1-9 нМ), как определено с помощью, например, поверхностного плазмонного резонанса или интерферометрии биослоя.
[0039] Термин "koff" относится к константе скорости диссоциации конкретного взаимодействия антитело-антиген. Константу скорости диссоциации koff можно измерять, например, с помощью интерферометрии биослоя.
[0040] Используемый в данном документе термин "эпитоп" относится к части (детерминанте) антигена, которая специфически связывается с антителом. Эпитопные детерминанты обычно состоят из химически активных группировок на поверхности молекул, таких как аминокислоты или боковые цепи углеводородов или сахаров, и они обычно обладают специфическими характеристиками трехмерной структуры, а также специфическими характеристиками заряда. Эпитоп может быть "линейным" или "конформационным". В линейном эпитопе все точки взаимодействия между белком (например, антигеном) и взаимодействующей молекулой (такой как антитело) расположены линейно вдоль первичной аминокислотной последовательности белка. В конформационном эпитопе точки взаимодействия возникают у совокупности аминокислотных остатков белка, которые отделены друг от друга в первичной аминокислотной последовательности. После того как требуемый эпитоп на антигене определен, можно создавать антитела к данному эпитопу с применением методик, хорошо известных в данной области техники. Например, антитело к линейному эпитопу можно получать, например, посредством иммунизации животного с помощью пептида, содержащего аминокислотные остатки линейного эпитопа. Антитело к конформационному эпитопу может быть получено, например, путем иммунизации животного с помощью мини-домена, содержащего соответствующие аминокислотные остатки конформационного эпитопа. Антитело к конкретному эпитопу также может быть получено, например, путем иммунизации животного с помощью представляющей интерес молекулы-мишени или ее соответствующей части, а затем проведения скрининга в отношении связывания с эпитопом.
[0041] Можно определить, связывается ли антитело с тем же эпитопом, что и описанное в данном документе антитело, или конкурирует ли оно за связывание с ним с применением способов, известных в данной области техники, включая без ограничения анализы конкурентного связывания, сортировку по группам эпитопов и аланиновое сканирование. В некоторых вариантах осуществления тестируемое антитело и описанное в данном документе антитело связываются с по меньшей мере одним общим остатком (например, по меньшей мере двумя, тремя, четырьмя, пятью, шестью, семью, восемью, девятью или десятью остатками) на белке-мишени (т.е. TGF-β или CD38). В дополнительных вариантах осуществления контактные остатки на белке-мишени для тестируемого антитела и описанного в данном документе антитела полностью идентичны. В одном варианте осуществления можно обеспечить связывание описанного в данном документе антитела с белком-мишенью в условиях насыщения, а затем измерить способность тестируемого антитела связываться с белком-мишенью. Если тестируемое антитело способно связываться с белком-мишенью одновременно с эталонным антителом, тогда тестируемое антитело связывается с эпитопом, отличным от эпитопа для эталонного антитела. Однако, если тестируемое антитело не способно одновременно связываться с белком-мишенью, то тестируемое антитело связывается с тем же эпитопом, перекрывающимся эпитопом или эпитопом, который находится в непосредственной близости от эпитопа, связанного описанным в данном документе антителом. Данный эксперимент можно выполнять с применением, например, ELISA, RIA, BIACORE™, SPR, интерферометрии биослоя или проточной цитометрии. Для тестирования того, присутствует ли перекрестная конкуренция антитела с другим антителом, можно использовать вышеописанный способ конкурентного связывания в двух направлениях, т.е. определить, блокирует ли известное антитело тестируемое антитело, и наоборот.
[0042] Термин "гуманизировать" относится к тому факту, что, если антитело полностью или частично имеет отличное от человеческого происхождение (например, представляет собой мышиное антитело, полученное в результате иммунизации мышей представляющим интерес антигеном, или химерное антитело на основе такого мышиного антитела), можно заменять определенные аминокислоты, в частности, в каркасных областях и константных областях тяжелых и легких цепей, чтобы избежать или минимизировать иммунный ответ у людей. Хотя иммуногенность невозможно предсказать точно и, вследствие этого, ответ человека на антитело в отношении конкретного антитела, отличные от человеческих антитела чаще оказываются более иммуногенными для людей, чем человеческие антитела. Как было показано, химерные антитела, в которых чужеродные (например, происходящие от грызунов) константные области были заменены последовательностями человеческого происхождения, обычно являются менее иммуногенными, чем антитела полностью чужеродного происхождения, и общая тенденция в области терапевтических антител направлена в сторону гуманизированных или полностью человеческих антитела. Таким образом, химерные антитела или другие антитела отличного от человеческого происхождения можно гуманизировать для снижения риска ответа человека на антитело.
[0043] В случае химерных антител гуманизация, как правило, предусматривает модификацию каркасных областей последовательностей вариабельных доменов. Аминокислотные остатки, которые представляют собой часть определяющих комплементарность областей (CDR), чаще всего не будут изменять в связи с гуманизацией, хотя в определенных случаях может быть необходимо изменить отдельные аминокислотные остатки CDR, например, чтобы удалить участок гликозилирования, участок дезамидирования, участок изомеризации аспартата или нежелательный остаток цистеина или метионина. N-связанное гликозилирование происходит путем прикрепления олигосахаридной цепи к аспарагиновому остатку в трипептидной последовательности Asn-X-Ser или Asn-X-Thr, где X может представлять собой любую аминокислоту за исключением Pro. Удаления участка N-гликозилирования можно достичь за счет мутирования либо остатка Asn, либо остатка Ser/Thr в другой остаток, предпочтительно путем консервативной замены. Дезамидирование аспарагинового и глутаминового остатков может происходить в зависимости от таких факторов, как pH и нахождение их на поверхности. Аспарагиновые остатки особенно подвержены дезамидированию в основном, если находятся в последовательности Asn-Gly, и в меньшей степени в других дипептидных последовательностях, таких как Asn-Ala. Если такой участок дезамидирования, в частности Asn-Gly, присутствует в последовательности CDR, тогда может потребоваться удалить данный участок, как правило, за счет осуществления консервативной замены для удаления одного из задействованных остатков.
[0044] Из уровня техники известны многочисленные способы гуманизации последовательности антитела; см., например, обзор в Almagro & Fransson Front Biosci. 13:1619-1633 (2008). Одним из широко используемых способов является прививка CDR, которая, например в случае химерного антитела мышиного происхождения, включает идентификацию генов зародышевой линии человека, являющихся аналогами генов вариабельных доменов мыши, и прививание последовательностей CDR мыши на этот каркас. Специфичность взаимодействия антитела с антигеном-мишенью обусловлена, в первую очередь, аминокислотными остатками, расположенными в шести CDR тяжелой и легкой цепи. Следовательно, у отдельных антител аминокислотные последовательности в пределах CDR являются гораздо более вариабельными, чем последовательности за пределами CDR. Поскольку последовательности CDR отвечают за большинство взаимодействий антитело-антиген, возможно экспрессировать рекомбинантные антитела, которые имитируют свойства специфического встречающегося в природе антитела или, в более общем смысле, любого специфического антитела с данной аминокислотной последовательностью, например, путем конструирования векторов экспрессии, которые экспрессируют последовательности CDR от специфического антитела, привитые на каркасные последовательности от другого антитела. В результате можно "гуманизировать" отличное от человеческого антитело, и при этом в значительной степени сохранить специфичность связывания и аффинность исходного антитела. Прививка CDR может быть основана на определениях CDR по Kabat, хотя в более поздней публикации (Magdelaine-Beuzelin et al., Crit Rev.Oncol Hematol. 64:210-225 (2007)) было высказано предположение, что определение по IMGT® (международная информационная система ImMunoGeneTics®, www.imgt.org) может улучшить результат гуманизации (см. Lefranc et al., Dev. Comp Immunol. 27:55-77 (2003)).
[0045] В некоторых случаях прививка CDR может снижать специфичность и аффинность связывания и, таким образом, биологическую активность отличного от человеческого антитела с привитыми CDR по сравнению с исходным антителом, из которого получены CDR. Обратные мутации (иногда называемые "восстановление каркаса") могут быть введены в выбранные положения антитела с привитыми CDR, как правило, в каркасных областях, чтобы восстановить специфичность связывания и аффинность исходного антитела. Положения для возможных обратных мутаций можно идентифицировать с применением информации, доступной в литературе и базах данных антител. Аминокислотные остатки, которые являются кандидатами на проведение обратных мутаций, как правило, представляют собой остатки, расположенные на поверхности молекулы антитела, в то время как остатки, которые погружены вглубь или характеризуются низкой степенью нахождения на поверхности, обычно изменять не будут.
[0046] Методикой гуманизации, служащей альтернативой привитию CDR и проведению обратных мутаций, является изменение поверхности, при котором не находящиеся на поверхности остатки, отличного от человеческого происхождения, оставляют, при этом поверхностные остатки изменяют на человеческие остатки.
[0047] В определенных случаях может потребоваться изменить один или несколько аминокислотных остатков CDR, чтобы улучшить аффинность связывания с эпитопом-мишенью. Это известно как "созревание аффинности". В данной области техники известны различные способы созревания аффинности, например, способ насыщающего мутагенеза при сканировании in vitro, описанный Burks et al., Proc Natl Acad Sci USA, 94: 412-417 (1997), и способ ступенчатого созревания аффинности in vitro Wu et al., Proc Natl Acad Sci USA 95: 6037-6042 (1998).
[0048] Термин "человеческое антитело" относится к антителу, в котором последовательности вариабельного домена и константной области получены из человеческих последовательностей. Термин охватывает антитела с последовательностями, полученными из генов человека, при этом данные последовательности были модифицированы, например, для уменьшения иммуногенности, увеличения аффинности и увеличения стабильности. Термин охватывает антитела, продуцируемые рекомбинантным путем в отличных от человеческих клетках, которые могут придавать им гликозилирование, не характерное для антител из клеток человека. Термин также охватывает антитела, продуцируемые в трансгенных отличных от человека организмах с генами человеческих антител.
[0049] Термин "антигенсвязывающая часть" или "антигенсвязывающий фрагмент" антитела относится к части или фрагменту антитела, который сохраняет способность специфически связываться с антигеном. В некоторых вариантах осуществления антигенсвязывающий фрагмент по настоящему изобретению представляет собой фрагмент Fab, Fab', F(ab')2, Fv или scFv. В некоторых вариантах осуществления антигенсвязывающий фрагмент по настоящему изобретению представляет собой фрагмент F(ab’)2, который является бивалентным фрагментом, содержащим два фрагмента Fab, связанных дисульфидным мостиком в шарнирной области (Fab представляет собой моновалентный фрагмент антитела, состоящий из доменов VL, VH, CL и CH1). В некоторых вариантах осуществления антигенсвязывающий фрагмент по настоящему изобретению также может содержать домен CH2 или CH3. Фрагменты антител могут быть получены, например, из целых антител с применением традиционных методик, таких как расщепление целых антител папаином или пепсином. Более того, антитела, фрагменты антител и молекулы иммуноадгезии можно получать с использованием стандартных методик рекомбинантной ДНК, например, описанных в данном документе.
[0050] Антитела и антигенсвязывающие фрагменты, описанные в данном документе, могут быть выделенными. Термин "выделенный белок", "выделенный полипептид" или "выделенное антитело" относится к белку, полипептиду или антителу, которые в силу своего происхождения или источника получения (1) не связаны с естественным образом связанными с ними компонентами, сопутствующими им в их нативном состоянии, (2) практически не содержат других белков от того же биологического вида, (3) экспрессируются в клетке другого биологического вида или (4) не встречаются в природе. Таким образом, полипептид, синтезированный химическим путем или синтезированный в клеточной системе, отличной от клетки, из которой он происходит естественным образом, будет "выделенным" из естественным образом связанных с ним компонентов. Белок также можно сделать практически не содержащим естественным образом связанных с ним компонентов путем выделения с использованием методик очистки белка, хорошо известных в данной области техники.
[0051] Класс (изотип) и подкласс антител, описанных в данном документе, можно определить с помощью любого способа, известного в данной области техники. В целом, класс и подкласс антитела можно определить с применением антител, которые являются специфическими для конкретного класса и подкласса антител. Такие антитела доступны коммерчески. Класс и подкласс можно определить с помощью ELISA и вестерн-блоттинга, а также с помощью других методик. В качестве альтернативы класс и подкласс можно определить путем секвенирования всех или части константных областей тяжелой и/или легкой цепей антител, сравнения их аминокислотных последовательностей с известными аминокислотными последовательностями различных классов и подклассов иммуноглобулинов и определения класса и подкласса антител. Предпочтительным изотипом по настоящему изобретению является изотип IgG.
Средства, которые ингибируют TGF-β
[0052] В некоторых вариантах осуществления средство, которое специфически связывается с TGF-β, используемым в описанной в данном документе комбинированной терапии, представляет собой антитело к TGF-β или его антигенсвязывающий фрагмент (например, Ab1, фрезолимумаб, XOMA 089/NIS793 (Gramont et al., Oncoimmunology 6(1):e1257453 (2017)), SRK-181 (Scholar Rock), ABBV-151 (AbbVie), лерделимумаб или метелимумаб) или молекулу-ловушку TGF-β (например, M7824 (Knudson et al., Oncoimmunology 7(5):e1426519 (2018)) или AVID200 (Thwaites et al., Blood 130:2532 (2017))). В определенных вариантах осуществления антитело к TGF-β представляет собой человеческое моноклональное антитело. В некоторых вариантах осуществления антитело к TGF-β представляет собой пан-TGF-β-специфическое моноклональное антитело, которое менее склонно к образованию полуантител по сравнению с известными ранее антителами, такими как фрезолимумаб. В некоторых вариантах осуществления антитело к TGF-β имеет превосходные фармакокинетические профили, такие как большая степень воздействия на организм по сравнению с фрезолимумабом.
[0053] В некоторых вариантах осуществления антитело к TGF-β представляет собой антитело, описанное в патентной публикации согласно PCT WO 2018/134681, патентной публикации согласно PCT WO 2006/086469, патентной публикации согласно PCT WO 2014/153435, патенте США 8569462 или патенте США 7527791, которые включены в данный документ посредством ссылки во всей своей полноте. В определенных вариантах осуществления антитело к TGF-β представляет собой антитело Ab1 или его вариант, где вариант может содержать, например, определенные минимальные аминокислотные изменения по сравнению с Ab1 (например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 аминокислотных замен, которые могут находиться, например, в каркасных областях) без потери антигенсвязывающей специфичности антитела.
[0054] Расчетная молекулярная масса антитела Ab1 в негликозилированной форме составляет 144 кДа. Аминокислотные последовательности его тяжелой и легкой цепей представляют собой SEQ ID NO: 1 и 2 соответственно. Эти две последовательности показаны ниже. Вариабельные домены выделены курсивом. CDR показаны в рамках. Участок гликозилирования в константном домене тяжелой цепи выделен жирным шрифтом и указан с помощью букв нижнего регистра (N297). Ab1 содержит константную область IgG4 человека, где остаток 228 (нумерация EU) в шарнирной области был мутирован с серина на пролин. P228 заключен в рамку и выделен жирным шрифтом в последовательности под SEQ ID NO: 1, показанной ниже.

[0055] В некоторых вариантах осуществления антитело к TGF-β или антигенсвязывающий фрагмент, описанные в настоящем документе, конкурируют за связывание с TGF-β или связываются с тем же эпитопом на TGF-β, что и Ab1.
[0056] В некоторых вариантах осуществления антитело к TGF-β, описанное в данном документе, содержит тяжелую цепь, которая содержит:
a) CDR1-3 тяжелой цепи (HCDR1-3), которые содержат аминокислотные последовательности под SEQ ID NO: 5-7 соответственно;
b) вариабельный домен тяжелой цепи (VH), последовательность которого на по меньшей мере 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности под SEQ ID NO: 3;
c) VH, который содержит аминокислотную последовательность под SEQ ID NO: 3; или
d) аминокислотную последовательность под SEQ ID NO: 1.
[0057] В некоторых вариантах осуществления антитело к TGF-β, описанное в данном документе, содержит легкую цепь, которая содержит:
a) CDR1-3 легкой цепи (LCDR1-3), которые содержат аминокислотные последовательности под SEQ ID NO: 8-10 соответственно;
b) вариабельный домен легкой цепи (VL), последовательность которого на по меньшей мере 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности под SEQ ID NO: 4;
c) VL, который содержит аминокислотную последовательность под SEQ ID NO: 4; или
d) аминокислотную последовательность под SEQ ID NO: 2.
[0058] В некоторых вариантах осуществления антитело к TGF-β, описанное в данном документе, содержит любую из вышеуказанных тяжелых цепей в комбинации с любой из вышеуказанных легких цепей.
[0059] В некоторых вариантах осуществления антитело к TGF-β, описанное в данном документе, содержит:
а) HCDR1-3 и LCDR1-3, которые содержат аминокислотные последовательности под SEQ ID NO: 5-10 соответственно;
b) VH, последовательность которого на по меньшей мере 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности под SEQ ID NO: 3, и VL, последовательность которого на по меньшей мере 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности под SEQ ID NO: 4;
c) VH, который содержит аминокислотную последовательность под SEQ ID NO: 3, и VL, который содержит аминокислотную последовательность под SEQ ID NO: 4; и
d) HC, которая содержит аминокислотную последовательность под SEQ ID NO: 1, и LC, которая содержит аминокислотную последовательность под SEQ ID NO: 2.
[0060] В некоторых вариантах осуществления антитело к TGF-β, описанное в данном документе (например, антитело к TGF-β с шестью CDR или VH и VL Ab1), содержит константную область IgG4 человека. В некоторых вариантах осуществления остаток 228 (нумерация EU) в шарнирной области константной области IgG4 был мутирован с серина на пролин. Константный домен антитела к TGF-β, описанного в данном документе, также можно модифицировать, например, по остатку L248 согласно Kabat (например, путем введения мутации L248E), чтобы уменьшить любую нежелательную эффекторную функцию молекулы.
[0061] В некоторых вариантах осуществления антитело к TGF-β, описанное в данном документе, содержит область легкой каппа-цепи иммуноглобулина человека.
[0062] В некоторых вариантах осуществления антитело к TGF-β или антигенсвязывающий фрагмент, описанные в данном документе, специфически связываются с TGF-β1, -β2 и -β3 человека.
[0063] В некоторых вариантах осуществления антитело к TGF-β или антигенсвязывающий фрагмент, описанные в данном документе, связывают TGF-β1, -β2 и/или -β3 (например, TGF-β1, -β2 и -β3) с KD, составляющей 1×10-8 M или меньше, например, 9×10-9 M, 8×10-9 M, 7×10-9 M, 6×10-9 M, 5×10-9 M, 4×10-9 M, 3×10-9 M, 2×10-9 M или 1×10-9 M. В определенных вариантах осуществления антитело к TGF-β или антигенсвязывающий фрагмент связывают TGF-β1, -β2 и - β3 с KD, составляющей 3×10-9 M или меньше.
[0064] В некоторых вариантах осуществления антитело к TGF-β или антигенсвязывающий фрагмент, описанные в данном документе, характеризуются одним или несколькими из следующих свойств:
a) ингибируют передачу сигнала от TGF-β;
b) нейтрализуют TGF-β при проведении анализа на эпителиальных клетках легкого норки;
c) характеризуются EC50, составляющей приблизительно 0,05-1 мкг/мл, как определено в анализе индукции IL-11 в клетках A549;
d) ингибируют дифференцировку CD4-положительных T-клеток в индуцируемые регуляторные T-клетки (iTreg);
e) ослабляют иммуносупрессорное микроокружение опухоли;
f) увеличивают уровни MIP2 у пациента (например, в опухолевой ткани пациента);
g) увеличивают уровни KC/GRO у пациента (например, в опухолевой ткани пациента);
h) содействуют активации или инфильтрации в опухолевую ткань CD8-положительных Т-клеток, таких как INF-γ-положительные CD8-положительные Т-клетки;
i) увеличивают кластеризацию натуральных киллеров (NK) у пациента (например, в опухолевой ткани пациента); и
j) восстанавливают цитолитическую активность клеток NK-92 после инкубации с рекомбинантным TGF-β человека.
В некоторых вариантах осуществления антитело к TGF-β или антигенсвязывающий фрагмент, описанные в данном документе, характеризуются 1, 2, 3, 4, 5, 6, 7, 8, 9 или всеми из указанных свойств.
[0065] В некоторых вариантах осуществления антитело к TGF-β или антигенсвязывающий фрагмент, описанные в данном документе, характеризуются увеличенным периодом полужизни, увеличенным воздействием или и тем, и другим по сравнению с фрезолимумабом. Например, увеличение составляет 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% или 100% или больше. Воздействие лекарственного средства, такого как антитело или его фрагмент, описанные в данном документе, представляет собой зависимость концентрации лекарственного средства в организме от времени. Концентрацию лекарственного средства в организме часто указывают как уровень лекарственного средства в крови, плазме крови или сыворотке крови. Период полужизни и воздействие (биологическое воздействие) лекарственного средства можно измерить с помощью хорошо известных способами (например, как описано в патентной публикации согласно РСТ WO 2018/134681).
Средства, которые ингибируют CD38
[0066] В некоторых вариантах осуществления средство, которое специфически связывается с CD38, используемое в комбинированной терапии, описанной в данном документе, представляет собой антитело к CD38 или его антигенсвязывающий фрагмент. В определенных вариантах осуществления антитело к CD38 представляет собой гуманизированное моноклональное антитело. В некоторых вариантах осуществления антитело к CD38 представляет собой антитело, описанное в патенте США 8153765, который включен в данный документ посредством ссылки во всей своей полноте. В некоторых вариантах осуществления антитело к CD38 продуцируется в линии клеток гибридомы, депонированной в Американской коллекции типовых культур под номером депонирования PTA-7670. В некоторых вариантах осуществления антитело к CD38 представляет собой Ab2, Ab3, Ab4, даратумумаб, MOR202 (Raab et al., Blood 128:1152 (2016)), TAK-079 (Roepcke et al., Pharmacol Res Perspect 6(3):e00402 (2018)), TAK-573 (Takeda), TAK-169 (Takeda), HexaBody®-CD38 (Genmab/Janssen), антитело к CD38 SIFbody (Momenta) или TSK011010 (CASI).
[0067] В конкретных вариантах осуществления антитело к CD38 представляет собой антитело Ab2 или его вариант, где вариант может содержать, например, определенные минимальные аминокислотные изменения по сравнению с Ab2 (например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 аминокислотных замен, которые могут находиться, например, в каркасных областях) без потери антигенсвязывающей специфичности антитела.
[0068] Аминокислотные последовательности тяжелой и легкой цепей Ab2 представляют собой SEQ ID NO: 11 и 12 соответственно. Эти две последовательности показаны ниже. Вариабельные домены выделены курсивом. CDR показаны в рамках. Ab2 содержит константную область IgG1 человека.

[0069] В некоторых вариантах осуществления антитело к CD38 или антигенсвязывающий фрагмент конкурирует за связывание с CD38 или связывается с тем же эпитопом на CD38, что и Ab2.
[0070] В некоторых вариантах осуществления антитело к CD38 содержит тяжелую цепь, которая содержит:
a) CDR1-3 тяжелой цепи (HCDR1-3), которые содержат аминокислотные последовательности под SEQ ID NO: 15-17 соответственно;
b) вариабельный домен тяжелой цепи (VH), последовательность которого на по меньшей мере 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности под SEQ ID NO: 13;
c) VH, который содержит аминокислотную последовательность под SEQ ID NO: 13; или
d) аминокислотную последовательность под SEQ ID NO: 11.
[0071] В некоторых вариантах осуществления антитело к CD38 содержит легкую цепь, которая содержит:
a) CDR1-3 легкой цепи (LCDR1-3), которые содержат аминокислотные последовательности под SEQ ID NO: 18-20 соответственно;
b) вариабельный домен легкой цепи (VL), последовательность которого на по меньшей мере 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности под SEQ ID NO: 14;
c) VL, который содержит аминокислотную последовательность под SEQ ID NO: 14; или
d) аминокислотную последовательность под SEQ ID NO: 12.
[0072] В некоторых вариантах осуществления антитело к CD38, описанное в данном документе, содержит любую из вышеуказанных тяжелых цепей в комбинации с любой из вышеуказанных легких цепей.
[0073] В некоторых вариантах осуществления антитело к CD38, описанное в данном документе, содержит:
а) HCDR1-3 и LCDR1-3, которые содержат аминокислотные последовательности под SEQ ID NO: 15-20 соответственно;
b) VH, последовательность которого на по меньшей мере 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности под SEQ ID NO: 13, и VL, последовательность которого на по меньшей мере 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности под SEQ ID NO: 14;
c) VH, который содержит аминокислотную последовательность под SEQ ID NO: 13, и VL, который содержит аминокислотную последовательность под SEQ ID NO: 14; и
d) HC, которая содержит аминокислотную последовательность под SEQ ID NO: 11, и LC, которая содержит аминокислотную последовательность под SEQ ID NO: 12.
[0074] В определенных вариантах осуществления антитело к CD38 представляет собой антитело Ab3 или его вариант, где вариант может содержать, например, определенные минимальные аминокислотные изменения по сравнению с Ab3 (например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 аминокислотных замен, которые могут находиться, например, в каркасных областях) без потери антигенсвязывающей специфичности антитела.
[0075] Аминокислотные последовательности тяжелой и легкой цепей Ab3 представляют собой SEQ ID NO: 25 и 26 соответственно. Эти две последовательности показаны ниже. Вариабельные домены выделены курсивом. CDR показаны в рамках.

[0076] В некоторых вариантах осуществления антитело к CD38 или антигенсвязывающий фрагмент конкурируют за связывание с CD38 или связываются с тем же эпитопом на CD38, что и Ab3.
[0077] В некоторых вариантах осуществления антитело к CD38 содержит тяжелую цепь, которая содержит:
a) CDR1-3 тяжелой цепи (HCDR1-3), которые содержат аминокислотные последовательности под SEQ ID NO: 29-31 соответственно;
b) вариабельный домен тяжелой цепи (VH), последовательность которого на по меньшей мере 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности под SEQ ID NO: 27;
c) VH, который содержит аминокислотную последовательность под SEQ ID NO: 27; или
d) аминокислотную последовательность под SEQ ID NO: 25.
[0078] В некоторых вариантах осуществления антитело к CD38 содержит легкую цепь, которая содержит:
a) CDR1-3 легкой цепи (LCDR1-3), которые содержат аминокислотные последовательности под SEQ ID NO: 32-34 соответственно;
b) вариабельный домен легкой цепи (VL), последовательность которого на по меньшей мере 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности под SEQ ID NO: 28;
c) VL, который содержит аминокислотную последовательность под SEQ ID NO: 28; или
d) аминокислотную последовательность под SEQ ID NO: 26.
[0079] В некоторых вариантах осуществления антитело к CD38, описанное в данном документе, содержит любую из вышеуказанных тяжелых цепей в комбинации с любой из вышеуказанных легких цепей.
[0080] В некоторых вариантах осуществления антитело к CD38, описанное в данном документе, содержит:
а) HCDR1-3 и LCDR1-3, которые содержат аминокислотные последовательности под SEQ ID NO: 29-34 соответственно;
b) VH, последовательность которого на по меньшей мере 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности под SEQ ID NO: 27, и VL, последовательность которого на по меньшей мере 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности под SEQ ID NO: 28;
c) VH, который содержит аминокислотную последовательность под SEQ ID NO: 27, и VL, который содержит аминокислотную последовательность под SEQ ID NO: 28; и
d) HC, которая содержит аминокислотную последовательность под SEQ ID NO: 25, и LC, которая содержит аминокислотную последовательность под SEQ ID NO: 26.
[0081] В определенных вариантах осуществления антитело к CD38 представляет собой антитело Ab4 или его вариант, где вариант может содержать, например, определенные минимальные аминокислотные изменения по сравнению с Ab4 (например, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 аминокислотных замен, которые могут находиться, например, в каркасных областях) без потери антигенсвязывающей специфичности антитела.
[0082] Аминокислотные последовательности тяжелой и легкой цепей Ab4 представляют собой SEQ ID NO: 35 и 36 соответственно. Эти две последовательности показаны ниже. Вариабельные домены выделены курсивом. CDR показаны в рамках.

[0083] В некоторых вариантах осуществления антитело к CD38 или антигенсвязывающий фрагмент конкурируют за связывание с CD38 или связываются с тем же эпитопом на CD38, что и Ab4.
[0084] В некоторых вариантах осуществления антитело к CD38 содержит тяжелую цепь, которая содержит:
a) CDR1-3 тяжелой цепи (HCDR1-3), которые содержат аминокислотные последовательности под SEQ ID NO: 39-41 соответственно;
b) вариабельный домен тяжелой цепи (VH), последовательность которого на по меньшей мере 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности под SEQ ID NO: 37;
c) VH, который содержит аминокислотную последовательность под SEQ ID NO: 37; или
d) аминокислотную последовательность под SEQ ID NO: 35.
[0085] В некоторых вариантах осуществления антитело к CD38 содержит легкую цепь, которая содержит:
a) CDR1-3 легкой цепи (LCDR1-3), которые содержат аминокислотные последовательности под SEQ ID NO: 42-44 соответственно;
b) вариабельный домен легкой цепи (VL), последовательность которого на по меньшей мере 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности под SEQ ID NO: 38;
c) VL, который содержит аминокислотную последовательность под SEQ ID NO: 38; или
d) аминокислотную последовательность под SEQ ID NO: 36.
[0086] В некоторых вариантах осуществления антитело к CD38, описанное в данном документе, содержит любую из вышеуказанных тяжелых цепей в комбинации с любой из вышеуказанных легких цепей.
[0087] В некоторых вариантах осуществления антитело к CD38, описанное в данном документе, содержит:
а) HCDR1-3 и LCDR1-3, которые содержат аминокислотные последовательности под SEQ ID NO: 39-44 соответственно;
b) VH, последовательность которого на по меньшей мере 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности под SEQ ID NO: 37, и VL, последовательность которого на по меньшей мере 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности под SEQ ID NO: 38;
c) VH, который содержит аминокислотную последовательность под SEQ ID NO: 37, и VL, который содержит аминокислотную последовательность под SEQ ID NO: 38; и
d) HC, которая содержит аминокислотную последовательность под SEQ ID NO: 35, и LC, которая содержит аминокислотную последовательность под SEQ ID NO: 36.
[0088] В некоторых вариантах осуществления антитело к CD38, описанное в данном документе, содержит константную область IgG1 человека.
[0089] В некоторых вариантах осуществления антитело к CD38, описанное в данном документе, содержит область легкой каппа-цепи иммуноглобулина человека.
[0090] В некоторых вариантах осуществления антитело к CD38 или антигенсвязывающий фрагмент, описанные в данном документе, связывают CD38 с KD, составляющей 1×10-8 M или меньше, например, 9×10-9 M, 8×10-9 M, 7×10-9 M, 6×10-9 M, 5×10-9 M, 4×10-9 M, 3×10-9 M, 2×10-9 M или 1×10-9 M. В определенных вариантах осуществления антитело к CD38 или антигенсвязывающий фрагмент связывают CD38 с KD, составляющей 3×10-9 M или меньше.
[0091] В некоторых вариантах осуществления антитело к CD38 или антигенсвязывающий фрагмент, описанные в данном документе, осуществляют уничтожение CD38-положительной клетки посредством апоптоза, ADCC и CDC; в определенных вариантах осуществления уничтожение указанных CD38-положительных клеток посредством апоптоза может происходить в отсутствие стромальных клеток или цитокинов, производимых стромой. В некоторых вариантах осуществления CD38-положительная клетка представляет собой злокачественную клетку. В некоторых вариантах осуществления CD38-положительная клетка представляет собой В-клетку. В некоторых вариантах осуществления CD38-положительная клетка представляет собой опухолевую клетку, полученную из гемопоэтического злокачественного новообразования. В более предпочтительном варианте осуществления CD38-положительная клетка представляет собой клетку лимфомы, клетку лейкоза или клетку множественной миеломы. В дополнительном предпочтительном варианте осуществления CD38-положительная клетка представляет собой клетку NHL, BL, MM, B-CLL, ALL, TCL, AML, HCL, HL или CML.
[0092] В некоторых вариантах осуществления антитело к CD38 или антигенсвязывающий фрагмент, описанные в данном документе, способны уничтожать по меньшей мере 10%, 15%, 20%, 21%, 22%, 23%, 24%, 25%, 26%, 27%, 28%, 29%, 30%, 35% или 40% (например, по меньшей мере 24%) клеток лимфомы Дауди в отсутствие клеток стромы или цитокинов, производимых стромой, in vitro.
[0093] В некоторых вариантах осуществления антитело к CD38 или антигенсвязывающий фрагмент, описанные в данном документе, способны уничтожать по меньшей мере 3%, 4%, 5%, 6%, 7%, 8%, 9% или 10% (например, по меньшей мере 7%) клеток лимфомы Рамоса в отсутствие клеток стромы или цитокинов, производимых стромы, in vitro.
[0094] В некоторых вариантах осуществления антитело к CD38 или антигенсвязывающий фрагмент, описанные в данном документе, способны уничтожать по меньшей мере 5%, 6%, 7%, 8%, 9%, 10%, 11%, 12%, 13%, 14%. %, 15%, 16%, 17%, 18%, 19% или 20% (например, по меньшей мере 11%) клеток множественной миеломы MOLP-8 в отсутствие клеток стромы или цитокинов, производимых стромой, in vitro.
[0095] В некоторых вариантах осуществления антитело к CD38 или антигенсвязывающий фрагмент, описанные в данном документе, способны уничтожать по меньшей мере 25%, 30%, 31%, 32%, 33%, 34%, 35%, 36%, 37%, 38%, 39%, 40%, 45% или 50% (например, по меньшей мере 36%) клеток лимфомы SU-DHL-8 в отсутствие клеток стромы или цитокинов, производимых стромой, in vitro.
[0096] В некоторых вариантах осуществления антитело к CD38 или антигенсвязывающий фрагмент, описанные в данном документе, способны уничтожать по меньшей мере 20%, 25%, 26%, 27%, 28%, 29%, 30% или 35% (например, по меньшей мере 27%) клеток лимфомы NU-DUL-1 в отсутствие клеток стромы или цитокинов, производимых стромы, in vitro.
[0097] В некоторых вариантах осуществления антитело к CD38 или антигенсвязывающий фрагмент, описанные в данном документе, способны уничтожать по меньшей мере 50%, 55%, 60%, 61%, 62%, 63%, 64%, 65%, 70% или 75% (например, по меньшей мере 62%) клеток лейкоза DND-41 в отсутствие клеток стромы или цитокинов, производимых стромой, in vitro.
[0098] В некоторых вариантах осуществления антитело к CD38 или антигенсвязывающий фрагмент, описанные в данном документе, способны уничтожать по меньшей мере 5%, 6%, 7%, 8%, 9%, 10%, 11%,12% или 13% (например, по меньшей мере 9%) клеток лейкоза JVM-13 в отсутствие клеток стромы или цитокинов, производимых стромой, in vitro.
[0099] В некоторых вариантах осуществления антитело к CD38 или антигенсвязывающий фрагмент, описанные в данном документе, способны уничтожать по меньшей мере 1%, 2%, 3%, 4%, 5%, 6%, 7% или 8% (например, по меньшей мере 4%) клеток лейкоза HC-1 в отсутствие клеток стромы или цитокинов, производимых стромой, in vitro.
[0100] В некоторых вариантах осуществления средство, которое специфически связывается с CD38, представляет собой конъюгат, содержащий описанные в данном документе антитело к CD38 или антигенсвязывающий фрагмент, связанные с цитотоксическим средством. Цитотоксическое средство, например, может быть выбрано из майтанзиноида, низкомолекулярного лекарственного средства, производного томаймицина, производного лептомицина, пролекарства, таксоида, CC-1065 и аналога CC-1065 или любого цитотоксического средства, описанного в патенте США 8153765 (который включен в данный документ посредством ссылки во всей своей полноте).
[0101] Класс антитела к TGF-β или антитела к CD38, описанных в данном документе, может быть изменен или переключен на другой класс или подкласс. В одном аспекте молекулу нуклеиновой кислоты, кодирующую VL или VH, выделяют с использованием способов, хорошо известных в данной области техники, так что она не включает последовательности нуклеиновой кислоты, кодирующие CL или CH. Затем молекулы нуклеиновой кислоты, кодирующие VL или VH, функционально связывают с последовательностью нуклеиновой кислоты, кодирующей CL или CH соответственно, из другого класса молекулы иммуноглобулина. Этого можно достичь с применением вектора или молекулы нуклеиновой кислоты, которые содержат цепь CL или CH, описанную выше. Например, антитело, которое изначально относилось к IgM, может быть переключено на класс IgG. Кроме того, переключение класса можно использовать для преобразования одного подкласса IgG в другой, например, из IgG1 в IgG2. Константная область легкой κ-цепи может быть изменена, например, на константную область легкой λ-цепи. Предпочтительный способ получения описанного в данном документе антитела с требуемым изотипом Ig включает стадии выделения молекулы нуклеиновой кислоты, кодирующей тяжелую цепь антитела, и молекулы нуклеиновой кислоты, кодирующей легкую цепь антитела, получения вариабельного домена тяжелой цепи, лигирования вариабельного домена тяжелой цепи с константной областью тяжелой цепи требуемого изотипа, экспрессии легкой цепи и лигированной тяжелой цепи в клетке и сбора антитела с требуемым изотипом.
[0102] Описанное в данном документе антитело может представлять собой молекулу IgG, IgM, IgE, IgA или IgD, но, как правило, для него характерен изотип IgG, например подкласс IgG, IgG1, IgG2a или IgG2b, IgG3 или IgG4.
[0103] В одном варианте осуществления антитело может содержать по меньшей мере одну мутацию в Fc-области. Известен целый ряд различных мутаций Fc, при этом данные мутации обеспечивают измененную эффекторную функцию. Например, во многих случаях будет требоваться уменьшение или устранение эффекторной функции, например, когда нежелательным являются взаимодействия лиганд/рецептор, или в случае конъюгатов антитело-лекарственное средство.
[0104] В некоторых вариантах осуществления антитела, описанные в данном документе, например антитела к TGF-β и к CD38, не содержат С-концевого лизина в тяжелой цепи. С-концевой лизин может быть удален во время изготовления или с помощью рекомбинантной технологии (т.e. последовательность, кодирующая тяжелую цепь, не содержит кодон для С-концевого лизина). Таким образом, в рамках настоящего изобретения также предусмотрены антитела, содержащие аминокислотную последовательность тяжелой цепи под SEQ ID NO: 1 или 11 без С-концевого лизина.
Виды комбинированной терапии
[0105] В настоящем изобретении представлена комбинированная терапия, содержащая средство, которое специфически связывается с TGF-β человека, и средство, которое специфически связывается с CD38 человека. В некоторых вариантах осуществления средство, которое специфически связывается с TGF-β, может представлять собой любое из антител к TGF-β или их антигенсвязывающих фрагментов, описанных в данном документе. В некоторых вариантах осуществления средство, которое специфически связывается с CD38, может представлять собой любое из антител к CD38 или их антигенсвязывающих фрагментов, описанных в данном документе. В настоящем изобретении также представлена комбинированная терапия посредством одного или нескольких других средств, которые ингибируют TGF-β (например, галунисертиб, LY3200882, PF-06952229 (Pfizer), GFH-018 (GenFleet) и/или вактосертиб) и/или одного или нескольких других средств, которые ингибируют CD38. Комбинированная терапия, описанная в данном документе, может приобретать вид способа лечения с применением указанных средств или фармацевтической композиции, содержащей указанные средства.
[0106] В настоящем изобретении также предусмотрена комбинированная терапия, содержащая средство, которое специфически связывается с CD38 человека (например, антитело к CD38 или его антигенсвязывающий фрагмент, такие как описаны в данном документе), и средство, которое специфически связывается с LAP (например, антитело к LAP).
[0107] В некоторых вариантах осуществления комбинированная терапия по настоящему изобретению предусматривает применение антитела Ab1 к TGF-β и антитела Ab2 к CD38. В некоторых вариантах осуществления комбинированная терапия по настоящему изобретению предусматривает применение антитела или его антигенсвязывающего фрагмента, которые конкурируют за связывание или связываются с тем же эпитопом TGF-β, что и Ab1, и антитело, которое конкурирует за связывание или связывается с тем же эпитопом CD38, что и Ab2. В определенных вариантах осуществления средства Ab1 и Ab2 используются в отдельных композициях (например, вводятся последовательно). В определенных вариантах осуществления средства Ab1 и Ab2 используются в одной композиции.
[0108] В определенных вариантах осуществления комбинированная терапия по настоящему изобретению предусматривает применение:
- антитела к TGF-β или его антигенсвязывающего фрагмента, содержащих HCDR1-3 и LCDR1-3 с аминокислотными последовательностями под SEQ ID NO: 5-10 соответственно; и антитела к CD38, содержащего HCDR1-3 и LCDR1-3 с аминокислотными последовательностями под SEQ ID NO: 15-20 соответственно;
- антитела к TGF-β или его антигенсвязывающего фрагмента, содержащих VH, последовательность которого на по меньшей мере 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности под SEQ ID NO: 3, и VL, последовательность которого на по меньшей мере 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности под SEQ ID NO: 4; и антитела к CD38, содержащего VH, последовательность которого на по меньшей мере 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности под SEQ ID NO: 13, и VL, последовательность которого на по меньшей мере 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентична аминокислотной последовательности под SEQ ID NO: 14;
- антитела к TGF-β или его антигенсвязывающего фрагмента, содержащих VH и VL с аминокислотными последовательностями под SEQ ID NO: 3 и 4 соответственно; и антитела к CD38, содержащего VH и VL с аминокислотными последовательностями под SEQ ID NO: 13 и 14 соответственно; или
- антитела к TGF-β, содержащего HC и LC с аминокислотными последовательностями под SEQ ID NO: 1 и 2 соответственно; и антитела к CD38, содержащего HC и LC с аминокислотными последовательностями под SEQ ID NO: 11 и 12 соответственно.
[0109] В некоторых вариантах осуществления антитела к TGF-β и CD38, используемые в комбинированной терапии, имеют изотипы IgG4 и IgG1 соответственно. В определенных вариантах осуществления антитело к TGF-β содержит константную область IgG4 человека, где остаток 228 (нумерация EU) в шарнирной области был мутирован с серина на пролин.
[0110] В некоторых вариантах осуществления антитело к TGF-β или его антигенсвязывающий фрагмент, описанные в данном документе, ослабляют иммуносупрессорные эффекты TGF-β в отношении опосредованной NK-клетками ADCC под действием антитела к CD38, описанного в данном документе, что делает комбинированную терапию по настоящему изобретению более эффективной, чем лечение антителом к CD38 отдельно.
[0111] В некоторых вариантах осуществления комбинированная терапия, содержащая средство, которое специфически связывается с TGF-β человека, и средство, которое специфически связывается с CD38 человека (например, антитело к TGF-β и антитело к CD38, такие как Ab1 и Ab2 соответственно), может дополнительно предусматривать дополнительное средство или терапию. В определенных вариантах осуществления дополнительное средство или терапия могут представлять собой, например, леналидомид, помалидомид, бортезомиб, метилпреднизолон, дексаметазон, преднизон, мелфалан, бортезомиб, иксазомиб, карфилзомиб, талидомид, циклофосфамид, пембролизумаб, пан-ингибитор гистондеацетилазы (например, панобиностат), ретиноевую кислоту (например, полностью транс-ретиноевую кислоту), радиоиммунотерапию, химиотерапию и т.д. В определенных вариантах осуществления дополнительное средство или терапия представляют собой комбинацию леналидомида и дексаметазона. В определенных вариантах осуществления дополнительное средство или терапия представляют собой комбинацию бортезомиба, мелфалана и преднизона. В определенных вариантах осуществления дополнительное средство или терапия представляют собой комбинацию бортезомиба и дексаметазона. В определенных вариантах осуществления дополнительное средство или терапия представляют собой комбинацию помалидомида и дексаметазона. В определенных вариантах осуществления дополнительное средство или терапия представляют собой дексаметазон. В некоторых вариантах осуществления дополнительное средство или терапия представляют собой средство лечения для состояния, на которое нацеливается комбинированная терапия по настоящему изобретению. Например, если состояние представляет собой миелому (например, множественную миелому), средство лечения может представлять собой, например, элотузумаб.
[0112] В некоторых вариантах осуществления средства в комбинированной терапии по настоящему изобретению вводятся более чем в одной композиции. В определенных вариантах осуществления каждое средство предоставлено в отдельной композиции. В случае, когда имеется более одной композиции, композиции можно вводить одновременно, последовательно или отдельно. В других вариантах осуществления средства вводят в одной композиции. Например, комбинированная терапия, содержащая антитело к TGF-β и антитело к CD38, может предусматривать введение одной композиции, содержащей оба антитела, или отдельной композиции для каждого антитела (при этом отдельные композиции можно вводить последовательно или одновременно) .
Терапевтические пути применения видов комбинированной терапии по настоящему изобретению
[0113] В одном аспекте виды комбинированной терапии по настоящему изобретению применяются для лечения состояния, которое зависит от экспрессии CD38. В некоторых вариантах осуществления виды комбинированной терапии по настоящему изобретению применяются для лечения гиперпролиферативного нарушения, воспалительного заболевания, аутоиммунного заболевания или фиброзного состояния. В определенных вариантах осуществления виды комбинированной терапии по настоящему изобретению применяются для лечения рака.
[0114] В некоторых вариантах осуществления виды комбинированной терапии по настоящему изобретению нацелены на CD38-положительные клетки (например, на CD38-положительные раковые клетки, такие как злокачественные В-клетки). Клетка может быть идентифицирована как CD38-положительная с помощью любого подходящего способа определения экспрессии гена или белка, например, с помощью гистологического исследования, проточной цитометрии, RT-PCR или RNA-Seq. Раковые клетки, используемые для определения, могут быть получены посредством биопсии опухоли или путем сбора циркулирующих опухолевых клеток. Без ограничения теорией предполагается, что средство, которое специфически связывается с CD38, будет связываться с CD38-положительными клетками и опосредовать ADCC/CDC в отношении клетках, и что средство, которое специфически связывается с TGF-β, будет снижать иммуносупрессорный эффект TGF-β, тем самым повышая эффективность противораковой терапии.
[0115] В некоторых вариантах осуществления виды комбинированной терапии по настоящему изобретению применяются для лечения миеломы, такой как множественная миелома (например, рецидивирующая и/или рефрактерная множественная миелома, впервые диагностированная множественная миелома (необязательно не подходящая для трансплантации), тлеющая множественная миелома, миелома с легкими цепями, несекреторная миелома, миелома с иммуноглобулином D или миелома с иммуноглобулином E). В определенных вариантах осуществления применение видов комбинированной терапии по настоящему изобретению приводит к меньшему разрушению кости при миеломных поражениях кости, чем терапия с помощью средства, которое специфически связывается с CD38 (например, антитело к CD38), отдельно. В конкретных вариантах осуществления применение видов комбинированной терапии по настоящему изобретению может приводить к улучшенному заживлению миеломных поражений кости. Без ограничения теорией предполагается, что средство, которое специфически связывается с TGF-β (например, антитело к TGF-β), будет ингибировать супрессорную активность TGF-β в отношении дифференцировки остеобластов и минерализации матрикса, за счет чего усиливается образование кости, и это приводит к ремоделированию кости и заживлению кости. Кроме того, поскольку зрелые остеобласты усиливают апоптоз и остановку клеточного цикла клеток множественной миеломы, средство, которое специфически связывается с TGF-β, может также подавлять рост клеток множественной миеломы.
[0116] В некоторых вариантах осуществления виды комбинированной терапии по настоящему изобретению применяются для лечения, например, амилоидоза (такого как рецидивирующий или рефрактерный первичный амилоидоз или амилоидоз легких цепей), миелодиспластического синдрома (MDS), моноклональной гаммапатии, солитарной плазмоцитомы, экстрамедуллярной плазмоцитомы или макроглобулинемии Вальденстрема.
[0117] В некоторых вариантах осуществления виды комбинированной терапии по настоящему изобретению применяются для лечения гематологического злокачественного новообразования, например лейкоза или лимфомы. Например, злокачественное новообразование может представлять собой хронический лимфоцитарный лейкоз, острый В- и Т-лимфоцитарный лейкоз, острый лимфобластный лейкоз (например, острый В-клеточный лимфобластный лейкоз или острый лимфобластный лейкоз из клеток-предшественников В-клеток или T-клеток), хронический лимфоцитарный острый миелоидный лейкоз, хронический миелоидный лейкоз, острый миелогенный лейкоз, хронический миелогенный лейкоз, промиелоцитарный лейкоз и злокачественный ретикулоэндотелиоз), неходжкинскую лимфому, лимфому Ходжкина, лимфому Беркитта, B-клеточную лимфому (такую как диффузная крупноклеточная B-клеточная лимфома или В-клеточная лимфома из клеток зародышевого центра), Т-клеточную лимфому (такую как периферическая Т-клеточная лимфома), лимфому из натуральных киллеров/T-клеток (например, носового типа), лимфобластную лимфому, лимфому из клеток мантийной зоны и фолликулярную лимфому. В определенных вариантах осуществления виды комбинированной терапии по настоящему изобретению применяются для лечения лимфобластного лейкоза.
[0118] Другие виды рака, которые можно лечить с помощью видов комбинированной терапии по настоящему изобретению, могут представлять собой солидные опухоли и могут включать без ограничения рак кожи (например, меланому, включая неоперабельную или метастатическую меланому, плоскоклеточный рак кожи, пигментную ксеродермию и кератоакантому), рак щитовидной железы, рак легкого (например, немелкоклеточный рак легкого), рак пищевода, рак желудка, рак толстой кишки, колоректальный рак, рак поджелудочной железы, рак печени (например, гепатоцеллюлярную карциному), первичный перитонеальный рак, рак мочевого пузыря, рак почек или рак почки (например, почечно-клеточную карциному), уротелиальную карциному, рак молочной железы (например, Her2-положительный рак молочной железы или трижды негативный рак молочной железы), рак яичника, рак фаллопиевой трубы, рак шейки матки, рак матки, рак предстательной железы, рак яичка, рак головы и шеи (например, плоскоклеточную карциному головы и шеи), рак головного мозга, нейробластому, глиобластому, глиому, астроцитому, шванному, мезотелиому, фибросаркому, рабдомиосаркому, остеосаркому, саркому Капоши, семиному и тератокарциному. В некоторых вариантах осуществления комбинированная терапия по настоящему изобретению применяется для лечения немелкоклеточного рака легкого, рака предстательной железы (например, аденокарциномы предстательной железы), глиобластомы, гепатоцеллюлярного рака, рака яичника, рака головы и шеи, уротелиального рака или колоректального рака.
[0119] Виды комбинированной терапии по настоящему изобретению также могут быть применимы для ингибирования опосредованного циклоспорином прогрессирования злокачественного новообразования или рака (например, метастазирования).
[0120] В некоторых вариантах осуществления виды комбинированной терапии по настоящему изобретению применимы для лечения рака на ранней, промежуточной, поздней или метастатической стадии. В некоторых вариантах осуществления виды комбинированной терапии применяются для лечения пациента (например, пациента с множественной миеломой), который получил по меньшей мере одну предшествующую терапию. В некоторых вариантах осуществления виды комбинированной терапии применимы при лечении рецидивирующего или рефрактерного рака.
[0121] В некоторых вариантах осуществления виды комбинированной терапии по настоящему изобретению применяются для лечения любого из состояний, описанных в данном документе (например, рака, описанного в настоящем документе), у пациента, у которого произошло прогрессирование во время применения стандартной терапии указанного состояния или после него, или для которого не существует эффективной стандартной терапии для указанного состояния.
[0122] В некоторых вариантах осуществления виды комбинированной терапии по настоящему изобретению применяются для лечения любого из состояний, описанных в данном документе (например, рака, описанного в данном документе), у пациента, у которого проявляется устойчивость к одному или нескольким видам стандартной терапии для указанного состояния. В определенных вариантах осуществления у пациента может иметься состояние (например, рак, такой как множественная миелома), рефрактерный к лечению посредством Ab2, Ab3, Ab4, галунисертиба, LY3200882, XOMA 089, даратумумаба, MOR202, TAK-079, TAK-573, TAK-169, HexaBody®-CD38 или любой их комбинации. Состояние может характеризоваться рефрактерностью в отношении лечения посредством средства, которое специфически связывается с CD38. В конкретных вариантах осуществления у пациента может иметься состояние (например, рак, такой как множественная миелома), рефрактерное к лечению посредством Ab2 или лечению посредством даратумумаба или рефрактерное к обоим видам лечения.
[0123] В некоторых вариантах осуществления виды комбинированной терапии по настоящему изобретению применяются для лечения рака, описанного в данном документе, при этом рак демонстрирует высокие уровни экспрессии TGF-β. В определенных вариантах осуществления рак демонстрирует высокие уровни экспрессии TGF-β и является резистентным к лечению посредством средства, которое специфически связывается с CD38 (например, Ab2, Ab3, Ab4, даратумумаба, MOR202, TAK-079, TAK-573, TAK-169, HexaBody®-CD38 или любой их комбинации). В конкретных вариантах осуществления рак может быть рефрактерным к лечению посредством Ab2 или лечению посредством даратумумаба или к обоим видам лечения.
[0124] В некоторых вариантах осуществления виды комбинированной терапии по настоящему изобретению применяются для лечения пациента с впервые диагностированной множественной миеломой, который не может получить такой тип трансплантации стволовых клеток, при котором используются его собственные стволовые клетки (трансплантация аутологичных стволовых клеток). В качестве дополнения или альтернативы пациент получал по меньшей мере один предшествующий лекарственный препарат для лечения множественной миеломы. В конкретных вариантах осуществления виды комбинированной терапии дополнительно содержат:
a) леналидомид и/или дексаметазон,
b) бортезомиб, леналидомид и/или дексаметазон,
c) бортезомиб, мелфалан и/или преднизон, или
d) бортезомиб и/или дексаметазон.
[0125] В некоторых вариантах осуществления виды комбинированной терапии по настоящему изобретению применяются для лечения пациента, который ранее получал по меньшей мере два предшествующих лекарственных препарата для лечения множественной миеломы. В некоторых вариантах осуществления два предшествующих лекарственных препарата включают леналидомид и/или ингибитор протеасомы.
[0126] В некоторых вариантах осуществления виды комбинированной терапии по настоящему изобретению применяются для лечения пациента, который ранее получал по меньшей мере три лекарственных препарата для лечения множественной миеломы. В определенных вариантах осуществления три предшествующих лекарственных препарата включают ингибитор протеасомы и/или иммуномодулирующее средство.
[0127] В некоторых вариантах осуществления виды комбинированной терапии по настоящему изобретению применяются для лечения пациента, у которого отсутствовал ответ на ингибитор протеасомы и/или иммуномодулирующее средство.
[0128] В некоторых вариантах осуществления виды комбинированной терапии по настоящему изобретению применяются для лечения пациента с рецидивирующей/рефрактерной множественной миеломой в комбинации с помалидомидом и/или дексаметазоном (например, дексаметазоном в низких дозах). В определенных вариантах осуществления пациент получал по меньшей мере два предшествующих лекарственных препарата для лечения множественной миеломы. В конкретных вариантах осуществления два предшествующих лекарственных препарата включают леналидомид и/или ингибитор протеасомы.
[0129] "Лечить", "осуществлять лечение" и "лечение" относятся к способу облегчения или устранения биологического нарушения и/или по меньшей мере одного из его сопутствующих симптомов. Используемый в данном документе термин "облегчить" заболевание, нарушение или состояние означает уменьшение тяжести и/или частоты проявления симптомов заболевания, нарушения или состояния. Кроме того, в данном документе ссылки на "лечение" включают ссылки на радикальное, паллиативное и профилактическое лечение. Разумеется, понятно, что применительно к терапии рака "лечение" включает любое медицинское вмешательство, приводящее к замедлению темпов роста раковой опухоли, задержке прогрессирования или рецидива рака или снижению темпов метастазирования рака, а также частичной ремиссии рака с целью увеличения ожидаемой продолжительности жизни пациента.
[0130] Используемые в данном документе термины "совместное введение", "совместно введенный" и "в комбинации с" без ограничения относятся к (i) одновременному введению терапевтических средств пациенту, нуждающемуся в лечении, когда такие средства составлены вместе в единую лекарственную форму, (ii) практически одновременному введению таких средств пациенту, нуждающемуся в лечении, когда такие средства составлены отдельно друг от друга в отдельные лекарственные формы, и (iii) последовательному введению таких средств пациенту, нуждающемуся в лечении, когда такие средства составлены отдельно друг от друга в отдельные лекарственные формы, которые пациент принимает в разное время.
[0131] Соотношение между средством, которое специфически связывается с TGF-β (например, антителом к TGF-β), и средством, которое специфически связывается с CD38 (например, антителом к CD38), может быть таким, что средства вводятся в одинаковых количествах (т.е. при соотношении 1:1), но это не обязательно. В зависимости от характеристик отдельных средств может потребоваться применение неравных количеств средств.
[0132] Понятно, что виды комбинированной терапии по настоящему изобретению могут применяться в способе лечения, описанном в данном документе, могут быть предназначены для применения при лечении, описанном в данном документе, и/или могут быть предназначены для применения в изготовлении лекарственного препарата для лечения, описанного в данном документе.
Схема введения доз
[0133] Виды комбинированной терапии по настоящему изобретению будут вводиться в эффективном количестве для лечения рассматриваемого состояния, т.е. в дозировках и в течение периодов времени, необходимых для достижения требуемого результата. Терапевтически эффективное количество может варьироваться в зависимости от таких факторов, как конкретное состояние, подлежащее лечению, возраст, пол, состояние здоровья и масса пациента, и от того, вводятся ли средства в качестве обособленного вида лечения или в комбинации с одним или несколькими дополнительными видами лечения рака.
[0134] "Терапевтически эффективное количество" относится к количеству подлежащего введению терапевтического средства, которое будет в некоторой степени ослаблять один или несколько симптомов нарушения, подлежащего лечению. Это количество может определять медицинский работник на основе общепринятых принципов. Терапевтически эффективное количество противоракового терапевтического средства, например, может приводить к уменьшению размера опухоли, увеличению выживаемости, элиминации раковых клеток, снижению прогрессирования заболевания, обращению метастазирования или другим клиническим конечным точкам, требуемых для медицинских работников.
[0135] В некоторых вариантах осуществления пациенты находятся под наблюдением на предмет сердечных и легочных побочных эффектов, когда они подвергаются лечению посредством видов комбинированной терапии по настоящему изобретению.
Клетки-хозяева и способы получения антител и композиций на основе антител
[0136] Один аспект настоящего изобретения относится к способам получения антител для видов комбинированной терапии по настоящему изобретению. Один вариант осуществления относится к способу получения антител, описанных в данном документе, предусматривающему обеспечение рекомбинантных клеток-хозяев, способных экспрессировать антитела, культивирование указанных клеток-хозяев в условиях, подходящих для экспрессии антител, и выделение полученных антител. Антитела, полученные посредством такой экспрессии в таких рекомбинантных клетках-хозяевах, называются в данном документе "рекомбинантными антителами". Также описаны клетки-потомки таких клеток-хозяев и полученные в них антитела.
[0137] Используемый в данном документе термин "рекомбинантная клетка-хозяин" (или просто "клетка-хозяин") обозначает клетку, в которую был введен рекомбинантный вектор экспрессии. Клетка-хозяин может содержать, например, один или несколько векторов, описанных в данном документе. Клетки-хозяева могут содержать, например, нуклеотидную последовательность, кодирующую тяжелую цепь или ее антигенсвязывающий фрагмент, нуклеотидную последовательность, кодирующую легкую цепь или ее антигенсвязывающий фрагмент, или их обе из антитела к TGF-β и/или антитела к CD38 или его антигенсвязывающего фрагмента, описанных в данном документе. Следует понимать, что "рекомбинантная клетка-хозяин" и "клетка-хозяин" означают не только конкретную рассматриваемую клетку, но также потомство такой клетки. Поскольку в последующих поколениях могут возникать определенные модификации вследствие мутации или влияния окружающей среды, в действительности, такое потомство может не быть идентичным исходной клетке, но оно по-прежнему включается в объем термина "клетка-хозяин", используемого в данном документе.
[0138] В некоторых вариантах осуществления клетка-хозяин по настоящему изобретению содержит:
- нуклеотидную последовательность, которая кодирует тяжелую цепь или ее антигенсвязывающий фрагмент, нуклеотидную последовательность, которая кодирует легкую цепь или ее антигенсвязывающий фрагмент, или их обе из антитела к TGF-β, описанного в данном документе, и
- нуклеотидную последовательность, которая кодирует тяжелую цепь или ее антигенсвязывающий фрагмент, нуклеотидную последовательность, которая кодирует легкую цепь или ее антигенсвязывающий фрагмент, или их обе из антитела к CD38, описанного в данном документе.
[0139] Молекулы нуклеиновых кислот, кодирующие аминокислотные последовательности тяжелой и/или легкой цепи антител к TGF-β и/или к CD38 или их антигенсвязывающих фрагментов, могут содержаться в векторах экспрессии. Векторы экспрессии, в которых представляющие интерес последовательности нуклеиновых кислот связаны с необходимыми последовательностями контроля экспрессии, такими как последовательности контроля транскрипции и трансляции, включают плазмиды, ретровирусы, аденовирусы, аденоассоциированные вирусы (AAV), вирусы растений, такие как вирус мозаики цветной капусты, вирус табачной мозаики, космиды, YAC, эписомы, происходящие от EBV, и т.п. Последовательность, кодирующая легкую цепь антитела, и последовательность, кодирующая тяжелую цепь антитела, могут быть встроены в отдельные векторы и могут быть функционально связаны с одинаковыми или разными последовательностями контроля экспрессии (например, промоторами). В одном варианте осуществления обе кодирующие последовательности встроены в один и тот же вектор экспрессии и могут быть функционально связаны с одними и теми же последовательностями контроля экспрессии (например, общим промотором), с отдельными идентичными последовательностями контроля экспрессии (например, промоторами) или с различными последовательностями контроля экспрессии (например, промоторами). Кодирующие последовательности антитела можно встроить в вектор экспрессии стандартными способами (например, с помощью лигирования комплементарных сайтов рестрикции на фрагменте гена антитела и векторе или лигирования тупых концов, если сайты рестрикции отсутствуют).
[0140] Векторы экспрессии, кодирующие антитела и антигенсвязывающие фрагменты, описанные в данном документе, можно вводить в клетки-хозяева для экспрессии. В некоторых вариантах осуществления векторы экспрессии, кодирующие антитело к TGF-β, и векторы экспрессии, кодирующие антитело к CD38, вводят в отдельные клетки-хозяева. В других вариантах осуществления векторы экспрессии вводят в одну и ту же клетку-хозяина. Клетки-хозяева культивируют в условиях, подходящих для экспрессии антитела, которое затем собирают и выделяют. Клетки-хозяева включают клеток-хозяев, представляющих собой клетки млекопитающих, растений, бактерий или дрожжей. Линии клеток млекопитающих, доступные в качестве хозяев для экспрессии, хорошо известны в данной области техники и включают множество иммортализованных клеточных линий, доступных из Американской коллекции типовых культур (АТСС). К ним относятся, среди прочего, клетки яичника китайского хомячка (CHO), клетки NS0, клетки SP2, клетки HEK-293T, клетки 293 Freestyle (Invitrogen), клетки NIH-3T3, клетки HeLa, клетки почки новорожденного хомячка (BHK), клетки почки африканской зеленой мартышки (COS), клетки гепатоцеллюлярной карциномы человека (например, Hep G2), клетки A549 и целый ряд других клеточных линий. Клеточные линии могут быть выбраны на основе их уровней экспрессии. Другими клеточными линиями, которые можно использовать, являются линии клеток насекомых, такие как клетки Sf9 или Sf21.
[0141] Кроме того, экспрессию антител можно усилить с использованием целого ряда известных методик. Например, система для экспрессии гена глутаминсинтетазы (система GS) является общепринятым подходом для усиления экспрессии в определенных условиях.
[0142] Среда для культивирования тканей, предназначенная для клеток-хозяев, может содержать или не содержать компоненты животного происхождения (ADC), такие как бычий сывороточный альбумин. В некоторых вариантах осуществления для безопасности человека предпочтительны среды для культивирования без ADC. Культивирование ткани можно выполнять с использованием способа периодического культивирования с подпиткой, способа непрерывной перфузии или любого другого способа, подходящего для клеток-хозяев и требуемого выхода продукта.
[0143] В некоторых вариантах осуществления настоящее изобретение относится к способу получения композиции на основе антител, содержащей антитело к TGF-β или его антигенсвязывающий фрагмент и антитело к CD38 или его антигенсвязывающий фрагмент, при этом способ предусматривает:
- обеспечение первой и второй клеток-хозяев, где первая клетка-хозяин способна экспрессировать антитело к TGF-β или его антигенсвязывающий фрагмент, описанные в данном документе, а вторая клетка-хозяин способна экспрессировать антитело к CD38 или его антигенсвязывающий фрагмент, описанные в данном документе,
- культивирование первой и второй клеток-хозяев в условиях, подходящих для экспрессии антитела к TGF-β или его антигенсвязывающего фрагмента и антитела к CD38 или его антигенсвязывающего фрагмента,
- выделение полученных антител или антигенсвязывающих фрагментов, и
- необязательно объединение антител или антигенсвязывающих фрагментов с получением композиции на основе антител.
Фармацевтические композиции
[0144] Другой аспект настоящего изобретения представляет собой фармацевтические композиции, содержащие в качестве активных ингредиентов (например, в качестве единственных активных ингредиентов) средство, которое специфически связывается с TGF-β человека (например, антитело к TGF-β или его антигенсвязывающий фрагмент), и средство, которое специфически связывается с CD38 человека (например, антитело к CD38 или его антигенсвязывающий фрагмент). Средство, которое специфически связывается с TGF-β, и средство, которое специфически связывается с CD38, могут быть составлены вместе, например, смешаны и обеспечены в одной композиции. В настоящем изобретении также представлены: (1) фармацевтическая композиция, содержащая средство, которое специфически связывается с TGF-β человека, и (2) фармацевтическая композиция, содержащая средство, которое специфически связывается с CD38 человека, где фармацевтические композиции применяться в одной и той же комбинированной терапии.
[0145] В некоторых вариантах осуществления фармацевтические композиции, описанные в данном документе, когда вводятся в комбинированной терапии по настоящему изобретению, предназначены для лечения (например, уменьшения интенсивности и/или предупреждения) нарушения, заболевания или состояния, которое улучшает или замедляет его прогрессирование путем модуляции активности или экспрессии TGF-β и CD38. В некоторых вариантах осуществления фармацевтические композиции предназначены для лечения (например, уменьшения интенсивности и/или предупреждения) рака. В конкретных вариантах осуществления рак представляет собой множественную миелому.
[0146] В некоторых вариантах осуществления фармацевтическая композиция по настоящему изобретению содержит антитело к TGF-β, описанное в данном документе, в котором полуантитело составляет менее 1%. Образование полуантител можно определить путем анализа чистоты препаратов моноклональных антител с использованием, например, капиллярного электрофореза в присутствии SDS в невосстанавливающих условиях, или анализа методом SDS-PAGE в невосстанавливающих условиях с последующей денситометрией, или RP-HPLC (Angal et al., Mol Immunol 30(1):105-8 (1993); Bloom et al., Protein Science 6:407-415 (1997); Schuurman et al., 38(1):1-8 (2001); и Solanos et al., Anal Chem 78:6583-94 (2006)).
[0147] В целом, фармацевтические композиции, описанные в данном документе, подходят для введения в виде состава в сочетании с одним или несколькими фармацевтически приемлемыми вспомогательными веществами, например, описанными ниже.
[0148] Термин "вспомогательное вещество" или "носитель" используется в данном документе для описания любого ингредиента, отличного от соединения(-ий) по настоящему изобретению. Выбор вспомогательных веществ в значительной степени будет зависеть от таких факторов, как конкретный способ введения, влияние наполнителя на растворимость и стабильность и природа лекарственной формы. "Фармацевтически приемлемое вспомогательное вещество" включает все без исключения растворители, дисперсионные среды, покрытия, антибактериальные и противогрибковые средства, изотонические и замедляющие абсорбцию средства и т.п., которые являются физиологически совместимыми. Некоторыми примерами фармацевтически приемлемых вспомогательных веществ являются вода, солевой раствор, фосфатно-солевой буферный раствор, декстроза, глицерин, этанол и т.п., а также их комбинации. В некоторых случаях в композицию будут включены изотонические средства, например, сахара, многоатомные спирты, такие как маннит, сорбит, или хлорид натрия. Дополнительными примерами фармацевтически приемлемых веществ являются смачивающие средства или незначительные количества вспомогательных веществ, таких как смачивающие или эмульгирующие средства, консерванты или буферы, которые повышают срок хранения или эффективность антитела. В некоторых вариантах осуществления фармацевтическая композиция по настоящему изобретению может содержать гиалуронидазу (например, рекомбинантную гиалуронидазу человека). В определенных вариантах осуществления фармацевтическая композиция, содержащая гиалуронидазу, может быть предназначена для подкожного введения.
[0149] Фармацевтическую композицию по настоящему изобретению можно получать, упаковывать или обеспечивать в нерасфасованном виде, в виде единичной стандартной дозы и/или в виде множества единичных стандартных доз. Используемая в данном документе "стандартная доза" представляет собой дискретное количество фармацевтической композиции, содержащее предварительно определенное количество активного(-ых) ингредиента(-ов). Количество каждого активного ингредиента обычно равно дозировке активного ингредиента, которая будет вводиться субъекту, или подходящей доле такой дозировки, такой как, например, половина или одна треть такой дозировки.
[0150] Фармацевтические композиции по настоящему изобретению, как правило, подходят для парентерального введения. Используемый в данном документе термин "парентеральное введение" фармацевтической композиции включает любой путь введения, характеризующийся физическим проделыванием отверстия в ткани субъекта и введением фармацевтической композиции через отверстие в ткани, что, обычно, приводит к непосредственному введению в кровоток, в мышцу или во внутренний орган. Таким образом, парентеральное введение включает без ограничения введение фармацевтической композиции посредством инъекции композиции, посредством нанесения композиции через хирургический разрез, посредством нанесения композиции через проникающую в ткань нехирургическую рану и т.п. В частности, предполагается, что парентеральное введение включает без ограничения подкожную, внутрибрюшинную, внутримышечную, внутригрудинную, внутривенную, внутриартериальную, интратекальную, внутрижелудочковую, интрауретральную, внутричерепную, внутриопухолевую и внутрисуставную инъекцию или инфузию; а также методики диализной инфузии в почки. Также предполагается регионарная перфузия. Предпочтительные варианты осуществления могут включать внутривенные и подкожные пути введения.
[0151] Составы на основе фармацевтической композиции, подходящие для парентерального введения, как правило, содержат активный(-ые) ингредиент(-ы) в комбинации с фармацевтически приемлемым носителем, таким как стерильная вода или стерильный изотонический солевой раствор. Такие составы можно получать, упаковывать или обеспечивать в форме, подходящей для болюсного введения или для непрерывного введения. Инъекционные составы можно получать, упаковывать или обеспечивать в стандартной лекарственной форме, такой как ампулы или многодозовые контейнеры, содержащие консервант. Составы для парентерального введения включают без ограничения суспензии, растворы, эмульсии в масляных или водных средах-носителях, пасты и т.п. Такие составы могут дополнительно содержать один или несколько дополнительных ингредиентов, включая без ограничения суспендирующие, стабилизирующие или диспергирующие средства. В одном варианте осуществления состава для парентерального введения активный(-ые) ингредиент(-ы) обеспечивается(-ются) в сухой (т.е. порошкообразной или гранулированной) форме для разбавления подходящей средой-носителем (например, стерильной апирогенной водой) перед парентеральным введением разбавленной композиции. Составы для парентерального введения также включают водные растворы, которые могут содержать вспомогательные вещества, такие как соли, углеводы и буферные средства (например, с рН от 3 до 9), но для некоторых способов применения для большего удобства их можно составлять в виде стерильного неводного раствора или в виде высушенной (например, лиофилизированной) формы для применения в сочетании с подходящей средой-носителем, такой как стерильная апирогенная вода. Иллюстративные формы для парентерального введения включают растворы или суспензии в стерильных водных растворах, например, водных растворах пропиленгликоля или декстрозы. При необходимости для удобства такие лекарственные формы могут содержать буферные растворы. Другие составы для парентерального введения, которые являются применимыми, включают составы, которые содержат активный(-ые) ингредиент(-ы) в микрокристаллической форме или в виде липосомного препарата. Составы для парентерального введения можно составлять для немедленного и/или модифицированного высвобождения. Составы с модифицированным высвобождением включают составы с отсроченным, замедленным, прерывистым, контролируемым, направленным и запрограммированным высвобождением.
Готовые изделия и наборы
[0152] В настоящем описании также представлены готовые изделия, содержащие средство, которое специфически связывается с TGF-β человека, и средство, которое специфически связывается с CD38 человека. В некоторых вариантах осуществления готовое изделие по настоящему изобретению содержит антитело к TGF-β или его антигенсвязывающий фрагмент, описанные в данном документе, и антитело к CD38 или его антигенсвязывающий фрагмент, описанные в данном документе. В некоторых вариантах осуществления готовое изделие содержит Ab1 и Ab2. В настоящем изобретение дополнительно представлены способы изготовления указанных изделий.
[0153] В настоящем изобретении также представлены наборы, содержащие средство, которое специфически связывается с TGF-β человека, и средство, которое специфически связывается с CD38 человека, а также инструкции по применению данных средств в комбинации. В некоторых вариантах осуществления набор по настоящему изобретению содержит антитело к TGF-β или его антигенсвязывающий фрагмент, описанные в данном документе, и антитело к CD38 или его антигенсвязывающий фрагмент, описанные в данном документе. В некоторых вариантах осуществления набор содержит Ab1 и Ab2.
[0154] Если в данном документе не определено иное, научные и технические термины, используемые в контексте настоящего изобретения, должны иметь значения, которые общеизвестны средним специалистам в данной области техники. Иллюстративные способы и материалы описаны ниже, хотя при практическом осуществлении или при тестировании настоящего изобретения также можно применять способы и материалы, аналогичные или эквивалентные описанным в данном документе. В случае противоречий настоящее описание, включая определения, будет иметь преимущественную силу.
[0155] Как правило, используемая номенклатура, связанная с культивированием клеток и тканей, молекулярной биологией, иммунологией, микробиологией, генетикой, аналитической химией, синтетической органической химией, медицинской и фармацевтической химией и химией и гибридизацией белков и нуклеиновых кислот, а также соответствующие методики, описанные в данном документе, являются общеизвестными и широко используемыми в данной области техники. Ферментативные реакции и методики очистки выполняют в соответствии с описаниями производителя, как обычно осуществляется в данной области техники или как описано в данном документе.
[0156] Кроме того, если иное не требуется по контексту, термины в единственном числе включают множественное число, а термины во множественном числе включают единственное число. На протяжении всего настоящего описания и вариантов осуществления слова "иметь" и "содержать" или их варианты, такие как "имеет", "имеющий", "содержит" или "содержащий", следует понимать как подразумевающие включение указанного целого числа или группы целых чисел, но не исключение любого другого целого числа или группы целых чисел.
[0157] Все публикации и другие литературные источники, упомянутые в данном документе, включены посредством ссылки во всей своей полноте. Хотя в данном документе цитируется ряд документов, данное цитирование не является признанием того, что любой из этих документов образует часть общеизвестных знаний в данной области техники.
ПРИМЕРЫ
[0158] Для лучшего понимания настоящего изобретения приведены следующие примеры. Эти примеры приведены только для иллюстрации и не должны истолковываться как ограничивающие каким-либо образом объем настоящего изобретения.
Пример 1. Высвобождение TGF- β линиями клеток множественной миеломы и лимфомы
[0159] Клетки JJN3, NCI-H929, RPMI8226, LP1, MOLP8, SUDHL-4, DAUDI, OCI-LY19 и SUDHL8 культивировали в RPMI 1640 (Invitrogen, № по каталогу 22400-089), дополненной 10% фетальной телячьей сывороткой (Invitrogen, № по каталогу 10082-147).
[0160] Для количественной оценки TGF-β, высвобождаемого линиями клеток MM и лимфомы, 1×106 клеток каждой клеточной линии высевали в один 96-луночный обработанный для выращивания тканевой культуры планшет в объеме 100 мкл RPMI, дополненной 10% фетальной телячьей сывороткой. Клетки инкубировали при 37°C в течение 1 дня, 2 дней или 3 дней в инкубаторе с увлажнением при 37°C, содержащем 5% CO2. После центрифугирования в течение 5 минут при 250 g собирали по 40 мкл супернатанта из каждой лунки и определяли уровень общего человеческого TGF-β с использованием набора для анализа TGF-β1 человека MSD с 96-луночным планшетом MULTI-ARRAY (Meso Scale Discovery, № по каталогу K151IUC-1) в соответствии с инструкциями производителя. Вкратце, образцы активировали обработкой кислотой, а впоследствии нейтрализовали с последующей инкубацией с захватывающим антителом. Затем антитело подвергали обнаружению методом ELISA, а результаты считывали на приборе для визуализации MSD SECTOR.
[0161] Обнаружили, что общий TGF-β в супернатантах всех линий клеток MM и лимфомы находится на уровнях, превышающих 500 пг/мл, и в большинстве клеточных линий, особенно в клетках JJN3, RPMI8226 и MOLP8 наблюдалось накопление с течением времени (фиг. 1).
Пример 2. Снижение TGF- β цитолитической активности человеческих NK-клеток, а также снижение Ab2-опосредованной ADCC
[0162] Клетки NK92V в логарифмической фазе роста (NK92-05 CD16 V/V; Conkwest) суспендировали в среде для роста (Middle MyeloCult H5100 (Stemcell Technologies, № по каталогу 05150), дополненной 100 единицами/мл человеческого интерлейкина-2 (R&D, № по каталогу 202-IL-010/CF)), и высевали в чашки диаметром 10 см при плотности 0,8×105 клеток на мл. Клетки обрабатывали рекомбинантным человеческим TGF-β в конечной концентрации 10 нг/мл в течение ночи, 24 часов, 48 часов или 72 часов при 37°C.
[0163] Клетки MOLP8 культивировали в RPMI 1640 (Invitrogen, № по каталогу 22400-089), дополненной 20% фетальной телячьей сывороткой (Invitrogen, № по каталогу 10082-147).
[0164] Меченные кальцеином (AM) (Invitrogen, № по каталогу C3100MP) клетки-мишени MOLP8 и эффекторные клетки NK92V высевали в 96-луночные планшеты при плотности 4×104 клеток-мишеней (MOLP8) и 1,2×105 эффекторных клеток (NK92V) на лунку. Клетки обрабатывали Ab2 в концентрации 0, 0,001, 0,1 или 1 мкг/мл или контрольным IgG1 (данные не показаны) в течение 1 часа при 37°C. Флуоресценцию высвобожденного из лизированных клеток-мишеней кальцеина в супернатантах измеряли с использованием многорежимного планшет-ридера (Envision). Интенсивность сигнала флуоресценции являлась прямо пропорциональной количеству лизированных клеток-мишеней.
[0165] Инкубация человеческих NK-клеток с TGF-β в течение периода вплоть до 72 часов приводила к зависимому от времени снижению Ab2-опосредованной ADCC (E:T=3:1). В то время как NK-клетки, инкубированные с TGF-β в течение 24 часов, сохраняли свою литическую активность, лизис посредством NK-клеток, инкубируемых в течение 48 или 72 часов, снижался на примерно 25-60% (фиг. 2).
Пример 3. Нейтрализация TGF- β восстанавливает цитолитическую активность NK и Ab2-опосредованную ADCC
[0166] Клетки NK92V в логарифмической фазе роста (NK92-05 CD16 V/V; Conkwest) суспендировали в среде для роста (Middle MyeloCult H5100 (Stemcell Technologies, № по каталогу 05150), дополненной 100 единицами/мл человеческого интерлейкина-2 (R&D, № по каталогу 202-IL-010/CF)), и высевали в чашки диаметром 10 см при плотности 0,8×105 клеток на мл. Клетки обрабатывали рекомбинантным человеческим TGF-β в конечной концентрации 10 нг/мл и 1D11 (мышиный суррогат Ab1) или антителом изотипического контроля (13C4; данные не показаны) в конечной концентрации 50 мкг/мл в течение 90 часов при 37°C.
[0167] Меченные кальцеином (AM) (Invitrogen, № по каталогу C3100MP) клетки-мишени MOLP8 и эффекторные клетки NK92V высевали в 96-луночные планшеты при плотности 4×104 клеток-мишеней (MOLP8) и 1,2×105 эффекторных клеток (NK92V) на лунку. Клетки обрабатывали Ab2 при 0, 0,001, 0,01, 0,1 или 1 мкг/мл или контрольным IgG1 при 1 мкг/мл в течение 1 часа при 37°C. Флуоресценцию высвобожденного из лизированных клеток-мишеней кальцеина в супернатантах измеряли с использованием многорежимного планшет-ридера (Envision). Интенсивность сигнала флуоресценции являлась прямо пропорциональной количеству лизированных клеток-мишеней.
[0168] Уровни литической активности NK-клеток и Ab2-опосредованной ADCC, снижение которых индуцировал TGF-β, полностью восстанавливались, когда TGF-β подвергали нейтрализации с помощью Ab1, но не контрольного антитела (фиг. 3).
Пример 4. Подавление TGF- β Ab2-опосредованной ADCC клеток NCI-H929 и блокирование Ab1 этого подавления
[0169] Человеческие NK-клетки выделяли с помощью отрицательной селекции из организма здоровых людей-доноров (Stem Cell Technologies). Обогащенные NK-клетки культивировали в присутствии IL-2 (при 100 МЕ/мл), TGF-β (как указано) и/или Ab1 или изотипического контроля в течение 3 дней при 37°C в инкубаторе с увлажнением. На этом этапе экспоненциально растущие клетки NCI-H929 метили кальцеином (AM) и инкубировали с Ab2 при 1 мкг/мл в течение 30 минут. Затем эффекторные NK-клетки ресуспендировали и объединяли с мечеными клетками-мишенями NCI-H929 в течение 1 часа в инкубаторе с увлажнением. Ab2-опосредованную ADCC определяли количественно путем измерения уровней клеток-мишеней, меченных кальцеином (AM), с использованием спектрофотометра. Показано, что возрастающие дозы TGF-β подавляют способность нормальных человеческих NK-клеток уничтожать предварительно обработанные с помощью Ab2 клетки NCI-H929 с оказанием незначительного эффекта в отношении лизиса клеток, опосредованного NK-клетками, при 0,1 нг/мл, но с блокированием ADCC при 1 и 10 нг/мл на примерно 50% (фиг. 4). Затем ADCC оценивали при 2 различных концентрациях Ab1 (100 и 200 мкг/мл). Ни Ab изотипического контроля (IgG4), ни Ab1 не оказывали какого-либо эффекта в отношении ADCC при добавлении в культуры в отсутствие TGF-β (фиг. 5 и 6). Было показано, что Ab1 блокирует способность TGF-β подавлять ADCC (фиг. 5 и 6, p<0,005 по сравнению с необработанными), в то время как контроль IgG4 не продемонстрировал способность блокировать эффекты TGF-β в той же степени. Таким образом, эти данные демонстрируют, что Ab1 способно ослаблять иммуносупрессорные эффекты TGF-β в отношении опосредованной NK-клетками ADCC.
Пример 5. Нейтрализация эндогенного TGF- β с помощью Ab1 восстанавливает первичную цитолитическую активность NK и Ab2-опосредованную ADCC
[0170] Клетки JJN3, K562 и RPMI8226 культивировали в RPMI 1640 (Invitrogen, № по каталогу 22400-089), дополненной 10% фетальной телячьей сывороткой (Invitrogen, № по каталогу 10082-147).
[0171] Первичные человеческие NK-клетки выделяли путем отрицательной селекции из нормальных человеческих PBMC в соответствии с протоколами, предложенными производителем (StemCell Technologies, номер по каталогу 17955RF). Выделенные NK-клетки либо культивировали отдельно, либо совместно культивировали в присутствии клеток JJN3 в 6-луночных планшетах с трансвел-вкладышами в присутствии или в отсутствие 100 мг/мл Ab1 или изотипического контроля в течение 90 часов при 37°C в инкубаторе с 5% CO2.
[0172] После 90 часов совместного культивирования NK-клетки из планшетов с трансвел-вкладышами инкубировали либо с клетками K562, меченными кальцеином (AM) (Invitrogen, № по каталогу C3100MP), в течение 2 часов при 37°C для определения цитолитической функции NK-клеток, либо с меченными кальцеином (AM) RPMI8226 в присутствии 0,001 или 0,1 мг/мл Ab2 или 0,1 мг/мл контрольного мутантного Ab2 (Ab*) в течение 1 часа при 37°C для обнаружения Ab2-опосредованной ADCC. Флуоресценцию высвобожденного из лизированных клеток-мишеней кальцеина в супернатантах измеряли с использованием многорежимного планшет-ридера (Envision). Интенсивность сигнала флуоресценции являлась прямо пропорциональной количеству лизированных клеток-мишеней.
[0173] Повышенная цитолитическая активность первичных NK-клеток (фиг. 7) и повышенная Ab2-опосредованная ADCC (фиг. 8) демонстрируют, что присутствие Ab1 нейтрализовало высвобождаемый клетками JJN3 эндогенный TGFβ во время 90-часового совместного культивирования.
Пример 6. Комбинированное лечение с помощью Ab1 и Ab2 для пациентов с множественной миеломой
[0174] Эффект комбинированного лечения с помощью антител Ab1 и Ab2 можно дополнительно оценивать у пациентов-людей, например у пациентов с множественной миеломой, резистентных к одному или нескольким другим видам лечения, нацеливающегося на CD38 (например, изатуксимаб или даратумумаб). Пациенты с множественной миеломой могут, например, не отвечать на другое лечение, нацеливающееся на CD38, или демонстрировать прогрессирование в ходе прохождения другого вида лечения, нацеливающегося на CD38.
[0175] Ожидается, что посредством комбинации Ab1 и Ab2 будет достигнуто более эффективное лечение множественной миеломы по сравнению с лечением с помощью Ab2 отдельно. Например, комбинированное лечение может приводить к ослаблению симптомов, уменьшению разрушения кости, усиленному образованию кости, приводящему к ремоделированию кости и/или заживлению кости, задержке прогрессирования или возникновения рецидива рака или увеличению продолжительности жизни по сравнению с лечением с помощью Ab2 отдельно.
[0176] Ab1 и Ab2 можно вводить в дозах (например, 1-20 мг/кг), используя схемы введения доз (например, каждые одну, две, три или четыре недели) и в течение периодов времени, которые необходимы для достижения желаемого результата, например, как определено врачом. В некоторых вариантах осуществления любое одно или оба антитела можно вводить посредством внутривенной инфузии. В некоторых вариантах осуществления Ab2 вводят в дозе 10 мг/кг или 16 мг/кг фактической массы тела каждые одну, две, три или четыре недели или при любой их комбинации в течение курса лечения.
--->
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
SEQ ID NO: 1 (тяжелая цепь Ab1)
QVQLVQSGAE VKKPGSSVKV SCKASGYTFS SNVISWVRQA PGQGLEWMGG VIPIVDIANY
AQRFKGRVTI TADESTSTTY MELSSLRSED TAVYYCASTL GLVLDAMDYW GQGTLVTVSS
ASTKGPSVFP LAPCSRSTSE STAALGCLVK DYFPEPVTVS WNSGALTSGV HTFPAVLQSS
GLYSLSSVVT VPSSSLGTKT YTCNVDHKPS NTKVDKRVES KYGPPCPPCP APEFLGGPSV
FLFPPKPKDT LMISRTPEVT CVVVDVSQED PEVQFNWYVD GVEVHNAKTK PREEQFNSTY
RVVSVLTVLH QDWLNGKEYK CKVSNKGLPS SIEKTISKAK GQPREPQVYT LPPSQEEMTK
NQVSLTCLVK GFYPSDIAVE WESNGQPENN YKTTPPVLDS DGSFFLYSRL TVDKSRWQEG
NVFSCSVMHE ALHNHYTQKS LSLSLGK
SEQ ID NO: 2 (легкая цепь Ab1)
ETVLTQSPGT LSLSPGERAT LSCRASQSLG SSYLAWYQQK PGQAPRLLIY GASSRAPGIP
DRFSGSGSGT DFTLTISRLE PEDFAVYYCQ QYADSPITFG QGTRLEIKRT VAAPSVFIFP
PSDEQLKSGT ASVVCLLNNF YPREAKVQWK VDNALQSGNS QESVTEQDSK DSTYSLSSTL
TLSKADYEKH KVYACEVTHQ GLSSPVTKSF NRGEC
SEQ ID NO: 3 (вариабельный домен тяжелой цепи Ab1)
QVQLVQSGAE VKKPGSSVKV SCKASGYTFS SNVISWVRQA PGQGLEWMGG VIPIVDIANY
AQRFKGRVTI TADESTSTTY MELSSLRSED TAVYYCASTL GLVLDAMDYW GQGTLVTVSS
SEQ ID NO: 4 (вариабельный домен легкой цепи Ab1)
ETVLTQSPGT LSLSPGERAT LSCRASQSLG SSYLAWYQQK PGQAPRLLIY GASSRAPGIP
DRFSGSGSGT DFTLTISRLE PEDFAVYYCQ QYADSPITFG QGTRLEIK
SEQ ID NO: 5 (CDR1 тяжелой цепи Ab1)
SNVIS
SEQ ID NO: 6 (CDR2 тяжелой цепи Ab1)
GVIPIVDIAN Y
SEQ ID NO: 7 (CDR3 тяжелой цепи Ab1)
TLGLVLDAMD Y
SEQ ID NO: 8 (CDR1 легкой цепи Ab1)
RASQSLGSSY LA
SEQ ID NO: 9 (CDR2 легкой цепи Ab1)
GASSRAP
SEQ ID NO: 10 (CDR3 легкой цепи Ab1)
QQYADSPIT
SEQ ID NO: 11 (тяжелая цепь Ab2)
QVQLVQSGAE VAKPGTSVKL SCKASGYTFT DYWMQWVKQR PGQGLEWIGT IYPGDGDTGY
AQKFQGKATL TADKSSKTVY MHLSSLASED SAVYYCARGD YYGSNSLDYW GQGTSVTVSS
ASTKGPSVFP LAPSSKSTSG GTAALGCLVK DYFPEPVTVS WNSGALTSGV HTFPAVLQSS
GLYSLSSVVT VPSSSLGTQT YICNVNHKPS NTKVDKKVEP KSCDKTHTCP PCPAPELLGG
PSVFLFPPKP KDTLMISRTP EVTCVVVDVS HEDPEVKFNW YVDGVEVHNA KTKPREEQYN
STYRVVSVLT VLHQDWLNGK EYKCKVSNKA LPAPIEKTIS KAKGQPREPQ VYTLPPSRDE
LTKNQVSLTC LVKGFYPSDI AVEWESNGQP ENNYKTTPPV LDSDGSFFLY SKLTVDKSRW
QQGNVFSCSV MHEALHNHYT QKSLSLSPGK
SEQ ID NO: 12 (легкая цепь Ab2)
DIVMTQSHLS MSTSLGDPVS ITCKASQDVS TVVAWYQQKP GQSPRRLIYS ASYRYIGVPD
RFTGSGAGTD FTFTISSVQA EDLAVYYCQQ HYSPPYTFGG GTKLEIKRTV AAPSVFIFPP
SDEQLKSGTA SVVCLLNNFY PREAKVQWKV DNALQSGNSQ ESVTEQDSKD STYSLSSTLT
LSKADYEKHK VYACEVTHQG LSSPVTKSFN RGEC
SEQ ID NO: 13 (вариабельный домен тяжелой цепи Ab2)
QVQLVQSGAE VAKPGTSVKL SCKASGYTFT DYWMQWVKQR PGQGLEWIGT IYPGDGDTGY
AQKFQGKATL TADKSSKTVY MHLSSLASED SAVYYCARGD YYGSNSLDYW GQGTSVTVSS
SEQ ID NO: 14 (вариабельный домен легкой цепи Ab2)
DIVMTQSHLS MSTSLGDPVS ITCKASQDVS TVVAWYQQKP GQSPRRLIYS ASYRYIGVPD
RFTGSGAGTD FTFTISSVQA EDLAVYYCQQ HYSPPYTFGG GTKLEIK
SEQ ID NO: 15 (CDR1 тяжелой цепи Ab2)
DYWMQ
SEQ ID NO: 16 (CDR2 тяжелой цепи Ab2)
TIYPGDGDTG YAQKFQG
SEQ ID NO: 17 (CDR3 тяжелой цепи Ab2)
GDYYGSNSLD Y
SEQ ID NO: 18 (CDR1 легкой цепи Ab2)
KASQDVSTVV A
SEQ ID NO: 19 (CDR2 легкой цепи Ab2)
SASYRYI
SEQ ID NO: 20 (CDR3 легкой цепи Ab2)
QQHYSPPYT
SEQ ID NO: 21 (TGF-β1 человека): SwissProt P01137
MPPSGLRLLL LLLPLLWLLV LTPGRPAAGL STCKTIDMEL VKRKRIEAIR GQILSKLRLA
SPPSQGEVPP GPLPEAVLAL YNSTRDRVAG ESAEPEPEPE ADYYAKEVTR VLMVETHNEI
YDKFKQSTHS IYMFFNTSEL REAVPEPVLL SRAELRLLRL KLKVEQHVEL YQKYSNNSWR
YLSNRLLAPS DSPEWLSFDV TGVVRQWLSR GGEIEGFRLS AHCSCDSRDN TLQVDINGFT
TGRRGDLATI HGMNRPFLLL MATPLERAQH LQSSRHRRAL DTNYCFSSTE KNCCVRQLYI
DFRKDLGWKW IHEPKGYHAN FCLGPCPYIW SLDTQYSKVL ALYNQHNPGA SAAPCCVPQA
LEPLPIVYYV GRKPKVEQLS NMIVRSCKCS
SEQ ID NO: 22 (TGF-β2 человека): SwissProt P08112
MHYCVLSAFL ILHLVTVALS LSTCSTLDMD QFMRKRIEAI RGQILSKLKL TSPPEDYPEP
EEVPPEVISI YNSTRDLLQE KASRRAAACE RERSDEEYYA KEVYKIDMPP FFPSENAIPP
TFYRPYFRIV RFDVSAMEKN ASNLVKAEFR VFRLQNPKAR VPEQRIELYQ ILKSKDLTSP
TQRYIDSKVV KTRAEGEWLS FDVTDAVHEW LHHKDRNLGF KISLHCPCCT FVPSNNYIIP
NKSEELEARF AGIDGTSTYT SGDQKTIKST RKKNSGKTPH LLLMLLPSYR LESQQTNRRK
KRALDAAYCF RNVQDNCCLR PLYIDFKRDL GWKWIHEPKG YNANFCAGAC PYLWSSDTQH
SRVLSLYNTI NPEASASPCC VSQDLEPLTI LYYIGKTPKI EQLSNMIVKS CKCS
SEQ ID NO: 23 (TGF-β3 человека): SwissProt P10600
MKMHLQRALV VLALLNFATV SLSLSTCTTL DFGHIKKKRV EAIRGQILSK LRLTSPPEPT
VMTHVPYQVL ALYNSTRELL EEMHGEREEG CTQENTESEY YAKEIHKFDM IQGLAEHNEL
AVCPKGITSK VFRFNVSSVE KNRTNLFRAE FRVLRVPNPS SKRNEQRIEL FQILRPDEHI
AKQRYIGGKN LPTRGTAEWL SFDVTDTVRE WLLRRESNLG LEISIHCPCH TFQPNGDILE
NIHEVMEIKF KGVDNEDDHG RGDLGRLKKQ KDHHNPHLIL MMIPPHRLDN PGQGGQRKKR
ALDTNYCFRN LEENCCVRPL YIDFRQDLGW KWVHEPKGYY ANFCSGPCPY LRSADTTHST
VLGLYNTLNP EASASPCCVP QDLEPLTILY YVGRTPKVEQ LSNMVVKSCK CS
SEQ ID NO: 24 (CD38 человека): GenBank NP_001766
MANCEFSPVS GDKPCCRLSR RAQLCLGVSI LVLILVVVLA VVVPRWRQQW SGPGTTKRFP
ETVLARCVKY TEIHPEMRHV DCQSVWDAFK GAFISKHPCN ITEEDYQPLM KLGTQTVPCN
KILLWSRIKD LAHQFTQVQR DMFTLEDTLL GYLADDLTWC GEFNTSKINY QSCPDWRKDC
SNNPVSVFWK TVSRRFAEAA CDVVHVMLNG SRSKIFDKNS TFGSVEVHNL QPEKVQTLEA
WVIHGGREDS RDLCQDPTIK ELESIISKRN IQFSCKNIYRPDKFLQCVKN PEDSSCTSEI
SEQ ID NO: 25 (тяжелая цепь Ab3)
QVQLVQSGAE VVKPGASVKV SCKASGYTFT SYAMHWVKEA PGQRLEWIGY IYPGQGGTNY
NQKFQGRATL TADTSASTAY MELSSLRSED TAVYFCARTG GLRRAYFTYW GQGTLVTVSS
ASTKGPSVFP LAPSSKSTSG GTAALGCLVK DYFPEPVTVS WNSGALTSGV HTFPAVLQSS
GLYSLSSVVT VPSSSLGTQT YICNVNHKPS NTKVDKKVEP KSCDKTHTCP PCPAPELLAG
PDVFLFPPKP KDTLMISRTP EVTCVVVDVS HEDPEVKFNW YVDGVEVHNA KTKPREEQYN
STYRVVSVLT VLHQDWLNGK EYKCKVSNKA LPLPEEKTIS KAKGQPREPQ VYTLPPSRDE
LTKNQVSLTC LVKGFYPSDI AVEWESNGQP ENNYKTTPPV LDSDGSFFLY SKLTVDKSRW
QQGNVFSCSV MHEALHNHYT QKSLSLSPG
SEQ ID NO: 26 (легкая цепь Ab3)
DIVLTQSPAT LSLSPGERAT ISCRASQSVS SYGQGFMHWY QQKPGQPPRL LIYGASSRAT
GIPARFSGSG SGTDFTLTIS PLEPEDFAVY YCQQNKEDPW TFGGGTKLEI KRTVAAPSVF
IFPPSDEQLK SGTASVVCLL NNFYPREAKV QWKVDNALQS GNSQESVTEQ DSKDSTYSLS
STLTLSKADY EKHKVYACEV THQGLSSPVT KSFNRGEC
SEQ ID NO: 27 (вариабельный домен тяжелой цепи Ab3)
QVQLVQSGAE VVKPGASVKV SCKASGYTFT SYAMHWVKEA PGQRLEWIGY IYPGQGGTNY
NQKFQGRATL TADTSASTAY MELSSLRSED TAVYFCARTG GLRRAYFTYW GQGTLVTVSS
SEQ ID NO: 28 (вариабельный домен легкой цепи Ab3)
DIVLTQSPAT LSLSPGERAT ISCRASQSVS SYGQGFMHWY QQKPGQPPRL LIYGASSRAT
GIPARFSGSG SGTDFTLTIS PLEPEDFAVY YCQQNKEDPW TFGGGTKLEI K
SEQ ID NO: 29 (CDR1 тяжелой цепи Ab3)
GYTFTSYA
SEQ ID NO: 30 (CDR2 тяжелой цепи Ab3)
IYPGQGGT
SEQ ID NO: 31 (CDR3 тяжелой цепи Ab3)
ARTGGLRRAY FTY
SEQ ID NO: 32 (CDR1 легкой цепи Ab3)
QSVSSYGQGF
SEQ ID NO: 33 (CDR2 легкой цепи Ab3)
GAS
SEQ ID NO: 34 (CDR3 легкой цепи Ab3)
QQNKEDPWT
SEQ ID NO: 35 (тяжелая цепь Ab4)
QVQLVESGGG VVQPGRSLRL SCAASGFTFS SYGMHWVRQA PGKGLEWVAV IWYDGSNKYY
ADSVKGRFTI SGDNSKNTLY LQMNSLRAED TAVYYCARMF RGAFDYWGQG TLVTVSSAST
KGPSVFPLAP SSKSTSGGTA ALGCLVKDYF PEPVTVSWNS GALTSGVHTF PAVLQSSGLY
SLSSVVTVPS SSLGTQTYIC NVNHKPSNTK VDKKVEPKSC DKTHTCPPCP APELLAGPDV
FLFPPKPKDT LMISRTPEVT CVVVDVSHED PEVKFNWYVD GVEVHNAKTK PREEQYNSTY
RVVSVLTVLH QDWLNGKEYK CKVSNKALPL PEEKTISKAK GQPREPQVYT LPPSRDELTK
NQVSLTCLVK GFYPSDIAVE WESNGQPENN YKTTPPVLDS DGSFFLYSKL TVDKSRWQQG
NVFSCSVMHE ALHNHYTQKS LSLSPG
SEQ ID NO: 36 (легкая цепь Ab4)
AIQMTQSPSS LSASVGDRVT ITCRASQGIR NDLGWYQQKP GKAPKLLIYA ASSLQSGVPS
RFSGSGSGTD FTLTISGLQP EDSATYYCLQ DYIYYPTFGQ GTKVEIKRTV AAPSVFIFPP
SDEQLKSGTA SVVCLLNNFY PREAKVQWKV DNALQSGNSQ ESVTEQDSKD STYSLSSTLT
LSKADYEKHK VYACEVTHQG LSSPVTKSFN RGEC
SEQ ID NO: 37 (вариабельный домен тяжелой цепи Ab4)
QVQLVESGGG VVQPGRSLRL SCAASGFTFS SYGMHWVRQA PGKGLEWVAV IWYDGSNKYY
ADSVKGRFTI SGDNSKNTLY LQMNSLRAED TAVYYCARMF RGAFDYWGQG TLVTVSS
SEQ ID NO: 38 (вариабельный домен легкой цепи Ab4)
AIQMTQSPSS LSASVGDRVT ITCRASQGIR NDLGWYQQKP GKAPKLLIYA ASSLQSGVPS
RFSGSGSGTD FTLTISGLQP EDSATYYCLQ DYIYYPTFGQ GTKVEIK
SEQ ID NO: 39 (CDR1 тяжелой цепи Ab4)
GFTFSSYG
SEQ ID NO: 40 (CDR2 тяжелой цепи Ab4)
IWYDGSNK
SEQ ID NO: 41 (CDR3 тяжелой цепи Ab4)
ARMFRGAFDY
SEQ ID NO: 42 (CDR1 легкой цепи Ab4)
QGIRND
SEQ ID NO: 43 (CDR2 легкой цепи Ab4)
AAS
SEQ ID NO: 44 (CDR3 легкой цепи Ab4)
LQDYIYYPT
ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
<110> САНОФИ
<120> ВИДЫ КОМБИНИРОВАННОЙ ТЕРАПИИ РАКА, НАЦЕЛИВАЮЩИЕСЯ НА CD38 И
TGF-БЕТА
<130> 022548.WO025
<140>
<141>
<150> 62/696,198
<151> 2018-07-10
<160> 44
<170> PatentIn версия 3.5
<210> 1
<211> 447
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 1
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Ser Asn
20 25 30
Val Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Val Ile Pro Ile Val Asp Ile Ala Asn Tyr Ala Gln Arg Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Thr Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Thr Leu Gly Leu Val Leu Asp Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
210 215 220
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly Lys
435 440 445
<210> 2
<211> 215
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 2
Glu Thr Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Leu Gly Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Pro Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Ala Asp Ser Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 3
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 3
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Ser Ser Asn
20 25 30
Val Ile Ser Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Val Ile Pro Ile Val Asp Ile Ala Asn Tyr Ala Gln Arg Phe
50 55 60
Lys Gly Arg Val Thr Ile Thr Ala Asp Glu Ser Thr Ser Thr Thr Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ser Thr Leu Gly Leu Val Leu Asp Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 4
<211> 108
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 4
Glu Thr Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Leu Gly Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Pro Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Ala Asp Ser Pro
85 90 95
Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105
<210> 5
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 5
Ser Asn Val Ile Ser
1 5
<210> 6
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 6
Gly Val Ile Pro Ile Val Asp Ile Ala Asn Tyr
1 5 10
<210> 7
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 7
Thr Leu Gly Leu Val Leu Asp Ala Met Asp Tyr
1 5 10
<210> 8
<211> 12
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 8
Arg Ala Ser Gln Ser Leu Gly Ser Ser Tyr Leu Ala
1 5 10
<210> 9
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 9
Gly Ala Ser Ser Arg Ala Pro
1 5
<210> 10
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 10
Gln Gln Tyr Ala Asp Ser Pro Ile Thr
1 5
<210> 11
<211> 450
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 11
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Ala Lys Pro Gly Thr
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Trp Met Gln Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Thr Ile Tyr Pro Gly Asp Gly Asp Thr Gly Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser Lys Thr Val Tyr
65 70 75 80
Met His Leu Ser Ser Leu Ala Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asp Tyr Tyr Gly Ser Asn Ser Leu Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Ser Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 12
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 12
Asp Ile Val Met Thr Gln Ser His Leu Ser Met Ser Thr Ser Leu Gly
1 5 10 15
Asp Pro Val Ser Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Thr Val
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Arg Arg Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Ile Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ala Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Val Gln Ala
65 70 75 80
Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln His Tyr Ser Pro Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 13
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 13
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Ala Lys Pro Gly Thr
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Trp Met Gln Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Thr Ile Tyr Pro Gly Asp Gly Asp Thr Gly Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Lys Ala Thr Leu Thr Ala Asp Lys Ser Ser Lys Thr Val Tyr
65 70 75 80
Met His Leu Ser Ser Leu Ala Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gly Asp Tyr Tyr Gly Ser Asn Ser Leu Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Ser Val Thr Val Ser Ser
115 120
<210> 14
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 14
Asp Ile Val Met Thr Gln Ser His Leu Ser Met Ser Thr Ser Leu Gly
1 5 10 15
Asp Pro Val Ser Ile Thr Cys Lys Ala Ser Gln Asp Val Ser Thr Val
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Arg Arg Leu Ile
35 40 45
Tyr Ser Ala Ser Tyr Arg Tyr Ile Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ala Gly Thr Asp Phe Thr Phe Thr Ile Ser Ser Val Gln Ala
65 70 75 80
Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln His Tyr Ser Pro Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 15
<211> 5
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 15
Asp Tyr Trp Met Gln
1 5
<210> 16
<211> 17
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 16
Thr Ile Tyr Pro Gly Asp Gly Asp Thr Gly Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 17
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 17
Gly Asp Tyr Tyr Gly Ser Asn Ser Leu Asp Tyr
1 5 10
<210> 18
<211> 11
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 18
Lys Ala Ser Gln Asp Val Ser Thr Val Val Ala
1 5 10
<210> 19
<211> 7
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 19
Ser Ala Ser Tyr Arg Tyr Ile
1 5
<210> 20
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 20
Gln Gln His Tyr Ser Pro Pro Tyr Thr
1 5
<210> 21
<211> 390
<212> БЕЛОК
<213> Homo sapiens
<400> 21
Met Pro Pro Ser Gly Leu Arg Leu Leu Leu Leu Leu Leu Pro Leu Leu
1 5 10 15
Trp Leu Leu Val Leu Thr Pro Gly Arg Pro Ala Ala Gly Leu Ser Thr
20 25 30
Cys Lys Thr Ile Asp Met Glu Leu Val Lys Arg Lys Arg Ile Glu Ala
35 40 45
Ile Arg Gly Gln Ile Leu Ser Lys Leu Arg Leu Ala Ser Pro Pro Ser
50 55 60
Gln Gly Glu Val Pro Pro Gly Pro Leu Pro Glu Ala Val Leu Ala Leu
65 70 75 80
Tyr Asn Ser Thr Arg Asp Arg Val Ala Gly Glu Ser Ala Glu Pro Glu
85 90 95
Pro Glu Pro Glu Ala Asp Tyr Tyr Ala Lys Glu Val Thr Arg Val Leu
100 105 110
Met Val Glu Thr His Asn Glu Ile Tyr Asp Lys Phe Lys Gln Ser Thr
115 120 125
His Ser Ile Tyr Met Phe Phe Asn Thr Ser Glu Leu Arg Glu Ala Val
130 135 140
Pro Glu Pro Val Leu Leu Ser Arg Ala Glu Leu Arg Leu Leu Arg Leu
145 150 155 160
Lys Leu Lys Val Glu Gln His Val Glu Leu Tyr Gln Lys Tyr Ser Asn
165 170 175
Asn Ser Trp Arg Tyr Leu Ser Asn Arg Leu Leu Ala Pro Ser Asp Ser
180 185 190
Pro Glu Trp Leu Ser Phe Asp Val Thr Gly Val Val Arg Gln Trp Leu
195 200 205
Ser Arg Gly Gly Glu Ile Glu Gly Phe Arg Leu Ser Ala His Cys Ser
210 215 220
Cys Asp Ser Arg Asp Asn Thr Leu Gln Val Asp Ile Asn Gly Phe Thr
225 230 235 240
Thr Gly Arg Arg Gly Asp Leu Ala Thr Ile His Gly Met Asn Arg Pro
245 250 255
Phe Leu Leu Leu Met Ala Thr Pro Leu Glu Arg Ala Gln His Leu Gln
260 265 270
Ser Ser Arg His Arg Arg Ala Leu Asp Thr Asn Tyr Cys Phe Ser Ser
275 280 285
Thr Glu Lys Asn Cys Cys Val Arg Gln Leu Tyr Ile Asp Phe Arg Lys
290 295 300
Asp Leu Gly Trp Lys Trp Ile His Glu Pro Lys Gly Tyr His Ala Asn
305 310 315 320
Phe Cys Leu Gly Pro Cys Pro Tyr Ile Trp Ser Leu Asp Thr Gln Tyr
325 330 335
Ser Lys Val Leu Ala Leu Tyr Asn Gln His Asn Pro Gly Ala Ser Ala
340 345 350
Ala Pro Cys Cys Val Pro Gln Ala Leu Glu Pro Leu Pro Ile Val Tyr
355 360 365
Tyr Val Gly Arg Lys Pro Lys Val Glu Gln Leu Ser Asn Met Ile Val
370 375 380
Arg Ser Cys Lys Cys Ser
385 390
<210> 22
<211> 414
<212> БЕЛОК
<213> Homo sapiens
<400> 22
Met His Tyr Cys Val Leu Ser Ala Phe Leu Ile Leu His Leu Val Thr
1 5 10 15
Val Ala Leu Ser Leu Ser Thr Cys Ser Thr Leu Asp Met Asp Gln Phe
20 25 30
Met Arg Lys Arg Ile Glu Ala Ile Arg Gly Gln Ile Leu Ser Lys Leu
35 40 45
Lys Leu Thr Ser Pro Pro Glu Asp Tyr Pro Glu Pro Glu Glu Val Pro
50 55 60
Pro Glu Val Ile Ser Ile Tyr Asn Ser Thr Arg Asp Leu Leu Gln Glu
65 70 75 80
Lys Ala Ser Arg Arg Ala Ala Ala Cys Glu Arg Glu Arg Ser Asp Glu
85 90 95
Glu Tyr Tyr Ala Lys Glu Val Tyr Lys Ile Asp Met Pro Pro Phe Phe
100 105 110
Pro Ser Glu Asn Ala Ile Pro Pro Thr Phe Tyr Arg Pro Tyr Phe Arg
115 120 125
Ile Val Arg Phe Asp Val Ser Ala Met Glu Lys Asn Ala Ser Asn Leu
130 135 140
Val Lys Ala Glu Phe Arg Val Phe Arg Leu Gln Asn Pro Lys Ala Arg
145 150 155 160
Val Pro Glu Gln Arg Ile Glu Leu Tyr Gln Ile Leu Lys Ser Lys Asp
165 170 175
Leu Thr Ser Pro Thr Gln Arg Tyr Ile Asp Ser Lys Val Val Lys Thr
180 185 190
Arg Ala Glu Gly Glu Trp Leu Ser Phe Asp Val Thr Asp Ala Val His
195 200 205
Glu Trp Leu His His Lys Asp Arg Asn Leu Gly Phe Lys Ile Ser Leu
210 215 220
His Cys Pro Cys Cys Thr Phe Val Pro Ser Asn Asn Tyr Ile Ile Pro
225 230 235 240
Asn Lys Ser Glu Glu Leu Glu Ala Arg Phe Ala Gly Ile Asp Gly Thr
245 250 255
Ser Thr Tyr Thr Ser Gly Asp Gln Lys Thr Ile Lys Ser Thr Arg Lys
260 265 270
Lys Asn Ser Gly Lys Thr Pro His Leu Leu Leu Met Leu Leu Pro Ser
275 280 285
Tyr Arg Leu Glu Ser Gln Gln Thr Asn Arg Arg Lys Lys Arg Ala Leu
290 295 300
Asp Ala Ala Tyr Cys Phe Arg Asn Val Gln Asp Asn Cys Cys Leu Arg
305 310 315 320
Pro Leu Tyr Ile Asp Phe Lys Arg Asp Leu Gly Trp Lys Trp Ile His
325 330 335
Glu Pro Lys Gly Tyr Asn Ala Asn Phe Cys Ala Gly Ala Cys Pro Tyr
340 345 350
Leu Trp Ser Ser Asp Thr Gln His Ser Arg Val Leu Ser Leu Tyr Asn
355 360 365
Thr Ile Asn Pro Glu Ala Ser Ala Ser Pro Cys Cys Val Ser Gln Asp
370 375 380
Leu Glu Pro Leu Thr Ile Leu Tyr Tyr Ile Gly Lys Thr Pro Lys Ile
385 390 395 400
Glu Gln Leu Ser Asn Met Ile Val Lys Ser Cys Lys Cys Ser
405 410
<210> 23
<211> 412
<212> БЕЛОК
<213> Homo sapiens
<400> 23
Met Lys Met His Leu Gln Arg Ala Leu Val Val Leu Ala Leu Leu Asn
1 5 10 15
Phe Ala Thr Val Ser Leu Ser Leu Ser Thr Cys Thr Thr Leu Asp Phe
20 25 30
Gly His Ile Lys Lys Lys Arg Val Glu Ala Ile Arg Gly Gln Ile Leu
35 40 45
Ser Lys Leu Arg Leu Thr Ser Pro Pro Glu Pro Thr Val Met Thr His
50 55 60
Val Pro Tyr Gln Val Leu Ala Leu Tyr Asn Ser Thr Arg Glu Leu Leu
65 70 75 80
Glu Glu Met His Gly Glu Arg Glu Glu Gly Cys Thr Gln Glu Asn Thr
85 90 95
Glu Ser Glu Tyr Tyr Ala Lys Glu Ile His Lys Phe Asp Met Ile Gln
100 105 110
Gly Leu Ala Glu His Asn Glu Leu Ala Val Cys Pro Lys Gly Ile Thr
115 120 125
Ser Lys Val Phe Arg Phe Asn Val Ser Ser Val Glu Lys Asn Arg Thr
130 135 140
Asn Leu Phe Arg Ala Glu Phe Arg Val Leu Arg Val Pro Asn Pro Ser
145 150 155 160
Ser Lys Arg Asn Glu Gln Arg Ile Glu Leu Phe Gln Ile Leu Arg Pro
165 170 175
Asp Glu His Ile Ala Lys Gln Arg Tyr Ile Gly Gly Lys Asn Leu Pro
180 185 190
Thr Arg Gly Thr Ala Glu Trp Leu Ser Phe Asp Val Thr Asp Thr Val
195 200 205
Arg Glu Trp Leu Leu Arg Arg Glu Ser Asn Leu Gly Leu Glu Ile Ser
210 215 220
Ile His Cys Pro Cys His Thr Phe Gln Pro Asn Gly Asp Ile Leu Glu
225 230 235 240
Asn Ile His Glu Val Met Glu Ile Lys Phe Lys Gly Val Asp Asn Glu
245 250 255
Asp Asp His Gly Arg Gly Asp Leu Gly Arg Leu Lys Lys Gln Lys Asp
260 265 270
His His Asn Pro His Leu Ile Leu Met Met Ile Pro Pro His Arg Leu
275 280 285
Asp Asn Pro Gly Gln Gly Gly Gln Arg Lys Lys Arg Ala Leu Asp Thr
290 295 300
Asn Tyr Cys Phe Arg Asn Leu Glu Glu Asn Cys Cys Val Arg Pro Leu
305 310 315 320
Tyr Ile Asp Phe Arg Gln Asp Leu Gly Trp Lys Trp Val His Glu Pro
325 330 335
Lys Gly Tyr Tyr Ala Asn Phe Cys Ser Gly Pro Cys Pro Tyr Leu Arg
340 345 350
Ser Ala Asp Thr Thr His Ser Thr Val Leu Gly Leu Tyr Asn Thr Leu
355 360 365
Asn Pro Glu Ala Ser Ala Ser Pro Cys Cys Val Pro Gln Asp Leu Glu
370 375 380
Pro Leu Thr Ile Leu Tyr Tyr Val Gly Arg Thr Pro Lys Val Glu Gln
385 390 395 400
Leu Ser Asn Met Val Val Lys Ser Cys Lys Cys Ser
405 410
<210> 24
<211> 300
<212> БЕЛОК
<213> Homo sapiens
<400> 24
Met Ala Asn Cys Glu Phe Ser Pro Val Ser Gly Asp Lys Pro Cys Cys
1 5 10 15
Arg Leu Ser Arg Arg Ala Gln Leu Cys Leu Gly Val Ser Ile Leu Val
20 25 30
Leu Ile Leu Val Val Val Leu Ala Val Val Val Pro Arg Trp Arg Gln
35 40 45
Gln Trp Ser Gly Pro Gly Thr Thr Lys Arg Phe Pro Glu Thr Val Leu
50 55 60
Ala Arg Cys Val Lys Tyr Thr Glu Ile His Pro Glu Met Arg His Val
65 70 75 80
Asp Cys Gln Ser Val Trp Asp Ala Phe Lys Gly Ala Phe Ile Ser Lys
85 90 95
His Pro Cys Asn Ile Thr Glu Glu Asp Tyr Gln Pro Leu Met Lys Leu
100 105 110
Gly Thr Gln Thr Val Pro Cys Asn Lys Ile Leu Leu Trp Ser Arg Ile
115 120 125
Lys Asp Leu Ala His Gln Phe Thr Gln Val Gln Arg Asp Met Phe Thr
130 135 140
Leu Glu Asp Thr Leu Leu Gly Tyr Leu Ala Asp Asp Leu Thr Trp Cys
145 150 155 160
Gly Glu Phe Asn Thr Ser Lys Ile Asn Tyr Gln Ser Cys Pro Asp Trp
165 170 175
Arg Lys Asp Cys Ser Asn Asn Pro Val Ser Val Phe Trp Lys Thr Val
180 185 190
Ser Arg Arg Phe Ala Glu Ala Ala Cys Asp Val Val His Val Met Leu
195 200 205
Asn Gly Ser Arg Ser Lys Ile Phe Asp Lys Asn Ser Thr Phe Gly Ser
210 215 220
Val Glu Val His Asn Leu Gln Pro Glu Lys Val Gln Thr Leu Glu Ala
225 230 235 240
Trp Val Ile His Gly Gly Arg Glu Asp Ser Arg Asp Leu Cys Gln Asp
245 250 255
Pro Thr Ile Lys Glu Leu Glu Ser Ile Ile Ser Lys Arg Asn Ile Gln
260 265 270
Phe Ser Cys Lys Asn Ile Tyr Arg Pro Asp Lys Phe Leu Gln Cys Val
275 280 285
Lys Asn Pro Glu Asp Ser Ser Cys Thr Ser Glu Ile
290 295 300
<210> 25
<211> 449
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 25
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Ala Met His Trp Val Lys Glu Ala Pro Gly Gln Arg Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Tyr Pro Gly Gln Gly Gly Thr Asn Tyr Asn Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Ala Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Phe Cys
85 90 95
Ala Arg Thr Gly Gly Leu Arg Arg Ala Tyr Phe Thr Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Ala Gly
225 230 235 240
Pro Asp Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Leu Pro Glu Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly
<210> 26
<211> 218
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 26
Asp Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Ile Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Gly Gln Gly Phe Met His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Arg Leu Leu Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Pro Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Asn Lys
85 90 95
Glu Asp Pro Trp Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 27
<211> 120
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 27
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Val Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Ala Met His Trp Val Lys Glu Ala Pro Gly Gln Arg Leu Glu Trp Ile
35 40 45
Gly Tyr Ile Tyr Pro Gly Gln Gly Gly Thr Asn Tyr Asn Gln Lys Phe
50 55 60
Gln Gly Arg Ala Thr Leu Thr Ala Asp Thr Ser Ala Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Phe Cys
85 90 95
Ala Arg Thr Gly Gly Leu Arg Arg Ala Tyr Phe Thr Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 28
<211> 111
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 28
Asp Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Ile Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Gly Gln Gly Phe Met His Trp Tyr Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Arg Leu Leu Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Pro Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Asn Lys
85 90 95
Glu Asp Pro Trp Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 29
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 29
Gly Tyr Thr Phe Thr Ser Tyr Ala
1 5
<210> 30
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 30
Ile Tyr Pro Gly Gln Gly Gly Thr
1 5
<210> 31
<211> 13
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 31
Ala Arg Thr Gly Gly Leu Arg Arg Ala Tyr Phe Thr Tyr
1 5 10
<210> 32
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 32
Gln Ser Val Ser Ser Tyr Gly Gln Gly Phe
1 5 10
<210> 33
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 33
Gly Ala Ser
1
<210> 34
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 34
Gln Gln Asn Lys Glu Asp Pro Trp Thr
1 5
<210> 35
<211> 446
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 35
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Gly Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Met Phe Arg Gly Ala Phe Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu
115 120 125
Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys
130 135 140
Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser
145 150 155 160
Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser
165 170 175
Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser
180 185 190
Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn
195 200 205
Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His
210 215 220
Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Ala Gly Pro Asp Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu
260 265 270
Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Ala Leu Pro Leu Pro Glu Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
435 440 445
<210> 36
<211> 214
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 36
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp
20 25 30
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Gly Leu Gln Pro
65 70 75 80
Glu Asp Ser Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Ile Tyr Tyr Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 37
<211> 117
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 37
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Asn Lys Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Gly Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Met Phe Arg Gly Ala Phe Asp Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 38
<211> 107
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический полипептид"
<400> 38
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Arg Asn Asp
20 25 30
Leu Gly Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Gly Leu Gln Pro
65 70 75 80
Glu Asp Ser Ala Thr Tyr Tyr Cys Leu Gln Asp Tyr Ile Tyr Tyr Pro
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 39
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 39
Gly Phe Thr Phe Ser Ser Tyr Gly
1 5
<210> 40
<211> 8
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 40
Ile Trp Tyr Asp Gly Ser Asn Lys
1 5
<210> 41
<211> 10
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 41
Ala Arg Met Phe Arg Gly Ala Phe Asp Tyr
1 5 10
<210> 42
<211> 6
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 42
Gln Gly Ile Arg Asn Asp
1 5
<210> 43
<211> 3
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 43
Ala Ala Ser
1
<210> 44
<211> 9
<212> БЕЛОК
<213> Искусственная последовательность
<220>
<221> источник
<223> /примечание="Описание искусственной последовательности:
синтетический пептид"
<400> 44
Leu Gln Asp Tyr Ile Tyr Tyr Pro Thr
1 5
<---
| название | год | авторы | номер документа |
|---|---|---|---|
| СЛИТЫЙ БЕЛОК НА ОСНОВЕ АНТИТЕЛА К ЕТА И TGF-β TRAP, СОДЕРЖАЩАЯ ЕГО ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ИХ ПРИМЕНЕНИЕ | 2020 |
|
RU2832190C2 |
| БИСПЕЦИФИЧНЫЙ СЛИТЫЙ БЕЛОК И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2801528C2 |
| СЛИТЫЕ МОЛЕКУЛЫ ЭКТОДОМЕНА РЕЦЕПТОРА TGF-БЕТА И ИХ ПРИМЕНЕНИЯ | 2018 |
|
RU2797464C2 |
| ТРИСПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ БЕЛКИ, ОТНОСЯЩИЕСЯ К НИМ СПОСОБЫ И ВАРИАНТЫ ИХ ПРИМЕНЕНИЯ | 2020 |
|
RU2822200C2 |
| СЛИТЫЙ БЕЛОК И ЕГО ПРИМЕНЕНИЕ | 2019 |
|
RU2800923C2 |
| СЛИТЫЙ БЕЛОК, СОДЕРЖАЩИЙ РЕЦЕПТОР TGF-БЕТА, И ЕГО ФАРМАЦЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2018 |
|
RU2776204C1 |
| ТРИСПЕЦИФИЧЕСКИЕ СВЯЗЫВАЮЩИЕ БЕЛКИ, СВЯЗЫВАЮЩИЕ CD38, CD28 И CD3, А ТАКЖЕ СПОСОБЫ ПРИМЕНЕНИЯ ДЛЯ ЛЕЧЕНИЯ ВИРУСНОЙ ИНФЕКЦИИ | 2019 |
|
RU2820351C2 |
| АНТИТЕЛА К CD38 И СОСТАВЫ | 2020 |
|
RU2826957C2 |
| АНТИТЕЛА К БЕЛКУ CD38 И ИХ ПРИМЕНЕНИЕ | 2019 |
|
RU2776795C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ СЛИТОГО БЕЛКА РЕЦЕПТОРА ТРАНСФОРМИРУЮЩЕГО ФАКТОРА РОСТА БЕТА И ЕЕ ПРИМЕНЕНИЕ | 2019 |
|
RU2791683C2 |
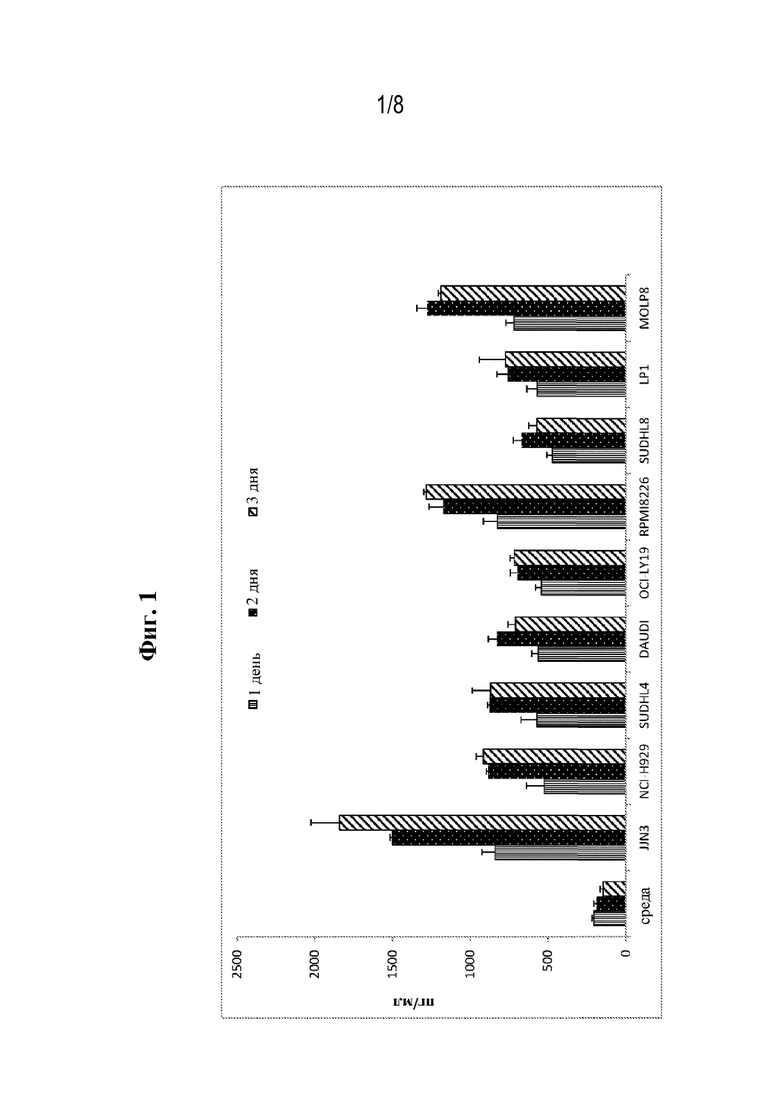
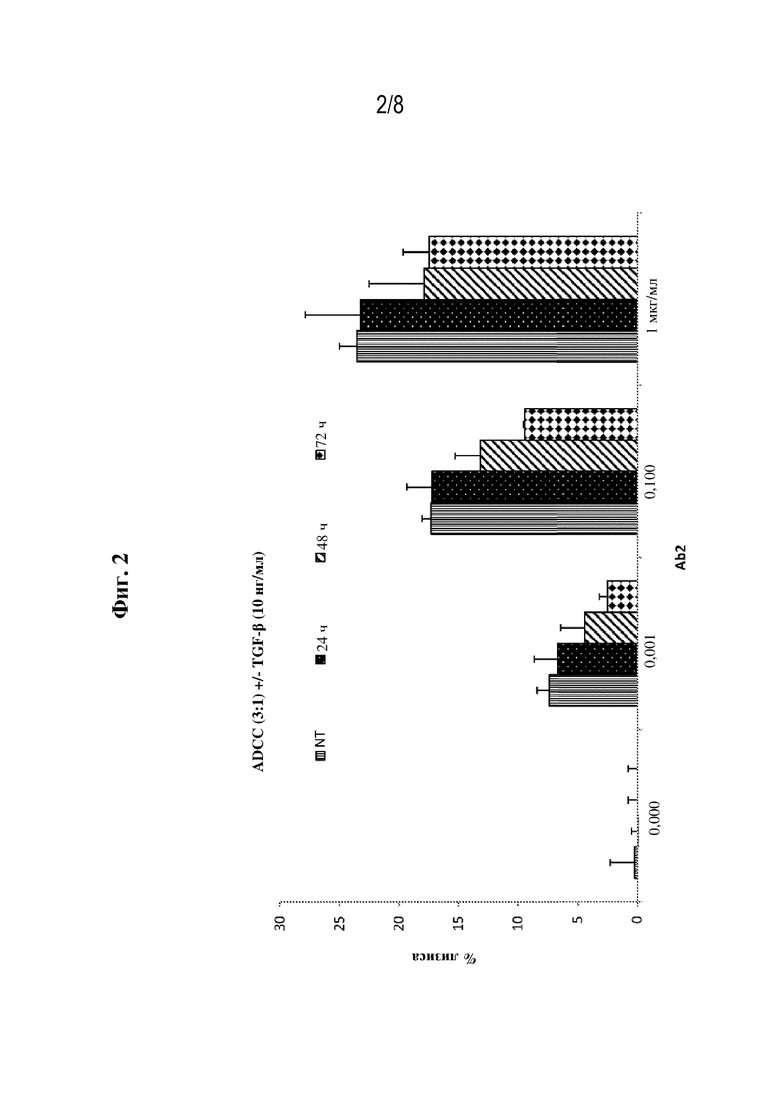
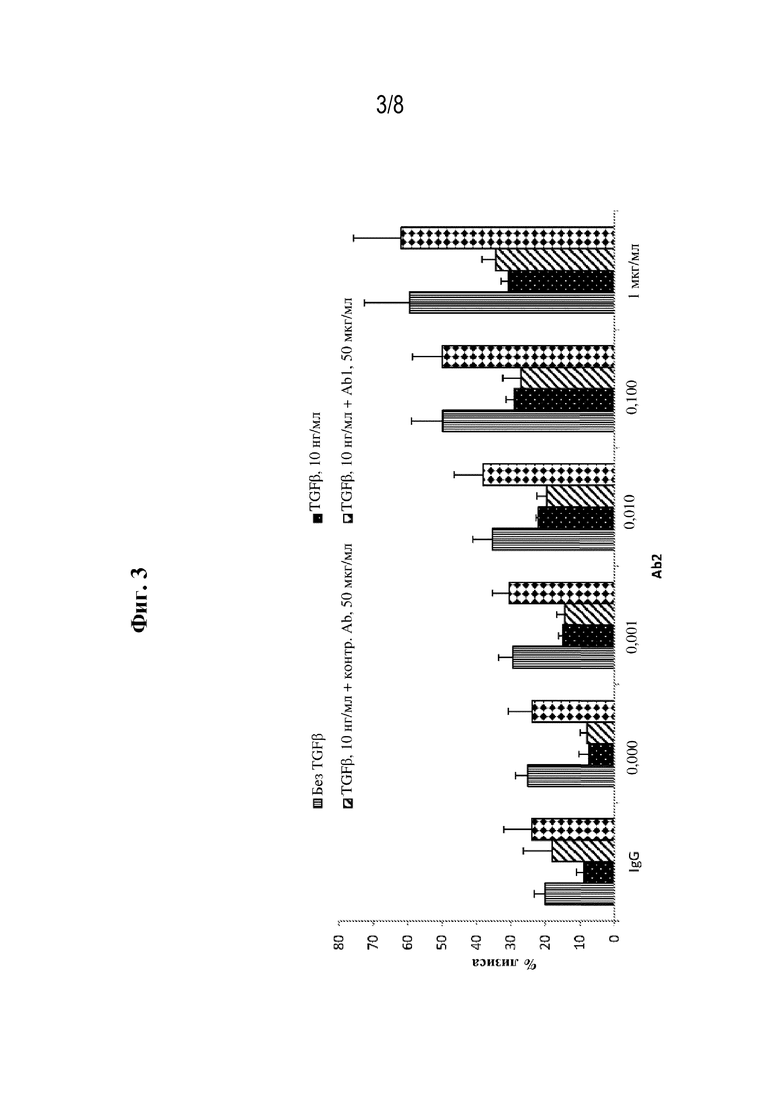
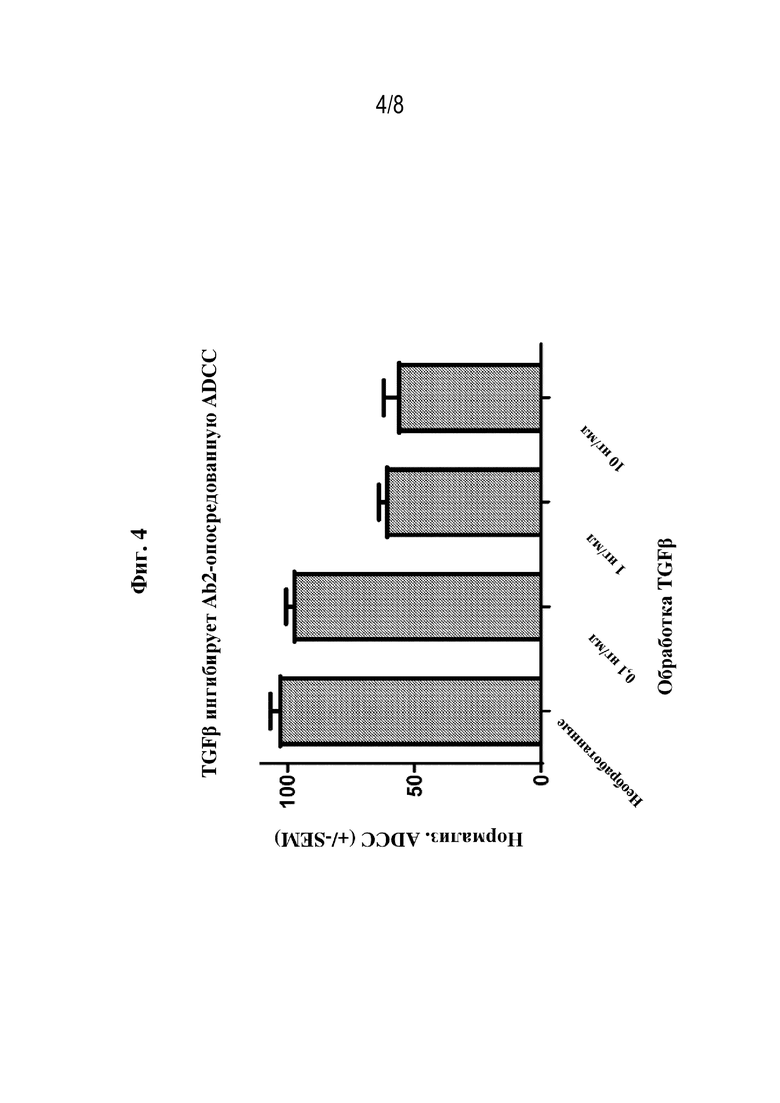
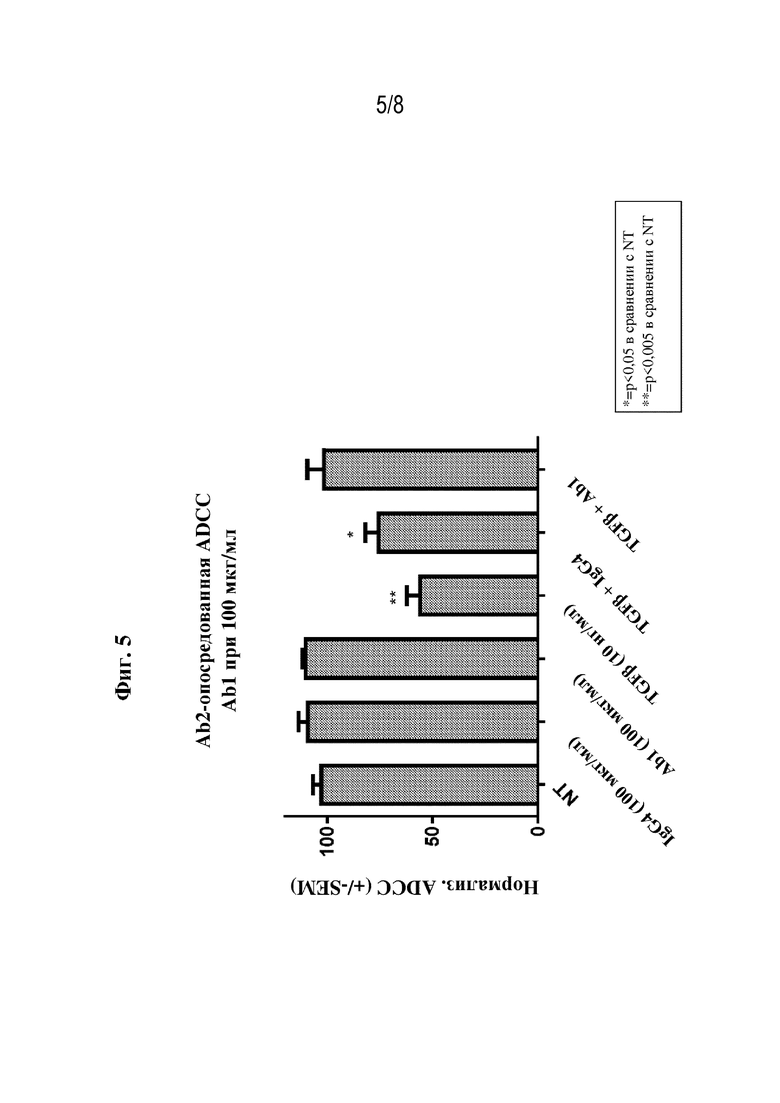
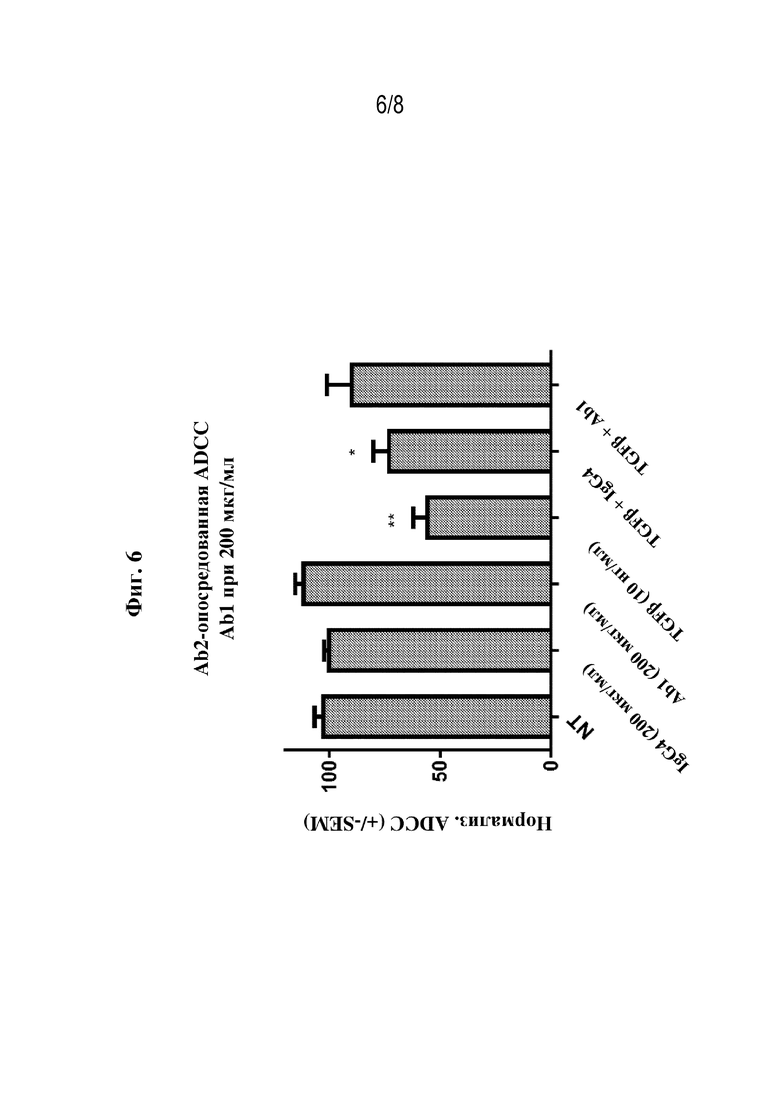
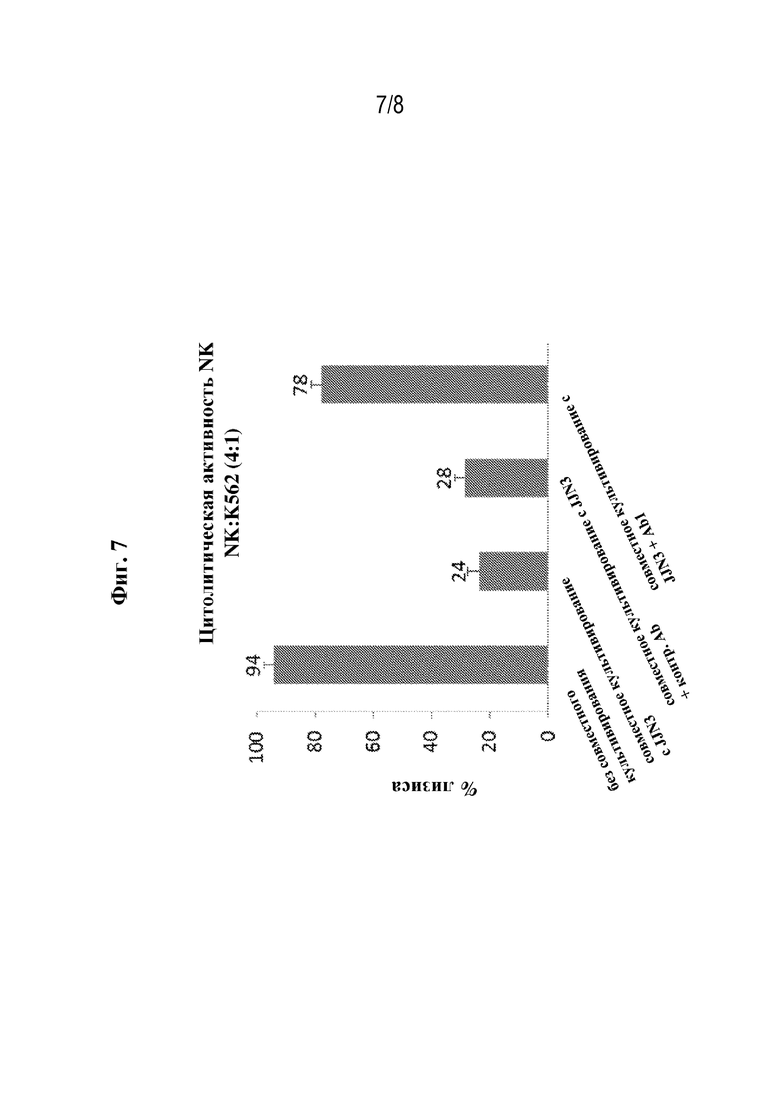
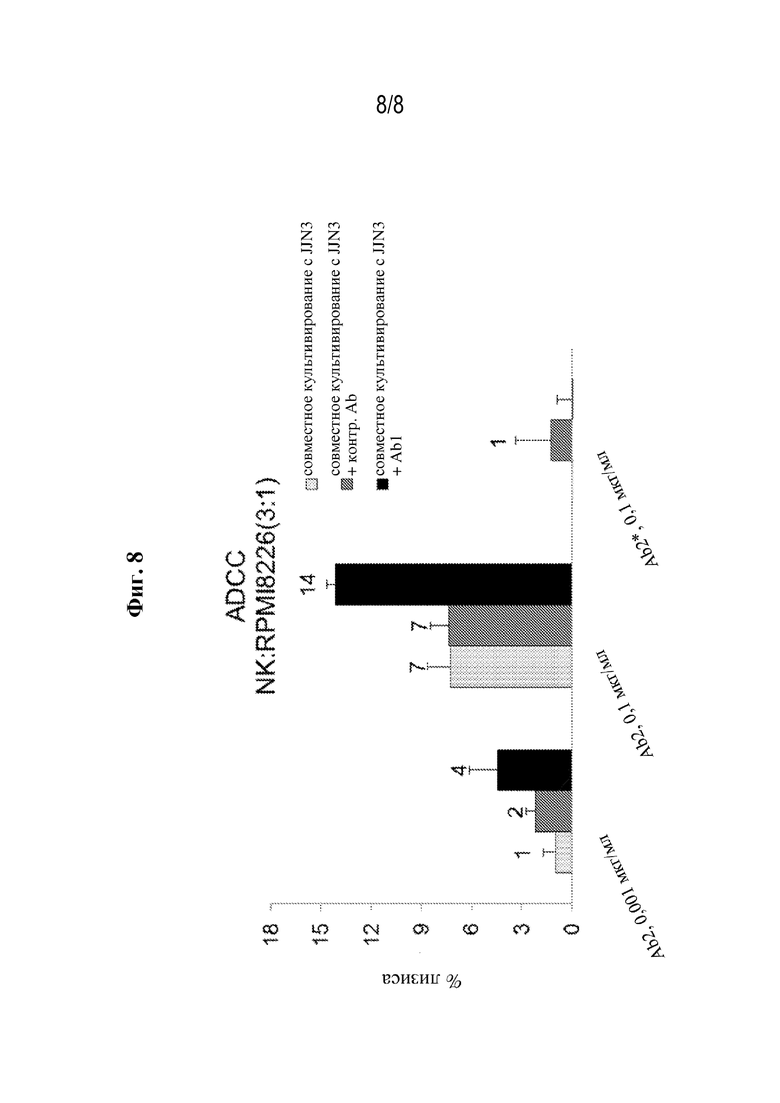
Группа изобретений относится к комбинированной терапии, нацеливающейся на CD38 и TGF-β. Предложены способы лечения множественной миеломы у пациента-человека с использованием комбинации анти-CD38 антитела, которое содержит HCDR1, HCDR2, HCDR3, LCDR1, LCDR2 и LCDR3, содержащие аминокислотные последовательности SEQ ID NO: 15-20, соответственно, и анти-TGF-β антитела или его антигенсвязывающего фрагмента, которое содержит HCDR1, HCDR2, HCDR3, LCDR1, LCDR2 и LCDR3, содержащие аминокислотные последовательности SEQ ID NO: 5-10, соответственно. Антитело к TGF-β может блокировать способность TGF-β ослаблять противоопухолевый эффект антитела к CD38, тем самым обеспечивается эффективное лечение множественной миеломы, в том числе резистентной к одному или нескольким другим видам лечения, нацеливающимся на CD38. 6 н. и 15 з.п. ф-лы, 8 ил., 6 пр.
1. Способ лечения множественной миеломы у пациента-человека, предусматривающий введение пациенту
анти-CD38 антитела, которое содержит CDR1 тяжелой цепи (HCDR1), HCDR2, HCDR3, CDR1 легкой цепи (LCDR1), LCDR2 и LCDR3, содержащие аминокислотные последовательности SEQ ID NO: 15-20, соответственно, и
анти-TGF-β антитела или его антигенсвязывающего фрагмента, которое содержит HCDR1, HCDR2, HCDR3, LCDR1, LCDR2 и LCDR3, содержащие аминокислотные последовательности SEQ ID NO: 5-10, соответственно.
2. Способ по п.1, где анти-CD38 антитело содержит вариабельный домен тяжелой цепи (VH) и вариабельный домен легкой цепи (VL), содержащие аминокислотные последовательности SEQ ID NO: 13 и 14, соответственно; и
где анти-TGF-β антитело содержит VH и VL, содержащие аминокислотные последовательности SEQ ID NO: 3 и 4, соответственно.
3. Способ по п.2, где анти-CD38 антитело содержит тяжелую цепь (HC) и легкую цепь (LC), содержащие аминокислотные последовательности SEQ ID NO: 11 и 12, соответственно; и
где анти-TGF-β антитело содержит HC и LC, содержащие аминокислотные последовательности SEQ ID NO: 1 и 2, соответственно.
4. Способ лечения множественной миеломы у больного человека, предусматривающий введение пациенту анти-CD38 антитела и анти-TGF-β антитела или его антигенсвязывающего фрагмента,
где анти-CD38 антитело имеет:
HCDR1-3 и LCDR1-3, содержащие аминокислотные последовательности SEQ ID NO: 15-20, соответственно;
вариабельный домен тяжелой цепи (VH) и вариабельный домен легкой цепи (VL), содержащие аминокислотные последовательности SEQ ID NO: 13 и 14, соответственно; или
тяжелую цепь (HC) и легкую цепь (LC), содержащие аминокислотные последовательности SEQ ID NO: 11 и 12, соответственно, и
анти-TGF-β антитело или антигенсвязывающий фрагмент имеет:
HCDR1-3 и LCDR1-3, содержащие аминокислотные последовательности SEQ ID NO: 5-10, соответственно;
VH и VL, содержащие аминокислотные последовательности SEQ ID NO: 3 и 4, соответственно; или
HC и LC, содержащие аминокислотные последовательности SEQ ID NO: 1 и 2, соответственно.
5. Способ по любому из пп.1-4, где анти-CD38 антитело содержит Fc-область IgG1 человека, и анти-TGF-β антитело содержит Fc-область IgG4 человека.
6. Способ лечения множественной миеломы у больного человека, предусматривающий введение пациенту
анти-CD38 антитела, которое содержит вариабельный домен тяжелой цепи (VH) с аминокислотной последовательностью SEQ ID NO: 13 и вариабельный домен легкой цепи (VL) с аминокислотной последовательностью SEQ ID NO: 14, и
анти-TGF-β антитела, которое содержит VH с аминокислотной последовательностью SEQ ID NO: 3 и VL с аминокислотной последовательностью SEQ ID NO: 4.
7. Способ лечения множественной миеломы у больного человека, предусматривающий введение пациенту
анти-CD38 антитела, которое содержит тяжелую цепь (HC) с аминокислотной последовательностью SEQ ID NO: 11 и легкую цепь (LC) с аминокислотной последовательностью SEQ ID NO: 12, и
анти-TGF-β антитела, которое содержит HC с аминокислотной последовательностью SEQ ID NO: 1 и LC с аминокислотной последовательностью SEQ ID NO: 2.
8. Способ по любому из предыдущих пунктов, где анти-CD38 антитело и анти-TGF-β антитело или его фрагмент вводят пациенту последовательно.
9. Применение анти-CD38 антитела для изготовления лекарственного препарата для лечения множественной миеломы у больного человека в комбинации с анти-TGF-β антителом или его антигенсвязывающим фрагментом, где
анти-CD38 антитело имеет CDR1 тяжелой цепи (HCDR1), HCDR2, HCDR3, CDR1 легкой цепи (LCDR1), LCDR2 и LCDR3, содержащие аминокислотные последовательности SEQ ID NO: 15-20, соответственно, и
анти-TGF-β антитело или его антигенсвязывающий фрагмент имеют HCDR1, HCDR2, HCDR3, LCDR1, LCDR2 и LCDR3, содержащие аминокислотные последовательности SEQ ID NO: 5-10, соответственно.
10. Применение по п.9, где анти-CD38 антитело имеет VH и VL, содержащие аминокислотные последовательности SEQ ID NO: 13 и 14, соответственно; или HC и LC, содержащие аминокислотные последовательности SEQ ID NO: 11 и 12, соответственно.
11. Применение по п.9, где анти-TGF-β антитело или его антигенсвязывающий фрагмент имеет VH и VL, содержащие аминокислотные последовательности SEQ ID NO: 3 и 4, соответственно; или HC и LC, содержащие аминокислотные последовательности SEQ ID NO: 1 и 2, соответственно.
12. Применение анти-TGF-β антитела или его антигенсвязывающего фрагмента для изготовления лекарственного препарата для лечения CD38-положительного рака у больного человека в комбинации с анти-CD38 антителом, где
анти-CD38 антитело имеет CDR1 тяжелой цепи (HCDR1), HCDR2, HCDR3, CDR1 легкой цепи (LCDR1), LCDR2 и LCDR3, содержащие аминокислотные последовательности SEQ ID NO: 15-20, соответственно,
анти-TGF-β антитело или его антигенсвязывающий фрагмент имеют HCDR1, HCDR2, HCDR3, LCDR1, LCDR2 и LCDR3, содержащие аминокислотные последовательности SEQ ID NO: 5-10, соответственно.
13. Применение по п.12, где анти-CD38 антитело имеет VH и VL, содержащие аминокислотные последовательности SEQ ID NO: 13 и 14, соответственно; или HC и LC, содержащие аминокислотные последовательности SEQ ID NO: 11 и 12, соответственно.
14. Применение по п.12, где анти-TGF-β антитело или его антигенсвязывающий фрагмент содержит VH и VL, содержащие аминокислотные последовательности SEQ ID NO: 3 и 4, соответственно; или HC и LC, содержащие аминокислотные последовательности SEQ ID NO: 1 и 2, соответственно.
15. Способ по любому из пп.1-8 или применение по любому из пп.9-11, где рак является CD38-положительным.
16. Способ по любому из пп.1-8 или применение по любому из пп.9-14, где лечение приводит к меньшему разрушению костей, чем лечение одним анти-CD38-антителом.
17. Способ по любому из пп.1-8 или применение по любому из пп.9-14, где лечение способствует заживлению костей.
18. Способ по любому из пп.1-8 или применение по любому из пп.9-14, где лечение дополнительно включает дексаметазон.
19. Способ по любому из пп.1-8 или применение по любому из пп.9-14, где множественная миелома или рак устойчивы к лечению анти-CD38-антителом или даратумумабом или устойчивы как к лечению анти-CD38-антителом, так и к лечению даратумумабом.
20. Готовое изделие, содержащее анти-CD38-антитело и анти-TGF-β-антитело, где указанное промышленное изделие подходит для лечения CD38-положительного рака у пациента способом по любому из пп.1-8.
21. Изделие по п.20,
где анти-CD38 антитело
имеет VH и VL, содержащие аминокислотные последовательности SEQ ID NO: 13 и 14, соответственно; или
имеет HC и LC, содержащие аминокислотные последовательности SEQ ID NO: 11 и 12, соответственно; и
где анти-TGF-β антитело
имеет VH и VL, содержащие аминокислотные последовательности SEQ ID NO: 3 и 4, соответственно; или
имеет HC и LC, содержащие аминокислотные последовательности SEQ ID NO: 1 и 2, соответственно.
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| XIAOYAN FENG ET AL | |||
| Способ сужения чугунных изделий | 1922 |
|
SU38A1 |
| NYMAN JEFFRY S ET AL | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2023-11-30—Публикация
2019-07-10—Подача