Изобретение относится к медицине, а именно к биохимии, фармакологии и клинической фармакологии, и может быть использовано для изучения механизмов миогенеза и оценки влияния на него лекарственных веществ.
Клеточная линия C2C12 - это мышиные миобласты, происходящие из сателлитных клеток, которые могут спонтанно дифференцироваться в мышечные волокна после удаления сыворотки [D. Yaffe, O. Saxel. Serial passaging and differentiation of myogenic cells isolated from dystrophic mouse muscle. Nature. Vol. 270. P. 725 – 727. 1977; H.M. Blau, C.P. Chiu, C. Webster. Cytoplasmic activation of human nuclear genes in stable heterocaryons. Cell. Vol. 32, P. 1171-1180. 1983]. Однако дифференцируется около 50% миобластов, а остальные клетки остаются в недифференцированном состоянии [N. Yoshida, S. Yoshida, K. Koishi, K. Masuda, Y. Nabeshima. Cell heterogeneity upon myogenic differentiation: down-regulation of MyoD and Myf-5 generates 'reserve cells. J. Cell Sci. Vol. 111. P. 769-779. 1998].
Линия клеток C2C12 широко применяется для изучения механизмов миогенеза и оценки влияния на него лекарственных веществ.
Известно, что флаваноид (-)-Epicatechin, альфа-магостин, эпикатехин активируют миогенез клеточной линии С2С12 вследствие стимуляции прегнан Х рецептора [M. Ortiz-Flores et al. PXR is a target of (-)-epicatechin in skeletal muscle. Heliyon. Vol. 6, N 10, e05357 (2020); doi: 10.1016/j.heliyon.2020.e05357; M. Lin, S. Zhou, K. Sakamoto. Alpha Mangostin promotes myogenic differentiation of C2C12 mouse myoblast cells. Biochemical and Biophysical Research Communications. Vol. 528, Is.1, 2020, P. 193-198. DOI: 10.1016 / j.bbrc.2020.04.128; Lee S.J. et al. Epicatechin elicits MyoD-dependent myoblast differentiation and myogenic conversion of fibroblasts. Plos One. 2017. DOI: 10.1371 / journal.pone.0175271].
Техническим результатом изобретения является разработка простого, эффективного способа стимуляции миогенеза клеточной линии C2C12.
Для достижения технического результата проведен следующий эксперимент.
Исследование было выполнено на клеточной линии мышиных миобластов С2С12, предоставленной Институтом биологии гена (Москва). Клетки культивировали при 37ºС и 5% содержании СО2 в инкубаторе WS-189C (World Science, Корея) в Дульбекко модифицированной среде Игла (DMEM), содержащей глюкозу в концентрации 4500 мг/л (Sigma-Aldrich, Германия), L-глутамин в концентрации 4 мМ (Sigma-Aldrich, Германия), 10% эмбриональной бычьей сыворотки (Sigma-Aldrich, Германия), пенициллин в концентрации 100 ЕД/мл и стрептомицин в концентрации 100 мкг/мл (Sigma-Aldrich, Германия). При достижения 70−90% конфлюентности клетки снимали с флакона за счет добавления раствора трипсин-ЭДТА (0,25% трипсина и 0,2% ЭДТА, Sigma-Aldrich, Германия), высевали в 6-луночные планшеты (Сorning, США).
Были сформированы следующие экспериментальные группы:
- клетки до дифференцировки – инкубация в течение 7 суток с питательной средой, содержащей 10% эмбриональной бычьей сыворотки (n=3);
- индукция миогенеза – клетки инкубировали в течение 7 суток с дифференцировочной питательной средой, содержащей 2% лошадиной сыворотки (Sigma-Aldrich, Германия), L-глутамин в концентрации 4 мМ, пенициллин в концентрации 100 ЕД/мл и стрептомицин в концентрации 100 мкг/мл (n=3) [J. Sin et al. Mitophagy is required for mitochondrial biogenesis and myogenic differentiation of C2C12 myoblasts. Autophagy. Vol.12 (2), P. 369-380. 2016; doi: 10.1080/15548627.2015.1115172];
- индукция миогенеза с добавлением сукцината (Acros Organics, США) – клетки инкубировали 7 дней в дифференцировочной питательной среде, содержащей сукцинат в концентрации 10 мкМ в течение 7 дней (n=3).
Для микроскопирования применяли инвертированный микроскоп Olympus CKX-53 («Olympus», Япония).
После окончания экспозиции, клетки снимали с лунок раствором трипсин-ЭДТА (Sigma-Aldrich, США), трижды промывали раствором фосфатного буфера (BioRad, США) и лизировали в NP40 Cell Lysis Buffer Thermo (Thermo Fisher Scientific, США) c добавлением смеси ингибиторов протеиназ (Sigma-Aldrich, США) в течение 30 минут при +4°С и постоянном перемешивании из расчета 107 клеток на 100 мкл буфера. Полученный лизат центрифугировали при 13000 об/мин в течение 10 минут (AvantiJXN-3, BeckmanCoulter, США).
Цитоплазматические белки (30 мкг) подвергали электрофорезу с использованием TGX Stain-Free FastCast Acrylamide Kit (Bio-Rad, США) в буферной системе Laemmli (BioRad,США). Перед загрузкой образцы обрабатывались в соответствии с протоколом Bio-Rad, их смешивали с буфером для образцов Laemmli (Bio-Rad, США), содержащем 2,5% β-меркаптоэтанола (Bio-Rad, США) в соотношении 1:3, инкубировали 10 мин при температуре 70°C. Гели прогоняли при 100 В в течение 90 мин.
Относительное количество миозина, α-актина, Myod, миогенина определяли методом вестерн-блот с использованием первичных мышиных моноклональных антител (sc-377460 MyoD (G-1) Monoclonal Antibody, Santa cruz biotechnology,inc, США; sc-12732 myogenin (F5D) Monoclonal Antibody, Santa cruz biotechnology,inc, США; sc-53092, MYH1/2/3 (N3.36) Monoclonal Antibody, Santa cruz biotechnology,inc, США; sc-53142, Smooth Muscle Actin (B4), Monoclonal Antibody, Santa cruz biotechnology,inc, США) в концентрации 1:200. Визуализацию первичных антител осуществляли с применением вторичных кроличьих антител (Rabbit anti-Mouse IgG (H+L) Secondary Antibody, HRP, Invitrogen) в разведении 1:4000.
Белки визуализировали хемилюминесценцией с использованием Chemi Doc XRS+ (Bio-Rad, США). Интенсивность полученных полос (бэндов) анализировали денситометрически с применением программы ImageLab (Bio-Rad, США).
Количество белков оценивали относительно содержания белка домашнего хозяйства GAPDH (первичные GAPDH Loading Control Monoclonal Antibody (GA1R), DyLight 68, Invitrogen, США, разведение 1:1000, вторичные антитела - вторичные кроличьи антитела к первичным антителам GAPDH - Rabbitanti-Mouse IgG (H+L) Secondary Antibody, HRP, Invitrogen, США, разведение 1:4000).
Полученные результаты анализировали с помощью программ «Stat Soft Statistica 13.0» (США, номер лицензии JPZ811I521319AR25ACD-W) и Microsoft Excel for MAC ver. 16.24 (ID02984-001-000001). Результаты представлены в виде M±SD. Для оценки статистической значимости различий использовали дисперсионный анализ (ANOVA), множественные сравнения выполняли с помощью критерия Ньюмена-Кейлса. Статистически значимыми считали различия при p<0,05.
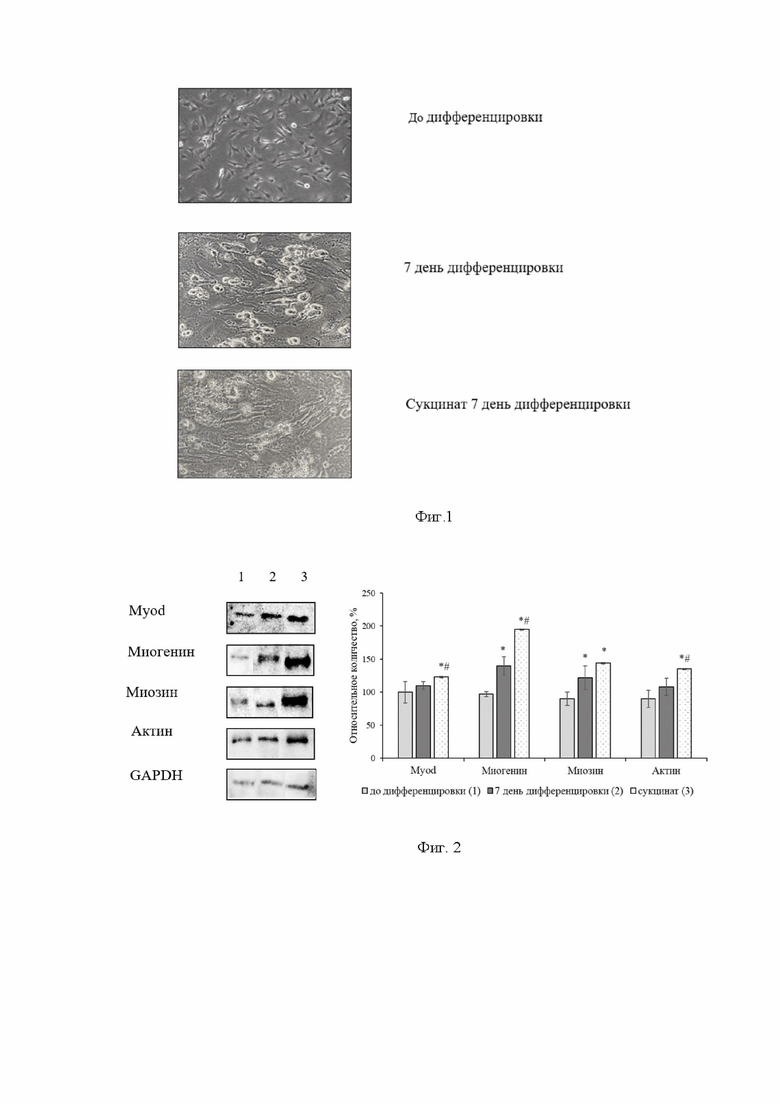
Смена питательной среды, содержащей 10% эмбриональной бычьей сыворотки, на среду с содержанием 2% лошадиной сыворотки индуцировала процесс миогенеза. Клетки становились из отростчатых или веретенообразных более вытянутыми. Далее некоторые миобласты сливались и формировали миотубы – многоядерные веретенообразные структуры длиной 100-600 мкм, шириной 30-50 мкм. Максимальные изменения отмечались на 7 сутки (фиг. 1).
Добавление сукцината активировало процесс миогенеза: большее количество клеток изменяли форму, сливаясь в миотубы.
Также отмечалась следующая динамика клеточных белков (фиг. 2). Содержание миозина в клетках линии С2С12 на 7 сутки эксперимента при использовании обычной дифференцировочной среды и среды с добавлением сукцината статистически значимо увеличивалось по сравнению с показателями клеток до дифференцировки на 35,6% (р=0,004) и 60% (р=0,005) соответственно. В группе с сукцинатом достоверных отличий от клеток на 7 сутки при инкубации в обычной дифференцировочной среде отмечено не было.
Количество α-актина статистически значимо не отличалось в клетках до и после дифференцировки. Однако при добавлении сукцината отмечалось увеличение содержания α-актина на 50% (р=0,04) по сравнению с клетками до дифференцировки и на 25% (р=0,05) по сравнению с клетками на 7 день дифференцировки.
Уровень Myod (Myogenic determination gene number 1) - основного регулятора дифференцировки миобластов - в клетках линии С2С12 до дифференцировки и на 7 день дифференцировки достоверно не отличался. Добавление в дифференцировочную питательную среду сукцината привело к повышению содержания Myod на 23,0 % (р=0,037) по сравнению с клетками до дифференцировки и на 12,8% (р=0,01) по сравнению с клетками на 7 день дифференцировки.
Количество регуляторного белка миогенина достоверно увеличивалось в клетках на 7 день при обычных условиях дифференцировки на 44,3% (р=0,02), а при добавлении сукцината в питательную среду на 101,1% (р=0,009) по сравнению с клетками линии С2С12 до дифференцировки. Сукцинат также активировал повышение количества миогенина по сравнению с клетками на 7 день в обычных условиях дифференцировки на 39,2% (р=0,04).
Краткое описание чертежей
Фиг. 1. Влияние сукцината 10 мкМ на миогенез на линии клеток С2С12, х200. Фазово-контрастная микроскопия.
Фиг. 2. Относительное количество Myod, миогенина, миозина, актина в клетках линии С2С12 под влиянием сукцината в концентрации 10 мкМ в течение 7 дней. Примечание: статистически значимые отличия * - p<0,05 по сравнению с клетками до дифференцировки; # - p<0,05 по сравнению с клетками на 7 день дифференцировки.
Таким образом, установлено, что инкубирование клеточной линии С2С12 в дифференцировочной питательной среде с добавлением сукцината до достижения концентрации в среде 10 мкМ в течение 7 суток активирует миогенез, что подтверждается морфологическими изменениями клеток, повышением количества специфических мышечных белков - α-актина, миозина и факторов миогенной дифференцировки – MyoD и миогенина.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ активации миогенной дифференцировки миобластов | 2021 |
|
RU2780589C1 |
| КОМПОЗИЦИИ ИЗ КУЛЬТИВИРУЕМОГО МЯСА | 2018 |
|
RU2778255C2 |
| СПОСОБ ПОВЫШЕНИЯ КОЛИЧЕСТВА БЕЛКА РЕЗИСТЕНТНОСТИ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ В ЭКСПЕРИМЕНТЕ НА КЛЕТОЧНОЙ ЛИНИИ ГЕПАТОЦЕЛЛЮЛЯРНОЙ КАРЦИНОМЫ ЧЕЛОВЕКА | 2023 |
|
RU2803336C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОПУЛЯЦИИ СТРОМАЛЬНЫХ КЛЕТОК ЖИРОВОЙ ТКАНИ, ИНДУЦИРОВАННЫХ К НЕЙРАЛЬНОЙ ДИФФЕРЕНЦИРОВКЕ | 2008 |
|
RU2396345C1 |
| КОМПОЗИЦИИ ГУМАНИЗИРОВАННЫХ СЛИТЫХ БЕЛКОВ NOTCH И СПОСОБЫ ЛЕЧЕНИЯ | 2008 |
|
RU2532830C2 |
| Штамм гибридных культивируемых клеток Homo sapiens/Mus musculus 1B9C7 - продуцент человеческих моноклональных антител, специфичных к протеолитическому домену ботулинического токсина типа A | 2021 |
|
RU2783897C1 |
| ШТАММ ГИБРИДНЫХ КЛЕТОК ЖИВОТНЫХ Mus musculus 3F11 - ПРОДУЦЕНТ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ, СПЕЦИФИЧНЫХ К БОТУЛИНИЧЕСКОМУ ТОКСИНУ ТИПА B | 2014 |
|
RU2566553C1 |
| ШТАММ ГИБРИДНЫХ КЛЕТОК ЖИВОТНЫХ Mus musculus 1G7 - ПРОДУЦЕНТ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ, СПЕЦИФИЧНЫХ К БОТУЛИНИЧЕСКОМУ ТОКСИНУ ТИПА В | 2014 |
|
RU2571208C1 |
| Штамм гибридных клеток животных Mus musculus 2E1B5 - продуцент моноклонального антитела к рецептор-связывающему домену белка S вируса SARS-CoV-2 | 2021 |
|
RU2771288C1 |
| КЛЕТОЧНЫЙ ПРОДУКТ ИНСУЛИН-ПРОДУЦИРУЮЩИХ КЛЕТОК МЛЕКОПИТАЮЩИХ И ЕГО ИСПОЛЬЗОВАНИЕ ДЛЯ ТЕРАПИИ САХАРНОГО ДИАБЕТА | 2017 |
|
RU2663118C1 |
Настоящее изобретение относится к медицине, в частности к биохимии, фармакологии и клинической фармакологии, и может быть использовано для изучения механизмов миогенеза и оценки влияния на него лекарственных веществ. Настоящее изобретение раскрывает способ стимуляции миогенеза линии клеток C2C12. Для осуществления указанного способа клетки C2C12 инкубируют в течение 7 дней с дифференцировочной питательной средой, содержащей 2% лошадиной сыворотки, L-глутамин в концентрации 4 мМ, пенициллин в концентрации 100 ЕД/мл и стрептомицин в концентрации 100 мкг/мл с добавлением в среду сукцината до достижения концентрации 10 мкМ. Настоящее изобретение позволяет повысить эффективность миогенеза линии клеток C2C12. 2 ил., 1 пр.
Способ стимуляции миогенеза линии клеток C2C12, включающий инкубирование клеток в течение 7 дней с дифференцировочной питательной средой, содержащей 2% лошадиной сыворотки, L-глутамин в концентрации 4 мМ, пенициллин в концентрации 100 ЕД/мл и стрептомицин в концентрации 100 мкг/мл, отличающийся добавлением в среду сукцината до достижения концентрации 10 мкМ.
| BLAND CHRISTOPHER S | |||
| et al., Global regulation of alternative splicing during myogenic differentiation, Nucleic Acids Research, 2010, Vol | |||
| Способ сужения чугунных изделий | 1922 |
|
SU38A1 |
| Выбрасывающий ячеистый аппарат для рядовых сеялок | 1922 |
|
SU21A1 |
| Устройство для электрической колокольной сигнализации на одно путных железных дорогах | 1927 |
|
SU7651A1 |
| ARNESON-WISSINK PAIGE C | |||
| et al., The wasting-associated metabolite succinate disrupts myogenesis and impairs skeletal muscle regeneration, JCSM Rapid | |||
Авторы
Даты
2022-07-12—Публикация
2021-12-13—Подача