ПЕРЕКРЕСТНАЯ ССЫЛКА НА СВЯЗАННЫЕ ЗАЯВКИ
Данная заявка испрашивает преимущество предварительной заявки на патент США №62/615848, поданной 10 января 2018 года. Данная заявка включена посредством ссылки, как если бы она была полностью переписана в настоящем документе.
УРОВЕНЬ ТЕХНИКИ
Рак печени является второй по значимости причиной смертности от любого типа рака и 16-ой по частоте встречаемости причиной смерти в мире (Llovet JM, et al., 2015 "Advances in targeted therapies for hepatocellular carcinoma in the genomic era." Nat. Rev. Clin Oncology 12, 408-424). Гепатоцеллюлярная карцинома (hepatocellular carcinoma (HCC)) вызывает до 90% всех случаев первичного рака печени (Llovet JM et al. 2015).
Соединение 1 представляет собой селективный, перорально биодоступный низкомолекулярный ингибитор FGFR4 со структурой, представленной формулой I, и химическим названием N-(2-((6-(3-(2,6-дихлор-3,5-диметоксифенил)-1-метилуреидо)пиримидин-4-ил)амино)-5-(4-этилпиперазин-1-ил)фенил)акриламид:
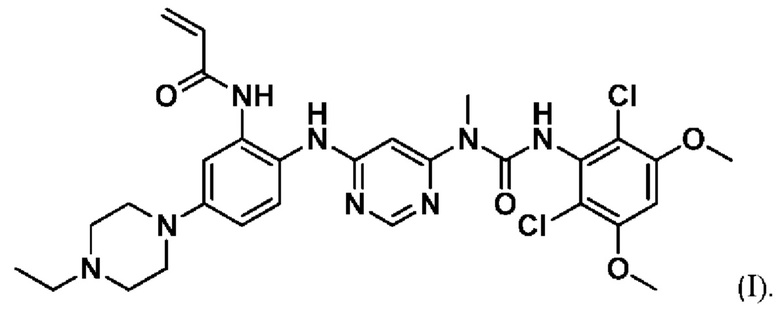
Соединение 1 и его синтез описаны в публикации международной заявки РСТ № WO 2015/057938, опубликованной 23 апреля 2015 г. Данный документ включен в данное описание посредством ссылки.
Ленватиниб (4-[3-хлор-4-(N'-циклопропилуреидо)фенокси]-7-метоксихинолин-6-карбоксамид) представляет собой ингибитор рецепторов тирозинкиназ (receptor tyrosine kinase (RTK)), который ингибирует киназные активности рецепторов фактора роста эндотелия сосудов (vascular endothelial growth factor (VEGF)) VEGFR1 (FLT1), VEGFR2 (KDR) и VEGFR3 (FLT4). Ленватиниб также ингибирует другие RTK, которые участвуют в патогенном ангиогенезе, росте опухоли и прогрессировании злокачественного заболевания в дополнение к их нормальным клеточным функциям, включая рецепторы фактора роста фибробластов (FGF) FGFR1, 2, 3 и 4; полученный из тромбоцитов рецептор фактора роста альфа (PDGFRα), KIT и RET. О ленватинибе сообщается в патентах США №№7,253,286; 7,612,208; и 9,006,256; все из которых включены в данное описание посредством ссылки.
Несмотря на достижения в лечении НСС, было бы полезно обеспечить альтернативное лечение НСС, включая лечение пациентов, у которых НСС может быть устойчивой к современным схемам лечения, плохо реагирующей или не полностью реагирующей на них.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Варианты осуществления изобретения обеспечивают комбинированную терапию, содержащую количество соединения 1 и количество ленватиниба в количестве, эффективном для пациента, нуждающегося в лечении гепатоцеллюлярной карциномы (НСС). Комбинированная терапия, обеспеченная в настоящем документе, может приводить к синергетическому снижению жизнеспособности клеток НСС и может приводить к ингибированию роста опухоли НСС у пациентов, нуждающихся в лечении.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
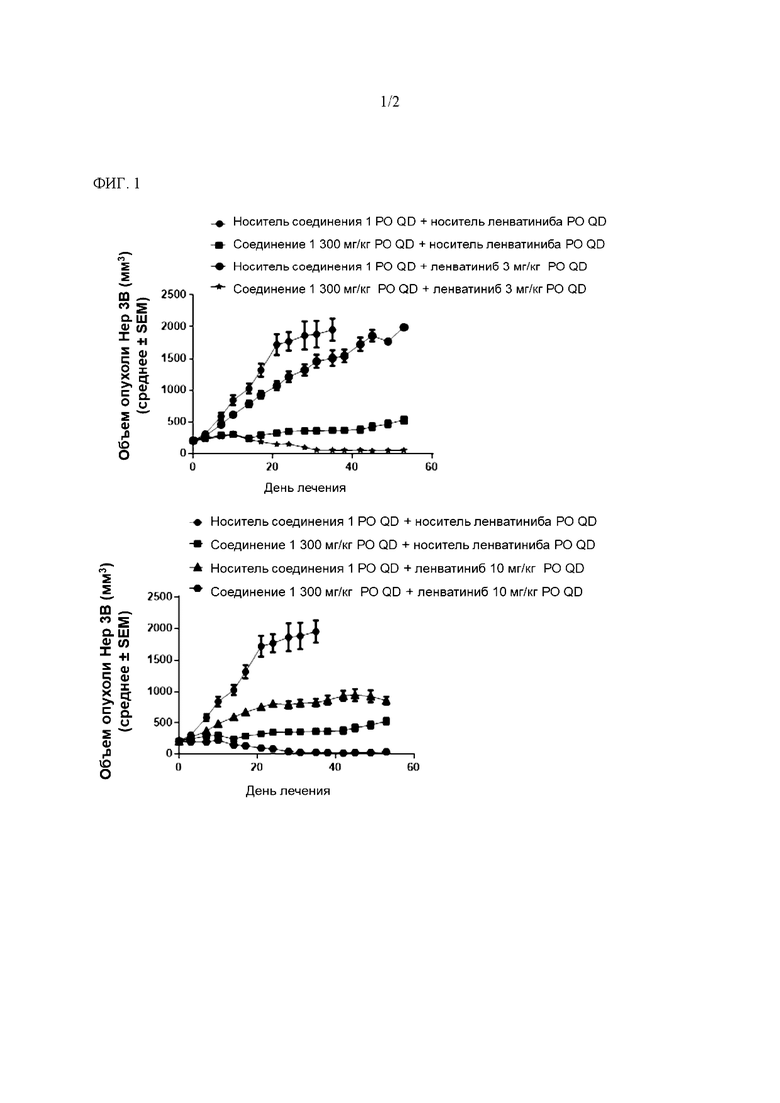
На ФИГ. 1 показаны противоопухолевые эффекты соединения 1 и ленватиниба в модели ксенотрансплантата гепатоцеллюлярной карциномы Нер3В. Соединение 1 и ленватиниб вводили перорально (РО) один раз в день (QD) в течение 53 дней. Данные представляют собой среднее ± SEM для объема опухоли.
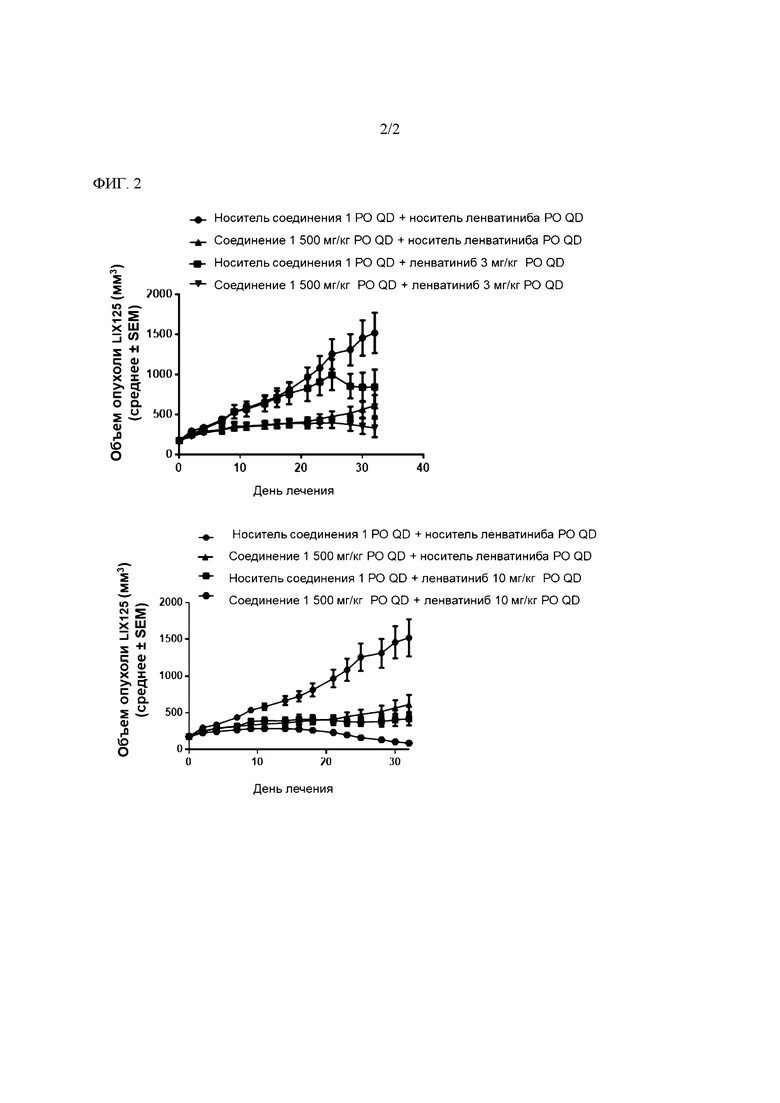
На ФИГ. 2 показаны результаты приведенного в примере 2 исследования ксенотрансплантата PDX in vivo.
ПОДРОБНОЕ ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ
Настоящее изобретение относится к комбинированным способам лечения, применимым для лечения гепатоцеллюлярной карциномы (НСС). В некоторых вариантах комбинированная терапия включает введение соединения 1 в комбинации с ленватинибом.
Настоящее изобретение относится к комбинациям терапевтических средств и способам введения комбинации средств с целью лечения гепатоцеллюлярной карциномы. Используемый в настоящем описании термин «комбинация терапевтических средств» и аналогичные термины относятся к комбинации двух типов терапевтических средств: (1) соединение 1 и/или фармакологически активные метаболиты, соли, сольваты и рацематы соединения 1 и (2) ленватиниб и/или фармакологически активные метаболиты, соли, сольваты и рацематы ленватиниба. Фармакологически активные метаболиты включают те, которые являются неактивными, но превращаются в фармакологически активные формы в организме после введения.
Соединение 1 представляет собой селективный перорально биодоступный низкомолекулярный ингибитор FGFR4 со структурой, показанной в формуле I:
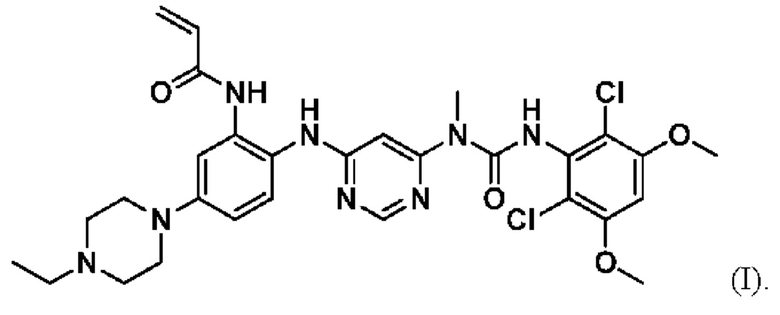
Соединение 1 и его синтез описаны в публикации международной заявки РСТ № WO 2015/0 57938, опубликованной 23 апреля 2015 г. Данный документ включен в настоящее описание посредством ссылки.
Ленватиниб (4-[3-хлор-4-(N'-циклопропилуреидо)фенокси]-7-метоксихинолин-6-карбоксамид) представляет собой ингибитор рецепторов тирозинкиназ (RTK), который ингибирует киназные активности рецепторов фактора роста эндотелия сосудов (VEGF) VEGFR1 (FLT1), VEGFR2 (KDR) и VEGFR3 (FLT4). Ленватиниб также ингибирует другие RTK, которые участвуют в патогенном ангиогенезе, росте опухоли и прогрессировать злокачественного заболевания в дополнение к их нормальным клеточным функциям, включая рецепторы фактора роста фибробластов (FGF) FGFR1, 2, 3 и 4; полученный из тромбоцитов рецептор фактора роста альфа (PDGFRα), KIT и RET. Ленватиниб имеет следующую структуру:
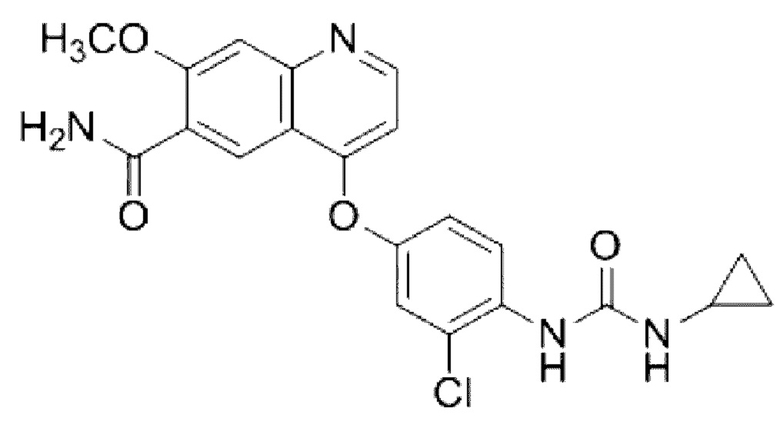
Мезилатная соль ленватиниба, известная как LENVIMA® от Eisai, Inc., 4-[3-хлор-4-(N'-циклопропилурейдо)фенокси]-7-метоксихинолин-6-карбоксамид метансульфонат, имеет следующую структуру:
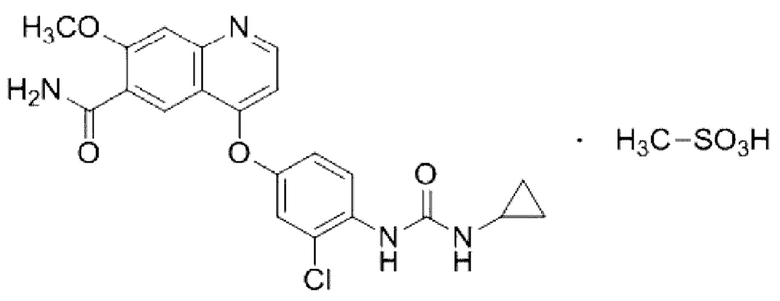
О ленватинибе сообщается в патентах США №№7,253,286; 7,612,208; и 9,006,256; все из которых включены в данное описание посредством ссылки.
Введение комбинации терапевтических средств включает в себя введение индивидуальных терапевтических средств в сочетании в одной композиции или в стандартной лекарственной форме, введение индивидуальных терапевтических средств комбинации одновременно, но по отдельности, или введение индивидуальных средств комбинации последовательно любым подходящим путем введения. Дозировка индивидуальных терапевтических средств комбинации может потребовать более частого введения одного из средств по сравнению с другим средством в комбинации. Следовательно, для обеспечения надлежащей дозировки упакованные фармацевтические продукты могут содержать одну или несколько лекарственных форм, которые содержат комбинацию средств, и одну или несколько лекарственных форм, которые содержат одну из комбинаций средств, но не другое средство(а) комбинации.
Терапевтические средства могут содержать один или несколько асимметричных элементов, таких как стереогенные центры или стереогенные оси, например, асимметричные атомы углерода, так что соединения могут существовать в различных стереоизомерных формах. Такие соединения могут быть, например, рацематами или оптически активными формами. Для соединений с двумя или более асимметричными элементами данные соединения могут дополнительно представлять собой смеси диастереомеров. Для соединений, имеющих асимметричные центры, следует понимать, что все оптические изомеры и их смеси охватываются. Кроме того, соединения с углерод-углеродными двойными связями могут встречаться в Z- и Е-формах; все изомерные формы соединений включены в настоящее изобретение. В данных ситуациях отдельные энантиомеры (оптически активные формы) могут быть получены асимметричным синтезом, синтезом из оптически чистых предшественников или разделением рацематов. Разделение рацематов также может быть достигнуто, например, обычными способами, такими как кристаллизация в присутствии разделительного агента, или хроматография с использованием, например, хиральной ВЭЖХ-колонки.
Комбинации, как сообщалось в данном описании, могут включать варианты осуществления, в которых одно или более из соединения 1 и ленватиниба вводятся в виде фармацевтически приемлемой соли или в виде свободного основания. Не требуется, чтобы оба соединения вводились в виде одной и той же фармацевтически приемлемой соли, но это возможно. В конкретных вариантах осуществления соединение 1 вводится в виде хлористоводородной соли и ленватиниб вводится в виде мезилатной соли.
«Фармацевтически приемлемая соль», как используется в данном описании, относится к кислотно-аддитивным солям или основно-аддитивным солям соединений в настоящем описании. Фармацевтически приемлемая соль представляет собой любую соль, которая сохраняет активность исходного соединения и не оказывает какого-либо чрезмерно вредного или нежелательного воздействия на субъекта, которому ее вводят, и в контексте, в котором ее вводят. Фармацевтически приемлемые соли включают, но не ограничиваются ими, комплексы металлов и соли как неорганических, так и карбоновых кислот.Фармацевтически приемлемые соли также включают соли металлов, таких как алюминий, кальций, железо, магний, марганец и комплексные соли. Кроме того, фармацевтически приемлемые соли включают, но не ограничиваются ими, соли кислот, примеры которых включают уксусную, аспарагиновую, алкилсульфоновую, арилсульфоновую, аксетильную, бензолсульфоновую, бензойную, бикарбоновую, бисульфурную, битартарную, масляную, эдетат кальция, камсиловую (camsylic), угольную, хлорбензойную, лимонную, этилендиаминтетрауксусную, 1,2-этандисульфоновую (edisylic), лаурилсерную (estolic), этансульфоновую кислоту (esyl), этансульфиновую (esylic), муравьиную, фумаровую, глюкогептоновую (gluceptic), глюконовую, глутаминовую, гликолиларсаниловую (glycollylarsanilic), гексамовую (hexamic), гексилрезорциновую (hexylresorcinoic), гидрабаминовую (hydrabamic), бромоводородную, соляную, йодводородную, гидроксинафтойную (hydroxynaphthoic), изэтионовую, молочную, лактобионовую, малеиновую, яблочную, малоновую, миндальную, метансульфоновую, метилазотную, метилсерную, слизевую, муконовую, 2-нафталинсульфоновую (napsylic), азотную, щавелевую, р-нитрометансульфоновую, памоиновую, пантотеновую, фосфорную, двузамещенную соль фосфорной кислоты, однозамещенную соль фосфорной кислоты, фталевую, полигалактуроновую, пропионовую, салициловую, стеариновую, янтарную, сульфаминовую, сульфаниловую, сульфоновую, серную, дубильную, винную, 8-хлортеофиллиновую (teoclic) толуолсульфоновую и тому подобное.
Варианты осуществления могут включать в себя гидрохлоридные соли соединения 1. Фармацевтически приемлемые соли могут быть получены из аминокислот, включая, но не ограничиваясь этим, цистеин. Способы получения соединений в виде солей известны специалистам в данной области (см., например, Stahl et al., Handbook of Pharmaceutical Salts: Properties, Selection, and Use, Wiley-VCH; Verlag Helvetica Chimica Acta, Zurich, 2002; Berge et al., J. Pharm. Sci. 66: 1, 1977).
«Эффективное количество» комбинации терапевтических средств (например, соединения 1 и ленватиниба) представляет собой количество, достаточное для обеспечения заметного терапевтического эффекта по сравнению с базовым уровнем НСС.
Активные средства, описанные в данном описании, могут быть объединены с фармацевтически приемлемым носителем для получения их фармацевтических композиций. Конкретный выбор носителя и композиции будет зависеть от конкретного пути введения, для которого предназначена композиция.
«Фармацевтически приемлемый носитель» в контексте настоящего описания относится к нетоксичному носителю, адъюванту или наполнителю, который не нарушает фармакологическую активность соединения, с которым он образует лекарственный состав. Фармацевтически приемлемые носители, адъюванты или наполнители, которые могут быть использованы в композициях по настоящему изобретению, включают, но не ограничиваются ими, сорбиновую кислоту, сорбат калия, смеси неполных глицеридов насыщенных растительных жирных кислот, воду, соли или электролиты, динатрийгидрофосфат, гидрофосфат калия, хлорид натрия, соли цинка, коллоидный кремнезем, трисиликат магния, поливинилпирролидон, вещества на основе целлюлозы, полиэтиленгликоль, натрий-карбоксиметилцеллюлозу, полиакрилаты, воски, полиэтиленгликоль и шерстяной жир.
Композиции по настоящему изобретению могут быть подходящими для парентерального, перорального введения, ингаляционного спрея, местного, ректального, назального, буккального, вагинального введения или имплантированного введения в резервуаре и т.д. В некоторых вариантах осуществления фармацевтическая композиция содержит ингредиенты, которые получены из природных или неприродных источников. В некоторых вариантах фармацевтическая композиция или носитель могут быть обеспечены в стерильной форме. Неограничивающие примеры стерильного носителя включают не содержащую эндотоксинов воду или апирогенную воду.
Термин «парентеральный», как он использован в данном описании, включает способы подкожной, внутривенной, внутримышечной, внутрисуставной, внутрисиновиальной, интрастеркальной, интратекальной, внутрипеченочной, внутрипочечной и внутричерепной инъекции или инфузии. В конкретных вариантах осуществления соединения вводят внутривенно, перорально, подкожно или посредством внутримышечного введения. Стерильные инъекционные формы композиций по данному изобретению могут представлять собой водную или масляную суспензию. Данные суспензии могут быть составлены в соответствии с методиками, известными в данной области техники, с использованием подходящих диспергирующих или смачивающих средств и суспендирующих средств. Стерильный инъецируемый препарат также может представлять собой стерильный инъекционный раствор или суспензию в нетоксичном парентерально приемлемом разбавителе или растворителе. Приемлемыми носителями и растворителями, которые можно использовать, служат вода, раствор Рингера и изотонический раствор хлорида натрия. Кроме того, стерильные жирные масла обычно используются в качестве растворителя или суспендирующей среды.
Для данной цели можно использовать любое мягкое жирное масло, включая синтетические моно- или диглицериды. Жирные кислоты и их глицеридные производные применимы при приготовлении инъекционных препаратов, как и природные фармацевтически приемлемые масла, такие как оливковое масло или касторовое масло, особенно в их полиоксиэтилированных вариантах. Данные масляные растворы или суспензии могут также содержать спиртовой разбавитель или диспергатор с длинной цепью, такой как карбоксиметилцеллюлоза или аналогичные диспергирующие средства, которые обычно используются в рецептуре фармацевтически приемлемых лекарственных форм, включая эмульсии и суспензии. Другие обычно используемые поверхностно-активные вещества, такие как Tweens, Spans и другие эмульгирующие средства, которые обычно используются при изготовлении фармацевтически приемлемых твердых, жидких или других лекарственных форм, также могут использоваться для целей составления.
Для перорального введения соединение или соль могут быть предоставлены в приемлемой пероральной дозированной форме, включая, без ограничения, капсулы, таблетки, водные суспензии или растворы. В случае таблеток для перорального применения обычно используются носители, включая лактозу и кукурузный крахмал. Также могут быть добавлены смазывающие средства, такие как стеарат магния. Для перорального введения в форме капсул применимые разбавители включают лактозу и высушенный кукурузный крахмал. Когда для перорального применения требуются водные суспензии, активный ингредиент можно комбинировать с эмульгирующими и суспендирующими средствами. При желании, также могут быть добавлены определенные подсластители, ароматизаторы или красители. Кроме того, могут быть добавлены консерванты. Подходящие примеры фармацевтически приемлемых консервантов включают, но не ограничиваются ими, различные антибактериальные и противогрибковые средства, такие как растворители, например, этанол, пропиленгликоль, бензиловый спирт, хлорбутанол, соли четвертичного аммония и парабены (такие как метилпарабен, этилпарабен, пропилпарабен и др.).
Под «немедленным высвобождением» подразумевается обычное высвобождение, при котором высвобождение лекарственного средства начинается сразу после введения. Используемый в данном описании термин «немедленное высвобождение» включает лекарственные формы, которые позволяют лекарству растворяться в желудочно-кишечном содержимом, не имея намерения задерживать или продлевать растворение или всасывание лекарственного средства. Цель состоит в том, чтобы лекарство быстро высвобождалось после введения, например, чтобы было возможно высвободить в тесте на растворение по меньшей мере 80% лекарственного средства в течение приблизительно 30 минут после начала растворения.
Термин «пролонгированное высвобождение» или «замедленное высвобождение» включает лекарственные формы, характеристики которых по времени и/или месту высвобождения выбраны для обеспечения терапевтических целей или удобства, не предлагаемых традиционными лекарственными формами, такими как раствор или лекарственная форма с немедленным высвобождением.
Термин «стационарное состояние» означает, что уровень в плазме для данного активного средства или комбинации активных средств был достигнут и поддерживается последующими дозами активного средства (средств) на уровне, который находится на уровне или выше минимального эффективного терапевтического уровня и ниже минимального токсического уровня в плазме для данного активного средства (средств).
Термин «одна фармацевтическая композиция», используемый в данном описании, относится к одному носителю или наполнителю, приготовленному для доставки эффективных количеств обоих терапевтических средств пациенту. Один носитель предназначен для доставки эффективного количества каждого из средств вместе с любым фармацевтически приемлемым носителем или вспомогательными веществами. В некоторых вариантах осуществления носитель представляет собой таблетку, капсулу, пилюлю или пластырь.
Термин «унифицированная доза» используется в данном описании для обозначения одновременного введения обоих средств вместе, в одной лекарственной форме, пациенту, которого лечат. В некоторых вариантах осуществления унифицированная доза представляет собой одну композицию. В определенных вариантах осуществления унифицированная доза включает один или несколько носителей, так что каждый носитель включает эффективное количество по меньшей мере одного из средств (левантиниба или соединения 1) вместе с фармацевтически приемлемыми носителями и вспомогательными веществами. В некоторых вариантах осуществления унифицированная доза представляет собой одну или несколько таблеток, капсул, пилюль или пластырей, вводимых пациенту одновременно.
Используемый в данном описании термин «диапазон доз» относится к верхнему и нижнему пределам приемлемого изменения количества указанного средства. Обычно, дозу средства в любом количестве в пределах указанного диапазона можно вводить пациентам, подвергающимся лечению.
Термин «лечить» используется в данном описании для обозначения облегчения, уменьшения или ослабления по меньшей мере одного симптома заболевания у субъекта. Например, в отношении НСС, термин «лечить» может означать остановку, задержку начала (то есть период до клинического проявления заболевания или симптома заболевания) и/или снижение риска развития или ухудшения симптома заболевания. Термин «защищать» используется в данном описании для обозначения предотвращения задержки или лечения, или того и другого, сообразно обстоятельствам, развития или продолжения или обострения симптомов заболевания у субъекта.
Термин «субъект» предназначен для обозначения животных, которые могут страдать от НСС или страдают от них. Примеры субъектов включают млекопитающих, например, людей, собак, коров, лошадей, свиней, овец, коз, кошек, мышей, кроликов, крыс и трансгенных животных, не являющихся людьми. В определенных вариантах осуществления субъект представляет собой человека, например, человека, страдающего от НСС, подверженного риску НСС или потенциально способного страдать от НСС.
Термин «около» или «приблизительно», обычно, означает в пределах 20%, более предпочтительно в пределах 10% и наиболее предпочтительно еще в пределах 5% от заданного значения или диапазона. В качестве альтернативы, особенно в биологических системах, термин «около» означает в пределах одной единицы логарифмической шкалы (то есть в пределах одного порядка величины), предпочтительно в два раза от заданного значения.
Использование терминов «а», «an» и «the» для обозначения форм единственного числа и аналогичных ссылок в контексте описания изобретения (особенно в контексте следующей формулы изобретения) должно толковаться как охватывающее как единственное, так и множественное число, если иное не указано в настоящем документе или явно не противоречит контексту. Термины «содержит», «имеющий», «включающий» и «содержащий» следует понимать как открытые термины (то есть означающие «включающий, но не ограничивающийся»), если не указано иное. Перечисление диапазонов значений в данном документе предназначено лишь для того, чтобы служить сокращенным способом индивидуальной ссылки на каждое отдельное значение, попадающее в данный диапазон, если в данном описании не указано иное, и каждое отдельное значение включается в описание, как если бы оно было отдельно указано в данном описании.
Термин «синергетический эффект», как он используется в настоящем документе, относится к действию двух средств, таких как, например, соединение 1 и ленватиниб, оказывающих эффект, например, замедляющий прогрессирование НСС, который больше, чем простая сумма эффектов каждого из препаратов, вводимых по отдельности. Синергетический эффект может быть рассчитан, например, с использованием подходящих способов, таких как уравнение Sigmoid-Emax (Holford, N.Н.G. and Scheiner, L.В., Clin. Pharmacokinet. 6: 429-453 (1981)), уравнение аддитивности Loewe (Loewe, S, and Muischnek, H., Arch. Exp. Pathol Pharmacol. 114: 313-326 (1926)) и уравнение медианного эффекта (Chou, Т.С. and Talalay, P., Adv. Enzyme Regul. 22: 27-55 (1984)). Каждое уравнение, упомянутое выше, может быть применено к экспериментальным данным для создания соответствующего графика, чтобы помочь в оценке эффектов комбинации лекарств. Соответствующие графики, связанные с уравнениями, упомянутыми выше, представляют собой кривую зависимости эффекта от концентрации, кривую изоболограммы и кривую комбинированного индекса, соответственно.
В некоторых вариантах осуществления лечение обеспечивается субъекту, имеющему гепатоцеллюлярную карциному с измененным статусом FGFR4 и/или FGF19 (фактор роста фибробластов 19).
В некоторых вариантах осуществления лечение может включать анализ статуса FGFR4 и/или Fgf19 в биологическом образце, содержащем клетки указанной гепатоцеллюлярной карциномы, или может быть выполнено в сочетании с анализом статуса FGFR4 и/или Fgf19 в биологическом образце, содержащем клетки указанной гепатоцеллюлярной карциномы, и если указанная гепатоцеллюлярная карцинома демонстрирует изменение в FGFR4 и/или Fgf19, лечение субъекта происходит с эффективным для лечения количеством терапевтической комбинации, как описано в данном документе.
Для того чтобы варианты осуществления, описанные в данном документе, могли быть более понятны, изложены следующие примеры. Следует понимать, что данные примеры предназначены только для иллюстративных целей и не должны рассматриваться как ограничивающие.
Способы лечения
Настоящее изобретение относится к комбинированной терапии, применимой для лечения НСС. Как обсуждается ниже, комбинации, обеспеченные в данном документе, могут иметь ряд преимуществ.
Одним из преимуществ комбинации, раскрытой в данном описании, является неожиданный синергический эффект комбинации соединения 1 и ленватиниба при лечении для ингибирования роста опухолей и лечении НСС.
В некоторых вариантах осуществления в настоящем документе обеспечена единая фармацевтическая композиция, содержащая комбинацию соединения 1 и ленватиниба. Преимущество, обеспеченное в данном документе, заключается в синергетическом эффекте, который приводит к лечению НСС по сравнению с лечением однократной дозой любого из препаратов. Когда лекарственные средства предоставляются в виде единичной дозы или единичного препарата, «таблеточная нагрузка (pill burden)», то есть суточное количество принимаемых таблеток, пациента, страдающего НСС, не увеличивается.
Как указано выше, в одном аспекте в данном описании обеспечена комбинация лекарственных средств, применимая для лечения, предотвращения, остановки, задержки начала и/или снижения риска развития или реверсии НСС у млекопитающего, включающая введение указанному млекопитающему комбинированной терапии, содержащей соединение 1 и ленватиниб, вместе в эффективном количестве.
В некоторых вариантах осуществления субъект, подлежащий лечению (например, пациент), определяется как не реагирующий на один или несколько способов лечения НСС или устойчивый к ним, например, к соединению 1. В других вариантах осуществления индивидум, подлежащий лечению, реагирует на терапию соединения 1, но терапия улучшается с введением ленватиниба. Например, пациенту вводят соединение 1 (например, от 50 мг до 600 мг в день, от 200 мг до 400 мг в день или 300 мг в день) в течение некоторого периода времени, например, более одного дня, более двух дней, более трех дней, более одной недели, более одного месяца и т.д. После данного времени пациенту можно назначать ленватиниб в сочетании с соединением 1.
Количество ленватиниба может варьироваться. Например, ленватиниб можно вводить в количестве 8 мг/день или 12 мг/день. Суточная доза может быть частью циклического режима, который длится от 14 дней до 21 дня или дольше. Количество суточной дозы можно вводить в виде единичной дозы или в виде нескольких доз.
Специалист в данной области техники понимает, что эффективная доза активного лекарственного средства может быть ниже, чем фактическое введенное количество. Как таковые, в данном описании обеспечены дозы, необходимые для достижения терапевтической дозы.
В различных вариантах осуществления в настоящем документе обеспечены способы лечения НСС путем введения эффективного количества соединения 1 и ленватиниба индивидууму, имеющему НСС. Количество комбинированных средств эффективно для лечения НСС. В одном варианте осуществления комбинация средств обладает синергетическим эффектом. В одном варианте осуществления, даже если одно или несколько средств, вводимых отдельно в определенной дозировке, могут быть эффективными, при введении в комбинации при той же дозировке каждого средства лечение более эффективно. Например, в одном варианте осуществления комбинация соединения 1 и ленватиниба является более эффективной, чем введение каждого средства по отдельности.
Дозировки
Оптимальная доза комбинации средств для лечения НСС может быть определена эмпирически для каждого индивидуума с использованием известных способов и будет зависеть от множества факторов, включая активность средств; возраст, массу тела, общее состояние здоровья, пол и диету индивидуума; время и путь введения; и другие лекарственные средства, которые принимает индивидуум. Оптимальные дозировки могут быть установлены с использованием обычного тестирования и процедур, которые хорошо известны в данной области техники.
Для комбинированной терапии по настоящему изобретению суточная доза соединения 1 находится в диапазоне от 50 мг до 600 мг. В некоторых вариантах осуществления суточная доза соединения 1 составляет до 600 мг. В определенных вариантах осуществления суточная доза соединения 1 составляет до 400 мг. В различных вариантах осуществления суточная доза соединения 1 составляет до 300 мг. В определенных вариантах осуществления суточная доза соединения 1 составляет от 200 мг до 400 мг. В одном варианте осуществления суточная доза составляет 300 мг.
В некоторых вариантах осуществления суточная доза ленватиниба составляет 8 мг. В определенных вариантах осуществления суточная доза ленватиниба составляет 12 мг. В определенных вариантах осуществления суточная доза ленватиниба составляет от 7 мг до 13 мг. В определенных вариантах осуществления суточная доза лентабиниба составляет от 8 мг до 12 мг.
Время введения может быть выбрано таким, чтобы оба лекарственных средства вводились одновременно, по отдельности или последовательно, либо утром, либо ночью. В качестве альтернативы, одно лекарственное средство можно вводить утром и вечером. В определенных вариантах осуществления оба лекарственных средства могут вводиться в виде одной таблетки, капсулы, пилюли, пластыря или желе, один раз в день, утром или ночью.
Количество комбинированных средств, которые можно объединять с носителями для получения единичной дозированной формы, будет варьироваться в зависимости от индивидуума, которого лечат, и конкретного способа введения. В некоторых вариантах осуществления унифицированные лекарственные формы, содержащие комбинацию средств, как описано в данном документе, будут содержать количества каждого средства комбинации, которые обычно вводят, когда средства вводятся по отдельности.
Фармацевтические композиции и пути введения
В данном документе обеспечены фармацевтические композиции, содержащие комбинацию средств для лечения НСС. Фармацевтические композиции могут дополнительно содержать носитель или вспомогательное вещество, стабилизатор, ароматизатор и/или краситель.
Комбинация средств может быть введена с использованием различных путей введения, известных специалисту в данной области техники. Пути введения включают пероральное введение. В определенных вариантах осуществления фармацевтическую композицию, содержащую комбинацию средств, можно принимать перорально в форме жидкости, сиропа, таблетки, капсулы, порошка, обсыпки, жевательной резинки или растворимого диска. В качестве альтернативы, фармацевтические композиции по настоящему изобретению можно вводить внутривенно или трансдермально. Специалистам в данной области техники известны дополнительные пути введения (см., например, Remington's Pharmaceutical Sciences, Gennaro A.R., Ed., 20.sup.th Edition, Mack Publishing Co., Easton, Pa.).
В некоторых вариантах соединение 1 и ленватиниб составлены в виде пасты, желе или суспензии. Например, лекарственные средства растворяют, захватывают или суспендируют в форме частиц лекарственного средства, микрокапсулированных частиц или частиц лекарственное средство-полимер в желатиновом растворе или полутвердом веществе. Преимущество перорального желеобразного композиции состоит в том, что лекарственные средства легче вводить пациентам, которым трудно глотать таблетки, капсулы или пилюли. В определенных вариантах осуществления оба средства тщательно перемешивают и суспендируют в подходящей среде для образования пасты или геля. Добавочные средства необязательно могут быть смешаны для придания аромата при пероральном введении. Арахисовое масло или альгинат, приправленные малиной и подсластителем, являются примерами многих подходящих средств, маскирующих вкус. В различных вариантах осуществления паста или желе также могут быть приготовлены с подходящими связующими или вспомогательными веществами, известными в данной области техники для местного применения.
Способы получения композиций с замедленным высвобождением в форме таблеток, капсул или пилюль известны в данной области техники. В некоторых вариантах осуществления композицию с замедленным высвобождением получают, покрывая активный ингредиент лекарственного средства полимером, предпочтительно нерастворимым в воде полимером. Например, нерастворимый в воде полимер, используемый в фармацевтической области в качестве покрывающего средства с замедленным высвобождением, кишечнорастворимого покрывающего средства или желудочного покрывающего средства. Нерастворимый в воде полимер может включать, например, этилцеллюлозу, очищенный шеллак, белый шеллак, аминоалкил-метакрилатный сополимер RS, фталат гидроксипропилметилцеллюлозы, ацетатсукцинат гидроксипропилметилцеллюлозы, карбоксиметилэтилцеллюлозу, ацетатфталат целлюлозы, сополимер метакриловой кислоты L, сополимер метакриловой кислоты LD, сополимер метакриловой кислоты S, аминоалкил-метакрилатный сополимер Е или диэтиламиноацетат полив инилацеталя.
Тип, степень замещения и молекулярная масса нерастворимых в воде полимеров могут зависеть от растворимости активного ингредиента в воде или спирте, желаемого уровня замедленного высвобождения и тому подобного. Нерастворимые в воде полимеры можно использовать отдельно или в комбинации. Кроме того, могут быть включены гидрогенизированное масло, стеариновая кислота или цетанол в качестве вспомогательного покрытия и триглицерид с цепью средней длины, триацетин, триэтилцитрат или цетанол в качестве пластификатора.
В некоторых вариантах осуществления композиция с замедленным высвобождением представляет собой таблетку или гранулу матричного типа. Активный ингредиент может быть покрыт до 3 различных типов полимеров. Данные три различных типа полимеров могут включать: 1) нерастворимый в воде полимер, такой как этилцеллюлоза; 2) рН-независимый гелеобразующий полимер, такой как гидроксипропилметилцеллюлоза; и 3) рН-зависимый гелеобразующий полимер, такой как альгинат натрия. Данные три различных типа полимеров можно использовать вместе для ослабления скорости высвобождения лекарств.
Лекарственные формы: свойства высвобождения
Композиции с замедленным высвобождением могут достигать определенной степени устойчивого эффекта. Однако воздействие и/или биологическая доступность активного ингредиента могут варьироваться в зависимости от множества факторов, таких как, например, интервал поглощения, носители или вспомогательные вещества, используемые в композиции, способ доставки композиции и/или время прохождения активного ингредиента через желудочно-кишечный тракт пациента.
Комбинированная терапия может содержать по меньшей мере одну часть с замедленным высвобождением для выполнения функции замедленного высвобождения и одну часть с немедленным высвобождением для выполнения функции немедленного высвобождения. В некоторых вариантах осуществления, когда комбинированная терапия представляет собой единичную лекарственную форму, она может быть в виде таблеток, образованных из смеси гранул с замедленным высвобождением, составляющих часть с замедленным высвобождением, и гранул с немедленным высвобождением, составляющих часть с немедленным высвобождением, препарата капсулы, полученного путем наполнения капсулы гранулами замедленного высвобождения и гранулами немедленного высвобождения, или в виде таблеток с покрытием, нанесенным прессованием, в которых внешний слой, составляющий часть немедленного высвобождения, сформирован на внутреннем ядре, составляющем часть замедленного высвобождения. Однако нет никаких ограничений для вышеупомянутых вариантов осуществления.
Кроме того, нет особых ограничений в отношении состояния содержания каждого лекарственного средства в композиции или в части с немедленным высвобождением или в части с замедленным высвобождением; соединение 1 может быть равномерно диспергировано в композиции, части с немедленным высвобождением или части с замедленным высвобождением, или может содержаться только в одной части композиции, части с немедленным высвобождением или части с замедленным высвобождением, или может содержаться так, что существует градиент концентрации.
Часть с замедленным высвобождением в композиции по настоящему изобретению может содержать по меньшей мере одно независимое от рН полимерное вещество или зависимое от рН полимерное вещество для контроля высвобождения лекарственного средства.
Используемое в данном описании независимое от рН полимерное вещество может содержать полимерное вещество, состояние заряда которого практически не изменяется в условиях рН, обычно встречающихся в желудочно-кишечном тракте, в частности, в диапазоне от рН 1 до рН 8. Это означает, например, полимерное вещество, которое не имеют функциональных групп, состояние заряда которых изменяется в зависимости от рН, таких как основные функциональные группы, такие как аминогруппы, или кислотные функциональные группы, такие как группы карбоновых кислот. Следует отметить, что независимое от рН полимерное вещество может быть включено для придания композиции в соответствии с настоящим изобретением функции замедленного высвобождения, но также может быть включено для другой цели. Кроме того, независимое от рН полимерное вещество, используемое в настоящем изобретении, может быть нерастворимым в воде или может набухать в воде или растворяться в воде с образованием геля.
Примеры нерастворимых в воде независимых от рН полимерных веществ включают, но не ограничиваются ими, простые эфиры целлюлозы, сложные эфиры целлюлозы и сополимеры метакриловой кислоты и акриловой кислоты (торговое наименование Eudragit, производимые Rohm GmbH & Co. KG, Darmstadt, Germany). Примеры включают, но не ограничиваются ими, алкиловые эфиры целлюлозы, такие как этилцеллюлоза (торговое наименование Ethocel, производимые Dow Chemical Company, USA), этилметилцеллюлоза, этилпропилцеллюлоза или изопропилцеллюлоза и бутилцеллюлоза, целлюлозо-аралкиловые эфиры, такие как бензилцеллюлоза, целлюлозо-цианоалкиловые эфиры, такие как цианоэтилцеллюлоза, эфиры целлюлозы и органических кислот, такие как ацетатбутират целлюлозы, ацетат целлюлозы, пропионат целлюлозы или бутират целлюлозы и пропионат-ацетат целлюлозы, этилакрилат-метилметакрилатные сополимеры (торговое наименование Eudragit NE, производимые Rohm GmbH & Co. KG, Darmstadt, Germany) и аминоалкил-метакрилатный сополимер RS (торговые наименования Eudragit RL, Eudragit RS). He существует особых ограничений в отношении среднего диаметра частиц нерастворимого в воде полимера, используемого в настоящем изобретении, но, обычно, чем ниже данный средний диаметр частиц, тем лучше рабочие характеристики, причем средний диаметр частиц предпочтительно составляет от 0,1 до 100 мкм, более предпочтительно от 1 до 50 мкм, особенно предпочтительно от 3 до 15 мкм, наиболее предпочтительно от 5 до 15 мкм. Кроме того, примеры водорастворимых или набухающих в воде независимых от рН полимерных веществ включают, но не ограничиваются ими, полиэтиленоксид (торговое наименование Polyox, производство Dow Chemical Company, молекулярный вес от 100000 до 7000000), низкозамещенную гидроксипропилцеллюлозу (торговое наименование L-HPC, производство Shin-Etsu Chemical, Japan), гидроксипропилцеллюлозу (торговое наименование НРС, производство Nippon Soda, Co., Ltd, Japan), гидроксипропилметилцеллюлозу (торговые наименования Metolose 60SH, 65SH, 90SH, выпускаемые Shin-Etsu Chemical, Japan) и метилцеллюлозу (торговое наименование Metolose SM, производство Shin-Etsu Chemical, Japan).
В некоторых вариантах осуществления в композиции может содержаться одно независимое от рН полимерное вещество или может содержаться множество независимых от рН полимерных веществ. Независимое от рН полимерное вещество, если оно используется в вариантах осуществления, описанных в настоящем документе, может представлять собой нерастворимое в воде полимерное вещество, более предпочтительно этилцеллюлозу, этилакрилат-метилметакрилатный сополимер (торговое наименование Eudragit NE) или аминоалкил-метакрилатный сополимер RS (торговое наименование Eudragit RL, Eudragit RS). Особенно предпочтительным является по меньшей мере одно из этилцеллюлозы и аминоалкилметакрилатного сополимера RS. Наиболее предпочтительной является этилцеллюлоза. Нет особых ограничений на количество независимого от рН полимерного вещества, содержащегося в композиции; данное количество может быть скорректировано соответствующим образом в соответствии с целью, такой как контроль замедленного высвобождения лекарственного средства.
Зависимое отрН полимерное вещество, которое можно использовать в описанных в данном документе вариантах осуществления, может представлять собой полимерное вещество, состояние заряда которого изменяется в условиях рН, обычно встречающихся в желудочно-кишечном тракте, в частности, в диапазоне от рН 1 до рН 8. Это означает, например, полимерное вещество, имеющие функциональные группы, состояние заряда которых изменяется в зависимости от рН, такие как основные функциональные группы, такие как аминогруппы, или кислотные функциональные группы, такие как группы карбоновых кислот. Зависимые от рН функциональные группы зависимого от рН полимерного вещества предпочтительно представляют собой кислотные функциональные группы, причем зависимое от рН полимерное вещество наиболее предпочтительно имеет группы карбоновых кислот.
Зависимое от рН полимерное вещество, используемое в настоящем изобретении, может быть нерастворимым в воде или может набухать в воде или растворяться в воде с образованием геля. Примеры зависимых от рН полимерных веществ, используемых в настоящем изобретении, включают, но не ограничиваются ими, энтеросолюбильные полимерные вещества. Примеры энтеросолюбильных полимерных веществ включают, но не ограничиваются ими, сополимеры метакриловой кислоты и метилметакрилата (Eudragit L100, Eudragit S100, производимые Rohm GmbH & Co. KG, Darmstadt, Germany), сополимеры метакриловой кислоты и этилакрилата (Eudragit L100- 55, Eudragit L30D-55, производимые Rohm GmbH & Co. KG, Darmstadt, Germany), фталат гидроксипропилметилцеллюлозы (HP-55, HP-50, производства Shin-Etsu Chemical, Japan), ацетат сукцинат гидроксипропилметилцеллюлозы (AQOAT) производства Shin-Etsu Chemical, Japan), карбоксиметилэтилцеллюлозу (СМЕС, производства Freund Corporation, Japan) и ацетат фталат целлюлозы.
Примеры зависимых от рН полимерных веществ, которые набухают в воде или растворяются в воде с образованием геля, включают, но не ограничиваются ими, альгиновую кислоту, пектин, карбоксивиниловый полимер и карбоксиметилцеллюлозу. В настоящем изобретении в композицию может быть включено одно зависимое от рН полимерное вещество или может содержаться множество зависящих от рН полимерных веществ, зависимое от рН полимерное вещество, используемое в настоящем изобретении, предпочтительно представляет собой энтеросолюбильное полимерное вещество, более предпочтительно, сополимер метакриловой кислоты и этилакрилата, сополимер метакриловой кислоты и метилметакрилата, фталат гидроксипропилметилцеллюлозы или ацетат-сукцинат гидроксипропилметилцеллюлозы, особенно предпочтительно сополимер метакриловой кислоты и этилакрилата.
При использовании зависимого от рН полимерного вещества в процессе изготовления композиции в соответствии с настоящим изобретением, коммерчески доступный продукт порошкового или гранулированного типа или суспензионного типа, в котором диспергировано зависимое от рН полимерное вещество в качестве растворителя, заранее можно использовать как есть, или такой коммерчески доступный продукт можно использовать диспергированным в воде или органическом растворителе. Чем меньше диаметр частиц рН-зависимого полимерного вещества, тем лучше рабочие характеристики, причем зависимое от рН полимерное вещество предпочтительно относится к порошковому типу. В случае сополимера метакриловой кислоты и этилакрилата примером является Eudragit L100-55. Нет особых ограничений на средний диаметр частиц зависимого от рН полимерного вещества, используемого в настоящем изобретении, но средний диаметр частиц предпочтительно составляет от 0,05 до 100 мкм, более предпочтительно от 0,05 до 70 мкм, наиболее предпочтительно от 0,05 до 50 мкм. Кроме того, нет особых ограничений на количество зависимого от рН полимерного вещества, например, в случае энтеросолюбильного полимерного вещества, количество обычно составляет от 0,1 до 90 массовых частей, предпочтительно от 1 до 70 массовых частей, более предпочтительно от 5 до 60 массовых частей, особенно предпочтительно от 10 до 50 массовых частей в расчете на 100 массовых частей композиции.
Комбинированная терапия в соответствии с вариантами осуществления, описанными в данном документе, может дополнительно содержать любую из различных добавок, таких как любой из различных фармакологически приемлемых носителей, таких как разбавители, смазочные вещества, связующие вещества и дезинтегранты, а также консерванты, красители, подсластители, пластификаторы, средства пленочного покрытия и так далее, по мере необходимости. Примеры разбавителей включают в себя, но не ограничиваются ими, лактозу, маннит, двухосновный фосфат кальция, крахмал, преэгатинизированный крахмал, кристаллическую целлюлозу, легкий кремниевый ангидрид, синтетический силикат алюминия, метасиликат алюмината магния или тому подобное. Примеры смазывающих веществ включают, но не ограничиваются ими, стеарат магния, стеарат кальция, тальк, стеарилфумарат натрия или тому подобное. Примеры связующих включают, но не ограничиваются ими, гидроксипропилцеллюлозу, метилцеллюлозу, натрийкарбоксиметилцеллюлозу, гидроксипропилметилцеллюлозу, поливинилпирролидон или тому подобное. Примеры дезинтеграторов включают, но не ограничиваются ими, карбоксиметилцеллюлозу, карбоксиметилцеллюлозу кальция, кроскармеллозу натрия, карбоксиметилкрахмал натрия, низкозамещенную гидроксипропилцеллюлозу или тому подобное. Примеры консервантов включают, но не ограничиваются ими, сложные эфиры параоксибензойной кислоты, хлорбутанол, бензиловый спирт, фенетиловый спирт, дегидроуксусную кислоту, сорбиновую кислоту или тому подобное. Предпочтительные примеры красителей включают, но не ограничиваются ими, нерастворимые в воде красочные пигменты, природные пигменты (например, β-каротин, хлорофилл, красный оксид железа), желтый оксид железа, красный оксид железа, черный оксид железа или тому подобное. Предпочтительные примеры подсластителей включают, но не ограничиваются ими, натриевый сахарин, дикалиевый глицирризат, аспартам, стевию или тому подобное. Примеры пластификаторов включают, но не ограничиваются ими, сложные эфиры глицерина и жирных кислот, триэтилцитрат, пропиленгликоль, полиэтиленгликоль или тому подобное. Примеры средств для пленочного покрытия включают, но не ограничиваются ими, гидроксипропилметилцеллюлозу, гидроксипропилцеллюлозу или тому подобное.
Способы изготовления
Для изготовления вариантов осуществления, описанных в настоящем документе, можно использовать один стандартный способ или комбинацию стандартных способов. Например, при изготовлении гранул, содержащих лекарственное средство, в виде части с замедленным высвобождением или части с немедленным высвобождением, грануляция является основной операцией, но это может сочетаться с другими операциями, такими как смешивание, сушка, просеивание и классификация. В качестве способа грануляции служит, например, способ влажной грануляции, при котором к порошку добавляют связующее и растворитель и проводят грануляцию, способ сухой грануляции, при котором порошок сжимают под давлением и проводят грануляцию, способ грануляции расплава, при котором добавляют связующее, которое плавится при нагревании, и проводят нагревание и грануляцию или тому подобное.
Кроме того, в соответствии со способом грануляции, может быть использован такой рабочий способ, как способ грануляции с перемешиванием с использованием планетарного миксера, шнекового смесителя или тому подобного, способ грануляции с быстрым перемешиванием с использованием миксера Henschel, супермиксера или тому подобного, способ экструдирования гранулята с использованием цилиндрического гранулятора, роторного гранулятора, шнекового экструдера, гранулятора гранулирующего типа или тому подобного, способ влажной грануляции с высоким сдвиговым усилием, способ грануляции в псевдоожиженном слое, способ грануляции под давлением, способ грануляции с дроблением или способ грануляции с распылением. После грануляции можно проводить сушку с использованием сушилки, псевдоожиженного слоя или тому подобного, крекинга и просеивания, чтобы получить гранулы или мелкие гранулы для использования. Кроме того, при приготовлении композиции по настоящему изобретению может быть использован растворитель для грануляции. Нет особых ограничений в отношении такого растворителя для грануляции, который может представлять собой воду или любой из различных органических растворителей, например, воду, низший спирт, такой как метанол или этанол, кетон, такой как ацетон или метилэтилкетон, метиленхлорид или их смесь.
Для гранул с замедленным высвобождением, содержащихся в вариантах осуществления, по меньшей мере одно лекарственное средство и по меньшей мере одно соединение, выбранное из независимых от рН полимерных веществ и зависимых от рН полимерных веществ, смешивают вместе, разбавитель и связующее добавляют по необходимости и проводят грануляцию для получения сыпучего вещества. Полученное гранулированное вещество сушат с использованием лотковой сушилки, сушилки с псевдоожиженным слоем или тому подобного, и проводят просеивание с использованием мельницы или генератора, в результате чего могут быть получены гранулы с замедленным высвобождением. В качестве альтернативы, как способ изготовления гранул с замедленным высвобождением в настоящем изобретении, можно добавить по меньшей мере одно лекарственное средство, по меньшей мере одно, выбранное из независимых от рН полимерных веществ и зависимых от рН полимерных веществ, и, при необходимости, разбавитель и связующее вещество с использованием сухого уплотнителя, такого как роликовый уплотнитель или таблетировочная машина для слизи, и выполнить формование прессованием во время смешивания, а затем провести грануляцию путем крекинга до подходящего размера. Гранулированный материал, полученный с использованием такого гранулятора, может быть использован как есть в виде гранул или мелких гранул в соответствии с настоящим изобретением или может быть дополнительно подвергнут крекингу с использованием силовой мельницы, валкового гранулятора, роторной мельницы и т.п. и просеян с получением гранул с замедленным высвобождением. Обратите внимание, что гранулы с немедленным высвобождением могут быть изготовлены так же, как и гранулы с замедленным высвобождением.
Формованный прессованием продукт может быть изготовлен в виде содержащей лекарственное средство части с замедленным высвобождением или части с немедленным высвобождением, или в виде композиции, описанной в данном описании, с использованием одного стандартного способа или комбинации стандартных способов. Например, используются по меньшей мере одно лекарственное средство, по меньшей мере одно соединение, выбранное из независимых от рН полимерных веществ и зависимых от рН полимерных веществ, разбавитель, такой как маннит или лактоза, связующее вещество, такое как поливинилпирролидон или кристаллическая целлюлоза, дезинтегратор, такой, как кармеллоза натрия или кросповидон, и смазывающее вещество, такое как стеарат магния или тальк, и проводится таблетирование с использованием обычного способа, в результате чего может быть получен прессованный продукт. В данном случае таблетирование является основной операцией в способе изготовления прессованного продукта, но это может сочетаться с другими операциями, такими как смешивание, сушка, формирование сахарного покрытия и нанесение покрытия.
Примеры способа таблетирования включают в себя, но не ограничиваются этим, прямое прессование в форме, при котором по меньшей мере одно лекарственное средство и фармакологически приемлемые добавки смешиваются вместе, а затем смесь прессуется непосредственно в таблетки с использованием машины для таблетирования, и сжатие сухих гранул или сжатие влажных гранул, при котором гранулы с замедленным высвобождением или гранулы с немедленным высвобождением в соответствии с настоящим изобретением подвергаются формованию прессованием после добавления смазки или разрыхлителя, если необходимо. Нет особых ограничений на машину для таблетирования, используемую при прессовании; например, можно использовать таблетировочную машину с одним пуансоном, ротационную таблетировочную машину или таблетировочную машину с нанесением прессованного покрытия.
Содержащие лекарственное средство гранулы с замедленным высвобождением или гранулы с немедленным высвобождением, или формованный прессованием продукт в соответствии с представленными в данном описании вариантами осуществления могут использоваться как композиция в виде гранул или таблетки, но также могут подвергаться дополнительной обработке для изготовления композиции. Например, на формованный прессованием продукт или гранулы можно нанести пленочное покрытие с использованием материала основы пленки, такого как этилцеллюлоза, казеин, метилцеллюлоза, гидроксипропилметилцеллюлоза, сополимер метакриловой кислоты L, фталат ацетат целлюлозы, шеллак или тому подобное, или нанести сахарное покрытие с использованием сахарной жидкости для покрытия, содержащей сахарозу, сахарный спирт, порошок гуммиарабика, тальк или тому подобное, с получением таблеток с пленочным покрытием или таблеток с сахарным покрытием. Одним из растворителей в данной технологии нанесения покрытия может быть очищенная вода, но также можно использовать органический растворитель, такой как спирт, кетон, простой эфир или хлорированный углеводород, или их смесь. Например, этанол, ацетон, метиленхлорид или тому подобное можно использовать в качестве органического растворителя. Кроме того, в качестве устройства для нанесения покрытия может быть использовано устройство, обычно используемое в способах нанесения покрытия для изготовления лекарственных средств, с примерами, включающими устройство для нанесения покрытия распылением, в котором нанесение покрытия осуществляется путем распыления жидкости для нанесения покрытия или тому подобного, и псевдоожиженный слой ротора гранулятор для наслоения.
В случае изготовления капсульных препаратов, капсульные препараты могут быть изготовлены путем заполнения гранул с замедленным высвобождением или гранул с немедленным высвобождением, как указано выше, или мини-таблеток в твердые желатиновые капсулы или капсулы НРМС с использованием автоматической машины для заполнения капсул. В качестве альтернативы, в случае препаратов, предназначенных для введения через трубку, или сухого сиропа, который используется в смеси с водой или тому подобным при употреблении, гранулы замедленного высвобождения или гранулы немедленного высвобождения, как указано выше, могут быть смешаны с загустителем или диспергатором, чтобы диспергировать данные гранулы, причем смесь затем преобразуется в гранулы или таблетки. Кроме того, жидкость или желе могут быть приготовлены с использованием воды и веществ, выбранных из диспергаторов, эмульгаторов, загустителей, консервантов, регуляторов рН, подсластителей, ароматизаторов, ароматизаторов и так далее. Тем не менее, в отношении других способов изготовления, нет никаких ограничений для вышеизложенного.
Для того чтобы варианты осуществления, описанные в данном документе, могли быть более понятны, изложены следующие примеры. Следует понимать, что данные примеры предназначены только для иллюстративных целей и не должны рассматриваться как ограничивающие.
ПРИМЕРЫ
Материалы и способы
Соединения и лекарственные средства
Соединение 1 представляет собой селективный перорально биодоступный низкомолекулярный ингибитор FGFR4, который разрабатывается фирмой Н3 Biomedicine. Ленватиниб представляет собой одобренный FDA ингибитор множественных рецепторов тирозинкиназ. Ленватиниб вводили в виде мезилатной соли, и соединение 1 вводили в виде свободного основания.
Протестированные клеточные линии
Использованная клеточная линия, Нер3В (также называемая НЕР3В.1-7), была получена из Американской коллекции типовых культур (American Type Culture Collection (АТСС)), проверена на отсутствие микобактериального загрязнения и подтверждена на идентичность с помощью короткого тандемного повторного анализа 9 маркеров.
Создание ксенотрансплантата Нер3В
Для ксенотрансплантатов линии клеток Нер3В гепатоцеллюлярной карциномы человека клетки Нер3В культивировали в среде RPMI1640, содержащей 10% FBS при 37°С в атмосфере 5% CO2, и хранили в фазе экспоненциального роста. Для сбора клетки промывали PBS, инкубировали с 0,25% трипсин-ЭДТА и суспендировали в 1:1 смеси среды RPMI1640, содержащей 10% FBS. Для приготовления инокулята в конечной концентрации 5×107 клеток/мл клетки осаждали и ресуспендировали в RPMI1640 и Matrigel (Coming). Для получения ксенотрансплантатов 0,1 мл инокулята инъецировали подкожно в область правого бока самок мышей BALB/c nu/nu, приблизительно 8-недельного возраста, массой от 18 до 20 г, что дало конечную концентрацию 5×106 клеток/мышь.
Создание полученного от пациента ксенотрансплантата (patient derived xenograft (PDX)) LIX125
Модель LIX125 первичной гепатоцеллюлярной карциномы человека от ChemPartner (shangpharma.com) была имплантирована самкам мышей с тяжелым комбинированным иммунодефицитом (severe combined immunodeficiency (SCID)). Когда опухоли развивались у мышей, их умерщвляли и резецированные опухоли имплантировали самкам мышей NU/NU для сохранения опухоли, гистологического диагноза и исследования эффективности in vivo. Твердые опухолевые ткани освобождали от некротических компонентов, разрезали на кусочки массой от 10 до 15 мг и смешивали. От трех до пяти кусочков смешивали с от 15 до 30 мл Matrigel и имплантировали в бок мышам линии NU/NU с ослабленным иммунитетом в возрасте от 6 до 8 недель массой от 18 до 20 г. Все первичные опухоли, использованные в данном исследовании, проходили от 3 до 5 пассажей in vivo, и гистологию опухоли из каждого пассажа сохраняли в течение серийной трансплантации.
Дозирование и измерение противоопухолевой активности
Когда средний объем опухоли (tumor volume (TV)) достигал приблизительно 170 мм3 (через 10 дней после имплантации), мышей отбирали на основе их TV и сортировали по нескольким группам лечения по 8 животных на группу. Per os (РО) лечение соединением 1 (300 мг/кг для Нер3В и 500 мг/кг для LIX125), отдельно или в сочетании с носителем ленватиниба (контроль) или ленватинибом (10 мг/кг или 3 мг/кг), вводили один раз в день (QD). Дополнительные группы включали лечение ленватинибом (10 мг/кг или 3 мг/кг) в сочетании с носителем соединения 1. (Носитель ленватиниба включает носитель, в котором вводят ленватиниб; но без ленватиниба. Аналогично, носитель соединения 1 включает носитель, в котором вводят соединение 1; но без соединения 1.)
Объем введения (0,1 мл/10 г массы тела) рассчитывали из массы тела отдельной мыши (body weight (BW)) перед введением. Массу тела измеряли ежедневно, и измерения опухолей проводили два раза в неделю. Мышей с потерей массы тела >20% по сравнению с массой тела в день 1 или опухолями с самым длинным диаметром >2000 мм немедленно подвергали эвтаназии, чтобы предотвратить любую боль или страдания животного.
Объем опухоли (TV) в мм3 рассчитывали по следующей формуле: TV = длина × ширина2 × 0,5, где длина представляла собой самую длинную ось (мм), а ширина представляла собой измерение под прямыми углами относительно длины (мм). % ингибирования роста опухоли (tumor growth inhibition (TGI)) рассчитывали по следующей формуле: % ингибирования роста опухоли (TGI) = [(средний контрольный TV на день X - TV при лечении на день Х)/(средний контрольный TV на день X)] × 100, где день X представлял собой любой день лечения. Противоопухолевые эффекты лечения, частичную регрессию (PR) и полную регрессию (CR), стабильное заболевание (SD) и прогрессирующее заболевание (PD) определяли следующим образом:
PD: 3 последовательных измерения >120% от начального объема или 3 последовательных увеличивающихся измерения от лучшего ответа; SD: 3 последовательных измерения >50% и <120% от начального объема; PR: 3 последовательных измерения <50% от начального объема; CR: 3 последовательных измерения <30 мм3.
Статистический анализ
Данные представляют собой среднее ± стандартная ошибка (SEM) для объема опухоли (N=8). Различия в TV между группами анализировали с помощью нескольких непарных t-тестов, значимость которых определяли с помощью способа Холма-Сидака. Статистический анализ был выполнен с использованием GraphPad Prism версии 7 (GraphPad Software, La Jolla, CA).
Результаты
Пример 1. Исследование in vivo ксенотрансплантата клеток Нер3В
Чтобы определить, усиливает ли ленватиниб ингибирование роста опухоли (TGI), вызываемое соединением 1, клеточную линию Нер3В выращивали в виде ксенотрансплантата у самок мышей nude с ослабленным иммунитетом. Несущим опухоль мышам вводили перорально ежедневно в течение 53 дней (а) 300 мг/кг соединения 1 в качестве единственного средства с носителем ленватиниба; (b)(i) 10 мг/кг ленватиниба в качестве единственного средства с носителем соединения 1; (b)(ii) 3 мг/кг ленватиниба в качестве единственного средства с носителем соединения 1; (c)(i) 300 мг/кг соединения 1 и 10 мг/кг ленватиниба в комбинации; или (c)(ii) 300 мг/кг соединения 1 и 3 мг/кг ленватиниба в комбинации. Результаты показаны на ФИГ. 1.
Соединение 1 в качестве единственного средства в дозе 300 мг/кг приводило к ингибированию роста опухоли с 81% TGI, по сравнению с контрольным носителем (Р<0,00001). Ленватиниб в качестве единственного средства в дозе 10 мг/кг, ингибировал рост опухоли с 58% TGI по сравнению с контрольными носителями (Р<0,00005). Ленватиниб, в качестве единственного средства, в дозе 3 мг/кг ингибировал рост опухоли в данной модели Нер3В с 23% TGI по сравнению с контрольными носителями (Р>0,05). Комбинация 300 мг/кг соединения 1 и 10 мг/кг ленватиниба приводила к усилению ингибирования роста опухоли по сравнению с группами единичных средств с 98% TGI (Р<0,00001). Комбинация 300 мг/кг соединения 1 и 3 мг/кг ленватиниба также приводила к усилению ингибирования роста опухоли по сравнению с группами единственных средств с 97% TGI. (Р<0,00001). Полученные данные демонстрируют, что ленватиниб может усиливать противоопухолевые эффекты соединения 1.
Лечение соединением 1 в качестве единственного средства вызвало 2/8 SD и 6/8 PD в данной модели. Лечение с 10 мг/кг ленватиниба в качестве единственного средства вызвало 8/8 PD в данной модели. Лечение с 3 мг/кг ленватиниба в качестве единственного средства вызвало 8/8 PD в данной модели. Лечение с помощью соединения 1 в комбинации с ленватинибом в дозе 10 мг/кг вызвало 4/8 CR и 4/8 SD в данной модели. Лечение с помощью соединения 1 в комбинации с ленватинибом в дозе 3 мг/кг вызвало 3/8 CR и 5/8 SD в данной модели.
Все группы с комбинированным дозированием хорошо переносили лечение на основании измерений массы тела и рутинных клинических наблюдений.
Пример 2: In vivo исследование PDX ксенотрансплантата. Поддержание клеточной линии
Чтобы определить, усиливает ли ленватиниб ингибирование роста опухоли (TGI) с помощью соединения 1 на моделях PDX, самкам мышей NU/NU инокулировали подкожно в правый бок фрагменты LIX125, модели ксенотрансплантата, полученного у пациента с гепатоцеллюлярной карциномой (PDX). Когда объемы опухолей LTX125 составили от 100 до 300 мм3, животных рандомизировали в шесть различных групп по восемь животных в каждой группе. Мышей, несущих опухоль, перорально обрабатывали ежедневно в течение 32 дней с (а) 500 мг/кг соединения 1 в качестве единственного средства с носителем ленватиниба; (b)(i) 10 мг/кг ленватиниба в качестве единственного средства с носителем соединения 1; (b)(ii) 3 мг/кг ленватиниба в качестве единственного средства с носителем соединения 1; (c)(i) 500 мг/кг соединения 1 и 10 мг/кг ленватиниба в комбинации; или (c)(ii) 500 мг/кг соединения 1 и 3 мг/кг ленватиниба в комбинации; (d) носителем соединения 1 и носителем ленватиниба. Результаты показаны на ФИГ. 2.
Ленватиниб, как единственное средство, значительно ингибировал рост опухоли при дозе 10 мг/кг, но не при дозе 3 мг/кг (р<0,0007 и р>0,05, соответственно) по сравнению с контрольным носителем, с 72% и 44% TGI, соответственно. Соединение 1 как единственное средство в дозе 500 мг/кг существенно не ингибировало рост опухоли (р>0,05) по сравнению с контрольными носителями, с 60% TGI.
Комбинация 500 мг/кг соединения 1 и 10 мг/кг ленватиниба привела к значительному усилению ингибирования роста опухоли (р<0,005) по сравнению с 500 мг/кг соединения 1, взятого по отдельности, с TGI 94%. Данная комбинация привела к SD у 3/8 животных, PR у 4/8 животных и PD у 1/8 животных. Комбинация 500 мг/кг соединения 1 и 3 мг/кг ленватиниба не привела к значительному усилению ингибирования роста опухоли (р>0,05) по сравнению с 500 мг/кг соединения 1, взятого по отдельности, с 78% TGI. Данная комбинация привела к SD у 2/8 животных и PD у 6/8 животных. В целом, комбинация хорошо переносится.
В соответствии с представлением о том, что ленватиниб может усиливать эффект соединения 1 в моделях НСС, дополнительное тестирование на большем количестве моделей, полученных от пациентов с НСС, показало улучшение у 4/6 моделей. Все упомянутые в данном описании модели PDX являются РОП9-экспрессирующими.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМБИНИРОВАННАЯ ТЕРАПИЯ ДЛЯ ЛЕЧЕНИЯ ГЕПАТОЦЕЛЛЮЛЯРНОЙ КАРЦИНОМЫ | 2017 |
|
RU2769251C2 |
| КРИСТАЛЛИЧЕСКИЙ ИНГИБИТОР FGFR4 И ЕГО ПРИМЕНЕНИЕ | 2016 |
|
RU2763328C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ОПУХОЛИ | 2018 |
|
RU2750539C2 |
| КОМБИНАЦИЯ АНТАГОНИСТА PD-1, ИНГИБИТОРА ТИРОЗИНКИНАЗЫ VEGFR/FGFR/RET И ИНГИБИТОРА CBP/БЕТА-КАТЕНИНА ДЛЯ ЛЕЧЕНИЯ РАКА | 2020 |
|
RU2838452C1 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ ДЛЯ ЛЕЧЕНИЯ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ | 2018 |
|
RU2764724C2 |
| ПРОТИВООПУХОЛЕВОЕ ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО | 2016 |
|
RU2718048C2 |
| БИОМАРКЕРЫ ДЛЯ КОМБИНИРОВАННОЙ ТЕРАПИИ, ВКЛЮЧАЮЩЕЙ ЛЕНВАТИНИБ И ЭВЕРОЛИМУС | 2016 |
|
RU2745060C2 |
| ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ ГЕПАТОЦЕЛЛЮЛЯРНОЙ КАРЦИНОМЫ | 2019 |
|
RU2777535C2 |
| ЛЕЧЕНИЕ ПОЧЕЧНО-КЛЕТОЧНОЙ КАРЦИНОМЫ ЛЕНВАТИНИБОМ И ЭВЕРОЛИМУСОМ | 2017 |
|
RU2785893C2 |
| ИНГИБИТОРЫ FGFR4 | 2014 |
|
RU2715708C2 |
Группа изобретений относится к области медицины, а именно к онкологии и терапии, и предназначена для лечения гепатоцеллюлярной карциномы у пациента. Способ лечения гепатоцеллюлярной карциномы у пациента, нуждающегося в этом, включает введение пациенту комбинации N-(2-((6-(3-(2,6-дихлор-3,5-диметоксифенил))-1-метилуреидо)пиримидин-4-ил)амино)-5-(4-этилпиперазин-1-ил)фенил)акриламида или его фармацевтически приемлемой соли и 4-[3-хлор-4-(N'-циклопропилуреидо)фенокси]-7-метоксихинолин-6-карбоксамида или его фармацевтически приемлемой соли. Также представлена фармацевтическая композиция, содержащая указанные соединения. В других воплощениях обеспечиваются применения комбинации указанных соединений в лечении гепатоцеллюлярной карциномы и в приготовлении лекарственного средства для лечения гепатоцеллюлярной карциномы. Использование группы изобретений позволяет синергетически снизить жизнеспособность клеток гепатоцеллюлярной карциномы и ингибировать рост опухоли гепатоцеллюлярной карциномы у пациентов, нуждающихся в лечении. 4 н. и 17 з.п. ф-лы, 2 ил., 2 пр.
1. Способ лечения гепатоцеллюлярной карциномы у пациента, нуждающегося в этом, включающий введение пациенту комбинации N-(2-((6-(3-(2,6-дихлор-3,5-диметоксифенил))-1-метилуреидо)пиримидин-4-ил)амино)-5-(4-этилпиперазин-1-ил)фенил)акриламида или его фармацевтически приемлемой соли и 4-[3-хлор-4-(N'-циклопропилуреидо)фенокси]-7-метоксихинолин-6-карбоксамида или его фармацевтически приемлемой соли.
2. Способ по п. 1, в котором N-(2-((6-(3-(2,6-дихлор-3,5-диметоксифенил))-1-метилуреидо)пиримидин-4-ил)амино)-5-(4-этилпиперазин-1-ил)фенил)акриламид или его фармацевтически приемлемую соль вводят в суточной дозе от 50 мг до 600 мг.
3. Способ по п. 2, в котором N-(2-((6-(3-(2,6-дихлор-3,5-диметоксифенил))-1- метилуреидо)пиримидин-4-ил)амино)-5-(4-этилпиперазин-1-ил)фенил)акриламид или его фармацевтически приемлемую соль вводят в суточной дозе от 200 мг до 400 мг.
4. Способ по п. 3, в котором N-(2-((6-(3-(2,6-дихлор-3,5-диметоксифенил))-1-метилуреидо)пиримидин-4-ил)амино)-5-(4-этилпиперазин-1-ил)фенил)акриламид или его фармацевтически приемлемую соль вводят в суточной дозе 300 мг.
5. Способ по любому из пп. 1-4, в котором 4-[3-хлор-4-(N'-циклопропилуреидо)фенокси]-7-метоксихинолин-6-карбоксамид или его фармацевтически приемлемую соль вводят в суточной дозе 8 мг.
6. Способ по любому из пп. 1-4, в котором 4-[3-хлор-4-(N'-циклопропилуреидо)фенокси]-7-метоксихинолин-6-карбоксамид или его фармацевтически приемлемую соль вводят в суточной дозе 12 мг.
7. Способ по любому из пп. 1-6, в котором N-(2-((6-(3-(2,6-дихлор-3,5-диметоксифенил))-1-метилуреидо)пиримидин-4-ил)амино)-5-(4-этилпиперазин-1-ил)фенил)акриламид или его фармацевтически приемлемую соль и 4-[3-хлор-4-(N'-циклопропилуреидо)фенокси]-7-метоксихинолин-6-карбоксамид или его фармацевтически приемлемую соль вводят в виде отдельных композиций.
8. Способ по любому из пп. 1-6, в котором N-(2-((6-(3-(2,6-дихлор-3,5-диметоксифенил))-1-метилуреидо)пиримидин-4-ил)амино)-5-(4-этилпиперазин-1-ил)фенил)акриламид или его фармацевтически приемлемую соль и 4-[3-хлор-4-(N'-циклопропилуреидо)фенокси]-7-метоксихинолин-6-карбоксамид или его фармацевтически приемлемую соль вводят в виде одной композиции.
9. Способ по любому из пп. 1-6, в котором N-(2-((6-(3-(2,6-дихлор-3,5-диметоксифенил))-1-метилуреидо)пиримидин-4-ил)амино)-5-(4-этилпиперазин-1-ил)фенил)акриламид или его фармацевтически приемлемую соль и 4-[3-хлор-4-(N'-циклопропилуреидо)фенокси]-7-метоксихинолин-6-карбоксамид или его фармацевтически приемлемую соль вводят последовательно.
10. Способ по любому из пп. 1-6, в котором N-(2-((6-(3-(2,6-дихлор-3,5-диметоксифенил))-1-метилуреидо)пиримидин-4-ил)амино)-5-(4-этилпиперазин-1-ил)фенил)акриламид или его фармацевтически приемлемую соль и 4-[3-хлор-4-(N'-циклопропилуреидо)фенокси]-7-метоксихинолин-6-карбоксамид или его фармацевтически приемлемую соль вводят одновременно.
11. Способ по любому из пп. 1-6, в котором N-(2-((6-(3-(2,6-дихлор-3,5-диметоксифенил))-1-метилуреидо)пиримидин-4-ил)амино)-5-(4-этилпиперазин-1-ил)фенил)акриламид находится в форме свободного основания.
12. Способ по любому из по пп. 1-6, в котором фармацевтический приемлемая соль N-(2-((6-(3-(2,6-дихлор-3,5-диметоксифенил))-1-метилуреидо)пиримидин-4-ил)амино)-5-(4-этилпиперазин-1-ил)фенил)акриламида представляет собой N-(2-((6-(3-(2,6-дихлор-3,5-диметоксифенил))-1-
метилуреидо)пиримидин-4-ил)амино)-5-(4-этилпиперазин-1-ил)фенил)акриламид в форме свободного основания.
13. Способ по любому из пп. 1-6, в котором фармацевтически приемлемая соль 4-[3-хлор-4-(N'-циклопропилуреидо)фенокси]-7-метоксихинолин-6-карбоксамида представляет собой мезилатную соль 4-[3-хлор-4-(N'-циклопропилуреидо)фенокси]-7-метоксихинолин-6-карбоксамида.
14. Способ по любому из пп. 1-6, в котором фармацевтически приемлемая соль N-(2-((6-(3-(2,6-дихлор-3,5-диметоксифенил))-1-метилуреидо)пиримидин-4-ил)амино)-5-(4-этилпиперазин-1-ил)фенил)акриламида представляет собой N-(2-((6-(3-(2,6-дихлор-3,5-диметоксифенил))-1-метилуреидо)пиримидин-4-ил)амино)-5-(4-этилпиперазин-1-ил)фенил)акриламид в форме свободного основания и где фармацевтически приемлемая соль 4-[3-хлор-4-(N'-циклопропилуреидо)фенокси]-7-метоксихинолин-6-карбоксамида представляет собой мезилатную соль 4-[3-хлор-4-(N'-циклопропилуреидо)фенокси]-7-метоксихинолин-6-карбоксамида.
15. Фармацевтическая композиция для лечения гепатоцеллюлярной карциномы, содержащая N-2-((6-(3-(2,6-дихлор-3,5-диметоксифенил))-1-метилуреидо)пиримидин-4-ил)амино)-5-(4-этилпиперазин-1-ил)фенил)акриламид или его фармацевтически приемлемую соль, 4-[3-хлор-4-(N'-циклопропилуреидо)фенокси]-7-метоксихинолин-6-карбоксамид или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель.
16. Фармацевтическая композиция по п. 15, содержащая в форме свободного основания N-(2-((6-(3-(2,6-дихлор-3,5-диметоксифенил))-1-метилуреидо)пиримидин-4-ил)амино)-5-(4-этилпиперазин-1-ил)фенил)акриламид.
17. Фармацевтическая композиция по п. 15, в которой фармацевтически приемлемая соль N-(2-((6-(3-(2,6-дихлор-3,5-диметоксифенил))-1-метилуреидо)пиримидин-4-ил)амино)-5-(4-этилпиперазин-1-ил)фенил)акриламида представляет собой N-(2-((6-(3-(2,6-дихлор-3,5-диметоксифенил))-1-метилуреидо)пиримидин-4-ил)амино)-5-(4-этилпиперазин-1-ил)фенил)акриламид в форме свободного основания.
18. Фармацевтическая композиция по п. 15, в которой фармацевтически приемлемая соль 4-[3-хлор-4-(N'-циклопропилуреидо)фенокси]-7-метоксихинолин-6-карбоксамида представляет собой мезилатную соль 4-[3-хлор-4-(N'-циклопропилуреидо)фенокси]-7-метоксихинолин-6-карбоксамида.
19. Фармацевтическая композиция по п. 15, в которой фармацевтически приемлемая соль N-(2-((6-(3-(2,6-дихлор-3,5-диметоксифенил))-1-метилуреидо)пиримидин-4-ил)амино)-5-(4-этилпиперазин-1-ил)фенил)акриламида представляет собой N-(2-((6-(3-(2,6-дихлор-3,5-диметоксифенил))-1-метилуреидо)пиримидин-4-ил)амино)-5-(4-этилпиперазин-1-ил)фенил)акриламид в форме свободного основания и где фармацевтически приемлемая соль 4-[3-хлор-4-(N'-циклопропилуреидо)фенокси]-7-метоксихинолин-6-карбоксамида представляет собой мезилатную соль 4-[3-хлор-4-(N'-циклопропилуреидо)фенокси]-7-метоксихинолин-6-карбоксамида.
20. Применение комбинации N-(2-((6-(3-(2,6-дихлор-3,5-диметоксифенил))-1-метилуреидо)пиримидин-4-ил)амино)-5-(4-этилпиперазин-1-ил)фенил)акриламида или его фармацевтически приемлемой соли и 4-[3-хлор-4-(N'-циклопропилуреидо)фенокси]-7-метоксихинолин-6-карбоксамида в лечении гепатоцеллюлярной карциномы.
21. Применение комбинации N-(2-((6-(3-(2,6-дихлор-3,5-диметоксифенил))-1-метилуреидо)пиримидин-4-ил)амино)-5-(4-этилпиперазин-1-ил)фенил)акриламида или его фармацевтически приемлемой соли и 4-[3-хлор-4-(N'-циклопропилуреидо)фенокси]-7-метоксихинолин-6-карбоксамида в приготовлении лекарственного средства для лечения гепатоцеллюлярной карциномы.
| WO 2017196854 A1, 16.11.2017 | |||
| US 2016089365 A1, 31.03.2016 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| J Gastroenterol., 2017, 52(4), 512-519, doi: 10.1007/s00535-016-1263-4 | |||
| IKEDA М et al | |||
| Safety and Pharmacokinetics of Lenvatinib in Patients with Advanced Hepatocellular Carcinoma | |||
| Clin Cancer | |||
Авторы
Даты
2023-01-16—Публикация
2019-01-09—Подача