Использование: в производстве удобрений и химикатов.
Изобретение относится к способу очистки от ионов железа и алюминия соляно- или азотнокислых растворов, полученных путем взаимодействия растворов соляной или азотной кислоты с концентратами фосфатных руд, фосфатными рудами, или отходами их переработки, содержащими фосфат кальция и нерастворимые в указанных кислотах примеси.
Предлагаемый способ позволяет очистить от ионов железа и алюминия соляно- или азотнокислотные растворы, содержащие фосфорную кислоту, ионы кальция, нитрат или хлорид-ионы и азотную или соляную кислоту, используемые при получении кислых и/или среднего фосфатов кальция.
Цель изобретения: разработать способ очистки от ионов железа и алюминия соляно- или азотнокислотных растворов, содержащих фосфорную, азотную или соляную кислоты, ионы кальция, нитрат или хлорид-ионы, используемые при получении кислых и/или среднего фосфатов кальция, которые можно использовать как минеральные удобрения, либо как реагенты для производства минеральных удобрений. Способ позволяет существенно снизить содержание соединений железа и алюминия в кислых и/или среднем фосфате кальция, которые предназначены для использования в качестве минеральных удобрений либо как сырье для получения минеральных удобрений.
В известном азотно- или солянокислотном методе [1] действием избытка раствора азотной или соляной кислоты на фосфатную руду, содержащую фосфат кальция, получают раствор, содержащий остаток азотной или соляной кислоты, хлорид или нитрат кальция и фосфорную кислоту:
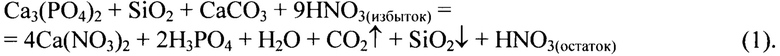
Реакция (1) протекает в прямом направлении, поскольку азотная или соляная кислота являются сильными кислотами, а фосфорная кислота является кислотой средней силы.
Фторид-ионы, присутствующие в руде в качестве примеси, удаляются из реакционной смеси в виде летучей газообразной плавиковой кислоты:

Реакция (2) протекает в прямом направлении, поскольку азотная или соляная кислота являются сильными, а фтористоводородная (плавиковая) кислота относится к легколетучим кислотам слабой силы.
Пары плавиковой кислоты улавливаются известным методом -поглощением раствором щелочи:

Необходимо отметить, что в большинстве случаев в фосфатных рудах и в их концентратах мольное отношение Са : Р больше, чем 1,5, что характерно для Са3(PO4)2, и обусловлено присутствием в руде примеси CaCO3.
Одновременно с протеканием реакции (1) протекают реакции, приводящие к загрязнению раствора соединениями железа и алюминия. В несколько упрощенном виде их протекание можно записать так:


Присутствие в растворе для обработке фосфатной руды соляной кислоты, содержащей коррозионно-активные хлорид-ионы, плавиковой кислоты, интенсивно разрушающей силикаты, азотной кислоты, обладающей окислительными свойствами, фосфорной кислоты, обладающей умеренными комплексообразующими свойствами, а также тепло, выделяющееся при протекании реакции, и время, требуемое для протекание реакции (1), способствуют накоплению соединений железа и алюминия в получаемом растворе, содержащем фосфорную кислоту, ионы кальция, нитрат или хлорид-ионы, соляную или азотную кислоту, который далее используется при получении кислых и/или среднего фосфатов кальция.
После отделения нерастворимых примесей соляно- или азотнокислотный раствор подвергают взаимодействию с щелочными реагентами (чаще всего применяют газообразный аммиак, реже водный раствор аммиака, гидроксида натрия или калия) для повышения рН до необходимых значений за счет нейтрализации кислоты, при которых осаждается умеренно растворимый дигидрофосфат кальция:
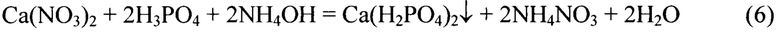
и малорастворимый гидрофосфат кальция, которые применяемые далее в качестве удобрения [1]:
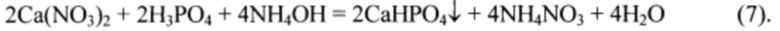
Одновременно с протеканием реакции (6) и (7) создаются условия для осаждения фосфатов железа и алюминия в виде аморфных гелеобразных студенистых осадков, которые затрудняют отделение фильтрованием полученного дигидро- или гидрофосфата кальция. Наличие в готовом продукте примеси фосфатов железа и алюминия уменьшает долю фосфат-ионов, которые могут быть использованы сельскохозяйственными растениями в природных условиях. В связи с этим существуют регламентные ограничения на содержание соединений железа и алюминия в фосфатной руде, обрабатываемой соляно- или азотнокислотным методом [1]. При превышении этих ограничений фосфатную руду (концентраты фосфатной руды) в производстве удобрений не обрабатывают кислотным методом. Особенно это касается отходов обогащения фосфатной руды, поскольку содержание в них различных примесей, по определению, намного больше, чем в исходной природной руде и, тем более, в концентрате фосфатной руды.
Для решения указанных выше проблем с получением возможности перерабатывать любой тип фосфатного сырья (руда, концентраты, отходы обогащения) в кислые и средние фосфаты кальция, пригодные для использования в качестве удобрений, либо в качестве сырья для производства удобрений, необходимо снизить содержание ионов железа и алюминия в соляно- или азотнокислотном растворе, содержащем фосфорную кислоту, ионы кальция, нитрат или хлорид-ионы и соляную или азотную кислоту, получаемом, например, по реакции (1).
Предлагаемый метод позволяет снизить содержание ионов железа и алюминия в соляно- или азотнокислотном растворе, содержащем фосфорную кислоту, ионы кальция, нитрат или хлорид-ионы и соляную или азотную кислоту.
Сущность изобретения
После действия избытка раствора азотной или соляной кислоты на природную руду (концентрат природной руды или отходы обогащения фосфатной руды), содержащую фосфат кальция, и отделения нерастворимых примесей (см. реакцию (1)) фильтрованием, получают водный раствор, содержащий остаток азотной или соляной кислоты, хлорид или нитрат кальция и фосфорную кислоту. Как правило, в зависимости от производства и выбора исходного фосфат-содержащего сырья (концентрат природной руды, фосфатная руда или отходы обогащения фосфатной руды) такие растворы содержат следующие основные компоненты (моль/л, М): Са2+ 0,1-5 М, NO3- 0,2-12 М, РО43- 0,05-3 М, свободную кислоту (определяется по концентрации Н+), Н+ 0,1-5 М и примеси (моль/л): Fe3+ 0,01-1 М, AI3+ 0,01-1 М. Для очистки фильтрата от соединений железа и алюминия его необходимо подвергнуть тепловой обработке, а именно выдержать при температуре от 50°С до 100°С либо до соответствующей температуры кипения раствора в течение от 5 мин до 24 ч. Предварительное, перед тепловой обработкой, разбавление фильтрата водой от 1 до 10 раз способствует процессу очистки фильтрата от соединений железа и алюминия, и это разбавление рекомендуется выполнять в случае необходимости.
Разбавление и нагревание приводят к протеканию следующих процессов:
а) последовательному гидролизу солей трехвалентного железа и сильных кислот [2]:

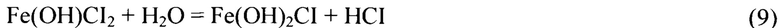

Протеканию гидролиза способствует удаление газообразного HCI вместе с парами воды при нагревании.
б) последовательному переводу кислых солей трехвалентного железа и многоосновных кислот в среднюю соль:

Повышенная температура приводит к "старению" осадка фосфата трехвалентного железа, т.е. к уменьшению его растворимости и, соответственно, к смещению равновесия реакции (12) вправо.
в) взаимодействию основных солей трехвалентного железа (продуктом реакции (8-9)) с кислыми солями трехвалентного железа (исходным веществом и продуктом реакции (11)), например:
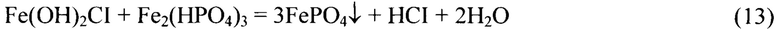
Аналогично идет протекание реакции между продуктом реакции (10) -Fe(OH)3 и исходным веществом и/или продуктом(-ами) реакции (11), например:
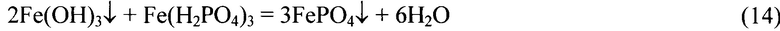
Протеканию процесса реакции (13) способствует удаление газообразного HCI вместе с парами воды при нагревании.
Использование азотной кислоты вместо соляной кислоты предпочтительнее, поскольку приводит к более глубокому смещению равновесия реакции (8)-(10), а также (13) в связи со значительно более слабыми комплексообразующими свойствами нитрат-ионов по отношению к ионам трехвалентного железа по сравнению с хлорид-ионами.
Рассмотренные выше реакции (8-14), характерные для соединений трехвалентного железа, справедливы и для соединений алюминия.
Использование азотной кислоты и нагревания приводит к окислению органических веществ, иногда содержащихся в природной руде либо в продуктах ее переработки. Часто эти вещества являются сильными комплексообразователями, и их разрушение приводит к облегчению протекания процессов осаждения нерастворимых соединений трехвалентного железа и алюминия. Окисление серосодержащих либо азотсодержащих органических веществ, используемых при обогащении фосфатной руды флотационным методом, приводит к образованию сульфат-ионов, либо, как было сказано выше, к разрушению комплексообразующих свойств используемых органических веществ. Образование сульфат-ионов приводит к образованию осадка малорастворимого сульфата кальция, мельчайшие кристаллы которого могут служить центрами кристаллизации для осаждения нерастворимых соединений трехвалентного железа и алюминия.
Удаление отстаиванием (декантацией) либо фильтрованием (периодическое либо непрерывное) осадков, образующихся в результате протекания реакций (10, 12-14), способствует смещению равновесия указанных реакций вправо и, соответственно, повышает степень и глубину очистки соляно- или азотнокислотного раствора, содержащего фосфорную кислоту, ионы кальция, нитрат или хлорид-ионы и соляную или азотную кислоту от соединений трехвалентного железа и алюминия.
Удаление отстаиванием (декантацией) либо фильтрованием (периодическим либо непрерывным) образующихся осадков рекомендуется проводить, не охлаждая раствор, но, в случае необходимости, перед удаление отстаиванием (декантацией) либо фильтрованием (периодическим либо непрерывным) образующихся осадков можно охладить раствор до требуемой температуры, например, комнатной.
После отделения фильтрованием нерастворимых соединений трехвалентного железа и алюминия очищенный фильтрат, при необходимости, можно упарить (нагреванием, испарением и т.д.) до исходного объема (при использовании предварительного разбавления для очистки) либо до достижения нужной концентрации содержащихся в нем веществ.
Осадок, содержащий фосфат трехвалентного железа и/или алюминия, можно переработать на растворимые фосфаты, используя данные патентов [3], [4], а после получение растворимых фосфатов переработать их на кислые фосфаты кальция [5].
Дальнейшую переработку очищенного фильтрата на кислые и средний фосфат кальция можно осуществить классическими способами, изложенными в [1], либо используя данные [6].
Пример 1.
500 мл азотнокислотного раствора, содержащего (моль/л, М): кислородсодержащие соединения P(V), в пересчете на РО43-, 0,34, Са 0,52, NO3- 0,83, Н+ 0,56, а также примеси (г/л): Fe3+=1,2 и AI3+=0,6, нагрели до 100°С и выдержали при этой температуре 1 час, периодически отделяя выпадающие осадки фильтрованием из горячего раствора. Средний элементный состав выпавших осадков близок к гидратированному фосфату трехвалентного железа, содержащего примесь AI(III) и Са(II), поскольку содержит, % атомн: Fe - 11,7, Р - 14,1, AI - 0,90, Са - 0,86. После отделения осадков очищенный раствор содержит Fe3+=0,013 г/л и AI3+=0,33 г/л.
Источники информации
1. Химия и основы технологии минеральных удобрений: учебное пособие / И.А. Петропавловский, Б.А. Дмитревский, Б.В. Левин, И.А. Почиталкина. - СПб.: Проспект Науки, 2021. - 344 с.
2. Краткий справочник по химии. Под редакцией академика АН УССР А.Т. Пилипенко. Киев, Наукова думка, 1987, с. 829.
3. Тураев Д.Ю., Почиталкина И.А. Способ получения растворимых фосфатов натрия, калия и аммония (варианты). Патент RU 2701320. Заявлено 23.11.18. Опубликовано 25.09.2019. Бюл. №27.
4. Тураев Д.Ю., Почиталкина И.А. Способ получения кислых и средних фосфатов натрия, калия и аммония. Патент RU 2701907. Заявлено 03.12.18. Опубликовано 02.10.19. Бюл. №28.
5. Тураев Д.Ю., Почиталкина И.А. Способ получения кислых фосфатов кальция. Патент RU 2720285. Заявлено 19.08.19. Опубликовано 28.04.2020 Бюл. №13.
6. Тураев Д.Ю., Почиталкина И.А. Заявка RU 2021122931. Заявлено 02.08.21.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ КИСЛЫХ И СРЕДНЕГО ФОСФАТОВ КАЛЬЦИЯ | 2021 |
|
RU2768022C1 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРИМЫХ ОРТОФОСФАТОВ | 2019 |
|
RU2703777C1 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРИМЫХ ФОСФАТОВ НАТРИЯ, КАЛИЯ И АММОНИЯ (ВАРИАНТЫ) | 2018 |
|
RU2701320C1 |
| СПОСОБ ПОЛУЧЕНИЯ КИСЛЫХ И СРЕДНИХ ФОСФАТОВ НАТРИЯ, КАЛИЯ И АММОНИЯ | 2018 |
|
RU2701907C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ СОЕДИНЕНИЙ МАГНИЯ ИЗ РУДЫ, СОДЕРЖАЩЕЙ ФОСФАТ КАЛЬЦИЯ | 2021 |
|
RU2768215C1 |
| СПОСОБ ПОЛУЧЕНИЯ КИСЛЫХ ФОСФАТОВ КАЛЬЦИЯ | 2019 |
|
RU2720285C1 |
| Способ получения сложных удобрений из фосфатных руд | 1978 |
|
SU688488A1 |
| Способ кислотной переработки бедного фосфатного сырья | 2016 |
|
RU2634948C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПЛЕКСНЫХ МИНЕРАЛЬНЫХ УДОБРЕНИЙ ИЗ ФОСФАТНОЙ РУДЫ И УСТАНОВКА ДЛЯ ЕГО РЕАЛИЗАЦИИ | 2016 |
|
RU2634936C2 |
| СПОСОБ ПОЛУЧЕНИЯ СЛОЖНЫХ УДОБРЕНИЙ | 1999 |
|
RU2162071C2 |
Изобретение относится к сельскому хозяйству. Способ очистки азотно- или солянокислотных растворов, используемых для производства минеральных удобрений, полученных после действия избытка раствора азотной или соляной кислоты на природную руду, содержащую фосфат кальция, от ионов железа и алюминия, характеризуется тем, что полученные растворы, содержащие, моль/л: Ca2+ 0,1-5, PO43- 0,05-3, H+ 0,1-5, Fe3+ 0,01-1, AI3+ 0,01-1, подвергают тепловой обработке в течение времени от 5 минут до 24 часов при температуре от 50°С до 100°С для образования нерастворимых соединений, содержащих ионы железа и алюминия, с последующим их отделением фильтрованием либо декантацией. Изобретение позволяет существенно снизить содержание соединений железа и алюминия в кислых и/или среднем фосфате кальция, которые предназначены для использования в качестве минеральных удобрений либо как сырье для получения минеральных удобрений. 4 з.п. ф-лы, 1 пр.
1. Способ очистки азотно- или солянокислотных растворов, используемых для производства минеральных удобрений, полученных после действия избытка раствора азотной или соляной кислоты на природную руду, содержащую фосфат кальция, от ионов железа и алюминия, отличающийся тем, что полученные растворы, содержащие, моль/л: Ca2+ 0,1-5, PO43- 0,05-3, H+ 0,1-5, Fe3+ 0,01-1, AI3+ 0,01-1, подвергают тепловой обработке в течение времени от 5 минут до 24 часов при температуре от 50°С до 100°С для образования нерастворимых соединений, содержащих ионы железа и алюминия, с последующим их отделением фильтрованием либо декантацией.
2. Способ по п. 1, отличающийся тем, что перед тепловой обработкой осуществляют разбавление раствора водой от 1 до 10 раз.
3. Способ по п. 1, отличающийся тем, что очистку раствора от образовавшихся нерастворимых соединений железа и алюминия проводят в непрерывном либо периодическом режиме, используя декантацию либо фильтрование, не охлаждая при этом раствор.
4. Способ по п. 1, отличающийся тем, что очистку раствора от образовавшихся нерастворимых соединений железа и алюминия проводят в непрерывном либо периодическом режиме, используя декантацию либо фильтрование при охлаждении раствора до комнатной температуры.
5. Способ по п. 2, отличающийся тем, что при использовании предварительного разбавления раствора для очистки, после отделения фильтрованием нерастворимых соединений железа и алюминия, очищенный фильтрат можно упарить до исходного объема при необходимости.
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРИМЫХ ОРТОФОСФАТОВ | 2019 |
|
RU2703777C1 |
| СПОСОБ КИСЛОТНОЙ ПЕРЕРАБОТКИ БЕДНЫХ ФОСФОРИТОВ | 2008 |
|
RU2389712C2 |
| EP 2991935 B1, 13.11.2019 | |||
| BR 112020002477 A2, 28.07.2020. | |||
Даты
2022-09-20—Публикация
2021-09-21—Подача