Использование: в производстве химических веществ различного назначения.
Изобретение относится к способу получения растворимых фосфатов (натрия, калия или аммония) путем переработки сырья, содержащего фосфат кальция, в частности, руды, содержащей фосфат кальция, реагентным методом.
Предлагаемый способ позволяет из руды, содержащей фосфат кальция, получить кислые и средние фосфаты щелочных металлов, в частности, натрия, калия или аммония.
Цель изобретения: разработать способ переработки природной руды, содержащей фосфат кальция с получением ассортимента продуктов: кислых и средних фосфатов натрия, калия или аммония. Желательно, чтобы в результате предложенного способа переработки руды не образовывалось техногенных отходов.
Действием серной кислоты на природную руду, содержащую фосфат кальция, в промышленности получают фосфорную кислоту [1], [2] из которой можно получить различные фосфаты. Основной недостаток сернокислотного способа получения фосфорной кислоты - это образование сульфата кальция (гипса), который находит весьма ограниченное применение, и поэтому чаще всего утилизируется путем захоронения.
Действием азотной кислоты на природную руду, содержащую фосфат кальция, получают смесь кислых фосфатов кальция. Добавлением к азотной кислоте сульфата калия избыток ионов кальция удаляется в виде осадка сульфата кальция [3].
Замена серной кислоты на азотную кислоту позволяет избежать образования слабо утилизируемого отхода - осадка сульфата кальция. В азотнокислом способе после отделения кислых фосфатов кальция избыток ионов кальция можно удалить за счет кристаллизации нитрата кальция при низкой температуре [4] или действием карбоната натрия или аммония получить нитрат натрия или аммония [5]. Необходимо отметить, что азотнокислый способ не рассматривает дальнейшую переработку полученных кислых фосфатов кальция.
Необходимо отметить, что действием раствора карбоната натрия или калия или аммония на порошок фосфата кальция получить растворы фосфатов этих щелочных металлов или аммония невозможно, т.к. произведение растворимости карбоната кальция, ПР СаСО3=3,8×10-9, намного больше, чем произведение растворимости фосфата кальция, ПР Са3(РО4)2=2,0×10-29 [6].
В тоже время, действуя на кислые фосфаты кальция, например, на дигидрофосфат кальция, Са(H2PO4)2 (растворимость 18 г/л), или гидрофосфат кальция, СаНРО4 (растворимость 0,2 г/л), раствором гидроксида, карбоната или гидроксокарбоната натрия, или калия или аммония можно получить, в зависимости от используемого реагента и его количества, соответствующие растворы кислых и средних фосфатов натрия или калия или аммония и нерастворимый фосфат кальция согласно уравнениям реакций, например:
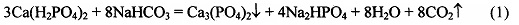
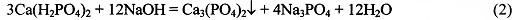
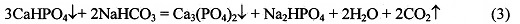
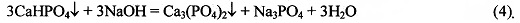
Реакции (1-4) идут слева направо благодаря тому, что конечный продукт фосфат кальция Са3(PO4)2 обладает значительно меньшей растворимостью, чем исходные реагенты в условиях протекания (рН раствора) реакций (1-4).
После отделения осадка фосфата кальция из фильтрата, содержащего кислый фосфат натрия, калия или аммония, при необходимости, можно получить соответствующие средние фосфаты, например:

Осадок фосфата кальция, полученный по реакциям (1-4), отделяется от раствора кислого или среднего фосфата натрия или калия или аммония и может быть возвращен в производственный цикл для получения кислых фосфатов кальция действием раствора азотной кислоты на фосфат кальция по уравнению реакции, например:
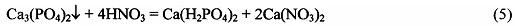
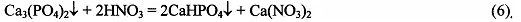
Рассматривая уравнения (1), (3), (5) и (6) можно видеть, что за 1 цикл обработки фосфата кальция в растворимые соединения - кислый и средний фосфат натрия, калия или аммония будет превращено от 2/3 до 1/3 взятого в переработку фосфата кальция.
Также необходимо отметить, что в способе [3] авторы стараются провести процесс таким образом, чтобы минимизировать экстракцию в раствор соединений железа и алюминия, считая эти ионы нежелательными для процесса.
Для увеличения эффективности и глубины переработки фосфата кальция необходимо предложить метод, который позволит за один цикл полностью превращать взятую порцию фосфата кальция в растворимые кислые и средние фосфаты натрия, калия или аммония.
Согласно литературному источнику [7] кислый фосфат, например, аммония, может использоваться для удаления ионов тяжелых металлов, например, алюминия из электролита хромирования, т.е. из кислого раствора, при определенном значении рН.
Анализ литературных источников [3, 7] позволил предложить оригинальный способ переработки руды, содержащей фосфат кальция, путем ее взаимодействия с раствором азотной кислоты, после которого фосфат ионы селективно извлекаются из раствора при заданном значении рН, реагентом, например, ионами алюминия. Способ позволяет раздельно подвергать дальнейшей обработке осадок фосфата алюминия (на кислые и средние фосфаты натрия, калия или аммония) и фильтрат, содержащий нитрат кальция. Необходимо отметить, что при использовании ионов алюминия отсутствует рецикл фосфата кальция.
Сущность изобретения.
Руда, содержащая фосфат кальция и примесь, например, карбоната кальция и диоксида кремния, смешивается с избытком 0,5-50% (масс.) раствора азотной кислоты при температуре 204÷100°С. Реакция идет по уравнению:
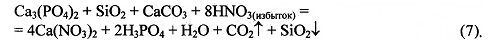
Кремниевая кислота и другие примеси, нерастворимые в ходе этого процесса, отделяются фильтрованием.
В большинстве случаев в полученном по реакции (7) растворе мольное соотношение Са2+ к P(V) (в пересчете на РО43-) оказывается больше, чем 1,5 к 1, характерному для фосфата кальция, Са3(PO4)2, поэтому количество азотной кислоты, требуемое для растворения сырья, содержащего фосфат кальция, как правило, будет больше, чем необходимое по уравнению (7а):
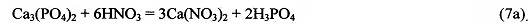
Далее фильтрат, полученный при протекании реакции (7), смешивается с 0,5-50% масс. раствором азотной кислоты, содержащей эквивалентное, по отношению к фосфат-ионам, количество ионов алюминия (используемая при этом концентрация нитрата алюминия 1-1000 г/л, а рекомендуемое мольное отношение AI3+:РО43-=(1,2÷0,8): 1). Далее рН полученного раствора постепенно увеличивают до значений 1,5÷4,5 (рекомендуемое значение рН=2,0÷4,0) добавлением при перемешивании раствора гидроксида (1-40% масс.) или карбоната (1-20% масс.) или гидроксокарбоната (1-10% масс.) натрия, калия или аммония. При этом избыток азотной кислоты нейтрализуется, например, по реакции (8) или (9), а далее реакция идет по уравнению (10) при нейтрализации выделяющейся азотной кислоты:


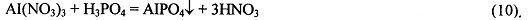
Для более полного смещения обратимой реакции (10) в сторону образования осадка фосфата алюминия, рекомендуется в период образования осадка фосфата алюминия продолжить нейтрализацию выделяющейся азотной кислоты раствором гидроксида (1-40% масс.) или карбоната (1-20% масс.) или гидроксокарбоната (1-10% масс.) натрия, калия или аммония.
Выпавший осадок фосфата алюминия отделяют фильтрованием.
При увеличении значения рН раствора от сильнокислых значений к слабокислым, осадок фосфата алюминия будет образовываться раньше, чем осадок дигидрофосфата кальция, Са(H2PO4)2, и гидрофосфата кальция, CaHPO4, т.к. произведение растворимости фосфата алюминия ПР (AIPO4)=5,75×10-19, значительно меньше, чем ПР (Са(H2PO4)2)=1,45×10-3 и ПР (СаНРО4)=2,7×10-7, несмотря на то, что первая константа диссоциации фосфорной кислоты, приводящей к образованию, соответственно ионов H2PO4-, K1=7,1×10-3 значительно больше, чем K2=6,2×10-8 (отвечает за образование ионов HPO42-) и K3=5,0×10-13 (отвечает за образование ионов PO43)[6].
Осадок фосфата алюминия также будет образовываться раньше, чем осадок фосфата кальция, поскольку равновесная концентрация фосфат ионов, [PO43-], необходимая для образования фосфата алюминия меньше, чем необходимая для фосфата кальция, несмотря на то, что численное значение произведения растворимости фосфата алюминия ПР (AIPO4)=5,75×10-19 больше, чем для фосфата кальция ПР (Са3(РО4)2)-2,0×10-29 [6], следовательно, возможно протекание следующей реакции:
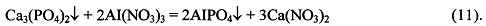
Полученный осадок фосфата алюминия в отдельной емкости смешивают с раствором гидроксида (1-40% масс.) или карбоната (1-20% масс.) или гидроксокарбоната (1-10% масс.) натрия, калия или аммония. Реакция идет по уравнению:
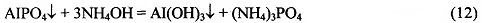
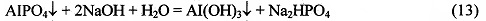
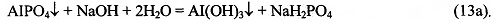
После отделения осадка гидроксида алюминия, из фильтрата, содержащего кислый фосфат натрия, калия или аммония, при необходимости, можно получить соответствующие средние фосфаты, проведя реакцию по уравнению (4а).
Осадок гидроксида алюминия отделяют, промывают и растворяют в отдельной емкости в 0,5-50% масс. растворе азотной кислоты. Реакция идет по уравнению:
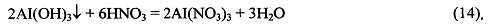
Полученный раствор нитрата алюминия с концентрацией 1-1000 г/л подкисляют азотной кислотой и используют повторно в процессе селективного осаждения фосфат ионов по реакции (10).
Фильтрат, после отделения осадка гидроксида алюминия, представляет собой целевой продукт - раствор кислого или среднего фосфата калия или аммония (можно использовать для получения минеральных удобрений) или раствор кислого или среднего фосфата натрия (можно использовать для получения моющих средств).
Если при проведении реакции (10) осадок фосфата алюминия содержит примесь дигидрофосфата кальция, Са(H2PO4)2, или гидрофосфата кальция, CaHPO4, то при дальнейшем проведении реакции (12), (13) одновременно будут протекать и реакции (1)-(4). Дальнейшее растворение полученного осадка смеси гидроксида алюминия и фосфата кальция в избытке азотной кислоты по реакции (14) приведет к полному растворению фосфата кальция по реакции (7а), что приведет к возврату ионов кальция и фосфорной кислоты в производственный цикл, т.к. полученный раствор будет повторно использоваться при осаждении фосфата алюминия по реакции (10).
Если при отделении осадка фосфата алюминия фильтрат содержит примесь ионов алюминия, фосфорной кислоты и ее анионов, то к фильтрату добавляют при перемешивании раствор гидроксида (1-40% масс.) или карбоната (1-20% масс.) или гидроксокарбоната (1-10% масс.) натрия, калия или аммония до рН=4,5-6, при котором образуется осадок гидроксида алюминия:
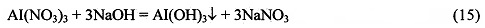
и осадок малорастворимого гидрофосфата кальция, CaHPO4, по реакции (16) при нейтрализации выделяющейся азотной кислоты:
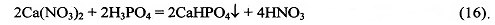
Полученные осадки отделяются от раствора и растворяются в растворе азотной кислоты по реакциям (14) и (17):

Данный процесс также приведет к возврату ионов кальция и фосфорной кислоты в производственный цикл, т.к. полученный раствор будет повторно использоваться при осаждении фосфата алюминия по реакции (10).
Фильтрат, после отделения осадка фосфата алюминия, в том числе, дополнительно очищенный от ионов алюминия, фосфорной кислоты и ее анионов, представляет собой смесь растворов нитрата кальция и нитрата натрия или калия или аммония. К полученному фильтрату добавляют рассчитанное количество раствора карбоната натрия или калия или аммония. Реакция идет по уравнению (18):
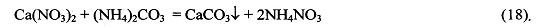
Выпавший осадок карбоната кальция отделяют фильтрованием.
Нитрат кальция, образующийся также по реакциям (5) и (6), может быть переработан на другие нитраты, например, нитрат аммония [5].
Продукт реакции (18) - карбонат кальция - находит широкое применение в различных отраслях народного хозяйства (стекольной, строительной и т.д.).
Фильтрат - раствор нитрата натрия, калия или аммония может найти применение в производстве удобрений.
При использовании ионов алюминия отсутствует рецикл фосфата кальция. Ионы алюминия используются в предложенном цикле многократно и в небольших количествах, т.е. образуется замкнутый цикл по ионам алюминия. Если в перерабатываемой руде присутствуют заметные количества соединений алюминия, то количество используемых в замкнутом цикле соединений алюминия будет увеличиваться. При необходимости, избыточное количество соединений алюминия можно вывести из цикла, используя, например, уравнения (12) и (13). Гидроксид алюминия может быть использован, например, в производстве соединений алюминия и металлического алюминия. Отходом процесса является осадок карбоната кальция, который находит широкое применение, например, в производстве стекла, строительных материалов и в других производствах.
Таким образом, заявленный процесс позволяет получить из нерастворимого фосфата кальция целевой основной продукт индивидуальные кислые и средние фосфаты натрия, калия или аммония. Попутно образуются соответствующие нитраты.
Пример 1. 100 г руды, содержащей 20% фосфата кальция, смешали с 100 мл 30% раствора азотной кислоты. Нерастворимый остаток отделили фильтрованием. К полученному фильтрату добавили 100 мл 6% раствора азотной кислоты, содержащей 275 г/л нитрата алюминия и перемешали. К полученному раствору добавляли при перемешивании 100 мл 26% водного раствора аммиака до рН=3. Выпавший осадок фосфата алюминия отделили от раствора, содержащего нитрат кальция и аммония, фильтрованием и промыли. Осадок фосфата алюминия в отдельной емкости смешали с 60 мл 26% раствора аммиака. Выпавший осадок гидроксида алюминия отделили фильтрованием и растворили в 70 мл 30% раствора азотной кислоты для повторного использования ионов алюминия. Фильтрат, после отделения осадка гидроксида алюминия содержит 320 г/л фосфата аммония.
Источники информации.
1. Технология фосфорных и комплексных удобрений. / Под ред. Эвенчика С.Д. и Бродского А.А. - М.: Химия, 1987. - 464 с.
2. Технология минеральных удобрений / М.Е. Позин. 5-е изд. - Л.: Химия, 1983. - 335 с.
3. Почиталкина И.А., Филенко И.А., Кондаков Д.Ф., Сибирякова Е.М., Колесников В.А. Способ кислотной переработки бедного фосфатного сырья. Патент RU 2634948. Заявлено: 06.12.2016. Опубликовано: 08.11.2017 Бюл. №31
4. Кислотные методы переработки фосфатного сырья / Е.Л. Яхонтова, И.А. Петропавловский., В.Ф. Кармышов, И. А. Спиридонова - М.: Химия, 1988. - 288 с.
5. Технология минеральных удобрений: учебное пособие / И.А. Петропавловский, Б.А. Дмитревский, Б.В. Левин, И.А. Почиталкина. - СПб.: Проспект Науки, 2018. - 312 с.
6. Краткий справочник по химии. Под редакцией академика АН УССР А.Т. Пилипенко. Киев, Наукова думка, 1987, с. 829.
7. Степаненко Е.К., Смирнов А.Л. Способ регенерации отработанных хромовых электролитов. Патент №2061802. Заявлено 06.12.1991, опубликовано 10.06.1996.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРИМЫХ ФОСФАТОВ НАТРИЯ, КАЛИЯ И АММОНИЯ (ВАРИАНТЫ) | 2018 |
|
RU2701320C1 |
| СПОСОБ ПОЛУЧЕНИЯ РАСТВОРИМЫХ ОРТОФОСФАТОВ | 2019 |
|
RU2703777C1 |
| СПОСОБ ПОЛУЧЕНИЯ КИСЛЫХ ФОСФАТОВ КАЛЬЦИЯ | 2019 |
|
RU2720285C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ СОЕДИНЕНИЙ МАГНИЯ ИЗ РУДЫ, СОДЕРЖАЩЕЙ ФОСФАТ КАЛЬЦИЯ | 2021 |
|
RU2768215C1 |
| СПОСОБ ПОЛУЧЕНИЯ КИСЛЫХ И СРЕДНЕГО ФОСФАТОВ КАЛЬЦИЯ | 2021 |
|
RU2768022C1 |
| Способ переработки фосфатного сырья | 2023 |
|
RU2801382C1 |
| СПОСОБ ОЧИСТКИ ОТ ПРИМЕСЕЙ ЖЕЛЕЗА И АЛЮМИНИЯ РАСТВОРА, СОДЕРЖАЩЕГО ИОНЫ КАЛЬЦИЯ, ФОСФОРНУЮ И АЗОТНУЮ (СОЛЯНУЮ) КИСЛОТУ | 2021 |
|
RU2780212C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПЛЕКСНОГО МИНЕРАЛЬНОГО УДОБРЕНИЯ | 2004 |
|
RU2276123C2 |
| СПОСОБ ПОЛУЧЕНИЯ КАРБОНАТА КАЛЬЦИЯ (ВАРИАНТЫ) | 2005 |
|
RU2281921C1 |
| ФОСФОР-КАЛИЙ-АЗОТСОДЕРЖАЩЕЕ NPK-УДОБРЕНИЕ И СПОСОБ ПОЛУЧЕНИЯ ГРАНУЛИРОВАННОГО ФОСФОР-КАЛИЙ-АЗОТСОДЕРЖАЩЕГО NPK-УДОБРЕНИЯ | 2016 |
|
RU2628292C1 |
Изобретение относится к получению растворимых кислых и средних фосфатов натрия, калия или аммония. Способ включает взаимодействие руды, содержащей фосфат кальция, с раствором азотной кислоты и отделение фильтрованием нерастворимых примесей. Причем содержащую фосфат кальция руду смешивают с избытком 0,5-50 мас.% раствора азотной кислоты при температуре 20÷100°С. Полученный фильтрат смешивают с 1-50 мас.% раствором азотной кислоты, содержащей ионы алюминия в виде нитрата алюминия с концентрацией 1-1000 г/л, и раствором щелочного реагента в виде гидроксида, карбоната или гидроксокарбоната натрия, калия или аммония до достижения в растворе значения рН 1,5-4,5 и получения осадка фосфата алюминия, который отделяют фильтрованием и в отдельной емкости смешивают с раствором щелочного реагента до образования осадка гидроксида алюминия, который отделяют фильтрованием от полученного целевого продукта. Изобретение обеспечивает увеличение эффективности переработки фосфата кальция и позволяет за один цикл полностью превратить порцию фосфата кальция в растворимые кислые и средние фосфаты натрия, калия или аммония. 4 з.п. ф-лы, 1 пр.
1. Способ получения растворимых кислых и средних фосфатов, включающий взаимодействие руды, содержащей фосфат кальция, с раствором азотной кислоты и отделение фильтрованием нерастворимых примесей, отличающийся тем, что содержащую фосфат кальция руду смешивают с избытком 0,5-50 мас.% раствора азотной кислоты при температуре 20÷100°С, а полученный фильтрат смешивают с 1-50 мас.% раствором азотной кислоты, содержащей ионы алюминия в виде нитрата алюминия с концентрацией 1-1000 г/л, и раствором щелочного реагента в виде гидроксида, карбоната или гидроксокарбоната натрия, калия или аммония до достижения в растворе значения рН 1,5-4,5 и получения осадка фосфата алюминия, который отделяют фильтрованием и в отдельной емкости смешивают с раствором щелочного реагента до образования осадка гидроксида алюминия, который отделяют фильтрованием от полученного целевого продукта - раствора, содержащего кислые или средние фосфаты натрия, или калия, или аммония.
2. Способ по п. 1, отличающийся тем, что осаждение фосфат-ионов ионами алюминия с получением осадка фосфата алюминия осуществляют при мольном отношении Al3+:PO43-= (1,2÷0,8):1.
3. Способ по п. 1, отличающийся тем, что в качестве раствора щелочного реагента используют раствор 1-40 мас.% гидроксида, или 1-20 мас.% карбоната, или 1-10 мас.% гидроксокарбоната натрия, калия или аммония.
4. Способ по п. 1, отличающийся тем, что осаждение фосфата алюминия проводят при значении рН 2,0-4,0.
5. Способ по п. 1, отличающийся тем, что осадок гидроксида алюминия растворяют в отдельной емкости в 1-50 мас.% растворе азотной кислоты с получением азотнокислого раствора нитрата алюминия с концентрацией 1-1000 г/л для повторного использования при осаждении фосфат-ионов.
| Способ кислотной переработки бедного фосфатного сырья | 2016 |
|
RU2634948C1 |
| СПОСОБ ПОЛУЧЕНИЯ ФОСФАТОВ ЩЕЛОЧНЫХ МЕТАЛЛОВ | 2007 |
|
RU2318724C1 |
| MXNL 05000002 A, 03.07.2006 | |||
| Приспособление для крепления деталей | 1982 |
|
SU1049197A1 |
Даты
2019-10-02—Публикация
2018-12-03—Подача